Изобретение относится к области фармации и касается получения лекарственного средства, обладающего противовоспалительным и антибактериальным действием.
В последние годы отмечается увеличение заболеваемости хроническим простатитом. Многообразие и тяжесть клинических проявлений заболевания, нерешенность многих вопросов его выявления, неудовлетворительные результаты лечения негативно влияют на такие показатели, как качество жизни, рождаемость, а также являются причиной разводов и нередко приводят к инвалидности в относительно молодом возрасте. Эти факторы придают хроническому простатиту все возрастающую медико-социальную значимость и требуют дальнейшего изучения и решения этой актуальной проблемы [15, 16].
Простатит - острое или хроническое воспаление предстательной железы. Это наиболее частое воспалительное заболевание половой сферы мужчин. Согласно статистическим данным заболеванием страдают от 25-40% мужчин (а по некоторым данным до 80%), как правило, в самом трудоспособном возрасте 25-40 лет, что имеет большое социальное значение [7].
В этиологии хронических простатитов могут играть разные факторы. В связи с этим их подразделяют на инфекционный простатит, вызванный бактериями, трихоманадами, вирусами, грибами, хламидиями, и неинфекционный (застойный) - вследствие нарушения микроциркуляции, аллергии [1, 6].
К числу факторов развития простатита также относится обусловленная застойными процессами в железе активность перекисного окисления липидов, являющаяся причиной мембрано-деструктивных процессов, и связанное с этим усиление тканевых изменений. При этом уменьшается резерв местных клеточных антиоксидантных возможностей, что еще больше усугубляет изменения, способствуя микробной контаминации предстательной железы [1].
В развитии неинфекционного простатита играют роль различные иммунные, гормональные и вегетативные нарушения. В связи с сочетанием нескольких инициирующих факторов простатит считают полиэтиологическим заболеванием [1].
Хронический простатит - заболевание с упорным и длительным течением, склонное к рецидивам и серьезным осложнениям. Течение простатита у каждого пациента сугубо индивидуальное и требует соответствующего терапевтического подхода [16].
Лечение простатита включает несколько этапов: этиологическое лечение - ликвидация возбудителя (антибиотикотерапия); патогенетическое лечение с учетом местных и общих факторов (восстановление микроциркуляции в простате, улучшение оттока секрета из протоков ацинусов, повышение интенсивности обменных и репаративных процессов в очаге воспаления); лечение, направленное на нормализацию эндокринной системы; повышение иммунологической реактивности организма; общеукрепляющее лечение; психотерапия и др [6].
Одной из наиболее актуальных, но пока, к сожалению, нерешенных проблем лекарственной терапии больных является выбор препарата той или иной группы, который будет наиболее эффективным и безопасным для пациента. В настоящее время на фармацевтическом рынке много препаратов синтетического происхождения с выраженным фармакотерапевтическим действием, без которых безусловно не обойтись в урогентной урологии. Однако в случаях, не требующих экстренного вмешательства, все большее значение для лечения и профилактики хронического простатита приобретает фитотерапия [5]. Это связано с ростом числа побочных действий и с удорожанием синтетических лекарственных средств, изменением фармакологического эффекта при одновременном применении нескольких препаратов, особенно при лечении лиц пожилого и старческого возраста. Преимущество отдается комплексным растительным препаратам, в которых лекарственные растения хорошо сочетаются друг с другом, отличаются широтой терапевтического действия, низкой токсичностью и, связанной с этим, возможностью длительного применения без развития существенных побочных действий.
В этой связи поиск и создание новых эффективных средств, получаемых из растительного сырья и предназначенных для профилактики и лечения хронического простатита, является актуальной задачей фармации.
Известен растительный сбор «Бруснивер», выпускаемый АО «Красногорсклексредства», рекомендуемый для лечения воспалительных заболеваний мочеполовой системы. Препарат используется в виде водного отвара, приготовленного по ГФ СССР XI издания (1990) [4]. В составе сбора лист брусники 50%, плоды шиповника и трава зверобоя по 20%, трава череды 10%.
Отвар из лекарственного растительного сырья не обеспечивает максимального выхода биологически активных веществ (БАВ) в извлечениях и обычно составляет 20-40% от содержащихся БАВ в сырье. При приготовлении отвара трудно оценить степень выхода действующих веществ при каждом получении отвара. Недостатком указанного способа является также недостаточная фармакологическая активность.
Нами разработано комплексное средство растительного происхождения в виде сухого экстракта, обладающее выраженным противовоспалительным и антибактериальным действием, состоящее из семи лекарственных растений.
Технический результат изобретения - расширение ассортимента лекарственных средств растительного происхождения, обладающих противовоспалительным и антибактериальным действием, за счет использования широко распространенного растительного сырья, имеющего надежную и обеспеченную сырьевую базу, повышение фармакологической активности за счет многокомпонентности лекарственного средства.
Технический результат достигается тем, что заявляемое лекарственное средство включает высушенные измельченные экстракты из следующих растений: ортосифона тычиночного (лист), толокнянки обыкновенной (листья), горца птичьего (трава), календулы лекарственной (цветки), солодки уральской (корень).
Лист ортосифона тычиночного экстрагируют трехкратно в соотношении сырье:экстрагент 1:(10) 40% этанолом. Извлечения объединяют, фильтруют и упаривают до 1/15 первоначального объема. Концентрированный экстракт очищают сепарированием, сушат в вакуумной сушилке и измельчают. Выход готового продукта составляет 16% от массы растительного сырья.
Лист толокнянки обыкновенной экстрагируют трехкратно в соотношении сырье:экстрагент 1:(10) 50% этанолом. Извлечения объединяют, фильтруют и упаривают до 1/15 первоначального объема. Концентрированный экстракт очищают сепарированием, сушат в вакуумной сушилке и измельчают. Выход готового продукта составляет 30% от массы растительного сырья.
Траву горца птичьего экстрагируют трехкратно в соотношении сырье:экстрагент 1:(10) 40% этанолом. Извлечения объединяют, фильтруют и упаривают до 1/15 первоначального объема. Концентрированный экстракт очищают сепарированием, сушат в вакуумной сушилке и измельчают. Выход готового продукта составляет 12% от массы растительного сырья.
Цветки календулы лекарственной экстрагируют трехкратно в соотношении сырье:экстрагент 1:(10), 1-ю экстракцию выполняют 70% этанолом, 2-ю и 3-тью 50% этанолом. Извлечения объединяют, фильтруют и упаривают до 1/15 первоначального объема. Концентрированный экстракт очищают сепарированием, сушат в вакуумной сушилке и измельчают. Выход готового продукта составляет 28% от массы растительного сырья.
Корни солодки экстрагируют трехкратно в соотношении сырье:экстрагент 1:(10), 1-ю экстракцию выполняют 70% этанолом, 2-ю экстракцию выполняют 40% этанолом и 3-тью очищенной водой. 1-е и 2-е извлечения объединяют, фильтруют, упаривают до 1/15 первоначального объема. 3-тье извлечение фильтруют, упаривают до 1/15 первоначального объема, объединяют с упаренными 1-м и 2-м извлечениями. Концентрированный экстракт очищают сепарированием, сушат в вакуумной сушилке и измельчают. Выход готового продукта составляет 29% от массы растительного сырья.
Полученные экстракты ортосифона тычиночного, толокнянки обыкновенной, горца птичьего, календулы лекарственной и солодки уральской в следующих соотношениях (масс. части) 30:20:35:5:10 смешивают и получают продукт (полиэкстракт), представляющий собой мелкодисперсный аморфный гигроскопичный порошок со специфическим запахом, с содержанием суммы флавоноидов в пересчете на рутин не менее 2,0% и суммы фенологликозидов в пересчете на арбутин не менее 5,0%. Полученный нами продукт характеризуется как средство, обладающее выраженным противовоспалительным и антибактериальным действием.
Нами изучен фитохимический состав полученного средства. Методом бумажной и тонкослойной хроматографии обнаружены некоторые фенольные вещества.
Вещества флавоноидного характера и фенолкарбоновые кислоты исследовали методом двумерной хроматографии на бумаге FN-17, FN-6 (Германия) в системах растворителей 1 (н-бутанол-уксусная кислота-вода (4:1:2)) и 2 (15% раствор уксусной кислоты). При просматривании хроматограмм в УФ-свете наблюдали зоны адсорбции веществ флавоноидного характера по собственной флюоресценции от желтого до коричневого цвета. После опрыскивания 2% раствором алюминия хлорида наблюдается усиление интенсивности свечения. В качестве растворов сравнения использовали 0,05% растворы хроматографически чистых образцов, кислот (галловой, хлорогеновой); флавоноидов (рутина, кверцетина, апигенина, гиперозида, лютеолин-7-гликозида).
На хроматограмме подтверждено наличие кверцетина Rf~0,68 (I), Rf~0,39 (II); рутина Rf~0,45 (I), Rf~0,57 (II); лютеолин-7-гликозида Rf~0,50 (I), Rf~0,65 (II); мирицетина Rf~0,35 (I), Rf~0,25 (II).
Наличия арбутина определяли на пластинке «Silufol» при хроматографировании водно-спиртового раствора экстракта в системе растворителей этилацетат-этанол в соотношении 95:5 с последующей обработкой 10% водно-спиртовым раствором едкого натра и свежеприготовленным диазореактивом, арбутин открывается в виде ярко-красного пятна на уровне стандарта свидетеля с Rf~0,29.
Методом ТСХ проанализированы этилацетатные извлечения из экстракта. Неподвижная фаза: пластинки "Kiselgel 60 "F-254", размером 20×20 см. Подвижная фаза, смесь растворителей: этилацетат-метилэтилкетон-муравьиная кислота-вода (50:30:10:10), время насыщения камеры 2 ч. На линию старта хроматографической пластинки наносили по 30 мкл испытуемых растворов и 20 мкл рабочих стандартных образцов растворов. Пластинки с нанесенными пробами помещали в камеру для хроматографирования и хроматографировали восходящим способом. Длина пробега 18 см. После чего хроматограмму вынимали из камеры и сушили до полного удаления растворителей, затем проявляли ее 5% раствором фосфорно-молибденовой кислоты в 95% этаноле с нагреванием в сушильном шкафу при температуре 100-105°C в течение 5 минут. Обнаружено не менее 8 зон, окрашенных в синий цвет с Rf~0,29, соответствовавший рутину, с Rf~0,36 - хлорогеновой кислоте, Rf~0,55 - арбутину; с Rf~0,72 - галловой кислоте и Rf~0,82 - кверцетину.
Количественное определение флавоноидов в сухом экстракте проводили спектрофотометрическим методом
Около 0,2 г (точная навеска) полиэкстракта растворяют в мерной колбе вместимостью 50 мл в спирте 70% и доводят объем раствора до метки спиртом 70%, тщательно перемешивают, фильтруют через бумажный фильтр, отбрасывая первые 10 мл фильтрата (раствор А).
2 мл раствора А переносят в мерную колбу вместимостью 25 мл, прибавляют 2 мл 2% раствора алюминия хлорида в спирте 96%, доводят объем раствора спиртом 96% до метки и перемешивают (раствор Б).
Через 40 минут измеряют оптическую плотность раствора Б при длине волны 418 нм в кювете толщиной слоя 10 см. Раствор сравнения готовят параллельно в мерной колбе на 25 мл: 2 мл раствора А, 2 капель 15% уксусной кислоты, доведенный 96% этанолом до 25 мл.
Содержание суммы флавоноидов в пересчете на рутин и абсолютно сухое вещество в процентах (Х) вычисляют по формуле
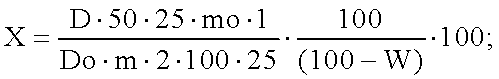
где D - оптическая плотность испытуемого раствора,
Do - оптическая плотность раствора РСО рутина,
m - масса гранул в граммах,
mo - масса РСО рутина в граммах,
W - потеря в массе при высушивании в процентах.
Метрологическая характеристика методики количественного определения суммы флавоноидов представлена в таблице 1.
Как видно из данных таблицы, относительная ошибка определения с 95% вероятностью составляет ±2,82%. В различных сериях экстракта обнаружено от 2,20 до 2,37% флавоноидов.
Количественное определение фенологликозидов методом УФ-спектрофотометрии
2 мл раствора А, полученного при количественном определении флавоноидов, наносят на колонку, заполненную оксидом алюминия, и элюируют 25 мл 60% этанола со скоростью 4 мл/мин. Раствор собирают в мерную колбу вместимостью 25 мл и доводят тем же растворителем до метки (раствор Б). Перемешивают и измеряют оптическую плотность раствора Б при длине волны 280 нм в кювете толщиной 10 мм. В качестве раствора сравнения используют 60% этанол.
Параллельно измеряют оптическую плотность РСО арбутина в 60% спирте. Для этого 0,05 г (точная навеска) помещают в мерную колбу вместимостью 100 мл, прибавляют 50 мл 60% спирта, перемешивают до растворения и доводят тем же растворителем до метки (раствор А). 4 мл раствора А помещают в мерную колбу вместимостью 50 мл, доводят тем же растворителем (раствор Б). Перемешивают и измеряют оптическую плотность раствора Б при длине волны 280 нм в кювете толщиной 10 мм. В качестве раствора сравнения используют 60% этанол.
Содержание фенологликозидов в пересчете на арбутин и абсолютно сухое вещество в процентах (X) вычисляют по формуле
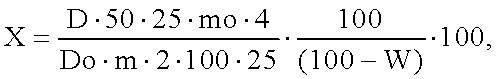
где D - оптическая плотность испытуемого раствора,
Do - оптическая плотность РСО арбутина,
mo - масса РСО арбутина в граммах,
m - масса сухого экстракта в граммах.
W - потеря в массе при высушивании экстракта в процентах,
Результаты количественного анализа фенологликозидов в пересчете на арбутин-стандарт приведены в таблице 2.
Как видно из данных таблицы, относительная ошибка единичного определения с 95% вероятностью не превышает 5%. Содержание фенологликозидов в пересчете на арбутин в сухом экстракте в различных партиях составило от 3,57 до 4,58%.
Фармакологические испытания на экспериментальных моделях у лабораторных животных установили выраженную противовоспалительную и антимикробную активность полученного средства.
Пример конкретного выполнения
Измельченную и просеянную траву ортосифона тычиночного - 100,0 - экстрагируют 1300 мл 40% этанолом при комнатной температуре в соотношении сырья и экстрагента 1:10 с учетом коэффициента водопоглощения (k=1,3). Кратность экстракции 3.
По окончании экстракции получают водно-спиртовой экстракт в количестве 850 мл (плотность 0,958 г/см3). Аналогичным образом проводят еще две экстракции действующих веществ из сырья 40% спиртом этиловым, подавая каждый раз в экстрактор количество растворителя, равное объему слитого экстракта. Получают 750 мл второго экстракта (плотность 0,952 г/см3) и 740 мл третьего экстракта (плотность 0,956 г/см3).
Первый, второй и третий экстракты последовательно, по мере их получения, фильтруют через серошинельное сукно в сборник и упаривают до 1/15 первоначального объема. Концентрированный экстракт очищают сепарированием, сушат в вакуумной сушилке в течение 12 часов и измельчают на мельнице. Получают 16,0 г сухого экстракта ортосифона, что составляет 16% от веса исходного растительного сбора. Сухой экстракт представляет собой мелкодисперсный порошок зеленовато-коричневого цвета со специфическим запахом. Гигроскопичен, слегка комкуется. Содержание влаги - 2,4%.
Измельченные и просеянные листья толокнянки обыкновенной - 100,0 - экстрагируют 1300 мл 50% этанолом при комнатной температуре в соотношении сырья и экстрагента 1:10 с учетом коэффициента водопоглощения (k=1,3). Кратность экстракции 3.
По окончании экстракции получают водно-спиртовой экстракт в количестве 1170 мл (плотность 0,943 г/см3). Аналогичным образом проводят еще две экстракции действующих веществ из сырья 50% спиртом этиловым, подавая каждый раз в экстрактор количество растворителя, равное объему слитого экстракта. Получают 1150 мл второго экстракта (плотность 0,937 г/см3) и 1160 мл третьего экстракта (плотность 0,940 г/см3).
Первый, второй и третий экстракты последовательно, по мере их получения, фильтруют через серошинельное сукно в сборник и упаривают до 1/15 первоначального объема. Концентрированный экстракт очищают сепарированием, сушат в вакуумной сушилке в течение 12 часов и измельчают на мельнице. Получают 30,0 г сухого экстракта толокнянки, что составляет 30,0% от веса исходного растительного сбора. Сухой экстракт представляет собой мелкодисперсный порошок желто-зеленого цвета со специфическим запахом. Гигроскопичен, слегка комкуется. Содержание влаги - 2,2%.
Измельченную и просеянную траву горца птичьего - 100,0 - экстрагируют 1300 мл 40% этанолом при комнатной температуре в соотношении сырья и экстрагента 1:10 с учетом коэффициента водопоглощения (k=1,3). Кратность экстракции 3. По окончании первой экстракции получают водно-спиртовой экстракт в количестве 940 мл (плотность 0,954 г/см3). Аналогичным образом проводят еще две экстракции действующих веществ из сырья 40% спиртом этиловым, подавая каждый раз в экстрактор количество растворителя, равное объему слитого экстракта. Получают 930 мл второго экстракта (плотность 0,951 г/см3) и 920 мл третьего экстракта (плотность 0,949 г/см3).
Первый, второй и третий экстракты последовательно, по мере их получения, фильтруют через серошинельное сукно в сборник и упаривают до 1/15 первоначального объема. Концентрированный экстракт очищают сепарированием, сушат в вакуумной сушилке в течение 12 часов и измельчают на мельнице. Получают 12,0 г сухого экстракта горца птичьего, что составляет 12,0% от веса исходного растительного сбора. Сухой экстракт представляет собой мелкодисперсный порошок коричневого цвета со специфическим запахом. Гигроскопичен, слегка комкуется. Содержание влаги - 1,74%.
Измельченные и просеянные корни солодки уральской - 100,0 - экстрагируют при комнатной температуре в соотношении сырья и экстрагента 1:10 с учетом коэффициента водопоглощения (k=1,3). Кратность экстракции 3. Первая экстракция выполняется 70% этанолом 1300 мл, вторая экстракция 40% этанолом и третья экстракция водой очищенной. Объем экстрагента равен количеству экстракта, полученному при предыдущей экстракции.
По окончании первой экстракции получают первый водно-этанольный экстракт в количестве 960,0 мл (плотность 0,888 г/см3). Экстрагируют шрот еще два раза, 2-й слив - 970,0 мл (плотность 0,952 г/см3), 3-й слив - 890,0 мл (плотность 0,982 г/см3). Первый, второй и третий экстракты последовательно, по мере их получения, фильтруют через серошинельное сукно в сборник и упаривают до 1/15 первоначального объема. Концентрированный экстракт очищают сепарированием, сушат в вакуумной сушилке в течение 12 часов и измельчают на мельнице. Получают 29,5 г экстракта солодки, что составляет 29,5% от веса исходного растительного сбора. Сухой экстракт представляет собой мелкодисперсный порошок коричневого цвета со специфическим запахом. Гигроскопичен, слегка комкуется. Содержание влаги - 3,5%.
Измельченные и просеянные цветки календулы лекарственной - 100,0 - экстрагируют при комнатной температуре в соотношении сырья и экстрагента 1:10 с учетом коэффициента водопоглощения (k=1,3). Кратность экстракции 3. Первая экстракция выполняется 1300 мл 70% этанолом, вторая и третья экстракция 50% этанолом.
По окончании первой экстракции получают первый водно-этанольный экстракт в количестве 990,0 мл (плотность 0,88 г/см3). Экстрагируют шрот еще два раза, подавая каждый раз в экстрактор 50% этанол, в количестве, равном объему слитого извлечения 2-й слив - 990,0 мл (плотность 0,933 г/см3), 3-й слив - 980,0 мл (плотность 0,935 г/см3). Первый, второй и третий экстракты последовательно, по мере их получения, фильтруют через серошинельное сукно в сборник и упаривают до 1/15 первоначального объема. Концентрированный экстракт очищают сепарированием, сушат в вакуумной сушилке в течение 12 часов и измельчают на мельнице. Получают 28,6 г экстракта календулы, что составляет 28,6% от веса исходного растительного сбора. Сухой экстракт представляет собой мелкодисперсный порошок коричневого цвета со специфическим запахом. Гигроскопичен, слегка комкуется. Содержание влаги - 2,5%.
Полученные экстракты ортосифона тычиночного, толокнянки обыкновенной, горца птичьего, календулы лекарственной и солодки уральской смешивают в соотношении (масс. части) (30:20:35:5:10). Получают суммарный полиэкстракт, обладающий выраженным противовоспалительным и антибактериальным действием.
Определение острой токсичности средства, обладающего противовоспалительным и антибактериальным действием
Определение острой токсичности испытуемого полиэкстракта (ИПЭ) проводили на белых мышах линии СВА обоего пола массой 18-20 г с использованием метода Кербера [12]. Результаты исследований показали, что при внутрибрюшинном введении высоких доз полиэкстракта (от 3000 мг/кг и выше) у белых мышей наблюдаются признаки интоксикации, которые выражались вначале снижением двигательной активности, а затем появлением клонико-тонических судорог. Животные погибали при явлениях остановки дыхания преимущественно в течение 1-2 суток с начала введения испытуемого экстракта. DL50 «фитопроста» при его внутрибрюшинном введении составила 1580,0±75,2 мг/кг.
При внутрижелудочном введении данного средства в максимально возможной дозе (8000 мг/кг) гибели белых мышей не наблюдалось в течение всего периода наблюдения (14 суток). Однако при этом имели место отдельные признаки интоксикации в виде снижения аппетита, учащения дыхания, гиподинамии в течение первых суток с момента введения полиэкстракта.
Полученные данные позволяют отнести испытуемый полиэкстракт к классу малотоксичных веществ по классификации К.К.Сидорова [17].
Определение противовоспалительной активность ИПЭ
А. Определение влияния ИПЭ на процессы альтерации и регенерации в очаге воспаления
Опыты проведены на белых крысах линии Wistar обоего пола массой 180-200 г. Моделирование воспалительного процесса осуществляли по методу Менкина [9] путем подкожного введения 0,5 мл 9% раствора уксусной кислоты в область спины животного с предварительно выстриженной шерстью. Одновременно с этим внутрибрюшинно вводили раствор декстрана в дозе 300 мг/кг. Первое введение ИПЭ в дозе 150 мг/кг осуществляли за 1 час до введения уксусной кислоты, а затем ежедневно 1 раз в сутки в течение 25 дней. Крысы контрольной группы получали эквиобъемное количество дистиллированной воды по аналогичной схеме. В качестве препарата сравнения использовали «бруснивер» в виде настоя в объеме 10 мл/кг, вводимый по аналогичной схеме. На 7, 14 и 21 сутки эксперимента оценивали площадь альтерации планиметрическим методом. Статистическую обработку полученных данных проводили с использованием U-критерия Манна-Уитни [13]. Полученные данные представлены в таблице 3.
Как следует из данных, приведенных в таблице 3, введение ИПЭ в дозе 150 мг/кг на фоне асептического воспаления, вызванного химическим ожогом, оказывает противовоспалительное действие, уменьшая степень альтерации тканей и укоряя их регенерацию. Так, на 7, 14 и 21 сутки эксперимента площадь альтерированной ткани у крыс, получавших ИПЭ, была соответственно на 52, 55 и 39% меньше, чем в контроле. При этом во все сроки наблюдения противовоспалительная активность у ИПЭ превосходила таковую у препарата сравнения «бруснивер».
Б. Определение антиэкссудативной активности ИПЭ
Исследование проведено на крысах линии Wistar обоего пола массой 160-180 г. Для оценки влияния ИПЭ на экссудативную фазу воспаления отек конечности вызывали субплантарным введением в заднюю лапку мыши 0,1 мл 3,0% раствора формалина [14], а также 0,1 мл 0,25% раствора каррагенина [11]. Животным опытной группы вводили полиэкстракт в дозе 40 мг/кг в объеме 10 мл/кг за 1 ч до введения флогогенного агента. Величину отека определяли весовым методом по разности масс между воспаленной и невоспаленной конечностями животных. Полученные данные приведены в таблице 4.
Как следует из данных, приведенных в таблице 4, испытуемый полиэкстракт оказывает антиэкссудативное действие, о чем свидетельствует уменьшение выраженности отека конечности животных при асептическом воспалении, индуцированном формалином, на 18% и каррагенином, на 27% по отношению к соответствующему контролю. При этом антиэкссудативная активность полиэкстракта при каррагениновом отеке превосходила, а при формалиновом - была аналогичной таковой у препарата сравнения «бруснивер».
Определение антибактериальной активности испытуемого полиэкстракта
Оценку антимикробной активности ИПЭ проводили методом двукратных серийных разведений в жидкой среде [10]. В качестве тест-объектов использовали следующие виды микроорганизмов: Staphylococcus aureus 209 р, Proteus vulgaris H5D, Escherichia coli - 408, Streptococcus faecalis, Pseudomonas aeruginosa. Микробная нагрузка составляла 250 тыс. клеток в 1 мл. Испытуемый полиэкстракт исследовали в концентрациях от 30,0 до 0,46 мг/мл. В качестве препарата сравнения использовали отвар «бруснивер» (1:10) в исходном объеме 1 мл. Культуры бактерий с исследуемыми фитосредствами в указанных концентрациях инкубировали в термостате при 37°C в течение 20 часов. Контролем служили культуры бактерий без добавления фитосредств. Полученные данные приведены в таблице 5.
Как следует из данных, приведенных в таблице 5, испытуемый полиэкстракт в высоких концентрациях обладает выраженной антибактериальной активностью по отношению ко всем исследованным штаммам бактерий, наиболее часто вызывающих инфекционные заболевания органов мочеполовой системы. Так, по отношению к Staphylococcus aureus высокие концентрации средства (30,0 и 15,0 мг/мл) оказывают бактерицидное действие, а все остальные (до 0,46 мг/мл) проявляют бактериостатические свойства. По отношению к Proteus vulgaris ИПЭ оказывает бактериостатическое действие во всех концентрациях с наиболее сильным угнетением роста бактерий в концентрациях 30,0 и 15,0 мг/мл. Бактерицидное действие испытуемого средства проявляется по отношению к Streptococcus faecalis в концентрации 30,0 мг/мл и бактериостатическое - в более низких (до концентрации 1,87 мг/мл). Слабое бактериостатическое действие ИПЭ оказывает по отношению к Pseudomonas aerigenosae (до концентрации 7,50 мг/мл). По отношению к Escherichia coli испытуемое средство не активно во всех исследованных концентрациях. Установлено, что антибактериальная активность ИПЭ превосходит таковую у препарата сравнения «бруснивер» по отношению ко всем исследованным микроорганизмам.
Определение фармакотерапевтической эффективности испытуемого полиэкстракта при экспериментальном хроническом простатите
Эксперименты проведены на 20 половозрелых белых крысах-самцах линии Wistar с исходной массой 200-220 г, содержавшихся в стандартных условиях вивария при температуре 21-22°C и естественном световом дне. Экспериментальный хронический простатит вызывали интраоперационной аппликацией ортоксилола на заднюю поверхность предстательной железы предварительно кастрированных животных под барбамиловым наркозом (60 мг/кг) [2]. На следующие сутки после инициации экспериментального простатита животным опытной группы вводили водный раствор испытуемого полиэкстракта в экспериментально-терапевтической дозе 150 мг/кг в объеме 1 мл на 100 г массы животного 1 раз в день в течение 21 суток. Крысы контрольной группы получали эквиобъемное количество дистиллированной воды по аналогичной схеме. Наблюдение проводили на 7, 14 и 21 сутки после начала введения полифитоэкстракта. Для оценки фармакотерапевтической эффективности ИПЭ определяли содержание лейкоцитов и СОЭ в крови, содержание лейкоцитов в секрете предстательной железы [6]. Интенсивность процессов свободнорадикального окисления оценивали по содержанию ТБК-активных продуктов в сыворотке крови [3]. Для патоморфологических исследований предстательную железу фиксировали в 10% растворе формалина и заливали в целлоидин-парафин. Парафиновые срезы окрашивали гематоксилин-эозином и по ван Гизон [8]. Полученные данные представлены в таблице 6.
Результаты патоморфологических исследований показали, что аппликация ортоксилола на предстательную железу сопровождается развитием острого простатита. При этом во все сроки эксперимента у животных контрольной группы наблюдали более выраженные структурные изменения в предстательной железе, чем у крыс опытной группы. Так, у животных контрольной группы на 7 сутки отмечали расширенные железистые ячейки предстательной железы. Эпителиальные клетки, выстилающие расширенные железки, были уплощены. В просвете некоторых железок просматривали мелкозернистые массы секрета, десквамированные клетки эпителия и полиморфно-ядерные лейкоциты, единично лимфоциты. У животных, получавших ИПЭ, в этот срок эксперимента указанные явления были менее выражены: был отмечен лишь отек эпителиальных клеток, выстилающих выводные протоки железы. На 14 сутки эксперимента у животных в контрольной группе отмечали некроз секретирующих клеток в концевых отделах железы, отек соединительной ткани между циркулярными слоями гладких мышечных волокон. Железистые ячейки предстательной железы были также более расширены, чем у животных в опытной группе. В группе животных, получавших ИПЭ, указанные явления, характерные для крыс контрольной группы, практически отсутствовали. Отмечали умеренную инфильтрацию вокруг желез и протоков предстательной железы, менее выраженный отек интерстициальной ткани между циркулярными слоями гладких мышечных волокон. На 21-е сутки исследования у животных в контрольной группе отмечали выраженную инфильтрацию лимфоцитов вокруг секреторных отделов и их выводных протоков. В выводных протоках животных контрольной группы наблюдали дистрофические изменения эпителиальных клеток секреторного отдела с десквамированием их в просвет железы с примесью полиморфно-ядерных лейкоцитов. У животных, получавших ИПЭ, к этому сроку наблюдения не отмечали выраженных органических изменений в предстательной железе. Структура секреторного отдела соответствовала норме.
Развитие острого воспалительного процесса в предстательной железе было подтверждено результатами исследования показателей крови и секрета предстательной железы (табл.6). Так, на 7 сутки эксперимента у крыс контрольной группы отмечали выраженный лейкоцитоз с появлением лейкоцитов в секрете предстательной железы, повышение СОЭ и индукцию процессов свободнорадикального окисления, на что указывает почти двукратное увеличение концентрации ТБК-активных продуктов в сыворотке крови крыс этой группы. Установлено, что у животных, получавших ИПЭ в дозе 150 мг/кг, на 7 сутки эксперимента содержание лейкоцитов в крови уменьшалось на 27%, СОЭ снижалось на 54%, а также наблюдалась тенденция к уменьшению содержания лейкоцитов в секрете предстательной железы (на 9%) по сравнению с таковыми показателями у животных контрольной группы. На 14 и 21 сутки наблюдений у животных опытной группы содержание лейкоцитов в крови уменьшалось на 24 и 19%, в секрете предстательной железы - на 68 и 61%, СОЭ - на 70 и 67% соответственно по сравнению с данными у контрольных животных (табл.6). Также показано, что во все сроки наблюдений у животных опытной группы содержание ТБК-активных продуктов в сыворотке крови было ниже этого показателя у контрольных животных на 10, 17 и 21% соответственно, что свидетельствует об ингибировании процессов свободнорадикального окисления под влиянием испытуемого средства.
Таким образом, полученные данные свидетельствуют, что курсовое введение испытуемого полиэкстракта в экспериментально-терапевтической дозе 150 мг/кг на фоне хронического простатита у белых крыс оказывает выраженное фармакотерапевтическое влияние, характеризующееся уменьшением выраженности деструктивных изменений в предстательной железе и признаков воспаления, нормализацией показателей периферической крови, состава секрета предстательной железы и ингибированием свободнорадикальных процессов. Данный фармакотерапевтический эффект полиэкстракта обусловлен представленным в нем комплексом биологически активных веществ: флавоноидов, фенологликозидов, фенолкарбоновых и органических кислот и других соединений. Полученные данные характеризуют испытуемый полиэкстракт как средство, обладающее выраженным противовоспалительным и антибактериальным действием, и аргументируют целесообразность его применения в комплексном лечении и профилактике простатитов.
Литература
1. Арнольди Э.Г. Хронический простатит. Ростов-на-Дону, 1999.
2. Батрудинов М.Г., Горбачев А.Г., Агулянский Л.И. Рацпредложение №157/85. - 1985. - I ЛМИ им. акад. И.П.Павлова.
3. Владимиров Ю.А., Арчаков А.И. Перекисное окисление липидов в биологических мембранах. - М., 1972. - 115 с.
4. Государственная фармакопея СССР: вып.2. Общие методы анализа. Лекарственное растительное сырье. 11-е изд., доп. - М., 1987. - 400 с.
5. Ефремов А.П. Фитотерапия заболеваний предстательной железы. 1999. - с 120.
6. Корик И.Г. Хронический простатит. - Л., 1975. - 167 с.
7. Кругляк Л.Г. Простатит.- Элиста, 1996. - 64 с.
8. Микроскопическая техника: Руководство / Под ред. Д.С.Саркисова, Ю.Л. - М., 1996. - 544 с.
9. Ойвин И.А., Шетель С.Л. Методика изучения нарушений капиллярной проницаемости // Материалы по патогенезу воспаления и патологии белков крови. - Душанбе, 1961. - Т. 49. - №5. - С.167-173.
10. Першин Г.Н. (ред.) Методы экспериментальной химиотерапии. - М. - 1971. - 539 с.
11. Пидэмский Е.Л., Тульбович Г.А., Голенева А.Ф. и др. Перекисное окисление липидов при асептическом воспалении и воздействии флоголитиков и антиоксидантов // Пат. физиол. и экспер. терапия. - 1990. - №1. - С.19-23.
12. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. - М., 2000. - 678 с.
13. Сергиенко В.И., Бондарева И.Б. Математическая статистика в клинических исследованиях. - М., 2000. - 263 с.
14. Стрельников Ю.Е. Сравнительная характеристика противовоспалительного действия некоторых пипримидиновых производных // Фармакол. и токсикол. - 1960. - №6. - С.526-531.
15. Тареев Е.М., Ермоленко В.М. // Клинич. нефрология - М.: Медицина, 1983. - Т.1. - С.207-230.
16. Ткачук В.Н., Горбачев А.Г., Агулянский Л.И. хронический простатит. - Л.: Медицина. 1989. - 208 с.
17. Требования по доклиническому изучению общетоксического действия новых фармакологических веществ. - М., 1984. - 49 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО "ЧАЙ БАЙКАЛЬСКИЙ-6", ОБЛАДАЮЩЕЕ ДИУРЕТИЧЕСКОЙ АКТИВНОСТЬЮ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2004 |
|
RU2237488C1 |
| Способ получения средства, обладающего антигипоксической активностью | 2017 |
|
RU2669365C1 |
| УРОЛОГИЧЕСКИЙ СБОР "ФИТО-ПРО" ДЛЯ КОМПЛЕКСНОГО ЛЕЧЕНИЯ ПРОСТАТИТА И СПОСОБ ЕГО ЛЕЧЕНИЯ | 2002 |
|
RU2238750C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОВОСПАЛИТЕЛЬНЫМ ДЕЙСТВИЕМ | 2016 |
|
RU2636818C2 |
| Средство, обладающее антигипоксическим и адаптогенным действием | 2021 |
|
RU2771555C1 |
| Средство, обладающее гиполипидемическим, гепатозащитным и антиоксидантным действием | 2016 |
|
RU2636817C2 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО АНКСИОЛИТИЧЕСКОЙ АКТИВНОСТЬЮ | 2011 |
|
RU2460534C1 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА ДЛЯ ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ МУЖСКОЙ МОЧЕПОЛОВОЙ СФЕРЫ | 2006 |
|
RU2310343C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ КОМПЛЕКСНЫМ ДИУРЕТИЧЕСКИМ, АНТИМИКРОБНЫМ И ПРОТИВОВОСПАЛИТЕЛЬНЫМ ДЕЙСТВИЕМ | 2006 |
|
RU2314116C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2372934C1 |
Изобретение относится к химико-фармацевтической промышленности, а именно к созданию средства, обладающего противовоспалительным и антибактериальным действием, представляющее собой сухой полиэкстракт, состоящий их сухих экстрактов следующего растительного сырья: ортосифона тычиночного (лист), толокнянки обыкновенной (листья), горца птичьего (трава), календулы лекарственной (цветки), солодки уральской (корень). Средство эффективно для лечения и профилактики простатита. 6 табл.
Лекарственное средство, обладающее противовоспалительным и антибактериальным действием, представляющее собой сухой полиэкстракт, состоящий их сухих экстрактов следующего растительного сырья: ортосифон тычиночный (лист), толокнянка обыкновенная (листья), горец птичий (трава), календула лекарственная (цветки), солодка уральская (корень), взятых в соотношении, мас.ч.:
при этом содержание суммы флавоноидов в пересчете на рутин не менее 2,0% и суммы фенологликозидов в пересчете на арбутин не менее 5,0%.
| СБОР ЛЕКАРСТВЕННЫХ РАСТЕНИЙ, ОБЛАДАЮЩИЙ ОБЩЕУКРЕПЛЯЮЩИМ И ПРОТИВОВОСПАЛИТЕЛЬНЫМ ДЕЙСТВИЕМ (ВАРИАНТЫ) | 2001 |
|
RU2195303C1 |
| ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКОЕ СРЕДСТВО ПРИ ЗАБОЛЕВАНЯХ МОЧЕПОЛОВОЙ СИСТЕМЫ У МУЖЧИН | 2004 |
|
RU2259205C1 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА К ПИЩЕ ДЛЯ ПРОФИЛАКТИКИ И ВСПОМОГАТЕЛЬНОЙ ТЕРАПИИ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ | 2004 |
|
RU2270585C2 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКОГО ПРОСТАТИТА | 2003 |
|
RU2255753C1 |
| ЛЕЧЕБНО-ОЗДОРОВИТЕЛЬНАЯ БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА К ПИЩЕ "МИЛОНА" И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1998 |
|
RU2178660C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ХРОНИЧЕСКОГО ПИЕЛОНЕФРИТА | 2001 |
|
RU2224531C2 |
Авторы
Даты
2011-03-10—Публикация
2009-08-21—Подача