Область техники, к которой относится изобретение
Настоящее изобретение относится к формованному пластинчатому продукту и гемостатическому материалу, содержащему его. В частности, настоящее изобретение относится к формованному пластинчатому продукту, содержащему фибриноген и/или тромбин, обладающему хорошим свойством растворения и поддерживающими характеристиками для этих гемостатических белков, и отличным гемостатическим свойством; и к гемостатическому материалу, содержащему его.
Уровень техники
Фибриноген является фактором коагуляции крови, присутствующим на конечном этапе каскада коагуляции крови. При повреждении кровеносного сосуда система коагуляции активируется, и в итоге активированный тромбин превращает растворимый фибриноген в нерастворимый фибрин. Этот фибрин обладает адгезивной силой, и выполняет важные функции в гемостазе и заживлении ран.
Операции гемостаза и тканевой адгезии, такие как закрытие ткани в важном положении в медицинском участке, особенно при хирургических операциях, и адгезивные средства в виде фибринового клея, к которым относится этот принцип, применяются в широком ряде областей при хирургических операциях.
Были проведены различные исследования, и были внесены усовершенствования в способы применения адгезивного средства в виде фибринового клея; и их примеры включают жидкие препараты для нанесения или распыления раствора фибриногена и раствора тромбина на пораженный участок (двухкомпонентные препараты: см. рассмотренную Японскую заявку на патент № Н9-2971, описание, и Международную заявку на патент № WO 97/33633), и способ, в котором листовой препарат, содержащий фибриноген и тромбин в смеси, фиксированные на подложке, такой как коллаген, прикрепляют к пораженному участку (см. нерассмотренную Японскую заявку на патент №2004-521115, описание).
Однако, в случае существующих жидких препаратов, поскольку лиофилизированный фибриноген и тромбин растворяют по отдельности при использовании, это занимает несколько минут для растворения лиофилизированного препарата, и таким образом, эти препараты нельзя назвать удовлетворительными с точки зрения оперативности для экстренной хирургии и удобства.
Кроме того, в случае вышеупомянутых адгезивных средств в виде фибринового клея, поскольку более высокая концентрация фибриногена обеспечивает большую силу адгезии, малое количество тромбина в высокой концентрации должно действовать на фибриноген с высокой концентрацией.
Однако, в случае существующих жидких препаратов, поскольку равные объемы раствора фибриногена и раствора тромбина смешивают при использовании, их концентрации уменьшаются на 50%, предотвращая проявление максимальной эффективности фибриногена. Далее, поскольку предел концентрации фибриногена в растворе в действительности составляет около 10%, трудно достичь улучшения концентрации для системы, в которой две жидкости смешивают в равном объеме.
В связи с этим, поскольку пластинчатый препарат позволяет наносить раствор фибриногена в высокой концентрации на пораженный участок, теоретически можно ожидать более высокую силу адгезии, по сравнению с двухкомпонентным препаратом. Кроме того, пластинчатый препарат обеспечивает вяжущее/компрессионное закрывание истекающего/экссудативного участка кровотечения, и как ожидается, будет очень удобным.
Когда применяют пластинчатое средство для адгезии тканей, проникновение в ткани пластинчатого препарата должно быть повышено при нанесении на раневой участок, для нанесения раствора фибриногена с высокой концентрацией на пораженную область. Далее, поскольку пластинчатый препарат может свертываться или складываться для тесного прилегания к участку раны, гибкость и мощность удерживания двух компонентов пластины должна быть повышена, для предотвращения повреждения пластины или потери фибриногенового компонента и тромбинового компонента в результате такого усилия.
Описаны пластинчатые средства для адгезии тканей и пластинчатые гемостатические материалы, в которых активный ингредиент фиксирован на различных субстратах (см. рассмотренную Японскую заявку на патент №61-34830, описание; нерассмотренную Японскую заявку на патент №2002-513645; Международную публикацию № WO 2004/064878 и Международную публикацию № WO 2005/113030). Рассмотренная Японская заявка на патент №61-34830, описание, раскрывает пластинчатый препарат, в котором фибриноген и тромбин фиксированы на поверхностном слое лошадиного коллагена, внедренный в практику (зарегистрированная торговая марка ТахоКомб). Однако, поскольку коллагеновый субстрат является толстым и относительно твердым, адгезивность к раневому участку может снижаться, затрудняя эффективное закрывание раны. Пластинчатые препараты имеют подложку из лошадиного коллагена, и таким образом, при использовании у человеческого индивидуума существует риск появления антител против гетерологичного белка, и возникновения зоонозных инфекций, таких как прионное заболевание, и этот пластинчатый препарат нельзя назвать идеальным.
Международная публикация Японской заявки на патент №2002-513645, описание, раскрывает бумагоподобную композицию, в которой однородно распределено гемостатическое соединение. Эту композицию готовят путем формирования фиброзной массы, содержащей биоадсорбирующий полимер и гемостатическое соединение (главным образом тромбин, фибриноген) в неводном растворителе, и обработки фиброзной массы с получением бумаги. Эта композиция снижает время, необходимое для гемостаза, посредством фактора 14, по сравнению с ТахоКомбом, и обеспечивает повторное прикрепление. Однако благодаря бумаго-подобной форме, возможно улучшение свойства соответствия ткани.
Международная публикация WO 2004/064878 и международная публикация WO 2005/113030 раскрывают материал с применением пластины, в которой тромбин фиксирован на биоадсорбирующем синтетическом нетканом материале, и раствор фибриногена в комбинации. Для этих композиций нетканый материал погружают в водный раствор активного ингредиента с последующей лиофилизацией для получения композиции. Проблемами этого способа являются низкий выход на стадии лиофилизации, низкая гибкость пластины, и плохие поддерживающие характеристики для фиксированного бежа, приводящие к отслаиванию от пластины.
В Японской заявке на патент №2009-183649, описание, раскрыт пластинчатый тканевой гемостатический материал, включающий фибриноген-содержащий слой и тромбин-содержащий слой, обеспеченные промежуточным слоем между ними, включающим производное целлюлозы в качестве материала; однако имеются такие проблемы, как недостаточная растворимость фибриногена, находящегося в тканевом гемостатическом материале, и плохая способность к обработке; и материал нельзя обрезать, поскольку он является лиофилизированным продуктом.
В дополнение, в качестве пластинчатых препаратов, в японской заявке на патент №2010-069031, описание, раскрыто пластинчатое адгезивное средство в виде фибринового клея, содержащее биоабсорбирующую подложку, на которой фиксирован фибриноген, содержащий не-ионный сурфактант, и биоадгезивную подложку, на которой фиксирован тромбин; в Японской нерассмотренной заявке на патент №2002-515300, описание, раскрыт многослойный бандаж для гемостаза, содержащий фибриногеновый слой, тромбиновый слой, слой абсорбирующего материала и тому подобное; и в Японской нерассмотренной заявке на патент №2009-533135 раскрыт пористый продукт для лечения ран, содержащий первый абсорбирующий нетканый материал, и по меньшей мере один второй абсорбирующий тканый материал или вязаный материал, и тромбин и/или фибриноген. Однако, поскольку такие гемостатические материалы производят путем лиофилизации фибриногена и тромбина, фибриноген и тромбин быстро удаляются, материал является недостаточно гибким, и эффект адгезии ткани, описанный выше, является недостаточным, поскольку фибриноген и тромбин присутствуют рядом друг с другом. В дополнение, когда препарат находится в форме, в которой фибриноген и тромбин присутствуют в прямом контакте друг с другом, происходит реакция коагуляции с формированием фибрина даже при следовых количествах воды во время хранения, что создает проблему стабильности при хранении. Далее, также имеется проблема затраты огромного количества времени и труда для производства из-за необходимости этапа лиофилизации.
Отсутствует пластинчатый гемостатический материал, для которого действительно можно ожидать эффекта и удобства при комбинации фибриногена и тромбина, как описано выше. Далее, хотя фибриноген в высокой концентрации необходим для сильного эффекта адгезии ткани, поскольку фибриноген плохо растворим, он почти не растворяется при фиксации фибриногена на подложке при сохранении обычного состава из-за плохой растворимости фибриногена, и таким образом, нельзя ожидать проявления достаточной эффективности лекарственного средства.
Раскрытие изобретения
Задачей настоящего изобретения является обеспечение формованного пластинчатого продукта, обладающего хорошими поддерживающими характеристиками и растворимостью для гемостатических белков, то есть, фибриногена и/или тромбина, и отличной гибкостью (свойством соответствия ткани), в итоге обеспечивая гемостаз.
Другой задачей настоящего изобретения является обеспечение гемостатического материала, содержащего формованный пластинчатый продукт в соответствии с настоящим изобретением, как описано выше, с которым достигается отличный гемостатический эффект после нанесения на раневой участок.
Другие объекты и преимущества настоящего изобретения станут понятными из следующего описания.
В соответствии с настоящим изобретением, задачи и преимущества настоящего изобретения, как описано выше, могут быть достигнуты в первую очередь с помощью формованного пластинчатого продукта из полимерной композиции, содержащего по меньшей мере один белок, выбранный из группы, состоящей из фибриногена и тромбина, и по меньшей мере один полимер, выбранный из группы, состоящей из алифатического полиэфира и водорастворимого полимера.
В соответствии с настоящим изобретением, объекты и преимущества настоящего изобретения, как описано выше, могут быть достигнуты, во-вторых, посредством ламинированного формованного пластинчатого продукта, содержащего первый слой формованного пластинчатого продукта, состоящий из фибриногена и водорастворимого полимера, и второй слой формованного пластинчатого продукта, состоящий из тромбина и алифатического полиэфира, в виде формованного пластинчатого продукта, описанного в предыдущем параграфе.
Далее, в соответствии с настоящим изобретением, объекты и преимущества настоящего изобретения, как описано выше, могут быть достигнуты, в-третьих, с помощью гемостатического материала, содержащего формованный пластинчатый продукт или ламинированный формованный пластинчатый продукт, описанный выше. Другими словами, эти формованные продукты наносят на раневой участок, и применяют в качестве гемостатического материала для лечения раневого участка.
Краткое описание чертежей
На фигуре 1 показано растворение тромбина из формованного волокнистого продукта из сополимера полигликолевой кислоты - полимолочной кислоты, содержащего тромбин.
Предпочтительные варианты осуществления изобретения
Формованный пластинчатый продукт в соответствии с настоящим изобретением является формованным пластинчатым продуктом из полимерной композиции, содержащей по меньшей мере один белок, выбранный из группы, состоящей из фибриногена и тромбина, и по меньшей мере одного полимера, выбранного из группы, состоящей из алифатического полиэфира и водорастворимого полимера (далее обозначенного как «субстратный полимер»). Выражение «содержать белок» в настоящей заявке означает состояние, где по меньшей мере часть белка встроена в субстратную полимерную композицию. Такая структура обладает отличными характеристиками поддержки белка, в отличие от лиофилизированных композиций, в которых белок присутствует на поверхности композиции или в зазорах композиции.
Формованный пластинчатый продукт в соответствии с настоящим изобретением не ограничивается, в частности, как продукт, находящийся в пластинчатой форме, но его предпочтительные примеры включают формованный волокнистый продукт и формованный пленочный продукт. Формованный волокнистый продукт является трехмерным формованным продуктом, полученным путем ламинирования, тканья, вязания или обработки посредством других методик из одного или множества полученных волокон. Специфические примеры формованного волокнистого продукта включают нетканый материал. Кроме того, трубка, сетка и тому подобное, приготовленное из нее, включено в формованный волокнистый продукт. Формованный пленочный продукт, применяемый в настоящей заявке, означают пленкообразный формованный продукт, приготовленный путем таких способов формования, как экструзионные способы формования, такие как экструзия раздувом и экструзия с Т-образным пуансоном, каландрирование и литье.
Формованный пластинчатый продукт в соответствии с настоящим изобретением может проявлять свой эффект при применении по отдельности или в комбинации со второй пластиной, содержащий комплементарный белок (фибриноген для тромбина, или тромбин для фибриногена) в фибриновом клее. При использовании по отдельности, предпочтительно он является формованным волокнистым продуктом, содержащим тромбин в алифатическом полиэфире.
Кроме того, формованный пластинчатый продукт, описанный выше, можно применять в качестве формованного пластинчатого продукта для составления ламинированного формованного пластинчатого продукта со вторым формованным пластинчатым продуктом в соответствии с настоящим изобретением; а ламинированный формованный пластинчатый продукт со вторым формованным пластинчатым продуктом в соответствии с настоящим изобретением является ламинированным формованным пластинчатым продуктом, содержащим первый формованный пластинчатый продукт, состоящий из фибриногена и водорастворимого полимера, и второй формованный пластинчатый продукт, состоящий из тромбина и алифатического полиэфира.
Фибриноген и тромбин, используемые в качестве гемостатических белков в настоящем изобретении, могут быть белками животного происхождения и белками, полученными путем генной рекомбинантной технологии. Когда фибриноген и тромбин являются белками животного происхождения, предпочтительными являются человеческие белки. Можно также применять белки, имеющие модифицированную аминокислотную последовательность.
В настоящей заявке частично фибрин может продуцироваться при хранении, особенно когда вышеуказанная полимерная композиция содержит фибриноген и тромбин, и композиция, содержащая такой фибрин, включена в диапазон настоящего изобретения.
Фармацевтически пригодные добавки могут быть добавлены к гемостатическому белку, использованному в настоящем изобретении. Примеры таких добавок включают одну или несколько добавок, выбранных из группы, состоящей из фактора коагуляции XIII, альбумина, изолейцина, глицина, аргинина, глутаминовой кислоты, фенилаланина, гистидина, сурфактантов, хлорида натрия, сахароспиртов (глицерина, маннитола, и т.д.), трегалозы, цитрата натрия, апротинина и хлорида кальция.
Гемостатический белок или смесь гемостатического белка и добавки (добавок) могут быть диспергированы как соответствующие молекулы в субстратном полимере, но предпочтительно, чтобы частицы, образованные соответствующими молекулами, собранными вместе (далее можно применять выражение «белковые частицы», включая смешанные частицы, содержащие добавку(и)), были диспергированы в субстратном полимере. Это может улучшать растворение гемостатического белка и гибкость пластины, когда формованный пластинчатый продукт является волокнисто-подобным формованным продуктом.
В настоящем изобретении средний диаметр содержащихся частиц бежа составляет от 0,1 до 200 мкм. Технически трудно приготовить частицы, имеющие диаметр частицы меньше 0,1 мкм. Далее, когда диаметр частицы составляет более 200 мкм, формованный пластинчатый продукт становится ломким, и его трудно обрабатывать, что не является предпочтительным. Средний диаметр частиц продукта предпочтительно составляет от 0,5 до 150 мкм, и более предпочтительно, от 1 до 100 мкм.
Формованный пластинчатый продукт в соответствии с настоящим изобретением включает, в случае формованного волокнистого продукта, белок-содержащие частицы, как правило, в количестве от 1 до 200 масс. %, предпочтительно, от 10 до 10 масс. %, более предпочтительно, от 20 до 100 масс. %, и еще более предпочтительно, от 50 до 100 масс. %, на основе субстратного полимера. Когда количество белок-содержащих частиц меньше этого значения, то растворение бежа из формованного пластинчатого продукта, и гибкость или гемостатическое свойство формованного пластинчатого продукта могут ухудшаться; в то время как когда содержание повышается, самоподдерживающее свойство формованного пластинчатого продукта само по себе снижается, что не является предпочтительным. В дополнение, в случае формованного пленчатого продукта, белок-содержащие частицы содержатся в количестве 100 масс. % или больше, предпочтительно 500 масс. % или больше, и еще более предпочтительно от 800 до 950 масс. %, на основе субстратного полимера. Когда содержание меньше этих значений, гемостатическое свойство может ухудшаться; а когда содержание выше, формуемость пленки может ухудшаться.
Специфические примеры алифатического полиэфира, используемого в настоящем изобретении, включают полимолочную кислоту, полигликолевую кислоту, сополимер полимолочной кислоты - полигликолевой кислоты, поликапролактон, полиглицерин себакат, полигидроксиалкановую кислоту, полибутилен сукцинат, и их производные. Среди них алифатический полиэфир предпочтительно выбран из группы, состоящей из полимолочной кислоты, полигликолевой кислоты, поликапролактона, и их сополимера, и их смеси.
В настоящей заявке, когда применяют сополимер полимолочной кислоты, может быть включен мономерный компонент, придающий свойство растяжимости. Примеры мономерного компонента, придающего свойство растяжимости, включают капролактоновый мономер, и мягкий компонент, такой как этиленгликоль, 1,2-пропиленгликоль, 1,3-пропиленгликоль, 1,2-бутандиол, 1,4-бутандиол, поликапролактондиол, полиалкилен-карбонат-диол, полиэтигенгликольная единица, и тому подобное. Меньшие количества этих мягких компонентов являются предпочтительными, и количество предпочтительно ниже 50 моль % на единицу полимера. Когда количество мягкого компонента выше этого значения, отмечается тенденция к утрате самоподдерживающего свойства, и продукт становится слишком мягким для легкой обработки.
Когда применяют полимолочную кислоту или ее сополимер, примеры мономеров, составляющих полимер, могут включать L-молочную кислоту и D-молочную кислоту, но не ограничиваются конкретно. Хотя оптическая чистота, молекулярная масса, отношение в композиции L-формы и D-формы, или последовательность полимера не ограничены конкретно, предпочтительным является полимер, содержащий L-форму в большем количестве, и также можно применять стерео комплекс из поли-L-молочной кислоты и поли-D-молочной кислоты. Молекулярная масса полимера обычно составляет от 1×103 до 5×106, предпочтительно от 1×104 до 1×106, и более предпочтительно от 5×104 до 5×105. Далее, терминальная структура полимера и катализатора для полимеризации для получения полимера может быть выбрана произвольно.
Предпочтительные примеры водорастворимого полимера, используемого в настоящем изобретении, включают полимер, содержащий N-виниловую циклическую лактамную единицу и водорастворимое производное целлюлозы.
Примеры полимера, имеющего N-виниловую циклическую лактамную единицу, включают гомополимеры или сополимеры, полученные путем полимеризации или сополимеризации N-винилпирролидона и N-винилкапролактама. Специфические примеры гомополимера включают поли(N-винил-2-пирролидон), поли(N-винил-5-метил-2-пирролидон), поли(N-винил-2-пиперидон), поли(N-винил-6-метил-2-пиперидон), поли(N-винил-ε-калролактам), и поли(N-винил-7-метил-ε-капролактам).
Далее, специфические примеры сополимера, описанного выше, включают сополимеры, полученные путем сополимеризации N-винилпирролидона, N-винилкапролактама, или тому подобного, например, с винилацетатом, сложным эфиром (мет)акриловой кислоты, сложным эфиром малеиновой кислоты, малеиновой кислотой, акрилонитрилом, стиролом, алкилвиниловым эфиром, N-винилимидазолом, винилпиридином, аллиловым спиртом, или олефинами. В настоящей заявке примеры сложного эфира включают алкиловые сложные эфиры, имеющие от 1 до 20 углеродных атомов, диметиламиноалкиловые сложные эфиры и их четвертичную соль, и гидроксиалкиловые сложные эфиры. В качестве основного полимера можно применять только один полимер, или можно применять два полимера в комбинации. Поливинилпирролидон является наиболее предпочтительным благодаря простоте производства и доступности.
Средняя молекулярная масса полимера, имеющего N-виниловую циклическую лактамную единицу, используемого в настоящем изобретении, не ограничивается конкретно, но как правило, составляет от 1×103 до 5×106, предпочтительно от 1×104 до 1×106, и более предпочтительно от 5×104 до 5×105. Далее, терминальная структура полимера и катализатор для полимеризации для получения полимера могут быть выбраны произвольно.
Далее, водорастворимое производное целлюлозы выбрано из группы, состоящей из гидроксипропилцеллюлозы, метилцеллюлозы, гидроксиэтилцеллюлозы, гидроксипропилметилцеллюлозы, карбоксиметилцеллюлозы натрия, и их смеси.
Среди них водорастворимое производное целлюлозы предпочтительно выбрано из группы, состоящей из гидроксипропилцеллюлозы, гидроксиэтилцеллюлозы, гидроксипропилметилцеллюлозы, и их смеси, и наиболее предпочтительно является гидроксипропилцеллюлозой.
Молекулярная масса водорастворимого производного целлюлозы, используемого в настоящем изобретении, не ограничивается конкретно, и например, вязкость, измеренная при концентрации 2% при 20°C, как правило, составляет от 1 до 10000 мПа⋅с, предпочтительно от 2 до 5000 мПа⋅с, и более предпочтительно от 2 до 4000 мПа⋅с.
В формованном пластинчатом продукте в соответствии с настоящим изобретением другие полимеры и другие соединения можно применять в комбинации, когда они не повреждают объект настоящего изобретения. Например, могут быть обеспечены сополимеры, смеси полимеров, или смеси соединений. Примеры соединения для встраивания включают фосфолипиды и сурфактанты.
Полимер, используемый в настоящем изобретении, предпочтительно имеет высокую чистоту, и в частности, количества остаточных веществ, таких как добавки, пластификатор, остаточный катализатор, остаточные мономеры, и остаточные растворители, используемые в процессе формования и последующей обработке, предпочтительно являются как можно более низкими. В особенности, при использовании в медицинской практике, содержание должно контролироваться до уровня ниже стандартов безопасности.
Средняя толщина формованного пластинчатого продукта в соответствии с настоящим изобретением составляет для формованного волокнистого продукта, как правило, от 10 до 1000 мкм, предпочтительно от 50 до 200 мкм, и более предпочтительно от 100 до 150 мкм. Когда толщина меньше этих значений, формованный пластинчатый продукт не может сохранять свою прочность, так что нельзя выполнить обрезку, что не является предпочтительным; в то время как если толщина больше этих значений, гибкость и/или гемостатическое свойство формованного пластинчатого продукта уменьшается, что не является предпочтительным. Когда формованный пластинчатый продукт является формованным пленочным продуктом, его средняя толщина составляет, как правило, от 5 до 200 мкм, и предпочтительно от 10 до 100 мкм.
Когда формованный пластинчатый продукт в соответствии с настоящим изобретением содержит фибриноген, то фибриноген предпочтительно находится в количестве в диапазоне от 0,05 до 30 мг/см2. Когда содержание фибриногена составляет менее 0,05 мг/см2, то эффект на основе свойства белка не проявляется; в то время как если его содержание выше 30 мг/см2, то формованный волокнистый продукт сам по себе становится ломким, что не является предпочтительным. Содержание предпочтительно составляет от 0,1 до 25 мг/см2, и более предпочтительно от 0,2 до 25 мг/см2. Кроме того, особенно когда формованный пластинчатый продукт является формованным пленочным продуктом, содержание фибриногена составляет 2 мг/см2 или меньше, предпочтительно 1,5 мг/см2 или меньше, и более предпочтительно 1,4 мг/см2 или меньше, с точки зрения гемостаза.
Когда формованный пластинчатый продукт в соответствии с настоящим изобретением содержит тромбин, содержание тромбина предпочтительно находится в диапазоне от 0,1 до 100 Ед/см2. Когда содержание тромбина составляет менее 0,1 Ед/см2, гемостатический эффект не проявляется; а когда содержание выше 100 Ед/см2, то формованный пластинчатый продукт становится ломким, что не является предпочтительным. Содержание предпочтительно составляет от 2 до 80 Ед/см2, и более предпочтительно от 5 до 50 Ед/см2.
Формованный волокнистый продукт в настоящем изобретении означает трехмерный формованный продукт, полученный путем ламинирования, тканья, вязания или обработки посредством других методик из одного или множества полученных волокон. Специфические примеры формованного волокнистого продукта включают нетканый материал. Кроме того, трубка, сетка и тому подобное, приготовленное из них, включено в формованный волокнистый продукт.
Когда формованный пластинчатый продукт в соответствии с настоящим изобретением является формованным волокнистым продуктом, предпочтительный средний диаметр волокна составляет от 0,01 до 50 мкм. Когда средний диаметр волокна меньше 0,01 мкм, формованный волокнистый продукт не может сохранять прочность, что не является предпочтительным. Далее, когда средний диаметр волокон больше 50 мкм, удельная площадь волокон снижается, и таким образом, растворимость гемостатического белка ухудшается, что не является предпочтительным. Более предпочтительно, средний диаметр волокна составляет от 0,02 до 30 мкм. В настоящей заявке диаметр волокна означает диаметр поперечного сечения волокна. Форма поперечного сечения волокна не ограничивается кругом, и может быть эллиптической или неправильной. В этом случае диаметр волокна рассчитывают в виде среднего значения длины эллипса в направлении главной оси и длины в направлении второстепенной оси. Когда поперечное сечение волокна не является ни круглым, ни эллиптическим, то диаметр волокна рассчитывают путем приближения к кругу или эллипсу.
Когда формованный пластинчатый продукт в соответствии с настоящим изобретением является формованным волокнистым продуктом, масса волокна на единицу площади (далее обозначаемая как METSUKE) предпочтительно составляет от 0,1 до 50 мг/см2. Когда величина METSUKE меньше 0,1 мг/см2, то гемостатический белок не может поддерживаться в достаточной степени, что не является предпочтительным. Далее, когда величина METSUKE больше 50 мг/см2, то возрастает вероятность индукции воспаления, что не является предпочтительным. Величина METSUKE более предпочтительно составляет от 0,2 до 20 мг/см2.
Когда формованный пластинчатый продукт в соответствии с настоящим изобретением является формованным волокнистым продуктом, то его объемная плотность предпочтительно составляет от 100 до 200 мг/см3. Когда объемная плотность ниже 100 мг/см3, нарушается способность к обработке, что не является предпочтительным. Далее, когда объемная плотность выше 200 мг/см3, поры в формованном волокнистом продукте уменьшаются, и гибкость и растворение гемостатического белка снижается, что не является предпочтительным.
Когда формованный пластинчатый продукт в соответствии с настоящим изобретением является формованным волокнистым продуктом, способ производства не ограничивается конкретно, и может быть использован любой способ, принятый для производства пластического волокна; однако, предпочтительно способ осуществляют путем формования раствора, так чтобы гемостатический белок или частицы, содержащие гемостатический белок, легко диспергировались, для предотвращения снижения активности гемостатического белка. Кроме того, формованный волокнистый продукт предпочтительно находится в форме филамента. Филамент специфически означает формованный волокнистый продукт, полученный без этапа резки волокон, во время процесса от прядения до обработки формованного волокнистого продукта, и может быть получен путем электропрядения, прядения из раствора, плавления с раздувом, и тому подобного, но предпочтительно применяют электропрядение.
Электропрядение является способом, при котором полимер растворяют в растворителе, и прилагают высокое напряжение к раствору до получения формованного волокнистого продукта на электроде. Способ включает этап растворения полимера в растворителе до получения раствора, этап приложения высокого напряжения к раствору, этап выталкивания раствора, и этап испарения растворителя из вытолкнутого раствора с получением формованного волокнистого продукта, и факультативный этап удаления электрического заряда с формованного волокнистого продукта, и этап накопления формованного волокнистого продукта путем удаления электрического заряда.
Этап получения прядильного сиропа в элекропрядении разъясняется. В качестве прядильного сиропа в настоящем изобретении предпочтительно применяют суспензию, состоящую из раствора субстратного полимера и частиц гемостатического белка.
Концентрация субстратного полимера в суспензии предпочтительно составляет от 1 до 30 масс. %. Когда концентрация полимера ниже 1 масс. %, трудно получать формованный волокнистый продукт, что не является предпочтительным. Далее, когда концентрация превышает 30 масс. %, то диаметр волокна полученного формованного волокнистого продукта увеличивается, и вязкость суспензии возрастает, что не является предпочтительным. Более предпочтительной концентрацией полимера в суспензии является 1,5-20 масс. %.
Растворитель для водорастворимого полимера не ограничивается конкретно, с тем условием, что растворитель может растворять водорастворимый полимер и формировать суспензию из частиц гемостатического белка, испаряется во время этапа прядения, и формирует волокно, и можно применять один растворитель или множество растворителей в комбинации. Примеры растворителя включают хлороформ, 2-пропанол, толуол, бензол, бензиловый спирт, дихлорметан, тетрахлорид углерода, циклогексан, циклогексанон, трихлорэтан, метилэтилкетон, этил ацетат, ацетон, этанол, метанол, тетрагидрофуран, 1,4-диоксан, 1-пропанол, фенол, пиридин, уксусную кислоту, муравьиную кислоту, гексафтор-2-пропанол, гексафторацетон, N,N-диметилформамид, N,N-диметилацетамид, ацетонитрил, N-метил-2-пирролидинон, N-метилморфолин-N-оксид, 1,3-диоксолан, воду, и смеси из этих растворителей. Среди них дихлорметан, хлороформ, 2-пропанол, этанол и N,N-диметилформамид являются предпочтительными с точки зрения возможности обработки, физических свойств, и тому подобного.
Растворители для растворения алифатического полиэфира не ограничиваются конкретно, с тем условием, что растворитель, способный растворять алифатический полиэфир и формировать суспензию с частицами гемостатического белка, испаряется во время этапа прядения, и формирует волокно, и можно применять один растворитель или множество растворителей в комбинации. Примеры растворителя включают хлороформ, 2-пропанол, толуол, бензол, бензиловый спирт, дихлорметан, тетрахлорид углерода, циклогексан, циклогексанон, трихлорэтан, метилэтилкетон, этил ацетат, и смеси из этих растворителей. Далее, такие растворители, как ацетон, этанол, метанол, тетрагидрофуран, 1,4-диоксан, 1-пропанол, фенол, пиридин, уксусная кислота, муравьиная кислота, гексафтор-2-пропанол, гексафторацетон, N,N-диметилформамид, N,N-диметилацетамид, ацетонитрил, N-метил-2-пирролидинон, N-метилморфолин-N-оксид, 1,3-диоксолан могут содержаться, когда формируется эмульсия. Среди них дихлорметан и этанол являются предпочтительными с точки зрения возможности обработки и физических свойств.
Способы приготовления такой суспензии не ограничиваются конкретно, и можно применять ультразвуковой и другие способы перемешивания. В качества способа перемешивания можно применять высокоскоростное перемешивание, такое как с помощью гомогенизатора, и способы перемешивания с применением дезинтегратора, шаровой мельницы, или тому подобного. Среди них предпочтительным является способ диспергирования с применением ультразвуковой обработки.
Далее, прядильный сироп можно приготовить путем получения суспензии с растворителем и частицами гемостатического бежа, с последующим добавлением водорастворимого полимера или алифатического полиэфира.
Кроме того, перед приготовлением суспензии частицы гемостатического бежа можно подвергнуть очистительной обработке. Очистительная обработка включает сухое измельчение и влажное измельчение, и можно применять оба способа, и комбинацию этих способов в настоящем изобретении. Обработка сухим измельчением включает обработку с применением шаровой мельницы, обработку с применением планетарной мельницы или вибрационной мельницы, обработку измельчением в ступке с пестиком, с пульверизатором с перемешиванием среды, с ударной мельницей тонкого помола, такой как молотковая мельница, струйная мельница; и измельчительную обработку с применением точильного камня. Обработка влажным измельчением включает обработку, в которой гемостатический белок, диспергированный в подходящей дисперсионной среде, перемешивают с применением перемешивающего устройства с высоким сдвиговым усилием, пластикатора, или тому подобного; обработку дисперсии в среде шаровой мельницей, и бисерной мельницей. Далее, можно также применять частицы гемостатического белка, приготовленные с применением распылительной сушки.
Далее описан этап приложения высокого напряжения к раствору, этап выталкивания раствора, и этап испарения растворителя из вытолкнутого раствора с получением формованного волокнистого продукта.
В способе производства формованного волокнистого продукта в соответствии с настоящим изобретением высокое напряжение должно прилагаться к суспензии для выталкивания суспензии, состоящей из раствора полимера и частиц гемостатического белка, с получением формованного волокнистого продукта. Способ приложения напряжения не ограничивается конкретно, если способ позволяет выталкивать суспензию с получением формованного волокнистого продукта; однако способ включает способ, в котором электрод погружают в раствор для приложения напряжения, и способ, в котором напряжение прилагают к форсунке, выталкивающей раствор.
Кроме того, вспомогательный электрод может быть обеспечен в дополнение к электроду, прилагающему напряжение к раствору. Значение прилагаемого напряжения не ограничивается конкретно, если может быть получен формованный волокнистый продукт, но как правило, предпочтительно находится в диапазоне от 5 до 50 кВ. При приложении напряжения ниже 5 кВ прядильный раствор не выталкивается, так что не образуется формованный волокнистый продукт, что не является предпочтительным; а когда прилагаемое напряжение превышает 50 кВ, возникает электрический разряд от электрода к заземлителю, что не является предпочтительным. Более предпочтительно, напряжение находится в диапазоне от 10 до 30 кВ. Необходимый потенциал может быть создан путем подходящего способа.
Соответственно, немедленно после выталкивания суспензии, состоящей из раствора полимера и частиц гемостатического белка, растворитель испаряется с получением формованного волокнистого продукта. Прядение, как правило, проводят при атмосферном давлении и комнатной температуре, но его можно проводить при отрицательном давлении, когда испарение является недостаточным, или в атмосфере при высокой температуре. Кроме того, температура прядения зависит от характеристик испарения растворителя и от вязкости прядильного раствора, но как правило, находится в диапазоне от 0 до 50°C.
Далее описан этап, в котором формованный волокнистый продукт обрабатывают для удаления электрического заряда и накапливают. Способ удаления электрического заряда из формованного волокнистого продукта и накопления волокнистого продукта не ограничен конкретно, но его примеры включают способ, в котором формованный волокнистый продукт собирают на заземлителе для удаления электрического заряда и накапливают одновременно. Способ, в котором электрический заряд удаляют перед накоплением, использующий ионизатор и тому подобное, также включен. В этом случае способ накопления формованного волокнистого продукта не ограничивается конкретно, но общие способы включают способ, в котором электростатическую силу гасят путем удаления электрического заряда, где формованный волокнистый продукт падает за счет собственного веса, а затем накапливается. Далее, когда необходимо, можно применять способ, в котором формованный волокнистый продукт, где электростатическая сила удалена, засасывается и накапливается на сетке; способ, в котором воздух переносится в аппарат для накопления на сетке, или тому подобный. Ионизатор, используемый в настоящей заявке, означает аппарат, в котором ионы генерируются встроенным генератором ионов, и ионы выгружаются на заряженный материал, чтобы вызвать удаление электрического заряда заряженного материала. Примеры предпочтительного генератора ионов, составляющего ионизатор, используемый в способе получения формованного волокнистого продукта в соответствии с настоящим изобретением, включают аппарат, который генерирует ионы путем приложения высокого напряжения к встроенной выводной игле.
Такие способы электропрядения известны, и аппараты или условия не ограничиваются, если можно приготовить формованный волокнистый продукт в соответствии с настоящим изобретением. Однако в дополнение к примерам, приведенным ниже, можно упомянуть то, что изложено, например, в Международной публикации № WO 2004/072336, описание, и Международной публикации №2005/087988, описание.
Когда формованный пластинчатый продукт в соответствии с настоящим изобретением является формованным пленочным продуктом, любой способ, обычно применяемый в качестве способа производства пленки, можно применять для получения продукта. Примеры способа включают литье. Такое формование можно проводить путем формования расплава, а также формования раствора; однако для предотвращения снижения активности гемостатического белка предпочтительным является формование раствора, чтобы гемостатический белок легко диспергировался.
Далее описан ламинированный формованный пластинчатый продукт в соответствии с настоящим изобретением.
Ламинированный формованный пластинчатый продукт в соответствии с настоящим изобретением содержит первый слой полимерной композиции, содержащий фибриноген и водорастворимый полимер, и второй слой полимерной композиции, содержащий тромбин и алифатический полиэфир.
Водорастворимый полимер выбран из производного целлюлозы, полимера, содержащего N-виниловую циклическую лактамную единицу, полиэтиленоксида, поливинилового спирта, гиалуроновой кислоты, декстрана, пуллулана или крахмала, или их смеси.
Водорастворимый полимер предпочтительно является производным целлюлозы или полимером, содержащим N-виниловую циклическую лактамную единицу, или предпочтительно, их смесью.
Специфическими примерами производного целлюлозы являются производные, выбранные из группы, состоящей из гидроксипропилцеллюлозы, метилцеллюлозы, гидроксиэтилцеллюлозы, гидроксипропилметилцеллюлозы, и карбоксиметилцеллюлозы натрия, и их смеси.
Среди них, производное целлюлозы предпочтительно выбрано из группы, состоящей из гидроксипропилцеллюлозы, гидроксиэтилцеллюлозы, гидроксипропилметилцеллюлозы, поливинилпирролидона, и их смеси, и наиболее предпочтительно, гидроксипропилцеллюлозы или поливинилпирролидона.
Далее, средняя молекулярная масса полимера, содержащего N-виниловую циклическую лактамную единицу, в качестве водорастворимого полимера, не ограничивается конкретно, но составляет от ×103 до 5×106, предпочтительно от 1×104 до 1×106, и более предпочтительно от 5×104 до 5×105. Кроме того, терминальная структура полимера и катализатора для полимеризации полимера может быть выбрана произвольно.
Вязкость производного целлюлозы в качестве водорастворимого полимера, измеренная при концентрации 2% при 20°C, предпочтительно составляет от 0,01 до 10000 мПа⋅с, более предпочтительно от 0,1 до 5000 мПа⋅с, еще более предпочтительно от 0,1 до 1000 мПа⋅с, и наиболее предпочтительно от 0,1 до 100 мПа⋅с.
Другие полимеры и другие соединения можно применять в комбинации с водорастворимым полимером, когда они не нарушают объект из настоящего изобретения. Например, можно упомянуть сополимеры, смеси полимеров или сложную смесь.
Такой водорастворимый полимер предпочтительно имеет высокую чистоту, и в частности, количества пластификатора, содержащегося в полимере, остаточного катализатора, остаточного мономера, и остаточных веществ, таких как остаточные растворители, использованные для формования и последующей обработки, предпочтительно являются низкими. В особенности, когда продукт применяют в медицинской практике, количества остаточных веществ должны контролироваться до уровня ниже стандартов безопасности.
Далее, слой, состоящий из водорастворимого полимера и фибриногена, может дополнительно содержать фармацевтически пригодные добавки. Примеры таких добавок могут включать добавки, описанные выше, в пояснении к формованному пластинчатому продукту. В частности, когда фибриноген является частицами, имеющими средний диаметр от 0,01 до 100 мкм, эти добавки предпочтительно добавляют в частицы.
В качестве алифатического полиэфира также можно применять то, что описано выше в пояснении к формованному пластинчатому продукту.
Другие полимеры и другие соединения можно применять в комбинации с алифатическим полиэфиром, если они не нарушают объект настоящего изобретения. Например, можно упомянуть сополимеры, смеси полимеров или сложную смесь.
Такой алифатический полиэфир предпочтительно имеет высокую чистоту, и в частности, количества добавок, содержащихся в полимере, остаточного катализатора, остаточного мономера, и остаточных веществ, таких как остаточные растворители, использованные для формования и последующей обработки, предпочтительно являются низкими. В особенности, когда продукт применяют в медицинской практике, количества остаточных веществ должны контролироваться до уровня ниже стандартов безопасности.
Далее, слой, состоящий из алифатического полиэфира и тромбина, может дополнительно содержать фармацевтически пригодные добавки. Примерами таких добавок могут быть одна или несколько добавок, выбранных из группы, состоящей из многоатомных спиртов, олигосахаридов, хлорида натрия, цитрата натрия, и хлорида кальция. Это может приводить к улучшению стабильности и растворимости тромбина, гибкости, и тому подобному.
Первый слой полимерной композиции, состоящий из водорастворимого полимера и фибриногена, предпочтительно состоит из формованного волокнистого продукта или пленки. Формованный волокнистый продукт, используемый в настоящей заявке, означает трехмерный формованный продукт, приготовленный путем ламинирования, тканья, вязания или обработки посредством других методик из одного или множества полученных волокон. Специфические примеры формованного волокнистого продукта включают нетканый материал. Кроме того, трубка, сетка и тому подобное, приготовленные из него, включены в формованный волокнистый продукт.
Пленка может быть произведена любым обычно используемым способом. Примером способа является литье. Такое формование можно проводить путем формования расплава, а также формования раствора; однако, для предотвращения снижения активности гемостатического белка предпочтительно формование раствора, так чтобы гемостатический белок легко диспергировался.
Средний диаметр волокон формованного волокнистого продукта, состоящего из водорастворимого полимера и фибриногена, составляет от 0,01 до 50 мкм. Когда средний диаметр волокон составляет менее 0,01 мкм, формованный волокнистый продукт не может сохранять прочность, что не является предпочтительным. Далее, когда средний диаметр волокон составляет более 50 мкм, удельная площадь волокон снижается, поэтому растворимость гемостатического белка ухудшается, что не является предпочтительным. Более предпочтительно, средний диаметр волокон составляет от 0,02 до 30 мкм. В настоящей заявке диаметр волокон означает диаметр поперечного сечения волокна. Форма поперечного сечения волокна не ограничивается круглой, и может быть эллиптической или неправильной. В этом случае диаметр волокна рассчитывают как среднее значение от длины эллипса в направлении основной оси, и длины в направлении второстепенной оси. Когда поперечное сечение волокна не является ни круглым, ни эллиптическим, диаметр волокна рассчитывают путем приближения к кругу или эллипсу.
Средняя толщина ламинированного формованного пластинчатого продукта в соответствии с настоящим изобретением предпочтительно составляет от 50 до 350 мкм, более предпочтительно от 100 до 300 мкм, и еще более предпочтительно от 100 до 250 мкм.
Значение METSUKE формованного волокнистого продукта, состоящего из водорастворимого полимера и фибриногена, предпочтительно составляет от 0,1 до 50 мг/см2. Когда значение METSUKE меньше 0,1 мг/см2, фибриноген не может поддерживаться в достаточной степени, что не является предпочтительным. Также, когда значение METSUKE больше 50 мг/см2, возможность индукции воспаления повышается, что не является предпочтительным.
Объемная плотность формованного волокнистого продукта, состоящего из водорастворимого полимера и фибриногена, предпочтительно составляет от 100 до 200 мг/см3. Когда объемная плотность ниже 100 мг/см3, нарушается возможность обработки, что не является предпочтительным. Далее, когда объемная плотность выше 200 мг/см3, уменьшаются поры в формованном волокнистом продукте, снижая гибкость и растворение гемостатического белка, что не является предпочтительным.
Формованный волокнистый продукт, состоящий из водорастворимого полимера и фибриногена, как правило, содержит фибриноген в количестве в диапазоне от 0,05 до 30 мг/см2. Когда содержание фибриногена ниже 0,05 мг/см2, гемостатический эффект не проявляется, а когда содержание выше 30 мг/см2, формованный волокнистый продукт как таковой становится ломким, что не является предпочтительным. Содержание предпочтительно составляет от 0,1 до 25 мг/см2, и более предпочтительно от 0,2 до 25 мг/см2. Кроме того, особенно когда формованный пластинчатый продукт является формованным пленочным продуктом, с точки зрения гемостаза, содержание фибриногена составляет 2 мг/см2 или меньше, предпочтительно 1,5 мг/см2 или меньше, и более предпочтительно 1,4 мг/см2 или меньше.
Формованный волокнистый продукт, состоящий из водорастворимого полимера и фибриногена, предпочтительно находится в форме филамента. Филамент специфически означает формованный волокнистый продукт, полученный без этапа обрезки волокон, во время процесса от прядения до обработки формованного волокнистого продукта, и может быть получен путем электропрядения, прядения из раствора, плавления с раздувом, и тому подобного, но предпочтительно применяют электропрядение.
С электропрядением диаметр порошка фибриногена предпочтительно находится в диапазоне от 0,01 до 100 мкм, когда суспензию готовят путем смешивания водорастворимого полимера и порошка фибриногена, описанных в разъяснении к формованному пластинчатому продукту, приведенному выше. Технически трудно приготовить частицы, имеющие диаметр менее 0,01 мкм, а когда диаметр частицы больше 100 мкм, диспергируемость ухудшается, и формованный волокнистый продукт становится ломким и трудно обрабатываемым, что не является предпочтительным.
Пленку, состоящую из водорастворимого полимера и фибриногена, можно получить любым способом, который обычно применяют. Примером способа является литье. Такое формование можно проводить путем формования расплава, а также формования раствора; однако для предотвращения снижения активности гемостатического белка, предпочтительным является формование раствора, чтобы гемостатический белок легко диспергировался.
Содержание водорастворимого полимера в пленке, состоящей из водорастворимого полимера и фибриногена, предпочтительно составляет от 0,1 до 50 масс. %, и более предпочтительно от 0,5 до 20 масс. %, хотя это зависит от типа полимера. Кроме того, белок-содержащие частицы фибриногена присутствуют, как правило, в количестве 100 масс. % или больше, предпочтительно 500 масс. % или больше, и еще более предпочтительно, 800-950 масс. %, на основе водорастворимого полимера. Когда содержание ниже этих значений, гемостатическое свойство может ухудшаться, а когда содержание выше этих значений, формуемость пленки может ухудшаться.
Средняя толщина пленки, состоящей из водорастворимого полимера и фибриногена, предпочтительно составляет от 10 до 1000 мкм.
Пленка, состоящая из водорастворимого полимера и фибриногена, предпочтительно содержит фибриноген в количестве в диапазоне от 0,05 до 10 мг/см2. Когда содержание фибриногена составляет меньше 0,05 мг/см2, гемостатический эффект не проявляется, а когда содержание больше 10 мг/см2, пленка как таковая становится ломкой, что не является предпочтительным. Содержание более предпочтительно составляет от 0,1 до 8 мг/см2, и боле предпочтительно от 0,2 до 4 мг/см2.
В настоящем изобретении второй слой полимерной композиции, состоящий из алифатического полиэфира и тромбина, предпочтительно состоит из формованного волокнистого продукта. Определение формованного волокнистого продукта дано выше.
Средний диаметр волокна формованного волокнистого продукта, состоящего из алифатического полиэфира и тромбина, составляет от 0,01 до 50 мкм. Когда средний диаметр волокна меньше 0,01 мкм, формованный волокнистый продукт не может сохранять прочность, что не является предпочтительным. Кроме того, когда средний диаметр волокна больше 50 мкм, удельная площадь поверхности волокна становится маленькой, и таким образом, высвобождение тромбина нарушается, что не является предпочтительным. Более предпочтительно, средний диаметр волокна составляет от 0,02 до 30 мкм.
Средняя толщина формованного волокнистого продукта, состоящего из алифатического полиэфира и тромбина, составляет от 10 до 1000 мкм. Когда средняя толщина меньше 10 мкм, формованный волокнистый продукт не может сохранять прочность, так что нельзя выполнить обрезку, что не является предпочтительным. Кроме того, когда толщина больше 1000 мкм, гибкость и/или гемостатическое свойство формованного пластинчатого продукта снижается, что не является предпочтительным. Средняя толщина более предпочтительно составляет от 20 до 500 мкм.
Значение METSUKE формованного волокнистого продукта, состоящего из алифатического полиэфира и тромбина, предпочтительно составляет от 0,1 до 50 мг/см2. Когда значение METSUKE меньше 0,1 мг/см2, тромбин не может поддерживаться в достаточной степени, что не является предпочтительным. Также, когда значение METSUKE больше 50 мг/см2, возможность индукции воспаления повышается, что не является предпочтительным. Значение METSUKE более предпочтительно составляет от 0,2 до 20 мг/см2.
Объемная плотность формованного волокнистого продукта, состоящего из алифатического полиэфира и тромбина, предпочтительно составляет от 100 до 200 мг/см3. Когда объемная плотность ниже 100 мг/см3, нарушается возможность обработки, что не является предпочтительным. Далее, когда объемная плотность выше 200 мг/см3, уменьшаются поры в формованном волокнистом продукте, снижая гибкость и высвобождение гемостатического белка, что не является предпочтительным.
В настоящем изобретении формованный волокнистый продукт, состоящий из алифатического полиэфира и тромбина, предпочтительно содержит тромбин в количестве от 0,1 до 100 Ед/см2. Когда содержание тромбина ниже 0,1 Ед/см2, гемостатический эффект является недостаточным, что не является предпочтительным. Когда содержание выше 100 Ед/см2, формованный волокнистый продукт как таковой становится ломким, что не является предпочтительным. Содержание предпочтительно составляет от 2 до 80 Ед/см2, и более предпочтительно от 5 до 50 Ед/см2. Белок-содержащие частицы тромбина присутствуют, как правило, в количестве от 1 до 20 масс. %, предпочтительно от 10 до 100 масс. %, более предпочтительно от 20 до 100 масс. %, и еще более предпочтительно от 50 до 100 масс. %, на основе алифатического полиэфира. Когда содержание белок-содержащих частиц ниже этого значения, растворение тромбина из формованного пластинчатого продукта и гибкость или гемостатическое свойство формованного пластинчатого продукта могут ухудшаться; в то время как когда содержание выше этого значения, самоподдерживающее свойство формованного пластинчатого продукта как такового снижается, что не является предпочтительным.
Формованный волокнистый продукт, состоящий из алифатического полиэфира и тромбина, предпочтительно находится в форме филамента. Значение и способ производства филамента описаны выше.
Такой формованный волокнистый продукт, состоящий из алифатического полиэфира и тромбина, можно получить с помощью способа электропрядения. Способ электропрядения является таким, как описан для формованного пластинчатого продукта выше. Когда алифатический полиэфир и порошок тромбина смешивают для приготовления суспензии, диаметр частиц порошка тромбина не ограничивается конкретно, но предпочтительно находится в диапазоне от 0,01 до 100 мкм. Технически трудно приготовить порошок тромбина диаметром частиц меньше 0,01 мкм, а когда диаметр частиц порошка тромбина больше 100 мкм, диспергируемость ухудшается, и формованный волокнистый продукт становится ломким, что не является предпочтительным.
Обработку, такую как дополнительное ламинирование хлопко-подобной волокнистой структуры на поверхности формованного пластинчатого продукта в соответствии с настоящим изобретением, или на поверхности каждого слоя ламинированного формованного пластинчатого продукта, и помещение хлопкоподобной структуры между слоями ламинированного формованного пластинчатого продукта в соответствии с настоящим изобретением с целью получения многослойной структуры, можно проводить произвольно, с тем условием, чтобы это не нарушало объект настоящего изобретения.
Лекарственное средство может факультативно содержаться внутри волокон формованного волокнистого продукта из формованного пластинчатого продукта и ламинированного формованного пластинчатого продукта в соответствии с настоящим изобретением. Когда электропрядение используют для формования, любое лекарство можно применять, без конкретного ограничения, если лекарство является растворимым в органическом растворителе или водном растворе, и не теряет своей физиологической активности при растворении.
Ламинированный формованный пластинчатый продукт в соответствии с настоящим изобретением состоит из одного или нескольких слоев первой полимерной композиции, состоящей из водорастворимого полимера и фибриногена, и одного или нескольких слоев второй полимерной композиции, состоящей из алифатического полиэфира и тромбина; однако можно дополнительно применять иные слои, чем эти. Порядок ламинирования этих слоев не ограничен, и подобные слои могут быть рядом друг с другом в некоторых частях.
В ламинированном формованном пластинчатом продукте в соответствии с настоящим изобретением слой первой полимерной композиции, состоящей из водорастворимого полимера и фибриногена, и слой второй полимерной композиции, состоящей из алифатического полиэфира и тромбина, могут быть наложены друг на друга, и слой может быть дополнительно ламинирован с помощью общего способа нанесения покрытия на любой из формованных слоев. Могут выполняться такие способы, как электропрядение, электрораспыление, литье, погружение, выталкивание, прессование, и тремопрессование. В частности, в качестве способа ламинирования слоя, состоящего из формованного волокнистого продукта, предпочтительным является способ электропрядения. Формованный волокнистый продукт, состоящий из формованного волокна алифатического полиэфира и тромбина, может быть ламинирован на формованном волокнистом продукте, состоящем из водорастворимого полимера и фибриногена, или формованный волокнистый продукт, состоящий из водорастворимого полимера и фибриногена, ламинируют на формованном волокнистом продукте, состоящем из алифатического полиэфира и тромбина.
Когда ламинированный формованный пластинчатый продукт в соответствии с настоящим изобретением наносят на раневой участок в качестве гемостатического материала, предпочтительно, чтобы слой, состоящий из водорастворимого полимера и фибриногена, находился в контакте с раневым участком. Это позволяет слою, состоящему из водорастворимого полимера и фибриногена, начинать растворяться, как только слой, состоящий из водорастворимого полимера и фибриногена, приходит в контакт с раневым участком, так чтобы фибриноген в достаточной степени проникал в рану; а затем тромбин немедленно высвобождался из слоя, состоящего из алифатического полиэфира и тромбина, так чтобы проходила реакция коагуляции, приводящая к образованию фибрина. Здесь, после того, как алифатический полиэфир в слое, состоящем из алифатического полиэфира и тромбина, функционирует в качестве укрепляющего элемента, необходимого для остановки кровотечения, полиэфир разрушается со временем.
Формованный пластинчатый продукт и ламинированный формованный пластинчатый продукт в соответствии с настоящим изобретением является тонким и обладает отличной гибкостью, и таким образом, обеспечивает хорошее адгезивное свойство для раневого участка. Кроме того, поскольку формованный пластинчатый продукт и ламинированный формованный пластинчатый продукт в соответствии с настоящим изобретением содержат активные ингредиенты, фибриноген и/или тромбин в формованном волокнистом продукте, поддерживающие характеристики являются отличными, в отличие от лиофилизированных продуктов. В то же самое время, поскольку растворимость фибриногена и высвобождение и растворение в фибриногеновом слое тромбина являются превосходными, гемостатический эффект проявляется за короткое время. Поскольку гемостатический эффект проявляется за короткое время, необходимое количество фибриногена мало, так что продукт также обладает отличными характеристиками по затратам. Формованный пластанчатый продукт в соответствии с настоящим изобретением обладает отличной различимостью в раневом участке после нанесения на раневой участок путем выбора используемого материала. Благодаря этому, поскольку можно подтвердить гемостатическое состояние визуально, хотя это было трудно до настоящего времени, можно легко определить участок, который следует зашивать, в случае, если требуется шов. Далее, поскольку не требуется этап лиофилизации для производства формованного пластинчатого продукта и ламинированного формованного пластинчатого продукта в соответствии с настоящим изобретением, производительность является отличной.
Примеры
Варианты осуществления настоящего изобретения далее разъясняются со ссылкой на примеры, но эти примеры не ограничивают объем настоящего изобретения. Способы анализа для примеров 1-6 и 16-29 и сравнительных примеров 1 и 2
1А. Диаметр частиц белка (средний диаметр частиц)
Лиофилизированный порошок фибриногена, измельченный в ступке, фотографировали с увеличением ×1000 с применением цифрового микроскопа (KEYENCE Corporation: торговое наименование «VHX-100»), произвольно выбирали 10 частиц на фотографии и измеряли диаметр, и полученное среднее значение использовали в качестве среднего диаметра частиц.
2А. Средний диаметр волокон
Поверхность полученного формованного волокнистого продукта фотографировали с увеличением ×3000 с применением сканирующего электронного микроскопа (KEYENCE Corporation: торговое наименование «VE8800»), и произвольно выбирали 20 участков на фотографии, на которых определяли диаметр волокон для всех волокон, и полученное среднее значение использовали в качестве среднего диаметра волокон. n=20.
3А. Средняя толщина.
Измеряли толщину полученной пленки формованного волокнистого продукта (n=15) с применением высокоточного цифрового измерительного инструмента (Mitutoyo Corporation: торговое наименование «Litematic VL-50») при мощности измерения 0,01 N, и рассчитывали среднюю толщину пленки. При этом измерении использовали минимальную возможную мощность измерения для прибора.
4A. METSUKE (масса волокна на единицу площади).
Полученный формованный волокнистый продукт нарезали на куски размером 50 мм × 100 мм и взвешивали, и массу преобразовывали в METSUKE.
5А. Объемная плотность
Объемную плотность рассчитывали из значения METSUKE, определенного, как описано выше, и средней толщины.
6А. Анализ растворения.
Полученный формованный волокнистый продукт нарезали на куски 1 см × 1 см, и добавляли 15 мкл обычного солевого раствора к кусочку для подтверждения растворимости.
7А. Иммуноферментный анализ
(1) Фибриноген
На планшете для ИФА (N UNC 468667), фиксировали антитела к фибриногену человека (DAKO А0080) при 10 мкг/мл. После отмывания ФБР, содержащим 0,05% Твин 20, в каждую лунку добавляли Block Асе (DS Pharma Biomedical Co., Ltd., UK-B80) для блокирования неспецифического связывания. После промывания ФБР, содержащим 0,05% Твин 20, добавляли образец. Человеческий фибриноген (Enzyme Research Laboratories No. FIB3) использовали в качестве эталона для получения калибровочной кривой. После промывания ФБР, содержащим 0,05% Твин 20, добавляли антитела к фибриногену человека, меченые пероксидазой хрена (CPL5523), и проводили реакцию в смеси, а затем реакционную смесь промывали ФБР, содержащим 0,05% Твин 20. Затем добавляли ТМБ (тетраметилбензидин) реагент (KPL 50-76-02 50-65-02), и смесь выдерживали в течение 6 минут для развития окраски. Добавляли 1 М Н3РО4 для прекращения развития окраски, и измеряли ОП в диапазоне от 450 до 650 нм посредством ридера микропланшетов.
(2) Тромбин
В планшете для ИФА (N UNC 468667) антитела к тромбину человека (Affinity Biologicals Inc., No. SAHT-AP) фиксировали при 5 мкг/мл. После промывания ФБР, содержащим 0,05% Твин 20, в каждую лунку добавляли Block Асе (DS Pharma Biomedical Co., Ltd., UK-B80) для блокирования неспецифического связывания. После промывания ФБР, содержащим 0,05% Твин 20, добавляли образец. Человеческий тромбин (Haematologic Technologies, Inc.: НСТ-0020) использовали в качестве эталона для получения калибровочной кривой. После промывания ФБР, содержащим 0,05% Твин 20, добавляли антитела к тромбину человека, меченые пероксидазой хрена (Affinity Biologicals Inc., No. SAHT-HRP), в концентрации 0,1 мкг/мл. После реакции смесь промывали ФБР, содержащим 0,05% Твин 20, добавляли ТМБ реагент (DAKO S1599), и смесь выдерживали в течение 10 минут для развития окраски. Добавляли 0,5 М H2SO4 для прекращения развития окраски, и определяли ОП в диапазоне от 450 до 650 нм посредством ридера для микропланшетов.
8А. Измерение активности тромбина.
В 2008 пробирку Falcon добавляли 20 мкл образца, 60 мкл буферного раствора, содержащего 50 мМ Трис-HCl (pH 8,5)+50 мМ NaCl, и 20 мкл 0,1% PLURONIC F-68, и смесь инкубировали при at 37°C в течение 3 минут. В качестве эталона использовали очищенный α-тромбин, выделенный из плазмы человека (от Haematologic Technologies, Inc.: НСТ-0020), разбавленный тем же самым буферным раствором до 5; 2,5; 1,25; 0,625 и 0,3215 Ед/мл. К каждому из этих реакционных растворов добавляли 100 мкл хромогенного субстрата Testzym S-2238 (1 мМ: Daiichi Kagaku Yakuhin Kogyo), и смесь перемешивали и проводили реакцию при 37°C в течение 5 минут, а затем добавляли 800 мкл 0,1 М раствора лимонной кислоты для остановки реакции. 200 мкл реакционного раствора переносили в 96-луночный планшет, и измеряли ОП в диапазоне от 450 до 650 нм.
Пример 1
Порошок лиофилизированного фибриногена (BOLHEAL (зарегистрированная торговая марка, то же самое применяется ниже) для средства адгезии тканей: флакон 1) измельчали в ступке до получения измельченного порошка лиофилизированного фибриногена, имеющего средний диаметр частиц 14 мкм. После диспергирования измельченного порошка лиофилизированного фибриногена в этаноле, растворяли поливинилпирролидон (K90, Wako Pure Chemical Industries, Ltd.) до получения 10 масс. %, до получения прядильного сиропа порошка лиофилизированного фибриногена/поливинилпирролидона = 100/100 (м/м). Проводили прядение при температуре 22°C и влажности 26% или ниже посредством способа электропрядения, до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 13,5 кВ, скорость потока прядильного сиропа составила 12 мл/ч, а расстояние между выводной форсункой и пластиной составило 15 см. Средний диаметр волокна формованного волокнистого продукта составил 0,51 мкм, средняя толщина 285 мкм, METSUKE 2,35 мг/см2, и объемная плотность 82 мг/см3. Полученный формованный волокнистый продукт подвергали анализу растворимости, и он растворялся в пределах 1 секунды. Далее, полученную пластину нарезали кусками 0,5×0,5 см, белок экстрагировали с применением 62,5 мкл нормального солевого раствора, и проводили ИФА. Результаты показали, что количество фиксированного белка составило 0,54 мг/см2. Полученную пластину можно было разрезать ножницами.
Пример 2
После диспергирования порошка лиофилизированного фибриногена в примере 1, растворяли поливинилпирролидон (K90, Wako Pure Chemical Industries, Ltd.) до получения 10 масс. %, для приготовления прядильного сиропа порошка лиофилизированного фибриногена/поливинилпирролидона = 100/200 (м/м). Прядение проводили при температуре 22°C и влажности 26% или ниже посредством способа электропрядения, до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 17 кВ, скорость потока прядильного сиропа составила 1,2 мл/ч, а расстояние между выводной форсункой и пластиной составило 15 см. Средний диаметр волокна формованного волокнистого продукта составил 0,33 мкм, средняя толщина 469 мкм, METSUKE 5,28 мг/см2, и объемная плотность 113 мг/см3. Полученный формованный волокнистый продукт подвергали анализу растворимости, и он растворялся в пределах 1 секунды. Далее, полученную пластину нарезали кусками 0,5×0,5 см, белок экстрагировали с применением 62,5 мкл нормального солевого раствора, и проводили ИФА. Результаты показали, что количество фиксированного белка составило 1,61 мг/см2. Полученную пластину можно было разрезать ножницами.
Пример 3
После диспегирования порошка лиофилизированного фибриногена из примера 1 в 2-пропаноле, растворяли гидроксипропилцеллюлозу (6-10 мПа⋅с, Wako Pure Chemical Industries, Ltd.) до получения 16 масс. %, для приготовления прядильного сиропа порошка лиофилизированного фибриногена/гидроксипропилцеллюлозы = 20/100 (м/м). Прядение проводили при температуре 22°C и влажности 26% или ниже посредством способа электропрядения, до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 11 кВ, скорость потока прядильного сиропа составила 1,2 мл/ч, а расстояние между выводной форсункой и пластиной составило 15 см. Средний диаметр волокна формованного волокнистого продукта составил 0,86 мкм, средняя толщина 137 мкм, METSUKE 1,59 мг/см2, и объемная плотность 116 мг/см3. Полученный формованный волокнистый продукт подвергали анализу растворимости, и он растворялся в пределах 1 секунды. Далее, полученную пластину нарезали кусками 0,5×0,5 см, белок экстрагировали с применением 62,5 мкл нормального солевого раствора, и проводили ИФА. Результаты показали, что количество фиксированного белка составило 0,17 мг/см. Полученную пластину можно было разрезать ножницами.
Сравнительный пример 1
Измельченный лиофилизированный порошок фибриногена из примера 1 растворяли в 1,1,1,3,3,3-гексафтор-2-пропаноле/минимальной эссенциальной среде Игла Sigma-Aldrich Co. LLC.) 10×(9/1=о/о) до получения 15 м/о %. Прядение проводили при температуре 22°C и влажности 26% или ниже, посредством способа электропрядения, до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 23,5 кВ, скорость потока прядильной жидкости составила 2,45 мл/ч, а расстояние между выводной форсункой и пластиной составило 12 см. Полученный формованный волокнистый продукт подвергали анализу растворимости, и он не растворялся.
Сравнительный пример 2
После растворения порошка лиофилизированного фибриногена в растворе для растворения фибриногена (оба содержались в BOLHEAL для средства адгезии тканей) гидроксипропилцеллюлозу (6-10 мПа⋅с, Wako Pure Chemical Industries, Ltd.) растворяли до получения 16 масс. %, для приготовления прядильного сиропа порошка лиофилизированного фибриногена/гидроксипропилцеллюлозы = 20/100 (о/о); однако, отмечалось разделение фаз между гидроксипропилцеллюлозой и фибриногеном, и фибриноген осаждался, так что нельзя было провести электропрядение.
Пример 4
После диспергирования измельченного порошка лиофилизированного фибриногена из примера 1 в 2-пропаноле, гидроксипропилцеллюлозу (6-10 мПа⋅с, Wako Pure Chemical Industries, Ltd.) растворяли до получения 16 масс. %, для приготовления прядильного раствора порошка лиофилизированного фибриногена/гидроксипропилцеллюлозы = 40/100 (м/м). Прядение проводили при температуре 22°C и влажности 26% или ниже, посредством способа электропрядения, до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 12,5 кВ, скорость потока прядильного сиропа составила 1,2 мл/ч, а расстояние между выводной форсункой и пластиной составило 15 см. Средний диаметр волокна формованного волокнистого продукта составил 0,43 мкм, средняя толщина 152 мкм, METSUKE 1,86 мг/см2, и объемная плотность 122 мг/см3. Полученный формованный волокнистый продукт подвергали анализу растворимости, и он растворялся в пределах 1 секунды. Далее, полученную пластину нарезали кусками 0,5×0,5 см, белок экстрагировали с применением 62,5 мкл нормального солевого раствора, и проводили ИФА. Результаты показали, что количество фиксированного белка составило 0,30 мг/см2. Полученную пластину можно было разрезать ножницами.
Пример 5
После диспергирования измельченного порошка лиофилизированного фибриногена из примера 1 в 2-пропаноле, гидроксипропилцеллюлозу (6-10 мПа⋅с, Wako Pure Chemical Industries, Ltd.) растворяли до получения 16 масс. %, для приготовления прядильного раствора порошка лиофилизированного фибриногена/гидроксипропилцеллюлозы = 100/100 (м/м). Прядение проводили при температуре 22°C и влажности 26% или ниже, посредством способа электропрядения, до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 12,5 кВ, скорость потока прядильного сиропа составила 1,2 мл/ч, а расстояние между выводной форсункой и пластиной составило 15 см. Средний диаметр волокна формованного волокнистого продукта составил 0,35 мкм, средняя толщина 191 мкм, METSUKE 2,74 мг/см2, и объемная плотность 143 мг/см3. Полученный формованный волокнистый продукт подвергали анализу растворимости, и он растворялся в пределах 1 секунды. Далее, полученную пластину нарезали кусками 0,5×0,5 см, белок экстрагировали с применением 62,5 мкл нормального солевого раствора, и проводили анализ активности и ИФА. Результаты показали, что количество фиксированного белка составило 0,51 мг/см2. Полученную пластину можно было разрезать ножницами.
Пример 6
Приготовление слоя, состоящего из алифатического полиэфира и тромбина
После диспергирования измельченного в ступке порошка лиофилизированного тромбина (BOLHEAL для средства адгезии тканей: флакон 3), как в примере 1, в этаноле, добавляли дихлорметан, и растворяли полимолочную кислоту (PL 18, Purac Biomaterials) до получения 10 масс. %, для приготовления прядильного сиропа из порошка лиофилизированного тромбина/полимолочной кислоты = 100/100 (м/м). Прядение проводили при температуре 22°C и влажности 26% или ниже, посредством способа электропрядения, до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 15 кВ, скорость потока прядильного сиропа составила 3,0 мл/ч, а расстояние между выводной форсункой и пластиной составило 25 см. Полученную пластину нарезали кусками 2×2 см, белок экстрагировали с применением 1 мл нормального солевого раствора, и проводили анализ активности и ИФА. Результаты показали, что измеренное значение активности составило 23 Ед/см2, а величина, измеренная посредством ИФА, составила 16 мкг/см2.
Анализ для определения эффекта тканевой адгезии
Для подтверждения активности фибриногена проводили анализ адгезии при комбинации слоя, состоящего из водорастворимого полимера и фибриногена, приготовленного в примере 5, и слоя, состоящего из алифатического полиэфира и тромбина, приготовленного в примере 6. Для оценки адгезивной силы кожу кролика приклеивали к пластине (2 см × 2 см), и проверяли, формируется ли и прилипает ли фибриновый гель. При этой процедуре добавляли заранее 200 мкл воды к слою, состоящему из водорастворимого полимера и фибриногена, и слой, состоящий из водорастворимого полимера и фибриногена, прикрепляли к коже кролика спустя 40 секунд после смачивания. После этого кожу и пластину оставляли при 37°C на 3 минуты, и затем исследовали адгезию между кожей и листом. В качестве контроля использовали препарат из коллагеновой пластины, на которой фиксировано фибриновое адгезивное средство (торговое наименование: ТахоКомб/ CSL Behring Co., Ltd.): такие компоненты, как фибриноген и тромбин, плотно фиксированы на одной стороне губкообразной пластины лошадиного коллагена в качестве подложки, посредством вакуумной сушки: 2 см × 2 см). Результаты показали, что исследуемая пластина показала адгезивную силу, равную или превышающую показатели для препарата коллагеновой пластины, используемого при сравнении в качестве контроля.
Обсуждение
Применение 1,1,1,3,3,3-гексафтор-2-пропанола/минимальной эссенциальной среды Игла 10×(9/1=о/о) в сравнительном примере 1 обеспечило получение формованного волокнистого продукта из порошка лиофилизированного фибриногена посредством способа электропрядения. Поскольку фибриноген трудно растворить в водной среде, этот порошок лиофилизированного фибриногена содержит добавку для повышения растворимости фибриногена. Хотя этот порошок лиофилизированного фибриногена использовали как таковой, фибриноген не растворялся в формованном волокнистом продукте, приготовленном из этого порошка лиофилизированного фибриногена в сравнительном примере 1.
Напротив, в примерах 1-5 фибриноген был использован в виде частиц со средним диаметром 0,01-100 мкм, и готовили дисперсию частиц. Когда дисперсия содержала полимер, растворимый в воде и этаноле, можно было достичь растворения за 1 секунду. Кроме того, в примере 6 показано, что физиологическая активность гемостатического белка сохранялась в формованном пластинчатом продукте в соответствии с настоящим изобретением.
С другой стороны, в сравнительном примере 2, относящемся к международной публикации WO 2009/031620, была сделана попытка растворения лиофилизованного порошка фибриногена из BOLHEAL как такового в растворе, для растворения фибриногена, и смешивания полученного раствора с раствором водорастворимого производного целлюлозы; однако однородный раствор нельзя было получить.
Способы измерения для примеров 7-13
1В. Диспергируемость фибриногена, тромбина и фибрина в прядильном сиропе.
Дисперсии фибриногена, тромбина и фибрина немедленно перед добавлением алифатического полиэфира анализировали визуально для подтверждения диспергируемости этих белков.
2В. Толщина формованного волокнистого продукта: ее измеряли таким же способом, как в 1А.
3В. Диаметр волокна (средний диаметр волокна): его измеряли таким же способом, как в 2А.
4В. Способность пластины к обработке: проводили качественную оценку, можно ли легко обрабатывать полученный формованный волокнистый продукт.
Пример 7
Порошок лиофилизированного фибриногена (BOLHEAL для средства адгезии тканей: флакон 1) измельчали на частицы с применением струйной мельницы (SWISHING ENTERPRISE Co., Ltd.: торговое наименование «АО струйная мельница»). Частицы добавляли в этанол (Wako Pure Chemical Industries, Ltd.), и смесь обрабатывали в ультразвуковой бане в течение 5 минут для приготовления дисперсии фибриногена, обладающей отличной диспергируемостью. Однородный раствор готовили путем добавления дихлорметана (Wako Pure Chemical Industries, Ltd.) и полимолочной кислоты в L-форме до 100% (Purser PL 18, Purac) к полученной дисперсии для растворения полимолочной кислоты. Готовили раствор полимолочной кислоты для прядения с концентрацией полимолочной кислоты 10 масс. %, порошка лиофилизированного фибриногена 4 масс. % (1,8 масс. % фибриногена), и отношением этанола к дихлорметану 1:8 по массе. Дисперсию бежа/органического растворителя перед добавлением полимолочной кислоты оценивали визуально, и было установлено, что дисперсия была в однородном диспергированном состоянии без осаждения. Прядение полученного раствора полимолочной кислоты проводили при влажности 30% или ниже путем способа электропрядения до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 12 кВ, расстояние между выводной форсункой и пластиной 25 см. Пластину, указанную выше, использовали в качестве анода при прядении. Полученный формованный волокнистый продукт имел средний диаметр волокна 3,3 мкм и толщину 161 мкм, был гибким и способным к обработке. Здесь, когда дихлорметан использовали вместо вышеприведенного этанола (в примере 14), способность к обработке полученного формованного волокнистого продукта уменьшалась, и с этой точки зрения этанол был признан более предпочтительным.
Пример 8
Порошок лиофилизированного тромбина (BOLHEAL для тканевого адгезивного средства: флакон 3) добавляли в этанол (Wako Pure Chemical Industries, Ltd.), и смесь обрабатывали в ультразвуковой бане в течение 5 минут для приготовления дисперсии тромбина, обладающей отличной диспергируемостью. Однородный раствор готовили путем добавления дихлорметана (Wako Pure Chemical Industries, Ltd.) и полимолочной кислоты в L-форме до 100% (Purser PL18, Purac) к полученной дисперсии для растворения полимолочной кислоты. Готовили раствор полимолочной кислоты для прядения с концентрацией полимолочной кислоты 10 масс. %, порошка лиофилизированного тромбина 4 масс. % (0,045 масс. % тромбина), и отношением этанола к дихлорметану 1:8 по массе. Дисперсию бежа/органического растворителя перед добавлением полимолочной кислоты оценивали визуально, и было установлено, что дисперсия была в однородном диспергированном состоянии без осаждения. Прядение полученного раствора полимолочной кислоты проводили при влажности 30% или ниже путем способа электропрядения до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 12 кВ, расстояние между выводной форсункой и пластиной 25 см. Пластину, указанную выше, использовали в качестве анода при прядении. Полученный формованный волокнистый продукт имел средний диаметр волокна 6,2 мкм и толщину 170 мкм, был гибким и способным к обработке. Здесь, когда дихлорметан использовали вместо вышеприведенного этанола (в примере 15), способность к обработке полученного формованного волокнистого продукта уменьшалась, и с этой точки зрения этанол был признан более предпочтительным.
Пример 9
Порошок лиофилизированного тромбина (BOLHEAL для тканевого адгезивного средства: флакон 3) добавляли в этанол (Wako Pure Chemical Industries, Ltd.), и смесь обрабатывали в ультразвуковой бане в течение 5 минут для приготовления дисперсии тромбина, обладающей отличной диспергируемостью. Однородный раствор готовили путем добавления дихлорметана (Wako Pure Chemical Industries, Ltd.) и полимолочной кислоты в L-форме до 100% (Purser PL18, Purac) к полученной дисперсии для растворения полимолочной кислоты. Готовили раствор полимолочной кислоты для прядения с концентрацией полимолочной кислоты 10 масс. %, порошка лиофилизированного тромбина 7 масс. % (0,078 масс. % тромбина), и отношением этанола к дихлорметану 1:8 по массе. Дисперсию белка/органического растворителя перед добавлением полимолочной кислоты оценивали визуально, и было установлено, что дисперсия была в однородном диспергированном состоянии без осаждения. Прядение полученного раствора полимолочной кислоты проводили при влажности 30% или ниже путем способа электропрядения до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 12 кВ, расстояние между выводной форсункой и пластиной 25 см. Пластину, указанную выше, использовали в качестве анода при прядении. Полученный формованный волокнистый продукт имел средний диаметр волокна 8,1 мкм и толщину 175 мкм, был гибким и способным к обработке.
Пример 10
Порошок лиофилизированного тромбина (BOLHEAL для средства адгезии тканей: флакон 3) добавляли в этанол (Wako Pure Chemical Industries, Ltd.), и смесь обрабатывали в ультразвуковой бане в течение 5 минут для приготовления дисперсии тромбина, обладающей отличной диспергируемостью. Однородный раствор готовили путем добавления дихлорметана (Wako Pure Chemical Industries, Ltd.) и полимолочной кислоты в L-форме до 100% (Purser PL18, Purac) к полученной дисперсии для растворения полимолочной кислоты. Готовили раствор полимолочной кислоты для прядения с концентрацией полимолочной кислоты 10 масс. %, порошка лиофилизированного тромбина 10 масс. % (0,11 масс. % тромбина), и отношением этанола к дихлорметану 1:8 по массе. Дисперсию белка/органического растворителя перед добавлением полимолочной кислоты оценивали визуально, и было установлено, что дисперсия была в однородном диспергированном состоянии без осаждения. Прядение полученного раствора полимолочной кислоты проводили при влажности 30% или ниже путем способа электропрядения до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 12 кВ, расстояние между выводной форсункой и пластиной 25 см. Пластину, указанную выше, использовали в качестве анода при прядении. Полученный формованный волокнистый продукт имел средний диаметр волокна 9,4 мкм и толщину 210 мкм, был гибким и способным к обработке.
Пример 11
Порошок лиофилизированного тромбина (BOLHEAL для средства адгезии тканей: флакон 3) добавляли в этанол (Wako Pure Chemical Industries, Ltd.), и смесь обрабатывали в ультразвуковой бане в течение 5 минут для приготовления дисперсии тромбина, обладающей отличной диспергируемостью. Однородный раствор готовили путем добавления дихлорметана (Wako Pure Chemical Industries, Ltd.) и сополимера полигликолевой кислоты - полимолочной кислоты (Purasorb PL5010, Purac) к полученной дисперсии для растворения сополимера полигликолевой кислоты - полимолочной кислоты. Готовили раствор сополимера полигликолевой кислоты - полимолочной кислоты для прядения с концентрацией полимера 10 масс. %, порошка лиофилизированного тромбина 5 масс. % (0,06 масс. % тромбина), и отношением этанола к дихлорметану 1:8 по массе. Дисперсию белка/органического растворителя перед добавлением сополимера полигликолевой кислоты - полимолочной кислоты оценивали визуально, и было установлено, что дисперсия была в однородном диспергированном состоянии без осаждения. Прядение полученного раствора сополимера полигликолевой кислоты - полимолочной кислоты проводили при влажности 30% или ниже путем способа электропрядения до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 15 кВ, расстояние между выводной форсункой и пластиной 25 см. Пластину, указанную выше, использовали в качестве анода при прядении. Полученный формованный волокнистый продукт имел средний диаметр волокна 4,8 мкм и толщину 330 мкм, был гибким и способным к обработке.
Пример 12
Порошок лиофилизированного тромбина (BOLHEAL для средства адгезии тканей: флакон 3) добавляли в 2-пропанол (Wako Pure Chemical Industries, Ltd.), и смесь обрабатывали в ультразвуковой бане в течение 5 минут для приготовления дисперсии тромбина, обладающей отличной диспергируемостью. Однородный раствор готовили путем добавления дихлорметана (Wako Pure Chemical Industries, Ltd.) и сополимера полигликолевой кислоты - полимолочной кислоты (Purasorb PL5010, Purac) к полученной дисперсии для растворения сополимера полигликолевой кислоты - полимолочной кислоты. Готовили раствор сополимера полигликолевой кислоты - полимолочной кислоты для прядения с концентрацией полимера 10 масс. %, порошка лиофилизированного тромбина 5 масс. % (0,06 масс. % тромбина), и отношением 2-пропанола к дихлорметану 1:8 по массе. Дисперсию белка/органического растворителя перед добавлением сополимера полигликолевой кислоты - полимолочной кислоты оценивали визуально, и было установлено, что дисперсия была в однородном диспергированном состоянии без осаждения. Прядение полученного раствора сополимера полигликолевой кислоты - полимолочной кислоты проводили при влажности 30% или ниже путем способа электропрядения до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 15 кВ, расстояние между выводной форсункой и пластиной 25 см. Пластину, указанную выше, использовали в качестве анода при прядении. Полученный формованный волокнистый продукт имел средний диаметр волокна 6,4 мкм и толщину 320 мкм, был гибким и способным к обработке.
Пример 13
После диспергирования порошка лиофилизированного тромбина (приготовленного путем лиофилизации рекомбинантного тромбина 1 мг/мл, 3,4% хлорида натрия, 1,2% цитрата натрия, 0,29% хлорида кальция, 1% маннитола при pH 7) в этаноле, к дисперсии добавляли дихлорметан, и растворяли сополимер полигликолевой кислоты -полимолочной кислоты (Purasorb PDLG5010, Purac) до получения 10 масс. %, для приготовления прядильного сиропа порошка лиофилизированного тромбина/сополимера полигликолевой кислоты - полимолочной кислоты = 100 (1,67 тромбина)/100 (м/м). Прядение проводили при температуре 26°C и влажности 29% или ниже посредством способа электропрядения, до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 20 кВ, скорость потока прядильного раствора 4,0 мл/ч, и расстояние между выводной форсункой и заземленной пластиной 35 см. Полученный формованный волокнистый продукт имел толщину 136 мкм, был гибким и способным к обработке. Растворение тромбина из полученной пластины оценивали посредством анализа растворимости. Метод анализа описан ниже.
Анализ растворимости
(1) Образец перфорировали до получения диаметра 6 мм, и измеряли его массу.
(2) Образец помещали в микротрубку, и проводили анализ растворимости в ГПЦ-содержащем нормальном солевом растворе, или в нормальном солевом растворе.
(3) Время отбора образцов составило 10, 30,60 и 120 секунд.
(4) Отбирали образец, и подвергали его анализу посредством жидкостной хроматографии, и содержание тромбина определяли по площади пика.
(5) Скорость растворения получали с применением следующего уравнения:
Скорость растворения (%) = Содержание полученного тромбина / Теоретическое содержание фиксированного тромбина × 100.
Теоретическое содержание фиксированного тромбина рассчитывали на основе количества внесенного тромбина (масс. %) и METSUKE формованного волокнистого продукта.
Результаты анализа растворимости показаны на Фигуре 1. Скорость растворения была лучше в ГПЦ-содержащем нормальном солевом растворе, чем в нормальном солевом растворе. Это свидетельствует, что включение ГПЦ в пластину вносит вклад в улучшение скорости растворения тромбина в ламинированном формованном пластинчатом продукте в соответствии с настоящим изобретением.
Способы определения для примеров 14 и 15 и сравнительных примеров 3-4
1С. Диаметр частиц гемостатического белка (средний диаметр частиц):
Прядильный сироп фотографировали с увеличением ×1000 с помощью цифрового микроскопа (KEYENCE Corporation: торговое наименование «VHX-100»), произвольно отбирали 10 частиц на фотографии, и измеряли их диаметр. Использовали среднее значение в качестве среднего диаметра частиц.
2С. Толщина формованного волокнистого продукта: ее измеряли тем же способом, как в 1А.
3С. Диаметр волокна (средний диаметр волокна): его измеряли тем же способом, как в 2А.
4С. Анализ растворимости гемостатического белка.
Формованный волокнистый продукт нарезали кусочками 2 см × 2 см, и кусочек погружали в 1 мл нормального солевого раствора на 3 минуты или 3 часа для растворения водорастворимого компонента. Изменение массы до и после погружения (n=3-6) и среднюю скорость экстракции рассчитывали с помощью следующего уравнения. Теоретическую массу водорастворимого компонента рассчитывали на основе загруженного гемостатического белка (масс. %) и METSUKE формованного волокнистого продукта.
Скорость экстракции [%] = (снижение массы [мг] / теоретическая масса [мг] водорастворимого компонента) × 100
5С. Анализ поддерживающих характеристик для гемостатического белка.
Полученный формованный волокнистый продукт нарезали на кусочки 1 см × 1 см, и кусочек разделяли на 4 части ножницами. Измеряли массу до и после разделения, и рассчитывали изменение массы.
Изменение массы [%] = (Масса после разделения [мг] / масса до разделения [мг]) × 100
6С. Анализ гибкости формованного волокнистого продукта.
Что касается способа для слайдов (способ JIS-L-1906 8,19,2 В), размер опытного образца устанавливали 0,5 см × 3,5 см, и гибкость измеряли посредством следующей процедуры. После выравнивания корпуса аппарата с верхней поверхностью передвижной платформы, опытный образец помещали с 0,5 см в ширину, сложенным между покровным стеклом и корпусом аналитического аппарата. Передвижную платформу снижали, и рассчитывали нижнее значение δ, при котором свободные концы опытного образца отделялись от передвижной платформы (большие значения δ указывают на большую гибкость).
Пример 14
Порошок лиофилизированного фибриногена (BOLHEAL для средства адгезии тканей: флакон 1) измельчали на частицы с применением струйной мельницы (SEISHTN ENTERPRISE Co., Ltd.: торговое наименование «АО струйная мельница»). Частицы добавляли в дихлорметан (Wako Pure Chemical Industries, Ltd.), и смесь обрабатывали в ультразвуковой бане в течение 5 минут для приготовления дисперсии фибриногена, обладающей отличной диспергируемостью. Раствор готовили путем добавления полимолочной кислоты в L-форме до 100% (Purser PL 18, Purac) для растворения полимера. Готовили раствор полимера для прядения с концентрацией полимера 10 масс. % и порошка лиофилизированного фибриногена 4 масс. % (1,8 масс. % фибриногена). Диаметр частиц фибриногена, диспергированных в прядильном сиропе, составил 12 мкм. Прядение полученного раствора полимера проводили при влажности 30% или ниже путем способа электропрядения до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 12 кВ, расстояние между выводной форсункой и пластиной 25 см. Пластину, указанную выше, использовали в качестве анода при прядении. Полученный формованный волокнистый продукт имел средний диаметр волокна 14,9 мкм и толщину 325 мкм. Количество фибриногена, содержащегося в пластине, рассчитанное по массе пластины и отношению к внесенной массе, составило 0,43 мг/см2. Степень экстракции после погружения на 3 часа составила 40%. Не отмечалось изменения массы при анализе поддерживающих характеристик (100% удерживание). Значение δ, полученное при анализе гибкости, составило 2,7 см.
Пример 15
Порошок лиофилизированного тромбина (BOLHEAL для средства адгезии тканей: флакон 3) (содержащий 1,12% тромбина (750 единиц) в 40 мг лиофилизированного порошка) добавляли в дихлорметан (Wako Pure Chemical Industries, Ltd.), и смесь обрабатывали в ультразвуковой бане в течение 5 минут для приготовления дисперсии тромбина. Раствор готовили путем добавления полимолочной кислоты в L-форме до 100% (Purser PL 18, Purac) для растворения полимера. Готовили раствор полимера для прядения с концентрацией полимера 10 масс. % и порошка лиофилизированного тромбина 4 масс. % (0,045 масс. % или 750 единиц (Ед)/г тромбина). Диаметр частиц тромбина, диспергированных в прядильном сиропе, составил 9 мкм. Прядение полученного раствора полимера проводили при влажности 30% или ниже путем способа электропрядения до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 12 кВ, расстояние между выводной форсункой и пластиной 25 см. Пластину, указанную выше, использовали в качестве анода при прядении. Полученный формованный волокнистый продукт имел средний диаметр волокна 16,6 мкм и толщину 291 мкм. Количество тромбина, содержащегося в пластине, рассчитанное по массе пластины и отношению к внесенной массе, составило 31,39 Ед/см2.
Сравнительный пример 3
Порошок лиофилизированного тромбина (BOLHEAL для средства адгезии тканей: флакон 3) добавляли в этанол (Wako Pure Chemical Industries, Ltd.), и смесь обрабатывали в ультразвуковой бане в течение 5 минут для приготовления дисперсии тромбина. Однородный раствор готовили путем добавления дихлорметана (Wako Pure Chemical Industries, Ltd.) и полимолочной кислоты в L-форме до 100% (Purser PL18, Purac) к полученной дисперсии для растворения полимера. Готовили раствор полимера для прядения с концентрацией полимера 10 масс. % и порошка лиофилизированного тромбина 4 масс. % (0,045 масс. % или 750 единиц (Ед)/г тромбина), с отношением этанола к дихлорметану 1:8 по массе. Диаметр частиц тромбина, диспергированных в прядильном сиропе, составил 12 мкм. Раствор полимера сушили на воздухе до твердого состояния. Его подвергали анализу растворимости, как для формованного волокнистого продукта, и в результате примерно 3% водорастворимого компонента экстрагировалось после погружения в течение 3 минут.
Сравнительный пример 4
NEOVEIL (зарегистрированная торговая марка, Gunze Limited), нетканый материал на основе полигликолевой кислоты, применяли в качестве формованного волокнистого продукта для приготовления пластины с фиксированным фибриногеном посредством следующей процедуры (способа лиофилизации). Вышеуказанный формованный волокнистый продукт (5×5 см2) пропитывали 1,25 мл раствора фибриногена, содержащегося в коммерческом биотканевом адгезивном средстве (торговое наименование: набор BOLHEAL:KAKETSUKEN (Исследовательский институт химио-серо-терапии)). Этот образец замораживали, а затем лиофилизировали в течение 24 часов, и полученный материал использовали в качестве пластины с фиксированным фибриногеном. При анализе поддерживающих характеристик фиксированный фибриноген разрушался до получения порошка, и терялся (изменение массы 89%). Значение δ, полученное при анализе гибкости, составило 0,7 см.
Способы анализа для примеров 16-29
1D. Диаметр частиц белкового порошка (средний диаметр частиц)
Порошок лиофилизированного фибриногена измельчали в ступке и подвергали анализу распределения частиц по размеру с применением аппарата лазерной дифракции для анализа распределения по размеру частиц (Malvern: торговое наименование «Master Sizer 2000»), и определяли значение D50 (средний диаметр) в качестве среднего диаметра частиц.
2D. Анализ содержания фибриногена
Полученную пластину нарезали диаметром 0,5 см, а затем экстрагировали фибриноген с 0,1% раствором ТФУК, и проводили количественное определение с помощью высокоэффективной жидкостной хроматографии.
Условия анализа
Детектор: УФ абсорбционный спектрофотометр (измеряемая длина волны: 214 нм)
Колонка: Agilent Bio SEC-3 (3 мкм, 30 нм, 4,6×300 мм, Agilent Technologies)
Температура колонки: 35°C
Температура устройства для отбора образцов: 5°C
Мобильная фаза: Вода, содержащая 0,1% ТФУК/ацетонитрил, содержащий 0,1% ТФУК = 50/50
Скорость потока: 0,5 мл/мин
Продолжительность анализа: 10 мин
Пример 16
Приготовление формованного пластинчатого продукта, состоящего из водорастворимого полимера и фибриногена
После диспергирования порошка лиофилизированного фибриногена (BOLHEAL для средства адгезии тканей: флакон 1) в 2-пропаноле, гидроксипропилцеллюлозу (6-10 мПа⋅с, Wako Pure Chemical Industries, Ltd.) растворяли до 16 масс. % до приготовления прядильного сиропа порошка лиофилизированного фибриногена/гидроксипропилцеллюлозы = 100 (46 в качестве фибриногена)/100 (м/м). Прядение проводили при температуре 22°C и влажности 26% или ниже посредством способа электропрядения, до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 12,5 кВ, скорость потока прядильного сиропа 1,2 мл/ч, а расстояние между выводной форсункой и заземляющей пластиной 15 см. Средний диаметр волокна полученного волокнистого продукта составил 0,35 мкм, средняя толщина 191 мкм, METSUKE 2,74 мг/см2, а объемная плотность 143 мг/см3. Полученную пластину нарезали на кусочки 0,5 см × 0,5 см, белок экстрагировали с применением 62,5 мкл нормального солевого раствора, и подвергали ИФА (способ описан в разделе «7А. ИФА (1) фибриноген»). Результаты показали, что количество фиксированного белка составило 0,51 мг/см2.
Пример 17
Приготовление формованного пластинчатого продукта, состоящего из алифатического полиэфира и тромбина.
После диспергирования порошка лиофилизированного тромбина (BOLHEAL для средства адгезии тканей: флакон 3) в этаноле, в дисперсию добавляли дихлорметан, и растворяли полимолочную кислоту (PL 18 Purac Biomaterials) до получения 10 масс. %. для приготовления прядильного сиропа порошка лиофилизированного тромбина/полимолочной кислоты = 100 (1,1 в качестве тромбина)/100 (м/м). Прядение проводили при температуре 22°C и влажности 26% или ниже, посредством способа электропрядения, до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 15 кВ, скорость потока прядильного сиропа 3,0 мл/ч, а расстояние между выводной форсункой и заземляющей пластиной 25 см. Средний диаметр волокна полученного волокнистого продукта составил 9,37 мкм, средняя толщина 210 мкм, METSUKE 3,15 мг/см2, а объемная плотность 150 мг/см3. Полученную пластину нарезали на кусочки 2 см × 2 см, белок экстрагировали с применением 1 мл нормального солевого раствора, и подвергали анализу активности (способ описан в «8А. Определение активности тромбина») и ИФА (способ описан в «7А. ИФА (2) тромбин»). Результаты показали, что измеренная активность составила 23,0 Ед/см2, а значение, измеренное при ИФА, составило 16 мкг/см2.
Пример 18
Анализ для оценки эффекта тканевой адгезии для ламинированного формованного пластинчатого продукта
Для подтверждения эффекта, полученного при использовании формованного пластинчатого продукта, состоящего из водорастворимого полимера и фибриногена, приготовленного в примере 16, и формованного пластинчатого продукта, состоящего из алифатического полиэфира и фибриногена, приготовленного в примере 18, в комбинации, проводили сравнение адгезивной силы. Для адгезивной силы кожу кролика приклеивали на лист (2 см × 2 см), и оценивали, формируется ли и прилипает ли фибриновый гель. При этой процедуре 200 мкл воды заранее добавляли к формованному пластинчатому продукту, состоящему из водорастворимого полимера и фибриногена, и формованный пластинчатый продукт, состоящий из водорастворимого полимера и фибриногена, прикрепляли к коже кролика спустя 40 секунд после смачивания. После этого кожу и пластину оставляли при 37°C на 3 минуты, и оценивали адгезию между кожей и пластиной. В качестве контроля использовали препарат коллагеновой пластины, на которой был фиксирован компонент фибринового адгезивного средства (торговое наименование TachoComb/CSL Behring Co., Ltd.; такие компоненты, как фибриноген и тромбин, плотно фиксированы на одной стороне губкообразной пластины лошадиного коллагена в качестве подложки путем вакуумной сушки; 2 см × 2 см), результаты показали, что ламинированный формованный пластинчатый продукт в соответствии с настоящим изобретением имел адгезивную силу, равную или большую, чем у препарата коллагеновой пластины, использованной в качестве контроля при сравнении.
Пример 19
Приготовление формованного пластинчатого продукта, состоящего из водорастворимого полимера и фибриногена
После диспергирования порошка лиофилизированного фибриногена (BOLHEAL для средства адгезии тканей: флакон 1) в 2-пропаноле, гидроксипропилцеллюлозу (6-10 мПа⋅с, Wako Pure Chemical Industries, Ltd.) растворяли до 16 масс. % до приготовления прядильного сиропа порошка лиофилизированного фибриногена/гидроксипропилцеллюлозы = 100 (46 в качестве фибриногена)/100 (м/м). Прядение проводили при температуре 22°C и влажности 26% или ниже, посредством способа электропрядения, до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 12,5 кВ, скорость потока прядильного сиропа 1,2 мл/ч, а расстояние между выводной форсункой и заземляющей пластиной 15 см. Средний диаметр волокна полученного волокнистого продукта составил 0,35 мкм, средняя толщина 191 мкм, METSUKE 2,74 мг/см2, а объемная плотность 143 мг/см3. Полученную пластину стерилизовали электронным пучком при 20 кГрэй. Стерилизованную пластину нарезали кусками 0,5 см × 0,5 см, и белок экстрагировали с применением 62,5 мкл нормального солевого раствора, и подвергали ИФА (способ описан в «7А. ИФА (1) фибриноген»). Результаты показали, что количество фиксированного белка составило 0,78 мг/см2.
Пример 20
Приготовление формованного пластинчатого продукта, состоящего из алифатического полиэфира и тромбина
После диспергирования порошка лиофилизированного тромбина (BOLHEAL для средства адгезии тканей: флакон 3) в этаноле, в дисперсию добавляли дихлорметан, и растворяли полимолочную кислоту (PL18 Purac Biomaterials) до получения 10 масс. %. для приготовления прядильного сиропа порошка лиофилизированного тромбина/полимолочной кислоты = 100 (1,1 в качестве тромбина)/100 (м/м). Прядение проводили при температуре 22°C и влажности 26% или ниже, посредством способа электропрядения, до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 15 кВ, скорость потока прядильного сиропа 3,0 мл/ч, а расстояние между выводной форсункой и заземляющей пластиной 25 см. Средний диаметр волокна полученного волокнистого продукта составил 9,37 мкм, средняя толщина 210 мкм, METSUKE 3,15 мг/см2, а объемная плотность 150 мг/см3. Полученную пластину стерилизовали электронным пучком при 20 кГрэй. Полученный формованный пластинчатый продукт нарезали кусками 2 см × 2 см, белок экстрагировали с применением 1 мл нормального солевого раствора, и подвергали анализу активности (способ описан в «8А. Измерение активности тромбина») и ИФА (способ описан в «7А. ИФА (2) тромбин»). Результаты показали, что измеренное значение активности составило 14,7 Ед/см2, а значение, измеренное посредством ИФА, составило 11,4 мкг/см2.
Пример 21
Гемостатический эффект при экссудативном кровотечении в печени кролика
Гемостатический эффект, полученный, когда формованный пластинчатый продукт, состоящий из водорастворимого полимера и фибриногена, приготовленный в примере 19, и формованный пластинчатый продукт, состоящий из алифатического полиэфира и тромбина, приготовленный в примере 20, использовали в комбинации, сравнивали с гемостатическим эффектом, полученный при применении препарата ТахоКомб.
Кроликов использовали в качестве животной модели гемостаза. У кроликов проводили лапаротомию для удаления части печени, и формованный пластинчатый продукт, состоящий из водорастворимого полимера и фибриногена, и формованный пластинчатый продукт, состоящий из алифатического полиэфира и тромбина, применяли при наложении на участок кровотечения, и наблюдали гемостатический эффект (наличие/отсутствие гемостаза, объем кровотечения). Способ анализа показан ниже.
(1) Селактар в дозе 10 мг/кг (около 1,0 мл) и кеталар в дозе 50 мг/кг (около 3,0 мл) вводили внутримышечно.
(2) Определяли массу тела, брили живот, и кролика оставляли в положении на спине.
(3) Длительную анестезию (2% кеталар, нормальный солевой раствор, содержащий гепарин в дозе 20 Ед/мл) обеспечивали введением в вену уха.
(4) Проводили срединный разрез непосредственно под мечевидным отростком грудины к нижней части живота для лапаротомии.
(5) Раствор гепарина натрия для инъекций в дозе 300 Ед/кг вводили в вену уха.
(6) Доли печени (латеральную левую долю, среднюю левую долю и правую долю), имеющие толщину, достаточную для осуществления повреждения, извлекали с помощью щипцов для кишечника, марли, и тому подобного.
(7) Перфоратор для кожи использовали для получения повреждения диаметром 10 мм и глубиной 4 мм в доле печени, и участок удаляли хирургическим ножом.
(8) Кровотечение из резекционной раны абсорбировали пластинами Ben в течение 10 секунд, и измеряли массу. В анализе использовали раны с кровотечением 0,5 г или более.
(9) Слой, состоящий из водорастворимого полимера и фибриногена, и слой, состоящий из алифатического полиэфира и тромбина, нарезанные кусками 2,5×2,5 см, накладывали друг на друга в раневом участке, где слой, состоящий из водорастворимого полимера и фибриногена, налагали на участок кровотечения, и участок кровотечения прижимали в течение 1 минуты. В случае использования ТахоКомба в качестве контроля, его нарезали кусками 2,5×2,5 см, добавляли по каплям 312,5 мкл нормального солевого раствора на пластину, и прижимали участок кровотечения в течение 1 минуты.
(10) После нажимания наблюдали наличие/отсутствие кровотечения, и определяли массу крови из раневого участка, абсорбированной на пластине Ben.
Результаты показали, что когда применяли ламинированный формованный пластинчатый продукт в соответствии с настоящим изобретением, отмечался гемостаз (n=1), количество потерянной крови в течение 1 минуты после применения было достаточно малым, 0,003 г. В случае применения ТахоКомба в качестве контроля (n=5), количество потерянной крови в течение 1 минуты после применения составило 1,57 г, таким образом, гемостатический эффект был недостаточным, и количество кровопотери было большим.
Пример 22
Приготовления формованного пластинчатого продукт, состоящего из алифатического полиэфира и тромбина
Порошок лиофилизированного тромбина (рекомбинантный тромбин 1 мг/мл, 3,4% хлорид натрия, 1,2% цитрат натрия, 0,29% хлорид кальция, 1% маннитол при pH 7, который был лиофилизирован) диспергировали в этаноле, к дисперсии добавляли дихлорметан, и растворяли сополимер полигликолевой кислоты - полимолочной кислоты (Purasorb PDLG5010, Purac) до получения 10 масс. %, для приготовления прядильного сиропа из порошка лиофилизированного тромбина/сополимера полигликолевой кислоты - полимолочной кислоты = 100 (1,67 в виде тромбина)/100 (м/м). Прядение проводили при температуре 22°C и влажности 26% или ниже посредством способа электропрядения, до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 20 кВ, скорость потока прядильного сиропа 4,0 мл/ч, а расстояние между выводной форсункой и заземляющей пластиной 35 см. Средний диаметр волокна полученного формованного волокнистого продукта составил 3,8 мкм, средняя толщина 127 мкм, METSUKE 1,38 мг/см2, и объемная плотность 109 мг/см3. Полученный формованный пластинчатый продукт нарезали диаметром 1 см, и белок экстрагировали с применением 200 мкл нормального солевого раствора, и подвергали анализу активности тромбина (в соответствии со способом, описанным в «8А. Определение активности тромбина»). В результате измеренное значение активности составило 18,3 Ед/см2.
Пример 23
Приготовление ламинированного формованного пластинчатого продукта, построенного из слоя, состоящего из водорастворимого полимера и фибриногена, и слоя, состоящего из алифатического полиэфира и тромбина
Порошок лиофилизированного фибриногена (рекомбинантный фибриноген 10 мг/мл, 10 мМ аргинин, 130 мМ хлорид натрия, 0,5% маннитол, при pH 8,5, который был лиофилизирован) измельчали в ступке до получения порошка лиофилизированного фибриногена со средним диаметром частиц 30 мкм. После этого порошок лиофилизированного фибриногена диспергировали в 2-пропаноле, растворяли гидроксипропилцеллюлозу (2,0-2,9 мПа⋅с, Nippon Soda Co., Ltd.) и MACROGOL (молекулярная масса: 400, Sanyo Chemical Industries, Ltd.) до 15 масс. %, для приготовления прядильной жидкости из порошка лиофилизированного фибриногена/гидроксипропилцеллюлозы/MACROGOL = 51 (25,92 в качестве фибриногена)/34/15 (м/м/м). Использовали полученную прядильную жидкость, и получали пленку посредством литья. Расстояние покрытия составило 127 мкм, а скорость нанесения покрытия составила 30,1 мм/сек. Слой, состоящий из алифатического полиэфира и тромбина, приготовленный в примере 22, наносили на пленку в течение 1 минуты после получения пленки, для изготовления ламинированного формованного пластинчатого продукта, построенного из слоя, состоящего из водорастворимого полимера и фибриногена, и слоя, состоящего из алифатического полиэфира и тромбина, до получения ламинированного формованного пластинчатого продукта. Полученный ламинированный формованный пластинчатый продукт имел среднюю толщину пленки 157 мкм. Полученный ламинированный формованный пластинчатый продукт стерилизовали электронным пучком при 20 кГрэй. Полученный ламинированный формованный пластинчатый продукт нарезали кусками диаметром 1 см, белок экстрагировали с применением 200 мкл нормального солевого раствора, и подвергали ИФА для определения фибриногена (в соответствии со способом, описанным в «7А. ИФА анализ (1) фибриногена»). Результаты показали, что количество фиксированного белка составило 0,58 мг/см2.
Пример 24
Гемостатический эффект при экссудативном кровотечении в печени кроликов
Гемостатический эффект ламинированного формованного пластинчатого продукта, состоящего из водорастворимого полимера и фибриногена, и слоя, состоящего из алифатического полиэфира и тромбина, приготовленного в примере 23, сравнивали с гемостатическим эффектом TachoSil.
Кроликов использовали в качестве животной модели гемостаза. У кроликов проводили лапаротомию, удаляли часть печени, и формованный пластинчатый продукт, построенный из слоя, состоящего из водорастворимого полимера и фибриногена, и слоя, состоящего из алифатического полиэфира и тромбина, налагали на участок кровотечения, и наблюдали гемостатический эффект (наличие/отсутствие гемостаза, объем кровотечения). Способ анализа был таким же, как описан в примере 21.
Результаты показали, что когда использовали ламинированный формованный пластинчатый продукт в соответствии с настоящим изобретением (n=4), кровопотеря в течение 1 минуты после применения была очень маленькой, 0,003 г. С другой стороны, когда в качестве контроля применяли TachoSil (n=4) кровопотеря в течение 1 минуты после применения составила 0,65 г, и была высокой, указывая, что гемостатический эффект был недостаточным.
Пример 25
Приготовление формованного пластинчатого продукта, состоящего из алифатического полиэфира и тромбина
Порошок лиофилизированного тромбина (рекомбинантный тромбин 1 мг/мл, 3,4% хлорид натрия, 1,2% цитрат натрия, 0,29% хлорида кальция, 1% маннитол, при pH 7, который был лиофилизирован) диспергировали в этаноле, затем к дисперсии добавляли дихлорметан, и растворяли сополимер полигликолевой кислоты - полимолочной кислоты (Purasorb PDLG5010, Purac) до получения 10 масс. %, для приготовления прядильного сиропа из порошка лиофилизированного тромбина/сополимера полигликолевой кислоты - полимолочной кислоты = 100 (1,67 в виде тромбина)/100 (м/м). Прядение проводили при температуре 22°С и влажности 26% или ниже посредством способа электропрядения, до получения пластинчатого формованного волокнистого продукта. Внутренний диаметр выводной форсунки составил 0,8 мм, напряжение 20 кВ, скорость потока прядильного сиропа 4,0 мл/ч, а расстояние между выводной форсункой и заземляющей пластиной 35 см. Средний диаметр волокна полученного формованного волокнистого продукта составил 2,97 мкм, средняя толщина 137 мкм, METSUKE 1,49 мг/см2, и объемная плотность 108 мг/см3.
Пример 26
Приготовление ламинированного формованного пластинчатого продукта, построенного из слоя, состоящего из водорастворимого полимера и фибриногена, и слоя, состоящего из алифатического полиэфира и тромбина
Порошок лиофилизированного фибриногена (рекомбинантный фибриноген 10 мг/мл, 10 мМ аргинин, 130 мМ хлорид натрия, 0,5% маннитол, при pH 8,5, который был лиофилизирован) измельчали в ступке до получения порошка лиофилизированного фибриногена со средним диаметром частиц 30 мкм. После этого порошок лиофилизированного фибриногена диспергировали в 2-пропаноле, растворяли гидроксипропилцеллюлозу (2,0-2,9 мПа⋅с, Nippon Soda Co., Ltd.) до получения 2,9 масс. % и MACROGOL (молекулярная масса: 400, Sanyo Chemical Industries, Ltd.) для приготовления прядильной жидкости из порошка лиофилизированного фибриногена/гадроксипропилцеллюлозы/MACROGOL = 90 (36,98 в качестве фибриногена)/7/3 (м/м/м). Использовали полученную прядильную жидкость, и получали пленку посредством литья. Расстояние покрытия составило 50,8 мкм, а скорость нанесения покрытия составила 30,1 мм/сек. Слой, состоящий из алифатического полиэфира и тромбина, приготовленный в примере 25, наносили на пленку в течение 1 минуты после получения пленки, для изготовления ламинированного формованного пластинчатого продукта, построенного из слоя, состоящего из водорастворимого полимера и фибриногена, и слоя, состоящего из алифатического полиэфира и тромбина, до получения ламинированного формованного пластинчатого продукта. Средняя толщина пленки полученного ламинированного формованного пластинчатого продукта составила 169 мкм. Полученный ламинированный формованный пластинчатый продукт стерилизовали электронным пучком при 20 кГрэй. Полученный ламинированный формованный пластинчатый продукт нарезали кусками диаметром 0,5 см, белок экстрагировали с применением 0,1% раствора ТФУК, и проводили количественное определение посредством высокоэффективной жидкостной хроматографии (способ описан в «2D. Измерение содержания фибриногена»). Результаты показали, что количество фиксированного белка составило 0,54 мг/см2.
Пример 27
Гемостатический эффект при экссудативном кровотечении в печени кроликов
Гемостатический эффект ламинированного формованного пластинчатого продукта, состоящего из водорастворимого полимера и фибриногена, и слоя, состоящего из алифатического полиэфира и тромбина, приготовленного в примере 26, сравнивали с гемостатическим эффектом TachoSil.
Кроликов использовали в качестве животной модели гемостаза. У кроликов проводили лапаротомию, удаляли часть печени, и формованный пластинчатый продукт, построенный из слоя, состоящего из водорастворимого полимера и фибриногена, и слоя, состоящего из алифатического полиэфира и тромбина, налагали на участок кровотечения, и наблюдали гемостатический эффект (наличие/отсутствие гемостаза, объем кровотечения). Способ анализа был таким же, как описан в примере 21.
Результаты показали, что когда использовали ламинированный формованный пластинчатый продукт в соответствии с настоящим изобретением (n=6), кровопотеря в течение 1 минуты после применения была очень маленькой, 0,003 г. С другой стороны, когда в качестве контроля применяли TachoSil (n=4), как показано в примере 24, кровопотеря в течение 1 минуты после применения составила 0,65 г, и была высокой, указывая, что гемостатический эффект был недостаточным.
Пример 28
Порошок лиофилизированного фибриногена (рекомбинантный фибриноген 10 мг/мл, 10 мМ аргинин, 110 мМ хлорид натрия, 1% глицин, 0,2% маннитол, 0,25% фенилаланин, 0,4% гистидин, 0,1% тринатрий цитрат, при pH 8,5, который был лиофилизирован) измельчали в ступке до получения порошка лиофилизированного фибриногена со средним диаметром частиц 22 мкм. После этого молотый порошок лиофилизированного фибриногена диспергировали в 2-пропаноле, растворяли гидроксипропилцеллюлозу (2,0-2,9 мПа⋅с, Nippon Soda Co., Ltd.) до получения 4,2 масс. % для приготовления прядильной жидкости из порошка лиофилизированного фибриногена/гидроксипропилцеллюлозы = 90 (26,55 в качестве фибриногена)/10 (м/м). Использовали полученную прядильную жидкость для получения пленки посредством литья. Расстояние покрытия составило 101,6 мкм, а скорость нанесения покрытия составила 30,1 мм/сек. Пластинчатые формованные волокнистые продукты, имеющие доли порошка лиофилизированного тромбина/сополимера полигликолевой кислоты - полимолочной кислоты = 20/100, 40/100, 60/100, 80/100 и 100/100, приготовленные способом, описанным в примере 25, наносили на пленку в течение 3 минут после получения пленки, для изготовления ламинированного формованного пластинчатого продукта, построенного из слоя, состоящего из водорастворимого полимера и фибриногена, и слоя, состоящего из алифатического полиэфира и тромбина. Гемостатический эффект этих ламинированных формованных пластинчатых продуктов оценивали на крысиной дренажной модели оценки эффективности лекарств. В этом тесте оценки использовали модель экссудативного кровотечения у крыс, где формировали рану в печени. Опытный формованный пластинчатый продукт прижимали к раневому участку в течение определенного времени (5 минут в этом примере), и затем наличие/отсутствие кровотечения визуально оценивали в течение 1 минуты. Анализ проводили с n=6 для подтверждения наличия/отсутствия кровотечения.
В результате, как показано в таблице 1, был подтвержден гемостатический эффект, превышающий эффект, полученный с TachoSil, для порошка лиофилизированного тромбина/сополимера полигликолевой кислоты - полимолочной кислоты, в диапазоне пропорций от 20/100 до 100/100.
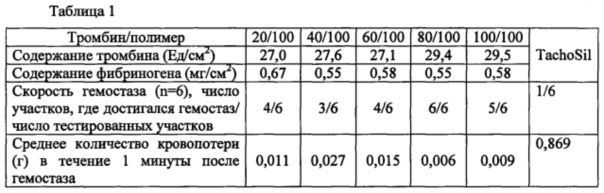
Пример 29
Пластинчатые формованные волокнистые продукты, имеющие различное содержание тромбина (содержание тромбина 0,23 Ед/см2, 2,8 Ед/см2, 11,4 Ед/см2, и 28,5 Ед/см2), были получены посредством способа, описанного в примере 25. Затем ламинированный формованный пластинчатый продукт, построенный из слоя, состоящего из водорастворимого полимера и фибриногена, имеющий постоянное содержание фибриногена, и слоя, состоящего из алифатического полиэфира и тромбина, готовили посредством способа, описанного в примере 26. Способ анализа был следующим:
(1) Ламинированный формованный пластинчатый продукт и препарат положительного контроля (TachoSil) (1 см × 1 см) приклеивали ко дну пластиковой прямоугольной призмы (1 см × 1 см) двусторонней адгезивной лентой.
(2) Ламинированный формованный пластинчатьш продукт и препарат положительного контроля (TachoSil) погружали в 1 мл нормального солевого раствора на 10 секунд, и плотно прикрепляли к лауановой пластине.
(3) Прилагали груз 100 г в вышеуказанной прямоугольной призме на 5 минут.
(4) Прямоугольную призму продвигали со скоростью 30 мм/мин, и измеряли растягивающую силу посредством цифрового датчика усилия.
Анализ проводили с n=5, и оценивали среднюю растягивающую силу в качестве адгезивной силы (g). В результате, как показано в таблице 2, все ламинированные формованный пластинчатые продукты были отличными, и проявляли большую адгезивную силы, чем TachoSil.
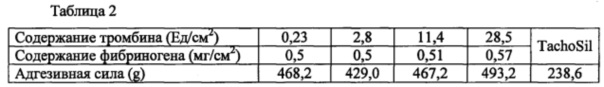
Пример 30
Формованный пластинчатый продукт, состоящий из алифатического полиэфира и тромбина (содержание тромбина 24,2 Ед/см2), получали способом, описанным в примере 25, и гемостатический эффект этого формованного пластинчатого продукта оценивали способом, описанным в примере 28 (время прижимания 3 минуты). Анализ проводили с n=6. В результате гемостаз был подтвержден во всех образцах.
Пример 31
Формованный пластинчатый продукт, состоящий из алифатического полиэфира и тромбина (диапазон содержания тромбина 19-26 Ед/см2), получали способом, описанным в примере 25, а затем ламинированный формованный пластинчатый продукт, построенный из слоя, состоящего из водорастворимого полимера и фибриногена в различных содержаниях, и слоя, состоящего из алифатического полиэфира и тромбина, получали способом, описанным в примере 26. Гемостатический эффект этого полученного ламинированного формованного пластинчатого продукта, имеющего содержание тромбина в определенном диапазоне и различное содержание фибриногена, оценивали способом, описанным в примере 28. В результате, как показано в таблице 3, высокий гемостатический эффект был подтвержден для всех содержаний фибриногена, но был слегка снижен при 1,47 мг/см2.
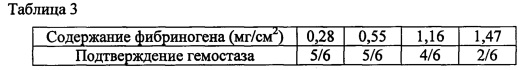
Промышленная применимость
Формованный пластинчатый продукт в соответствии с настоящим изобретением использовали в качестве гемостатического материала, и он может применяться в промышленности, производящей медицинские продукты.
| название | год | авторы | номер документа |
|---|---|---|---|
| СТЕРИЛЬНАЯ КОМПОЗИЦИЯ | 2013 |
|
RU2695522C2 |
| БЕЛКОВАЯ КОМПОЗИЦИЯ, УСТОЙЧИВАЯ К СТЕРИЛИЗАЦИИ ОБЛУЧЕНИЕМ | 2013 |
|
RU2678828C2 |
| НИЗКОЗАРЯЖЕННОЕ ВОЛОКНО И СПОСОБ ЕГО ПРОИЗВОДСТВА | 2011 |
|
RU2557623C2 |
| КОМПОЗИЦИЯ НА ОСНОВЕ ПОЛИМЕРА, ВКЛЮЧАЮЩАЯ ЦИКЛИЧЕСКИЙ КАРБОДИИМИД | 2009 |
|
RU2538602C2 |
| АРМИРОВАННАЯ РАССАСЫВАЮЩАЯСЯ СИНТЕТИЧЕСКАЯ МАТРИЦА ДЛЯ ГЕМОСТАТИЧЕСКИХ ПРИМЕНЕНИЙ | 2011 |
|
RU2574016C2 |
| СРЕДСТВО ДЛЯ ГЕМОСТАТИЧЕСКОЙ ОБРАБОТКИ РАНЫ | 2013 |
|
RU2661036C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КОМПОЗИТНОГО СФОРМОВАННОГО ВОЛОКНА ТИПА ОСТРОВА-В-МОРЕ | 2006 |
|
RU2387744C2 |
| ВОЛОКНО ИЗ ПОЛНОСТЬЮ АРОМАТИЧЕСКОГО ПОЛИАМИДА МЕТАТИПА | 2010 |
|
RU2534767C2 |
| ИСКУССТВЕННАЯ ТВЕРДАЯ МОЗГОВАЯ ОБОЛОЧКА И СПОСОБ ЕЕ ПРОИЗВОДСТВА | 2010 |
|
RU2491961C2 |
| ГЕМОСТАТИЧЕСКОЕ БИОЛОГИЧЕСКИ АБСОРБИРУЕМОЕ УСТРОЙСТВО С ПОЛИЭТИЛЕНГЛИКОЛЕМ В КАЧЕСТВЕ СВЯЗУЮЩЕГО ВЕЩЕСТВА | 2012 |
|
RU2646728C1 |

Группа изобретений относится к медицине. Описан формованный пластинчатый продукт из полимерной композиции, включающий по меньшей мере один белок, выбранный из группы, состоящей из фибриногена и тромбина, и по меньшей мере один полимер, выбранный из группы, состоящей из алифатического полиэфира и водорастворимого полимера; и ламинированный формованный пластинчатый продукт, содержащий первый слой полимерной композиции, состоящий из фибриногена и водорастворимого полимера, и второй слой полимерной композиции, состоящий из тромбина и алифатического полиэфира. Эти формованные продукты наносятся на раневой участок и функционируют в качестве гемостатического материала. Продукт обладает хорошими поддерживающими характеристиками и растворимостью для гемостатических белков и отличной гибкостью. 4 н. и 15 з.п. ф-лы, 1 ил., 3 табл., 31 пр.
1. Формованный пластинчатый продукт для адгезии тканей или для закрытия ран из полимерной композиции, содержащий по меньшей мере один белок, выбранный из группы, состоящей из фибриногена и тромбина, и по меньшей мере один полимер в виде волокна, выбранный из группы, состоящей из алифатического полиэфира и водорастворимого полимера, в котором по меньшей мере часть белка встроена в этот полимер, причем указанный формованный пластинчатый продукт из полимерной композиции получен путем удаления растворителя из суспензии, в которой диспергированы частицы по меньшей мере одного белка.
2. Формованный пластинчатый продукт по п. 1, где по меньшей мере один полимер, выбранный из группы, состоящей из алифатического полиэфира и водорастворимого полимера, выбран из группы, состоящей из производного целлюлозы, полимера, содержащего N-виниловую циклическую лактамную единицу, полиэтиленоксида, поливинилового спирта, гиалуроновой кислоты, декстрана, пуллулана, крахмала и их смеси.
3. Формованный пластинчатый продукт по п. 1, где по меньшей мере один полимер, выбранный из группы, состоящей из алифатического полиэфира и водорастворимого полимера, выбран из группы, состоящей из гидроксипропилцеллюлозы, метилцеллюлозы, гидроксиэтилцелллюлозы, гидроксипропилметилцеллюлозы, карбоксиметилцеллюлозы натрия и их смеси.
4. Формованный пластинчатый продукт по п. 1, где по меньшей мере один полимер, выбранный из группы, состоящей из алифатического полиэфира и водорастворимого полимера, выбран из группы, состоящей из полигликолевой кислоты, полимолочной кислоты, поликапролактона, их сополимера и их смеси.
5. Формованный пластинчатый продукт по любому из пп. 1-4, где формованный пластинчатый продукт является формованным пленочным продуктом или формованным волокнистым продуктом.
6. Ламинированный формованный пластинчатый продукт для адгезии тканей или для закрытия ран, содержащий первый слой полимерной композиции, состоящий из фибриногена и водорастворимого полимера, и второй слой полимерной композиции, состоящий из тромбина и алифатического полиэфира, в котором по меньшей мере часть тромбина включена в алифатический полиэфир.
7. Ламинированный формованный пластинчатый продукт по п. 6, где водорастворимый полимер является по меньшей мере одним выбранным из группы, состоящей из производного целлюлозы, полимера, содержащего N-виниловую циклическую лактамную единицу, полиэтиленоксида, поливинилового спирта, гиалуроновой кислоты, декстрана, пуллулана, крахмала и их смеси.
8. Ламинированный формованный пластинчатый продукт по п. 6, где водорастворимый полимер является по меньшей мере одним выбранным из группы, состоящей из гидроксипропилцеллюлозы, метилцеллюлозы, гидроксиэтилцеллюлозы, гидроксипропилметилцеллюлозы, карбоксиметилцеллюлозы натрия и их смеси.
9. Ламинированный формованный пластинчатый продукт по п. 6, где алифатический полиэфир является по меньшей мере одним выбранным из группы, состоящей из полигликолевой кислоты, полимолочной кислоты, поликапролактона, их сополимера и их смеси.
10. Ламинированный формованный пластинчатый продукт по любому из пп. 6-9, где первый слой полимерной композиции содержит по меньшей мере одну добавку, выбранную из группы, состоящей из фактора коагуляции XIII, альбумина, изолейцина, глицина, аргинина, глутаминовой кислоты, фенилаланина, гистидина, сурфактанта, хлорида натрия, сахароспирта, трегалозы, цитрата натрия, апротинина и хлорида кальция.
11. Ламинированный формованный пластинчатый продукт по любому из пп. 6-9, где первый слой полимерной композиции состоит из формованного пленочного продукта или формованного волокнистого продукта.
12. Ламинированный формованный пластинчатый продукт по любому из пп. 6-9, где первый слой полимерной композиции состоит из формованного пленочного продукта.
13. Ламинированный формованный пластинчатый продукт по п. 12, где формованный пленочный продукт имеет содержание водорастворимого полимера от 0,1 до 50 мас.%.
14. Ламинированный формованный пластинчатый продукт по п. 12, где формованный пленочный продукт имеет содержание фибриногена от 0,05 до 10 мг/см2.
15. Ламинированный формованный пластинчатый продукт по любому из пп. 6-9, где второй слой полимерной композиции состоит из формованного волокнистого продукта.
16. Ламинированный формованный пластинчатый продукт по любому из пп. 6-9, где фибриноген или смесь фибриногена и добавок и/или тромбин или смесь тромбина и добавок диспергирован/диспергированы в виде белковых частиц в по меньшей мере одном полимере, выбранном из группы, состоящей из алифатического полиэфира и водорастворимого полимера.
17. Ламинированный формованный пластинчатый продукт по п. 16, где массовое отношение белковых частиц к алифатическому полиэфиру составляет 10:10-100.
18. Гемостатический материал, включающий формованный пластинчатый продукт по любому из пп. 1-4 или ламинированный формованный пластинчатый продукт по любому из пп. 6-9.
19. Материал для адгезии тканей или материал для закрытия тканей, включающий формованный пластинчатый продукт по любому из пп. 1-4 или ламинированный формованный пластинчатый продукт по любому из пп. 6-9.
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
Авторы
Даты
2018-10-12—Публикация
2013-05-13—Подача