Область техники
Настоящее изобретение относится к биохимическому способу увеличения селективной выработки спирта с помощью микробиологической ферментации сахаров.
В частности, к участвующим в данном процессе микроорганизмам вводят водород в необходимой концентрации, что может иметь место при непрерывном, полунепрерывном или периодическом режиме получения, причем в указанном способе задействованы сахаристое сусло, микроорганизмы, относящиеся к родам грибов или бактерий, существующие в природе или обладающие специально селектированными или адаптированными свойствами или свойствами рекомбинантных, флокулирующих линий, находящиеся в суспензии в ферментируемом сусле или в иммобилизованном слое и в присутствии микронутриентов.
Уровень техники
Спирты представляют собой органические соединения, имеющие функциональную гидроксильную группу (-ОН), присоединенную к одному или более насыщенным углеводородам, содержащим один или более атомов углерода. Наиболее известным соединением данного класса является этанол, или этиловый спирт. Последний может содержаться в алкогольных напитках, моющих средствах, фармацевтических продуктах, таких как химические растворители, а также в продукте, относящемся к его наиболее обширной области применения, - топливе для двигателей внутреннего сгорания.
Более 90% этанола во всем мире производят путем ферментации сахаров, полученных напрямую из сырья, такого как сахарный тростник, меласса и фруктовое пюре, или образующихся непосредственно путем гидролиза крахмала и целлюлозы. Среди указанных крахмалсодержащих неочищенных и целлюлозных источников следует отметить большое разнообразие зерновых, таких как кукуруза, маниока, другие клубеньковые, сорго, пшеницу, ячмень, жмых сахарного тростника, картофель, молочную сыворотку и т.д.
Получение этанола путем ферментации и дистилляции, главным образом, разделено на 4 стадии: подготовку сырья или осахаривание, ожижение, ферментацию и дистилляцию. В производстве вина и пива стадия дистилляции отсутствует. Подготовка сырья, такая как измельчение, дробление и выщелачивание, включает прохождение источника сахара, крахмала или целлюлозы через перерабатывающие устройства. На второй стадии происходит разбавление субстратов, которые могут быть либо переработаны в процессе ферментации, либо переданы на дополнительные стадии промежуточной обработки для разрушения крахмальных или целлюлозных цепей до молекул сахаров в процессе гидролиза. Полученный сахарный сироп или сусло подвергают ферментации.
Стадия ферментации включает в себя добавление микроорганизмов, грибов или бактерий, преобразующих сахара в спирт вследствие ряда ферментативных реакций. После указанного процесса, в промышленных масштабах, которые характеризуются периодами ферментации, указанными в таблице 1, получают ферментированное сусло или вино.

Вино затем направляют на четвертую и последнюю стадию фракционной перегонки, в результате которой образуется гидратированный или безводный спирт, в зависимости от требуемых и используемых характеристик способа дистилляции и дегидратации.
Стадией, которая в большей степени непосредственно влияет на результат выработки спирта и, следовательно, является одной из наиболее изученных, является ферментация, также называемая спиртовой или этанольной ферментацией в случае 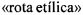 (этиловый путь), которая представляет собой биохимический процесс трансформации в спирт сахаров, таких как полисахариды и моносахариды, например, триозы, тетрозы, пентозы и гексозы, среди которых следует отметить сахарозу, глюкозу, фруктозу и ксилозу. В указанном процессе микроорганизмы отвечают за превращение сахаров в молекулы пировиноградной кислоты или пирувата в ряде внутриклеточных ферментативных реакций, обычно именуемых гликолитическим путем. Далее в анаэробных условиях происходят две другие ферментативные реакции, которыми характеризуются процесс ферментации. Первая реакция - декарбоксилирование пирувата - осуществляется с помощью фермента пируватдекарбоксилазы, посредством которого от молекулы пирувата отщепляется карбоксильная группа с превращением молекулы пирувата в молекулу ацетальдегида с выделением диоксида углерода. Вторая реакция - восстановление ацетальдегида до этанола, осуществляемое с помощью фермента алкогольдегидрогеназы, - соответственно завершает ферментативную реакцию.
(этиловый путь), которая представляет собой биохимический процесс трансформации в спирт сахаров, таких как полисахариды и моносахариды, например, триозы, тетрозы, пентозы и гексозы, среди которых следует отметить сахарозу, глюкозу, фруктозу и ксилозу. В указанном процессе микроорганизмы отвечают за превращение сахаров в молекулы пировиноградной кислоты или пирувата в ряде внутриклеточных ферментативных реакций, обычно именуемых гликолитическим путем. Далее в анаэробных условиях происходят две другие ферментативные реакции, которыми характеризуются процесс ферментации. Первая реакция - декарбоксилирование пирувата - осуществляется с помощью фермента пируватдекарбоксилазы, посредством которого от молекулы пирувата отщепляется карбоксильная группа с превращением молекулы пирувата в молекулу ацетальдегида с выделением диоксида углерода. Вторая реакция - восстановление ацетальдегида до этанола, осуществляемое с помощью фермента алкогольдегидрогеназы, - соответственно завершает ферментативную реакцию.
В основном, ферментативные процессы характеризуются тем, что в них скомбинированы субстраты, виды и штаммы микроорганизмов и в первую очередь надлежащие условия проведения процесса с целью обеспечения максимального выхода процесса и особых характеристик превращения ферментируемого сусла, поскольку оно подвергается действию различных условий, активирующих и ингибирующих ферментацию, что в свою очередь влияет на эффективность и качество самого процесса.
Выход процесса ферментации
Основными признаками, характеризующими все реакции, независимо от того, являются ли они химическими или ферментативными, являются признаки, связанными с коэффициентами превращения, или более конкретно с эффективностью или выходом, достигаемыми в результате указанных превращений. Концепция спиртовой ферментации, развитая из теории самозарождения, претерпела экспериментальные оценки и теоретические соображения, и данный процесс считается одним из наиболее результативных способов, известных из уровня техники. В сочетании с клеточной природой микроорганизмов, главным образом грибы, как эукариотические одноклеточные организмы, имеющие сходство с клетками животного происхождения, были выбраны в качестве легко доступного экспериментального объекта для изучения и понимания аэробных и анаэробных процессов дыхания (последние известны как спиртовое и молочнокислое брожение) и свободного развития.
В 1810 году Луи Жозеф Гей-Люссак сформулировал стехиометрическое уравнение, которое относилось к получению этанола и двуокиси углерода в результате спиртовой ферментации глюкозы, на сегодняшний день известное в следующем виде:
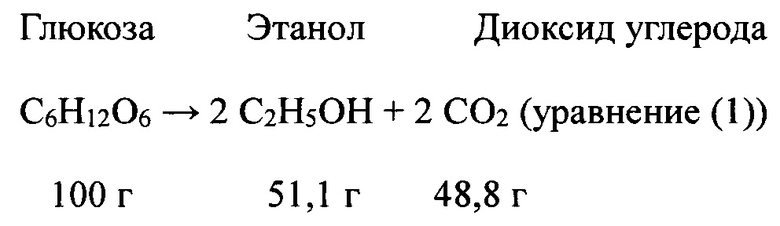
В 1863 году Луи Пастер представил концепцию действия микроорганизмов, ответственных за превращение глюкозы (моносахарида) в этанол и двуокись углерода.
Тридцать четыре года спустя, в 1897 году, Эдуард Бюхнер ферментировал сахар в лаборатории без использования живых микроорганизмов, представив концепцию действия ферментов в ферментативном процессе, рассмотренную ниже:
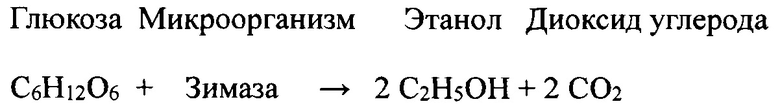
Зимаза относится к ферментативным комплексам, которые катализируют ферментацию сахара в этанол и углекислый газ.
Таким образом, Бюхнер представил гипотезу, заключающуюся в том, что дрожжевые клетки секретируют в среду белки, приводящие к ферментации сахара. В дальнейшем было показано, что указанные ферментативные реакции протекали внутри дрожжевой клетки.
Все указанные разработки согласуются с эффективностью или выходом в результате превращения сахаров в спирт, и это подтверждалось тем фактом, что в естественных условиях ферментации молекула глюкозы может образовывать до двух молекул этанола и двух молекул диоксида углерода. Такая концепция достаточно хорошо известна как выход Гей-Люссака (G-L), максимальное значение которого в процессе ферментации глюкозы составляет 51,1% (масса/масса). На фиг. 1 и 2 продемонстрирована последовательность реакций и максимальный выход при ферментации глюкозы.
С целью сравнения ниже показаны упрощенные уравнения для выхода процессов ферментации пентозы, гексозы и дисахарида (сахарозы). Дисахарид сахароза представляет собой преобладающий сахар в сахарном тростнике.
Пентоза: 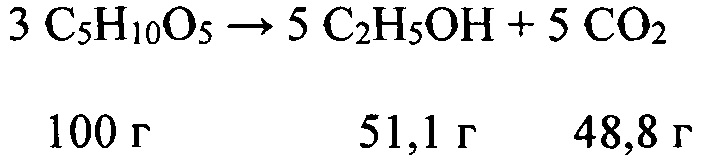
Гексоза: 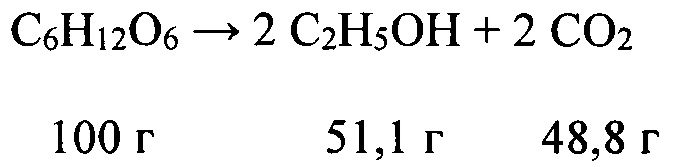
Сахароза: 
Инвертаза представляет собой фермент, который катализирует гидролиз сахарозы в гексозы, фруктозу и глюкозу, смесь которых также называют инвертированным сахарным сиропом.
В спиртовой промышленности при получении спирта путем ферментации сахаров постоянно имеет место поиск возможности увеличения выхода процесса, что предполагает полные и комплексные исследования и эксперименты в физико-химических и биологических областях. В общем случае уравнение для полного цикла процесса спиртовой ферментации с точки зрения эффективности или выхода спирта можно составить следующим образом:
[Сахар]+[Микроорганизмы]→[Этанол]+[CO2]+[Побоч. продукты]+энергия
В настоящем описании в качестве максимального реального выхода подразумевается соотношение между концентрацией получаемого этанола [этанол] и концентрацией сахаров [сахар], утилизируемых в процессе переработки.
В течение процесса ферментации свой вклад в потребление сахара могут внести микроорганизмы различной природы, такие как дрожжи и другие грибы и бактерии. Указанные микроорганизмы утилизируют сахаристый субстрат для клеточного роста популяции, а также для получения побочных продуктов, таких как кислоты и высшие спирты, переходя к побочным процессам и вызывая снижение выхода ферментации.
В 1937 году Firmin Boinot получил патент во Франции, а в 1941 году получил патент США 2230318 на способ осуществления спиртовой ферментации в промышленных условиях. В тридцатые годы указанный способ попадает в Бразилию, заметно способствует увеличению выхода ферментации, он в настоящее время широко распространен в мире и известен под названием способа Melle-Boinot, и главным образом, но не исключительно, применителен к ферментации с помощью дрожжей. Достоинством указанного способа является непосредственное одновременное снижение сахара, обеспечиваемое повторным использованием микроорганизмов и утилизацией и их возвращением в рабочий цикл, с применением центробежной сепарации, с последующей обработкой кислотой от двух до четырех часов в среде с рН от 2 до 3 в концентрированной форме, что способствует резкому снижению популяции бактерий. После указанной обработки, дрожжевое молоко, так называется центрифугат дрожжей, концентрируют и обрабатывают перед возвращением в процесс. Указанная операция может привести к сокращению потребления сахара до менее 1% (одного процента) от доступного сахара.
Диоксид углерода, как продукт, получаемый при декарбоксилировании пирувата, рассматривается в качестве параллельного продукта ферментативного процесса.
В этой связи побочные продукты, образуются в результате побочных процессов, как описано выше, остальные продукты образуются в процессе спиртовой ферментации, такие как: глицерин, органические кислоты (янтарная, уксусная, пировиноградная кислоты и другие) и высшие спирты, ацетальдегид, ацетон, бутиленгликоль и другие соединения. По оценкам, от 3% до 5% (от трех до пяти процентов) сахара, доступного в процессе, утилизируется в результате указанных превращений.
В энергетических единицах, для демонстрации, в анаэробных условиях, дрожжи изменяют свой метаболизм в направлении спиртовой ферментации (спиртового брожения), при котором этанол и диоксид углерода представляют собой два единственных продукта всего процесса. Таким образом, следует, что:
С6Н12О6+2Pi+2АДФ→2С2Н5ОН+2CO2+2H2O+2АТФ
(ΔG0=-56 ккал / моль)
С другой стороны, в аэробных условиях, особенно в фазе клеточного размножения, происходит дыхание дрожжей. В отличие от ферментации, которая осуществляется в цитоплазме, дыхание, которое происходит в митохондриях, приводит к образованию количества АТФ (аденозинтрифосфата) (подразумевается энергетический обмен) в девятнадцать раз больше полученного при спиртовом брожении, что продемонстрировано ниже:
C6H12O6+6O2+38Pi+38АДФ→6CO2+38АТФ+6H2O
(ΔG0=-686 ккал/моль)
По-прежнему принимаются множество действий на протяжении процесса ферментации в качестве мероприятий по сокращению потребления сахаров в побочных процессах и нежелательных побочных продуктов. Контроль рН и температуры ферментируемого сусла, а также контроль присутствия микронутриентов и контаминирующих веществ, представляют собой показатели, которые предполагают значимые позиции процесса и могут стимулировать или ингибировать биохимическую динамику.
Низкий уровень рН среды (рН<4,0), в частности, связанный с высокой температурой эксплуатации (Тор>38°С), оказывается фактором наибольшего значения для физиологии дрожжей, полученных и используемых в установках промышленного производства этанола, по сравнению с другими ингибиторами, такими как сульфиты, молочная кислота, содержание спирта и высокие концентрации сахаров). рН 4,5 сусла при температуре от 20°С до 37°С, обеспечивает защиту от стресс-факторов, и приводит к увеличению жизнеспособности клетки, почкованию, выходу спирта, нормальной морфологии дрожжей, снижению остаточного сахара и снижению высвобождения аминокислот в среду, обеспечивая улучшение продуктивности по спирту и стабильность процесса.
В отношении питания дрожжи представляют собой гетеротрофные микроорганизмы, которые питаются путем абсорбции. Основные питательные вещества, необходимые для развития дрожжей, удовлетворительного протекания процесса ферментация, представляют собой: (I) азот, пластичный преобразующийся элемент, необходимый для роста дрожжей; (II) фосфор, элемент для переноса энергии - при его отсутствии ферментация не будет происходить; (III) калий, (IV) магний; (V) цинк; (VI) марганец, все из которых имеют важное значение в ферментативных реакциях; витамины группы В, которые ускоряют ферментацию, помимо присутствия других солей, таких как соли кобальта, меди, серы, бора, которые относятся к микронутриентам.
Дрожжи также представляют собой сапрофитные микроорганизмы, которые требуют сложного источника углерода - глюкозы или другого сахара, которые поставляет химическую энергию и карбоновый скелет для их клеточных структур, состоящих преимущественно из углерода, кислорода и водорода. Помимо указанного требуются некоторые витамины, такие как тиамин и пантотеновая кислота.
Что касается источника азота, дрожжи используют указанный элемент в аммиачной (NH4+), амидной (мочевина) или аминной (в виде аминокислот) форме, отсутствует метаболическая способность использовать нитраты и частично или полностью отсутствует способность использования белков из среды.
Поскольку аммиачная форма является преобладающей, при ее отсутствии дрожжи ищут другие формы, такие как аминокислоты, тем самым вызывая увеличение производства вторичных продуктов, таких как изоамиловый, амиловый, пропиловый, изопропиловый, бутиловый, изобутиловый спирты. Фосфор абсорбируется в виде ионов Н2РО4-, главным образом при рН 4,5, в то время как сера может быть ассимилирована из сульфата, сульфита или тиосульфата. При использовании серной кислоты в обработке дрожжей по способу, представленному выше, или при использовании мелассы в смешанном сусле, можно исключить дополнительного использования серы, которая при избытке оказывает летальное воздействие на микроорганизмы, хотя присутствие серы представляется достаточным условием для осуществления способа.
На основании вышеизложенного и принимая во внимание, к примеру, указанный выход спиртовой ферментации по глюкозному субстрату или непосредственно ферментируемого сахара, при максимальном теоретическом массовом выходе GL 0,511 масс/масс, в соответствии с уравнением (1), в качестве 100% максимального теоретического выхода, фактический выход способа ферментации может достигать максимальных значений в пределах от 92% до 94% и, более того, в максимально асептических и контролируемых производственных условиях. В оборудовании со сниженными контролем и асептикой, указанное значение может составлять менее 85%, что подразумевает значительные потери в производственном процессе.
В связи с указанным обстоятельством, постоянно осуществляют поиск всевозможных мер повышения эффективности, сосредоточенный на улучшении и соответствии производственного контроля, штаммов и свойств микроорганизмов, селектированных, комбинированных и модифицированной, с более высокой продуктивностью и повышенной устойчивостью к технологической среде. Увеличение выхода ферментации от 0,1% до 0,5% уже оправдывает значительные капиталовложения, ввиду большого количества спиртовой продукции в указанных сферах промышленности.
Развитие существующего уровня техники
Разработаны различные документы для увеличения выхода процесса получения этанола, в соответствии с примерами, указанными в настоящем описании:
В документе US 4451566 описаны способы и устройство для ферментативного получения этанола из ферментируемых сахаров. Последовательность ферментов для каталитического превращения сахаров в этанол сохраняется в разнообразных зонах реакции. Ферментируемый сахарный раствор последовательно проходит через указанные зоны, и получение спирта происходит в последней зоне. Несмотря на то, что данный способ обеспечивает более эффективную реакцию по сравнению с традиционным способом, указанный документ относится к дорогому, сложному и трудному в обслуживании решению.
В заявке на патент WO 2007/064546 описан способ повышения выхода этанола, позволяющий уменьшить время ферментации и снизить образование побочных продуктов путем мониторинга и управления окислительно-восстановительным потенциалом в ферментаторе. Тем не менее, указанный способ требует очень специфичного и сложного в обслуживании мониторинга за счет высоких расходов, снижающих промышленное применение указанного решения.
В патентном документе WO 2008/024331 описан способ магнитной ферментации, который подразумевает, что биологический материал подвергают воздействию статического магнитного поля для осуществлении ферментации биологического материала в ферментированный продукт. Реакция ферментации может проходить в щелочной или кислой среде, а магнитное поле может быть положительным или отрицательным. В указанном документе применяют статическое магнитное поле, чтобы сделать среду более пригодной для размножения клеток микроорганизмов. Несмотря на увеличение количества микроорганизмов при спиртовой ферментации, повышающее выход реакции, за указанным процессом необходимо постоянное наблюдение и осуществление полного контроля над реакцией, что делает его слишком дорогим и, следовательно, экономически нецелесообразным для промышленного применения.
В известном уровне техники также раскрыты способы повышения эффективности улавливания диоксида углерода, как описано в патенте США 8377665. Указанный способ включает ферментацию бактериями с использованием газообразных субстратов согласно метаболическому пути Вуда-Льюнгдаля, включающему последовательность ферментативных реакций, происходящих в бактериальных культурах.
Несмотря на то, что существует множество библиографических ссылок, которые описывают ферментативные процессы, повышающие выход получения этанола, в известном уровне техники детально не описано действие водорода в метаболическом процессе ферментации для селективного производства, указанный способ составляет инновационную и оригинальную технологию. Более того, все разработанные способы претендовали на повышение фактического выхода до теоретического ограничения G-L выхода.
Задачи настоящего изобретения
Задачей настоящего изобретения является обеспечение способа микробиологической ферментации сахаристых субстратов, который включает введение водорода в микроорганизмы родов, относящихся к грибам или бактериям, с природными характеристиками, или специально селектированным или адаптированым, или рекомбинантным, флокулирующим линиям, или к суспензии, находящейся в ферментируемом сусле или в иммобилизованном слое.
Вторая задача изобретения заключается в применении водорода в ионном, атомарном или газообразном состоянии, или их смеси, для введения водорода в микроорганизмы родов, относящихся к грибам или бактериям, с природными характеристиками, или специально селектированным или адаптированым, или рекомбинантным, флокулирующим линиям, или к суспензии, находящейся в ферментируемом сусле или в иммобилизованном слое для селективного производства спирта.
Третья задача настоящего изобретения заключается в разработке оригинального биохимического способа селективного производства спирта путем ферментации сахаров, таких как полисахариды и моносахариды, например, триозы, тетрозы, пентозы и гексозы, причем предпочтительными являются сахароза, глюкоза, фруктоза и ксилоза, с более полной утилизацией углерода и, как следствие, увеличением селективного производства спирта, которое превышает теоретический выход G-L, а также сокращением выделения диоксида углерода в процессе ферментации.
Под термином «атомарное или ионное состояние» в настоящем описании понимается водород в атомарной (Н) или ионной (Н+) форме.
Под термином «газообразное состояние» в настоящем описании понимается молекулярный водород (H2).
Четвертая задача настоящего изобретения заключается в создании эффективного и экологически целесообразного способа с увеличением утилизации углерода при превращении сахаров в спирт процессе ферментации и одновременным снижением выделения диоксида углерода в окружающую среду.
Пятая задача настоящего изобретения заключается в устранении предела производительности на более высоких уровнях, преобразовании клеточного метаболизма микроорганизмов без их генетического изменения.
В силу своей простоты, экономичности и эффективности способ согласно настоящему изобретению может быть применен в новых промышленных установках для производства, или реализован на уже установленных конструкциях и установках.
Краткое описание изобретения
Настоящее изобретение относится к способу получения микробилогической ферментации сахаристых субстратов, который включает введение водорода в микрооорганизмы родов, относящихся к грибам или бактериям, находящиеся в суспензии в ферментируемом сусле или в иммобилизованном слое, причем указанное ферментируемое сусло или иммобилизованный слой содержат сахаристый субстрат и микронутриенты.
Введение водорода в атомарном, ионном или газообразном состоянии в микроорганизмы, осуществляющие ферментацию, происходит при помощи по меньшей мере двух электродов, которые непосредственно погружают в ферментируемое сусло или иммобилизованный слой, с подачей напряжения в режиме предварительного или полного электролиза. Указанный газообразный водород также образуется в биореакторе путем электролиза воды, и в указанном случае происходит инокуляция микроорганизмов посредством прямой подачи в указанный биореактор.
Управление водородом, находящимся в атомарном, ионном или газообразном состоянии осуществляют посредством подачи напряжения к электродам, воздействующим на ферментируемое сусло или иммобилизованный слой, напряжение в режиме предварительного электролиза находится в диапазоне от 0,1 В до 1,24 В, а напряжение в режиме полного электролиза находится в диапазоне от 1,24 В до 30 В постоянного или переменного тока, частота последнего составляет от 50 Гц до 100 Гц, от 100 Гц до 500 Гц, и от 500 Гц до 1000 Гц.
Настоящее изобретение также относится к применению водорода в атомарном, ионном или газообразном состоянии или их смеси, характеризующееся тем, что указанный водород предназначен для введения в микроорганизмы, находящиеся в ферментативной среде, содержащей сахаристые субстраты, такие как полисахариды и моносахариды, такие как триозы, тетрозы, пентозы и гексозы, среди которых предпочтительными являются сахароза, глюкоза, фруктоза и ксилоза, для селективной выработки спирта.
Способ, описанный в настоящем изобретении, состоит, таким образом, в изменении ограничения эффективности выработки спирта по массе до более высоких параметров путем преобразования клеточного метаболизма микроорганизмов без их генетических изменений. Восстановительное действие водорода в сочетании с легким проникновением через клеточные мембраны микроорганизмов с достижением их внутренних компартментов, цитоплазмы, митохондрий и внутриклеточных органелл обеспечивает инновационный биохимический способ селективной выработки спирта путем ферментации сахаров, приводящий к более эффективному использованию углерода с последующим увеличением выхода спирта в реакции ферментации и уменьшением выделения диоксида углерода.
Описание чертежей
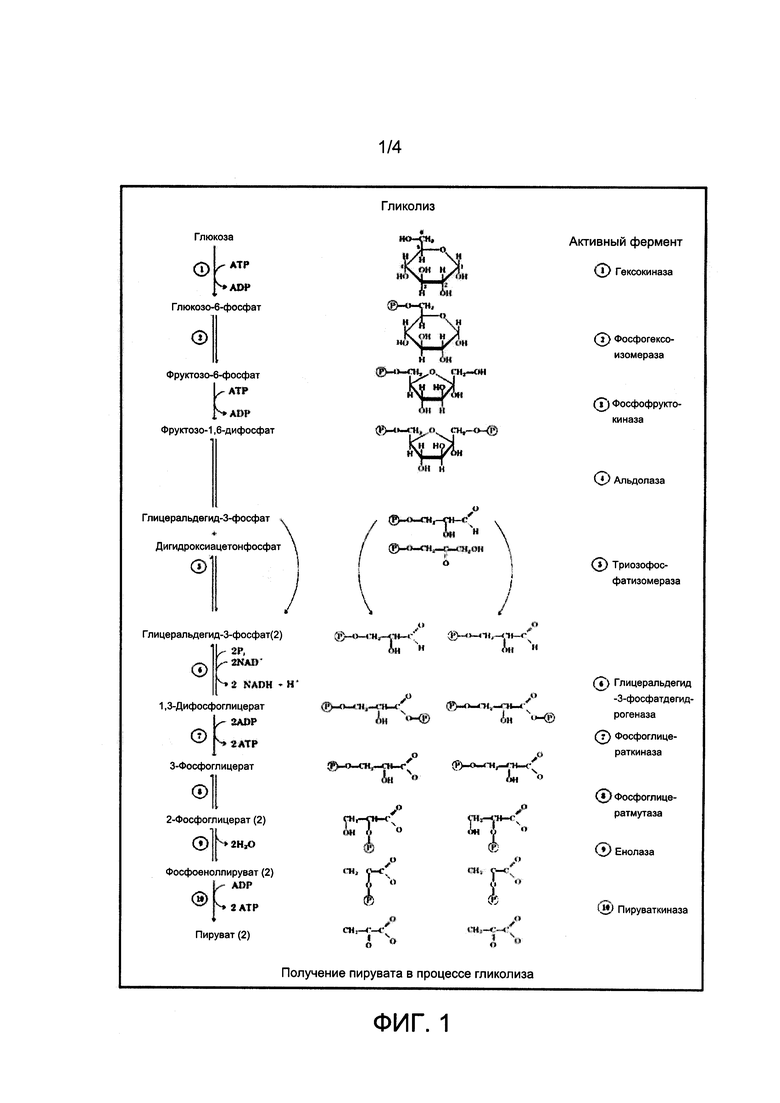
Фиг. 1 относится к гликолитическому метаболическому пути (гликолизу), известному из уровня техники, происходящему в цитоплазме микроорганизма или эукариотической или прокариотической клетки при преобразовании глюкозы, включающем последние этапы указанной последовательности - получение пирувата.
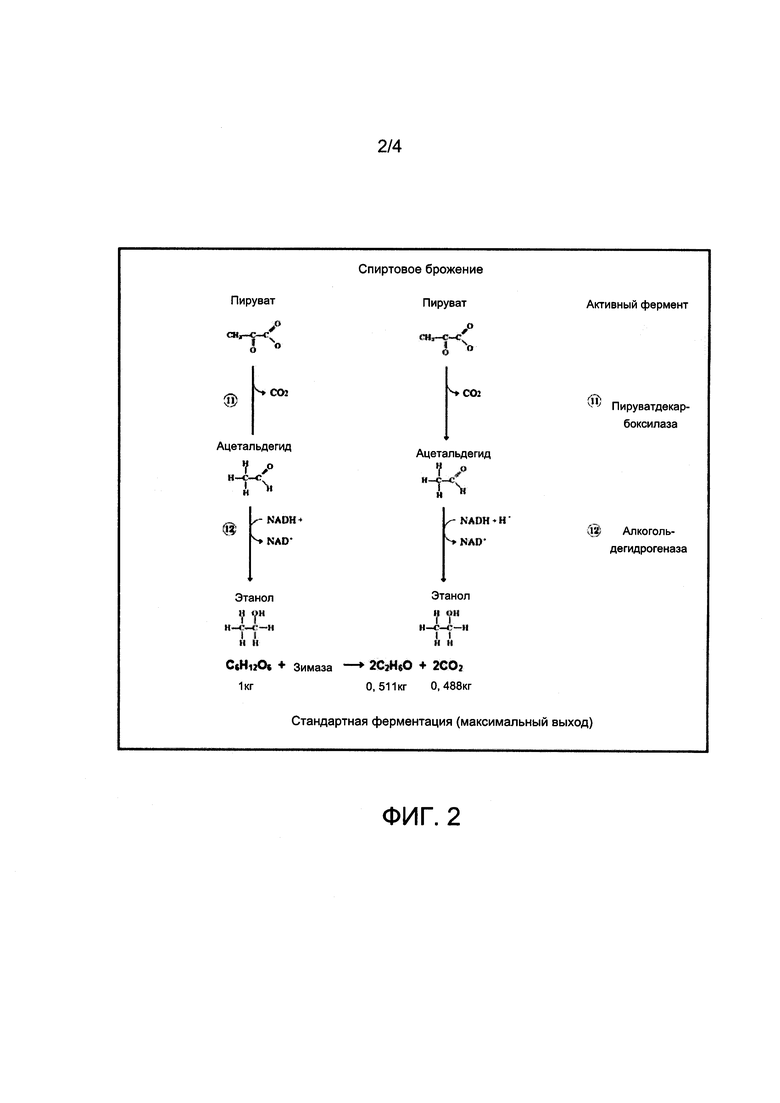
На фиг. 2 схематично представлены реакции спиртовой ферментации, имеющие место в способе ферментации, известном из уровня техники, согласно которому от каждой молекулы пирувата под действием пируватдекарбоксилазы отщепляется карбоксильная группа, соответственно высвобождаются молекулы диоксида углерода и молекулы ацетальдегида, и последний превращается в этанол под действием фермента алкогольдегидрогеназы.
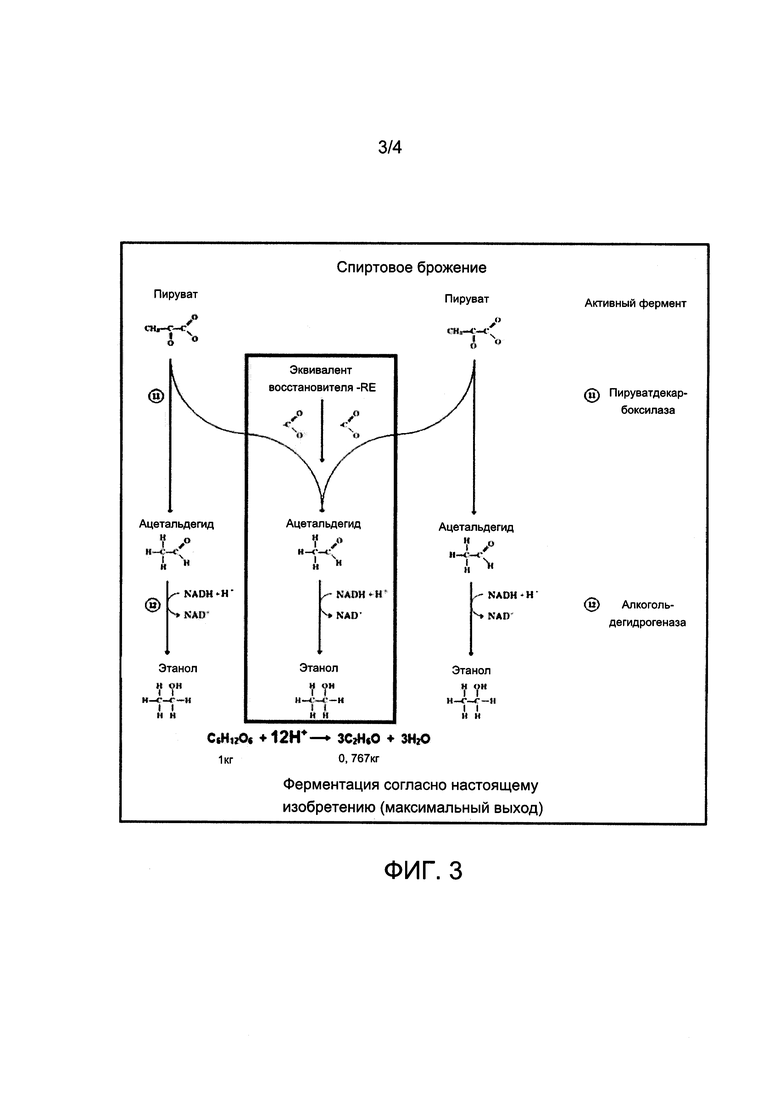
На фиг. 3 схематично представлены реакции ферментации, имеющие место в способе, описанном в настоящем изобретении, согласно которому происходит восстановление карбоксильной группы с помощью гидроксильной группы, полученной путем декарбоксилирования двух молекул пирувата под действием фермента пируватдекарбоксилазы, в дополнение к эквивалентам восстановителя, предпочтительно восстанавливаемых путем повышения доступности водорода, приводящего к образованию молекулы ацетальдегида, синтезируемого за счет двух карбоксильных групп, в качестве продукта нового пути спиртовой ферментации.
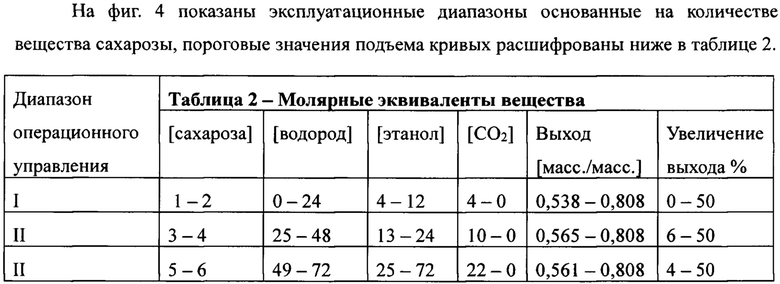
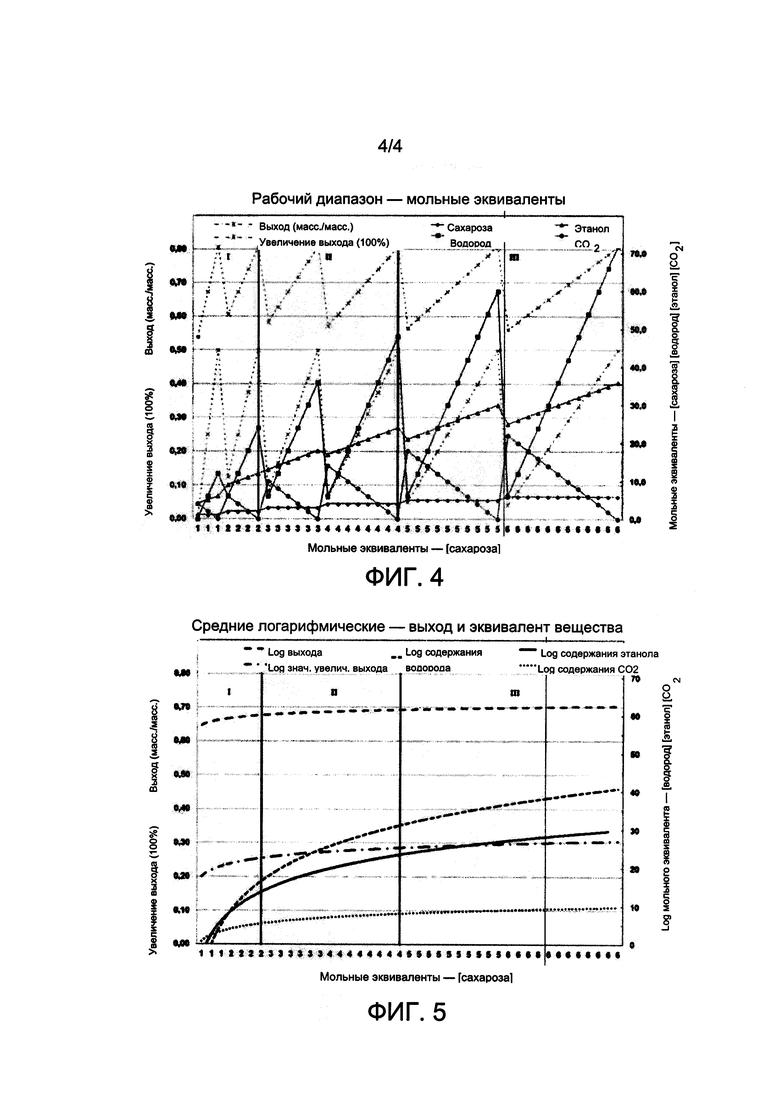
Фиг. 4 относится к графику, содержащему рабочие диапазоны, основанные на молярных эквивалентах вещества, согласно настоящему изобретению, содержащие границы кривой для сахарозы, водорода, этанола, диоксида углерода, массового (масс./масс.) выхода и увеличения массового выхода по отношению к G-L (%) максимальному массовому теоретическому выходу сахарозы в соответствии с уравнением (3).
Фиг. 5 относится к графику, содержащему логарифмические параметры кривых массового выхода, процентного увеличения по массовому выходу и по концентрации, в настоящем изобретении выраженной в молярных эквивалентах вещества для [водорода], [этанола] и [СО2].
Подробное описание изобретения
Как было описано ранее, способы получения спирта путем ферментации сахаров, известны к настоящему времени специалистам в указанной области техники и повсеместно применяются в их пределах эффективности согласно стехиометрическому уравнению, составленным Гей-Люссаком в 1810 году (уравнение (1)). Согласно указанному выражению в современном известном уровне техники молекула глюкозы при ферментации способна образовывать максимум 2 молекулы этилового спирта и 2 молекулы диоксида углерода, как показано в уравнении (2).
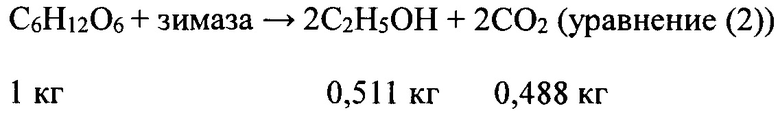
В свою очередь, принимая во внимание ферментацию сахарозы, содержащейся в значительной степени в сахарах сахарного тростника, получим альтернативное следующее уравнение:
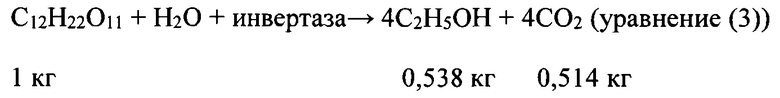
Как следует из уравнений (2) и (3), условие максимальной массовой эффективности - 0,511 (масс./масс.) при ферментации глюкозы и 0,538 масс./масс. при ферментации сахарозы. Даже путем более поздних условий уравнения, рассматривающего влияние ферментативной реакции, указанные ограничения рассматривались в оценке глобального выхода в способах, имеющихся в современном известном уровне техники.
В соответствии с предшествующим уровнем техники, в гликолитическом метаболическом пути, именуемым также гликолизом, представляющим собой последовательность ферментативных реакций, которые происходят в цитоплазме клетки микроорганизма, представляющего собой эукариотический или прокариотический одноклеточный организм, в процессе переработки глюкозы (сахара с шестью атомами углерода в молекуле), на последних этапах указанной последовательности имеет место получение пирувата:
(иона 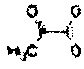 ), кислотообразующего, содержащего 3 (три) атома углерода, что показано на фиг. 1. Из указанных реакций, таким образом, две молекулы пирувата образуются начиная с молекулы глюкозы. Затем, в анаэробном режиме, в отсутствии кислорода, имеет место спиртовая ферментация. В указанном способе ферментации, из каждой молекулы пирувата под действием пируватдекарбоксилазы, происходит отщепление карбоксильной группы, а также последующее высвобождение молекулы диоксида углерода и молекулы ацетальдегида, после чего последний превращается в этанол под действием фермента алкогольдегидрогеназы, что показано на фиг. 2. Указанные ферментативные реакции представляют собой обратимые реакции.
), кислотообразующего, содержащего 3 (три) атома углерода, что показано на фиг. 1. Из указанных реакций, таким образом, две молекулы пирувата образуются начиная с молекулы глюкозы. Затем, в анаэробном режиме, в отсутствии кислорода, имеет место спиртовая ферментация. В указанном способе ферментации, из каждой молекулы пирувата под действием пируватдекарбоксилазы, происходит отщепление карбоксильной группы, а также последующее высвобождение молекулы диоксида углерода и молекулы ацетальдегида, после чего последний превращается в этанол под действием фермента алкогольдегидрогеназы, что показано на фиг. 2. Указанные ферментативные реакции представляют собой обратимые реакции.
Таким образом, в соответствии с предшествующим уровнем техники, существует взаимосвязь максимального получения двух молекул этанола и двух молекул диоксида углерода из каждой молекулы сахара глюкозы в процессе спиртовой ферментации, именуемой также этиловой ферментацией.
Таким образом, восстановление карбоксильной группы:
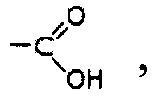
представляющей собой производное от объединения карбонильной группы
(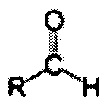 ), радикала кетонов и альдегидов, с гидроксильной группой (ОН), радикала спиртов и фенолов, полученного путем декарбоксилирования двух молекул пирувата с помощью фермента пируватдекарбоксилазы, в дополнение к восстанаваливающим эквивалентам - RE/ER, предпочтительно восстанавливаемых высоко доступным или избыточным водородом, что приводит к образованию молекулы ацетальдегида, синтезированного с промежуточным образованием двойной карбоксильной группы в качестве продукта нового пути спиртовой ферментации. При избытке водорода, происходит увеличение концентрации коферментов NADH, NADPH и FADH2 среди других необходимых переносчиков электронов в цитоплазматических или митохондриальных окислительно-восстановительных процессах. Следующие уравнения демонстрируют окислительно-восстановительные процессы, осуществляемые при участии указанных коферментов:
), радикала кетонов и альдегидов, с гидроксильной группой (ОН), радикала спиртов и фенолов, полученного путем декарбоксилирования двух молекул пирувата с помощью фермента пируватдекарбоксилазы, в дополнение к восстанаваливающим эквивалентам - RE/ER, предпочтительно восстанавливаемых высоко доступным или избыточным водородом, что приводит к образованию молекулы ацетальдегида, синтезированного с промежуточным образованием двойной карбоксильной группы в качестве продукта нового пути спиртовой ферментации. При избытке водорода, происходит увеличение концентрации коферментов NADH, NADPH и FADH2 среди других необходимых переносчиков электронов в цитоплазматических или митохондриальных окислительно-восстановительных процессах. Следующие уравнения демонстрируют окислительно-восстановительные процессы, осуществляемые при участии указанных коферментов:
Восстановление кофермента никотинамидадениндинуклеотида
НАД++Н++2е-↔НАДН (уравнение (4))
Восстановление кофермента никотинамидадениндинуклеотидфосфата
НАДО+Н++2е-↔НАДФН (уравнение (5))
Восстановление кофермента флавинадениндинуклеотида
ФАД++2Н++2е-↔FADH2 (уравнение (6))
Затем молекула ацетальдегида восстанавливается до молекулы этанола с помощью восстанавливающего действия фермента алкогольдегидрогеназы, как показано на фиг. 3.
Таким образом, настоящее изобретение позволяет получить типичные и упрощенные уравнения, такие как нижеследующее уравнение (7), для типичных концентраций сахаров, водорода, микроорганизмов и продуктов, полученных в указанном типе ферментации, таких как концентрации этанола, диоксида углерода и воды:
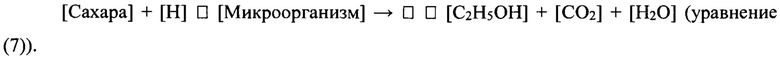
Термины 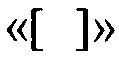 обозначают соответствующие концентрации сахаров, водорода, живых микроорганизмов, этанола, диоксида углерода и воды, агентов и продуктов спиртовой ферментации в присутствии водорода, в типичной реакции ферментации сахаристого сусла, с применением дрожжей, эукариотических одноклеточных грибов. Символ «
обозначают соответствующие концентрации сахаров, водорода, живых микроорганизмов, этанола, диоксида углерода и воды, агентов и продуктов спиртовой ферментации в присутствии водорода, в типичной реакции ферментации сахаристого сусла, с применением дрожжей, эукариотических одноклеточных грибов. Символ « » предназначен для демонстрации введения водорода в микроорганизм.
» предназначен для демонстрации введения водорода в микроорганизм.
Указанный принцип изобретения, наряду с общим уравнением (7), также применяется в ферментации, предусматривающей применение бактерий, прокариотических клеток при переработке углеводов, таких как полисахариды и моносахариды, например триоз, тетроз, пентоз и гексоз, причем предпочтительными являются сахароза, глюкоза, фруктоза и ксилоза, в селективной выработке этанола или высших спиртов.
В силу своей простоты, экономичности и эффективности, указанное изобретение может применять на новом производственном оборудовании, или внедрять на уже установленные конструкции и оборудование.
Настоящее изобретение относится, таким образом, к биохимическому способу повышения селективного выхода получения спирта за счет модификаций и усовершенствований на стадии ферментации растворов, содержащих сахара, с применением ферментативных микроорганизмов родов грибов или бактерий. Указанные усовершенствования включают введение водорода в атомарной, ионной форме или их смесей, растворенных в воде к микроорганизмам, участвующим в реакции ферментации сахаристого сусла.
Указанный способ включает в себя добавление от 5% до 30% (масса/объем) сахаристых субстратов, от 5% до 25% (масса/объем) микроорганизмов. Подача микроорганизмов завершается автоматически и контролируется в зависимости от их необходимого содержания и содержания микроорганизмов, участвующих в переработке ферментируемого сусла.
Для введения водорода необходима система для получения указанного водорода, включающая:
i. подачу преэлектролизного напряжения в ферментативную среду с помощью электродов, указанное напряжение имеет меньшие значения, чем напряжение, необходимое для возникновения электролиза воды в среде, свойственное ионному состоянию ферментируемого сусла, предпочтительно от 0,1 В до 1,124 В или
ii. подачу в ферментативную среду напряжения, осуществляющего полный электролиз воды, свойственное ионному состоянию ферментируемого сусла, предпочтительно в диапазоне от 1,24 В и 30 В, более предпочтительно от 1,24 В до 20 В и наиболее предпочтительно от 1,24 В и 10 В;
iii. получение водорода вне реактора, происходящее за счет электролиза воды при напряжении от 1,5 В до 30 В.
Электроды, применяемые для ферментативной среды включают по меньшей мере один катод и один анод, где указанные катод и анод предпочтительно эксплуатируют непосредственно в ферментируемом сусле.
В одном из вариантов реализации настоящего изобретения электроды, анод и катод, воздействуют непосредственно на микроорганизмы на стадии их загрузки в биореактор.
Во втором варианте реализации изобретения электроды, используемые в ферментативной среде, включают по меньшей мере один катод и один анод, причем катод предпочтительно погружают непосредственно в ферментируемое сусло, а анод может быть погружен в другой электролит, где последний представляет собой альтернативный солевой раствор, т.е. в два электролита, разделенных ионной проницаемой разделительной мембраной.
Сахаристое сусло содержит сахара, такие как полисахариды и моносахариды, такие как триозы, тетрозы, пентозы и гексозы, причем предпочтительными являются сахароза, глюкоза, фруктоза и ксилоза, или их смеси.
В одном из вариантов осуществления настоящего изобретения, микроорганизмы для ферментации, используемые в настоящем изобретении, выбраны из дрожжевых групп грибов, таких как род Saccharomyces, а точнее из штаммов Saccharomyces cerevisiae и видов родов Schizosaccharomycespombe, Pichia stipites, Torula, Candida shehatae, линий, встречающихся в природе, или специально селектированных или адаптированых, или рекомбинантных, флокулирующих линий, находящихся в виде суспензии в ферментируемом сусле или в иммобилизованном слое.
Во втором варианте реализации изобретения микроорганизмы для ферментации выбраны из группы, включающей бактерии, точнее, такие виды родов Zymomonas mobilis, Escherichia coli и Clostridium, линий, встречающихся в природе, или специально селектированных или адаптированых, или рекомбинантных, флокулирующих линий, находящихся в виде суспензии в ферментируемом сусле или в иммобилизованном слое.
В предпочтительном варианте реализации изобретения, селектированные микроорганизмы для ферментации включают грибы вида Saccharomyces cerevisiae.
В альтернативном предпочтительном варианте реализации изобретения, ферментативные селектированные микроорганизмы содержат бактерии вида Zymomonasmobilis.
Ферментация сусла также допускает добавление микронутриентов, таких как азот, фосфор, калий, магний, кальций, цинк, марганец, медь, железо, сера, кобальт, йод или их смеси.
Микроорганизмы добавляют в переменном содержании и регулируют по мере требования.
В частности, способ согласно настоящему изобретению заключается во введении атомарного, ионного или молекулярного водорода в адекватных концентрациях, указанный водород получен в условиях предварительного или полного электролиза, к микроорганизмам во время процесса, управляемого способом в соответствии с уравнением (7), таблицей 2 и фигурой 4. В настоящем изобретении предусмотрены периодический режим, непрерывный и полунепрерывный процессы ферментации, а также возможно внедрение схем биореакторов, в количестве и объемах, для аналогичных или различающихся функций по их условиям эксплуатации, концентраций субстратов, микроорганизмов и доступности вводимого водорода в ионном или молекулярном состояниях.
Несмотря на то, что пути превращений сахаров в спирты, как в анаэробных, так и аэробных режимах, в присутствии грибов или бактерий в средах с избыточной концентрацией водорода окончательно и теоретически до сих пор не установлены, уже возможно наблюдение селективной выработки веществ, участвующих в указанных дыхательных и ферментативных процессах.
Сравнительные эксперименты показали в настоящем изобретении значение теоретического увеличения выхода получения этанола до 50%, приводящие к максимальной массовой теоретической эффективности 0,8 масс./масс. при ферментации сахаров (сахарозы) дрожжами Saccharomyces cerevisiae с последовательным уменьшением выделения диоксида углерода до 100%.
В настоящем изобретении, с в результате проведенных экспериментов, отмечено, что в этиловом пути ферментации сахаров дрожжами, две молекулы пирувата, образующихся в результате гликолиза, при их декарбоксилировании под действием фермента пируватдекарбоксилазы, активизируется отщепление двух карбоксильных групп
(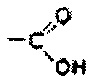 ), которые впоследствии восстанавливаются за счет восстановительных эквивалентов - ER/RE, под действием водорода, присутствующем в среде в избыточном количестве, способны к образованию другой молекулы ацетальдегида, от которого отщепляется молекула воды под действием фермента алкогольдегидрогеназы при восстановлении до этанола, что приводит к селективному повышению (как указано в исходном тексте). В результате происходит снижение выделяемого диоксида углерода, что можно предположить из фиг. 3.
), которые впоследствии восстанавливаются за счет восстановительных эквивалентов - ER/RE, под действием водорода, присутствующем в среде в избыточном количестве, способны к образованию другой молекулы ацетальдегида, от которого отщепляется молекула воды под действием фермента алкогольдегидрогеназы при восстановлении до этанола, что приводит к селективному повышению (как указано в исходном тексте). В результате происходит снижение выделяемого диоксида углерода, что можно предположить из фиг. 3.
В то время как увеличение получения этанола может достигать теоретического предела 50%, снижение диоксида углерода может достигнуть результата предельного теоретического уровня 100% относительно стандартного способа. Далее в указанной ферментативной модели, внезапное увеличение концентрации сахара при переработке внутри клетки в результате увеличения концентрации доступного водорода является причиной усложнения ферментативных реакций, что можно подтвердить снижением кинетики реакции, приводящим к увеличению времени ферментации.
Присутствие водорода в ферментационной среде возможно в атомарном, ионном или газообразном состоянии, или их смеси. Для получения водорода необходима система для генерации водорода, и указанная система может включать в себя: (I) подвергание ферментативной среды электрическому напряжению предварительного электролиза (напряжение ниже напряжения, необходимого для возникновения электролиза воды, характеризующееся ионными условиями ферментируемого сусла) или (II) подвергание ферментативной среды напряжению для полного электролиза, равному или превышающему напряжение для электролиза воды, характеризующееся ионными условиями ферментируемого сусла.
В режиме предварительного электролиза, происходит образование ионов и атомарного водорода, без образования газообразного водорода. Образование указанного ионного и атомарного водорода требует всего лишь меньшего электрического напряжения, чем необходимо для возникновения электролиза воды, которое характеризуется ионными условиями ферментируемого сусла. Указанное электрическое напряжение находится в диапазоне от 0,1 В до 1,24 В, предпочтительно, от 0,7 В до 1,1 В.
Системы для генерации водорода предварительным и полным электролизом могут быть осуществлены таким образом, что электрический ток будет постоянным или переменным, причем последний может быть с частотой в пределах от 50 до 2000 Гц, предпочтительно от 50 Гц до 150 Гц, или от 100 Гц до 500 Гц или 400 Гц до 1000 Гц.
В одном из вариантов осуществления настоящего изобретения, система включает в себя постоянный ионный ток в условиях полного электролиза, избегая добавления кислорода в ферментируемое сусло, чтобы способствовать анаэробным условиям. Предпочтительно катод воздействует непосредственно на ферментируемое сусло, в то время как анод будет эксплуатироваться в другом электролите, где последний представляет солевой раствор, что соответствует двум электролитам в среде, разделенной ионопроницаемой разделительной мембраной, мембрана содержит поры и изготовлена предпочтительно из пористого материала.
После запуска системы генерации водорода, в реакторе, работающем в полунепрерывном, непрерывном или периодическом режиме, для осуществления способа важно непрерывное контролирование измерений рН, температуры, концентрации сахара, концентрации водорода, концентрации живых микроорганизмов, концентрации спирта, концентрации диоксида углерода и содержания и концентрации микронутриентов.
В дополнение или исключительно, водород в газовой фазе может быть введен непосредственно в биореактор во время ферментации, путем непосредственной подачи в ферментируемое сусло, находящееся в биореакторе, или через контуры подачи питательного субстрата или циркуляции сусла в биореакторе. Указанный газообразный водород может быть получен с помощью ферментации бактериями или водорослями в альтернативных параллельных ферментативных процессах, характеризующимися получением водорода, или путем электролиза воды вне реактора, или также может иметь место водород для промышленного применения.
Далее следует обратить внимание, что водород может быть введен либо сразу в начале процесса ферментации или до указанного этапа, а именно на этапе подготовки микроорганизмов.
Способ, описанный в настоящем изобретении, отражает характер эксплуатации, отличающийся от способов ферментации известного уровня техники, например:
- высокая доза водорода действует как сильнодействующий восстановитель;
- способ обеспечивает лучший выход по концентрации спирта;
- отсутствует генетическая модификация микроорганизмов;
- имеет место последовательное уменьшение доли выделяющегося диоксида углерода; а также
- имеет место изменение кинетики реакции.
Более того, способ согласно настоящему изобретению предусматривает следующие преимущества в сравнении со стандартным способом ферментации:
1. Способ предусматривает легкую диффузию водорода через клеточную мембрану микроорганизмов, грибов или бактерий, обеспечивая возможность проникновения во внутриклеточные компартменты;
2. Способ не влияет на физиологические параметры клетки (температуру, давление, рН и рО2);
3. Способ не оказывает препятствий окислительным реакциям метоболизма, не оказывает отрицательного воздействия на рекационноспособные частицы активных форм кислорода и передачу клеточных сигналов;
4. Высокие концентрации водорода хорошо переносятся и, следовательно, оказывают минимальное количество побочных эффектов на организм клетки; а также
5. Способ может быть применен при ферментации в полунепрерывном, непрерывном, периодическом режиме, легко адаптирован к существующим способам и оборудованию для ферментации.
Управление способом и выходом продуктов согласно настоящему изобретению
В соответствии с общим уравнением (7) способ ферментации в настоящем описании предусматривает и требует оперативного управления переменными технологическими параметрами.
В соответствии с общим уравнением (7) способ ферментации в настоящем описании предусматривает и требует оперативного управления переменными технологическими параметрами. Перечень параметров состоит из параметров, включаемых в данный перечень в уровне техники, предназначенных для поддержания процесса в пределах физических, химических стандартов процесса, обычно используемых в процессах ферментации, охватываемых предшествующим уровнем техники, таких как рН и температура, контроль уровней, подача питательной среды и разгрузка, дополненных в свете инноваций к элементам управления и концентрациям реагентов и продуктов, включая микронутриенты. Указанное управление осуществляется в течение всего производственного процесса, что позволяет направлять указанный процесс в надлежащие и предполагаемые условия эксплуатации.
Управление концентрациями, в настоящем изобретении, отличается от управления концентрациями растворимых сухих веществ и сахаров, как и в случае высокоплотной (VHG) ферментации, при которой получают концентрацию спирта более 12% по объему в результате ферментативной переработки сусла с высоким содержанием сахара, предотвращающего повреждение микроорганизмов или недостаточную и замедленную ферментацию, а также от способов, в которых целью является управление или ограничение времени ферментации в качестве инструмента для производительного управления. В указанных традиционных случаях, управление концентрацией сахаров и микроорганизмов сводится к установлению технологических эксплуатационных ограничений.
Ферментация очень высокой плотности представляет собой ферментацию субстратов с высокой их концентрацией на начальном этапе с целью получения вин с высоким содержанием спирта, обычно с концентрацией более 12% по объему.
Недостаточная и замедленная ферментация имеет место при прерывании процесса ферментации или при резком снижении кинетики процесса даже при наличии субстрата, в результате стрессовых факторов, таких как избыточное содержание спирта или недостаток структурных микронутриентов для микроорганизмов.
В соответствии с настоящим изобретением управление концентрацией выходит за вышеуказанные ограничения, представляя управление биохимических процессов, направленное на продуктивный выход в представлении, предусмотренным общим уравнением (7).
Схематический баланс общего и упрощенного уравнения (7) непосредственно связан с ограничениями продуктивного выхода, с учетом концентрации субстратов, сахара, живых микроорганизмов и вводимого водорода [Н], в отношении селективной выработки спирта и последующего сокращения получения диоксида углерода.
С целью упрощения внедрения режимов управления установлено три эксплуатационных диапазона для концентраций, начиная с концентрации субстрата и водорода и заканчивая концентрацией восстановленного спирта. Указанные значения, при этом, не ограничивают настоящее изобретение используемыми в качестве примера эксплуатационными диапазонами способа, выполняемого в полном объеме в режиме непрерывного управления.
На фиг. 5 показаны логарифмические параметры кривых массового выхода, процентное увеличение массового выхода и концентрации, выраженные в молярном эквиваленте вещества для [Н], [этанола] и [СО2]. Указанные значения, принимая во внимание статистические условия внутриклеточных ферментативных реакций, оказались более приемлемыми в отношении наиболее подходящих результатов в процессе работы.
Исследования, подтверждающие изобретение
Проведено несколько исследований для проверки и оценки эффективности способа на ферментируемом сусле, с использованием вытяжки сахарного тростника и дрожжевых микроорганизмов вида Saccharomyces cerevisiae, бурно используемых в индустрии топливного этанола и напитков. Ниже приведен пример способа без намерения ограничить объем охраны изобретения. Условия эксперимента и результаты, а также подтверждение биохимической модели, представлены далее.
Пример 1 - Сравнение стандартной ферментации и ферментации, соответствующей настоящему изобретению в режиме предварительного электролиза
В настоящем исследовании установлено влияние водорода на этиловую ферментацию сахаристых сусел при электрическом напряжении ниже, чем необходимо для возникновения электролиза воды. В настоящем исследовании, включая следующие, в качестве реагентов при проведении периодической ферментации использовали сахар-сырец и промышленные дрожжи Saccharomyces cerevisiae.
Сконструировано два биореактора, один принят за основу или в качестве стандартного, а другой собран с системой генерации водорода (с использованием напряжения постоянного тока 0,95 В) для получения ионного и атомарного водорода в процессе ферментации.
В два биореактора, с максимальным объемом 100 литров, добавляли реагенты и воду до рабочего объема 50 л.
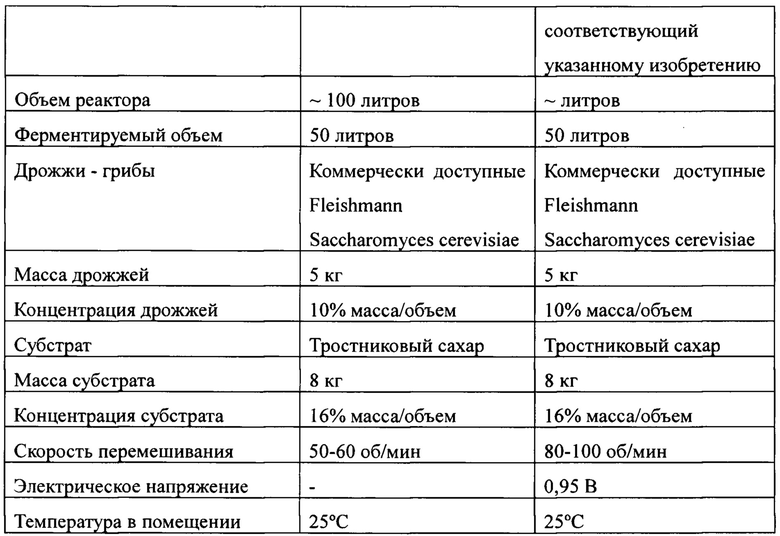
Точнее, в каждом биореакторе проведено два исследования по ферментации 8 кг тростникового сахара в качестве субстрата (в основном состоящего из сахарозы) с добавлением 5 кг коммерчески доступных дрожжей (грибы, Saccharomyces cerevisiae) параллельно в двух отдельных сериях.
Субстрат и грибы растворяли и подготавливали перед перемешиванием в биореакторах с помощью мешалки с плоским лезвием при 60-90 оборотах в минуту. Образцы собирали из реакторов сразу после перемешивания двух компонентов, и измеряли начальные параметры, такие, как содержание растворимых сухих веществ по шкале Брикса [Brix], температуру [°С] и кислотность [рН]. Измерение содержания растворимых сухих веществ по шкале Брикса, температуры и рН проводили через каждый час, с помощью дистиллятора и цифрового денситометра, принимая за стандарты лабораторные нормы подобного рода. Ни один микронутриент не добавляли в течение процесса, с целью обособления показателей.
В таблице 3 указаны ингредиенты, используемые в экспериментах, и условия проведения испытаний предварительного электролиза. Два исследования проведены параллельно в двух реакторах.

В таблице 4 указаны оборудование, используемое для управления параметрами рН, температуры, содержанием сухих растворимых веществ по шкале Брикса и концентрацией этанола. В исследованиях наблюдали изменения показателей при управлении ферментацией.
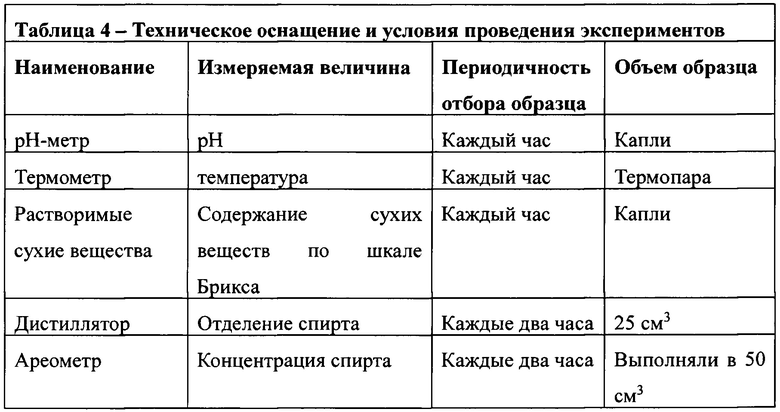
Результаты, полученные в указанных двух экспериментах, описаны ниже в таблице 5.
Таблица 5 - Результаты, полученные в результате ферментации в биореакторе, содержащем систему генерации водорода в режиме предварительного электролиза, и стандартном биореакторе.
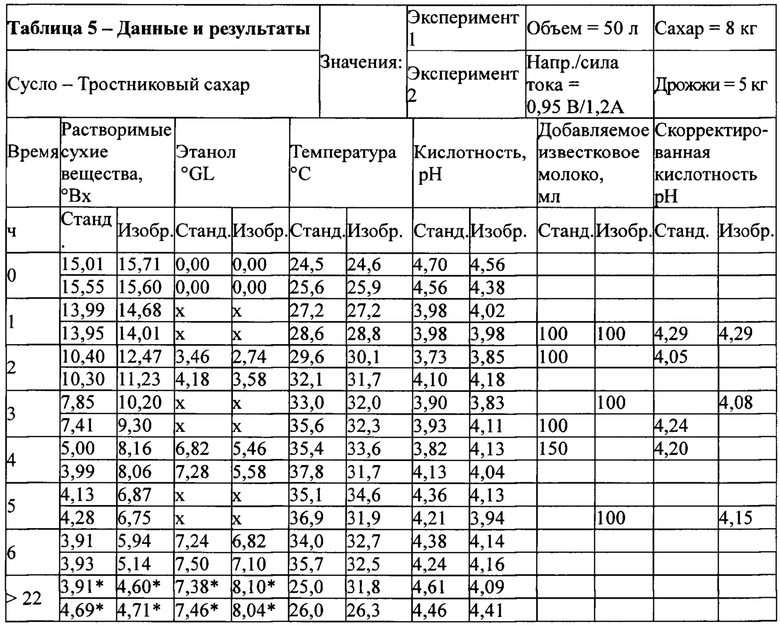
* - Завершение ферментации - электрическая система ферментера, соответствующая настоящему изобретением, отключена после 6-го часа. Реакторы оставляли в рабочем состоянии, при перемешивании, после последних измерений на 6-м часе. Оставшуюся ферментацию продолжали еще в течение 16 часов.
Увеличение получения этанола легко можно наблюдать в момент времени 6 часов, что можно подтвердить, в среднем, более 1,62°С сахара для способа, соответствующего настоящему изобретению. Из указанного дополнительного содержания сахара можно выработать этанола на 1,1°GL больше, следуя из уравнения Гей-Люссака (1) для расчета теоретического значения превращения сахара в этанол.
В результате выход при получении этанола, непосредственно указанный в таблице 5, увеличился на 6,8% и 8,3% по сравнению со стандартным ожидаемым теоретическим значением (выход Гей-Люссака), имеющим аналогичные экспериментальные критерии и расчеты выхода. Увеличение концентрации этанола и наблюдаемое снижение выделения двуокиси углерода сопровождались изменениями в химической кинетике, которая показывает, что может быть использована упрощенная биохимическая модель.
Пример 2 - Сравнение стандартной ферментации и ферментации, соответствующей настоящему изобретению, в режиме полного электролиза
В настоящем исследовании, в два биореактора (принятый за основу и относящийся к настоящему изобретению) помещали 9 кг тростникового сахара с 6 кг промышленных дрожжей, Saccharomyses cerevisiae.
Два биореактора, используемые в примере 1, один в качестве принятого за основу или стандартного биореактора, а другой был снабжен системой генерации водорода, являлись такими же, которые применяли в примере 2, В указанном примере использовали электрическое напряжение 1,6 В - в режиме полного электролиза, вырабатывающего ионный и газообразный водород в процессе ферментации.
В таблице 6 указаны ингредиенты, применяемые в эксперименте, и условия эксперимента при полном электролизе.
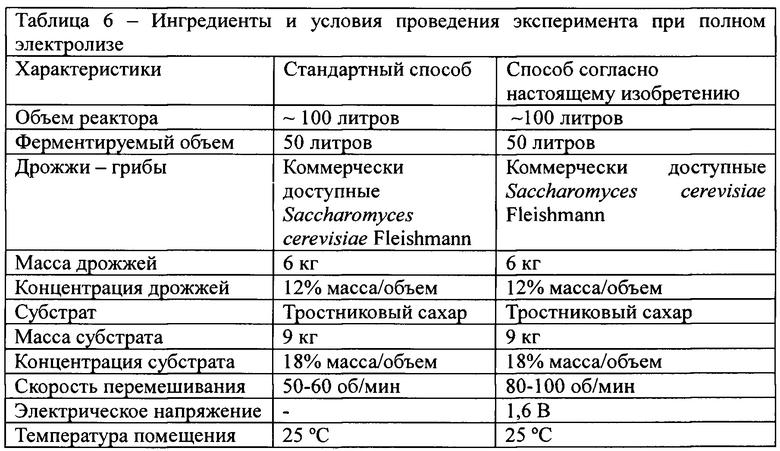
Образцы из реакторов отбирали сразу после добавления ингредиентов, а также измеряли исходные параметры, например, содержание растворимых сухих веществ по шкале Брикса [Brix], температуру [°С] и кислотность [рН]. Измерения содержания растворимых сухих веществ по шкале Брикса, температуры, рН и концентрации спирта проводили через каждый час. Ни один микронутриент не добавляли в течение процесса, с целью обособления показателей. На двух биореактора проведен только один эксперимент.
Результаты анализа указанного эксперимента описаны в таблицах 7 и 8.
Таблицы 7 и 8 - Результаты, полученные при ферментации в биореакторе, содержащем систему генерации водорода в режиме полного электролиза, и стандартном биореакторе.
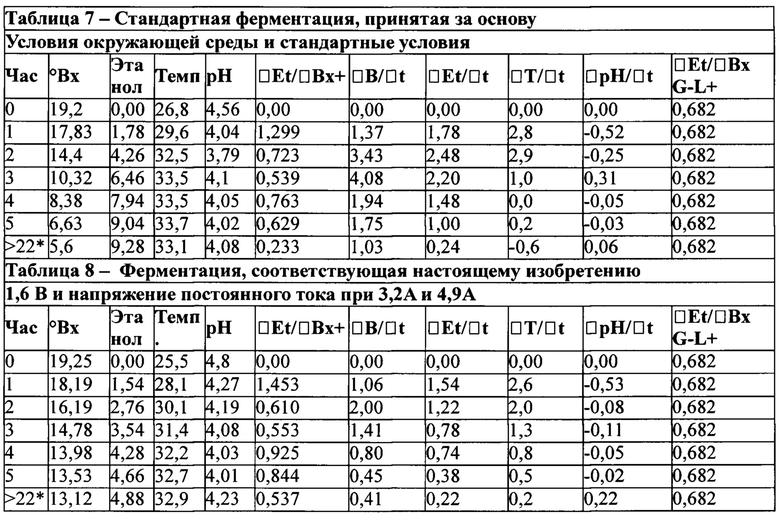
* - Завершение ферментации - электрическую систему ферментера согласно настоящему изобретения отключали после 6-го часа. Реакторы продолжали работу после последних измерений на 6 часе. Оставшуюся ферментацию продолжали в течение последующих 16 часов.
+ Примечание: значения 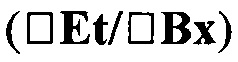 относятся к парциальному выходу, соответствующему выходу G-L. Для сахарозы максимальный выход составляет 0,538 масс./масс. и 0,682 об./об. в соответствии со значениями, приведенными в последнем правом столбце обеих таблиц 7 и 8.
относятся к парциальному выходу, соответствующему выходу G-L. Для сахарозы максимальный выход составляет 0,538 масс./масс. и 0,682 об./об. в соответствии со значениями, приведенными в последнем правом столбце обеих таблиц 7 и 8.
В результате выход при выработке этанола в биореакторе, соответствующему настоящему изобретению, превышает максимальное ожидаемое традиционное расчетное значение (выход по Гей-Люссаку) от 17% до 20%, что можно более ясно наблюдать в таблице 11.
Что касается отдельных значений, известно, что аналитические методы несут ошибки между подготовкой образцов вследствие и продолжительностью ферментативного процесса даже в отобранном образце, что может являться причиной значительных отклонений, когда моменты отбора образца происходят в периоды повышения кинетики в ходе ферментативной реакции.
Результаты и подтверждение биохимической модели
С целью представления вышеуказанных результатов лучшим способом, нижеследующие таблицы описывают значения, относящиеся к промежуточному получению этанола, в течение процесса и в конце ферментативного процесса, всегда сопровождаемые параметрами биореактора, соответствующего настоящему изобретению, и параметрами, полученными в стандартном биореакторе, принятым за основу. Отмечено, что указанные приведенные значения получены напрямую, а не только из результатов, полученных во время исследования.
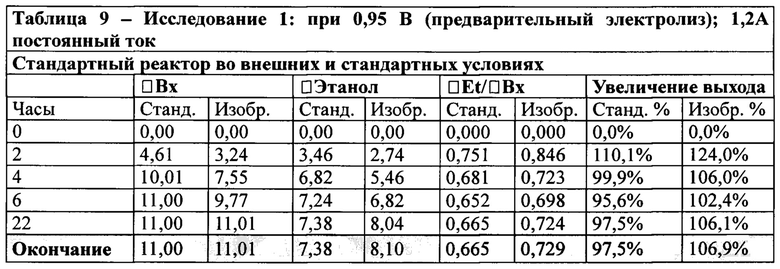
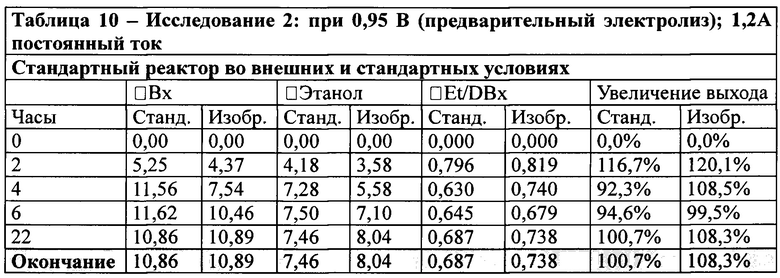

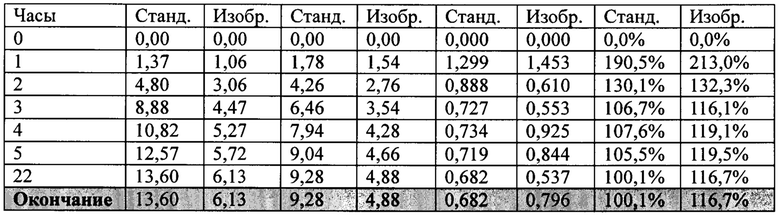
Отмечено, что в таблицах 9, 10 и 11 значения в столбцах «Увеличение выхода» демонстрируют накопление и конечные промежуточные значения, всегда выше по отношению к таковым, полученным в соответствии с настоящим изобретением. Конечные значения, 6,9% и 8,3%, по отношению к максимальному выходу ферментации, принимая во внимание известный уровень техники, составляющему 0,538 масс./масс. или 0,682 объем/объем, полученные в соответствующих исследованиях 1 и 2, при приложении напряжения в режиме предварительного электролиза и при постоянном токе, по сути только характеризуют изобретение относительно ограничений по производительности. Концентрации [сахарозы], [водорода] и [дрожжей] находятся в диапазоне от низкого (I) до среднего (II) молярного эквивалента вещества.
Значения, приведенные в таблице И, относящиеся к исследованию 3, в графе «Увеличение выхода», как промежуточные, так и конечные, являются убедительными и определяющими. Можно наблюдать, что окончательное или накопленное значение в исследовании 3 16,7% отражает быстрый отклик в способе, относящемуся к настоящему изобретению, на увеличение концентрации водорода в атомарном, ионном и газообразном состоянии, в режиме работы, ожидаемом в соответствии с фиг. 4 и 5.
Биохимическая модель в первых двух исследованиях, а также величины и особенности, продемонстрированные в исследовании 3, оказывались технически обоснованными в своих технологических и инновационных ограничениях.
Как и следовало ожидать, в исследовании 3, выполняемом в умеренном диапазоне (II) молярных эквивалентов вещества, кинетика реакции существенно изменялась, поскольку в процессе происходило снижение скорости образования этанола при утилизации сахара 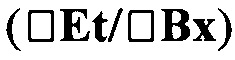 , оставляя большое количество сахара, присутствующего в среде. Доступность микронутриентов, главным образом N (азота), в условиях высокой активности микроорганизмов, имеет фундаментальное значение для увеличения биомассы, что представляет собой естественное явление в ферментативном процессе.
, оставляя большое количество сахара, присутствующего в среде. Доступность микронутриентов, главным образом N (азота), в условиях высокой активности микроорганизмов, имеет фундаментальное значение для увеличения биомассы, что представляет собой естественное явление в ферментативном процессе.
Недостаток главным образом азота предотвращает размножение микроорганизмов, осуществляющих ферментацию, и акцентирует на состоянии ферментации.
В дополнение к исследованиям, выполненным и изложенным в настоящем описании, более тщательно проверено снижение выделения диоксида углерода в ходе процесса, и было показано четкое уменьшение такого выделения по сравнению с процессом, одновременно проходящем в стандартном биореакторе. Специалисты указанной области техники владеют указанными методами: - определение внешнего вида и запаха - для оценки указанного свойства.
В таблице 12, представлено краткое описание результатов ферментации, с учетом объема этанола, полученного в трех исследованиях.
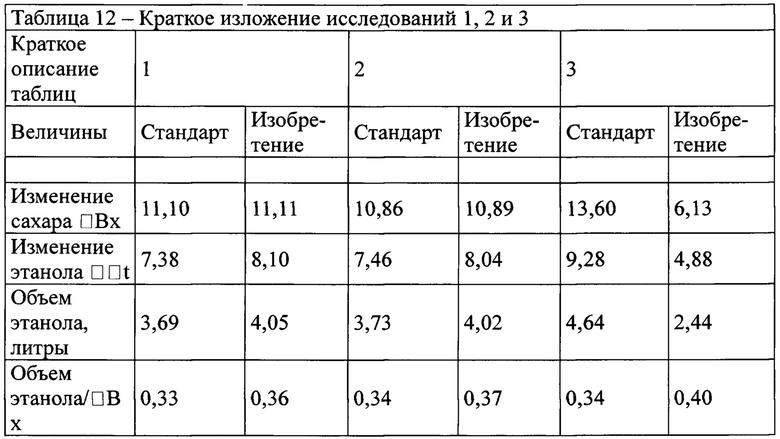
Таким образом, рассмотрен обоснованный способ согласно настоящему изобретению в соответствии с результатами, достигнутыми в ходе лабораторных исследований.
Сокращение выделения углекислого газа, в результате биохимического процесса, с селективным увеличением производства спирта, представляет собой технологическое дополнение к огромному значению для окружающей среды и эксплуатации. Некоторые экономические и экологические преимущества, обеспечиваемые настоящим изобретением, могут быть перечислены следующим образом:
1. Непосредственный экономический рост, связанный с увеличением выработки спирта;
2. Увеличение выработки без необходимости увеличения производственных площадей;
3. Сокращение выработки диоксида углерода;
4. Технологическое оборудование не требует настройки в отношении объема производства, это же касается биореакторов и оборудования для дистилляции;
5. Уменьшение размеров и потребления энергии оборудованием для выделения спирта, извлекаемого диоксидом углерода в процессе ферментации;
6. Увеличение квот на выброс углерода, связанное с увеличением выработки спирта и снижением выделения диоксида углерода;
7. Технология, направленная на улучшение состояния окружающей среды. Этанол в конечном итоге представляет собой экологически чистое топливо и экономически более рентабелен.
Группа изобретений относится к области биохимии. Предложен способ микробиологической ферментации сахаристых субстратов, а также средство для селективной выработки спирта. Способ включает введение водорода в относящийся к грибам или бактериям микроорганизм, где микроорганизм находится в суспензии в ферментируемом сусле или в иммобилизованном слое. Причём указанные ферментируемое сусло или иммобилизованный слой содержат сахара и микронутриенты, а микробиологическую ферментацию осуществляют в биореакторе. Средство для селективной выработки спирта представляет собой водород в атомарном, ионном или газообразном состоянии или их смеси. Изобретения обеспечивают увеличение выхода спирта в реакции ферментации и уменьшение выделения диоксида углерода. 2 н. и 17 з.п. ф-лы, 5 ил., 12 табл., 2 пр.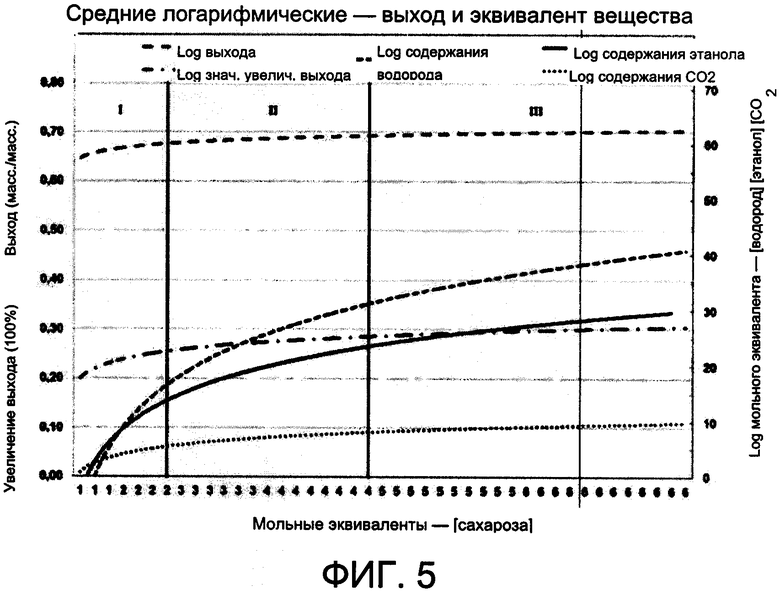
1. Способ микробиологической ферментации сахаристых субстратов, характеризующийся тем, что он включает введение водорода в микроорганизм, относящийся к грибам или бактериям, находящийся в суспензии в ферментируемом сусле или в иммобилизованном слое, где указанные ферментируемое сусло или иммобилизованный слой содержат сахара и микронутриенты; где микробиологическую ферментацию осуществляют в биореакторе.
2. Способ по п. 1, отличающийся тем, что водород получают путем приложения электрического напряжения по меньшей мере к двум электродам, погруженным в ферментируемое сусло или иммобилизованный слой.
3. Способ по п. 2, отличающийся тем, что водород получают путем помещения электродов, включающих по меньшей мере один катод и один анод, причем указанный катод погружают непосредственно в ферментируемое сусло, а указанный анод погружают в другой электролит, где последний представляет собой солевой раствор, соответственно в два электролита, имеющих разделяющую мембрану.
4. Способ по п. 1, отличающийся тем, что он включает добавление:
- от 5 до 30% (масса/объем) сахаристых субстратов;
- от 5 до 25% (масса/объем) микроорганизмов, относящихся к грибам или бактериям.
5. Способ по п. 1 или 4, отличающийся тем, что водород находится в атомарном, ионном, газообразном состоянии или их смеси.
6. Способ по пп. 1-4, отличающийся тем, что электроды эксплуатируют в режиме предварительного электролиза воды при электрическом напряжении в диапазоне от 0,1 до 1,24 В с получением ионного и атомарного водорода.
7. Способ по п. 6, отличающийся тем, что режим предварительного электролиза включает диапазон напряжения от 0,7 до 1,1 В.
8. Способ по пп. 1-4, отличающийся тем, что электроды эксплуатируют в режиме полного электролиза воды при электрическом напряжении в диапазоне от 1,24 до 30 В с получением атомарного, ионного и газообразного водорода или их смеси.
9. Способ по п. 8, отличающийся тем, что режим полного электролиза включает диапазон электрического напряжения от 1,24 до 20 В или предпочтительно от 1,24 до 10 В.
10. Способ по пп. 1-4, 7, 9, отличающийся тем, что электрическое напряжение, прилагаемое к электродам, подают в режиме постоянного или переменного тока с частотой в диапазоне от 50 до 2000 Гц.
11. Способ по п. 10, отличающийся тем, что электрическое напряжение, приложенное к электродам, подается в режиме переменного тока с частотой предпочтительно в диапазоне от 50 до 150 Гц, от 100 до 500 Гц или от 400 до 1000 Гц.
12. Способ по п. 1, отличающийся тем, что указанные сахара выбраны из полисахаридов и моносахаридов, включая триозы, тетрозы, пентозы и гексозы, причем предпочтительными являются сахароза, глюкоза, фруктоза и ксилоза или их смеси.
13. Способ по п. 1, отличающийся тем, что микроорганизмы, относящиеся к грибам, находящиеся в ферментируемом сусле или иммобилизованном слое, выбраны из видов Saccharomyces cerevisiae и Schizosaccharomyces pompe, Pichia stipites, Candida schehatae, a также из рода Torula.
14. Способ по п. 1, отличающийся тем, что микроорганизмы, относящиеся к бактериям, находящиеся в ферментируемом сусле или в иммобилизованном слое, выбраны из группы бактерий, относящихся к видам Zymomonas mobilis, Escherichia coli, а также к роду Clostridium.
15. Способ по п. 1, отличающийся тем, что микронутриенты выбраны из азота, фосфора, калия, магния, кальция, цинка, марганца, меди, железа, кобальта, серы, йода или их смеси.
16. Способ по п. 1, отличающийся тем, что газообразный водород дополнительно получают вне биореактора путем приложения электрического напряжения в диапазоне от 1,24 до 30 В в режиме предварительного электролиза воды, а затем непосредственно осуществляют подачу в биореактор.
17. Способ по п. 1, отличающийся тем, что процесс ферментации осуществляют непрерывным, полунепрерывным или периодическим способом.
18. Способ по пп. 1-4, 7, 9 и 11-17, отличающийся тем, что в процессе ферментации непрерывно контролируют рН, температуру, осуществляют регулирование уровня, подачи питательной среды и разгрузки, концентрации реагентов, таких как сахара, концентрации водорода, концентрации живых микроорганизмов и концентрации продукта, такой как концентрация спирта, концентрации двуокиси углерода и концентрации микронутриентов.
19. Применение водорода в атомарном, ионном или газообразном состоянии или их смеси, характеризующееся его введением в микроорганизмы, находящиеся в ферментационной среде, содержащей сахаристые субстраты, для селективной выработки спирта, как описано в пп. 1-18.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ производства спирта | 1987 |
|
SU1465458A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
Авторы
Даты
2018-10-17—Публикация
2014-08-29—Подача