УРОВЕНЬ ТЕХНИКИ
Бромдомены относятся к сохраненным протеиновым структурным складкам, которые связываются с N-ацетилированными остатками лизина, которые обнаруживают в некоторых протеинах. BET семейство содержащих бромдомен протеинов состоит из четырех членов (BRD2, BRD3, BRD4 и BRDt). Каждый член BET семейства имеет два бромдомена, чтобы распознавать N-ацетилированные остатки лизина, обнаруживаемые главным образом, но не исключительно, на амино-терминальных хвостах гистоновых протеинов. Эти взаимодействия модулируют генную экспрессию факторами рекрутинговой транскрипции на специфических геномных местоположениях в хроматине. Например, связанный с гистоном BRD4 рекрутирует фактор транскрипции P-TEFb к промотерам, имея результатом экспрессию подмножества генов, вовлекаемых в прогрессию клеточного цикла (Yang et al., Mol. Cell. Biol. 28: 967-976 (2008)). BRD2 и BRD3 также функционируют как транскрипционные регуляторы промотирующих рост генов (LeRoy et al., Mol. Cell 30: 51-60 (2008)). Члены BET семейства в последнее время были признаны важными для поддерживающего лечения некоторых типов рака (Zuber et al., Nature 478: 524-528 (2011); Mertz et al; Proc.Nat'l. Acad. SCl. 108: 16669-16674 (2011); Delmore et al., Cell 146: 1-14, (2011); Dawson et al., Nature 478: 529-533 (2011)). Члены BET семейства также принимают участие как медиаторы в острых воспалительных реакциях по каноническому пути NF-KB (Huang et al., Mol. Cell. Biol. 29: 1375-1387 (2009)), что приводит в результате к апрегуляции генов, ассоциируемых с продуцированием цитокинов (Nicodeme et al., Nature 468: 1119-1123, (2010)). В дополнение, функция бромдомена вовлечена в болезнь почек (Zhang, et al., J. Biol. Chem. 287: 28840-28851 (2012)). Функция BRD2 также связана с предрасположенностью к дислипидемии или неправильной регуляции адипогенеза, повышенным воспалительным профилям и с повышенной восприимчивостью к аутоиммунным заболеваниям (Denis, Discovery MediClne 10: 489-499 (2010)). Вирус иммунодефицита человека использует BRD4 для инициирования транскрипции вирусной RNA из стабильно интегрированной вирусной DNA (Jang et al., Mol. Cell, 19: 523-534 (2005)). Ингибиторы BET бромдомена также были показаны как способные реактивировать транскрипцию ВИЧ на моделях латентной Т-клеточной инфекции и латентной моноцитарной инфекции (Banerjee, et al, J. leukocyte Biol. doi:10,1189/jlb, 0312165). BRDt играет важную роль в сперматогенезе (Matzuk, et al., Cell 150: 673-684 (2012)). Соответственно, продолжает сохраняться медицинская потребность в разработке новых лекарств для лечения болезней и симптомов с вовлечением функции бромдомена, включая функцию BET бромдомена.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В одном аспекте данное изобретение относится к соединениям формулы (I) или их фармацевтически приемлемым солям

где
Rx представляет водород или C1-C3 алкил;
Ry представляет C1-C3 алкил, -(C2-C3 алкиленил)-OH или C1-C3 галогеналкил;
X1 представляет N или CRx1, где
Rx1 представляет водород, C2-C6 алкенил, C2-C6 алкинил, -C(О)ORах1, -C(О)NRbx1Rcx1, -C(О)Rdx1, S(О)2Rdx1, -S(О)2NRbx1Rcx1, Gx1, C1-C6 галогеналкил или C1-C6 алкил; где C1-C6 алкил является необязательно замещенным одним заместителем, выбранным из группы, состоящей из ORаx1, SRax1, S(О)Rdx1, S(О)2Rdx1, NRbx1Rcx1, -C(О)Rax1, -C(О)ORax1, -C(О)NRbx1Rcx1, -S(О)2NRbx1Rcx1 и Gx1;
Rax1, Rbx1 и Rcx1, в каждом случае, каждый независимо, представляют водород, C1-C6 алкил, C1-C6 галогеналкил, Ga или -(C1-C6 алкиленил)-Ga;
Rdx1, в каждом случае, каждый независимо, представляют C1-C6 алкил, C1-C6 галогеналкил, Ga или -(C1-C6 алкиленил)-Ga;
X2 представляет N или CRx2; где
Rx2 представляет водород, C2-C6 алкенил, C2-C6 алкинил, -C(О)ORax2, -C(О)NRbx2Rcx2, -C(О)Rdx2, -C(О)H, S(О)2Rdx2, -S(О)2NRbx2Rcx2, Gx2, C1-C6 галогеналкил или C1-C6 алкил; где C1-C6 алкил является необязательно замещенным одним заместителем, выбранным из группы, состоящей из ORax2, SRax2, S(О)Rdx2, S(О)2Rdx2, NRbx2Rcx2, -C(О)Rax2, -C(О)ORax2, -C(О)NRbx2Rcx2, -S(О)2NRbx2Rcx2 и Gx2;
Rax2, Rbx2 и Rcx2, в каждом случае, каждый независимо, представляют водород, C1-C6 алкил, C1-C6 галогеналкил, Gb или -(C1-C6 алкиленил)-Gb;
Rdx2, в каждом случае, независимо представляет C1-C6 алкил, C1-C6 галогеналкил, Gb или -(C1-C6 алкиленил)-Gb;
Y1 представляет N или CRu; где Ru представляет водород, C1-C6 алкил, галоген или C1-C6 галогеналкил;
A1 представляет N или CR1, A2 представляет N или CR2, A3 представляет N или CR3 и A4 представляет N или CR4; при условии, что ноль, один, два или три из A1, A2, A3 и A4 являются N;
R1, R3 и R4, каждый независимо, представляют водород, C1-C6 алкил, С2-C6 алкенил, С2-C6 алкинил, галоген, C1-C6 галогеналкил, CN, или NO2;
R2 представляет водород, C1-C6 алкил, С2-C6 алкенил, С2-C6 алкинил, галоген, C1-C6 галогеналкил, -CN, NO2, G2a, -OR2a, -OC(О)R2d, -OC(О)NR2bR2с, -SR2a, -S(О)2R2d, -S(О)2NR2bR2c, -C(О)R2d, -C(О)OR2a, -C(О)NR2bR2c, -NR2bR2с, -N(R2e)C(О)R2d, -N(R2е)S(О)2R2d, -N(R2е)C(О)O(R2d), -N(R2е)C(О)NR2bR2c, -N(R2е)S(О)2NR2bR2c, -(C1-C6 алкиленил)-G2a, -(C1-C6 алкиленил)-OR2a, -(С1-C6 алкиленил)-OC(О)R2d, -(C1-C6 алкиленил)-OC(О)NR2bR2c, -(C1-C6 алкиленил)-S(О)2R2d, -(C1-C6 алкиленил)-S(О)2NR2bR2c, -(C1-C6 алкиленил)-C(О)R2d, -(C1-C6 алкиленил)-C(О)OR2a, -(C1-C6 алкиленил)-C(О)NR2bR2c, -(C1-C6 алкиленил)-NR2bR2c, -(C1-C6 алкиленил)-N(R2е)C(О)R2d, -(C1-C6 алкиленил)-N(R2е)S(О)2R2d, -(C1-C6 алкиленил)-N(R2е)C(О)O(R2a), -(C1-C6 алкиленил)-N(R2е)C(О)NR2bR2c, -(C1-C6 алкиленил)-N(R2е)S(О)2NR2bR2c и -(C1-C6 алкиленил)-CN;
R2a, R2b, R2c и R2e, в каждом случае, каждый независимо, представляют водород, С2-С6 алкенил, С2-С6 алкинил, C1-C6 галогеналкил, G2b или C1-C6 алкил, где C1-C6 алкил является необязательно замещенным одним заместителем, выбранным из группы, состоящей из -ORz1, NRz1Rz2, -C(О)ORz1, -C(О)NRz1Rz2, -S(О)2Rz1, -S(О)2NRz1Rz2 и G2b;
R2d, в каждом случае, независимо представляет С2-С6 алкенил, С2-С6 алкинил, C1-C6 галогеналкил, G2b или C1-C6 алкил, где C1-C6 алкил является необязательно замещенным одним заместителем, выбранным из группы, состоящей из -ORz1, NRz1Rz2, -C(О)ORz1, -C(О)NRz1Rz2, -S(О)2Rz1, - S(О)2NRz1Rz2 и G2b;
Rz1 и R z2, в каждом случае, каждый независимо, представляют водород, С1-С6-алкил или С1-С6 галогеналкил;
Gx1, Gx2, Ga, Gb, G2a и G2b, в каждом случае, каждый независимо, представляют арил, гетероарил, гетероцикл, циклоалкил или циклоалкенил, и каждый из которых является независимо незамещенным или замещенным 1, 2, 3, 4 или 5 Rv;
L1 отсутствует или означает CH2, C(O), C(H)(OH), (CH2)mO, (CH2)mS(О)n, где n означает 0, 1 или 2; или (CH2)mN(Rz), где Rz представляет водород, C1-C3 алкил, C1-C3 галогеналкил, (C2-C3 алкиленил)-OH или незамещенный циклопропил;
m означает 0 или 1;
G1 представляет С1-C6 алкил, алкоксиалкил, G1a или -(C1-C6 алкиленил)-G1a; где каждый G1a независимо представляет арил, гетероарил, гетероцикл, циклоалкил или циклоалкенил, и каждый G1a независимо является незамещенным или замещенным 1, 2, 3, 4 или 5 Rw;
Rv и Rw, в каждом случае, каждый независимо, представляют C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил, галоген, C1-C6 галогеналкил, -CN, оксо, -ORh, -OC(О)Ri, -OC(О)NRjRk, -SRh, -S(О)2Rh, -S(О)2NRjRk, -C(О)Rh, -C(О)-моноциклический гетероцикл, -C(О)-моноциклический гетероарил, -C(О)ORh, -C(О)NRjRk, -NRjRk, -N(Rh)C(О)Ri, -N(Rh)S(О)2Ri, -N(Rh)C(О)O(Ri), -N(Rh)C(О)NRjRk, -(C1-C6 алкиленил)-ORh, -(C1-C6 алкиленил)-ОС(О)Ri, -(C1-C6 алкиленил)-OC(О)NRjRk, -(C1-C6 алкиленил)-S(О)2Rh, -(C1-C6 алкиленил)-S(О)2NRJRk, -(C1-C6 алкиленил)-C(О)Rh, -(C1-C6 алкиленил)-C(О)ORh, -(C1-C6 алкиленил)-C(О)NRjRk, -(C1-C6 алкиленил)-NRjRk, -(C1-C6 алкиленил)-N(Rh)C(О)Ri, -(C1-C6 алкиленил)-N(Rh)S(О)2Ri, -(C1-C6 алкиленил)-N(Rh)C(О)O(Ri), -(C1-C6 алкиленил)-N(Rh)C(О)NRjRk или -(C1-C6 алкиленил)-CN;
Rh, Rj, Rk, в каждом случае, каждый независимо, представляют водород, C1-C6 алкил или C1-C6 галогеналкил; и
Ri, в каждом случае, независимо представляет C1-C6 алкил или C1-C6 галогеналкил.
В одном аспекте данное изобретение относится к соединениям формулы (I) или их фармацевтически приемлемым солям,
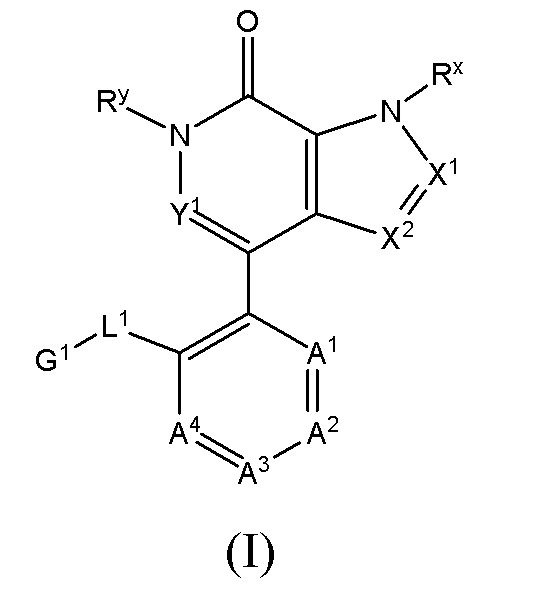
где
Rx представляет водород или С1-С3 алкил;
Ry представляет С1-С3 алкил, -(C2-C3 алкиленил)-OH или С1-С3 галогеналкил;
X1 представляет N или CRx1, где
Rx1 представляет водород, C2-C6 алкенил, C2-C6 алкинил, -C(О)ORax1, -C(О)NRbx1Rcx1, -C(О)Rdx1, S(О)2Rdx1, -S(О)2NRbx1Rcx1, Gx1, C1-C6 галогеналкил или C1-C6 алкил; где C1-C6 алкил является необязательно замещенным одним заместителем, выбранным из группы, состоящей из ORax1, SRax1, S(О)Rdx1, S(О)2Rdx1, NRbx1Rcx1, -C(О)Rax1, -C(О)ORax1, -C(О)NRbx1Rcx1, -S(О)2NRbx1Rcx1 и Gx1;
Rax1, Rbx1 и Rcx1, в каждом случае, каждый независимо, представляют водород, C1-C6 алкил, C1-C6 галогеналкил, Ga или -(C1-C6 алкиленил)-Ga;
Rdx1, в каждом случае, каждый независимо, представляют C1-C6 алкил, C1-C6 галогеналкил, Ga или -(C1-C6 алкиленил)-Ga;
X2 представляет N или CRx2; где
Rx2 представляет водород, C2-C6 алкенил, C2-C6 алкинил, -C(О)ORax2, -C(О)NRbx2Rcx2, -C(О)Rdx2, S(О)2Rdx2, -S(О)2NRbx2Rcx2, Gx2, C1-C6 галогеналкил или C1-C6 алкил; где C1-C6 алкил является необязательно замещенным одним заместителем, выбранным из группы, состоящей из ORax2, SRax2, S(О)Rdx2, S(О)2Rdx2, NRbx2Rcx2, -C(О)Rax2, -C(О)ORax2, -C(О)NRbx2Rcx2, -S(O)2NRbx2Rсx2 и Gx2;
Rax2, Rbx2 и Rcx2, в каждом случае, каждый независимо, представляют водород, C1-C6 алкил, C1-C6 галогеналкил, Gb или -(C1-C6 алкиленил)-Gb;
Rdx2, в каждом случае, независимо представляет C1-C6 алкил, C1-C6 галогеналкил, Gb или -(C1-C6 алкиленил)-Gb;
Y1 представляет N или CRu; где Ru представляет водород, C1-C6 алкил, галоген или C1-C6 галогеналкил;
A1 представляет N или CR1, A2 представляет N или CR2, A3 представляет N или CR3 и A4 представляет N или CR4; при условии, что ноль, один, два или три из A1, A2, A3 и A4 представляют N;
R1, R3 и R4, каждый независимо, представляют водород, C1-C6 алкил, С2-С6 алкенил, С2-С6 алкинил, галоген, C1-C6 галогеналкил, CN или NO2;
R2 представляет водород, C1-C6 алкил, С2-С6 алкенил, С2-С6 алкинил, галоген, C1-C6 галогеналкил, -CN, NO2, G2a, -OR2a, -OC(О)R2d, -OC(О)NR2bR2c, -SR2a, -S(О)2R2d, -S(О)2NR2bR2c, -C(О)R2d, -C(О)OR2a, -C(О)NR2bR2c, -NR2bR2c, -N(R2e)C(О)R2d, -N(R2e)S(О)2R2d, -N(R2e)C(О)O(R2d), -N(R2e)C(О)NR2bR2c, -N(R2e)S(О)2NR2bR2c, -(C1-C6 алкиленил)-G2a, -(C1-C6 алкиленил)-OR2a, -(С1-C6 алкиленил)-OC(О)R2d, -(C1-C6 алкиленил)-OC(О)NR2bR2c, -(С1-C6 алкиленил)-S(О)2R2d, -(C1-C6 алкиленил)-S(О)2NR2bR2c, -(C1-C6 алкиленил)-C(О)R2d, -(C1-C6 алкиленил)-C(О)OR2a, -(C1-C6 алкиленил)-C(О)NR2bR2c, -(C1-C6 алкиленил)-NR2bR2c, -(C1-C6 алкиленил)-N(R2e)C(О)R2d, -(C1-C6 алкиленил)-N(R2e)S(О)2R2d, -(C1-C6 алкиленил)-N(R2e)C(О)O(R2a), -(C1-C6 алкиленил)-N(R2e)C(О)NR2bR2c, -(C1-C6 алкиленил)-N(R2e)S(О)2NR2bR2° и -(C1-C6 алкиленил)-CN;
R2a, R2b, R2c и R2е, в каждом случае, каждый независимо, представляют водород, С2-С6 алкенил, С2-С6 алкинил, C1-С6 галогеналкил, G2b или C1-C6 алкил, где C1-C6 алкил является необязательно замещенным одним заместителем, выбранным из группы, состоящей из -ORz1, NRz1Rz2, -C(О)ORz1, -C(О)NRz1Rz2, -S(О)2Rz1, -S(О)2NRz1Rz2 и G2b;
R2d, в каждом случае, независимо представляет С2-С6 алкенил, С2-С6 алкинил, C1-C6 галогеналкил, G2b или C1-C6 алкил, где C1-C6 алкил является необязательно замещенным одним заместителем, выбранным из группы, состоящей из -ORz1, NRz1Rz2, -C(О)ORz1, -C(О)NRz1Rz2, -S(О)2Rz1, -S(О)2NRz1Rz2 и G2b;
Rz1 и Rz2, в каждом случае, каждый независимо, представляют водород, C1-C6 алкил или C1-C6 галогеналкил;
Gx1, Gx2, Ga, Gb, G2a и G2b, в каждом случае, каждый независимо, представляют арил, гетероарил, гетероцикл, циклоалкил или циклоалкенил и каждый из которых независимо является незамещенным или замещенным 1, 2, 3, 4 или 5 Rv;
L1 отсутствует или представляет CH2, C(O), (CH2)mO, (CH2)mS(О)n, где n означает 0, 1 или 2; или (CH2)mN(Rz), где Rz представляет водород, C1-C3 алкил, C1-C3 галогеналкил, (C2-C3 алкиленил)-OH или незамещенный циклопропил;
m означает 0 или 1;
G1 представляет G1a или -(C1-C6 алкиленил)-G1a, где каждый G1a независимо представляет арил, гетероарил, гетероцикл, циклоалкил или циклоалкенил, и каждый G1a независимо является незамещенным или замещенным 1, 2, 3, 4 или 5 Rw;
Rv и Rw, в каждом случае, каждый независимо, представляют C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил, галоген, C1-C6 галогеналкил, -CN, оксо, -ORh, -OC(О)Ri, -OC(О)NRjRk, -SRh, -S(О)2Rh, -S(О)2NRjRk, -C(О)Rh, -C(О)ORh, -C(О)NRjRk, -NRjRk, -N(Rh)C(О)Ri, -N(Rh)S(О)2, -N(Rh)C(О)O(Ri), -N(Rh)C(О)NRjRk, -(C1-C6 алкиленил)-ORh, -(C1-C6 алкиленил)-OС(О)Ri, -(C1-C6 алкиленил)-OC(О)NRjRk, -(C1-C6 алкиленил)-S(О)2Rh, -(C1-C6 алкиленил)-S(О)2NRjRk, -(C1-C6 алкиленил)-C(О)Rh, -(C1-C6 алкиленил)-C(О)ORh, -(C1-C6 алкиленил)-C(О)NRjRk, -(C1-C6 алкиленил)-NRjRk, -(C1-C6 алкиленил)-N(Rh)C(О)Ri, -(C1-C6 алкиленил)-N(Rh)S(О)2Ri, -(C1-C6 алкиленил)-N(Rh)C(О)O(Ri), -(C1-C6 алкиленил)-N(Rh)C(O)NRjRk или -(C1-C6 алкиленил)-CN;
Rh, Rj, Rk, в каждом случае, каждый независимо, представляют водород, C1-C6 алкил или C1-C6 галогеналкил; и
Ri, в каждом случае, независимо представляет C1-C6 алкил или C1-C6 галогеналкил.
В другом аспекте, данное изобретение относится к способам лечения или предотвращения расстройств, которые облегчают ингибированием BET. Такие способы содержат введение субъекту терапевтически эффективного количества соединения формулы (I), одного или в сочетании с фармацевтически приемлемым носителем.
Некоторые из способов направлены на лечение или предотвращение воспалительной болезни или рака или СПИД.
В другом аспекте, данное изобретение относится к способам лечения рака у субъекта, содержему введение терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли субъекту при необходимости этого. В конкретных вариантах осуществления, рак выбран из группы, состоящей из таких членов как: неврилеммома слухового нерва, острая лейкемия, острая лимфоцитарная лейкемия, острая миелоцитарная лейкемия (моноцитарная, миелобластная, аденокарцинома, злокачественная гемангиома, астроцитома, миеломоноцитарная и промиелоцитарная), острая t-клеточная лейкемия, базально-клеточная карцинома, карцинома желчных путей, рак мочевого пузыря, рак головного мозга, рак молочной железы, бронхогенная карцинома, цервикальный рак, хондросаркома, хордома, хориокарцинома, хроническая лейкемия, хроническая лимфоцитарная лейкемия, хроническая миелоцитарная (гранулоцитарная) лейкемия, хроническая миелогенная лейкемия, рак толстой кишки, колоректальный рак, краниофарингиома, цистаденокарцинома, диффузная крупноклеточная лимфома, диспролиферативные изменения (дисплазии и метаплазии), эмбриональная карцинома, карцинома эндометрия, эндотелиосаркома, эпендимома, эпителиальный рак, эритролейкемия, рак пищевода, позитивный в отношении эстрогенового рецептора рак молочной железы, существенная тромбоцитемия, Болезнь Юинга, фибросаркома, фолликулярная лимфома, эмбриональноклеточный тестикулярный рак, глиома, глиобластома, глиосаркома, болезнь тяжелой (пептидной) цепи, гемангиобластома, гепатома, гепатоцеллюлярный рак, гормональны интенсивный рак простаты, лейомиосаркома, лейкемия, липосаркома, рак легкого, лимфагиоэндотелиосаркома, лимфангиосаркома, лимфобластная лейкемия, лимфома (Ходжкина и неходжкинская), злокачественные новообразования и гиперпролиферативные расстройства мочевого пузыря, молочной железы, толстой кишки, легких, яичников, поджелудочной железы, простаты, кожи и матки, лимфоидные злокачественные новообразования T-клеточного или B-клеточного происхождения, лейкемия, лимфома, медуллярный рак, медуллобластома, меланома, менингиома, мезотелиома, множественная миелома, миелогенная лейкемия, миелома, миксосаркома, нейробластома, NUT срединная карцинома (NMC), немелкоклеточный рак легкого, олигодендроглиома, рак ротовой полости, остеогенная саркома, рак яичников, панкреатический рак, сосковидные аденокарциномы, сосковидная карцинома, пинеалома, истинная полицитемия, рак простаты, ректальный рак, почечно-клеточная (светлоклеточная) карцинома, ретинобластома, рабдомиосаркома, саркома, карцинома сальных желез, семинома, рак кожи, мелкоклеточная карцинома легких, солидные опухоли (карциномы и саркомы), мелкоклеточный рак легкого, рак желудка, сквамозноклеточная карцинома, синовиальная эндотелиома, карцинома потовых желез, рак щитовидной железы, макроглобулинемия Вальденштрома, тестикулярные опухоли, рак матки и Опухоль Вильмса. В конкретных вариантах осуществления, способы дополнительно содержат введение терапевтически эффективного количества по меньшей мере одного дополнительного терапевтического агента. В конкретных вариантах осуществления, дополнительный терапевтический агент является противораковым агентом. В особенных вариантах осуществления, дополнительные терапевтические агенты выбраны из группы, состоящей из цитарабина, бортезомиба и 5-азацитидина.
В другом аспекте, данное изобретение относится к способам лечения болезни или состояния субъекта, содержащим введение терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли субъекту при необходимости этого, где указанная болезнь или состояние выбраны из группы, состоящей из таких членов как: болезнь Эддисона, острая подагра, анкилозирующий спондилоартрит, астма, атеросклероз, болезнь Бехчета, буллезные кожные болезни, хроническая обструктивная легочная болезнь (COPD), болезнь Крона, дерматит, экзема, гигантоклеточный аортит, гломерулонефрит, гепатит, гипофизит, воспалительная болезнь кишечника, болезнь Кавасаки, люпус-нефрит, рассеянный склероз, миокардит, миозит, нефрит, отторжение трансплантированного органа, остеоартрит, панкреатит, перикардит, нодозный полиартериит, пульмонит, билиарный первичный цирроз печени, псориаз, псориатический артрит, ревматоидный артрит, склерит, склерозирующий холангит, сепсис, системная красная волчанка, артериит Такаясу, токсический шок, тиреоидит, диабет типа I, язвенный колит, увеит, витилиго, васкулит и грануломатоз Вегенера. В конкретных вариантах осуществления, способы дополнительно содержат введение терапевтически эффективного количества по меньшей мере одного дополнительного терапевтического агента. В конкретных вариантах осуществления, способы дополнительно содержат введение терапевтически эффективного количества по меньшей мере одного дополнительного терапевтического агента.
В другом аспекте, данное изобретение относится к способам лечения хронической почечной болезни или состояния у субъекта, содержащему введение терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли субъекту при необходимости этого, где указанная болезнь или состояние выбраны из группы, состоящей из таких членов как: диабетическая нефропатия, гипертензивная нефропатия, связанная с ВИЧ нефропатия, гломерулонефрит, люпус-нефрит, IgA нефропатия, очаговый сегментарный гломерулосклероз, мембранный гломерулонефрит, болезнь минимальной альтерации, поликистозная почечная болезнь и канальцевый интерстициальный нефрит. В конкретных вариантах осуществления, способы дополнительно содержат введение терапевтически эффективного количества по меньшей мере одного дополнительного терапевтического агента. В конкретных вариантах осуществления, способы дополнительно содержат введение терапевтически эффективного количества по меньшей мере одного дополнительного терапевтического агента.
В другом аспекте, данное изобретение относится к способам лечения острого почечного поражения, или болезни, или состояния у субъекта, содержащим введение терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли субъекту при необходимости этого, где указанное острое почечное поражение, или болезнь, или состояние выбрано из группы, состоящей из таких членов как: вызванные ишемией-реперфузией, вызванные сердечной и радикальной хирургией, вызванные перкутанным коронарным вмешательством, вызванные радиоактивным контрастным агентом, вызванные сепсисом, вызванные пневмонией и вызванные токсичностью лекарства. В конкретных вариантах осуществления, способы дополнительно содержат введение терапевтически эффективного количества по меньшей мере одного дополнительного терапевтического агента. В конкретных вариантах осуществления, способы дополнительно содержат введение терапевтически эффективного количества по меньшей мере одного дополнительного терапевтического агента.
В другом аспекте, данное изобретение относится к способам лечения СПИД у субъекта, содержащим введение терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли субъекту при необходимости этого. В конкретных вариантах осуществления, способы дополнительно содержат введение терапевтически эффективного количества по меньшей мере одного дополнительного терапевтического агента.
В другом аспекте, данное изобретение относится к способам лечения ожирения, дислипидемии, гиперхолестеринемии, болезни Альцгеймера, метаболического синдрома, ожирения печени, диабета типа II, резистентности к инсулину, диабетической ретинопатии или диабетической невропатии у субъекта, содержащим введение терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли субъекту при необходимости этого. В конкретных вариантах осуществления, способы дополнительно содержат введение терапевтически эффективного количества по меньшей мере одного дополнительного терапевтического агента.
В другом аспекте, данное изобретение относится к способам предотвращения концепции путем ингибирования сперматогенеза у субъекта, содержащим введение терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли субъекту при необходимости этого. В конкретных вариантах осуществления, способы дополнительно содержат введение терапевтически эффективного количества по меньшей мере одного дополнительного терапевтического агента.
Дополнительный аспект изобретения относится к применению соединения формулы (I), одного или в сочетании со вторым активным фармацевтическим агентом, в производстве медикамента для лечения или предотвращения состояний и расстройств, раскрытых в данном описании, с фармацевтически приемлемым носителем или без него.
Фармацевтические композиции, содержащие соединение формулы (I) или его фармацевтически приемлемую соль, одно или в сочетании со вторым активным фармацевтическим агентом, также предложены.
ПОДРОБНОЕ ОПИСАНИЕ
В данном описании раскрыты соединения формулы (I)
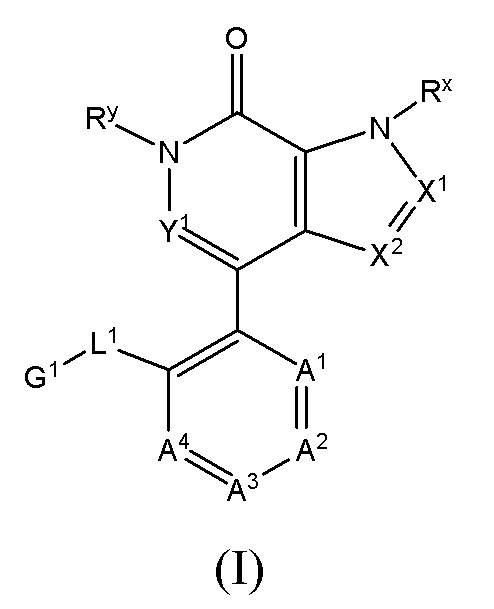
где A1, A2, A3, A4, X1, X2, Y1, L1, G1, Rx и Ry имеют значения, указанные выше в разделе "Сущность изобретения" и ниже в "Подробном описании". Дополнительно, композиции, содержащие такие соединения, и способы лечения состояний и расстройств с применением таких соединений и композиций также раскрыты.
Соединения, раскрытые в данном описании, могут содержать одну или несколько переменных, которые встречаются более чем один раз в каком-либо заместителе или в приведенной здесь формуле. Определение переменной в каждом случае является независимым от ее определения в другом случае. Дополнительно, комбинации заместителей допустимы только, если такие комбинации имеют результатом устойчивые соединения. Устойчивые соединения - это соединения, которые могут быть изолированы из реакционной смеси.
a). Определения
Следует отметить, что используемые в данном описании и предполагаемой формуле изобретения формы единственного числа включают множественные объекты ссылки, если контекст ясно не диктует иное. Так, например, ссылка на "соединение" включает единственное соединение, а также одно или несколько одинаковых или разных соединений, ссылка на "необязательный фармацевтически приемлемый носитель" относится к единственному необязательному фармацевтически приемлемому носителю, а также к одному или нескольким фармацевтически приемлемым носителям и тому подобное.
Используемые в данном описании и прилагаемой формуле изобретения, если не оговорено противоположное, следующие термины имеют указанные значения:
Используемый в данном описании термин "алкенил" означает прямую или разветвленную углеводородную цепь, содержащую от 2 до 10 атомов углерода и содержащую по меньшей мере одну углерод-углеродную двойную связь, необязательно замещенную 1, 2 или 3 атомами галогена. Термин "С2-С6 алкенил" означает алкенильную группу, содержащую 2-6 атомов углерода. Неограничительные примеры алкенила включают бута-1,3-диенил, этенил, 2-пропенил, 2-метил-2-пропенил, 3-бутенил, 4-пентенил, 5-гексенил, 2-гептенил, 2-метил-1-гептенил и 3-деценил.
Термин "алкенилен" означает двухвалентную группу, которая является производной углеводорода с прямой или разветвленной углеводородной цепью из 2-4 атомов углерода и содержит по меньшей мере одну углерод-углеродную двойную связь. Характерные примеры алкенилена включают, но без ограничения указанным, -CH=CH- и -CH2CH=CH-.
Термин "алкил", используемый в данном описании, означает насыщенный радикал с прямой или разветвленной углеводородной цепью. В некоторых случаях, число атомов углерода в алкильной части молекулы обозначают префиксом "Cx-Cy", где x означает минимальное и у означает максимальное число атомов углерода в заместителе. Так, например, "C1-С6 алкил" относится к алкильному заместителю, содержащему от 1 до 6 атомов углерода и "C1-С3 алкил" относится к алкильному заместителю, содержащему от 1 до 3 атомов углерода. Характерные примеры алкила включают, но без ограничения указанным, метил, этил, н-пропил, изо-пропил, н-бутил, втор-бутил, изо-бутил, трет-бутил, н-пентил, изопентил, неопентил, н-гексил, 1-метилбутил, 2-метилбутил, 3-метилбутил, 1,1-диметилпропил, 1,2-диметилпропил, 2,2-диметилпропил, 1-метилпропил, 1-этилпропил, 1,2,2-триметилпропил, 3-метилгексил, 2,2-диметилпентил, 2,3-диметилпентил, н-гептил, н-октил, н-нонил и н-децил.
Термин "алкилен" или "алкиленил" означает двухвалентный радикал, полученный из приямой или разветвленной насыщенной углеводородной цепи, например, из 1-10 атомов углерода, или из 1-6 атомов углерода (С1-С6 алкиленил), или из 1-4 атомов углерода, или из 2-3 атомов углерода (С2-С3 алкиленил). Примеры алкилена и алкиленила включают, но без ограничения указанным, -CH2-, - CH2CH2-, -CH2CH2CH2-, -CH2CH2CH2CH2- и -CH2CH(CH3)CH2-.
Термин "алкинил", используемый в данном описании, означает углеводородный радикал с прямой или разветвленной цепью, содержащий от 2 до 10 атомов углерода и содержащий по меньшей мере одну углерод-углеродную тройную связь, необязательно замещенный 1, 2 или 3 атомами галогена. Термин "С2-С6 алкинил" означает алкинильную группу из 2-6 атомов углерода. Характерные примеры алкинила включают, но без ограничения, ацетиленил, 1-пропинил, 2-пропинил, 3-бутинил, 2-пентинил и 1-бутинил.
Термин "арил", используемый в данном описании, означает фенил или бициклический арил. Бициклический арил представляет нафтил или фенил, слитый с моноциклическим циклоалкилом, или фенил, слитый с моноциклическим циклоалкенилом. Неограничительные примеры арильных групп включают дигидроинденил, инденил, нафтил, дигидронафталинил и тетрагидронафталинил. Бициклические арилы присоединены к родительской части молекулы через какой-либо атом углерода, находящийся в бициклических кольцевых системах, и могут быть незамещенными или замещенными.
Термин "циклоалкил", используемый в данном описании, относится к радикалу, который является моноциклическим циклическим алкилом, бициклическим циклоалкилом или спиро циклоалкилом. Моноциклический циклоалкил представляет собой карбоциклическую кольцевую систему, содержащую от трех до восьми атомов углерода, ноль гетероатомов и ноль двойных связей. Примеры моноциклических кольцевых систем включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. Бициклический циклоалкил представляет собой моноциклический циклоалкил, слитый с моноциклическим циклоалкильным кольцом. Моноциклические и бициклические циклоалкильные группы могут содержать один или два алкиленовых мостика, каждый из которых состоит из одного, двух, трех или четырех атомов углерода по длине, и каждый мостик связывает два несоседних атома углерода кольцевой системы. Неограничительные примеры бициклических кольцевых систем включают бицикло[3.1.1]гептан, бицикло[2.2.1]гептан, бицикло[2.2.2]октан, бицикло[3.2.2]нонан, бицикло[3.3.1]нонан, и бицикло[4.2.1]нонан, трицикло[3.3.1.03,7]нонан (октагидро-2,5-метанопентален или норадамантан) и трицикло[3.3.1.13,7]декан (адамантан). Спиро циклоалкил представляет собой моноциклический циклоалкил, где два заместителя на одном и том же атоме углерода моноциклического циклоалкильного кольца вместе с указанным атомом углерода образуют второе моноциклическое циклоалкильное кольцо. Моноциклические, бициклические и спиро циклоалкильные группы могут быть незамещенными или замещенными и присоединены к родительской части молекулы через какой-либо замещаемый атом, находящийся в кольцевой системе.
Термин "циклоалкенил", используемый в данном описании, относится к моноциклическому или бициклическому углеводородному кольцевому радикалу. Моноциклический циклоалкенил имеет четыре, пять, шесть, семь или восемь атомов углерода и ноль гетероатомов. Четырехчленные кольцевые системы имеют одну двойную связь, пяти- или шестичленные кольцевые системы имеют одну или две двойные связи, и семи- или восьмичленные кольцевые системы имеют одну, две или три двойных связи. Характерные примеры моноциклических циклоалкенильных групп включают, но без ограничения указанным, циклобутенил, циклопентенил, циклогексенил, циклогептенил и циклооктенил. Бициклический циклоалкенил представляет собой моноциклический циклоалкенил, слитый с моноциклической циклоалкильной группой, или моноциклический циклоалкенил, слитый с моноциклической циклоалкенильной группой. Моноциклическое или бициклическое циклоалкенильное кольцо может содержать один или два алкиленовых мостика, каждый из которых состоит из одного, двух или трех атомов углерода и каждый связывает два несоседних атома углерода кольцевой системы. Характерные примеры бициклических циклоалкенильных групп включают, но без ограничения указанным, 4,5,6,7-тетрагидро-3aH-инден, октагидронафталинил и 1,6-дигидро-пентален. моноциклические и бициклические циклоалкенилы могут быть присоединены к родительской части молекулы через какой-либо замещаемый атом, находящийся в кольцевых системах, и могут быть незамещенными или замещенными.
Термин "гало" или "галоген", используемый в данном описании, означает Cl, Br, I и F.
Термин "галогеналкил", используемый в данном описании, означает алкильную группу, определение которой приведено в данном описании, в которой один, два, три, четыре, пять или шесть атомов водорода замещены галогеном. Термин "C1-С6 галогеналкил" означает C1-С6 алкильную группу, определение которой приведено в данном описании, в которой один, два, три, четыре, пять или шесть атомов водорода замещены галогеном. Термин "C1-С3 галогеналкил" означает C1-С3 алкильную группу, определение которой приведено в данном описании, в которой один, два или три атома водорода замещены галогеном. Характерные примеры галогеналкила включают, но без ограничения указанным, хлорметил, 2-фторэтил, 2,2-дифторэтил, 2,2,2-трифторэтил, трифторметил, дифторметил, петафторэтил, 2-хлор-3-фторпентил, трифторбутил и трифторпропил.
Термин "гетероцикл" или "гетероциклический", используемый в данном описании, означает радикал моноциклического гетероцикла, бициклического гетероцикла и спиро гетероцикла. Моноциклический гетероцикл представляет собой трех-, четырех-, пяти-, шести-, семи- или восьмичленное карбоциклическое кольцо, также содержащее по меньшей мере один гетероатом, независимо выбранный из группы, состоящей из O, N и S. Трех- или четырехчленное кольцо содержит ноль или одну двойную связь и один гетероатом, выбранный из группы, состоящей из O, N и S. Когда два О атома или один О атом и один S атом присутствуют в гетероциклическом кольце, тогда два О атома или один О атом и один S атом не связаны непосредственно друг с другом. Пятичленное кольцо содержит ноль или одну двойную связь и один, два или три гетероатома, выбранные из группы, состоящей из O, N и S. Примеры пятичленных гетероциклических колец включают те, которые содержат в кольце 1 О; 1 S; 1 N; 2 N; 3 N; 1 S и 1 N; 1 S и 2 N; 1 О и 1 N или 1 О и 2 N. Примеры 5-членных гетероциклических групп включают тетрагидрофуранил, дигидрофуранил, тетрагидротиенил, дигидротиенил, имидазолидинил, оксазолидинил, имидазолинил, изоксазолидинил, изоксазолидинил, пирролидинил, 2-пирролинил и 3-пирролинил. Шестичленное кольцо содержит ноль, одну или две двойные связи и один, два или три гетероатома, выбранные из группы, состоящей из O, N и S. Примеры шестичленных гетероциклических колец включают те, которые содержат в кольце 1 O; 2 О; 1 S; 2 S; 1 N; 2 N; 3 N; 1 S, 1 O, и 1 N; 1 S и 1 N; 1 S и 2 N; 1 S и 1 О; 1 S и 2 О; 1 О и 1 N и 1 О и 2 N. Примеры 6-членных гетероциклических групп включают тетрагидропиранил, дигидропиранил, диоксанил, 1,3-диоксоланил, 1,4-дитианил, гексагидропиримидин, морфолинил, пиперазинил, пиперидинил, 2H-пиранил, 4Н-пиранил, пиразолидинил, пиразолинил, 1,2,3,6-тетрагидропиридинил, тетрагидротиопиранил, 1,1-диоксо- гексагидро-1-тиопиранил, 1,1-диоксо-1λ6-тиоморфолинил, тиоморфолинил, тиоксанил и тритианил. Семи- и восьмичленные кольца содержат ноль, один, два или три двойных связи и один, два или три гетероатома, выбранных из группы, состоящей из O, N и S. Характерные примеры моноциклических гетероциклов включают, но без ограничения указанным, азетидинил, азепанил, азиридинил, диазепанил, 1,3-диоксанил, 1,3-диоксоланил, 1,3-дитиоланил, 1,3-дитианил, имидазолинил, имидазолидинил, изотиазолинил, изотиазолидинил, изоксазолинил, изоксазолидинил, морфолинил, оксадиазолинил, оксадиазолидинил, оксазолинил, оксазолидинил, оксетанил, пиперазинил, пиперидинил, пиранил, пиразолинил, пиразолидинил, пирролинил, пирролидинил, тетрагидрофуранил, тетрагидропиридинил, тетрагидропиранил, тетрагидротиенил, тиадиазолинил, тиадиазолидинил, тиазолинил, тиазолидинил, тиоморфолинил, тиопиранил и тритианил. Бициклический гетероцикл представляет собой моноциклический гетероцикл слитый с фенильной группой, или моноциклический гетероцикл, слитый с моноциклическим циклоалкилом, или моноциклический гетероцикл, слитый с моноциклическим циклоалкенилом, или моноциклический гетероцикл, слитый с моноциклическим гетероциклом. Характерные примеры бициклических гетероциклов включают, но без ограничения указанным, бензопиранил, бензотиопиранил, 2,3-дигидробензофуранил, 2,3-дигидробензотиенил, 2,3-дигидро-1H-индолил, 3,4-дигидроизохинолин-2(1H)-ил, 2,3,4,6-тетрагидро-1H-пиридо[1,2-a]пиразин-2-ил, гексагидропирано[3,4-b][1,4]оксазин-1(5H)-ил. Моноциклический гетероцикл и бициклический гетероцикл могут содержать один или два алкиленовых мостика или алкениленовый мостик или их смесь, каждый из которых содержит не более чем четыре атома углерода и каждый связывает два несоседних атома кольцевой системы. Примеры такого мостикового гетероцикла включают, но без ограничения указанным, азабицикло[2.2.1]гептил (включая 2-азабицикло[2.2.1]гепт-2-ил), 8-азабицикло[3.2.1]окт-8-ил, октагидро-2,5-эпоксипентален, гексагидро-2Н-2,5-метаноциклопента[b]фуран, гексагидро-1H-1,4-метаноциклопента[c]фуран, аза-адамантан (1-азатрицикло[3.3.1.13,7]декан) и окса-адамантан (2-оксатрицикло[3.3.1.13,7]декан). Cпиро гетероцикл представляет собой моноциклический гетероцикл, где два заместителя на одном и том же атоме углерода моноциклического гетероциклического кольца вместе с указанным атомом углерода образуют кольцевую систему, выбранную из моноциклического циклоалкила, бициклического циклоалкила, моноциклического гетероцикла или бициклического гетероцикла. Примеры спиро гетероцикла включают, но без ограничения перечисленным, 6-азаспиро[2,5]окт-6-ил, 1'H, 4H-спиро[1,3-бензодиоксин-2,4'-пиперидин]-1'-ил, 1'H, 3H-спиро[2-бензофуран-1,4'-пиперидин]-1'-ил и 1,4-диокса-8-азаспиро[4,5]дес-8-ил. Моноциклические, бициклические и спиро гетероциклы могут быть незамещенными или замещенными. Моноциклические, бициклические и спиро гетероциклы присоединены к родительской части молекулы через какой-либо атом углерода или какой-либо атом азота, находящийся в кольцевых системах. Гетероатомы азота и серы в гетероциклических кольцах могут быть необязательно окисленными (например, 1,1-диоксидотетрагидротиенил, 1,1-диоксидо-1,2-тиазолидинил, 1,1-диоксидотиоморфолинил)) и атомы азота могут быть необязательно кватернизованы.
Термин "гетероарил", используемый в данном описании, означает моноциклический гетероарил и бициклический гетероарил. Моноциклический гетероарил представляет собой пяти- или шестичленное кольцо. Пятичленное кольцо содержит две двойные связи. Пятичленное кольцо может содержать один гетероатом, выбранный из О или S; или один, два, три или четыре атома азота и необязательно один атом кислорода или один серы атом. Шестичленное кольцо содержит три двойные связи и один, два, три или четыре атома азота. Характерные примеры моноциклического гетероарила включают, но без ограничения указанным, фуранил, имидазолил, изоксазолил, изотиазолил, оксадиазолил, 1,3-оксазолил, пиридинил, пиридазинил, пиримидинил, пиразинил, пиразолил, пирролил, тетразолил, тиадиазолил, 1,3-тиазолил, тиенил, триазолил и триазинил. Бициклический гетероарил состоит из моноциклического гетероарила, слитого с фенилом, или моноциклического гетероарила, слитого с моноциклическим циклоалкилом, или моноциклического гетероарила, слитого с моноциклическим циклоалкенилом, или моноциклического гетероарила, слитого с моноциклическим гетероарилом, или моноциклического гетероарила, слитого с моноциклическим гетероциклом. Характерные примеры бициклических гетероарильных групп включают, но без ограничения указанным, бензофуранил, бензотиенил, бензоксазолил, бензимидазолил, бензоксадиазолил, фталазинил, дигидропирроло[3,4-c]пиразол-5(4H)-ил, 6,7-дигидро-пиразолo[1,5-a]пиразин-5(4H)-ил, 6,7-дигидро-1,3-бензотиазолил, имидазо[1,2-a]пиридинил, индазолил, индолил, изоиндолил, изохинолинил, нафтиридинил, пиридоимидазолил, хинолинил, 2,4,6,7-тетрагидро-5H-пиразолo[4,3-c]пиридин-5-ил, тиазолo[5,4-b]пиридин-2-ил, тиазолo[5,4-d]пиримидин-2-ил и 5,6,7,8-тетрагидрохинолин-5-ил. Моноциклические и бициклические гетероарильные группы могут быть замещенными или незамещенными и присоединены к родительской части молекулы через какой-либо замещаемый атом углерода или какой-либо замещаемый атом азота, находящиеся в кольцевых системах. Атом азота в гетероарильных кольцах может быть необязательно окисленным и может быть необязательно кватернизован.
Термин "гетероатом", используемый в данном описании, означает азот, кислород и серу.
Термин "оксо", используемый в данном описании, означает =О группу.
Если часть молекулы описана как "замещенная", неводородный радикал находится на месте водородного радикала какого-либо замещаемого атома части молекулы. Так, например, замещенная гетероциклическая часть молекулы представляет собой гетероциклическую часть молекулы, в которой по меньшей мере один неводородный радикал находится на месте водородного радикала на гетероцикле. Следует осознавать, что если на части молекулы имеется более чем одно замещение, каждый неводородный радикал может быть идентичным или другим (если не оговорено иное).
Если часть молекулы описана как "необязательно замещенная", часть молекулы может быть или (1) незамещенной, или (2) замещенной. Если часть молекулы описана как необязательно замещенная неводородными радикалами в количестве вплоть до конкретного их числа, то часть молекулы может быть или (1) незамещенной, или (2) замещенной неводородными радикалами в количестве вплоть до конкретного их числа или вплоть до максимального числа замещаемых положений на части молекулы, которое меньше его. Так, например, если часть молекулы описана как гетероарил, необязательно замещенный неводородными радикалами в количестве вплоть до 3, тогда какой-либо гетероарил, имеющий менее чем 3 замещаемых положения, мог бы быть необязательно замещенным неводородными радикалами только вплоть до количества замещаемых положений в гетероариле. Для пояснения, тетразолил (который имеет только одно замещаемое положение) способен быть необязательно замещенным неводородным радикалом в количестве вплоть до одного. Для дополнительного пояснения, амино азот описан как необязательно замещенный неводородными радикалами в количестве вплоть до 2, тогда первичный амино азот будет необязательно замещенным неводородными радикалами в количестве вплоть до 2, тогда как вторичный амино азот будет необязательно замещенным неводородными радикалами в количестве только до 1.
Термины "лечить", "процесс лечения" и "лечение" относятся к способу облегчения или устранения болезни и/или ее сопутствующих симптомов. Термины "предотвращать", "предотвращение" и "профилактика" относятся к способу предотвращения начала болезни и/или сопуствующих ей симптомов или избавления субъекта от приобретения болезни.
Используемые в данном описании, "предотвращать", "предотвращение" и "профилактика" также включают задержку начала болезни и/или ее сопутствующих симптомов и снижение для субъекта риска приобретения им болезни.
Выражение "терапевтически эффективное количество" означает количество соединения или его фармацевтически приемлемой соли, достаточное для предотвращения развития или для облегчения до некоторой степени одного или нескольких симптомов состояния или расстройства, подвергаемого лечению, когда соединение вводят одно или в сочетании с другим фармацевтическим агентом или для лечения конкретного субъета или целой популяции. Например, для человека или другого млекопитающего, терапевтически эффективное количество может быть определено экспериментально в лабораторных или клинических условиях, или может быть количеством, требуемым руководящими указаниями United States Food and Drug Administration, или эквивалентного иностранного агентства, для конкретной болезни и субъекта, подвергаемого лечению.
Термин "субъект" относится в данном описании к животным, таким как млекопитающие, включая, но без ограничения перечисленным, приматов (например, людей), коров, овец, коз, лошадей, собак, кошек, кроликов, крыс, мышей и тому подобное. В предпочтительных вариантах осуществления, субъектом является человек.
b. Соединения
Соединения по изобретению имеют общую формулу (I), которая описана выше.
Конкретные значения переменных групп в соединениях формулы (I) приведены далее. Такие значения могут быть использованы, где это подходит, с какими-нибудь другими значениями, определениями, пунктами формулы изобретения или вариантами осуществления, указанными выше или ниже по тексту.
В соединениях формулы (I) Rx имеет значения, указанные в разделе "Сущность изобретения". Например, в конкретных вариантах осуществления, Rx представляет водород или метил. В конкретных вариантах осуществления, Rx представляет водород.
Ry, в соединениях формулы (I), имеет значения, указанные в разделе "Сущность изобретения". Например, в конкретных вариантах осуществления, Ry представляет С1-С3 алкил (например, метил, этил). В конкретных вариантах осуществления, Ry представляет метил.
X1 имеет значения, указанные в разделе "Сущность изобретения". Например, в конкретных вариантах осуществления, X1 представляет N. В конкретных вариантах осуществления, X1 представляет СRx1. Rx1 имеет значения, указанные в разделе "Сущность изобретения" или в вариантах осуществления, приведенных в данном описании. В конкретных вариантах осуществления, Rx1 представляет водород, C2-C6 алкенил, -C(О)ORax1, -C(О)NRbx1Rcx1, -C(О)Rdx1, Gx1 или С1-С6 алкил, где С1-С6 алкил является необязательно замещенным одним заместителем, выбранным из группы, состоящей из ORax1, NRbx1Rcx1 и Gx1. В конкретных вариантах осуществления, Rx1 представляет водород, -C(О)ORax1, -C(О)NRbx1Rcx1, Gx1 или С1-С6 алкил, где С1-С6 алкил является необязательно замещенным ORax1. В конкретных вариантах осуществления, Rx1 представляет водород, -C(О)ORax1, -C(О)NRbx1Rcx1, необязательно замещенный фенил или С1-С6 алкил, где С1-С6 алкил является необязательно замещенным ORax1. В конкретных вариантах осуществления, Rx1 представляет водород, -C(О)ORax1 или -C(О)NRbx1Rcx1. В конкретных вариантах осуществления, Rx1 представляет водород или незамещенный С1-С6 алкил. В конкретных вариантах осуществления, Rx1 представляет -C(О)ORax1, -C(О)NRbx1Rcx1 или C1-C6 алкил, замещенный ORax1. В конкретных вариантах осуществления, Rx1 представляет водород или -C(О)NRbx1Rcx1. В конкретных вариантах осуществления, Rx1 представляет водород. Rax1, Rbx1, Rcx1, Rdx1 и Gx1, имеют значения, указанные в разделе "Сущность изобретения". Например, Rax1 и Rbx1, каждый независимо, представляют водород, C1-C6 алкил (например, метил, этил, изопропил) или C1-C6 галогеналкил (например, трифторметил). В конкретных вариантах осуществления, Rax1 и Rbx1, каждый независимо, представляют водород или C1-C6 алкил (например, метил, этил, изопропил). В конкретных вариантах осуществления, Rax1 и Rbx1, каждый независимо, представляют водород, метил или этил. Rсx1, например, представляет водород, C1-C6 алкил (например, метил, этил, изопропил) или C1-C6 галогеналкил (например, трифторметил, 2,2,2 трифторэтил), где C1-C6 алкил является необязательно замещенным Gx1. В конкретных вариантах осуществления, Rcx1, например, представляет водород или C1-C6 алкил (например, метил, этил, изопропил). В конкретных вариантах осуществления, Rcx1, например, представляет Gx1 или C1-C6 алкил, замещенный Gx1; где Gx1 представляет тиазолил, морфолинил, пиперазинил, тетрагидрофуранил или фенил, каждый из которых является необязательно замещенным 1, 2 или 3 заместителями, выбранными из группы, состоящей из С1-С3 алкила и С1-С3 галогеналкила.
X2 имеет значения, указанные в разделе "Сущность изобретения". Например, в конкретных вариантах осуществления, X2 представляет N. В конкретных вариантах осуществления, X2 представляет СRx2. Rx2 имеет значения, указанные в разделе "Сущность изобретения" или в вариантах осуществления, указанных в данном описании. В конкретных вариантах осуществления, X2 представляет С(О)H или С1-С6 алкил, замещенный одним Gx2. В конкретных вариантах осуществления, X2 представляет С(О)H или С1-С3 алкил, замещенный одним Gx2, где Gx2 представляет пиперидинил, пиперазинил или морфолинил, каждый из которых является необязательно замещенным 1, 2 или 3 С1-С3 алкилами. В конкретных вариантах осуществления, Rx2 представляет водород или незамещенный С1-С6 алкил (например, метил). В конкретных вариантах осуществления, Rx2 представляет водород.
Y1 представляет N или CRu. Например, в конкретных вариантах осуществления, Y1 представляет N. В конкретных вариантах осуществления, Y1 представляет СRu. Ru имеет значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, в конкретных вариантах осуществления, Ru представляет водород или С1-С6 алкил (например, метил). В конкретных вариантах осуществления, Ru представляет водород или С1-С3 алкил (например, метил). В конкретных вариантах осуществления, Ru представляет водород или метил. В конкретных вариантах осуществления, Ru представляет водород.
A1, A2, A3 и A4 имеют значения, указанные в разделе "Сущность изобретения". В конкретных вариантах осуществления, A1 представляет СR1, A2 представляет СR2, A3 представляет СR3 и A4 представляет СR4; или один из A1, A2, A3 и A4 представляет N. В конкретных вариантах осуществления, A1 представляет СR1, A2 представляет СR2, A3 представляет СR3 и A4 представляет СR4. В конкретных вариантах осуществления, один из A1, A2, A3 и A4 представляет N. В вариантах осуществления, в которых один из A1, A2, A3 и A4 представляет N, пример группы соединения включает, но без ограничения перечисленным, такие, где A1 представляет СR1, A2 представляет СR2, A3 представляет СR3 и A4 представляет N. В конкретных вариантах осуществления, два из A1, A2, A3 и A4 представляют N, например, A1 представляет N, A2 представляет СR2, A3 представляет N и A4 представляет СR4; или, например, A1 представляет N, A2 представляет СR2, A3 представляет СR3 и A4 представляет N. В конкретных вариантах осуществления, три из A1, A2, A3 и A4 представляют N, например, A1 представляет N, A2 представляет СR2, A3 представляет N и A4 представляет N.
R1, R3 и R4 имеют значения, указанные в разделе "Сущность изобретения". Например, в конкретных вариантах осуществления, R1, R3 и R4, каждый независимо, представляют водород, С1-С6 алкил (например, метил, этил), галоген (например, Br, F или Cl) или CN. Например, в конкретных вариантах осуществления, R1, R3 и R4, каждый независимо, представляют водород, С1-С6 алкил (например, метил, этил) или С1-С6 галогеналкил (например, трифторметил). В конкретных вариантах осуществления, R1, R3 и R4, каждый независимо, представляют водород или метил. В конкретных вариантах осуществления, R1, R3 и R4 представляют водород.
R2 имеет значения, указанные в разделе "Сущность изобретения". В конкретном варианте осуществления, R2, например, представляет галоген, галогеналкил (например, CF3) или -(С1-С3 алкиленил)-CN. В конкретных вариантах осуществления, R2, например, представляет водород, С1-С6 алкил, NO2, G2a, -S(О)2R2d, -S(О)2NR2bR2c, -C(О)R2d, -C(О)OR2a, -C(О)NR2bR2c, -NR2bR2c, -N(R2e)C(О)R2d, -N(R2e)S(О)2R2d, -N(R2e)S(О)2NR2bR2c, -(C1-C6 алкиленил)-G2a, -(C1-C6 алкиленил)-OR2a, -(C1-C6 алкиленил)-S(О)2R2d, -(C1-C6 алкиленил)-S(О)2NR2bR2c, -(C1-C6 алкиленил)-C(О)R2d, -(C1-C6 алкиленил)-C(О)OR2a, -(C1-C6 алкиленил)-C(О)NR2bR2c, -(C1-C6 алкиленил)-NR2bR2c, -(C1-C6 алкиленил)-N(R2e)C(О)R2d, -(C1-C6 алкиленил)-N(R2e)S(О)2R2d или -(C1-C6 алкиленил)-N(R2e)S(О)2NR2bR2c. В конкретных вариантах осуществления, R2, например, представляет водород или NO2. В конкретных вариантах осуществления, R2, например, представляет G2a, -S(О)2R2d, -S(О)2NR2bR2c, -C(О)R2d, -C(О)OR2a, -C(О)NR2bR2c, -NR2bR2c, -N(R2e)C(О)R2d, -N(R2e)S(О)2R2d, -N(R2e)S(О)2NR2bR2c, -(C1-C6 алкиленил)-G2a, -(C1-C6 алкиленил)-OR2a, -(C1-C6 алкиленил)-S(О)2R2d, -(C1-C6 алкиленил)-S(О)2NR2bR2c, -(C1-C6 алкиленил)-C(О)R2d, -(C1-C6 алкиленил)-C(О)OR2a, -(C1-C6 алкиленил)-C(О)NR2bR2c, -(C1-C6 алкиленил)-NR2bR2c, -(C1-C6 алкиленил)-N(R2e)C(О)R2d, -(C1-C6 алкиленил)-N(R2e)S(О)2R2d или -(C1-C6 алкиленил)-N(R2e)S(О)2NR2bR2c. В конкретных вариантах осуществления, R2, например, представляет -S(О)2R2d, -S(О)2NR2bR2c, -C(О)R2d, -C(О)NR2bR2c, -N(R2e)C(О)R2d, -N(R2e)S(О)2R2d, -N(R2e)S(О)2NR2bR2c, -(C1-C6 алкиленил)-S(О)2R2d, -(C1-C6 алкиленил)-S(О)2NR2bR2c, -(C1-C6 алкиленил)-C(О)R2d, -(C1-C6 алкиленил)-C(О)NR2bR2c, -(C1-C6 алкиленил)-N(R2e)C(О)R2d, -(C1-C6 алкиленил)-N(R2e)S(О)2R2d или -(C1-C6 алкиленил)-N(R2e)S(О)2NR2bR2c. В конкретных вариантах осуществления, R2, например, представляет -S(О)2R2d, -S(О)2NR2bR2c, -N(R2e)S(О)2R2d или -N(R2e)S(О)2NR2bR2c. В конкретном варианте осуществления, R2, например, представляет -S(О)2R2d, -S(О)2NR2bR2°, -N(R2e)S(О)2R2d или -(C1-C6 алкиленил)-S(О)2R2d. В конкретном варианте осуществления, R2, например, представляет -(C1-C3 алкиленил)-S(О)2R2d, где R2d представляет C1-C3 алкил. В конкретном варианте осуществления, R2, например, представляет -(CH2)-S(О)2R2d, где R2d представляет метил или этил.
G2a, R2a, R2b, R2c, R2d и R2e имеют значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, приведенных в данном описании ниже.
В вариантах осуществления, где R2 представляет G2a, G2a имеет значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, приведенных в данном описании. Например, в конкретных вариантах осуществления, G2a представляет необязательно замещенный гетероцикл. В конкретных вариантах осуществления, G2a представляет необязательно замещенный моноциклический гетероцикл. В конкретных вариантах осуществления, G2a представляет 1,2-диоксидо-1,2-тиазолидин-2-ил или тетрагидропиридинил, каждый из которых является необязательно замещенным. В конкретных вариантах осуществления, G2a является необязательно замещенным 1,2-диоксидо-1,2-тиазолидин-2-илом. В конкретном варианте осуществления, G2a представляет арил или гетероарил, каждый из которых является необязательно замещенным. В конкретных вариантах осуществления, G2a является необязательно замещенным фенилом. В конкретных вариантах осуществления, G2a представляет пиридинил или пиразолил, каждый из которых является необязательно замещенным. В конкретных вариантах осуществления, G2a является незамещенным.
В вариантах осуществления, где R2 представляет -(С1-С6 алкиленил)-G2a, G2a имеет значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, в конкретных вариантах осуществления, G2a представляет гетероцикл или гетероарил, каждый из которых является необязательно замещенным. В конкретных вариантах осуществления, G2a представляет моноциклический гетероцикл или моноциклический гетероарил, каждый из которых является необязательно замещенным. В конкретных вариантах осуществления, G2a представляет 1,1-диоксидо-1,2-тиазолидин-2-ил, пирролидинил, морфолинил или пиразолил, каждый из которых является необязательно замещенным. В конкретных вариантах осуществления, G2a является незамещенным. В конкретных вариантах осуществления, G2a представляет необязательно замещенный фенил.
Когда G2a группа является необязательно замещенной, она, например, необязательно замещена 1, 2, 3, 4 или 5 Rv. Rv имеет значения, указанные в разделе "Сущность изобретения", например, Rv представляет С1-С6 алкил (например, метил), галоген (например, F, Cl), С1-С6 галогеналкил, -CN, -NRjRk или -C(О)ORh; или например, Rv представляет С1-С6 алкил (например, метил), галоген (например, F, Cl) или С1-С6 галогеналкил.
В вариантах осуществления, где R2 представляет -S(О)2R2d, R2d имеет значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. В конкретных вариантах осуществления, R2d представляет С1-С6 галогеналкил (например, CF3), G2b, незамещенный С1-С6 алкил (например, метил, этил, изопропил) или С1-С6 алкил, замещенн одной G2b группой, где G2b представляет фенил, моноциклический циклоалкил или моноциклический гетероцикл, каждый из которых является необязательно замещенным. В некоторых таких вариантах осуществления, G2b групп является необязательно замещенной 1, 2 или 3 Rv группами, где Rv имеет значения, указанные в разделе "Сущность изобретения" и здесь, например, каждый Rv независимо представляет С1-С6 алкил (например, метил), галоген (например, F, Cl), С1-С6 галогеналкил, -ORh, -CN или –NRjRk. В конкретных вариантах осуществления, R2d представляет С1-С6 галогеналкил или незамещенный С1-С6 алкил. В конкретных вариантах осуществления, R2d представляет метил или этил.
В вариантах осуществления, где R2 представляет -S(О)2NR2bR2c, R2b и R2c имеют значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, в конкретных вариантах осуществления, R2b представляет водород или незамещенный С1-С6 алкил (например, метил, этил) и R2c представляет водород, незамещенный С1-С6 алкил (например, метил, этил) или С1-С6 галогеналкил (например, 2,2,2-трифторэтил, 2-фторэтил). В конкретных вариантах осуществления, R2b представляет водород и R2c представляет необязательно замещенный фенил или R2c представляет С1-С3 алкил, замещенный одной G2b группой, где G2b представляет необязательно замещенный пиридинил.
В вариантах осуществления, где R2 представляет -C(О)R2d, R2d имеет значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, в конкретных вариантах осуществления, R2d представляет G2b, где G2b имеет значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, в конкретных вариантах осуществления, G2b представляет необязательно замещенный гетероцикл. В конкретных вариантах осуществления, G2b представляет необязательно замещенный моноциклический гетероцикл. В конкретных вариантах осуществления, G2b представляет 1,1-диоксидотиоморфолин-4-ил, пиперазинил, пиперидинил, пирролидин-1-ил или морфолин-4-ил, каждый из которых является необязательно замещенным. Каждый G2b является необязательно замещенным, как описано в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, каждый G2b независимо является незамещенным или замещенным 1, 2 или 3 Rv. Rv имеет значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления. Например, каждый Rv независимо представляет С1-С6 алкил (например, метил), оксо, N(H)C(О)O(С1-С6 алкил), -CH2-C(О)NRjRk, -C(О)-моноциклический гетероцикл или -C(О)-моноциклический гетероарил. В конкретных вариантах осуществления, каждый Rv независимо представляет С1-С6 алкил (например, метил), оксо или N(H)C(О)O(С1-С6 алкил).
В вариантах осуществления, где R2 представляет -C(О)OR2a, R2a имеет значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления. Например, в конкретных вариантах осуществления, R2a представляет водород или незамещенный С1-С6 алкил (например, метил, этил).
В вариантах осуществления, где R2 представляет -C(О)NR2bR2c, R2b и R2c имеют значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, в конкретных вариантах осуществления, R2b представляет водород или незамещенный С1-С6 алкил (например, метил) и R2c представляет водород, G2b, С1-С6 галогеналкил (например, 2,2-дифторэтил), С1-С6 алкил (например, метил, этил), где С1-С6 алкил является необязательно замещенным одним заместителем, выбранным из группы, состоящей из -ORz1, NRz1Rz2 и G2b. Rz1, Rz2 и G2 имеют значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, в конкретных вариантах осуществления, G2b является необязательно замещенным фенилом. В конкретных вариантах осуществления, G2b представляет циклоалкил, гетероарил, или гетероцикл, каждый из которых является необязательно замещенным. В конкретных вариантах осуществления, G2b представляет моноциклический циклоалкил, моноциклический гетероарил или моноциклический гетероцикл, каждый из которых является необязательно замещенным. В конкретных вариантах осуществления, G2b представляет пиридинил, пиримидинил, индазолил, индолил, циклопентил, тиазолил, 1,1-диоксидотетрагидротиенил, тетрагидрофуранил, пиперазинил, пиперидинил или пирролидинил, каждый из которых является необязательно замещенным. Каждый G2b является необязательно замещенным, как описано в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, каждый G2b независимо является незамещенным или замещенным 1, 2 или 3 Rv. Rv имеет значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, приведенных в данном описании. Например, каждый Rv независимо представляет С1-С6 алкил (например, метил), С1-С6 галогеналкил, -ORh, -C(О)ORh, -S(О)2Rh, галоген или оксо. В конкретных вариантах осуществления, каждый Rv независимо представляет С1-С6 алкил (например, метил) или оксо.
В вариантах осуществления, где R2 представляет -NR2bR2c, R2b и R2c имеют значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, в конкретных вариантах осуществления, R2b и R2c, каждый независимо, представляют водород или незамещенный С1-С6 алкил (например, метил, этил).
В вариантах осуществления, где R2 представляет -N(R2е)C(О)R2d, R2d и R2e имеют значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, в конкретных вариантах осуществления, R2e - водород или незамещенный С1-С6 алкил (например, метил, этил), и R2d представляет незамещенный С1-С6 алкил (например, метил, этил, трет-бутил) или С1-С6 галогеналкил (например, 2,2,2-трифторэтил).
В вариантах осуществления, где R2 представляет -N(R2e)S(О)2R2d, R2d и R2e имеют значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, в конкретных вариантах осуществления, R2e представляет водород или незамещенный С1-С6 алкил (например, метил, этил) и R2d представляет незамещенный С1-С6 алкил (например, метил, этил) или С1-С6 галогеналкил (например, 2,2,2-трифторэтил, 2-фторэтил, 2,2-дифторэтил). В конкретных вариантах осуществления, R2e представляет водород и R2d представляет незамещенный С1-С6 алкил (например, метил, этил). В конкретных вариантах осуществления, R2e представляет С1-С6 галогеналкил или С1-С6 алкил, замещенный одним заместителем, выбранным из группы, состоящей из -ORz1, -NRz1Rz2 и G2b, и R2d представляет незамещенный алкил (например, метил, этил). В конкретных вариантах осуществления, R2e представляет С1-С6 галогеналкил (например, 3,3,3-трифторпропил) или С1-С3 алкил, замещенный одним заместителем, выбранным из группы, состоящей из -ORz1, -NRz1Rz2 и G2b, и R2d представляет незамещенный С1-С6 алкил (например, метил, этил), где G2b представляет моноциклический циклоалкил (например, циклопропил), моноциклический гетероцикл (например, пирролидинил или тетрагидрофуранил) или моноциклический гетероарил (например, пиридинил), каждый из которых является необязательно замещенным.
В вариантах осуществления, где R2 представляет -N(R2e)S(О)2NR2bR2c, R2b, R2c и R2е имеют значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, в конкретных вариантах осуществления, R2b, R2c и R2е, каждый независимо, представляют водород или незамещенный С1-С6 алкил (например, метил, этил).
В вариантах осуществления, где R2 представляет -(С1-С6 алкиленил)-OR2a, R2a имеет значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. В конкретных вариантах осуществления R2a представляет водород. В конкретных вариантах осуществления, R2 представляет -CH2-OH или -CH2CH2-OH.
В вариантах осуществления, где R2 представляет -(С1-С6 алкиленил)-C(О)OR2a, R2a имеет значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, R2a представляет водород или незамещенный С1-С6 алкил (например, метил, этил).
В вариантах осуществления, где R2 представляет -(С1-С6 алкиленил)-C(О)NR2bR2c, R2b и R2c имеют значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, в конкретных вариантах осуществления, R2b и R2c, каждый независимо, представляют водород или незамещенный С1-С6 алкил (например, метил, этил).
В вариантах осуществления, где R2 представляет -(С1-С6 алкиленил)-N(R2e)C(О)R2d, R2d и R2e имеют значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, в конкретных вариантах осуществления, R2е представляет водород или незамещенный С1-С6 алкил (например, метил, этил) и R2d представляет С1-С6 алкил (например, метил), необязательно замещенный C(О)ORz1.
В вариантах осуществления, где R2 представляет -(С1-С6 алкиленил)-S(О)2R2d, R2d имеет значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, в конкретных вариантах осуществления, R2d представляет необязательно замещенный фенил или незамещенный С1-С6 алкил. В конкретных вариантах осуществления, R2d представляет незамещенный С1-С3 алкил. В конкретных вариантах осуществления, R2d представляет метил или этил. В конкретных вариантах осуществления, R2d представляет необязательно замещенный фенил.
L1 имеет значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, в конкретных вариантах осуществления, L1 отсутствует или означает CH2, C(H)(OH), C(O), (CH2)mO или (CH2)mN(Rz). Например, в конкретных вариантах осуществления, L1 представляет СH2, C(O), (CH2)mO или (CH2)mN(Rz). В конкретных вариантах осуществления, L1 представляет (CH2)mO или (CH2)mN(Rz). В конкретных вариантах осуществления, L1 представляет (CН2)mO. В конкретных вариантах осуществления, L1 представляет (CH2)mN(Rz).
Переменная m означает 0 или 1. В конкретных вариантах осуществления, m означает 0. В конкретных вариантах осуществления, m означает 1.
Rz, имеет значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, Rz представляет водород или С1-С3 алкил. В конкретных вариантах осуществления, Rz представляет водород.
G1 имеет значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, G1 представляет G1a. В конкретных вариантах осуществления, G1 представляет -(С1-С6 алкиленил)-G1a. В конкретных вариантах осуществления, G1 представляет С1-С6 алкил или алкоксиалкил. В конкретных вариантах осуществления, G1 представляет С1-С6 алкил (например, метил, этил, изобутил или 2,2-диметилпропил). В конкретных вариантах осуществления, G1 представляет алкоксиалкил.
G1a имеет значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления, указанных в данном описании. Например, в конкретных вариантах осуществления, G1a представляет арил, гетероцикл или циклоалкил, каждый из которых является необязательно замещенным. В конкретных вариантах осуществления, G1a представляет арил, гетероцикл, гетероарил или циклоалкил, каждый из которых является необязательно замещенным. В конкретных вариантах осуществления, G1a представляет необязательно замещенный арил. В конкретных вариантах осуществления G1a представляет необязательно замещенный гетероцикл. В конкретных вариантах осуществления G1a представляет необязательно замещенный гетероарил. В конкретных вариантах осуществления G1a представляет необязательно замещенный циклоалкил.
В вариантах осуществления, где G1a является необязательно замещенным арилом, G1a, например, представляет фенил, нафтил или инданил, каждый из которых является необязательно замещенным. В конкретных вариантах осуществления, G1a, например, является необязательно замещенным фенилом. В конкретных вариантах осуществления, G1a, например, представляет фенил, необязательно замещенный одним или двумя атомами галогена (например, F). В конкретных вариантах осуществления, G1a представляет
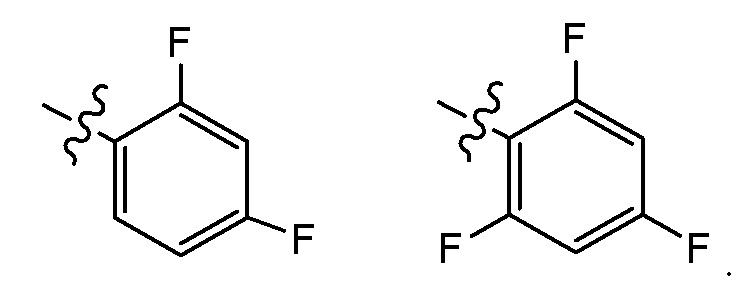
В конкретных вариантах осуществления, G1a представляет фенил или
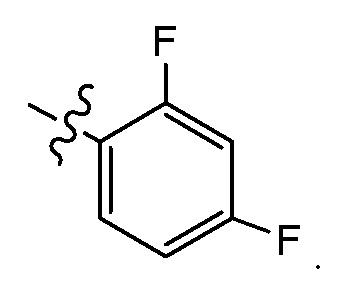
В вариантах осуществления, где G1а является необязательно замещенным гетероциклом, примеры гетероцикла включают, но без ограничения указанным, оксетанил, тетрагидрофуранил (например, тетрагидрофуран-2-ил, тетрагидрофуран-3-ил), пирролидинил, морфолинил, пиперидинил, тетрагидротиопиранил и тетрагидропиранил (например, тетрагидропиран-4-ил, тетрагидропиран-3-ил), каждый из которых (включая типичные кольца) является необязательно замещенным.
В вариантах осуществления, где G1a является необязательно замещенным гетероарилом, G1a, например, представляет пиразолил, пиридинил, пиримидинил, 2,1,3-бензотиадиазолил, хинолинил или изохинолинил, каждый из которых является необязательно замещенным.
В вариантах осуществления, где G1a является необязательно замещенным циклоалкилом (например, необязательно замещенным моноциклическим циклоалкилом), примеры циклоалкила включают, но без ограничения указанным, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, бицикло[2.2.1]гептил и адамантил, каждый из которых является необязательно замещенным. В конкретных вариантах осуществления, G1a является необязательно замещенным циклоалкилом. В конкретных вариантах осуществления, G1a представляет незамещенный циклоалкил. В конкретных вариантах осуществления, G1a представляет замещенный циклоалкил. В конкретных вариантах осуществления, G1a представляет циклогексил, необязательно замещенный 1 или двумя заместителями, выбранными из группы, состоящей из С1-С3 алкила (например, метила), О(С1-С3 алкила) и галогена. В конкретных вариантах осуществления, G1a представляет циклогексил, необязательно замещенный 1 или двумя заместителями, выбранными из группы, состоящей из метила и О(СН3). В конкретных вариантах осуществления, G1a представляет 4,4-дифторциклогексил. В конкретных вариантах осуществления, G1а представляет необязательно замещенный циклопропил. В конкретных вариантах осуществления, G1a представляет незамещенный циклопропил.
Необязательные заместители G1a указаны в разделе "Сущность изобретения" и в вариантах осуществления. Например, каждый G1a независимо является незамещенны или замещенным 1, 2, 3, 4 или 5 Rw. В конкретных вариантах осуществления, Rw представляет, например, С1-С6 алкил, -CN, галоген (например, F, Cl), оксо, С1-С6 галогеналкил (например, трифторметил), -ORh, NRjRk, -S(О)2Rh, -C(О)Rh, -C(О)ORh, -C(О)NRjRk, -(С1-С3 алкиленил)-ORh или -(С1-С3 алкиленил)C(О)NRjRk. В конкретных вариантах осуществления, Rw представляет, например, С1-С6 алкил, -CN, галоген (например, F, Cl) или С1-С6 галогеналкил (например, трифторметил). В конкретных вариантах осуществления, Rw представляет галоген, -ORh или С1-С6 алкил. В конкретных вариантах осуществления, Rw представляет галоген. В конкретных вариантах осуществления, Rw представляет F.
Следует принимать во внимание, что соединения формулы (I) с комбинациями указанных вариантов осуществления, включая конкретные, более конкретные и предпочтительные варианты осуществления рассматриваются. Все варианты осуществления соединений формулы (I), образованные путем комбинирования вариантов заместителя, обсуждавшиеся выше, находятся в сфере действия данного изобретения и некоторые варианты осуществления соединений формулы (I) представлены ниже.
Соответственно, один аспект изобретения относится к группе соединений формулы (I), где L представляет (CH2)mO и G1 представляет G1a и G1a имеет значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления выше.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет N, X1 представляет СRx1 и X2 представляет СRx2.
Еще одни примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет N, X1 представляет СRx1, X2 представляет СRx2 и Ry представляет метил.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет N, X1 представляет СRx1, X2 представляет СRх2, Ry представляет метил и L1 представляет СH2, C(O), (CH2)mO или (CH2)mN(Rz). В конкретных вариантах осуществления, L1 представляет (CH2)mO. В еще одних вариантах осуществления, L1 представляет (CH2)mO и m означает 0. В еще одних вариантах осуществления, L1 представляет (CH2)mO и m означает 1. В конкретных вариантах осуществления, L1 представляет (CH2)mN(Rz). В конкретных вариантах осуществления, L1 представляет (CH2)mN(Rz) и m означает 0. В еще одних вариантах осуществления, L1 представляет (CH2)mN(Rz) и m означает 1. Rz имеет значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления выше.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет N, X1 представляет СRx1, X2 представляет СRx2, Ry представляет метил, L1 представляет (CH2)mO и G1 представляет -(C1-C6 алкиленил)-G1a, где G1a представляет необязательно замещенный фенил.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет N, X1 представляет СRx1, X2 представляет СRx2, Ry представляет метил, L1 представляет (CH2)mO и G1 представляет -(C1-C6 алкиленил)-G1a, где G1a представляет необязательно замещенный циклоалкил. В некоторых вариантах осуществления, G1a представляет незамещенный циклопропил.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y' представляет N, X1 представляет СRx1, X2 представляет СRx2, Ry представляет метил, L1 представляет (CH2)mO и G1 представляет G1a.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет N, X1 представляет СRx1, X2 представляет СRх2, Ry представляет метил, L1 представляет (CH2)mO, G1 представляет G1a и G1a представляет необязательно замещенный арил.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет N, X1 представляет СRx1, X2 представляет СRх2, Ry представляет метил, L1 представляет (CH2)mO, G1 представляет G1a и G1a представляет необязательно замещенный фенил.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет N, X1 представляет СRx1, X2 представляет СRx2, Ry представляет метил, L1 представляет (CH2)mO, G1 представляет G1a и G1a представляет необязательно замещенный циклоалкил (например, необязательно замещенный моноциклический циклоалкил).
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет N, X1 представляет СRx1, X2 представляет СRx2, Ry представляет метил, L1 представляет (CH2)mO, G1 представляет G1a, и G1a представляет необязательно замещенный гетероцикл (например, необязательно замещенный моноциклический гетероцикл).
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu, X1 представляет СRx1 и X2 представляет СRх2.
Еще одни примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu, X1 представляет СRx1, X2 представляет СRх2 и Ry представляет метил.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu; X1 представляет СRx1, X2 представляет СRx2, Ry представляет метил и L1 представляет СH2, C(O), (CH2)mO или (CH2)mN(Rz). В конкретных вариантах осуществления, L1 представляет (CH2)mO. В еще одних вариантах осуществления, L1 представляет (CH2)mO и m означает 0. В еще одних вариантах осуществления, L1 представляет (CH2)mO и m означает 1. В конкретных вариантах осуществления, L1 представляет (CH2)mN(Rz). В конкретных вариантах осуществления, L1 представляет (CH2)mN(Rz) и m означает 0. В еще одних вариантах осуществления, L1 представляет (CH2)mN(Rz) и m означает 1. Rz имеет значения, описанные в разделе "Сущность изобретения" и в вариантах осуществления выше.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu; X1 представляет СRx1, X2 представляет СRx2, Ry представляет метил, L1 представляет (CH2)mN(Rz) и G1 представляет G1a или -(C1-C6 алкиленил)-G1a, где G1a представляет фенил, моноциклический гетероцикл (например, тетрагидрофуранил) или моноциклический циклоалкил (например, циклопропил, циклопентил, циклогексил), каждый из которых (включая типичные кольца) является необязательно замещенным.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu; X1 представляет СRx1, X2 представляет СRх2, Ry представляет метил, L1 представляет (CH2)mN(Rz), m означает 0, Rz представляет водород и G1 представляет G1a, где G1a представляет фенил, моноциклический гетероцикл (например, тетрагидрофуранил) или моноциклический циклоалкил (например, циклопропил, циклопентил, циклогексил), каждый из которых (включая типичные кольца) является необязательно замещенным.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu; X1 представляет СRx1, X2 представляет СRx2, Ry представляет метил, L1 представляет (CH2)mN(Rz), m означает 0, Rz представляет водород и G1 представляет -(C1-C6 алкиленил)-G1a, где G1a представляет моноциклический гетероцикл (например, тетрагидрофуранил) или моноциклический циклоалкил (например, циклопропил, циклопентил, циклогексил), каждый из которых (включая типичные кольца) является необязательно замещенным. В некоторых вариантах осуществления, G1 представляет -(С1-С3 алкиленил)-G1a, где G1a представляет необязательно замещенный моноциклический циклоалкил (например, циклопропил, циклопентил, циклогексил, каждый из которых является необязательно замещенным). В некоторых вариантах осуществления, G1 представляет -(CH2)-G1a, где G1a представляет необязательно замещенный моноциклический циклоалкил (например, циклопропил, циклопентил, циклогексил, каждый из которых является необязательно замещенным). В конкретных вариантах осуществления, G1a является необязательно замещенным и представляет моноциклический гетероцикл (например, необязательно замещенный тетрагидрофуранил). В конкретных вариантах осуществления, G1a представляет необязательно замещенный циклопропил. В некоторых вариантах осуществления, G1a представляет незамещенный циклопропил.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu; X1 представляет СRx1, X2 представляет СRx2, Ry представляет метил, L1 представляет (CH2)mO и G1 представляет С1-C6 алкил или алкоксиалкил. В конкретных вариантах осуществления, G1 представляет С1-C6 алкил (например, метил, этил, изoбутил или 2,2-диметилпропил). В конкретных вариантах осуществления, G1 представляет алкоксиалкил.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu; X1 представляет СRx1; X2 представляет СRx2, Ry представляет метил, L1 представляет (CH2)mO и G1 представляет -(C1-C6 алкиленил)-G1a, где G1a представляет необязательно замещенный фенил.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu; X1 представляет СRx1, X2 представляет СRx2, Ry представляет метил, L1 представляет (CH2)mO и G1 представляет -(C1-C6 алкиленил)-G1a, где G1a представляет необязательно замещенный циклоалкил. В некоторых вариантах осуществления, G1a представляет необязательно замещенный циклопропил. В некоторых вариантах осуществления, G1a представляет незамещенный циклопропил.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu; X1 представляет СRx1, X2 представляет СRx2, Ry представляет метил, L1 представляет (CH2)mO и G1 представляет G1a.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu, X1 представляет СRx1, X2 представляет СRx2, Ry представляет метил, L1 представляет (CH2)mO G1 представляет G1a и G1a представляет необязательно замещенный арил.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu; X1 представляет СRx1, X2 представляет СRx2, Ry представляет метил, L1 представляет (CH2)mO, G1 представляет G1a и G1a представляет необязательно замещенный фенил.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu, X1 представляет СRx1, X2 представляет СRx2, Ry представляет метил, L1 представляет (CH2)mO, G1 представляет G1a и G1a представляет необязательно замещенный циклоалкил (например, необязательно замещенный моноциклический циклоалкил).
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu, X1 представляет СRx1, X2 представляет СRх2, Ry представляет метил, L1 представляет (CH2)mO, G1 представляет G1a и G1a представляет необязательно замещенный гетероцикл (например, необязательно замещенный моноциклический гетероцикл).
Еще другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu, X1 представляет N, X2 представляет СRх2 и Ry представляет метил.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu, X1 представляет N, X2 представляет СRx2, Ry представляет метил и L1 представляет СH2, C(O), (CH2)mO или (CH2)mN(Rz). В конкретных вариантах осуществления, L1 представляет (CH2)mO. В еще других вариантах осуществления, L1 представляет (CH2)mO и m означает 0. В еще других вариантах осуществления, L1 представляет (CH2)mO и m означает 1. В конкретных вариантах осуществления, L1 представляет (CH2)mN(Rz). В конкретных вариантах осуществления, L1 представляет (CH2)mN(Rz) и m означает 0. В еще других вариантах осуществления, L1 представляет (CH2)mN(Rz) и m означает 1. Rz имеет имеет значения, описанные в разделе "Сущность изобретения" и в вариантах осуществления выше.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu, X1 представляет N, X2 представляет СRx2, Ry представляет метил, L1 представляет (CH2)mO и G1 представляет G1a.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu, X1 представляет N, X2 представляет СRx2, Ry представляет метил, L1 представляет (CH2)mO, G1 представляет G1a и G1a представляет необязательно замещенный арил.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu, X1 представляет N, X2 представляет СRх2, Ry представляет метил, L1 представляет (CH2)mO, G1 представляет G1a и G1a представляет необязательно замещенный фенил.
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu, X1 представляет N, X2 представляет СRх2, Ry представляет метил, L1 представляет (CH2)mO, G1 представляет G1a и G1a представляет необязательно замещенный циклоалкил (например, необязательно замещенный моноциклический циклоалкил).
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu, X1 представляет N, X2 представляет СRx2, Ry представляет метил, L1 представляет (CH2)mO, G1 представляет G1a и G1a представляет необязательно замещенный гетероцикл (например, необязательно замещенный моноциклический гетероцикл).
Другие примеры группы соединений формулы (I) относятся к тем, в которых Y1 представляет СRu, X1 представляет N, X2 представляет СRx2, Ry представляет метил, L1 представляет (CH2)mO и G1 представляет -(C1-C6 алкиленил)-G1a, где G1a представляет необязательно замещенный циклоалкил. В некоторых вариантах осуществления, G1a представляет необязательно замещенный циклопропил. В некоторых вариантах осуществления, G1a представляет незамещенный циклопропил.
Внутри каждой группы соединений формулы (I), описанной выше, A1, A2, A3 и A4 имеют значения, указанные в разделе "Сущность изобретения" и в вариантах осуществления выше.
Например, в каждой группе соединений формулы (I), описанной выше, примеры подгруппы включают те, в которых A представляет СR1, A2 представляет СR2, A3 представляет СR3 и A4 представляет CR4 или одна из A1, A2, A3 и A4 представляет N.
Другие примеры подгруппы включают, но без ограничения указанным, такие, где A1 представляет СR1, A2 представляет СR2, A3 представляет СR3 и A4 представляет СR4.
Другие примеры подгруппы включают, но без ограничения указанным, такие, где одна из A1, A2, A3 и A4 представляет N.
Еще другие примеры подгруппы включают, но без ограничения указанным, такие, где A1 представляет CR1, A2 представляет СR2, A3 представляет СR3 и A4 представляет N.
Еще другие примеры подгруппы включают, но без ограничения указанным, такие, где две из A1, A2, A3 и A4 представляют N.
Еще другие примеры подгруппы включают, но без ограничения указанным, такие, где A1 представляет N, A2 представляет СR2, A3 представляет N и A4 представляет СR4.
Еще другие примеры подгруппы включают, но без ограничения указанным, такие, где A1 представляет N, A2 представляет СR2, A3 представляет СR3 и A4 представляет N.
Еще другие примеры подгруппы включают, но без ограничения указанным, такие, где три из A1, A2, A3, и A4 представляют N.
Еще другие примеры подгруппы включают, но без ограничения указанным, такие, где A1 представляет N, A2 представляет СR2, A3 представляет N и A4 представляет N.
Различные группы и подгруппы соединений формулы (I), раскрытые в предыдущих разделах, R1, R2, R3, R4, Rx, Ru, Rx1, Rx2, m и необязательные заместители G1 являются такими, как описано в разделе "Сущность изобретения" и в вариантах осуществления выше.
Например, из всех групп и подгрупп соединений формулы (I), раскрытых в предыдущих разделах, R2 представляет водород, C1-C6 алкил, NO2, G2a, -S(О)2R2d, -S(О)2NR2bR2c, -C(О)R2d, -C(О)OR2a, -C(О)NR2bR2c, -NR2bR2c, -N(R2e)C(О)R2d, -N(R2e)S(О)2R2d, -N(R2e)S(О)2NR2bR2c, -(C1-C6 алкиленил)-G2a, -(C1-C6 алкиленил)-OR2a, -(C1-C6 алкиленил)-S(О)2R2d, -(C1-C6 алкиленил)-S(О)2NR2bR2c, -(C1-C6 алкиленил)-C(О)R2d, -(C1-C6 алкиленил)-C(О)OR2a, -(C1-C6 алкиленил)-C(О)NR2bR2c, -(C1-C6 алкиленил)-NR2bR2c, -(C1-C6 алкиленил)-N(R2e)C(О)R2d, -(C1-C6 алкиленил)-N(R2e)S(О)2R2d или -(C1-C6 алкиленил)-N(R2e)S(О)2NR2bR2c. В конкретных вариантах осуществления, R2 представляет -S(О)2R2d, -S(О)2NR2bR2c, -N(R2e)S(О)2R2d или -N(R2e)S(О)2NR2bR2c. В некоторых вариантах осуществления, R2 представляет -S(О)2R2d, -S(О)2NR2bR2c, -N(R2e)S(О)2R2d или -(C1-C6 алкиленил)-S(О)2R2d.
Например, из всех групп и подгрупп соединений формулы (I), раскрытых в предыдущих разделах, R2 представляет -S(О)2R2d, -S(О)2NR2bR2с, -N(R2e)S(О)2R2d или -N(R2e)S(О)2NR2bR2c и Rx представляет водород или метил. В конкретных вариантах осуществления, Rx представляет водород.
Например, из всех групп и подгрупп соединений формулы (I), раскрытых в предыдущих разделах, R2 представляет -S(О)2R2d, -S(О)2NR2bR2c, -N(R2e)S(О)2R2d или -N(R2e)S(О)2NR2bR2c, Rx представляет водород и Rx1 представляет водород, -C(О)ORax1, -C(О)NRbx1Rcx1, Gx1 или C1-C6 алкил, где C1-C6 алкил является необязательно замещенным ORax1. В конкретных вариантах осуществления, Rx1 представляет водород, -C(О)ORax1 или -C(О)NRbx1Rcx1.
Например, из всех групп и подгрупп соединений формулы (I), раскрытых в предыдущих разделах, R2 представляет -S(О)2R2d, -S(О)2NR2bR2c, -N(R2e)S(О)2R2d или -N(R2e)S(О)2NR2bR2c, Rx представляет водород, Rx1 представляет водород, -C(О)ORax1 или -C(О)NRbx1Rcx1 и Rx2 представляет водород.
Например, из всех групп и подгрупп соединения формулы (I), раскрытых в предыдущих разделах, R2 представляет -S(О)2R2d, -S(О)2NR2bR2c, -N(R2e)S(О)2R2d или -(C1-C6 алкиленил)S(О)2R2d, Rx представляет водород, Rx1 представляет водород или -C(О)NRbx1Rcx1 и Rx2 представляет водород.
Один аспект изобретения относится к соединениям формулы (I) или их фармацевтически приемлемым солям, где
Rx представляет водород;
Ry представляет метил;
Y1 представляет СRu, где Ru представляет водород;
X1 представляет СRx1, где Rx1 представляет водород или -C(О)NRbx1Rcx1;
X2 представляет СRх2, где Rx2 представляет водород;
L1 представляет (CH2)mO, где m означает 0;
G1 представляет G1a или -(C1-C6 алкиленил)-G1a, где G1a представляет необязательно замещенный фенил или необязательно замещенный циклоалкил, и
R2 представляет -S(О)2R2d, -S(О)2NR2bR2c, -N(R2e)S(О)2R2d или -(C1-C6 алкиленил)-S(О)2R2d.
В некоторых таких вариантах осуществления, A1 представляет СR1, A2 представляет СR2, A3 представляет СR3 и A4 представляет СR4. В таких дополнительных вариантах осуществления, A1 представляет СR1, A2 представляет СR2, A3 представляет СR3 и A4 представляет N.
Другой аспект изобретения относится к соединениям формулы (I) или их фармацевтически приемлемым солям, где
Rx представляет водород;
Ry представляет метил;
Y1 представляет СRu, где Ru представляет водород;
X1 представляет СRx1, где Rx1 представляет водород;
X2 представляет СRх2, где Rx2 представляет водород;
L1 представляет (CH2)mN(Rz) или где m означает 0 и Rz представляет водород;
G1 представляет -(C1-C6 алкиленил)-G1a, где G1a представляет необязательно замещенный циклоалкил и
R2 представляет -S(О)2R2d, -S(О)2NR2bR2c, -N(R2e)S(О)2R2d или -(C1-C6 алкиленил)-S(О)2R2d.
В некоторых таких вариантах осуществления, A1 представляет СR1, A2 представляет СR2, A3 представляет СR3 и A4 представляет СR4. В таких дополнительных вариантах осуществления, A1 представляет СR1, A2 представляет СR2, A3 представляет СR3 и A4 представляет N.
В одном аспекте данное изобретение относится к соединениям формулы (I) или их фармацевтически приемлемым солям,

где
Rx представляет водород или C1-C3 алкил;
Ry представляет C1-C3 алкил, -(C2-C3 алкиленил)-OH или C1-C3 галогеналкил;
X1 представляет N или CRx1, где
Rx1 представляет водород, C2-C6 алкенил, C2-C6 алкинил, -C(О)ORax1, -C(О)NRbx1Rcx1, -C(О)Rdx1, S(О)2Rdx1, -S(О)2NRbx1Rcx1, Gx1, C1-C6 галогеналкил или C1-C6 алкил; где C1-C6 алкил является необязательно замещенным одним заместителем, выбранным из группы, состоящей из ORax1, SRax1, S(О)Rdx1, S(О)2Rdx1, NRbx1Rcx1, -C(О)Rax1, C(О)ОRax1, -C(О)NRbx1Rcx1, -S(О)2NRbx1Rcx1 и Gx1;
Rax1, Rbx1 и Rcx1, в каждом случае, каждый независимо, представляют водород, C1-C6 алкил, C1-C6 галогеналкил, Ga или -(C1-C6 алкиленил)-Ga;
Rdx1, в каждом случае, каждый независимо, представляют C1-C6 алкил, C1-C6 галогеналкил, Ga или -(C1-C6 алкиленил)-Ga;
X2 представляет N или CRx2; где
Rx2 представляет водород, C2-C6 алкенил, C2-C6 алкинил, -C(О)ORax2, -C(О)NRbx2Rcx2, -C(О)Rdx2, S(О)2Rdx2, -S(О)2NRbx2Rcx2, Gx2, C1-C6 галогеналкил или C1-C6 алкил, где C1-C6 алкил является необязательно замещенным одним заместителем, выбранным из группы, состоящей из ORax2, SRax2, S(О)Rdx2, S(О)2Rdx2, NRbx2Rcx2, -C(О)Rax2, -C(О)ORax2, -C(О)NRbx2Rcx2, -S(О)2NRbx2Rcx2 и Gx2;
Rax2, Rbx2 и Rcx2, в каждом случае, каждый независимо, представляют водород, C1-C6 алкил, C1-C6 галогеналкил, Gb или -(C1-C6 алкиленил)-Gb;
Rdx2, в каждом случае независимо, представляет C1-C6 алкил, C1-C6 галогеналкил, Gb или -(C1-C6 алкиленил)-Gb;
Y1 представляет N или CRu, где Ru представляет водород, C1-C6 алкил, галоген или C1-C6 галогеналкил;
A1 представляет N или CR1, A2 представляет N или CR2, A3 представляет N или CR3 и A4 представляет N или CR4 при условии, что ноль, один, два или три из A1, A2, A3 и A4 представляют N;
R1, R3 и R4, каждый независимо, представляют водород, C1-C6 алкил, С2-C6 алкенил, С2-C6 алкинил, галоген, C1-C6 галогеналкил, CN или NO2;
R2 представляет водород, C1-C6 алкил, С2-C6 алкенил, С2-C6 алкинил, галоген, C1-C6 галогеналкил, -CN, NO2, G2a, -OR2a, -OC(О)R2d, -OC(О)NR2bR2c, -SR2a, -S(О)2R2d, -S(О)2NR2bR2c, -C(О)R2d, -C(О)OR2a, -C(О)NR2bR2c, -NR2bR2c, -N(R2e)C(О)R2d, -N(R2e)S(О)2R2d, -N(R2e)C(О)O(R2d), -N(R2e)C(О)NR2bR2c, -N(R2e)S(О)2NR2bR2c, -(C1-C6 алкиленил)-G2a, -(C1-C6 алкиленил)-OR2a, -(C1-C6 алкиленил)-OC(О)R2d, -(C1-C6 алкиленил)-OC(О)NR2bR2c, -(C1-C6 алкиленил)-S(О)2R2d, -(C1-C6 алкиленил)-S(О)2NR2bR2c, -(C1-C6 алкиленил)-C(О)R2d, -(C1-C6 алкиленил)-C(О)OR2a, -(C1-C6 алкиленил)-C(О)NR2bR2c, -(C1-C6 алкиленил)-NR2bR2c, -(C1-C6 алкиленил)-N(R2e)C(О)R2d, -(C1-C6 алкиленил)-N(R2e)S(О)2R2d, -(C1-C6 алкиленил)-N(R2e)C(О)O(R2a), -(C1-C6 алкиленил)-N(R2e)C(О)NR2bR2c, -(C1-C6 алкиленил)-N(R2e)S(О)2NR2bR2c и -(C1-C6 алкиленил)-CN;
R2a, R2b, R2c и R2e, в каждом случае, каждый независимо, представляют водород, С2-С6 алкенил, С2-С6 алкинил, C1-C6 галогеналкил, G2b или C1-C6 алкил, где C1-C6 алкил является необязательно замещенным одним заместителем, выбранным из группы, состоящей из -ORz1, NRz1Rz2, -C(О)ORz1, -C(О)NRz1Rz2, -S(О)2Rz1, -S(О)2NRz1Rz2 и G2b;
R2d, в каждом случае независимо, представляет С2-С6 алкенил, С2-С6 алкинил, C1-C6 галогеналкил, G2b или C1-C6 алкил, где C1-C6 алкил является необязательно замещенным одним заместителем, выбранным из группы, состоящей из -ORz1, NRz1Rz2, -C(О)ORz1, -C(О)NRz1Rz2, -S(О)2Rz1, -S(О)2NRz1Rz2 и G2b;
Rz1 и Rz2, в каждом случае, каждый независимо, представляют водород, C1-C6 алкил или C1-C6 галогеналкил;
Gx1, Gx2, Ga, Gb, G2a и G2b, в каждом случае, каждый независимо, представляют арил, гетероарил, гетероцикл, циклоалкил или циклоалкенил, и каждый из них независимо является незамещенным или замещенным 1, 2, 3, 4 или 5 Rv;
L1 отсутствует или означает CH2, C(O), (CH2)mO, (CH2)mS(О)n, где n означает 0, 1 или 2, или (CH2)mN(Rz), где Rz представляет водород, C1-C3 алкил, C1-C3 галогеналкил, (C2-C3 алкиленил)-OH или незамещенный циклопропил;
m означает 0 или 1;
G1 представляет G1a или -(C1-C6 алкиленил)-G1a, где каждый G1a независимо представляет арил, гетероарил, гетероцикл, циклоалкил или циклоалкенил и каждый G1a независимо является незамещенным или замещенным 1, 2, 3, 4 или 5 Rw;
Rv и Rw, в каждом случае, каждый независимо, представляют С1-С6 алкил, С2-С6 алкенил, C2-C6 алкинил, галоген, С1-С6 галогеналкил, -CN, оксо, -ORh, -ОС(О)Ri, -OC(О)NRjRk, -SRh, -S(О)2Rh, -S(О)2NRjRk, -C(О)Rh, -C(О)ORh, -C(О)NRjRk, -NRJRk, -N(Rh)C(О)Ri, -N(Rh)S(О)2Ri, -N(Rh)C(О)O(Ri), -N(Rh)C(О)NRjRk, -(С1-С6 алкиленил)-ORh, -(С1-С6 алкиленил)OС(О)Ri, -(С1-С6 алкиленил)-OC(О)NRjRk, -(С1-С6 алкиленил)-S(О)2Rh, -(С1-С6 алкиленил)-S(О)2NRjRk, -(С1-С6 алкиленил)-C(О)Rh, -(С1-С6 алкиленил)-(О)ORh, -(С1-С6 алкиленил)-C(О)NRjRk, -(С1-С6 алкиленил)-NRjRk, -(С1-С6 алкиленил-N(Rh)C(О)Ri, -(С1-С6 алкиленил)-N(Rh)S(О)2Ri, -(С1-С6 алкиленил)-N(Rh)C(О)O(Ri), -(С1-С6 алкиленил)-N(Rh)C(О)NRjRk или -(С1-С6 алкиленил)-CN;
Rh, Rj, Rk, в каждом случае, каждый независимо, представляют водород, С1-С6 алкил или С1-С6 галогеналкил, и
Ri, в каждом случае независимо, представляет С1-С6 алкил или С1-С6 галогеналкил.
Соединения формулы (I) могут содержать один или несколько асимметрично замещенных атомов. Соединения формулы I могут также существовать как отдельные стереоизомеры (включая энантиомеры и диастереомеры) и их смеси. Отдельные стереоизомеры соединений формулы I могут быть получены синтетически из коммерчески доступных исходных материалов, которые содержат асимметричные или хиральные центры или путем приготовления рацемических смесей с последующим отделением конкретного стереоизомера с использованием способов, которые известны специалисту в этой области. Примерами отделения являются, например, (i) присоединение смеси энантиомеров к хиральному вспомогательному средству, разделение полученной смеси диастереомеров путем перекристаллизации или хроматографии, с последующим высвобождением оптически чистого продукта, или (ii) разделение смеси энантиомеров или диастереомеров на хиральных хроматографических колонках.
Соединения формулы I могут также включать различные геометрические изомеры и их смеси, являющиеся результатом расположения заместителей вокруг углерод-углеродной двойной связи, углерод-азотной двойной связи, циклоалкильной группы или гетероциклической группы. Заместители вокруг углерод-углеродной двойной связи или углерод-азотной двойной связи обозначают как находящиеся в Z или E конфигурации и заместители вокруг циклоалкила или гетероцикла обозначают как находящиеся в цис или транс конфигурации.
В рамках данного изобретения, следует понимать, что раскрытые соединения могут обнаруживать феномен таутомеризма и все таутомерные изомеры включены в сферу действия изобретения.
Так, изображения формулы в данном описании могут представлять только одну из возможных таутомерных, геометрических или стереоизомерных форм. Следует понимать, что изобретение охватывает любую таутомерную, геометрическую или стереоизомерную форму и их смеси, и не должно ограничиваться исключительно какой-либо одной таутомерной, геометрической или стереоизомерной формой, используемой в изображениях формулы.
Типичные соединения формулы (I) включают, но без ограничения указанным:
6-метил-4-(2-феноксифенил)-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-(5-нитро-2-феноксифенил)-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-(5-амино-2-феноксифенил)-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]метансульфонамид;
2,2,2-трифтор-N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]этансульфонамид;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]ацетамид;
N-метил-N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]метансульфонамид;
этил 3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-с]пиридин-4-ил)-4-феноксибензоат;
3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензойная кислота;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(пиридин-3-илокси)фенил]метансульфонамид;
6-метил-4-[2-(морфолин-4-илметил)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
N-этил-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензамид;
3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-фенокси-N-(тетрагидрофуран-2-илметил)бензамид;
N-циклопентил-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензамид;
N-(2,2-дифторэтил)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензамид;
3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-фенокси-N-(1,3-тиазол-2-ил)бензамид;
N-(1,1-диоксидотетрагидротиофен-3-ил)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензамид;
3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензамид;
4-[5-(гидроксиметил)-2-феноксифенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]этансульфонамид;
N,N-диметил-N'-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]серный диамид;
N-[5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-6-феноксипиридин-3-ил]метансульфонамид;
N-[3-фтор-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]метансульфонамид;
N-[4-(2-цианофенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид;
N-[4-(4-фторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид;
N-[3-хлор-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]метансульфонамид;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-4-илокси)фенил]метансульфонамид;
6-метил-4-[2-фенокси-5-(1H-пиразол-1-илметил)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидрофуран-3-илокси)фенил]метансульфонамид;
N-{3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-[2-(трифторметил)фенокси]фенил}метансульфонамид;
N-[4-(4-цианофенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид;
N-[4-(2-хлор-4-фторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид;
[4-(бензилокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]уксусная кислота;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]ацетамид;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-3,3,3-трифторпропанамид;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-2,2-диметилпропанамид;
этил 4-(циклопентиламино)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензоат;
4-{5-[(1,1-диоксидо-1,2-тиазолидин-2-ил)метил]-2-феноксифенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензил]амино}-4-оксобутановая кислота;
4-[2-(2,4-дифторфенокси)-5-(1,1-диоксидо-1,2-тиазолидин-2-ил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(бензилокси)-5-(2-гидроксиэтил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
метил [4-(бензилокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]ацетат;
2-[4-(бензилокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-N-этилацетамид;
2-[4-(бензилокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-N,N-диметилацетамид;
N-[4-(3,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(2,4,6-трифторфенокси)фенил]метансульфонамид;
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид;
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-(тетрагидрофуран-3-ил)бензамид;
4-{2-(2,4-дифторфенокси)-5-[(1,1-диоксидотиоморфолин-4-ил)карбонил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-(1-метил-2-оксопирролидин-3-ил)бензамид;
трет-бутил{1-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензоил]пирролидин-3-ил}карбамат;
4-[2-(2,4-дифторфенокси)-5-(пирролидин-1-илкарбонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(морфолин-4-илкарбонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
N-[4-(циклогексилокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид;
N-[4-(циклопентилокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид;
N-{4-[(4,4-дифторциклогексил)окси]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил}метансульфонамид;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-3-илокси)фенил]метансульфонамид;
6-метил-4-[2-(морфолин-4-илкарбонил)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(2,4,6-трифторфенокси)фенил]этансульфонамид;
N-[4-(бензилокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-2-фторэтансульфонамид;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-N'-метилсерный диамид;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидрофуран-3-илокси)фенил]этансульфонамид;
метил 6-метил-7-оксо-4-(2-феноксифенил)-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат;
метил 1,6-диметил-7-оксо-4-(2-феноксифенил)-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат;
этил 4-(5-амино-2-феноксифенил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-с]пиридин-2-карбоксилат;
6-метил-4-(5-(метилсульфонамидо)-2-феноксифенил)-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоновая кислота;
этил 6-метил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат;
N-этил-6-метил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид;
6-метил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид;
этил 4-(5-амино-2-феноксифенил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-пиридазин-2-карбоксилат;
этил 4-[5-(этиламино)-2-феноксифенил]-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-2-карбоксилат;
этил 4-{5-[этил(метилсульфонил)амино]-2-феноксифенил}-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-2-карбоксилат;
6-метил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-2-карбоновая кислота;
6-метил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-2-карбоксамид;
6-метил-N-[2-(4-метилпиперазин-1-ил)этил]-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-2-карбоксамид;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-4-ил)-4-феноксифенил]метансульфонамид;
N-этил-6-метил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-2-карбоксамид;
6-метил-4-(2-феноксифенил)-1,6-дигидро-7H-пирроло[2,3-d]пиридазин-7-он;
N-этил-N,6-диметил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-2-карбоксамид;
4-{4-[(этилсульфонил)амино]-2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенокси}бензамид;
6-метил-4-[5-(метилсульфонил)-2-феноксифенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-6-(тетрагидрофуран-3-илокси)пиридин-3-сульфонамид;
N-метил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-6-(тетрагидрофуран-3-илокси)пиридин-3-сульфонамид;
6-метил-4-(2-феноксифенил)-2-фенил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
N-{3-[2-(гидроксиметил)-6-метил-7-оксо-6,7-дигидро-1Н-пирроло[2,3-c]пиридин-4-ил]-4-феноксифенил}метансульфонамид;
N-[4-(4-цианофенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид;
2-фтор-N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидрофуран-3-илокси)фенил]этансульфонамид;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидрофуран-3-илокси)фенил]пропан-1-сульфонамид;
N-[4-(4-цианофенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]пропан-1-сульфонамид;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(2,4,6-трифторфенокси)фенил]пропан-1-сульфонамид;
3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензолсульфонамид;
6-(циклогексиламино)-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид;
6-(циклогексиламино)-N-метил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид;
N-метил-N'-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(2,4,6-трифторфенокси)фенил]серный диамид;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-4-илокси)фенил]пропан-1-сульфонамид;
2,2,2-трифтор-N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-4-илокси)фенил]этансульфонамид;
N-(4-[(4,4-дифторциклогексил)окси]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил}этансульфонамид;
N-{4-[(4,4-дифторциклогексил)окси]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил}пропан-1-сульфонамид;
N-{4-[(4,4-дифторциклогексил)окси]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил}-2,2,2-трифторэтансульфонамид;
N-{4-[(4,4-дифторциклогексил)окси]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил}-N'-метилсерный диамид;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-3-илокси)фенил]этансульфонамид;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-3-илокси)фенил]пропан-1-сульфонамид;
2,2,2-трифтор-N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-3-илокси)фенил]этансульфонамид;
N-метил-N'-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-3-илокси)фенил]серный диамид;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-4-илокси)фенил]этансульфонамид;
N,N-диметил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-6-(тетрагидрофуран-3-илокси)пиридин-3-сульфонамид;
5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-6-(фениламино)пиридин-3-сульфонамид;
N-метил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-6-(фениламино)пиридин-3-сульфонамид;
N-[4-(4-цианофенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-2-фторэтансульфонамид;
2-фтор-N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(2,4,6-трифторфенокси)фенил]этансульфонамид;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]пропан-1-сульфонамид;
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-(пиримидин-2-ил)бензамид;
4-(2,4-дифторфенокси)-N-(2,6-диметоксипиридин-3-ил)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид;
4-(2,4-дифторфенокси)-N-(1H-индазол-6-ил)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид;
4-[2-(2,4-дифторфенокси)-5-{[4-(пирролидин-1-илкарбонил)пиперазин-1-ил]карбонил}фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-(2,4-дифторфенокси)-N-[4-(диметиламино)фенил]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид;
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-с]пиридин-4-ил)-N-(пиридин-4-илметил)бензамид;
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-[2-(2-оксопирролидин-1-ил)этил]бензамид;
4-(2,4-дифторфенокси)-N-(2-гидрокси-2-метилпропил)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид;
4-(2,4-дифторфенокси)-N-[2-(5-метокси-1H-индол-3-ил)этил]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид;
N-(3,4-дифторбензил)-4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид;
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-[4-(трифторметокси)бензил]бензамид;
2-{4-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензоил]пиперазин-1-ил}-N,N-диметилацетамид;
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-(пиридин-3-илметил)бензамид;
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-(пиридин-2-илметил)бензамид;
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-(3,4,5-триметоксибензил)бензамид;
4-(2,4-дифторфенокси)-N-[2-(диметиламино)этил]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид;
N-[2-(1,3-бензодиоксол-5-ил)этил]-4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид;
4-(2,4-дифторфенокси)-N-[2-(1H-индол-3-ил)этил]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид;
4-[2-(2,4-дифторфенокси)-5-{[4-(фуран-2-илкарбонил)пиперазин-1-ил]карбонил}фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
трет-бутил {1-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензоил]пиперидин-4-ил}карбамат;
трет-бутил 4-{[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензоил]амино}пиперидин-1-карбоксилат;
4-[2-(2,4-дифторфенокси)-5-{[4-(этилсульфонил)пиперазин-1-ил]карбонил}фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(4-хлорбензоил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[(4-хлорфенил)(гидрокси)метил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(пиримидин-5-илокси)фенил]этансульфонамид;
N-{3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-[(1-метил-1H-пиразол-5-ил)метокси]фенил}этансульфонамид;
N-{4-[(1,3-диметил-1H-пиразол-5-ил)метокси]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил}этансульфонамид;
N-[4-(2,2-диметилпропокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид;
N-[4-(циклопропилметокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-с]пиридин-4-ил)фенил]этансульфонамид;
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид;
4-[2-(циклогексиламино)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[5-амино-2-(2,4-дифторфенокси)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-d]пиридазин-7-он;
4-[2-(2-фторфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(3-фторфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(4-фторфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2-хлорфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(3-хлорфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(4-хлорфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
3-[2-(6-метил-7-оксо-6,7-дигидро-1H-пиролло[2,3-c]пиридин-4-ил)-4-(метилсульфонил)фенокси]бензонитрил;
4-[2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(метилсульфонил)фенокси]бензонитрил;
6-метил-4-{5-(метилсульфонил)-2-[3-(трифторметил)фенокси]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(циклопропилметокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-4-ил)фенил]метансульфонамид;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-4-ил)фенил]этансульфонамид;
4-[2-(изохинолин-5-илокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-[5-(метилсульфонил)-2-(хинолин-6-илокси)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[2-хлор-5-(трифторметил)фенокси]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[2-фтор-5-(трифторметил)фенокси]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
2-{4-[2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(метилсульфонил)фенокси]фенил}ацетамид;
4-[2-(3-аминофенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-[5-(метилсульфонил)-2-(тетрагидрофуран-3-иламино)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(этилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[(4,4-дифторциклогексил)окси]-5-(этилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{5-(этилсульфонил)-2-[(1-метилпиперидин-4-ил)окси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,1,3-бензотиадиазол-4-илокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(изохинолин-7-илокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,5-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(3,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-{5-(метилсульфонил)-2-[(1-оксо-2,3-дигидро-1H-инден-4-ил)окси]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(3,5-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-[2-(4-метилфенокси)-5-(метилсульфонил)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2-метоксифенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-{2-[(2-метилпиридин-3-ил)окси]-5-(метилсульфонил)фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[3-(диметиламино)фенокси]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-{5-(метилсульфонил)-2-[(1-оксо-2,3-дигидро-1H-инден-5-ил)окси]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-{5-(метилсульфонил)-2-[(3-оксо-2,3-дигидро-1H-инден-5-ил)окси]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
2-[2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(метилсульфонил)фенокси]бензонитрил;
4-[2-(3-хлор-2-фторфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-[5-(метилсульфонил)-2-(нафталин-1-илокси)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2-фтор-5-метилфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(5-фтор-2-метилфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-[5-(метилсульфонил)-2-(хинолин-7-илокси)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(4-хлор-3-фторфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-[5-(метилсульфонил)-2-(пиридин-3-илокси)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,3-дигидро-1H-инден-5-илокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-{5-(метилсульфонил)-2-[4-(пропан-2-ил)фенокси]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(изохинолин-8-илокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-[5-(метилсульфонил)-2-(3,4,5-трифторфенокси)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-(2-бензилфенил)-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-(бифенил-2-ил)-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(1,4-диоксаспиро[4,5]дец-8-илокси)-5-(этилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(циклопропилметокси)-5-(этилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{5-(этилсульфонил)-2-[(4-оксоциклогексил)окси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[(циклопропилметил)амино]-5-(этилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-{5-(метилсульфонил)-2-[(тетрагидрофуран-3-илметил)амино]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{5-(этилсульфонил)-2-[(цис-4-гидроксициклогексил)окси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{5-(этилсульфонил)-2-[(транс-4-гидроксициклогексил)окси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(циклопропилметокси)-5-(этилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-d]пиридазин-7-он;
6-метил-4-[5-(метилсульфонил)-2-(тетрагидрофуран-3-илокси)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[(3-фтороксетан-3-ил)метокси]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-(циклопропилметокси)-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид;
6-(циклопропилметокси)-N-метил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид;
6-[(циклопропилметил)амино]-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-с]пиридин-4-ил)пиридин-3-сульфонамид;
6-[(циклопропилметил)амино]-N-метил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид;
4-{5-(этилсульфонил)-2-[(цис-4-гидрокси-4-метилциклогексил)окси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{5-(этилсульфонил)-2-[(транс-4-гидрокси-4-метилциклогексил)окси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(циклобутилокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(циклопентилметокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(циклогексилокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(циклопентилокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-[5-(метилсульфонил)-2-(тетрагидрофуран-3-илметокси)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-{5-(метилсульфонил)-2-[2-(2-оксоимидазолидин-1-ил)этокси]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2-циклопропилэтокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(циклогептилокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-[2-(2-метилпропокси)-5-(метилсульфонил)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-[2-{[(2S)-1-метилпирролидин-2-ил]метокси}-5-(метилсульфонил)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-{2-[(2-метилциклопропил)метокси]-5-(метилсульфонил)фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(циклогексилметокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-{2-[2-(1-метилпирролидин-2-ил)этокси]-5-(метилсульфонил)фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-[5-(метилсульфонил)-2-{[(2R)-5-оксопирролидин-2-ил]метокси}фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-{5-(метилсульфонил)-2-[2-(морфолин-4-ил)этокси]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-[5-(метилсульфонил)-2-{[(2S)-5-оксопирролидин-2-ил]метокси}фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[(1-трет-бутоксипропан-2-ил)окси]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[(1S,4R)-бицикло[2.2.1]гепт-2-илметокси]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-{2-[(1-метилциклопропил)метокси]-5-(метилсульфонил)фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-{5-(метилсульфонил)-2-[2-(2-оксопирролидин-1-ил)этокси]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-метил-4-{2-[(4-метилциклогексил)окси]-5-(метилсульфонил)фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(циклобутилметокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]циклопропансульфонамид;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-2-метоксиэтансульфонамид;
6-метил-4-{5-(метилсульфонил)-2-[трицикло[3.3.1.13,7]дец-2-илокси]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[(циклопропилметил)амино]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид;
4-[(циклопропилметил)амино]-N-метил-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид;
4-{2-[(2,2-дифторциклопропил)метокси]-5-(этилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-(4-бром-2-метоксифенил)-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-(2,4-дифторфенокси)-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид;
4-{2-(циклопропилметокси)-5-[(трифторметил)сульфонил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[(циклопропилметил)амино]-5-[(трифторметил)сульфонил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-[(циклопропилметил)амино]-N,N-диметил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид;
6-(2,4-дифторфенокси)-N-метил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид;
4-[2-(циклопропилметокси)-6-метилфенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{5-(этилсульфонил)-2-[(цис-4-метоксициклогексил)окси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-(циклопропилметокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид;
4-(циклопропилметокси)-N-метил-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид;
N-[4-(циклопропилметокси)-2-метил-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-N-этил-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-7-оксо-N-(2,2,2-трифторэтил)-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-(морфолин-4-илкарбонил)-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-[(4-метилпиперазин-1-ил)карбонил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-7-оксо-N-(1,3-тиазол-2-ил)-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид;
этил 4-[2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(метилсульфонил)фенокси]пиперидин-1-карбоксилат;
4-[2-этокси-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{5-(этилсульфонил)-2-[(транс-4-метоксициклогексил)окси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[(циклопропилметил)амино]-5-(пропан-2-илсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
N-[4-(циклопропилметокси)-2-метил-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид;
N-[4-(циклопропилметокси)-2-метил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид;
4-[5-(этилсульфонил)-2-(тетрагидро-2H-тиопиран-4-илокси)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[(1,1-диоксидотетрагидро-2H-тиопиран-4-ил)окси]-5-(этилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-(2,4-дифторфенокси)-N,N-диметил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид;
4-[2-(циклопропиламино)-5-(этилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-(5-(этилсульфонил)-2-(цис-4-метокси-4-метилциклогексилокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-N,N,6-триметил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид;
6-метил-4-{5-(метилсульфонил)-2-[4-(метилсульфонил)фенокси]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(пропан-2-илсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
6-(циклопропилметокси)-N,N-диэтил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид;
4-(циклопропилметокси)-N,N-диметил-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид;
4-[2-(циклопропилметокси)-5-фторфенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(трифторметил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-2-(гидроксиметил)-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,3-дигидро-1H-инден-2-илокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-2-(1-гидроксиэтил)-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-2-[(диметиламино)метил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-(морфолин-4-илметил)-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-[(4-метилпиперазин-1-ил)метил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-[(фениламино)метил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-[(1,3-тиазол-2-иламино)метил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-[(тетрагидрофуран-3-иламино)метил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(циклопропилметокси)-5-(фенилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(циклопропилметокси)-5-(морфолин-4-илсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-(2,4-дифторфенокси)-5-[(метилсульфонил)метил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)пиридин-3-ил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-[(пиридин-3-илокси)метил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[5-(циклопропилсульфонил)-2-(2,4-дифторфенокси)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-(проп-1-eн-2-ил)-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-(феноксиметил)-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(морфолин-4-илсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(этилсульфонил)пиридин-3-ил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-с]пиридин-4-ил)фенил]-2-(морфолин-4-ил)этансульфонамид;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-N-[2-(диметиламино)этил]этансульфонамид;
4-{2-(2,4-дифторфенокси)-5-[(этилсульфонил)метил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-(2,4-дифторфенокси)-5-[2-(этилсульфонил)пропан-2-ил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(пирролидин-1-илсульфонил)фенил]-6-мети1-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-2-(диметиламино)этансульфонамид;
этил 4-[4-(этилсульфонил)-2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенокси]пиперидин-1-карбоксилат;
4-[2-(циклопропилметокси)-5-(пирролидин-1-илсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[(1-ацететилпиперидин-4-ил)окси]-5-(этилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[4-(этилсульфонил)-2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенокси]бензонитрил;
4-[2-(циклопропилметокси)-5-(2,3-дигидро-1H-индол-1-илсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-(2,4-дифторфенокси)-5-[(фенилсульфонил)метил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[(2,2-дифторциклопропил)метокси]-5-(пирролидин-1-илсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-(циклопропилметокси)-5-[(3,3-дифторазетидин-1-ил)сульфонил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[2-(2-гидроксиэтил)фенокси]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(циклопропилметокси)-5-{[3-(диметиламино)пирролидин-1-ил]сульфонил}фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-(2,4-дифторфенокси)-5-[(метансульфонил)метил]пиридин-3-ил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
трет-бутил 4-[4-(этилсульфонил)-2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенокси]пиперидин-1-карбоксилат;
4-(циклопропилметокси)-3-(6-метил-7-оксо-6,7-дигидро-1Н-пирроло[2,3-c]пиридин-4-ил)-N-фенилбензолсульфонамид;
4-[2-(циклопропилметокси)-5-(пирролидин-1-илметил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(циклопропилметокси)-5-(пиридин-3-ил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(циклопропилметокси)-5-(морфолин-4-илметил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{5-(этилсульфонил)-2-[3-(гидроксиметил)фенокси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(циклопропилметокси)-5-(1-метил-1H-пиразол-4-ил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(2,3-дигидро-1H-индол-1-илсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пиразолo[3,4-c]пиридин-4-ил)фенил]этансульфонамид;
4-{2-(2,4-дифторфенокси)-5-[(метилсульфонил)метил]фенил}-6-метил-1,6-дигидро-7H-пиразолo[3,4-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(этилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пиразолo[3,4-c]пиридин-7-он;
4-[2-(циклопропилметокси)-5-(этилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пиразолo[3,4-c]пиридин-7-он;
N-[2-циано-4-(2,4-дифторфенокси)-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид;
трет-бутил 4-[4-(циклопропилметокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-3,6-дигидропиридин-1(2H)-карбоксилат;
4-[5-(6-аминопиридин-3-ил)-2-(циклопропилметокси)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[(2,2-дифторциклопропил)метокси]-5-(этилсульфонил)фенил}-6-метил-7-оксо-N-(2,2,2-трифторэтил)-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид;
4-{2-[(циклопропилметил)амино]-5-[(метилсульфонил)метил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[(циклопропилметил)амино]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[5-(этилсульфонил)-2-(пирролидин-1-ил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[5-(этилсульфонил)-2-(4-метилпиперазин-1-ил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[(4-фторфенил)амино]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-(циклопропилметокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-(пиридин-3-илметил)бензолсульфонамид;
4-[4-(циклопропилметокси)-3'-фторбифенил-3-ил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[(4-фторфенил)амино]-5-[(метилсульфонил)метил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
[4-(циклопропилметокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]ацетoнитрил;
N-{4-(2,4-дифторфенокси)-3-[2-(гидроксиметил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил]фенил}этансульфонамид;
N-[4-(2,4-дифторфенокси)-3-{6-метил-2-[(4-метилпиперазин-1-ил)карбонил]-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил}фенил]этансульфонамид;
N-[4-(2,4-дифторфенокси)-3-{6-метил-2-[(4-метилпиперазин-1-ил)метил]-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил}фенил]этансульфонамид;
4-[2-(циклопропилметокси)-5-(1,2,3,6-тетрагидропиридин-4-ил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-N-(2-метоксиэтил)этансульфонамид;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-N-(пиридин-2-илметил)этансульфонамид;
N-(циклопропилметил)-N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-N-[2-(2-оксопирролидин-1-ил)этил]этансульфонамид;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-N-(тетрагидрофуран-2-илметил)этансульфонамид;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-N-(3,3,3-трифторпропил)этансульфонамид;
4-(циклопропилметокси)-N-(4-фторфенил)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид;
4-[2-(циклопропилметокси)-5-(6-фторпиридин-3-ил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
N-[4-(2,4-дифторфенокси)-3-(3-формил-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид;
N-{4-(2,4-дифторфенокси)-3-[6-метил-3-(морфолин-4-илметил)-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил]фенил}этансульфонамид;
N-[4-(2,4-дифторфенокси)-3-{6-метил-3-[(4-метилпиперазин-1-ил)метил]-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил}фенил]этансульфонамид;
4-{2-[(циклопропилметил)амино]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4'-(циклопропилметокси)-3'-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бифенил-3-карбонитрил; и
4-{2-(циклопропилметокси)-5-[(4-гидроксипиперидин-1-ил)сульфонил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он.
В конкретных вариантах осуществления, соединение формулы I выбрано из группы, состоящей из таких членов, как:
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид;
6-метил-4-[5-(метилсульфонил)-2-феноксифенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
N-метил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-6-(тетрагидрофуран-3-илокси)пиридин-3-сульфонамид;
N-[4-(2-хлор-4-фторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид;
6-метил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]метансульфонамид;
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(2,4,6-трифторфенокси)фенил]этансульфонамид;
N-{4-[(4,4-дифторциклогексил)окси]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил}метансульфонамид; и
N-[4-(4-фторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид или их фармацевтически приемлемой соли.
В конкретных вариантах осуществления, соединение формулы I выбрано из группы, состоящей из таких членов, как:
4-{2-(2,4-дифторфенокси)-5-[(метилсульфонил)метил]пиридин-3-ил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид;
4-(циклопропилметокси)-N-метил-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид;
4-{2-[(4,4-дифторциклогексил)окси]-5-(этилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-(5-(этилсульфонил)-2-(цис-4-метокси-4-метилциклогексилокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он;
6-метил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид;
4-{2-(2,4-дифторфенокси)-5-[(метилсульфонил)метил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(2,4-дифторфенокси)-5-(этилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{5-(этилсульфонил)-2-[(транс-4-метоксициклогексил)окси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-{2-[(циклопропилметил)амино]-5-(этилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[(циклопропилметил)амино]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид;
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид;
4-[2-(циклопропилметокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он;
4-[2-(циклогексилокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он и
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]этансульфонамид
или их фармацевтически приемлемой соли.
В конкретных вариантах осуществления, соединение по данному изобретению представляет собой N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид или его фармацевтически приемлемую соль.
Соединения формулы I могут быть использованы в форме фармацевтически приемлемых солей. Выражение "фармацевтически приемлемая соль" означает такие соли, которые, в сфере действия озвученного медицинского законодательства, являются подходящими для применения в контакте с тканями людей или низших животных без чрезмерной токсичности, раздражения, аллергической реакции и тому подобного и соответствуют обоснованному соотношению польза/риск.
Фармацевтически приемлемые соли описаны в S. M. Berge et al. J. Pharmaceutical SClences, 1977, 66: 1-19.
Соединения формулы (I) могут содержать функциональные группы основного характера или кислотного или и те, и другие и могут быть превращены в фармацевтически приемлемую соль, когда это желательно, с использованием подходящей кислоты или основания. Соли могут быть получены на месте во время окончательной изоляции и очистки соединения по изобретению.
Примеры аддитивных солей с кислотой включают, но без ограничения указанным, ацетат, адипинат, альгинат, цитрат, аспартат, бензоат, бензолсульфонат, бисульфат, бутират, камфорат, камфорсульфонат, диглюконат, глицерофосфат, гемисульфат, гептаноат, гексаноат, фумарат, гидрохлорид, гидробромид, гидройодид, 2-гидроксиэтансульфонат (изотионат), лактат, малат, малеат, метансульфонат, никотинат, 2-нафталинсульфонат, оксалат, пальмитоат, пектинат, персульфат, 3-фенилпропионат, пикрат, пивалат, пропионат, сукцинат, тартрат, тиоцианат, фосфат, глутамат, бикарбонат, п-толуолсульфонат и ундеканоат. Также, азотсодержащие группы основного характера могут быть кватернизованы такими агентами, как низшие алкил галогениды, такие как, но без ограничения указанным, метил, этил, пропил и бутил хлориды, бромиды и йодиды; диалкил сульфаты, такие как диметил, диэтил, дибутил и диамил сульфаты; длинноцепочечные галогениды, такие как, но без ограничения указанным, децил, лаурил, миристил и стеарил хлориды, бромиды и йодиды; арилалкил галогениды, такие как бензил и фенетил бромиды и другие. Таким образом получают раствориые или диспергируемые в воде или масле продукты. Примеры кислот, которые могут быть использованы для образования фармацевтически приемлемых аддитивных солей с кислотами включают такие неорганические кислоты, как хлороводородная кислота, бромоводородная кислота, серная кислота и фосфорная кислота, и такие органические кислоты, как уксусная кислота, фумаровая кислота, малеиновая кислота, 4-метилбензолсульфоновая кислота, янтарная кислота и лимонная кислота.
Аддитивные соли с основанием могут быть получены на месте во время окончательной изоляции и очистки соединений по данному изобретению при взаимодействии содержащей карбоновую кислоту части молекулы с подходящим основанием, таким как, но без ограничения указанным, гидроксид, карбонат или бикарбонат фармацевтически приемлемого катиона металла или с аммиаком, или с органическим первичным, вторичным или третичным амином. Фармацевтически приемлемые соли включают, но без ограничения указанным, катионы на основе щелочных металлов или щелочноземельных металлов, такие как, но без ограничения указанным, соли лития, натрия, калия, кальция, магния и алюминия и тому подобное и нетоксиных катионов четвертичного аммония и амина, включая аммоний, тетраметиламмоний, тетраэтиламмоний, метиламин, диметиламин, триметиламин, триэтиламин, диэтиламин, этиламин и тому подобное. Другие примеры органических аминов, применимых для получения аддитивныж солей с основаниями, включают этилендиамин, этаноламин, диэтаноламин, пиперидин, пиперазин и тому подобное.
Термин "фармацевтически приемлемое пролекарство" или "пролекарство", используемый в данном описании, представляет такие пролекарства соединений по данному изобретению, которые, в сфере действия озвученного медицинского законодательства, являются подходящими для применения в контакте с тканями людей и низших животных без чрезмерной токсичности, раздражения, аллергической реакции и тому подобного, согласуются с обоснованным соотношением польза/риск и эффективны при соответствующем применении.
Данное изобретение относится к соединениям формулы (I), полученным синтетическими средствами или образуемым in vivo биопреобразованием пролекарства.
Соединения в данном описании могут существовать в несольватированных, а также в сольватированных формах, включая гидратированные формы, такие как полугидраты. Как правило, сольватированные формы с фармацевтически приемлемыми растворителями, такими как вода и этанол, наряду с прочими, эквивалентны несольватированным формам для целей изобретения.
Общий синтез
Соединения, указанные в данном описании, включая соединения общей формулы (I) и конкретные примеры, могут быть получены, например, путем реакций, указанных на схемах 1-5. Переменные A1, A2, A3, A4, X1, X2, Y1, L1, G1, Rx и Ry, используемые на следующих схемах, имеют значения, установленные в разделе "Сущность изобретения" и в подробном описании, если не оговорено иное.
Сокращения, используемые в описаниях схем и конкретных примеров, имеют следующие значения: н-BuLi или BuLi - н-бутил лития, DBU - 1,8-диазабицикло[5.4.0]ундец-7-ен, DIAD - диизопропил азодикарбоксилат; DME - 1,2-диметоксиэтан, DMF - диметилформамид, DMSO - диметил сульфоксид, EtOAc - этил ацетат; mCPBA - 3-хлорпербензойная кислота, MeOH - метанол; Pd(PPh3)4 - тетракис(трифенилфосфин)палладий(0), препаративная HPLC - препаративная ВЭЖХ; THF - тетрагидрофуран, TFA - трифторуксусная кислота и ВЭЖХ – высокоэффективная жидкостная хроматография.
Соединения общей формулы (I) могут быть получены (a) обработкой арил галогенида, арил мезилата или арил трифлата арил бороновой кислотой или ее производными (например, бороновыми сложными эфирами) в условиях реакции сочетания Suzuki (N. Miyama and A. Suzuki, Chem. Rev. 1995, 95:2457-2483, J. Organomet. Chem. 1999, 576:147-148) и (b) удалением защитной группы (PG), как пояснено на схеме 1. Сочетание соединений формулы (1), где R101 представляет Br, Cl, мезилат или трифлат, с соединениями формулы (2), где R102 представляет бороновую кислоту или ее производные (например, бороновые сложные эфиры), или сочетание (1), где R101 представляет бороновую кислоту или ее производные (например, бороновые сложные эфиры) с соединениями (2), где R102 представляет Br, Cl, мезилат или трифлат, дает промежуточные соединения формулы (3). Обычно, реакция сочетания происходит в присутствии палладиевого катализатора и основания и необязательно в присутствии лиганда и в подходящем растворителе при повышенной температуре (например, от около 80°C до около 150°C). Реакция может быть облегчена микроволновым излучением. Примеры палладиевого катализатора включают, но без ограничения указанным, тетракис(трифенилфосфин)палладий(0), трис(дибензилиденацетон)дипалладий(0) и палладий(II)ацетат. Примеры подходящих оснований, которые могут быть использованы, включают, но без ограничения указанным, карбонаты или фосфаты натрия, калия и цезия и фторид цезия. Примеры подходящих лигандов включают, но без ограничения указанным, 1,3,5,7-тетраметил-6-фенил-2,4,8-триокса-6-фосфаадамант, 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (X-phos) и 1,1'-бис(дифенилфосфанил)ферроцен. Неограничительные примеры подходящих растворителей включают метанол, диметоксиэтан, N,N-диметилформамид, диметилсульфоксид, диоксан, тетрагидропиран и воду или их смесь.
В качестве варианта, обработка соединения формулы (1), где R101 представляет Br, Cl или трифлат, бороновой кислотой формулы (4) с последующим вытеснением атома фтора в (4) соответствующим спиртом или амином формулы G1-L1-H, где L1 представляет О или NH, дает соединения формулы (3) или формулы (I), где Rx представляет водород.
Вытеснение фтора спиртом или амином может быть достигнуто в растворителе, таком как, но без ограничения указанным, диметилсульфоксид, диметилформамид, диоксан или тетрагидрофуран, и в присутствии основания, такого как, но без ограничения указанным, карбонат цезия, карбонат калия или гидрид натрия, и при температуре от около 40°C до около 120°C.
Защитная группа (PG) может быть удалена на месте во время и в условиях реакций вытеснения или сочетания, описанных выше.
В качестве варианта, удаление защитной группы (PG) для получения соединений общей формулы (I), где Rx представляет водород, может быть осуществлено с использованием известных специалисту условий реакции или их модификаций. Например, тозильная защитная группа может быть удалена в присутствии основания, такого как, но без ограничения указанным, карбонат цезия, гидроксид натрия или гидрид натрия. Реакцию обычно проводят в присутствии подходящего растворителя, такого как, но без ограничения указанным, диметилсульфоксид, метанол или тетрагидрофуран, и при температуре от около 40°C до около 120°C. Бензильная защитная группа может быть удалена гидрированием в присутствии катализатора, такого как, но без ограничения указанным, палладий на углероде, и в атмосфере водорода. Реакцию обычно проводят в присутствии растворителя, такого как, но без ограничения указанным, метанол или этилацетат, и приблизительно при комнатной температуре.
Удаление (триметилсилил)этокси)метильной защитной группы может быть достигнуто обработкой основанием, таким как, но без ограничения указанным, карбонат цезия или гидрид натрия, или фторидным рeагентом таким как, но без ограничения указанным, TBAF (фторид тетрабутиламмония). Реакцию обычно проводят в присутствии подходящего растворителя, такого как, но без ограничения указанным, диметилсульфоксид, этанол или тетрагидрофуран, и при температуре от около 40°C до около 120°C. Удаление (триметилсилил)этокси)метильной защитной группы может быть также достигнуто обработкой умеренной кислотой, такой как, но без ограничения указанным, водная хлороводородная кислота. Реакцию обычно проводят в присутствии подходящего растворителя, такого как, но без ограничения указанным, этанол или метанол, и при температуре от около 25°C до около 80°C.
Превращение соединений формулы (I), где Rx представляет водород, в (I), где Rx представляет С1-С3 алкил, может быть осуществлено с алкилирующим агентом формулы RXR103, где R103 представляет галоген, трифлат или мезилат. Обычно, реакция может проведена в присутствии основания, такого как, но без ограничения указанным, гидрид натрия или карбонат калия, и в растворителе, таком как, но без ограничения указанным, тетрагидрофуран или диметилформамид, и при температуре от около 40°C до около 120°C.
Схема 1

Соединения формулы (1), где Y1 представляет CRu, X1 и X2 представляют CH и Ru представляет водород, С1-С6 алкил или С1-С6 галогеналкил, могут быть получены общими синтетическими способами, как показано на схеме 2.
Обработка соединений формулы (6), где галоген представляет Br, Cl или I, 1,1-диметокси-N,N-диметилметанамином при повышенной температуре (например, от около 60°C до около 100°C), в присутствии или без основания и в растворителе, таком как, но без ограничения указанным, DMF, дает соединения формулы (7). Примеры подходящих оснований включают, но без ограничения указанным, метанолят лития или натрия. Каталитическое гидрирование (7) в присутствии катализатора, такого как, но без ограничения указанным, никель Реннея, и в атмосфере водорода (около 30 фунт на кв.дюйм) и в растворителе, таком как, но без ограничения указанным, этилацетат, приблизительно при комнатной температуре обычно дает соединения формулы (8). Защита атома азота защитной группой, такой как, но без ограничения указанным, бензил, тозил и (триметилсилил)этокси)метил, может быть создана путем взаимодействия с подходящим галогенидом в присутствии сильного основания, такого как, но без ограничения указанным, гидрид натрия, до образования соединения формулы (9).
Обработка (9) кислотой, такой как, но без ограничения указанным, хлороводородная кислота или бромоводородная кислота, и в растворителе, таком как, но без ограничения указанным, диоксан или вода, от около 40°C до около 100°C, обычно обеспечивает соединения формулы (10).
Алкилирование (10) галогенидом или мезилатом, в присутствии основания, такого как, но без ограничения указанным, гидрид натрия, карбонат цезия или карбонат калия, и в растворителе таком как, но без ограничения указанным, диметилформамид или диметилсульфоксид, при температуре от около 0°C до около 50°C обычно дает соединения формулы (11).
Обработка соединений формулы (11) 4,4,4',4',5,5,5',5'-октаметил-2,2'-би(1,3,2-диоксабороланом) обычно дает соединения формулы (12). Как правило, превращение может быть облегчено палладиевым катализатором, таким как, но без ограничения указанным, тетракис(трифенилфосфин)палладий(0), трис(дибензилиденацетон)дипалладий(0) или палладий(II)ацетат, необязательным лигандом таким как, но без ограничения указанным, 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил, 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (X-phos) или 1,1'-бис(дифенилфосфанил)ферроцен, и основанием, таким как, но без ограничения указанным, карбонаты, ацетаты или фосфаты натрия, калия и цезия и фторид цезия. Неограничительные примеры подходящих растворителей включают метанол, диметоксиэтан, N,N- диметилформамид, диметилсульфоксид, диоксан, тетрагидропиран и воду или их смесь.
Схема 2

Путь получения соединений формулы (1), где Y1 представляет N, R101 представляет Cl и X1 и X2 представляют CH, представлен в общих чертах на схеме 3.
Обработка (13) гидроксидом аммония при около 100°C до около 150°C может давать амины формулы (14).
Йодирование (14) N-йодсукцинимидом в растворителе, таком как, но без ограничения указанным, ацетонитрил или ацетон, при температуре от около 40°C до около 85°C, обычно дает соединения формулы (15). Последующее сочетание с (E)-2-(2-этоксивинил)-4,4,5,5-тетраметил-1,3,2-диоксабороланом с использованием условий реакции сочетания Suzuki, как описано на схеме 1, дает соединения формулы (16). Циклизация (16) с последующей защитой атома азота обычно дает соединения формулы (17).
Циклизация (16) может быть осуществлена в присутствии кислоты, такой как, но без ограничения указанным, уксусная кислота или хлороводородная кислота, и при повышенной температуре (например, от около 50°C до около 100°C).
Схема 3
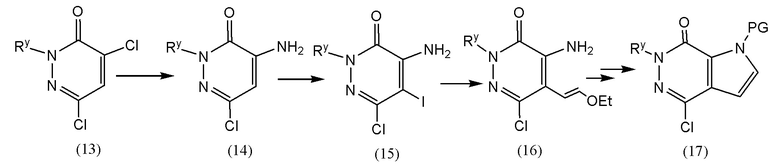
Соединения формулы (1), где Y1 представляет N, R101 представляет Cl, X1 представляет –COORах1 или -C(О)NRbx1Rcx1, Rax1, Rbx1 и Rcx1 представляют водород или С1-С6 алкил и X2 представляет СH, могут быть получены по синтетическому пути, представленному на схеме 4.
Обработка (15) пировиноградной кислотой в присутствии палладиевого катализатора, такого как, но без ограничения указанным, палладий(II)ацетат, и основания такого как, но без ограничения указанным, DBU, и в растворителе, таком как, но без ограничения указанным, DMF, и при повышенной температуре (например, от около 80°C до около 150°C) обычно имеет результатом кислоту формулы (18). Этерификация (18) до (19) может быть осуществлена в условиях реакции, известных специалисту в этой области, например, путем обработки спиртом в кислотных условиях. Последующая защита (19) с использованием условий реакции, описанных на схеме 2, для превращения (8) в (9) может обеспечивать соединения формулы (20). Преобразование (20) в (21) может быть осуществлено поэтапной реакцией (a) гидролиза сложного эфира до соответствующей кислоты и (b) превращения кислоты в соответствующие амиды.
Кислота может быть преобразована в соответствующий хлорангидрид кислоты обработкой оксалилхлоридом в присутствии каталитического количества DMF, при температуре около комнатной и в подходящем растворителе, таком как, но без ограничения указанным, тетрагидрофуран или дихлорметан.
Полученный хлорангидрид кислоты может быть превращен в амиды формулы (21) обработкой амином формулы HNRbx1Rcx1 в растворителе, таком как, но без ограничения указанным, тетрагидрофуран, диметилформамид или дихлорметан, при температуре от около комнатной до около 50°C, необязательно в присутствии основания, такого как, но без ограничения указанным, триэтиламин, диизопропилэтиламин или карбонат калия, и необязательно в присутствии катализатора, такого как 4-диметиламинопиридин. В качестве варианта, кислота может быть подвергнута взаимодействию с амином формулы HNRbx1Rcx1 в растворителе, таком как, но без ограничения указанным, тетрагидрофуран или диметилформамид, в присутствии рeагента сочетания, такого как 1,1-карбонилдиимидазол (GDI), бис(2-оксо-3-оксазолидинил)фосфиновый хлорид (BOPC1), 1,3-дициклогексилкарбодиимид (DCC), 1,3-дициклогексилкарбодиимид (PS-DCC) на полимерном носителе, О-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония гексафторфосфат (HATU) или O-бензотриазол-1-ил-N,N,N',N'-тетраметилурония тетрафторборат (TBTU), в присутствии или без вспомогательного средства сочетания, такого как, но без ограничения указанным, 1-гидрокси-7-азабензотриазол (HOAT) или гидрат 1-гидроксибензотриазола (HOBT). Реакция может быть обычно проведена в присутствии или без основания, такого как, но без ограничения указанным, N-метил морфолин, триэтиламин или диизопропилэтиламин.
Схема 4
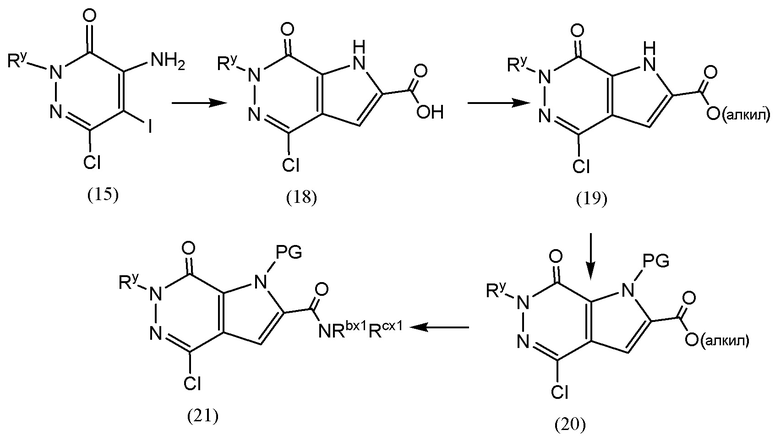
Схема 5 общий подход к получению соединений формулы (1), где Y1 представляет СRu, R101 представляет галоген, X1 представляет -COORax1 или -C(O)NRbx1Rсх1, Rax1, Rbx1 и Rсx1 представляют водород или C1-C6 алкил и X2 представляет СH.
Сложный эфир формулы (23) может быть получен путем (a) обработки соединения (6) диэтил оксалатом в присутствии основания, такого как, но без ограничения указанным, этоксид калия или этоксид натрия, в растворителе, таком как, но без ограничения указанным, этоксид калия или этоксид натрия, в растворителе, таком как, но без ограничения указанным, этанол, диоксан или простой диэтиловый эфир, и при температуре от около 40°C до около 80°C, и (b) циклизации полученного (22) в присутствии железа и в этаноле и уксусной кислоте, при температуре от около 80°C до около 100°C. Превращение (23) в (26) может быть достигнуто при использовании условий реакции, указанных выше.
Этиловый сложный эфир формулы (26) впоследствии может быть гидролизован до соответствующих кислот. Полученные кислоты могут преобразованы в подходящий сложный эфир или амид, как описано на схеме 4.
Схема 5
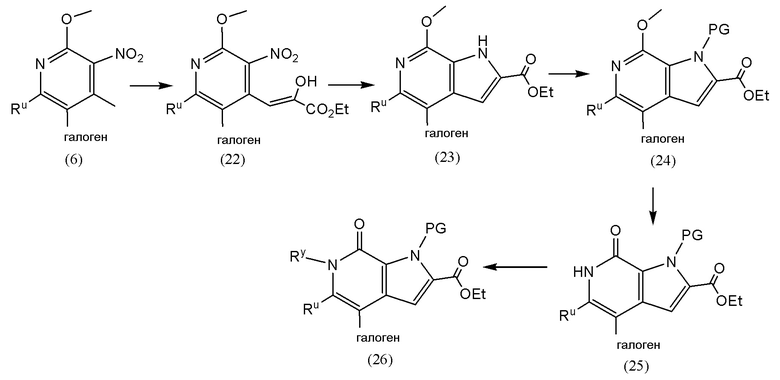
Оптимальные условия реакции и время реакции для каждой отдельной стадии могут изменяться в зависимости от конкретных используемых реагентов и заместителей, присутствующих в используемых реагентах. Если не оговорено иное, растворители, температуры и другие условия реакции легко могут быть выбраны специалистом в этой области. Конкретные процедуры представлены в разделе "Синтетические примеры". Реакции могут быть дополнительно продвинуты обычным образом, например, исключением растворителя из остатка и дополнительно очищены согласно методологиям, обычно известным в технике, таким как, но без ограничения указанным, кристаллизация, дистилляция, экстракция, растирание в порошок и хроматография. Если не оговорено иное, исходные материалы и реагенты либо коммерчески доступны или могут быть получены специалистом из коммерчески доступных материалов способами, описанными в химической литературе.
Рутинное экспериментирование, включая соответствующее манипулирование условиями реакции, реагентами и последовательностью синтетического пути, защитой какой-либо функциональной группы, которая не может быть совместимой с условиями реакции, и удаление защиты в подходящий момент последовательности реакций способа, включены в сферу действия изобретения. Подходящие защитные группы и способы защиты и устраняющие защиту различные заместители, использующие такие подходящие защитные группы хорошо известны специалистам в этой области; их примеры могут быть найдены в публикации T. Greene and P. Wuts, Protecting Groups in Chemical Synthesis (3rd ed.), John Wiley & Sons, NY (1999), приобщенной к сему ссылкой во всей ее полноте. Синтез соединений по изобретению может быть осуществлен способами, аналогичными описанным на приведенных выше синтетических схемах и в конкретных примерах.
Исходные материалы, если они коммерчески не доступны, могут быть получены путем процедур, выбранных из стандартных органических химических технологий, технологий, которые аналогичны синтезу известных структурно подобных соединений, или технологий, которые аналогичны описанным выше схемам или процедурам, описанным в разделе синтетических примеров.
Когда требуется оптически активная форма соединения по изобретению, она может быть получена путем проведения одной из процедур, приведенных в данном описании, с использованием оптически активного исходного материала (полученного, например, асимметричной инициацией подходящей стадии реакции), или разделения смеси стереоизомеров соединения или промежуточных соединений с использованием стандартных процедур (таких как хроматографическое разделение, перекристаллизация или ферментативное разделение).
Подобным образом, когда требуется чистый геометрический изомер соединения по изобретению, он может быть получен путем проведения одной из указанных процедур с использованием чистого геометрического изомера в качестве исходного материала или путем разделения смеси геометрических изомеров соединения или промежуточных соединений с использованием стандартных процедур, таких как хроматографическое разделение.
Фармацевтические композиции
Данное изобретение также относится к фармацевтическим композициям, содержащим терапевтически эффективное количество соединения формулы I или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем, разбавителем или наполнителем. Выражение "фармацевтическая композиция" относится к композиции, подходящей для введения при медицинском или ветеринарном применении.
Фармацевтические композиции, которые содержат соединение формулы (I), одно или в сочетании со вторым активным фармацевтическим агентом, могут быть введены субъектам перорально, ректально, парентерально, интрацистернально, интравагинально, интраперитонеально, местно (в виде порошков, мазей или капель), буккально или как оральный или назальный спрей. Термин "парентерально", используемый в данном описании, относится к способам введения, которые включают внутривенную, внутримышечную, интраперитонеальную, интрастернальную, подкожную и интраартикулярную инъекцию и вливание.
Термин "фармацевтически приемлемый носитель", используемый в данном описании, означает нетоксичный инертный твердый, полутвердый или жидкий наполнитель, разбавитель, инкапсулирующие материалы или вспомогательные средства для составов любого типа. Некоторыми примерами материалов, которые могут служить в качестве фармацевтически приемлемых носителей, являются сахара, такие как, но без ограничения указанным, лактоза, глюкоза и сахароза; крахмалы, такие как, но без ограничения указанным, кукурузный крахмал и картофельный крахмал; целлюлоза и ее производные, такие как, но без ограничения указанным, натрий карбоксиметил целлюлоза, этил целлюлоза и ацетат целлюлозы; порошкообразный трагакант, солод, желатин, тальк, наполнители, такие как, но без ограничения указанным, какао-масло и воски для суппозиториев; масла, такие как, но без ограничения указанным, арахисовое масло, масло из семян хлопчатника, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; гликоли, такие как пропиленгликоль; сложные эфиры, такие как, но без ограничения указанным, этил олеат и этил лаурат; агар; буферные агенты, такие как, но без ограничения указанным, гидроксид магния и гидроксид алюминия; альгиновая кислота; апирогенная вода; изотонический солевой раствор; раствор Рингера; этиловый спирт и фосфатные буферные растворы, а также другие нетоксичные совместимые смазки, такие как, но без ограничения указанным, лаурил сульфат натрия и стеарат магния, а также окрашивающие агенты, высвобождающие агенты, кроющие агенты, подслащивающие, вкусовые и ароматизирующие агенты, консерванты и антиоксиданты также могут присутствовать в композиции, согласно решению составителя.
Фармацевтические композиции для парентеральной инъекции содержат фармацевтически приемлемые стерильные водные или неводные растворы, дисперсии, суспензии или эмульсии, а также стерильные порошки для восстановления в стерильные растворы или дисперсии для инъекций непосредственно перед применением. Примеры подходящих водных и неводных носителей, разбавителей, растворителей или переносчиков включают воду, этанол, полиолы (такие как глицерин, пропилен гликоль, полиэтилен гликоль и тому подобное), растительные масла (такие как оливковое масло), органические сложные эфиры для инъекций (такие как этил олеат) и подходящие их смеси. Надлежащую текучесть можно обеспечить, например, используя кроющие материалы, такие как лецитин, поддерживая необходимый размер частиц в случае дисперсии и используя поверхностно-активные вещества.
Такие композиции могут также содержать адъюванты, такие как консерванты, смачивающие агенты, эмульгирующие агенты и диспергирующие агенты. Предотвращение действия микроорганизмов может быть гарантировано включением в состав различных антибактериальных и противогрибковых агентов, например, парабена, хлорбутанола, фенола, сорбиновой кислоты и тому подобного. Может быть также желательно включать изотонические агенты, такие как сахара, хлорид натрия и тому подобное. Пролонгированная абсорбция фармацевтической формы для инъекций может быть обеспечена включением агентов, которые задерживают абсорбцию, таких как моностеарат алюминия и желатин.
В некоторых случаях, чтобы продлить эффект лекарства, желательно замедлить абсорбцию лекарства из подкожной или внутримышечной инъекции. Это может быть осуществлено путем использования жидкой суспензии кристаллического или аморфного материала с плохой растворимостью в воде. Скорость абсорбции лекарства тогда зависит от скорости его растворения, которая, в свою очередь, зависит от размера кристаллов и кристаллической формы. В качестве варианта, замедленная абсорбция парентерально введенной лекарственной формы может быть достигнута растворением или суспендированием лекарства в масляном носителе.
Формы для инъекций депо получают, формируя микроинкапсулирующие матрицы лекарства в биоразложимых полимерах, таких как полилактид-полигликолид. В зависимости от отношения лекарства к полимеру и природы конкретного используемого полимера скорость высвобождения лекарства может быть регулируемой. Примеры других биоразложимых полимеров включают поли(сложные ортоэфиры) и поли(ангидриды). Составы для инъекций депо также получают путем улавливания лекарства в липосомах или микроэмульсиях, которые совместимы с тканями тела.
Составы для инъекций могут быть стерилизованы, например, фильтрованием через задерживающий бактерии фильтр или включением в состав стерилизующих агентов в форме стерильных твердых композиций, которые могут быть растворены или диспергированы в стерильной воде или другой стерильной для инъекций среде непосредственно перед применением.
Твердые дозированные формы для перорального введения включают капсулы, таблетки, пилюли, порошки и гранулы. В конкретных вариантах осуществления, твердые дозированные формы могут содержат от 1% до 95% (масс./масс.) соединения формулы I. В конкретных вариантах осуществления, соединение формулы I может присутствовать в твердой дозированной форме в пределах от 5% до 70% (масс./масс.). В таких твердых дозированных формах, активное соединение может быть смешано по меньшей мере с одним инертным фармацевтически приемлемым наполнителем или носителем, таким как цитрат натрия или дикальций фосфат, и/или a) наполнителями или объемными носителями, такими как крахмалы, лактоза, сахароза, глюкоза, маннит и кремниевая кислота; b) связующими, такими как карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидон, сахароза и камедь акации; c) увлажнителями, такими как глицерин; d) дезинтегрирующими агентами, такими как агар-агар, карбонат кальция, картофельный или тапиоковый крахмал, альгиновая кислота, некоторые силикаты и карбонат натрия; e) раствором замедляющим агенты, таким как парафин; f) акселераторами абсорбции, такими как соединения четвертичного аммония; г) смачивающими агентами, такими как цетиловый спирт и моностеарат глицерина; h) абсорбентами, такими как каолиновая и бентонитовая глина и i) смазками, такими как тальк, стеарат кальция, стеарат магния, твердые полиэтилен гликоли, лаурил сульфат натрия и их смеси. В случае капсул, таблеток и пилюль, дозированная форма может также содержат буферные агенты.
Фармацевтическая композиция может быть унифицированной дозированной формой. В такой форме препарат подразделен на единичные дозы, содержащие соответствующие количества активного компонента. Унифицированная дозированная форма может быть упакованным препаратом, причем упаковка содержит дискретные количества препарата, например, упакованные таблетки, капсулы и порошки в пузырьках или ампулах. Также, унифицированная дозированная форма может быть сама по себе капсулой, таблеткой, саше или пастилкой или это может быть соответствующее число каких-либо из них в упакованной форме. Количество активного компонента в унифицированном дозированном препарате может быть изменяемым или устанавливаемым от 0,1 мг до 1000 мг, от 1 мг до 100 мг или от 1% до 95% (масс./масс.) унифицированной дозы согласно конкретному применению и силе активного компонента. Композиция, если желательно, может также содержать другие совместимые терапевтические агенты.
Доза, которая должна быть введена субъекту, может быть определена по эффективности конкретного используемого соединения и состоянию субъекта, а также по массе тела или площади поверхности субъекта, которого нужно лечить. Размер дозы также будет определяться наличием, характером и величиной каких-либо вредных побочных эффектов, которые сопровождают введение конкретного соединения конкретному субъекту. При определении эффективного количества соединения, которое должно быть введено для лечения или профилактики расстройства, требующего лечения, лечащий врач может учитывать такие факторы, как циркулирующие в плазме уровни соединения, токсичности соединений и/или прогрессирование болезни и т.д. Как правило, эквивалент дозы соединения равен от около 1 мкг/кг до 100 мг/кг для типичного субъекта.
Что касается введения, соединения формулы I могут быть введены при норме, определяемой факторами, которые могут включать, но без ограничения указанным, LD50 соединения, фармакокинетический профиль соединения, противопоказанные лекарства и побочные эффекты соединения при различных концентрациях применительно к массе и общему состоянию здоровья субъекта. Введение может быть осуществлено единой или раздельными дозами.
Соединения, используемые в фармацевтическом способе по изобретению, могут быть введены при начальной дозировке от около 0,001 мг/кг до около 100 мг/кг ежедневно. В конкретных вариантах осуществления, пределы суточной дозы от около 0,1 мг/кг до около 10 мг/кг. Дозировки, однако, могут изменяться в зависимости от потребностей субъекта, тяжести состояния, подвергаемого лечению, и используемого соединения. Определение надлежащей дозировки для конкретной ситуации относится к компетенции практикующего врача. Лечение может быть начато с меньших дозировок, которые меньше чем оптимальная доза соединения, после чего дозировку увеличивают малыми приращениями до достижения оптимального эффекта в таких обстоятельствах. Для удобства общая суточная дозировка может быть разделена и введена порциями в течение дня, если желательно.
Твердые композиции подобного типа могут быть также использованы как наполнители в мягких и твердых заполненных желатиновых капсулах с использованием таких носителей, как лактоза или молочный сахар, а также высокомолекулярные полиэтилен гликоли и тому подобное.
Твердые дозированные формы в виде таблеток, драже, капсул, пилюль и гранул могут быть получены с покрытиями и оболочками, такими как растворимые в кишечнике покрытия и другие покрытия, хорошо известные в фармацевтической практике. Они необязательно могут содержать придающие матовость агенты и могут также быть из композиции такой, что они высвобождают активный ингредиент(ы), только или преимущественно, в конкретной части кишечного тракта, необязательно, с отсрочкой. Примеры внедренных композиций, которые могут быть использованы, включают полимерные вещества и воски.
Активные соединения также могут быть в микроинкапсулированной форме, если это является подходящим, с одним или несколькими из указанных носителей.
Жидкие дозированные формы для перорального введения включают фармацевтически приемлемые эмульсии, растворы, суспензии, сиропы и эликсиры. В дополнение к активным соединениям жидкие дозированные формы могут содержать инертные разбавители, широко используемые в технике, такие как, например, вода или другие растворители, солюбилизирующие агенты и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этил карбонат, этил ацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, масла (в частности, из семян хлопчатника, земляных орехов, кукурузных зародышей, оливковое, касторовое и кунжутное масла), глицерин, тетрагидрофурфуриловый спирт, полиэтиленгликоли и жирнокислотные сложные эфиры ангидросорбита и их смеси.
Помимо инертных разбавителей оральные композиции могут также включать адъюванты, такие как смачивающие агенты, эмульгирующие и суспендирующие агенты, подслащивающие, вкусовые и ароматизирующие агенты.
Суспензии, в дополнение к активным соединениям, могут содержать суспендирующие агенты как, например, этоксилированные изостеариловые спирты, полиоксиэтилен сорбит и сложные эфиры ангидросорбита, макрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар, трагакант и их смеси.
Композиции для ректального или вагинального введения предпочтительно являются суппозиториями, которые могут быть получены смешиванием соединения по данному изобретению с подходящими нераздражающими носителями или такими носителями, как какао-масло, полиэтиленгликоль или воск для суппозиториев, который является твердым при комнатной температуре, но жидким при температуре тела и поэтому плавится в прямой кишке или в вагинальной полости и высвобождает активное соединение.
Соединения формулы I могут быть также введены в форме липосом. Липосомы обычно могут быть получены из фосфолипидов или других липидных веществ. Липосомы формируют моно- или многослойными гидратированными жидкими кристаллами, которые диспергируют в водной среде. Любой нетоксичный физиологически приемлемый и метаболизируемый липид, способный образовывать липосомы может быть использован. Данные композиции в липосомной форме могут содержать, в дополнение к соединению формулы (I), стабилизаторы, консерванты, наполнители и тому подобное. Примеры липидов включают, но без ограничения указанным, натуральные и синтетические фосфолипиды и фосфатидил холины (лецитины), используемые раздельно или вместе.
Способы формирования липосом описаны, смотри, например, Prescott, Ed., Methods in Cell Biology, Volume XIV, Academic Press, New York, N.Y. (1976), p. 33 et seq.
Дозированные формы для местного введения соединения из данного описания включают порошки, спреи, мази и средства для ингаляции. Активное соединение может быть смешано в стерильных условиях с фармацевтически приемлемым носителем и какими-либо необходимыми консервантами, буферами или пропеллентами, которые могут быть необходимы. Глазные составы, глазные мази, порошки и растворы также рассматриваются как входящие в объем данного изобретения.
Способы применения
Соединения формулы I или их фармацевтически приемлемые соли и фармацевтические композиции, содержащие соединение формулы I или его фармацевтически приемлемую соль, могут быть введены субъекту, страдающему от опосредуемого бромдоменом расстройства или состояния. Термин "введение" относится к способу приведения в контакт соединения с субъектом. Так, соединения формулы I могут быть введены инъекцией, то есть внутривенно, внутримышечно, внутрикожно, подкожно, интрадуоденально, парентерально или интраперитонеально. Также, соединения из данного описания могут быть введены ингаляцией, например, интраназально. Дополнительно соединения формулы I могут быть введены трансдермально, местно, посредством имплантации, трансдермально, местно и посредством имплантации. В конкретных вариантах осуществления, соединения формулы I могут быть доставлены перорально. Соединения также могут быть доставлены ректально, буккально, интравагинально, окулярно, андиально или вдуванием. Опосредуемые бромдоменом расстройства и состояния могут быть обработаны профилактически, остро и хронически с использованием соединений формулы I, в зависимости от характера расстройства или состояния. Обычно, хозяин или субъект в каждом из указанных способов является человеком, хотя другие млекопитающие также могут получать пользу от введения соединений формулы I.
"Опосредуемое бромдоменом расстройство или состояние" характеризуется участием одного или нескольких бромдоменов (например, BRD4) в начале, проявлении одного или нескольких симптомов или признаков болезни, тяжести или прогрессирования расстройства или состояния. Соответственно, соединения формулы I могут быть использованы для лечения рака, включая, но без ограничения указанным, неврилеммому слухового нерва, острую лейкемию, острую лимфоцитарную лейкемию, острую миелоцитарную лейкемию (моноцитарную, миелобластную аденокарциному, злокачественную гемангиому, астроцитому, миеломоноцитарную и промиелоцитарную), острую Т-клеточную лейкемию, базально-клеточную карциному, карциному желчных путей, рак мочевого пузыря, рак головного мозга, рак молочной железы, бронхогенную карциному, цервикальный рак, хондросаркому, хордому, хориокарциному, хроническую лейкемию, хроническую лимфоцитарную лейкемию, хроническую миелоцитарную (гранулоцитарную) лейкемию, хроническую миелогенную лейкемию, рак толстой кишки, колоректальный рак, краниофарингиомуа, цистаденокарциному, диффузную крупноклеточную лимфому, диспролиферативные изменения (дисплазии и метаплазии), эмбриональную карциному, карциному эндометрия, эндотелиосаркому, эпендимому, эпителиальный рак, эритролейкемию, рак пищевода, позитивный в отношении эстрогенового рецептора рак молочной железы, существенную тромбоцитемию, болезнь Юинга, фибросаркому, фолликулярную лимфому, эмбриональноклеточный тестикулярный рак, глиому, глиобластому, глиосаркому, болезнь тяжелой (пептидной) цепи, гемангиобластому, гепатому, гепатоцеллюлярный рак, гормональный интенсивный рак простаты, лейомиосаркому, лейкемию, липосаркому, рак легкого, лимфагиоэндотелиосаркому, лимфангиосаркому, лимфобластную лейкемию, лимфому (Ходжкина и неходжкинскую), злокачественные новообразования и гиперпролиферативные расстройства мочевого пузыря, молочной железы, толстой кишки, легких, яичников, поджелудочной железы, простаты, кожи и матки, лимфоидные злокачественные новообразования T-клеточного или В-клеточного происхождения, лейкемию, лимфому, медуллярный рак, медуллобластому, меланому, менингиому, мезотелиому, множественная миелома, миелогенная лейкемия, миелома, миксосаркому, нейробластому, NUT срединную карциному (NMC), немелкоклеточный рак легкого, олигодендроглиому, рак ротовой полости, остеогенную саркому, рак яичников, панкреатический рак, сосковидные аденокарциномы, сосковидную карциному, пинеалому, истинную полицитемию, рак простаты, ректальный рак, почечно-клеточную [светлоклеточную] карциному, ретинобластому, рабдомиосаркому, саркому, карциному сальных желез, семиному, рак кожи, мелкоклеточную карциному легких, солидные опухоли (карциномы и саркомы), мелкоклеточный рак легкого, рак желудка, сквамозноклеточную карциному, синовиальную эндотелиому, карциному потовых желез, рак щитовидной железы, макроглобулинемию Вальденштрома, тестикулярные опухоли, рак матки и опухоль Вильмса.
Дополнительно, соединения формулы I могут быть использованы для лечения воспалительных болезней, воспалительных состояний и аутоиммунных болезней, включая, но без ограничения указанным: Болезнь Эддисона, острую подагру, анкилозирующий спондилоартрит, астму, атеросклероз, болезнь Бехчета, буллезные кожные болезни, хроническую обструктивную легочную болезнь (COPD), болезнь Крона, дерматит, экзему, гигантоклеточный аортит, гломерулонефрит, гепатит, гипофизит, воспалительную болезнь кишечника, болезнь Кавасаки, люпус-нефрит, рассеянный склероз, миокардит, миозит, нефрит, отторжение трансплантированного органа, остеоартрит, панкреатит, перикардит, нодозный полиартериит, пульмонит, билиарный первичный цирроз печени, псориаз, псориатический артрит, ревматоидный артрит, склерит, склерозирующий холангит, сепсис, системную красную волчанку, артериит Такаясу, токсический шок, тиреоидит, диабет типа I, язвенный колит, увеит, витилиго, васкулит и грануломатоз Вегенера.
Соединения формулы I или их фармацевтически приемлемые соли могут быть использованы для лечения СПИД.
Соединения формулы I или их фармацевтически приемлемые соли могут быть использованы для лечения хронической почечной болезни или состояния, включая, но без ограничения указанным: диабетическую нефропатию, гипертензивную нефропатию, связанную с ВИЧ нефропатию, гломерулонефрит, люпус-нефрит, IgA нефропатию, очаговый сегментарный гломерулосклероз, мембранный гломерулонефрит, болезнь минимальной альтерации, поликистозную почечную болезнь и канальцевый интерстициальный нефрит.
Соединения формулы I или их фармацевтически приемлемые соли могут быть использованы для лечения острого почечного поражения или болезни или состояния, включая, но без ограничения указанным: вызванные ишемией-реперфузией, вызванные сердечной и радикальной хирургией, вызванные перкутанным коронарным вмешательством, вызванные радиоактивным контрастным агентом, вызванные сепсисом, вызванные пневмонией и вызванные токсичностью лекарства.
Соединения формулы I или их фармацевтически приемлемые соли могут быть использованы для лечения ожирения, дислипидемии, гиперхолестеринемии, болезни Альцгеймера, метаболического синдрома, ожирения печени, диабета типа II, резистентности к инсулину, диабетической ретинопатии или диабетической невропатии.
Соединения формулы I или их фармацевтически приемлемые соли могут быть использованы для контрацепции у субъекта мужского рода путем введения терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли субъекту мужского рода при необходимости этого.
Соединения формулы I могут быть совместно введены субъекту. Термин "совместно введены" означает введение двух или более различных фармацевтических агентов или обработок (например, обработки облучением), которые назначают субъекту, объединяя в одной и той же фармацевтической композиции или в раздельных фармацевтических композициях. Так, совместное введение предусматривает введение в одно и то же время единой фармацевтической композиции, содержащей два или более фармацевтических агентов, или введение двух или более различных композиций одному и тому же субъекту в одно и то же время или в разные моменты времени.
Соединения по изобретению могут быть совместно введены с терапевтически эффективным количеством одного или нескольких агентов для лечения рака, где примеры агентов включают такие как облучение, алкилирующие агенты, ингибиторы ангиогенеза, антитела, антиметаболиты, антимитотические средства, антипролиферативные средства, антивирусные средства, ингибиторы aurora киназы, промоторы апоптоза (например, BCl-xL, BCl-w и Bfl-1) ингибиторы, активаторы пути рецептора смерти, ингибиторы Bcr-Abl киназы, BiTE (Bi-специфический T клеточный Engager) антитела, конъюгаты антитела и лекарства, модификаторы биологической реакции, ингибиторы циклин-зависимой киназы, ингибиторы клеточного цикла, ингибиторы циклооксигеназы-2, DVD (антитела двойного вариабельного домена), ингибиторы лейкозного вирусного онкогенного гомологичного (ErbB2) рецептора, ингибиторы фактора роста, ингибиторы протеина (HSP)-90 теплового шока, ингибиторы гистон деацетилазы (HDAC), гормональные терапии, иммунологические средства, ингибиторы ингибиторов протеина апоптоза (IAP), интеркалирующие антибиотики, ингибиторы киназы, ингибиторы кинезина, Jak2 ингибиторы, ингибиторы относящейся к млекопитающим мишени рапамицина, микроRNA, ингибиторы активируемой митогеном внеклеточной сигнал-регулируемой киназы, многовалентные связывающие протеины, нестероидные противовоспалительные лекарства (NSAID), ингибиторы полимерaзы поли ADP (аденозин дифосфат)-рибозы (PARP), платиновые химиотерапевтические средства, ингибиторы киназы поло-типа (Plk), ингибиторы фосфоинозитид-3 киназы (бромдомен), ингибиторы протеосомы, аналоги пурина, аналоги пиримидина, ингибиторы рецепторной тирозин киназы, растительные алкалоиды этиноиды/делтоиды, малые ингибиторные рибонуклеиновые кислоты (siRNA), ингибиторы топоизомеразы, ингибиторы убиквитин лигазы и тому подобное, и в сочетании с одним или несколькими из указанных агентов.
BiTE антитела являются би-специфическими антителами, которые нацеливают T-клетки атаковать раковые клетки путем одновременного связывания с двумя клетками. T-клетки затем нападают на целевую раковую клетку. Примеры BiTE антител включают адекатумумаб (Micromet MT201), блинатумомаб (Micromet MT103) и тому подобное. Без ограничения связыванием с теорией, одним из механизмов, посредством которого T-клетки вызывают апоптоз целевой раковой клетки является экзоцитоз цитолитических компонентов гранул, которые включают перфорин и гранзим B. В этом отношении, BCl-2, как было показано, ослабляет запуск апоптоза как перфорином, так и гранзимом В. Эти данные подтверждают, что ингибирование BCl-2 могло бы усовершенствовать цитотоксичные эффекты, вызываемые T-клетками, когда нацелены на раковые клетки (V.R. Sutton, D.L. Vaux и J.A. Trapani, J. of Immunology 1997, 158 (12), 5783).
SiRNA представляют собой молекулы, имеющие эндогенные RNА основания, или химически модифицированные нуклеотиды. Модификации не отменяют клеточную активность, но скорее придают повышенную стабильность и/или повышенную клеточную потенцию. Примеры химических модификаций включают фосфоротиоатные группы, 2'-дезоксинуклеотид, 2'-OCH3-содержащие рибонуклеотиды, 2'-F- рибонуклеотиды, 2'-метоксиэтил рибонуклеотиды, их сочетания и тому подобное. siRNA могут иметь изменяющиеся длины (например, 10-200 пар оснований) и структуры (например, шпильки, одинарные/двойные тяжи, петли, ники/гэпы, нарушения парности) и подвергаются процессу в клетках, чтобы обеспечить молчание активного гена. Двухтяжевая siRNA (dsRNA) может иметь одно и то же число нуклеотидов на каждом тяже (тупые концы) или асимметричные концы (выступы). Выступ из 1-2 нуклеотидов может присутствовать на смысловом и/или антисмысловом тяже, а также присутствовать на 5'- и/или 3'-концах данного тяжа.
Многовалентные связывающие протеины являются связывающими протеинами, содержащими два или более сайтов связывания антигена. Многовалентные связывающие протеины являются сконструированными, чтобы иметь три или более сайтов связывания антигена, и обычно являются не встречающимися в природе антителами. Термин "мультиспецифический связывающий протеин" означает связывающий протеин, способный к связыванию двух или более родственных или неродственных мишений. Протеины, связывающие двойной вариабельный домен (DVD), являются четырехвалентными или многовалентными связывающими протеинами, содержащими два или более сайтов связывания антигена. Такие DVD могут быть моноспецифическими (т.е. способными к связыванию одного антигена) или мультиспецифическими (т.е. способными к связыванию двух или более антигенов). Связывающие DVD протеины, содержащие два DVD полипептида с тяжелой цепью и два DVD полипептида с легкой цепью, упоминаются как DVD Ig. Каждая половина DVD Ig содержит DVD полипептид с тяжелой цепью, DVD полипептид с легкой цепью и два сайта связывания антигена. Каждый сайт связывания содержит вариабельный домен тяжелой цепи и вариабельный домен легкой цепи с общим числом 6 CDR, вовлекаемых в связывание, на сайт связывания антигена. Мультиспецифические DVD включают связывающие DVD протеины, которые связывают DLL4 и VEGF, или C-met и EFGR, или ErbB3 и EGFR.
Алкилирующие агенты включают алтретамин, AMD-473, AP-5280, апазиквон, бендамустин, бросталлицин, бусулфан, карбоквон, кармустин (BCNU), хлорамбуцил, CLORETAZINE® (ларомустин, VNP 40101M), циклофосфамид, декарбазин, эстрамустин, фотемустин, глуфосфамид, ифосфамид, KW-2170, ломустин (CCNU), мафосфамид, мелфалан, митобронитол, митолактол, нимустин, азотный горчичный N-оксид, ранимустин, темозоломид, тиотепа, TREANDA® (бендамустин), треосулфан, рофосфамид и тому подобное.
Ингибиторы ангиогенеза включают ингибиторы эндотелиально-специфической рецепторной тирозин киназы (Tie-2), ингибиторы рецептора эпидермального ростового фактора (EGFR), ингибиторы рецептора инсулинового ростового фактора-2 (IGFR-2), ингибиторы матричной металлопротеиназы-2 (MMP-2), ингибиторы матричной металлопротеиназы-9 (MMP-9), ингибиторы рецептора выделенного из тромбоцитов ростового фактора (PDGFR), аналоги тромбоспондина, тирозинкиназные ингибиторы рецептора сосудистого эндотелиального ростового фактора (VEGFR) и тому подобное.
Антиметаболиты включают ALIMTA® (пеметрексед динатрий, LY231514, MTA), 5-азацитидин, XELODA® (капецитабин), кармофур, 1eUSTAT® (кладрибин), клофарабин, цитарабин, цитарабин окфостат, цитозин арабинозид, децитабин, дефероксамин, диоксифлуридин, эфлорнитин, EICAR (5-этинил-1-β-D-рибофуранoзилимидазол-4- карбоксамид), эноцитабин, этинилцитидин, флударабин, 5-фторурацил один или в сочетании с лейковорином, GEMZAR® (гемцитабин), гидроксимочевину, ALKERAN® (мелфалан), меркаптопурин, 6-меркаптопурин рибозид, метотрексат, микофеноловую кислоту, наларабин, нолатрексед, окфостат, пелитрексол, пентостатин, ралтрексед, рибавирин, триапин, триметрексат, S-1, тиазофурин, тегафур, TS-1, видарабин, UFT и тому подобное.
Антивирусные средства включают ритонавир, гидроксихлорквин и тому подобное.
Ингибиторы aurora киназы включают ABT-348, AZD-1152, MLN-8054, VX-680, ингибиторы Aurora A-специфической киназы, ингибиторы Aurora B-специфической киназы и ингибиторы пан-Aurora киназы и тому подобное.
Ингибиторы BCl-2 протеина включают AT-101 ((-)госсипол), GENASENSE® (G3139 или облимерсен (BCl-2-нацеленный антисмысловой олигонуклеотид)), IPI-194, IPI-565, N-(4-(4-((4'-хлор(1,1'-бифенил)-2-ил)метил)пиперазин-1-ил)бензоил)-4-(((1R)-3-диметиламино)-1-((фенилсульфанил)метил)пропил)амино)-3-нитробензолсульфонамид) (ABT-737), N-(4-(4-((2-(4-хлорфенил)-5,5-диметил-1-циклогекс-1-eн-1-ил)метил)пиперазин-1-ил)бензоил)-4-(((1R)-3-(морфолин-4-ил)-1-((фенилсульфанил)метил)пропил)амино)-3-((трифторметил)сульфонил)бензолсульфонамид (ABT-263), GX-070 (обатоклакс), ABT-199 и тому подобное.
Ингибиторы Bcr-Abl киназы включают DASATINIB® (BMS-354825), GLEEVEC® (иматиниб) и тому подобное.
Ингибиторы CDK включают AZD-5438, BMI-1040, BMS-032, BMS-387, CVT-2584, флавопиридол, GPC-286199, MCS-5A, PD0332991, PHA-690509, селициклиб (CYC-202, R-росковитин), ZK-304709 и тому подобное.
Ингибиторы COX-2 включают ABT-963, ARCOXIA® (эторикоксиб), BEXTRA® (валдекоксиб), BMS347070, CELEBREX® (целекоксиб), COX-189 (лумеракоксиб), CT-3, DERAMAXX® (деракоксиб), JTE-522, 4-метил-2-(3,4-диметилфенил)-1-(4-сульфамоилфенил-1H-пиррол), MK-663 (эторикоксиб), NS-398, парекоксиб, RS-57067, SC-58125, SD-8381, SVT-2016, S-2474, T-614, VIOXX® (рофекоксиб) и тому подобное.
Ингибиторы EGFR включают антитела EGFR, ABX-EGF, анти-EGFR иммунолипосомы, EGF-вакцину, EMD-7200, ERBITUX® (цетуксимаб), HR3, антитела IgA, IRESSA® (гефитиниб), TARCEVA® (эрлотиниб или OSI-774), TP-38, EGFR интегрированный протеин, TYKERB® (лапатиниб) и тому подобное.
Ингибиторы ErbB2 рецептора включают CP-724-714, Cl-1033 (канертиниб), HERCEPTIN® (трастузумаб), TYKERB® (лапатиниб), OMNITARG® (2C4, петезумаб), TAK-165, GW-572016 (ионафарниб), GW-282974, EKB-569, PI-166, dHER2 (HER2 вакцина), APC-8024 (HER-2 вакцина), анти-HER/2neu биспецифическое антитело, B7.her2IgG3, AS HER2 трифункциональные биспецифические антитела, mAB AR-209, mAB 2B-1 и тому подобное.
Ингибиторы гистон деацетилазы включают депсипептид, LAQ-824, MS-275, трапоксин, субероиланилил гидроксамовую кислоту (SAHA), TSA, валпроевую кислоту и тому подобное.
Ингибиторы HSP-90 включают 17-AAG-nab, 17-AAG, CNF-101, CNF-1010, CNF-2024, 17-DMAG, гелданамицин, IPI-504, KOS-953, MYCOGRAB® (рекомбинантное антитело человека к HSP-90), NCS-683664, PU24FC1, PU-3, радицикол, SNX-2112, STA-9090 VER49009 и тому подобное.
Ингибиторы ингибиторов протеинов апоптоза включают HGS1029, GDC-0145, GDC-0152, LCL-161, LBW-242 и тому подобное.
Конъюгаты антитело-лекарство включают анти-CD22-MC-MMAF, анти-CD22-MC-MMAE, анти-CD22-MCC-DM1, CR-011-vcMMAE, PSMA-ADC, MEDI-547, SGН-19Am SGН-35, SGН-75 и тому подобное.
Активаторы пути рецептора смерти включают TRAIL, антитела или другие агенты, которые нацеливают TRAIL или рецепторы смерти (например, DR4 и DR5), такие как Apomab, конатумумаб, ETR2-ST01, GDC0145, (лексатумумаб), HGS-1029, LBY-135, PRO-1762 и трастузумаб.
Ингибиторы кинезина включают Eg5 ингибиторы, такие как AZD4877, ARRY-520; CENPE ингибиторы, такие как GSK923295A и тому подобное.
Ингибиторы JAK-2 включают CEP-701 (лесауртиниб), XL019 и INCBO18424 и тому подобное.
Ингибиторы MEK включают ARRY-142886, ARRY-438162 PD-325901, PD-98059 и тому подобное.
Ингибиторы mTOR включают AP-23573, CCI-779, эверолимус, RAD-001, рапамицин, темсиролимус, ATP-конкурентные TORC1/TORC2 ингибиторы, включая PI-103, PP242, PP30, торин 1 и тому подобное.
Нестероидные противовоспалительные лекарства включают AMIGESIC® (салсалат), DOLOBID® (дифлунизал), MOTRIN® (ибупрофен), ORUDIS® (кетопрофен), RELAFEN® (набуметон), FELDENE® (пироксикам), крем ибупрофена, ALEVE® (напроксен) и NAPROSYN® (напроксен), VOLTAREN® (диклофенас), INDOCIN® (индометацин), CLINORIL® (сулиндак), TOLECTIN® (толметин), LODINE® (этодолак), TORADOL® (кеторолак), DAYPRO® (оксапрозин) и тому подобное.
Ингибиторы PDGFR включают C-451, CP-673, CP-868596 и тому подобное.
Платиновые химиотерапевтические средства включают цисплатин, ELОКСАTIN® (оксалиплатин) эптаплатин, лобарплатин, недаплатин, PARAPLATIN® (карбоплатин), сатраплатин, пикоплатин и тому подобное.
Ингибиторы рolo-подобной киназы включают BI-2536 и тому подобное.
Ингибиторы фосфоинозитид-3 киназы (PI3K) включают вортманнин, LY294002, XL-147, CAL-120, ONC-21, AEZS-127, ETP-45658, PX-866, GDC-0941, BGT226, BEZ235, XL765 и тому подобное.
Аналоги тромбоспондина включают ABT-510, ABT-567, ABT-898, TSP-1 и тому подобное.
Ингибиторы VEGFR включают AVASTIN® (бевацизумаб), ABT-869, AEE-788, ANGIOZYME™ (рибозим, который ингибирует ангиогенез (Ribozyme Pharmaceuticals (Boulder, CO.) и Chiron, (Emeryville, CA)), акситиниб (AG-13736), AZD-2171, CP-547,632, IM-862, MACUGEN (пегаптамиб), NEXAVAR® (сорафениб, BAY43-9006), пазопаниб (GW-786034), ваталаниб (PTK-787, ZK-222584), SUTENT® (санитиниб, SU-11248), YEGF trap, ZACTIMA™ (вандетаниб, ZD-6474), GA101, афатумумаб, ABT-806 (mAb-806), ЕrbBЗ специфические антитела, BSG2 специфические антитела, DLL4 специфические антитела и C-met специфические антитела и тому подобное.
Антибиотики включают интеркалирующие антибиотики акларубицин, актиномицин D, амрубицин, аннамицин, адриамицин, BLENОКСАNE® (блеомицин), даунорубицин, CAELYX® или MYOCET® (липосомный доксорубицин), элсамитруцин, эпирбуцин, гларбуцин, ZAVEDOS® (идарубицин), митомицин C, неморубицин, неокарзиностатин, пепломицин, пирарубицин, ребеккамицин, стимаоамер, сирептозоцин, VALSTAR (валрубицин), зиностатин и тому подобное.
Ингибиторы топоизомеразы включают акларубицин, 9-аминокамптотецин, амонафалид, амсакрин, бекатекарин, белотекан, BН-80915, CAMPTOSAR® (иринотекан гидрохлорид), камптотецин, CARДИОКСАН® (декстразоксин), дифломотекан, эдотекарин, ELLENCE® или PHARMORUBICLN® (эпирубицин), этопозид, эксатекан, 10-гидроксисамптотецин, гиматекан, луртотекан, миоксантрон, оратецин, пирарбуцин, пиксантрон, рубитекан, собузоксан, SН-38, тафлупозид, топотекан и тому подобное.
Антитела включают AVASTIN® (бевацизумаб), CD40-специфические антитела, chTNT-1/B, деносумаб, ERBITUX® (цетуксимаб), HUMAX-CD4® (занолимумаб), IGFIR-специфические антитела, линтузумаб, PANOREX® (эдреколомаб), RENCAREX® (WX G250), RITUXAN® (ритуксимаб), тицилимумаб, трастузимаб, CD20 антитела типа I и II и тому подобное.
Гормональные терапевтические средства включают ARIMIDEX® (анастрозол), AROMASIN® (экземестан), арзоксифен, CASODEX® (бикалутамид), CETROTIDE® (цетрореликс), дегареликс, деслорелин, DESOPAN® (трилостан), дексаметазон, DROGENIL® (флутамид), EVISTA® (ралоксифен), AFEMA™ (фадрозол), FARESTON® (торемифен), FASLODEX® (фулвестрант), FEMARA® (летрозол), форместан, глюкокортикоиды, HECTOROL® (доксеркальциферол), RENAGEL® (севеламер карбонат), лазофоксилан, лейпролид ацетат, MEGACE® (мегестрол), MIFEPREX® (мифепрестон), NILANDRON™ (нилутамид), NOLVADEX® (тамоксифен цитрат), PLENAXIS™ (абареликс), преднизон, PROPECIA® (финастерид), рилостан, SUPREFACT® (бусерелин), TRELSTAR® (гормон, высвобождающий лютенизирующий гормон, (1HRPI)), VANTAS® (Histrelin имплантат), VETORИЛ® (трилостан или модрастан), ZOLADEX® (форселин, госерелин) и тому подобное.
Делтоиды и ретиноиды включают сеокальцитол (EB1089, CB1093), лексакальцитол (KH1060), фенретинид, PANRETIN® (алиретиноин), ATRAGEN® (липосомный третиноин), TARGRETIN® (бексатротен), LGD-1550 и тому подобное.
Ингибиторы PARP включают ABT-888 (велипариб), олапариб, KU-59436, AZD-2281, AG-014699, BSI-201, BGP-15, INO-1001, ONO-2231 и тому подобное.
Растительные алкалоиды включают, но без ограничения указанным, винкристин, винбластин, виндестин, винорелбин и тому подобное.
Ингибиторы протеосомы включают VELCADE® (бортезомиб), MG132, NPI-0052, PR-171 и тому подобное.
Примеры иммунологических средств включают интерфероны и другие повышающие иммунитет агенты. Интерфероны включают интерферон альфа, интерферон альфа-2a, интерферон альфа-2b, интерферон бета, интерферон гамма-1a, ACTIMMUNE® (интерферон гамма-1b) или интерферон гамма-n1, их сочетания и тому подобное. Другие агенты включают ALFAFERONE®,(IFN-α), BAM-002 (оксиленный глутатион), BEROMUN® (тазонермин), BEXXAR® (тозитумомаб), CAMPATH® (алемтузумаб), CTLA4 (цитотоксичный лимфоцитарный антиген 4), декарбазин, денилейкин, эпратузумаб, GRANOCYTE® (ленограстим), лентинан, лейкоцитарный альфа интерферон, имиквимод, MDX-010 (анти-CTLA-4), вакцина меланомы, митумомаб, молграмостим, MИЛOTARG™ (гемтузумаб озогамицин), NEUPOGEN® (филграстим), OncoVAC-Cl, OVAREX® (ореговомаб), пемтумомаб (Y-muHMFG1), PROVENGE® (сипулейцел-T), саргарамостим, сизофилан, тецелейкин, THERACYS® (Bacillus Calmette-Guerin), убенимекс, VIRULIZIN® (иммунотерапевтическое средство, Lorus Pharmaceuticals), Z-100 (специфическая субстанция Maruyama (SSM)), WF-10 (тетрахлордекаоксид (TCDO)), PROLEUKIN® (альдеслейкин), ZADAXIN® (тималфазин), ZENAPAX® (даклизумаб), ZEVALIN® (90Y-ибритумомаб тиукситан) и тому подобное.
Модификаторы биологической реакции являются агентами, которые модифицируют механизмы защитной реакции живых организмов или биологические реакции, такие как выживание, рост или дифференциация клеток ткани, чтобы придать им противоопухолевую активность, и включают крестин, лентинан, сизоферан, пицибанил PF-3512676 (CpG-8954), убенимекс и тому подобное.
Аналоги пиримидина включают цитарабин (ара С или арабинозид C), цитозин арабинозид, доксифлуридин, FLUDARA® (флударабин), 5-FU (5-фторурацил), флоксуридин, GEMZAR® (гемцитабин), TOMUDEX® (ратитрексед), TRОКСАTИЛ™ (триацетилуридин троксацитабин) и тому подобное.
Аналоги пурина включают LANVIS® (тиогуанин) и PURI-NETHOL® (меркаптопурин).
Антимитотические агенты включают батабулин, эпотилон D (KOS-862), N-(2-((4-гидроксифенил)амино)пиридин-3-ил)-4-метоксибензолсульфонамид, иксабепилон (BMS 247550), паклитаксел, TAXOTERE® (доцетаксел), PNU100940 (109881), патупилон, XRP-9881 (ларотаксел), винфлунин, ZK-EPO (синтетический эпотилон) и тому подобное.
Ингибиторы убиквитин липазы включают MDM2 ингибиторы, такие как нутлины, NEDD8 ингибиторы, такие как млN4924 и тому подобное.
Соединения по данному изобретению могут быть также использованы в качестве радиосенсибилизирующих средств, которые повышают эффективность радиотерапии. Примеры радиотерапии включают радиотерапию внешним пучком, телетерапию, брахитерапию и радиотерапию с применением герметичного или негерметичного источника и тому подобное.
Дополнительно, соединения, имеющие Формулу (I), могут быть объединены с другими химиотерапевтическими агентами, такими как ABRAXANE™ (ABI-007), ABT-100 (ингибитор фарнезил трансферазы), ADVEXIN® (Ad5CMV-p53 вакцина), ALTOCOR® или MEVACOR® (ловастатин), AMPLIGEN® (поли I:поли C12U, синтетическая RNA), APTOSYN® (экзисулинд), AREDIA® (пальмидроновая кислота), арглабин, 1-аспарагиназа, атаместан (1-метил-3,17-дион-андроста-1,4-диен), AVAGE® (тазаротен), AVE-8062 (производное комбреастатина) BEC2 (митумомаб), кахектин или кахексин (фактор некроза опухоли), канваксин (вакцина), CEAVAC® (вакцина рака), CELEUK® (целмолейкин), CEPLENE® (гистамин дигидрохлорид), CERVARIX® (вакцина папиломавируса человека), CHOP® (C:CYTОКСАN® (циклофосфамид); H: ADRIAMYCIN® (гидроксидоксорубицин); O: Vincristine (ONCOVIN®); P:преднизон), CYPAT™ (ципротерон ацетат), комбрестатин A4P, DAB(389)EGF (каталитические и транслокационные домены токсина дифтерии, объединенные посредством линкера His-Ala с эпидермальным фактором роста человека) или TransMID-107R™ (токсины дифтерии), дакарбазин, дактиномицин, 5,6-диметилксантенон-4-уксусная кислота (DMXAA), энилурацил, EVIZON™ (скваламин лактат), DIMERICLNE® (T4N5 липосомный лосьон), дискодермолид, DX-8951f (эксатекан мезилат), энзастаурин, EP0906 (эпитилон B), GARDASIL® (рекомбинантная вакцина четырехвалентного папиломавируса человека (типы 6, 11, 16, 18)), GASTRIMMUNE®, GENASENSE®, GMK (вакцина конъюгата ганглиозида), GVAX® (вакцина рака простаты), галофугинон, гистерилин, гидроксикарбамид, ибандроновая кислота, IGN-101, IL-13-PE38, IL-13-PE38QQR (цинтредекин бесудотокс), экзотоксин IL-13-pseudomonas, интерферон-α, интерферон-γ, JUNOVAN™ или МЕРACT™ (мифамуртид), лонафарниб, 5,10-метилентетрагидрофолат, милтефозин (гексадецилфосфохолин), NEOVASTAT®(AE-941), NEUTREXIN® (триметрексат глюкуронат), NIPENT® (пентостатин), ONCONASE® (фермент рибонуклеаза), ONCOPHAGE® (обработка вакциной меланомы), ONCOVAX® (IL-2 вакцина), ORATHECLN™ (рубитекан), OSIDEM® (клеточное лекарство на основе антитела), OVAREX® MAb (мышиное моноклональное антитело), паклитаксел, PANDIMEX™ (агликон сапонины из женьшеня, содержащие 20(S)протопанаксадиол (aPPD) и 20(S)протопанаксаериол (aPPT)), панитумумаб, PANVAC-VF (исследовательская вакцина рака), пегаспаргаза, PEG Интерферон A, феноксодиол, прокарбазин, ребимастат, REMOVAB® (катумаксомаб), REVLIMID® (ленолидомид), RSR13 (эфопроксирал), SOMATULINE® LA (ланреотид), SORIATANE® (ацитретин), стауроспорин (Streptomyces staurospores), талабостат (PT100), TARGRETIN® (бексаротен), TAXOPREXIN® (DHA-паклитаксел), TELCYTA® (канфосфамид, TLK286), темилифен, TEMODAR® (темозоломид), тесмилифен, талидомид, THERATOPE® (STn-K1H), тимитаг (2-амино-3,4-дигидро-6-метил-4-оксо-5-(4-пиридилтио)хиназолин дигидрохлорид), TNFERADE™ (аденовектор: DNA носитель, содержащий ген для фактора-α некроза опухоли), TRACLEER или ZAVESCA® (босентан), третиноин (ретин-A), тетрандрин, ТRIСENOX® (мышьяковый триоксид), VIRULIZIN®, украин (производное алкалоидов из растения большой чистотел), витаксин (анти-альфаvбета3 антитело), XCYTRIN® (мотексафин гадолиний), XINLAY™ (атрасентан), XYOTAX™ (паклитаксел полиглумекс), YONDELIS® (трабектедин), ZD-6126, ZINECARD® (декстразоксан), ZOMETA® (золендроновая кислота), зорубицин и тому подобное.
Соединения по изобретению также могут быть совместно введены с терапевтически эффективным количеством одного или нескольких агентов для лечения воспалительной болезни или состояния, или аутоиммунной болезни, где примеры агентов включают, такие как метотрексат, тофацитиниб, 6-меркаптопурин, азатиоприн сульфасалазин, мезасалазин, олсалазин хлорхинин/гидроксихлорквин, пенцилламин, ауротиомалат (внутримышечный и оральный), азатиоприн, кохицин, кортикостероидны средства (оральное, вдыхаемое и местная инъекция), бета-2 адренорецептор агонисты (салбутамол, тербуталин, салметерал), ксантины (теофиллин, аминофиллин), кромогликат, недокромил, кетотифен, ипратропин и окситропин, циклоспорин, FK506, рапамицин, микофенолят мофетил, лефлуномид, NSAID, например, ибупрофен, кортикостероиды, такие как преднизолон, ингибиторы фосфодиэстеразы, агонисты аденозина, антитромботические агенты, ингибиторы комплемента, адренергические агенты, агенты, которые мешают передаче сигналов провоспалительных цитокинов, таких как TNF или IL-1 (например, ингибиторы киназы NIK, IKK, p38 или MAP), ингибиторы IL-1 превращающего фермента, ингибиторы передачи сигналов T-клеток, такие как ингибиторы киназы, ингибиторы металлoпротеинaзы, сулфасалазин, 6-меркаптопурины, ингибиторы ангиотензин превращающего фермента, рецепторы растворимого цитокина и их производные (например, рецепторы растворимого p55 или p75 TNF и производные p75TNFRIgG (этанерцепт) и p55TNFRIgG (ленерцепт), sIL-1RI, sIL-1RII, sIL-6R), противовоспалительные цитокины (например, IL-4, IL-10, IL-11, IL-13 и TGF), селекоксиб, фолиевая кислота, гидроксихлороквин сульфат, рофекоксиб, этенерцепт, инфликсимаб, адалимубаб, цертолизумаб, толисилизумаб, аватасепт, напроксен, валдекоксиб, сульфалазин, метилпреднизолон, мелоксикам, метилпреднизолон ацетат, тиомалат золота натрия, аспирин, триамцинолон ацетoнид, пропоксифен напсилат/апап, фолат, набуметон, диклофенак, пироксикам, этодолак, диклофенак натрий, оксапрозин, оксикодон НCl, гидрокодон битартрат/апап, диклофенак натрий/мисопростол, фентанил, анакинра, трамадол HCl, салсалат, сулиндак, цианокобаламин/фа/пиридоксин, ацетаминофен, алендронат натрий, преднизолон, кортизон, бетаметазон, морфин сульфат, лидокаин гидрохлорид, индометацин, глюкозамин сульф/хондроитин, амитриптилин НCl, сульфадиазин, оксикодон HCl/ацетаминофен, олопатадин HCl мисопростол, напроксен натрий, омепразол, циклофосфамид, ритуксимаб, IL-1 TRAP, MRA, CTLA4-IG, IL-18 BP, анти-IL-12, анти-IL15, BIRB-796, SClO-469, VX-702, AMG-548, VX-740, рофлумиласт, IC-485, CDC-801, S1P1 агонисты (такие как FTY720), ингибиторы PKC семейства (такие как рубоксистаурин или AEB-071) и мезопрам. В конкретных вариантах осуществления, сочетания включают метотрексат или лефлуномид и в случаях умеренного или тяжелого ревматоидного артрита циклоспорин и анти-TNF антитела, как указано выше.
Неограничительные примеры терапевтических агентов против воспалительной болезни кишечника, с которыми соединения формулы (I) по изобретению могут быть совместно введены, включают следующие: буденозид, эпидермальный фактор роста, кортикостероиды, циклоспорин, сульфасалазин, аминосалицилаты, 6-меркаптопурин, азатиоприн, метронидазол, ингибиторы липоксигеназы, месаламин, олсалазин, балсалазид, антиоксиданты, ингибиторы тромбоксана, антагонисты IL-1 рецептора, анти-IL-1 моноклональные антитела, анти-IL-6 моноклональные антитела, факторы роста, ингибиторы эластазы, соединения пиридинил-имидазол, антитела к или антагонисты других цитокинов или факторов роста человека, например, TNF, LT, IL-1, IL-2, IL-6, IL-7, IL-8, IL-12, IL-15, IL-16, IL-23, EMAP-II, GM-CSF, FGF и PDGF; молекулы поверхности клетки, такие как CD2, CD3, CD4, CD8, CD25, CD28, CD30, CD40, CD45, CD69, CD90 или их лиганды; метотрексат; циклоспорин; FK506; рапамицин; микофенолят мофетил; лефлуномид; NSAIDs, например, ибупрофен; кортикостероиды, такие как преднизолон; ингибиторы фосфодиэстеразы; агонисты аденозина; антитромботические агенты; ингибиторы комплемента; адренергические агенты; агенты, которые мешают передаче сигналов провоспалительными цитокинами, такие как TNF или IL-1 (например, ингибиторы киназы NIK, IKK или MAP); ингибиторы IL-1 превращающего фермента; ингибиторы TNF превращающего фермента; Ингибиторы передачи сигналов Т-клеток, такие как ингибиторы киназы; ингибиторы металлопротеиназы; сульфасалазин; азатиоприн; 6-меркаптопурины; ингибиторы ангиотензин превращающего фермента; рецепторы растворимого цитокина и их производные (например, рецептор растворимого p55 или p75 TNF, sIL-1RI, sIL-1RII, sIL-6R) и противовоспалительные цитокины (например, IL-4, IL-10, IL-11, IL-13 и TGF). Предпочтительные примеры терапевтических агентов против болезни Крона, с которыми соединение формулы (I) может быть объединено, включают следующие: TNF антагонисты, например, анти-TNF антитела, D2E7 (адалимубаб), CA2 (инфликсимаб), CDP 571, конструкты TNFR-Ig, ингибиторы (p75TNFRIgG (этанерцепт) и p55TNFRIgG (LENERCEPT™) и ингибиторы PDE4. Соединение формулы (I) может быть объединено с кортикостероидами, например, буденозидом и дексаметазоном, с сульфасалазином, 5-аминосалициловой кислотой, олсалазином и агентами, которые влияют на синтез или действие провоспалительных цитокинов, такими как IL-1, например, ингибиторы IL-1 превращающего фермента и IL-1ra; ингибиторы передачи сигналов Т клеток, например, ингибиторы тирозин киназы; 6-меркаптопурин; IL-11; месаламин; преднизон; азатиоприн; меркаптопурин; инфликсимаб; метилпреднизолон натрий сукцинат; дифеноксилат/атроп сульфат; лоперамид гидрохлорид; метотрексат; омепразол; фолат; ципрофлоксацин/декстроза-вода; гидрокодон витартрат/апап; тетрациклин гидрохлорид; флуоцинонид; метронидазол; тимеросал/борная кислота; холестирамин/сахароза; ципрофлоксацин гидрохлорид; хиосциамин сульфат; меперидин гидрохлорид; мидазолам гидрохлорид; оксикодон HCl/ацетаминофен; прометазин гидрохлорид; фосфат натрия; сульфаметоксазол/триметоприм; целекоксиб; поликарбофил; пропоксифен напсилат; гидрокортизон; поливитамины; балсалазид динатрий; кодеин фосфат/апап; колесевелам HCl; цианокобаламин; фолиевая кислота; левофлоксацин; метилпреднизолон; натализумаб и интерферон-гамма.
Неограничительные примеры терапевтических агентов против рассеянного склероза, с которыми соединение формулы (I) может быть совместно введено, включают следующее: кортикостероиды; преднизолон; метилпреднизолон; азатиоприн; циклофосфамид; циклоспорин; метотрексат; 4-аминопиридин; тизанидин; интерферон-1a (AVONEX®; Biogen); интерферон-1b (BETASERON®; Chiron/Berlex); интерферон-n3) (Интерферон Sciences/Fujimoto), интерферон- (Alfa Wassermann/J&J), интерферон 1A-IF (Serono/Inhale Therapeutics), пегинтерферон 2b (Enzon/Schering-Plough), coполимер 1 (Cop-1; COPAXONE®; Teva Pharmaceutic Industries, Inc.); гипербарический кислород; внутривенный иммуноглобулин; кладрибин; антитела к или антагонисты других цитокинов человека или факторов роста и их рецепторов, например, TNF, LT, IL-1, IL-2, IL-6, IL-7, IL-8, IL-12, IL-23, IL-15, IL-16, EMAP-II, GM-CSF, FGF и PDGF. Соединение формулы (I) может быть объединено с антителами к молекулам поверхности клетки, такими как CD2, CD3, CD4, CD8, CD 19, CD20, CD25, CD28, CD30, CD40, CD45, CD69, CD80, CD86, CD90 или их лиганды. Соединение формулы (I) может быть также объединено с агентами, такими как метотрексат, циклоспорин, FK506, рапамицин, микофенолят мофетил, лефлуномид, S1P1 агонист, NSAIDs, например, ибупрофен, кортикостероид, такие как преднизолон, ингибиторы фосфодиэстеразы, агонисты аденозина, антитромботические агенты, ингибиторы комплемента, адренергические агенты, агенты, которые мешают передаче сигналов провоспалительных цитокинов, такие как TNF или IL-1 (например, NIK, IKK, p38 или ингибиторы MAP киназы), ингибиторы IL-1 превращающего фермента, TACE ингибиторы, ингибиторы передачи сигналов T-клеток, такие как ингибиторы киназы, ингибиторы металлопротеиназы, сульфасалазин, азатиоприн, 6-меркаптопурины, ингибиторы ангиотензин превращающего фермента, рецепторы растворимого цитокина и их производные (например, рецепторы растворимого p55 или p75 TNF, sIL-1RI, sIL-1RII, sIL-6R) и противовоспалительные цитокины (например, IL-4, IL-10, IL-13 и TGF).
Соединение формулы (I) может быть также совместно введено с агентами, такими как алемтузумаб, дронабинол, даклизумаб, митоксантрон, халипроден гидрохлорид, фампридин, глатирамер ацетат, натализумаб, синнабидол, -иммунокин NNSО3, ABR-215062, AnergiX.MS, антагонисты рецептора хемокина, BBR-2778, калагуалин, CPI-1189, 1eM (липосомный инкапсулированный митоксантрон), THC.CBD (агонист каннабиоида), MBP-8298, мезопрам (PDE4 ингибитор), MNA-715, антитело анти-IL-6 рецептора, неуровакс, пирфенидон аллотрап 1258 (RDP-1258), sTNF-Rl, талампанел, терифлуномид, TGF-бета2, типлимотилид, VLA-4 антагонисты (например, TR-14035, VLA4 Ultrahaler, Antegran-ELAN/Biogen), антагонисты интерферона гамма и IL-4 агонисты.
Неограничительные примеры терапевтических агентов против анкилозирующего спондилоартрита, с которыми соединение формулы (I) может быть совместно введено, включают следующее: ибупрофен, диклофенак, мисопростол, напроксен, мелоксикам, индометацин, диклофенак, целекоксиб, рофесоксиб, сульфасалазин, метотрексат, азатиоприн, миносиклин, преднизон и анти-TNF антитела, D2E7 (HUMIRA®), CA2 (инфликсимаб), CDP 571, TNFR-Ig конструкты, (p75TNFRIgG (ENBREL®) и p55TNFRIgG (LENERCEPT®).
Неограничительные примеры терапевтических агентов против астмы, с которыми соединение формулы (I) может быть совместно введено, включают следующее: албутерол, салметерол/флутикасон, монтелукаст натрий, флутикасон пропионат, будесонид, преднизон, салметерол ксинафоат, левалбутерол HCl, албутерол сульфат/ипратропиум, преднизолон натрий фосфат, триамцинолон ацетонид, беклометазон дипропионат, ипратропиум бромид, азитромицин, пирбутерол ацетат, преднизолон, теофиллин безводный, метилпреднизолон натрий сукцинат, кларитромицин, зафирлукаст, формотерол фумарат, вакцина вируса гриппа, амоксициллин тригидрат, фланизолид, аллергическая инъекция, кромолин натрий, фексофенадин гидрохлорид, фланизолид/ментол, амоксициллин/клавуналат, левофлоксацин, устройство для ингаляции, гуаифенезин, дексаметазон натрий фосфат, моксифлоксацин HCl, доксициклин гиклат, гуаифенезин/d-меторфан, p-эфедрин/код/хлорфенир, гатифлоксацин, цетиризин гидрохлорид, мометазон фуроат, салметерол ксинафоат, бензонатат, цефалексин, пe/гидрокодон/хлорфенир, цетиризин HCl/псевдоэфед, фенилэфрин/код/прометазин, кодеин/прометазин, цефпрозил, дексаметазон, гуаифенезин/псевдоэфедрин, хлорфенирамин/гидрокодон, недокромил натрий, тербуталин сульфат, эпинефрин, метилпреднизолон, анти-IL-13 антитело и метапротеренол сульфат.
Неограничительные примеры терапевтических агентов против COPD, с которыми соединение формулы (I) может быть совместно введено, включают следующее: албутерол сульфат/ипратропиум, ипратропиум бромид, салметерол/флутикасон, албутерол, салметерол ксинафоат, флутикасон пропионат, преднизон, теофиллин безводный, метилпреднизолон натрий сукцинат, монтелукаст натрий, будесонид, формотерол фумарат, триамцинолон ацетонид, левофлоксацин, гуаифенезин, азитромицин, беклометазон дипропионат, левалбутерол HCl, фланизолид, цефтриаксон натрий, амоксициллин тригидрат, гатифлоксацин, зафирлукаст, амоксициллин/клавуналат, фланизолид/ментол, хлорфенирамин/гидрокодон, метапротеренол сульфат, метилпреднизолон, мометазон фуроат, p-эфедрин/код/хлорфенир, пирбутерол ацетат, p-эфедрин/лоратадин, тербуталин сульфат, тиотропиум бромид, (R,R)-формотерол, TgAAT, Силомиласт и рофлимуласт.
Неограничительные примеры терапевтических агентов против псориаза, с которыми соединение формулы (I) может быть совместно введено, включают следующее: кальципотриен, Клобетазол пропионат, триамцинолон ацетонид, галобетазол пропионат, тазаротен, метотрексат, флуоцинонид, бетаметазон дипроп-дополненный, флуоцинолон ацетонид, ацитретин, дегтярный шампунь, бетаметазон валерат, мометазон фуроат, кетоконазол, прамоксин/флуоцинолон, гидрокортизон валерат, флурандренолид, мочевина, бетаметазон, клобетазол пропионат/эмолл, флутикасон пропионат, азитромицин, гидрокортизон, увлажняющий состав, фолиевая кислота, десонид, пимекролимус, деготь, дифлоразон диацетат, этанерцепт фолат, молочная кислота, метоксален, hc/висмут субгал/знокс/ресор, метилпреднизолон ацетат, преднизон, средство для защиты от солнечного света, галцинонид, салициловая кислота, антралин, клокорталон пивалат, угольный экстракт, деготь/салициловая кислота, деготь/салициловая кислота/сера, дезоксиметазон, диазепам, увлажнитель, флуоцинонид/увлажнитель, минеральное масло/касторовое масло/na lact, минеральное масло/арахисовое масло, нефть/изопропил миристат, псорален, салициловая кислота, мыло/трибромсалан, тимеросал/борная кислота, целекоксиб, инфликсимаб, циклоспорин, алефасепт, эфализумаб, такролимус, пимекролимус, PUVA, UVB, сульфасалазин, ABT-874 и устекинамаб.
Неограничительные примеры терапевтических агентов против псориатического артрита, с которыми соединение формулы (I) может быть совместно введено, включают следующее: метотрексат, этанерцепт, рофесоксиб, целекоксиб, фолиевую кислоту, сульфасалазин, напроксен, лефлуномид, метилпреднизолон ацетат, индометацин, гидроксихлорквин сульфат, преднизон, сулиндак, бетаметазон дипроп-дополненный, инфликсимаб, метотрексат, фолат, триамцинолон ацетонид, диклофенак, диметилсульфоксид, пироксикам, диклофенак натрий, кетопрофен, мелоксикам, метилпреднизолон, набуметон, толметин натрий, кальципотриен, циклоспорин, диклофенак натрий/мисопростол, флуоцинонид, глюкозамин сульфат, тиомалат золота натрия, гидрокодон витартрат/апап, ибупрофен, риседронат натрий, сульфадиазин, тиогуанин, валдекоксиб, алефацепт, D2E7 (адалимумаб) и эфализумаб.
Предпочтительные примеры терапевтических агентов протиа SLE (волчанки), с которыми соединение формулы (I) может быть совместно введено, включают следующее: NSAIDs, например, диклофенак, напроксен, ибупрофен, пироксикам, индометацин; COX2 ингибиторы, например, целекоксиб, рофесоксиб, валдекоксиб; антималярийные средства, например, гидроксихлорхин; стероиды, например, преднизон, преднизолон, буденозид, дексаметазон; цитотоксичные средства, например, азатиоприн, циклофосфамид, микофенолят мофетил, метотрексат; ингибиторы PDE4 или ингибитор синтеза пурина, например, Cellcept®. Соединение формулы (I) может быть также объединено с агентами, такими как сульфасалазин, 5-аминосалициловая кислота, олсалазин, Imuran® и агенты, которые мешают синтезу, продуцированию или действию провоспалительных цитокинов, такие как IL-1, например, ингибиторы капсазы типа ингибиторов IL-1 превращающего фермента и IL-1ra. Соединение формулы (I) может быть также использовано ингибиторами передачи сигналов Т-клеток, например, ингибиторами тирозин киназы; или молекулами, которые нацелины на молекулы активации T клеток, например, CTLA-4-IgG или антитела анти-B7 семейства, антитела анти-PD-1 семейства. Соединение формулы (I) может быть объединено с IL-11 или анти-цитокиновыми антителами, например, фонотолизумабом (анти-IFNg антитело), или антителами анти-рецептор рецептора, например, антитело анти-IL-6 рецептора и антитела к молекулам поверхности B-клеток. Соединение формулы (I) может быть также использовано с LJP 394 (абетимус), агентами, которые уменьшают количество или инактивируют В-клетки, например, Rituximab (анти-CD20 антитело), лимфостат-B (анти-BlyS антитело), TNF антагонисты, например, анти-TNF антитела, D2E7 (адалимумаб), CA2 (инфликсимаб), конструкты CDP 571, TNFR-Ig, (p75TNFRIgG (этанерцепт) и p55TNFRIgG (LENERCEPT™).
Соединения по изобретению могут быть также совместно введены с терапевтически эффективным количеством одного или нескольких агентов, используемых для профилактики или лечения СПИД, примеры таких агентов включают ингибиторы обратимой транскриптазы ВИЧ, ингибиторы протеазы ВИЧ, иммуномодуляторы и дрцгие ретровирусные лекарства. Примеры ингибиторов обратимой транскриптазы включают, но без ограничения указанным, абакавир, адефовир, диданозин, производные дипивоксила, эфавиренц, эмтрицитабин, ламивудин, невирапин, рилпивирин, ставудин, тенофувир, залцитабин и зидовидин. Примеры ингибиторов протеазы включают, но без ограничения указанным, ампренавир, атазанавир, дарунавир, индинавир, фозампренавир, лопинавир, нелфмнавир, ритонавир, сакьюнавир и типранавир. Примеры других ретровирусных лекарств включают, но без ограничения указанным, элвитегавир, энфувиртид, маравирос и ралтегравир.
Соединения по изобретению могут быть совместно введены стерапевтически эффективным количеством одного или нескольких агентов для профилактики или лечения диабета типа II, ожирения печени, резистентности к инсулину, метаболического синдрома и подобных расстройств, примеры таких агентов включают, но без ограничения указанным, инсилин и инсилины, которые модифицированы для усовершенствования продолжительности действия в организме, агенты, которые стимулируют секрецию инсилина, такие как ацетoгексамид, хлорпропамид, глибурид, глимепирид, глипизид, гликазид, гликопирамид, глиеквидон, рапаглинид, натаглинид, толазамид и толбутамид; агенты, которые являются агонистами глюкагон-подобного пептида, такие как эксанатид, лираглтид и таспоглютид; агенты, которые ингибируют дипептидил-пептидазу IV, такие как вилдаглитин, ситаглитин, саксаглитин, линаглитин, аллоглитин и септаглитин; агенты, которые связываются с пероксисомным пролифератор-активирующим рецептором гамма, такие как розиглитазон и пиоглитазон; агенты, которые уменьшают резистентность к инсулину, такие как метформин; агенты, которые уменьшают абсорбируемость глюкозы в тонком кишечнике, такие как aкарбоза, миглитол и воглибоза.
Соединения по изобретению могут быть совместно введены с терапевтически эффективным количеством одного или нескольких агентов для профилактики или лечения острых почечных расстройств и хронических почечных болезней, примеры таких агентов включают, но без ограничения указанным, допамин, диуретики, такие как фуросемид, буметанид, тиазид и тому подобное, маннит, глюконат кальция, бикарбонат натрия, албутерол, парикальцитол, доксеркальциферол, цинакальцет и бардоксалон метил.
Соединения по изобретению могут быть совместно введены с терапевтически эффективным количеством одного или нескольких агентов субъекту мужского рода для обеспечения мужской контрацепции.
Следующие примеры могут быть использованы для пояснения и не должны рассматриваться как сужающие объем изобретения.
Примеры
Пример 1
6-метил-4-(2-феноксифенил)-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 1a
(E)-2-(5-бром-2-метокси-3-нитропиридин-4-ил)-N,N-диметилэтенамин
5-Бром-2-метокси-4-метил-3-нитропиридин (15,0 г, 60,7 ммоль) растворяли в диметилформамиде (300 мл) и добавляли метанолят лития (6,07 мл, 6,07 ммоль, 1 M). Реакционную смесь нагревали до 100°C. К этой смеси добавляли 1,1-диметокси-N,N-диметилметанамин (64,5 мл, 486 ммоль) в течение 10 минут. Реакционную смесь перемешивали при 95°C втечение 16 часов. Реакционную смесь охлаждали до комнатной температуры и добавляли воду осторожно (300 мл, экзотермическая). Полученный осадок собирали вакуумным фильтрованием, промывали водой и сушили, получая указанное в заголовке соединение (13,9 г, 45,9 ммоль, выход 76%).
Пример 1b
4-бром-7-метокси-1H-пирроло[2,3-c]пиридин
Продукт примера 1a (13,9 г, 45,8 ммоль) и этил ацетат (150 мл) добавляли к Ra-Ni 2800 (предварительно промытому этанолом), водную суспензию (6,9 г, 118 ммоль) в работающем под давлением сосуде из нержавеющей стали и перемешивали в течение 30 минут при 30 фунтах на кв.дюйм и комнатной температуре. Реакционную смесь фильтровали и концентрировали. Остаток растирали с дихлорметаном и твердое вещество отфильтровывали, получая указанное в заголовке соединение (5,82 г). Маточную жидкость выпаривали и остаток растирали снова с дихлорметаном и фильтровали, получая дополнительно 1,63 г указанного в заголовке соединения. Общий выход=7,45 г, выход 72%.
Пример 1c
4-бром-7-метокси-1-тозил-1H-пирроло[2,3-c]пиридин
Раствор продукта примера 1b (7,42 г, 32,7 ммоль) в диметилформамиде (235 мл) перемешивали при комнатной температуре. К этому раствору добавляли гидрид натрия (1,18 г, 1,96 г 60% дисперсии в масле, 49,0 ммоль) и реакционную смесь перемешивали в течение 10 мин. П-толуолсульфонил хлорид (9,35 г, 49,0 ммоль) затем добавляли порциями и смесь перемешивали при комнатной температуре в атмосфере азота в течение 16 часов. Реакционную смесь осторожно гасили водой и полученное бежевое твердое вещество собирали вакуумным фильтрованием на воронке Бюхнера и промывали водой. Твердое вещество собирали и сушили в вакуумной печи при 50°C, получая 12,4 г (100%) указанного в заголовке соединения.
Пример 1d
4-бром-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Раствор продукта примера 1c (12,4 г, 32,6 ммоль) в диоксане (140 мл) перемешивали при комнатной температуре. К этому раствору добавляли 4M HCl в диоксане (140 мл). Реакционную смесь перемешивали при 40°C в течение 16 часов. Реакционную смесь охлаждали до комнатной температуры и концентрировали. Остаток растирали с простым диэтиловым эфиром, фильтровали и промывали дополнительным простым диэтиловым эфиром и сушили, получая указанное в заголовке соединение (11,23 г, 30,6 ммоль, выход 94%) в виде бежевого твердого вещества.
Пример 1e
4-бром-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Гидрид натрия (0,875 г, 36,5 ммоль, 1,46 г 60% в масляной дисперсии) добавляли к перемешиваемому раствору продукта примера 1d (11,2 г, 30,4 ммоль) в диметилформамиде (217 мл) в атмосфере азота. Через 30 минут добавляли йодметан (2,27 мл, 36,5 ммоль) и раствор перемешивали при комнатной температуре в течение 3 ч. После добавления воды (250 мл) образовывася осадок. Осадок собирали вакуумным фильтрованием, промывали водой (50 мл) и сушили в вакуумной печи при 55°C в течение ночи, получая 11,2 г указанного в заголовке соединения (96%).
Пример 1f
6-метил-4-(2-феноксифенил)-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Смесь продукта примера 1e (152 мг, 0,40 ммоль), 2-феноксифенилбороновой кислоты (0,111 г, 0,520 ммоль, 1,3 эквивалента), Pd(PPh3)4 (0,023 г, 5 мол.%) и фторида цезия (0,182 г, 1,2 ммоль) в DME (3 мл) и метаноле (1,5 мл) нагревали микроволновым излучением (120°C, 30 минут). К этой смеси добавляли карбонат калия (0,055 г, 0,40 ммоль) и воду (1 мл) и реакционную смесь повторно нагревали в микроволновой печи при 120°C в течение еще 2 часов. Органический слой отделяли и очищали флаш-хроматографией (силикагель, этилацетат). Полученный материал растирали с ацетоном и фильтровали, получая 0,075 г указанного в заголовке соединения (59%). 1H ЯМР (500 МГц, DMSO-d6) δ 3,50 (с, 3H), 6,21-6,23 (м, 1H), 6,88 (д, J=7,62 Гц, 2H), 6,99-7,04 (м, 2H), 7,24-7,30 (м, 5H), 7,36-7,40 (м, 1H), 7,50 (дд, J=7,48, 1,68 Гц, 1H), 11,98 (с, 1H). MS (ESI+) m/z 317 (M+H)+.
Пример 2
6-метил-4-(5-нитро-2-феноксифенил)-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 2a
4-(2-фтор-5-нитрофенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Способ A:
Продукт примера 1e (0,687 г, 1,802 ммоль), 2-фтор-5-нитрофенилбороновую кислоту (0,500 г, 2,70 ммоль), Pd(PPh3)4 (0,104 г, 0,090 ммоль) и карбонат натрия (2,70 мл, 5,41 ммоль) объединяли в DME (7 мл) и воде (7 мл) в 20 мл пробирке для микроволнового нагрева, уплотняли, продували азотом и нагревали микроволновым излучением при 120°C в течение 30 минут. Смесь распределяли между EtAOc и водой. Органический слой промывали насыщенным раствором соли, сушили (Na2SО4), фильтровали и концентрировали. Сырой продукт очищали флаш-хроматографией (силикагель, 0-100% этилацетат в гексанах), получая 0,41 г (52%) указанного в заголовке соединения.
Способ B:
Продукт примера 1e (6,00 г, 15,7 ммоль), 2-фтор-5-нитрофенилбороновую кислоту (5,82 г, 31,5 ммоль), Pd(PPh3)4 (0,909 г, 0,787 ммоль) и карбонат натрия (3,34 г, 31,5 ммоль) объединяли в толуоле (60 мл), этаноле (15 мл) и воде (15 мл) и смесь дегазировали и оставляли в атмосфере азота. Реакционную смесь нагревали при 90°C в течение ночи и затем охлаждали до комнатной температуры. Смесь распределяли между этилацетатом и водой. Органический слой промывали насыщенным раствором соли, сушили (MgSО4), фильтровали и концентрировали. Сырой продукт очищали флаш-хроматографией (силикагель, 20-50% этилацетат в гексанах), получая 6,95 г (61%) указанного в заголовке соединения.
Пример 2b
6-метил-4-(5-нитро-2-феноксифенил)-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Фенол (0,094 г, 0,997 ммоль), продукт примера 2a (0,4 г, 0,906 ммоль) и карбонат цезия (0,325 г, 0,997 ммоль) объединяли в DMSO (4,53 мл) и нагревали при 100°C в течение 2 часов. Реакционную смесь распределяли между этилацетатом и водой и pH доводили до pH 7. Органический слой промывали насыщенным раствором соли, сушили (Na2SО4), фильтровали и концентрировали. Очистка флаш-хроматографией (силикагель, 0-4% метанол в дихлорметане) давала 0,28 г (84%) указанного в заголовке соединения. 1H ЯМР (300 МГц, DMSO-d6) δ 3,57 (с, 3H) 6,28-6,34 (м, 1H) 6,98 (д, J=9,12 Гц, 1H) 7,16 (д, J=7,54 Гц, 2H) 7,21-7,32 (м, 2H) 7,40-7,49 (м, 3H) 8,22 (дд, J=9,12, 2,78 Гц, 1H) 8,32 (д, J=2,78 Гц, 1H) 12,07-12,11 (м, 1H). MS (ESI+) m/z 362 [M+H]+
Пример 3
4-(5-амино-2-феноксифенил)-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 2b (0,25 г, 0,692 ммоль), порошок железа (0,193 г, 3,46 ммоль) и аммоний хлорид (0,056 г, 1,038 ммоль) объединяли в тетрагидрофуране (6 мл), этаноле (6 мл) и воде (2 мл). Смесь нагревали при 95°C при энергичном перемешивании в течение 1,5 часа. Реакционную смесь охлаждали до комнатной температуры и фильтровали через прокладку из целита, чтобы удалить твердые вещества. Прокладку промывали повторно метанолом и тетрагидрофураном. Фильтрат концентрировали и остаток распределяли между этилацетатом и водой. Слой этилацетата промывали насыщенным раствором соли, сушили (Na2SO4), фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 1-4% метанол в дихлорметане), получая 0,21 г (82%) указанного в заголовке соединения. 1H ЯМР (300 МГц, DMSO-d6) δ 3,43 (с, 3H) 5,07 (с, 2H) 6,22-6,25 (м, 1H) 6,59 (дд, J=8,48, 2,71 Гц, 1H) 6,68 (д, J=7,80 Гц, 2H) 6,74 (д, J=2,71 Гц, 1H) 6,80-6,88 (м, 2H) 7,11-7,19 (м, 3H) 7,24 (т, J=2,71 Гц, 1H) 11,91 (с, 1H). MS (ESI+) m/z 362 [M+H]+.
Пример 4
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]метансульфонамид
Способ A:
К раствору продукта примера 3 (0,125 г, 0,377 ммоль) и триэтиламина (0,131 мл, 0,943 ммоль) в дихлорметане (3,0 мл) добавляли по каплям метансульфонил хлорид (0,064 мл, 0,830 ммоль). Реакционную смесь перемешивали в течение 2 часов при температуре окружающей среды и затем концентрировали. Остаток растворяли в смеси диоксана (5 мл) и 1M гидроксида натрия (2 мл) и нагревали в течение 1 часа при 90°C. Реакционную смесь охлаждали и разбавляли этилацетатом, доводили до pH 7 с помощью 1M HCl и распределяли. Органический слой промывали насыщенным раствором соли, сушили (Na2SО4), фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 0-4% метанол в дихлорметане), получая 0,20 г (77%) указанного в заголовке соединения. 1H ЯМР (300 МГц, DMSO-d6) δ 3,02 (с, 3H) 3,48 (с, 3H) 6,23-6,30 (м, 1H) 6,85 (д, J=7,46 Гц, 2H) 6,99 (т, J=7,29 Гц, 1H) 7,04 (д, J=8,82 Гц, 1H) 7,20-7,29 (м, 5H) 7,39 (д, J=2,71 Гц, 1H) 9,72 (с, 1H) 12,01 (с, 1H). MS (ESI+) m/z 410 [M+H]+.
Способ B:
Продукт примера 7d (1,127 г, 2 ммоль), гидроксид калия (1,82 г, 52,5 ммоль) и бромид цетилтриметиламмония (0,036 г, 0,100 ммоль) объединяли в тетрагидрофуране (15,00 мл) и воде (5,00 мл) и смесь нагревали при 100°C в течение 14 часов. Реакционную смесь распределяли между равными объемами EtOAc и воды и pH доводили до pH 7 осторожным добавлением концентрированной HCl. Органический слой отделяли, промывали три раза насыщенным раствором соли, сушили (Na2SO4) и концентрировали. Очистка растиранием в порошок в дихлорметане давала указанное в заголовке соединение (0,76 г, 93%).
Пример 5
2,2,2-трифтор-N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]этансульфонамид
К раствору продукта примера 3 (0,05 г, 0,151 ммоль) и триэтиламина (0,053 мл, 0,377 ммоль) в дихлорметане (1,0 мл) добавляли по каплям 2,2,2-трифторэтансульфонил хлорид (0,036 г, 0,196 ммоль). Реакционную смесь перемешивали в течение 1 часа при комнатной температуре и затем очищали флаш-хроматографией (силикагель, 0-5% метанол в дихлорметане), получая 0,050 г (68%) указанного в заголовке соединения. 1H ЯМР (300 МГц, DMSO-d6) δ 3,49 (с, 3H) 4,55 (кв., J=9,91 Гц, 2H) 6,28 (т, J=2,38 Гц, 1H) 6,86 (д, J=7,54 Гц, 2H) 6,95-7,07 (м, 2H) 7,20-7,31 (м, 5H) 7,40 (д, J=2,78 Гц, 1H) 10,43 (с, 1H) 12,02 (с, 1H), MS (APCI+) m/z 478 [M+H]+.
Пример 6
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]ацетамид
Пример 6a
6-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 1e (6,55 г, 17,2 ммоль), 4,4,4',4',5,5,5',5'-октаметил-2,2'-би(1,3,2-диоксаборолан) (8,73 г, 34,4 ммоль), ацетат калия (3,71 г, 37,8 ммоль), трис(дибензилиденацетон)дипалладий(0) (0,393 г, 0,430 ммоль) и 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (X-PHOS, 0,819 г, 1,72 ммоль) объединяли и продували аргоном в течение 1 часа при перемешивании. Диоксан (86 мл) продували азотом в течение 1 часа, подавали через канюлю в атмосфере азота к твердым компонентам и смесь нагревали в атмосфере аргона при 80°C в течение 5 часов. Реакционную смесь охлаждали до комнатной температуры, распределяли между этилацетатом и водой и фильтровали через целит. Слой этилацетата промывали дважды насыщенным раствором соли, сушили (Na2SO4), фильтровали и концентрировали. Остаток очищали хроматографией (силикагель, 25-80% этилацетат в гексане). Полученный материал после хроматографии растирали с минимальным количеством гексанов (30 мл) и частицы твердого вещества собирали фильтрованием, промывали минимальным количеством гексанов и сушили до постоянной массы, получая указанное в заголовке соединение (5,4 г, 73%).
Пример 6b
N-(3-бром-4-феноксифенил)ацетамид
Продукт примера 7b (0,2 г, 0,757 ммоль) и уксусный ангидрид (1 мл, 10,60 ммоль) объединяли в 5 мл пробирке для микроволнового нагрева, уплотняли и нагревали микроволновым излучением при 100°C в течение 30 минут. Смесь концентрировали и остаток очищали хроматографией (силикагель, 0-50% этилацетат в гексанах), получая указанное в заголовке соединение (0,22 г, 95%).
Пример 6c
N-(3-(6-метил-7-оксо-1-тозил-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил)ацетамид
Продукт примера 6a (0,07 г, 0,163 ммоль), продукт примера 6b (0,075 г, 0,245 ммоль), тетракис(трифенилфосфин)палладий(0) (9,44 мг, 8,17 мкмоль) и карбонат натрия (2,0 M, 0,245 мл, 0,490 ммоль) объединяли в DME (0,817 мл) и воде (0,817 мл) в 5 мл пробирке для микроволнового нагрева, уплотняли, продували азотом и нагревали микроволновым излучением при 120°C в течение 30 минут. Смесь распределяли между этилацетатом и водой. Органический слой промывали насыщенным раствором соли, сушили (Na2SO4), фильтровали и концентрировали. Очистка хроматографией (силикагель, 0-5% метанол в дихлорметане) давала указанное в заголовке соединение (0,048 г, 56%).
Пример 6d
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]ацетамид
Продукт примера 6c (0,048 г, 0,091 ммоль) и карбонат калия (0,044 г, 0,318 ммоль) объединяли в метаноле (2 мл) и воде (0,200 мл) в 2 мл пробирке для микроволнового нагрева, уплотняли и нагревали микроволновым излучением при 110°C в течение 30 минут. Реакционную смесь концентрировали и остаток распределяли между этилацетатом и водой, доводя pH до 6 с помощью 1M HCl. Органический слой отделяли и концентрировали. Очистка флаш-хроматографией (силикагель, 0-4% метанол в дихлорметане) давала 0,018 г (53%) указанного в заголовке соединения. 1H ЯМР (300 МГц, DMSO-d6) δ 2,05 (с, 3H) 3,48 (с, 3H) 6,25-6,30 (м, 1H) 6,80 (д, J=7,46 Гц, 2H) 6,96 (т, J=7,29 Гц, 1H) 7,01 (д, J=8,82 Гц, 1H) 7,18-7,31 (м, 4H) 7,56 (дд, J=8,65, 2,54 Гц, 1H) 7,79 (д, J=2,71 Гц, 1H) 10,04 (с, 1H) 11,97 (с, 1H). MS (ESI+) m/z 374 [M+H]+.
Пример 7
N-(3-{6-метил-1-[(4-метилфенил)сульфонил]-7-оксо-6,7-дигидро-1H-пирроло[2,3–c]пиридин-4-ил}-4-феноксифенил)метансульфонамид
Пример 7a
2-бром-4-нитро-1-феноксибензол
2-Бром-1-фтор-4-нитробензол (2,5 г, 11,4 ммоль), фенол (1,28 г, 13,6 ммоль) и карбонат цезия (4,44 г, 13,6 ммоль) объединяли в диметилсульфоксиде (140 мл) и нагревали до 110°C в течение 1 часа. Реакционную смесь распределяли между этилацетатом и насыщенным раствором соли. Объединенные органические вещества промывали насыщенным раствором соли, сушили (MgSO4), фильтровали и концентрировали, получая указанное в заголовке соединение.
Пример 7b
3-бром-4-феноксианилин
Продукт примера 7a (3,43 г, 11,7 ммоль), порошок железа (3,26 г, 58,4 ммоль) и хлорид аммония (1,25 г, 23,4 ммоль) объединяли в этаноле (50 мл), тетрагидрофуране (50 мл) и воде (16,7 мл) и нагревали при 100°C в течение 2 часов. Реакционную смесь охлаждали до температуры чуть ниже кипения с возвращением флегмы, подвергали вакуумному фильтрованию через диатомовую землю, осадок на фильтре промывали теплым метанолом (3 × 35 мл) и фильтрат концентрировали при пониженном давлении. Остаток распределяли между насыщенным водным NaHCО3 и этилацетатом (3 × 125 мл). Объединенные органические вещества промывали насыщенным раствором соли, сушили (MgSO4), подвергали безнапорному фильтрованию, затем концентрировали, получая указанное в заголовке соединение.
Пример 7c
N-(3-бром-4-феноксифенил)метансульфонамид
Продукт примера 7b (2,86 г, 10,8 ммоль) и триэтиламин (6,03 мл, 43,3 ммоль) перемешивали в дихлорметане (48,1 мл) при температуре окружающей среды. Метансульфонил хлорид (2,53 мл, 32,4 ммоль) добавляли по каплям и раствор перемешивали при температуре окружающей среды в течение 1 часа. Реакционную смесь концентрировали при пониженном давлении, добавляли диоксан (24 мл) и гидроксид натрия (10% м/о, 12 мл, 0,427 ммоль) и раствор нагревали до 70°C в течение 1 ч. Раствор нейтрализовали до pH 7 насыщенным водным раствором NH4Cl (200 мл). Водную фазу экстрагировали этилацетатом (3 × 125 мл). Объединенные органические вещества промывали насыщенным раствором соли, сушили (MgSO4), фильтровали, затем концентрировали. Остаток очищали флаш-хроматографией (силикагель, градиент 0-25% этилацетат/гексан), получая указанное в заголовке соединение.
Пример 7d
N-(3-{6-метил-1-[(4-метилфенил)сульфонил]-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил}-4-феноксифенил)метансульфонамид
Продукт примера 6a (0,670 г, 1,564 ммоль), продукт примера 7c (0,562 г, 1,643 ммоль), трис(дибензилиденацетон)дипалладий(0) (0,036 г, 0,039 ммоль), 1,3,5,7-тетраметил-6-фенил-2,4,8-триокса-6-фосфаадамант (0,023 г, 0,078 ммоль) и трехосновный фосфат калия (1,03 г, 4,85 ммоль) объединяли и продували аргоном в течение 30 минут. Раствор 4:1 диоксан/вода (общий объем 10 мл) продували азотом в течение 30 минут и переносили шприцем в реакционный сосуд в атмосфере аргона. Реакционную смесь перемешивали при 60°C в течение 2 часов, охлаждали до комнатной температуры и распределяли между этилацетатом и водой. Органический слой промывали насыщенным раствором соли, сушили (Na2SO4), обрабатывали силикагелем, функционализованным 3-меркаптопропилом (Aldrich, 538086-100G), в течение 45 минут, фильтровали и концентрировали. Очистка хроматографией (силикагель, 20-100% этилацетат в гексанах) давала 0,68 г (74%) указанного в заголовке соединения. 1H ЯМР (300 МГц, DMSO-d6) δ 2,38 (с, 3H) 3,02 (с, 3H) 3,38 (с, 3H) 6,52 (д, J=3,39 Гц, 1H) 6,82 (д, J=7,80 Гц, 2H) 6,96-7,04 (м, 2H) 7,19-7,28 (м, 4H) 7,41 (д, J=8,14 Гц, 2H) 7,48 (с, 1H) 7,89-7,97 (м, 3H) 9,73 (с, 1H). MS (ESI+) m/z 564 [M+H]+.
Пример 8
N-метил-N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]метансульфонамид
Смесь продукта примера 7d (0,113 г, 0,2 ммоль) и карбоната калия (0,111 г, 0,800 ммоль) в метаноле (0,9 мл) и воде (0,1 мл) нагревали при 100°C в течение 1 часа. Реакционную смесь распределяли между этилацетатом и водой, доводя pH до 7. Органический слой отделяли, сушили (Na2SO4), фильтровали и концентрировали. Остаток очищали ВЭЖХ с обращенной фазой(C18, 10-100% CH3CN/вода (0,1% TFA)), получая указанное в заголовке соединение (0,012 г, 14%). 1H ЯМР (300 МГц, DMSO-d6) δ 2,99 (с, 3H) 3,27 (с, 3H) 3,51 (с, 3H) 6,27-6,32 (м, 1H) 6,93 (д, J=7,80 Гц, 2H) 6,99 (д, J=8,82 Гц, 1H) 7,03-7,10 (м, 1H) 7,25-7,34 (м, 4H) 7,40 (дд, J=8,65, 2,88 Гц, 1H) 7,55 (д, J=2,71 Гц, 1H) 12,01 (с, 1H). MS (ESI+) m/z 424 [M+H]+.
Пример 9
этил 3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензоат
Пример 9a
этил 4-фтор-3-(6-метил-7-оксо-1-тозил-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензоат
Смесь продукта примера 1e (1,33 г, 3,5 ммоль), 5-(этоксикарбонил)-2-фторфенилбороновой кислоты (1,04 г, 4,9 ммоль), Pd(PPh3)4 (0,20 г, 5 мол.%) и карбоната натрия (0,742 г, 7,0 ммоль) в толуоле (12 мл), этаноле (3 мл) и воде (3 мл) дегазировали и перемешивали в атмосфере азота. Реакционную смесь нагревали при 90°C в течение 24 часов. Реакционную смесь охлаждали до комнатной температуры и распределяли между водой и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным раствором соли, сушили над MgSO4, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 20-50% этилацетат в гексанах), получая 1,43 г (87%) указанного в заголовке соединения.
Пример 9b
этил 3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензоат
Смесь продукта примера 9a (1,43 г, 3,05 ммоль), фенола (,0344 г, 3,66 ммоль) и карбоната цезия (0,995, 3,05 ммоль) в DMSO (15 мл) нагревали при 110°C в течение 12 часов. После охлаждения до комнатной температуры реакционную смесь распределяли между водой и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным раствором соли, сушили над MgSO4, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 30-80% этилацетат/гексан), получая 0,85 г (72%) указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6) δ 1,31 (т, J=7,02 Гц, 3H), 3,55 (с, 3H), 4,32 (кв., J=7,22 Гц, 2H), 6,23 (т, J=2,29 Гц,1H), 6,97 (д, J=8,54 Гц, 1H), 7,06 (д, J=8,24 Гц, 2H), 7,17 (т, J=7,32 Гц, 1H), 7,28 (т, J=2,75 Гц, 1H), 7,36-7,51 (м, 3H), 7,94 (дд, J=8,7, 2,29 Гц, 1H), 8,04 (д, J=2,14 Гц, 1H), 12,02 (с, 1H). MS (ESI+) m/z 389,2 (M+H)+.
Пример 10
3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензойная кислота
Смесь продукта примера 9b (0,23 г, 0,59 ммоль) и гидроксида натрия (0,89 мл 2,0 M водного раствора) в диоксане (10 мл) нагревали при 60°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры и выливали в воду (100 мл). После добавления концентрированной HCl (5 мл) смесь экстрагировали этилацетатом (3 × 40 мл). Объединенные органические слои промывали насыщенным раствором соли, сушили над MgSO4, фильтровали и концентрировали, получая 0,21 г (98%) указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6) δ 3,55 (с, 3H), 6,24-6,25 (м,1H), 6,94 (д, J=8,54 Гц, 1H), 7,05 (д, J=7,63 Гц, 2H), 7,16 (т, J=7,32 Гц, 1H), 7,27 (т, J=2,9 Гц,1H), 7,35-7,40 (м, 3H), 7,92 (дд, J=8,7, 2,29 Гц, 1H), 8,04 (д, J=2,14 Гц, 1H), 12,03 (с, 1H). MS (ESI+) m/z 361,2 (M+H)+.
Пример 11
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(пиридин-3-илокси)фенил]метансульфонамид
Пример 11a
6-метил-4-(5-нитро-2-(пиридин-3-илокси)фенил)-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 11a получали согласно процедуре, используемой для получения продукта примера 2b, заменяя пиридин-3-олом фенол, получая указанное в заголовке соединение.
Пример 11b
4-(5-амино-2-(пиридин-3-илокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 11b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 11a продукт примера 2b, получая указанное в заголовке соединение.
Пример 11c
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(пиридин-3-илокси)фенил]метансульфонамид
Продукт примера 11с получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 11b продукт примера 3 и очищая препаративной ВЭЖХ (C18, 10-100% ацетoнитрила в 0,1% TFA/воде), получая TFA соль указанного в заголовке соединения. 1H ЯМР (300 МГц, DMSO-d6) δ 3,49 (с, 3H), 3,05 (с, 3H), 6,25 (дд, J=2,8, 1,9 Гц, 1H), 7,16 (д, J=8,7 Гц, 1H), 7,34-7,21 (м, 5H), 7,40 (д, J=2,6 Гц, 1H), 8,23-8,16 (м, 2H), 9,80 (с, 1H), 12,02 (ушир.с, 1H). MS (ESI+) m/z 411,1 (M+H)+.
Пример 12
6-метил-4-[2-(морфолин-4-илметил)фенил]-1,6-дигидро-7Н-пирроло[2,3-c]пиридин-7-он
Продукт примера 12 получали согласно процедуре, используемой для получения продукта примера 1f, заменяя 2-(морфолинoметил)фенилбороновой кислотой 2-феноксифенилбороновую кислоту, с последующей очисткой препаративной ВЭЖХ (C18, 10-100% ацетoнитрила в 0,1% TFA в воде), получая TFA соль указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6) δ 2,85 (ушир., 2H), 3,09 (ушир., 2H), 3,56 (с, 3H), 3,74 (ушир., 2H), 4,26 (ушир., 2H), 5,89-5,90 (м, 1H), 7,20 (с, 1H), 7,29 (т, J=2,75 Гц, 1H), 7,39-7,43 (м, 1H), 7,53-7,55 (м, 2H), 7,75-7,77 (м, 1H),9,73 (ушир., 1H), 12,12 (с, 1H). MS (ESI+) m/z 324,0 (M+H)+.
Пример 13
N-этил-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензамид
Пример 13a
3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензоил хлорид
Раствор продукта примера 10 (0,24 г, 0,67 ммоль) в дихлорметане (10 мл) обрабатывали оксалил хлоридом (0,17 г, 1,33 ммоль) и диметилформамидом (5 мг, 10 мол.%). Реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Растворитель удаляли при пониженном давлении, получая указанное в заголовке соединение (0,25 г, количественный).
Пример 13b
N-этил-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензамид
Раствор продукта примера 13a (0,040 г, 0,11 ммоль) в тетрагидрофуране (1 мл) обрабатывали этиламином (0,21 мл 2M раствора в тетрагидрофуране, 0,42 ммоль) в течение 2 ч. Реакционную смесь концентрировали и остаток очищали препаративной ВЭЖХ (C18, 10-90% ацетoнитрила в 0,1% TFA в воде), получая указанное в заголовке соединение (0,025 г, 61%). 1H ЯМР (500 МГц, DMSO-d6) δ 1,12 (т, J=7,32 Гц, 3H), 3,25-3,32 (м, 2H), 3,54 (с, 3H), 6,23-6,24 (м, 1H), 6,95-6,99 (м, 3H), 7,11 (т, J=7,48 Гц, 1H), 7,27 (т, J=2,75 Гц, 1H), 7,31-7,37 (м, 3H), 7,84 (дд, J=8,54, 2,44 Гц, 1H), 7,98 (д, J=2,44 Гц, 1H), 8,46 (т, J=5,49 Гц, 1H), 11,99 (с, 1H). MS (ESI+) m/z 388,2 (M+H)+.
Пример 14
3-(6-метил-7-оксо-6,7-дигидро-1Н-пирроло[2,3-c]пиридин-4-ил)-4-фенокси-N-(тетрагидрофуран-2-илметил)бензамид
Продукт примера 14 получали согласно процедуре, используемой для получения продукта примера 13b, заменяя (тетрагидрофуран-2-ил)метанамином этиламин и дихлорметаном тетрагидрофуран, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 1,56-1,57 (м, 1H), 1,79-1,89 (м, 3H), 3,26-3,32 (м, 3H), 3,53 (с, 3H), 3,58-3,63 (м, 1H), 3,73-3,78 (м, 1H), 3,94-3,97 (м, 1H), 6,21-6,22 (м, 1H), 6,93-6,98 (м, 3H), 7,10 (т, J=7,48 Гц, 1H), 7,25 (т, J=2,9 Гц, 1H), 7,30-7,35 (м, 3H), 7,84 (дд, J=8,54, 2,44 Гц, 1H), 7,98 (д, J=2,14 Гц, 1H), 8,52 (т, J=5,8 Гц, 1H), 12,00 (с, 1H). MS (ESI+) m/z 444,2 (M+H)+.
Пример 15
N-циклопентил-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензамид
Продукт примера 15 получали согласно процедуре, используемой для получения продукта примера 13b, заменяя циклопентиламином этиламин и дихлорметаном тетрагидрофуран, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 1,49-1,66 (м, 4H), 1,65-1,69 (м, 2H), 1,85-1,91 (м, 2H), 3,54 (с, 3H), 4,20-4,26 (м, 1H), 6,20-6,22 (м, 1H), 6,95-6,98 (м,3H), 7,01 (т, J=7,32 Гц, 1H), 7,26 (т, J=2,75 Гц, 1H), 7,30-7,36 (м, 3H), 7,85 (дд, J=8,54, 2,14 Гц, 1H), 7,99 (д, J=2,44 Гц, 1H), 8,52 (т, J=5,8 Гц, 1H), 12,01 (с, 1H). MS (ESI+) m/z 428,3 (M+H)+.
Пример 16
N-(2,2-дифторэтил)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензамид
Продукт примера 16 получали согласно процедуре, используемой для получения продукта примера 13b, заменяя 2,2-дифторэтанамином этиламин и дихлорметаном тетрагидрофуран, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 3,55 (с, 3H), 3,62-3,72 (м, 3H), 5,97 (т, J=3,97 Гц, 0,25H), 6,11 (т, J=4,12 Гц, 0,5H), 6,23-6,26 (м, 1,25H), 6,98 (д, J=8,54 Гц, 1H), 7,01 (д, J=7,63 Гц, 2H), 7,13 (т, J=7,48 Гц, 1H), 7,27 (т, J=2,75 Гц, 1H), 7,33-7,36 (м, 3H), 7,88 (дд, J=8,54, 2,44 Гц, 1H), 8,03 (д, J=2,14 Гц, 1H), 8,85 (т, J=5,8 Гц, 1H), 12,03 (с, 1H). MS (ESI+) m/z 424,2 (M+H)+.
Пример 17
3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-фенокси-N-(1,3-тиазол-2-ил)бензамид
Продукт примера 17 получали согласно процедуре, используемой для получения продукта примера 13b, заменяя тиазол-2-амином этиламин и дихлорметаном тетрагидрофуран, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 3,58 (с, 3H), 6,30-6,31 (м, 1H), 6,23-6,26 (м, 1H), 6,98 (д, J=8,54 Гц, 1H), 7,07 (д, J=7,63 Гц, 2H), 7,17 (т, J=7,32 Гц, 1H), 7,27-7,29 (м, 2H), 7,38-7,42 (м, 3H), 7,56 (д, J=3,36 Гц, 1H), 8,09 (дд, J=8,55, 2,44 Гц, 1H), 8,28 (д, J=2,44 Гц, 1H), 12,04 (с, 1H), 12,61 (с, 1H). MS (ESI+) m/z 443,1 (M+H)+.
Пример 18
N-(1,1-диоксидотетрагидротиофен-3-ил)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензамид
Продукт примера 18 получали согласно процедуре, используемой для получения продукта примера 13b, заменяя 1,1-диоксидотетрагидротиен-3-иламином этиламин и дихлорметаном тетрагидрофуран, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 2,20-2,23 (м, 1H), 2,41-2,45 (м, 1H), 3,04-3,09 (м, 1H), 3,19-3,23 (м, 1H), 3,34-3,37 (м, 1H), 3,48-3,53 (м, 1H), 3,55 (с, 3H), 4,66-4,76 (м, 1H), 6,30-6,31 (м, 1H), 6,21-6,22 (м, 1H), 6,99 (дд, J=8,09, 2,59 Гц, 2H), 7,12 (т, J=7,48 Гц, 1H), 7,27 (т, J=2,75 Гц, 1H), 7,31-7,37 (м, 3H), 7,87 (дд, J=8,54, 2,14 Гц, 1H), 8,02 (д, J=2,14 Гц, 1H), 8,72 (д, J=7,02 Гц, 1H), 12,03 (с, 1H). MS (ESI+) m/z 478,2 (M+H)+.
Пример 19
3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензамид
Продукт примера 19 получали согласно процедуре, используемой для получения продукта примера 13b, заменяя водным гидроксидом аммония этиламин, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 3,54 (с, 3H), 6,23-6,24 (м, 1H), 6,94 (д, J=8,54 Гц, 1H), 6,98-7,00 (м, 2H), 7,11 (т, J=7,48 Гц, 1H), 7,26 (т, J=2,75 Гц, 1H), 7,31-7,37 (м, 4H), 7,86 (дд, J=8,54, 2,44 Гц, 1H), 7,96 (с, 1H), 8,02 (д, J=2,44 Гц, 1H), 12,01 (с, 1H). MS (ESI+) m/z 360,2 (M+H)+.
Пример 20
4-[5-(гидроксиметил)-2-феноксифенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 20a
этил 3-(6-метил-7-оксо-1-тозил-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензоат
Продукт примера 20a получали согласно процедуре, используемой для получения продукта примера 1c, заменяя продуктом примера 9b продукт примера 1b, получая указанное в заголовке соединение.
Пример 20b
4-[5-(гидроксиметил)-2-феноксифенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 20a (0,32 г, 0,59 ммоль) в тетрагидрофуране (5 мл) охлаждали до 0°C. К этому раствору добавляли 1,0 н. гидрид алюминия лития (0,59 мл, 0,59 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь гасили 2,0 н. HCl (5 мл) и затем распределяли между водой и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным раствором соли, сушили над MgSO4, фильтровали и концентрировали. Остаток очищали флаш-хроматографией на силикагеле, элюируя 50-100% этилацетатом в гексанах, получая 0,08 г (39%) указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6) δ 3,49 (с, 3H), 4,54 (д, J=5,49 Гц, 2H), 5,21 (т, J=5,8 Гц, 1H), 6,23-6,24 (м, 1H), 6,94 (д, J=7,93 Гц, 2H), 6,97-7,01 (м, 2H), 7,22-7,28 (м, 4H), 7,32 (дд, J=8,39, 2,29 Гц, 1H), 7,16 (д, J=1,83 Гц, 1H), 11,97 (с, 1H). MS (ESI+) m/z 347,3 (M+H)+.
Пример 21
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]этансульфонамид
Продукт примера 21 получали согласно процедуре, используемой в способе A примера 4, заменяя этансульфонил хлоридом метансульфонил хлорид, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 1,24 (т, J=7,3 Гц, 3H), 3,13 (кв., J=7,3 Гц, 2H), 3,48 (с, 3H), 6,26 (т, J=2,3 Гц, 1H), 6,88-6,80 (м, 2H), 7,07-6,95 (м, 2H), 7,31-7,18 (м, 5H), 7,40 (д, J=2,7 Гц, 1H), 9,79 (с, 1H), 12,02 (ушир.с, 1H). MS (ESI+) m/z 424,2 (M+H)+.
Пример 22
N,N-диметил-N'-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]серный диамид
Продукт примера 22 получали согласно процедуре, используемой в способе A примера 4, заменяя диметилсульфамоил хлоридом метансульфонил хлорид, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 2,74 (с, 6H), 3,48 (с, 3H), 6,28-6,23 (м, 1H), 6,85-6,78 (м, 2H), 7,06-6,93 (м, 2H), 7,31-7,17 (м, 5H), 7,40 (д, J=2,7 Гц, 1H), 9,91 (с, 1H), 12,04-12,00 (м, 1H). MS (ESI+) m/z 439,1 (M+H)+.
Пример 23
N-[5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-6-феноксипиридин-3-ил]метансульфонамид
Пример 23a
3-бром-5-нитро-2-феноксипиридин
Фенол (0,416 г, 4,42 ммоль), 3-бром-2-хлор-5-нитропиридин (Combi-Blocks, CAS [5470-17-7], 1 г, 4,21 ммоль) и карбонат цезия (1,372 г, 4,21 ммоль) объединяли в DMSO (8 мл) и нагревали при 80°C в течение 30 минут. Реакционную смесь охлаждали и распределяли между этилацетатом и водой. Органический слой промывали насыщенным раствором соли, сушили (Na2SO4), фильтровали и концентрировали. Очистка остатка хроматографией (силикагель, 0-30% этилацетат в гексанах) давала указанное в заголовке соединение (1,13 г, 91%).
Пример 23b
6-метил-4-(5-нитро-2-феноксипиридин-3-ил)-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 23b получали согласно процедуре, используемой для получения продукта примера 7d, заменяя продуктом примера 23 продукт примера 7c и перемешивая при 60°C в течение 24 часов, получая указанное в заголовке соединение.
Пример 23c
4-(5-амино-2-феноксипиридин-3-ил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 23c получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 23b продукт примера 2, получая указанное в заголовке соединение.
Пример 23d
N-[5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-6-феноксипиридин-3-ил]метансульфонамид
Продукт примера 23d получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 23с продукт примера 3, получая указанное в заголовке соединение (0,035 г, 36%). 1H ЯМР (300 МГц, DMSO-d6) δ 3,05 (с, 3H) 3,57 (с, 3H) 6,28-6,36 (м, 1H) 7,10 (д, J=7,54 Гц, 2H) 7,16 (т, J=7,54 Гц, 1H) 7,28-7,41 (м, 3H) 7,48 (с, 1H) 7,78 (д, J=2,78 Гц, 1H) 7,96 (д, J=2,38 Гц, 1H) 9,79 (с, 1H) 12,11 (с, 1H). MS (ESI+) m/z 411,0 (M+H)+.
Пример 24
N-[3-фтор-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]метансульфонамид
Пример 24a
4-(2,3-дифтор-5-нитрофенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 24a получали согласно процедуре, используемой для получения продукта примера 7d, заменяя 1-бром-2,3-дифтор-5-нитробензолом (Oakwood Products) продукт примера 7c, получая указанное в заголовке соединение.
Пример 24b
4-(3-фтор-5-нитро-2-феноксифенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Фенол (0,043 г, 0,457 ммоль), продукт примера 24a (0,2 г, 0,435 ммоль) и карбонат цезия (0,142 г, 0,435 ммоль) объединяли в DMSO (2,177 мл) и нагревали при 80°C в течение 30 минут. Реакционную смесь охлаждали и распределяли между этилацетатом и водой. Органический слой промывали насыщенным раствором соли, сушили (Na2SO4), фильтровали и концентрировали, получая указанное в заголовке соединение.
Пример 24c
4-(5-амино-3-фтор-2-феноксифенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 24c получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 24b продукт примера 2, получая указанное в заголовке соединение.
Пример 24d
N-[3-фтор-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]метансульфонамид
Продукт примера 24d получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 24c продукт примера 3, получая указанное в заголовке соединение (0,13 г, 67%). 1H ЯМР (300 МГц, DMSO-d6) δ 3,05 (с, 3H) 3,57 (с, 3H) 6,28-6,36 (м, 1H) 7,10 (д, J=7,54 Гц, 2H) 7,16 (т, J=7,54 Гц, 1H) 7,28-7,41 (м, 3H) 7,48 (с, 1H) 7,78 (д, J=2,78 Гц, 1H) 7,96 (д, J=2,38 Гц, 1H) 9,79 (с, 1H) 12,11 (с, 1H).
Пример 25
N-[4-(2-цианофенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Пример 25a
2-(2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-нитрофенокси)бензонитрил
Продукт примера 25a получали согласно процедуре, используемой для получения продукта примера 2b, заменяя 2-гидроксибензонитрилом фенол, получая указанное в заголовке соединение.
Пример 25b
2-(4-амино-2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенокси)бензонитрил
Продукт примера 25b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 25a продукт примера 2b, получая указанное в заголовке соединение.
Пример 25c
N-[4-(2-цианофенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Продукт примера 25c получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 25b продукт примера 3, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 3,07 (с, 3H), 3,50 (с, 3H), 6,26 (дд, J=2,8, 1,9 Гц, 1H), 6,73 (дд, J=8,6, 0,9 Гц, 1H), 7,07 (тд, J=7,6, 0,9 Гц, 1H), 7,34-7,23 (м, 4H), 7,53-7,40 (м, 2H), 7,71 (дд, J=7,7, 1,7 Гц, 1H), 9,89 (с, 1H), 12,03 (ушир.с, 1H). MS (ESI+) m/z 435,2 (M+H)+.
Пример 26
N-[4-(4-фторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Пример 26a
4-(2-(4-фторфенокси)-5-нитрофенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6Н)-он
Пример 26a получали согласно процедуре, используемой для получения продукта примера 2b, заменяя 4-фторфенолом фенол, получая указанное в заголовке соединение.
Пример 26b
4-(5-амино-2-(4-фторфенокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 26b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 26a продукт примера 2b, получая указанное в заголовке соединение.
Пример 26c
N-[4-(4-фторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Продукт примера 26c получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 26b продукт примера 3, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 3,02 (с, 3H), 3,50 (с, 3H), 6,29-6,23 (м, 1H), 6,94-6,82 (м, 2H), 7,14-6,96 (м, 3H), 7,21 (дд, J=8,7, 2,7 Гц, 1H), 7,31-7,24 (м, 2H), 7,38 (д, J=2,7 Гц, 1H), 9,71 (с, 1H), 12,02 (ушир.с, 1H). MS (ESI+) m/z 428,1 (M+H)+.
Пример 27
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Пример 27a
4-(2-(2,4-дифторфенокси)-5-нитрофенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 27a получали согласно процедуре, используемой для получения продукта примера 2b, заменяя 2,4-дифторфенолом фенол, получая указанное в заголовке соединение.
Пример 27b
4-(5-амино-2-(2,4-дифторфенокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 27b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 27a продукт примера 2b, получая указанное в заголовке соединение.
Пример 27c
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Продукт примера 27b (50 мг, 0,136 ммоль) и триэтиламин (0,057 мл, 0,408 ммоль) объединяли в CH2Cl2 (9 мл). Метансульфонил хлорид (0,042 мл, 0,544 ммоль) добавляли по каплям и раствор перемешивали при температуре окружающей среды в течение 1 часа. Раствор концентрировали при пониженном давлении, диоксан (5 мл) и гидроксид натрия (10% м/о, 3 мл, 0,136 ммоль) добавляли и раствор нагревали при 70°C в течение 1 часа. Смесь охлаждали до температуры окружающей среды и затем нейтрализовали насыщенным NH4Cl (100 мл) до pH 8. Органический слой отделяли и водную фазу экстрагировали этилацетатом (3 × 25 мл). Объединенные органические слои промывали насыщенным раствором соли, сушили (MgSO4), фильтровали и концентрировали. Очистка ВЭЖХ с обращенной фазой (C18, 10-100% ацетoнитрил/вода, 0,1% TFA) давала 27,5 мг (45,4%) указанного в заголовке соединения. 1H ЯМР (300 МГц, DMSO-d6) δ 3,01 (с, 3H), 3,53 (с, 3H), 6,29-6,23 (м, 1H), 7,04-6,90 (м, 2H), 7,09 (тд, J=9,1, 5,6 Гц, 1H), 7,44-7,14 (м, 5H), 9,70 (с, 1H), 12,04 (ушир.с, 1H). MS (ESI+) m/z 446,1 (M+H)+.
Пример 28
N-[3-хлор-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]метансульфонамид
Пример 28a
4-(3-хлор-2-фтор-5-нитрофенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 28a получали согласно процедуре, используемой для получения продукта примера 6c, заменяя 1,3-дихлор-2-фтор-5-нитробензолом (0,176 г, 0,841 ммоль) продукт примера 6b, получая указанное в заголовке соединение.
Пример 28b
N-[3-хлор-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксифенил]метансульфонамид
Продукт примера 28b получали согласно процедурам, используемым для получения продуктов примеров 24b-24d, заменяя продуктом примера 28a продукт примера 24a, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 3,12 (с, 3H) 3,43 (с, 3H) 6,25-6,29 (м, 1H) 6,63 (д, J=7,93 Гц, 2H) 6,87 (т, J=7,34 Гц, 1H) 7,10-7,18 (м, 2H) 7,27-7,31 (м, 2H) 7,39 (с, 2H) 10,05 (с, 1H) 12,04 (с, 1H). MS (ESI+) m/z 444 (M+H)+.
Пример 29
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-4-илокси)фенил]метансульфонамид
Пример 29a
6-метил-4-(5-нитро-2-(тетрагидро-2H-пиран-4-илокси)фенил)-1H-пирроло[2,3-c]пиридин-7(6H)-он
Тетрагидро-2H-пиран-4-ол (0,046 г, 0,453 ммоль) в тетрагидрофуране (2 мл) обрабатывали гидридом натрия (0,022 г, 0,906 ммоль, 0,036 г 60% дисперсии в масле) при комнатной температуре. Реакционную смесь перемешивали в течение 10 минут. К этому раствору добавляли продукт примера 2a (0,1 г, 0,227 ммоль). Реакционную смесь нагревали при 50°C в течение 2 часов. После охлаждения до комнатной температуры реакционную смесь распределяли между водой и этилацетатом. Водный слой экстрагировали дважды дополнительным этилацетатом. Объединенные органические слои промывали насыщенным раствором соли, сушили над MgSO4, фильтровали и концентрировали. Остаток очищали флаш-хроматографией на силикагеле, элюируя этилацетатом, получая 0,055 г указанного в заголовке соединения.
Пример 29b
4-(5-амино-2-(тетрагидро-2H-пиран-4-илокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Смесь продукта примера 29b (0,055 г) и 10% палладия на углероде (0,050 г) в этилацетате (10 мл) обрабатывали баллоном водорода в течение ночи. Твердое вещество удаляли фильтрованием. Фильтрат концентрировали при пониженном давлении, получая 0,042 г указанного в заголовке соединения.
Пример 29c
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-4-илокси)фенил]метансульфонамид
Продукт примера 29c получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 29b продукт примера 3, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 1,45-1,51 (м, 2H), 1,82-1,87 (м, 2H), 2,94 (с, 3H), 3,35-3,41 (м, 2), 3,56 (с, 3H), 3,60-3,68 (м, 2H), 4,45-4,49 (м, 1H), 6,20 (т, J=2,29 Гц, 1H), 7,14-7,16 (м, 2H), 7,28-7,29 (м, 3H), 9,45 (с, 1H), 12,01 (с, 1H), (ESI+) m/z 418,2 (M+H)+.
Пример 30
6-метил-4-[2-фенокси-5-(1H-пиразол-1-илметил)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Смесь продукта примера 20b (0,04 г, 0,115 ммоль), 1H-пиразола (0,016 г, 0,231 ммоль) и трифенилфосфина (0,061 г, 0,231 ммоль) в тетрагидрофуране (1 мл) перемешивали в течение 2 минут. К этому раствору добавляли ди-трет-бутил азодикарбоксилат (DTBAD, 0,053 г, 0,231 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 3 часов. Растворитель удаляли при пониженном давлении и остаток очищали препаративной ВЭЖХ (C18, 10-80% ацетoнитрил/вода с 0,1% TFA), получая 0,006 г указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6) δ 3,49 (с, 3H), 5,37 (с, 2H), 5,21 (т, J=5,8 Гц, 1H), 6,17-6,18 (м, 1H), 6,28 (т, J=1,98 Гц, 1H), 6,86 (д, J=7,63 Гц, 2H), 6,97 (д, J=8,24 Гц, 1H), 7,02 (т, J=7,32 Гц, 4H), 7,22-7,29 (м, 5H), 7,39 (д, J=2,14 Гц, 1H), 7,47 (д, J=1,83 Гц, 1H), 7,53-7,46 (м, 3H), 7,86 (д, J=2,44 Гц, 1H), 11,97 (с, 1H), (ESI+) m/z 397,2 (M+H)+.
Пример 31
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидрофуран-3-илокси)фенил]метансульфонамид
Пример 31a
6-метил-4-(5-нитро-2-(тетрагидрофуран-3-илокси)фенил)-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 31a получали согласно процедуре, используемой для получения продукта примера 29a, заменяя тетрагидрофуран-3-олом тетрагидро-2H-пиран-4-ол, получая указанное в заголовке соединение.
Пример 31b
4-(5-амино-2-(тетрагидрофуран-3-илокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 31b получали согласно процедуре, используемой для получения продукта примера 29b, заменяя продуктом примера 31a продукт примера 29a, получая указанное в заголовке соединение.
Пример 31c
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидрофуран-3-илокси)фенил]метансульфонамид
Продукт примера 31 получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 31b продукт примера 3, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 1,84-1,90 (м, 1H), 2,08-2,17 (м, 1H), 2,95 (с, 3H), 3,35-3,41 (м, 2), 3,56 (с, 3H), 3,62-3,69 (М, 2H), 3,80-3,84 (м, 1H), 4,96-4,98 (м, 1H), 6,17-6,18 (м, 1H), 7,06-7,08 (м, 1H), 7,16-7,18 (м, 1H), 7,25 (с, 1H), 7,27-7,29 (м, 2H), 9,45 (с, 1H), 12,00 (с, 1H), (ESI+) m/z 404,2 (M+H)+.
Пример 32
N-{3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-[2-(трифторметил)фенокси]фенил}метансульфонамид
Пример 32a
6-метил-4-(5-нитро-2-(2-(трифторметил)фенокси)фенил)-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 32a получали согласно процедуре, используемой для получения продукта примера 2b, заменяя 2-(трифторметил)фенолом фенол, получая указанное в заголовке соединение.
Пример 32b
4-(5-амино-2-(2-(трифторметил)фенокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 32b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 32a продукт примера 2b, получая указанное в заголовке соединение.
Пример 32c
N-{3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-[2-(трифторметил)фенокси]фенил}метансульфонамид
Продукт примера 32c получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 32b продукт примера 3, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 3,05 (с, 3H), 3,44 (с, 3H), 6,32-6,26 (м, 1H), 6,75 (д, J=8,4 Гц, 1H), 7,17-7,07 (м, 2H), 7,34-7,18 (м, 3H), 7,53-7,38 (м, 2H), 7,65 (дд, J=7,8, 1,6 Гц, 1H), 9,84 (с, 1H), 12,09-11,99 (м, 1H). MS (ESI+) m/z 478,1 (M+H)+.
Пример 33
N-[4-(4-цианофенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Пример 33a
4-(2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-нитрофенокси)бензонитрил
Продукт примера 33a получали согласно процедуре, используемой для получения продукта примера 2b, заменяя 4-гидроксибензонитрилом фенол, получая указанное в заголовке соединение.
Пример 33b
4-(4-амино-2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенокси)бензонитрил
Продукт примера 33b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 33a продукт примера 2b, получая указанное в заголовке соединение.
Пример 33c
N-[4-(4-цианофенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Продукт примера 33c получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 33b продукт примера 3, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 3,07 (с, 3H), 3,46 (с, 3H), 6,27-6,21 (м, 1H), 6,94-6,87 (м, 2H), 7,32-7,20 (м, 4H), 7,42 (д, J=2,5 Гц, 1H), 7,70-7,63 (м, 2H), 9,87 (с, 1H), 12,03 (ушир.с, 1H). MS (ESI+) m/z 435,2 (M+H)+.
Пример 34
N-[4-(2-хлор-4-фторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Пример 34a
4-(2-(2-хлор-4-фторфенокси)-5-нитрофенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 34a получали согласно процедуре, используемой для получения продукта примера 2b, заменяя 2-хлор-4-фторфенолом фенол, получая указанное в заголовке соединение.
Пример 34b
4-(5-амино-2-(2-хлор-4-фторфенокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 34b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 34a продукт примера 2b, получая указанное в заголовке соединение.
Пример 34c
N-[4-(2-хлор-4-фторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Продукт примера 34c получали согласно процедуре, используемой в способе А примера 4, заменяя продуктом примера 34b продукт примера 3, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 3,02 (с, 3H), 3,52 (с, 3H), 6,29 (т, J=2,3 Гц, 1H), 6,99-6,88 (м, 2H), 7,14-7,03 (м, 1H), 7,21 (дд, J=8,7, 2,7 Гц, 1H), 7,28 (т, J=2,8 Гц, 1H), 7,34 (с, 1H), 7,41 (д, J=2,7 Гц, 1H), 7,49 (дд, J=8,3, 3,0 Гц, 1H), 9,75 (с, 1H), 12,05 (ушир.с, 1H). MS (ESI+) m/z 462,1 (M+H)+.
Пример 35
[4-(бензилокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]уксусная кислота
Пример 35a
этил 2-(3-бром-4-гидроксифенил)ацетат
К раствору этил 2-(4-гидроксифенил)ацетата (Alfa, 2,70 г, 15 ммоль) в уксусной кислоте (20 мл) добавляли по каплям в течение 15 минут раствор брома (0,773 мл, 15,00 ммоль) в уксусной кислоте (15 мл). Смесь перемешивали при температуре окружающей среды в течение 30 минут и выпаривали. Очистка хроматографией (силикагель, 10-20% этилацетат в гексане) дает указанное в заголовке соединение (3,66 г, 94%).
Пример 35b
этил 2-(4-(бензилокси)-3-бромфенил)ацетат
Раствор продукта примера 35a (2,011 мл, 16,90 ммоль) и карбоната калия (5,84 г, 42,3 ммоль) в этаноле (100 мл) кипятили с возвращением флегмы в течение 2 часов, охлаждали, концентрировали и остаток распределяли между этилацетатом и водой. Органический слой промывали насыщенным раствором соли, сушили (Na2SO4), фильтровали и концентрировали. Очистка хроматографией с обращенной фазой (силикагель, 0-20% этилацетат в гексане) давала указанное в заголовке соединение (4,84 г, 98%).
Пример 35c
этил 2-(4-(бензилокси)-3-(6-метил-7-оксо-1-тозил-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил)ацетат
Продукт примера 35c получали согласно процедуре, используемой для получения продукта примера 7d, заменяя продуктом примера 35b продукт примера 7c, получая указанное в заголовке соединение.
Пример 35d
[4-(бензилокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]уксусная кислота
Продукт примера 35c (0,4 г, 0,701 ммоль), гидроксид калия (0787 г, 14,02 ммоль) и бромид цетилтриметиламмония (0,013 г, 0,035 ммоль) объединяли в диоксане (10 мл) и воде (5 мл) и нагревали при 100°C в течение 3 часов, охлаждали и распределяли между равными объемами этилацетата и воды (20 мл каждый). pH доводили до pH 2 осторожным добавлением концентрированной HCl. Органический слой отделяли и промывали насыщенным раствором соли, сушили (Na2SO4), фильтровали и концентрировали. Растирание остатка в гексане давало указанное в заголовке соединение (0,27 г, 98%). 1H ЯМР (300 МГц, DMSO-d6) δ 3,52 (с, 3H) 3,55 (с, 2H) 5,09 (с, 2H) 6,14-6,21 (м, 1H) 7,10-7,33 (м, 10H) 11,97 (с, 1H) 12,25 (с, 1H). MS (ESI+) m/z 389,0 (M+H)+.
Пример 36
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид
Пример 36a
2-бром-1-(2,4-дифторфенокси)-4-нитробензол
Смесь 2-бром-1-фтор-4-нитробензола (15 г, 68 ммоль), 2,4-дмфторфенола (7,82 мл, 82 ммоль) и карбоната цезия (26,7 г, 82 ммоль) в диметилсульфоксиде (75 мл) нагревали до 110°C в течение 1 часа. Реакционную смесь охлаждали до температуры окружающей среды и добавляли воду (1000 мл) и насыщенный водный раствор хлорида натрия (1000 мл). Смесь экстрагировали этилацетатом (3 × 200 мл). Объединенные органические веществаа промывали насыщенным водным раствором хлорида натрия, сушили (безводным сульфатом магния), фильтровали и концентрировали при пониженном давлении, получая указанное в заголовке соединение (22,5 г, количественный).
Пример 36b
3-бром-4-(2,4-дифторфенокси)анилин
Смесь продукта примера 36a (22,5 г, 68,2 ммоль), порошка железа (19,04 г, 341 ммоль) и хлорида аммония (7,30 г, 136 ммоль) в тетрагидрофуране (117 мл), этаноле (117 мл) и воде (39,0 мл) нагревали при кипении с возвращением флегмы при 100°C в течение 2 часов. Реакционную смесь охлаждали до температуры чуть ниже температуры кипения с возвращением флегмы, фильтровали через целит и осадок на фильтре промывали теплым метанолом (3 × 50 мл). Полученный раствор концентрировали при пониженном давлении и затем нейтрализовали до pH 8 насыщенным раствором гидрокарбоната натрия (150 мл). Смесь экстрагировали этилацетатом (3 × 100 мл). Объединенные органические вещества промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. остаток очищали флаш-хроматографией (силикагель, градиент этилацетат/гексан 0-15%), получая указанное в заголовке соединение (16,8 г, выход 82%).
Пример 36c
4-(5-амино-2-(2,4-дифторфенокси)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Смесь продукта примера 6a (5,0 г, 11,67 ммоль), продукта примера 36b (3,85 г, 12,84 ммоль), 1,3,5,7-тетраметил-6-фенил-2,4,8-триокса-6-фосфаадамантана (0,399 г, 1,366 ммоль), трис(дибензилиденацетон)дипалладия(0) (0,321 г, 0,350 ммоль) и фосфата калия (6,19 г, 29,2 ммоль) в диоксане (50 мл) и воде (12,5 мл) дегазировали и снова насыщали азотом несколько раз. Реакционную смесь нагревали при 60°C в течение 16 часов и затем охлаждали до температуры окружающей среды. Реакционную смесь распределяли между водой и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом три раза. Объединенные органические слои промывали насыщенным раствором соли, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали колоночной флаш-хроматографией (силикагель, 60% этилацетат/гексаны), получая указанное в заголовке соединение (4,40 г, выход 72,3%).
Пример 36d
N-(4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-1-тозил-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил)-N-(этилсульфонил)этансульфонамид
Раствор продукта примера 36c (4,35 г, 8,34 ммоль) в дихлорметане (50 мл) охлаждали до 0°C. К этому раствору добавляли этансульфонил хлорид (2,37 мл, 25,0 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Растворитель выпаривали и остаток распределяли между этилацетатом и водой. Водный слой экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным водным раствором жлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 80% этилацетат/гексаны), получая указанное в заголовке соединение (5,34 г, выход 91%).
Пример 36e
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид
Смесь продукта примера 36d (5,3 г, 7,5 ммоль), гидроксида калия (8,43 г, 150 ммоль) и бромида N,N,N-триметилгексадекан-1-аминия (0,137 г, 0,375 ммоль) в тетрагидрофуране (60 мл) и воде (30 мл) нагревали при 90°C в течение 16 часов. Тетрагидрофуран удаляли при пониженном давлении и остаток распределяли между водой и этилацетатом. Водный слой нейтрализовали до pH=7, используя 10% HCl. Водный слой затем экстрагировали этилацетатом. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, этилацетат). Желательные фракции объединяли и концентрировали. Остаток растирали с 20 мл ацетoнитрила, получая указанное в заголовке соединение (2,82 г, выход 82%). 1H ЯМР (300 МГц, DMSO-d6) δ 1,23 (т, J=7,3 Гц, 3H), 3,11 (кв., J=7,3 Гц, 2H), 3,53 (с, 3H), 6,27-6,22 (м, 1H), 6,91 (д, J=8,7 Гц, 1H), 7,13-6,93 (м, 2H), 7,19 (дд, J=8,8, 2,7 Гц, 1H), 7,32-7,25 (м, 2H), 7,42-7,31 (м, 2H), 9,77 (с, 1H), 12,04 (ушир.с, 1H). MS (ESI+) m/z 460,1 (M+H)+.
Пример 37
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]ацетамид
Продукт примера 27b (50 мг, 0,136 ммоль) и триэтиламин (56,9 мкл, 0,408 ммоль) объединяли в CH2Cl2 (10 мл). Ацетил хлорид (11,6 мкл, 0,163 ммоль) добавляли по каплям и раствор перемешивали в течение 1 часа при температуре окружающей среды. Добавляли воду (25 мл) и насыщенный водный раствор бикарбоната натрия (25 мл) и смесь экстрагировали CH2Cl2 (3 × 25 мл). Объединенные органические вещества промывали насыщенным раствором соли, сушили (MgSO4), фильтровали и концентрировали. Очистка остатка ВЭЖХ с обращенной фазой (C18, 10-100% ацетoнитрил/вода, 0,1% TFA) давала 15 мг (28%) указанного в заголовке соединения. 1H ЯМР (300 МГц, DMSO-d6) δ 2,04 (с, 3H), 3,52 (с, 3H), 6,29 6,23 (м, 1H), 7,08-6,85 (м, 3H), 7,39-7,25 (м, 3H), 7,53 (дд, J=8,8, 2,6 Гц, 1H), 7,77 (д, J=2,6 Гц, 1H), 10,00 (с, 1H), 12,07-11,96 (м, 1H). MS (ESI+) m/z 410,3 (M+H)+.
Пример 38
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-3,3,3-трифторпропанамид
Продукт примера 38 получали согласно процедуре, используемой для получения продукта примера 37, заменяя 3,3,3-трифторпропаноил хлоридом ацетил хлорид, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 3,54-3,46 (м, 2H), 3,53 (с, 3H), 6,27 (т, J=2,3 Гц, 1H), 7,14-6,87 (м, 3H), 7,28 (т, J=2,7 Гц, 1H), 7,31 (с, 1H), 7,37 (ддд, J=11,3, 8,7, 2,8 Гц, 1H), 7,50 (дд, J=8,8, 2,6 Гц, 1H), 7,76 (д, J=2,6 Гц, 1H), 10,38 (с, 1H), 12,03 (ушир.с, 1H). MS (ESI+) m/z 478,2 (M+H)+.
Пример 39
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-2,2-диметилпропанамид
Продукт примера 39 получали согласно процедуре, используемой для получения продукта примера 37, заменяя пивалоил хлоридом ацетил хлорид, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 1,22 (с, 9H), 3,53 (с, 3H), 6,31-6,25 (м, 1H), 6,88 (д, J=8,8 Гц, 1H), 7,08-6,92 (м, 2H), 7,31-7,24 (м, 2H), 7,40-7,29 (м, 1H), 7,62 (дд, J=8,8, 2,6 Гц, 1H), 7,83 (д, J=2,6 Гц, 1H), 9,28 (с, 1H), 12,00 (ушир.с, 1H). MS (ESI+) m/z 452,3 (M+H)+.
Пример 40
Этил 4-(циклопентиламино)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензоат
Смесь продукта примера 9a (0,094 г, 0,2 ммоль), циклопентанамина (0,034 г, 0,4 ммоль) и триэтиламина (0,081 г, 0,8 ммоль) в DMSO (2 мл) нагревали при 120°C в течение ночи. Реакционную смесь очищали препаративной ВЭЖХ (C18, 10-80% ацетoнитрил в 0,1% TFA/воде), получая 0,019 г указанного в заголовке продукта. 1H ЯМР (500 МГц, DMSO-d6) δ 1,27 (т, J=7,02 Гц, 3H), 1,32-1,36 (м, 2H), 1,47-1,55 (м, 3H), 1,88-1,93 (м, 2H), 3,55 (с, 3H), 3,83-3,88 (м, 1H), 4,22 (кв., J=7,02 Гц, 2H), 5,94 (т, J=2,29 Гц, 1H), 6,77 (д, J=8,85 Гц, 1H), 7,22 (с, 1H), 7,28 (т, J=2,75 Гц, 1H), 7,63 (д, J=1,83 Гц, 1H), 7,82 (дд, J=8,54, 2,14, 1H), 12,01 (с, 1H). MS (ESI+) m/z 380,2 (M+H)+.
Пример 41
4-{5-[(1,1-диоксидо-1,2-тиазолидин-2-ил)метил]-2-феноксифенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 41a
4-(5-(гидроксиметил)-2-феноксифенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 41a изолировали как побочный продукт из препарата продукта примера 20b.
Пример 41b
3-(6-метил-7-оксо-1-тозил-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензил метансульфонат
Смесь продукта примера 41a (0,15 г, 0,3 ммоль), метансульфонил хлорида (0,069 г, 0,6 ммоль) и триэтиламина (0,121 г, 1,2 ммоль) в дихлорметане (5 мл) перемешивали при комнатной температуре в течение 2 часов. Растворитель удаляли и остаток очищали флаш-хроматографией на силикагеле, элюируя 20-40% этилацетатом в гексанах, получая 0,105 г указанного в заголовке продукта.
Пример 41c
4-{5-[(1,1-диоксидо-1,2-тиазолидин-2-ил)метил]-2-феноксифенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
1,2-тиазолидин 1,1-диоксид (0,031 г, 0,259 ммоль) в диметилформамиде (1 мл) обрабатывали 60% гидридом натрия (0,012 г, 0,518 ммоль, 0,021 г 60% дисперсия в масле). Реакционную смесь перемешивали в течение 5 мин. К этому раствору добавляли продукт примера 41b (0,05 г, 0,086 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 2 часов. 2 н. NaOН (1 мл) добавляли и реакционную смесь нагревали при 65°C в течение 2 часов. После охлаждения до комнатной температуры реакционную смесь распределяли между водой и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным раствором соли, сушили над MgSO4, фильтровали и концентрировали. Остаток очищали препаративной ВЭЖХ (C18, 10-80% ацетoнитрил в 0,1% TFA вода), получая 0,025 г (64%) указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6) δ 2,21-2,25 (м, 2H), 3,15 (т, J=6,97 Гц, 2H), 3,23-3,27 (м, 2H), 3,50 (с, 3H), 4,13 (с, 2H), 6,25-6,26 (м, 1H), 6,88 (д, J=7,63 Гц, 2H), 7,00 (д, J=8,54 Гц, 1H), 7,03-7,05 (м, 1H), 7,25-7,30 (м, 4H), 7,34 (дд, J=8,39, 2,29, 1H), 7,48 (д, J=2,44 Гц, 1H), 12,00 (с, 1H). MS (ESI+) m/z 450,2 (M+H)+.
Пример 42
4-{[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензил]амино}-4-оксобутановая кислота
Продукт примера 42 получали согласно процедуре, используемой для получения продукта примера 41c, заменяя пирролидин-2,5-дионом 1,2-тиазолидин 1,1-диоксид, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 2,37-2,40 (м, 2H), 2,44-2,48 (м, 2H), 3,50 (с, 3H), 4,31 (д, J=5,8 Гц, 2H), 6,23-6,24 (м, 1H), 6,84 (д, J=7,63 Гц, 2H), 6,96 (д, J=8,24 Гц, 1H), 7,00 (т, J=7,32 Гц, 1H), 7,22-7,29 (м, 5H), 7,40 (д, J=2,14, 1H), 8,40 (т, J=5,95 Гц, 1H), 11,98 (с, 1H). MS (ESI+) m/z 446,1 (M+H)+.
Пример 43
4-[2-(2,4-дифторфенокси)-5-(1,1-диоксидо-1,2-тиазолидин-2-ил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 43a
3-хлор-N-(3-хлорпропилсульфонил)-N-(4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил)пропан-1-сульфонамид
Смесь продукта примера 27b (0,1 г, 0,272 ммоль), 3-хлорпропан-1-сульфонил хлорида (0,145 г, 0,817 ммоль) и триэтиламина (0,165 г, 1,633 ммоль) в дихлорметане (3 мл) перемешивали в течение 2 часов. Растворитель удаляли и остаток использовали непосредственно для следующей реакции.
Пример 43b
4-[2-(2,4-дифторфенокси)-5-(1,1-диоксидо-1,2-тиазолидин-2-ил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Натрий (0,064 г, 2,78 ммоль) растворяли в этаноле (15 мл). К этому раствору добавляли продукт примера 43a (0,18 г, 0,278 ммоль) в этаноле (5 мл). Реакционную смесь нагревали при 75°C в течение 2 часов. После охлаждения растворитель удаляли при пониженном давлении и остаток очищали препаративной ВЭЖХ (C18, 10-80% ацетoнитрил в 0,1% TFA/воде), получая 0,055 г указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6) δ 2,37-2,44 (м, 2H), 3,49-3,53 (м, 2H), 3,54 (с, 3H), 3,76 (т, J=6,56 Гц, 2H), 6,27-6,28 (м, 1H), 6,95 (д, J=8,85 Гц, 1H), 7,00-7,12 (м, 2H), 7,20 (дд, J=8,85, 2,75 Гц, 1H), 7,28 (т, J=2,75 Гц, 1H), 7,32 (с, 1H), 7,35-7,41 (м, 2H), 12,05 (с, 1H). MS (ESI+) m/z 472,2 (M+H)+.
Пример 44
4-[2-(бензилокси)-5-(2-гидроксиэтил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 35d (0,039 г, 0,1 ммоль) в тетрагидрофуране (2 мл) обрабатывали по каплям комплексом боран-тетрагидрофуран (1M, 0,200 мл, 0,200 ммоль) и смесь перемешивали при 40°C в течение 1 часа, разбавляли 5 мл метанола, нагревали при 50°C в течение 30 минут и концентрировали. Очистка хроматографией (силикагель, 0,5-4% метанол в дихлорметане) давала указанное в заголовке соединение (0,03 г, 79%). 1H ЯМР (300 МГц, DMSO-d6) δ 2,70 (т, J=6,94 Гц, 2H) 3,52 (с, 3H) 3,57-3,64 (м, 2H) 4,59-4,63 (м, 1H) 5,06 (с, 2H) 6,14-6,18 (м, 1H) 7,08-7,18 (м, 2H) 7,20-7,32 (м, 8H) 11,95 (с, 1H). MS (ESI+) m/z 375,0 (M+H)+.
Пример 45
метил [4-(бензилокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]ацетат
Пример 45a
2-(4-(бензилокси)-3-(6-метил-7-оксо-6,7-гидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил)ацетил хлорид
Продукт примера 35d (0,18 г, 0,463 ммоль) в тетрагидрофуране (4,63 мл) обрабатывали одной каплей диметилформамида с последующим добавлением по каплям оксалил хлорида (0,122 мл, 1,390 ммоль), перемешивали в течение двадцати минут и концентрировали.
Пример 45b
метил [4-(бензилокси)-3-(6-метил7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]ацетат
Продукт примера 45a (0,058 г, 0,143 ммоль) в тетрагидрофуране (4 мл) обрабатывали метанолом (5 мл, 124 ммоль), перемешивали в течение 1 часа при комнатной температуре и концентрировали. Очистка хроматографией (силикагель, 0,5-3% метанол в дихлорметане) давала указанное в заголовке соединение (0,048 г, 79%). 1H ЯМР (300 МГц, DMSO-d6) δ 3,52 (с, 3H) 3,62 (с, 3H) 3,66 (с, 2H) 5,09 (с, 2H) 6,15-6,20 (м, 1H) 7,10-7,37 (м, 10H) 11,97 (с, 1H). MS (ESI+) m/z 403,0 (M+H)+.
Пример 46
2-[4-(бензилокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-N-этилацетамид
Продукт примера 46 получали согласно процедуре, используемой для получения продукта примера 45b, заменяя этиламином метанол, получая указанное в заголовке соединение (0,039 г, 64%). 1H ЯМР (300 МГц, DMSO-d6) δ 1,01 (т, J=7,29 Гц, 3H) 2,99-3,11 (м, 2H) 3,35 (с, 2H) 3,52 (с, 3H) 5,07 (с, 2H) 6,14-6,21 (м, 1H) 7,08-7,35 (м, 10H) 7,98 (т, J=5,43 Гц, 1H) 11,96 (с, 1H). MS (ESI+) m/z 416,0 (M+H)+.
Пример 47
2-[4-(бензилокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-N,N-диметилацетамид
Продукт примера 47 получали согласно процедуре, используемой для получения продукта примера 45b, заменяя диметиламидом метанол, получая указанное в заголовке соединение (0,058 г, 98%). 1H ЯМР (300 МГц, DMSO-d6) δ 2,83 (с, 3H) 3,02 (с, 3H) 3,52 (с, 3H) 3,66 (с, 2H) 5,08 (с, 2H) 6,12-6,24 (м, 1H) 7,06-7,36 (м, 10H) 11,96 (с, 1H). MS (ESI+) m/z 416,0 (M+H)+.
Пример 48
N-[4-(3,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Пример 48a
4-(2-(3,4-дифторфенокси)-5-нитрофенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 48a получали согласно процедуре, используемой для получения продукта примера 2b, заменяя 3,4-дифторфенолом фенол, получая указанное в заголовке соединение.
Пример 48b
4-(5-амино-2-(3,4-дифторфенокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 48b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 48a продукт примера 2b, получая указанное в заголовке соединение.
Пример 48c
N-[4-(3,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Пример 48c получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 48b продукт примера 3, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 3,04 (с, 3H), 3,50 (с, 3H), 6,28-6,23 (м, 1H), 6,72-6,62 (м, 1H), 6,97 (ддд, J=11,9, 6,7, 3,0 Гц, 1H), 6,97 (ддд, J=11,9, 6,7, 3,0 Гц, 1H), 7,11 (д, J=8,7 Гц, 1H), 7,41-7,19 (м, 5H), 9,78 (с, 1H), 12,03 (ушир.с, 1H). MS (ESI+) m/z 446,1 (M+H)+.
Пример 49
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(2,4,6-трифторфенокси)фенил]метансульфонамид
Пример 49a
6-метил-4-(5-нитро-2-(2,4,6-трифторфенокси)фенил)-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 49a получали согласно процедуре, используемой для получения продукта примера 2b, заменяя 2,4,6-трифторфенолом фенол, получая указанное в заголовке соединение.
Пример 49b
4-(5-амино-2-(2,4,6-трифторфенокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 49b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 49a продукт примера 2b, получая указанное в заголовке соединение.
Пример 49c
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(2,4,6-трифторфенокси)фенил]метансульфонамид
Пример 49c получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 49b продукт примера 3, получая указанное в заголовке соединение. 1H ЯМР ЯМР (300 МГц, DMSO-d6) δ 2,99 (с, 3H), 3,57 (с, 3H), 6,23 (т, J=2,3 Гц, 1H), 6,80 (д, J=8,8 Гц, 1H), 7,15 (дд, J=8,8, 2,7 Гц, 1H), 7,34-7,27 (м, 3H), 7,45-7,34 (м, 2H), 9,66 (с, 1H), 12,07 (ушир.с, 1H). MS (ESI+) m/z 464,1 (M+H)+.
Пример 50
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид
Пример 50a
Этил 4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензоат
Продукт примера 50a получали согласно процедуре, используемой для получения продукта примера 9b, заменяя 2,4-дифторфенолом фенол, получая указанное в заголовке соединение.
Пример 50b
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензойная кислота
Продукт примера 50b получали согласно процедуре, используемой для получения продукта примера 10, заменяя продуктом примера 50a продукт примера 9b, получая указанное в заголовке соединение.
Пример 50c
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид
Продукт примера 50c получали согласно процедуре, используемой для получения продукта примера 13a, заменяя продуктом примера 50b продукт примера 10, получая указанное в заголовке соединение.
Пример 50d
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид
Продукт примера 50d получали согласно процедуре, используемой для получения продукта примера 13b, заменяя продуктом примера 50c продукт примера 13a, и водным гидроксидом аммония этиламин, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 3,57 (с, 3H), 6,24-6,25 (м, 1H), 6,83 (д, J=8,24 Гц, 1H), 7,07-7,13 (м, 1H), 7,27-7,34 (м, 4H), 7,42-7,48 (м, 1H), 7,85 (дд, J=8,54, 2,44, 1H), 7,96 (с, 1H), 8,00 (д, J=2,44 Гц, 1H), 12,04 (с, 1H). MS (ESI+) m/z 396,3 (M+H)+.
Пример 51
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-(тетрагидрофуран-3-ил)бензамид
Продукт примера 51 получали согласно процедуре, используемой для получения продукта примера 13b, заменяя продуктом примера 50c пример 13a и тетрагидрофуран-3-амином этиламин, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 1,87-1,94 (м, 1H), 2,10-2,19 (м, 1H), 3,57 (с, 3H), 3,67-3,73 (м, 2H), 3,81-3,87 (м, 2H), 4,42-4,49 (м, 1H), 6,22-6,23 (м, 1H), 6,85 (д, J=8,54 Гц, 1H), 7,07-7,13 (м, 1H), 7,25-7,34 (м, 3H), 7,42-7,47 (м, 1H), 7,85 (дд, J=8,85, 2,14, 1H), 7,96 (с, 1H), 8,00 (д, J=2,14 Гц, 1H), 8,50 (д, J=6,41 Гц, 1H), 12,03 (с, 1H). MS (ESI+) m/z 466,3 (M+H)+.
Пример 52
4-{2-(2,4-дифторфенокси)-5-[(1,1-диоксидотиоморфолин-4-ил)карбонил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 52 получали согласно процедуре, используемой для получения продукта примера 13b, заменяя 1,1-диоксо-1-тиоморфолином этиламин и продуктом примера 50c продукт примера 13a, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 3,25-3,28 (м, 4H), 3,56 (с, 3H), 3,78 (м, 4H), 4,45-4,61 (м, 1H), 3,81-3,87 (м, 2H), 6,26-6,27 (м, 1H), 6,86 (д, J=8,24 Гц, 1H), 7,07-7,12 (м, 1H), 7,27-7,33 (м, 3H), 7,42-7,48 (м, 2H), 7,63 (д, J=2,14, 1H), 12,04 (с, 1H). MS (ESI+) m/z 514,2 (M+H)+.
Пример 53
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-(1-метил-2-оксопирролидин-3-ил)бензамид
Продукт примера 53 получали согласно процедуре, используемой для получения продукта примера 13b, заменяя продуктом примера 50c продукт примера 13a и 3-амино-1-метилпирролидин-2-оном этиламин, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 1,87-1,97 (м, 1H), 2,29-2,38 (м, 1H), 2,76 (с, 3H), 3,30-3,34 (м, 2H), 3,57 (с, 3H), 4,45-4,61 (м, 1H), 3,81-3,87 (м, 2H), 4,42-4,49 (м, 1H), 6,23-6,24 (м, 1H), 6,87 (д, J=8,54 Гц, 1H), 7,08-7,13 (м, 1H), 7,25-7,34 (м, 3H), 7,43-7,48 (м, 1H), 7,85 (дд, J=8,54, 2,44 Гц, 1H), 7,96 (с, 1H), 7,99 (д, J=2,14 Гц, 1H), 8,73 (д, J=8,85 Гц, 1H), 12,03 (с, 1H). MS (ESI+) m/z 493,2 (M+H)+.
Пример 54
трет-бутил {1-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензоил]пирролидин-3-ил}карбамат
Продукт примера 54 получали согласно процедуре, используемой для получения продукта примера 13b, заменяя продуктом примера 50c продукт примера 13a и трет-бутил пирролидин-3-илкарбаматом этиламин, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 1,33-1,40 (м, 9H), 1,74-1,83 (м, 1H), 2,01-2,0,3 (м, 1H), 3,27-3,31 (м, 1H), 3,56 (с, 3H), 3,62-3,56 (м, 1H), 3,93-4,07 (м, 1H), 6,24 (д, J=2,29 Гц, 1H), 6,83 (д, J=8,54 Гц, 1H), 7,0-7,13 (м, 1H), 7,20-7,33 (м, 3H), 7,41-7,52 (м, 2H), 7,60 (д, J=16,2 Гц, 1H), 12,03 (с, 1H). MS (ESI+) m/z 565,2 (M+H)+.
Пример 55
4-[2-(2,4-дифторфенокси)-5-(пирролидин-1-илкарбонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 55 получали согласно процедуре, используемой для получения продукта примера 13b, заменяя продуктом примера 50c продукт примера 13a и пирролидином этиламин, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 1,82-1,86 (м, 4H), 3,45-3,48 (м, 4H), 3,56 (с, 3H), 6,24-6,26 (м, 1H), 6,82 (д, J=8,24 Гц, 1H), 7,06-7,12 (м, 1H), 7,26-7,33 (м, 3H), 7,41-7,46 (м, 1H), 7,52 (дд, J=8,54, 2,14 Гц, 1H), 7,61 (д, J=2,14 Гц, 1H), 12,03 (с, 1H). MS (ESI+) m/z 450,3 (M+H)+.
Пример 56
4-[2-(2,4-дифторфенокси)-5-(морфолин-4-илкарбонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 56 получали согласно процедуре, используемой для получения продукта примера 13b, заменяя продуктом примера 50c продукт примера 13a и морфолином этиламин, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 3,56 (с, 3H), 3,60-3,68 (м, 8H), 6,24-6,25 (м, 1H), 6,84 (д, J=8,54 Гц, 1H), 7,06-7,12 (м, 1H), 7,26-7,33 (м, 3H), 7,40 (дд, J=8,54, 2,14 Гц, 1H), 7,44-7,46 (м, 1H), 7,50 (дд, J=2,14 Гц, 1H), 12,03 (с, 1H). MS (ESI+) m/z 466,3 (M+H)+.
Пример 57
N-[4-(циклогексилокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Пример 57a
4-(2-(циклогексилокси)-5-нитрофенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 57a получали согласно процедуре, используемой для получения продукта примера 29a, заменяя циклогексанолом тетрагидро-2H-пиран-4-ол, получая указанное в заголовке соединение.
Пример 57b
4-(5-амино-2-(циклогексилокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 57b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 57a продукт примера 2b, получая указанное в заголовке соединение.
Пример 57c
N-[4-(циклогексилокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Продукт примера 57c получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 57b продукт примера 3, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 1,47-1,10 (м, 6H), 1,61-1,47 (м, 2H), 1,84-1,69 (м, 2H), 2,94 (с, 3H), 3,55 (с, 3H), 4,31-4,22 (м, 1H), 6,21 (т, J=2,3 Гц, 1H), 7,18-7,06 (м, 2H), 7,31-7,25 (м, 3H), 9,39 (с, 1H), 11,98 (ушир.с, 1H). MS (ESI+) m/z 416,2 (M+H)+.
Пример 58
N-[4-(циклопентилокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Пример 58a
4-(2-(циклопентилокси)-5-нитрофенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 58a получали согласно процедуре, используемой для получения продукта примера 29a, заменяя циклопентанолом тетрагидро-2H-пиран-4-ол, получая указанное в заголовке соединение.
Пример 58b
4-(5-амино-2-(циклопентилокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 58b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 58a продукт примера 2b, получая указанное в заголовке соединение.
Пример 58c
N-[4-(циклопентилокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Продукт примера 58c получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 58b продукт примера 3, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 1,70-1,43 (м, 6H), 1,88-1,70 (м, 2H), 2,94 (с, 3H), 3,55 (с, 3H), 4,78-4,70 (м, 1H), 6,16 (т, J=2,3 Гц, 1H), 7,06 (д, J=8,8 Гц, 1H), 7,16 (дд, J=8,7, 2,7 Гц, 1H), 7,22 (с, 1H), 7,30-7,23 (м, 2H), 9,39 (с, 1H), 11,97 (ушир.с, 1H),MS (ESI+) m/z 402,1 (M+H)+.
Пример 59
N-{4-[(4,4-дифторциклогексил)окси]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил}метансульфонамид
Пример 59a
4-(2-(4,4-дифторциклогексилокси)-5-нитрофенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 59a получали согласно процедуре, используемой для получения продукта примера 29a, заменяя 4,4-дифторциклогексанолом тетрагидро-2H-пиран-4-ол, получая указанное в заголовке соединение.
Пример 59b
4-(5-амино-2-(4,4-дифторциклогексилокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 59b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 59a продукт примера 2b, получая указанное в заголовке соединение.
Пример 59c
N-{4-[(4,4-дифторциклогексил)окси]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил}метансульфонамид
Продукт примера 59c получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 59b продукт примера 3, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 1,95-1,61 (м, 8H), 2,95 (с, 3H), 3,55 (с, 3H), 4,55-4,46 (м, 1H), 6,22-6,17 (м, 1H), 7,20-7,15 (м, 2H), 7,31-7,25 (м, 3H), 9,47 (с, 1H), 12,01 (ушир.с, 1H),MS (ESI+) m/z 452,2 (M+H)+.
Пример 60
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-3-илокси)фенил]метансульфонамид
Пример 60a
6-метил-4-(5-нитро-2-(тетрагидро-2H-пиран-3-илокси)фенил)-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 60a получали согласно процедуре, используемой для получения продукта примера 29a, заменяя тетрагидро-2H-пиран-3-олом тетрагидро-2H-пиран-4-ол, получая указанное в заголовке соединение.
Пример 60b
4-(5-амино-2-(тетрагидро-2H-пиран-3-илокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 60b получали согласно процедуре, используемой для получения продукта примера 29b, заменяя продуктом примера 60a продукт примера 29a, получая указанное в заголовке соединение.
Пример 60c
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-3-илокси)фенил]метансульфонамид
Продукт примера 60c получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 60b продукт примера 3, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 1,39-1,45 (м, 1H), 1,55-1,70 (м, 2H), 1,89-1,96 (м, 1H), 2,95 (с, 3H), 3,41-3,57 (м, 7H), 3,65-3,69 (м, 1H), 6,24-6,26 (м, 1H), 6,84 (д, J=8,54 Гц, 1H), 7,14 (м, 2H), 7,29-7,31 (м, 2H), 7,38 (с, 1H), 9,45 (с, 1H), 12,03 (с, 1H). MS (ESI+) m/z 418,2 (M+H)+.
Пример 61
6-метил-4-[2-(морфолин-4-илкарбонил)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 61 получали согласно процедуре, используемой для получения продукта примера 1f, заменяя морфолинo(2-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)метаноном 2-феноксифенилбороновую кислоту, с последующей очисткой препаративной ВЭЖХ (C18, 10-100% ацетoнитрил в 0,1% TFA в воде), получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 2,80-2,83 (м, 2H), 2,91-2,99 (м, 2H), 3,20-3,25 (м, 2H), 3,54-3,57 (м, 5H), 6,17-6,18 (м, 1H), 7,06 (с, 1H), 7,32 (т, J=2,9 Гц, 1H), 7,40 (д, J=7,32 Гц, 1H), 7,42-7,53 (м, 3H), 1H), 12,15 (с, 1H). MS (ESI+) m/z 338,1 (M+H)+.
Пример 62
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(2,4,6-трифторфенокси)фенил]этансульфонамид
Продукт примера 62 получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 33b продукт примера 3 и заменяя этансульфонил хлоридом метансульфонил хлорид, соответственно, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 1,22 (т, J=7,3 Гц, 3H), 3,09 (кв., J=7,3 Гц, 2H), 3,56 (с, 3H), 6,22 (т, J=2,3 Гц, 1H), 6,79 (д, J=8,8 Гц, 1H), 7,15 (дд, J=8,8, 2,7 Гц, 1H), 7,44-7,27 (м, 5H), 9,72 (с, 1H), 12,06 (ушир.с, 1H). MS (ESI+) m/z 478,1 (M+H)+.
Пример 63
N-[4-(бензилокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Пример 63a
4-(2-(бензилокси)-5-нитрофенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 63a получали согласно процедуре, используемой для получения продукта примера 29a, заменяя фенилметанолом тетрагидро-2H-пиран-4-ол, получая указанное в заголовке соединение.
Пример 63b
4-(5-амино-2-(бензилокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 63b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 63a продукт примера 2b, получая указанное в заголовке соединение.
Пример 63c
N-[4-(бензилокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Продукт примера 63c получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 63b продукт примера 3, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 2,94 (с, 3H), 3,51 (с, 3H), 5,07 (с, 2H), 6,24-6,18 (м, 1H), 7,22-7,16 (м, 2H), 7,37-7,24 (м, 8H), 9,45 (с, 1H), 12,00 (ушир.с, 1H). MS (ESI+) m/z 424,2 (M+H)+.
Пример 64
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-2-фторэтансульфонамид
Продукт примера 64 получали согласно процедуре, используемой для получения продукта примера 27c, заменяя 2-фторэтансульфонил хлоридом метансульфонил хлорид и игнорируя стадию гидролиза гидроксида натрия, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 3,52 (с, 3H), 3,63 (т, J=6,0 Гц, 2H), 4,12 (кв., J=6,0 Гц, 2H), 6,25-6,19 (м, 1H), 7,08-6,62 (м, 5H), 7,27-7,20 (м, 3H), 11,99-11,92 (м, 1H). MS (ESI+) m/z 478,2 (M+H)+.
Пример 65
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-N'-метилсерный диамид
Продукт примера 65 получали согласно процедуре, используемой для получения продукта примера 27c, заменяя метилсульфамоил хлоридом метансульфонил хлорид, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 2,50 (м, 3H растворитель скрыт), 3,52 (с, 3H), 6,28-6,22 (м, 1H), 7,08-6,86 (м, 3H), 7,15 (дд, J=8,8, 2,7 Гц, 1H), 7,39-7,21 (м, 5H), 9,65 (с, 1H), 12,02 (ушир.с, 1H). MS (ESI+) m/z 461,1 (M+H)+.
Пример 66
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидрофуран-3-илокси)фенил]этансульфонамид
Продукт примера 66 получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 31b продукт примера 3 и этансульфонил хлоридом метансульфонил хлорид, соответственно, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 1,22 (т, J=7,3 Гц, 3H), 1,93-1,80 (м, 1H), 2,20-2,04 (м, 1H), 3,02 (кв., J=7,3 Гц, 2H), 3,55 (с, 3H), 3,65 (м, 3H), 3,82 (дд, J=10,0, 4,5 Гц, 1H), 5,00-4,91 (м, 1H), 6,16 (т, J=2,3 Гц, 1H), 7,06 (д, J=8,8 Гц, 1H), 7,16 (дд, J=8,7, 2,7 Гц, 1H), 7,24 (с, 1H), 7,31-7,25 (м, 3H), 9,53 (с, 1H), 12,01 (ушир.с, 1H). MS (ESI+) m/z 418,1 (M+H)+.
Пример 67
Метил 6-метил-7-оксо-4-(2-феноксифенил)-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Пример 67a
Этил 4-бром-6-метил-7-оксо-1-тозил-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Диизопропиламин (0,111 г, 1,102 ммоль) в тетрагидрофуране (3 мл) обрабатывали BuLi (2,5 M, 0,44 мл, 1,102 ммоль) при -78°C. Раствор перемешивали в течение 20 минут при -78°C и нагревали до комнатной температуры в течение 5 минут и охлаждали до -78°C снова. К этому раствору добавляли N1,N1,N2,N2-тетраметилэтан-1,2-диамин (0,128 г, 1,102 ммоль). Затем продукт примера 1e (0,30 г, 0,787 ммоль) в тетрагидрофуране (3 мл) добавляли к реакционной смеси посредством канюли в атмосфере азота. Реакционную смесь перемешивали при -78°C в течение 1 часа, нагревали до 0°C коротко и охлаждали до -78°C. К этой суспензии добавляли этил карбонохлоридат (0,205 г, 1,889 ммоль) с помощью шприца. Реакционной смеси давали нагреться до комнатной температуры постепенно в течение ночи. Смесь затем распределяли между водой и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом три раза. Объединенные органические слои промывали насыщенным раствором соли, сушили над MgSO4, фильтровали и концентрировали. Остаток очищали флаш-хроматографией на силикагеле, элюируя 30-50% этилацетатом в гексанах, получая 0,074 г указанного в заголовке соединения.
Пример 67b
Метил 6-метил-7-оксо-4-(2-феноксифенил)-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Продукт примера 67b получали согласно процедуре, используемой для получения продукта примера 1f, заменяя продуктом примера 67a продукт примера 1e и пренебрегая применением карбоната калия, с последующей очисткой препаративной ВЭЖХ (C18, 10-100% ацетoнитрил в 0,1% TFA в воде), получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 3,50 (с, 3H), 3,80 (с, 3H), 6,80-6,82 (м, 3H), 7,00 (т, J=7,32 Гц, 1H), 7,06 (д, J=7,02 Гц, 1H), 7,23-7,32 (м, 4H), 7,40-7,42 (м, 1H), 7,52 (дд, J=7,48, 1,68 Гц, 1H), 12,85 (с, 1H). MS (ESI+) m/z 375 (M+H)+.
Пример 68
Метил 1,6-диметил-7-оксо-4-(2-феноксифенил)-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Указанное в заголовке соединение получали как побочный продукт из препарата продукта примера 67b. 1H ЯМР (500 МГц, DMSO-d6) δ 3,48 (с, 3H), 3,81 (с, 3H), 4,38 (с, 3H), 6,81-6,84 (м, 3H), 6,98-7,07 (м, 2H), 7,25-7,31 (м, 3H), 7,34 (с, 1H), 7,41-7,47 (м, 1H), 7,48 (дд, J=7,48, 1,68 Гц, 1H). MS (ESI+) m/z 389 (M+H)+.
Пример 69
Этил 4-(5-амино-2-феноксифенил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Пример 69a
Этил 1-бензил-4-бром-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Продукт примера 69a получали согласно процедуре, используемой для получения продукта примера 2a (способ B), заменяя продуктом примера 67a продукт примера 1e, получая указанное в заголовке соединение.
Пример 69b
Этил 6-метил-4-(5-нитро-2-феноксифенил)-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Продукт примера 69b получали согласно процедуре, используемой для получения продукта примера 2b, заменяя продуктом примера 69a продукт примера 2a, получая указанное в заголовке соединение.
Пример 69c
Этил 4-(5-амино-2-феноксифенил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Продукт примера 69c получали согласно процедуре, используемой для получения продукта примера 29b, заменяя продуктом примера 69b продукт примера 29a, и очищали препаративной ВЭЖХ (C18, 10-100% ацетoнитрил в 0,1% TFA/воде), получая TFA соль указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6) δ 1,30 (т, J=7,02 Гц, 3H), 3,49 (с, 3H), 4,27 (кв., J=7,12 Гц, 2H), 6,77 (д, J=7,93 Гц, 2H), 6,86 (д, J=2,14 Гц, 1H), 6,93-7,03 (м, 3H), 7,11 (с, 1H), 7,20-7,24 (м, 2H), 7,31 (с, 1H), 12,86 (с, 1H). MS (ESI+) m/z 404,1 (M+H)+.
Пример 70
6-метил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоновая кислота
Пример 70a
(Z)-этил 3-(5-бром-2-метокси-3-нитропиридин-4-ил)-2-гидроксиакрилат
К раствору этанола (15 мл) и простого эфира (150 мл) добавляли 5-бром-2-метокси-4-метил-3-нитропиридин (14,82 г, 60 ммоль), диэтил оксалат (13,15 г, 90 ммоль) и этоксид калия (6,06 г, 72 ммоль). Реакционную смесь нагревали при 45°C в течение 24 часов. Во время реакции колбу встряхивали рукой несколько раз. После охлаждения реакционную смесь распределяли между водой и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом три раза. Объединенные органические слои промывали насыщенным раствором соли, сушили над MgSO4, фильтровали и концентрировали. Остаток очищали флаш-хроматографией на силикагеле, элюируя 10-20% этилацетатом в гексанах до 9,5 г указанного в заголовке соединения (выход 46%).
Пример 70b
Этил 4-бром-7-метокси-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Смесь продукта примера 70a (9,5 г, 27,4 ммоль) и железа (7,64 г, 137 ммоль) в этаноле (60 мл) и уксусной кислоте (60 мл) нагревали при 100°C в течение 1 часа. Раствор превращался из красного в серый. Твердое вещество отфильтровывали и затем промывали дополнительным этилацетатом. Растворители удаляли при пониженном давлении до 20% исходного объема и это распределяли между водой и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом несколько раз. Объединенные органические слои промывали насыщенным раствором соли, сушили над MgSO4, фильтровали и концентрировали. Остаток очищали флаш-хроматографией на силикагеле, элюируя 20-40% этилацетатом в гексанах, получая 6,05 г указанного в заголовке соединения.
Пример 70c
Этил 1-бензил-4-бром-7-метокси-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Продукт примера 70b (0,88 г, 2,94 ммоль) в диметилформамиде (15 мл) обрабатывали 60% гидридом натрия (0,106 г, 4,41 ммоль, 0,117 г 60% дисперсия в масле). Раствор перемешивали при комнатной температуре в течение 10 минут. К этому раствору добавляли бензил бромид (0,59 г, 3,45 ммоль). Реакционную смесь перемешивали в течение еще 2 часов. Ее распределяли между водой и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным раствором соли, сушили над MgSO4, фильтровали и концентрировали. Остаток очищали флаш-хроматографией на силикагеле, элюируя 20-40% этилацетатом в гексанах, получая 1,07 г указанного в заголовке соединения.
Пример 70d
Этил 1-бензил-4-бром-7-оксо-6,7-дигидро-1H-пирроло[2,3-с]пиридин-2-карбоксилат
Продукт примера 70d получали согласно процедуре, используемой для получения продукта примера 1d, заменяя продуктом примера 70c продукт примера 1c, получая указанное в заголовке соединение.
Пример 70e
Этил 1-бензил-4-бром-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Продукт примера 70e получали согласно процедуре, используемой для получения продукта примера 1e, заменяя продуктом примера 70d продукт примера 1d, получая указанное в заголовке соединение.
Пример 70f
Этил 1-бензил-4-(2-фтор-5-нитрофенил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Продукт примера 70f получали согласно процедуре, используемой для получения продукта примера 2a (способ B), заменяя продуктом примера 70e продукт примера 1e, получая указанное в заголовке соединение.
Пример 70g
Этил 1-бензил-6-метил-4-(5-нитро-2-феноксифенил)-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Продукт примера 70g получали согласно процедуре, используемой для получения продукта примера 2b, заменяя продуктом примера 70f продукт примера 2a, получая указанное в заголовке соединение.
Пример 70h
Этил 4-(5-амино-2-феноксифенил)-1-бензил-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Продукт примера 70h получали согласно процедуре, используемой для получения продукта примера 29b, заменяя продуктом примера 70g пример 29a, получая указанное в заголовке соединение.
Пример 70i
Этил 1-бензил-6-метил-4-(5-(N-(метилсульфонил)метилсульфонамидо)-2-феноксифенил)-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Продукт примера 70i получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 70h продукт примера 3, за исключением применения 1M NaOH, получая указанное в заголовке соединение.
Пример 70j
Этил 6-метил-4-(5-(N-(метилсульфонил)метилсульфонамидо)-2-феноксифенил)-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Смесь продукта примера 70i (0,53 г, 0,816 ммоль), анизола (0,176 г, 1,631 ммоль) и концентрированной H2SО4 (0,5 мл) в TFA (10 мл) нагревали при 90°C в течение 4 часов. Избыток TFA удаляли при пониженном давлении и остаток распределяли между водой и этилацетатом. Органический слой отделяли и водный слой экстрагировали дополнительным этилацетатом несколько раз. Объединенные органические слои промывали насыщенным водным раствором бикарбоната натрия, а затем насыщенным раствором соли, сушили над MgSO4, фильтровали и концентрировали, получая 0,48 г указанного в заголовке соединения. Сырой материал использовали непосредственно для следующей реакции.
Пример 70k
6-метил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоновая кислота
Продукт примера 70j (0,4 г, 0,858 ммоль) в диоксане (5 мл) обрабатывали 2,0 н. NaOH (1,72 мл, 3,43 ммоль). Реакционную смесь нагревали при 65°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры и выливали в воду (100 мл). После добавления концентрированной HCl (1 мл) смесь экстрагировали этилацетатом три раза (3 × 30 мл). Объединенные органические слои промывали насыщенным раствором соли, сушили над MgSO4, фильтровали и концентрировали, получая 0,36 г (93%) указанного в заголовке соединения. Небольшое количество образца очищали препаративной ВЭЖХ (C18, 10-70% ацетoнитрил в 0,1% TFA/воде), получая TFA соль указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6) δ 3,03 (с, 3H), 3,49 (с, 3H), 6,81 (д, J=7,63 Гц, 2H), 6,84 (д, J=2,14 Гц, 1H), 6,96-7,00 (м, 1H), 7,08 (д, J=8,85 Гц, 1H), 7,22-7,27 (м, 3H), 7,34 (с, 1H), 7,37 (д, J=2,75 Гц, 1H), 9,77 (с, 1H), 12,62 (д, J=1,53 Гц, 1H), 13,00 (с, ушир., 1H). MS (ESI+) m/z 454,1 (M+H)+.
Пример 71
Этил 6-метил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Продукт примера 70k (0,2 г, 0,441 ммоль) в этаноле (10 мл) обрабатывали концентрированной H2SO4 (0,5 мл). Реакционную смесь нагревали при кипении с возвращением флегмы в течение ночи. Растворитель удаляли и остальное распределяли между водой и этилацетатом. Органический слой отделяли и водный слой экстрагировали дополнительным этилацетатом несколько раз. Объединенные органические слои промывали насыщ. NaHCO3, насыщенным раствором соли, сушили над MgSO4, фильтровали и концентрировали, получая 0,19 г указанного в заголовке соединения. Небольшое количество сырого продукта очищали препаративной ВЭЖХ, получая чистый продукт для биологического испытания. 1H ЯМР (500 МГц, DMSO-d6) δ 1,30 (т, J=7,17 Гц, 3H), 3,04 (с, 3H), 3,50 (с, 3H), 4,26 (кв., J=7,22 Гц, 2H), 6,80 (д, J=7,63 Гц, 2H), 6,86 (д, J=2,14 Гц, 1H), 6,96-7,00 (м, 1H), 7,09 (д, J=8,85 Гц, 1H), 7,21-7,28 (м, 3H), 7,35 (с, 1H), 7,36 (д, J=2,75 Гц, 1H), 9,78 (с, 1H), 12,86 (с, 1H), (ESI+) m/z 482,1 (M+H)+.
Пример 72
N-этил-6-метил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид
Пример 72a
6-метил-4-(5-(метилсульфонамидо)-2-феноксифенил)-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбонил хлорид
Продукт примера 72a получали согласно процедуре, используемой для получения продукта примера 13a, заменяя продуктом примера 70k продукт примера 10, получая указанное в заголовке соединение.
Пример 72b
N-этил-6-метил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид
Продукт примера 72b получали согласно процедуре, используемой для получения продукта примера 13b, заменяя продуктом примера 72a продукт примера 13a, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 1,12 (т, J=7,17 Гц, 3H), 3,03 (с, 3H), 3,23-3,30 (М, 2H), 3,49 (с, 3H), 6,81 (д, J=7,63 Гц, 2H), 6,86 (д, J=2,44 Гц, 1H), 6,96-7,00 (м, 1H), 7,07 (д, J=8,54 Гц, 1H), 7,22-7,28 (м, 3H), 7,30 (с, 1H), 7,34 (д, J=2,75 Гц, 1H), 8,34 (т, J=5,34 Гц, 1H), 9,79 (с, 1H), 12,22 (с, 1H), (ESI+) m/z 481,1 (M+H)+.
Пример 73
6-метил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид
Пример 73 получали согласно процедуре, используемой для получения продукта примера 13b, заменяя продуктом примера 72a продукт примера 13a и водным гидроксидом аммония этиламин, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 3,03 (с, 3H), 3,50 (с, 3H), 6,82 (д, J=7,63 Гц, 2H), 6,88 (д, J=2,44 Гц, 1H), 6,97-7,01 (м, 1H), 7,06 (д, J=8,54 Гц, 1H), 7,22-7,28 (м, 3H), 7,31 (с, 1H), 7,35 (д, J=2,75 Гц, 1H), 7,46 (с, 1H), 7,81 (с, 1H), 9,78 (с, 1H), 12,22 (с, 1H). MS (ESI+) m/z 453,1 (M+H)+.
Пример 74
Этил 4-(5-амино-2-феноксифенил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-2-карбоксилат
Пример 74a
4-амино-6-хлор-2-метилпиридазин-3(2H)-он
Смесь 4,6-дихлор-2-метилпиридазин-3(2H)-она (5,0 г, 27,9 ммоль) и гидроксида аммония (55 мл, 1412 ммоль) нагревали при 150°C в течение 2 часов и затем охлаждали до комнатной температуры. Растворитель удаляли и остаток растворяли в этилацетате и промывали водой. Водный слой экстрагировали дополнительным этилацетатом три раза. Объединенные органические слои промывали насыщенным раствором соли, сушили и концентрировали. Остаток очищали флаш-хроматографией (силикагель, элюировали 40% этилацетатом в гексанах), получая 3,85 г (87%) указанного в заголовке соединения.
Пример 74b
4-амино-6-хлор-5-йод-2-метилпиридазин-3(2H)-он
Смесь продукта примера 74a (2,12 г, 13,3 ммоль) и N-йодсукцинимида (5,38 г, 23,9 ммоль) в ацетoнитриле (30 мл) нагревали при кипении с возвращением флегмы в течение 6 часов. Реакционную смесь охлаждали до комнатной температуры и распределяли между этилацетатом и водой. Водный слой экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным раствором соли, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией на силикагеле, элюируя 20-40% этилацетатом в гексанах, получая 3,27 г (86%) указанного в заголовке соединения.
Пример 74c
4-хлор-6-метил-7-оксо-6,7-дигидро-1H-пирроло[3,2-d]пиридазин-2-карбоновая кислота
Смесь продукта примера 74b (0,59 г, 2,1 ммоль), пировиноградной кислоты (0,546 г, 6,2 ммоль), 1,4-диазабицикло[2.2.2]октана (0,695 г, 6,2 ммоль) и палладий(II)ацетата (0,046 г, 10 мол.%) в диметилформамиде (8 мл) дегазировали и снова насыщали азотом три раза. Реакционную смесь затем нагревали при 105°C в течение ночи. Реакционную смесь охлаждали до комнатной температуры и распределяли между этилацетатом и водой. Водный слой экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным раствором соли, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток растирали в 30% этилацетате в гексанах, получая 0,25 г (53%) указанного в заголовке соединения.
Пример 74d
Этил 4-хлор-6-метил-7-оксо-6,7-дигидро-1H-пирроло[3,2-d]пиридазин-2-карбоксилат
Продукт примера 74c (0,45 г, 2,0 ммоль) в этаноле (15 мл) обрабатывали концентрированной серной кислотой (1 мл). Реакционную смесь нагревали при кипении с возвращением флегмы в течение 16 часов. Реакционную смесь охлаждали до комнатной температуры и распределяли между этилацетатом и водой. Водный слой экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным раствором соли, сушили над безводным сульфатом магния, фильтровали и концентрировали, получая 0,45 г (89%) указанного в заголовке соединения.
Пример 74e
Этил 4-хлор-6-метил-7-оксо-1-((2-(триметилсилил)этокси) метил)-6,7-дигидро-1H-пирроло[3,2-d] пиридазин-2-карбоксилат
Раствор продукта примера 74d (0,41 г, 1,6 ммоль) в диметилформамиде (15 мл) обрабатывали 60% гидридом натрия (0,096 г, 2,4 ммоль) при комнатной температуре. Реакционную смесь перемешивали в течение 30 мин и затем обрабатывали (2-(хлорметокси)этил)триметилсиланом (0,40 г, 2,4 ммоль). Реакционную смесь затем перемешивали в течение 2 часов. Ее распределяли между этилацетатом и водой. Водный слой экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным раствором соли, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией на силикагеле, элюируя 20% этилацетатом, получая 0,50 г (81%) указанного в заголовке соединения.
Пример 74f
Этил 4-(2-фтор-5-нитрофенил)-6-метил-7-оксо-1-((2-(триметилсилил)этокси)метил)-6,7-дигидро-1H-пирроло[3,2-d]пиридазин-2-карбоксилат
Продукт примера 74f получали согласно процедуре, используемой для получения продукта примера 2a (способ B), заменяя продуктом примера 74e продукт примера 1e, получая указанное в заголовке соединение.
Пример 74g
Этил 6-метил-4-(5-нитро-2-феноксифенил)-7-оксо-6,7-дигидро-1H-пирроло[3,2-d]пиридазин-2-карбоксилат
Смесь продукта примера 74f (0,26 г, 0,53 ммоль), фенола (0,060 г, 0,64 ммоль) и карбоната цезия (0,21 г, 0,63 ммоль) в диметилсульфоксиде (5 мл) нагревали при 110°C в течение 6 часов. После охлаждения до комнатной температуры реакционную смесь распределяли между водой и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом три раза. Объединенные органические слои промывали насыщенным раствором соли, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток затем обрабатывали 15 мл этанола и 1 мл концентрированной H2SO4. Смесь нагревали при кипении с возвращением флегмы в течение ночи. Реакционную смесь охлаждали до комнатной температуры и распределяли между этилацетатом и водой. Органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией на силикагеле, элюируя 40-80% этилацетатом, получая 0,14 г (61%) указанного в заголовке соединения.
Пример 74h
Этил 4-(5-амино-2-феноксифенил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-2-карбоксилат
Продукт примера 74h получали согласно процедуре, используемой для получения продукта примера 29b, заменяя продуктом примера 74g продукт примера 29a и этанолом этилацетат, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 1,29 (т, J=7,02 Гц, 3H), 3,61 (с, 3H), 4,28 (кв., J=7,22 Гц, 2H), 5,22 (с, 2H), 6,65 (д, J=7,33 Гц, 2H), 6,74 (дд, J=8,85, 2,75 Гц, 1H), 6,79 (т, J=2,75 Гц, 1H), 6,87 (д, J=7,32 Гц, 1H), 6,91-6,93 (м, 2H), 7,13-7,17 (м, 2H), 13,37 (ушир. с, 1H). MS (ESI+) m/z 405,1 (M+H)+.
Пример 75
Этил 4-[5-(этиламино)-2-феноксифенил]-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-2-карбоксилат
Продукт примера 75 получали как побочный продукт из препарата продукта примера 74h. 1H ЯМР (500 МГц, DMSO-d6) δ 1,19 (т, J=7,17 Гц, 3H), 1,30 (т, J=7,02 Гц, 3H), 3,03-3,08 (м, 2H), 3,62 (с, 3H), 4,29 (кв., J=7,02 Гц, 2H), 5,71 (т, J=5,19 Гц, 1H), 6,65 (д, J=7,63 Гц, 2H), 6,72-6,74 (м, 2H), 6,87 (т, J=7,32 Гц, 1H), 6,91 (с, 1H), 6,99 (д, J=9,16 Гц, 1H), 7,13-7,17 (м, 2H), 13,47 (ушир. с, 1H). MS (ESI+) m/z 433,1 (M+H)+.
Пример 76
Этил 4-{5-[этил(метилсульфонил)амино]-2-феноксифенил}-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-2-карбоксилат
Продукт примера 76 получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 75 продукт примера 3, за исключением применения NaOН, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 1,07 (т, J=7,02 Гц, 3H), 1,30 (т, J=7,17 Гц, 3H), 3,02 (с, 3H), 3,67-3,72 (м, 5H),4,23 (кв., J=7,22 Гц, 2H), 6,93 (д, J=7,93 Гц, 2H), 6,99 (д, J=2,14 Гц, 1H), 7,07-7,12 (м, 2H), 7,30-7,34 (м, 2H), 7,52-7,55 (м, 1H), 7,85 (д, J=2,75 Гц, 1H). MS (ESI+) m/z 511,1 (M+H)+.
Пример 77
6-метил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-2-карбоновая кислота
Продукт примера 77 получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 74h продукт примера 3, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 3,04 (с, 3H), 3,66 (с, 3H), 6,39-6,40 (м, 1H), 6,81-6,83 (м, 2H), 6,93 (д, J=1,53 Гц, 1H), 6,98-7,01 (м, 1H), 7,14 (д, J=8,85 Гц, 1H), 7,23-7,27 (м, 2H), 7,37-7,42 (м, 1H), 7,43 (д, J=2,75 Гц, 1H), 9,82 (с, 1H), 13,35 (с, 1H). MS (ESI+) m/z 455,1 (M+H)+.
Пример 78
6-метил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H- пирроло[2,3-d]пиридазин-2-карбоксамид
Пример 78a
6-метил-4-(5-(метилсульфонамидо)-2-феноксифенил)-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-2-карбонил хлорид
Продукт примера 78a получали согласно процедуре, используемой для получения продукта примера 13a, заменяя продуктом примера 77 продукт примера 10, получая указанное в заголовке соединение.
Пример 78b
6-метил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-2-карбоксамид
Продукт примера 78b получали согласно процедуре, используемой для получения продукта примера 13b, заменяя продуктом примера 78a продукт примера 13a и водным гидроксидом аммония этиламин, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 3,03 (с, 3H), 3,67 (с, 3H), 6,85 (д, J=7,63 Гц, 2H), 6,99-7,04 (м, 2H), 7,10 (д, J=8,54 Гц, 1H), 7,23-7,28 (м, 2H), 7,37-7,40 (м, 2H), 7,57 (с, 1H), 7,91 (с, 1H), 9,82 (с, 1H), 12,95 (с, 1H). MS (ESI+) m/z 454,1 (M+H)+.
Пример 79
6-метил-N-[2-(4-метилпиперазин-1-ил)этил]-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-2-карбоксамид
Продукт примера 79 получали согласно процедуре, используемой для получения продукта примера 13b, заменяя продуктом примера 78a продукт примера 13a и 2-(4-метилпиперазин-1-ил)этанамином этиламин, соответственно, получая TFA соль указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6) δ 2,67-2,80 (м, 6H), 3,04 (с, 3H), 3,49 (ушир., 8H), 3,67 (с, 3H), 6,82 (д, J=7,63 Гц, 2H), 6,99-7,03 (м, 2H), 7,13 (д, J=8,85 Гц, 1H), 7,24-7,28 (м, 2H), 7,37-7,40 (м, 2H), 8,50-8,52 (м, 1H), 9,85 (с, 1H), 13,03 (с, 1H). MS (ESI+) m/z 580,2 (M+H)+.
Пример 80
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-4-ил)-4-феноксифенил]метансульфонамид
Пример 80a
(E)-4-амино-6-хлор-5-(2-этоксивинил)-2-метилпиридазин-3(2H)-он
Продукт примера 80a получали согласно процедуре, используемой для получения продукта примера 2a (способ B), заменяя продуктом примера 74b продукт примера 1e и (E)-2-(2-этоксивинил)-4,4,5,5-тетраметил-1,3,2-диоксабороланом 2-фтор-5-нитрофенилбороновую кислоту, соответственно, получая указанное в заголовке соединение.
Пример 80b
4-хлор-6-метил-1H-пирроло[3,2-d]пиридазин-7(6H)-он
Продукт примера 80a (0,1 г, 0,435 ммоль) в уксусной кислоте (5 мл) нагревали при 90°C в течение ночи. Растворитель выпаривали при пониженном давлении, получая 0,071 г указанного в заголовке соединения.
Пример 80c
4-хлор-6-метил-1-((2-(триметилсилил)этокси)метил)-1H-пирроло[3,2-d]пиридазин-7(6H)-он
Продукт примера 80c получали согласно процедуре, используемой для получения продукта примера 74e, заменяя продуктом примера 80b продукт примера 74c, получая указанное в заголовке соединение.
Пример 80d
4-(2-фтор-5-нитрофенил)-6-метил-1-((2-(триметилсилил)этокси)метил)-1H-пирроло[3,2-d]пиридазин-7(6H)-он
Продукт примера 80d получали согласно процедуре, используемой для получения продукта примера 2a (Способ B), заменяя продуктом примера 80c продукт примера 1e, получая указанное в заголовке соединение.
Пример 80e
6-метил-4-(5-нитро-2-феноксифенил)-1H-пирроло[3,2-d]пиридазин-7(6H)-он
Продукт примера 80e получали согласно процедуре, используемой для получения продукта примера 2b, заменяя продуктом примера 80d продукт примера 2a, получая указанное в заголовке соединение.
Пример 80f
4-(5-амино-2-феноксифенил)-6-метил-1H-пирроло[3,2-d]пиридазин-7(6H)-он
Продукт примера 80f получали согласно процедуре, используемой для получения продукта примера 29b, заменяя продуктом примера 80e продукт примера 29a, получая указанное в заголовке соединение.
Пример 80g
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-4-ил)-4-ил)феноксифенил]метансульфонамид
Продукт примера 80g получали согласно процедуре, используемой в способе A примера 4, заменяя продуктом примера 80f продукт примера 3, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 3,03 (с, 3H), 3,67 (с, 3H),6,39-6,40 (м, 1H), 6,87 (д, J=7,63 Гц, 2H), 7,01 (т, J=7,48 Гц, 1H), 7,08 (д, J=8,54 Гц, 1H), 7,24-7,28 (м, 2H), 7,35 (дд, J=8,85, 2,75 Гц, 1H), 7,42-7,43 (м, 2H), 9,80 (с, 1H), 12,67 (с, 1H). MS (ESI+) m/z 411,1 (M+H)+.
Пример 81
N-этил-6-метил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-2-карбоксамид
Продукт примера 81 получали согласно процедуре, используемой для получения продукта примера 13b, заменяя продуктом примера 78a продукт примера 13a, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 1,12 (т, J=7,17 Гц, 3H), 3,03 (с, 3H), 3,27-3,30 м, 2H), 3,66 (с, 3H), 6,82-6,84 (м, 2H), 6,98-7,02 (м, 2H), 6,97-7,01 (м, 1H), 7,12 (д, J=9,16 Гц, 1H), 7,23-7,28 (м, 2H), 7,37-7,40 (м, 2H), 8,44 (т, J=5,34 Гц, 1H), 9,83 (с, 1H), 12,97 (с, 1H). MS (ESI+) m/z 482,1 (M+H)+.
Пример 82
6-метил-4-(2-феноксифенил)-1,6-дигидро-7H-пирроло[2,3-d]пиридазин-7-он
Продукт примера 82 получали согласно процедуре, используемой для получения продукта примера 1f, заменяя продуктом примера 80b продукт примера 1e, за исключением применения карбоната калия, с последующей очисткой препаративной ВЭЖХ (C18, 10-100% ацетoнитрил в 0,1% TFA в воде), получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 3,70 (с, 3H), 6,36-6,37 (м, 1H), 6,91-6,93 (м, 2H), 7,02-7,07 (м, 2H), 7,27-7,31 (м, 3H), 7,41 (т, J=2,75 Гц, 1H), 7,47-7,52 (м, 1H), 7,56 (дд, J=7,63, 1,83 Гц, 1H), 12,65 (с, 1H). MS (ESI+) m/z 318,1 (M+H)+.
Пример 83
N-этил-N,6-диметил-4-{5-[(метилсульфонил)амино]-2-феноксифенил}-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-2-карбоксамид
Продукт примера 83 получали согласно процедуре, используемой для получения продукта примера 13b, заменяя продуктом примера 78a продукт примера 13a и N-метилэтанамином этиламин, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 1,07 (ушир., 3H), 2,94 (с, 3H), 3,03 (с, 3H), 3,45 (ушир., 2H), 3,68 (с, 3H), 6,88 (д, J=7,93 Гц, 2H), 7,01 (т, J=7,32 Гц, 1H), 7, 12 (д, J=8,85 Гц, 1H), 7,24-7,28 (м, 2H), 7,36 (дд, J=8,85, 2,75 Гц, 1H), 7,43 (д, J=2,75 Гц, 1H), 9,81 (с, 1H), 13,01 (с, 1H). MS (ESI+) m/z 496,1 (M+H)+.
Пример 84
4-{4-[(этилсульфонил)амино]-2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенокси}бензамид
К смеси продукта примера 33b (50 мг, 0,14 ммоль) и триэтиламина (0,043 г, 0,42 ммоль) в дихлорметане (4 мл) добавляли по каплям этансульфонил хлорид (0,072 г, 0,56 ммоль) и реакционную смесь перемешивали при температуре окружающей среды в течение 1 часа. Реакционную смесь концентрировали при пониженном давлении, диоксан (4 мл) и гидроксид натрия (10% м/о, 3 мл, 0,14 ммоль) добавляли и реакционную смесь нагревали при 70°C в течение 1 часа. Смесь охлаждали до температуры окружающей среды и затем нейтрализовали насыщенным водным раствором хлорида аммония (50 мл) до pH 7. Органический слой отделяли и водную фазу экстрагировали этилацетатом (3 × 25 мл). Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили (безводный сульфат магния), фильтровали и концентрировали. Остаток очищали препаративной ВЭЖХ (C18, 10-100% ацетoнитрил/вода, 0,1% TFA), получая указанное в заголовке соединение (22 мг, 35%). 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,01 (с, 1H) 9,86 (с, 1H) 7,77 (с, 1H) 7,74 (д, J=8,82 Гц, 2H) 7,42 (д, J=2,37 Гц, 1H) 7,22-7,30 (м, 3H) 7,18 (с, 1H) 7,11-7,16 (м, 1H) 6,83 (д, J=8,82 Гц, 2H) 6,23-6,28 (м, 1H) 3,47 (с, 3H) 3,15 (кв., J=7,35 Гц, 2H) 1,21-1,29 (м, 3H). MS (ESI+) m/z 467,2 (M+H)+.
Пример 85
6-метил-4-[5-(метилсульфонил)-2-феноксифенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 85a
4-(метилсульфонил)-2-нитро-1-феноксибензол
Продукт примера 85a получали согласно процедуре, используемой для получения продукта примера 2b, заменяя 1-фтор-4-(метилсульфонил)-2-нитробензолом продукт примера 2a, получая указанное в заголовке соединение.
Пример 85b
5-(метилсульфонил)-2-феноксианилин
Продукт примера 85b получали согласно процедуре, используемой для получения продукта примера 29b, заменяя продуктом 85a продукт примера 29a, получая указанное в заголовке соединение.
Пример 85c
2-йод-4-(метилсульфонил)-1-феноксибензол
Продукт примера 85b (0,27 г, 1,025 ммоль) в диоксане (1 мл) обрабатывали концентрированной HCl (6 мл) при 0°C. Реакционную смесь перемешивали при 0°C в течение 10 минут. К этому раствору добавляли нитрит натрия (0,085 г, 1,23 ммоль) в воде (1 мл). Реакционную смесь перемешивали при 0°C в течение еще 1 часа. К этому раствору добавляли йодид калия (0,34 г, 1,051 ммоль) в воде (2 мл). Реакционную смесь перемешивали в течение 1 часа при комнатной температуре. Реакционную смесь распределяли между водой и этилацетатом. Органический слой экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным раствором соли, сушили над MgSO4, фильтровали и концентрировали. Остаток очищали флаш-хроматографией на силикагеле, элюируя 10-30% этилацетатом в гексанах, получая 0,28 г указанного в заголовке продукта.
Пример 85d
6-метил-4-[5-(метилсульфонил)-2-феноксифенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 85d получали согласно процедуре, используемой для получения продукта примера 1f, заменяя продуктом 85c продукт примера 1e и продуктом примера 6a 2-феноксифенилбороновую кислоту с последующей очисткой препаративной ВЭЖХ (C18, 10-100% ацетoнитрил/0,1% TFA в воде), получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 3,26 (с, 3H), 3,57 (с, 3H), 6,29-6,30 (м, 1H), 7,03 (д, J=8,54 Гц, 1H), 7,11 (д, J=7,63 Гц, 2H), 7,20 (т, J=7,32 Гц, 1H), 7,30 (т, J=2,75 Гц, 1H), 7,40-7,44 (м, 3H), 7,88 (дд, J=8,54, 2,44 Гц, 1H), 8,00 (д, J=2,44 Гц, 1H), 12,07 (с, 1H). MS (ESI+) m/z 395,2 (M+H)+.
Пример 86
5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-6-(тетрагидрофуран-3-илокси)пиридин-3-сульфонамид
Пример 86a
5-бром-6-хлорпиридин-3-сульфонамид
5-Бром-6-хлорпиридин-3-сульфонил хлорид (8,2 г) в метаноле (20 мл) охлаждали до 0°C. К этому раствору добавляли 7н. NH3 в метаноле (80 мл). Реакционную смесь перемешивали в течение ночи при комнатной температуре. Растворитель удаляли при низкой температуре и остаток распределяли между этилацетатом и водой. Водный слой экстрагировали этилацетатом три раза. Объединенные органические слои промывали насыщенным раствором соли, сушили (MgSО4), фильтровали и концентрировали. Твердое вещество очищали колоночной флаш-хроматографией на силикагеле, получая 4,2 г чистого продукта.
Пример 86b
5-бром-6-(тетрагидрофуран-3-илокси)пиридин-3-сульфонамид
Продукт примера 86b получали согласно процедуре, используемой для получения продукта примера 29a, заменяя продуктом 86a продукт примера 2a и тетрагидрофуран-3-олом тетрагидро-2H-пиран-4-ол, получая указанное в заголовке соединение.
Пример 86c
5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-6-(тетрагидрофуран-3-илокси)пиридин-3-сульфонамид
Продукт примера 86c получали согласно процедуре, используемой для получения продукта примера 1f, заменяя продуктом 86b продукт примера 1e и продуктом примера 6a 2-феноксифенилбороновую кислоту с последующей очисткой препаративной ВЭЖХ (C18, 10-100% ацетoнитрил в 0,1% TFA в воде), получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 1,91-1,97 (м, 1H), 2,18-2,25 (м, 1H), 3,59 (с, 3H), 3,66-3,76 (м, 3H), 3,92-3,95 (м, 1H), 5,63-5,66 (м, 1H), 6,19-6,21 (м, 1H), 7,34 (т, J=2,75 Гц, 1H), 7,41 (с, 1H), 7,47 (с, 2H), 8,14 (д, J=2,44 Гц, 1H), 8,54 (д, J=2,44 Гц, 1H), 12,11 (с, 1H). MS (ESI+) m/z 391,1 (M+H)+.
Пример 87
N-метил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-6-(тетрагидрофуран-3-илокси)пиридин-3-сульфонамид
Продукт примера 87 получали как побочный продукт из препарата продукта примера 86c. 1H ЯМР (500 МГц, DMSO-d6) δ 1,93-1,98 (м, 1H), 2,17-2,24 (м, 1H), 2,48 (д, J=5,19 Гц, 3H), 3,57 (с, 3H), 3,67-3,78 (м, 3H), 3,91-3,94 (м, 1H), 5,65-5,67 (м, 1H), 6,19 (т, J=2,29 Гц, 1H), 7,33 (т, J=2,75 Гц, 1H), 7,43 (с, 1H), 7,55 (кв., J=4,88 Гц, 1H), 8,06 (д, J=2,44 Гц, 1H), 8,51 (д, J=2,44 Гц, 1H), 12,13 (с, 1H). MS (ESI+) m/z 405,1 (M+H)+.
Пример 88
6-метил-4-(2-феноксифенил)-2-фенил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
4-бром-2-йод-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Пример 88a
К холодному (-78°C, баня сухой лед/ацетон) раствору продукта примера 1e (0,2 г, 0,525 ммоль) в тетрагидрофуране (6 мл) добавляли свежеприготовленный раствор литий ди-изопропиламида (1,2 эквивалента). Реакционную смесь перемешивали при -78°C в течение 45 минут. Раствор йода (0,054 мл, 1,049 ммоль) в тетрагидрофуране (0,5 мл) добавляли при -78°C. Охлаждающую баню удаляли и реакционной смеси позволяли нагреться до комнатной температуры и перемешивали в течение 1 часа. Реакцию гасили добавлением насыщенного водного раствора тиосульфата натрия (20 мл). Реакционную смесь распределяли между водой и этилацетатом. Слои разделяли и водный слой экстрагировали дополнительным этилацетатом. Объединенные органические вещества промывали насыщенным раствором соли, сушили безводным MgSO4, фильтровали и концентрировали до сухости. Остаток очищали флаш-хроматографией (силикагель, 1-100% этилацетат/гексан). Извлеченный материал дополнительно очищали ВЭЖХ с обращенной фазой (C18, 10-100% ацетoнитрил в 0,1% TFA/воде), получая указанное в заголовке соединение (55 мг, 21%).
Пример 88b
4-бром-6-метил-2-фенил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Смесь продукта примера 88a (0,1 г, 0,197 ммоль), фенилбороновой кислоты (0,024 г, 0,197 ммоль), Pd(PPh3)4 (0,011 г, 0,0096 ммоль) и гидрокарбоната натрия (0,041 г, 0,493 ммоль) в диметилформамиде (2 мл) и воде (0,6 мл) нагревали при 85°C в течение 4 часов. После охлаждения реакционную смесь распределяли между водой и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным раствором соли, сушили над MgSО4, фильтровали и концентрировали. Остаток очищали флаш-хроматографией на силикагеле, элюируя 30% этилацетатом, получая 0,084 г указанного в заголовке соединения.
Пример 88c
6-метил-4-(2-феноксифенил)-2-фенил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 88c получали согласно процедуре, используемой для получения продукта примера 1f, заменяя продуктом 88b продукт примера 1e с последующей очисткой препаративной ВЭЖХ (C18, 10-100% ацетoнитрил в 0,1% TFA в воде), получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 3,53 (с, 3H), 6,67 (д, J=1,22 Гц, 1H), 6,93 (д, J=7,63 Гц, 2H), 7,01-7,04 (м, 2H), 7,26-7,31 (м, 5H), 7,36-7,43 (м, 3H), 7,56 (дд, J=7,48, 1,68 Гц, 1H), 7,89 (д, J=7,32 Гц, 1H), 12,31 (с, 1H). MS (ESI+) m/z 393,3 (M+H)+.
Пример 89
N-{3-[2-(гидроксиметил)-6-метил-7-оксо-6,7-дигидро-1Н-пирроло[2,3-c]пиридин-4-ил]-4-феноксифенил}метансульфонамид
Пример 89 получали согласно процедуре, используемой для получения продукта примера 20b, заменяя продуктом примера 71 продукт примера 20a, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 3,02 (с, 3H), 3,47 (с, 3H), 4,50 (с, 2H), 6,19 (д, J=1,83 Гц, 1H), 6,82 (д, J=7,63 Гц, 2H), 6,99 (т, J=7,32 Гц, 1H), 7,05 (д, J=8,85 Гц, 1H), 7,21-7,27 (м, 4H), 7,38 (д, J=2,75 Гц, 1H), 9,75 (с, 1H), 11,60 (с, 1H). MS (ESI+) m/z 440,1 (M+H)+.
Пример 90
N-[4-(4-цианофенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид
Пример 90a
4-(2-бром-4-нитрофенокси)бензонитрил
Продукт примера 90a получали согласно процедуре, используемой для получения продукта примера 7a, заменяя 4-гидроксибензонитрилом фенол, получая указанное в заголовке соединение.
Пример 90b
4-(4-амино-2-бромфенокси)бензонитрил
В работающий под давлением сосуд из нержавеющей стали емкостью 250 мл добавляли продукт примера 90a (3,21 г, 10,1 ммоль), оксид платины(IV) (0,642 г, 2,83 ммоль) и тетрагидрофуран (70 мл) в потоке азота. Реакционную колбу заполняли водородом до 0,207 МПа (30 фунтов на кв. дюйм) и содержимое перемешивали при температуре окружающей среды в течение 45 минут. Смесь фильтровали через нейлоновую мембрану. Фильтрат концентрировали. Остаток очищали флаш-хроматографией (силикагель, 1:1 этилацетат/гексаны), получая указанное в заголовке соединение (1,75 г, выход 60%).
Пример 90c
4-(4-амино-2-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенокси)бензонитрил
Смесь продукта примера 90b (1,75 г, 6,05 ммоль), 4,4,4',4',5,5,5',5'-октаметил-2,2'-би(1,3,2-диоксаборолана) (3,07 г, 12,1 ммоль), 1,3,5,7-тетраметил-6-фенил-2,4,8-триокса-6-фосфаадаманта (0,159 г, 0,545 ммоль), ацетата калия (1,31 г, 13,3 ммоль) и трис(дибензилиденацетон)дипалладия(0) (0,166 г, 0,182 ммоль) в диоксане (30 мл) дегазировали и снова насыщали азотом. Реакционную смесь нагревали при 80°C в течение 20 часов и затем охлаждали до температуры окружающей среды. Смесь концентрировали и остаток распределяли между этилацетатом и водой. Органический слой отделяли и промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, гексан/этилацетат), получая указанное в заголовке соединение (2,0 г, выход 98%).
Пример 90d
4-(4-амино-2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенокси)бензонитрил
Продукт примера 90d получали согласно процедуре, используемой для получения продукта примера 1f, заменяя продуктом примера 90c 2-феноксифенилбороновую кислоту, с очисткой препаративной ВЭЖХ (C18, 10-100% ацетoнитрил в 0,1% TFA в воде), получая указанное в заголовке соединение.
Пример 90e
N-[4-(4-цианофенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид
Продукт примера 90e получали согласно процедуре, используемой для получения продукта примера 4, способ A, заменяя этансульфонил хлоридом метансульфонил хлорид и продуктом примера 90d продукт примера 3, соответственно, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,01-12,05 (м, 1H) 9,94 (с, 1H) 7,62-7,69 (м, 2H) 7,43 (д, J=2,75 Гц, 1H) 7,21-7,33 (м, 4H) 6,86-6,93 (м, 2H) 6,22 (дд, J=2,75, 2,14 Гц, 1H) 3,46 (с, 3H) 3,16 (кв., J=7,32 Гц, 2H) 1,25 (т, J=7,32 Гц, 3H). MS (ESI+) m/z 449,1 (M+H)+.
Пример 91
2-фтор-N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидрофуран-3-илокси)фенил]этансульфонамид
Пример 91a
6-метил-4-(5-нитро-2-(тетрагидрофуран-3-илокси)фенил)-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 91a получали согласно процедуре, используемой для получения продукта примера 29a, заменяя тетрагидрофуран-3-олом тетрагидро-2H-пиран-4-ол, получая указанное в заголовке соединение.
Пример 91b
4-(5-амино-2-(тетрагидрофуран-3-илокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 91b получали согласно процедуре, используемой для получения продукта примера 29b, заменяя продуктом примера 91a продукт примера 29a, получая указанное в заголовке соединение.
Пример 91c
2-фтор-N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-с]пиридин-4-ил)-4-(тетрагидрофуран-3-илокси)фенил]этансульфонамид
К смеси продукта примера 91b (80,0 мг, 0,246 ммоль) и триэтиламина (74,6 мг, 0,738 ммоль) в дихлорметане (4 мл) добавляли по каплям 2-фторэтансульфонил хлорид (144 мг, 0,984 ммоль) и реакционную смесь перемешивали при температуре окружающей среды около 1 часа. Реакционную смесь нейтрализовали насыщенным водным раствором хлорида аммония (50 мл) и смесь экстрагировали этилацетатом (3 × 50 мл). Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили (безводный сульфат магния), фильтровали и концентрировали. Остаток очищали препаративной ВЭЖХ (C18, 10-80% ацетoнитрил в 0,1% TFA/воде), получая указанное в заголовке соединение (7,0 мг, выход 6,5%). 1H ЯМР (300 МГц, CDCl3) δ м.д. 11,54 (ушир.с, 1H), 7,45 (т, J=2,8 Гц, 1H), 7,19 (с, 1H), 6,88 (д, J=8,7 Гц, 1H), 6,73 (д, J=2,7 Гц, 1H) 6,67 (дд, J=3,1, 8,8 Гц, 1H), 6,40 (дд, J=2,0, 2,7 Гц, 1H), 4,76 (м, 1H), 3,82 (с, 3H), 3,85-3,62 (м, 8H), 2,97 (ушир.с, 1H), 2,24-1,85 (м, 2H). MS (ESI+) m/z 436,2 (M+H)+.
Пример 92
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидрофуран-3-илокси)фенил]пропан-1-сульфонамид
Продукт примера 92 получали согласно процедуре, используемой для получения продукта примера 4, (способ A), заменяя продуктом примера 91b продукт примера 3 и заменяя пропан-1-сульфонил хлоридом метансульфонил хлорид, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, CDCl3) δ м.д. 10,63 (ушир.с, 1H), 7,25 (м, 3H), 6,90 (д, J=8,7 Гц, 1H), 6,46 6,35 (м, 2H), 4,88 (ушир.с, 1H), 4,01 3,66 (м, 7H), 3,12 3,03 (м, 2H), 2,2 (ушир.с, 1H), 2,19 1,80 (м, 4H), 1,06 (т, J=7,4 Гц, 3H). MS (ESI+) m/z 432,2 (M+H)+.
Пример 93
N-[4-(4-цианофенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]пропан-1-сульфонамид
Продукт примера 93 получали согласно процедуре, используемой для получения продукта примера 4, (способ A), заменяя продуктом примера 33b продукт примера 3 и заменяя пропан-1-сульфонил хлоридом метансульфонил хлорид, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δδ м.д. 12,03 (ушир.с, 1H), 9,91 (с, 1H), 7,70-7,63 (м, 2H), 7,42 (д, J=2,5 Гц, 1H), 7,32-7,17 (м, 4H), 6,93-6,86 (м, 2H), 6,22 (дд, J=2,8, 1,9 Гц, 1H), 3,46 (с, 3H), 3,18-3,09 (м, 2H), 1,92-1,65 (м, 2H), 0,98 (т, J=7,4 Гц, 3H). MS (ESI+) m/z 463,2 (M+H)+.
Пример 94
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(2,4,6-трифторфенокси)фенил]пропан-1-сульфонамид
Пример 94a
6-метил-4-(5-нитро-2-(2,4,6-трифторфенокси)фенил)-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 94a получали согласно процедуре, используемой для получения продукта примера 2b, заменяя 2,4,6-трифторфенолом фенол, получая указанное в заголовке соединение.
Пример 94b
4-(5-амино-2-(2,4,6-трифторфенокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 94b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 94a продукт примера 2b, получая указанное в заголовке соединение.
Пример 94c
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(2,4,6-трифторфенокси)фенил]пропан-1-сульфонамид
Продукт примера 94c получали согласно процедуре, используемой для получения продукта примера 4, (способ A), заменяя продуктом примера 94b продукт примера 3 и заменяя пропан-1-сульфонил хлоридом метансульфонил хлорид, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,07 (ушир.с, 1H), 9,72 (с, 1H), 7,44 7,33 (м, 2H), 7,33 7,28 (м, 3H), 7,14 (дд, J=8,8, 2,7 Гц, 1H), 6,80 (д, J=8,8 Гц, 1H), 6,24 6,19 (м, 1H), 3,56 (с, 3H), 3,11 3,02 (м, 2H), 1,78 1,62 (м, 2H), 0,95 (т, J=7,4 Гц, 3H). MS (ESI+) m/z 492,1 (M+H)+.
Пример 95
3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензолсульфонамид
Пример 95a
3-нитро-4-феноксибензолсульфонамид
Фенол (1,282 г, 13,63 ммоль) в диметилформамиде (20 мл) обрабатывали 60% гидридом натрия (0,545 г, 13,63 ммоль). Реакционную смесь перемешивали в течение 10 минут. К этому раствору добавляли 4-фтор-3-нитробензолсульфонамид (0,75 г, 3,41 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 2 часов. Реакционную смесь распределяли между водой и этилацетатом. Водный слой нейтрализовали 10% HCl и экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (1:1 этилацетат/гексаны) на силикагеле, получая 0,96 г указанного в заголовке продукта.
Пример 95b
3-амино-4-феноксибензолсульфонамид
Продукт примера 95b получали согласно процедуре, используемой для получения продукта примера 29b, заменяя продуктом 95a продукт примера 29a, получая указанное в заголовке соединение.
Пример 95c
3-йод-4-феноксибензолсульфонамид
Продукт примера 95c получали согласно процедуре, используемой для получения продукта примера 85c, заменяя продуктом 95b продукт примера 85b, получая указанное в заголовке соединение.
Пример 95d
3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-феноксибензолсульфонамид
Смесь продукта примера 6a (0,086 г, 0,20 ммоль), продукта примера 95c (0,083 г, 0,22 ммоль), Pd(PPh3)4 (0,012 г, 5 мол.%) и фторида цезия (0,091 г, 0,6 ммоль) в диметоксиметане (2 мл) и метаноле (1 мл) нагревали микроволновым излучением (110°C, 30 минут). Реакционную смесь охлаждали до температуры окружающей среды и распределяли между этилацетатом и водой. Органический слой отделяли и сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали препаративной ВЭЖХ (C18, 10-100% ацетoнитрил в 0,1% TFA/воде), получая указанное в заголовке соединение (48 мг, выход 61%). 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,08 (с, 1H), 7,95 (д, J=2,14 Гц, 1H), 7,79 (дд, J=8,54, 2,44 Гц, 1H), 7,36-7,39 (м, 5H), 7,16 (т, J=7,48 Гц, 1H), 7,03-7,05 (м, 3H), 6,28 (т, J=2,29 Гц, 1H), 3,55 (с, 3H). MS (ESI+) m/z 396,2 (M+H)+.
Пример 96
6-(циклогексиламино)-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид
Пример 96a
5-бром-6-(циклогексиламино)пиридин-3-сульфонамид
Смесь продукта примера 86a (0,136 г, 0,5 ммоль) и циклогексанамина (0,198 г, 2,0 ммоль) в диоксане (2 мл) нагревали микроволновым излучением (140°C, 1 часа). Растворитель удаляли и остаток очищали флаш-хроматографией (3:2 этилацетат/гексаны) на силикагеле, получая 0,164 г указанного в заголовке продукта.
Пример 96b
6-(циклогексиламино)-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид
Продукт примера 96b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 96a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,17 (с, 1H), 8,38 (д, J=2,44 Гц, 1H), 7,69 (д, J=2,44 Гц, 1H), 7,32 (т, J=2,75 Гц, 1H), 7,29 (с, 1H), 7,18 (ушир. с, 2H), 6,04 (т, J=2,29 Гц, 1H), 5,97 (д, J=7,63 Гц, 1H), 3,56 (с, 3H), 1,81-1,82 (м, 2H), 1,54-1,65 (м, 3H), 1,01-1,33 (м, 5H) MS (ESI+) m/z 402,1 (M+H)+.
Пример 97
6-(циклогексиламино)-N-метил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид
Продукт примера 97 изолировали как меньший продукт во время получения продукта примера 96b. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,16 (с, 1H), 8,35 (д, J=2,44 Гц, 1H), 7,69 (д, J=2,44 Гц, 1H), 7,32 (т, J=2,75 Гц, 1H), 7,29 (с, 1H), 7,18 (кв., J=4,88 Гц, 1H), 6,02 (т, J=2,29 Гц, 1H), 5,96 (д, J=7,24 Гц, 1H), 3,99-4,05 (м, 1H), 3,55 (с, 3H), 2,42 (д, J=4,88 Гц, 3H), 1,80-1,82 (м, 2H), 1,54-1,65 (м, 3H), 1,01-1,33 (м, 6H) MS (ESI+) m/z 416,1 (M+H)+.
Пример 98
N-метил-N'-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(2,4,6-трифторфенокси)фенил]серный диамид
К смеси продукта примера 94b (76,3 мг, 0,198 ммоль) и триэтиламина (60,1 мг, 0,594 ммоль) в дихлорметане (4 мл) добавляли по каплям метилсульфамоил хлорид (103 мг, 0,792 ммоль) и реакционную смесь перемешивали при температуре окружающей среды в течение 1 часа. Реакционную смесь концентрировали при пониженном давлении и остаток смешивали с диоксаном (5 мл) и 1M водным раствором гидроксида натрия (3 мл, 0,2 ммоль) и нагревали при 70°C в течение 1 часа. Реакционную смесь охлаждали до температуры окружающей среды и затем нейтрализовали насыщенным водным раствором хлорида аммония (50 мл) и водную фазу экстрагировали этилацетатом (3 × 50 мл). Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили (безводный сульфат магния), фильтровали и концентрировали. Остаток очищали препаративной ВЭЖХ (C18, 10-80% ацетoнитрил в 0,1% TFA/воде), получая указанное в заголовке соединение (11 мг, выход 11%). 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,04 (ушир.с, 1H), 9,58 (с, 1H), 7,43-7,32 (м, 6H), 7,32-7,16 (м, 1H), 7,10 (дд, J=8,8, 2,7 Гц, 1H), 6,75 (д, J=8,8 Гц, 1H), 6,23 (т, J=2,3 Гц, 1H), 3,57 (ушир.с, 3H), 2,35 (д, J=4,9 Гц, 3H). MS (ESI+) m/z 479,1 (M+H)+.
Пример 99
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-4-илокси)фенил]пропан-1-сульфонамид
Пример 99a
6-метил-4-(5-нитро-2-(тетрагидро-2H-пиран-4-илокси)фенил)-1H-пирроло[2,3-c]пиридин-7(6H)-он
К раствору тетрагидро-2H-пиран-4-ола (231 мг, 2,265 ммоль) в тетрагидрофуране (10 мл) добавляли гидрид натрия (181 мг, 4,53 ммоль) порциями. После перемешивания в течение 10 минут добавляли продукт примера 2a (500 мг, 1,133 ммоль). Смесь нагревали при 50°C в течение 2 часов. После охлаждения реакционную смесь гасили насыщенным раствором хлорида аммония (10 мл), разбавляли 50% водным раствором хлорида натрия (80 мл) и экстрагировали этилацетатом (75 мл, 2 × 50 мл). Объединенные органические вещества сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток очищали колоночной флаш-хроматографией (силикагель, 0,5-4% метанол в дихлорметане), получая указанное в заголовке соединение (220 мг, выход 52,6%).
Пример 99b
4-(5-амино-2-(тетрагидро-2H-пиран-4-илокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 99b получали согласно процедуре, используемой для получения продукта примера 29b, заменяя продуктом примера 99a продукт примера 29a, получая указанное в заголовке соединение.
Пример 99c
N-[3-(6-метил-7-оксо-6,7-дигидро-1Н-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-4-илокси)фенил]пропан-1-сульфонамид
Продукт примера 99c получали согласно процедуре, используемой для получения продукта примера 4 (способ A), заменяя продуктом примера 99b продукт примера 3 и пропан-1-сульфонил хлоридом метансульфонил хлорид за исключением того, что реакционную смесь в начале перемешивали в течение 18 часов при температуре окружающей среды и затем нагревали при 50°C в течение 1 часа в присутствии гидроксида натрия, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,00 (с, 1H), 9,50 (с, 1H), 7,24-7,33 (м, 3H), 7,14 (с, 2H), 6,19 (т, J=2,37 Гц, 1H), 4,39-4,53 (м, 1H), 3,53-3,68 (м, 5H), 3,33-3,45 (м, 2H), 2,96-3,06 (м, 2H), 1,78-1,92 (м, 2H), 1,63-1,78 (м, 2H), 1,39-1,54 (м, 2H), 0,95 (т, J=7,46 Гц, 3H). MS (ESI+) m/z 446,1 (M+H)+.
Пример 100
2,2,2-трифтор-N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-4-илокси)фенил]этансульфонамид
К раствору продукта примера 99b (43,2 мг, 0,127 ммоль) в дихлорметане (2 мл) добавляли 2,2,2-трифторэтансульфонил хлорид (0,015 мл, 0,140 ммоль) и триэтиламин (0,053 мл, 0,382 ммоль). Смесь перемешивали в течение 18 часов при температуре окружающей среды. Реакционную смесь концентрировали и остаток очищали колоночной флаш-хроматографией (силикагель, 0,5-5% метанол в дихлорметане), получая указанное в заголовке соединение (20,8 мг, выход 33,7%). 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,00 (с, 1H), 10,16 (с, 1H), 7,25-7,32 (м, 3H), 7,14-7,20 (м, 2H), 6,18-6,24 (м, 1H), 4,36-4,55 (м, 3H), 3,52-3,68 (м, 5H), 3,33-3,45 (м, 2H), 1,79-1,94 (м, 2H), 1,39-1,57 (м, 2H). MS (ESI+) m/z 486,1 (M+H)+.
Пример 101
N-{4-[(4,4-дифторциклогексил)окси]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил}этансульфонамид
Пример 101a
4-(2-(4,4-дифторциклогексилокси)-5-нитрофенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Пример 101a получали согласно процедуре, используемой для получения продукта примера 99a, заменяя 4,4-дифторциклогексанолом тетрагидро-2H-пиран-4-ол, получая указанное в заголовке соединение.
Пример 101b
4-(5-амино-2-(4,4-дифторциклогексилокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 101b получали согласно процедуре, используемой для получения продукта примера 29b, заменяя продуктом примера 101a продукт примера 29a, получая указанное в заголовке соединение.
Пример 101c
N-{4-[(4,4-дифторциклогексил)окси]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил}этансульфонамид
Продукт примера 101c получали согласно процедуре, используемой для получения продукта примера 4 (способ A), заменяя продуктом примера 101b продукт примера 3 и этансульфонил хлоридом метансульфонил хлорид за исключением того, что реакционную смесь в начале перемешивали в течение 18 часов при температуре окружающей среды и затем нагревали при 50°C в течение 1 часа в присутствии гидроксида натрия, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,02 (с, 1H), 9,56 (с, 1H), 7,24-7,34 (м, J=4,36 Гц, 3H), 7,17 (с, 2H), 6,15-6,23 (м, 1H), 4,48 (с, 1H), 3,49-3,61 (м, 3H), 3,05 (кв., J=7,27 Гц, 2H), 1,62-1,88 (м, 8H), 1,22 (т, J=7,34 Гц, 3H). MS (ESI+) m/z 466,1 (M+H)+.
Пример 102
N-{4-[(4,4-дифторциклогексил)окси]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил}пропан-1-сульфонамид
Продукт примера 102 получали согласно процедуре, используемой для получения продукта примера 4 (способ A), заменяя продуктом примера 101b продукт примера 3 и пропан-1-сульфонил хлоридом метансульфонил хлорид за исключением того, что реакционную смесь в начале перемешивали в течение 18 часов при температуре окружающей среды и затем нагревали при 50°C в течение 1 часа в присутствии гидроксида натрия, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,02 (с, 1H), 9,54 (с, 1H), 7,25-7,31 (м, 3H), 7,17 (с, 2H), 6,14-6,22 (м, 1H), 4,44-4,56 (м, J=2,78 Гц, 1H), 3,51-3,57 (м, 3H), 2,96-3,08 (м, 2H), 1,61-1,89 (м, 10H), 0,95 (т, J=7,54 Гц, 3H). MS (ESI+) m/z 480,2 (M+H)+.
Пример 103
N-{4-[(4,4-дифторциклогексил)окси]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил}-2,2,2-трифторэтансульфонамид
Продукт примера 103 получали согласно процедуре, используемой для получения продукта примера 100, заменяя продуктом примера 101b продукт примера 99b, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,00 (с, 1H), 10,19 (с, 1H), 7,25-7,32 (м, 3H), 7,19 (с, 2H), 6,17-6,24 (м, 1H), 4,36-4,60 (м, 3H), 3,55 (с, 3H), 1,60-1,88 (м, J=4,07 Гц, 8H). MS (ESI+) m/z 520,1 (M+H)+.
Пример 104
N-{4-[(4,4-дифторциклогексил)окси]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил}-N'-метилсерный диамид
Продукт примера 104 получали согласно процедуре, используемой для получения продукта примера 100, заменяя продуктом примера 101b продукт примера 99b и метилсульфамоил хлоридом 2,2,2-трифторэтансульфонил хлорид, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 11,98 (с, 1H), 9,41 (с, 1H), 7,21-7,30 (м, 3H), 7,06-7,17 (м, 3H), 6,15-6,24 (м, 1H), 4,44 (с, 1H), 3,55 (с, 3H), 2,51 (с, 3H), 1,59-1,86 (м, 8H). MS (ESI+) m/z 467,1 (M+H)+.
Пример 105
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-3-илокси)фенил]этансульфонамид
Пример 105a
6-метил-4-(5-нитро-2-(тетрагидро-2H-пиран-3-илокси)фенил)-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 105a получали согласно процедуре, используемой для получения продукта примера 99a, заменяя тетрагидро-2H-пиран-3-олом тетрагидро-2H-пиран-4-ол, получая указанное в заголовке соединение.
Пример 105 b
4-(5-амино-2-(тетрагидро-2H-пиран-3-илокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 105b получали согласно процедуре, используемой для получения продукта примера 29b, заменяя продуктом примера 105a продукт примера 29a, получая указанное в заголовке соединение.
Пример 105c
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-3-илокси)фенил]этансульфонамид
Продукт примера 105c получали согласно процедуре, используемой для получения продукта примера 4 (способ A), заменяя продуктом примера 105b продукт примера 3 и этансульфонил хлоридом метансульфонил хлорид за исключением того, что реакционную смесь в начале перемешивали в течение 18 часов при температуре окружающей среды и затем нагревали при 50°C в течение 1 часа в присутствии гидроксида натрия, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,02 (с, 1H), 9,53 (с, 1H), 7,37 (с, 1H), 7,27-7,33 (м, 2H), 7,09-7,17 (м, 2H), 6,23 (т, J=2,18 Гц, 1H), 4,23-4,34 (м, 1H), 3,67 (дд, J=11,70, 2,58 Гц, 1H), 3,37-3,59 (м, 6H), 3,04 (кв., J=7,54 Гц, 2H), 1,85-2,00 (м, 1H), 1,51-1,73 (м, 2H), 1,33-1,49 (м, 1H), 1,21 (т, J=7,34 Гц, 3H). MS (ESI+) m/z 432,2 (M+H)+.
Пример 106
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-3-илокси)фенил]пропан-1-сульфонамид
Продукт примера 106 получали согласно процедуре, используемой для получения продукта примера 4 (способ A), заменяя продуктом примера 105b продукт примера 3 и пропан-1-сульфонил хлоридом метансульфонил хлорид за исключением того, что реакционную смесь в начале перемешивали в течение 18 часов при температуре окружающей среды и затем нагревали при 50°C в течение 1 часа в присутствии гидроксида натрия, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,02 (с, 1H), 9,52 (с, 1H), 7,37 (с, 1H), 7,30 (с, 2H), 7,12 (с, 2H), 6,23 (т, J=2,18 Гц, 1H), 4,22-4,34 (м, 1H), 3,67 (дд, J=11,50, 2,78 Гц, 1H), 3,36-3,59 (м, 6H), 2,96-3,07 (м, 2H), 1,85-1,99 (м, 1H), 1,52-1,79 (м, 4H), 1,32-1,50 (м, 1H), 0,95 (т, J=7,54 Гц, 3H). MS (ESI+) m/z 446,2 (M+H)+.
Пример 107
2,2,2-трифтор-N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-3-илокси)фенил]этансульфонамид
Продукт примера 107 получали согласно процедуре, используемой для получения продукта примера 100, заменяя продуктом примера 105b продукт примера 99b, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,02 (с, 1H), 10,17 (с, 1H), 7,38 (с, 1H), 7,26-7,33 (м, 2H), 7,12-7,18 (м, J=1,59 Гц, 2H), 6,26 (т, J=2,38 Гц, 1H), 4,43 (кв., J=9,92 Гц, 2H), 4,27-4,36 (м, 1H), 3,68 (дд, J=11,50, 2,38 Гц, 1H), 3,39-3,59 (м, 6H), 1,86-2,01 (м, 1H), 1,53-1,73 (м, 2H), 1,36-1,49 (м, 1H). MS (ESI+) m/z 486,1 (M+H)+.
Пример 108
N-метил-N'-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(тетрагидро-2H-пиран-3-илокси)фенил]серный диамид
Продукт примера 108 получали согласно процедуре, используемой для получения продукта примера 100, заменяя продуктом примера 105b продукт примера 99b и метилсульфамоил хлоридом 2,2,2-трифторэтансульфонил хлорид, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 11,99 (с, 1H), 9,38 (с, 1H), 7,33 (с, 1H), 7,26-7,30 (м, J=2,54, 2,54 Гц, 2H), 7,05-7,13 (м, 3H), 6,22-6,27 (м, 1H), 4,16-4,27 (м, 1H), 3,65 (дд, J=11,53, 2,37 Гц, 1H), 3,37-3,59 (м, 6H), 2,50-2,53 (м, J=1,70 Гц, 3H), 1,84-1,96 (м, 1H), 1,50-1,71 (м, 2H), 1,35-1,47 (м, 1H). MS (ESI+) m/z 433,1 (M+H)+.
Пример 109
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-с]пиридин-4-ил)-4-(тетрагидро-2H-пиран-4-илокси)фенил]этансульфонамид
Продукт примера 109 получали согласно процедуре, используемой для получения продукта примера 4 (способ A), заменяя продуктом примера 99b продукт примера 3 и этансульфонил хлоридом метансульфонил хлорид за исключением того, что реакционную смесь в начале перемешивали в течение 18 часов при температуре окружающей среды и затем нагревали при 50°C в течение 1 часа в присутствии гидроксида натрия, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,00 (с, 1H), 9,50 (с, 1H), 7,24-7,33 (м, 3H), 7,14 (с, 2H), 6,19 (т, J=2,37 Гц, 1H), 4,39-4,53 (м, 1H), 3,53-3,68 (м, 5H), 3,33-3,45 (м, 2H), 2,96-3,06 (м, 2H), 1,78-1,92 (м, 2H), 1,63-1,78 (м, 2H), 1,39-1,54 (м, 2H), 0,95 (т, J=7,46 Гц, 3H). MS (ESI+) m/z 432,1 (M+H)+.
Пример 110
N,N-диметил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-6-(тетрагидрофуран-3-илокси)пиридин-3-сульфонамид
Пример 110a
5-бром-6-хлор-N,N-диметилпиридин-3-сульфонамид
5-Бром-6-хлорпиридин-3-сульфонил хлорид (1,455 г, 5 ммоль) в метаноле (20 мл) обрабатывали 2,0 н. диметиламином (6,25 мл, 12,50 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 16 часов. Растворитель удаляли и твердое вещество промывали водой несколько раз. Твердое вещество затем очищали хроматографией на силикагеле, элюируя 15% этилацетатом в гексанах, получая 0,8 г указанного в заголовке соединения.
Пример 110b
5-бром-N,N-диметил-6-(тетрагидрофуран-3-илокси)пиридин-3-сульфонамид
Продукт примера 110b получали согласно процедуре, используемой для получения продукта примера 29a, заменяя продуктом 110a продукт примера 2a и тетрагидрофуран-3-олом тетрагидро-2H-пиран-4-ол, соответственно, получая указанное в заголовке соединение.
Пример 110c
N,N-диметил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-6-(тетрагидрофуран-3-илокси)пиридин-3-сульфонамид
Продукт примера 110c получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 110b продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,11 (с, 1H), 8,53 (д, J=2,44 Гц, 1H), 8,00 (д, J=2,44 Гц, 1H), 7,43 (с, 1H), 7,32 (д, J=2,75 Гц, 1H), 6,17 (т, J=2,29 Гц, 1H), 5,67 (д, J=1,53 Гц, 1H), 3,93 (дд, J=10,38, 4,58 Гц, 1H), 3,78 (д, J=10,07 Гц, 1H), 3,68-3,72 (м, 2H), 3,57 (с, 3H), 2,69 (с, 6H), 2,54-2,56 (м, 5H), 2,17-2,24 (м, 1H), 1,94-1,98 (м, 1H). MS (ESI+) m/z 419,2 (M+H)+.
Пример 111
5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-6-(фениламино)пиридин-3-сульфонамид
Пример 111a
5-бром-6-(фениламино)пиридин-3-сульфонамид
Смесь продукта примера 86a (0,136 г, 0,5 ммоль), анилина (0,186 г, 2,0 ммоль) и 60% гидрида натрия (0,12 г, 3,0 ммоль) в диоксане (2 мл) перемешивали и нагревали при 60°C в течение 16 часов. После охлаждения реакционную смесь распределяли между водой и этилацетатом. Водный слой нейтрализовали 10% HCl и экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией на силикагеле (2:3 этилацетат/гексаны), получая 0,095 г указанного в заголовке продукта.
Пример 111b
5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-6-(фениламино)пиридин-3-сульфонамид
Продукт примера 111b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 111a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,17 (с, 1H), 8,49 (д, J=2,44 Гц, 1H), 8,25 (с, 1H), 7,87 (д, J=2,44 Гц, 1H), 7,55 (д, J=7,63 Гц, 2H), 7,42 (с, 1H), 7,24-7,31 (м, 5H), 6,99 (т, J=7,32 Гц, 1H), 6,04 (м, 1H), 3,58 (с, 3H). MS (ESI+) m/z 396,2 (M+H)+.
Пример 112
N-метил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-6-(фениламино)пиридин-3-сульфонамид
Продукт примера 112 изолировали как меньший продукт во время получения продукта примера 111b. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,17 (с, 1H), 8,44 (д, J=2,44 Гц, 1H), 8,31 (с, 1H), 7,78 (д, J=2,44 Гц, 1H), 7,56 (д, J=7,63 Гц, 2H), 7,45 (с, 1H), 7,34-7,37 (м, 1H), 7,25-7,30 (м, 3H), 7,00 (т, J=7,32 Гц, 1H), 6,04 (м, 1H), 3,58 (с, 3H), 2,46 (д, J=4,88 Гц, 3H). MS (ESI+) m/z 410,2 (M+H)+.
Пример 113
N-[4-(4-цианофенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-2-фторэтансульфонамид
Пример 33b (50 мг, 0,140 ммоль) и триэтиламин (42,6 мг, 0,421 ммоль) объединяли в дихлорметане (4 мл). 2-Фторэтансульфонил хлорид (82 мг, 0,561 ммоль) добавляли по каплям и реакционную смесь перемешивали в течение 1 часа при температуре окружающей среды. Реакционную смесь затем экстрагировали насыщенным водным раствором хлорида натрия, раделяли, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали препаративной ВЭЖХ (C18, 10-100% ацетoнитрил/вода, 0,1% TFA), получая указанное в заголовке соединение (1,4 мг, выход 2%). 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 11,98-11,92 (м, 1H), 7,62-7,56 (м, 2H), 7,25 (т, J=2,7 Гц, 1H), 7,17 (с, 1H), 7,05 (д, J=8,6 Гц, 1H), 6,82-6,70 (м, 4H), 6,24-6,13 (м, 1H), 4,19-4,09 (м, 2H), 3,70-3,62 (м, 2H) 3,45 (с, 3H). MS (ESI+) m/z 467,1 (M+H)+.
Пример 114
2-фтор-N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(2,4,6-трифторфенокси)фенил]этансульфонамид
Пример 114 получали согласно процедуре, используемой для получения продукта примера 91c, заменяя продуктом примера 94b продукт примера 91b, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,00-11,94 (м, 1H), 7,33 (д, J=8,8 Гц, 1H), 7,27 (м, 2H), 7,25 (с, 1H), 6,69 (д, J=2,5 Гц, 1H), 6,63-6,47 (м, 2H), 6,22 (дд, J=2,8, 2,0 Гц, 1H), 4,08 (кв., J=6,3, 5,7, 6,0 Гц, 2H), 3,60 (т, J=6,3, 6,0 Гц, 2H), 3,55 (ушир.с, 3H). MS (ESI+) m/z 496,2 (M+H)+.
Пример 115
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]пропан-1-сульфонамид
Продукт примера 115 получали согласно процедуре, используемой для получения продукта примера 27c, заменяя пропан-1-сульфонил хлоридом метансульфонил хлорид, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,04 (ушир.с, 1H), 9,76 (с, 1H), 7,42-7,26 (м, 4H), 7,18 (дд, J=8,8, 2,7 Гц, 1H), 7,13-6,94 (м, 2H), 6,91 (д, J=8,7 Гц, 1H), 6,24 (т, J=2,3 Гц, 1H), 3,53 (с, 3H), 3,13-3,04 (м, 2H), 1,79-1,64 (м, 2H), 0,96 (т, J=7,4 Гц, 3H). MS (ESI+) m/z 474,1 (M+H)+.
Пример 116
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-(пиримидин-2-ил)бензамид
Раствор продукта примера 50b (24 мг, 0,06 ммоль) в 4 мл склянке растворяли в безводном тетрагидрофуране (1,0 мл) с последующим добавлением 1-хлор-N,N,2-триметил-1-пропениламина (65 мкл, 0,48 ммоль). Закрывали крышкой и подвергали встряхиванию в течение 2 часов при температуре окружающей среды. Затем добавляли раствор пиримидин-2-амина (9 мг, 0,09 ммоль) в безводном тетрагидрофуране (0,3 мл) и потом раствор 4-(диметиламино)пиридина (37 мг, 0,3 ммоль) в безводном тетрагидрофуране (0,5 мл). Смесь перемешивали при 60°C в течение 16 часов, охлаждали и концентрировали до сухости. Остатки растворяли в 1:1 DMSO/MeOH и очищали ВЭЖХ с обращенной фазой (10-80% ацетoнитрил в 0,1% TFA вода). 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 8,73 (д, J=4,88 Гц, 2H) 8,09 (д, J=2,44 Гц, 1H) 7,95 (дд, J=8,70, 2,29 Гц, 1H) 7,42-7,48 (м, 1H) 7,41 (с, 1H) 7,32-7,38 (м, 2H) 7,27 (т, J=4,88 Гц, 1H) 7,11-7,17 (м, 1H) 6,90 (д, J=8,85 Гц, 1H) 6,32 (д, J=2,75 Гц, 1H) 3,60 (с, 3H); (ESI) m/z 474 (M+H)+.
Пример 117
4-(2,4-дифторфенокси)-N-(2,6-диметоксипиридин-3-ил)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид
Продукт примера 117 получали согласно процедуре, используемой для получения продукта примера 116, заменяя 2,6-диметоксипиридин-3-амин гидрохлоридом пиримидин-2-амин, получая TFA соль указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 8,08 (д, J=1,53 Гц, 1H) 7,94 (дд, J=8,85, 2,14 Гц, 1H) 7,74-7,78 (м, 1H) 7,40-7,47 (м, 1H) 7,38 (с, 1H) 7,28-7,35 (м, 2H) 7,09-7,15 (м, 1H) 6,91 (д, J=8,54 Гц, 1H) 6,43 (д, J=8,24 Гц, 1H) 6,29 (д, J=2,75 Гц, 1H) 3,88 (д, J=9,46 Гц, 6H) 3,60 (с, 3H); (ESI) m/z 533 (M+H)+.
Пример 118
4-(2,4-дифторфенокси)-N-(1H-индазол-6-ил)-3-(6-метил-7-оксо-6,7-дигидро-1Н-пирроло[2,3-c]пиридин-4-ил)бензамид
Продукт примера 118 получали согласно процедуре, используемой для получения продукта примера 116, заменяя 1H-индазол-6-амином пиримидин-2-амин, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 8,22 (с, 1H) 8,12 (д, J=2,44 Гц, 1H) 8,02 (с, 1H) 7,97 (дд, J=8,54, 2,44 Гц, 1H) 7,73 (д, J=8,54 Гц, 1H) 7,42-7,48 (м, 1H) 7,41 (с, 1H) 7,30-7,38 (м, 3H) 7,11-7,16 (м, 1H) 6,93 (д, J=8,54 Гц, 1H) 6,31 (д, J=2,75 Гц, 1H) 3,61 (с, 3H); (ESI) m/z 512 (M+H)+.
Пример 119
4-[2-(2,4-дифторфенокси)-5-{[4-(пирролидин-1-илкарбонил)пиперазин-1-ил]карбонил}фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 119 получали согласно процедуре, используемой для получения продукта примера 116, заменяя пиперазин-1-ил(пирролидин-1-ил)метаноном пиримидин-2-амин, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C ) δ м.д. 7,51 (д, J=2,14 Гц, 1H) 7,39-7,46 (м, 2H) 7,35 (с, 1H) 7,32-7,34 (м, J=2,90, 2,90 Гц, 1H) 7,25-7,31 (м, 1H) 7,07-7,13 (м, 1H) 6,87 (д, J=8,54 Гц, 1H) 6,28 (д, J=2,75 Гц, 1H) 3,59-3,71 (м, 1H) 3,56-3,58 (м, 4H) 3,40-3,55 (м, 2H) 3,18-3,33 (м, J=6,41, 6,41 Гц, 8H) 1,75 (т, J=6,26 Гц, 4H); (ESI) m/z 562 (M+H)+.
Пример 120
4-(2,4-дифторфенокси)-N-[4-(диметиламино)фенил]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид
Продукт примера 120 получали согласно процедуре, используемой для получения продукта примера 116, заменяя N1,N1-диметилбензол-1,4-диамином пиримидин-2-амин, получая TFA соль указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 8,09 (д, J=2,44 Гц, 1H) 7,94 (дд, J=8,70, 2,29 Гц, 1H) 7,76 (д, J=9,16 Гц, 2H) 7,41-7,47 (м, 1H) 7,39 (с, 1H) 7,29-7,36 (м, 2H) 7,26 (д, J=8,85 Гц, 2H) 7,10-7,16 (м, 1H) 6,92 (д, J=8,54 Гц, 1H) 6,29 (д, J=3,05 Гц, 1H) 3,60 (с, 3H) 3,06 (с, 6H); (ESI) m/z 515 (M+H)+.
Пример 121
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-(пиридин-4-илметил)бензамид
Продукт примера 121 получали согласно процедуре, используемой для получения продукта примера 116, заменяя пиридин-4-илметанамином пиримидин-2-амин, получая TFA соль указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 8,79 (д, J=6,41 Гц, 2H) 8,05 (д, J=2,14 Гц, 1H) 7,87-7,96 (м, 3H) 7,41-7,47 (м, 1H) 7,28-7,38 (м, 3H) 7,09-7,16 (м, 1H) 6,91 (д, J=8,54 Гц, 1H) 6,28 (д, J=2,75 Гц, 1H) 4,73 (с, 2H) 3,59 (с, 3H); (ESI) m/z 487 (M+H)+.
Пример 122
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-[2-(2-оксопирролидин-1-ил)этил]бензамид
Продукт примера 122 получали согласно процедуре, используемой для получения продукта примера 116, заменяя 1-(2-аминоэтил)пирролидин-2-оном пиримидин-2-амин, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 7,91 (д, J=2,44 Гц, 1H) 7,77 (дд, J=8,70, 2,29 Гц, 1H) 7,38-7,47 (м, 1H) 7,32-7,36 (м, 2H) 7,26-7,31 (м, 1H) 7,07-7,13 (м, 1H) 6,86 (д, J=8,54 Гц, 1H) 6,27 (д, J=2,75 Гц, 1H) 3,59 (с, 3H) 3,33-3,46 (м, 6H) 2,19 (т, J=8,09 Гц, 2H) 1,86-1,95 (м, 2H); (ESI) m/z 507 (M+H)+.
Пример 123
4-(2,4-дифторфенокси)-N-(2-гидрокси-2-метилпропил)-3-(6-метил-7-оксо-6,7-дигидро-1H-)пирроло[2,3-c]пиридин-4-ил)бензамид
Продукт примера 123 получали согласно процедуре, используемой для получения продукта примера 116, заменяя 1-амино-2-метилпропан-2-олом пиримидин-2-амин, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C)δ м.д. 7,98 (д, J=2,14 Гц, 1H) 7,85 (дд, J=8,70, 2,29 Гц, 1H) 7,39-7,45 (м, 1H) 7,35 (с, 1H) 7,32 (д, J=3,05 Гц, 1H) 7,25-7,31 (м, 1H) 7,07-7,13 (м, 1H) 6,86 (д, J=8,54 Гц, 1H) 6,26 (д, J=2,75 Гц, 1H) 3,58-3,60 (м, 3H) 3,27 (с, 2H) 1,11 (с, 6H); (ESI) m/z 468 (M+H)+.
Пример 124
4-(2,4-дифторфенокси)-N-[2-(5-метокси-1H-индол-3-ил)этил]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид
Продукт примера 124 получали согласно процедуре, используемой для получения продукта примера 116, заменяя 2-(5-метокси-1H-индол-3-ил)этанамином пиримидин-2-амин, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 7,93 (д, J=2,14 Гц, 1H) 7,83 (дд, J=8,54, 2,14 Гц, 1H) 7,39-7,45 (м, 1H) 7,30-7,33 (м, 2H) 7,26-7,30 (м, 1H) 7,24 (д, J=8,85 Гц, 1H) 7,14 (с, 1H) 7,07-7,13 (м, 1H) 7,03 (д, J=2,44 Гц, 1H) 6,86 (д, J=8,54 Гц, 1H) 6,72 (дд, J=8,85, 2,44 Гц, 1H) 6,24 (д, J=2,75 Гц, 1H) 3,67 (с, 3H) 3,59 (с, 3H) 3,53 (т, J=7,32 Гц, 2H) 2,92 (т, J=7,32 Гц, 2H); (ESI) m/z 569 (M+H)+.
Пример 125
N-(3,4-дифторбензил)-4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид
Продукт примера 125 получали согласно процедуре, используемой для получения продукта примера 116, заменяя (3,4-дифторфенил)метанамином пиримидин-2-амин, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 8,00 (д, J=2,14 Гц, 1H) 7,87 (дд, J=8,54, 2,14 Гц, 1H) 7,26-7,46 (м, 6H) 7,15-7,20 (м, 1H) 7,08-7,13 (м, 1H) 6,88 (д, J=8,54 Гц, 1H) 6,26 (д, J=2,75 Гц, 1H) 4,45 (с, 2H) 3,58 (с, 3H); (ESI) m/z 522 (M+H)+.
Пример 126
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-[4-(трифторметокси)бензил]бензамид
Продукт примера 126 получали согласно процедуре, используемой для получения продукта примера 116, заменяя (4-(трифторметокси)фенил)метанамином пиримидин-2-амин, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 8,01 (д, J=2,44 Гц, 1H) 7,88 (дд, J=8,54, 2,14 Гц, 1H) 7,39-7,47 (м, 3H) 7,35 (с, 1H) 7,26-7,34 (м, 4H) 7,08-7,14 (м, 1H) 6,88 (д, J=8,54 Гц, 1H) 6,26 (д, J=2,75 Гц, 1H) 4,50 (с, 2H) 3,58 (с, 3H); (ESI) m/z 570 (M+H)+.
Пример 127
2-{4-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензоил]пиперазин-1-ил}-N,N-диметилацетамид
Продукт примера 127 получали согласно процедуре, используемой для получения продукта примера 116, заменяя N,N-диметил-2-(пиперазин-1-ил)ацетамидом пиримидин-2-амин, получая TFA соль указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 7,56 (д, J=2,14 Гц, 1H) 7,40-7,48 (м, 2H) 7,35 (с, 1H) 7,33 (д, J=2,75 Гц, 1H) 7,26-7,32 (м, 1H) 7,08-7,13 (м, 1H) 6,88 (д, J=8,24 Гц, 1H) 6,28 (д, J=2,75 Гц, 1H) 4,26 (с, 2H) 2,99-3,71 (м, 11H) 2,92 (д, J=5,49 Гц, 6H); (ESI) m/z 550 (M+H)+.
Пример 128
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-(пиридин-3-илметил)бензамид
Продукт примера 128 получали согласно процедуре, используемой для получения продукта примера 116, заменяя пиридин-3-илметанамином пиримидин-2-амин, получая TFA соль указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 8,78 (с, 1H) 8,72 (д, J=5,19 Гц, 1H) 8,36 (д, J=7,93 Гц, 1H) 8,01 (д, J=2,14 Гц, 1H) 7,85-7,92 (м, 2H) 7,40-7,46 (м, 1H) 7,35 (с, 1H) 7,33 (т, J=3,36 Гц, 1H) 7,27-7,31 (м, 1H) 7,09-7,14 (м, 1H) 6,89 (д, J=8,54 Гц, 1H) 6,26 (д, 1H) 4,63 (с, 2H) 3,59 (с, 3H); (ESI) m/z 487 (M+H)+.
Пример 129
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-(пиридин-2-илметил)бензамид
Продукт примера 129 получали согласно процедуре, используемой для получения продукта примера 116, заменяя пиридин-2-илметанамином пиримидин-2-амин, получая TFA соль указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 8,68 (д, J=5,49 Гц, 1H) 8,23-8,29 (м, 1H) 8,04 (д, J=2,44 Гц, 1H) 7,90 (дд, J=8,70, 2,29 Гц, 1H) 7,75 (д, J=7,93 Гц, 1H) 7,69-7,73 (м, 1H) 7,39-7,47 (м, 1H) 7,36 (с, 1H) 7,33 (д, J=2,75 Гц, 1H) 7,26-7,32 (м, 1H) 7,09-7,15 (м, 1H) 6,90 (д, J=8,85 Гц, 1H) 6,27 (д, J=2,75 Гц, 1H) 4,73 (с, 2H) 3,59 (с, 3H); (ESI) m/z 487 (M+H)+.
Пример 130
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-(3,4,5-триметоксибензил)бензамид
Продукт примера 130 получали согласно процедуре, используемой для получения продукта примера 116, заменяя (3,4,5-тиметоксифенил)метанамином пиримидин-2-амин, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 8,00 (д, J=2,14 Гц, 1H) 7,87 (дд, J=8,70, 2,29 Гц, 1H) 7,39-7,45 (м, 1H) 7,35 (с, 1H) 7,32 (д, J=2,75 Гц, 1H) 7,26-7,31 (м, 1H) 7,11 (м, 1H) 6,87 (д, J=8,54 Гц, 1H) 6,66 (с, 2H) 6,26 (д, J=2,75 Гц, 1H) 4,41 (с, 2H) 3,75 (с, 6H) 3,63 (с, 3H) 3,58 (с, 3H); (ESI) m/z 576 (M+H)+.
Пример 131
4-(2,4-дифторфенокси)-N-[2-(диметиламино)этил]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид
Продукт примера 131 получали согласно процедуре, используемой для получения продукта примера 116, заменяя N1,N1-диметилэтан-1,2-диамином пиримидин-2-амин, получая TFA соль указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 7,97 (д, J=2,14 Гц, 1H) 7,85 (дд, J=8,70, 2,29 Гц, 1H) 7,39-7,46 (м, 1H) 7,31-7,35 (м, 2H) 7,25-7,31 (м, 1H) 7,09-7,15 (м, 1H) 6,90 (д, J=8,55 Гц, 1H) 6,25 (д, J=2,75 Гц, 1H) 3,62 (т, J=5,95 Гц, 2H) 3,59 (с, 3H) 3,26 (т, J=5,95 Гц, 2H) 2,84 (с, 6H); (ESI) m/z 467 (M+H)+.
Пример 132
N-[2-(1,3-бензодиоксол-5-ил)этил]-4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид
Продукт примера 132 получали согласно процедуре, используемой для получения продукта примера 116, заменяя 2-(бензо[d][1,3]диоксол-5-ил)этанамином пиримидин-2-амин, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 7,92 (д, J=2,14 Гц, 1H) 7,79 (дд, J=8,70, 2,29 Гц, 1H) 7,39-7,45 (м, 1H) 7,31-7,34 (м, 2H) 7,25-7,31 (м, 1H) 7,06-7,14 (м, 1H) 6,80-6,87 (м, 3H) 6,70 (д, J=7,02 Гц, 1H) 6,25 (д, J=3,05 Гц, 1H) 5,94 (с, 2H) 3,59 (с, 3H) 3,44 (т, J=7,32 Гц, 2H) 2,76 (т, J=7,32 Гц, 2H); (ESI) m/z 544 (M+H)+.
Пример 133
4-(2,4-дифторфенокси)-N-[2-(1H-индол-3-ил)этил]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензамид
Продукт примера 133 получали согласно процедуре, используемой для получения продукта примера 116, заменяя 2-(1H-индол-3-ил)этанамином пиримидин-2-амин, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 8,65 (т, J=5,49 Гц, 1H) 7,94 (д, J=2,14 Гц, 1H) 7,83 (дд, J=8,70, 2,29 Гц, 1H) 7,58 (д, J=7,93 Гц, 1H) 7,39-7,45 (м, 1H) 7,36 (д, J=7,93 Гц, 1H) 7,32-7,34 (м, 2H) 7,25-7,31 (м, 1H) 7,18 (с, 1H) 7,05-7,13 (м, 2H) 6,98 (т, J=7,32 Гц, 1H) 6,86 (д, J=8,54 Гц, 1H) 6,25 (д, J=2,75 Гц, 1H) 3,59 (с, 3H) 3,48-3,58 (м, 2H) 2,96 (т, J=7,48 Гц, 2H); (ESI) m/z 539 (M+H)+.
Пример 134
4-[2-(2,4-дифторфенокси)-5-{[4-(фуран-2-илкарбонил)пиперазин-1-ил]карбонил}фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 134 получали согласно процедуре, используемой для получения продукта примера 116, заменяя фуран-2-ил(пиперазин-1-ил)метаноном пиримидин-2-амин, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 7,82 (с, 1H) 7,55 (д, J=2,14 Гц, 1H) 7,39-7,48 (м, 2H) 7,25-7,37 (м, 3H) 7,07-7,13 (м, 1H) 7,05 (д, J=3,36 Гц, 1H) 6,88 (д, J=8,24 Гц, 1H) 6,64 (дд, J=3,36, 1,83 Гц, 1H) 6,29 (д, J=2,75 Гц, 1H) 3,74-3,89 (м, 4H) 3,41-3,70 (м, 7H); (ESI) m/z 559 (M+H)+.
Пример 135
трет-бутил {1-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензоил]пиперидин-4-ил}карбамат
Продукт примера 135 получали согласно процедуре, используемой для получения продукта примера 116, заменяя трет-бутил пиперидин-4-илкарбаматом пиримидин-2-амин, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 7,45 (д, J=1,83 Гц, 1H) 7,36-7,44 (м, 2H) 7,34 (с, 1H) 7,32 (д, J=2,75 Гц, 1H) 7,25-7,31 (м, 1H) 7,06-7,13 (м, 1H) 6,86 (д, J=8,54 Гц, 1H) 6,27 (д, J=2,75 Гц, 1H) 4,31 (с, 1H) 3,42-3,69 (м, 5H) 2,85-3,24 (м, 2H) 1,77 (с, 2H) 1,21-1,47 (м, 11H); (ESI) m/z 579 (M+H)+.
Пример 136
трет-бутил 4-{[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензоил]амино}пиперидин-1-карбоксилат
Продукт примера 136 получали согласно процедуре, используемой для получения продукта примера 116, заменяя трет-бутил 4-аминопиперидин-1-карбоксилатом пиримидин-2-амин, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 7,95 (д, J=2,14 Гц, 1H) 7,83 (дд, J=8,54, 2,14 Гц, 1H) 7,43 (д, J=8,54 Гц, 1H) 7,31-7,35 (м, 2H) 7,24-7,51 (м, 1H) 7,10 (д, J=1,83 Гц, 1H) 6,86 (д, J=8,54 Гц, 1H) 6,24 (д, J=2,75 Гц, 1H) 3,87-4,08 (м, 3H) 3,58 (с, 3H) 2,91 (д, J=85,75 Гц, 2H) 1,78 (д, 2H) 1,34-1,45 (м, 11H); (ESI) m/z 579 (M+H)+.
Пример 137
4-[2-(2,4-дифторфенокси)-5-{[4-(этилсульфонил)пиперазин-1-ил]карбонил}фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 137 получали согласно процедуре, используемой для получения продукта примера 116, заменяя 1-(этилсульфонил)пиперазином пиримидин-2-амин, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6/D2O, Темп.=25°C) δ м.д. 7,53 (д, J=2,14 Гц, 1H) 7,38-7,47 (м, 2H) 7,35 (с, 1H) 7,33 (д, J=3,05 Гц, 1H) 7,26-7,32 (м, 1H) 7,07-7,13 (м, 1H) 6,87 (д, J=8,54 Гц, 1H) 6,28 (д, J=2,75 Гц, 1H) 3,43-3,70 (м, 7H) 3,25 (с, 4H) 3,07 (кв., J=7,43 Гц, 2H) 1,22 (т, J=7,32 Гц, 3H); (ESI) m/z 557 (M+H)+.
Пример 138
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 138a
4-(2-фтор-5-(метилсульфонил)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Смесь продукта примера 6a (0,642 г, 1,5 ммоль), 2-бром-1-фтор-4-(метилсульфонил)бензола (0,380 г, 1,500 ммоль), 1,3,5,7-тетраметил-6-фенил-2,4,8-триокса-6-фосфaадамантана (0,051 г, 0,176 ммоль), трис(дибензилиденацетон)дипалладия(0) (0,041 г, 0,045 ммоль) и фосфата калия (0,796 г, 3,75 ммоль) в диоксане (10 мл) и воде (2,500 мл) дегазировали и снова насыщали азотом несколько раз. Реакционную смесь нагревали при 60°C в течение 16 часов. Реакционную смесь распределяли между водой и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом три раза. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали колоночной флаш-хроматографией на силикагеле, элюируя 30% этилацетатом в гексанах, получая указанное в заголовке соединение (0,63 г, 1,328 ммоль, выход 89%).
Пример 138b
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Смесь продукта примера 138a (0,05 г, 0,105 ммоль), 2,4-дифторфенола (0,016 г, 0,126 ммоль) и карбоната цезия (0,069 г, 0,211 ммоль) в DMSO (1 мл) нагревали при 120°C в течение 16 часов. Реакционную смесь распределяли между водой и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом три раза. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали препаративной ВЭЖХ с обращенной фазой (10-80% ацетoнитрил в 0,1% TFA/воде), получая указанное в заголовке соединение (0,036 г, 0,084 ммоль, выход 79%). 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,10 (с, 1H), 7,99 (д, J=2,44 Гц, 1H), 7,86 (дд, J=8,54, 2,44 Гц, 1H), 7,40-7,56 (м, 3H), 7,31 (т, J=2,9 Гц, 1H), 7,14-7,20 (м, 1H), 6,98 (д, J=8,54 Гц, 1H), 6,28-6,30 (м, 1H), 3,59 (с, 3H), 3,26 (с, 3H). MS (ESI+) m/z 431,1 (M+H)+.
Пример 139
4-[2-(4-хлорбензоил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 139 получали согласно процедуре, используемой для получения продукта примера 95d, заменяя (2-бромфенил)(4-хлорфенил)метаноном продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 11,96 (с, 1H), 7,86-7,73 (м, 1H), 7,55-7,62 (м, 3H), 7,39-7,43 (м, 2H), 7,25-7,29 (м, 2H), 7,21 (т, J=2,75 Гц, 1H), 6,88 (с, 1H), 6,05-6,06 (м, 1H), 3,39 (с, 3H), MS (DCI+) m/z 363,0 (M+H)+.
Пример 140
4-{2-[(4-хлорфенил)(гидрокси)метил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Смесь продукта примера 139 (0,05 г, 0,138 ммоль) и тетрагидробората натрия (2) (5,21 мг, 0,138 ммоль) в тетрагидрофуране (2 мл) нагревали при 60°C в течение 3 часов. Растворитель удаляли и остаток очищали препаративной ВЭЖХ с обращенной фазой (10-80% ацетoнитрил в 0,1% TFA/воде), получая указанное в заголовке соединение (0,042 г, 0,115 ммоль, выход 84%). 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 11,70 (с, 1H), 7,56 (д, J=7,63 Гц, 1H), 7,35-7,39 (м, 1H), 7,27-7,31 (м, 1H), 7,21-7,23 (м, 4H), 7,00 (д, J=8,54 Гц, 2H), 6,79 (с, 1H), 5,94 (т, J=2,29 Гц, 1H), 5,75 (с, 1H), 3,47 (с, 3H), MS (DCI+) m/z 365,0 (M+H)+.
Пример 141
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(пиримидин-5-илокси)фенил]этансульфонамид
Пример 141a
6-метил-4-(5-нитро-2-(пиримидин-5-илокси)фенил)-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 141a получали согласно процедуре, используемой для получения продукта примера 2b, заменяя пиримидин-5-олом фенол, получая указанное в заголовке соединение.
Пример 141b
4-(5-амино-2-(пиримидин-5-илокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Пример 141b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 141a продукт примера 2b, получая указанное в заголовке соединение.
Пример 141c
N-[3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(пиримидин-5-илокси)фенил]этансульфонамид
Продукт примера 141c получали согласно процедуре, используемой для получения продукта примера 4 (способ A), заменяя продуктом примера 141b продукт примера 3 и заменяя этансульфонил хлоридом метансульфонил хлорид, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,03 (ушир.с, 1H), 9,90 (с, 1H), 8,35 (с, 2H), 7,40 (д, J=2,3 Гц, 1H), 7,31-7,22 (м, 4H), 6,25-6,20 (м, 1H), 3,49 (с, 3H), 3,17 (кв., J=7,3 Гц, 2H), 1,24 (т, J=7,3 Гц, 3H). MS (ESI+) m/z 462,2 (M+H)+.
Пример 142
N-{3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-[(1-метил-1H-пиразол-5-ил)метокси]фенил}этансульфонамид
Пример 142a
6-метил-4-(2-((1-метил-1H-пиразол-5-ил)метокси)-5-нитрофенил)-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 142a получали согласно процедуре, используемой для получения продукта примера 29a, заменяя (1-метил-1H-пиразол-5-ил)метанолом тетрагидро-2H-пиран-4-ол, получая указанное в заголовке соединение.
Пример 142b
4-(5-амино-2-((1-метил-1H-пиразол-5-ил)метокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 142b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 142a продукт примера 2b, получая указанное в заголовке соединение.
Пример 142c
N-{3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-[(1-метил-1H-пиразол-5-ил)метокси]фенил}этансульфонамид
Продукт примера 142c получали согласно процедуре, используемой для получения продукта примера 4 (способ A), заменяя продуктом примера 142b продукт примера 3 и заменяя этансульфонил хлоридом метансульфонил хлорид, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,01 (ушир.с, 1H), 9,58 (с, 1H), 7,32-7,14 (м, 6H), 6,20 (д, J=1,8 Гц, 1H), 6,10 (дд, J=2,8, 1,9 Гц, 1H), 5,10 (с, 2H), 3,63 (с, 3H), 3,50 (с, 3H), 3,04 (кв., J=7,4 Гц, 2H), 1,21 (т, J=7,4 Гц, 3H). MS (ESI+) m/z 442,1 (M+H)+.
Пример 143
N-{4-[(1,3-диметил-1H-пиразол-5-ил)метокси]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил}этансульфонамид
Пример 143a
4-(2-((1,3-диметил-1H-пиразол-5-ил)метокси)-5-нитрофенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 143a получали согласно процедуре, используемой для получения продукта примера 29a, заменяя (1,3-диметил-1H-пиразол-5-ил)метанолом тетрагидро-2H-пиран-4-ол, получая указанное в заголовке соединение.
Пример 143b
4-(5-амино-2-((1,3-диметил-1H-пиразол-5-ил)метокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 143b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 143a продукт примера 2b, получая указанное в заголовке соединение.
Пример 143c
N-{4-[(1,3-диметил-1H-пиразол-5-ил)метокси]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил}этансульфонамид
Продукт примера 143c получали согласно процедуре, используемой для получения продукта примера 4 (способ A), заменяя продуктом примера 143b продукт примера 3 и заменяя этансульфонил хлоридом метансульфонил хлорид, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,04-11,99 (м, 1H), 9,57 (с, 1H), 7,29-7,13 (м, 5H), 6,12-6,07 (м, 1H), 5,98 (с, 1H), 5,03 (с, 2H), 3,54 (с, 3H), 3,50 (с, 3H), 3,04 (кв., J=7,3 Гц, 2H), 2,05 (с, 3H), 1,21 (т, J=7,3 Гц, 3H). MS (ESI+) m/z 456,2 (M+H)+.
Пример 144
N-[4-(2,2-диметилпропокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил] этансульфонамид
Пример 144a
6-метил-4-(2-(неопентилокси)-5-нитрофенил)-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 144a получали согласно процедуре, используемой для получения продукта примера 29a, заменяя 2,2-диметилпропан-1-олом тетрагидро-2H-пиран-4-ол, получая указанное в заголовке соединение.
Пример 144b
4-(5-амино-2-(неопентилокси)фенил)-6-метил-1H-пирроло[2,3-с]пиридин-7(6H)-он
Продукт примера 144b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 144a продукт примера 2b, получая указанное в заголовке соединение.
Пример 144c
Продукт примера 144c получали согласно процедуре, используемой для получения продукта примера 4 (способ A), заменяя продуктом примера 144b продукт примера 3 и заменяя этансульфонил хлоридом метансульфонил хлорид, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,00 (с, 1H) 9,50 (с, 1H) 7,26-7,33 (м, 3H) 7,15 (дд, J=2,71, 8,82 Гц, 1H) 7,06 (д, J=9,16 Гц, 1H) 6,17-6,22 (м, 1H) 3,59 (с, 2H) 3,54 (с, 3H) 3,03 (кв., J=7,23 Гц, 2H) 1,21 (т, J=7,29 Гц, 3H) 0,84 (с, 9H). MS (ESI+) m/z 416,5 (M-H)+.
Пример 145
N-[4-(циклопропилметокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид
Пример 145a
4-(2-(циклопропилметокси)-5-нитрофенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 145a получали согласно процедуре, используемой для получения продукта примера 29a, заменяя циклопропилметанолом тетрагидро-2H-пиран-4-ол, получая указанное в заголовке соединение.
Пример 145b
4-(5-амино-2-(циклопропилметокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 145b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 145a продукт примера 2b, получая указанное в заголовке соединение.
Пример 145c
N-[4-(циклопропилметокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид
Продукт примера 145c получали согласно процедуре, используемой для получения продукта примера 4 (способ A), заменяя продуктом примера 145b продукт примера 3 и заменяя этансульфонил хлоридом метансульфонил хлорид, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,02-11,97 (м, 1H), 9,49 (с, 1H), 7,32-7,24 (м, 3H), 7,14 (дд, J=8,7, 2,7 Гц, 1H), 7,05 (д, J=8,8 Гц, 1H), 6,21-6,16 (м, 1H), 3,80 (д, J=6,7 Гц, 2H), 3,56 (с, 3H), 3,02 (кв., J=7,3 Гц, 2H), 1,21 (т, J=7,3 Гц, 3H), 1,08 (м, 1H), 0,50-0,39 (м, 2H), 0,27 0,18 (м, 2H). MS (ESI+) m/z 402,1 (M+H)+.
Пример 146
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид
Пример 146a
4-(2,4-дифторфенокси)-3-нитробензолсульфонамид
Раствор 2,4-дифторфенола (5,39 г, 41,4 ммоль) в N,N-диметилформамиде (34,5 мл) охлаждали до 10°C и обрабатывали порциями гидридом натрия (1,66 г, 41,4 ммоль). После перемешивания 15 минут добавляли порциями 4-фтор-3-нитробензолсульфонамид (2,28 г, 10,36 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 1,5 часов, разбавляли в этилацетате и гасили 0,5M HCl до pH 6. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали, получая указанное в заголовке соединение (3,24 г, 95%).
Пример 146b
3-амино-4-(2,4-дифторфенокси)бензолсульфонамид
Продукт примера 146a (3,24 г, 9,81 ммоль), железо (2,74 г, 49,1 ммоль) и хлорид аммония (0,787 г, 14,72 ммоль) перемешивали в смесм тетрагидрофурана (21 мл), этанола (21 мл) и воды (7 мл) при 95°C в течение 3 часов. Смесь фильтровали через нейлоновую мембрану и концентрировали. Остаток распределяли между этилацетатом и водой. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали, получая указанное в заголовке соединение (2,81 г, 95%).
Пример 146c
4-(2,4-дифторфенокси)-3-йодбензолсульфонамид
К раствору продукта примера 146b (2,8 г, 9,32 ммоль) в диоксане (20 мл) при 0°C добавляли концентрированную хлороводородную кислоту (40 мл, 9,32 ммоль). Смесь перемешивали 15 минут и добавляли раствор нитрита натрия (0,772 г, 11,19 ммоль) в воде (10 мл). Смесь перемешивали в течение 1 часа при 0°C. Раствор йодида калия (3,10 г, 18,7 ммоль) в воде (10 мл) добавляли и перемешивание продолжали 1 час при температуре окружающей среды. Смесь распределяли между этилацетатом и водой. Органический слой промывали насыщенным раствором тиосульфата натрия, водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали колоночной флаш-хроматографией (силикагель, 0-60% этилацетат в гексане), получая указанное в заголовке соединение (2,24 г, выход 58,4%).
Пример 146d
4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1Н-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид
Суспензию продукта примера 146c (111 мг, 0,270 ммоль), продукта примера 6a (150 мг, 0,351 ммоль), тетракис(трифенилфосфин)палладия(0) (31,2 мг, 0,027 ммоль) и фторида цезия (123 мг, 0,810 ммоль) в смеси 1,2 диметоксиэтана (4,6 мл) и метанола (2,3 мл) нагревали микроволновым излучением при 150°С в течение 5 минут. Реакционную смесь распределяли между этилацетатом (75 мл) и 50% водным раствором хлорида натрия (75 мл). Органический слой сушили над безводным сульфатом натрия, фильтровали и концентрировали. К раствору остатка в диоксане (4 мл) добавляли раствор гидрата гидроксида лития (113 мг, 2,7 ммоль) в воде (1 мл) и смесь нагревали микроволновым излучением при 120°С в течение 30 минут. Реакционную смесь распределяли между этилацетатом (75 мл) и водой (75 мл). Органический слой сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток очищали колоночной флаш-хроматографией (силикагель, 0,5-10% метанол в дихлорметане), получая указанное в заголовке соединение (74 мг, выход 63,5%). 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,09 (с, 1H), 7,92 (д, J=2,37 Гц, 1H), 7,76 (дд, J=8,82, 2,37 Гц, 1H), 7,43-7,53 (м, 1H), 7,28-7,40 (м, 5H), 7,08-7,18 (м, 1H), 6,95 (д, J=8,82 Гц, 1H), 6,27 (д, J=2,71 Гц, 1H), 3,58 (с, 3H). MS (ESI+) m/z 432,2 (M+H)+.
Пример 147
4-[2-(циклогексиламино)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 147a
2-бром-N-циклогексил-4-(метилсульфонил)анилин
Смесь 2-бром-1-фтор-4-(метилсульфонил)бензола (0,05 г, 0,198 ммоль) и циклогексанамина (0,059 г, 0,593 ммоль) в диоксане (1 мл) в склянке закрывали крышкой и нагревали при 110°C в течение трех дней. Реакционную смесь распределяли между водой и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали колоночной флаш-хроматографией на силикагеле, элюируя 40% этилацетатом в гексанах, получая указанное в заголовке соединение (0,044 г, 0,132 ммоль, выход 67,0%).
Пример 147b
4-[2-(циклогексиламино)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 147b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 147a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,13 (с, 1H), 7,66 (дд, J=8,7, 2,29 Гц, 1H), 7,51 (д, J=2,14 Гц, 1H), 7,30 (т, J=2,75 Гц, 1H), 7,26 (с, 1H), 6,86 (д, J=8,85 Гц, 1H), 6,00-6,01 (м, 1H), 4,83 (ушир., с, 1H), 3,56 (с, 3H), 3,35-3,44 (м, 1H), 1,84-1,87 (м, 2H), 1,53-1,62 (м, 3H), 1,27-1,37 (м, 2H), 1,03-1,12 (м, 3H), MS (APCI+) m/z 400,1 (M+H)+.
Пример 148
4-[5-амино-2-(2,4-дифторфенокси)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-d]пиридазин-7-он
Пример 148a
Продукт примера 148a получали согласно процедуре, используемой для получения продукта примера 2b, заменяя 2-бром-1-фтор-4-нитробензолом продукт примера 2a и 2,4-дифторфенолом фенол, соответственно, получая указанное в заголовке соединение.
Пример 148b
3-бром-4-(2,4-дифторфенокси)анилин
Продукт примера 148b получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 148a продукт примера 2b, получая указанное в заголовке соединение.
Пример 148c
4-(2,4-дифторфенокси)-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)анилин
Продукт примера 148c получали согласно процедуре, используемой для получения продукта примера 6a, заменяя продуктом примера 148b продукт примера 1e, получая указанное в заголовке соединение.
Пример 148d
4-[5-амино-2-(2,4-дифторфенокси)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-d]пиридазин-7-он
Продукт примера 148d получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 80b продукт примера 95c и продуктом примера 148c продукт примера 6a, соответственно, получая TFA соль указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,69 (с, 1H), 7,44 (т, J=2,59 Гц, 1H), 7,32-7,37 (м, 2H), 7,16 (д, J=2,75 Гц, 1H), 7,05-7,12 (м, 1H), 6,97-7,02 (м, 1H), 6,92 (д, J=8,54 Гц, 1H), 3,37-6,39 (м, 1H), 3,70 (с, 3H). MS (ESI+) m/z 369,4 (M+H)+.
Пример 149
4-[2-(2-фторфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 149 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 2-фторфенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,99 (д, J=2,4 Гц, 1H), 7,89 (дт, J=7,7, 3,9 Гц, 1H), 7,50-7,38 (м, 2H), 7,35-7,24 (м, 4H), 6,98 (д, J=8,6 Гц, 1H), 6,32 (д, J=2,8 Гц, 1H), 3,60 (с, 3H), 3,26 (с, 3H). MS (ESI+) m/z 413(M+H)+.
Пример 150
4-[2-(3-фторфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 150 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 3-фторфенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,01 (т, J=3,4 Гц, 1H), 7,93 (дт, J=7,1, 3,5 Гц, 1H), 7,47-7,37 (м, 2H), 7,34 (т, J=3,3 Гц, 1H), 7,21 (т, J=6,3 Гц, 1H), 6,96 (дддд, J=26,2, 21,5, 8,3, 2,2 Гц, 3H), 6,30 (д, J=2,8 Гц, 1H), 3,57 (с, 3H), 3,27 (с, 3H). MS (ESI+) m/z 413(M+H)+.
Пример 151
4-[2-(4-фторфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 151 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 4-фторфенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,98 (д, J=2,4 Гц, 1H), 7,89 (дд, J=8,7, 2,4 Гц, 1H), 7,43 (с, 1H), 7,34 (д, J=2,8 Гц, 1H), 7,31-7,22 (м, 2H), 7,22-7,10 (м, 2H), 7,04 (д, J=8,7 Гц, 1H), 6,31 (д, J=2,8 Гц, 1H), 3,59 (с, 3H), 3,25 (с, 3H). MS (ESI+) m/z 413(M+H)+.
Пример 152
4-[2-(2-хлорфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 152 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 2-хлорфенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,02 (дд, J=7,0, 1,6 Гц, 1H), 7,96-7,85 (м, 1H), 7,65-7,57 (м, 1H), 7,47 (с, 1H), 7,44-7,34 (м, 2H), 7,33-7,21 (м, 2H), 6,92 (д, J=8,7 Гц, 1H), 6,37 (д, J=2,8 Гц, 1H), 3,59 (с, 3H), 3,26 (с, 3H). MS (ESI+) m/z 429(M+H)+.
Пример 153
4-[2-(3-хлорфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 153 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 3-хлорфенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,01 (д, J=2,4 Гц, 1H), 7,99-7,88 (м, 1H), 7,43-7,37 (м, 2H), 7,35 (т, J=3,3 Гц, 1H), 7,27-7,19 (м, 2H), 7,16 (дд, J=10,2, 8,1 Гц, 1H), 7,08-6,93 (м, 1H), 6,30 (д, J=2,8 Гц, 1H), 3,57 (с, 3H), 3,27 (с, 3H). MS (ESI+) m/z 429(M+H)+.
Пример 154
4-[2-(4-хлорфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 154 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 4-хлорфенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,00 (д, J=2,4 Гц, 1H), 7,91 (дд, J=8,3, 2,0 Гц, 1H), 7,56-7,38 (м, 3H), 7,34 (т, J=3,3 Гц, 1H), 7,19-7,07 (м, 3H), 6,29 (д, J=2,8 Гц, 1H), 3,58 (с, 3H), 3,26 (с, 3H). MS (ESI+) m/z 429(M+H)+.
Пример 155
3-[2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(метилсульфонил)фенокси]бензонитрил
Продукт примера 155 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 3-цианофенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,02 (д, J=2,4 Гц, 1H), 7,99-7,91 (м, 1H), 7,68-7,49 (м, 3H), 7,46-7,38 (м, 2H), 7,38-7,32 (м, 1H), 7,24 (д, J=8,6 Гц, 1H), 6,30 (д, J=2,8 Гц, 1H), 3,56 (с, 3H), 3,28 (с, 3H). MS (ESI+) m/z 420(M+H)+.
Пример 156
4-[2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(метилсульфонил)фенокси]бензонитрил
Продукт примера 156 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 4-цианофенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,05 (д, J=2,4 Гц, 1H), 8,02-7,94 (м, 1H), 7,80-7,73 (м, 2H), 7,38 (т, J=4,3 Гц, 2H), 7,33 (т, J=3,3 Гц, 1H), 7,17-7,03 (м, 2H), 6,25 (д, J=2,8 Гц, 1H), 3,54 (с, 3H), 3,29 (с, 3H). MS (ESI+) m/z 420(M+H)+.
Пример 157
6-метил-4-{5-(метилсульфонил)-2-[3-(трифторметил)фенокси]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 157 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 3-трифторметилфенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,03 (д, J=2,4 Гц, 1H), 7,95 (дд, J=8,6, 2,4 Гц, 1H), 7,62-7,56 (м, 1H), 7,54-7,48 (м, 1H), 7,42 (д, J=7,1 Гц, 1H), 7,37-7,31 (м, 3H), 7,25 (д, J=8,6 Гц, 1H), 6,30 (д, J=2,8 Гц, 1H), 3,55 (с, 3H), 3,28 (с, 3H). MS (ESI+) m/z 463(M+H)+.
Пример 158
4-[2-(циклопропилметокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Циклопропилметанол (0,014 г, 0,19 ммоль) в тетрагидрофуране (2 мл) обрабатывали 60% гидридом натрия (10,11 мг, 0,253 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 5 минут. К этому раствору добавляли продукт примера 138a (0,03 г, 0,063 ммоль). Реакционную смесь нагревали при 60°C в течение 16 часов. Растворитель удаляли и остаток очищали препаративной ВЭЖХ (C18, 10-80% CH3CN/вода (0,1% TFA)), получая указанное в заголовке соединение (0,012 г, 0,032 ммоль, выход 51,0%). 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,88 (дд, J=8,6, 2,5 Гц, 1H), 7,84 (д, J=2,4 Гц, 1H), 7,37 (с, 1H), 7,34 (д, J=2,4 Гц, 2H), 7,32 (д, J=3,5 Гц, 2H), 6,17 (д, J=2,8 Гц, 1H), 3,99 (д, J=6,8 Гц, 2H), 3,20 (с, 3H), 1,17-1,06 (м, 1H), 0,52-0,41 (м, 2H), 0,34-0,24 (м, 2H),MS (ESI+) m/z 373 (M+H)+.
Пример 159
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-4-ил)фенил]метансульфонамид
Продукт примера 159 получали согласно процедуре, используемой для получения продукта примера 4 (способ A), заменяя продуктом примера 148d продукт примера 3, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,72 (с, 1H), 9,79 (с, 1H), 7,45 (т, J=2,59 Гц, 1H), 7,40 (т, J=2,44 Гц, 1H), 7,31-7,38 (м, 2H), 7,11-7,17 (м, 1H), 6,89-7,03 (м, 1H), 6,39-6,40 (м, 1H), 3,70 (с, 3H), 3,02 (с, 3H). MS (ESI+) m/z 447,1 (M+H)+.
Пример 160
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-d]пиридазин-4-ил)фенил]этансульфонамид
Продукт примера 160 получали согласно процедуре, используемой для получения продукта примера 4 (способ A), заменяя продуктом примера 148d продукт примера 3 и этансульфонил хлоридом метансульфонил хлорид, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,72 (с, 1H), 9,86 (с, 1H), 7,45 (т, J=2,75 Гц, 1H), 7,41 (д, J=2,75 Гц, 1H), 7,31-7,40 (м, 2H), 7,10-7,16 (м, 1H), 6,98-7,03 (м, 1H), 6,38-6,39 (м, 1H), 3,70 (с, 3H), 3,11 (кв., J=7,43 Гц, 2H), 1,23 (т, J=7,32 Гц, 3H). MS (ESI+) m/z 461,1 (M+H)+.
Пример 161
4-[2-(изохинолин-5-илокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 161 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя изохинолин-5-олом 2,4-дифторфенол, получая TFA соль указанного в заголовке соединения. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 9,68 (с, 1H), 8,58 (д, J=6,4 Гц, 1H), 8,30 (д, J=6,4 Гц, 1H), 8,11 (т, J=4,9 Гц, 2H), 8,00 (дд, J=8,6, 2,4 Гц, 1H), 7,78 (т, J=8,1 Гц, 1H), 7,55-7,46 (м, 2H), 7,40 (д, J=8,6 Гц, 1H), 7,33 (д, J=2,8 Гц, 1H), 6,39 (д, J=2,8 Гц, 1H), 3,97 (с, 1H), 3,47 (с, 3H), 3,31 (с, 3H). MS (ESI+) m/z 445 (M+H)+.
Пример 162
6-метил-4-[5-(метилсульфонил)-2-(хинолин-6-илокси)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 162 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя хинолин-6-олом 2,4-дифторфенол, получая TFA соль указанного в заголовке соединения. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 9,03 (дд, J=4,8, 1,4 Гц, 1H), 8,71 (д, J=8,1 Гц, 1H), 8,15 (д, J=9,0 Гц, 1H), 8,08 (д, J=2,4 Гц, 1H), 7,99 (дд, J=8,6, 2,4 Гц, 1H), 7,88-7,80 (м, 1H), 7,74 (дт, J=3,7, 2,5 Гц, 2H), 7,45 (с, 1H), 7,37 (д, J=8,6 Гц, 1H), 7,32 (т, J=3,3 Гц, 1H), 6,34 (д, J=2,8 Гц, 1H), 3,53 (д, J=6,8 Гц, 3H), 3,30 (с, 3H). MS (ESI+) m/z 446 (M+H)+.
Пример 163
4-{2-[2-хлор-5-(трифторметил)фенокси]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 163 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 2-хлор-5-трифторметилфенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,03 (д, J=2,4 Гц, 1H), 7,94 (дд, J=8,7, 2,4 Гц, 1H), 7,79 (д, J=8,3 Гц, 1H), 7,58 (дд, J=16,2, 8,4 Гц, 1H), 7,49 (д, J=1,8 Гц, 1H), 7,44 (с, 1H), 7,34 (д, J=2,8 Гц, 1H), 7,27-7,13 (м, 2H), 6,33 (д, J=2,9 Гц, 1H), 3,56 (с, 3H), 3,28 (с, 3H). MS (ESI+) m/z 496 (M+H)+.
Пример 164
4-{2-[2-фтор-5-(трифторметил)фенокси]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 164 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 2-фтор-5-трифторметилфенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,01 (д, J=2,4 Гц, 1H), 7,93 (дд, J=8,6, 2,4 Гц, 1H), 7,67-7,55 (м, 3H), 7,43 (с, 1H), 7,34 (д, J=2,8 Гц, 1H), 7,23-7,15 (м, 2H), 6,29 (д, J=2,8 Гц, 1H), 3,57 (с, 3H), 3,27 (с, 3H). MS (ESI+) m/z 480 (M+H)+.
Пример 165
2-{4-[2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(метилсульфонил)фенокси]фенил}ацетамид
Продукт примера 165 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 2-(4-гидроксифенил)ацетамидом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,97 (д, J=2,4 Гц, 1H), 7,88 (дд, J=8,6, 2,4 Гц, 1H), 7,43 (с, 1H), 7,36-7,30 (м, 3H), 7,09-7,00 (м, 3H), 6,31 (д, J=2,8 Гц, 1H), 3,59 (с, 3H), 3,39 (с, 2H), 3,24 (с, 3H). MS (ESI+) m/z 452(M+H)+.
Пример 166
4-[2-(3-аминофенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 166 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 3-аминофенолом 2,4-дифторфенол, получая TFA соль указанного в заголовке соединения. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,00 (д, J=2,4 Гц, 1H), 7,92 (дд, J=8,6, 2,4 Гц, 1H), 7,40 (с, 1H), 7,36-7,24 (м, 2H), 7,15 (д, J=8,6 Гц, 1H), 6,78 (дд, J=8,0, 1,9 Гц, 1H), 6,70-6,62 (м, 2H), 6,27 (д, J=2,8 Гц, 1H), 3,96 (с, 1H), 3,58 (с, 3H), 3,26 (с, 3H). MS (ESI+) m/z 410(M+H)+.
Пример 167
6-метил-4-[5-(метилсульфонил)-2-(тетрагидрофуран-3-иламино)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 167a
N-(2-бром-4-(метилсульфонил)фенил)тетрагидрофуран-3-амин
Продукт примера 167a получали согласно процедуре, используемой для получения продукта примера 147a, заменяя тетрагидрофуран-3-амином циклогексанамин, получая указанное в заголовке соединение.
Пример 167b
6-метил-4-[5-(метилсульфонил)-2-(тетрагидрофуран-3-иламино) фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 167b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 167a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,12 (с, 1H), 7,70 (дд, J=8,7, 2,29 Гц, 1H), 7,54 (д, J=2,44 Гц, 1H), 7,29 (т, J=2,75 Гц, 1H), 7,27 (с, 1H), 6,87 (д, J=8,85 Гц, 1H), 6,00 (т, J=2,29 Гц, 1H), 5,25 (ушир. с, 1H), 4,17 (ушир. с, 1H), 3,68 (кв., J=7,32, Гц, 2H), 3,56 (с, 3H), 3,49 (дд, J=9, 3,51 Гц, 1H), 3,12 (с, 3H), 2,12-2,19 (м, 1H), 1,74-1,77 (м, 1H). MS (ESI+) m/z 388,2 (M+H)+.
Пример 168
4-[2-(2,4-дифторфенокси)-5-(этилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 168a
(3-бром-4-фторфенил)(этил)сульфан
Смесь 3-бром-4-фторбензолтиола (3,89 г, 18,79 ммоль) и гидроксида натрия (3,95 мл, 19,73 ммоль) в MeOH перемешивали при 0°C в течение 10 минут. К этому раствору добавляли йодэтан (1,803 мл, 22,54 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 6 часов. Растворитель удаляли и остаток распределяли между водой и этилацетатом. Водный слой экстрагировали добавлением этилацетата три раза. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали, получая указанное в заголовке соединение (4,35 г, 18,50 ммоль, выход 98%). Его использовали непосредственно для следующей реакции.
Пример 168b
2-бром-4-(этилсульфонил)-1-фторбензол
Продукт примера 168a (4,4 г, 18,71 ммоль) в дихлорметане (250 мл) охлаждали до 0°C. К этому раствору добавляли mCPBA (10,15 г, 41,2 ммоль) порциями. Реакционную смесь перемешивали при температуре окружающей среды в течение 6 часов. Твердое вещество из реакционной смеси удаляли фильтрованием. Фильтрат промывали насыщенным водным раствором бикарбоната натрия несколько раз. Водный слой затем экстрагировали дополнительным дихлорметаном три раза. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией на силикагеле, элюируя 15% этилацетат/гексаны, получая указанное в заголовке соединение (4,4 г, 16,47 ммоль, выход 88%).
Пример 168c
4-(5-(этилсульфонил)-2-фторфенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 168c получали согласно процедуре, используемой для получения продукта примера 138a, заменяя продуктом примера 168b 2-бром-1-фтор-4-(метилсульфонил)бензол, получая указанное в заголовке соединение.
Пример 168d
4-[2-(2,4-дифторфенокси)-5-(этилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 168d получали согласно процедуре, используемой для получения продукта примера 138b, заменяя продуктом примера 168c продукт примера 138a, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,31 (с, 1H), 7,93 (д, J=2,44 Гц, 1H), 7,83 (дд, J=8,54, 2,44 Гц, 1H), 7,52-7,54 (м, 1H), 7,42-7,46 (м, 2H), 7,32 (т, J=2,75 Гц, 1H), 7,16-7,19 (м, 1H), 6,99 (д, J=8,54 Гц, 1H), 6,27-6,28 (м, 1H), 3,59 (с, 3H), 3,38 (кв., J=7,32, Гц, 2H), 1,15 (т, J=7,32 Гц, 1H). MS (ESI+) m/z 445,2 (M+H)+.
Пример 169
4-{2-[(4,4-дифторциклогексил)окси]-5-(этилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 169 получали согласно процедуре, используемой для получения продукта примера 158, заменяя продуктом примера 168c продукт примера 138a и 4,4-дифторциклогексанолом циклопропилметанол, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,05 (с, 1H), 7,81-7,85 (м, 2H), 7,45 (д, J=8,85 Гц, 1H), 7,33 (с, 1H), 7,29 (т, J=2,75 Гц, 1H), 6,12-6,13 (м, 1H), 4,81 (с, 1H), 3,56 (с, 3H), 3,29 (кв., J=7,32, Гц, 2H), 1,70-1,87 (м, 8H), 1,14 (т, J=7,32 Гц, 1H). MS (ESI+) m/z 451,2 (M+H)+.
Пример 170
4-{5-(этилсульфонил)-2-[(1-метилпиперидин-4-ил)окси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 170 получали согласно процедуре, используемой для получения продукта примера 158, заменяя продуктом примера 168c продукт примера 138a и 1-метилпиперидин-4-олом циклопропилметанол, соответственно, получая TFA соль указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,13 (с, 1H), 7,81-7,87 (м, 2H), 7,46 (д, J=8,85 Гц, 1H), 7,34 (с, 1H), 7,32 (т, J=2,75 Гц, 1H), 6,11-6,12 (м, 1H), 4,86 (с, 1H), 3,56 (с, 3H), 3,30 (с, 3H), 3,29 (кв., J=7,32, Гц, 2H), 3,24-3,29 (м, 1H), 3,04-3,10 (м,1H), 2,25-2,29 (м, 2H), 1,91-2,05 (м, 2H), 1,14 (т, J=7,32 Гц, 1H). MS (ESI+) m/z 430,2 (M+H)+.
Пример 171
4-[2-(2,1,3-бензотиадиазол-4-илокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 171 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя бензо[c][1,2,5]тиадиазол-5-олом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,04 (д, J=2,4 Гц, 1H), 7,93 (д, J=8,4 Гц, 1H), 7,84 (дд, J=8,6, 2,4 Гц, 1H), 7,69 (дд, J=8,8, 7,5 Гц, 1H), 7,50 (с, 1H), 7,36 (д, J=7,1 Гц, 1H), 7,29 (д, J=2,8 Гц, 1H), 7,09 (д, J=8,7 Гц, 1H), 6,49 (д, J=2,8 Гц, 1H), 3,55 (с, 3H), 3,27 (с, 3H). MS (ESI+) m/z 453(M+H)+.
Пример 172
4-[2-(изохинолин-7-илокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 172 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя изохинолин-7-олом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,65 (с, 1H), 8,39 (с, 1H), 8,24 (д, J=8,9 Гц, 1H), 8,16-8,04 (м, 1H), 8,03 (дд, J=8,6, 2,4 Гц, 1H), 7,95-7,76 (м, 2H), 7,47 (дд, J=20,3, 11,7 Гц, 2H), 7,31 (т, J=5,9 Гц, 1H), 6,32 (д, J=2,8 Гц, 1H), 3,51 (с, 3H), 3,31 (с, 3H). MS (ESI+) m/z 446(M+H)+.
Пример 173
4-[2-(2,5-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 173 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 2,5-дифторфенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,08-7,98 (м, 1H), 7,97-7,83 (м, 1H), 7,50-7,39 (м, 2H), 7,35 (т, J=3,3 Гц, 1H), 7,33-7,21 (м, 1H), 7,20-7,08 (м, 2H), 6,31 (д, J=2,8 Гц, 1H), 3,59 (с, 3H), 3,25 (д, J=6,7 Гц, 3H) MS (ESI+) m/z 431(M+H)+.
Пример 174
4-[2-(3,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 174 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 3,4-дифторфенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,99 (д, J=2,4 Гц, 1H), 7,91 (дд, J=8,6, 2,4 Гц, 1H), 7,53-7,40 (м, 2H), 7,34 (д, J=2,8 Гц, 1H), 7,29 (ддд, J=11,4, 6,8, 2,9 Гц, 1H), 7,16 (д, J=8,7 Гц, 1H), 6,95 (дд, J=8,8, 5,0 Гц, 1H), 6,31 (д, J=2,8 Гц, 1H), 3,58 (с, 3H), 3,25 (с, 3H). MS (ESI+) m/z 431(M+H)+.
Пример 175
6-метил-4-{5-(метилсульфонил)-2-[(1-оксо-2,3-дигидро-1H-инден-4-ил)окси]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 175 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 4-гидрокси-2,3-дигидро-1H-инден-1-оном 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,02 (д, J=2,4 Гц, 1H), 7,92 (дд, J=8,6, 2,4 Гц, 1H), 7,50-7,41 (м, 1H), 7,36 (д, J=2,8 Гц, 1H), 7,28 (дд, J=7,3, 1,4 Гц, 1H), 7,16 (д, J=8,6 Гц, 1H), 6,32 (д, J=2,8 Гц, 1H), 3,62-3,54 (м, 2H), 3,27 (с, 1H), 2,89-2,82 (м, 1H), 2,65-2,59 (м, 1H). MS (ESI+) m/z 449(M+H)+.
Пример 176
4-[2-(3,5-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 176 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 3,5-дифторфенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,02 (д, J=2,4 Гц, 1H), 7,96 (дд, J=8,6, 2,4 Гц, 1H), 7,40 (с, 1H), 7,34 (дд, J=5,7, 2,8 Гц, 2H), 6,98 (тт, J=9,3, 2,3 Гц, 1H), 6,83-6,62 (м, 2H), 6,29 (д, J=2,8 Гц, 1H), 3,56 (с, 3H), 3,27 (с, 3H). MS (ESI+) m/z 431(M+H)+.
Пример 177
6-метил-4-[2-(4-метилфенокси)-5-(метилсульфонил)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 177 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 4-метилфенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,96 (д, J=2,4 Гц, 1H), 7,88-7,79 (м, 1H), 7,42 (с, 1H), 7,33 (д, J=2,8 Гц, 1H), 7,24 (д, J=8,4 Гц, 2H), 7,00 (дд, J=8,6, 4,3 Гц, 3H), 6,30 (д, J=2,8 Гц, 1H), 3,59 (с, 3H), 3,24 (с, 3H). MS (ESI+) m/z 409(M+H)+.
Пример 178
4-[2-(2-метоксифенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 178 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 2-метоксифенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,94 (д, J=2,4 Гц, 1H), 7,81 (дд, J=8,7, 2,4 Гц, 1H), 7,47 (с, 1H), 7,39-7,25 (м, 2H), 7,26-7,13 (м, 2H), 7,03 (тд, J=7,6, 1,5 Гц, 1H), 6,75 (д, J=8,7 Гц, 1H), 6,43 (д, J=2,8 Гц, 1H), 3,61 (с, 3H), 3,23 (с, 3H). MS (ESI+) m/z 425(M+H)+.
Пример 179
6-метил-4-{2-[(2-метилпиридин-3-ил)окси]-5-(метилсульфонил)фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 179 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 2-метилпиридин-3-олом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,38 (д, J=2,1 Гц, 1H), 8,05 (д, J=2,4 Гц, 1H), 7,98 (дд, J=8,5, 2,4 Гц, 1H), 7,73 (д, J=8,3 Гц, 1H), 7,53 (дд, J=8,4, 4,9 Гц, 1H), 7,43 (с, 1H), 7,35 (д, J=2,8 Гц, 1H), 7,28 (д, J=8,5 Гц, 1H), 6,30 (д, J=2,8 Гц, 1H), 3,56 (с, 3H), 3,28 (с, 3H), 2,41 (с, 3H). MS (ESI+) m/z 410(M+H)+.
Пример 180
4-{2-[3-(диметиламино)фенокси]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 180 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 3-(диметиламино)фенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,97 (д, J=2,4 Гц, 1H), 7,88 (дд, J=8,6, 2,4 Гц, 1H), 7,42 (с, 1H), 7,34 (д, J=2,8 Гц, 1H), 7,26 (т, J=8,1 Гц, 1H), 7,08 (д, J=8,6 Гц, 1H), 6,68 (дд, J=8,3, 2,4 Гц, 1H), 6,52-6,43 (м, 2H), 6,31 (д, J=2,8 Гц, 1H), 3,58 (с, 3H), 3,24 (с, 3H), 2,90 (с, 6H). MS (ESI+) m/z 438(M+H)+.
Пример 181
6-метил-4-{5-(метилсульфонил)-2-[(1-оксо-2,3-дигидро-1H-инден-5-ил)окси]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 181 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 5-гидрокси-2,3-дигидро-1H-инден-1-оном 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,04 (д, J=2,4 Гц, 1H), 7,98 (дд, J=8,6, 2,4 Гц, 1H), 7,60 (д, J=8,4 Гц, 1H), 7,40 (с, 1H), 7,34 (дд, J=6,9, 5,8 Гц, 2H), 7,11 (с, 1H), 7,08-6,97 (м, 1H), 6,28 (д, J=2,9 Гц, 1H), 3,54 (с, 3H), 3,29 (с, 3H), 3,00 (д, J=5,0 Гц, 2H), 2,62-2,58 (м, 2H). MS (ESI+) m/z 449(M+H)
Пример 182
6-метил-4-{5-(метилсульфонил)-2-[(3-оксо-2,3-дигидро-1H-инден-5-ил)окси]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 182 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 6-гидрокси-2,3-дигидро-1H-инден-1-оном 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,01 (д, J=2,5 Гц, 1H), 7,92 (д, J=8,6 Гц, 1H), 7,61 (д, J=8,7 Гц, 1H), 7,42 (д, J=14,0 Гц, 2H), 7,34 (д, J=2,8 Гц, 1H), 7,22-7,10 (м, 2H), 6,30 (д, J=2,8 Гц, 1H), 3,56 (с, 3H), 3,26 (с, 3H), 3,06 (с, 2H), 2,69 (с, 3H). MS (ESI+) m/z 449(M+H)+.
Пример 183
2-[2-(6-метил-7-оксо-6,7-дигидро-1H-pyн-олo[2,3-c]пиридин-4-ил)-4-(метилсульфонил)фенокси]бензонитрил
Продукт примера 183 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 2-цианофенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,06 (д, J=2,4 Гц, 1H), 7,99 (дд, J=8,5, 2,4 Гц, 1H), 7,81 (дд, J=7,7, 1,6 Гц, 1H), 7,67-7,59 (м, 1H), 7,41 (с, 1H), 7,39-7,24 (м, 3H), 7,09 (д, J=8,4 Гц, 1H), 6,30 (д, J=2,8 Гц, 1H), 3,56 (с, 3H), 3,29 (с, 3H). MS (ESI+) m/z 420(M+H)+.
Пример 184
4-[2-(3-хлор-2-фторфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 184 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 2-фтор-3-хлорфенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,00 (д, J=2,4 Гц, 1H), 7,92 (дд, J=8,6, 2,4 Гц, 1H), 7,47-7,41 (м, 2H), 7,35 (д, J=2,8 Гц, 1H), 7,28-7,23 (м, 2H), 7,13 (д, J=8,6 Гц, 1H), 6,28 (д, J=2,8 Гц, 1H), 3,59 (с, 3H), 3,26 (с, 3H). MS (ESI+) m/z 447(M+H)+.
Пример 185
6-метил-4-[5-(метилсульфонил)-2-(нафталин-1-илокси)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 185 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя нафталин-1-олом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,02 (д, J=2,4 Гц, 1H), 7,99 (д, J=8,9 Гц, 2H), 7,96-7,87 (м, 2H), 7,86 (д, J=8,0 Гц, 1H), 7,59-7,44 (м, 4H), 7,36-7,28 (м, 2H), 7,15 (д, J=8,6 Гц, 1H), 6,37 (д, J=2,8 Гц, 1H), 3,58 (с, 3H), 3,26 (с, 3H). MS (ESI+) m/z 445(M+H)+.
Пример 186
4-[2-(2-фтор-5-метилфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 186 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 2-фтор-5метилфенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,98 (д, J=2,4 Гц, 1H), 7,89 (дд, J=8,6, 2,4 Гц, 1H), 7,43 (с, 1H), 7,35 (д, J=2,8 Гц, 1H), 7,27 (дд, J=10,9, 8,1 Гц, 1H), 7,14-7,06 (м, 2H), 6,98 (д, J=8,6 Гц, 1H), 6,31 (д, J=2,8 Гц, 1H), 3,60 (с, 3H), 3,25 (с, 3H), 2,27 (с, 3H). MS (ESI+) m/z 427(M+H)+.
Пример 187
4-[2-(5-фтор-2-метилфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 187 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 5-фтор-2-метилфенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,11-7,96 (м, 1H), 7,91 (дт, J=5,1, 2,8 Гц, 1H), 7,43 (с, 1H), 7,38-7,28 (м, 2H), 7,07-6,91 (м, 2H), 6,91-6,81 (м, 1H), 6,31 (т, J=3,9 Гц, 1H), 3,58 (с, 3H), 3,26 (с, 3H), 2,04 (с, 3H). MS (ESI+) m/z 427(M+H)+.
Пример 188
6-метил-4-[5-(метилсульфонил)-2-(хинолин-7-илокси)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 188 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя хинолин-7-олом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,97 (с, 1H), 8,67 (д, J=8,5 Гц, 1H), 8,12 (дд, J=12,8, 5,7 Гц, 2H), 8,02 (дд, J=8,6, 2,4 Гц, 1H), 7,69 (дд, J=8,3, 4,8 Гц, 1H), 7,55-7,41 (м, 4H), 7,32 (д, J=2,8 Гц, 1H), 6,32 (с, 1H), 3,50 (д, J=16,9 Гц, 3H), 3,30 (д, J=9,2 Гц, 3H). MS (ESI+) m/z 446(M+H)+.
Пример 189
4-[2-(4-хлор-3-фторфенокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 189 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 3-фтор-4-хлорфенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,01 (т, J=3,5 Гц, 1H), 7,99-7,90 (м, 1H), 7,68-7,52 (м, 1H), 7,40 (с, 1H), 7,33 (д, J=2,8 Гц, 1H), 7,29-7,24 (м, 1H), 7,20 (дд, J=10,3, 2,7 Гц, 1H), 7,00-6,86 (м, 1H), 6,29 (т, J=3,4 Гц, 1H), 3,57 (с, 3H), 3,27 (с, 3H). MS (ESI+) m/z 447(M+H)+.
Пример 190
6-метил-4-[5-(метилсульфонил)-2-(пиридин-3-илокси)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 190 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя пиридин-3-олом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,03 (д, J=2,3 Гц, 1H), 8,01-7,90 (м, 1H), 7,72-7,64 (м, 1H), 7,42 (д, J=7,2 Гц, 1H), 7,37-7,30 (м, 1H), 7,30-7,15 (м, 1H), 6,36-6,24 (м, 1H), 3,56 (с, 3H), 3,27 (с, 3H). MS (ESI+) m/z 395(M+H)+.
Пример 191
4-[2-(2,3-дигидро-1H-инден-5-илокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 191 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 2,3-дигидро-1H-инден-5-олом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,96 (д, J=2,4 Гц, 1H), 7,86 (дд, J=8,6, 2,4 Гц, 1H), 7,42 (с, 1H), 7,34 (д, J=2,8 Гц, 1H), 7,26 (д, J=8,1 Гц, 1H), 7,00 (д, J=8,7 Гц, 2H), 6,98 (д, J=2,2 Гц, 1H), 6,85 (дд, J=8,1, 2,3 Гц, 1H), 6,31 (д, J=2,8 Гц, 1H), 3,59 (с, 3H), 3,23 (с, 3H), 2,88-2,79 (м, 4H), 2,03 (p, J=7,4 Гц, 2H). MS (ESI+) m/z 435(M+H)+.
Пример 192
6-метил-4-{5-(метилсульфонил)-2-[4-(пропан-2-ил)фенокси]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 192 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 4-изопропилфенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,97 (д, J=2,4 Гц, 1H), 7,88 (дд, J=8,6, 2,4 Гц, 1H), 7,42 (с, 1H), 7,33 (д, J=2,8 Гц, 1H), 7,32-7,26 (м, 2H), 7,06-6,98 (м, 3H), 6,30 (д, J=2,8 Гц, 1H), 3,58 (с, 3H), 3,24 (с, 3H), 2,89 (p, J=6,9 Гц, 1H), 1,19 (д, J=6,9 Гц, 6H) MS (ESI+) m/z 437(M+H)+.
Пример 193
4-[2-(изохинолин-8-илокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 193 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя изохинолин-8-олом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,34 (ушир.с, 1H), 8,12 (д, J=2,3 Гц, 1H), 8,05 (дд, J=8,4, 2,4 Гц, 1H), 7,86 (т, J=7,9 Гц, 1H), 7,79 (д, J=8,2 Гц, 1H), 7,55 (д, J=8,5 Гц, 1H), 7,48 (с, 1H), 7,32 (д, J=2,6 Гц, 1H), 7,17-7,11 (м, 1H), 6,40 (д, J=2,6 Гц, 1H), 3,44 (с, 3H), 3,32 (с, 3H). MS (ESI+) m/z 446(M+H)+.
Пример 194
6-метил-4-[5-(метилсульфонил)-2-(3,4,5-трифторфенокси)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 194 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 3,4,5-трифторфенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 8,00 (д, J=2,4 Гц, 1H), 7,94 (дд, J=8,6, 2,4 Гц, 1H), 7,41 (с, 1H), 7,34 (д, J=2,8 Гц, 1H), 7,28 (д, J=8,6 Гц, 1H), 7,18-7,10 (м, 2H), 6,31 (д, J=2,8 Гц, 1H), 3,57 (с, 3H), 3,26 (с, 3H). MS (ESI+) m/z 449(M+H)+.
Пример 195
4-(2-бензилфенил)-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 195 получали согласно процедуре, используемой для получения продукта примера 95d, заменяя 1-бензил-2-бромбензолом продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,08 (с, 1H), 7,23-7,34 (м, 5H), 7,16-7,19 (м, 2H), 7,09-7,12 (м, 1H), 6,92-6,93 (м, 3H), 5,95 (т, J=2,29 Гц, 1H), 3,89 (с, 2H), 3,47 (с, 3H). MS (ESI+) m/z 315,3 (M+H)+.
Пример 196
4-(бифенил-2-ил)-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 196 получали согласно процедуре, используемой для получения продукта примера 95d, заменяя бифенил-2-илбороновой кислотой продукт примера 6a и продуктом примера 1e продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 11,88 (с, 1H), 7,44-7,49 (м, 4H), 7,18-7,24 (м, 4H), 7,13-7,16 (м, 1H), 7,08 (т, J=2,75 Гц, 1H), 6,93 (с, 1H), 5,77-5,78 (м, 1H), 3,38 (с, 3H). MS (ESI+) m/z 301,2 (M+H)+.
Пример 197
4-[2-(1,4-диоксаспиро[4.5]дец-8-илокси)-5-(этилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 197 получали согласно процедуре, используемой для получения продукта примера 158, заменяя продуктом примера 168c продукт примера 138a и 1,4-диоксаспиро[4,5]декан-8-олом циклопропилметанол, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,05 (с, 1H), 7,79-7,81 (м, 2H), 7,40-7,42 (м, 1H), 7,28-7,34 (м, 2H), 6,6,12-6,13 (м, 1H), 4,70-4,73 (м, 1H), 3,79-3,34 (м, 3H), 3,65 (с, 3H), 3,26-3,31 (м, 2H), 1,99-2,21 (м, 1H), 1,67-1,99 (м, 2H), 1,48-1,52 (м, 3H), 1,14 (т, J=7,32 Гц, 3H). MS (ESI+) m/z 473,2 (M+H)+.
Пример 198
4-[2-(циклопропилметокси)-5-(этилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 198 получали согласно процедуре, используемой для получения продукта примера 158, заменяя продуктом примера 168c продукт примера 138a, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,04 (с, 1H), 7,79-7,82 (м, 2H), 7,37 (с, 1H), 7,29-7,33 (м, 2H), 6,13-6,14 (м, 1H), 3,99 (д, J=6,71 Гц, 2H), 3,58 (с, 3H), 3,27 (кв., J=7,32 Гц, 2H), 1,11-1,14 (м, 4H), 0,45-,048 (м, 2H), 0,26-0,29 (м, 2H). MS (ESI+) m/z 387,2 (M+H)+.
Пример 199
4-{5-(этилсульфонил)-2-[(4-оксоциклогексил)окси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 197 (0,192 г, 0,406 ммоль) обрабатывали 4,0 н. хлоридом водорода в диоксане (1,016 мл, 4,06 ммоль), тетрагидрофуране (10 мл) и воде (2 мл). Реакционную смесь нагревали при 60°C в течение 2 часов. Растворитель удаляли и остаток очищали ВЭЖХ с обращенной фазой (C18, 10-80% CH3CN/вода (0,1% TFA)), получая указанное в заголовке соединение (0,154 г, 0,359 ммоль, выход 88%). 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,05 (с, 1H), 7,82-7,86 (м, 2H), 7,51 (д, J=8,85 Гц, 1H), 7,34 (с, 1H), 7,28 (т, J=2,75 Гц, 1H), 6,14 (т, J=2,29 Гц, 1H), 4,97-4,99 (м, 1H), 3,56 (с, 3H), 3,30 (кв., J=7,32 Гц, 2H), 1,96-2,24 (м, 8H), 1,15 (т, J=7,48 Гц, 3H). MS (ESI+) m/z 429,2 (M+H)+.
Пример 200
4-{2-[(циклопропилметил)амино]-5-(этилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 200a
2-бром-N-(циклопропилметил)-4-(этилсульфонил)анилин
Продукт примера 200a получали согласно процедуре, используемой для получения продукта примера 147a, заменяя циклопропилметанамином циклогексанамин и продуктом примера 168b 2-бром-1-фтор-4-(метилсульфонил)бензол, получая указанное в заголовке соединение.
Пример 200b
4-{2-[(циклопропилметил)амино]-5-(этилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 200b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 200a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,14 (с, 1H), 7,62 (дд, J=8,7, 2,29 Гц, 1H), 7,45 (д, J=2,14 Гц, 1H), 7,30 (т, J=2,75 Гц, 1H), 7,26 (с, 1H), 6,86 (J=8,85 Гц, 1H), 6,00-6,01 (м, 1H), 5,50 (ушир. с, 1H), 3,56 (с, 3H), 3,16 (кв., J=7,12 Гц, 2H), 3,04 (д, J=6,71 Гц, 2H), 1,15 (т, J=7,48 Гц, 3H), 0,97-1,04 (м, 1H), 0,36-0,41 (м, 2H), 0,14-0,18 (м, 2H). MS (ESI+) m/z 386,2 (M+H)+.
Пример 201
6-метил-4-{5-(метилсульфонил)-2-[(тетрагидрофуран-3-илметил)амино]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 201a
2-бром-4-(этилсульфонил)-N-((тетрагидрофуран-3-ил)метил)анилин
Продукт примера 200a получали согласно процедуре, используемой для получения продукта примера 147a, заменяя (тетрагидрофуран-3-ил)метанамином циклогексанамин, и продуктом примера 168b 2-бром-1-фтор-4-(метилсульфонил)бензол, получая указанное в заголовке соединение.
Пример 201b
6-метил-4-{5-(метилсульфонил)-2-[(тетрагидрофуран-3-илметил)амино]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 201b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 201a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,10 (с, 1H), 7,67 (дд, J=8,85, 2,44 Гц, 1H), 7,50 (д, J=2,14 Гц, 1H), 7,28 (т, J=2,9 Гц, 1H), 7,23 (с, 1H), 6,84 (J=8,85 Гц, 1H), 5,95-5,97 (м, 1H), 5,70 (ушир. с, 1H), 3,55-3,70 (м, 7H), 3,38 (дд, J=8,54, 4,88 Гц, 2H), 3,10 (м, 5H), 1,84-1,92 (м, 1H), 1,47-1,55 (м, 1H). MS (ESI+) m/z 402,2 (M+H)+.
Пример 202
4-{5-(этилсульфонил)-2-[(цис-4-гидроксициклогексил)окси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Смесь продукта примера 199 (0,052 г, 0,121 ммоль) и тетрагидробората натрия (6,89 мг, 0,182 ммоль) в тетрагидрофуране (5 мл) нагревали при 60°C в течение 2 часов. Растворитель удаляли и твердое вещество обрабатывали MeOH и парой камель TFA. Полученный раствор очищали препаративной ВЭЖХ (C18, 10-80% CH3CN/вода (0,1% TFA)), получая указанное в заголовке соединение (второй пик элюирования, 0,036 г, 0,084 ммоль, выход 68,9%). 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,06 (с, 1H), 7,78-7,82 (м, 2H), 7,36-7,38 (м, 2H), 7,30 (т, J=2,75 Гц, 1H), 6,14-6,16 (м, 1H), 4,62-4,63 (м, 1H), 3,51-3,58 (м, 5H), 3,25-3,31 (м, 2H), 1,75-1,81 (м, 2H), 1,50-1,64 (м, 4H), 1,32-1,40 (м, 2H), 1,14 (т, J=7,32 Гц, 3H). MS (ESI+) m/z 431,2 (M+H)+.
Пример 203
4-{5-(этилсульфонил)-2-[(транс-4-гидроксициклогексил)окси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Указанное в заголовке соединение (первый пик элюирования) изолировали как меньший продукт во время получения продукта примера 202. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,02 (с, 1H), 7,77-7,81 (м, 2H), 7,40 (д, J=8,54 Гц, 1H), 7,31 (с, 1H), 7,28 (т, J=2,75 Гц, 1H), 6,09-6,11 (м, 1H), 4,53-4,55 (м, 1H), 3,56 (с, 3H), 3,27 (кв., J=7,32 Гц, 2H), 1,95-2,00 (м, 2H), 1,68-1,71 (м, 4H), 1,27-1,38 (м, 4H), 1,13 (т, J=7,32 Гц, 3H). MS (ESI+) m/z 431,2 (M+H)+.
Пример 204
4-[2-(циклопропилметокси)-5-(этилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-d]пиридазин-7-он
Пример 204a
2-бром-1-(циклопропилметокси)-4-(этилсульфонил)бензол
Продукт примера 204a получали согласно процедуре, используемой для получения продукта примера 158, заменяя продуктом примера 168b продукт примера 138a, получая указанное в заголовке соединение.
Пример 204b
2-(2-(циклопропилметокси)-5-(этилсульфонил)фенил)-4,4,5,5-тетраметил-1,3,2-диоксаборолан
Продукт примера 204b получали согласно процедуре, используемой для получения продукта примера 6a, заменяя продуктом примера 204a продукт примера 1e, получая указанное в заголовке соединение.
Пример 204c
4-[2-(циклопропилметокси)-5-(этилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-d]пиридазин-7-он
Продукт примера 204c получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 80b продукт примера 95c и продуктом примера 204b продукт примера 6a, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,67 (с, 1H), 7,92 (дд, J=8,85, 2,44 Гц, 1H), 7,83 (д, J=2,44 Гц, 1H), 7,43 (т, J=2,75 Гц, 1H), 7,40 (д, J=8,85 Гц, 1H), 6,29-6,30 (м, 1H), 4,02 (д, J=7,02 Гц, 2H), 3,80 (с, 3H), 3,29 (кв., J=7,12 Гц, 2H), 1,12 (т, J=7,32 Гц, 3H), 1,01-1,08 (м, 1H), 0,40-0,45 (м, 2H), 0,21-0,25 (м, 2H). MS (ESI+) m/z 388,0 (M+H)+.
Пример 205
6-метил-4-[5-(метилсульфонил)-2-(тетрагидрофуран-3-илокси)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 205 получали согласно процедуре, используемой для получения продукта примера 158, заменяя тетрагидрофуран-3-олом циклопропилметанол, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,03 (с, 1H), 7,85-7,89 (м, 2H), 7,31-7,33 (м, 1H), 7,28 (т, J=2,75 Гц, 1H), 6,11-6,12 (м, 1H), 5,17-5,20 (м, 1H), 3,89-3,91 (м, 2H), 3,63-3,70 (м, 3H), 3,57 (с, 3H), 3,22 (с, 3H), 2,17-2,26 (м, 1H), 1,85-1,91 (м, 1H). MS (ESI+) m/z 389,1 (M+H)+.
Пример 206
4-{2-[(3-фтороксетан-3-ил)метокси]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 206 получали согласно процедуре, используемой для получения продукта примера 158, заменяя (3-фтороксетан-3-ил)метанолом циклопропилметанол, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,06 (с, 1H), 7,90-7,93 (м, 2H), 7,42 (д, J=8,54 Гц, 1H), 7,37 (с, 1H), 7,30 (т, J=2,75 Гц, 1H), 6,16-6,17 (м, 1H), 4,52-4,64 (м, 8H), 3,56 (с, 3H), 3,23 (с, 3H). MS (ESI+) m/z 407,1 (M+H)+.
Пример 207
6-(циклопропилметокси)-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид
Пример 207a
5-бром-6-(циклопропилметокси)пиридин-3-сульфонамид
Продукт примера 207a получали согласно процедуре, используемой для получения продукта примера 29a, заменяя продуктом 86a продукт примера 2a и циклопропилметанолом тетрагидро-2H-пиран-4-ол, получая указанное в заголовке соединение.
Пример 207b
6-(циклопропилметокси)-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид
Пример 207b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 207a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,12 (с, 1H), 8,52 (д, J=2,44 Гц, 1H), 8,12 (д, J=2,44 Гц, 1H), 7,44-7,45 (м, 3H), 7,33 (т, J=2,75 Гц, 1H), 6,22-6,24 (м, 1H), 4,23 (д, J=7,02 Гц, 2H), 3,58 (с, 3H), 1,14-1,24 (м, 1H), 0,47-0,52 (м, 2H), 0,29-0,33 (м, 2H). MS (ESI+) m/z 374,9 (M+H)+.
Пример 208
6-(циклопропилметокси)-N-метил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид
Указанное в заголовке соединение изолировали как меньший продукт во время получения продукта примера 207b. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,12 (с, 1H), 8,49 (с, 1H), 8,05 (д, J=2,44 Гц, 1H), 7,53 (кв., J=4,88 Гц, 1H), 7,46 (с, 1H), 7,33 (т, J=2,75 Гц, 1H), 6,21-6,22 (м, 1H), 4,25 (д, J=7,32 Гц, 2H), 3,58 (с, 3H), 2,47 (д, J=4,88 Гц, 3H), 1,14-1,24 (м, 1H), 0,47-0,52 (м, 2H), 0,29-0,33 (м, 2H). MS (ESI+) m/z 389,2 (M+H)+.
Пример 209
6-[(циклопропилметил)амино]-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид
Пример 209a
5-бром-6-(циклопропилметиламино)пиридин-3-сульфонамид
Продукт примера 209a получали согласно процедуре, используемой для получения продукта примера 96a, заменяя циклопропилметанамином циклогексанамин, получая указанное в заголовке соединение.
Пример 209b
6-[(циклопропилметил)амино]-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид
Продукт примера 209b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 209a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,17 (с, 1H), 8,38 (д, J=2,44 Гц, 1H), 7,69 (д, J=2,44 Гц, 1H), 7,32 (т, J=2,75 Гц, 1H), 7,30 (с, 1H), 7,18 (ушир. с, 2H), 6,62 (с, 1H), 6,05-6,06 (м, 1H), 3,56 (с, 3H), 3,22 (д, J=3,97 Гц, 2H), 1,06-1,10 (м, 1H), 0,34-0,38 (м, 2H), 0,15-0,17 (м, 2H). MS (ESI+) m/z 374,2 (M+H)+.
Пример 210
6-[(циклопропилметил)амино]-N-метил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид
Указанное в заголовке соединение изолировали как меньший продукт во время получения продукта примера 209b. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,17 (с, 1H), 8,35 (д, J=2,44 Гц, 1H), 7,60 (д, J=2,44 Гц, 1H), 7,31-7,32 (м, 2H), 7,21 (д, J=4,58 Гц, 1H), 6,55 (с, 1H), 6,04-6,05 (м, 1H), 3,56 (с, 3H), 3,22 (д, J=5,19 Гц, 2H), 2,43 (д, J=2,75 Гц, 3H), 1,05-1,12 (м, 1H), 0,34-0,39 (м, 2H), 0,15-0,19 (м, 2H). MS (ESI+) m/z 386,7 (M+H)+.
Пример 211
4-{5-(этилсульфонил)-2-[(цис-4-гидрокси-4-метилциклогексил) окси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 199 (0,052 г, 0,121 ммоль) в тетрагидрофуране обрабатывали 3,0 M бромидом метилмагния в тетрагидрофуране (0,485 мл, 0,485 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 2 часов. Растворитель удаляли и твердое вещество обрабатывали MeOH и несколькими каплями TFA. Полученный раствор очищали препаративной ВЭЖХ с обращенной фазой (C18, 10-80% CH3CN/вода (0,1% TFA)), получая указанное в заголовке соединение (первый пик элюирования, 0,018 г, 0,040 ммоль, выход 33,4%). 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,04 (с, 1H), 7,78-7,80 (м, 2H), 7,38 (д, J=9,77 Гц, 1H), 7,33 (с, 1H), 7,29 (т, J=2,75 Гц, 1H), 6,11-6,12 (м, 1H), 4,46-4,49 (м, 1H), 3,57 (с, 3H), 3,27 (кв., J=7,32 Гц, 2H), 1,39-1,76 (м, 8H), 1,13 (т, J=7,32 Гц, 3H), 1,10 (с, 3H). MS (ESI+) m/z 445,1 (M+H)+.
Пример 212
4-{5-(этилсульфонил)-2-[(транс-4-гидрокси-4-метилциклогексил)окси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Указанное в заголовке соединение (второй пик элюирования) изолировали как меньший продукт при получении продукта примера 211. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,04 (с, 1H), 7,79-7,81 (м, 2H), 7,37 (д, J=9,46 Гц, 1H), 7,30 (с, 1H), 7,29 (т, J=2,75 Гц, 1H), 6,10-6,11 (м, 1H), 4,46-4,49 (м, 1H), 3,56 (с, 3H), 3,28 (кв., J=7,32 Гц, 2H), 1,80-1,86 (м, 2H), 1,54-1,59 (м, 2H), 1,23-1,26 (м, 4H), 1,13 (т, J=7,32 Гц, 3H), 0,91 (с, 3H). MS (ESI+) m/z 445,1 (M+H)+.
Пример 213
4-[2-(циклобутилокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
В склянку емкостью 4 мл загружали мешалку, раствор продукта примера 138a (30 мг, 0,063 ммоль) в тетрагидрофуране (1 мл), раствор циклобутанола (32 мг, 7 эквивалентов, 0,46 ммоль) в тетрагидрофуране (1 мл) и неразбавленный гидрид натрия (19 мг, 7 эквивалентов, 0,46 ммоль). Реакционную смесь перемешивали при 60°C в течение 16 часов. Сырой материал фильтровали, концентрировали и очищали ВЭЖХ с обращенной фазой (C18, 10-100% CH3CN/вода (0,1% TFA)), получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,98-7,75 (м, 2H), 7,33 (д, J=1,4 Гц, 2H), 7,16 (д, J=8,7 Гц, 1H), 6,15 (д, J=2,8 Гц, 1H), 4,82 (p, J=7,2 Гц, 1H), 3,59 (с, 3H), 3,19 (д, J=8,5 Гц, 3H), 2,47-2,38 (м, 2H), 1,96 (p, J=9,6 Гц, 2H), 1,81-1,72 (м, 1H), 1,72-1,57 (м, 1H). MS (ESI+) m/z 373 (M+H)+.
Пример 214
4-[2-(циклопентилметокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 214 получали согласно процедуре, используемой для получения продукта примера 213, заменяя циклопентилметанолом циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,93-7,81 (м, 2H), 7,40-7,29 (м, 3H), 6,14 (д, J=2,8 Гц, 1H), 3,99 (д, J=6,6 Гц, 2H), 3,58 (с, 3H), 3,20 (с, 3H), 2,18 (дт, J=14,6, 7,2 Гц, 1H), 1,59 (дт, J=17,2, 8,5 Гц, 2H), 1,44 (дд, J=10,1, 4,8 Гц, 4H), 1,31-1,16 (м, 2H). MS (ESI+) m/z 401 (M+H)+.
Пример 215
4-[2-(циклогексилокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 215 получали согласно процедуре, используемой для получения продукта примера 213, заменяя циклогексанолом циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,85 (дт, J=4,1, 2,4 Гц, 2H), 7,35 (дд, J=17,3, 5,9 Гц, 3H), 6,16 (д, J=2,8 Гц, 1H), 4,66-4,49 (м, 1H), 3,58 (с, 3H), 3,20 (с, 3H), 1,94-1,79 (м, 2H), 1,54 (д, J=5,1 Гц, 2H), 1,50-1,28 (м, 5H), 1,21 (д, J=8,9 Гц, 1H). MS (ESI+) m/z 401 (M+H)+.
Пример 216
4-[2-(циклопентилокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 216 получали согласно процедуре, используемой для получения продукта примера 213, заменяя циклопентанолом циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,88 (дд, J=8,7, 2,5 Гц, 1H), 7,82 (д, J=2,4 Гц, 1H), 7,32 (дд, J=10,3, 7,4 Гц, 3H), 6,10 (д, J=2,8 Гц, 1H), 4,96 (дт, J=8,3, 2,8 Гц, 1H), 3,58 (с, 3H), 3,19 (д, J=8,6 Гц, 3H), 2,53 (дд, J=3,5, 1,7 Гц, 2H), 1,98-1,82 (м, 2H), 1,69-1,56 (м, 2H), 1,56-1,46 (м, 4H) MS (ESI+) m/z 387 (M+H)+.
Пример 217
6-метил-4-[5-(метилсульфонил)-2-(тетрагидрофуран-3-илметокси)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 217 получали согласно процедуре, используемой для получения продукта примера 213, заменяя (тетрагидрофуран-3-ил)метанолом циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,90 (дд, J=8,6, 2,5 Гц, 1H), 7,85 (д, J=2,4 Гц, 1H), 7,37 (д, J=8,7 Гц, 1H), 7,33 (д, J=2,8 Гц, 2H), 6,14 (д, J=2,8 Гц, 1H), 4,10 (дд, J=9,4, 6,2 Гц, 1H), 4,03 (дд, J=9,4, 7,5 Гц, 1H), 3,58 (с, 5H), 3,62-3,52 (м, 6H), 3,40 (дд, J=8,6, 5,8 Гц, 1H), 3,20 (с, 3H), 1,93-1,80 (м, 1H), 1,63-1,51 (м, 1H). MS (ESI+) m/z 403 (M+H)+.
Пример 218
6-метил-4-{5-(метилсульфонил)-2-[2-(2-оксоимидазолидин-1-ил)этокси]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 218 получали согласно процедуре, используемой для получения продукта примера 213, заменяя 1-(2-гидроксиэтил)имидазолидин-2-оном циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,90 (дд, J=8,6, 2,4 Гц, 1H), 7,86 (д, J=2,4 Гц, 1H), 7,39 (д, J=8,7 Гц, 1H), 7,34 (д, J=2,8 Гц, 2H), 6,15 (д, J=2,8 Гц, 1H), 4,20 (т, J=5,2 Гц, 2H), 3,58 (с, 3H), 3,35 (т, J=5,2 Гц, 2H), 3,21 (с, 3H), 3,07 (с, 4H). MS (ESI+) m/z 431 (M+H)+.
Пример 219
4-[2-(2-циклопропилэтокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 219 получали согласно процедуре, используемой для получения продукта примера 213, заменяя 2-циклопропилэтанолом циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,93 (дд, J=8,6, 2,4 Гц, 1H), 7,86 (д, J=2,4 Гц, 1H), 7,43-7,32 (м, 3H), 6,14 (д, J=2,8 Гц, 1H), 4,18 (т, J=6,3 Гц, 2H), 3,23 (с, 3H), 1,54 (кв., J=6,5 Гц, 2H), 0,72-0,60 (м, 1H), 0,39-0,29 (м, 2H) MS (ESI+) m/z 387 (M+H)+.
Пример 220
4-[2-(циклогептилокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 220 получали согласно процедуре, используемой для получения продукта примера 213, заменяя циклогептанолом циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,91-7,80 (м, 2H), 7,32 (д, J=2,8 Гц, 2H), 7,34-7,27 (м, 3H), 6,14 (д, J=2,8 Гц, 1H), 4,77-4,67 (м, 1H), 3,20 (с, 3H), 1,98-1,84 (м, 2H), 1,69-1,57 (м, 2H), 1,57-1,30 (м, 8H). MS (ESI+) m/z 415 (M+H)+.
Пример 221
6-метил-4-[2-(2-метилпропокси)-5-(метилсульфонил)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 221 получали согласно процедуре, используемой для получения продукта примера 213, заменяя 2-метилпропан-1-олом циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,92-7,82 (м, 2H), 7,38-7,32 (м, 3H), 7,32 (д, J=2,8 Гц, 2H), 6,13 (д, J=2,8 Гц, 1H), 3,88 (д, J=6,3 Гц, 2H), 3,20 (с, 3H), 0,83 (д, J=6,7 Гц, 6H). MS (ESI+) m/z 375 (M+H)+.
Пример 222
6-метил-4-[2-{[(2S)-1-метилпирролидин-2-ил]метокси}-5-(метилсульфонил)фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 222 получали согласно процедуре, используемой для получения продукта примера 213, заменяя (S)-(1-метилпирролидин-2-ил)метанолом циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,96 (дд, J=8,6, 2,4 Гц, 1H), 7,89 (д, J=2,4 Гц, 1H), 7,43-7,33 (м, 3H), 6,20 (д, J=2,8 Гц, 1H), 4,49 (дд, J=11,0, 3,3 Гц, 1H), 4,27 (дд, J=10,9, 8,2 Гц, 1H), 3,59 (с, 3H), 3,44-3,34 (м, 1H), 3,25-3,16 (м, 3H), 3,07-2,95 (м, 1H), 2,32-2,09 (м, 1H), 2,01-1,83 (м, 1H), 1,85-1,62 (м, 2H). MS (ESI+) m/z 416 (M+H)+.
Пример 223
6-метил-4-{2-[(2-метилциклопропил)метокси]-5-(метилсульфонил)фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 223 получали согласно процедуре, используемой для получения продукта примера 213, заменяя (2-метилциклопропил)метанолом циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,94-7,79 (м, 2H), 7,41-7,28 (м, 3H), 6,16 (т, J=3,0 Гц, 1H), 4,10-3,97 (м, 1H), 3,91 (дд, J=10,3, 7,3 Гц, 1H), 3,59 (д, J=2,7 Гц, 3H), 3,19 (с, 3H), 0,91 (т, J=11,4 Гц, 3H), 0,89-0,75 (м, 1H), 0,77-0,63 (м, 1H), 0,48-0,36 (м, 1H), 0,29-0,19 (м, 1H). MS (ESI+) m/z 387 (M+H)+.
Пример 224
4-[2-(циклогексилметокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 224 получали согласно процедуре, используемой для получения продукта примера 213, заменяя циклогексилметанолом циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,91-7,82 (м, 2H), 7,38-7,30 (м, 3H), 6,14 (д, J=2,8 Гц, 1H), 3,91 (д, J=5,7 Гц, 2H), 3,58 (с, 3H), 3,20 (с, 3H), 1,65-1,57 (м, 5H), 1,28-0,85 (м, 5H). MS (ESI+) m/z 415 (M+H)+.
Пример 225
6-метил-4-{2-[2-(1-метилпирролидин-2-ил)этокси]-5-(метилсульфонил)фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 225 получали согласно процедуре, используемой для получения продукта примера 213, заменяя 2-(1-метилпирролидин-2-ил)этанолом циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,93 (дд, J=8,7, 2,4 Гц, 1H), 7,85 (д, J=2,4 Гц, 1H), 7,36 (дд, J=10,4, 7,7 Гц, 3H), 6,15 (д, J=2,8 Гц, 1H), 4,30-4,12 (м, 2H), 3,59 (с, 3H), 3,57-3,42 (м, 1H), 3,19 (д, J=14,3 Гц, 3H), 3,04 (дт, J=9,9, 5,0 Гц, 1H), 2,93 (дт, J=11,5, 8,5 Гц, 1H), 2,53 (дт, J=3,5, 1,7 Гц, 2H), 2,34-2,19 (м, 1H), 2,06 (дтд, J=12,9, 8,1, 5,0 Гц, 1H), 1,96-1,72 (м, 3H), 1,51 (ддд, J=16,7, 13,2, 9,3 Гц, 1H). MS (ESI+) m/z 430 (M+H)+.
Пример 226
6-метил-4-[5-(метилсульфонил)-2-{[(2R)-5-оксопирролидин-2-ил]метокси}фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 226 получали согласно процедуре, используемой для получения продукта примера 213, заменяя (R)-5-(гидроксиметил)пирролидин-2-оном циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,91 (дд, J=8,7, 2,4 Гц, 1H), 7,86 (д, J=2,4 Гц, 1H), 7,42-7,29 (м, 3H), 6,15 (д, J=2,8 Гц, 1H), 4,08 (кв.д, J=9,9, 4,2 Гц, 2H), 3,81 (дт, J=28,2, 14,1 Гц, 1H), 3,58 (с, 3H), 3,19 (д, J=11,5 Гц, 3H), 2,09-1,87 (м, 2H), 1,86-1,66 (м, 2H). MS (ESI+) m/z 416 (M+H)+.
Пример 227
6-метил-4-{5-(метилсульфонил)-2-[2-(морфолин-4-ил)этокси]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 227 получали согласно процедуре, используемой для получения продукта примера 213, заменяя 2-морфолинoэтанолом циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,97 (дд, J=8,6, 2,4 Гц, 1H), 7,87 (д, J=2,4 Гц, 1H), 7,42 (д, J=8,7 Гц, 1H), 7,35 (д, J=2,8 Гц, 2H), 6,12 (д, J=2,8 Гц, 1H), 4,48 (т, J=4,6 Гц, 2H), 3,96 (с, 1H), 3,59 (с, 3H), 3,57-3,36 (м, 3H), 3,22 (с, 3H), 3,18 (с, 1H), 3,10-2,68 (м, 2H). MS (ESI+) m/z 432 (M+H)+.
Пример 228
6-метил-4-[5-(метилсульфонил)-2-{[(2S)-5-оксопирролидин-2-ил]метокси}фенил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 228 получали согласно процедуре, используемой для получения продукта примера 213, заменяя (S)-5-(гидроксиметил)пирролидин-2-оном циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,88 (тт, J=15,3, 7,7 Гц, 2H), 7,46-7,27 (м, 3H), 6,15 (д, J=2,8 Гц, 1H), 4,08 (кв.д, J=9,9, 4,2 Гц, 2H), 3,83 (дд, J=8,1, 4,1 Гц, 1H), 3,57 (д, J=9,0 Гц, 3H), 3,20 (с, 3H), 2,09-1,90 (м, 2H), 1,85-1,69 (м, 2H) MS (ESI+) m/z 416 (M+H)+.
Пример 229
4-{2-[(1-трет-бутоксипропан-2-ил)окси]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 229 получали согласно процедуре, используемой для получения продукта примера 213, заменяя 1-трет-бутоксипропан-2-олом циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,92-7,80 (м, 2H), 7,45-7,24 (м, 3H), 6,19 (д, J=2,8 Гц, 1H), 4,74-4,62 (м, 1H), 3,58 (с, 3H), 3,38 (т, J=7,6 Гц, 2H), 3,19 (д, J=8,9 Гц, 3H), 1,20 (т, J=8,9 Гц, 3H), 1,02 (с, 9H). MS (ESI+) m/z 433 (M+H)+.
Пример 230
4-{2-[(1S,4R)-бицикло[2.2.1]гепт-2-илметокси]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 230 получали согласно процедуре, используемой для получения продукта примера 213, заменяя (1S,4R)-бицикло[2,2,1]гептан-2-илметанолом циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,92-7,81 (м, 2H), 7,43-7,28 (м, 3H), 6,14 (дд, J=8,3, 2,8 Гц, 1H), 4,15-4,07 (м, 1H), 4,01-3,78 (м, 2H), 3,20 (с, 3H), 2,18-2,00 (м, 2H), 1,50-1,34 (м, 2H), 1,32-1,15 (м, 3H), 1,14-0,95 (м, 2H). MS (ESI+) m/z 427 (M+H)+.
Пример 231
6-метил-4-(2-[(1-метилциклопропил)метокси]-5-(метилсульфонил)фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 231 получали согласно процедуре, используемой для получения продукта примера 213, заменяя (1-метилциклопропилметанолом циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,90-7,83 (м, 2H), 7,33 (д, J=2,9 Гц, 1H), 7,30 (д, J=8,9 Гц, 1H), 6,17 (д, J=2,8 Гц, 1H), 3,90 (с, 2H), 3,19 (с, 3H), 0,97 (с, 3H), 0,48-0,41 (м, 2H), 0,31-0,25 (м, 2H). MS (ESI+) m/z 387 (M+H)+.
Пример 232
6-метил-4-{5-(метилсульфонил)-2-[2-(2-оксопирролидин-1-ил)этокси]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 232 получали согласно процедуре, используемой для получения продукта примера 213, заменяя 1-(2-гидроксиэтил)пирролидин-2-оном циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,91 (дд, J=8,6, 2,4 Гц, 1H), 7,84 (д, J=2,4 Гц, 1H), 7,41-7,30 (м, 3H), 6,10 (д, J=2,8 Гц, 1H), 4,21 (т, J=5,2 Гц, 2H), 3,58 (с, 3H), 3,45 (т, J=5,2 Гц, 2H), 3,23-3,16 (м, 3H), 3,01 (т, J=7,0 Гц, 2H), 2,08 (т, J=8,0 Гц, 2H), 1,67 (p, J=7,5 Гц, 2H). MS (ESI+) m/z 430 (M+H)+.
Пример 233
6-метил-4-{2-[(4-метилциклогексил)окси]-5-(метилсульфонил)фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 233 получали согласно процедуре, используемой для получения продукта примера 213, заменяя 4-метилциклогексанолом циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,89-7,83 (м, 2H), 7,39-7,31 (м, 3H), 6,17 (д, J=2,8 Гц, 1H), 4,78-4,71 (м, 1H), 3,20 (с, 3H), 1,86-1,75 (м, 2H), 1,57-1,45 (м, 2H), 1,41-1,22 (м, 3H), 0,96-0,82 (м, 2H), 0,68 (д, J=6,2 Гц, 3H). MS (ESI+) m/z 415 (M+H)+.
Пример 234
4-[2-(циклобутилметокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 234 получали согласно процедуре, используемой для получения продукта примера 213, заменяя циклобутилметанолом циклобутанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,94-7,80 (м, 2H), 7,34 (дд, J=13,2, 5,7 Гц, 3H), 6,14 (д, J=2,8 Гц, 1H), 4,07 (д, J=6,2 Гц, 2H), 3,57 (с, 3H), 3,19 (д, J=9,2 Гц, 3H), 2,61 (д, J=7,1 Гц, 1H), 1,99-1,62 (м, 6H). MS (ESI+) m/z 387 (M+H)+.
Пример 235
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]циклопропансульфонамид
Продукт примера 235 получали согласно процедуре, используемой для получения продукта примера 4 (способ A), заменяя продуктом примера 27c продукт примера 3 и циклопропансульфонил хлоридом метансульфонил хлорид, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,05 (с, 1H), 9,70 (с, 1H), 7,35-7,38 (м, 2H), 7,29-7,30 (м, 2H), 7,22 (дд, J=8,7, 2,59 Гц, 1H), 7,06-7,10 (м, 1H), 6,98-7,01 (м, 1H), 6,92 (д, J=8,54 Гц, 1H), 6,25-6,26 (м, 1H), 3,54 (с, 3H), 2,61-2,66 (м, 1H), 0,90-0,98 (м, 4H). MS (ESI+) m/z 472,1 (M+H)+.
Пример 236
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-2-метоксиэтансульфонамид
Продукт примера 236 получали согласно процедуре, используемой для получения продукта примера 4, способ A, заменяя продуктом примера 27b продукт примера 3 и 2-метоксиэтансульфонил хлоридом метансульфонил хлорид, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,05 (с, 1H), 9,76 (с, 1H), 7,34-7,39 (м, 2H), 7,28-7,30 (м, 2H), 7,19 (дд, J=8,85, 2,75 Гц, 1H), 7,05-7,10 (м, 1H), 6,98-7,01 (м, 1H), 6,91 (д, J=8,54 Гц, 1H), 6,25-6,26 (м, 1H), 3,68 (т, J=6,1 Гц, 2H), 3,53 (с, 3H), 3,37 (т, J=6,1 Гц, 2H), 3,20 (с, 3H). MS (ESI+) m/z 490,1 (M+H)+.
Пример 237
6-метил-4-{5-(метилсульфонил)-2-[трицикло[3.3.1.13,7]дец-2-илокси]фенил}-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 237 получали согласно процедуре, используемой для получения продукта примера 158, заменяя 2-адамантолом циклопропилметанол, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,04 (с, 1H), 7,88 (д, J=2,44 Гц, 1H), 7,83 (дд, J=8,85,2,44, ГЦ, 1H), 7,38 (с, 1H), 7,36 (д, J=8,85 Гц, 1H), 7,29 (т, J=2,75 Гц, 1H), 6,18-6,19 (м, 1H), 4,70 (с, 1H), 3,56 (с, 3H), 3,21 (с, 3H), 2,06 (с, 2H), 1,80 (с, 5H), 1,62-1,65 (м, 5H), 1,34 (д, J=11,29 Гц, 2H). MS (ESI+) m/z 453,2 (M+H)+.
Пример 238
4-[(циклопропилметил)амино]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид
Пример 238a
3-бром-4-(циклопропилметиламино)бензолсульфонамид
Продукт примера 238a получали согласно процедуре, используемой для получения продукта примера 96a, заменяя циклопропилметанамином циклогексанамин и 3-бром-4-фторбензолсульфонамидом продукт примера 86a, соответственно, получая указанное в заголовке соединение.
Пример 238b
4-[(циклопропилметил)амино]-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид
Продукт примера 238b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 238a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,13 (с, 1H), 7,61-7,63 (м, 1H), 7,50 (д, J=2,14 Гц, 1H), 7,30 (т, J=2,75 Гц, 1H), 7,20 (с, 1H), 6,97 (ушир. с, 2H), 6,80 (д, J=8,85 Гц, 1H), 6,01 (с, 1H), 3,56 (с, 3H), 3,02 (д, J=6,71 Гц, 2H), 0,97-1,03 (м, 1H), 0,35-0,39 (м, 2H), 0,13-0,16 (м, 2H). MS (ESI+) m/z 373,2 (M+H)+.
Пример 239
4-[(циклопропилметил)амино]-N-метил-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид
Указанное в заголовке соединение изолировали как меньший продукт при получении продукта примера 238b. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,13 (с, 1H), 7,56 (дд, J=8,54, 2,44 Гц, 1H), 7,42 (д, J=2,14 Гц, 1H), 7,23 (с, 1H), 7,30 (т, J=2,75 Гц, 1H), 7,02 (д, J=4,88 Гц, 1H), 6,83 (д, J=8,54 Гц, 1H), 6,00-6,01 (м, 1H), 3,56 (с, 3H), 3,02 (д, J=6,71 Гц, 2H), 2,38 (д, J=4,58 Гц, 3H), 0,99-1,18 (м, 1H), 0,36-0,40 (м, 2H), 0,13-0,17 (м, 2H). MS (ESI+) m/z 387,2 (M+H)+.
Пример 240
4-{2-[(2,2-дифторциклопропил)метокси]-5-(этилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 240a
2-бром-1-((2,2-дифторциклопропил)метокси)-4-(этилсульфонил)бензол
Продукт примера 240a получали согласно процедуре, используемой для получения продукта примера 158, заменяя продуктом примера 168b продукт примера 138a и (2,2-дифторциклопропил)метанолом циклопропилметанол, получая указанное в заголовке соединение.
Пример 240b
4-{2-[(2,2-дифторциклопропил)метокси]-5-(этилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 240b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 240a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,05 (с, 1H), 7,81-7,85 (м, 2H), 7,37-7,39 (м, 2H), 7,29 (т, J=2,75 Гц, 1H), 6,14-6,15 (м, 1H), 4,25-4,29 (м, 2H), 4,16-4,20 (м, 2H), 3,57 (с, 3H), 3,29 (кв., J=7,43 Гц, 2H), 2,08-2,16 (м, 1H), 1,63-1,66 (м, 1H), 1,44-1,46 (м, 1H), 1,13 (т, J=7,32 Гц, 3H). MS (ESI+) m/z 423,1 (M+H)+.
Пример 241
4-(4-бром-2-метоксифенил)-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 241a
4-(4-бром-2-метоксифенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 6a (0,2 г, 0,467 ммоль), 4-бром-1-йод-2-метоксибензол (0,16 г, 0,514 ммоль), трис (дибензилиденацетон)дипалладий(0) (0,013 г, 0,014 ммоль), 1,3,5,7-тетраметил-6-фенил-2,4,8-триокса-6-фосфаадамант (0,014 г, 0,047 ммоль) и трехосновный фосфат калия (0,347 г, 1,634 ммоль) объединяли и продували аргоном в течение 15 минут. Тем временем раствор 4:1 диоксан/вода (7,5 мл) продували азотом в течение 15 минут и переносили шприцем в реакционный сосуд в атмосфере аргона. Смесь перемешивали при температуре окружающей среды в течение 20 минут и распределяли между этилацетатом и водой. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили (Na2SО4), обрабатывали силикагелем, функционализованным 3-меркаптопропилом, в течение двадцати минут, фильтровали и концентрировали. Очистка хроматографией (силикагель, 10-80% этилацетат в гептанах) давала указанное в заголовке соединение (0,2 г, 88%).
Пример 241b
4-(4-бром-2-метоксифенил)-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 241a (0,2 г, 0,410 ммоль), гидроксид калия (0,460 г, 8,21 ммоль) и бромид цетилтриметиламмония (7,48 мг, 0,021 ммоль) объединяли в диоксане (8 мл) и воде (4 мл) и нагревали при 100°C в течение 18 часов. Реакционную смесь распределяли между равными объемами этилацетата и воды и pH доводили до pH 7 осторожным добавлением концентрированной HCl. Органический слой отделяли и промывали три раза насыщенным водным раствором хлорида натрия, сушили (Na2SО4), фильтровали и концентрировали. Очистка растиранием в порошок в дихлорметане давала указанное в заголовке соединение (0,1 г, 73%). 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 11,97 (с, 1H) 7,05-7,42 (м, 5H) 5,87-6,09 (м, 1H) 3,75 (с, 3H) 3,54 (с, 3H). MS (ESI+) m/z 333/335 (M +H)+.
Пример 242
6-(2,4-дифторфенокси)-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид
Пример 242a
5-бром-6-(2,4-дифторфенокси)пиридин-3-сульфонамид
Смесь продукта примера 86a (0,543 г, 2 ммоль), 2,4-дифторфенола (0,390 г, 3,00 ммоль) и карбоната цезия (1,955 г, 6,00 ммоль) в DMSO (10 мл) нагревали при 110°C в течение 16 часов. После охлаждения реакционную смесь распределяли между водой и этилацетатом. Водный слой нейтрализовали 10% HCl и экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (3:2 этилацетат/гексаны) на силикагеле, получая указанное в заголовке соединение (0,53 г, 1,451 ммоль, выход 72,6%).
Пример 242b
6-(2,4-дифторфенокси)-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид
Продукт примера 242b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 242a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,19 (с, 1H), 8,46 (д, J=2,44 Гц, 1H), 8,29 (д, J=2,14 Гц, 1H), 7,56 (с, 2H), 7,54 (с, 1H), 7,44-7,50 (м, 2H), 7,35 (т, J=2,75 Гц, 1H), 7,14-7,18 (м, 1H), 6,34 (т, J=2,44 Гц, 1H), 3,61 (с, 3H). MS (ESI+) m/z 433,2 (M+H)+.
Пример 243
4-{2-(циклопропилметокси)-5-[(трифторметил)сульфонил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 243a
(3-бром-4-фторфенил)(трифторметил)сульфан
3-Бром-4-фторбензолтиол (2,071 г, 10 ммоль) в диметилформамиде (10 мл) обрабатывали 60% гидридом натрия (0,480 г, 12,00 ммоль). Раствор перемешивали в течение 10 минут при комнатной температуре. Трифторйодметан (2,74 г, 14,00 ммоль) выпускали в баллон с трехходовым запорным краном. Баллон затем помещали на колбу и трифторйодметан выпускали в реакционную среду. Через 1 час все содержимое баллона было выпущено. И баллон заполнили 2,74 г трифторйодметана снова. Реакционную смесь перемешивали в течение 16 часов. Реакционную смесь выливали в воду и экстрагировали этилацетатом несколько раз. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Полученное масло использовали непосредственно в следующей реакции.
Пример 243b
2-бром-1-фтор-4-(трифторметилсульфонил)бензол
Продукт примера 243a (2,75 г, 10,00 ммоль) в ацетoнитриле (4 мл), тетрахлориде углерода (4,00 мл) и воде (16,00 мл) обрабатывали периодатом натрия (6,42 г, 30,0 ммоль) и гидратом хлорида рутения(III) (0,023 г, 0,100 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 16 часов. Дихлорметан (100 мл) добавляли к реакционной смеси, которую затем фильтровали через прокладку фильтрующего агента. Фильтрат обрабатывали насыщенным раствором бикарбоната натрия (50 мл). И органический слой отделяли. Водный слой затем экстрагировали дополнительным дихлорметаном три раза. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали колоночной хроматографией на силикагеле, элюируя 5% этилацетатом в гексанах, получая 2,14 г указанного в заголовке соединения (7,85 ммоль, выход 79%).
Пример 243c
2-бром-1-(циклопропилметокси)-4-(трифторметилсульфонил)бензол
Продукт примера 243c получали согласно процедуре, используемой для получения продукта примера 158, заменяя продуктом примера 243b продукт примера 138a, получая указанное в заголовке соединение.
Пример 243d
4-{2-(циклопропилметокси)-5-[(трифторметил)сульфонил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 243d получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 243c продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,10 (с, 1H), 8,08 (дд, J=8,85, 2,44 Гц, 1H), 7,95 (д, J=2,44 Гц, 1H), 7,50 (д, J=8,85 Гц, 1H), 7,44 (с, 1H), 7,35 (т, J=2,75 Гц, 1H), 6,12-6,13 (м, 1H), 4,09 (д, J=7,02 Гц, 2H), 3,58 (с, 3H), 1,11-1,17 (м, 1H), 0,48-0,50 (м, 2H), 0,29-0,33 (м, 2H). MS (ESI+) m/z 427,0 (M+H)+.
Пример 244
4-{2-[(циклопропилметил)амино]-5-[(трифторметил)сульфонил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 244a
Продукт примера 244a получали согласно процедуре, используемой для получения продукта примера 96a, заменяя циклопропилметанамином циклогексанамин и продуктом примера 243b продукт примера 86a, соответственно, получая указанное в заголовке соединение.
Пример 244b
4-{2-[(циклопропилметил)амино]-5-[(трифторметил)сульфонил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 244b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 244a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,16 (с, 1H), 7,80 (дд, J=8,85, 2,44 Гц, 1H), 7,53 (д, J=2,44 Гц, 1H), 7,29-7,31 (м, 2H), 7,02 (д, J=9,16 Гц, 1H), 6,41 (т, J=5,8 Гц, 1H), 5,96-5,97 (м, 1H), 3,56 (с, 3H), 3,10 (т, J=6,26 Гц, 2H), 1,01-1,06 (м, 1H), 0,39-0,43 (м, 2H), 0,16-0,20 (м, 2H). MS (ESI+) m/z 426,1 (M+H)+.
Пример 245
6-[(циклопропилметил)амино]-N,N-диметил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид
Пример 245a
5-бром-6-(циклопропилметиламино)-N,N-диметилпиридин-3-сульфонамид
Продукт примера 245a получали согласно процедуре, используемой для получения продукта примера 96a, заменяя циклопропилметанамином циклогексанамин и продуктом примера 110a продукт примера 86a, соответственно, получая указанное в заголовке соединение.
Пример 245b
6-[(циклопропилметил)амино]-N,N-диметил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид
Продукт примера 245b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 245a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,16 (с, 1H), 8,35 (д, J=2,44 Гц, 1H), 7,51 (д, J=2,44 Гц, 1H), 7,20-7,32 (м, 2H), 6,69 (т, J=5,34 Гц, 1H), 6,03-6,04 (м, 1H), 3,58 (с, 3H), 3,24 (т, J=5,95 Гц, 2H), 2,62 (с, 6H), 1,05-1,12 (м, 1H), 0,34-0,39 (м, 2H), 0,15-0,19 (м, 2H). MS (ESI+) m/z 402,1 (M+H)+.
Пример 246
6-(2,4-дифторфенокси)-N-метил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид
Указанное в заголовке соединение изолировали как меньший продукт при получении продукта примера 242b. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,19 (с, 1H), 8,45 (д, J=2,44 Гц, 1H), 8,22 (д, J=2,44 Гц, 1H), 7,60 (кв., J=4,78 Гц, 1H), 7,57 (с, 1H), 7,46-7,52 (м, 3H), 7,36 (т, J=2,75 Гц, 1H), 7,14-7,19 (м, 1H), 6,34-6,35 (м, 1H), 3,61 (с, 3H), 2,50 (д, J=4,88 Гц, 3H). MS (ESI+) m/z 477,1 (M+H)+.
Пример 247
4-[2-(циклопропилметокси)-6-метилфенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 247a
2-бром-1-(циклопропилметокси)-3-метилбензол
В 250 мл колбу с мешалкой загружали 2-бром-3-метилфенол (2,86 г, 15,3 ммоль), (бромметил)циклопропан (1,80 мл, 18,6 ммоль) и карбонат цезия (7,46 г, 22,9 ммоль) в диметилформамиде (50 мл). Смесь перемешивали в течение 16 часов при температуре окружающей среды и затем нагревали при 50°C в течение 3 часов. Смесь охлаждали до температуры окружающей среды и распределяли между этилацетатом (200 мл) и насыщенным водным раствором хлорида натрия (200 мл). Объединенные органические вещества промывали дважды насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали, получая указанное в заголовке соединение (3,7 г, 100%).
Пример 247b
4-(2-(циклопропилметокси)-6-метилфенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 247b получали согласно процедуре, используемой для получения продукта примера 7d, заменяя продуктом примера 247a продукт примера 7c и перемешивая при 65°C в течение 2,5 часов, получая указанное в заголовке соединение.
Пример 247c
4-(2-(циклопропилметокси)-6-метилфенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 247c получали согласно процедуре, используемой для получения продукта примера 4b, заменяя продуктом примера 247b продукт примера 4a, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 11,91 (ушир.дс, 1H), 7,23-7,18 (м, 2H), 6,99 (с, 1H), 6,91 (д, J=3,1 Гц, 1H), 6,89 (м, 1H), 5,79 (м, 1H), 3,74 (дд, J=6,6, 2,3 Гц, 2H), 3,54 (с, 3H), 2,06 (с, 3H) 0,99 (м, 1H), 0,33 (м, 2H), 0,08 (м, 2H), MS (DCI+) m/z 309,1 (M+H)+.
Пример 248
4-{5-(этилсульфонил)-2-[(цис-4-метоксициклогексил)окси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 248a
2-бром-4-(этилсульфонил)-1-(4-метоксициклогексилокси)бензол
4-Метоксициклогексанол (смесь 70% цис и 30% транс изомеров) (0,521 г, 4,00 ммоль) в диоксане (20 мл) обрабатывали гидридом натрия (0,240 г, 6,00 ммоль). Реакционную смесь перемешивали в течение 10 минут. К этому раствору добавляли продукт примера 168b (0,534 г, 2 ммоль). Реакционную смесь нагревали при 60°C в течение 16 часов. После охлаждения реакционную смесь распределяли между водой и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом два или более раз. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 70:30 этилацетат/гексаны), получая указанное в заголовке соединение (0,29 г, выход 38,4%).
Пример 248b
4-{5-(этилсульфонил)-2-[(цис-4-метоксициклогексил)окси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 248b (второй пик элюирования) получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 248a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,05 (с, 1H), 7,78-7,80 (м, 2H), 7,38-7,40 (м, 1H), 7,34 (с, 1H), 7,29 (т, J=2,75 Гц, 1H), 6,12-6,13 (м, 1H), 4,63-4,66 (м, 1H), 3,56 (с, 3H), 3,28 (т, J=7,32 Гц, 2H), 3,19-3,23 (м, 1H), 3,15 (с, 3H), 1,65-1,72 (м, 6H), 1,42-1,48 (м, 2H), 1,13 (т, J=7,32, 3H). MS (ESI+) m/z 445,0 (M+H)+.
Пример 249
4-(циклопропилметокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид
Пример 249a
3-бром-4-(циклопропилметокси)бензолсульфонамид
Продукт примера 249a получали согласно процедуре, используемой для получения продукта примера 29a, заменяя 3-бром-4-фторбензолсульфонамидом продукт примера 2a и циклопропилметанолом тетрагидро-2H-пиран-4-ол, получая указанное в заголовке соединение.
Пример 249b
4-(циклопропилметокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид
Продукт примера 249b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 249a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,03 (с, 1H), 7,80 (д, J=2,44 Гц, 1H), 7,76 (дд, J=8,54, 2,44 Гц, 1H), 7,31 (с, 1H), 7,30 (т, J=2,9 Гц, 1H), 7,22-7,25 (м, 3H), 6,15-6,16 (м, 1H), 3,93 (д, J=6,71 Гц, 2H), 3,57 (с, 3H), 1,08-1,13 (м, 1H), 0,44-0,49 (м, 2H), 0,25-0,28 (м, 2H). MS (ESI+) m/z 374,1 (M+H)+.
Пример 250
4-(циклопропилметокси)-N-метил-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид
Указанное в заголовке соединение изолировали как меньший продукт при получении продукта примера 249b. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,05 (с, 1H), 7,70-7,74 (м, 2H), 7,35 (с, 1H), 7,30 (т, J=2,9 Гц, 1H), 7,26-7,32 (м, 3H), 6,14 (т, J=2,44 Гц, 1H), 3,95 (д, J=6,71 Гц, 2H), 3,58 (с, 3H), 2,41 (д, J=4,88 Гц, 3H), 1,07-1,15 (м, 1H), 0,45-0,50 (м, 2H), 0,26-0,29 (м, 2H). MS (ESI+) m/z 388,1 (M+H)+.
Пример 251
N-[4-(циклопропилметокси)-2-метил-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид
Пример 251a
2-бром-1-(циклопропилметокси)-3-метил-4-нитробензол
Продукт примера 251a получали согласно процедуре, используемой для получения продукта примера 247a, заменяя 2-бром-3-метил-4-нитрофенолом 2-бром-3-метилфенол, получая указанное в заголовке соединение.
Пример 251b
4-(6-(циклопропилметокси)-2-метил-3-нитрофенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 251b получали согласно процедуре, используемой для получения продукта примера 7d, заменяя продуктом примера 251a продукт примера 7c и перемешивая при 65°C в течение 2,5 часов, получая указанное в заголовке соединение.
Пример 251c
4-(3-амино-6-(циклопропилметокси)-2-метилфенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 251c получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 251b продукт примера 2b, получая указанное в заголовке соединение.
Пример 251d
N-(4-(циклопропилметокси)-2-метил-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил)этансульфонамид
Продукт примера 251d получали согласно процедуре, используемой для получения продукта примера 4 (способ A), заменяя продуктом примера 251c продукт примера 3 и этансульфонил хлоридом метансульфонил хлорид, соответственно, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 11,93 (ушир.дс, 1H), 8,89 (ушир.дс, 1H), 7,23-7,19 (м, 2H), 6,99 (с, 1H), 6,91 (д, J=3,1 Гц, 1H), 5,75 (м, 1H), 3,74 (дд, J=6,6, 2,3 Гц, 2H), 3,54 (с, 3H), 3,07 (м, 2H), 2,06 (с, 3H), 1,27 (м, 3H), 0,99 (м, 1H), 0,33 (м, 2H), 0,08 (м, 2H). MS (ESI+) m/z 416,1 (M+H)+.
Пример 252
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид
Пример 252a
1-(2,4-дифторфенокси)-4-(метилсульфонил)-2-нитробензол
Смесь 1-фтор-4-(метилсульфонил)-2-нитробензола (20 г, 91 ммоль), 2,4-дифторфенола (11,87 г, 91 ммоль) и карбоната калия (12,6 г, 91 ммоль) в DMSO (90 мл) нагревали при 120°C в течение 2 часов. Реакционную смесь гасили водой и экстрагировали этилацетатом. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 1:1 этилацетат/гексаны), получая указанное в заголовке соединение (28 г, выход 89%).
Пример 252b
2-(2,4-дифторфенокси)-5-(метилсульфонил)анилин
Раствор продукта примера 252a (10,0 г, 30,4 ммоль) в тетрагидрофуране (150 мл) добавляли к 10% Pd/C (1,616 г, 15,18 ммоль) в 250 мл бутылке и смесь перемешивали в течение 24 часов в атмосфере водорода 0,207 МПа (30 фунтов на кв. дюйм) при 40°C. Смесь фильтровали через нейлоновую мембрану и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 70:30 этилацетат/гексаны), получая указанное в заголовке соединение (8,6 г, выход 55%).
Пример 252c
1-(2,4-дифторфенокси)-2-йод-4-(метилсульфонил)бензол
Продукт примера 252b (5,00 г, 16,7 ммоль) в диоксане (30 мл) обрабатывали концентрированной HCl (150 мл) при 0°C. Реакционную смесь перемешивали при 0°C в течение 10 минут. К этому раствору добавляли нитрит натрия (1,383 г, 20,05 ммоль) в воде (6 мл). Реакционную смесь перемешивали при 0°C в течение одного часа. К этому раствору добавляли йодид калия (5,55 г, 33,4 ммоль) в воде (20 мл). Реакционную смесь перемешивали в течение двух часов при 10°C. Реакционную смесь затем распределяли между водой и этилацетатом. Органический слой экстрагировали дополнительным этилацетатом дважды. Объединенный органический слой промывали насыщенным водным раствором хлорида натрия, сушили (безводный сульфат магния), фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 2:3 этилацетат/гексаны), получая указанное в заголовке соединение (8,9 г, выход 89%).
Пример 252d
Этил 1-бензил-6-метил-7-оксо-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Смесь продукта примера 70e (2 г, 5,14 ммоль), бис(пинаколято)дибора (2,61 г, 10,3 ммоль), ацетата калия (1,11 г, 11,3 ммоль), трис(дибензилиденацетон)дипалладия(0) (0,235 г, 0,257 ммоль) и 2-дициклогексилфосфино-2',4',6'-триизопропилбифенила (0,245 г, 0,514 ммоль) в диоксане (50 мл) перемешивали при 90°C в течение 16 часов в атмосфере аргона. Смесь фильтровали через целит, промывали этилацетатом несколько раз и концентрировали. Остаток очищали флаш-хроматографией (силикагель, градиент 50-75% этилацетат/петролейный эфир), получая указанное в заголовке соединение (1,15 г, выход 40%).
Пример 252e
этил 1-бензил-4-(2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Продукт примера 252d (2,3 г, 5,27 ммоль), продукт примера 252c (2,270 г, 5,54 ммоль), 1,3,5,7-тетраметил-6-фенил-2,4,8-триокса-6-фосфaадамантан (0,154 г, 0,527 ммоль), трис(дибензилиденацетон)дипалладий(0) (0,121 г, 0,132 ммоль) и фосфат калия (1,119 г, 5,27 ммоль) объединяли и продували аргоном в течение 30 минут. Смесь дегазированного диоксана (30 мл) и воды (7,5 мл) добавляли и реакционную смесь перемешивали при 60°C в течение 16 часов. Реакционную смесь охлаждали до температуры окружающей среды и распределяли между этилацетатом и водой. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили (безводный сульфат натрия), фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 20-100% этилацетат в петролейном эфире), получая указанное в заголовке соединение (1,77 г, выход 33,4%).
Пример 252f
этил 4-(2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Смесь продукта примера 252e, анизола (1,585 мл, 14,51 ммоль) и концентрированной серной кислоты (4,3 мл, 81 ммоль) в трифторуксусной кислоте (20 мл, 260 ммоль) нагревали при 90°C в течение 4 часов. Избыток трифторуксусной кислоты удаляли при пониженном давлении и остаток распределяли между водой (100 мл) и этилацетатом (200 мл). Органический слой отделяли и водный слой экстрагировали дополнительным этилацетатом (2 × 200 мл). Объединенные органические слои промывали насыщенным водным раствором бикарбоната натрия (100 мл), а затем насыщенным водным раствором хлорида натрия (100 мл), сушили над безводным сульфатом магния, фильтровали и концентрировали. Сырой материал забирали в метанол (50 мл) и полученное твердое вещество фильтровали, промывали метанолом и сушили, получая указанное в заголовке соединение (3,1 г, выход 63%).
Пример 252g
4-(2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоновая кислота
Продукт примера 252f (1,1 г, 2,2 ммоль) в диоксане (60 мл) обрабатывали 2,0 M водным раствором гидроксида лития (4,38 мл, 8,76 ммоль). Реакционную смесь нагревали при 65°C в течение двух часов. Реакционную смесь охлаждали до температуры окружающей среды и растворитель удаляли при пониженном давлении. Остаток растворяли в воде (50 мл) и pH доводили до 5 с помощью HCl (3M). Полученное твердое вещество фильтровали и растворяли в этилацетате(200 мл). Раствор сушили над безводным сульфатом натрия, фильтровали и концентрировали, получая указанное в заголовке соединение (0,85 г, выход 77%).
Пример 252h
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид
К раствору продукта примера 252g (0,10 г, 0,21 ммоль) в безводном дихлорметане (5 мл) добавляли оксалил хлорид (0,037 мл, 0,42 ммоль) и диметилформамид (0,816 мкл, 10,5 мкмоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 2 часов. Реакционную смесь концентрировали. Остаток повторно растворяли в дихлорметане (5 мл) и обрабатывали гидроксидом аммония (2 мл, 92 ммоль) и реакционную смесь перемешивали при температуре окружающей среды в течение 16 часов. Реакционную смесь распределяли между водой (15 мл) и этилацетатом (25 мл). Водный слой экстрагировали дополнительным этилацетатом (2 × 15 мл). Объединенные органические слои сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток растирали с этилацетатом и полученное твердое вещество фильтровали, промывали дихлорметаном и сушили в вакууме, получая указанное в заголовке соединение (48 мг, выход 47%). 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 12,33 (с, 1H), 7,98 (с, 1H), 7,98-7,88 (м, 1H), 7,82 (с, 1H), 7,56-7,40 (м, 4H), 7,19 (м, 1H), 7,00 (д, J=8,8 Гц, 1H), 6,87 (с, 1H), 3,59 (с, 3H), 3,27 (с, 3H). MS (ESI+) m/z 474,1 (M+H)+
Пример 253
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-N-этил-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид
Продукт примера 253 получали согласно процедуре, используемой для получения продукта примера 252h, заменяя этанамином гидроксид аммония, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 12,32 (с, 1H), 8,35-8,32 (м, 1H), 7,98 (с, 1H), 7,89 (дд, J=2,4, 6,4 Гц, 1H), 7,56-7,21 (м, 3H), 7,20-7,16 (м, 1H), 7,01 (д, J=8,4 Гц, 1H), 6,85 (с, 1H), 3,59 (с, 3H), 3,30-3,23 (м, 5H), 1,11 (т, J=7,2 Гц, 3H). MS (ESI+) m/z 502,1 (M+H)+.
Пример 254
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-7-оксо-N-(2,2,2-трифторэтил)-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид
Продукт примера 254 получали согласно процедуре, используемой для получения продукта примера 252h, заменяя 2,2,2-трифторэтанамином гидроксид аммония, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 12,56 (с, 1H), 8,94 (т, J=6 Гц, 1H), 7,99 (с, 1H), 7,98-7,89 (м, 1H), 7,52-7,50 (м, 2H), 7,42-7,40 (м, 1H), 7,17 (м, 1H), 7,03-7,00 (м, 2H), 4,13-4,08 (м, 2H), 3,59 (с, 3H), 3,26 (с, 3H). MS (ESI+) m/z 556,1 (M+H)+.
Пример 255
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-(морфолин-4-илкарбонил)-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 255 получали согласно процедуре, используемой для получения продукта примера 252h, заменяя морфолином гидроксид аммония, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 7,99 (с, 1H), 7,88 (дд, J=2,4, 6 Гц, 1H), 7,59-7,42 (м, 3H), 7,22-7,17 (м, 1H), 6,98 (д, J=8,4 Гц, 1H), 6,50 (с, 1H), 3,59 (с, 3H), 3,55 (м, 8H), 3,27 (с, 3H). MS (ESI+) m/z 544,2 (M+H)+.
Пример 256
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-[(4-метилпиперазин-1-ил)карбонил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 256 получали согласно процедуре, используемой для получения продукта примера 252h, заменяя 1-метилпиперазином гидроксид аммония, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 7,97 (д, J=2 Гц, 1H), 7,84 (дд, J=2,4, 6 Гц, 1H), 7,32 (с, 1H), 7,13-7,10 (м, 2H), 6,94-6,91 (м, 2H), 6,51 (с, 1H), 3,68-3,65 (м, 4H), 3,60 (с, 3H), 3,08 (с, 3H), 2,38 (м, 4H), 2,24 (с, 3H). MS (ESI+) m/z 557,2 (M+H)+.
Пример 257
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-7-оксо-N-(1,3-тиазол-2-ил)-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид
Продукт примера 257 получали согласно процедуре, используемой для получения продукта примера 252h, заменяя тиазол-2-амином гидроксид аммония, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 12,82 (с, 1H), 12,49 (с, 1H), 8,01 (с, 1H), 7,92 (дд, J=2,4, 6,4 Гц, 1H), 7,56-7,45 (м, 4H), 7,34-7,29 (м, 2H), 7,22-7,18 (м, 1H), 7,03 (д, J=8,4 Гц, 1H), 3,61 (с, 3H), 3,28 (с, 3H). MS (ESI+) m/z 557,1 (M+H)+.
Пример 258
Этил 4-[2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-4-(метилсульфонил)фенокси]пиперидин-1-карбоксилат
Продукт примера 258 получали согласно процедуре, используемой для получения продукта примера 158, заменяя этил 4-гидроксипиперидин-1-карбоксилатом циклопропилметанол, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,01 (с, 1H), 7,84-7,87 (м, 2H), 7,41 (д, J=9,46 Гц, 1H), 7,31 (с, 1H), 7,27 (т, J=2,59 Гц, 1H), 6,12 (с, 1H), 4,75-4,79 (м, 1H), 3,98 (кв., J=7,02 Гц, 2H), 3,56 (с, 3H), 3,22-3,26 (м, 2H), 3,20 (с, 3H), 2,10 (с, 1H), 1,83-1,88 (м, 2H), 1,43-1,55 (М, 2H), 1,13 (т, J=7,02 Гц, 3H). MS (ESI+) m/z 474,1 (M+H)+.
Пример 259
4-[2-этокси-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Указанное в заголовке соединение изолировали как меньший продукт при получении продукта примера 258. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,02 (с, 1H), 7,88 (дд, J=8,54, 2,44 Гц, 1H), 7,82 (д, J=2,44 Гц, 1H), 7,32-7,34 (м, 2H), 7,28 (т, J=2,75 Гц, 1H), 6,10-6,11 (м, 1H), 4,17 (кв., J=6,92 Гц, 2H), 3,57 (с, 3H), 3,21 (с, 3H), 3,20 (с, 3H), 1,22 (т, J=7,02 Гц, 3H). MS (ESI+) m/z 347,1 (M+H)+.
Пример 260
4-{5-(этилсульфонил)-2-[(транс-4-метоксициклогексил)окси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Указанное в заголовке соединение (первый пик элюирования) изолировали как второй продукт при получении продукта примера 248b. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,03 (с, 1H), 7,78-7,81 (м, 2H), 7,40 (д, J=8,54 Гц, 1H), 7,31 (с, 1H), 7,28 (т, J=2,75 Гц, 1H), 6,10-6,11 (м, 1H), 4,57-4,61 (м, 1H), 3,56 (с, 3H), 3,28 (т, J=7,32 Гц, 2H), 3,19 (с, 3H), 3,14-3,18 (м, 1H), 1,93-1,97 (м, 2H), 1,73-1,77 (м, 2H), 1,31-1,42 (м, 4H), 1,13 (т, J=7,32, 3H). MS (ESI+) m/z 445,0 (M+H)+.
Пример 261
4-{2-[(циклопропилметил)амино]-5-(пропан-2-илсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 261a
(3-бром-4-фторфенил)(изопропил)сульфан
Продукт примера 261a получали согласно процедуре, используемой для получения продукта примера 168a, заменяя 2-йодпропаном йодэтан, получая указанное в заголовке соединение.
Пример 261b
2-бром-1-фтор-4-(изопропилсульфонил)бензол
Продукт примера 261b получали согласно процедуре, используемой для получения продукта примера 168b, заменяя продуктом примера 261a продукт примера 168a, получая указанное в заголовке соединение.
Пример 261c
2-бром-N-(циклопропилметил)-4-(изопропилсульфонил)анилин
Продукт примера 261c получали согласно процедуре, используемой для получения продукта примера 147a, заменяя циклопропилметанамином циклогексанамин и продуктом примера 261b 2-бром-1-фтор-4-(метилсульфонил)бензол, получая указанное в заголовке соединение.
Пример 261d
4-{2-[(циклопропилметил)амино]-5-(пропан-2-илсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 261d получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 261c продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,12 (с, 1H), 7,59 (дд, J=8,7, 2,29 Гц, 1H), 7,40 (д, J=2,44 Гц, 1H), 7,30 (т, J=2,9 Гц, 1H), 7,25 (с, 1H), 6,88 (д, J=8,85 Гц, 1H), 5,98-5,99 (м, 1H), 5,61 (ушир. с, 1H), 3,56 (с, 3H), 3,22-3,30 (м, 2H), 3,03 (д, J=6,71 Гц, 2H), 1,16 (д, J=7,02 Гц, 6H), 0,98-1,14 (м, 1H), 0,36-0,41 (м, 2H), 0,14-0,18 (м, 2H). MS (ESI+) m/z 400,1 (M+H)+.
Пример 262
N-[4-(циклопропилметокси)-2-метил-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Продукт примера 262 получали согласно процедуре, используемой для получения продукта примера 4 (способ A), заменяя продуктом примера 251c продукт примера 3, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, CD3OD) δ м.д. 7,34 (д, J=8,9 Гц, 1H), 7,28 (д, J=2,8 Гц, 1H), 6,98 (с, 1H), 6,93 (д, J=8,9 Гц, 1H), 5,93 (д, J=2,8 Гц, 1H), 3,78 (м, 2H), 3,69 (с, 3H), 2,98 (с, 3H), 2,13 (м, 3H), 0,99 (м, 1H), 0,35 (м, 2H), 0,08 (м, 2H). MS (ESI+) m/z 402,1 (M+H)+.
Пример 263
N-[4-(циклопропилметокси)-2-метил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]метансульфонамид
Пример 263a
1-бром-2-(циклопропилметокси)-4-метил-5-нитробензол
Продукт примера 263a получали согласно процедуре, используемой для получения продукта примера 247a, заменяя 2-бром-5-метил-4-нитрофенолом 2-бром-3-метилфенол, получая указанное в заголовке соединение.
Пример 263b
4-(2-(циклопропилметокси)-4-метил-5-нитрофенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 263b получали согласно процедуре, используемой для получения продукта примера 7d, заменяя продуктом примера 263a продукт примера 7c и перемешивая при 65°C в течение 2,5 часов, получая указанное в заголовке соединение.
Пример 263c
4-(5-амино-2-(циклопропилметокси)-4-метилфенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 263c получали согласно процедуре, используемой для получения продукта примера 3, заменяя продуктом примера 263b продукт примера 2b, получая указанное в заголовке соединение.
Пример 263d
N-(4-(циклопропилметокси)-2-метил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил)метансульфонамид
Продукт примера 263d получали согласно процедуре, используемой для получения продукта примера 4 (способ A), заменяя продуктом примера 263c продукт примера 3, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, CD3OD) δ м.д. 7,36 (с, 1H), 7,31 (д, J=2,8 Гц, 1H), 7,28 (с, 1H), 6,96 (с, 1H), 6,35 (д, J=2,8 Гц, 1H), 3,84 (д, J=6,7 Гц, 2H), 3,69 (с, 3H), 3,11 (с, 3H), 2,41 (с, 3H), 1,11 (м, 1H), 0,47 (м, 2H), 0,24 (м, 2H). MS (ESI+) m/z 402,1 (M+H)+.
Пример 264
4-[5-(этилсульфонил)-2-(тетрагидро-2H-тиопиран-4-илокси)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 264a
4-(2-бром-4-(этилсульфонил)фенокси)тетрагидро-2H-тиопиран
Продукт примера 264a получали согласно процедуре, используемой для получения продукта примера 158, заменяя продуктом примера 168b продукт примера 138a и тетрагидро-2H-тиопиран-4-олом циклопропилметанол, соответственно, получая указанное в заголовке соединение.
Пример 264b
4-[5-(этилсульфонил)-2-(тетрагидро-2H-тиопиран-4-илокси) фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 264b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 264a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,05 (с, 1H), 7,79-7,82 (м, 2H), 7,40 (д, J=9,77 Гц, 1H), 7,34 (с, 1H), 7,30 (т, J=2,75 Гц, 1H), 6,12-6,13 (м, 1H), 4,69-4,72 (м, 1H), 3,58 (с, 3H), 3,28 (д, J=7,32 Гц, 2H), 2,50-2,62 (м, 4H), 2,06-2,12 (м, 2H), 1,74-1,81 (м, 2H), 1,13 (д, J=7,32 Гц, 6H). MS (ESI+) m/z 433,1 (M+H)+.
Пример 265
4-{2-[(1,1-диоксидотетрагидро-2H-тиопиран-4-ил)окси]-5-(этилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 265 получали согласно процедуре, используемой для получения продукта примера 168b, заменяя 264b продукт примера 168a, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,09 (с, 1H), 7,83-7,87 (м, 2H), 7,48 (д, J=8,85 Гц, 1H), 7,35 (с, 1H), 7,29 (т, J=2,75 Гц, 1H), 6,14-6,15 (м, 1H), 4,90-4,93 (м, 1H), 3,58 (с, 3H), 3,30 (кв., J=7,43 Гц, 2H), 3,01-3,04 (м, 2H), 2,76-2,82 (м, 2H), 2,12-2,18 (м, 4H), 1,14 (т, J=7,32 Гц, 3H). MS (ESI+) m/z 465,1 (M+H)+.
Пример 266
6-(2,4-дифторфенокси)-N,N-диметил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид
Пример 266a
5-бром-6-(2,4-дифторфенокси)-N,N-диметилпиридин-3-сульфонамид
Продукт примера 242a (0,365 г, 1 ммоль) в диметилформамиде (5 мл) обрабатывали 60% гидридом натрия (0,120 г, 3,00 ммоль). Раствор перемешивали в течение 10 минут. К этому раствору добавляли йодметан (0,355 г, 2,500 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 2 часов. Реакционную смесь распределяли между водой и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом два и более раз. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией на силикагеле, получая указанное в заголовке соединение (0,365 г, 0,928 ммоль, выход 93%).
Пример 266b
6-(2,4-дифторфенокси)-N,N-диметил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид
Продукт примера 266b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 266a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,17 (с, 1H), 8,50 (д, J=2,44 Гц, 1H), 8,18 (д, J=2,44 Гц, 1H), 7,57 (с, 1H), 7,46-7,51 (м, 2H), 7,35 (т, J=2,75 Гц, 1H), 7,15-7,18 (м, 1H), 6,33-6,34 (м, 1H), 3,61 (с, 3H), 2,71 (с, 6H). MS (ESI+) m/z 461,1 (M+H)+.
Пример 267
4-[2-(циклопропиламино)-5-(этилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 267a
2-бром-N-циклопропил-4-(этилсульфонил)анилин
Продукт примера 267a получали согласно процедуре, используемой для получения продукта примера 147a, заменяя циклопропиламином циклогексанамин и продуктом примера 168b 2-бром-1-фтор-4-(метилсульфонил)бензол, получая указанное в заголовке соединение.
Пример 267b
4-[2-(циклопропиламино)-5-(этилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 267b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 267a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,32 (с, 1H), 7,92 (дд, J=8,7, 2,29 Гц, 1H), 7,68 (д, J=2,44 Гц, 1H), 7,51 (т, J=2,75 Гц, 1H), 7,45 (с, 1H), 7,40 (д, J=8,54 Гц, 1H), 6,14-6,15 (м, 1H), 6,11 (с, 1H), 3,77 (с, 3H), 3,40 (кв., J=7,32 Гц, 2H), 2,63-2,67 (м, 1H), 1,35 (т, J=7,32 Гц, 3H), 0,95-0,97 (м, 2H), 0,62-0,68 (м, 2H). MS (ESI+) m/z 372,1 (M+H)+.
Пример 268
4-(5-(этилсульфонил)-2-(цис-4-метокси-4-метилциклогексилокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Пример 268a
8-(2-бром-4-(этилсульфонил)фенокси)-1,4-диоксаспиро[4,5]декан
Продукт примера 268a получали согласно процедуре, используемой для получения продукта примера 158, заменяя продуктом примера 168b продукт примера 138a и 1,4-диоксаспиро[4,5]декан-8-олом циклопропилметанол, соответственно, получая указанное в заголовке соединение.
Пример 268b
4-(2-бром-4-(этилсульфонил)фенокси)циклогексанон
Продукт примера 268b получали согласно процедуре, используемой для получения продукта примера 199, заменяя продуктом примера 268a продукт примера 197, получая указанное в заголовке соединение.
Пример 268c
(цис)-4-(2-бром-4-(этилсульфонил)фенокси)-1-метилциклогексанол
Продукт примера 268b (0,95 г, 2,63 ммоль) в THF (15 мл) охлаждали до 0°C. Этот раствор обрабатывали 3,0M бромидом метилмагния (2,63 мл, 7,89 ммоль) и перемешивали при комнатной температуре в течение ночи. Реакционную смесь гасили насыщенным раствором NH4Cl и распределяли между водой и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным раствором соли, сушили над MgSO4, фильтровали и концентрировали. Остаток очищали колоночной флаш-хроматографией на силикагеле, элюируя 1:1 этилацетат/гексаны, получая две фракции. Продукт примера 268c был первой фракцией, которую элюировали из колонки.
Пример 268d
2-бром-4-(этилсульфонил)-1-((цис)-4-метокси-4-метилциклогексилокси)бензол
Продукт примера 268c (0,43 г, 1,140 ммоль) в тетрагидрофуране (5 мл) обрабатывали 60% гидридом натрия (0,182 г, 4,5 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 10 минут. К этому раствору добавляли йодметан (2) (0,65 г, 4,5 ммоль). Реакционную смесь нагревали при 40°C в течение 16 часов. Реакционную смесь распределяли между водой и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом два или более раз. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией на силикагеле, получая указанное в заголовке соединение (0,356 г, 0,910 ммоль, выход 80%).
Пример 268е
4-(5-(этилсульфонил)-2-(цис-4-метокси-4-метилциклогексилокси)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 268e получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 268d продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,04 (с, 1H), 7,77-7,81 (м, 2H), 7,39 (д, J=8,85 Гц, 1H), 7,31 (с, 1H), 7,29 (т, J=2,75 Гц, 1H), 6,10-6,11 (м, 1H), 4,50-4,55 (м, 1H), 3,57 (с, 3H), 3,28 (кв., J=7,32 Гц, 2H), 1,69-1,78 (м, 4H), 1,46-1,53 (м, 2H), 1,33-1,38 (м, 2H), 1,13 (т, J=7,32 Гц, 3H), 1,05 (с, 3H). MS (ESI+) m/z 459,1 (M+H)+.
Пример 269
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-N,N,6-триметил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид
Пример 269 получали согласно процедуре, используемой для получения продукта примера 252h, заменяя диметиламином гидроксид аммония, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 8,08 (с, 1H), 7,95 (дд, J=2,4, 6 Гц, 1H), 7,43 (с, 1H), 7,26-7,15 (м, 2H), 7,05-6,99 (м, 2H), 6,69 (с, 1H), 3,72 (с, 3H), 3,25 (с, 3H), 3,19 (с, 3H), 3,12 (с, 1H). MS (ESI+) m/z 502,0 (M+H)+.
Пример 270
6-метил-4-{5-(метилсульфонил)-2-[4-(метилсульфонил)фенокси]фенил}-1,6-дигидро-7Н-пирроло[2,3-c]пиридин-7-он
Продукт примера 270 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 4-(метилсульфонил)фенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,08 (с, 1H), 8,06 (д, J=2,44 Гц, 1H), 7,97 (дд, J=8,7, 2,29 Гц, 1H), 7,85-7,88 (м, 2H), 7,40 (с, 1H), 7,35 (д, J-=8,54 Гц, 1H), 7,29 (т, J=2,75 Гц, 1H), 7,20-7,23 (м, 2H), 6,24-6,25 (м, 1H), 3,54 (с, 3H), 3,30 (с, 3H), 3,17 (с, 3H). MS (ESI+) m/z 471,2 (M+H)+.
Пример 271
4-[2-(2,4-дифторфенокси)-5-(пропан-2-илсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 271a
2-бром-1-(2,4-дифторфенокси)-4-(изопропилсульфонил)бензол
Продукт примера 271a получали согласно процедуре, используемой для получения продукта примера 138b, заменяя продуктом примера 261b продукт примера 138a, получая указанное в заголовке соединение.
Пример 271b
4-[2-(2,4-дифторфенокси)-5-(пропан-2-илсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 271b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 271a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,11 (с, 1H), 7,88 (д, J=2,44 Гц, 1H), 7,80 (дд, J=8,85, 2,44 Гц, 1H), 7,50-7,54 (м, 1H), 7,42-7,49 (м, 2H), 7,31 (т, J=2,75 Гц, 1H), 7,15-7,19 (м, 1H), 7,00 (д, J=8,54, Гц, 1H), 6,25-6,26 (м, 1H), 3,59 (с, 3H), 3,,44-3,48 (м, 1H), 1,20 (д, J=7,02 Гц, 6H). MS (ESI+) m/z 459,0 (M+H)+.
Пример 272
6-(циклопропилметокси)-N,N-диэтил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид
Пример 272a
5-бром-6-(циклопропилметокси)-N,N-диэтилпиридин-3-сульфонамид
Продукт примера 272a получали согласно процедуре, используемой для получения продукта примера 266a, заменяя продуктом примера 207a продукт примера 242a и этилйодидом йодметан, соответственно, получая указанное в заголовке соединение.
Пример 272b
6-(циклопропилметокси)-N,N-диэтил-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)пиридин-3-сульфонамид
Продукт примера 272b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 272a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,10 (с, 1H), 8,54 (д, J=2,44 Гц, 1H), 8,01 (д, J=2,44 Гц, 1H), 7,44 (с, 1H), 7,32 (т, J=2,75 Гц, 1H), 6,15-6,16 (м, 1H), 4,24 (д, J=7,02 Гц, 2H), 3,58 (с, 3H), 3,21 (кв., J=7,02 Гц, 4H), 1,17-1,20 (м, 4H), 1,08 (т, J=7,02 Гц, 6H), 0,47-0,51 (м, 2H), 0,29-0,32 (м, 2H). MS (ESI+) m/z 431,1 (M+H)+.
Пример 273
4-(циклопропилметокси)-N,N-диметил-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид
Пример 273a
3-бром-4-(циклопропилметокси)-N,N-диметилбензолсульфонамид
Продукт примера 273a получали согласно процедуре, используемой для получения продукта примера 266a, заменяя продуктом примера 249a продукт примера 242a, получая указанное в заголовке соединение.
Пример 273b
4-(циклопропилметокси)-N,N-диметил-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид
Продукт примера 273b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 273a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,05 (с, 1H), 7,70 (дд, J=8,54, 2,44 Гц, 1H), 7,66 (д, J=2,44 Гц, 1H), 7,37 (с, 1H), 7,29-7,32 (м, 2H), 6,12-6,13 (м, 1H), 3,98 (д, J=6,71 Гц, 2H), 3,57 (с, 3H), 2,62 (с, 6H), 3,21 (кв., J=7,02 Гц, 4H), 1,11-1,15 (м, 1H), 0,46-0,49 (м, 2H), 0,27-0,30 (м, 2H). MS (ESI+) m/z 402,1 (M+H)+.
Пример 274
4-[2-(циклопропилметокси)-5-фторфенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 274a
2-бром-1-(циклопропилметокси)-4-фторбензол
К раствору 2-бром-4-фторфенола (0,50 г, 2,6 ммоль) в тетрагидрофуране (13 мл) добавляли циклопропанметанол (0,209 мл, 2,62 ммоль), трифенилфосфин (0,687 г, 2,62 ммоль) и DIAD (0,509 мл, 2,62 ммоль). Реакционную смесь перемешивали в течение 16 часов при температуре окружающей среды. Растворитель удаляли при пониженном давлении. Остаток растирали с гексанами. Смесь фильтровали и фильтрат, содержащий продукт, концентрировали при пониженном давлении. Остаток очищали флаш-хроматографией (силикагель, гексаны), получая указанное в заголовке соединение (400 мг, выход 62%).
Пример 274b
(2-(циклопропилметокси)-5-фторфенил)бороновая кислота
К раствору продукта примера 274a (0,1 г, 0,408 ммоль) в тетрагидрофуране (2 мл) при -20°C добавляли nBuLi (0,180 мл 2,5M раствора в гексанах, 0,449 ммоль). Реакционную смесь перемешивали в течение 2 часов, затем охлаждали до -40°C. 2-Изoпропокси-4,4,5,5-тетраметил-1,3,2-диоксаборолан (0,092 мл, 0,449 ммоль) добавляли по каплям. Реакционную смесь перемешивали в течение 30 минут. Реакционную смесь гасили 1M лимонной кислотой при 0°C. Смесь перемешивали при температуре окружающей среды в течение 1 часа и затем экстрагировали этилацетатом. Слои разделяли и органический слой сушили над безводным сульфатом натрия, фильтровали и концентрировали. Сырой материал очищали флаш-хроматографией (силикагель, градиент 10-33% этилацетат/гексаны), получая указанное в заголовке соединение (23 мг, выход 20%).
Пример 274c
4-[2-(циклопропилметокси)-5-фторфенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Азот барботировали через раствор 4:1 диметоксиэтан/этанол в течение 20 минут. В склянку для микроволновой обработки загружали продукт примера 1e (0,05 г, 0,131 ммоль), продукт примера 274b (0,046 г, 0,144 ммоль), Pd(Ph3P)4 (7,58 мг, 6,56 мкмоль) и фторид цезия (0,060 г, 0,393 ммоль). Склянку уплотняли и продували азотом. Смесь 4:1 диметоксэтан/этанол (0,5 мл) добавляли. Реакционную смесь нагревали в микроволновом реакторе при 120°C в течение 40 минут. Реакционную смесь распределяли между водой и этилацетатом. Слои разделяли. Водный слой экстрагировали этилацетатом. Объединенные органические вещества сушили над безводным сульфатом натрия, фильтровали и концентрировали. Сырой материал очищали флаш-хроматографией (силикагель, градиент 20-80% этилацетат/гексаны), получая указанное в заголовке соединение (5 мг, выход 23%). 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 11,98 (с, 1H), 7,29 (с, 1H), 7,26 (т, J=2,71 Гц, 1H), 7,05-7,18 (м, 3H), 6,14 (дд, J=2,71, 2,03 Гц, 1H), 3,80 (д, J=6,78 Гц, 2H), 3,55 (с, 3H), 0,98-1,09 (м, 1H), 0,39-0,46 (м, 2H), 0,17-0,22 (м, 2H). MS (ESI+) m/z 313,1 (M+H)+.
Пример 275
4-[2-(2,4-дифторфенокси)-5-(трифторметил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 275a
2-бром-1-(2,4-дифторфенокси)-4-(трифторметил)бензол
Смесь 3-бром-4-фторбензотрифторида (0,5 мл, 3,52 ммоль), 2,4-дифторфенола (0,337 мл, 3,52 ммоль) и карбоната калия (0,486 г, 3,52 ммоль) в диметилформамиде (7 мл) нагревали при 80°C в течение 16 часов. Реакционную смесь охлаждали до температуры окружающей среды и распределяли между этилацетатом и водой. Слои разделяли и водный слой экстрагировали этилацетатом. Объединенные органические вещества промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали. Сырой материал очищали флаш-хроматографией (силикагель, градиент 0-10% этилацетат/гексаны), получая указанное в заголовке соединение (1,0 г, выход 80%).
Пример 275b
(2-(2,4-дифторфенокси)-5-(трифторметил)фенил)бороновая кислота
К суспензии магния (0,083 г, 3,42 ммоль) в тетрагидрофуране (1,00 мл) добавляли 0,5 мл раствора продукта примера 275a (1,099 г, 3,11 ммоль) в тетрагидрофуране (1,5 мл). Реакционную смесь нагревали (около 40-50°C), пока не начиналась реакция. Остальной раствор исходного бромида добавляли по каплям. Реакционную смесь перемешивали при температуре окружающей среды в течение 1 часа. Полученный раствор добавляли по каплям к раствору триметил бората (0,696 мл, 6,23 ммоль) в тетрагидрофуране (1,5 мл) при 0°C. Реакционную смесь перемешивали при температуре окружающей среды в течение 1 часа, гасили водой со льдом и затем нейтрализовали 2 M HCl. Смесь экстрагировали этилацетатом. Объединенные органические вещества промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, градиент 10-33% этилацетат/гексаны), получая указанное в заголовке соединение (650 мг, выход 66%).
Пример 275c
4-[2-(2,4-дифторфенокси)-5-(трифторметил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 275c получали согласно процедуре, используемой для получения продукта примера 274c, заменяя продуктом примера 275b продукт примера 274b, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,06 (с, 1H), 7,78 (д, J=2,37 Гц, 1H), 7,70 (дд, J=8,48, 1,70 Гц, 1H), 7,49 (тд, J=11,36, 8,65, 3,05 Гц, 1H), 7,40 (с, 1H), 7,34-7,43 (м, 1H), 7,28 (т, J=2,71 Гц, 1H), 7,10-7,17 (м, 1H), 6,95 (д, J=8,48 Гц, 1H), 6,24 (дд, J=2,71, 2,03 Гц, 1H), 3,57 (с, 3H). MS (ESI+) m/z 421,1 (M+H)+.
Пример 276
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-2-(гидроксиметил)-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
К суспензии продукта примера 252f (0,20 г, 0,40 ммоль) в тетрагидрофуране (5 мл), перемешиваемой при 0°C, добавляли гидрид лития алюминия (1M в тетрагидрофуране, 0,398 мл, 0,398 ммоль) и смесь перемешивали при 0°C в течение двух часов. Растворитель выпаривали при пониженном давлении и остаток распределяли между этилацетатом (30 мл) и водой (20 мл). Смесь фильтровали, чтобы удалить нерастворенные материалы. Водный слой экстрагировали этилацетатом (2 × 30 мл). Объединенные органические слои сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток растирали с дихлорметаном и полученное твердое вещество отфильтровывали и сушили, получая указанное в заголовке соединение (0,10 г, выход 55%). 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 11,91 (с, 1H), 7,97 (д, J=2,4 Гц, 1H), 7,86 (дд, J=2,4, 6,4 Гц, 1H), 7,56-7,38 (м, 3H), 7,20-7,15 (м, 1H),6,97 (д, J=8,4 Гц, 1H), 6,18 (с, 1H), 5,11 (т, J=5,6 Гц, 1H), 4,50 (д, J=5,6 Гц, 2H), 3,57 (с, 3H), 3,16 (с, 3H). MS (ESI+) m/z 461,2 (M+H)+.
Пример 277
4-[2-(2,3-дигидро-1H-инден-2-илокси)-5-(метилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 277 получали согласно процедуре, используемой для получения продукта примера 158, заменяя 2,3-дигидро-1H-инден-2-олом циклопропилметанол, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 11,97 (с, 1H), 7,91 (дд, J=8,54, 2,44 Гц, 1H), 7,85 (д, J=2,44 Гц, 1H), 7,47 (д, J=8,85 Гц, 1H), 7,20-7,23 (м, 2H), 7,12-7,17 (м, 3H), 7,07 (с, 1H), 6,00-6,01 (м, 1H), 5,41-5,44 (м, 1H), 3,36-3,42 (м, 2H), 3,56 (с, 3H), 3,23 (с, 3H), 3,20 (с, 3H), 2,97 (дд, J=16,94, 1,98 Гц, 2H). MS (ESI+) m/z 435,1 (M+H)+.
Пример 278
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-2-(1-гидроксиэтил)-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 278a
4-(2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбальдегид
К раствору продукта примера 276 (1,0 г, 2,2 ммоль) в дихлорметане (50 мл) при 0°C добавляли Dess-Martin Periodinane (1,84 г, 4,34 ммоль) и реакционную смесь перемешивали при 0°C в течение 30 минут. Реакционную смесь затем перемешивали при температуре окружающей среды в течение трех часов. Раствор бисульфита натрия (0,9 г, 9 ммоль) в насыщенном водном растворе бикарбоната натрия (5 мл) добавляли и реакционную смесь перемешивали в течение 15 минут и экстрагировали этилацетатом. Органический слой сушили (безводный сульфат натрия), фильтровали и концентрировали, получая указанное в заголовке соединение (0,80 г, выход 70% выход).
Пример 278b
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-2-(1-гидроксиэтил)-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
К раствору продукта примера 278a (0,20 г, 0,44 ммоль) в тетрагидрофуране (6 мл) при 0°C добавляли бромид метилмагния (1,0 M в тетрагидрофуране, 0,873 мл, 0,873 ммоль). Реакционную смесь перемешивали при 0°C в течение одного часа и затем добавляли 1M водную HCl (2 мл). Реакционную смесь концентрировали и распределяли между насыщенным водным раствором хлорида натрия (10 мл) и этилацетатом (2 × 30 мл). Объединенную органическую фазу промывали насыщенным водным раствором хлорида натрия (30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток очищали препаративной тонкослойной хроматографией (силикагель, дихлорметан/метанол, 15/1), получая указанное в заголовке соединение (51 мг, выход 24%). 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 11,83 (с, 1H), 7,96 (д, J=2,4 Гц, 1H), 7,86 (дд, J=2,4, 6,4 Гц, 1H), 7,55-7,50 (м, 1H), 7,42-7,36 (м, 2H), 7,20-7,15 (м, 1H), 6,97 (д, J=8,8 Гц, 1H), 6,15 (д, J=2 Гц, 1H), 5,13 (д, J=5,2 Гц, 1H), 4,80-4,77 (м, 1H), 3,57 (с, 3H), 3,25 (с, 3H), 1,38 (д, J=6,4 Гц, 3H). MS (ESI+) m/z 475,1 (M+1)+.
Пример 279
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-2-[(диметиламино)метил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
К раствору продукта примера 278a (0,20 г, 0,44 ммоль) и диметиламин гидрохлорида (0,071 г, 0,873 ммоль) в метаноле (6 мл) добавляли хлорид цмнка (0,059 г, 0,436 ммоль) при температуре окружающей среды. Реакционную смесь перемешивали при температуре окружающей среды в течение одного часа и затем добавляли цианоборгидрид натрия (0,055 г, 0,873 ммоль) и реакционную смесь перемешивали при температуре окружающей среды в течение трех дней. Полученное твердое вещество фильтровали и промывали метанолом (10 мл) и элюент концентрировали. Остаток очищали препаративной тонкослойной хроматографией (силикагель, дихлорметан/метанол, 15/1), получая указанное в заголовке соединение (75 мг, выход 34%). 1H ЯМР (400 МГц, CD3OD) δ м.д. 8,07 (д, J=2,4 Гц, 1H), 7,94 (дд, J=2,4, 6,4 Гц, 1H), 7,38 (с, 1H), 7,25-7,06 (м, 2H), 7,04-6,98 (м, 2H), 6,31 (с, 1H), 3,71 (с, 3H), 3,67 (с, 2H), 3,19 (с, 3H), 2,28 (с, 6H). MS (ESI+) m/z 488,1 (M+H)+.
Пример 280
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-(морфолин-4-илметил)-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 280 получали согласно процедуре, используемой для получения продукта примера 279, заменяя морфолином диметиламин гидрохлорид, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 11,98 (с, 1H), 7,98 (д, J=2,4 Гц, 1H), 7,87 (дд, J=2,4, 6,4 Гц, 1H), 7,56-7,50 (м, 1H), 7,44-7,38 (м, 2H), 7,19-7,16 (м, 1H), 6,99 (д, J=8,4 Гц, 1H), 6,15 (с, 1H), 3,58 (с, 3H), 3,55 (с, 2H), 3,49-3,47 (м, 4H), 3,26 (с, 3H), 2,31 (м, 4H). MS (ESI+) m/z 530,2 (M+H)+.
Пример 281
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-[(4-метилпиперазин-1-ил)метил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 281 получали согласно процедуре, используемой для получения продукта примера 279, заменяя 1-метилпиперазином диметиламин гидрохлорид, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 11,94 (с, 1H), 7,98 (д, J=2,4 Гц, 1H), 7,87 (дд, J=2,4, 6,4 Гц, 1H), 7,55-7,49 (м, 1H), 7,43-7,37 (м, 2H), 7,18-7,13 (м, 1H), 6,99 (д, J=8,4 Гц, 1H), 6,12 (с, 1H), 3,57 (с, 3H), 3,52 (с, 2H), 3,26 (с, 3H), 2,32-2,21 (м, 8H), 2,09 (с, 3H). MS (ESI+) m/z 543,2 (M+H)+.
Пример 282
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-[(фениламино)метил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 282 получали согласно процедуре, используемой для получения продукта примера 279, заменяя анилином диметиламин гидрохлорид, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 11,95 (с, 1H), 7,93 (д, J=2,4 Гц, 1H), 7,84 (дд, J=2,4, 6,8 Гц, 1H), 7,48 (м, 1H), 7,40 (с, 1H), 7,29-7,28 (м, 1H), 7,12 (м, 1H), 6,99-6,91 (м, 3H), 6,58 (д, J=7,6 Гц, 2H), 6,49 (т, J=7,2 Гц, 1H), 6,19 (д, J=2,0 Гц, 1H), 5,94 (м, 1H), 4,31 (д, J=6,4 Гц, 2H), 3,56 (с, 3H), 3,23 (с, 3H). MS (ESI+) m/z 536,2 (M+H)+.
Пример 283
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-[(1,3-тиазол-2-иламино)метил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 283 получали согласно процедуре, используемой для получения продукта примера 279, заменяя тиазол-2-амином диметиламин гидрохлорид, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 11,99 (с, 1H), 7,94 (д, J=2,4 Гц, 1H), 7,86-7,83 (м, 2H), 7,51-7,45 (м, 1H), 7,42 (с, 1H), 7,30-7,26 (м, 1H), 7,14-7,13 (м, 1H), 6,99-6,92 (м, 2H), 6,62 (д, J=3,6 Гц, 1H), 6,18 (с, 1H), 5,94 (м, 1H), 4,49 (д, J=5,6 Гц, 2H), 3,58 (с, 3H), 3,24 (с, 3H). MS (ESI+) m/z 543,2 (M+H)+.
Пример 284
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-[(тетрагидрофуран-3-иламино)метил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 284 получали согласно процедуре, используемой для получения продукта примера 279, заменяя тетрагидрофуран-3-амином диметиламин гидрохлорид, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 11,86 (с, 1H), 7,97 (д, J=2,4 Гц, 1H), 7,87-7,85 (м, 2H), 7,54-7,39 (м, 3H), 7,18-7,16 (м, 1H), 6,98 (д, J=8,4 Гц, 1H), 6,17 (с, 1H), 3,72-3,66 (м, 3H), 3,57-3,53 (м, 5H), 3,25 (с, 3H), 3,14-3,13 (м, 1H), 2,27-2,26 (м, 1H), 1,82-1,77 (м, 1H), 1,58-1,57 (м, 1H). MS (ESI+) m/z 530,2 (M+H)+.
Пример 285
4-[2-(циклопропилметокси)-5-(фенилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 285a
1-(циклопропилметокси)-4-(фенилсульфонил)бензол
Продукт примера 285a получали согласно процедуре, используемой для получения продукта примера 158, заменяя 1-фтор-4-(фенилсульфонил)бензолом продукт примера 138a, получая указанное в заголовке соединение.
Пример 285b
2-бром-1-(циклопропилметокси)-4-(фенилсульфонил)бензол
Продукт примера 285a (0,087 г, 0,3 ммоль) в уксусной кислоте (5 мл) охлаждали до 0°C. К этому раствору добавляли 1-бромпирролидин-2,5-дион (2) (0,059 г, 0,330 ммоль). Реакционную смесь нагревали при 80°C в течение 16 часов. После охлаждения реакционную смесь распределяли между водой и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом два или более раз. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией на силикагеле, получая указанное в заголовке соединение (0,032 г, 0,087 ммоль, выход 29%).
Пример 285c
4-[2-(циклопропилметокси)-5-(фенилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло [2,3-c]пиридин-7-он
Продукт примера 285c получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 285b продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 11,80 (с, 1H), 7,63-7,74 (м, 4H), 7,36-7,46 (м, 3H), 7,12 (с, 1H), 7,04-7,06 (м, 2H), 5,80-5,81 (м, 1H), 3,72 (д, J=6,71 Гц, 2H), 3,34 (с, 3H), 0,82-0,89 (м, 1H), 0,29-0,24 (м, 2H), 0,00-0,04 (м, 2H). MS (ESI+) m/z 434,9 (M-H)+.
Пример 286
4-[2-(циклопропилметокси)-5-(морфолин-4-илсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 286a
4-(3-бром-4-фторфенилсульфонил)морфолин
3-Бром-4-фторбензол-1-сульфонил хлорид (0,44 г, 1,609 ммоль) в тетрагидрофуране (10 мл) обрабатывали морфолином (0,294 г, 3,38 ммоль). Реакционную смесь перемешивали в течение 16 часов при температуре окружающей среды. Растворитель удаляли и остаток загружали на силикагелевую колонку и элюировали 20% этилацетатом в гексанах, получая указанное в заголовке соединение (0,45 г, 1,388 ммоль, выход 86%).
Пример 286b
4-(3-бром-4-(циклопропилметокси)фенилсульфонил)морфолин
Продукт примера 286b получали согласно процедуре, используемой для получения продукта примера 158, заменяя продуктом примера 286a продукт примера 138a, получая указанное в заголовке соединение.
Пример 286c
4-[2-(циклопропилметокси)-5-(морфолин-4-илсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 286c получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 286b продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,03 (с, 1H), 7,69 (дд, J=8,85, 2,44 Гц, 1H), 7,64 (д, J=2,44 Гц, 1H), 7,37 (с, 1H), 7,33 (д, J=8,85 Гц, 1H), 7,29 (т, J=2,75 Гц, 1H), 6,11-6,13 (м, 1H), 3,97 (д, J=6,71 Гц, 2H), 3,62-3,65 (м, 4H), 3,57 (с, 3H), 2,86-2,88 (м, 4H), 0,45-0,48 (м, 2H), 0,27-0,29 (м, 2H). MS (ESI+) m/z 444,1 (M+H)+.
Пример 287
4-{2-(2,4-дифторфенокси)-5-[(метилсульфонил)метил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 287a
3-бром-4-(2,4-дифторфенокси)бензальдегид
Смесь 3-бром-4-фторбензальдегида (4,06 г, 20 ммоль), 2,4-дифторфенола (2,60 г, 20 ммоль) и карбоната цезия (7,17 г, 22 ммоль) в диметил сульфоксиде (20 мл) нагревали при 100°C в течение 1 часа. Реакционную смесь распределяли между этилацетатом и водой. Органический слой промывали насыщенным водным раствором хлорида натрия дважды, сушили безводным сульфатом натрия, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 20% этилацетат в гептанах), получая указанное в заголовке соединение (5,94 г, 95%).
Пример 287b
(3-бром-4-(2,4-дифторфенокси)фенил)метанол
К раствору продукта примера 287a (3,76 г, 12 ммоль) в смеси этанола (10 мл) и тетрагидрофурана (10 мл) добавляли боргидрид натрия (0,136 г, 3,60 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 1 часа. Растворитель выпаривали и остаток распределяли с этилацетатом и водой. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили безводным сульфатом натрия, фильтровали и концентрировали, получая указанное в заголовке соединение (3,72 г, 98%).
Пример 287c
2-бром-4-(бромметил)-1-(2,4-дифторфенокси)бензол
К раствору продукта примера 287b (3,70 г, 11,74 ммоль) в дихлорметане (20 мл) добавляли трибромид фосфора (1,11 мл, 11,7 ммоль) по каплям. Реакционную смесь перемешивали при температуре окружающей среды в течение 3 часов и выливали в воду со льдом. pH доводили до щелочного осторожным добавлением насыщенного водного раствора бикарбоната натрия и смесь экстрагировали дихлорметаном. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили безводным сульфатом натрия, фильтровали и концентрировали, получая указанное в заголовке соединение (4,15 г, 93%).
Пример 287d
(3-бром-4-(2,4-дифторфенокси)бензил)(метил)сульфан
Смесь продукта примера 287c (1,512 г, 4,00 ммоль) и тиометоксида натрия (0,280 г, 4,00 ммоль) в диметилформамиде (8 мл) перемешивали при температуре окружающей среды в течение 6 часов. Реакционную смесь распределяли между этилацетатом и водой. Органический слой промывали насыщенным водным раствором хлорида натрия дважды, сушили безводным сульфатом натрия, фильтровали и концентрировали, получая указанное в заголовке соединение (1,38 г, 100%).
Пример 287e
2-бром-1-(2,4-дифторфенокси)-4-(метилсульфонилметил)бензол
К раствору продукта примера 287d (1,38 г, 4,00 ммоль) в метаноле (15 мл) добавляли оксон (5,16 г, 8,40 ммоль) в воде (15 мл) при 0°C. Реакционную смесь перемешивали при температуре окружающей среды в течение 1 часа. Реакционную смесь распределяли между этилацетатом и водой. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили безводным сульфатом натрия, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 20-40% этилацетат в гептанах), получая указанное в заголовке соединение (1,49 г, 98%).
Пример 287f
4-(2-(2,4-дифторфенокси)-5-(метилсульфонилметил)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 287e (94 мг, 0,25 ммоль), продукт примера 6a (107 мг, 0,250 ммоль), фосфат калия (186 мг, 0,875 ммоль), трис(дибензилиденацетон)дипалладий (6,9 мг, 7,5 мкмоль) и 1,3,5,7-тетраметил-6-фенил-2,4,8-триокса-6-фосфаадамант (6,6 мг, 0,023 ммоль) объединяли в пробирке для микроволнового нагрева и продували азотом в течение 15 минут. Смесь диоксана (2 мл) и воды (0,5 мл) продували азотом в течение 15 минут и переносили в пробирку для микроволнового нагрева. Реакционную смесь нагревали при 60°C в течение 1 часа. Реакционную смесь распределяли между этилацетатом и водой. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили безводным сульфатом натрия, обрабатывали силикагелем, функционализованным 3-меркаптопропилом, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 1-2% метанол в дихлорметане), получая указанное в заголовке соединение (62 мг, 41%).
Пример 287g
4-{2-(2,4-дифторфенокси)-5-[(метилсульфонил)метил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 287f (59,9 мг, 0,100 ммоль), гидроксид калия (84 мг, 1,5 ммоль) и бромид цетилтриметиламмония (1,8 мг, 5,0 мкмоль) объединяли в смеси тетрагидрофурана (4 мл) и воды (2 мл). Реакционную смесь нагревали при 100°C в течение 44 часов и затем охлаждали до температуры окружающей среды. К этой смеси добавляли воду и pH доводили до pH 7 добавлением 1M HCl. Смесь экстрагировали этилацетатом и органический слой промывали насыщенным водным раствором хлорида натрия дважды, сушили безводным сульфатом натрия, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 2-4% метанол в дихлорметане), получая указанное в заголовке соединение (31 мг, 70%). 1H ЯМР (300 МГц, DMSO-d6) δ м.д.12,04 (с, 1H) 7,57 (д, J=2,37 Гц, 1H) 7,26-7,48 (м, 4H) 7,16-7,26 (м, 1H) 7,00-7,11 (м, 1H) 6,88 (д, J=8,48 Гц, 1H) 6,23-6,33 (м, 1H) 4,51 (с, 2H) 3,55 (с, 3H) 2,94 (с, 3H). MS (ESI+) m/z 445 (M+H)+.
Пример 288
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)пиридин-3-ил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 288a
2-фтор-5-(метилтио)пиридин
Смесь 5-бром-2-фторпиридина (2,05 г, 11,7 ммоль) и N1,N1,N2, N2- тетраметилэтан-1,2-диамина (2,27 мл, 15,1 ммоль) продували азотом в течение 45 минут. Толуол (116 мл) добавляли и реакционную смесь охлаждали до -78°C. N-бутиллитий (2,5 M в гексанах, 5,59 мл, 14,0 ммоль) добавляли по каплям в течение 6 минут. Реакционную смесь перемешивали при -78°C в течение 1 часа. Диметил дисульфид (1,26 мл, 14,0 ммоль) добавляли. Реакционную смесь перемешивали при -78°C в течение 1 часа. Реакционную смесь нагревали до 0°C, затем сразу гасили насыщенным водным раствором хлорида аммония. Слои разделяли и органический слой промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (10% этилацетат/гептан), получая указанное в заголовке соединение (1,00 г, 60%).
Пример 288b
2-фтор-5-(метилсульфонил)пиридин
К раствору продукта примера 288a (2,17 г, 15,2 ммоль) в дихлорметане (50,5 мл) добавляли 3-хлорбензоперокси кислоту (7,15 г, 31,1 ммоль) порциями в течение 10 минут. Реакционную смесь перемешивали при температуре окружающей среды в течение 4 часов. Дополнительную 3-хлорбензоперокси кислоту (2,62 г, 15,16 ммоль) добавляли и реакционную смесь перемешивали при температуре окружающей среды в течение 1 часа. Реакционную смесь гасили насыщенным водным раствором карбоната натрия и слои разделяли. Водный слой экстрагировали дихлорметаном. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 0-10% метанол/дихлорметан), получая указанное в заголовке соединение (1,81 г, 68%).
Пример 288c
5-(метилсульфонил)пиридин-2(1H)-он
Продукт примера 288b (0,679 г, 3,88 ммоль) обрабатывали уксусной кислотой (35,2 мл) и водой (3,52 мл) при 110°C в течение 16 часов. Реакционную смесь охлаждали до температуры окружающей среды и растворитель удаляли, получая указанное в заголовке соединение (0,700 г, 100%).
Пример 288d
3-бром-5-(метилсульфонил)пиридин-2(1H)-он
К раствору продукта примера 288c (0,671 г, 3,87 ммоль) и ацетата натрия (0,318 г, 3,87 ммоль) в уксусной кислоте (8,50 мл) добавляли бром (0,201 мл, 3,91 ммоль) по каплям в виде раствора в уксусной кислоте (1,7 мл). Реакционную смесь перемешивали при 40°C в течение 3 часов. Бром (0,05 мл) добавляли и реакционную смесь перемешивали при 40°C в течение 2 часов. Реакционную смесь охлаждали до температуры окружающей среды и гасили 100 мл 10% водного раствора тиосульфата натрия. Полученную суспензию фильтровали и твердое вещество собирали и сушили в течение 16 часов, получая указанное в заголовке соединение (0,64 г, 66%).
Пример 288e
3-бром-2-хлор-5-(метилсульфонил)пиридин
Продукт примера 288d (0,6395 г, 2,54 ммоль) обрабатывали оксихлоридом фосфoра (12,7 мл) при 110°C в течение 4 часов. Реакционную смесь охлаждали до температуры окружающей среды и выливали на лед. Полученную суспензию фильтровали и промывали водой и несовсем белое твердое вещество собирали и сушили при 60°C в вакуумной печи в течение 16 часов, получая указанное в заголовке соединение (0,244 г, 35%).
Пример 288f
3-бром-2-(2,4-дифторфенокси)-5-(метилсульфонил)пиридин
Продукт примера 288f получали согласно процедуре, используемой для получения продукта примера 2b, заменяя 2,4-дифторфенолом фенол и продуктом примера 288e продукт примера 2a, соответственно, получая указанное в заголовке соединение.
Пример 288g
4-(2-(2,4-дифторфенокси)-5-(метилсульфонил)пиридин-3-ил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 288g получали согласно процедуре, используемой для получения продукта примера 4a, заменяя продуктом примера 288f продукт примера 7c, получая указанное в заголовке соединение.
Пример 288h
4-(2-(2,4-дифторфенокси)-5-(метилсульфонил)пиридин-3-ил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 288h получали согласно процедуре, используемой для получения продукта примера 4b, заменяя продуктом примера 288g продукт примера 4a, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,16 (с, 1H) 8,59 (д, J=2,37 Гц, 1H) 8,37 (д, J=2,37 Гц, 1H) 7,58 (с, 1H) 7,48 (м, 2H) 7,34 (т, J=2,71 Гц, 1H) 7,16 (м, 1H) 6,36 (дд, J=2,71, 2,03 Гц, 1H) 3,61 (с, 3H) 3,35 (с, 3H). MS (ESI+) m/z 432,4 (M+H)+.
Пример 289
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-[(пиридин-3-илокси)метил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 289a
2-(хлорметил)-4-(2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Смесь продукта примера 276 (0,50 г, 1,09 ммоль) и тионил хлорида (5,0 мл, 69 ммоль) нагревали при кипении с возвращением флегмы в течение 2 часов. Растворитель удаляли при пониженном давлении и остаток сушили в вакууме в течение 1 часа, получая указанное в заголовке соединение.
Пример 289b
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-[(пиридин-3-илокси)метил]-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
К раствору пиридин-3-ола (0,039 г, 0,407 ммоль) в тетрагидрофуране (5 мл) добавляли гидрид натрия (16 мг, 0,407 ммоль) при 0°C и смесь перемешивали в течение 30 минут. К этому раствору добавляли продукт примера 289a (0,25 г, O,204 ммоль) и реакционную смесь нагревали при кипении с возвращением флегмы в течение 16 часов. Реакционную смесь выливали в смесь этилацетата (30 мл) и насыщенного водного раствора хлорида натрия (20 мл). Водный слой экстрагировали этилацетатом (20 мл). Объединенные органические слои сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали ВЭЖХ с обращенной фазой (С18, вода (10 мM NH4HCО3):ацетoнитрил, градиент 25-50%), получая указанное в заголовке соединение (18 мг, выход 16%). 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 12,52 (с, 1H), 7,95 (д, J=2,4 Гц, 1H), 7,87 (дд, J=2,4, 6,4 Гц, 1H), 7,56-7,38 (м, 5H), 7,22-7,18 (м, 2H), 6,97 (д, J=8,4 Гц, 1H), 6,84-6,82 (м, 1H), 6,48 (с, 1H), 5,38 (с, 2H), 3,58 (с, 3H), 3,25 (с, 3H), ). MS (ESI+) m/z 538,1 (M+1)+.
Пример 290
4-[5-(циклопропилсульфонил)-2-(2,4-дифторфенокси)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 290a
(3-бром-4-фторфенил)(циклопропил)сульфан
Продукт примера 290a получали согласно процедуре, используемой для получения продукта примера 168a, заменяя бромциклопропаном йодэтан, получая указанное в заголовке соединение.
Пример 290b
2-бром-4-(циклопропилсульфонил)-1-фторбензол
Продукт примера 290b получали согласно процедуре, используемой для получения продукта примера 168b, заменяя продуктом примера 290a продукт примера 168a, получая указанное в заголовке соединение.
Пример 290c
2-бром-4-(циклопропилсульфонил)-1-(2,4-дифторфенокси)бензол
Продукт примера 290c получали согласно процедуре, используемой для получения продукта примера 138b, заменяя продуктом примера 290b продукт примера 138a, получая указанное в заголовке соединение.
Пример 290d
4-[5-(циклопропилсульфонил)-2-(2,4-дифторфенокси)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 290d получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 290c продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,11 (с, 1H), 7,94 (д, J=2,44 Гц, 1H), 7,83 (дд, J=8,54, 2,44 Гц, 1H), 7,42-7,55 (м, 3H), 7,32 (т, J=2,75 Гц, 1H), 7,15-7,20 (м, 1H), 6,97 (д, J=8,54 Гц, 1H), 6,28-6,29 (м, 1H), 3,59 (с, 3H), 2,90-2,96 (м, 1H), 1,12-1,15 (м, 2H), 1,03-1,09 (м, 2H). MS (ESI+) m/z 457,1 (M+H)+.
Пример 291
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-(проп-1-eн-2-ил)-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
К раствору продукта примера 252f (0,10 г, 0,20 ммоль) в тетрагидрофуране (6 мл), перемешиваемому при 0°C, добавляли бромид метилмагния (0,498 мл, 0,498 ммоль). Реакционную смесь перемешивали при 0°C в течение 1 часа и затем добавляли водную HCl (1M, 2 мл). Реакционную смесь концентрировали и распределяли между насыщенным водным раствором хлорида натрия (10 мл) и этилацетатом. Органическую фазу промывали насыщенным водным раствором хлорида натрия (30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток очищали ВЭЖХ с обращенной фазой (C18 40-90% градиент ацетoнитрил:вода (0,1% TFA)), получая указанное в заголовке соединение (25 мг, выход 25%). 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 12,05 (с, 1H), 7,98 (д, J=2,4 Гц, 1H), 7,87 (дд, J=8,7, 2,4 Гц, 1H), 7,61-7,36 (м, 3H), 7,18 (т, J=8,6 Гц, 1H), 6,98 (д, J=8,3 Гц, 1H), 6,34 (д, J=2,2 Гц, 1H), 5,85 (с, 1H), 5,07 (с, 1H), 3,60 (с, 3H), 3,26 (с, 3H), 2,02 (с, 3H). MS (ESI+) m/z 471,1 (M+1)+.
Пример 292
4-[2-(2,4-дифторфенокси)-5-(метилсульфонил)фенил]-6-метил-2-(феноксиметил)-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 292 получали согласно процедуре, используемой для получения продукта примера 289b, заменяя фенолом пиридин-3-ол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 12,32 (с, 1H), 7,96 (д, J=2,4 Гц, 1H), 7,86 (дд, J=2,4, 6,4 Гц, 1H), 7,55-7,50 (м, 1H), 7,49 (с, 1H), 7,45-7,36 (м, 1H), 7,26-7,16 (м, 3H), 6,98-6,89 (м, 4H), 6,37 (с, 1H), 5,11 (с, 2H), 3,59 (с, 3H), 3,23 (с, 3H). MS (ESI+) m/z 537,2 (M+1)+.
Пример 293
4-[2-(2,4-дифторфенокси)-5-(морфолин-4-илсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 293a
4-((3-бром-4-(2,4-дифторфенокси)фенил)сульфонил)морфолин
Продукт примера 293a получали согласно процедуре, используемой для получения продукта примера 138b, заменяя продуктом примера 286a продукт примера 138a, получая указанное в заголовке соединение.
Пример 293b
4-[2-(2,4-дифторфенокси)-5-(морфолин-4-илсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 293b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 293a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,10 (с, 1H), 7,76 (д, J=2,44 Гц, 1H), 7,83 (дд, J=8,7, 2,44 Гц, 1H), 7,42-7,54 (м, 3H), 7,30 (т, J=2,75 Гц, 1H), 7,14-7,16 (м, 1H), 7,01 (д, J=8,54 Гц, 1H), 6,25-6,27 (м, 1H), 3,64-3,66 (м, 4H), 3,59 (с, 3H), 2,88-2,92 (м, 4H). MS (ESI+) m/z 502,2 (M+H)+.
Пример 294
4-[2-(2,4-дифторфенокси)-5-(этилсульфонил)пиридин-3-ил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 294a
3-бром-2-хлор-5-(этилсульфонил)пиридин
Сульфит натрия (1,755 г, 13,92 ммоль) и бикарбонат натрия (1,231 г, 14,65 ммоль) растворяли в воде (37 мл), получая бесцветный раствор. Смесь нагревали при 75°C. 3-Бром-2-хлорпиридин-5-сульфонил хлорид (2,132 г, 7,33 ммоль) добавляли порциями в течение 1 часа. Реакционную смесь перемешивали при 75°C в течение 1 часа. Смесь концентрировали и N,N-диметилформамид (13,88 мл) добавляли. Бикарбонат натрия (1,231 г, 14,65 ммоль) и йодэтан (0,589 мл, 7,33 ммоль) добавляли. Полученную смесь нагревали до 75°C в течение 2 часов и затем охлаждали до температуры окружающей среды. Смесь распределяли между этилацетатом и водой. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 0-100% этилацетат/гептан), получая указанное в заголовке соединение.
Пример 294b
4-(2-хлор-5-(этилсульфонил)пиридин-3-ил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 294b получали согласно процедуре, используемой для получения продукта примера 4a, заменяя продуктом примера 294a продукт примера 7c, получая указанное в заголовке соединение.
Пример 294c
4-(2-(2,4-дифторфенокси)-5-(этилсульфонил)пиридин-3-ил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 294c получали согласно процедуре, используемой для получения продукта примера 2b, заменяя 2,4-дифторфенолом фенол и продуктом примера 294b продукт примера 2a, соответственно, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 12,17 (ушир.с, 1H), 8,56 (д, J=2,4 Гц, 1H), 8,32 (д, J=2,4 Гц, 1H), 7,58 (с, 1H), 7,54-7,43 (м, 2H), 7,34 (т, J=2,7 Гц, 1H), 7,21-7,12 (м, 1H), 6,35 (т, J=2,1 Гц, 1H), 3,61 (с, 3H), 3,44 (кв., J=7,3 Гц, 2H), 1,18 (т, J=7,3 Гц, 1H). MS (ESI+) m/z 446,2 (M+H)+.
Пример 295
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-2-(морфолин-4-ил)этансульфонамид
Пример 295a
4-(5-амино-2-(2,4-дифторфенокси)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 295a получали согласно процедуре, используемой для получения продукта примера 138a, заменяя продуктом примера 1e 2-бром-1-фтор-4-(метилсульфонил)бензол и продуктом примера 148c продукт примера 6a, соответственно, получая указанное в заголовке соединение.
Пример 295b
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-2-(морфолин-4-ил)этансульфонамид
Смесь продукта примера 295a, 2-хлорэтансульфонил хлорида (0,098 г, 0,600 ммоль) и триэтиламина (0,081 г, 0,800 ммоль) в дихлорметане (3 мл) перемешивали при температуре окружающей среды в течение 2 часов. Растворитель удаляли и остаток повторно растворяли в MeOH (5 мл). К этому раствору добавляли морфолин (0,697 г, 8,00 ммоль). Реакционную смесь нагревали при 50°C в течение 2 часов. К этому раствору добавляли 2,0 н. гидроксид натрия (2,00 мл, 4,00 ммоль). Реакционную смесь нагревали при 85°C в течение 2 часов. После охлаждения реакционную смесь распределяли между этилацетатом и 1,0 н. HCl. Водный слой экстрагировали дополнительным этилацетатом несколько раз. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали препаративной ВЭЖХ (10-80% ацетoнитрил в 0,1% TFA вода), получая TFA соль указанного в заголовке соединения (0,077 г, 0,117 ммоль, выход 58,5%). 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,08 (с, 1H), 10,18 (с, 1H), 7,37-7,43 (м, 2H), 7,30-7,31 (м, 2H), 7,22 (дд, J=8,85, 2,75 Гц, 1H), 7,08-7,14 (м, 1H), 7,00-7,04 (м, 1H), 6,91 (д, J=8,54 Гц, 1H), 6,28-6,29 (м, 1H), 3,51-3,62 (м, 11H), 3,24 (ушир. с, 4H). MS (ESI+) m/z 545,1 (M+H)+.
Пример 296
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-N-[2-(диметиламино)этил]этансульфонамид
Смесь продукта примера 36e (0,15 г, 0,326 ммоль), 2-(диметиламино)этанола (0,029 г, 20 0,326 ммоль) и трифенилфосфина (0,128 г, 0,490 ммоль) в тетрагидрофуране (3 мл) перемешивали при температуре окружающей среды в течение 10 минут. К этому раствору добавляли (E)-ди-трет-бутил диазен-1,2-дикарбоксилат (0,113 г, 0,490 ммоль). Раствор перемешивали в течение трех часов при температуре окружающей среды. Растворитель удаляли и остаток очищали препаративной ВЭЖХ (10-80% ацетoнитрил в 0,1% TFA вода), получая указанное в заголовке соединение (0,055 г, 0,104 25 ммоль, выход 31,8%). 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,06 (с, 1H), 7,51 (д, J=2,44 Гц, 1H), 7,41-7,47 (м, 1H), 7,35-7,37 (м, 2H), 7,23-7,31 (м, 2H), 7,06-7,11 (м, 1H), 6,85 (д, J=8,85 Гц, 1H), 3,57 (т, J=6,71 Гц, 2H), 3,56 (с, 3H), 3,17 (кв., J=7,32 Гц, 1H), 2,25 (м, 2H), 2,13 (с, 6H), 1,25 (кв., J=7,48 Гц, 3H). MS (ESI+) m/z 531,2 (M+H)+.
Пример 297
4-{2-(2,4-дифторфенокси)-5-[(этилсульфонил)метил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 297a
(3-бром-4-(2,4-дифторфенокси)бензил)(этил)сульфан
Продукт примера 297a получали согласно процедуре, используемой для получения продукта примера 287d, заменяя этантиолатом натрия тиометоксид натрия, получая указанное в заголовке соединение (1,04 г, 99%).
Пример 297b
2-бром-1-(2,4-дифторфенокси)-4-(этилсульфонилметил)бензол
Продукт примера 297b получали согласно процедуре, используемой для получения продукта примера 287e, заменяя продуктом примера 297a продукт примера 287d, получая указанное в заголовке соединение (1,01 г, 89%).
Пример 297c
4-(2-(2,4-дифторфенокси)-5-(этилсульфонилметил)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 297c получали согласно процедуре, используемой для получения продукта примера 287f, заменяя продуктом примера 297b продукт примера 287e. Очистка флаш-хроматографией (силикагель, 0-2% метанол в дихлорметане) давала указанное в заголовке соединение (63 мг, 51%).
Пример 297d
4-{2-(2,4-дифторфенокси)-5-[(этилсульфонил)метил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 297d получали согласно процедуре, используемой для получения продукта примера 287g, заменяя продуктом примера 297c продукт примера 287f, получая указанное в заголовке соединение (34 мг, 75%). 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,04 (с, 1H) 7,56 (д, J=2,37 Гц, 1H) 7,15-7,48 (м, 5H) 6,99-7,11 (м, 1H) 6,87 (д, J=8,14 Гц, 1H) 6,25-6,35 (м, 1H) 4,49 (с, 2H) 3,55 (с, 3H) 3,07 (кв., J=7,23 Гц, 2H) 1,23 (т, J=7,46 Гц, 3H). MS (ESI+) m/z 459 (M+H)+.
Пример 298
4-{2-(2,4-дифторфенокси)-5-[2-(этилсульфонил)пропан-2-ил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 298a
2-бром-1-(2,4-дифторфенокси)-4-(2-(этилсульфонил)пропан-2-ил)бензол
К раствору продукта примера 297b (469 мг, 1,20 ммоль) в тетрагидрофуране (10 мл) добавляли 60% гидрид натрия в минеральном масле (240 мг, 6,00 ммоль) при 0°C. Реакционную смесь перемешивали при температуре окружающей среды в атмосфере азота в течение 10 минут. Йодметан (0,750 мл, 12,0 ммоль) добавляли. Реакционную смесь перемешивали при температуре окружающей среды в течение 20 часов. Реакционную смесь распределяли между этилацетатом и водой. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили безводным сульфатом натрия, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 20-40% этилацетатом в гептанах), получая указанное в заголовке соединение (442 мг, 88%).
Пример 298b
4-(2-(2,4-дифторфенокси)-5-(2-(этилсульфонил)пропан-2-ил)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 298b получали согласно процедуре, используемой для получения продукта примера 287f, заменяя продуктом примера 298a продукт примера 287e. Очистка флаш-хроматографией (силикагель, 0-2% метанол в дихлорметане) давала указанное в заголовке соединение (80 мг, 62%).
Пример 298c
4-{2-(2,4-дифторфенокси)-5-[2-(этилсульфонил)пропан-2-ил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 298c получали согласно процедуре, используемой для получения продукта примера 287g, заменяя продуктом примера 298b продукт примера 287f, и время реакции было 16 часов вместо 44 часов, получая указанное в заголовке соединение (52 мг, 88%). 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 12,06 (с, 1H) 7,71 (д, J=2,44 Гц, 1H) 7,55 (дд, J=8,70, 2,59 Гц, 1H) 7,38-7,48 (м, 1H) 7,33 (с, 1H) 7,19-7,31 (м, 2H) 7,02-7,12 (м, 1H) 6,85 (д, J=8,24 Гц, 1H) 6,29 (д, J=2,14 Гц, 1H) 3,56 (с, 3H) 2,90 (кв., J=7,43 Гц, 2H) 1,77 (с, 6H) 1,06 (т, J=7,48 Гц, 3H). MS (ESI+) m/z 487 (M+H)+.
Пример 299
4-[2-(2,4-дифторфенокси)-5-(пирролидин-1-илсульфонил)фенил]-6-метил-1,6-дигидро-7Н-пирроло[2,3-c]пиридин-7-он
Пример 299a
1-((3-бром-4-фторфенил)сульфонил)пирролидин
К раствору 3-бром-4-фторбензол-1-сульфонил хлорида (1,0 г, 3,66 ммоль) в 20 мл дихлорметана при 0°C добавляли пирролидин (0,635 мл, 7,68 ммоль). Смесь перемешивали при 0°C в течение 30 минут и затем при комнатной температуре в течение ночи. Реакционную смесь разбавляли дихлорметаном, промывали 1% раствором HCl и водой, сушили над безводным сульфатом магния, фильтровали и концентрировали, получая указанное в заголовке соединение (0,86 г, выход 76%).
Пример 299b
1-((3-бром-4-(2,4-дифторфенокси)фенил)сульфонил)пирролидин
Смесь продукта примера 299a (250 мг, 0,811 ммоль), 2,4-дифторфенола (106 мг, 0,811 ммоль) и карбоната цезия (317 мг, 0,973 ммоль) в 5 мл диметилсульфоксида нагревали при 110°C в течение 2 часов. Воду добавляли и смесь экстрагировали этилацетатом. Органическую фазу промывали водой (2×), насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали, получая указанное в заголовке соединение (278 мг, выход 82%), которое использовали без дополнительной очистки.
Пример 299c
4-[2-(2,4-дифторфенокси)-5-(пирролидин-1-илсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Смесь продукта примера 299b (100 мг, 0,239 ммоль), продукта примера 6a (102 мг, 0,239 ммоль), тетракис(трифенилфосфин)палладия(0) (13,81 мг, 0,012 ммоль) и фторида цезия (109 мг, 0,717 ммоль) в 2 мл диметоксиэтана и 1 мл метанола нагревали при 120°C в микроволновой печи (Biotage Initiator) в течение 40 минут. Смесь затем обрабатывали 4 н. NaOH (1 мл) и перемешивали при температуре окружающей среды в течение 2 часов. Воду добавляли и смесь экстрагировали этилацетатом (2×). Органическую фазу промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, и фильтровали. Фильтрат концентрировали и остаток очищали флаш-хроматографией (силикагель, градиент 60-100% этилацетат/гептаны), получая указанное в заголовке соединение (75 мг, 64,6% выход). 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 12,06 (с, 1H), 12,06 (с, 1H), 7,81 (д, J=2,4 Гц, 1H), 7,81 (д, J=2,4 Гц, 1H), 7,77-7,72 (м, 1H), 7,79-7,72 (м, 1H), 7,47 (ддд, J=11,5, 8,8, 3,0 Гц, 1H), 7,47 (ддд, J=17,8, 10,4, 6,0 Гц, 1H), 7,42-7,39 (м, 1H), 7,43-7,35 (м, 2H), 7,30 (т, J=2,8 Гц, 1H), 7,30 (т, J=2,8 Гц, 1H), 7,28-7,09 (м, 1H), 7,17-7,09 (м, 1H), 6,98-6,93 (м, 1H), 6,99-6,93 (м, 1H), 6,24 (ддд, J=23,2, 2,6, 2,2 Гц, 1H), 6,22 (дд, J=2,6, 2,2 Гц, 1H), 3,57 (с, 3H), 3,57 (с, 3H), 3,22-3,09 (м, 4H), 3,19-3,11 (м, 4H), 1,72-1,64 (м, 4H), 1,75-1,61 (м, 4H), 1,17 (дд, J=18,8, 11,7 Гц, 1H), 0,87-0,74 (м, 1H). MS (ESI+) m/z 464,2 (M+H)+.
Пример 300
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-2-(диметиламино)этансульфонамид
Продукт примера 300 получали согласно процедуре, используемой для получения продукта примера 295b, заменяя N,N-диметиламином морфолин, получая TFA соль указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,07 (с, 1H), 10,18 (с, 1H), 9,86 (ушир. с, 1H), 7,37-7,42 (м, 2H), 7,29-7,31 (м, 2H), 7,22 (дд, J=8,54, 2,75 Гц, 1H), 7,09-7,14 (м, 1H), 7,01-7,07 (м, 1H), 6,91 (д, J=8,85 Гц, 1H), 6,28 (т, J=2,29 Гц, 1H), 3,62-3,65 (м, 2H), 3,54 (с, 3H), 3,48-3,51 (м, 2H), 2,83 (с, 6H). MS (ESI+) m/z 503,1 (M+H)+.
Пример 301
Этил 4-[4-(этилсульфонил)-2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенокси]пиперидин-1-карбоксилат
Пример 301a
Этил 4-(2-бром-4-(этилсульфонил)фенокси)пиперидин-1-карбоксилат
Продукт примера 301a получали согласно процедуре, используемой для получения продукта примера 158, заменяя продуктом примера 138a продукт примера 168b и этил 4-гидроксипиперидин-1-карбоксилатом циклопропилметанол, соответственно, получая указанное в заголовке соединение.
Пример 301b
Этил 4-[4-(этилсульфонил)-2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенокси]пиперидин-1-карбоксилат
Продукт примера 301b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 301a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,04 (с, 1H), 7,80-7,83 (м, 2H), 7,44 (д, J=8,54 Гц, 1H), 7,33 (с, 1H), 7,29 (т, J=2,75 Гц, 1H), 6,12-6,13 (м, 1H), 4,76-4,81 (м, 1H), 3,99 (кв., J=7,02 Гц, 2H), 3,57 (с, 3H), 3,24-3,39 (м, 6H), 1,86-1,90 (м, 2H), 1,49-1,53 (м, 2H), 1,12-1,16 (М, 6H). MS (ESI+) m/z 488,1 (M+H)+.
Пример 302
4-[2-(циклопропилметокси)-5-(пирролидин-1-илсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 302a
1-((3-бром-4-(циклопропилметокси)фенил)сульфонил)пирролидин
К раствору циклопропилметанола (115 мкл, 1,460 ммоль) в диоксане (8 мл) при комнатной температуре добавляли гидрид натрия (78 мг, 1,947 ммоль). После перемешивания при температуре окружающей среды в течение 10 минут продукт примера 299a (300 мг, 0,973 ммоль) добавляли как твердое вещество. Смесь затем нагревали при 65°C в течение ночи. Воду добавляли. Смесь экстрагировали этилацетатом, промывали водой (2×), насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, градиент 0-50% этилацетат/гептаны), получая указанное в заголовке соединение (156 мг, выход 44,5%)
Пример 302b
4-[2-(циклопропилметокси)-5-(пирролидин-1-илсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Смесь продукта примера 302a (84 мг, 0,233 ммоль), продукта примера 6a (100 мг, 0,233 ммоль), тетракис(трифенилфосфин)палладия(0) (13,49 мг, 0,012 ммоль) и фторида цезия (106 мг, 0,700 ммоль) в 2 мл диметоксиэтана и 1 мл метанола продували азотом и нагревали при 130°C микроволновым излучением (Biotage Initiator) в течение 40 минут. Смесь затем обрабатывали 4 н. NaOH (1 мл) и перемешивали при комнатной температуре в течение 2 часов. Воду добавляли и смесь экстрагировали этилацетатом, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток абсорбировали на силикагеле и очищали флаш-хроматографией (силикагель, градиент 0-10% метанол/дихлорметан), получая указанное в заголовке соединение (64 мг, выход 64,1%). 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 12,10-11,92 (м, 1H), 7,77-7,70 (м, 2H), 7,37 (с, 1H), 7,30 (дд, J=6,9, 4,1 Гц, 2H), 6,17-6,03 (м, 1H), 3,97 (д, J=6,8 Гц, 2H), 3,58 (с, 3H), 3,14 (т, J=6,7 Гц, 4H), 1,71-1,64 (м, 4H), 1,15-1,08 (м, 1H), 0,50-0,44 (м, 2H), 0,30-0,24 (м, 2H). MS (ESI+) m/z 482,2 (M+H)+.
Пример 303
4-{2-[(1-ацетилпиперидин-4-ил)окси]-5-(этилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 303a
1-(4-(2-бром-4-(этилсульфонил)фенокси)пиперидин-1-ил)этанон
Продукт примера 303a получали согласно процедуре, используемой для получения продукта примера 158, заменяя продуктом примера 168b продукт примера 138a и заменяя 1-(4-гидроксипиперидин-1-ил)этаноном циклопропилметанол, соответственно, получая указанное в заголовке соединение.
Пример 303b
4-{2-[(1-ацетилпиперидин-4-ил)окси]-5-(этилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 303b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 303a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,04 (с, 1H), 7,80-7,84 (м, 2H), 7,45 (д, J=8,54 Гц, 1H), 7,33 (с, 1H), 7,29 (т, J=2,75 Гц, 1H), 6,12-6,13 (м, 1H), 4,81-4,84 (м, 1H), 3,57 (с, 3H), 3,24-3,39 (м, 6H), 2,09 (с, 3H), 1,49-1,53 (м, 2H), 1,12-1,16 (м, 3H). MS (ESI+) m/z 458,2 (M+H)+.
Пример 304
4-[4-(этилсульфонил)-2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенокси]бензонитрил
Продукт примера 304 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя продуктом примера 168c продукт примера 138a и 4-цианофенолом 2,4-дифторфенол, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,09 (с, 1H), 8,00 (д, J=2,44 Гц, 1H), 7,92 (дд, J=8,54, 2,54 Гц, 1H), 7,79-7,82 (м, 2H), 7,39 (с, 1H), 7,35 (д, J=8,54 Гц, 1H), 7,29 (т, J=2,75 Гц, 1H), 7,14-7,17 (м, 2H), 6,22-6,23 (м, 1H), 3,54 (с, 3H), 3,38 (кв., J=7,32 Гц, 2H), 1,17 (т, J=7,32 Гц, 3H). MS (ESI+) m/z 434,2 (M+H)+.
Пример 305
4-[2-(циклопропилметокси)-5-(2,3-дигидро-1H-индол-1-илсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 305a
1-(3-бром-4-фторфенилсульфонил)индолин
Раствор 3-бром-4-фторбензол-1-сульфонил хлорида (Aldrich) (2,53 г, 8,33 ммоль), индолина (0,99 г, 8,33 ммоль), N,N-диизопропилэтиламина (1,60 мл, 9,16 ммоль) и тетрагидрофурана (20 мл) перемешивали при температуре окружающей среды в течение 16 часов. Реакционную смесь распределяли между водой и этилацетатом. Водный слой экстрагировали дважды дополнительным этилацетатом. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали, получая коричневое масло, которое затвердевало при стоянии. Сырой продукт перекристаллизовывали из смеси простой эфир/гептан, получая указанное в заголовке соединение (1,99 г, 5,59 ммоль, выход 67%).
Пример 305b
1-(3-бром-4-(циклопропилметокси)фенилсульфонил)индолин
Продукт примера 305b получали согласно процедуре, используемой для получения продукта примера 29a, заменяя циклопропилметанолом тетрагидро-2H-пиран-4-ол и заменяя продуктом примера 305a продукт примера 2a, получая указанное в заголовке соединение.
Пример 305c
4-(2-(циклопропилметокси)-5-(индолин-1-илсульфонил)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 305c получали согласно процедуре, используемой для получения продукта примера 6c, заменяя продуктом примера 305b продукт примера 6b, получая указанное в заголовке соединение.
Пример 305d
4-(2-(циклопропилметокси)-5-(индолин-1-илсульфонил)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 305d получали согласно процедуре, используемой для получения продукта примера 6d, заменяя продуктом примера 305c продукт примера 6c, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 0,24 (тт, J=13,4, 6,6 Гц, 2H) 0,35-0,50 (м, 2H) 1,01-1,18 (м, 1H) 2,90 (т, J=8,3 Гц, 2H) 3,54 (с, 3H) 3,90 (т, J=8,4 Гц, 2H) 3,92 (д, J=6,8 Гц, 2H) 5,80-5,86 (м, 1H) 7,04 (тд, J=7,4, 1,0 Гц, 1H) 7,14-7,36 (м, 5H) 7,50 (д, J=8,0 Гц, 1H) 7,66 (д, J=2,4 Гц, 1H) 7,77 (дд, J=8,7, 2,5 Гц, 1H) 12,02 (ушир.с, 1H). MS (ESI+) m/z 476 [M+H]+.
Пример 306
4-{2-(2,4-дифторфенокси)-5-[(фенилсульфонил)метил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 306a
(3-бром-4-(2,4-дифторфенокси)бензил)(фенил)сульфан
Продукт примера 306a получали согласно процедуре, используемой для получения продукта примера 287d, заменяя тиофеноксидом натрия тиометоксид натрия, получая указанное в заголовке соединение (815 мг, 100%).
Пример 306b
2-бром-1-(2,4-дифторфенокси)-4-(фенилсульфонилметил)бензол
Продукт примера 306b получали согласно процедуре, используемой для получения продукта примера 287e, заменяя продуктом примера 306a продукт примера 287d, получая указанное в заголовке соединение (867 мг, 99%).
Пример 306c
4-(2-(2,4-дифторфенокси)-5-(фенилсульфонилметил)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 306c получали согласно процедуре, используемой для получения продукта примера 287f, заменяя продуктом примера 306b продукт примера 287e. Очистка флаш-хроматографией (силикагель, 0-2% метанол в дихлорметане) давала указанное в заголовке соединение (51 мг, 52%).
Пример 306d
4-{2-(2,4-дифторфенокси)-5-[(фенилсульфонил)метил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 306d получали согласно процедуре, используемой для получения продукта примера 287g, заменяя продуктом примера 306c продукт примера 287f, получая указанное в заголовке соединение (30 мг, 80%). 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,02 (с, 1H) 7,69-7,81 (м, 3H) 7,55-7,67 (м, 2H) 7,34-7,46 (м, 1H) 7,20-7,29 (м, 2H) 6,98-7,18 (м, 4H) 6,80 (д, J=8,48 Гц, 1H) 6,09 (дд, J=2,37, 1,70 Гц, 1H) 4,71 (с, 2H) 3,52 (с, 3H). MS (ESI+) m/z 507 (M+H)+.
Пример 307
4-{2-[(2,2-дифторциклопропил)метокси]-5-(пирролидин-1-илсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 307a
1-((3-бром-4-((2,2-дифторциклопропил)метокси)фенил)сульфонил)пирролидин
Продукт примера 307a получали согласно процедуре, используемой для получения продукта примера 302a, заменяя (2,2-дифторциклопропил)метанолом циклопропилметанол, получая указанное в заголовке соединение.
Пример 307b
4-{2-[(2,2-дифторциклопропил)метокси]-5-(пирролидин-1-илсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 307b получали согласно процедуре, используемой для получения продукта примера 302b, заменяя продуктом 307a продукт 302a, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,05 (с, 1H), 12,05 (с, 1H), 7,76 (тт, J=6,9, 3,5 Гц, 2H), 7,81-7,71 (м, 2H), 7,35 (д, J=8,4 Гц, 2H), 7,38-7,27 (м, 3H), 7,30 (т, J=2,6 Гц, 1H), 6,12 (дд, J=2,5, 1,6 Гц, 1H), 6,12 (дд, J=2,5, 1,6 Гц, 1H), 4,21 (дт, J=18,8, 9,6 Гц, 2H), 3,57 (с, 3H), 3,57 (с, 3H), 3,15 (т, J=6,7 Гц, 4H), 3,15 (т, J=6,7 Гц, 4H), 2,21-2,04 (м, 1H), 2,19-1,98 (м, 1H), 1,74-1,57 (м, 5H), 1,77-1,57 (м, 5H), 1,52-1,36 (м, 1H), 1,53-1,38 (м, 1H). MS (ESI+) m/z 464,2 (M+H)+.
Пример 308
4-{2-(циклопропилметокси)-5-[(3,3-дифторазетидин-1-ил)сульфонил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 308a
1-((3-бром-4-фторфенил)сульфонил)-3,3-дифторазетидин
К суспензии 3,3-дифторазетидин хлороводородной кислоты (0,947 г, 7,31 ммоль) в 20 мл дихлорметана при 0°C добавляли N-этил-N-изопропилпропан-2-амин (2,80 мл, 16,1 ммоль) с последующим добавлением раствора 3-бром-4-фторбензол-1-сульфонил хлорида (2,0 г, 7,3 ммоль) в 4 мл дихлорметана. Смесь перемешивали при комнатной температуре в течение ночи и затем нагревали при 55°C в течение 5 часов, разбавляли дихлорметаном, промывали водой, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали и остаток очищали флаш-хроматографией (силикагель, градиент 10-50% этилацетат/гептаны), получая указанное в заголовке соединение (1,5 г, выход 62,1%).
Пример 308b
1-((3-бром-4-(циклопропилметокси)фенил)сульфонил)-3,3-дифторазетидин
Продукт примера 308b получали согласно процедуре, используемой для получения продукта примера 302a, заменяя продуктом примера 308a продукт примера 299a, получая указанное в заголовке соединение.
Пример 308c
4-{2-(циклопропилметокси)-5-[(3,3-дифторазетидин-1-ил)сульфонил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-с]пиридин-7-он
Продукт примера 308c получали согласно процедуре, используемой для получения продукта примера 302b, заменяя продуктом примера 308b продукт примера 302a, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 12,04 (с, 1H), 7,87 (дд, J=8,7, 2,4 Гц, 1H), 7,78 (д, J=2,4 Гц, 1H), 7,40 (с, 1H), 7,36 (д, J=8,8 Гц, 1H), 7,29 (т, J=2,7 Гц, 1H), 6,12-6,08 (м, 1H), 4,26 (т, J=12,7 Гц, 4H), 4,01 (д, J=6,8 Гц, 2H), 3,58 (с, 3H), 1,14-1,08 (м, 1H), 0,50-0,43 (м, 2H), 0,30-0,25 (м, 2H), MS (DCI+) m/z 491,4 (M+CH3CN)+.
Пример 309
4-{2-[2-(2-гидроксиэтил)фенокси]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 304 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 2-(2-гидроксиэтил)фенолом 2,4-дифторфенол, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,11 (с, 1H), 8,00 (д, J=2,44 Гц, 1H), 7,85 (дд, J=8,85, 2,44 Гц, 1H), 7,45 (с, 1H), 7,36 (дд, J=7,63, 1,53 Гц, 1H), 7,32 (т, J=2,9 Гц, 1H), 7,24-7,28 (м, 1H), 7,14-7,18 (м, 1H), 6,98-7,01 (м, 1H), 6,89 (д, J=8,54 Гц,1H), 6,29-6,31 (м, 1H), 3,57 (с, 3H), 3,46 (т, J=7,02 Гц, 2H), 3,25 (с, 3H), 2,63 (т, J=7,02 Гц, 2H). MS (ESI+) m/z 439,1 (M+H)+.
Пример 310
4-[2-(циклопропилметокси)-5-{[3-(диметиламино)пирролидин-1-ил]сульфонил}фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 310a
1-(3-бром-4-фторфенилсульфонил)-N,N-диметилпирролидин-3-амин
Раствор 3-бром-4-фторбензол-1-сульфонил хлорида (Combi-blocks) (250 мг, 0,91 ммоль), N,N-диметилпирролидин-3-амина (218 мгg, 1,9 ммоль) в тетрагидрофуране (5,7 мл) перемешивали при температуре окружающей среды в течение 16 часов. Растворитель выпаривали и остаток очищали флаш-хроматографией (силикагель, дихлорметан/градиент с MeOH), получая указанное в заголовке соединение (220 мг, выход 69%).
Пример 310b
1-(3-бром-4-(циклопропилметокси)фенилсульфонил-N,N-диметил-3-амин
Продукт примера 310b получали согласно процедуре, используемой для получения продукта примера 29a, заменяя циклопропилметанолом тетрагидро-2H-пиран-4-ол и заменяя продуктом примера 310a продукт примера 2a, получая указанное в заголовке соединение.
Пример 310c
4-(2-(циклопропилметокси)-5-(3-(диметиламино)пирролидин-1-илсульфонил)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 310c получали согласно процедуре, используемой для получения продукта примера 6c, заменяя продуктом примера 310b продукт примера 6b, получая указанное в заголовке соединение.
Пример 310d
4-(2-(циклопропилметокси)-5-(3-(диметиламино)пирролидин-1-илсульфонил)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 310d получали согласно процедуре, используемой для получения продукта примера 6d, заменяя продуктом примера 310c продукт примера 6c, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 0,25-0,31 (м, 2H) 0,44-0,51 (м, 2H) 1,06-1,17 (м, 1H) 1,45-1,59 (м, 1H) 1,86-1,97 (м, 1H) 2,04 (с, 6H) 2,52-2,57 (м, 1H) 2,82-2,90 (м, 1H) 3,07-3,18 (м, 1H) 3,25-3,28 (м, 1H) 3,34-3,42 (м, 1H) 3,57 (с, 3H) 3,98 (д, J=6,78 Гц, 2H) 6,12 (т, J=2,71, 2,03 Гц, 1H) 7,28-7,33 (м, 2H) 7,35 (с, 1H) 7,71-7,79 (м, 2H) 12,04 (с, 1H). MS (ESI+) m/z 471 [M+H]+.
Пример 311
4-{2-(2,4-дифторфенокси)-5-[(метилсульфонил)метил]пиридин-3-ил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 311a
5-бром-6-(2,4-дифторфенокси)никотиновая кислота
5-бром-6-хлорникотиновую кислоту (3 г, 12,69 ммоль), 2,4-дифторфенол (3,30 г, 25,4 ммоль) и карбонат цезия (16,54 г, 50,8 ммоль) объединяли в DMSO (25,4 мл), нагревали при 100°C в течение 6 часов, охлаждали, разбавляли 150 мл воды со льдом и pH доводили до pH 3 с использованием 12M HCl. Полученное твердое вещество собирали фильтрованием, промывали холодной водой и сушили до постоянной массы, получая указанное в заголовке соединение (2,84 г, 64%).
Пример 311b
(5-бром-6-(2,4-дифторфенокси)пиридин-3-ил)метанол
Продукт примера 311a (1,0 г, 3,03 ммоль) и комплекс боран тетрагидрофуран (6,06 мл, 6,06 ммоль) объединяли в тетрагидрофуране (15,15 мл) и нагревали при 50°C в течение 2 часов, охлаждали, обрабатывали 10 мл метанола, нагревали при 50°C в течение 1 часа, охлаждали и концентрировали. Остаток распределяли между этилацетатом и водой. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили (Na2SО4), фильтровали и концентрировали. Очистка хроматографией (силикагель, 0-50% этилацетат в гептанах) давала указанное в заголовке соединение (0,73 г, 76%).
Пример 311c
3-бром-5-(бромметил)-2-(2,4-дифторфенокси)пиридин
Раствор продукта примера 311b (0,73 г, 2,309 ммоль) в дихлорметане (11,55 мл) в атмосфере азота обрабатывали по каплям трибромфосфином (0,218 мл, 2,309 ммоль), перемешивали в течение одного часа при температуре окружающей среды и выливали в воду со льдом и pH доводили до pH 9 добавлением твердого бикарбоната натрия порциями. Образовывалась эмульсия, которую частично удаляли фильтрованием. Водный слой экстрагировали дихлорметаном и органические фракции объединяли, промывали насыщенным водным раствором хлорида натрия, сушили (Na2SО4) фильтровали и концентрировали, получая указанное в заголовке соединение (0,75 г, 86%).
Пример 311d
3-бром-2-(2,4-дифторфенокси)-5-(метилтиометил)пиридин
Продукт примера 311c (0,75 г, 1,979 ммоль) и тиометоксид натрия (0,139 г, 1,979 ммоль) объединяли в диметилформамиде (3,96 мл), перемешивали в течение 4 часов при температуре окружающей среды и распределяли в этилацетате и холодной воде. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили (Na2SО4), фильтровали и концентрировали, получая указанное в заголовке соединение (0,66 г, 96%).
Пример 311e
3-бром-2-(2,4-дифторфенокси)-5-(метилсульфонилметил)пиридин
Раствор продукта примера 311d (0,66 г, 1,906 ммоль) при 0°C в метаноле (7,33 мл) обрабатывали раствором оксона (2,461 г, 4,00 ммоль) в воде (7,33 мл), перемешивали при температуре окружающей среды в течение двух часов и распределяли между этилацетатом и водой. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили (Na2SО4), фильтровали и концентрировали. Очистка хроматографией (силикагель, 0-5% метанол в дихлорметане) давала указанное в заголовке соединение (0,433 г, 60%).
Пример 311f
4-(2-(2,4-дифторфенокси)-5-((метилсульфонил)метил)пиридин-3-ил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 311e (0,075 г, 0,198 ммоль), продукт примера 6a (0,085 г, 0,198 ммоль), трис(дибензилиденацетон)дипалладий(0) (5,45 мг, 5,95 мкмоль), 1,3,5,7-тетраметил-6-фенил-2,4,8-триокса-6-фосфаадамант (5,80 мг, 0,020 ммоль) и фосфат калия (0,126 г, 0,595 ммоль) объединяли и продували аргоном в течение 15 минут. Тем временем раствор 4:1 диоксан/вода (2 мл) продували азотом в течение 15 минут и переносили шприцем в реакционный сосуд в атмосфере аргона. Смесь перемешивали в течение 2 часов при 60°C и распределяли между этилацетатом и водой. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили (Na2SО4), обрабатывали силикагелем, функционализованным 3-меркаптопропилом, фильтровали и концентрировали. Очистка растиранием в порошок в дихлорметане давала указанное в заголовке соединение (0,083 г, 70%).
Пример 311g
4-{2-(2,4-дифторфенокси)-5-[(метилсульфонил)метил]пиридин-3-ил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 311f (0,083 г, 0,138 ммоль), гидроксид калия (0,194 г, 3,46 ммоль) и бромид N,N,N-триметилгексадекан-1-аминия (2,52 мг, 6,92 мкмоль) объединяли в диоксане (1,8 мл) /воде (0,9 мл) и нагревали при 100°C в течение 4 часов, охлаждали и распределяли в этилацетате, доводя pH до 7 с помощью 1 M HCl. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили (Na2SO4), фильтровали и концентрировали. Очистка хроматографией (силикагель, 0-4% метанол в дихлорметане) давала указанное в заголовке соединение (0,035 г, 57%). 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 12,14 (с, 1H) 8,03 (дд, J=22,74, 2,29 Гц, 2H) 7,30-7,51 (м, 4H) 7,03-7,17 (м, 1H) 6,39 (д, J=2,14 Гц, 1H) 4,57 (с, 2H) 3,60 (с, 3H) 3,00 (с, 3H). MS (ESI+) m/z 446 [M+H]+.
Пример 312
трет-бутил 4-[4-(этилсульфонил)-2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенокси]пиперидин-1-карбоксилат
Пример 312a
трет-бутил 4-(2-бром-4-(этилсульфонил)фенокси)пиперидин-1-карбоксилат
Продукт примера 312a получали согласно процедуре, используемой для получения продукта примера 158, заменяя продуктом примера 168b продукт примера 138a и трет-бутил 4-гидроксипиперидин-1-карбоксилатом циклопропилметанол, соответственно, получая указанное в заголовке соединение.
Пример 312b
трет-бутил 4-[4-(этилсульфонил)-2-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенокси]пиперидин-1-карбоксилат
Продукт примера 312b получали согласно процедуре, используемой для получения продукта примера 95d, заменяя продуктом примера 312a продукт примера 95c, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,02 (с, 1H), 7,79-7,842 (м, 2H), 7,42 (д, J=8,54 Гц, 1H), 7,31 (с, 1H), 7,27 (т, J=2,75 Гц, 1H), 6,10-6,11 (м, 1H), 4,74-4,78 (м, 1H), 3,55 (с, 3H), 3,14-3,32 (м, 6H), 1,82-1,87 (м, 2H), 1,43-1,51 (м, 2H), 1,35 (с, 9H), 1,12 (т, J=7,32 Гц, 3H). MS (ESI+) m/z 515,9 (M+H)+.
Пример 313
4-(циклопропилметокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-фенилбензолсульфонамид
Пример 313a
3-бром-4-фтор-N-фенилбензолсульфонамид
Продукт примера 313a получали согласно процедуре, используемой для получения продукта примера 305a, заменяя анилином индолин. Сырой продукт очищали флаш-хроматографией (силикагель, элюировали 10% этилацетатом в гептане), получая указанное в заголовке соединение.
Пример 313b
3-бром-4-(циклопропилметокси)-N-фенилбензолсульфонамид
Продукт примера 313b получали согласно процедуре, используемой для получения продукта примера 29a, заменяя циклопропилметанолом тетрагидро-2H-пиран-4-ол и заменяя продуктом примера 313a продукт примера 2a, получая указанное в заголовке соединение.
Пример 313c
4-(циклопропилметокси)-3-(6-метил-7-оксо-1-тозил-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-фенилбензолсульфонамид
Продукт примера 313c получали согласно процедуре, используемой для получения продукта примера 6c, заменяя продуктом примера 313b продукт примера 6b, получая указанное в заголовке соединение.
Пример 313d
4-(циклопропилметокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-фенилбензолсульфонамид
Продукт примера 313d получали согласно процедуре, используемой для получения продукта примера 6d, заменяя продуктом примера 313c продукт примера 6c, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 0,25 (тт, J=15,6, 7,6 Гц, 2H) 0,39-0,50 (м, 2H) 1,01-1,18 (м, 1H) 3,55 (с, 3H) 3,91 (д, J=6,8 Гц, 2H) 5,91 (дд, J=2,8, 2,0 Гц, 1H) 7,01-7,15 (м, 3H) 7,15-7,34 (м, 5H) 7,65-7,72 (м, 2H) 10,12 (с, 1H) 12,02 (ушир.с, 1H). MS (ESI+) m/z 450 [M+H]+.
Пример 314
4-[2-(циклопропилметокси)-5-(пирролидин-1-илметил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 314a
4-бром-1-(циклопропилметокси)-2-йодбензол
Смесь 4-бром-2-йодфенола (5,00 г, 16,7 ммоль), бромметилциклопропана (2,26 г, 16,7 ммоль) и карбоната цезия (6,54 г, 20,1 ммоль) в 15 мл диметилформамида перемешивали при 50°C в течение ночи. Воду добавляли и смесь экстрагировали этилацетатом. Органическую фазу промывали водой, насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали, получая указанное в заголовке соединение (5,84 г, выход 99%).
Пример 314b
4-(5-бром-2-(циклопропилметокси)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Смесь продукта примера 6a (1,1 г, 2,57 ммоль), продукта примера 314a (0,907 г, 2,57 ммоль), 1,3,5,7-тетраметил-6-фенил-2,4,8-триокса-6-фосфaадамантана (0,060 г, 0,21 ммоль), трис(дибензилиденацетон)дипалладия(0) (0,094 г, 0,103 ммоль) и фосфата калия (1,635 г, 7,70 ммоль) в 15 мл диоксана и 5 мл воды продували азотом и затем нагревали при 55°C в течение 3 часов. Насыщенный водный раствор хлорида натрия добавляли и смесь экстрагировали этилацетатом (2×). Объединенные органические фазы сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, градиент 0-80% этилацетат/гептаны), получая указанное в заголовке соединение (1,24 г, выход 92%).
Пример 314c
4-[2-(циклопропилметокси)-5-(пирролидин-1-илметил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Смесь продукта примера 314b (100 мг, 0,190 ммоль), трифтор(пирролидин-1-илметил)бората калия (36,2 мг, 0,190 ммоль), ацетата палладия(II) (2,55 мг, 0,011 ммоль), дициклогексил(2',4',6'-триизопропилбифенил-2-ил)фосфина (10,85 мг, 0,023 ммоль) и карбоната цезия (185 мг, 0,569 ммоль) в 4 мл смеси диоксан/вода (9:1) продували азотом и затем нагревали микроволновым излучением (Biotage Initiator) при 140°C в течение 40 минут. Реакционную смесь затем обрабатывали 2 мл 4 н. NaOH и нагревали в микроволновой печи (Biotage Initiator) при 100°C в течение 30 минут. Воду добавляли. Смесь экстрагировали этилацетатом, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали и остаток очищали флаш-хроматографией (силикагель, градиент 2-14% метанол/дихлорметан), получая указанное в заголовке соединение (8,0 мг, выход 11%). 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 11,93 (с, 1H), 7,29-7,17 (м, 4H), 7,00 (д, J=8,4 Гц, 1H), 6,11 (дд, J=2,6, 2,2 Гц, 1H), 3,81 (д, J=6,7 Гц, 2H), 3,56 (с, 3H), 3,53 (с, 2H), 2,43 (с, 4H), 1,68 (с, 4H), 1,13-0,98 (м, 1H), 0,48-0,36 (м, 2H), 0,26-0,16 (м, 2H). MS (ESI+) m/z 378,0 (M+H)+.
Пример 315
4-[2-(циклопропилметокси)-5-(пиридин-3-ил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Суспензию продукта примера 314b (100 мг, 0,190 ммоль), пиридин-3-илбороновой кислоты (23,31 мг, 0,190 ммоль), карбоната натрия (60,3 мг, 0,569 ммоль) и трис(дибензилиденацетон)-дипалладия(0) (15,48 мг, 0,019 ммоль) в 4 мл смеси диоксан-вода (3:1) нагревали в атмосфере азота микроволновым излучением (Biotage Initiator) при 120°C в течение 30 минут. Реакционную смесь обрабатывали 1 мл водного 4 н. раствора NaOH и нагревали при 120°C микроволновым излучением снова в течение 30 минут. Смесь разбавляли водой и экстрагировали этилацетатом (2×), промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали и остаток очищали флаш-хроматографией (силикагель, градиент 0-10% метанол/дихлорметан), получая указанное в заголовке соединение (53 мг, выход 75%). 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 11,95 (с, 1H), 8,90 (дд, J=2,4, 0,7 Гц, 1H), 8,56-8,49 (м, 1H), 8,07 (ддд, J=8,0, 2,4, 1,7 Гц, 1H), 7,71-7,64 (м, 2H), 7,45 (ддд, J=7,9, 4,8, 0,8 Гц, 1H), 7,34 (с, 1H), 7,26 (т, J=2,7 Гц, 1H), 7,21 (д, J=8,5 Гц, 1H), 6,18 (дд, J=2,6, 2,2 Гц, 1H), 3,91 (д, J=6,7 Гц, 2H), 3,58 (с, 3H), 1,15-1,04 (м, 1H), 0,49-0,42 (м, 2H), 0,28-0,21 (м, 2H). MS (ESI+) m/z 372,2 (M+H)+.
Пример 316
4-[2-(циклопропилметокси)-5-(морфолин-4-илметил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 316 получали согласно процедуре, используемой для получения продукта примера 314c, заменяя трифтор(морфолинoметил)боратом калия трифтор(пирролидин-1-илметил)борат калия, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,01 (с, 1H), 7,50 (д, J=1,9 Гц, 1H), 7,43 (д, J=8,4 Гц, 1H), 7,28 (дд, J=4,9, 2,0 Гц, 2H), 7,18 (д, J=8,5 Гц, 1H), 6,21-6,14 (м, 1H), 4,32 (с, 2H), 3,97 (д, J=12,4 Гц, 2H), 3,89 (д, J=6,7 Гц, 2H), 3,63 (д, J=11,7 Гц, 2H), 3,57 (с, 3H), 3,29 (д, J=12,8 Гц, 2H), 3,10 (д, J=10,4 Гц, 2H), 1,17-1,02 (м, 1H), 0,51-0,42 (м, 2H), 0,28-0,21 (м, 2H), ). MS (ESI+) m/z 394,0 (M+H)+.
Пример 317
4-{5-(этилсульфонил)-2-[3-(гидроксиметил)фенокси]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 317 получали согласно процедуре, используемой для получения продукта примера 138b, заменяя 3-(гидроксиметил)фенолом 2,4-дифторфенол и продуктом примера 168c продукт примера 138a, соответственно, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ 12,07 (с, 1H), 7,93 (д, J=2,44 Гц, 1H), 7,83 (дд, J=8,7, 2,29 Гц, 1H), 7,42 (с, 1H), 7,35 (т, J=7,93 Гц, 1H), 7,30 (т, J=2,75 Гц, 1H), 7,15 (д, J=7,63 Гц, 1H), 7,02-7,05 (м, 2H), 6,97 (дд, J=7,93, 2,14 Гц, 1H), 6,26 (т, J=2,44 Гц, 1H), 4,48 (с, 2H), 3,57 (с, 3H), 3,34 (кв., J=7,32 Гц, 2H), 1,15 (т, J=7,32 Гц, 3H). MS (ESI+) m/z 439,0 (M+H)+.
Пример 318
4-[2-(циклопропилметокси)-5-(1-метил-1H-пиразол-4-ил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 318 получали согласно процедуре, используемой для получения продукта примера 315, заменяя 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиразолом пиридин-3-илбороновую кислоту, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 11,93 (с, 1H), 8,05 (д, J=7,4 Гц, 1H), 7,77 (дд, J=6,3, 0,6 Гц, 1H), 7,48 (кв., J=2,2 Гц, 2H), 7,28-7,24 (м, 2H), 7,06 (д, J=8,3 Гц, 1H), 6,21-6,05 (м, 1H), 3,83 (д, J=4,9 Гц, 5H), 3,56 (д, J=5,7 Гц, 3H), 1,06-1,02 (м, 1H), 0,46-0,40 (м, 2H), 0,24-0,19 (м, 2H), ). MS (ESI+) m/z 375,2 (M+H)+.
Пример 319
4-[2-(2,4-дифторфенокси)-5-(2,3-дигидро-1H-индол-1-илсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 319a
1-(3-бром-4-(2,4-дифторфенокси)фенилсульфонил)индолин
Продукт примера 319a получали согласно процедуре, используемой для получения продукта примера 2b, заменяя 2,4-дифторфенолом фенол и заменяя продуктом примера 305a продукт примера 2a, получая указанное в заголовке соединение.
Пример 319b
4-(2-(2,4-дифторфенокси)-5-(индолин-1-илсульфонил)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 319b получали согласно процедуре, используемой для получения продукта примера 6c, заменяя продуктом примера 319a продукт примера 6b, получая указанное в заголовке соединение.
Пример 319c
4-[2-(2,4-дифторфенокси)-5-(2,3-дигидро-1H-индол-1-илсульфонил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 319c получали согласно процедуре, используемой для получения продукта примера 6d, и заменяя продуктом примера 319b продукт примера 6c, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ 2,92 (т, J=8,3 Гц, 2H) 3,55 (с, 3H) 3,93 (т, J=8,3 Гц, 2H) 5,98 (дд, J=2,8, 1,9 Гц, 1H) 6,91 (дд, J=9,3, 1,0 Гц, 1H) 6,98-7,29 (м, 6H) 7,34-7,58 (м, 3H) 7,74-7,91 (м, 2H) 12,08 (ушир.с, 1H). MS (ESI+) m/z 534 [M+H]+.
Пример 320
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пиразолo[3,4-c]пиридин-4-ил)фенил]этансульфонамид
Пример 320a
5-бром-1,4-диметил-3-нитропиридин-2(1H)-он
Продукт примера 320a получали согласно процедуре, используемой для получения продукта примера 1e, заменяя продуктом примера 1d 5-бром-4-метил-3-нитропиридин-2-ол, получая указанное в заголовке соединение.
Пример 320b
3-амино-5-бром-1,4-диметилпиридин-2(1H)-он
Продукт примера 320b получали согласно процедуре, используемой для получения продукта примера 7b, заменяя продуктом примера 320a продукт примера 7a, получая указанное в заголовке соединение.
Пример 320c
4-бром-6-метил-1H-пиразолo[3,4-c]пиридин-7(6H)-он
Продукт примера 320b (1 г, 4,61 ммоль), уксусный ангидрид (1,304 мл, 13,82 ммоль) и ацетат калия (0,543 г, 5,53 ммоль) перемешивали в толуоле (25 мл) в течение 18 часов. Изоамил нитрит (0,930 мл, 6,91 ммоль) добавляли по каплям и раствор нагревали при 80°C в течение 24 часов. Раствор охлаждали, воду добавляли, и водную фазу экстрагировали этилацетатом. Объединенные органические вещества промывали насыщенным водным раствором хлорида натрия, сушили (безводный сульфат магния), фильтровали и концентрировали. Остаток растирали с 30% этилацетатом в гексанах, получая 0,415 г указанного в заголовке соединения.
Пример 320d
4-бром-6-метил-1-((2-(триметилсилил)этокси)метил)-1H-пиразолo[3,4-c]пиридин-7(6H)-он
Продукт примера 320c (0,228 г, 1,000 ммоль) в диметилформамиде (5 мл) обрабатывали гидридом натрия (0,060 г, 1,500 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 10 минут. К этому раствору добавляли (2-(хлорметокси)этил)триметилсилан (0,200 г, 1,200 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 2 часов. Реакционную смесь распределяли между этилацетатом и водой и органическую фазу отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, градиент этилацетат/гептан), получая указанное в заголовке соединение (0,301 г, 0,840 ммоль, выход 84%).
Пример 320e
4-(5-амино-2-(2,4-дифторфенокси)фенил)-6-метил-1-((2-(триметилсилил)этокси)метил)-1H-пиразолo[3,4-c]пиридин-7(6H)-он
Продукт примера 320e получали согласно процедуре, используемой для получения продукта примера 138a, заменяя продуктом примера 320d 2-бром-1-фтор-4-(метилсульфонил)бензол и продуктом примера 148c продукт примера 6a, соответственно, получая указанное в заголовке соединение.
Пример 320f
N-(4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-1-((2-(триметилсилил)этокси)метил)-6,7-дигидро-1H-пиразолo[3,4-c]пиридин-4-ил)фенил)-N-(этилсульфонил)этансульфонамид
Смесь продукта примера 320e (0,1 г, 0,201 ммоль), этансульфонил хлорида (0,077 г, 0,602 ммоль) и триэтиламина (0,081 г, 0,802 ммоль) в дихлорметане перемешивали в течение 2 часов при комнатной температуре. Растворитель удаляли и остаток очищали флаш-хроматографией на силикагеле, (4:1 этилацетат/гексаны), получая указанное в заголовке соединение (0,11 г, 0,161 ммоль, выход 80%).
Пример 320g
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пиразолo[3,4-c]пиридин-4-ил)фенил]этансульфонамид
Продукт примера 320f в дихлорметане (3 мл) обрабатывали 2,2,2-трифторуксусной кислотой (1,837 г, 16,11 ммоль). Реакционную смесь перемешивали в течение 16 часов при температуре окружающей среды. Растворитель удаляли и остаток помещали в высокий вакуум на 1 час. Затем его обрабатывали диоксаном (5 мл) и 2,0 н. гидроксидом натрия (1,611 мл, 3,22 ммоль). Реакционную смесь нагревали при 85°C в течение 2 часов. После охлаждения реакционную смесь распределяли между 0,1% HCl и этилацетатом. Водный слой экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток затем очищали препаративной ВЭЖХ с обращенной фазой (10-80% ацетoнитрил в 0,1% TFA вода), получая TFA соль указанного в заголовке соединения (0,055 г, 0,119 ммоль, выход 74,1%). 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 9,80 (с, 1H), 7,86 (с, 1H), 7,36-7,42 (м, 3H), 7,22 (дд, J=8,85, 2,75 Гц, 1H), 7,13-7,15 (м, 1H), 6,99-7,04 (м, 1H), 6,92 (д, J=8,85 Гц,1H), 3,56 (с, 3H), 3,13 (т, J=7,32 Гц, 2H), 1,23 (т, J=7,32 Гц, 3H). MS (ESI+) m/z 461,0 (M+H)+.
Пример 321
4-{2-(2,4-дифторфенокси)-5-[(метилсульфонил)метил]фенил}-6-метил-1,6-дигидро-7H-пиразолo[3,4-c]пиридин-7-он
Пример 321a
2-(2-(2,4-дифторфенокси)-5-((метилсульфонил)метил)фенил)-4,4,5,5-тетраметил-1,3,2-диоксаборолан
Продукт примера 287e (1,13 г, 3 ммоль), 4,4,4',4',5,5,5',5'-октаметил-2,2'-би(1,3,2-диоксаборолан) (1,52 г, 6 ммоль), ацетат калия (1,18 г, 12 ммоль) и хлорид бис(трифенилфосфин)палладия(II) (0,126 г, 0,18 ммоль) объединяли в склянке для микроволновой обработки емкостью 20 мл и продували азотом в течение 30 минут. К этой смеси добавляли продутый азотом диоксан (15 мл). Реакционную смесь нагревали при 90°C в течение 8 часов. Реакционную смесь распределяли между водой и этилацетатом. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия, обрабатывали силикагелем, функционализованным 3-меркаптопропилом, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 0-10% этилацетат в дихлорметане) и затем растирали с гептаном, получая указанное в заголовке соединение (0,64 г, 50%).
Пример 321b
4-(2-(2,4-дифторфенокси)-5-((метилсульфонил)метил)фенил)-6-метил-1-((2-(триметилсилил)этокси)метил)-1H-пиразолo[3,4-c]пиридин-7(6H)-он
Продукт примера 320d (0,04 г, 0,112 ммоль), продукт примера 321a (0,052 г, 0,123 ммоль), трис(дибензилиденацетон)дипалладий(0) (0,0031 г, 3,35 мкмоль), (1S,3R,5R,7S)-1,3,5,7-тетраметил-8-фенил-2,4,6-триокса-8-фосфaадамантан (0,0033 г, 0,011 ммоль) и карбонат натрия (0,051 г, 0,48 ммоль) объединяли в 5-мл склянке для микроволновой обработки и продували азотом в течение 30 минут. К этой смеси добавляли продутый азотом диоксан (0,8 мл) и воду (0,2 мл). Реакционную смесь перемешивали при 60°C в течение 4,5 часов. Реакционную смесь охлаждали до температуры окружающей среды и затем распределяли между этилацетатом и водой. Органический слой промывали насыщенным водным раствором хлорида натрия, обрабатывали силикагелем, функционализованным 3-меркаптопропилом, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 0-10% метанол в дихлорметане), получая указанное в заголовке соединение (0,06 г, 93%).
Пример 321c
4-{2-(2,4-дифторфенокси)-5-[(метилсульфонил)метил]фенил}-6-метил-1,6-дигидро-7H-пиразолo[3,4-c]пиридин-7-он
Продукт примера 321b (0,06 г, 0,104 ммоль) обрабатывали 2,2,2-трифторуксусной кислотой (2 мл, 26,1 ммоль), перемешивали при температуре окружающей среды в течение 30 минут и затем концентрировали до сухости. Остаток очищали ВЭЖХ с обращенной фазой (С18, CH3CN/вода (0,1% TFA), 20-80%), получая указанное в заголовке соединение (0,03 г, 65%). 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 7,91 (с, 1H), 7,60 (д, J=2,14 Гц, 1H), 7,42 (м, 3H), 7,29 (м, J=9,23, 9,23, 5,65 Гц, 1H), 7,09 (м, 1H), 6,89 (д, J=8,54 Гц, 1H), 4,53 (с, 2H), 3,58 (с, 3H), 2,96 (с, 3H). MS (ESI+) m/z 446,1 (M+H)+.
Пример 322
4-[2-(2,4-дифторфенокси)-5-(этилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пиразолo[3,4-c]пиридин-7-он
Пример 322a
этил(4-фторфенил)сульфан
Триэтиламин (5,44 мл, 39 ммоль) добавляли к раствору 4-фторбензолтиола (5 г, 39 ммоль) и йодэтана (3,78 мл, 46,8 ммоль) в тетрагидрофуране (50 мл). Полученную смесь перемешивали при температуре окружающей среды в течение 2 часов и затем фильтровали. Фильтрат концентрировали, растирали с гексаном и сушили в вакууме, получая указанное в заголовке соединение (4,8 г, 76%).
Пример 322b
1-(этилсульфонил)-4-фторбензол
Пример 322a (5 г, 32 ммоль) в дихлорметане (200 мл) обрабатывали 3-хлорпероксибензойной кислотой (14,3 г, 70,4 ммоль) и перемешивали при температуре окружающей среды в течение 6 часов. Твердое вещество, образовавшееся во время реакции, удаляли фильтрованием и промывали дополнительным дихлорметаном. Объединенный фильтрат промывали 10% водным раствором гидроксида натрия (50 мл, дважды) и насыщенным водным раствором бикарбоната натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 15% этилацетат в петролейном эфире), получая указанное в заголовке соединение (4,6 г, 76%).
Пример 322c
2-бром-4-(этилсульфонил)-1-фторбензол
Продукт примера 322b (1 г, 5,31 ммоль) в серной кислоте (6 мл, 113 ммоль) обрабатывали N-бромсукцинимидом (1,04 г, 5,84 ммоль), перемешивали при температуре окружающей среды в течение 6 часов и затем при 50°C в течение 16 часов. Реакционную смесь затем выливали в воду со льдом и полученное твердое вещество собирали фильтрованием, промывали холодной водой три раза и сушили в вакуумной печи в течение 16 часов. Твердое вещество затем очищали флаш-хроматографией (силикагель, 9-20% этилацетат в петролейном эфире), получая указанное в заголовке соединение (1,1 г, 78%).
Пример 322d
2-(5-(этилсульфонил)-2-фторфенил)-4,4,5,5-тетраметил-1,3,2-диоксаборолан
4,4,4',4',5,5,5',5'-октаметил-2,2'-би(1,3,2-диоксаборолан) (0,665 г, 2,62 ммоль), продукт примера 322c (0,5 г, 1,9 ммоль), ацетат калия (0,367 г, 3,74 ммоль) и [1,1'- бис(дифенилфосфино)ферроцен]дихлорпалладий(II) (0,041 г, 0,056 ммоль) объединяли в промытой аргоном смеси диоксан (10 мл)/диметил сульфоксид (0,3 мл) и нагревали при 90°C в атмосфере аргона в течение 24 часов. Реакционную смесь распределяли между этилацетатом и водой и фильтровали через прокладку из целита, чтобы удалить элементарный палладий. Слои разделяли и органический слой промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия, обрабатывали силикагелем, функционализованным 3-меркаптопропилом, в течение 15 минут, фильтровали и концентрировали. Остаток растирали в минимальном количестве смеси гептан/простой диэтиловый эфир (20:1) и фильтровали, получая сырой продукт. Этот материал затем растворяли в этилацетате, обрабатывали снова силикагелем, функционализованным 3-меркаптопропилом, фильтровали и концентрировали. Остаток перекристаллизовывали из смеси гептан/этилацетат (9:1), получая указанное в заголовке соединение (0,3 г, 77%).
Пример 322e
4-(5-(этилсульфонил)-2-фторфенил)-6-метил-1-((2-(триметилсилил)этокси)метил)-1H-пиразолo[3,4-c]пиридин-7(6H)-он
Продукт примера 322e получали согласно процедуре, используемой для получения продукта примера 321b, заменяя продуктом примера 322d продукт примера 321a, получая указанное в заголовке соединение (0,0635 г, 55%).
Пример 322f
4-(2-(2,4-дифторфенокси)-5-(этилсульфонил)фенил)-6-метил-1-((2-(триметилсилил)этокси)метил)-1H-пиразолo[3,4-c]пиридин-7(6H)-он
Продукт примера 322e (0,0635 г, 0,136 ммоль), 2,4-дифторфенол (0,021 г, 0,164 ммоль) и карбонат цезия (0,089 г, 0,273 ммоль) объединяли в 4-мл склянке с диметил сульфоксидом (1,5 мл), перемешивали при 60°C в течение 8 часов и затем при температуре окружающей среды в течение 16 часов. Реакционную смесь распределяли между этилацетатом и водой. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 0-8% метанол в дихлорметане), получая указанное в заголовке соединение (0,0574 г, 73%).
Пример 322g
4-(2-(2,4-дифторфенокси)-5-(этилсульфонил)фенил)-6-метил-1H-пиразолo[3,4-c]пиридин-7(6H)-он
Продукт примера 322g получали согласно процедуре, используемой для получения продукта примера 321c, заменяя продуктом примера 322f продукт примера 321b, получая указанное в заголовке соединение (0,0299 г, 67%). 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 7,96 (д, J=2,14 Гц, 1H), 7,91 (с, 1H), 7,85 (дд, J=8,70, 2,29 Гц, 1H), 7,54 (м, 3H), 7,20 (м, 1H), 7,00 (д, J=8,85 Гц, 1H), 3,61 (с, 3H), 3,35 (кв., J=7,32 Гц, 2H), 1,15 (т, J=7,32 Гц, 3H). MS (ESI+) m/z 446,2 (M+H)+.
Пример 323
4-[2-(циклопропилметокси)-5-(этилсульфонил)фенил]-6-метил-1,6-дигидро-7H-пиразолo[3,4-c]пиридин-7-он
Пример 323a
4-(2-(циклопропилметокси)-5-(этилсульфонил)фенил)-6-метил-1-((2-(триметилсилил)этокси)метил)-1H-пиразолo[3,4-c]пиридин-7(6H)-он
Циклопропилметанол (0,018 г, 0,25 ммоль) в диоксане (0,75 мл) обрабатывали гидридом натрия (60% масляная дисперсия) (0,023 г, 0,587 ммоль) и перемешивали при температуре окружающей среды в течение 10 минут. Раствор продукта примера 322e (0,0683 г, 0,147 ммоль) в диоксане (0,75 мл) добавляли и смесь перемешивали при 60°C в течение 8 часов и затем при температуре окружающей среды в течение 16 часов. Дополнительный циклопропилметанол (0,018 г, 0,249 ммоль) и гидрид натрия (60% масляная дисперсия) (0,023 г, 0,587 ммоль) добавляли и смесь нагревали при 70°C в течение 9 часов. Реакционную смесь охлаждали до температуры окружающей среды и затем распределяли между этилацетатом и водой. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 0-30% этилацетат в дихлорметане), получая указанное в заголовке соединение (0,0685 г, 90%).
Пример 323b
4-(2-(циклопропилметокси)-5-(этилсульфонил)фенил)-6-метил-1H-пиразолo[3,4-c]пиридин-7(6H)-он
Продукт примера 323b получали согласно процедуре, используемой для получения продукта примера 321c, заменяя продуктом примера 323a продукт примера 321b, получая указанное в заголовке соединение (0,0302 г, 59%). 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 14,07 (с, 1H), 7,85 (дд, J=8,70, 2,29 Гц, 1H), 7,80 (д, J=2,14 Гц, 1H), 7,78 (м, 1H), 7,41 (с, 1H), 7,34 (д, J=8,54 Гц, 1H), 4,01 (д, J=7,02 Гц, 2H), 3,60 (с, 3H), 3,29 (кв., J=7,32 Гц, 2H), 1,13 (т, J=7,32 Гц, 3H), 1,06 (м, 1H), 0,45 (м, 2H), 0,27 (м, 2H). MS (ESI+) m/z 388,2 (M+H)+.
Пример 324
N-[2-циано-4-(2,4-дифторфенокси)-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид
Пример 324a
4-бром-5-(2,4-дифторфенокси)-2-нитробензойная кислота
Продукт примера 324a получали согласно процедуре, используемой для получения продукта примера 7a, заменяя 4-бром-5-фтор-2-нитробензойной кислотой 2-бром-1-фтор-4-нитробензол (Combi Blocks) и заменяя 2,4-дифторфенолом фенол, получая указанное в заголовке соединение.
Пример 324b
метил 4-бром-5-(2,4-дифторфенокси)-2-нитробензоат
Оксалил хлорид (1,4 мл, 16,6 ммоль) добавляли по каплям при 0°С к суспензии продукта примера 324a (5,47 г, 14,6 ммоль) в дихлорметане (65 мл). Добавляли 3 капли диметилформамида и реакционную смесь перемешивали при температуре окружающей среды в течение 2 часов. После охлаждения до 0°C добавляли по каплям метанол (12 мл, 296 ммоль). Раствор перемешивали в течение 15 минут при 0°С и в течение 2,5 часов при температуре окружающей среды. Раствор разбавляли дихлорметаном и промывали водой, насыщенным водным раствором бикарбоната натрия, насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали, получая указанное в заголовке соединение (5,42 г, выход 96%).
Пример 324c
метил 2-амино-4-бром-5-(2,4-дифторфенокси)бензоат
Пример 324c получали согласно процедуре, используемой для получения продукта примера 7b, заменяя продуктом примера 324b продукт примера 7a, получая указанное в заголовке соединение.
Пример 324d
4-бром-5-(2,4-дифторфенокси)-2-(этилсульфонамидо)бензойная кислота
Продукт примера 324d получали согласно процедуре, используемой для получения продукта примера 7c, заменяя продуктом примера 324c продукт примера 7b, получая указанное в заголовке соединение.
Пример 324e
4-бром-5-(2,4-дифторфенокси)-2-(этилсульфонамидо)бензамид
Оксалил хлорид (0,046 мл, 0,54 ммоль) добавляли по каплям к суспензии продукта примера 324d (214 мг, 0,49 ммоль) и дихлорметана (2,2 мл). Добавляли 1 каплю диметилформамида и реакционную смесь перемешивали при температуре окружающей среды в течение 2 часов. Растворитель выпаривали и остаток сушили (в вакууме). Полученный хлорангидрид кислоты суспендировали в тетрагидрофуране (1,0 мл) и охлаждали до 0°С, когда гидроксид аммония (0,65 мл, 4,7 ммоль) добавляли по каплям. Реакционную смесь перемешивали при температуре окружающей среды в течение 2 часов. Этилацетат добавляли и раствор промывали водой, насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, градиент 1-8% метанол/дихлорметан), получая указанное в заголовке соединение (176 мг, выход 82%).
Пример 324f
N-(5-бром-2-циано-4-(2,4-дифторфенокси)фенил)этансульфонамид
К суспензии продукта примера 324e (230 мг, 0,53 ммоль) и диоксана (1,5 мл) добавляли пиридин (0,14 мл, 1,7 ммоль), а затем ангидрид 2,2,2-трифторуксусной кислоты (0,14 мл, 0,99 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 1 часа. Воду добавляли и раствор экстрагировали этилацетатом. Органический слой промывали водой, насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, градиент 5-40% этилацетат/гептан), получая указанное в заголовке соединение (135 мг, 61% выход).
Пример 324g
N-(2-циано-4-(2,4-дифторфенокси)-5-(6-метил-7-оксо-1-тозил-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил)этансульфонамид
Продукт примера 324g получали согласно процедуре, используемой для получения продукта примера 6c, заменяя продуктом примера 324f продукт примера 6b, получая указанное в заголовке соединение.
Пример 324h
N-(2-циано-4-(2,4-дифторфенокси)-5-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил)этансульфонамид
Продукт примера 324h получали согласно процедуре, используемой для получения продукта примера 6d, заменяя продуктом примера 324g продукт примера 6c, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 1,32 (т, J=7,12 Гц, 3H) 3,20 (кв., J=7,46, 5,76 Гц, 2H) 3,54-3,57 (м, 3H) 6,32 (т, J=2,71, 2,03 Гц, 1H) 7,03-7,11 (м, 1H) 7,24-7,32 (м, 1H) 7,32 (т, J=2,71 Гц, 1H) 7,37 (с, 1H) 7,38-7,48 (м, 1H) 7,46 (с, 1H) 7,59 (с, 1H) 10,07 (с, 1H) 12,13 (ушир.с, 1H). MS (ESI+) m/z 485 [M+H]+.
Пример 325
трет-бутил 4-[4-(циклопропилметокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-3,6-дигидропиридин-1(2H)-карбоксилат
Продукт примера 325 получали согласно процедуре, используемой для получения продукта примера 315, заменяя трет-бутил 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-5,6-дигидропиридин-1(2H)-карбоксилатом пиридин-3-илбороновую кислоту, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 11,93 (с, 1H), 7,40-7,34 (м, 2H), 7,27-7,22 (м, 2H), 7,04 (д, J=9,0 Гц, 1H), 6,13-6,09 (м, 1H), 6,07 (с, 1H), 3,97 (с, 2H), 3,83 (д, J=6,7 Гц, 2H), 3,56 (с, 3H), 3,52 (дд, J=9,1, 3,4 Гц, 2H), 2,45 (с, 2H), 1,42 (д, J=5,3 Гц, 9H), 1,06-0,97 (м, 1H), 0,46-0,38 (м, 2H), 0,26-0,17 (м, 2H). MS (ESI+) m/z 476,2 (M+H)+.
Пример 326
4-[5-(6-аминопиридин-3-ил)-2-(циклопропилметокси)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 326 получали согласно процедуре, используемой для получения продукта примера 315, заменяя 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-амином пиридин-3-илбороновую кислоту, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 11,93 (с, 1H), 8,21 (д, J=2,4 Гц, 1H), 7,67 (дд, J=8,6, 2,5 Гц, 1H), 7,49 (дд, J=6,3, 2,4 Гц, 2H), 7,30 (с, 1H), 7,25 (т, J=2,7 Гц, 1H), 7,14-7,07 (м, 1H), 6,49 (т, J=7,5 Гц, 1H), 6,16 (т, J=2,4 Гц, 1H), 5,94 (с, 2H), 3,86 (д, J=6,7 Гц, 2H), 3,57 (с, 3H), 1,14-1,00 (м, 1H), 0,51-0,38 (м, 2H), 0,27-0,14 (м, 2H). MS (ESI+) m/z 387,2 (M+H)+.
Пример 327
4-{2-[(2,2-дифторциклопропил)метокси]-5-(этилсульфонил)фенил}-6-метил-7-оксо-N-(2,2,2-трифторэтил)-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид
Пример 327a
Этил 1-бензил-6-метил-7-оксо-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Продукт примера 327a получали согласно процедуре, используемой для получения продукта примера 6a, заменяя продуктом примера 70e продукт примера 1e, получая указанное в заголовке соединение.
Пример 327b
Этил 1-бензил-4-(5-(этилсульфонил)-2-фторфенил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Продукт примера 327b получали согласно процедуре, используемой для получения продукта примера 138a, заменяя продуктом примера 327a продукт примера 6a и продуктом примера 168b 2-бром-1-фтор-4-(метилсульфонил)бензол, соответственно, получая указанное в заголовке соединение.
Пример 327c
Этил 4-(5-(этилсульфонил)-2-фторфенил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Продукт примера 327c получали согласно процедуре, используемой для получения продукта примера 70j, заменяя продуктом примера 327b продукт примера 70i, получая указанное в заголовке соединение.
Пример 327d
4-(2-((2,2-дифторциклопропил)метокси)-5-(этилсульфонил)фенил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоновая кислота
К раствору продукта примера 327c (1 г, 2,460 ммоль) и (2,2-дифторциклопропил)метанола (0,532 г, 4,92 ммоль) в диметилсульфоксиде (10 мл) добавляли карбонат цезия (1,203 г, 3,69 ммоль). Реакционную смесь закрывали в пробирке для микроволнового нагрева и нагревали при 110°C в течение 5 дней. В течение 5 дней три дополнительных объема (2,2-дифторциклопропил)метанола (0,532 г, 4,92 ммоль) добавляли в реакционную смесь. Реакционную смесь выливали в этилацетат (150 мл) и воду (150 мл). Водный слой экстрагировали этилацетатом (100 мл × 2). Объединенные органические слои сушили над безводным сульфатом натрия, фильтровали и концентрировали, получая соответствующий этиловый сложный эфир (1,2 г, 1,869 ммоль, выход 76%). pH водного слоя доводили до около 3 с использованием 1 н. НCl и полученное твердое вещество отфильтровывали и сушили, получая указанное в заголовке соединение (0,30 г, 0,64 ммоль).
Пример 327e
4-{2-[(2,2-дифторциклопропил)метокси]-5-(этилсульфонил)фенил}-6-метил-7-оксо-N-(2,2,2-трифторэтил)-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксамид
К раствору продукта примера 327d (0,070 г, 0,15 ммоль) в безводном дихлорметане (5 мл) добавляли оксалил хлорид (0,026 мл, 0,300 ммоль) и диметилформамид (0,581 мкл, 7,50 мкмоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 2 часов и затем выпаривали. Остаток растворяли в дихлорметане (5 мл) и обрабатывали 2,2,2-трифторэтиламином (0,048 мл, 0,600 ммоль) и смесь перемешивали при температуре окружающей среды в течение ночи. Реакционную смесь распределяли между водой (15 мл) и этилацетатом (25 мл). Водный слой экстрагировали дополнительным этилацетатом (15 мл) дважды. Объединенные органические слои сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток очищали ВЭЖХ с обращенной фазой (С18, подвижная фаза A: вода (10 мM NН4HCO3); В: ацетoнитрил, градиент 25-60% В в A), получая указанное в заголовке соединение (70 мг, 85%). 1H ЯМР (400 МГц, CD3OD) δ м.д. 7,96-7,90 (м, 2H), 7,66-7,25 (м, 2H), 6,92 (с, 1H), 4,29 (т, J=7,5 Гц, 1H), 4,16 (т, J=9,2 Гц, 1H), 4,05 (тт, J=9,2, 4,5 Гц, 2H), 3,72 (с, 3H), 3,22 (кв., J=7,4 Гц, 2H), 2,00 (тд, J=12,0, 7,3 Гц, 1H), 1,58-1,46 (м, 1H), 1,32-1,25 (м, 4H). MS (ESI+) m/z 548,1 (M+H)+.
Пример 328
4-{2-[(циклопропилметил)амино]-5-[(метилсульфонил)метил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 328a
1-((метилсульфонил)метил)-4-нитробензол
К раствору 4-нитробензил бромида (10,02 г, 46,4 ммоль) в N,N-диметилформамиде (25 мл) добавляли метансульфинат натрия (7,10 г, 69,6 ммоль). Реакционную смесь перемешивали при 65°C в течение 1 часа. Реакционную смесь охлаждали до температуры окружающей среды и разбавляли водой. Полученную суспензию перемешивали в течение 10 минут и фильтровали через средний пористый барьер, получая указанное в заголовке соединение.
Пример 328b
4-((метилсульфонил)метил)анилин
Продукт примера 328a (8,2 г, 38,1 ммоль) и тетрагидрофуран (200 мл) добавляли к 5% Pd/C, влажный (1,6 г, 0,376 ммоль) в работающем под давлением сосуде емкостью 50 мл и перемешивали в течение 2 часов при 30 фунтах на кв. дюйм и 50°C. Смесь фильтровали через нейлоновую мембрану и промывали небольшим количеством тетрагидрофурана и метанола. Растворитель выпаривали, получая указанное в заголовке соединение.
Пример 328c
2-йод-4-((метилсульфонил)метил)анилин
К раствору продукта примера 328b (3,80 г, 20,5 ммоль) в N,N-диметилформамиде (103 мл) добавляли N-йодсукцинимид (5,08 г, 22,56 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 1 часа. Реакционную смесь гасили 150 мл 10% водного раствора тиосульфата натрия и 100 мл насыщенного водного раствора бикарбоната натрия. Реакционную смесь экстрагировали этилацетатом. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия и концентрировали. Воду добавляли и полученную суспензию перемешивали при температуре окружающей среды 10 минут. Суспензию фильтровали и собранные твердые вещества промывали водой и сушили в течение ночи, получая указанное в заголовке соединение.
Пример 328d
N-(циклопропилметил)-2-йод-4-((метилсульфонил)метил)анилин
Продукт примера 328c (0,200 г, 0,643 ммоль) и циклопропанкарбальдегид (0,062 мл, 0,836 ммоль) суспендировали в дихлорметане (3,21 мл) и метаноле (3,21 мл). Добавляли уксусную кислоту (0,368 мл, 6,43 ммоль). Реакционную смесь нагревали при 50°C в течение 30 минут и затем охлаждали до температуры окружающей среды. Цианоборгидрид на полимерном носителе (0,817 г, 1,928 ммоль) добавляли. Реакционную смесь перемешивали при температуре окружающей среды в течение ночи. Циклопропанкарбальдегид (0,062 мл, 0,836 ммоль) добавляли и реакционную смесь перемешивали при температуре окружающей среды в течение 2 часов. Реакционную смесь фильтровали, тщательно промывали дихлорметаном, концентрировали. Остаток очищали флаш-хроматографией (силикагель, градиент 20-100% этилацетатом/гептан), получая указанное в заголовке соединение.
Пример 328e
4-(2-((циклопропилметил)амино)-5-((метилсульфонил)метил)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 328e получали согласно процедуре, используемой для получения продукта примера 4a, заменяя продуктом примера 328d продукт примера 7c, получая указанное в заголовке соединение.
Пример 328f
4-(2-[(циклопропилметил)амино]-5-[(метилсульфонил)метил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 328f получали согласно процедуре, используемой для получения продукта примера 4b, заменяя продуктом примера 328e продукт примера 4a, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6) δ м.д. 12,08 (ушир.с, 1H), 7,29 (т, J=2,3 Гц, 1H), 7,21 (дд, J=8,3, 2,1 Гц, 1H), 7,17 (с, 1H), 7,12 (д, J=2,1 Гц, 1H), 6,73 (д, J=8,3 Гц, 1H), 6,05 (д, J=2,7 Гц, 1H), 4,67 (т, J=5,7 Гц, 1H), 4,30 (ушир.с, 2H), 3,55 (с, 3H), 2,96 (т, J=6,1 Гц, 2H), 2,86 (с, 3H), 1,05-0,92 (м, 1H), 0,41-0,29 (м, 2H), 0,19-0,10 (м, 2H). MS (ESI+) m/z 386,0 (M+H)+
Пример 329
4-{2-[(циклопропилметил)амино]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 329a
2-бром-N-(циклопропилметил)-4-(метилсульфонил)анилин
Продукт примера 329a получали согласно процедуре, используемой для получения продукта примера 147a, заменяя циклопропилметанамином циклогексанамин, получая указанное в заголовке соединение.
Пример 329b
4-(2-((циклопропилметил)амино)-5-(метилсульфонил)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 329b получали согласно процедуре, используемой для получения продукта примера 7d, заменяя продуктом примера 329a продукт примера 7c и перемешивая при 100°C в течение 30 минут, получая указанное в заголовке соединение.
Пример 329c
4-{2-[(циклопропилметил)амино]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 329c получали согласно процедуре, используемой для получения продукта примера 4 (способ B), заменяя продуктом примера 329b продукт примера 7d, и очищали препаративной ВЭЖХ (С18, 10-100% ацетoнитрил в 0,1% TFA/воде), получая TFA соль указанного в заголовке соединения. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,12 (ушир.дс, 1H), 7,67 (дд, J=2,4, 8,8 Гц, 1H), 7,51 (д, J=2,4 Гц, 1H), 7,29 (т, J=3,1 Гц, 1H), 7,26 (с, 1H), 6,86 (д, J=8,8 Гц, 1H), 6,02 (т, J=2,2 Гц, 1H), 5,45 (м, 1H), 3,56 (с, 3H), 3,10 (м, 2H), 3,04 (м, 2H), 1,01 (м, 1H), 0,37 (м, 2H), 0,16 (м, 2H). MS (ESI+) m/z 372,1 (M+H)+.
Пример 330
4-[5-(этилсульфонил)-2-(пирролидин-1-ил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 330a
4-(5-(этилсульфонил)-2-фторфенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Смесь продукта примера 168b (0,935 г, 3,50 ммоль), продукта примера 6a (1,5 г, 3,5 ммоль), тетракис(трифенилфосфин)палладия(0) (0,202 г, 0,175 ммоль) и фторида цезия (1,596 г, 10,51 ммоль) в 12 мл диметоксиэтана и 4 мл метанола нагревали при 120°C микроволновым излучением в течение 40 минут. Смесь концентрировали и остаток абсорбировали на силикагеле и очищали флаш-хроматографией (SiО2, градиент 0-10% метанол/дихлорметан), получая указанное в заголовке соединение (1,01 г, выход 86%).
Пример 330b
4-[5-(этилсульфонил)-2-(пирролидин-1-ил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Смесь продукта примера 330a (90 мг, 0,27 ммоль) и пирролидина (668 мкл, 8,08 ммоль) в 1 мл DMSO нагревали при 160°C микроволновым излучением в течение 30 минут. Продукт очищали препаративной ВЭЖХ (С18, 10-80% CH3CN/вода (0,1% TFA)), получая указанное в заголовке соединение (37 мг, выход 35,7%). 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,07 (с, 1H), 7,61 (дд, J=8,8, 2,4 Гц, 1H), 7,48 (д, J=2,4 Гц, 1H), 7,26 (т, J=2,8 Гц, 1H), 7,20 (с, 1H), 6,95 (д, J=8,9 Гц, 1H), 5,99-5,94 (м, 1H), 3,56 (с, 3H), 3,16 (кв., J=7,3 Гц, 2H), 3,06 (с, 4H), 1,69 (т, J=6,3 Гц, 4H), 1,10 (т, J=7,4 Гц, 3H). MS (ESI+) m/z 386,1 (M+H)+.
Пример 331
4-[5-(этилсульфонил)-2-(4-метилпиперазин-1-ил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 331 получали согласно процедуре, используемой для получения продукта примера 330b, заменяя N-метилпиперазином пирролидин, получая TFA соль указанного в заголовке соединения. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,12 (с, 1H), 9,57 (с, 1H), 7,80 (дд, J=8,5, 2,3 Гц, 1H), 7,71 (д, J=2,3 Гц, 1H), 7,45 (с, 1H), 7,32 (дд, J=8,6, 5,7 Гц, 2H), 6,17 (т, J=2,3 Гц, 1H), 3,60 (с, 3H), 3,49 (т, J=6,7 Гц, 2H), 3,28 (кв., J=7,4 Гц, 4H), 2,94 (т, J=11,8 Гц, 2H), 2,71 (с, 3H), 2,68-2,53 (м, 2H), 1,13 (т, J=7,3 Гц, 3H). MS (ESI+) m/z 415,2 (M+H)+.
Пример 332
4-{2-[(4-фторфенил)амино]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 332a
4-(2-амино-5-(метилсульфонил)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 6а (1,71 г, 4,00 ммоль), 2-бром-4-(метилсульфонил)анилин (1,00 г, 4,00 ммоль), трис(дибензилиденацетон)дипалладий (0,110 г, 0,120 ммоль), 1,3,5,7-тетраметил-6-фенил-2,4,8-триокса-6-фосфаадамант (0,117 г, 0,400 ммоль) и карбонат натрия (1,48 г, 14,0 ммоль) объединяли и продували аргоном в течение 15 минут. Смесь диоксана (21,3 мл) и воды (5,3 мл) продували азотом в течение 15 минут и переносили в реакционный сосуд. Реакционную смесь нагревали при 60°C в течение 3 часов, охлаждали до температуры окружающей среды и разбавляли водой. Полученное твердое вещество фильтровали, промывали водой и сушили, получая указанное в заголовке соединение (2,06 г, количественный выход).
Пример 332b
4-(2-((4-фторфенил)амино)-5-(метилсульфонил)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6Н)-он
Продукт примера 332a (47,2 мг, 0,100 ммоль), 1-бром-4-фторбензол (17,5 мг, 0,100 ммоль), диацетоксипалладий (0,9 мг, 4 мкмоль), дициклогексил(2',4',6'-триизопропил-[1,1'-бифенил]-2-ил)фосфин (3,8 мг, 8,0 мкмоль) и карбонат цезия (45,6 мг, 0,140 ммоль) объединяли в смеси толуола (1,6 мл) и трет-бутанола (0,4 мл). Реакционную смесь нагревали в микроволновом реакторе при 150°C в течение 15 минут. Реакционную смесь распределяли между этилацетатом и водой. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили безводным сульфатом натрия, обрабатывали силикагелем, функционализованным 3-меркаптопропилом, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 2-4% метанол в дихлорметане), получая указанное в заголовке соединение (30 мг, 53%).
Пример 332c
4-{2-[(4-фторфенил)амино]-5-(метилсульфонил)фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 332b (28 мг, 0,050 ммоль), гидроксид калия (41,7 мг, 0,743 ммоль) и бромид цетилтриметиламмония (0,90 мг, 2,5 мкмоль) объединяли в смеси тетрагидрофурана (2 мл) и воды (1 мл). Реакционную смесь нагревали при 100°C в течение 20 часов и затем охлаждали до температуры окружающей среды. К этой смеси добавляли воду и pH доводили до pН 7 добавлением 1M HCl. Смесь экстрагировали этилацетатом и органический слой промывали насыщенным водным раствором хлорида натрия дважды, сушили безводным сульфатом натрия, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 2-4% метанол в дихлорметане), получая указанное в заголовке соединение (13 мг, 64%). 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,04 (с, 1H) 7,57-7,71 (м, 3H) 7,34 (с, 1H) 7,08-7,27 (м, 6H) 6,06 (т, J=2,20 Гц, 1H) 3,57 (с, 3H) 3,15 (с, 3H). MS (ESI+) m/z 412 (M+H)+.
Пример 333
4-(циклопропилметокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-(пиридин-3-илметил)бензолсульфонамид
Пример 333a
3-бром-4-фтор-N-(пиридин-3-илметил)бензолсульфонамид
Продукт примера 333a получали согласно процедуре, используемой для получения продукта примера 305a, заменяя пиридин-3-илметанамином индолин. Сырой продукт очищали кристаллизацией из смеси этилацетат/этиловый простой эфир, получая указанное в заголовке соединение.
Пример 333b
3-бром-4-(циклопропилметокси)-N-(пиридин-3-илметил)бензолсульфонамид
Продукт примера 333b получали согласно процедуре, используемой для получения продукта примера 29a, заменяя циклопропилметанолом тетрагидро-2H-пиран-4-ол и заменяя продуктом примера 333a продукт примера 2a, получая указанное в заголовке соединение.
Пример 333c
4-(циклопропилметокси)-3-(6-метил-7-оксо-1-тозил-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-(пиридин-3-илметил)бензолсульфонамид
Продукт примера 333c получали согласно процедуре, используемой для получения продукта примера 6c, заменяя продуктом примера 333b продукт примера 6b, получая указанное в заголовке соединение.
Пример 333d
4-(циклопропилметокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)-N-(пиридин-3-илметил)бензолсульфонамид
Продукт примера 333d получали согласно процедуре, используемой для получения продукта примера 6d, заменяя продуктом примера 333c продукт примера 6c, и очищали препаративной ВЭЖХ (C18, 10-100% ацетoнитрил в 0,1% TFA/воде), получая TFA соль указанного в заголовке соединения. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,03 (с, 1H) 8,55 (с, 2H) 8,17 (т, J=6,44 Гц, 1H) 7,88 (д, J=7,80 Гц, 1H) 7,70-7,76 (м, 2H) 7,50 (дд, J=7,12, 4,75 Гц, 1H) 7,27-7,32 (м, 2H) 7,20-7,26 (м, 1H) 6,10-6,16 (м, 1H) 4,11 (д, J=6,44 Гц, 2H) 3,95 (д, J=6,78 Гц, 2H) 3,58 (с, 3H) 1,03-1,19 (м, 1H) 0,44-0,52 (м, 2H) 0,24-0,31 (м, 2H). MS (ESI+) m/z 465,0 [M+H]+.
Пример 334
4-[4-(циклопропилметокси)-3'-фторбифенил-3-ил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 334a
4-(5-бром-2-(циклопропилметокси)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 334a получали согласно процедуре, используемой для получения продукта примера 6c, заменяя продуктом примера 314a продукт примера 6b, получая указанное в заголовке соединение.
Пример 334b
4-(4-(циклопропилметокси)-3'-фторбифенил-3-ил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 334b получали согласно процедуре, используемой для получения продукта примера 6c, заменяя продуктом примера 334a продукт примера 6b и заменяя (3-фторфенил)бороновой кислотой продукт примера 6a, получая указанное в заголовке соединение.
Пример 334c
4-(4-(циклопропилметокси)-3'-фторбифенил-3-ил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 334c получали согласно процедуре, используемой для получения продукта примера 6d, заменяя продуктом примера 334b продукт примера 6c, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 0,22-0,28 (м, 2H) 0,42-0,49 (м, 2H) 1,03-1,14 (м, 1H) 3,58 (с, 3H) 3,90 (д, J=6,78 Гц, 2H) 6,17 (т, J=2,71, 2,03 Гц, 1H) 7,09-7,20 (м, 2H) 7,27 (т, J=3,05 Гц, 1H) 7,34 (с, 1H) 7,42-7,55 (м, 3H) 7,62-7,69 (м, 2H) 11,98 (ушир.с, 1H). MS (ESI+) m/z 389 [M+H]+.
Пример 335
4-{2-[(4-фторфенил)амино]-5-[(метилсульфонил)метил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 335a
4-(2-амино-5-((метилсульфонил)метил)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 335a получали согласно процедуре, используемой для получения продукта примера 4a, заменяя продуктом примера 328c продукт примера 7c, получая указанное в заголовке соединение.
Пример 335b
4-(2-((4-фторфенил)амино)-5-((метилсульфонил)метил)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
4-Бромфторбензол (0,027 мл, 0,25 ммоль), продукт примера 335a (0,100 г, 0,206 ммоль), ацетат палладия(II) (1,849 мг, 8,24 мкмоль), дициклогексил(2',4',6'-триизопропил-[1,1'-бифенил]-2-ил)фосфин (7,85 мг, 0,016 ммоль) и карбонат цезия (0,094 г, 0,29 ммоль) суспендировали в толуоле (1,37 мл) и трет-бутаноле (0,69 мл). Реакционную смесь нагревали при 150°C в течение 30 минут микроволновым излучением. Реакционную смесь фильтровали через колонку 2,5 г целита и промывали тщательно этилацетатом. Фильтрат промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и меркаптопропил силикагелем, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, градиент 0-4% метанол/дихлорметан), получая указанное в заголовке соединение.
Пример 335c
4-{2-[(4-фторфенил)амино]-5-[(метилсульфонил)метил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 335c получали согласно процедуре, используемой для получения продукта примера 4b, заменяя продуктом примера 335b продукт примера 4a, получая указанное в заголовке соединение. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 11,99 (ушир.с, 1H), 7,32 (д, J=2,1 Гц, 1H), 7,25 (дд, J=8,3, 2,0 Гц, 1H), 7,18-7,23 (м, 4H), 6,97-7,07 (м, 4H), 6,06 (т, J=2,0 Гц, 1H), 4,40 (ушир.с, 2H), 3,53 (с, 3H), 2,91 (с, 3H). MS (ESI+) m/z 426,2 (M+H)+.
Пример 336
[4-(циклопропилметокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]ацетoнитрил
Смесь продукта примера 314b (100 мг, 0,190 ммоль), 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)изоксазола (44,4 мг, 0,228 ммоль), комплекса [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия (II) с дихлорметаном (1:1) (15,5 мг, 0,019 ммоль) и фторида калия (44,1 мг, 0,758 ммоль) в диметилсульфоксиде (1,9 мл) и воде (0,75 мл) продували азотом и нагревали микроволновым излучением при 130°C в течение 1,5 часов. Смесь затем обрабатывали 1 мл 4 н. NaOH и перемешивали при температуре окружающей среды в течение 2 часов. Реакционную смесь распределяли между водой и этилацетатом и водные слои экстрагировали этилацетатом. Объединенные органические фазы промывали водой (2×), насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и фильтровали. Фильтрат концентрировали и остаток очищали флаш-хроматографией (силикагель, градиент 0-8% метанол/дихлорметан), получая указанное в заголовке соединение (30 мг, выход 48%). 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,00 (с, 1H), 12,00 (с, 1H), 7,32 (д, J=2,4 Гц, 1H), 7,34-7,25 (м, 4H), 7,30-7,25 (м, 3H), 7,10 (д, J=8,4 Гц, 1H), 7,10 (д, J=8,4 Гц, 1H), 6,14 (дд, J=2,6, 2,2 Гц, 1H), 6,14 (дд, J=2,6, 2,2 Гц, 1H), 3,99 (с, 2H), 3,99 (с, 2H), 3,84 (д, J=6,7 Гц, 2H), 3,84 (д, J=6,7 Гц, 2H), 3,56 (с, 3H), 3,56 (с, 3H), 1,11-1,02 (м, 1H), 1,12-1,02 (м, 1H), 0,48-0,39 (м, 2H), 0,49-0,35 (м, 2H), 0,31-0,18 (м, 2H), 0,26-0,19 (м, 2H). MS (ESI+) m/z 334,1 (M+H)+.
Пример 337
N-{4-(2,4-дифторфенокси)-3-[2-(гидроксиметил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил]фенил}этансульфонамид
Пример 337a
Этил 4-(5-амино-2-(2,4-дифторфенокси)фенил)-1-бензил-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Продукт примера 337a получали согласно процедуре, используемой для получения продукта примера 138a, заменяя продуктом примера 70e 2-бром-1-фтор-4-(метилсульфонил)бензол и продуктом примера 148c продукт примера 6a, соответственно, получая указанное в заголовке соединение.
Пример 337b
Этил 1-бензил-4-(2-(2,4-дифторфенокси)-5-(N-(этилсульфонил)этилсульфонамидо)фенил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Продукт примера 337b получали согласно процедуре, используемой для получения продукта примера 320f, заменяя продуктом примера 337a продукт примера 320e, получая указанное в заголовке соединение.
Пример 337c
Этил 4-(2-(2,4-дифторфенокси)-5-(N-(этилсульфонил)этилсульфонамидо)фенил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоксилат
Продукт примера 337c получали согласно процедуре, используемой для получения продукта примера 70j, заменяя продуктом примера 337b продукт примера 70i, получая указанное в заголовке соединение.
Пример 337d
4-(2-(2,4-дифторфенокси)-5-(этилсульфонамидо)фенил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбоновая кислота
Продукт примера 337d получали согласно процедуре, используемой для получения продукта примера 70k, заменяя продуктом примера 337c продукт примера 70j, получая указанное в заголовке соединение.
Пример 337e
N-{4-(2,4-дифторфенокси)-3-[2-(гидроксиметил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил]фенил}этансульфонамид
Продукт примера 337d (0,060 г, 0,12 ммоль) в тетрагидрофуране (5 мл) обрабатывали 1,0 н. раствором борана (0,119 мл, 0,119 ммоль). Реакционную смесь нагревали при 60°C в течение 2 часов. Реакционную смесь распределяли между водой и этилацетатом. Органический слой экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали ВЭЖХ с обращенной фазой (С18, 10-100% ацетoнитрил в 0,1% TFA/воде), получая указанный в заголовке продукт. (0,035 г, выход 60%). 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 11,81 (с, 1H), 9,78 (с, 1H), 7,33-7,39 (м, 2H), 7,28 (с, 1H), 7,20 (дд, J=8,7, 2,59 Гц, 1H), 6,97-7,08 (м, 2H), 6,91 (д, J=8,85 Гц, 1H), 6,15 (д, J=2,14 Гц, 1H), 4,50 (с, 2H), 3,52 (с, 3H), 3,10 (кв., J=7,32 Гц, 2H), 1,23 (т, J=7,32 Гц, 3H). MS (ESI+) m/z 490,2 (M+H)+.
Пример 338
N-[4-(2,4-дифторфенокси)-3-{6-метил-2-[(4-метилпиперазин-1-ил)карбонил]-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил}фенил]этансульфонамид
Пример 338a
4-(2-(2,4-дифторфенокси)-5-(этилсульфонамидо)фенил)-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-2-карбонил хлорид
Продукт примера 338a получали согласно процедуре, используемой для получения продукта примера 13a, заменяя продуктом примера 337d продукт примера 10, получая указанное в заголовке соединение.
Пример 338b
N-[4-(2,4-дифторфенокси)-3-{6-метил-2-[(4-метилпиперазин-1-ил)карбонил]-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил}фенил]этансульфонамид
Продукт примера 338b получали согласно процедуре, используемой для получения продукта примера 13b, заменяя продуктом примера 338a продукт примера 13a и 1-метилпиперазином этиламин, соответственно, получая TFA соль указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,53 (с, 1H), 10,14 (ушир. с, 1H), 9,81 (с, 1H), 7,34-7,40 (м, 3H), 7,20 (дд, J=8,85, 2,75 Гц, 1H), 7,06-7,12 (м, 1H), 6,98-7,04 (м, 1H), 6,93 (д, J=8,54 Гц, 1H), 6,53 (д, J=2,14 Гц, 1H), 3,55 (с, 3H), 3,02-3,43 (м, 6H), 2,84 (с, 3H), 1,24 (т, J=7,32 Гц, 3H). MS (ESI+) m/z 586,2 (M+H)+.
Пример 339
N-[4-(2,4-дифторфенокси)-3-{6-метил-2-[(4-метилпиперазин-1-ил)метил]-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил}фенил]этансульфонамид
Продукт примера 339 получали согласно процедуре, используемой для получения продукта примера 337e, заменяя продуктом примера 338b продукт примера 337d, получая TFA соль указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,01 (с, 1H), 9,80 (с, 1H), 7,34-7,39 (м, 2H), 7,31 (с, 1H), 7,19 (дд, J=8,85, 2,75 Гц, 1H), 7,05-7,11 (м, 1H), 6,98-7,04 (м, 1H), 6,91 (д, J=8,85 Гц, 1H), 6,19 (д, J=2,14 Гц, 1H), 3,75 (с, 2H), 3,11 (кв., J=7,32 Гц, 2H), 2,95 (ушир. с, 2H), 2,76 (с, 3H), 2,35 (ушир. с, 2H), 1,24 (т, J=7,32 Гц, 3H). MS (ESI+) m/z 572,0 (M+H)+.
Пример 340
4-[2-(циклопропилметокси)-5-(1,2,3,6-тетрагидропиридин-4-ил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 325 (100 мг, 0,210 ммоль) в 2 мл дихлорметана обрабатывали 1 мл трифторуксусной кислоты. Смесь перемешивали при температуре окружающей среды в течение 2 часов. Растворитель выпаривали. Остаток обрабатывали насыщенным водным раствором карбоната натрия и затем экстрагировали этилацетатом (4X). Органическую фазу сушили над безводным сульфатом магния, фильтровали и концентрировали, получая указанное в заголовке соединение (26 мг, выход 32,9%). 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 11,94 (с, 1H), 7,37-7,31 (м, 1H), 7,25 (дд, J=5,3, 3,0 Гц, 2H), 7,18 (д, J=2,2 Гц, 1H), 7,13 (дд, J=8,4, 2,3 Гц, 1H), 7,00 (д, J=8,4 Гц, 1H), 6,12 (м, 2H), 3,80 (д, J=6,7 Гц, 2H), 3,56 (с, 3H), 3,09 (д, J=12,1 Гц, 2H), 2,73-2,53 (м, 2H), 1,76 (д, J=11,0 Гц, 1H), 1,55 (кв.д, J=12,4, 3,8 Гц, 2H), 1,12-1,01 (м, 1H), 0,49-0,38 (м, 2H), 0,25-0,17 (м, 2H), MS ((DCI+) m/z 376,5 (M+H)+.
Пример 341
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-N-(2-метоксиэтил)этансульфонамид
В 4 мл склянку добавляли (азидокарбонил)дипиперидин (ADDP) (25,9 мг, 0,102 ммоль) в безводном толуоле. Склянку помещали в сухой бокс и добавляли трибутилфосфин (41,5 мг, 3 экв., 0,205 ммоль) в склянку. Эту смесь встряхивали, пока раствор не становился прозрачным. К этому раствору добавляли раствор 2-метоксиэтанола в безводном тетрагидрофуране (1,2 эквивалента, 0,082 ммоль, 6,24 мг). Эту смесь перемешивали в течение 10 минут при температуре окружающей среды. К этой смеси добавляли раствор продукта примера 36e (0,068 ммоль, 31,4 мг) в смеси безводный толуол/безводный тетрагидрофуран (1:1 об/об) (1 мл). Реакционную смесь перемешивали при комнатной температуре в течение ночи в сухом боксе. Реакционную смесь концентрировали до сухости и остаток очищали ВЭЖХ с обращенной фазой (С18, 10-100% ацетoнитрил в 0,1% TFA/воде), получая указанное в заголовке соединение (4,24%, 1,5 мг). 1H ЯМР (400 МГц, DMSO d6/D2O) δ м.д. 7,49 (д, J=2,75 Гц, 1H), 7,38-7,43 (м, 1H), 7,37 (д, J=2,75 Гц, 1H), 7,35-7,36 (м, 1H), 7,34 (д, J=2,75 Гц, 1H), 7,22-7,27 (м, 1H), 7,05-7,11 (м, 1H), 6,87 (д, J=8,54 Гц, 1H), 6,30 (д, J=2,75 Гц, 1H), 3,78-3,81 (м, 2H), 3,57 (с, 3H), 3,37 (т, J=5,65 Гц, 2H), 3,20 (с, 3H), 3,16 (т, J=7,32 Гц, 2H), 1,26 (т, J=7,48 Гц, 3H), ESI+ m/z=518,0 (M+H)+.
Пример 342
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-N-(пиридин-2-илметил)этансульфонамид
Продукт примера 342 получали согласно процедуре, используемой для получения продукта примера 341, заменяя пиридин-2-илметанолом 2-метоксиэтанол, получая TFA соль указанного в заголовке соединения. 1H ЯМР (400 МГц, DMSO d6/D2O) δ м.д. 8,60 (д, J=4,58 Гц, 1H), 8,07 (т, J=7,78 Гц, 1H), 7,70 (д, J=7,93 Гц, 1H), 7,56 (д, J=2,44 Гц, 1H), 7,53 (дд, J=7,02, 5,80 Гц, 1H), 7,45 (дд, J=8,85, 2,75 Гц, 1H), 7,35-7,41 (м, 1H), 7,33 (д, J=2,75 Гц, 1H), 7,29 (с, 1H), 7,17-7,23 (м, 1H), 7,03-7,09 (м, 1H), 6,81 (д, J=8,85 Гц, 1H), 6,17 (д, J=2,75 Гц, 1H), 5,10 (с, 2H), 3,56 (с, 3H), 3,33 (кв., J=7,43 Гц, 2H), 1,31 (т, J=7,32 Гц, 3H), ESI+ m/z=551,0 (M+H)+.
Пример 343
N~(циклопропилметил)-N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид
Продукт примера 343 получали согласно процедуре, используемой для получения продукта примера 341, заменяя циклопропилметанолом 2-метоксиэтанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO d6/D2O) δ м.д. 7,51 (д, J=2,44 Гц, 1H), 7,36-7,42 (м, 2H), 7,35 (с, 1H), 7,34 (д, J=2,75 Гц, 1H), 7,20-7,27 (м, 1H), 7,04-7,10 (м, 1H), 6,88 (д, J=8,85 Гц, 1H), 6,29 (д, J=2,75 Гц, 1H), 3,57 (с, 3H), 3,52 (д, J=7,02 Гц, 2H), 3,12-3,18 (м, 2H), 1,26 (т, J=7,32 Гц, 3H), 0,83-0,93 (м, 1H), 0,40-0,45 (м, 2H), 0,08-0,13 (м, 2H), ESI+ m/z=514,0 (M+H)+.
Пример 344
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-N-[2-(2-оксопирролидин-1-ил)этил]этансульфонамид
Продукт примера 344 получали согласно процедуре, используемой для получения продукта примера 341, заменяя 1-(2-гидроксиэтил)пирролидин-2-оном 2-метоксиэтанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO d6/D2O) δ м.д. 7,50 (д, J=2,44 Гц, 1H), 7,38-7,43 (м, 2H), 7,37 (с, 1H), 7,33 (д, J=2,75 Гц, 1H), 7,22-7,28 (м, 1H), 7,05-7,11 (м, 1H), 6,84 (д, J=8,54 Гц, 1H), 6,34 (д, J=2,75 Гц, 1H), 3,83 (т, J=5,65 Гц, 2H), 3,58 (с, 3H), 3,27-3,32 (м, 4H), 3,14 (кв., J=7,32 Гц, 2H), 2,11 (т, J=8,09 Гц, 2H), 1,74-1,82 (м, 2H), 1,25 (т, J=7,32 Гц, 3H), ESI+ m/z=571,1 (M+H)+.
Пример 345
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-N-(тетрагидрофуран-2-илметил)этансульфонамид
Продукт примера 345 получали согласно процедуре, используемой для получения продукта примера 341, заменяя (тетрагидрофуран-2-ил)метанолом 2-метоксиэтанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO d6/D2O) δ м.д. 7,51 (д, J=2,75 Гц, 1H), 7,37-7,43 (м, 2H), 7,36 (с, 1H), 7,34 (д, J=2,75 Гц, 1H), 7,21-7,27 (м, 1H), 7,04-7,11 (м, 1H), 6,86 (д, J=8,85 Гц, 1H), 6,31 (д, J=2,75 Гц, 1H), 3,78-3,84 (м, 1H), 3,58-3,70 (м, 4H), 3,57 (с, 3H), 3,13-3,19 (м, 2H), 1,73-1,93 (м, 3H), 1,51-1,59 (м, 1H), 1,25 (т, J=7,32 Гц, 3H), ESI+ m/z=544,0 (M+H)+.
Пример 346
N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]-N-(3,3,3-трифторпропил)этансульфонамид
Продукт примера 346 получали согласно процедуре, используемой для получения продукта примера 341, заменяя 3,3,3-трифторпропан-1-олом 2-метоксиэтанол, получая указанное в заголовке соединение. 1H ЯМР (400 МГц, DMSO-d6/D2O) δ м.д. 7,54 (д, J=2,75 Гц, 1H), 7,31-7,44 (м, 4H), 7,23-7,30 (м, 1H), 7,05-7,11 (м, 1H), 6,89 (д, J=8,54 Гц, 1H), 6,31 (д, J=2,75 Гц, 1H), 3,93-3,98 (м, 2H), 3,57 (с, 3H), 3,18 (кв., J=7,32 Гц, 2H), 2,41-2,51 (м, 2H), 1,25 (т, J=7,32 Гц, 3H), ESI+ m/z=556,0(M+H)+.
Пример 347
4-(циклопропилметокси)-N-(4-фторфенил)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид
Пример 347a
3-бром-4-фтор-N-(4-фторфенил)бензолсульфонамид
Продукт примера 347a получали согласно процедуре, используемой для получения продукта примера 305a, заменяя 4-фторанилином индолин. Сырой продукт очищали флаш-хроматографией (силикагель, 10% этилацетат в гептане), получая указанное в заголовке соединение.
Пример 347b
3-бром-4-(циклопропилметокси)-N-(4-фторфенил)бензолсульфонамид
Продукт примера 347b получали согласно процедуре, используемой для получения продукта примера 29a, заменяя циклопропилметанолом тетрагидро-2H-пиран-4-ол и заменяя продуктом примера 347a продукт примера 2a, получая указанное в заголовке соединение.
Пример 347c
4-(циклопропилметокси)-N-(4-фторфенил)-3-(6-метил-7-оксо-1-тозил-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид
Продукт примера 347c получали согласно процедуре, используемой для получения продукта примера 6c, заменяя продуктом примера 347b продукт примера 6b, получая указанное в заголовке соединение.
Пример 347d
4-(циклопропилметокси)-N-(4-фторфенил)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бензолсульфонамид
Продукт примера 347d получали согласно процедуре, используемой для получения продукта примера 6d, заменяя продуктом примера 347c продукт примера 6c, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 12,04 (с, 1H) 10,07 (с, 1H) 7,60-7,68 (м, 2H) 7,23-7,31 (м, 2H) 7,20 (д, J=9,16 Гц, 1H) 7,12 (д, J=6,78 Гц, 4H) 5,88-5,95 (м, 1H) 3,92 (д, J=6,78 Гц, 2H) 3,55 (с, 3H) 1,02-1,17 (м, 1H) 0,43-0,50 (м, 2H) 0,22-0,30 (м, 2H). MS (ESI+) m/z 468,1 [M+H]+.
Пример 348
4-[2-(циклопропилметокси)-5-(6-фторпиридин-3-ил)фенил]-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 348a
4-(2-(циклопропилметокси)-5-(6-фторпиридин-3-ил)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 348a получали согласно процедуре, используемой для получения продукта примера 6c, заменяя продуктом примера 334a продукт примера 6b и заменяя (6-фторпиридин-3-ил)бороновой кислотой продукт примера 6a, получая указанное в заголовке соединение.
Пример 348b
4-(2-(циклопропилметокси)-5-(6-фторпиридин-3-ил)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 348b получали согласно процедуре, используемой для получения продукта примера 6d, заменяя продуктом примера 348a продукт примера 6c, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 0,21-0,28 (м, 2H) 0,41-0,49 (м, 2H) 1,03-1,15 (м, 1H) 3,57 (с, 3H) 3,91 (д, J=6,78 Гц, 2H) 6,17 (т, J=2,71, 2,03 Гц, 1H) 7,17-7,28 (м, 3H) 733 (с, 1H) 7,63-7,69 (м, 2H) 8,23-8,32 (м, 1H) 8,54 (д, J=2,37 Гц, 1H) 11,95 (ушир.с, 1H). MS (ESI+) m/z 390 [M+H]+.
Пример 349
N-[4-(2,4-дифторфенокси)-3-(3-формил-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид
Пример 349a
4-бром-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Смесь продукта примера 1e (7 г, 18,36 ммоль) и моногидрата гидроксида лития (3,08 г, 73,4 ммоль) в тетрагидрофуране (50 мл) и воде (20 мл) нагревали при 80°C в течение ночи. После охлаждения до температуры окружающей среды реакционную смесь выливали в 300 мл воды. Полученное твердое вещество собирали вакуумным фильтрованием, получая указанное в заголовке соединение (3,92 г, 17,26 ммоль, выход 94%).
Пример 349b
4-бром-6-метил-1-((2-(триметилсилил)этокси)метил)-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 349a (3,92 г, 17,26 ммоль) в тетрагидрофуране (100 мл) обрабатывали 60% гидридом натрия (1,036 г, 25,9 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 10 минут. К этому раствору добавляли (2-(хлорметокси)этил)триметилсилан (4,58 мл, 25,9 ммоль). Реакционную смесь перемешивали в течение ночи. Полученное твердое вещество отфильтровывали и фильтрат концентрировали. Остаток очищали флаш-хроматографией (силикагель, 20% этилацетат в гептанах), получая указанное в заголовке соединение (5,84 г, выход 95%).
Пример 349c
4-бром-6-метил-7-оксо-1-((2-(триметилсилил)этокси)метил)-6,7-дигидро-1H-пирроло[2,3-c]пиридин-3-карбальдегид
Продукт примера 349b (3,92 г, 17,3 ммоль) в диметилформамиде (15 мл) обрабатывали оксихлоридом фосфoра (9,66 мл, 104 ммоль) по каплям при 0°C. После завершения добавления раствор нагревали при 80°C в течение 6 часов. После охлаждения до температуры окружающей среды реакционную смесь распределяли между водой и этилацетатом. Органический слой экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, 50-100% этилацетат/гептаны), получая указанное в заголовке соединение (1,35 г, выход 20,3%).
Пример 349d
4-(5-амино-2-(2,4-дифторфенокси)фенил)-6-метил-7-оксо-1-((2-(триметилсилил)этокси)метил)-6,7-дигидро-1H-пирроло[2,3-c]пиридин-3-карбальдегид
Продукт примера 349d получали согласно процедуре, используемой для получения продукта примера 138a, заменяя продуктом примера 349C 2-бром-1-фтор-4-(метилсульфонил)бензол и продуктом примера 148c продукт примера 6a, соответственно, получая указанное в заголовке соединение. После водной обработки сырой продукт использовали для следующей реакции без очистки.
Пример 349e
N-[4-(2,4-дифторфенокси)-3-(3-формил-6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид
Смесь продукта примера 349d (0,5 г, 0,951 ммоль), этансульфонил хлорида (0,226 мл, 2,38 ммоль) и триэтиламина (0,817 мл, 5,71 ммоль) в дихлорметане (10 мл) перемешивали при температуре окружающей среды в течение 2 часов. Растворитель выпаривали при пониженном давлении и остаток обрабатывали дихлорметаном (3 мл) и трифторуксусной кислотой (3 мл). Реакционную смесь перемешивали при температуре окружающей среды в течение 3 часов. Растворитель удаляли при пониженном давлении и остаток обрабатывали диоксаном (10 мл) и 2,0 н. NaOH (5 мл). Реакционную смесь нагревали при 90°C в течение 2 часов. После охлаждения до температуры окружающей среды реакционную смесь распределяли между водой и этилацетатом. Органический слой экстрагировали дополнительным этилацетатом дважды. Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, этилацетат), получая указанное в заголовке соединение (0,42 г, 0,862 ммоль, выход 91%). 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 13,07 (с, 1H), 9,78 (с, 1H), 9,40, (с, 1H), 7,99 (д, J=3,36 Гц, 1H), 7,38 (с, 1H), 7,23-7,31 (м, 3H), 6,89-6,97 (м, 3H), 3,55 (с, 3H), 3,10 (кв., J=7,32 Гц, 2H),1,21 (т, J=7,32 Гц, 3H). MS (ESI+) m/z 488,0 (M+H)+.
Пример 350
N-{4-(2,4-дифторфенокси)-3-[6-метил-3-(морфолин-4-илметил)-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил]фенил}этансульфонамид
Смесь продукта примера 349e (0,04 г, 0,082 ммоль), морфолина (0,014 г, 0,164 ммоль) и триацетоксигидробората натрия (0,035 г, 0,164 ммоль) в 1,2-дихлорэтане (2 мл) перемешивали при температуре окружающей среды в течение ночи. Растворитель выпаривали при пониженном давлении и остаток очищали ВЭЖХ с обращенной фазой (С18, 10-100% ацетoнитрил в 0,1% TFA/воде), получая TFA соль указанного в заголовке соединения (0,035 г, 0,052 ммоль, выход 63,4%). 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,59 (с, 1H), 9,86 (с, 1H), 9,58, (с, 1H), 7,56 (с, 1H), 7,26-7,38 (м, 4H), 7,00-7,09 (м, 2H), 6,93 (д, J=8,85 Гц, 1H), 4,23-4,29 (м, 1H), 3,75-3,81 (м, 3H), 3,52 (с, 3H), 3,16 (кв., J=7,32 Гц, 2H), 2,37-2,71 (м, 4H), 1,24 (т, J=7,32 Гц, 3H). MS (ESI+) m/z 558,9 (M+H)+.
Пример 351
N-[4-(2,4-дифторфенокси)-3-{6-метил-3-[(4-метилпиперазин-1-ил)метил]-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил}фенил]этансульфонамид
Продукт примера 351 получали согласно процедуре, используемой для получения продукта примера 350, заменяя 1-метилпиперазином морфолин, получая TFA соль указанного в заголовке соединения. 1H ЯМР (500 МГц, DMSO-d6) δ м.д. 12,11 (с, 1H), 9,86 (с, 1H), 9,58, (с, 1H), 7,29-7,35 (м, 2H), 7,20-7,22 (м, 2H), 7,11 (с, 1H), 6,97-7,06 (м, 2H), 6,91 (д, J=9,46 Гц, 1H), 3,85 (ушир. с, 4H), 3,48 (с, 3H), 3,12-3,40 (м, 4H), 2,69 (с, 3H), 1,25 (т, J=7,32 Гц, 3H). MS (ESI+) m/z 571,9 (M+H)+.
Пример 352
4-{2-[(циклопропилметил)амино]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 352a
2-бром-N-(циклопропилметил)анилин
Раствор 2-броманилина (1,720 г, 10,00 ммоль), циклопропанкарбальдегида (0,374 мл, 5,00 ммоль) и уксусной кислоты (2,86 мл, 50,0 ммоль) в дихлорметане (50 мл) нагревали при 50°C в течение 1 часа. Раствор охлаждали на бане со льдом и добавляли триацетоксиборгидрид натрия (2,119 г, 10,00 ммоль). Эту смесь перемешивали в течение 2 часов, пока она нагревалась до температуры окружающей среды, и затем распределяли между насыщенным раствором бикарбоната натрия (100 мл) и этилацетатом (100 мл). Органический слой сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток очищали колоночной флаш-хроматографией (силикагель, 0-10% этилацетат в гептане), получая указанное в заголовке соединение (1,05 г, выход 93%).
Пример 352b
4-(2-((циклопропилметил)амино)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 352b получали согласно процедуре, используемой для получения продукта примера 4a, заменяя продуктом примера 352a продукт примера 7c за исключением того, что реакционную смесь нагревали при 90°C в течение 2,5 часов и материал очищали колоночной флаш-хроматографией (силикагель, 0-5% метанол в дихлорметане), получая указанное в заголовке соединение.
Пример 352c
4-{2-[(циклопропилметил)амино]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Продукт примера 352c получали согласно процедуре, используемой для получения продукта примера 4b, заменяя продуктом примера 352b продукт примера 4a за исключением того, что реакционную смесь нагревали при 90°C в течение 2,5 часов и материал очищали колоночной флаш-хроматографией (силикагель, 0-5% метанол в дихлорметане), получая указанное в заголовке соединение. 1H ЯМР (400 МГц, CDCl3) δ м.д. 10,99 (с, 1H) 7,24-7,31 (м, 2H) 7,15 (дд, J=7,32, 1,53 Гц, 1H) 6,97 (с, 1H) 6,70-6,78 (м, 2H) 6,20-6,25 (м, 1H) 3,99 (с, 1H) 3,73 (с, 3H) 2,97 (д, J=6,41 Гц, 2H) 0,90-1,02 (м, 1H) 0,38-0,45 (м, 2H) 0,09-0,15 (м, 2H). MS (ESI+) m/z 294,0 (M+H)+.
Пример 353
4'-(циклопропилметокси)-3'-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бифенил-3-карбонитрил
Пример 353a
4'-(циклопропилметокси)-3'-(6-метил-7-оксо-1-тозил-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бифенил-3-карбонитрил
Продукт примера 353a получали согласно процедуре, используемой для получения продукта примера 6c, заменяя продуктом примера 334a продукт примера 6b и заменяя (3-цианофенил)бороновой кислотой продукт примера 6a, получая указанное в заголовке соединение.
Пример 353b
4'-(циклопропилметокси)-3'-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)бифенил-3-карбонитрил
Продукт примера 353b получали согласно процедуре, используемой для получения продукта примера 6d, заменяя продуктом примера 353a продукт примера 6c, получая указанное в заголовке соединение. 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 0,21-0,28 (м, 2H) 0,41-0,49 (м, 2H) 1,00-1,15 (м, 1H) 3,58 (с, 3H) 3,91 (д, J=6,78 Гц, 2H) 6,17 (т, J=2,03 Гц, 1H) 7,20 (д, J=8,48 Гц, 1H) 7,26 (т, J=2,71 Гц, 1H) 7,33 (с, 1H) 7,63 (т, J=7,80 Гц, 1H) 7,67-7,79 (м, 3H) 8,03 (д, J=8,14 Гц, 1H) 8,16 (т, J=1,70 Гц, 1H) 11,94 (ушир.с, 1H). MS (ESI+) m/z 396 [M+H]+.
Пример 354
4-{2-(циклопропилметокси)-5-[(4-гидроксипиперидин-1-ил)сульфонил]фенил}-6-метил-1,6-дигидро-7H-пирроло[2,3-c]пиридин-7-он
Пример 354a
1-(3-бром-4-фторфенилсульфонил)пиперидин-4-ол
Продукт примера 354a получали согласно процедуре, описанной для получения продукта примера 310a, заменяя пиперидин-4-олом N,N-диметилпирролидин-3-амин, получая указанное в заголовке соединение.
Пример 354b
1-(3-бром-4-фторфенилсульфонил)-4-(тетрагидро-2H-пиран-2-илокси)пиперидин
3,4-Дигидро-2H-пиран (0,28 мл, 3,1 ммоль) добавляли по каплям при 0°C к раствору продукта примера 354a (0,51 г, 1,5 ммоль), гидрату 4-метилбензолсульфоновой кислоты (0,59 г, 3,1 ммоль) и дихлорметана (28 мл). Реакционную смесь перемешивали при температуре окружающей среды в течение 5 часов. Воду добавляли и смесь экстрагировали дихлорметаном. Органический слой промывали водой, насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток очищали флаш-хроматографией (силикагель, дихлорметан/градиент с метанолом), получая указанное в заголовке соединение (420 мг, выход 65,9%).
Пример 354c
1-(3-бром-4-(циклопропилметокси)фенилсульфонил)-4-(тетрагидро-2H-пиран-2-илокси)пиперидин
Продукт примера 354c получали согласно процедуре, используемой для получения продукта примера 29a, заменяя циклопропилметаноом тетрагидро-2H-пиран-4-ол и заменяя продуктом примера 354b продукт примера 2a, получая указанное в заголовке соединение.
Пример 354d
4-(2-(циклопропилметокси)-5-(4-(тетрагидро-2H-пиран-2-илокси)пиперидин-1-илсульфонил)фенил)-6-метил-1-тозил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 354d получали согласно процедуре, используемой для получения продукта примера 6c, заменяя продуктом примера 354c продукт примера 6b, получая указанное в заголовке соединение.
Пример 354e
4-(2-(циклопропилметокси)-5-(4-(тетрагидро-2H-пиран-2-илокси) пиперидин-1-илсульфонил)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Продукт примера 354e получали согласно процедуре, используемой для получения продукта примера 6d, заменяя продуктом примера 354d продукт примера 6c, получая указанное в заголовке соединение.
Пример 354f
4-(2-(циклопропилметокси)-5-(4-гидроксипиперидин-1-илсульфонил)фенил)-6-метил-1H-пирроло[2,3-c]пиридин-7(6H)-он
Раствор продукта примера 354e (54 мг, 0,10 ммоль), уксусной кислоты (4 мл, 69,9 ммоль), тетрагидрофурана (2 мл) и воды (1 мл) перемешивали при 45°C в течение 2,5 часов. Реакционную смесь концентрировали до сухости и остаток сушили в течение ночи (в вакууме). Сырой продукт растирали с простым диэтиловым эфиром, фильтровали и сушили (в вакууме), получая указанное в заголовке соединение (30 мг, выход 66%). 1H ЯМР (300 МГц, DMSO-d6) δ м.д. 0,25-0,31 (м, 2H) 0,44-0,51 (м, 2H) 1,08-1,17 (м, 1H) 1,38-1,51 (м, 2H) 1,70-1,80 (м, 2H) 2,70-2,80 (м, 2H) 3,10-3,18 (м, 2H) 3,51-3,56 (м, 1H) 3,57 (с, 3H) 3,97 (д, J=6,78 Гц, 2H) 4,66 (д, J=4,07 Гц, 1H) 6,12 (т, J=2,71, 2,03 Гц, 1H) 7,27-7,32 (м, 2H) 7,36 (с, 1H) 7,64-7,70 (м, 2H) 12,04 (ушир.с, 1H). MS (ESI+) m/z 458 [M+H]+.
Биологические примеры
Анализ связывания бромдомена
Анализ флуоресцентного резонансного энергетического переноса с разрешением во времени (TR-FRET) использовали для определения сродства соединений из примеров, указанных в таблице 1 для каждого бромдомена BRD4 человека. His-нацеленные первый (BD1: аминокислоты K57-E168) и второй (BD2: аминокислоты E352-E168) бромдомены BRD4 человека экспрессировали и очищали. Alexa647-меченный BET-ингибитор использовали в качестве флуоресцентной пробы в анализе.
Синтез Alexa647-меченного бромдомен ингибирующего соединения 2-((6S,Z)-4-(4-хлорфенил)-2,3,9-триметил-6H-тиено[3,2-f][1,2,4]триазолo[4,3-a][1,4]диазепин-6-ил)уксусной кислоты. Метил 2-((6S,Z)-4-(4-хлорфенил)-2,3,9-триметил-6H-тиено[3,2-f][1,2,4]триазолo[4,3-a][1,4]диазепин-6-ил)ацетат (смотри, например, WO 2006129623) (100,95 мг, 0,243 ммоль) суспендировали в 1 мл метанола, к которому добавляли свежеприготовленный раствор моногидрата гидроксида лития (0,973 мл, 0,5 M, 0,487 ммоль) и встряхивали при температуре окружающей среды в течение 3 часов. Метанол выпаривали и pH доводили водной хлороводородной кислотой (1 M, 0,5 мл, 0,5 ммоль) и экстрагировали четыре раза этилацетатом. Объединенные этилацетатные слои сушили над сульфатом магния и концентрировали, получая 2-((6S,Z)-4-(4-хлорфенил)-2,3,9-триметил-6H-тиено[3,2-f][1,2,4]триазолo[4,3-a][1,4]диазепин-6-ил)уксусную кислоту (85,3 мг, 87,0%); ESI-MS m/z=401,1 [(M+H)+], которую использовали непосредственно в следующей реакции.
N-(2-(2-(2-аминоэтокси)этокси)этил)-2-((6S,Z)-4-(4-хлорфенил)-2,3,9-триметил-6H-тиено[3,2-f][1,2,4]триазолo[4,3-a][1,4]диазепин-6-ил)ацетамид бис(2,2,2-трифторацетат). 2-((6S,Z)-4-(4-хлорфенил)-2,3,9-триметил-6H-тиено[3,2-f][1,2,4]триазолo[4,3-a][1,4]диазепин-6-ил)уксусную кислоту (85,3 мг, 0,213 ммоль) объединяли с 2,2'-(этан-1,2-диилбис(окси))диэтанамином (Sigma-Aldrich, 0,315 мг, 2,13 ммоль) объединяли в 5 мл безводного диметилформамида. Гексафторфосфат(V) (1H-бензо[d][1,2,3]триазол-1-илокси)трипирролидин-1-илфосфoния (PyBOB, CSBio, Menlo Park CA; 332 мг, 0,638 ммоль) добавляли и реакционную смесь встряхивали при температуре окружающей среды в течение 16 часов. Реакционную смесь разбавляли до 6 мл смесью диметилсульфоксид:вода (9:1, об/об) и очищали в два впрыскивания в колонку time collection Waters Deltapak C18 200 × 25 мм, элюируя с градиентом 0,1% трифторуксусной кислоты (об/об) в воде и ацетoнитриле. Фракции, содержащие два очищенных продукта, лиофилизовали, получая N-(2-(2-(2-аминоэтокси)этокси)этил)-2-((6S,Z)-4-(4-хлорфенил)-2,3,9-триметил-6H-тиено[3,2-f][1,2,4]триазолo[4,3-a][1,4]диазепин-6-ил)ацетамид бис(2,2,2-трифторацетат) (134,4 мг, 82,3%); ESI-MS m/z=531,1 [(M+H)+]; 529,1 [(M-H)-] и (S,Z)-N,N'-(2,2'-(этан-1,2-диилбис(окси))бис(этан-2,1-диил))бис(2-((6S,Z)-4-(4-хлорфенил)-2,3,9-триметил-6H-тиено[3,2-f][1,2,4]триазолo[4,3-а][1,4]диазепин-6-ил)ацетамид) бис(2,2,2-трифторацетат) (3,0 мг, 1,5%); ESI-MS m/z=913,2 [(M+H)+]; 911,0 [(M-H)-].
N-(2-(2-(2-амидо-(Alexa647)этокси)этокси)этил)-2-((6S,Z)-4-(4-хлорфенил)-2,3,9-триметил-6H-тиено[3,2-f][1,2,4]триазолo[4,3-a][1,4]диазепин-6-ил)ацетамид(2,2,2-трифторацетат). N-(2-(2-(2-аминоэтокси)этокси)этил)-2-((6S,Z)-4-(4-хлорфенил)-2,3,9-триметил-6H-тиено[3,2-f][1,2,4]триазолo[4,3-a][1,4]диазепин-6-ил)ацетамид бис(2,2,2-трифторацетат) (5,4 мг, 0,0071 ммоль) объединяли с Alexa Fluor® 647 карбоновой кислотой, сукцинимидиловым сложным эфиром (Life Technologies, Grand Island, NY; 3 мг, 0,0024 ммоль), объединяли в 1 мл безводного диметилсульфоксида, содержащего диизопропилэтиламин (1% об/об), и встряхивали при температуре окружающей среды в течение 16 часов. Реакционную смесь разбавляли до 3 мл смесью диметилсульфоксид:вода (9:1, об:об) и очищали в один впрыск на колонке time collection Waters Deltapak С18 200 × 25 мм, элюируя с градиентом 0,1% трифторуксусной кислоты (об/об) в воде и ацетoнитриле. Фракции, содержащие очищенный продукт, лиофилизовали, получая N-(2-(2-(2-амидо-(Alexa647)-этокси)этокси)этил)-2-((6S,Z)-4-(4-хлорфенил)-2,3,9-триметил-6H-тиено[3,2-f][1,2,4]триазолo[4,3-a][1,4]диазепин-6-ил)ацетамид(2,2,2-трифторацетат) (1,8 мг); MALDI-MS m/z=1371,1, 1373,1 [(M+H)+], в виде темно-синего порошка.
Анализ
Последовательные разбавления соединения готовили в DMSO путем 3-кратного последовательного разбавления от 2,5 мM до 42 нM. Соединения затем разбавляли 6:100 в буфере для анализа (20 мM Фосфат натрия, pH 6,0, 50 мM NaCl, 1 мM дигидрат динатриевой соли этилендиаминтетрауксусной кислоты, 0,01% Triton X-100, 1 мM DL-дитиотреитол), получая 3X рабочие растворы. Шесть микролитров (мкл) рабочего раствора затем переносили на белые мелкосерийные планшеты для анализа (Costar #3673). 1,5X смеси для анализа, содержащей His-нацеленный бромдомен, европий-конъюгированное анти-His антитело (Invitrogen PV5596) и Alexa-647-конъюгированную пробную молекулу также готовили. Двенадцать мкл указанного раствора добавляли на планшет для анализа до достижения конечного объема 18 мкл. Конечная концентрация буфера для анализа IX содержит 2% DMSO, 50 мкM - 0,85 нM соединения, 8 нM His-нацеленного бромдомена, 1 нM европий-конъюгированного анти-His-tag антитела и 100 нM или 30 нM пробы (для BDI или BDII, соответственно). После одночасовой инкубации при комнатной температуре определяли отнощения TR-FRET, используя Envision мультимеченный планшет-ридер (Ex 340, Em 495/520).
Данные TR-FRET нормализовали до значений 24 контролей несоединений ("высокие") и 8 контролей, содержащих 1 мкМ немеченной пробы ("низкие"). Процентное ингибирование наносили на график как функцию концентрации соединения и данные приводили в соответствие с логистическим уравнением 4 параметров, чтобы получить IC50s. Крнстанты ингибирования (Ki) рассчитывали из IC50s, Kd пробы и концентрации пробы. Типичные Z' величины были между 0,65 и 0,75. Минимальное значимое отношение определяли для оценки воспроизводимости анализа (Eastwood et al., (2006) J Biomol. Screen, 11: 253-261). MSR определяли как 2,03 для BDI и 1,93 для BDII, и скользащий MSR (последние шесть прогонов овертайма MSR) и для BDI, и для BDII был обычно <3. Величины Ki представлены в таблице 1.
Анализ пролиферации MX-1 клеточной линии
Воздействие соединений из примеров на пролиферацию раковых клеток определяли, используя клеточную линию рака молочной железы MX-1 (ATCC) в анализе 3-дневной пролиферации. MX-1 клетки поддерживали в среде RPMI 1640 (Sigma), обогащенной 10% FBS (фетальная бычья сыворотка) при 37°C и в атмосфере 5% CО2. Для испытания соединения MX-1 клетки помещали в 96-луночные планшеты с черным дном при плотности 5000 клеток/лунка в 90 мкл культуральной среды и инкубировали при 37°C в течение ночи, чтобы дать возможность для клеточной адгезии и распространения. Последовательные разбавления соединения готовили в DMSO посредством 3-кратного последовательного разбавления от 3 мM до 0,1 мкM. Серии разбавлений DMSO затем разбавляли 1:100 в забуференном фосфатом солевом растворе и 10 мкл полученного раствора добавляли в соответствующие лунки планшета с MX-1 клетками. Конечные концентрации соединения в лунках были 3, 1, 0,3, 0,1, 0,03, 0,01, 0,003, 0,001, 0,0003 и 0,0001 мкM. После добавления соединений клетки инкубировали в течение 72 часов и количества живых клеток определяли с помощью набора для анализа Cell Titer Glo assay (Promega) в соответствии с утвержденным производителем протоколом. Данные по люминесценции из анализа Cell Titer Glo assay нормализовали к обработанным DMSO клеткам и анализировали с помощью компьютерных программ GraphPad Prism с аппроксимацией сигмоидальной кривой, чтобы получить EC50s. Минимальное значимое отношение (MSR) определяли для оценки воспоизводимости анализа (Eastwood et al., (2006) J Biomol. Screen, 11: 253-261). Общий MSR определяли как 2,1 и скользящий MSR (последние шесть прогонов овертайма MSR) был <2.
Панельный анализ пролиферации
Соединения из примеров 4 и 78 испытывали на их воздействие на пролиферацию панели типов линий раковых клеток (со специфическими испытуемыми клеточными линиями), как показано в таблице 2. Клетки помещали в 96-луночные планшеты при 1500 клеток/лунку в подходящей культуральной среде без испытуемого соединения и инкубировали в течение ночи при 37°C и в атмосфере 5% CО2. Серии разбавлений соединений готовили и добавляли в лунки как в анализе MX-1 пролиферации. После добавления соединений клетки инкубировали следующие 3 дня 37°C и в атмосфере 5% CО2. Количества живых клеток определяли с помощью набора для анализа Cell Titer Glo assay kit (Promega) в соответствии с протоколом, утвержденным производителем. Данные пролиферации клеток анализировали, как описано выше в анализе MX-1 пролиферации, получая EC50 для соединений из примеров 4 и 78, и представляли в таблице 2.
NA значения не определены
Анализ стабильности микросом человека, крысы и мыши
Анализы стабильности микросом проводили на соединениях примеров, указанных в таблице 3 ("испытуемые соединения"). Человечьи, крысиные и мышиные микросомальные инкубации проводили при 37°С с кончным объемом инкубации 135 мкл. Микросомы печени человека (смешанный пол, № по каталогу H2610) получали от XenoTech. Микросомы печени крысы (самец Sprague-Dawley, № по каталогу 42501) получали от BD Gentest. Микросомы печени мыши (самец CD1, № по каталогу 452701) получали от BD Gentest. Инкубации проводили, используя испытуемое соединение (в начале растворенное в DMSO при концентрации 5 мкM) в концентрации 0,5 мкM и 0,25 мг/мл микросомального белка в 50 мM фосфатном буфере при pH 7,4. Образцы времени ноль готовили путем перемещения 13,5 мкл смеси соединения и микросомальной фракции на гасящие планшеты, содержащие 45 мкл гасящего раствора, приготовленного из 10 нM буспирона (Sigma) или 50 нM кабутамида (Princeton Bio) в качестве внутреннего стандарта в смеси 1:1 метанол:ацетoнитрил. Аликвотную пробу 1,5 мкл редуцированной тетранатриевой соли никотинамид аденин динуклеотид фосфата (NADPH) также добавляли к планшетам времени ноль. Реакцию затем инициировали добавлением 13,5 мкл NADPH к смеси соединение-микросомальная фракция. В каждый из остальных моментов времени (5, 10, 15, 20 и 30 мин) 15 мкл смеси для инкубирования добавляли к 45 мкл гасящего раствора. Образцы центрифугировали в течение 15-30 минут при 3800 обор. в мин. Образцы затем сливали по 6 на группу. Аликвотную пробу 60 мкл супернатанта переносили на 384-луночный планшет и аликвотную пробу 5 мкл впрыскивали и анализировали LC-MS/MS (Applied Biosystems API 5500 QTrap). Собственный клиренс соединения рассчитывали путем преобразования отношений площадей пиков (площадь пика аналита/площадь пика IS) к % остающегося источника, принимая отношение площадей во время 0 за 100%. Наклон (k) определяли из графика % остающегося источника против времени инкубирования, из которого затем выводили период полужизни (t1/2; минуты), собственный клиренс (CLint; мкл/мин/мг белка для микросом печени и мкл/мин/миллион клеток для гепатоцитов) и относительный собственный клиренс (относительный CLint; л/ч/кг). Величины t1/2 приведены в таблице 3. Термин "N/A" означает "не определено".
Анализ на мышах индуцированного LPS (липополисахаридом) продуцирования IL-6
Соединения из примеров, указанных в таблице 4, анализировали на их стабильность в ингибировании индуцированного LPS (липополисахаридом) продуцирования IL-6 у мышей. Самки мышей Fox Chase SCID® (Charles Rivers Labs, 8 на группу) получали интраперитонеальное введение липополисахарида (2,5 мг/кг, L2630 E.coli 0111:B4) через час после перорального введения соединений. Мышей умерщвляли через 2 часа после инъекции липополисахарида, кровь удаляли пункцией сердца и затем сыворотку, собранную из проб крови, замораживали при -80°C. В день анализа пробы сыворотки доводили до комнатной температуры и затем разбавляли 1:20 в забуференном фосфатом солевом растворе, содержащем 2% альбумина бычьей сыворотки. Измерения интерлейкина-6 осуществляли, используя анализ цитокина от Meso Scale Discovery (Gaithersburg, Maryland) для анализа мышиной сыворотки согласно протоколу производителя и считывали данные на приборе SECTOR Imager 6000 (Meso Scale Discovery, Gaithersburg, Maryland). Статистический анализ проводили, используя компьютерную программу Prism (version 5,0) включающую Dunnett's one way ANOVA. Среднее значение IL-6 и стандартное отклонение для группы обработанных носителем животных сравнивали со средним значением IL-6 и стандартным отклонением для группы, обработанной испытуемым соединением. Величина p<0,05 означает, что существует вероятность менее чем 5% того, что средние величины в двух группах окажутся равными. Величины % ингибирования в таблице 4 все обнаруживали величину р менее чем 0,05.
Ингибирование индуцируемого LPS продуцирования IL-6 у мышей
Анализ ингибирования роста опухоли ксенотрансплантата
Воздействие соединения из примера 36 на ингибирование роста OPM-2 и MX-1 опухолей ксенотрансплантата, имплантированных мышам, оценивали. Кратко, 5 × 106 раковых клеток человека (OPM-2) или 1:10 tumor brie (MX-1) (в S-MEM (MEM, суспензия, без кальция, без глутамина)) (Life Technologies Corporation) инокулировали подкожно в правый задний бочок самки SCID-beige или самки Fox Chase SCID® (Charles River Labs) мыши, соответственно, на день 0 исследования. Введение соединения (в (2% EtOH, 5% Tween-80, 20% PEG-400, 73% HPMC))(PO, QDx14) начинали во время подходящего размера на день 17 (OPM-2) или день 12 (MX-1). Опуходи измеряли парой калибров дважды в неделю, начиная во время подходящего размера и объемы опухоли рассчитывали по формуле V=L×W2/2 (V: объем, мм3; L: длина, мм2. W: ширина, мм). Объем опухоли измеряли для продолжения эксперимента до тех пор, пока средний объем опухоли в каждой группе не достигнет конечной точки >1000 мм3 для OPM-2 или до дня 27 после инокуляции для MX-1. Результаты показаны в таблицах 5 и 6.
Модель на ксенотрансплантате рака множественной миеломы человека OPM-2
b. Задержка роста опухоли, % TGD=(T-С)/С×100, где T = среднее время до конечного пункта группы обработки и С = среднее время до конечного пункта контрольной группы. Величины p (как показано звездочками) выведены из сравнения Kaplan Meier log-rank группы обработки против контрольной группы. На основе конечного пункта 1000 мм3. *p<0,05, **p<0,01,***p<0,001.
Эффективность ВЕТ ингибитора на модели на ксенотрансплантате рака молочной железы человека МХ-1
Исследования эффективности на ксенотрансплантате проводили с дополнительными соединениями из примеров, используя OPM-2, MX-1, HT1080, MV4-11, SKM1 и Ramos раковые клетки человека. Раковые клетки получали из культуры или из tumor brie (MX-1), как описанно выше, и инокулировали подкожно в правый задний бочок самки мышей SCID-beige (OPM-2, HT1080, MV4-11) или самки мышей Fox Chase SCID® (Charles River Labs) (MX-1, SKM1, Ramos). Введение соединения начинали во время подходящего размера. Опухоли измеряли парой калибров дважды в неделю, начиная во время подходящего размера, и объемы опухоли рассчитывали по формуле V=L×W2/2 (V: объем, мм3; L: длина, мм2. W: ширина, мм). Объем опухоли измеряли для продолжения эксперимента до тех пор, пока средний объем опухоли в каждой группе не достигнет зависимой от модели конечной точки 500-2000 мм3. Результаты показаны в таблице 7.
Эффективность ВЕТ ингибиторов на модели на ксенотрансплантате человека
А: 10% EtOH, 30% PEG 400, 60% Phosol 53 MCT (Lipoid AG)
В: 10% EtOH, 30% PEG 400, 60% Phosol 53 MCT (Lipoid AG)/0,9% солевой раствор
С: 0,9% солевой раствор
D: 10% EtOH, 27,5% PEG 400, 60% Phosol 53 MCT (Lipoid AG)
E: 10% EtOH, 27,5% PEG 400, 60% Phosol 53 MCT (Lipoid AG)/0,9% солевой раствор
F: 2% EtOH, 5% Tween-80, 20% PEG400, 73% 0,2% HPMC
G: 2% EtOH, 5% Tween-80, 20% PEG400, 73% 0,2% НРМС/0,9% солевой раствор и
H: 5% EtOH, 30% PEG 400, 60% Phosol 53 MCT (Lipoid AG)
b. Ингибирование роста опухоли, % TGI=100 – средний объем опухоли группы обработки/средний объем опухоли контрольной группы × 100. Число мышей на группу обработки = 8 (MX-1, MV4-11, SKM1) или 10 (OPM-2). Величины p (как показано звездочками) выведены из сравнения критерия Стьюдента группы обработки против контрольной группы. На основе на день 31. *p<0,05, **p<0,01, ***p<0,001. Величины %TGI не представлены, если смертность ≥40%.
с. Задержка роста опухоли, % TGD=(T-С)/С×100, где T = среднее время до конечного пункта группы обработки и С = среднее время до конечного пункта контрольной группы. Величины p (как показано звездочками) выведены из сравнения Kaplan Meier log-rank группы обработки против контрольной группы. *p<0,05, **p<0,01, ***p<0,001 не представлены, если смертность ≥40%.
ND=не определено
Модель артрита, индуцированного коллагеном, на крысах in vivo
Соединение из примера 36 ингибирует опухание лапы из-за воспаления на крысиной модели индуцированного коллагеном артрита (rCIA). На день 0 самок крыс Lewis модели rCIA (n=9/группа) иммунизировали интрадермально (id) 600 мкг бычьего коллагена типа II в эмульсии с неполным адъювантом Фрейнда (IFA). Иммунизацию давали в трех местах интрадермальной инъекцией по 100 мкмл на каждом месте. На день 6 крыс поддерживали 600 мкг бычьего коллагена типа II способом идентичным протоколу первоначальной иммунизации. Контрольная группа крыс получала такой же объем только IFA также на день 0 и день 6. Используя систему вытеснения воды плетизмографа, объем лапы измеряли на день 7 (измерение базовой линии) и на дни 10, 12, 14 и 17. Группы, получающие дозы, включали иммунизированных IFA неартритных крыс, обработанных носителем PBS, обработанных преднизолоном (3 мг/кг, положительный контроль), обработанных носителем соединения (10% EtOH/30% PEG400/ 60% Phosal 53) и продуктом примера 36, дозируемым перорально при 1,0, 0,3, 0,1, и 0,03 мг/кг. Дозирование начинали на день 10 и животных обрабатывали раз в день до дня 17 путем перорального дозирования 1,0 мл объема. Опухание лапы представлено как изменение объема лапы от базовой линии и площадь над кривой (AUC) рассчитывали для опухания лапы в каждой получавшей дозу группе. Продукт примера 36 ингибировал воспаление артритной лапы в зависимости от дозы с ED50 0,21 мг/кг и ED80 0,69 мг/кг соответственно максимальным концентрациям в плазме 6,8 нг/мл и 22,3 нг/мл при ED50 и ED80, соответственно.
Понятно, что предшествующее подробное описание и сопровождающие примеры являются только пояснительными и не должны рассмативаться как ограничения объема изобретения, который определено только прилагаемыми пунктами формулы изобретения и их эквивалентами. Различные изменения и модификации раскрытых вариантов осуществления должны быть очевидны для специалистов в этой области. Такие изменения и модификации, включая, без ограничения, те, которые относятся к химическим структурам, заместителям, производным, промежуточным соединениям, синтезам, составам и/или способам применения изобретения, могут быть сделаны, не выходя за пределы сущности и объема изобретения. Все публикации, патенты и патентные заявки, цитируемые в данном описании, тем самым включены сюда ссылкой во всей их полноте для всех целей.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНГИБИТОРЫ БРОМДОМЕНА | 2012 |
|
RU2647592C2 |
| ИНГИБИТОРЫ БРОМОДОМЕНА | 2017 |
|
RU2741808C2 |
| ПРОИЗВОДНЫЕ ПИРРОЛОПИРИДИНОНА В КАЧЕСТВЕ TTX-S БЛОКАТОРОВ | 2013 |
|
RU2646754C2 |
| ЗАМЕЩЕННЫЕ ТРИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И СПОСОБ ПРИМЕНЕНИЯ | 2016 |
|
RU2744766C2 |
| НОВОЕ ПИРРОЛОПИРИМИДИНОВОЕ СОЕДИНЕНИЕ ИЛИ ЕГО СОЛЬ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЕЕ, В ЧАСТНОСТИ, АГЕНТ ДЛЯ ПРЕДОТВРАЩЕНИЯ И/ИЛИ ЛЕЧЕНИЯ ОПУХОЛЕЙ, И ТОМУ ПОДОБНОЕ, НА ОСНОВЕ ИНГИБИТОРНОГО ВОЗДЕЙСТВИЯ НА NAE | 2015 |
|
RU2658008C2 |
| ПРОИЗВОДНЫЕ ПИРИДИНОНА И ПИРИДАЗИНОНА | 2012 |
|
RU2632915C2 |
| БИЦИКЛИЧЕСКИЕ НИТРОИМИДАЗОЛЫ, КОВАЛЕНТНО СОЕДИНЕННЫЕ С ЗАМЕЩЕННЫМИ ФЕНИЛОКСАЗОЛИДИНОНАМИ | 2009 |
|
RU2504547C2 |
| УСИЛИТЕЛЬ ПРОТИВООПУХОЛЕВОГО ВОЗДЕЙСТВИЯ, СОДЕРЖАЩИЙ СОЕДИНЕНИЕ ПИРРОЛОПИРИМИДИНА | 2016 |
|
RU2710380C1 |
| ИНГИБИТОРЫ ПРОТЕИНКИНАЗ ДЛЯ УСИЛЕНИЯ РЕГЕНЕРАЦИИ ПЕЧЕНИ ИЛИ СНИЖЕНИЯ ИЛИ ПРЕДОТВРАЩЕНИЯ ГИБЕЛИ ГЕПАТОЦИТОВ | 2019 |
|
RU2822216C2 |
| СОЕДИНЕНИЯ АЗАЛАКТАМА В КАЧЕСТВЕ ИНГИБИТОРОВ HPK1 | 2019 |
|
RU2801140C2 |
Изобретение относится к соединению N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамиду или его фармацевтически приемлемой соли. Также предложены фармацевтическая композиция, содержащая указанное соединение, способы лечения рака, острой почечной болезни или состояния, синдрома приобретенного иммунодефицита (СПИД) и способ контрацепции у субъекта мужского рода. Технический результат: получено соединение, обладающее ингибирующей BET бромдомен активностью. 6 н. и 2 з.п. ф-лы, 8 табл., 354 пр.
1. Соединение N-[4-(2,4-дифторфенокси)-3-(6-метил-7-оксо-6,7-дигидро-1H-пирроло[2,3-c]пиридин-4-ил)фенил]этансульфонамид или его фармацевтически приемлемая соль.
2. Фармацевтическая композиция, обладающая ингибирующей бромдомен активностью, содержащая соединение по п.1 или его фармацевтически приемлемую соль в комбинации с фармацевтически приемлемым носителем.
3. Способ лечения рака у субъекта, выбранного из группы, включающей острую лейкемию, рак мочевого пузыря, рак молочной железы, рак толстой кишки, глиобластому, гепатоцеллюлярный рак, неходжкинскую лимфому, рак молочной железы, рак поджелудочной железы, рак простаты, немелкоклеточный рак легкого, почечно-клеточную [светлоклеточную] карциному, саркому, включающий введение терапевтически эффективного количества соединения формулы (I) по п.1 или его фармацевтически приемлемой соли субъекту, нуждающемуся в этом.
4. Способ лечения острой почечной болезни или состояния у субъекта, содержащий введение терапевтически эффективного количества соединения формулы (I) по п.1 или его фармацевтически приемлемой соли субъекту, нуждающемуся в этом, где указанная острая почечная болезнь или состояние выбраны из группы, состоящей из таких как: вызванные ишемией-реперфузией, вызванные сердечной и радикальной хирургией, вызванные перкутанным коронарным вмешательством, вызванные радиоактивным контрастным агентом, вызванные сепсисом, вызванные пневмонией и вызванные токсичностью лекарства.
5. Способ лечения синдрома приобретенного иммунодефицита (СПИД) у субъекта, содержащий введение терапевтически эффективного количества соединения формулы (I) по п.1 или его фармацевтически приемлемой соли субъекту, нуждающемуся в этом.
6. Способ контрацепции у субъекта мужского рода, содержащий введение терапевтически эффективного количества соединения формулы (I) по п.1 или его фармацевтически приемлемой соли субъекту мужского рода, нуждающемуся в этом.
7. Способ по п.3, где рак представляет собой рак простаты.
8. Способ по п.3, где рак представляет собой острую лейкемию.
| Качающийся парораспределительный золотник для паровых машин и в частности, для паровозных | 1933 |
|
SU39127A1 |
| WO 2004094417 A1, 04.11.2004 | |||
| WO 2011161031 A1, 29.12.2011 | |||
| НОВЫЕ КОНДЕНСИРОВАННЫЕ ПРОИЗВОДНЫЕ ИМИДАЗОЛА, ИНГИБИТОР ДИПЕПТИДИЛПЕПТИДАЗЫ IV, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЛЕЧЕНИЯ И ПРИМЕНЕНИЕ НА ИХ ОСНОВЕ | 2003 |
|
RU2297418C9 |
Авторы
Даты
2018-11-02—Публикация
2012-12-11—Подача