Изобретение относится к области молекулярной биологии, препаративной биохимии, биотехнологии, биофармакологии, а именно к созданию способов получения рекомбинантных белков семейства цистеиновых протеиназ пшеницы (Triticum aestivum) в растворимой форме и препараты белка тритикаина-альфа, состоящие из фрагмента тритикаина-альфа пшеницы. Изобретение может быть использовано в исследовательских целях для изучения функционирования папаин-подобных цистеиновых протеиназ, а также в медицине для разработки ферментных терапевтических препаратов.
Тритикаины (triticain-α, -β, -γ) - высококонсервативные папаин-подобные цистеиновые эндопротеазы пшеницы, состоящие из сигнального (лидерного) пептида, удаляющегося при активации про-пептидного домена, гранулин-подобного домена [GenBank АВ267407] и каталитического домена с каталитической триадой Cys-His-Asn [1]. Цистеиновые протеиназы распространены в растениях и экспрессируются в их различных органах [2, 3]. Предполагается, что эти ферменты участвуют в стадиеспецифическом расщеплении и пост-трансляционных модификациях запасающих белков [4, 5]. Среди папаин-подобных цистеиновых протеиназ растений наиболее широко изучены ферменты риса и ячменя - оризаины (oryzain-α, -β, -γ) и эндопептидазы ЕРВ (barley cysteine proteinase B-1, -2) [6, 7], однако протеазы пшеницы начали изучать относительно недавно [1, 8].
Основным преимуществом папаин-подобных цистеиновых протеиназ из семян растений на данный момент является их эндопептидазная активность, в частности, глютеназная активность - способность эффективно гидролизовать пептиды глютена (запасного белка пшеницы, состоящего из смеси мономерных глиадинов и полимерных глютенинов) или родственных запасных белков ржи и ячменя. Это свойство растительных ферментов позволяет считать их перспективными объектами при разработке лекарственных средств для борьбы с целиакией. Целиакия (глютеновая энтеропатия) представляет собой комплексное воспалительное заболевание человека, которое развивается при наличии соответствующей генетической предрасположенности в ответ на обогащенные остатками пролина и глутамина пептиды, являющиеся продуктами происходящего в пищеварительном тракте частичного протеолиза глютена [9, 10]. Распространенность глютеновой энтеропатии во взрослой популяции большинства стран мира оценена как 1:100 - 1:250 или 0.5-1% от общей популяции [11]. Доказанной эффективной терапией целиакии является пожизненная строгая безглютеновая диета, позволяющая предотвратить развитие осложнений и исключить клинические симптомы заболевания [12]. Однако главным недостатком безглютеновой диеты является сложность ее соблюдения из-за ее ограничительного характера, обусловленного как высокой стоимостью, так и сложностью подбора глютен-несодержащих продуктов питания.
В связи с этим, исследование и разработка способов получения высокоспецифичных протеиназ, стабильных и активных в присутствии эндогенных ферментов желудочно-кишечного тракта человека (т.е. в месте предполагаемого действия лекарственного препарата на их основе) имеет большое значение в терапевтических целях [13].
Из литературы известен метод получения проэнзимной формы цистеиновой протеиназы ячменя ЕР-В2 (proЕР-В2) в E.coli. [14, 15].
В рамках данного изобретения была выбрана протеиназа пшеницы Triticum aestivum - тритикаин-альфа, т.к. пшеница играет существенную роль как источник питания в России, а значит, наиболее подходящая для разработки отечественных терапевтических препаратов для лечения целиакии.
Молекула полноразмерного тритикаина-альфа состоит из 461 аминокислотного остатка с молекулярным весом 50,4 кДа. Впервые фермент был клонирован и экспрессирован в зародыше и алейроновом слое пшеницы для выяснения его роли в процессе созревания семян [1]. Однако непосредственно белок тритикаин-альфа выделен не был.
Биосинтез рекомбинантного тритикаина-альфа для исследования его протеолитических функций был осуществлен нами ранее [16, 17]. В описанном способе рекомбинантный тритикаин-альфа (фрагмент полноразмерного белка) синтезировался в бактериальных клетках в нерастворимой форме, что требовало включения дополнительной, трудно валидируемой, стадии рефолдинга в процессе выделения целевого белка. Также, полученные препараты обладали меньшей активностью, чем полученные препараты в настоящей заявке, а также обладали меньшим выходом при выделении и меньшей чистотой.
Задачей, решаемой в рамках настоящей заявки, является расширение ассортимента ферментативных препаратов, с потенциалом использования в качестве лекарственного средства, а также разработка эффективного способа получения высокоочищенного и высокоактивного препарата белка с последующим потенциальным применением в промышленных условиях. Существует необходимость разработки усовершенствованных экономически целесообразных технологий получения таких белков с сохранением высокого качества (степень чистоты, выход и активность) препаратов для исследовательских и прикладных целей.
Техническим результатом настоящего изобретения является получение высокоочищенного и высокоактивного препарата фрагмента протеазы пшеницы тритикаина-альфа, состоящего из пропептидного (продомена) и каталитического доменов полноразмерного тритикаина-альфа пшеницы (т.е. без лидерного пептида и гранулин-подобного домена), в растворимой форме с высоким выходом при выделении, для фундаментальных и прикладных исследований (в частности, для использования в составе ферментных терапевтических средств).
Поставленная задача решается следующим образом:
Пример 1. Клонирование усеченных фрагментов гена тритикаина-альфа для бактериальной экспрессии белков в растворимой форме.
На основе известной последовательности мРНК пшеницы (Triticum aestivum), кодирующей полноразмерный ген тритикаина-альфа (GenBank АВ267407), синтезируют комплементарную ДНК (кДНК) с использованием обратной транскриптазы мышиного вируса лейкемии Молони и праймера на 3'-нетранслируемую область мРНК 5'-gggggatccttacgcgctacttttcttgccg. Амплификацию кодирующей транслируемую область гена полноразмерного тритикаина-альфа ДНК, фланкированную сайтами рестрикции NdeI и BamHI (TRIT-α, фиг. 1, SEQ ID NO: 1), проводят с использованием следующих прямого и обратного праймеров: 5'-ccccatatgcatcatcatcatcatcatgccatgaggagctccatggccctc и 5'-gggggatccttacgcgctacttttcttgccg (сайты рестрикции NdeI и BamHI выделены подчеркиванием). Продукт амплификации и плазмидную ДНК рЕТ-42а(+) обрабатывают рестриктазами NdeI и BamHI, соединяют при помощи лигазной реакции, после чего реакционную смесь трансфицируют в компетентные клетки E.coli BL21-CodonPlus(DE3)-RIL. Трансформированные клетки высевают на агаризованную среду LB, содержащую антибиотик (канамицин). Из отобранных методом ПЦР (с помощью универсальных праймеров для рЕТ-векторов) клонов выделяют целевую плазмидную ДНК (pET_TRIT-α). Нуклеотидную последовательность встроенного фрагмента подтверждают секвенированием по Сенгеру. Отобранные клоны наращивают для оценки продуктивности, устойчивости к антибиотикам и стабильности трансформации.
Конструирование новой последовательности ДНК, кодирующей усеченный фрагмент гена тритикаина-альфа (6HIS-Triticain-α-GM, без лидерного пептида и гранулин-подобного домена, с N-концевой полигистидиновой последовательностью, фиг. 2, SEQ ID NO:2) для экспрессии в бактериальной системе, осуществляют на основе плазмидной ДНК pET_TRIT-α в качестве матрицы и праймеров: 5'-tatacatatgtcgatcgtgtcgtacgg (сайт рестрикции NdeI выделен подчеркиванием) и 5'-ttctcgagttagcccgtcttcgtcgg (сайт рестрикции XhoI выделен подчеркиванием). Продукт амплификации клонируют в экспрессионную плазмиду рЕТ-15b (Novagen, Germany) по сайтам рестрикции NdeI и XhoI, используя штамм E.coli Rosetta gami В (DE3). Скрининг колоний проводят методом рестрикционного анализа и последующего секвенирования.
Аналогичным образом осуществляют конструирование новой последовательности ДНК, кодирующей усеченный фрагмент гена тритикаина-альфа (Triticain-α-GM-6HIS), без лидерного пептида и гранулин-подобного домена, с С-концевой полигистидиновой последовательностью, фиг. 3, SEQ ID NO:3), используя следующую пару праймеров: 5'-ataccatggcgctgccggagaccgtcg и 5'-attctcgagtcagtggtggtggtggtggtggcccgtcttcgtcgggt и сайты рестрикции NcoI и XhoI соответственно (выделены подчеркиванием).
Пример 2. Клонирование фрагмента гена тритикаина-альфа для дрожжевой экспрессии белка в растворимой форме.
Конструирование новой последовательности ДНК, кодирующей усеченный фрагмент гена тритикаина-альфа (y-Triticain-α-GM, фиг. 4, SEQ ID NO:4) для экспрессии в дрожжевой системе, осуществляют на основе плазмидной ДНК pET_TRIT-α в качестве матрицы и праймеров: 5'-tgaattctccatcgtgtcgtacggg (сайт рестрикции EcoRI выделен подчеркиванием) и 5'-attgcggccgcttagcccgtcttcgtcgg (сайт рестрикции NotI выделен подчеркиванием). Продукт амплификации клонируют в экспрессионный вектор Pichia pastoris рРIС9 по указанным сайтам, который позволяет получать целевой белок в секретируемом виде за счет сигнальной последовательности (α-фактора, фиг. 4).
Пример 3. Экспрессия фрагмента тритикаина-альфа пшеницы в растворимой форме в E.coli.
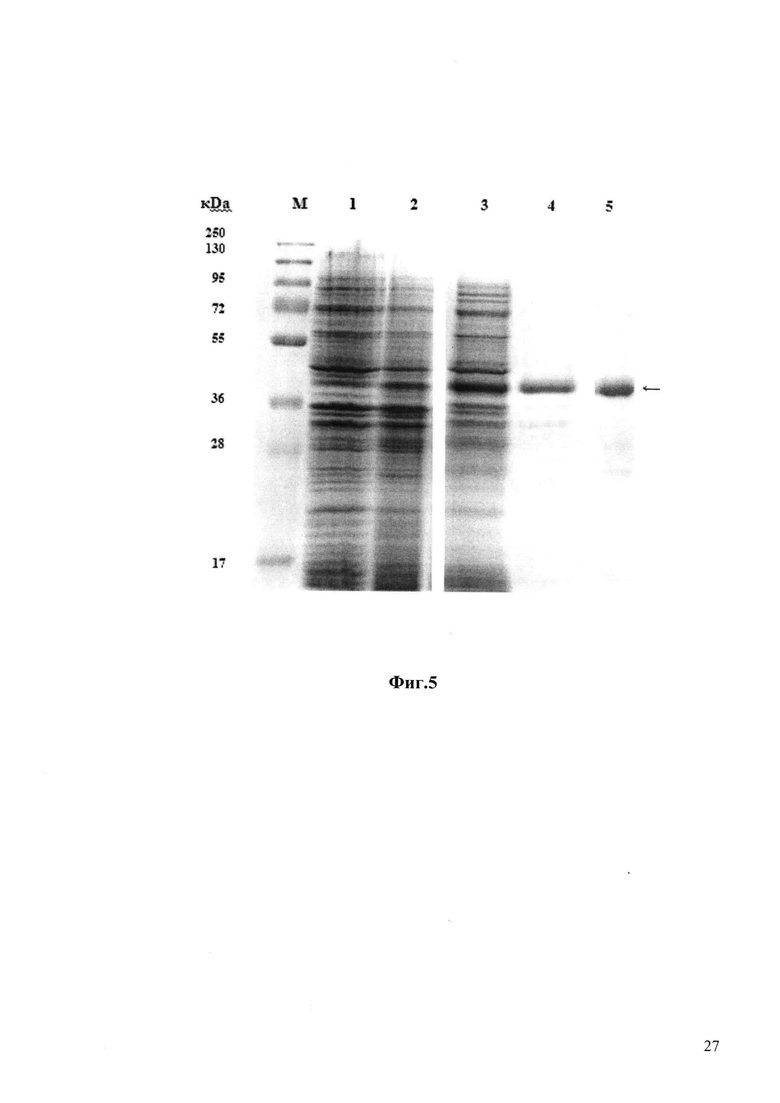
Штамм E.coli Rosetta gami В (DE3), трансформированный плазмидой pET15-6HIS-Triticain-α-GM выращивают в среде LB (10 г/л триптон, 5 г/л дрожжевой экстракт, 5 г/л NaCl) при 37°С в аэробных условиях с добавлением ампициллина (до конечной концентрации 50 мг/мл) в течение 12-14 ч (посевной материал), инокулируют новую порцию питательной среды в соотношении 1:50, растят культуру до достижения оптической плотности А600 0.6-0.8, охлаждают во льду в течение 15 мин и индуцируют изопропилтио-β-О-галактозидом (ИПТГ) до конечной концентрации 1 мМ, после чего клетки продолжают инкубировать 20 ч при 18°С. При индукции ИПТГ происходит биосинтез рекомбинантного 6HIS-Triticain-α-GM (SEQ ID NO:2), который накапливается в клетках как в растворимой форме, так и в тельцах включения (фиг. 5). Отбирают пробы клеточной суспензии до и после индукции в количестве, соответствующем 0.1 оптических единиц (о.е.), осаждают центрифугированием, суспендируют в лизирующем буфере (0.03 М Трис-HCl, рН 6.8, 10% глицерин, 1% додецилсульфат натрия, 3% меркаптоэтанол, 0.005% бромфеноловый синий), нагревают 5 мин при 95°С, и образцы объемом 20 мкл анализируют электрофорезом в 12% полиакриламидном геле с додецилсульфатом натрия. Гель прокрашивают кумасси R-250 по стандартной методике и сканируют для определения относительного количества белка в полосе целевого белка (фиг. 5). По данным сканирования содержание рекомбинантного 6HIS-Triticain-α-GM составляет 15-20% от всех клеточных белков.
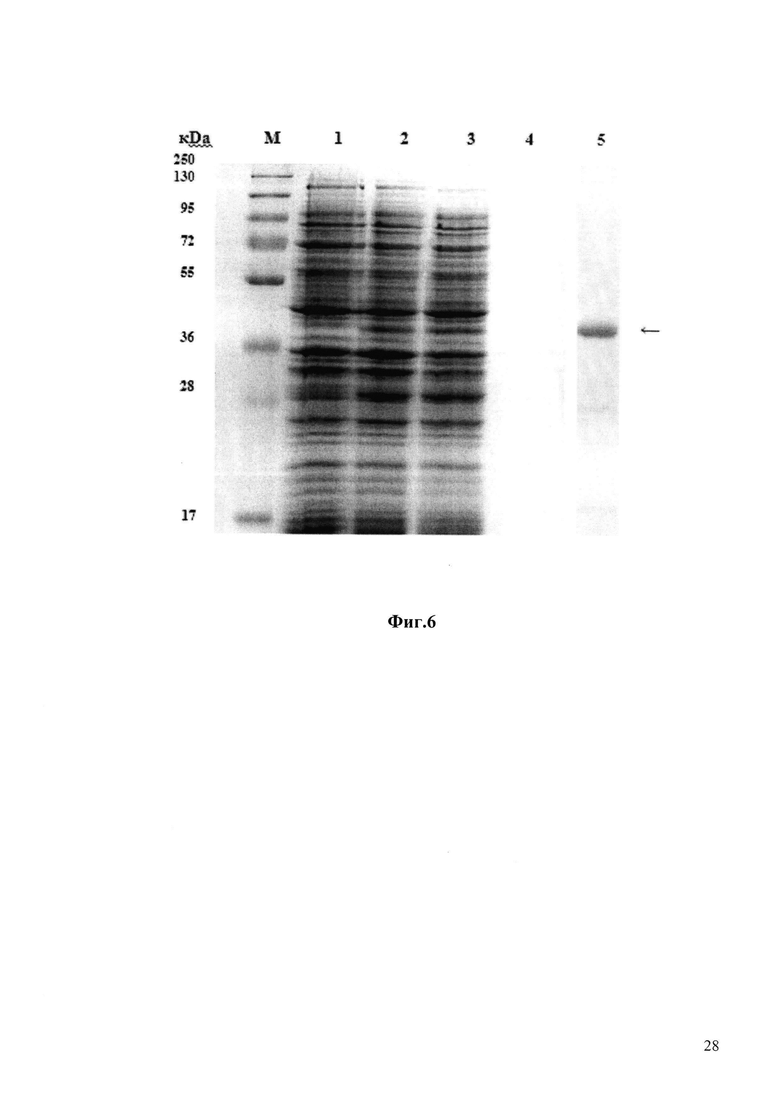
Аналогичным образом осуществляют экспрессию фрагмента тритикаина-альфа Triticain-α-GM-6HIS (SEQ ID NO:3), используя трансформированные плазмидой pET15-Triticain-α-GM-6HIS клетки штамма Rosetta gami В (DE3). Результат биосинтеза рекомбинантного белка анализируют электрофорезом в 12% полиакриламидном геле с додецилсульфатом натрия (фиг. 6). По данным сканирования геля содержание рекомбинантного Triticain-α-GM-6HIS составляет 15-20% от всех клеточных белков, причем целевой белок синтезируется в бактериальных клетках исключительно в растворимой форме.
Пример 4. Получение высокоочищенного препарата рекомбинантного фрагмента тритикаина-альфа из E.coli.
Очистку целевых белков 6HIS-Triticain-α-GM (SEQ ID NO:2) и Triticain-α-GM-6HIS (SEQ ID NO:3) проводят методом аффинной (металл-хелатной) хроматографии. Получение рекомбинантного 6HIS-Triticain-α-GM и Triticain-α-GM-6HIS из клеток штаммов-продуцентов Rosetta gami В (DE3)/pET15-6HIS-Triticain-α-GM и Rosetta gami В (DE3)/pET15-Triticain-α-GM-6HIS соответственно, включает несколько стадий. Осажденную центрифугированием клеточную биомассу экспрессионной культуры ресуспендируют в 0.02 М фосфатном буфере, рН 8.0, содержащем 0.5 М NaCl и 0.01 М имидазол (буфер А), и гомогенизируют на ультразвуковом дезинтеграторе в течение 1 мин (12×5 с) при 4°С. Полученную после центрифугирования лизата (10000×g, 4°С, 15 мин) надосадочную жидкость наносят на колонку с активированной ионами никеля иминодиацетат-сефарозой, уравновешенную буфером А. Процесс хроматографии проводят на системе BioLogic (BioRad) с детекцией при 280 нм. Сорбент последовательно промывают уравновешивающим буфером А. Связавшийся с сорбентом белок элюируют буфером А с содержанием 0.3 М имидазола. Раствор диализуют против 0.02 М фосфатного буфера, рН 8.0 при 4°С в течение 24 ч, трижды производя замену буфера на свежий. Концентрацию целевого белка определяют с помощью ВСА-реагента (бицинхониновой кислоты), аликвотируют по стеклянным флаконам, замораживают и лиофилизуют.
Выход полученных таким способом рекомбинантных вариантов усеченного тритикаина-альфа в растворимой форме составляет не менее 15 мг (15-24 мг) с 1 л для бактериальной культуры Rosetta gami В (DE3)/pET15-6HIS-Triticain-α-GM и не менее 5 мг с 1 л - для Rosetta gami В (DE3)/pET15-Triticain-α-GM-6HIS. Чистота полученных препаратов по данным электрофоретического анализа составляет не менее 85% (фиг. 5, 6; следует отметить, что целевые белки 6HIS-Triticain-α-GM (SEQ ID NO:2) и Triticain-α-GM-6HIS (SEQ ID NO:3), проявляющие протеолитическую активность, подвергаются автопротеолизу в процессе выделения).
Пример 5. Экспрессия фрагмента тритикаина-альфа пшеницы в растворимой форме в P.pastoris.
Для трансформации клеток Pichia pastoris дрожжевой экспрессионной плазмидой pPIC9-Triticain-α-GM был использован ауксотрофный по гистидину штамм Pichia pastoris GS115 (His-, Mut+). Плазмиду pPIC9-Triticain-α-GM линеаризуют по сайту BglII. Трансформацию клеток Pichia pastoris проводят методом электропорации. Клетки штамма GS115 высевают на чашку с агаризованной средой YPD (1% дрожжевой экстракт, 2% пептон, 2% глюкоза) и инкубируют при 30°С 2 дня до появления отдельных колоний. Одной колонией инокулируют 5 мл среды YPD в колбе объемом 50 мл и наращивают клетки в течение ночи при 30°С в шейкер-инкубаторе при 300 об/мин. Далее 200 мл свежей среды YPD засевают 0.2 мл ночной культуры и снова наращивают клетки в течение ночи при 30°С в шейкер-инкубаторе до достижения оптической плотности клеточной суспензии А600 1.5. Клетки осаждают центрифугированием (1500×g, 5 мин, 4°С), осадок дважды промывают 200 мл и 100 мл охлажденной во льду стерильной воды соответственно, после чего клетки снова осаждают и ресуспендируют в 8 мл холодного 1 М сорбита. Затем клетки снова осаждают и ресуспендируют в 0.6 мл ледяного 1 М сорбита. 40 мкл клеточной суспензии смешивают с 5 мкг линеаризованной плазмиды в 10 мкл буфера ТЕ (0.01 М Трис-HCl, 0.001 М ЭДТА, рН 8.0). Смесь помещают в охлажденную 2 мм кювету и охлаждают во льду 5 мин. Затем кювету помещают в отсек шоковой камеры электропоратора и генерируют единичный импульс. Кювету извлекают из камеры и быстро добавляют 1 мл ледяного 1 М сорбита. Содержимое кюветы переносят в стерильные микропробирки. По 100, 300 и 600 мкл клеточной суспензии, трансформированной линеаризованной плазмидой рРIС9-Triticain-α-GM, растирают на чашке Петри с минимальной безгистидиновой агаризованной средой. Для контроля выживаемости по 10 мкл клеточных суспензий после электропорации суспендируют в 100 мкл 1 М сорбита и по 10 мкл растирают на чашках Петри с агаризованной YPD средой. Чашки инкубируют при 30°С до появления колоний (2-4 дня).
В зависимости от способа рекомбинации и локуса встраивания линеаризованной плазмиды трансформированные клетки Pichia pastoris GS115 (Mut+) могут приобретать MutS фенотип. Для подтверждения Mut+ и MutS фенотипов трансформантов колонии высевают на чашки с минимальной агаризованной средой, содержащей метанол и глюкозу (ММ и MD соответственно), подразумевая, что дрожжевые клетки фенотипа MutS делятся в ММ среде медленнее, чем в MD среде (что визуально определяется сравнением размеров колоний на ММ и MD чашках через 2-3 суток инкубации при 30°С). Точную принадлежность дрожжевых трансформантов к Mut+ или MutS фенотипу подтверждают методом полимеразной цепной реакции. Для этого из выбранных клонов с ММ и MD чашек выделяют ДНК и анализируют методом ПЦР с использованием прямого 5'АОХ1 (gactggttccaattgacaagc) и обратного 3'АОХ1 (gcaaatggcattctgacatcc) праймеров при условиях амплификации: 95°С 3 мин, денатурация 95°С 30 с, 30 циклов, отжиг 54°С 30 с, элонгация 72°С 2 мин, затем 72°С 5 мин. Пробы анализируют методом горизонтального электрофореза в 1% агарозном геле с окрашиванием бромистым этидием. По размерам ампликонов ДНК клонов Mut+ и MutS фенотипа (2140 п.н. и 1476 п.н. соответственно) выявляют преобладающий фенотип (Mut+). Полученные трансформанты Pichia pastoris GS115/pPIC9-Triticain-α-GM содержат как минимум одну копию фрагмента гена тритикаина-альфа. По результатам анализа отбирают несколько клонов Mut+ и MutS фенотипов для экспрессии целевого рекомбинантного белка.
Для получения двойных трансформантов линеализированную по сайту рестрикции SalI плазмиду pPIC9K-Triticain-α-GM трансформировали в полученные ранее клетки Pichia pastoris GS 115/pPIC9-Triticain-α-GM (Mut+и MutS). Отбор двойных трансформантов проводили на генетицин-содержащей среде (0,15 мг/мл).
Для исследования способности трансформантов P.pastoris Mut+ и MutS фенотипов секретировать y-Triticain-α-GM (SEQ ID NO:4) одной колонией каждого клона трансформанта и контрольных штаммов со свежих чашек инокулируют 4 мл среды BMGY (1% дрожжевой экстракт, 2% пептон, 1.34% YNB, 4×10-5% биотин, 1% глицерин, 0.1 М фосфат калия, рН 6.0). Клеточную массу наращивают при 30°С в шейкер-инкубаторе при 300 об/мин до достижения А600 1 о.е. (для Mut+) и А600 5 о.е. (для MutS). Для АОХ-контролируемой индуции экспрессии клеточные суспензии в объеме, содержащем 5 о.е. (Mut+) или 25 о.е. (MutS), осаждают центрифугированием и осадки ресуспендируют в 5 мл среды BMMY (1% дрожжевой экстракт, 2% пептон, 1.34%) YNB, 4×10-5% биотин, 0.5% метанол, 0.1 М фосфат калия, рН 6.0). Клетки инкубируют в течение 96 ч при 30°С и 300 об/мин. Каждые 24 ч добавляют метанол до конечной концентрации 0.7%. После окончания инкубации клетки осаждают центрифугированием (4000×g, 5 мин, 4°С). Супернатанты отбирают, замораживают в жидком азоте и хранят при -70°С до последующего анализа. Наличие рекомбинантного y-Triticain-α-GM в супернатантах клеточной культуры P. pastoris определяют методом электрофореза в 14% полиакриламидном геле с додецилсульфатом натрия.
Пример 6. Получение высокоочищенного рекомбинантного y-Triticain-α-GM из Pichia pastoris.
Надосадочную культуральную жидкость Pichia pastoris GS115/pPIC9-Triticain-α-GM фильтруют (0.45 мкм) и диализуют против 0.02 М раствора фосфата натрия, рН 8.0 при 4°С в течение 24 ч, трижды производя замену буфера на свежий. Диализат концентрируют ультрафильтрацией на ячейке Amicon с мембраной RC-10 (Millipore) и наносят на колонку с сорбентом Sephacryl S-200HR, уравновешенную 0.02 М фосфатным буфером, рН 8.0, содержащем 130 мМ NaCl. Процесс гель-фильтрации проводят со скоростью 0,5 мл/мин, фракции по 6 мл собирают и анализируют на присутствие целевого белка методами электрофоретического анализа и определения протеолитической активности. Очищенный белок концентрируют на ячейке Amicon с мембраной RC-10 (Millipore), определяют концентрацию с помощью ВСА-реагента (бицинхониновой кислоты), аликвотируют по стеклянным флаконам, замораживают и лиофилизуют.
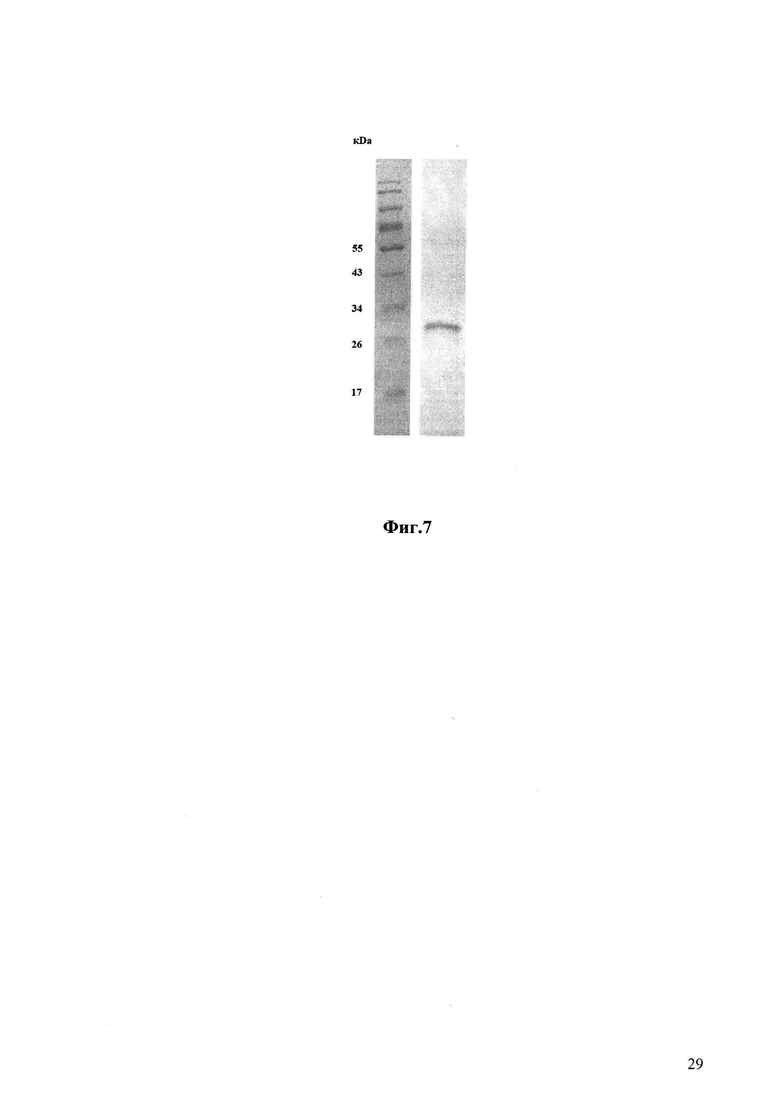
Выход полученного таким способом рекомбинантного y-Triticain-α-GM (SEQ ID NO:4) составляет 80-300 мг с 1 л дрожжевой культуры (с чистотой не менее 90% по данным электрофоретического анализа, фиг. 7; следует отметить, что целевой белок y-Triticain-α-GM (SEQ ID NO:4) в процессе секреции подвергается автопротеолизу).
Пример 7. Определение протеолитической активности вариантов рекомбинантных белков усеченного тритикаина-альфа (6HIS-Triticain-α-GM, Triticain-α-GM-6HIS и y-Triticain-α-GM).
Ферментативную (протеолитическую) активность рекомбинантного усеченного тритикаина-альфа определяют по способности гидролизовать синтетический модельный пептидный субстрат PLVQ-AMК, конъюгированный с 7-Амино-4-метилкумарином (АМК), с определением продуктов гидролиза по интенсивности флуоресценции свободного AMK. Последовательность и структура выбранного пептида PLVQ (пролин-лейцин-валин-глутамин), представляющего собой фрагмент глютена, являются оптимальными для связывания и гидролиза тритикаином-альфа [15].
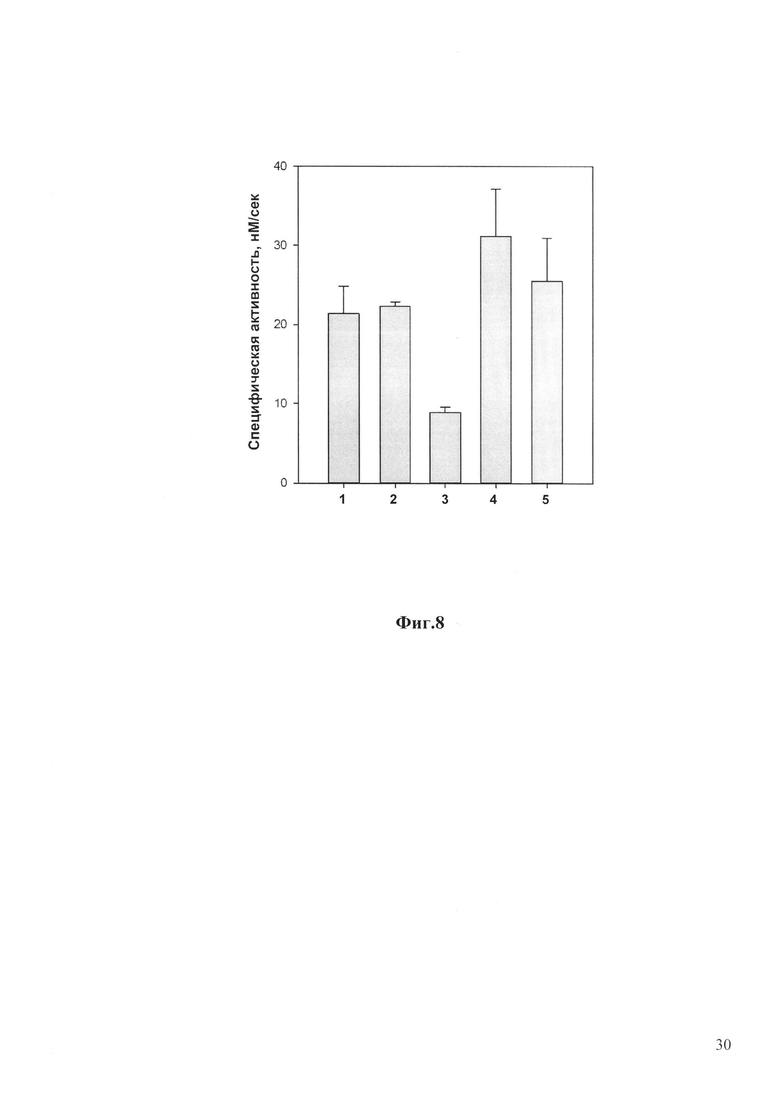
Анализ проводят при 25°С в реакционной смеси, состоящей из 20 нМ целевого белка (рекомбинантного тритикаина-альфа) и 50 мкМ PLVQ-АМК в 200 мМ ацетатном буфере, рН 5.6, содержащем 100 мМ NaCl, 15 мМ 2-меркаптоэтанол, 0.6 мМ ЭДТА, 0.5% ДМСО. Количество гидролизованного субстрата PLVQ-AMK определяют по интенсивности флуоресценции свободного AMK с использованием многорежимного автоматического спектрофлуориметра при длине волны возбуждения флуоресценции, равной 360 нм, и длине волны испускания флуоресценции, равной 460 нм. Скорость реакции определяли по графику зависимости количества субстрата (моль) от времени гидролиза (с) с последующей обработкой полученных данных с применением метода линейной регрессиии. Для репрезентативности данные по специфической активности представлены в виде гистограммы (фиг. 8).
Сравнивали активность полученных препаратов усеченного тритикаина-альфа, полученного в растворимой форме, с препаратами усеченного тритикаина-альфа, полученного ранее в нашей лаборатории в нерастворимой форме и папаином.
Активность белковых препаратов усеченного тритикаина-альфа, полученного в растворимой форме 6HIS-Triticain-α-GM (SEQ ID NO:2) и Triticain-α-GM-6HIS (SEQ ID NO:3) значительно превысила активность препарата усеченного тритикаина-альфа 6HIS-Triticain-α-GM, полученного в нерастворимой форме, а также папаина, что является существенным преимуществом препаратов, полученных нами в рамках данной заявки. Активность препарата усеченного тритикаина-альфа y-Triticain-α-GM (SEQ ID NO:4), полученного в дрожжевой экспрессионной системе, оказалась ниже, чем активность препарата усеченного тритикаина-альфа 6HIS-Triticain-α-GM, полученного в нерастворимой форме, и папаина, однако, принимая во внимание высокое содержание в препарате и высокий выход при экспрессии белка y-Triticain-α-GM, такой результат также является промышленно применимым и технически значимым.
Преимуществами заявленного технического решения являются, во-первых, получение протеолитически активного препарата тритикаина-альфа, состоящего из пропептидного (продомена) и каталитического доменов полноразмерного тритикаина-альфа пшеницы, который может быть использован для создания новых более эффективных лекарственных энзиматических средств, а также в исследовательстких целях, в частности, для изучения функционирования папаин-подобных цистеиновых протеиназ; во-вторых, возможность получения вариантов протеолитически активного тритикаина-альфа в растворимой форме как в бактериальных, так и в дрожжевых клетках; в-третьих, упрощенная методика выделения вариантов рекомбинантного белка из E.coli за счет исключения стадии рефолдинга in vitro, т.е. времязатратной и сложно валидируемой процедуры, что в последствии послужит основой для создания ферментных лекарственных средств в терапии некоторых заболеваний (в частности, целиакии).
Источники информации, принятые во внимание
1. Т. Kiyosaki, Т. Asakura, I. Matsumoto, et al. J Plant Physiol, 2009, 1, 166(1), 101-6.
2. K. Muntz, M.A. Belozersky, Y.E. Dunaevsky, et al. J Exp Bot, 2001, 52, 1741-52.
3. J.Q. Ling, T. Kojima, M. Shiraiwa, et al. Biochim Biophys Acta, 2003, 1627, 129-39.
4. A. Capocchi, M. Cinollo, L. Galleschi, et al. JAgric Food Chem, 2000, 48, 6271-79.
5. T. Okamoto, T. Shimada, I. Hara-Nishimura, et al. Plant Physiol, 2003, 132, 1892-1900.
6. A. Mikkonen, I Porali, M. Cercos, et al. Plant Mol Biol, 1996, 31(2), 239-54.
7. H. Kondo, K. Abe, I. Nishimura, et al. J Biol Chem, 1990, 15, 265(26), 15832-37.
8. T. Kiyosaki, I. Matsumoto, T. Asakura, et al. FEBS J, 2007, 274, 1908-17.
9. N. McGough, J.H. Cummings. Proc Nutr Soc, 2005, 64(4), 434-50.
10. J.S. Leeds, A.D. Hopper, D.S. Sanders. Br Med Bull, 2008, 88(1), 157-70.
11. WGO - OMGE: Practice guidelines. World Gastroenterology News, 10 (2, 2), 2005, 1-8.
12. S. Rashtak, J.A. Murray. Aliment Pharmacol Ther, 2012, 35(7), 768-81.
13. L.V. Savvateeva, A.A. Zamyatnin. Curr Pharm Des, 2016, 22(16), 2439-49.
14. H. Vora, J. McIntire, P. Kumar, et al. Biotechnol Bioeng, 2007, 1, 98(1), 177-85.
15. Патент WO 2008115428 A2, 25.09.2008.
16. L.V. Savvateeva, N.V. Gorokhovets, V.A. Makarov, et al. Int J Biochem Cell Biol, 2015, 62, 115-24.
17. Патент RU 2603054 C2, 20.11.2016.
Подписи к фигурам:
Фиг. 1. Аминокислотная и нуклеотидная последовательности рекомбинантного полноразмерного тритикаина-альфа, экспрессирующегося в E.coli (SEQ ID NO:1, TRIT-α, курсивом выделена последовательность от экспрессионной плазмиды рЕТ-42а(+); курсивом и подчеркиванием выделены сайты узнавания рестриктазами; подчеркиванием выделен лидерный пептид; курсивом и цветом выделена каталитическая триада Cys-His-Asn, определяющая принадлежность белка к цистеиновым протеазам; цветом выделен гранулин-подобный домен; подчеркиванием выделены сайты узнавания рестриктазами);
Фиг. 2. Аминокислотная и нуклеотидная последовательности рекомбинантного усеченного тритикаина-альфа с N-концевой полигистидиновой последовательностью, экспрессирующегося в E.coli в растворимой форме (SEQ ID NO:2, 6HIS-Triticain-α-GM; курсивом выделена последовательность от экспрессионной плазмиды рЕТ-15b; подчеркиванием выделены сайты узнавания рестриктазами; курсивом и цветом выделена каталитическая триада Cys-His-Asn, определяющая принадлежность белка к цистеиновым протеазам);
Фиг. 3. Аминокислотная и нуклеотидная последовательности рекомбинантного усеченного тритикаина-альфа с С-концевой полигистидиновой последовательностью, экспрессирующегося в E.coli в растворимой форме (SEQ ID NO:3, Triticain-α-GM-6HIS; курсивом выделена последовательность от экспрессионной плазмиды рЕТ-15b; подчеркиванием выделены сайты узнавания рестриктазами; курсивом и цветом выделена каталитическая триада Cys-His-Asn, определяющая принадлежность белка к цистеиновым протеазам);
Фиг. 4. Аминокислотная и нуклеотидная последовательности рекомбинантного усеченного тритикаина-альфа, экспрессирующегося в P.pastoris (SEQ ID NO:4, y-Triticain-α-GM; курсивом выделена последовательность от экспрессионной плазмиды рPIС9; цветом выделен α-фактор; стрелкой выделен сигнал отщепления α-фактора; подчеркиванием выделены сайты узнавания рестриктазами);
Фиг. 5. Электрофореграмма в 12% полиакриламидном геле в присутствии SDS: лизатов клеток штамма-продуцента E.coli Rosetta gami B(DE3) / pET15-6HIS-Triticain-α-GM до индукции (дорожка 1), лизатов клеток штамма-продуцента E.coli Rosetta gami B(DE3) / pET15-6HIS-Triticain-α-GM после индукции изопропилтио-β-D-галактозидом (дорожка 2); растворимая клеточная фракция (дорожка 3), нерастворимая клеточная фракция (дорожка 4); рекомбинантный усеченный тритикаин-альфа (SEQ ID NO:2, 6HIS-Triticain-α-GM, дорожка 5) после хроматографического выделения; М - белковые маркеры молекулярной массы (кДа).
Фиг. 6. Электрофореграмма в 12% полиакриламидном геле в присутствии SDS: лизатов клеток штамма-продуцента E.coli Rosetta gami B(DE3) / Triticain-α-GM-6HIS до индукции (дорожка 1), лизатов клеток штамма-продуцента E.coli Rosetta gami B(DE3) / Triticain-α-GM-6HIS после индукции изопропилтио-β-D-галактозидом (дорожка 2); растворимая клеточная фракция (дорожка 3), нерастворимая клеточная фракция (дорожка 4); рекомбинантный усеченный тритикаин-альфа (SEQ ID NO:3, Triticain-α-GM-6HIS, дорожка 5) после хроматографического выделения; М - белковые маркеры молекулярной массы (кДа).
Фиг. 7. Рекомбинантный усеченный тритикаин-альфа (SEQ ID NO:4, y-Triticain-α-GM, экспрессированный в клетках P.pastoris) после хроматографического выделения в 14% полиакриламидном геле в присутствии SDS (М - белковые маркеры молекулярной массы, кДа); (М - белковые маркеры молекулярной массы, кДа);
Фиг. 8. Специфическая (протеолитическая) активность вариантов рекомбинантных белков усеченного тритикаина-альфа и папаина (как контроля цистеиновых папаин-подобных протеиназ): 1 - папаин; 2 - рекомбинантный фрагмент тритикаин-альфа из нерастворимой фракции; 3 - усеченный тритикаин-альфа, экспрессированный в клетках P.pastoris (SEQ ID NO:4, y-Triticain-α-GM); 4 - усеченный тритикаин-альфа с N-концевой полигистидиновой последовательностью (SEQ ID NO:2, 6HIS-Triticain-α-GM); 5 - усеченный тритикаин-альфа с С-концевой полигистидиновой последовательностью (SEQ ID NO:3, Triticain-α-GM-6HIS).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ БЕЛКОВ СЕМЕЙСТВА ЦИСТЕИНОВЫХ ПРОТЕАЗ ПШЕНИЦЫ (TRITICUM AESTIVUM) И ПРЕПАРАТ БЕЛКА ТРИТИКАИН-АЛЬФА, ПОЛУЧЕННЫЙ ЭТИМ СПОСОБОМ | 2015 |
|
RU2603054C2 |
| СПОСОБ ПОВЫШЕНИЯ АКТИВНОСТИ ТРИТИКАИНА-АЛЬФА | 2020 |
|
RU2740319C1 |
| Способ получения препарата рекомбинантной нуклеазы CAS, по существу, свободного от бактериальных эндотоксинов, полученный данным способом препарат и содержащий его набор для использования в системе CRISPR/Cas | 2019 |
|
RU2707542C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК PNDCTR1, КОДИРУЮЩАЯ ГИБРИДНЫЙ ПОЛИПЕПТИД GST-NDCTR1, ШТАММ БАКТЕРИЙ ESCHERICHIA COLI BL21(DE3)/PNDCTR1 - ПРОДУЦЕНТ ГИБРИДНОГО ПОЛИПЕПТИДА GST-NDCTR1 И ГИБРИДНЫЙ ПОЛИПЕПТИД GST-NDCTR1, ОБЛАДАЮЩИЙ СПОСОБНОСТЬЮ ХЕЛАТИРОВАТЬ ИОНЫ МЕДИ, СЕРЕБРА И ПЛАТИНЫ | 2015 |
|
RU2603092C1 |
| Способ получения каспазы-3 | 2022 |
|
RU2792795C1 |
| ПЛАЗМИДА 40Gal, ОПРЕДЕЛЯЮЩАЯ СИНТЕЗ α-ГАЛАКТОЗИДАЗЫ α-PsGal, ШТАММ E.coli Rosetta(DE3)/40Gal - ПРОДУЦЕНТ ХИМЕРНОГО БЕЛКА, ВКЛЮЧАЮЩЕГО АМИНОКИСЛОТНУЮ ПОСЛЕДОВАТЕЛЬНОСТЬ α-PsGal, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2012 |
|
RU2504583C1 |
| ПЛАЗМИДА 40NaGal, ОПРЕДЕЛЯЮЩАЯ СИНТЕЗ α-N-АЦЕТИЛГАЛАКТОЗАМИНИДАЗЫ α-AlNaGal, ШТАММ E.coli Rosetta(DE3)/40NaGal - ПРОДУЦЕНТ ХИМЕРНОГО БЕЛКА, ВКЛЮЧАЮЩЕГО АМИНОКИСЛОТНУЮ ПОСЛЕДОВАТЕЛЬНОСТЬ РЕКОМБИНАНТНОЙ α-N-АЦЕТИЛГАЛАКТОЗАМИНИДАЗЫ α-AlNaGal, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2013 |
|
RU2525682C1 |
| Рекомбинантный штамм бактерий Escherichia coli Rosetta 2(DE3)/pET28c-Mau - продуцент ДНК-полимеразы А | 2023 |
|
RU2815455C1 |
| ТЕРМОСТАБИЛЬНАЯ АЛКОГОЛЬДЕГИДРОГЕНАЗА ИЗ АРХЕИ THERMOCOCCUS SIBIRICUS | 2009 |
|
RU2413766C1 |
| Штамм-продуцент фермента ДНК-зависимой РНК-полимеразы фага Т7 | 2022 |
|
RU2825469C2 |




Изобретение относится к области молекулярной биологии и биотехнологии и представляет собой биологически активный белковый препарат, обладающий специфической активностью папаин-подобных цистеиновых протеиназ, характеризующийся тем, что представляет собой аминокислотную последовательность, выбранную из SEQ ID NO:2-4, экспрессирующийся в растворимой форме. Изобретение относится также к способу получения биологически активного белкового препарата, где способ включает трансформацию клеток плазмидами, содержащими ДНК, кодирующую белок с аминокислотной последовательностью, выбранной из SEQ ID NO: 2-4, культивирование и выделение биологически активного препарата. Изобретение обеспечивает возможность получения препарата тритикаина-альфа с высоким и стабильным выходом, высоким уровнем очистки и функциональной активности. 5 н. и 4 з.п. ф-лы, 8 ил., 7 пр.
1. Биологически активный белковый препарат, обладающий специфической активностью папаин-подобных цистеиновых протеиназ, характеризующийся тем, что представляет собой аминокислотную последовательность, выбранную из SEQ ID NO:2-4, экспрессирующийся в растворимой форме.
2. Способ получения биологически активного белкового препарата по п. 1, обладающего специфической активностью папаин-подобных цистеиновых протеиназ, характеризующийся тем, что включает трансформацию клеток плазмидами, содержащими ДНК, кодирующую белок с аминокислотной последовательностью, выбранной из SEQ ID NO: 2-4, культивирование и выделение биологически активного препарата.
3. Способ по п. 2, характеризующийся тем, что для трансформации плазмидами, содержащими последовательности ДНК, кодирующие белки с аминокислотной последовательностью, выбранной из SEQ ID NO:2-3, используют клетки E.coli штамма Rosetta gami В (DE3), в качестве среды культивирования используют среду LB с добавлением ампициллина и инкубируют при 37°С в аэробных условиях в течение 12-14 ч, посевным материалом инокулируют питательную среду, растят культуру до достижения оптической плотности А600 0.6-0.8, индуцируют 1 мМ изопропилтио-β-D-галактозидом и растят еще 20 ч при 18°С с накоплением растворимой формы белка, а выделение биологически активного препарата осуществляют осаждением путем центрифугирования экспрессионной культуры, после чего осадок ресуспендируют в 0.02 М фосфатном буфере, рН 8.0, содержащем 0.5 М NaCl и 0.01 М имидазол (буфер А), и гомогенизируют на ультразвуковом дезинтеграторе в течение 1 мин при 4°С, полученный лизат центрифугируют, надосадочную жидкость наносят на колонку с активированной ионами никеля иминодиацетат-сефарозой, уравновешенную буфером А, сорбент последовательно промывают уравновешивающим буфером А, затем белок элюируют буфером А с содержанием G.3 М имидазола, далее раствор белка диализуют против 0.02 М фосфатного буфера, рН 8.0 и после определения концентрации и протеолитической активности белка в полученном препарате аликвотируют по стеклянным флаконам, замораживают и лиофилизуют.
4. Способ по п. 2, характеризующийся тем, что для трансформации плазмидой, содержащей последовательность ДНК, кодирующую белок с аминокислотной последовательностью SEQ ID NO:4, используют клетки P.pastoris штамма GS115, в качестве среды культивирования используют среду YPD и инкубируют при 30°С в шейкере-инкубаторе до достижения оптической плотности А600 1-5, клеточные суспензии растирают на чашке Петри с минимальной безгистидиновой агаризованной средой и инкубируют при 30°С до появления колоний, затем одной колонией полученных трансформантов Pichia pastoris GS115/pPIC9-Triticain-α-GM, содержащих одну или две копии фрагмента гена усеченного тритикаина-альфа, инокулируют питательную среду BMGY и наращивают клеточную массу при 30°С в шейкере-инкубаторе до оптической плотности 5 о.е. (Mut+) или 25 о.е. (MutS), выделение биологически активного препарата осуществляют осаждением путем центрифугирования, полученный осадок ресуспендируют в среде BMMY с последующим инкубированием в течение 96 ч при 30°С и 300 об/мин, добавляя каждые 24 ч в качестве индуктора экспрессии метанол до конечной концентрации 0.7%, затем клетки осаждают, отбирают супернатанты; далее надосадочную культуральную жидкость фильтруют (0.45 мкм) и диализуют против 0.02 М раствора фосфата натрия, рН 8.0 при 4°С в течение 24 ч, диализат концентрируют и наносят на колонку с сорбентом Sephacryl S-200HR, уравновешенную 0.02 М фосфатным буфером, рН 8.0, содержащим 130 мМ NaCl, далее собирают белковые фракции по 6 мл и анализируют на присутствие белка методами электрофоретического анализа и определяют концентрацию и протеолитическую активность, далее биологически активный белковый препарат аликвотируют по стеклянным флаконам, замораживают и лиофилизуют.
5. Нуклеиновая кислота, кодирующая биологически активный белковый препарат, обладающий специфической активностью папаин-подобных цистеиновых протеиназ, по п. 1, характеризующаяся тем, что предназначена для использования в способе по п. 2.
6. Вектор экспрессии, характеризующийся тем, что содержит нуклеиновую кислоту по п. 5 для использования в способе по п. 2.
7. Вектор экспрессии по п. 6, характеризующийся тем, что представляет собой вектор на основе pET15b или pPIC9.
8. Клетка-хозяин, характеризующаяся тем, что содержит нуклеиновую кислоту по п. 5, кодирующую биологически активный белковый препарат по п. 1, для использования в способе по п. 2.
9. Клетка-хозяин по п. 8, характеризующаяся тем, что представляет собой клетку E.coli штамма Rosetta gami В (DE3) или P.pastoris штамма GS115.
| СПОСОБ ПОЛУЧЕНИЯ БЕЛКОВ СЕМЕЙСТВА ЦИСТЕИНОВЫХ ПРОТЕАЗ ПШЕНИЦЫ (TRITICUM AESTIVUM) И ПРЕПАРАТ БЕЛКА ТРИТИКАИН-АЛЬФА, ПОЛУЧЕННЫЙ ЭТИМ СПОСОБОМ | 2015 |
|
RU2603054C2 |
| WO 2008115428 A2, 25.09.2008. | |||
Авторы
Даты
2018-12-27—Публикация
2017-06-28—Подача