Изобретение относится к медицине, радиобиологии, а именно к медицинской физике, радиотерапии, онкологии и урологии, и может быть использовано для моделирования лучевого цистита in vivo на крысах или кроликах.
Известен способ создания модели лучевого цистита, заключающийся в извлечении мочевого пузыря из брюшной полости живой крысы, облучении мочевого пузыря 2 Гр, и погружении его обратно в брюшную полость (Zabbarova I, Wipf Р, Birder L, Epperly M, De Groat W, Kanai A. University of Pittsburgh. Mouse model for characterization of radiation cystitis and its prevention using a new class of radioprotectors. https://www.ics.org/Abstracts/Publish/47/000268.pdf).
Однако, данный метод имеет ряд ограничений: его применение приводит к повышенному риску гибели крыс, не нужном страдании животного, а также изменению физиологии мочевого пузыря, как следствие оперативного вмешательства.
Известен способ создания модели лучевого цистита на мелких животных, заключающийся в подведении больших разовых доз до 40 Гр маленьким размером поля от 2.5×2.5 мм2 до 5×5 мм2 с визуализацией положения мочевого пузыря по ортогональным КТ снимкам на специальных радиационных установках типа: X-RAD 225Сх; Precision X-Ray, Inc; SARRP (радиационная исследовательская платформа для мелких животных на базе рентгеновского облучателя Gulmay). (J Urol. 2015 August; 194(2): 578-584. doi:10.1016/j.juro.2015.03.108).
Данный способ так же имеет ряд ограничений, а именно: указанные выше радиационные установки отсутствуют в исследовательских центрах в Российской Федерации. SARRP используется исключительно для облучения небольших животных, и условия создаваемые SARRP резко отличаются от условий облучения по физико-техническим параметрам излучения от применяемого для лечения пациентов на линейном ускорителе, используемом в клинической практике.
Наиболее близким является способ моделирования лучевого цистита, включающий анестезию животного, формирование области облучения свинцовым окном с последующим облучением мочевого пузыря (Histological Changes After Fractionated Whole or Partial Irradiation of the Rabbit Urinary Bladder.Markus Kohler, Christian Michel & Arthur Zimmermann http://www.tandfonline.eom/doi/abs/10.3109/02841869509093956). В данном способе кролики анестезировались и фиксировались в удерживающем устройстве. Свинцовое окно формировало область облучения, установленное при рентген-контроле. 4 группы животных получали 0, 33, 36, 39 Гр в 5 фракциях в течение 5 последовательных дней. Облучение проводилось рентгеновским излучением энергией 300 KB, расстояние источник-поверхность (РИП) 50 см, через 2 встречных поля интенсивность 0.8 Гр/мин.
Недостатками этого способа являются: использование рентгеновского излучения низкой энергии (300 КВ) с максимумом ионизации в воздухе, длительное облучение, во время которого необходимо полностью обездвижить и держать под наркозом животное. Все это может негативно сказываться на результатах, так как не исключается смещение облучаемых животных и появление тяжелых лучевых осложнений в окружающих тканях (язвенный дерматит, целлюлит и др.).
Задачей предлагаемого изобретения является устранение указанных недостатков, создание высокоэффективной модели лучевого цистита на крысах и кроликах за счет подведения необходимой дозы излучения и гарантированного создания модели радиоиндуцированного цистита со сроками развития от 1,5 до 2 месяцев для дальнейшего использования при тестировании фармакологических препаратов.
Для решения поставленной задачи, при моделировании лучевого цистита in vivo на животных, включающем анестезию животного, формирование области облучения свинцовым окном с последующим облучением мочевого пузыря на линейном ускорителе, предложено центрировать животное на столе линейного ускорителя по световому полю и анатомическим костным ориентирам. При этом осуществляют формирование поля размером 2,5 см в направлении право-лево, и 2,3 см - 4,0 см в направление голова-хвост животного в проекции нижней трети мочевого пузыря. В области поля облучения устанавливают тканеэквивалентный болюс толщиной 1 см, смещающий максимум ионизации дозы до 0,5 см в глубину на уровень мочевого пузыря животного, устанавливают расстояние источник-поверхность до равного 100 м. При этом облучение осуществляют фотонами с граничной энергией квантов 6 МэВ. Кроме того, при создании модели на крысе облучение проводилось одной фракцией в дозе 25 Гр, а при создании модели на кролике, облучение проводилось 5 фракциями с РОД 6 Гр до СОД 30 Гр.
Предлагаемая последовательность действий позволяет сократить время облучения более чем в 4 раза по сравнению с наиболее близким аналогом, что в свою очередь обеспечивает точность облучения и уменьшает токсичность лучевой терапии и наркоза. Использование стандартного линейного ускорителя позволяет получать модель в любом клиническом учреждении без необходимости закупать дорогостоящее, импортное, специализированное оборудование.
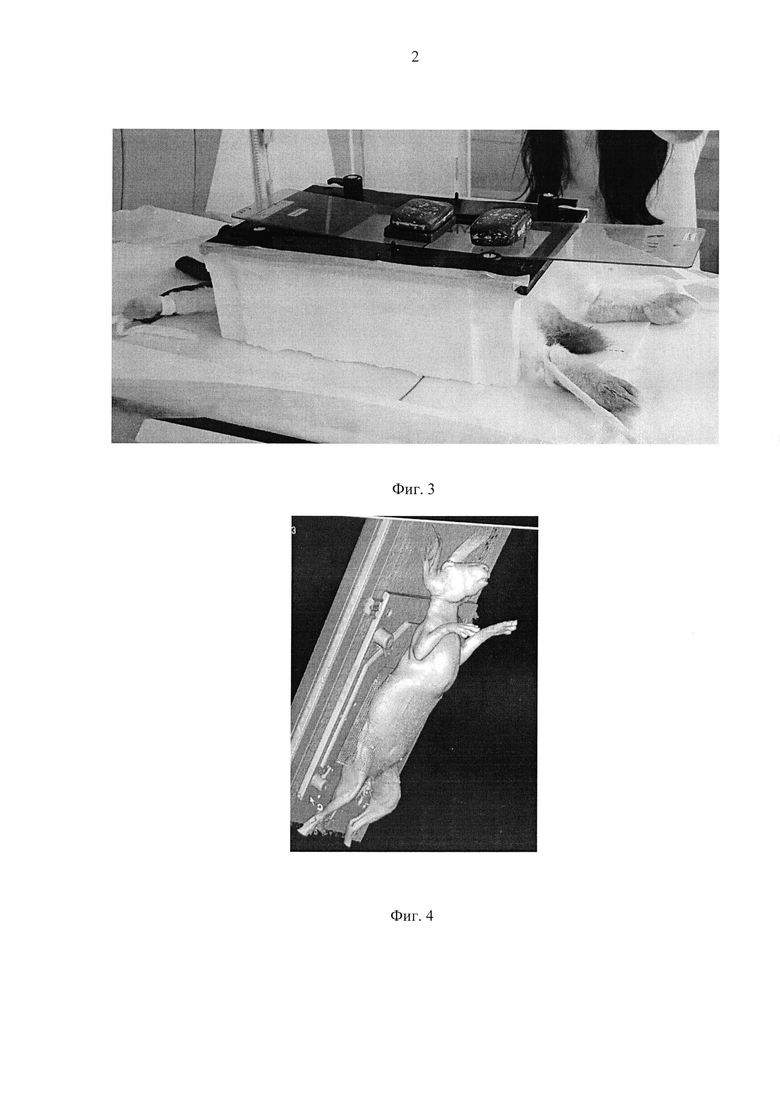
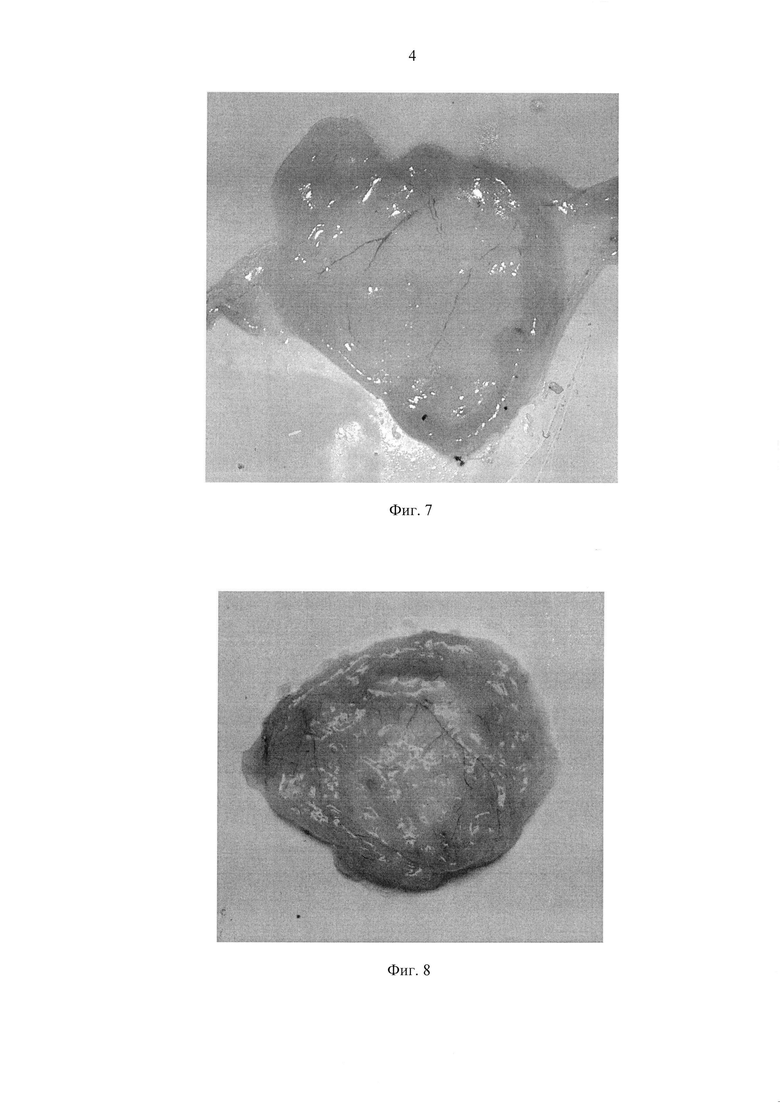
На фиг. 1 показана фиксация крысы на столе линейного ускорителя; на фиг. 2 - оконтуренный, контрастированный мочевой пузырь и трехмерная модель крысы; на фиг. 3 - фиксация кролика на столе линейного ускорителя; на фиг. 4 - 3D модель кролика с контрастным веществом в мочевом пузыре; фиг. 5 - мочевой пузырь кролика, слизистая нормальная; фиг. 6 - мочевой пузырь кролика, слизистая гиперплазирована и гиперемирована. Лучевой цистит; фиг. 7 - мочевой пузырь крысы, нормальная слизистая; фиг. 8 - мочевой пузырь крысы, отек и гиперемия слизистой, расширенные сосуды. Лучевой цистит.
По предлагаемому способу осуществлялось моделирование лучевого цистита на трех крысах и двух кроликах. Животным была проведена анестезия: Медитомедин 0,1% и Тилетамин + золазепам 50 мг в соотношении 2/1, в количестве 0,15-0,18 мл, кроликов препаратами Медитомедин 0,1% и Тилетамин + золазепам 50 мг в соотношении 2/1, в количестве 0,2-0,3 мл.
В области полей облучения шерстку животного выбривали, с запасом более 1 см от края полей. Затем, последовательно животные под анестезией позиционировались на пластине из акрила. Эта пластина устанавливалась на пластинчатый фантом из твердой воды. Укладка на спине: при этом задние и передние лапки растягивались специальными мягкими вязками из бинта и крепились к лечебному столу линейного ускорителя для однозначного положения.
Сверху животным на поле облучения устанавливали тканеэквивалентный болюс толщиной 1 см, смещающий максимум ионизации дозы на уровень залегания мочевого пузыря животного до 0,5 см.
Далее осуществляли формирование поля облучения: для крыс размером право-лево 2.5 см, голова-хвост 2.3-2.6 см, для кроликов формировали поле размером право-лево 2.5 см, голова-хвост 2.3-4 см, в зависимости от размера животного, на проекцию нижней трети мочевого пузыря (Фиг. 1, Фиг. 3).
Центрацию поля облучения осуществляли по границам светового поля головки линейного ускорителя и пальпаторно определенных анатомических костных ориентиров таза и бедренных костей. Расстояние источник-поверхность после этого устанавливали равным 100 см.
Затем формировали области облучения свинцовыми блоками, которые укладывали по краям поля облучения, тем самым формировали окно, гарантированно обеспечивая экранирование областей, лежащих выше и ниже поля в направлении голова-хвост.
Для обеспечения безопасности сосудов хвоста крыс, так как из него в дальнейшем забирали кровь для анализов, можно устанавливать дополнительный свинцовый блок на хвост.
Каждое животное облучали на линейном ускорителе электронов фотонами с граничной энергией квантов 6 МэВ, при этом крысы получали дозу 25 Гр в одной фракции, а кроликов облучали 5 последовательными фракциями с разовой очаговой дозой 6 Гр, до суммарной очаговой дозы 30 Гр.
Был получен лучевой цистит через 6-8 недель у всех животных (Фиг. 5, Фиг. 6, Фиг. 7, Фиг. 8), при этом летальных исходов не было, все животные были использованы в дальнейших исследованиях.
Вышеуказанные параметры подготовки модели были получены экспериментальным путем на 90 крысах и 32 кроликах.
Геометрические параметры облучения были установлены при определении объема и расположения мочевого пузыря животного путем исследования на компьютерном томографе Toshiba Aquillion при контрастном усилении с введением контрастного вещества непосредственно внутрь мочевого пузыря животного в положении лежа на спине. Исходя из полученных данных, была определена глубина залегания мочевого пузыря, которая составила 5-15 мм от передней брюшной стенки. Линейные размеры полей составили от 2.5×2.3 см для крысы до 2.5×4 см для кролика исходя из анализа полученных КТ изображений с учетом возможных погрешностей в укладке и вариаций в наполненности мочевого пузыря (Фиг. 2, Фиг. 4). В области полей облучения шерстку животного выбривали, с запасом более 1 см от края полей.
Расчет дозы был выполнен пользуясь системой дозиметрического планирования XiOCMS алгоритмом Clarkson на модели водного фантома, наиболее соответствующего плотности тканям живого организма. Расчетную точку доставки дозы задавали на глубину 1,5 см.
Контроль расчетной дозы был проведен на линейном ускорителе в водном фантоме IBAWP-1D дозиметром IBADOSE-1 ионизационными камерами среднего IBACC13 и малого IBACC01 объема. Данные ионизационные камеры имеют хорошее разрешение и подходят для измерений полей размерами меньше 3×3 см2. Полученные фактические, измеренные результаты совпали с рассчитанными на системе планирования с отклонениями +/- 1%.
Доставка дозы в мочевой пузырь животных осуществлялась на линейном ускорителе электронов с энергией фотонов 6 МэВ. Было установлено, что максимум ионизации дозы в этих условиях находится на глубине 1,5 см. Как известно, при облучении поля 10×10 см2 на глубине максимума ионизации дозы отпуск 100 мониторных единиц составляет дозу в 1 Гр. Как показали исследования, при мощности дозы 6 Гр/мин время облучения животных существенно сокращается.
Экспериментальные данные позволили установить оптимальные для получения модели лучевого цистита размеры полей облучения: для крыс право-лево 2.5 см, голова-хвост 2.3-2.6 см, для кроликов формировали поле размером право-лево 2.5 см, голова-хвост 2.3-4 см в зависимости от размера животного на проекцию нижней трети мочевого пузыря.
Пример 1.
Моделирование лучевого цистита было осуществлено с использованием предлагаемого способа на 18 кроликах линии «Калифорния», средним весом 2 кг, при этом еще 4 кролика были оставлены в группе контроля, однако все животные были введены в наркоз в одинаковой дозе для исключения влияния последнего. Облучение проводилось разовой очаговой дозой 6 Гр, один раз в сутки в течение 5 дней. При оценке результатов установлено, что через 6-8 недель после облучения у кроликов самцов и самок проявлялись симптомы лучевого цистита: тенденция к потере массы тела, тенденция к повышению ректальной температуры тела; тенденция к увеличению удельной плотности и снижению рН мочи, появление в моче белка и крови, увеличение в моче числа лейкоцитов; увеличение в крови абсолютного количества лейкоцитов и гранулоцитов. Произведена планировавшаяся программа исследований на всех облученных кроликах.
Пример 2.
По вышеописанной методике было осуществлено моделирование лучевого цистита с использованием 27 крыс породы "Вистар", при этом еще 3 крысы оставлены в контроле, однако все крысы были введены в наркоз в одинаковой дозе для исключения влияния последнего. Каждая крыса получала дозу 25 Гр в одной фракции.
Через 6-8 недель зафиксировано появление признаков постлучевого цистита в виде нарастания пиурии, микро-, а через 2 недели макрогематурии и протеинурии; увеличение в крови абсолютного количества лейкоцитов и гранулоцитов. Произведена планировавшаяся программа исследований на всех облученных крысах.
Использование способа позволяет создать модель лучевого цистита с целью проведения научных исследований, с высокой степенью достоверности позволяющих проводить доклинические исследования любых лекарственных препаратов для лечения лучевых циститов. Наряду с этим сокращаются расходы на приобретение и содержание лабораторных животных в связи с высоким процентом реализации экспериментального цистита при предлагаемых способом условиях. Кроме того, результат достигается без причинения дополнительных страданий экспериментальным животным.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ моделирования лучевого пульмонита в эксперименте | 2023 |
|
RU2816074C1 |
| Способ моделирования острой лучевой болезни в эксперименте | 2023 |
|
RU2811270C1 |
| Способ моделирования хронической ишемии у экспериментальных животных. | 2022 |
|
RU2777184C1 |
| СПОСОБ ФАРМАКОЛОГИЧЕСКОЙ ПРОФИЛАКТИКИ РАДИАЦИОННО-ИНДУЦИРОВАННОГО ЦИСТИТА И ФИБРОЗА МОЧЕВОГО ПУЗЫРЯ | 2024 |
|
RU2837550C2 |
| СПОСОБ КОМБИНИРОВАННОГО ЛЕЧЕНИЯ РАКА ТЕЛА МАТКИ Iв-IIа СТАДИИ | 2005 |
|
RU2322275C2 |
| Способ тотального облучения костного мозга и лимфатической системы | 2021 |
|
RU2791658C1 |
| Способ лечения больных раком кожи лица | 2019 |
|
RU2725048C1 |
| СПОСОБ КОМПЛЕКСНОГО ЛЕЧЕНИЯ РАННИХ СТАДИЙ ПЛОСКОКЛЕТОЧНОГО РАКА АНАЛЬНОГО КАНАЛА | 2013 |
|
RU2524419C1 |
| СПОСОБ СОЧЕТАННОЙ ФОТОННО-НЕЙТРОННОЙ ТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ | 2009 |
|
RU2428227C2 |
| Способ прогнозирования течения цистита в эксперименте | 2020 |
|
RU2739121C1 |


Изобретение относится к радиобиологии и экспериментальной медицине и может быть использовано для моделирования лучевого цистита. Для этого осуществляют анестезию животного, формирование области облучения свинцовым окном, с последующим облучением мочевого пузыря на линейном ускорителе. При этом центрируют поле облучения на животном на столе линейного ускорителя по световому полю и анатомическим костным ориентирам. Осуществляют формирование поля размером 2,5 см в направлении право-лево и 2,3-4,0 см в направлении голова-хвост животного в проекции нижней трети мочевого пузыря. Сверху в области поля облучения устанавливают ткане-эквивалентный болюс толщиной 1 см. Устанавливают расстояние источник-поверхность, равное 100 см. Облучение осуществляют фотонами с граничной энергией квантов 6 МэВ. При создании модели на крысе облучение проводят одной фракцией в дозе 25 Гр. При создании модели на кролике облучение проводят 5 фракциями с разовой очаговой дозой 6 Гр до суммарной очаговой дозы 30 Гр. Способ обеспечивает создание модели радиоиндуцированного цистита без применения дополнительных страданий экспериментальным животным с целью проведения научных исследований, позволяющих с высокой степенью достоверности осуществлять доклинические исследования лекарственных препаратов для лечения лучевых циститов. 8 ил., 2 пр.
Способ моделирования лучевого цистита, включающий анестезию животного, формирование области облучения свинцовым окном, с последующим облучением мочевого пузыря на линейном ускорителе, отличающийся тем, что центрируют поле облучения на животном на столе линейного ускорителя по световому полю и анатомическим костным ориентирам, осуществляют формирование поля размером 2,5 см в направлении право-лево и 2,3-4,0 см в направлении голова-хвост животного в проекции нижней трети мочевого пузыря, сверху в области поля облучения устанавливают ткане-эквивалентный болюс толщиной 1 см, устанавливают расстояние источник-поверхность, равное 100 см, при этом облучение осуществляют фотонами с граничной энергией квантов 6 МэВ, причем при создании модели на крысе облучение проводят одной фракцией в дозе 25 Гр, а при создании модели на кролике облучение проводят 5 фракциями с разовой очаговой дозой 6 Гр до суммарной очаговой дозы 30 Гр.
| KOHLER M | |||
| et al | |||
| "Histological Changes After Fractionated Whole or Partial Irradiation of the Rabbit Urinary Bladder" | |||
| Acta Oncologica | |||
| Нивелир для отсчетов без перемещения наблюдателя при нивелировании из средины | 1921 |
|
SU34A1 |
| СПОСОБ МОДЕЛИРОВАНИЯ СОЧЕТАННЫХ РАДИАЦИОННЫХ ПОРАЖЕНИЙ, ВКЛЮЧАЮЩИХ ОБЩЕЕ ГАММА-И МЕСТНОЕ БЕТА-ОБЛУЧЕНИЕ | 2013 |
|
RU2534802C1 |
| US 6667296 B1, 23.12.2003 | |||
| CN 2014453289 U, 12.05.2010 | |||
| ТАРАРОВА Е.А | |||
| "Патогенетические аспекты лучевого цистита" - автореферат дисс | |||
| на соиск | |||
| уч | |||
| ст | |||
| к.м.н., М., 2011, 24 c | |||
| MICHAILOV MC et al | |||
| "Influence of X-irradiation on the motor activity of rat urinary bladder in vitro and in vivo" | |||
| Strahlenter Onkol | |||
| Циркуль-угломер | 1920 |
|
SU1991A1 |
| BERNADETTE M.M | |||
| et al | |||
| "Modeling of chronic radiation-induced cystitis in mice" | |||
| Adv Radiat Oncol | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| ANTONAKOPOULOS GN et al | |||
| "Early and late morphological changes (including carcinoma of the urothelium) induced by irradiation of the rat urinary bladder" | |||
| Br J Cancer | |||
| Устройство для видения на расстоянии | 1915 |
|
SU1982A1 |
Авторы
Даты
2018-12-28—Публикация
2018-02-26—Подача