Изобретение относится к медицине, в частности, к радионуклидной диагностике злокачественных опухолей гортани и гортаноглотки методом однофотонной эмиссионной компьютерной томографии.
На сегодняшний день наиболее перспективными радиофармпрепаратами (РФП) для ранней диагностики злокачественных новообразований различных локализаций, в том числе опухолей головного мозга, являются меченные радиоактивными изотопами производные глюкозы. Это связано с тем, что в клетках опухоли отмечается повышенный по сравнению с нормальными клетками уровень метаболизма глюкозы. Поэтому при введении в организм радиофармацевтического препарата на основе меченой радионуклидом глюкозы отмечается гиперинтенсивная аккумуляция данного РФП в опухолевых клетках. Это в свою очередь позволяет на ранних стадиях выявлять злокачественные новообразования и оценивать распространенность процесса.
В настоящее время в России и за рубежом для диагностики опухолей и оценки эффективности противоопухолевой терапии применяется, главным образом, метод позитрон-эмиссионной томографии (ПЭТ) с РФП 2-фтор-2-дезокси-D-глюкоза (18F-ФДГ), содержащий позитрон-излучающий радионуклид фтор-18 [Baum R.P., Schmuecking М, Bonnet R. et all. F-18 FDG PET for metabolic 3D-radiation treatment planning of non-small cell lung cancer. // Eur. J. Nucl. Med. and Mol. Imag. - 2002. Vol. 43. - P. 96-99]. Несмотря на высокую диагностическую информативность метода ПЭТ, его широкое применение в России ограничено из-за высокой стоимости, а также малой распространенности ПЭТ-центров. Так стоимость одного обследования с 18F-ФДГ (в зависимости от исследуемой области) колеблется от 30 тыс. рублей и более, а ориентировочная стоимость строительства ПЭТ-центра составляет около 1 миллиарда рублей. В данное время в России реально функционируют около 30 центров позитронно-эмиссионной томографии, половина которых расположены в Москве и Санкт-Петербурге.
Вместе с тем, в стране существует более 250 центров, оснащенных гамма-камерами для проведения однофотонной эмиссионной компьютерной томографии (ОФЭКТ), где диагностика чаще всего осуществляется с использованием РФП на основе наиболее доступного для медицины радионуклида короткоживущего (Т1/2=6,02 ч) технеция-99м (99mТс). Как правило, технециевые РФП изготавливаются в виде стандартных наборов реагентов (лиофилизатов) к генератору технеция-99м, которые представляют собой смеси, приготовленные методом сублимационной сушки при низких температурах [Лыков А.В. Сублимационная сушка // В кн.: Теория сушки. - М., Энергия. -1968. - С. 334-362]. При их смешивании с элюатом технеция-99м (раствор натрия пертехнетата, 99mТс), выделенного из генератора, получается готовый РФП с заданными свойствами. Срок годности лиофилизатов обычно составляет 1 год.
Наиболее близким к предлагаемому является способ диагностики рака гортани и гортаноглотки с применением меченного технецием-99m метоксиизобутилизонитрила (99mТс-МИБИ). Используемый в известном способе радиофармацевтический препарат является неспецифическим препаратом, накапливающемся в опухолевых клетках. 99mТс-МИБИ проникает в клетки опухоли путем пассивной диффузии и аккумулируется в митохондриях. Известно, что количество митохондрий в цитоплазме опухолевых клеток зависит от метаболической активности клетки, соответственно, уровень аккумуляции 99mТс-МИБИ в опухолевых клетках прямо пропорционален количеству жизнеспособных клеток и количеству митохондрий в них. На сегодняшний день представлено большое количество работ посвященных применению 99mТс-МИБИ для визуализации опухолей гортани и гортаноглотки: [Зельчан Р.В., Чернов В.И., Медведева А.А., Синилкин И.Г., Брагина О.Д., Чижевская С.Ю., Чойнзонов Е.Л. Использование однофотонной эмиссионной компьютерной томографии с 99МТС-МИБИ И 199ТL-хлоридом в диагностике и оценке эффективности химиотерапии первичных и рецидивных опухолей гортани и гортаноглотки // Евразийский онкологический журнал. - 2016. - №1. - С. 9-16]. Однако, физиологическое накопление 99mТс-МИБИ в щитовидной железе, а также в различных группах слюнных желез экранирует область гортани и зоны регионарного лимфооттока, тем самым затрудняя интерпретацию полученных при исследовании данных и, как правило, ведет к гиподиагностике.
Новый технический результат - повышение точности и информативности способа.
Для достижения нового технического результата в способе радионуклидной диагностики рака гортани и гортаноглотки, включающем внутривенное введение радиофармпрепарата и последующую однофотонную эмиссионную компьютерную томографии, вводят радиофармацевтический препарат на основе на основе меченной технецием-99m производной глюкозы, содержащий 1-тио-D-глюкозы натриевая соль гидрат 0,625 мг, олова дихлорид 2-водный 0,044-0,052 мг, аскорбиновой кислоты не более 0,125 мг, натрия хлорида 8,0-10,0 мг вода для инъекций до 1 мл, в дозе 500 МБк, через 40 минут после введения выполняют однофотонную эмиссионную компьютерную томографию на двух детекторной гамма-камере, полученные изображения подвергают постпроцессинговой обработке с использованием пакета специализированных программ и при визуализации асимметричных участков гиперфиксации препарата в проекции гортани или гортаноглотки диагностируют злокачественное новообразование.
Способ осуществляют следующим образом
Пациенту с подозрением на рак гортани и гортаноглотки вводят радиофармацевтический препарат содержащий содержащий 1 однофотонной эмиссионной компьютерной томографии, в дозе 500 МБк. Радиофармацевтический препарат на основе меченной технецием-99m производной глюкозы готовили непосредственно перед введением согласно разработанному авторами лабораторному регламенту: 4 мл раствора натрия пертехнетата (Na99mTcO4) из генератора в асептических условиях вводили с помощью шприца во флакон с реагентом путем прокалывания резиновой пробки иглой. При необходимости предварительно проводили разбавление элюата изотоническим раствором натрия хлорида до требуемой величины объемной активности. Содержимое флакона перемешивали встряхиванием и инкубировали при комнатной температуре в течение 30 минут до полного растворения реагента (лабораторный регламент получения РФП ЛР-01895186-02-15 от 19.08.2015 г). Состав радиофармацевтического препарата представлен в таблице 1 Приложения.
Через 40 минут после внутривенного введения препарата выполняют однофотонную эмиссионную компьютерную томографию (ОФЭКТ) на двух детекторной гамма-камере Е.CAM фирмы SIEMENS в стандартном режиме, производят запись 64 проекций в матрицу 64×64 пикселя с применением низкоэнергетических коллиматоров с энергией 140 КэВ. Окно дифференциального дискриминатора настроено на 20%, аппаратное увеличение не использовалось.
Полученные при исследовании изображения (сцинтиграммы) подвергают постпроцессинговой обработке с использованием фирменного пакета программ E.Soft (SIEMENS, Германия). Патологическими считают асимметричные участки повышенной аккумуляции препарата в проекции гортани и гортаноглотки
Способ основан на анализе результатов экспериментальных клинических исследований. Для подтверждения эффективности способа в визуализации злокачественных опухолей гортани и гортаноглотки были проведены экспериментальные клинические исследования по изучению накопления радиофармацевтического препарата у пациентов с верифицированным диагнозом рака гортани или гортаноглотки T1-4N0-1M0 в количестве 10 человек. Всем пациентам внутривенно вводили разработанный радиофармацевтический препарат на основе меченной технецием-99m производной глюкозы, на который было получено разрешение на клинические испытания, содержащий: 1-тио-D-глюкозы натриевая соль гидрат 0,625 мг, олова дихлорид 2-водный 0,044-0,052 мг, аскорбиновой кислоты не более 0,125 мг, натрия хлорида 8,0-10,0 мг вода для инъекций до 1 мл. Радиофармацевтический препарат на основе меченной технецием-99m производной глюкозы готовили непосредственно перед введением согласно разработанному авторами лабораторному регламенту: 4 мл раствора натрия пертехнетата (Na99mTcO4) из генератора в асептических условиях вводили с помощью шприца во флакон с реагентом путем прокалывания резиновой пробки иглой. При необходимости предварительно проводили разбавление элюата изотоническим раствором натрия хлорида до требуемой величины объемной активности. Содержимое флакона перемешивали встряхиванием и инкубировали при комнатной температуре в течение 30 минут до полного растворения реагента (лабораторный регламент получения РФП ЛР-01895186-02-15 от 19.08.2015 г).
Через 40 минут после внутривенного введения препарата выполняли ОФЭКТ на двух детекторной гамма-камере Е.САМ фирмы SIEMENS в стандартном режиме, производили запись 64 проекций в матрицу 64×64 пикселя с применением низкоэнергетических коллиматоров с энергией 140 КэВ. Окно дифференциального дискриминатора настроено на 20%, аппаратное увеличение не использовалось.
Полученные при исследовании изображения (сцинтиграммы) подвергали постпроцессинговой обработке с использованием фирменного пакета программ E.Soft (SIEMENS, Германия). Патологическими считались асимметричные участки повышенной аккумуляции препарата в проекции гортани или гортаноглотки. Результаты исследования продемонстрировали 100% чувствительность способа в диагностике злокачественных опухолей гортани и гортаноглотки, то есть с применением указанного радиофармпрепарата удалось визуализировать опухоль у всех пациентов, включенных в исследование.
Клинический пример.
Пациент К., 56 лет.
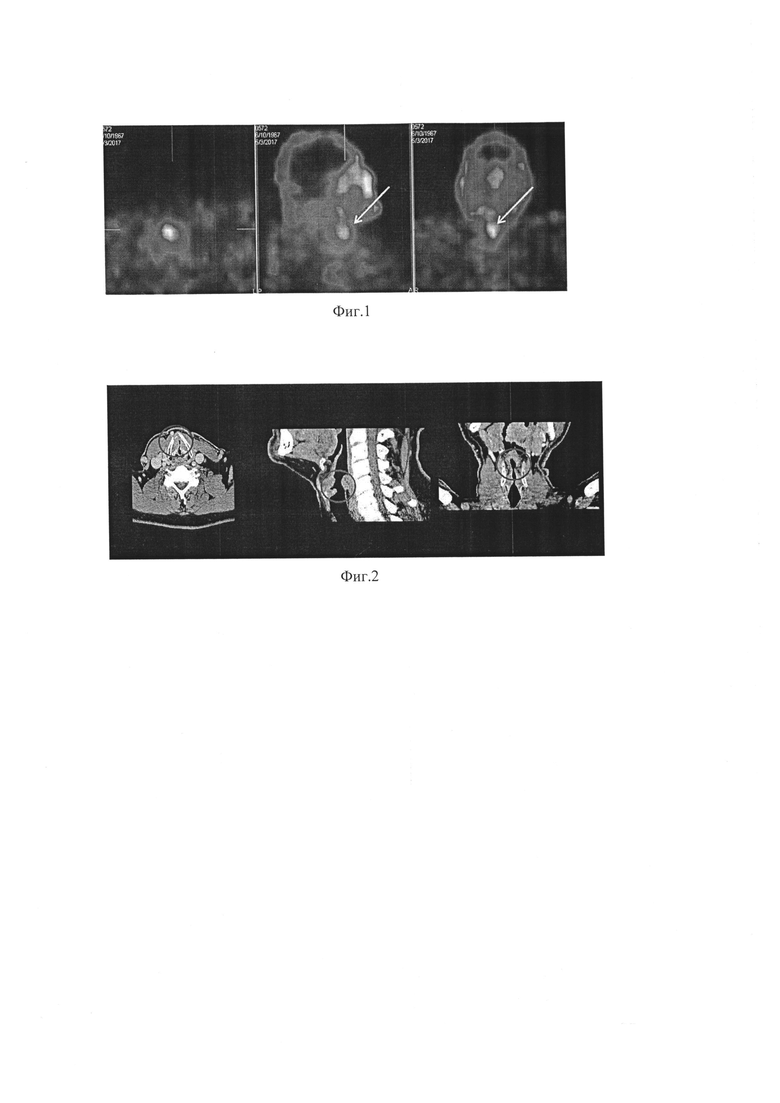
Ds.: Рак гортани T3N0M0, формирующийся стеноз. Обратился в поликлинику по месту жительства с жалобами на затруднение дыхания и осиплость голоса. Был направлен к онкологу в профильное учреждение. При обследовании были проведены видеоларингоскопия, компьютерная томография и исследование согласно предлагаемому способу-однофотонная эмиссионная компьютерная томография с РФП на основе меченной технецием-99m производной глюкозы. Результаты компьютерной томографии и однофотонной эмиссионной компьютерной томографии представлены на Фиг. 1 и 2.
На Фиг 1 - ОФЭКТ с РФП пациента с диагнозом Рак гортани T3N0M0, формирующийся стеноз: визуализируется очаг метаболической гиперфиксации препарата в проекции гортани занимающий обе половины гортани и переднюю комиссуру.
На Фиг 2 - КТ того же пациента с диагнозом Рак гортани T3N0M0, формирующийся стеноз: визуализируется объемное образование в проекции гортани занимающий обе половины гортани и переднюю комиссуру на фоне выраженного отека голосовых складок.
Таким образом, предлагаемый способ радионуклидной диагностики рака гортани и гортаноглотки с применением радиофармацевтического препарата на основе меченной технецием-99m производной глюкозы позволяет отчетливо визуализировать злокачественные опухоли гортани и гортаноглотки на метаболическом уровне, степень аккумуляции представленного радиофармпрепарата в опухоли дает возможность получать сцинтиграфические изображения надлежащего качества. Таким образом, применение нового способа позволит повысить эффективность диагностики злокачественных опухолей гортани и гортаноглотки методом однофотонной эмиссионной компьютерной томографии.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ оценки регионарной распространенности рака молочной железы методом однофотонной эмиссионной компьютерной томографии | 2017 |
|
RU2679302C1 |
| Способ радионуклидной диагностики рака легкого | 2020 |
|
RU2751103C1 |
| Способ радионуклидной диагностики рака молочной железы | 2017 |
|
RU2682880C1 |
| Способ радионуклидной диагностики опухолей головного мозга | 2017 |
|
RU2692451C2 |
| Способ диагностики рака ободочной кишки | 2021 |
|
RU2755010C1 |
| Способ оценки эффективности химиотерапии злокачественных лимфом | 2019 |
|
RU2700105C1 |
| Способ радионуклидной диагностики злокачественных лимфом | 2018 |
|
RU2706602C1 |
| Способ диагностики опухоли | 2017 |
|
RU2657761C1 |
| Способ радионуклидной диагностики рака предстательной железы | 2021 |
|
RU2776234C1 |
| Способ диагностики рака желудка с гиперэкспрессией Her2/neu | 2020 |
|
RU2739107C1 |

Изобретение относится к медицине, а именно к онкологии и лучевой диагностике, и может быть использовано для радионуклидной диагностики рака гортани и гортаноглотки. Изготавливают радиофармацевтический препарат (РФП) непосредственно перед его внутривенным введением. Для этого в асептических условиях вводят с помощью шприца 4 мл раствора натрия пертехнетата Na99mTcO4 из генератора во флакон с реагентом. Состав реагента следующий: 1-тио-D-глюкозы натриевой соли гидрат 0,625 мг, олова дихлорид 2-водный 0,044-0,052 мг, аскорбиновая кислота не более 0,125 мг, натрия хлорид 8,0-10,0 мг, вода для инъекций до 1 мл. Содержимое флакона перемешивают встряхиванием и инкубируют при комнатной температуре в течение 30 минут до полного растворения реагента. Вводят полученный РФП на основе меченной технецием-99m производной глюкозы в дозе 500 МБк. Через 40 минут после введения РФП выполняют однофотонную эмиссионную компьютерную томографию на двухдетекторной гамма-камере. Подвергают полученные изображения постпроцессионной обработке. Диагностируют злокачественное новообразование при визуализации участков гиперфиксации РФП в проекции гортани или гортаноглотки. Способ обеспечивает повышение точности и информативности радионуклидной диагностики рака гортани и гортаноглотки за счет использования РФП на основе меченной технецием-99m производной глюкозы и однофотонной эмиссионной компьютерной томографии. 2 ил., 1 табл., 1 пр.
Способ радионуклидной диагностики рака гортани и гортаноглотки, включающий внутривенное введение радиофармпрепарата и последующую однофотонную эмиссионную компьютерную томографию, отличающийся тем, что вводят радиофармацевтический препарат (РФП) на основе меченной технецием-99m производной глюкозы, изготавливаемый непосредственно перед введением, для чего 4 мл раствора натрия пертехнетата Na99mTcO4 в асептических условиях вводят с помощью шприца во флакон с реагентом в составе: 1-тио-D-глюкозы натриевой соли гидрат 0,625 мг, олова дихлорид 2-водный 0,044-0,052 мг, аскорбиновая кислота не более 0,125 мг, натрия хлорид 8,0-10,0 мг, вода для инъекций до 1 мл, содержимое флакона перемешивают встряхиванием, инкубируют при комнатной температуре в течение 30 минут до полного растворения реагента, вводят полученный РФП в дозе 500 МБк, через 40 минут после введения препарата выполняют однофотонную эмиссионную компьютерную томографию на двухдетекторной гамма-камере и при визуализации участков гиперфиксации РФП в проекции гортани или гортаноглотки диагностируют злокачественное новообразование.
| Зельчан Р.В | |||
| и др | |||
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| Минск | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| СПОСОБ И СОСТАВ ДЛЯ ПОЛУЧЕНИЯ РЕАГЕНТА ДЛЯ РАДИОНУКЛИДНОЙ ДИАГНОСТИКИ НА ОСНОВЕ МЕЧЕННОЙ ТЕХНЕЦИЕМ-99m 5-ТИО-D-ГЛЮКОЗЫ | 2014 |
|
RU2568888C1 |
| Состав и способ получения реагента для радионуклидной диагностики на основе меченной технецием-99m 1-тио-D-глюкозы | 2016 |
|
RU2644744C1 |
| WO 2001070724 A1, 27.09.2001 | |||
| US 20030228255 A1, 11.12.2003 | |||
| Оралов Д.В | |||
| и др | |||
| Значение однофотонной эмиссионной компьютерной томографии при первичном гиперпаратиреозе | |||
| // REJR | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Zeltchan R | |||
| et al | |||
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| // IOP Conference Series: Materials Science and Engineering | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| Способ обделки поверхностей приборов отопления с целью увеличения теплоотдачи | 1919 |
|
SU135A1 |
| Визирный прибор для определения координат точек разрыва | 1927 |
|
SU12054A1 |
Авторы
Даты
2019-02-06—Публикация
2017-10-02—Подача