Карбосилан-силоксановые дендримеры первой генерации
Изобретение относится к области химии кремнийорганических соединений и может найти промышленное применение при получении гидрокси-функционализированных гидрофобных гиперразветвленных полиорганосилоксанов, в том числе дендримерной структуры. Такие соединения могут найти применение в производстве гидрофобных наноструктурированных покрытий и композиций. Более конкретно, изобретение относится к новым функционализированным органосилоксановым полимерам, имеющим дендримерную разветвленную структуру, содержащие в качестве ядра дендримера циклооктасилсесквиоксановый фрагмент, и имеющим концевые алкильные и гидроксильные группы.
Под дендримерами понимают разветвленные молекулы со сложной, чаще всего трехмерной, структурой, молекулярная масса которых лежит в области молекулярных масс олигомеров или полимеров. Однако дендримеры имеют то преимущество, что их можно получать с точно заданными молекулярной массой и размерами, в то время как в случае обычных полимеров всегда имеется распределение по молекулярным массам и геометрии молекул. Это свойство дендримеров определяет их применение в качестве наноблоков для получения наногибридных полимерных материалов с заданным пространственным строением. Кроме того, имеющаяся возможность получения многофункциональных дендримеров с определенным количеством реакционноспособных (функциональных) концевых групп, позволяет контролировать поверхностные свойства и морфологию получаемых материалов на их основе, поэтому они являются исключительно важными соединениями для получения различных пленок и мембран. Материалы на основе дендримеров также находят широкое применение в электрохимии, оптике, катализе и других наукоемких отраслях.
Удобными исходными кремнийсодержащими наноблоками для получения наноструктурированных материалов с заданной пространственной структурой являются производные октаорганилсилсесквиоксанов, химия которых изучена достаточно широко.
Синтез карбосилановых дендримеров стандартно осуществляется чередованием реакций гидросилилирования и реакции хлор-функционализированных продуктов с соответствующими реактивами Гриньяра. В качестве ядер, помимо октавинилсилсесквиоксана, используются полифункциональные молекулы, содержащие винильные и аллильные группы, например, тетравинилсилан (US 5276110, дата публикации 04.01.1994) и тетрааллилсилан (Е.А. Татаринова, Е.А. Ребров, В.Д. Мякушев, И.Б. Мешков, Н.В. Демченко, А.В. Быстрова, О.В. Лебедева, A.M. Музафаров «Синтез и изучение свойств гомологического ряда полиаллилкарбосилановых дендримеров и их нефункциональных аналогов» Изв. АН, Сер. хим., 2004, 11, с. 2484-2493).
Известно получение диэтил- и дифенилфосфин-функционализированных дендримеров 1-ой и 2-ой генерации на основе октавинилсилсесквиоксана, которые были использованы в качестве лигандов в каталитической реакции гидроформилирования октена-1 (L. Ropartz, R.E. Morris, D.F. Foster, D.J. Cole-Hamilton. Phosphine-containing carbosilane dendrimers based on polyhedral silsesquioxane cores as ligands for hydroformylation reaction of oct-1-ene. J. Mol. Cat. A: Chem. 2002, Vol. 182-183, pp. 99-105).
Известно получение регенерируемых каталитически активных дендримеров нескольких поколений, содержащих концевые алкоксититановые группы на основе октавинилсилсесквиоксана, предназначенные для использования в реакциях переэтерификации, амидирования и полимеризации (WO 2004022231, дата публикации 18.03.2004).
Наиболее близкими по строению к заявленным дендримерам являются функционализированные дендримеры 1-ого поколения на основе октавинилсилсесквиоксана, содержащие на периферии алкильные и гидроксильные группы при атомах кремния (P.I. Coupar, P.-A. JaVres, R.E. Morris. Synthesis and characterisation of silanol-functionalised dendrimers. J. Chem. Soc., Dalton Trans., 1999, pp. 2183-2187). В данной статье описано получение дендримеров 1-ого и 2-ого поколения, содержащих концевые метильные и гидроксильные группы при атомах кремния. Для получения дендримеров последовательно применяли реакцию гидросилилирования октавинилсилсесквиоксана диметилхлорсиланом и замещения хлор-групп на гидроксо-группы либо путем прямого гидролиза, либо восстановлением до гидридных групп, с последующим замещением на гидроксогруппы. Получены достаточно устойчивые при хранении дендримеры с выходами 65% для 1-ого поколения. Возможность применения полученных дендримеров, по мнению авторов, заключается в использовании их в качестве наночастиц подобных наночастицам оксида кремния для координации на их поверхности атомов металлов, с целью получения каталитически активных комплексов.
Недостатками описанных соединений являются: - сложность введения алкильного заместителя отличного от метила, так как коммерчески доступным является только диметилхлорсилан, а получение других диалкилхлорсиланов является практически сложной задачей; - использование на стадиях замены заместителей таких дорогостоящих реагентов, как палладий на углероде и алюмогидрид лития. Описанные недостатки приводят к тому, что полученные соединения могут использоваться только в том виде, в котором они представлены, без возможности внесения изменений в структуру с целью достижения оптимальных результатов в практическом использовании.
В описании используются следующие обозначения дендримеров:
Т8 - октасилсесквиоксановое ядро дендримеров общей формулы (SiO1,5)8.
T8R8 - общая формула полнофункционализированных дендримеров на основе октасилсесквиоксанового ядра.
Т8(-CH2CH2SiAlk2.375OH0.625)8 - дендримеры карбосилан-силоксановой структуры 1-ого поколения с алкильными (бутил-, гептил-, цетил-) и гидроксильными группами на концевых атомах кремния.
Задача данного изобретения - получение новых карбосилан-силоксановых дендримеров первой генерации, с гидроксильными и алкильными заместителями различной длины во внешнем слое.
Технический результат заключается в получении новых карбосилан-силоксановых дендримеров, с алкильными заместителями различной длины во внешнем слое, не обладающими полидисперсностью и способными к дальнейшим превращениям за счет наличия во внешнем слое гидроксильных групп при атомах кремния, и при этом достаточно стабильными при хранении.
Задача решается тем, что получены новые карбосилан-силоксановые дендримеры 1-ого поколения, содержащие во внешнем слое соответствующее количество алкильных заместителей (бутил-, гептил-, цетил-) и гидроксильных групп, соединенных с концевыми атомами кремния дендримера, общей формулы (I)

В частности, получен карбосилан-силоксановыи дендример 1-ого поколения Т8(-CH2CH2-Si(Bu2.375OH0.625))8, где Bu=n-С4Н9.
В частности, получен карбосилан-силоксановый дендример 1-ого поколения Т8(-CH2CH2-Si(Hept2.375OH0.625))8, где Hept=n-С7Н15.
В частности, получен карбосилан-силоксановый дендример 1-ого поколения Т8(-CH2CH2-Si(Cet2.375OH0.625))8, где Cet=n-C16H33.
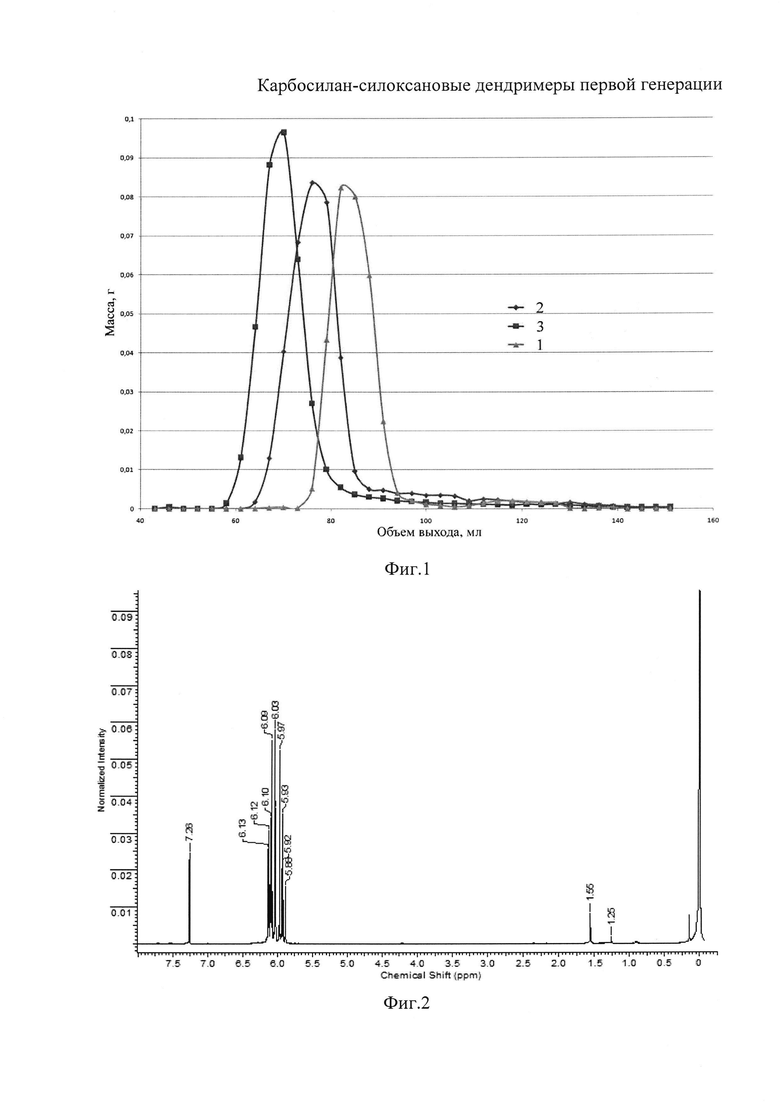
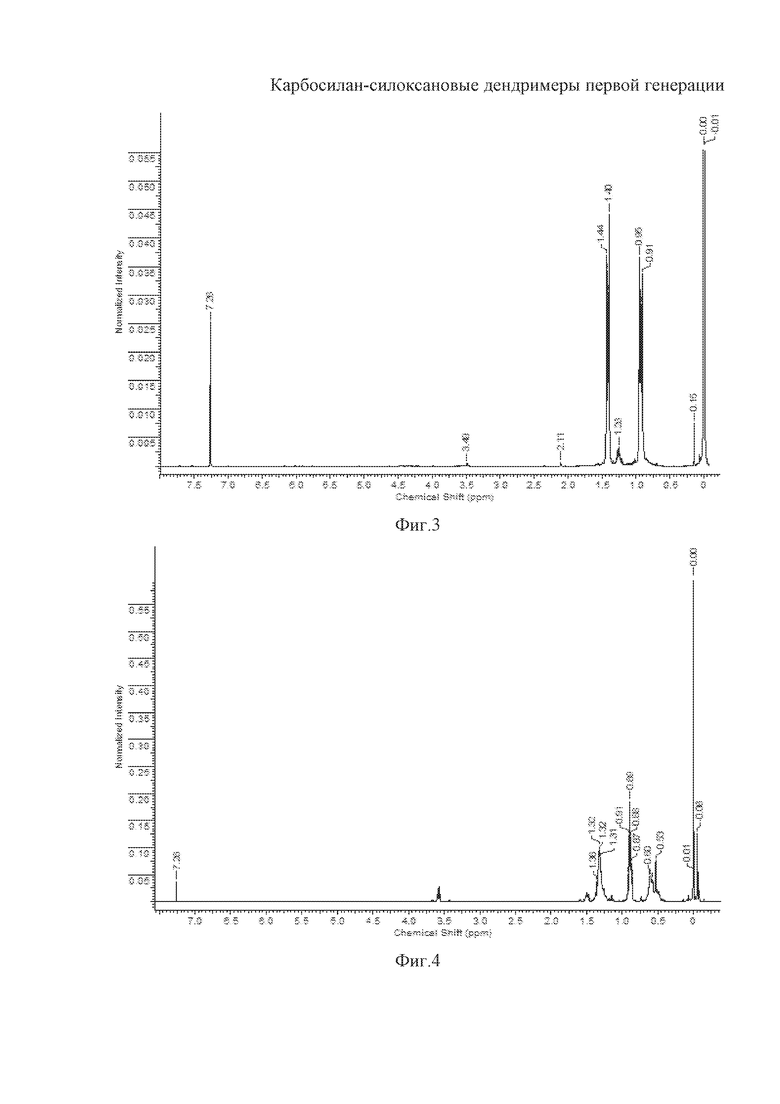
На фиг. 1 представлена хроматограмма соединений по примерам 1, 2 и 3 (зависимость массы вещества от объема выхода); на фиг. 2 представлен 1Н ЯМР спектр исходного октавинилсилоксана; на фиг. 3 представлен 1Н ЯМР спектр хлор-функционализированного производного октавинилсилсесквиоксана ((Т8(-CH2-CH2-SiCl3)8)); на фиг. 4 представлен 1Н ЯМР спектр целевого дендримера по примеру 1, с замещенными гидроксильными группами на метильные радикалы, для получения более точной информации по ЯМР.
Синтез карбосилан-силоксановых дендримеров Т8(-CH2CH2-Si(Alk2.375OH0.625))8 осуществляли в три стадии по схеме:
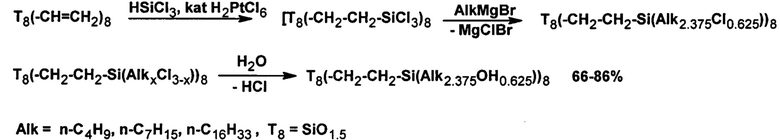
Первая стадия - реакция гидросилилирования октавинилсилсесквиоксана трихлорсиланом в присутствие катализатора гексахлорплатиновой кислоты. Вторая стадия - взаимодействие полученного 24-хлор-функционализированного производного (Т8(-CH2-CH2-SiCl3)8) с реактивами Гриньяра. Были использованы бутил-, гептил- и цетилмагнийбромид. Обычно подобные реакции проводятся в растворе диэтилового эфира при температуре его кипения, однако, в нашем случае вследствие высокой плотности расположения групп, при таких условиях возможно заместить не более половины атомов хлора на алкильный радикал, и чем длиннее радикал, тем меньше степень замещения. После проведения третьей стадии - стадии гидролиза - такие соединения с большим числом гидроксильных групп, оказываются неустойчивыми даже в растворе, образуя при хранении пространственно сшитые полимеры. Поэтому для повышения степени функционализации взаимодействие реактивов Гриньяра с Т8(-CH2-CH2-SiCl3)8 проводилось в растворе диэтилового эфира в автоклаве при температуре 120°С в течение 6 часов. Полученные соединения представляли собой вязкие прозрачные (для бутил- и гептил-производных) и белые парафинообразные вещества (для цетил-производного), устойчивые в растворе органических растворителей (более 6 месяцев), но в чистом виде поликонденсирующиеся с образованием сшитых полимеров в течение 10-14 дней.
Кривые ГПХ карбосилан-силоксановых дендримеров по примерам 1, 2 и 3, с замещенными гидроксильными группами на метильные, (Фиг. 1) указывают на узкодисперсное молекулярно-массовое распределение синтезированных соединений. Полноту прохождения реакций контролировали по спектрам 1Н-ЯМР. На Фиг. 2 приведены спектры 1Н-ЯМР исходного октавинилсилсесквиоксана, хлор-функционализированного производного (Т8(-CH2-CH2-SiCl3)8) (Фиг. 3) и карбосилан-силоксанового дендримера по примеру 1, с замещенными гидроксильными группами на метильные (Фиг. 4). Из спектра дендримера (Т8(-CH2-CH2-SiCl3)8) видно полное исчезновение сигналов протонов винильных групп октавинилсилсесквиоксана в области 5.88-6.13 м.д. Соотношение интегральных интенсивностей протонов различных групп в приведенных спектрах соответствует расчетным величинам.
Исходные соединения синтезировали по известным методикам.
Синтез октавинилсилсесквиоксана проводили по методике, схожей с описанной в работе (Т.Н. Мартынова, В.П. Корчков. ЖОХ, 1982, Том. 52, №. 7, стр. 1585-1591). ViSiCl3 (80.75 г, 0.5 моль) прибавлялся при интенсивном перемешивании к 680 мл 95% этанола. Соотношение реагентов составляло ν(ViSiCl3) : ν(H2O) : ν(EtOH) = 1:3:11. Реакционная смесь перемешивалась 4 ч при 50°С и 72 ч при 6°С. Выпавший осадок дважды перекристаллизовывался из ацетона. Выход октавинилсилсесквиоксана составил 7.32 г (18.5%). 1Н ЯМР (400 MHz, CDCl3, ppm, δ): 6.13-5.88 (m, 24Н); 13С ЯМР (100 MHz, CDCl3, ppm, δ): 137.19, 128.87; 29Si ЯМР (80 MHz, CDCl3, ppm, δ): -79.78; ИК (KBr, ν, cm-1): 3068, 3028, 2988, 2962, 1604, 1410, 1276, 1112, 1006, 972, 780, 584, 464; ESI-MS (m/z): 654.93 [M+Na]+, вычислено для C16H24O12S18, 631.94; Элементный анализ: Вычислено С, 30.36; Н, 3.82; Si, 35.49; найдено С, 30.22; Н, 3.91; Si, 35.43.
Хлор-функционализированный октасилсесквиоксан (Т8(-CH2-CH2-SiCl3)8) был получен по методике, описанной в работе (P.-A. JaVres, R.E. Morris, J. Chem. Soc, Dalton Trans., 1998, Iss. 16, pp. 2767-2770).
Изобретение иллюстрируется следующими примерами.
Пример 1
Синтез дендримера Т8(-CH2CH2-Si(Bu2.375OH0.625))8
В автоклаве объемом 100 мл к суспензии 1.06 г (0.617 ммоль) Т8(-CH2-CH2-SiCl3)8 в 20 мл диэтилового эфира прибавляли 25 мл (25 ммоль) 1М раствора бутилмагнийбромида в диэтиловом эфире и нагревали в течении 6 ч при 120°С. Затем реакционную смесь вливали при перемешивании в раствор 2.7 г (50 ммоль) хлорида аммония в 50 мл воды, отделяли органический слой, экстрагировали диэтиловым эфиром и сушили над сульфатом натрия. Раствор упаривали до минимального объема и хроматографировали. Собранную целевую фракцию упаривали до необходимого объема. Выход целевого соединения был определен после упаривания растворителя и составил: 1.24 г (86%). Для съемки ЯМР спектров гидроксильные группы замещались на метильные, путем взаимодействия с избытком метилмагнийиодида.
1Н ЯМР (400 МГц, CDCl3, м.д., δ): -0.06 (s, 15Н, Si-CH3), 0.5-0.61 (m, 67Н, Si-CH2), 0.86-0.91 (t, 62H, CH3-CH2), 1.25-1.36 (m, 77H, CH2(alkyl)). 13C ЯМР (100 МГц, CDCl3, м.д., δ): -3.95 (CH3-Si); 3.82, 4.59 (Si-CH2-CH2-Si); 12.65-14.37 (CH3-CH2); 25.34-35.05 (CH2(alkyl)). 29Si ЯМР (80 МГц, CDCl3, м.д., δ): -65.96, -65.80 (SiO1,5); 4.59, 5.19 (SiAlk2CH3); 16.73 (SiAlk3). ИК (KBr, ν, см-1): 473, 542, 635, 1123, 1256, 1410, 1464, 2874, 2924, 2959. Элементный анализ (%): рассчитано для C97H218O12Si16 С 57.50, Н 10.84, Si 22.18; найдено С 57.34, Н 10.99, Si 21.91.
Пример 2
Синтез дендримера Т8(-CH2CH2-Si(Hept2.375OH0.625))8
В автоклаве объемом 100 мл к суспензии 1.06 г (0.617 ммоль) Т8(-CH2-CH2-SiCl3)8 в 20 мл диэтилового эфира прибавляли 30 мл (30 ммоль) 1М раствора гептилмагнийбромида в диэтиловом эфире и нагревали в течении 9 ч при 120°С. Затем реакционную смесь вливали при перемешивании в раствор 4 г (75 ммоль) хлорида аммония в 60 мл воды, отделяли органический слой, экстрагировали диэтиловым эфиром и сушили над сульфатом натрия. Раствор упаривали до минимального объема и хроматографировали. Собранную целевую фракцию упаривали до необходимого объема. Выход целевого соединения был определен после упаривания растворителя и составил: 2.11 г (66%). Для съемки ЯМР спектров гидроксильные группы замещались на метильные, путем взаимодействия с избытком метилмагнийиодида.
1Н ЯМР (400 МГц, CDCl3, м.д., δ): -0.06 (s, 15Н, Si-CH3), 0.5-0.59 (m, 67Н, Si-CH2), 0.86-0.90 (t, 66H, CH3-CH2), 1.26-1.30 (m, 210H, CH2(alkyl)). 13С ЯМР (100 МГц, CDCl3, м.д., δ): -3.94 (СН3-Si); 3.84-4.66 (Si-CH2-CH2-Si); 12.95-14.71 (CH3-CH2); 22.67-33.77 (CH2(alkyl)). 29Si ЯМР (80 МГц, CDCl3, м.д., δ): -65.98, -65.82 (SiO1,5); 4.53 (SiAlk2CH3); 16.61 (SiAlk3). ИК (KBr, ν, см-1): 471, 540, 723, 775, 841, 885, 1124, 1254, 1379, 1408, 1464, 2854, 2924, 2957. Элементный анализ (%): рассчитано для C154H332O12Si16 С 65.46, Н 11.84, Si 15.90; найдено С 65.33, Н 11.78, Si 15.65.
Пример 3
Синтез дендримера Т8(-CH2CH2-Si(Cet2.375OH0.625))8
В автоклаве объемом 100 мл к суспензии 1.06 г (0.617 ммоль) Т8(-CH2-CH2-SiCl3)8 в 20 мл диэтилового эфира прибавляли 50 мл (50 ммоль) 1М раствора цетилмагнийбромида в диэтиловом эфире и нагревали в течении 12 ч при 120°С. Затем реакционную смесь вливали при перемешивании в раствор 5.3 г (100 ммоль) хлорида аммония в 80 мл воды, отделяли органический слой, экстрагировали диэтиловым эфиром и сушили над сульфатом натрия. Раствор упаривали до минимального объема и хроматографировали. Собранную целевую фракцию упаривали до необходимого объема. Выход целевого соединения был определен после упаривания растворителя и составил: 3.03 г (76%). Для съемки ЯМР спектров гидроксильные группы замещались на метильные, путем взаимодействия с избытком метилмагнийиодида.
1Н ЯМР (400 МГц, CDCl3, м.д., δ): -0.06 (s, 13Н, Si-CH3), 0.5-0.58 (m, 70Н, Si-CH2), 0.86-0.90 (t, 63H, CH3-CH2), 1.20-1.35 (m, 572H, CH2(alkyl)). 13С ЯМР (100 МГц, CDCl3, м.д., δ): -3.89 (СН3-Si); 3.83-4.70 (Si-CH2-CH2-Si); 13.01-14.79 (СН3-СН2); 22.72-33.84 (CH2(alkyl)). 29Si ЯМР (80 МГц, CDCl3, м.д., δ): -65.98 (SiO1,5); 4.53 (SiAlk2CH3); 16.60 (SiAlk3). ИК (KBr, ν, см-1): 473, 721, 787, 854, 1126, 1254, 1468, 2851, 2920, 2957. Элементный анализ (%): рассчитано для C325H674O12Si16 С 74.66, Н 12.90, Si 8.58; найдено С 75.02, Н 13.13, Si 8.17.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОБРАЗОВАНИЯ ПОЛИГЕДРАЛЬНЫХ ОЛИГОМЕРНЫХ СИЛСЕСКВИОКСАНОВ (ВАРИАНТЫ) | 2000 |
|
RU2293745C2 |
| КАРБОСИЛАН-СИЛОКСАНОВЫЕ ДЕНДРИМЕРЫ | 2009 |
|
RU2422473C1 |
| ПОЛИАРИЛСИЛАНОВЫЕ ДЕНДРИМЕРЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2007 |
|
RU2353629C1 |
| ПОЛИАРИЛСИЛАНОВЫЕ МОНОДЕНДРОНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2007 |
|
RU2348657C1 |
| СПОСОБ ПОЛУЧЕНИЯ SIOH-ФУНКЦИОНАЛЬНЫХ ДЕНДРИМЕРНЫХ КАРБОСИЛАНОВ | 1998 |
|
RU2193576C2 |
| ФУНКЦИОНАЛЬНЫЕ КАРБОКСИЛАНЫ, СОДЕРЖАЩИЕ ТРИС(ГАММА-ТРИФТОРПРОПИЛ)СИЛИЛЬНУЮ ГРУППУ | 1999 |
|
RU2164516C1 |
| ПРОИЗВОДНОЕ ГИАЛУРОНОВОЙ КИСЛОТЫ И СОДЕРЖАЩЕЕ ЕГО ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2005 |
|
RU2390529C2 |
| МОДИФИЦИРОВАННЫЕ ПОЛИМЕРНЫЕ КОМПОЗИЦИИ | 2010 |
|
RU2558597C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЗВЕЗДООБРАЗНЫХ ПОЛИМЕРОВ | 2011 |
|
RU2589876C2 |
| СПОСОБ ПОЛУЧЕНИЯ СОЕДИНЕНИЯ, СОЕДИНЕНИЯ, КОМПЛЕКСНЫЙ МЕТАЛЛООРГАНИЧЕСКИЙ КАТАЛИЗАТОР | 2012 |
|
RU2652807C2 |
Изобретение относится к новым функционализированным органосилоксановым полимерам, имеющим дендримерную разветвленную структуру, содержащие в качестве ядра дендримера циклооктасилсесквиоксановый фрагмент. Предложены новые функционализированные карбосилан-силоксановые дендримеры первой генерации, содержащие во внешнем слое соответствующее количество алкильных и гидроксильных групп общей формулы T8(-CH2-CH2-Si(Alk2,375ОН0,625))8, где T8=(SiO1,5)8. Технический результат - получение новых карбосилан-силоксановых дендримеров с алкильными заместителями различной длины во внешнем слое, не обладающих полидисперсностью и способных к дальнейшим превращениям за счет наличия во внешнем слое гидроксильных групп при атомах кремния и при этом достаточно стабильных при хранении. 3 з.п. ф-лы, 4 ил., 3 пр.
1. Карбосилан-силоксановые дендримеры первой генерации, содержащие во внешнем слое соответствующее количество алкильных и гидроксильных групп общей формулы (I):
T8(-CH2-CH2-Si(Alk2.375R0,625))8, (I)
где T8=(SiO1.5)8, Alk означает алкильный радикал.
2. Карбосилан-силоксановый дендример по п.1, отличающийся тем, что Alk=-C4H9.
3. Карбосилан-силоксановый дендример по п.1, отличающийся тем, что Alk=-C7H15.
4. Карбосилан-силоксановый дендример по п.1, отличающийся тем, что Alk=-C16H33.
| P.I.Coupar, P.-A.Javres, R.E.Morris | |||
| Synthesis and characterization of silanol-functionalised dendrimers | |||
| J | |||
| Chem | |||
| Soc., Dalton Trans., 1999, pp.2183-2187 | |||
| КАРБОСИЛАН-СИЛОКСАНОВЫЕ ДЕНДРИМЕРЫ | 2009 |
|
RU2422473C1 |
| US 5677410 A, 14.10.1997 | |||
| СПОСОБ ПОЛУЧЕНИЯ SIOH-ФУНКЦИОНАЛЬНЫХ ДЕНДРИМЕРНЫХ КАРБОСИЛАНОВ | 1998 |
|
RU2193576C2 |
Авторы
Даты
2019-02-12—Публикация
2018-06-15—Подача