Изобретение относится к области химии кремнийорганических соединений и может найти промышленное применение при получении полиорганосилоксанов разветвленного строения, в частности многолучевых звездообразных, и при получении трехмерных метилсилоксановых сетчатых структур с многоцентровыми дендритными узлами. Такие соединения могут найти применение в медицинской и биологических отраслях, в качестве мембран особого назначения, в качестве молекулярных контейнеров, а также в качестве прекурсоров для получения различных гибридных органо-неорганических материалов. Более конкретно, изобретение относится к новым органосилоксановым полимерам, имеющим внутреннюю дендритную карбосилановую структуру, и внешний слой, состоящий из восьмичленных диметилциклосилоксанов, соединенных с концевым атомом кремния дендримера углеводородным спейсером.
Карбосилановые дендримеры являются относительно новым полимерным объектом, отличающимся разветвленной трехмерной пространственной структурой, не содержащей циклических фрагментов. Дендримеры обладают заданными строением и молекулярной массой, большим и при этом строго определенным количеством функциональных групп во внешнем слое. Синтез карбосилановых дендримеров осуществляют чередованием реакций гидросилилирования и реакции Гриньяра, исходя из полифункционального разветвляющего центра, например, тетрааллилисилана (Пономаренко С.А., Ребров Е.А., Бойко Н.И., Музафаров A.M., Шибаев В.П. "Синтез жидкокристаллических карбосилановых дендримеров первой-пятой генераций, содержащих концевые цианобифенильные группы". Высокомолек. соед. 1998. V.40. №8. p.1253-1265; Е.А.Татаринова, Е.А.Ребров, В.Д.Мякушев, И.Б.Мешков, Н.В.Демченко, А.В.Быстрова, О.В.Лебедева, A.M.Музафаров "Синтез и изучение свойств гомологического ряда полиаллилкарбосилановых дендримеров и их нефункциональных аналогов" Изв. АН, Сер. хим., 2004, 11, с.2484-2493), тетравинилсилана - (US 5276110), алкил(арил)тривинилсиланов (US 5677410) и т.д.
Известно, что модификацией поверхности карбосилановых дендримеров различных генераций получают соединения, обладающие полезными свойствами. Например, введением различных типов сахаров во внешнюю сферу карбосилановых дендримеров (US 2004040554) получают противовирусный препарат, обладающий специфической способностью к связыванию определенных типов вирусов.
Известно получение и использование карбосилановых дендримеров с органическими концевыми группами в качестве реагентов для обезвреживания ядовитых веществ (JP 2003212893).
Известно получение карбосилановых дендримеров с короткими полиэфирными и полисульфидными группами во внешнем слое (CA 2279000), соединенными с концевыми атомами кремния дендримера углеводородными мостиками. Показано, что такие модификации внешнего слоя позволяют проводить дальнейшие полимераналогичные преобразования с целью получения звездообразных структур различной природы, причем на данном этапе соединения гидролитически устойчивы.
Известно получение карбосилановых дендримеров с гидроксисилильными группами во внешнем слое, на основе которых возможно получение гибридных органо-неорганических, в том числе металлсодержащих, соединений для различных покрытий (US 5,677,410).
Не известны карбосилановые дендримеры, модифицированные во внешнем слое циклическими фрагментами на основе силоксанов.
Наиболее близкими по строению к заявляемым дендримерным соединениям с внешним диметилсилоксановым слоем циклического строения являются многолучевые полидиметилсилоксаны с карбосилановым дендритным разветвляющим центром (N.G.Vasilenko, E.A.Rebrov, A.M.Muzafarov, B.Epwein, B.Striegel, M.MolIer. "Preparation of multi-arm star polymers with polylithiated carbosilane dendrimers". Macromol.Chem. Phys. 1998. V.199. p.889-895.) В данной статье представлены карбосилановые дендримеры с внешним слоем, модифицированным линейными диметилсилоксановыми лучами с концевыми функциональными литийокси-группами. Наличие этих групп позволяет использовать такие соединения как для получения сшитых структур, так и для дальнейших преобразований с целью введения новых модифицирующих групп. Недостатком предложенного соединения является высокая активность концевых силоксанолятных активных центров, поскольку как хранение, так и дальнейшие преобразования требуют абсолютного отсутствия влаги, то есть дорогого аппаратурного оформления. При этом способ получения таких соединений - анионная полимеризация гексаметилциклотрисилоксанов - нетехнологичен, и, кроме того, этот способ не позволяет получать короткие диметилсилоксановые олигомеры на поверхности дендримеров и, соответственно, плотные сетки с малым расстоянием между узлами-дендримерами.
В описании используются следующие общепринятые обозначения дендримеров:
G-n(All) - дендример карбосилановой структуры генерации n с аллильными группами на концевых атомах кремния;
G-n(Cycle), что соответствует [Sim m+3(Cycle)] - карбосилан-силоксановый дендример генерации n, содержащий во внутренней карбосилановой структуре m атомов кремния и (m+3) 1,3,3,5,5,7,7-гептаметилциклотетрасилоксановых фрагментов во внешнем силоксановом слое. G-0(Cycle) соответствует [Si1 4(Cycle)]; G-l(Cycle) соответствует [Si5 8(Cycle)]; G-2(Cycle) соответствует [Si13 16(Cycle)]; G-3(Cycle) соответствует [Si29 32(Cycle)]; G-4(Cycle) соответствует [Si61 64(Cycle)]; G-5(Cycle) соответствует [Si125 128(Cycle)]; G-6(Cycle) соответствует [Si253 256 (Cycle)].
Задача данного изобретения - получение нового результата, заключающегося в создании новых карбосилан-силоксановых дендримеров, с короткими диметилсилоксановыми фрагментами во внешнем слое, не обладающими полидисперсностью и способными к дальнейшим превращениям и при этом достаточно стабильными при хранении.
Задача решается тем, что получены новые карбосилан-силоксановые дендримеры от нулевой G-O(Cycle) до шестой генерации G-6(Cycle), содержащие во внешнем слое соответствующее количество восьмичленных диметилсилоксановых циклов, соединенных с концевым атомом кремния дендримера пропильной группой, общей формулы (I)
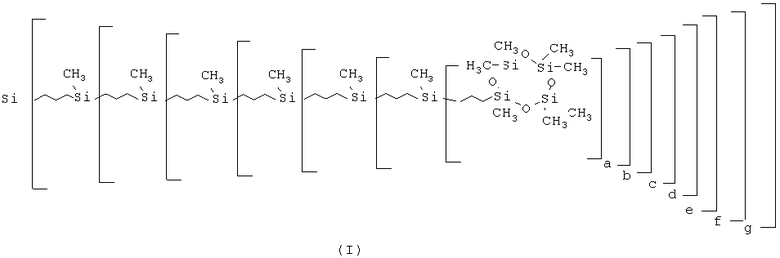
где a, b, c, d, e, f и g означает число групп, связанных с центром ветвления, и равно:
a равно 2 или 4;
b равно 0; 2 или 4;
c, d, e и f равно 0 или 2;
g равно 0 или 4.
В частности, получен карбосилан-силоксановый дендример нулевой генерации G-0(Cycle), где а равно 4, b, c, d, e, f и g равно 0. Соединение имеет следующую структуру и соответствует [Si1 4(Cycle)]:
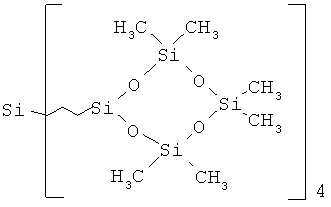
В частности, получен карбосилан-силоксановый дендример первой генерации G-l(Cycle), где а равно 2, b равно 4, c, d, e, f и g равно 0. Соединение имеет следующую структуру и соответствует [S1 5 (Cycle)]:
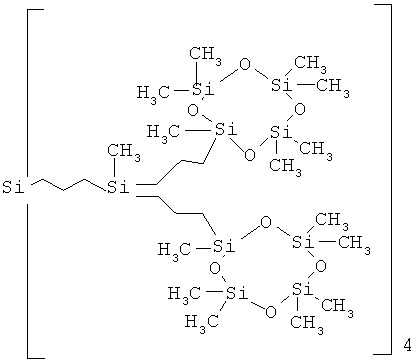
В частности, получен карбосилан-силоксановый дендример второй генерации G-2(Cycle), где а и в равно 2, c, d, e, f равно 0, g равно 4. Соединение имеет следующую структуру и соответствует [Si13 16(Cycle)]:
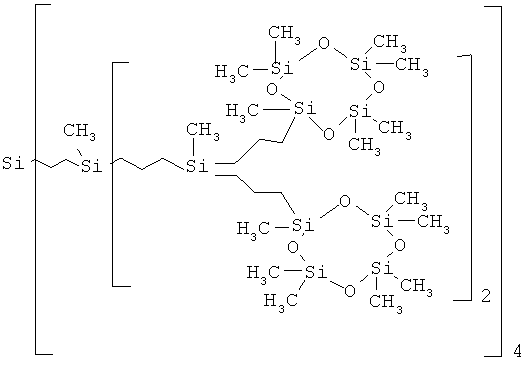
В частности, получен карбосилан-силоксановый дендример третьей генерации G-3(Cycle), где a, b и c равно 2, d, e, f равно 0, g равно 4. Соединение имеет следующую структуру и соответствует Si29 32(Cycle)]:
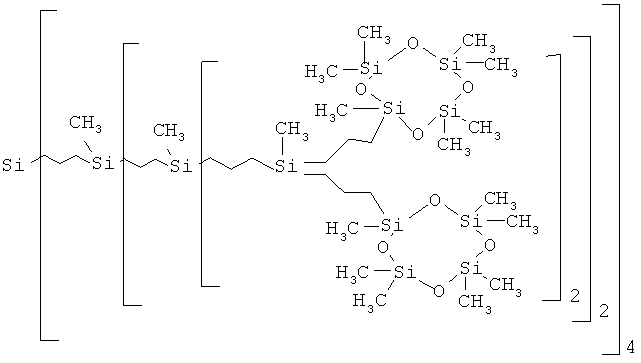
В частности, получен карбосилан-силоксановый дендример четвертой генерации G-4(Cycle), где a, b, c и d равно 2, e, f равно 0, g равно 4. Соединение имеет следующую структуру и соответствует [Si61 64(Cycle)]:
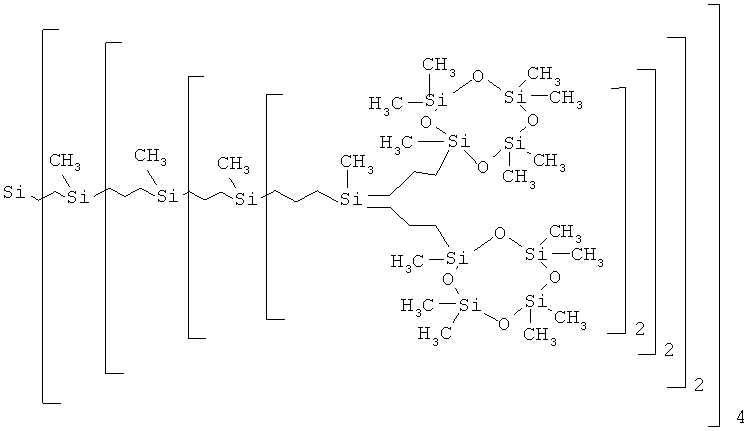
В частности, получен карбосилан-силоксановый дендример пятой генерации G-5(Cycle), где a, b, c, d и е равно 2, f равно 0, g равно 4. Соединение имеет следующую структуру и соответствует [Si125 128(Cycle)]:
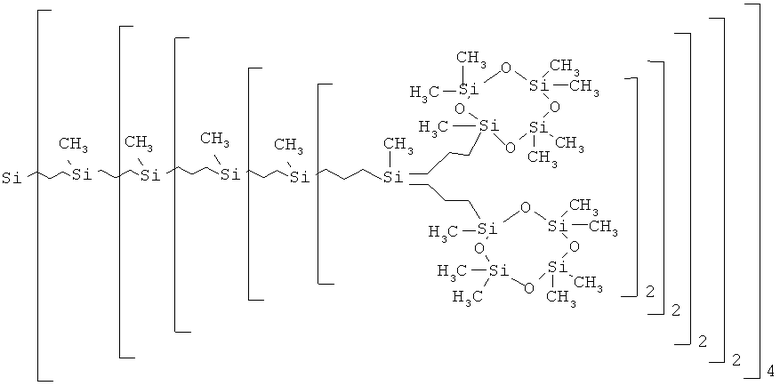
В частности, получен карбосилан-силоксановый дендример шестой генерации G-6(Cycle), где a, b, c, d, e и f равно 2, g равно 4. Соединение имеет следующую структуру и соответствует [Si253 256(Cycle)]:
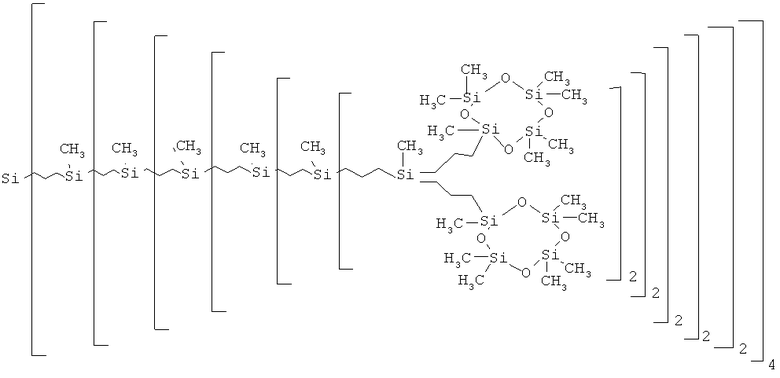
Синтез карбосилан-силоксановых дендримеров G-n(Cycle) осуществляли с использованием известной реакции гидросилилирования непредельных аллильных групп исходного карбосиланового дендримера G-n(All) гидридсилильной группой 1,3,3,5,5,7,7-гептаметилциклотетрасилоксана (US 5210247) в присутствии платиновых катализаторов по схеме:
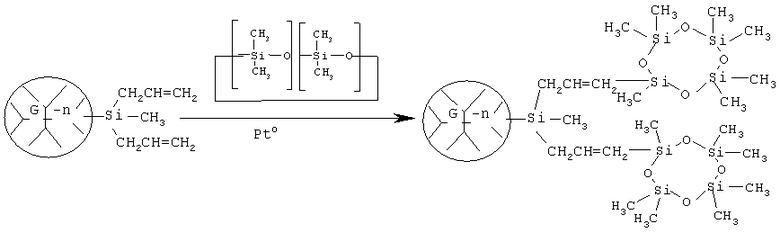
где 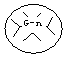 - карбосилановый дендример генерации n.
- карбосилановый дендример генерации n.
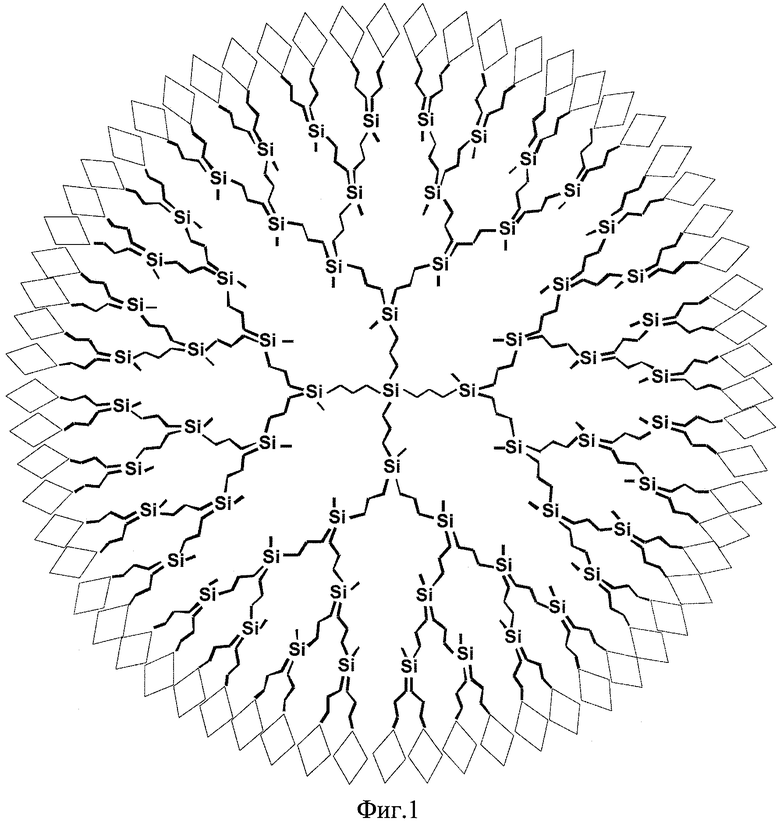
В качестве иллюстрации на Фиг.1 приведено схематическое изображение дендримера четвертой генерации с циклосилоксановым внешним слоем, где  соответствует
соответствует 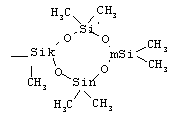 - атом кремния силоксанового цикла, связанный пропильной группой с карбосилановым дендримером. Кривые ГПХ карбосилан-силоксановых дендримеров по примерам 1, 4 и 7 (Фиг.2) указывают на мономодальное и узкодисперсное молекулярно-массовое распределение синтезированных соединений.
- атом кремния силоксанового цикла, связанный пропильной группой с карбосилановым дендримером. Кривые ГПХ карбосилан-силоксановых дендримеров по примерам 1, 4 и 7 (Фиг.2) указывают на мономодальное и узкодисперсное молекулярно-массовое распределение синтезированных соединений.
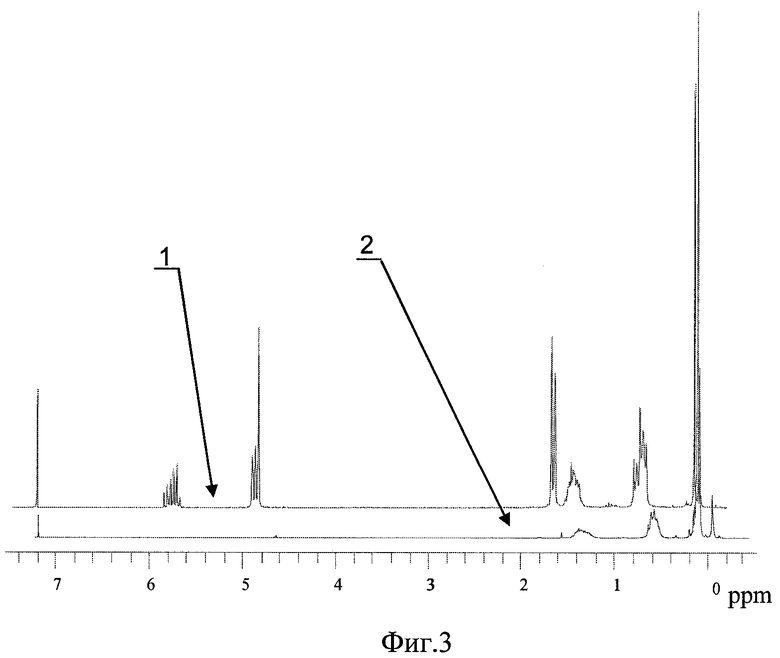
Полноту прохождения реакции контролировали по спектрам 1Н-ЯМР. На Фиг.3 приведены спектры 1H-ЯМР исходного карбосиланового дендримера с аллилфункциональным внешним слоем - G-3(All) - (кривая 1) и целевого карбосилан-силоксанового дендримера, образующегося после реакции гидридного присоединения 1,3,3,5,5,7,7-гептаметилциклотетрасилоксана - G-3(Cycle) - (кривая 2).
Из спектра видно полное исчезновение сигналов протонов аллильных групп внешнего слоя дендримера в области 4,8-5,0 и 5,6-5,9 м.д. Соотношение интегральных интенсивностей протонов различных групп соответствует расчетным величинам.
Исходные соединения синтезировали по известным методикам.
Способ синтеза карбосилановых дендримеров с аллил-функциональным внешним слоем описан в работе A.M.Музафаров, О.Б.Горбацевич, Е.А.Ребров, Г.М.Игнатьева, Т.Б.Ченская, В.Д.Мякушев, А.Ф.Булкин, B.C.Папков. «Кремнийорганические дендримеры: объемнорастущие полиаллилкарбосиланы». Высокомол. Соед. 1993. V.35. №11. p.1867-1872. Чистоту и строение дендримеров доказывали с помощью данных ГПХ (Фиг.2), 1Н ЯМР (Фиг.3) и 29Si ЯМР (Фиг.4) и элементного анализа.
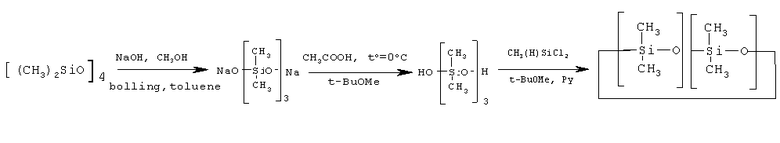
Синтез агента модификации внешнего слоя дендримеров - 1,3,3,5,5,7,7-гептаметилциклотетрасилоксана осуществляли с использованием следующей последовательности известных реакций:
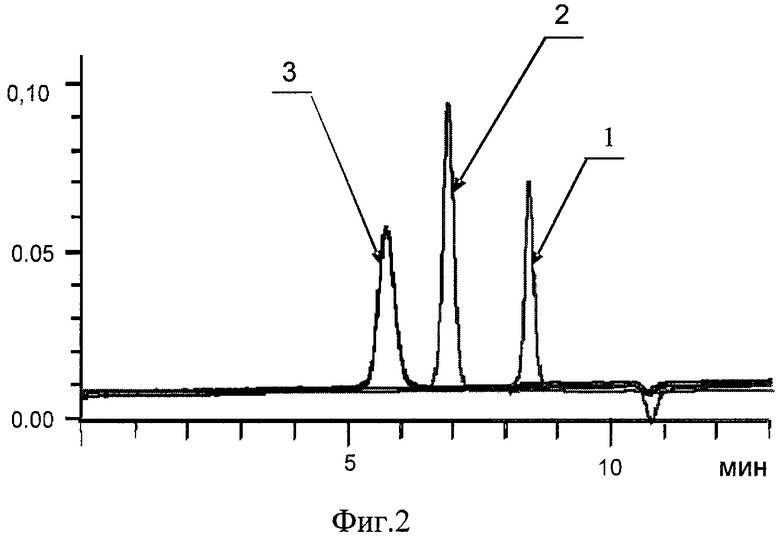
На Фиг.2 приведены кривые ГПХ карбосилан-силоксановых дендримеров:
1 - по примеру 1; 2 - по примеру 4; 3 - по примеру 7.
На Фиг.3 приведены спектры 1H ЯМР: 1 - исходного карбосиланового дендримера G-3(All) и 2-карбосилан-силоксанового дендримера G-3(Cycle), по примеру 4.
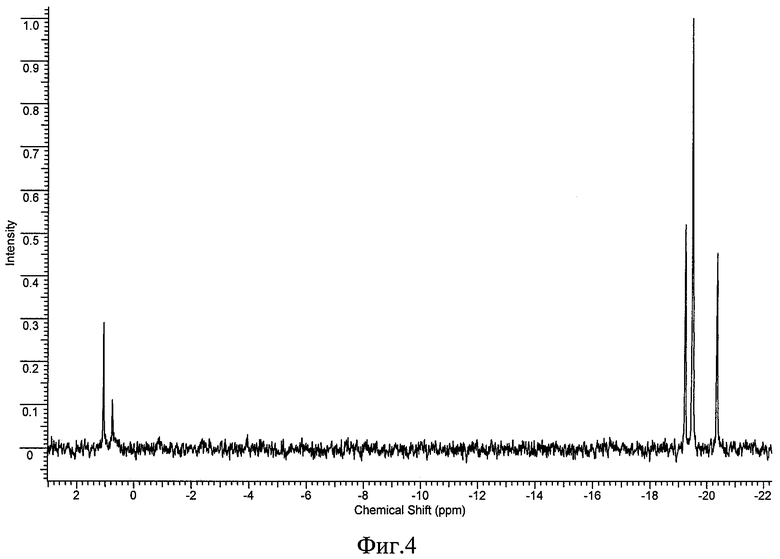
На Фиг.4 приведен спектр 29Si ЯМР карбосилан-силоксанового дендримера G-3 (Cycle) по примеру 4.
Изобретение иллюстрируется следующими примерами.
Пример 1
Синтез дендримера G-0(Cycle) [S1 4(Cycle)]
К раствору смеси 0,36 г (0,0019 г-м) тетрааллилсилана и 2,63 г (0,0093 г-м) 1,3,3,5,5,7,7-гептаметилциклотетрасилоксана в 5 мл сухого гексана добавили 12µ1 катализатора Карстедта. Реакцию проводили в течение 4 часов при температуре 25-40°C. После удаления летучих продуктов и очистки методом препаративной хроматографии (колонка Phenogel 75KD, растворитель ТГФ) выход продукта [Si1 4(Cycle)] составлял (72%).
1H ЯМР (CDCl3, 200 МГц), δ=1,36 (m, 8Н, -СН2-СН2-СН2-), δ=0,59 (m, 16H, Si-СН2-), δ=0,08-0,05 (c,c, 84H, Si-(CH3) в цикле).
29Si ЯМР (CDCl3, 500 МГц), δ=0,83 (c, 1 Si, Siцентр), δ=-19,16 (c, 4Si,=Sik(CH3)(C3H6) в цикле), δ=-19,40 (c, 8Si,=Si1,n(CH3)2 в цикле), δ=-20,29 (c, 4Si,=Sim(CH3)2 в цикле).
Элементный анализ, %: вычисл. Si - 36,06; C - 36,36; H - 8,18; найдено Si - 35,65, C - 37,01; H - 8,21.
Пример 2
Синтез дендримера G-1(Cycle).
К раствору смеси 2,30 г (0,0033 г-м) дендримера G-l(All) и 8,93 г (0,0317 г-м) 1,3,3,5,5,7,7-гептаметилциклотетрасилоксана в 5 мл сухого гексана добавили 26µ1 катализатора Карстедта. Реакцию проводили в течение 4 ч при температуре 25-40°C. После удаления летучих продуктов и очистки методом препаративной хроматографии выход продукта [Si5 8 (Cycle)] составлял 71%. 1H ЯМР (CDCl3, 200 МГц), δ=1,36 (m, 24Н, -СН2-СН2-СН2-), δ=0,58 (m, 48Н, Si-СН2-), δ=0,08-0,05 (c,c, 168H, Si-(CH3) в цикле), δ=-0,08 (c, 12Н, Siвнутр.(СР3).
29Si ЯМР (CDCl3,), δ=0,80 (c, ISi, Siцентр), δ=1,09 (c, 4Si, (CH3)Siвнешн., (C3H6)2), δ=-19,19 (c, 8Si,=Sik(CH3)(C3H6) в цикле), δ=-19,43 (c, 16Si,=Si1,n(CH3)2 в цикле), δ=-20,31 (c, 8Si,=Sim(CH3)2 в цикле).
Элементный анализ, %: вычисл. Si - 35,02; C - 38,94; H - 8,52; найдено Si - 35,80, C - 38,31; H - 8,44.
Пример 3
Синтез карбосилан-силоксанового дендримера G-2(Cycle).
К раствору смеси 3,07 г (0,0018 г-м) дендримера G-2(A11) и 9,75 г (0,0346 г-м) 1,3,3,5,5,7,7-гептаметилциклотетрасилоксана в 5 мл сухого гексана добавили 26µ1 катализатора Карстедта. Реакцию проводили в течение 4 ч при температуре 25-40°C. После удаления летучих продуктов и очистки методом препаративной хроматографии выход продукта [Si13 16(Cycle)] составлял 77%. 1H ЯМР (CDCl3, 200 МГц), δ=1,36 (m, 56H, -СН2-СН2-СН2-), δ=0,58 (m, 112H, Si-СН2-), δ=0,08-0,05 (c,c, 336H, Si-(CH3) в цикле), δ=-0,08 (c, 36Н, Siвнутр.(CH3).
29Si ЯМР (CDCl3, 500 МГц), δ=0,77 (c, 5Si, Siвнутр.), δ=1,07 (c, 8Si, (CH3)Siвнешн.(C3H6)2), δ=-19,22 (с, 16Si, =Sik(CH3)(C3H6) в цикле), δ=-19,46 (с, 32Si,=Si1,n(CH3)2 в цикле), δ=-20,33 (c, 16Si, =Sim(CH3)2 в цикле).
Элементный анализ, %: вычисл. Si - 34,61; C - 40,07; H - 8,67; найдено Si - 35,11, C - 39,37; H - 8,64.
Пример 4
Синтез карбосилан-силоксанового дендримера G-3(Cycle).
К раствору смеси 0,17 г (0,000046 г-м) дендримера G-3(All) и 0,5 г (0,00177 г-м) 1,3,3,5,5,7,7-гептаметилциклотетрасилоксана в 5 мл сухого гексана добавили 26µ1 катализатора Карстедта. Реакцию проводили в течение 4 ч при температуре 25-40°C. После удаления летучих продуктов и очистки методом препаративной хроматографии выход продукта [Si29 32 (Cycle)] составлял 70%. 1H ЯМР (CDCl3, 200 МГц), δ=1,35 (m, 120H, -СН2-СН2-СН2-), δ=0,56 (m, 240H, Si-CH2-), δ=0,08-0,05 (c,c, 672H, Si-(CH3) в цикле), δ=-0,08 (c, 84Н, Siвнутр.(CH3).
29Si ЯМР (CDCl3, 500 Гц), δ=0,73 (c, 13Si, Siвнутр.дендр.), δ=1,06 (с, 16Si, Siвнешн.дендр.), δ=-19,24 (с, 32Si,=Sik(CH3)(C3H6) в цикле), δ=-19,50 (с, 64S1,=Si1,n(CH3)2 в цикле), δ=-20,36 (c, 32Si,=Sim(CH3)2 в цикле).
Элементный анализ, %: вычисл. Si - 34,42; C - 40,59; H - 8,74; найдено Si - 35,02, C - 39,96; H - 8,72.
Пример 5
Синтез карбосилан-силоксанового дендримера G-4(Cycle).
К раствору смеси 3,42 г (0,00044 г-м) дендримера G-4(All) и 9,53 г (0,03386 г-м) 1,3,3,5,5,7,7-гептаметилциклотетрасилоксана в 5 мл сухого гексана добавили 26µ1 катализатора Карстедта. Реакцию проводили в течение 4 ч при температуре 25-40°C. После удаления летучих продуктов и очистки методом препаративной хроматографии выход продукта [Si61 64(Cycle)] составлял 74%. 1H ЯМР (CDCl3, 200 МГц), δ=1,35 (m, 248Н, -СН2-СН2-СН2-), δ=0,56 (m, 496H, Si-CH2-), δ=0,08-0,05 (c,c, 1344H, Si-(CH3) в цикле), δ=-0,08 (c, 180H, Siвнутр.(CH3).
29Si ЯМР (CDCl3, 500 МГц), δ=0,68 (c, 29Si, Siвнутр.дендр.), 5=1,04 (c, 32Si, Siвнешн.дендр..), δ=-19,28 (c, 64Si, =Sik(CH3)(C3H6) в цикле), δ=-19,55 (c, 128S1,=Si1,n(CH3)2 в цикле), δ=-20,43 (c, 64Si,=Sim(CH3)2 в цикле).
Элементный анализ, %: вычисл. Si - 34,33; C - 40,84; H - 8,77; найдено Si - 34,95, C - 40,32; H - 8,75.
Пример 6
Синтез карбосилан-силоксанового дендримера G-5(Cycle).
К раствору смеси 0,35 г (0,000022 г-м) дендримера G-5(A11) и 0,95 г (0,0034 г-м) 1,3,3,5,5,7,7-гептаметилциклотетрасилоксана в 5 мл сухого гексана добавили 26µ1 катализатора Карстедта. Реакцию проводили в течение 4 ч при температуре 25-40°C. После удаления летучих продуктов и очистки методом препаративной хроматографии выход продукта [Si125 128 (Сус1е)]составлял 71%. 1H ЯМР (CDCl3, 200 МГц), 5=1,35 (m, 504Н, -СН2-СН2-СН2-), δ=0,56 (m, 1008H, Si-CH2-), δ=0,08-0,05 (c,c, 2688H, Si-(CH3) в цикле), δ=-0,08 (c, 372H, 81внутр.(CH3).
29Si ЯМР (CDCl3, 500 МГц), δ=0,63 (c, 61 Si, Siвнутр.дендр.), δ=1,03 (c, 64Si, 81внешн.дендр.), δ=-19,34 (c, 128Si, =Sik(CH3)(C3H6) в цикле), δ=-19,61 (c, 256S1,=Si1,n(CH3)2 в цикле), δ=-20,43 (c, 128Si,=Sim(CH3)2 в цикле).
Элементный анализ, %: вычисл. Si - 34,29; C - 40,97; H - 8,79; найдено Si - 34,90; C - 40,65; H - 8,75.
Пример 7
Синтез карбосилан-силоксанового дендримера. G-6(Cycle).
К раствору смеси 0,42 г (0,000013 г-м) дендримера G-6(All) и 1,14 г (0,004 г-м) 1,3,3,5,5,7,7-гептаметилциклотетрасилоксана в 5 мл сухого гексана добавили 26µ1 катализатора Карстедта. Реакцию проводили в течение 7 ч при температуре 25-40°C. После удаления летучих продуктов и очистки методом препаративной хроматографии выход продукта [Si253 256 (Cycle)] составлял 69%. 1H ЯМР (CDCl3, 200 МГц), δ=1,35 (m, 1016H, -СН2-СН2-СН2-), δ=0,55 (m, 2032H, Si-CH2-), δ=0,07-0,04 (c,c, 5376Н, Si-(CH3) в цикле), δ=-0,08 (c, 756Н, Siвнутр.(CH3).
29Si ЯМР (CDCl3, 500 МГц), δ5=0,59 (c, 125Si, Siвнутр.дендр.), 5=1,02 (c, 128Si, 81внешн.дендр.), δ=-19,39 (c, 256Si,=Sik(CH3)(C3H6) в цикле), δ=-19,65 (c, 512Si, =Si1,n(CH3)2 в цикле), δ=-20,52 (c, 256Si, =Sim(CH3)2 в цикле).
Элементный анализ, %: вычисл. Si - 34,26; C - 41,03; H - 8,80; найдено Si - 34,93; C - 40,55; H - 8,77.
| название | год | авторы | номер документа |
|---|---|---|---|
| Карбосилан-силоксановые дендримеры первой генерации | 2018 |
|
RU2679633C1 |
| НОВЫЕ КАРБОСИЛАНОВЫЕ ДЕНДРИМЕРЫ, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2006 |
|
RU2422474C2 |
| МНОГОЛУЧЕВЫЕ ЗВЕЗДООБРАЗНЫЕ ПОЛИДИМЕТИЛСИЛОКСАНЫ | 2009 |
|
RU2415880C2 |
| СПОСОБ ПОЛУЧЕНИЯ НОВЫХ ПОЛИЛИТИЕВЫХ ПРОИЗВОДНЫХ КАРБОСИЛАНОВЫХ СОЕДИНЕНИЙ ДЕНДРИТНОЙ СТРУКТУРЫ | 1996 |
|
RU2147023C1 |
| ГРЕБНЕОБРАЗНЫЕ ПОЛИМЕТИЛСИЛОКСАНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2010 |
|
RU2440382C1 |
| ПОЛИАРИЛСИЛАНОВЫЕ МОНОДЕНДРОНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2007 |
|
RU2348657C1 |
| ФУНКЦИОНАЛЬНЫЕ КАРБОКСИЛАНЫ, СОДЕРЖАЩИЕ ТРИС(ГАММА-ТРИФТОРПРОПИЛ)СИЛИЛЬНУЮ ГРУППУ | 1999 |
|
RU2164516C1 |
| ПОЛИАРИЛСИЛАНОВЫЕ ДЕНДРИМЕРЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2007 |
|
RU2353629C1 |
| Pt-СОДЕРЖАЩАЯ РЕГЕНЕРИРУЕМАЯ КАТАЛИТИЧЕСКАЯ СИСТЕМА И СПОСОБ ГИДРОСИЛИЛИРОВАНИЯ НЕПРЕДЕЛЬНЫХ СОЕДИНЕНИЙ С ЕЁ ИСПОЛЬЗОВАНИЕМ | 2023 |
|
RU2806031C1 |
| Донорно-акцепторные сопряженные молекулы и способ их получения | 2014 |
|
RU2624820C2 |
Изобретение относится к химии кремнийорганических соединений разветвленного строения. Предложены новые карбосилан-силоксановые дендримеры от нулевой G-0(Cycle) до шестой генерации G-6(Cycle), содержащие во внешнем слое соответствующее количество восьмичленных диметилсилоксановых циклов, соединенных с атомом кремния внешнего слоя дендримера пропильной группой общей формулы:
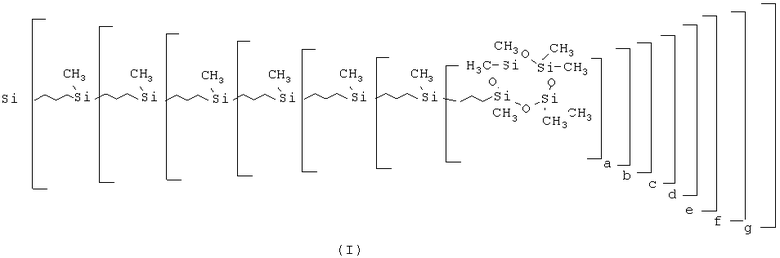
где а, b, с, d, e, f и g означает число групп, связанных с центром ветвления, и для дендримера нулевой генерации а равно 4, b, с, d, e, f и g равно 0; для дендримера первой генерации а равно 2, b равно 4, с, d, е, f и g равно 0; для дендримера второй генерации а и в равно 2, с, d, e, f равно 0, g равно 4; для дендримера третьей генерации а, b и с равно 2, d, e, f равно 0, g равно 4; для дендримера четвертой генерации а, b, с и d равно 2, е, f равно 0, g равно 4; для дендримера пятой генерации а, b, с, d и е равно 2, f равно 0, g равно 4; для дендримера шестой генерации а, b, с, d, е и f равно 2, g равно 4. Технический результат заключается в получении новых химических соединений. 7 з.п. ф-лы, 4 ил.
1. Карбосилан-силоксановые дендримеры от нулевой до шестой генерации с модифицированной восьмичленными диметилсилоксановыми циклами поверхностью общей формулы (I):

где а, b, с, d, е, f и g означает число групп, связанных с центром ветвления и равно: а равно 2 или 4; b равно 0; 2 или 4; с, d, е и f равно 0 или 2; g равно 0 или 4.
2. Карбосилан-силоксановый дендример по п.1, отличающийся тем, что для дендримера нулевой генерации а равно 4, b, с, d, е, f и g равно 0.
3. Карбосилан-силоксановый дендример по п.1, отличающийся тем, что для дендримера первой генерации а равно 2, b равно 4, с, d, е, f и g равно 0.
4. Карбосилан-силоксановый дендример по п.1, отличающийся тем, что для дендримера второй генерации а и b равно 2, с, d, е, f равно 0, g равно 4.
5. Карбосилан-силоксановый дендример по п.1, отличающийся тем, что для дендримера третьей генерации а, b и с равно 2, d, е, f равно 0, g равно 4.
6. Карбосилан-силоксановый дендример по п.1, отличающийся тем, что для дендримера четвертой генерации а, b, с и d равно 2, е, f равно 0, g равно 4.
7. Карбосилан-силоксановый дендример по п.1, отличающийся тем, что для дендримера пятой генерации а, b, с, d и е равно 2, f равно 0, g равно 4.
8. Карбосилан-силоксановый дендример по п.1, отличающийся тем, что для дендримера шестой генерации а, b, с, d, е и f равно 2, g равно 4.
| Vasilenko N.G | |||
| et al | |||
| "Preparation of multi-arm star polymers with polylithiated carbosilane dendrimers" | |||
| Macromol | |||
| Chem | |||
| Phys., 1998, v.199, pp.889-895 | |||
| СПОСОБ ПОЛУЧЕНИЯ НОВЫХ ПОЛИЛИТИЕВЫХ ПРОИЗВОДНЫХ КАРБОСИЛАНОВЫХ СОЕДИНЕНИЙ ДЕНДРИТНОЙ СТРУКТУРЫ | 1996 |
|
RU2147023C1 |
| Jean-Pierre Majoral, Anne-Marie Caminade "Dendrimers Containing Heteroatoms (Si, P, B, Ge, or Bi)" | |||
| Chem.Rev., 1999, v.99, N3, pp.845-880 | |||
| US 5276110 A, 04.01.1994 | |||
| СПОСОБ ПОЛУЧЕНИЯ SIOH-ФУНКЦИОНАЛЬНЫХ ДЕНДРИМЕРНЫХ КАРБОСИЛАНОВ | 1998 |
|
RU2193576C2 |
| СПОСОБ ЗАЩИТЫ ПОДШИПНИКОВОГО УЗЛА ОТ МИКРОДИСПЕРСНЫХ ЧАСТИЦ ИЗНОСА | 2004 |
|
RU2279000C1 |
Авторы
Даты
2011-06-27—Публикация
2009-12-08—Подача