Изобретение относится к области получения соединений хрома, в частности окиси хрома, которая может быть использована для производства металлического хрома.
Известен способ получения окиси хрома путем восстановления бихромата натрия сульфатом аммония, заключающийся в том, что смесь бихромата натрия и сульфата аммония подвергают термическому разложению в течение 6 часов при температуре 700-800°С с дальнейшим вымыванием сульфатов до получения готового продукта - окиси хрома, причем в качестве соли аммония используют сульфат аммония (патент Германии №728233, Способ получения пигментной окиси хрома, НПК 22 f7, приоритет от 03.04.1940 г., опубликован 23.11.1942 г.).
Недостатком данного способа является то, что можно получить только пигментную окись хрома, так как повышение температуры термического разложения свыше заявленной (700-800°С) ведет к плавлению сульфата натрия и образованию намотов в барабанных печах, что в свою очередь приводит к нарушению технологического процесса и трудоемким операциям по сбиванию намотов. Готовый продукт также имеет высокое содержание примесей серы, что делает его непригодным для получения металлического хрома.
Наиболее близким по технической сущности и достигаемому эффекту предлагаемому является способ получения окиси хрома путем разложения бихромата натрия и сульфата аммония, которое ведут в растворе с концентрацией 400-450 г/л по CrO3 при температуре 100-105°С в течение 45-60 минут при постоянном перемешивании с получением бихромата аммония и сульфата натрия (Патент РФ на изобретение 2258039, Способ получения окиси хрома, МПК C01G 37/02, от 10.08.2005). Сульфат натрия отделяют от раствора. Раствор, содержащий бихромат аммония, охлаждают до температуры его кристаллизации, после чего осуществляют термическое разложение кристаллов бихромата аммония при температуре 440-1400°С до образования окиси хрома. В способе используют кристаллический сульфат аммония с содержанием азота не менее 21%. Концентрация в растворе по CrO3 равна 400-450 г/л.
Недостатками наиболее близкого аналога является сложная и громоздкая технологическая схема производства за счет большого количества технологических операций, использования аппарата большого объема на стадии отделения сульфата натрия от раствора бихромата аммония, наличия стадии охлаждения раствора бихромата аммония. При использовании кристаллического сульфата аммония образующийся по реакции сульфат натрия выпадает в осадок и обволакивает кристаллы сульфата аммония, значительно снижая скорость его растворения и соответственно снижая скорость протекания реакции.
Несмотря на все предварительные операции, готовый продукт все равно необходимо подвергать отмывке от примесей с последующей сушкой. Кроме того разложение чистого бихромата аммония происходит самопроизвольно с выделением большого количества тепла (экзотермическая реакция), что делает стадию его термического разложения без примесей взрывоопасным. Применение ретура в виде окиси хрома (для исключения вероятности взрыва) приводит к значительному увеличению нагрузки на прокалочную печь, в которой происходит термическое разложение бихромата аммония, и соответственно к дополнительному расходу энергоресурсов на повторный нагрев ретура. Еще одним недостатком данного является получение сульфата натрия, который загрязнен кроме соединений шестивалентного хрома и соединениями аммиака, что создает дополнительные сложности при его использовании в производстве белого сульфата натрия. Кроме того, получаемая окись хрома достаточно мелкодисперсная (d50 менее 10 мкм), что при получении хрома металлического алюмотермическим способом дает дополнительные потери хрома из-за пылеуноса. Согласно данному способу готовый продукт содержит: серы S - 0,005%, углерода С - 0,005%, кремния SiO2 - 0,07%, железа FeO - 0,1%.
Таким образом, основными недостатками наиболее близкого аналога являются повышенная трудоемкость способа и низкое качество получаемой окиси хрома.
Технической проблемой является разработка эффективного упрощенного способа получения окиси хрома повышенного качества.
Техническим результатом предполагаемого изобретения является снижение трудоемкости способа, повышение качества окиси хрома, снижение расхода энергоресурсов.
Поставленный технический результат достигается тем, что в способе получения окиси хрома, включающий нагрев и постоянное перемешивание раствора бихромата натрия и сульфата аммония с образованием бихромата аммония и сульфата натрия, разложение бихромата аммония, отмывание продуктов разложения бихромата аммония от растворимых в воде веществ и окончательную термообработку до образования окиси хрома, согласно предлагаемому решению, предварительно перед смешиванием компонентов сульфат аммония растворяют в воде до получения концентрации 35-50,4% (NH4)2SO4, обменную реакцию ведут в течение 15-40 минут при температуре 90-100°С, затем полученную реакционную массу в виде водной суспензии смеси бихромата аммония и сульфата натрия нагревают до 235-400°С до разложения бихромата аммония.
То, что в способе получения хрома предварительно перед смешиванием компонентов сульфат аммония растворяют в воде до концентрации 35-50,4% (NH4)2SO4, выдерживают после смешивания компонентов при заявляемых режимах и дополнительно нагревают до 235-400°С до разложения бихромата аммония позволяет получить продукты разложения бихромата аммония в виде хорошо фильтруемого осадка, который легко отмывается от сульфата натрия.
Обменная реакция между бихроматом натрия Na2Cr2O7 и сульфатом аммония (NH4)2SO4 в растворе протекает по следующему уравнению (1):

Использование сульфата аммония в виде водного раствора заявляемой концентрации позволяет сократить время необходимое для протекания реакции по уравнению (1), гарантирует, что весь бихромат натрия переводится в бихромат аммония, и, тем самым, позволяет избежать дополнительного расхода воды на разбавление смеси для растворения сульфата аммония в сравнении с растворением кристаллического сульфата аммония в растворе бихромата натрия.
Термообработка полученной реакционной массы после смешения сульфата аммония и бихромата натрия при 235-400°С позволяет получить продукты разложения бихромата аммония по уравнению реакции (2):
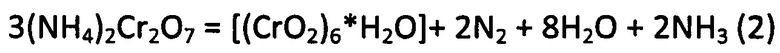
в виде хорошо фильтруемого осадка, который легко отмывается от сульфата натрия.
Стадии получения продуктов разложения бихромата аммония при 235-400°С и их отмывка от сульфата натрия в заявляемом способе позволяют заменить следующие стадии исключить свойственные наиболее близкому аналогу:
1. осаждение кристаллов сульфата натрия;
2. контрольная фильтрация раствора бихромата аммония;
3. обезвоживание кристаллов сульфата натрия;
4. охлаждение раствора бихромата аммония;
5. отделение кристаллов бихромата аммония;
6. упаривание маточного раствора;
7. отмывка полученной окиси хрома от водорастворимых солей;
8. сушка отмытого осадка окиси хрома.
Это позволяет снизить трудоемкость способа получения окиси хрома. Практически полное отсутствие после отмывки сульфата натрия в продуктах разложения бихромата аммония, полученных по заявляемому способу, также позволяет полностью исключить вероятность образования намотов в барабанной прокалочной печи, обусловленного плавлением сульфата натрия, который присутствует в бихромате аммония, полученного по наиболее близкому способу. Кроме того, при термическом разложении бихромата аммония при практическом отсутствии сульфата натрия при температурах выше 800°С снижается количество в окиси хрома нерастворимых в воде соединений серы, что повышает качество готового продукта.
Согласно заявляемому способу при термообработке отмытых продуктов разложения бихромата аммония при температуре 800-1400°С образуется окись хрома согласно уравнению реакции (3):
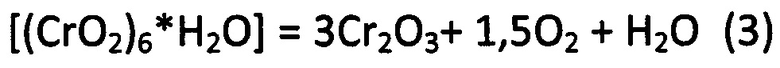
После термообработки отмытых продуктов разложения бихромата аммония при температуре 800-1400°С получается готовый продукт имеющий показатель d50 более 15 мкм.
При концентрации раствора ниже 35% (NH4)2SO4 в получаемой суспензии содержится большое количество воды, что увеличит расход теплоносителя для ее испарения. При концентрации раствора выше 50,4% (NH4)2SO4 будут присутствовать кристаллы сульфата аммония в растворе, что приведет к неполному переводу бихромата натрия в бихромат аммония.
При нагреве полученной смеси раствора сульфата аммония с бихроматом натрия температуре ниже 90°С снижается растворимость сульфата аммония и появляется вероятность неполного протекания реакции (1). При температуре выше 100°С возможно разложение сульфата аммония и происходит необоснованный расход теплоносителя для нагрева реакционной массы.
При времени выдержки реакционной массы менее 15 минут появляется вероятность неполного протекания реакции (1). При времени выдержки реакционной массы более 40 минут происходит необоснованный расход теплоносителя для нагрева реакционной массы.
При нагреве реакционной массы в виде водной суспензии смеси бихромата аммония и сульфата натрия ниже 235°С не происходит разложение бихромата аммония. При температуре выше 400°С продукт получается мелкодисперсный в трудно фильтруемой форме, что отрицательно влияет на качество последующей его отмывки.
Для получения окиси хрома используют следующее сырье:
1. Раствор бихромата натрия Na2Cr2O7 с концентрацией CrO3 не менее 1000 г/л или кристаллический бихромат натрия с концентрацией CrO3 не менее 75,5%;
2. Сульфат аммония кристаллический (NH4)2SO4 с содержанием азота не менее 21%.
3. Вода с содержанием растворимых веществ не более 0,4 г/л.
Способ получения окиси хрома осуществляется следующим образом.
Предварительно готовят раствор сульфата аммония путем растворения соответствующей навески кристаллического сульфата аммония в воде при температуре выше 90°С для получения концентрации 35-50,4% (NH4)2SO4, которая обеспечит полное протекание реакции (1). Далее в готовый раствор сульфата аммония задают бихромат натрия. По заявляемому способу допустимо использовать бихромат натрия в виде раствора с концентрацией выше 1000 г/л CrO3 или кристаллического бихромата натрия. При использовании бихромата натрия в виде раствора с концентрацией ниже 1000 г/л CrO3 в получаемой суспензии содержится большое количество воды, что увеличит расход теплоносителя для ее испарения. В результате смешения раствора сульфата аммония и бихромата натрия по заявляемому способу получается смесь, содержащая 500-550 г/л CrO3.
После задачи бихромата натрия в раствор сульфата аммония реакционная масса выдерживается при постоянном перемешивании и температуре 90-100°С в течение 15-40 минут.
После протекания реакции (1) реакционную массу в виде водной суспензии подвергают термообработке при температуре 235-400°С до разложения бихромата аммония по уравнению реакции (2). В результате получается продукт в хорошо фильтруемой форме, который легко отмывается от сульфата натрия.
После протекания реакции (2) продукты разложения бихромата аммония отмывают от водорастворимых солей до содержания сульфата натрия не более 0,05%. При более высоком содержании сульфата натрия возможно получение окиси хрома с неприемлемым для производства металлического хрома содержанием серы.
Отмытые от сульфата натрия продукты разложения бихромата аммония подвергают термообработке. Для получения окиси хрома термообработку ведут при температуре 800-1400°С. В результате образуется готовая окись хрома, пригодная для получения металлического хрома. При температуре ниже заявленного диапазона окись хрома получается с содержанием Cr2O3 ниже 99%. Повышение температуры выше заявленного диапазона экономически нецелесообразно из-за сложности аппаратурного оформления и не дает улучшения качества окиси хрома.
Предлагаемый способ получения окиси хрома опробован в Акционерном обществе «Новотроицкий завод хромовых соединений».
На весах отвешивали 500 кг кристаллического сульфата аммония, содержащего 21,14% азота, и растворяли при 90°С в 0,75 м3 воды. Получали раствор сульфата аммония с концентрацией 40% (NH4)2SO4. Согласно уравнению реакции (1) на такое количество сульфата аммония задали 1000 кг кристаллического бихромата натрия, содержащего 75,5% CrO3. На весах отвесили 1000 кг кристаллического бихромата натрия и задали в раствор сульфата аммония. Выдерживали смесь при постоянном перемешивании и температуре 100°С в течение 15 минут.
Полученную реакционную массу в виде водной суспензии задали в барабанную сушилку, где произошло испарение воды. Нагревали массу до 250°С, в результате чего произошло разложение бихромата аммония по реакции (2).
Для удаления сульфата натрия продукты разложения бихромата аммония подвергали двум последовательным репульпациям в воде при содержании твердого в пульпе 200 г/л с фильтрацией на фильтре-прессе после каждой репульпации. В результате отмытые продукты разложения бихромата аммония содержали 0,05% Na2SO4. Все образующиеся фильтраты передали в цех производства сульфат натрия.
Отмытые продукты разложения бихромата аммония в виде осадка с фильтра-пресса задали в барабанную прокалочную печь, где поддерживали температуру 1250°С. На выходе из прокалочной печи получили окись хрома, содержащую Cr2O3 - 99,3%, S - 0,004%, С - 0,004%, SiO2 - 0,03%, FeO - 0,03%, d50 - 16,2 мкм.
Предлагаемый способ найдет применение в химической промышленности для производства окиси хрома преимущественно для получения металлического хрома.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ОКИСИ ХРОМА | 2004 |
|
RU2258039C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХРОМОВОГО АНГИДРИДА | 2007 |
|
RU2349551C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСОХРОМАТОВ МЕДИ(+2) | 2012 |
|
RU2504517C1 |
| Способ получения пигментной окиси хрома | 1981 |
|
SU966014A1 |
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНЫХ ОКСИДНЫХ МАТЕРИАЛОВ НА ОСНОВЕ ХРОМА | 1995 |
|
RU2081837C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДА ХРОМА (III) | 2011 |
|
RU2591245C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРАТА ОКСИДА МЕТАЛЛА | 2008 |
|
RU2375306C1 |
| ГРАНУЛИРОВАННОЕ УДОБРЕНИЕ, СОДЕРЖАЩЕЕ ВОДОРАСТВОРИМЫЕ ФОРМЫ АЗОТА, МАГНИЯ И СЕРЫ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2007 |
|
RU2455270C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДА ХРОМА (III) | 2011 |
|
RU2568112C9 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕКСАГИДРАТА СУЛЬФАТА МЕДИ-АММОНИЯ | 2003 |
|
RU2251527C2 |
Изобретение относится к химической промышленности и может быть использовано для производства металлического хрома. Растворяют сульфат аммония в воде до получения концентрации 35-50,4% (NH4)2SO4. Растворяют бихромат натрия в растворе сульфата аммония при температуре 90-100°С в течение 15-40 минут при постоянном перемешивании с получением бихромата аммония и сульфата натрия. Полученную реакционную массу в виде водной суспензии подвергают термообработке при температуре 235-400°С до разложения бихромата аммония. Продукты разложения бихромата аммония отмывают от растворимых в воде веществ и подвергают повторной термообработке при температуре 800-1400°С до образования окиси хрома. Обеспечивается упрощение процесса, повышение чистоты окиси хрома Сr2O3 до 99,3% за счет уменьшения содержания примесей и увеличения крупности частиц.
Способ получения окиси хрома, включающий нагрев и постоянное перемешивание раствора бихромата натрия и сульфата аммония с образованием бихромата аммония и сульфата натрия, разложение бихромата аммония, отмывание продуктов разложения бихромата аммония от растворимых в воде веществ и окончательную термообработку до образования окиси хрома, отличающийся тем, что предварительно перед смешиванием компонентов сульфат аммония растворяют в воде до получения концентрации 35-50,4% (NH4)2SO4, обменную реакцию ведут в течение 15-40 мин при температуре 90-100°С, затем полученную реакционную массу в виде водной суспензии смеси бихромата аммония и сульфата натрия нагревают до 235-400°С до разложения бихромата аммония.
| СПОСОБ ПОЛУЧЕНИЯ ОКИСИ ХРОМА | 2004 |
|
RU2258039C1 |
| RU 2012131057 A, 27.01.2014 | |||
| US 4235862 A, 25.11.1980 | |||
| US 4067747 A, 10.01.1978 | |||
| US 4296076 A, 20.10.1981. | |||
Авторы
Даты
2019-05-13—Публикация
2018-04-26—Подача