Изобретение относится к химической технологии неорганических веществ, в частности к технологии получения хромового ангидрида - вещества, широко используемого во многих отраслях промышленности: химической, лакокрасочной, текстильной, металлургической и др. Так, например, значительные количества хромового ангидрида (оксида хрома VI) потребляет лакокрасочная промышленность для изготовления хромовых пигментов (например, «зеленая окись хрома», «изумрудно-зеленый гидрат окиси хрома» и др.) и лаков и красок на их основе, обладающих большой устойчивостью к действию высоких температур и коррозии.
Кроме того, водный раствор хромового ангидрида используется для получения высокочистого металлического хрома - основы для выплавки жаро- и коррозионно-стойких легированных сплавов.
Единственным сырьем для получения соединений хрома, в том числе хромового ангидрида, является хромитовая руда (хромит, хромпикотит) или обогащенная руда - хромитовый концентрат, который представляет собой твердый раствор ряда минералов (FeO Al2O3, MgO Fe2O3, MgO Al2O3 и других минералов) в хромите FeO Cr2О3, где хром находится в виде оксида трехвалентного хрома (Cr2О3) - при обычных условиях практически химически инертного к щелочам, кислотам и воде соединения. Поэтому для извлечения хрома из хромита его необходимо перевести из трехвалентного состояния в шестивалентное хорошо растворимое в воде соединение - CrO3. Это может быть достигнуто только в результате окисления оксида двухвалентного железа FeO (входящего в кристаллическую решетку хромита) в оксид трехвалентного железа - Fe2О3. При этом разрушается кристаллическая решетка солей, входящих в состав хромитового концентрата, и оксиды (Fe2О3, Al2О3, MgO, Cr2O3) вступают в химическое взаимодействие с различными реагентами: с кальцинированной содой или с серной кислотой.
Известен способ получения хромового ангидрида из хромита, который включает в себя:
- обогащение бедных хромитовых руд с получением концентратов;
- высокотемпературное окислительное прокаливание шихты, состоящей из хромита, кальцинированной соды и доломита, при температуре 1150-1200°С; выщелачивание спека, фильтрацию шламовой суспензии с получением монохромата натрия - Na2CrO4;
- очистку раствора монохромата натрия от алюминия с помощью серной кислоты при температуре 80°С и перевод монохромата натрия в бихромат натрия - Na2Cr2O7; выпуск товарного бихромата натрия в виде чешуйчатого или гранулированного продукта;
- разложение бихромата натрия серной кислотой при температуре 200°С
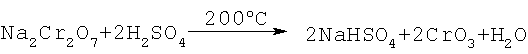
Образующиеся расплавленные жидкие хромовый ангидрид и бисульфат натрия мало растворимы друг в друге и легко разделяются декантацией благодаря разнице удельных весов. Расплав хромового ангидрида охлаждают, гранулируют и затаривают (Авербух, П.Г.Павлов. Технология соединений хрома. Л., 1967, стр.46, 156).
Процесс получения хромового ангидрида по такой схеме имеет следующие недостатки:
- соединения хроматов и бихроматов (натрия, калия и др.), а также их растворы очень токсичны;
- процесс очень сложный и многостадийный, требует использования высоких температур при спекании хромитового концентрата с кальцинированной содой и доломитом; сопровождается большим количеством побочных процессов;
- процесс требует сложную многоступенчатую очистку отходящих топочных газов и сточных вод.
В качестве прототипа взят наиболее близкий по технической сущности и достигаемому результату способ получения хромового ангидрида выщелачиванием хромитового концентрата (содержащего 53,7% Cr2O3 и 13,54% FeO с размером частиц - 2,0+0,0 мм) при температуре 140-150°С смесью 60-62%-ной серной кислоты и катализатора - хромового ангидрида CrO3 (или хромовой кислоты - Н2Cr2O7), взятых в количестве 3,4 т Н2SO4 (или 3,78 м2 60%-ой H2SO4) и 0,01172 т CrO3 на 1,0 т хромитового концентрата с последующим анодным окислением фильтрата - раствора, содержащего сульфаты хрома, примесных металлов и серную кислоту (ЖПХ, 13, №2, 170 (1940); I. Soc. Chem Ind (London), 69, 275, 1950).
В результате анодного окисления сульфат хрома переходит в хромовую и серную кислоты.
Раствор упаривают при температуре 140-150°С до концентрации серной кислоты в растворе - 940-1100 г/л. При этом хромовая кислота дегидратирует и переходит в хромовый ангидрид. Суспензию фильтруют (центрифугируют) и отделяют кристаллы хромового ангидрида от раствора серной кислоты и сульфатов Fe3+, Al3+, Mg2+ др. Осадок - кристаллы CrO3 и часть неразложившегося хромита сушат при температуре 105-150°С и затаривают, а маточный раствор возвращают на выщелачивание хромитового концентрата.
Было получено 482,5 кг хромового ангидрида, выход CrO3 - 68,3% от возможного - 706,6 кг.
Недостатком указанного способа является:
- малый выход основного вещества - хромового ангидрида (68,3%), что, очевидно, связано с низкой концентрацией в реакционной смеси катализатора - хромовой кислоты - 1,17% (или 8,64% от содержания FeO в хромитовом концентрате, что не способствует полному окислению оксида двухвалентного железа в трехвалентное. В результате этого не происходит полного разложения хромита, и часть Cr2О3 - в составе концентрата (31,7%) остается в нерастворимом остатке (см. стр.2 описания, прототип).
- высокое содержание примесей в готовом продукте в виде сульфатов Al3+, Fe3+, Mg2+ и др.
Технической задачей изобретения является разработка экономически эффективного способа получения хромового ангидрида из хромитового концентрата, обеспечивающего максимальный выход целевого продукта с минимальным содержанием примесей.
Техническим результатом от использования изобретения является обеспечение более полного разложения хромитового концентрата, повышение выхода хромового ангидрида с минимальным содержанием примесей, а также расширение объема использования бедных рудных смесей при одновременном комплексном извлечении ценных компонентов сырья.
Технический результат достигается за счет того, что в способе получения хромового ангидрида из хромитового концентрата, включающем выщелачивание при температуре 140-160°С смесью 60-62%-ной серной кислоты и катализатора - хромового ангидрида, центрифугирование суспензии, окисление методом электролиза сульфата хрома, полученного в результате выщелачивания, в хромовую кислоту, упаривание раствора электролита при температуре 140-150°С до концентрации серной кислоты в упаренном растворе 950-1100 г/л, отделение кристаллов хромового ангидрида от маточного раствора центрифугированием и сушку готового продукта, предварительно перед сернокислотным выщелачиванием хромитовый концентрат обогащают методом гравитации, количество катализатора при выщелачивании составляет 70-100% от содержания оксида двухвалентного железа (FeO) в хромитовом концентрате, а после отделения от маточного раствора кристаллы хромового ангидрида дополнительно отмывают в серной кислоте концентрации 60-62% при температуре 140-150°С.
Хромитовый концентрат подвергают дополнительному обогащению методом гравитации. Обогащенный хромитовый концентрат направляется на выщелачивание серной кислотой концентрации 60-62% при температуре 140-160°С в присутствии хромового ангидрида в качестве катализатора. Содержание хромового ангидрида в реакционной смеси принимается равным 70-100% от содержания FeO в хромитовом концентрате, при этом т:ж=1:(3,75-4,0).
Процесс выщелачивания минерала хромита, очевидно, протекает по схеме:
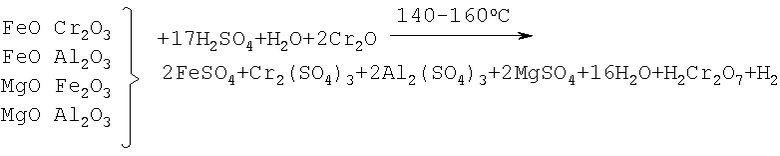
После выщелачивания раствор, содержащий сульфаты Cr3+, Mg2+, Al3+, Fe3+, Ni2+, хромовый ангидрид (в виде хромовой кислоты Н2Cr2О7) и избыток серной кислоты центрифугируют, отделяя от части неразложившегося хромита, и подвергают электролизу при 30-50°С в ванне с диафрагмой и свинцовым анодом с целью окисления трехвалентного сульфата хрома и перевода его в шестивалентный хромовый ангидрид (или хромовую кислоту).
Переход трехвалентного сульфата хрома в шестивалентный хромовый ангидрид (в результате электрохимической реакции) протекает по схеме:
процесс у анода:

процесс у катода:
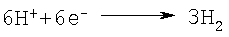 .
.
суммарная реакция:

Неразложившийся хромит возвращают на выщелачивание. После электролиза раствор сульфата концентрируют упариванием при температуре 140-150°С, при этом хромовая кислота дегидратирует, превращается в хромовый ангидрид и выпадает в осадок
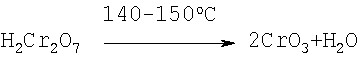
Степень упаривания контролируют по концентрации серной кислоты в суспензии, которая должна быть не ниже 950-1100 г/л H2SO4, поскольку при такой концентрации H2SO4 растворимость кристаллов CrO3 в растворе минимальна (0,49-1,01 мас.%) и они выпадают в осадок.
Суспензию центрифугируют, маточный раствор, содержащий серную кислоту (950-1100 г/л H2SO4) и сульфаты Al3+, Mg2+, Fe3+, Ni2+ и др., возвращают на выщелачивание хромитового концентрата, а осадок - кристаллы CrO3 - направляют в реактор с серной кислотой (1100 г/л H2SO4), где при температуре 140-150°С отмывают от примесей Al3+, Mg2+, Fe3+, Ni2+ и др. Отмытые таким образом кристаллы хромового ангидрида центрифугируют, маточный раствор (серная кислота) возвращается на выщелачивание хромитового концентрата, а кристаллы CrO3 сушат при 150°С и затаривают.
В табл.1 приведен минеральный состав хромитового концентрата до и после гравитационного обогащения.
В табл.2 приведен химический состав хромитового концентрата до и после гравитационного обогащения
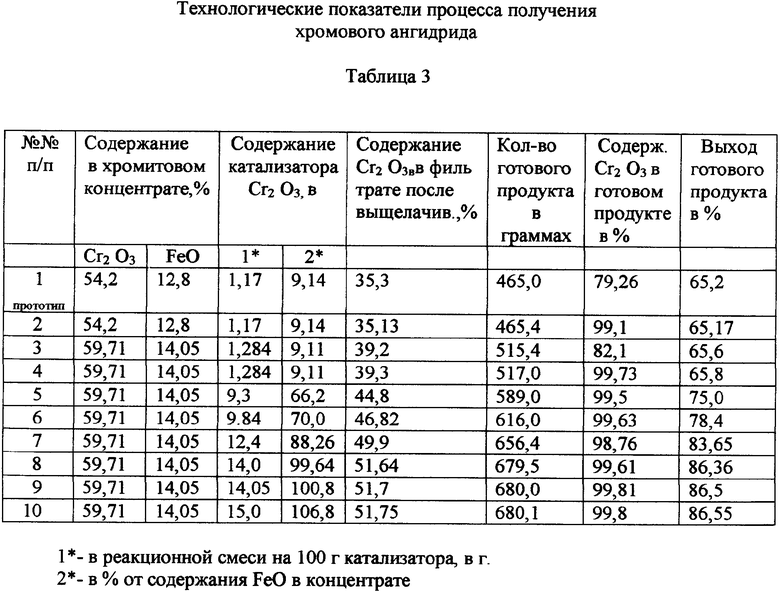
В табл.3 приведены технологические показатели процесса получения хромового ангидрида
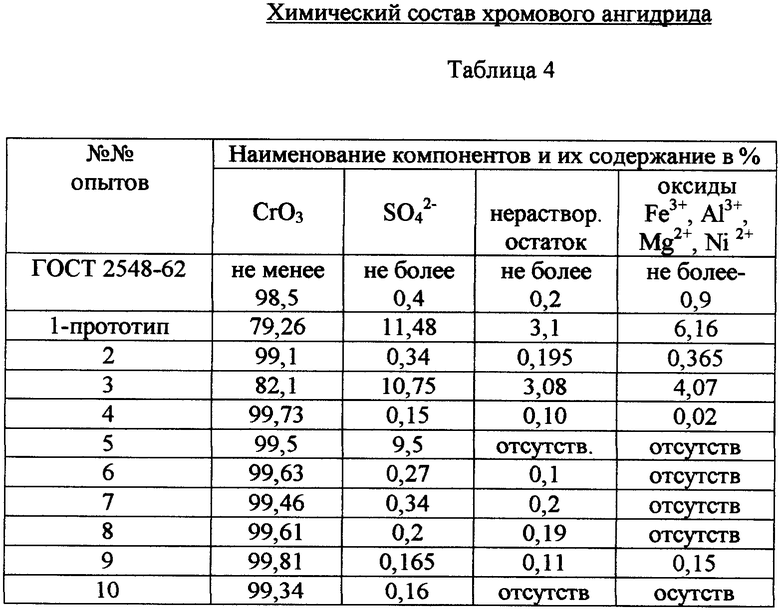
В табл.4 приведен химический состав готового продукта - хромового ангидрида.
Пример 1
Технология получения хромового ангидрида проведена по схеме прототипа.
1000 г хромитового концентрата, содержащего 54,2% Cr2О3 и 12,8% FeO с размером частиц 2,0+0,0 мм, обрабатывают раствором, состоящим из 3,7 л 60%-ной серной кислоты и 11,7 г хромового ангидрида, взятого в качестве катализатора. Выщелачивание проводят при температуре 140-150°С. Соотношение Т:Ж=1:3,7. Количество CrO3 в реакционной смеси, равное 11,7 г, соответствует 9,14% от содержания окислов двухвалентного железа в хромитовом концентрате. Количество Cr2O3, перешедшего в раствор в результате выщелачивания, - 35,3%.
После выщелачивания суспензию центрифугируют, нерастворимый остаток массой 380 г, представляющий собой неразложившиеся минералы, направляют на дальнейшую переработку, а фильтрат (объемом 6,75 л), состоящий из смеси сульфатов Cr3+, Al3+, Mg2+, Fe3+ и др. и серной кислоты, направляют на электролиз с целью окисления трехвалентного хрома в шестивалентный и перевода сульфата хрома в хромовую кислоту.
Электролиз ведут в специальных электролизерах с мембраной и со свинцовым анодом при температуре 30-50°С. Далее раствор направляют на упаривание при температуре 140-150°С до концентрации серной кислоты 1100 г/л с целью максимального извлечения CrO3.
Упаренную суспензию центрифугируют, маточный раствор, содержащий серную кислоту и сульфаты, направляют на выщелачивание хромитового концентрата, а осадок (готовый продукт) сушат при температуре 150°С и затаривают. Выход готового продукта составил 465,0 г или 65.2% от возможного - 713 г.
Пример 2
1000 г хромитового концентрата, содержащего 54,20% Cr2О3 (см. табл.2, ст.2), выщелачивают по схеме 1. Содержание CrO3 в реакционной смеси - 11,7 г. Количество Cr2O3, перешедшее в раствор после выщелачивания, - 35,13%. Суспензию центрифугируют, маточный раствор подвергают электролизу и упариванию (по схеме 1), упаренную суспензию центрифугируют, нерастворимый остаток отмывают в серной кислоте (1140 г/л) при температуре 140-150°С. Выпавшие кристаллы CrO3 сушат при температуре 150°С и затаривают. Выход готового продукта составил 465,4 г.
Пример 3
1000 г хромитового концентрата, обогащенного методом гравитации и содержащего 59,71% Cr2О3 и 14,05% FeO (табл.2, ст.3), выщелачивают по схеме 1. Содержание CrO3 в реакционной смеси - 12,84 г. Количество Cr2О3, перешедшее в раствор после выщелачивания, равно 39,13%. Далее процесс ведут по схеме 1. Выход готового продукта составил 515,4 г.
Пример 4
1000 г хромитового концентрата, обогащенного методом гравитации и содержащего 59,71% Cr2О3 и 14,05% FeO, выщелачивают по схеме 3. Содержание CrO3 в реакционной смеси - 12,84 г. Количество Cr2O3, перешедшее в раствор после выщелачивания, - 39,13%. Далее процессы электролиза, упаривания электролита, очистки нерастворимого осадка в серной кислоте и сушки кристаллов Cr2О3 ведут по схеме 2. Выход готового продукта составил 517,0 г.
Пример 5
1000 г хромитового концентрата, обогащенного методом гравитации и содержащего 59,71% Cr2О3 и 14,05% FeO, выщелачивают раствором, состоящим из серной кислоты (62% H2SO4) и 93,0 г и 14,05% FeO (по схеме 3). Количество Cr2О3, перешедшее в раствор, - 44,8%. Далее процессы электролиза, упаривания электролита, очистки кристаллов CrO3 от примесей в серной кислоте и их сушку проводят по схеме 2. Выход готового продукта составил ˜589 г или 75% от возможного 785,3 г.
Примеры 6-10
Получение кристаллического CrO3 проводят по схеме 5, изменяя концентрацию катализатора в процессе выщелачивания от 103 до 140 г, что составляет от 70,0 до 100% CrO3, от содержания FeO в хромитовом концентрате, равном 14,0%.
Таким образом, из приведенных примеров видно, что максимальный выход готового продукта - кристаллов CrO3 - 86,5% самого высокого качества (содержание CrO3=99,81-99,85%) обеспечивается в процессах, которые включают в себя:
- обогащение хромитового концентрата с методом гравитации;
- сернокислотное выщелачивание хромитового концентрата в смеси с катализатором - хромовым ангидридом, в количестве, равном 70-100% от содержания FeO в хромитовом концентрате. Дальнейшее увеличение концентрации катализатора в реакционном растворе для выщелачивания экономически нецелесообразно, поскольку приводит к существенному повышению коррозионной активности реакционной массы;
- электрохимическое окисление сульфата хрома в хромовую кислоту;
- упаривание раствора, содержащего смесь хромовой и серной кислот при температуре 140-150°С до содержания H2SO4 в упаренном растворе 940-1100 г/л;
- отмывку кристаллов CrO3 в серной кислоте концентрации 60-62% при температуре 140-150°С;
- сушку кристаллов CrO3 при температуре 150°С.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОМПЛЕКСНОЙ ПЕРЕРАБОТКИ МАГНИЙХРОМСОДЕРЖАЩЕГО РУДНОГО СЫРЬЯ | 2006 |
|
RU2344076C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХРОМИТОВОГО КОНЦЕНТРАТА | 2006 |
|
RU2312912C2 |
| СПОСОБ КОМПЛЕКСНОЙ ПЕРЕРАБОТКИ СЕРПЕНТИН-ХРОМИТОВОГО РУДНОГО СЫРЬЯ | 2013 |
|
RU2535254C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННЫХ КРАСНЫХ ЖЕЛЕЗООКСИДНЫХ ПИГМЕНТОВ | 2006 |
|
RU2309898C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ МЕТАЛЛОВ ПЛАТИНОВОЙ ГРУППЫ ИЗ ПЛАТИНОСОДЕРЖАЩЕГО СЫРЬЯ | 2009 |
|
RU2415954C1 |
| СПОСОБ ОБОГАЩЕНИЯ МАГНЕЗИАЛЬНЫХ ХРОМИТОВЫХ РУД | 2007 |
|
RU2341574C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОКИСИ ХРОМА | 2004 |
|
RU2258039C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОХРОМАТА НАТРИЯ | 2004 |
|
RU2281250C2 |
| Способ переработки хромита | 1990 |
|
SU1758004A1 |
| Способ получения комплексного минерального удобрения | 1986 |
|
SU1392066A1 |
Изобретение может быть использовано при получении хромового ангидрида, используемого в химической, лакокрасочной, текстильной, металлургической и других отраслях промышленности. Способ получения хромового ангидрида включает выщелачивание хромитового концентрата при температуре 140-160°С смесью 60-62%-ной серной кислоты и катализатора - хромового ангидрида, центрифугирование суспензии, окисление методом электролиза сульфата хрома, полученного в результате выщелачивания, в хромовую кислоту, упаривание раствора электролита при температуре 140-150°С до концентрации серной кислоты в упаренном растворе 950-1100 г/л, отделение кристаллов хромового ангидрида от маточного раствора центрифугированием и сушку готового продукта. Предварительно перед сернокислотным выщелачиванием хромитовый концентрат обогащают методом гравитации. Количество катализатора при выщелачивании составляет 70-100% от содержания оксида двухвалентного железа в хромитовом концентрате. После отделения от маточного раствора кристаллы хромового ангидрида дополнительно отмывают в серной кислоте концентрации 60-62% при температуре 140-150°С. Изобретение позволяет получить хромовый ангидрид из бедных рудных смесей с повышением выхода продукта и снижением содержания примесей. 4 табл.
Способ получения хромового ангидрида из хромитового концентрата, включающий выщелачивание при температуре 140-160°С смесью 60-62%-ной серной кислоты и катализатора - хромового ангидрида, центрифугирование суспензии, окисление методом электролиза сульфата хрома, полученного в результате выщелачивания, в хромовую кислоту, упаривание раствора электролита при температуре 140-150°С до концентрации серной кислоты в упаренном растворе 950-1100 г/л, отделение кристаллов хромового ангидрида от маточного раствора центрифугированием и сушку готового продукта, отличающийся тем, что предварительно перед серно-кислотным выщелачиванием хромитовый концентрат обогащают методом гравитации, количество катализатора при выщелачивании составляет 70-100% от содержания оксида двухвалентного железа в хромитовом концентрате, а после отделения от маточного раствора кристаллы хромового ангидрида дополнительно отмывают в серной кислоте концентрации 60-62% при температуре 140-150°С.
| CLAY J.L | |||
| et al., An acid process for the production of chromic anhydride from chromite ore, Journal of the society of chemical industry, 1950, vol.69, No.7, p.275-282 | |||
| Способ получения хромового ангидрида | 1983 |
|
SU1168511A1 |
| Способ получения хромового ангидрида | 1983 |
|
SU1161470A1 |
| GB 2005241 A, 19.04.1979 | |||
| ЛОСЕВ К.И | |||
| О переработке хромовых руд по мокрому способу действием серной кислоты с окислителями, | |||
Авторы
Даты
2009-03-20—Публикация
2007-06-09—Подача