ПРИОРИТЕТ
В настоящей международной заявке заявляется приоритет согласно Парижской конвенции и п. 35, 119 Свода федерального законодательства США на основании ранее поданной заявки на патент США № 14/098 353, поданной 5 декабря 2013 г., содержание которой включено в настоящую заявку посредством ссылки.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Сахарный диабет - хроническое метаболическое расстройство, вызванное неспособностью организма вырабатывать достаточное количество гормона инсулина, что приводит к снижению способности организма усваивать глюкозу. Такая неспособность ведет к гипергликемии, т.е. избыточному содержанию глюкозы в плазме крови. Устойчивая гипергликемия и/или гипоинсулинемия связаны с различными серьезными симптомами и долговременными, угрожающими жизни осложнениями, такими как обезвоживание, кетоацидоз, диабетическая кома, сердечнососудистые заболевания, хроническая почечная недостаточность, повреждение сетчатки и повреждение нервов с риском ампутации конечностей. Поскольку восстановить выработку эндогенного инсулина пока невозможно, необходима постоянная терапия для обеспечения непрерывного контроля гликемии, чтобы концентрация глюкозы в крови всегда оставалась в пределах нормы. Такой контроль гликемии достигается путем регулярного введения в организм пациента инсулина извне с целью снижения повышенной глюкозы.
Экзогенные биологические препараты, такие как инсулин, обычно назначаются в виде смеси быстродействующих лекарственных средств и препаратов с промежуточной длительностью действия, вводимой посредством многократных ежедневных подкожных инъекций с помощью шприца. Обнаружено, что достижимая таким способом степень контроля гликемии ниже оптимальной, так как подобная доставка препарата отличается от физиологической выработки гормона, когда гормон поступает в кровь с меньшей скоростью и на протяжении более длительного времени. Улучшить контроль гликемии возможно с помощью так называемой интенсивной гормональной терапии, основанной на многократных ежедневных инъекциях, включающих в себя одну или две инъекции гормона длительного действия в сутки для создания базальной концентрации гормона и дополнительные инъекции быстродействующего гормона перед каждым приемом пищи в количестве, пропорциональном размеру порции пищи. Хотя инсулиновые шприцы-ручки, по меньшей мере, частично заменили традиционные шприцы, частые инъекции очень неудобны для пациентов, особенно тех, кто не в состоянии делать себе инъекции надлежащим образом.
Разработка устройства для доставки лекарственных средств значительно улучшила лечение диабета, избавив пациента от необходимости многократных ежедневных инъекций с помощью шприцев или шприц-ручек. Устройство для доставки лекарственных средств позволяет вводить лекарственное средство способом, более близким к естественным физиологическим процессам, и для улучшения контроля гликемии у пациента может регулироваться в соответствии со стандартными или индивидуальными протоколами.
Кроме того, устройства для доставки лекарств позволяют вводить лекарственные средства непосредственно во внутрибрюшинное пространство или внутривенно. Устройства доставки лекарственных средств могут быть сконструированы в виде имплантируемых устройств для установки под кожу или в виде внешних устройств с инфузионной системой для подкожных инфузий посредством чрескожного катетера, канюли или трансдермального транспорта лекарственного средства, например через пластырь. Внешние устройства для подачи лекарственных средств размещаются поверх одежды, прячутся под одежду или внутри нее либо размещаются на поверхности тела и обычно управляются с помощью встроенного пользовательского интерфейса или отдельного устройства для дистанционного управления.
Для достижения приемлемого контроля гликемии необходимо периодическое измерение концентрации глюкозы в крови или тканевой жидкости. Например, доставка соответствующего количества инсулина с помощью устройства для доставки лекарственных средств требует от пациента регулярного определения концентрации глюкозы в его крови и ручного ввода этого значения с помощью пользовательского интерфейса для внешних насосов, который затем рассчитывает требуемое изменение протокола введения инсулина по умолчанию или текущего протокола, т.е. дозировки и времени введения, и взаимодействует с устройством для доставки лекарственного средства с целью регулировки его работы соответствующим образом. Для определения концентрации глюкозы в крови обычно используются устройства для эпизодического измерения, например ручные электронные анализаторы, использующие тест-полоски для анализа крови ферментативным методом и вычисляющие концентрацию глюкозы на основании ферментативной реакции.
На протяжении последних 20 лет также используется непрерывный контроль глюкозы в сочетании с устройствами для доставки лекарственных средств, что позволяет управлять инфузией больным диабетом инсулина с помощью механизма обратной связи. Для обеспечения возможности контроля инфузии инсулина применяются пропорционально-интегрально-дифференциальные (ПИД) контроллеры с математической моделью взаимодействий между глюкозой и инсулином у человека. ПИД-контроллеры можно настраивать на основании простых правил метаболических моделей. Однако если конфигурировать или настроить ПИД-контроллеры на агрессивную регулировку концентрации глюкозы в крови у пациента, то может произойти передозировка, превышающая установленный уровень, за которой часто следуют колебания, крайне нежелательные в контексте регуляции концентрации глюкозы в крови. Были исследованы альтернативные контроллеры. Установлено, что контроллер с прогнозирующей моделью (КПМ), применяющийся в нефтехимической промышленности и характеризующийся значительными временными задержками и системными откликами, наиболее подходит для регулировки сложных взаимоотношений между инсулином, глюкагоном и глюкозой в крови. Показано, что КПМ более устойчив, чем ПИД, так как КПМ учитывает эффекты изменений в ближайшем будущем и ограничения при определении выхода КПМ, в то время как ПИД обычно учитывает только предыдущие выходы при определении будущих изменений. В КПМ могут использоваться ограничения, например, таким образом, чтобы КПМ предотвращал выход системы из-под контроля, когда предел уже достигнут. Другим преимуществом КПМ является то, что модель в КПМ может в некоторых случаях теоретически компенсировать динамические изменения системы, в то время как при регулировке по принципу обратной связи, такой как ПИД-контроль, подобная динамическая компенсация невозможна.
Таким образом, КПМ можно рассматривать как сочетание регулирования по принципу обратной связи и опережающего регулирования. Однако КПМ обычно требует метаболической модели, как можно точнее имитирующей взаимоотношения между инсулином и глюкозой в биологической системе. Таким образом, из-за индивидуальных биологических различий процесс разработки и уточнения КПМ все еще продолжается в настоящее время. В качестве обзорной информации по КПМ, имеющей отношение к деталям КПМ, в следующих документах показаны и описаны варианты КПМ и математические модели, представляющие сложные взаимодействия между глюкозой и инсулином:
Патент США № 7,060,059;
заявки на патент США № 2011/0313680 и 2011/0257627;
Международная публикация WO 2012/051344;
Percival et al., «Closed-Loop Control and Advisory Mode Evaluation of an Artificial Pancreatic β Cell: Use of Proportional-Integral-Derivative Equivalent Model-Based Controllers» Journal of Diabetes Science and Technology, Vol. 2, Issue 4, July 2008.
Paola Soru et al.., «MPC Based Artificial Pancreas; Strategies for Individualization and Meal Compensation» Annual Reviews in Control 36, p.118-128 (2012),
Cobelli et al., «Artificial Pancreas: Past, Present, Future» Diabetes Vol. 60, Nov. 2011;
Magni et al., «Run-to-Run Tuning of Model Predictive Control for Type 1 Diabetes Subjects: In Silico Trial» Journal of Diabetes Science and Technology, Vol. 3, Issue 5, September 2009;
Lee et al., «A Closed-Loop Artificial Pancreas Using Model Predictive Control and a Sliding Meal Size Estimator» Journal of Diabetes Science and Technology, Vol. 3, Issue 5, September 2009;
Lee et al., «A Closed-Loop Artificial Pancreas based on MPC: Human Friendly Identification and Automatic Meal Disturbance Rejectionʺ Proceedings of the 17th World Congress, The International Federation of Automatic Control, Seoul Korea July 6-11, 2008;
Magni et al., «Model Predictive Control of Type 1 Diabetes: An in Silico Trial» Journal of Diabetes Science and Technology, Vol. 1, Issue 6, November 2007;
Wang et al., «Automatic Bolus and Adaptive Basal Algorithm for the Artificial Pancreatic β-Cell» Diabetes Technology and Therapeutics, Vol. 12, No. 11, 2010; и
Percival et al., «Closed-Loop Control of an Artificial Pancreatic β-Cell Using Multi-Parametric Model Predictive Control» Diabetes Research 2008.
Все статьи или документы, процитированные в этой заявке, включены в нее во всей своей полноте посредством ссылок.
ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Заявители разработали методику, позволяющую для способа работы с системой контроля диабета контролировать диабет пользователя. Система имеет инфузионный насос, по меньшей мере, один монитор глюкозы и контроллер. Способ может быть реализован путем следующих этапов, на которых: определяется измерение уровня глюкозы, в котором жидкая проба с глюкозой преобразовывается в продукт ферментативной реакции путем подачи электрических сигналов на образец; проводится расчет рекомендуемого болюса на основании измерения глюкозы, проведенного на этапе определения; проводится оценка соблюдения рекомендации болюса пользователем системы; в случае, если рекомендация болюса не соблюдена пользователем: проводится сохранение фактического болюса, доставленного инфузионным насосом; проводится измерение значения глюкозы в последующих жидких пробах и, если значения глюкозы в течение времени больше, чем предварительно заданный порог тенденции изменения значений в сторону повышения, тогда проводится информирование о тенденции к повышению значений глюкозы, наряду с рекомендуемым болюсом и фактическим болюсом, доставленным насосом, в противном случае, если значения глюкозы с течением времени меньше, чем предварительно заданный порог тенденции изменения значений в сторону понижения, тогда проводится информирование о тенденции к понижению значений глюкозы, наряду с рекомендуемым болюсом и фактическим болюсом, доставленным насосом.
В еще одном аспекте предлагается система контроля диабета, которая содержит глюкометр для эпизодического измерения, глюкометр для непрерывного измерения и соединенный с контроллером инфузионный насос. Глюкометр для эпизодического измерения выполнен с возможностью измерения уровня глюкозы в жидкой пробе пациента через дискретные и неоднородные временные интервалы и представления подобного эпизодического уровня концентрации глюкозы в виде входных данных для расчета болюса; глюкометр для непрерывного измерения для постоянного измерения уровня глюкозы у пациента через дискретные, и, как правило, равномерные временные интервалы и представления концентрации глюкозы для каждого интервала в виде данных измерения глюкозы, которые можно использовать для расчета болюса. Инфузионный инсулиновый насос выполнен с возможностью доставки инсулина в организм пациента; микроконтроллер, связанный с насосом, глюкометром и монитором глюкозы. Контроллер выполнен с возможностью обеспечения рекомендации болюса для пациента, оценки отличается ли фактического болюс, доставленный насосом от рекомендованного болюса. В случае отличия доставленного фактического болюса от рекомендованного болюса система определяет тенденцию изменения уровня глюкозы в течение определенного периода времени и информирует пользователя о тенденции к понижению или повышению значений наряду с фактическим болюсом, доставленным в организм и рекомендацией болюса.
В любом из описанных выше аспектов также можно использовать следующие элементы в комбинации с каждым из аспектов. Например, система может сохранять измерение глюкозы, сделанное на этапе измерения в контроллере; система может установить потребность в другой рекомендации болюса; система может определить скорость снижения изменения в измерениях глюкозы жидких проб пользователя; монитор глюкозы может включать в себя монитор для непрерывного измерения уровня глюкозы; информирование о тенденции к повышению уровня глюкозы может включать в себя отображение сообщения о том, что тенденция измерений глюкозы повышается после болюсного введения наряду с рекомендованным болюсом и фактическим болюсом, доставленным в организм; информирование о тенденции к понижению уровня глюкозы может включать в себя отображение текстового сообщения о том, что тенденция измерений глюкозы понижается после болюсного введения наряду с рекомендованным болюсом и фактическим болюсом, доставленным в организм; порог тенденции к понижению значений может включать снижение скорости или отрицательную скорость изменений в 20 мг/дл за каждые тридцать минут, а порог тенденции к повышению значений может включать в себя повышение скорости или положительную скорость изменений в 20 мг/дл за тридцать минут.
Эти и другие варианты осуществления, признаки и преимущества станут очевидны специалистам в данной области после изучения представленного ниже более подробного описания различных примеров осуществления настоящего изобретения в сочетании с сопроводительными рисунками, которые кратко описаны в начале заявки.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Сопроводительные чертежи, которые включены в настоящий документ и составляют неотъемлемую часть настоящего описания, иллюстрируют предпочтительные в настоящее время варианты осуществления изобретения и, вместе с приведенным выше общим описанием и представленным ниже подробным описанием, служат для разъяснения элементов изобретения (причем аналогичные элементы представлены под аналогичными номерами).
На Фиг. 1 показана система, в которой контроллер насоса или датчик(и) глюкозы отделен от инфузионного насоса и датчика(ов) глюкозы и в которой контроллер можно подключить к сети с целью проведения контроля в реальном времени.
На Фиг. 2 показан пример осуществления системы для лечения диабета в схематической форме.
На Фиг. 3 показана логика, применяющаяся в контроллере, представленном на Фиг. 1 или Фиг. 2;
На Фиг. 4A и 4B показаны сообщения из системы; и
На Фиг. 5 показаны графические и текстовые сообщения системы;
ВАРИАНТЫ ВЫПОЛНЕНИЯ ИЗОБРЕТЕНИЯ
Приведенное ниже подробное описание следует толковать со ссылкой на чертежи, на которых одинаковые элементы на разных чертежах обозначены одинаковыми номерами. Графические материалы, не обязательно выполненные в масштабе, показывают выбранные варианты осуществления и не призваны ограничить объем настоящего изобретения. В подробном описании принципы изобретения показаны с помощью примеров, которые не имеют ограничительного характера. Это описание, несомненно, позволит специалистам в данной области реализовать и применять изобретение, и в нем описано несколько вариантов осуществления, адаптаций, вариаций, альтернатив и вариантов применения изобретения, включая те, которые в настоящее время считаются наилучшими вариантами осуществления изобретения.
При использовании в настоящем документе термины «около» или «приблизительно» в отношении любых числовых значений или диапазонов указывают на подходящее допустимое отклонение, которое позволяет части или совокупности компонентов выполнять функцию, предусмотренную для них в настоящем документе. Кроме того, в настоящем документе термины «пациент», «оператор», «пользователь» и «субъект» относятся к любому субъекту-человеку или субъекту-животному и не предполагают ограничения применения систем или способов только у человека, хотя применение предмета изобретения у пациента-человека представляет собой предпочтительный вариант осуществления. Кроме того, термин «пользователь» включает в себя не только пациента, использующего инфузионную помпу для введения лекарственного средства, но и ответственных за него лиц (например, родителей или опекунов, сестринского персонала или работников, обеспечивающих уход за пациентом на дому). Термин «лекарственное средство» может включать в себя гормон, биологически активные материалы, фармацевтические препараты или другие химические вещества, вызывающие биологическую реакцию (например, гликемическую реакцию) в организме пользователя или пациента.
На Фиг. 1 представлена система 100 доставки лекарственного средства в соответствии с примером осуществления, в котором используются принципы настоящего изобретения. Система доставки лекарственных средств 100 включает устройство доставки лекарственных средств 102 и удаленный контроллер 104. Устройство 102 подачи лекарственного средства соединено с инфузионным набором 106 посредством гибкой трубки 108.
Устройство 102 подачи лекарственного средства выполнено с возможностью передачи данных на удаленный контроллер 104 и приема данных от него, например по радиочастотной связи 112. Устройство 102 доставки лекарственного средства также может функционировать как самостоятельное устройство со своим собственным встроенным микроконтроллером. В одном варианте осуществления устройство для доставки лекарственного средства 102 представляет собой устройство для инфузии инсулина, а удаленный контроллер 104 - ручной портативный контроллер. В таком варианте осуществления данные, переданные от устройства для доставки лекарственного средства 102 на удаленный контроллер 104, могут включать такую информацию, как, например, данные о доставке инсулина, информация о концентрации глюкозы, базальной концентрации, болюсном введении, соотношении инсулина и углеводов или коэффициенте чувствительности к инсулину, в качестве нескольких примеров. Конфигурация микроконтроллера 104 включает КПМ-контроллер 10, запрограммированный таким образом, чтобы непрерывно получать результаты измерения глюкозы от датчика для непрерывного измерения концентрации глюкозы в крови 112. Данные, переданные от удаленного микроконтроллера 104 на устройство для доставки инсулина 102, могут включать результаты измерения глюкозы и базу данных о приеме пищи, чтобы устройство для доставки лекарственного средства 102 могло вычислить количество инсулина, которое должно быть доставлено устройством для доставки 102. Альтернативно удаленный микроконтроллер 104 может выполнять расчеты базальной дозы или болюсного введения и направлять результаты таких расчетов на устройство доставки лекарственного средства. В альтернативном варианте осуществления глюкометр 114 для эпизодического измерения может применяться отдельно или в сочетании с датчиком 112 НКГ, подавая данные на микроконтроллер 104 и/или устройство 102 доставки лекарственного средства. Альтернативно удаленный микроконтроллер 104 может быть скомбинирован с измерителем 114, образуя либо (а) интегрированное цельное устройство; либо (b) два отдельных устройства, которые могут присоединяться друг к другу с образованием интегрированного устройства. Каждое из устройств 102, 104 и 114 имеет соответствующий микроконтроллер (не показан для краткости), запрограммированный на выполнение различных функций.
Устройство доставки лекарственных средств 102 также может быть сконфигурировано для двунаправленной беспроводной связи с удаленной станцией контроля состояния здоровья 116 через, например, беспроводную сеть связи 118. Удаленный контроллер 104 и удаленная станция 116 контроля могут быть сконфигурированы для двунаправленной проводной связи через, например, сеть связи на основе телефонной линии. Удаленная станция 116 контроля может применяться, например, для загрузки обновленного программного обеспечения на устройство 102 подачи лекарственного средства и для обработки информации от устройства 102 подачи лекарственного средства. Примеры удаленных станций 116 контроля могут включать без ограничений персональный или сетевой компьютер 126, сервер 128 с памятью для хранения, карманный персональный компьютер, другой мобильный телефон, базовую станцию контроля в больнице или специальную удаленную станцию клинического контроля.
Устройство 102 для доставки лекарственного средства включает в себя компоненты для обработки электронного сигнала, в том числе центральный процессор и элементы памяти для хранения программ управления и операционных данных, радиочастотный модуль 116 для отправки и приема радиокоммуникационных сигналов (т.е. сообщений) на удаленный контроллер 104 или от него, дисплей для отображения рабочей информации для пользователя, множество навигационных кнопок, позволяющих пользователю вводить информацию, аккумулятор для подачи питания системы, предупреждения (визуальные, звуковые или тактильные) для обратной связи с пользователем, вибрационное устройство для обратной связи с пользователем, механизм доставки лекарственного средства (например, насос и приводной механизм) для вытеснения инсулина из инсулинового резервуара (например, патрона с инсулином) через боковое отверстие, к которому подключена инфузионная система 108/106, в тело пользователя. Пример устройства 102 для доставки лекарственного средства (или насоса 16) может быть представлен в форме модифицированного инсулинового насоса Animas Vibe, произведенного компанией Animas Corporation, г. Уэйн, шт. Пенсильвания, США.
Уровни или концентрации глюкозы можно определять с применением датчика 112 НКГ. Датчик 112 для непрерывного контроля глюкозы использует технологию амперометрического электрохимического измерения для определения глюкозы с помощью трех электродов, функционально связанных с электроникой датчика и покрытых чувствительной мембраной и биоинтерфейсной мембраной, которые присоединены с помощью зажима.
Верхние концы электродов находятся в контакте с электролитной фазой (не показана), которая представляет собой свободно плавающую жидкую фазу, расположенную между чувствительной мембраной и электродами. Чувствительная мембрана может включать фермент (например, глюкооксидазу), который покрывает фазу электролита. В данном примере датчика предложен противоэлектрод для уравновешивания тока, генерируемого веществом при измерении на рабочем электроде. В случае датчика глюкозы на основе глюкооксидазы веществом, измеряемым на рабочем электроде, является H2O2. Ток, получаемый на рабочем электроде (и протекающий через схему к противоэлектроду), пропорционален диффузионному потоку H2O2, производимому путем электромеханического преобразования глюкозы в ферментативный побочный продукт. Соответственно, можно получить необработанный сигнал, который представляет концентрацию глюкозы в теле пациента и поэтому может быть использован для оценки содержательного значения глюкозы. Подробная информация о датчике и сопутствующих компонентах показана и описана в патенте США № 7276029, который полностью включен в настоящий документ посредством ссылки. В одном варианте осуществления может быть использован датчик непрерывного измерения глюкозы из системы Dexcom Seven® (производитель - компания Dexcom Inc.) с примерами осуществления, описанными в настоящем документе.
В одном варианте осуществления могут также использоваться следующие компоненты в качестве системы для лечения диабета, созданной по типу искусственной поджелудочной железы: система регулировки концентрации глюкозы OneTouch Ping® производства компании Animas Corporation, включающая по меньшей мере инфузионный насос и датчик для эпизодического измерения глюкозы; и DexCom® G4 Platinum® CGM производства DexCom Corporation с интерфейсом для соединения этих компонентов и программирования с помощью MATLAB®language и дополнительным аппаратным обеспечением для соединения компонентов друг с другом; а также алгоритмы управления в форме КПМ, автоматически регулирующие скорость доставки инсулина на основании концентрации глюкозы у пациента, прошлых результатов измерения глюкозы, прогнозируемых будущих тенденций изменения концентрации глюкозы и специфической информации о пациенте.
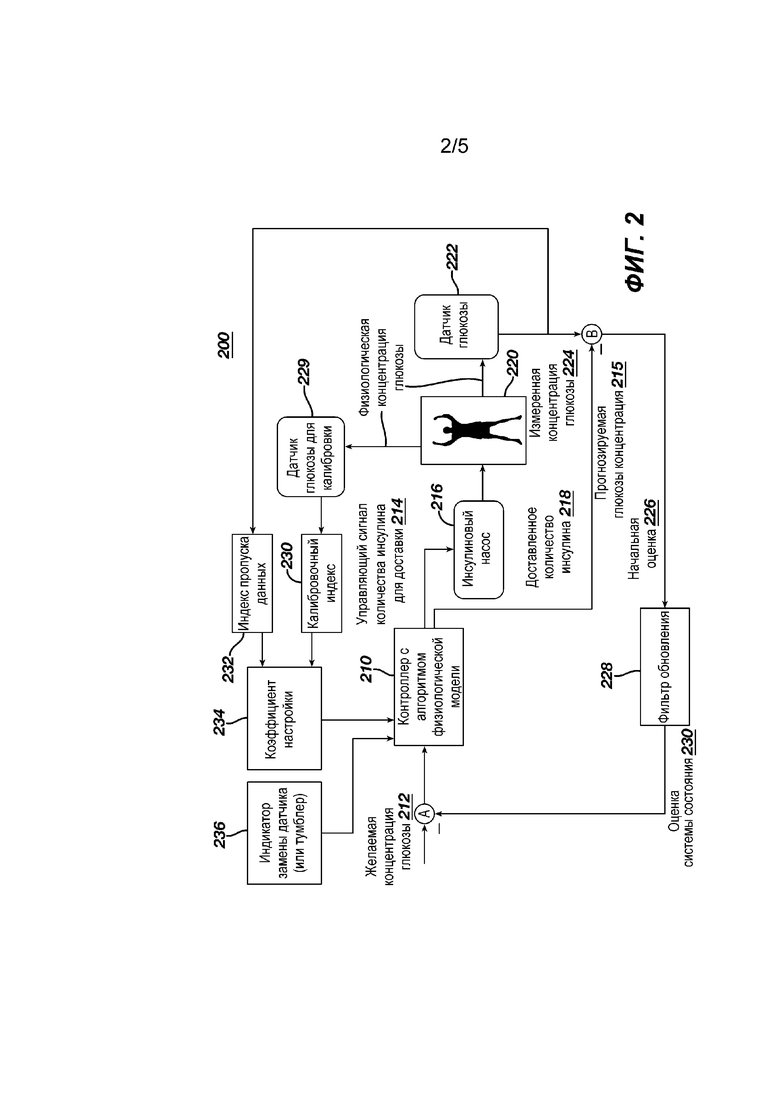
На Фиг. 2 показана схема 200 системы 100 с Фиг.1, запрограммированной с использованием разработанного заявителями решения, чтобы предотвратить снижение эффекта системы управления на основе обратной связи ниже желаемого. В частности, на Фиг. 2 представлен КПМ, запрограммированный как модуль логического управления 10, использующийся в контроллере 104. Модуль логического управления 10 КПМ получает необходимую концентрацию глюкозы или диапазон концентрации глюкозы 12 (наряду с любой модификацией от фильтра обновления 28) так, чтобы быть способным поддерживать выходной сигнал (т.е. концентрацию глюкозы) пациента в необходимом диапазоне концентрации глюкозы.
Как показано на Фиг. 2, первый выход 14 устройства 10 логического управления с активированным КПМ может быть управляющим сигналом для инсулинового насоса 16 на доставку желаемого количества инсулина 18 пациенту 20 через предварительно заданные временные интервалы, которые могут индексироваться каждые 5 минут при помощи индекса временных интервалов k. Второй выход в форме прогнозируемого значения концентрации глюкозы 15 может использоваться в управляющем соединении B. Датчик глюкозы 22 (или 112 на Фиг. 1) измеряет концентрацию глюкозы у пациента 20, чтобы подать сигналы 24, отражающие фактическую или измеренную концентрацию глюкозы, на управляющее соединение B, которое учитывает различие между результатом измерения концентрации глюкозы 24 и прогнозами КПМ относительно этой измеренной концентрации глюкозы. На основании этого различия на фильтр обновлений 26 переменных состояний модели подается информация. Разница 26 служит параметром оценки (также фильтр обновлений 28) и позволяет оценить переменные состояния в модели, которые нельзя измерить непосредственно. Предпочтительно, когда фильтр обновлений 28 является рекурсивным фильтром в форме фильтра Кальмана с подстройкой параметров для модели. Выходной сигнал фильтра обновлений 28, или рекурсивного фильтра, передается на управляющее соединение A, выход которого используется КПМ в устройстве 10 логического управления для дальнейшего уточнения управляющего сигнала 14 к насосу 16 (или 102 на Фиг. 1). Коэффициент настройки 34 используется с контроллером 10 КПМ для «настройки» контроллера при доставке инсулина. Для достижения этой цели для корректировки коэффициента настройки заявители разработали применение модуля 30 калибровочного индекса и модуля 32 пропуска данных. Модуль 30 калибровочного индекса выполнен с возможностью отслеживания количества калибровок измерения глюкозы, которое обычно проводится глюкометром для эпизодического измерения, такого как, например, тест-полоска для определения глюкозы в крови и система для измерения. Модуль 32 пропуска данных выполнен с возможностью отслеживания количества пропущенных измерений или данных, полученных от глюкометра 22 для непрерывного измерения глюкозы.
Подробная информация о контроллере с замкнутым контуром представлена в заявке на патент США № 13/834571, поданной 15 марта 2013 г. (патентный реестр № ANM5248USNP), содержание которой полностью включено в настоящую заявку посредством ссылки.
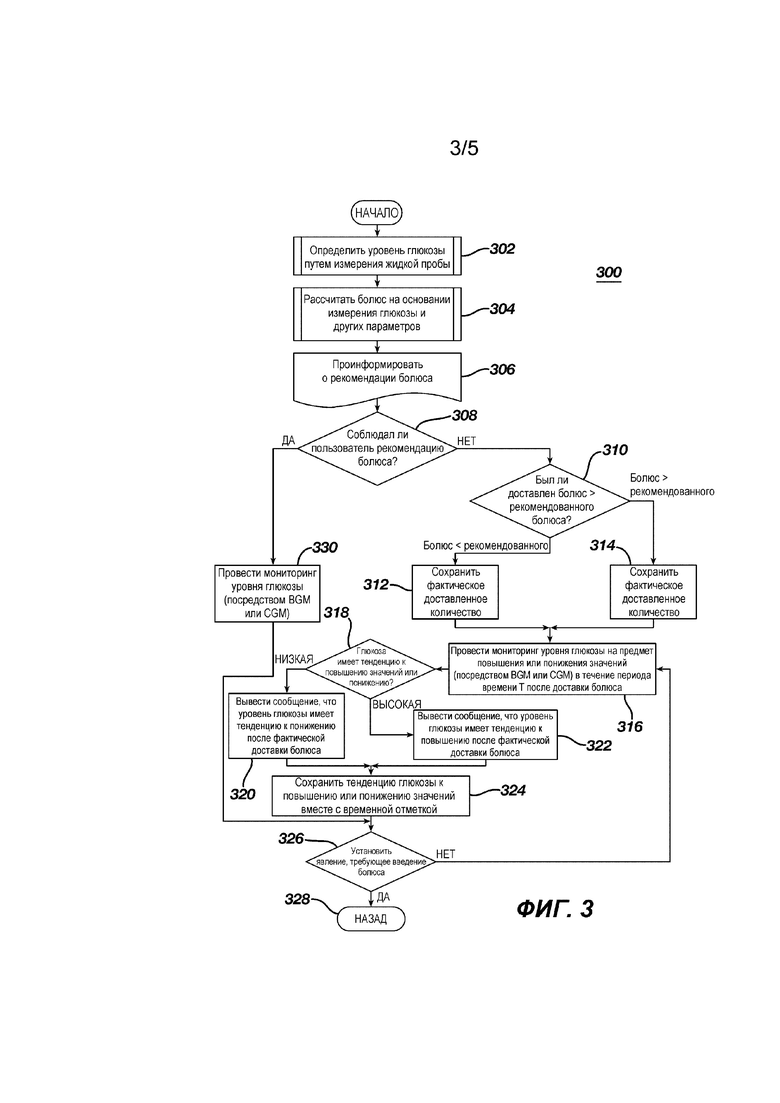
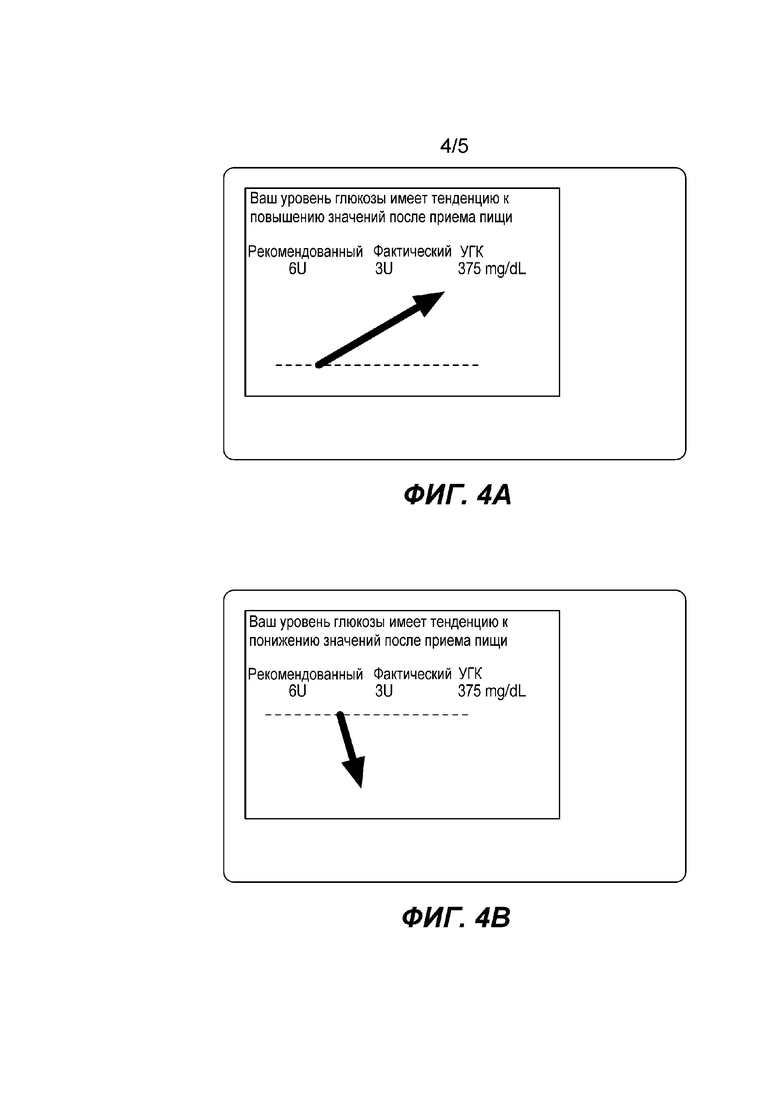
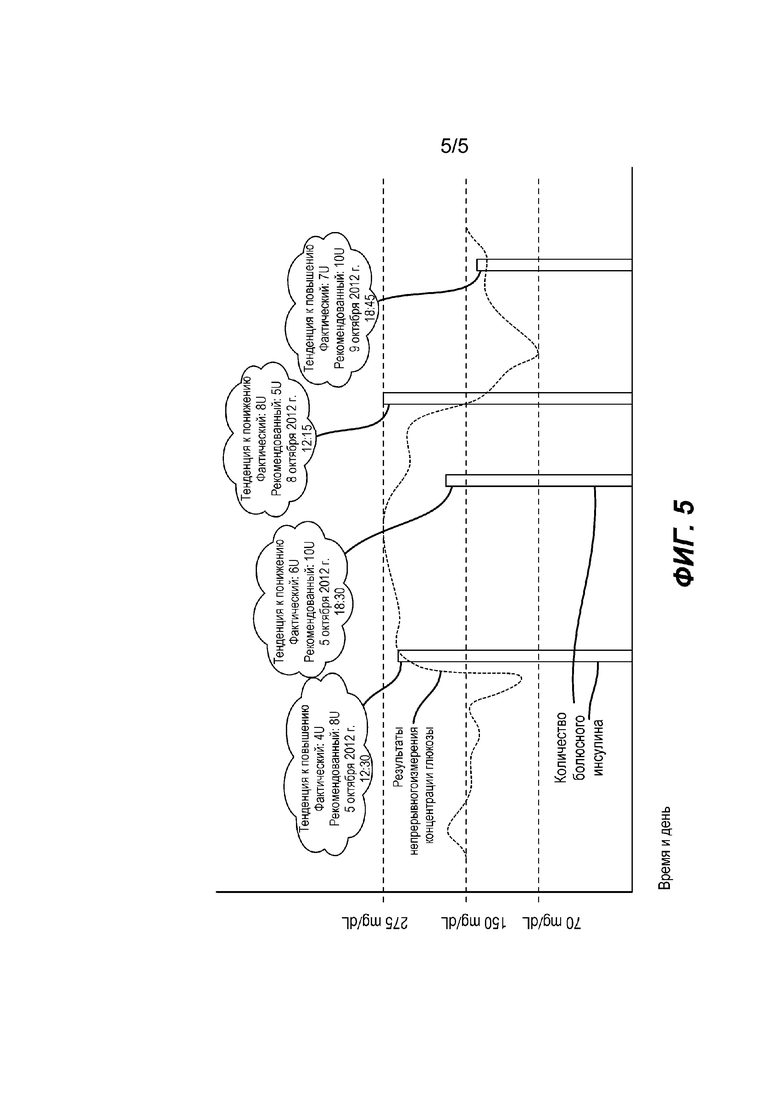
На Фиг. 3 показан логический процесс 300, который может быть использован (с соответствующими изменениями, которые доступны возможностям специалиста в данной области) для системы 100 или системы 200. Процесс 300 начинается с принятия решения (пользователем или контроллером) на этапе 302 о проведении измерения глюкозы в жидкой пробе (например, крови или межклеточная жидкости). Затем глюкоза в жидкой пробе физически преобразовывается в ферментативный побочный продукт вследствие электрохимической реакции с ферментом на электродах, чувствительных к глюкозе. На этапе 304 рассчитывается болюсное количество инсулина. Расчет болюсного инсулина известен в данной области науки, как, например, показано и описано в заявке на патент США № 20120095318 или патентах США №№ 6872200, 7815602, 7819843. На этапе 306 происходит информирование о рассчитанном болюсе как рекомендуемом болюсе для пользователя. На этапе 308 система проверяет, подтвердил ли пользователь доставку рекомендованного количества болюса. Если нет, то система проверяет насос на этапе 310, чтобы определить фактическое количество, введенное пользователю. На этапе 312, если фактическое количество введенного инсулина меньше рекомендованного количества, система сохраняет это количество. На этапе 314, если фактическое количество введенного инсулина больше рекомендованного количества, оно снова сохраняется. На этапе 316, система отслеживает непрерывное считывание глюкозы в течение периода времени T после доставки болюса. По истечении времени T система проверяет на этапе 318, чтобы убедиться, что скорость изменения считанных результатов измерения глюкозы имеет тенденцию к повышению или понижению значений. Если скорость изменения имеет тенденцию к понижению, то система выдает пользователю сообщение на этапе 320, что: (a) результаты измерения глюкозы имеют тенденцию к понижению значений по отношению к предварительно заданному порогу тенденции изменения значений в сторону понижения, например, таких, как отрицательное снижение приблизительно на 20 мг/дл за каждые тридцать минут; (b) фактическое количество, доставленного болюса и (с) рекомендуемого болюса. С другой стороны, если скорость изменения значений глюкозы повышается, то система выдает сообщение на этапе 322, что: (А) глюкоза имеет тенденцию к повышению значений по отношению к предварительно заданному порогу тенденции изменения значений в сторону повышения, например, таких, как положительное повышение приблизительно на 20 мг/дл за каждые тридцать минут, (б) фактическое количество, доставленного болюса; и (с) рекомендуемое количество. Следует понимать, что концентрация глюкозы в крови 20 мг/дл и временной интервал в тридцать минут являются лишь примерами и другие концентрации глюкозы в крови и периоды времени возможны в пределах сферы применения заявленного изобретения. Сообщения, предусмотренные на соответствующих этапах 320 и 322 могут быть в виде, показанном на Фиг.4А и 4В на контроллере или на насосе. Альтернативно, сообщения могут быть графическими и текстовыми, как показано на Фиг. 5. На этапе 324 система сохраняет скорость изменения (или отмечает флажком тенденцию к повышению или к понижению значений) вместе с временной отметкой. На этапе 326 система определяет (при помощи мониторинга непрерывного измерения концентрации глюкозы или посредством ввода пользователем), что имеет место жизненное явление (например, питание, перекусы, физические упражнения, напитки и тому подобное), которые могут потребовать другой расчет болюса. Если дело обстоит именно так, то система возвращается к основной процедуре на этапе 328, в противном случае, система продолжает мониторинг уровня глюкозы на этапе 316.
Существует множество преимуществ данного изобретения: например, пользователь имеет возможность получить четкое представление о влиянии дозы инсулина на уровень глюкозы пользователя; система обеспечивает почти мгновенную обратную связь для пользователя об уровне глюкозы пользователя после введения болюса таким образом, что пользователь сможет определить, нужно ли соблюдать рекомендованный болюс или дозирование, которое отличается от рекомендованного болюса, лучше для пользователя.
Хотя настоящее изобретение было описано в контексте конкретных модификаций и иллюстрирующих фигур, лица, имеющие средний навык в данной области, определят, что изобретение не ограничивается описанными модификациями или фигурами. Например, контроллер с замкнутым контуром регулирования не обязательно должен быть контроллером КПМ, а может быть, при соответствующей модификации специалистами, ПИД контроллером, ПИД контроллером с управлением с внутренней моделью (УВМ), с модельно-алгоритмическим управлением (МАУ), как обсуждается в публикации Percival et al., «Closed-Loop Control and Advisory Mode Evaluation of an Artificial Pancreatic β Cell: Use of Proportional-Integral-Derivative Equivalent Model-Based Controllers» Journal of Diabetes Science and Technology, Vol. 2, Issue 4, July 2008. Кроме того, лицам, имеющим средний навык в данной области, будет очевидно, что в тех случаях, когда описанные выше способы и этапы указывают на наступление определенных событий в определенном порядке, этот порядок для некоторых этапов может быть изменен, и что такие изменения соответствуют возможным вариантам осуществления настоящего изобретения. Кроме того, по возможности определенные этапы можно выполнять одновременно в рамках параллельного процесса, а также выполнять последовательно, как описано выше. Таким образом, в той мере, в которой возможны вариации настоящего изобретения, которые соответствуют сущности описания или эквивалентны изобретениям, описанным в формуле изобретения, настоящий патент призван охватывать также и все такие вариации.

Изобретение относится к области медицины, а именно к эндокринологии и терапии. Для контроля диабета используют систему контроля диабета, в состав которой входят глюкометры, инсулиновый насос и микроконтроллер. При помощи глюкометра для эпизодического измерения уровня глюкозы в жидкой пробе пациента получают уровень концентрации глюкозы в виде входных данных для расчета болюса. При помощи глюкометра для непрерывного измерения уровня глюкозы у пациента через равномерные временные интервалы определяют концентрацию глюкозы для каждого интервала в виде данных измерения глюкозы, которые можно использовать для расчета болюса. При помощи инфузионного инсулинового насоса доставляют инсулин в организм пациента. При этом микроконтроллер выполнен с возможностью обеспечения рекомендации болюса для пациента, оценки, отличается ли фактический болюс, доставленный насосом, от рекомендации болюса. В случае отличия доставленного фактического болюса от рекомендации болюса определения тенденции к понижению или к повышению скорости изменения уровня глюкозы в течение определенного периода времени после доставки болюса по отношению к предварительно заданному порогу тенденции к понижению или предварительно заданному порогу тенденции к повышению, и информирования пользователя о тенденции к понижению или повышению значений наряду с фактическим болюсом, доставленным в организм, и рекомендацией болюса. 1 з.п. ф-лы, 5 ил.
1. Система (100) контроля диабета, причем система содержит:
глюкометр (114) для эпизодического измерения для измерения
уровня глюкозы в жидкой пробе пациента через дискретные и неоднородные временные интервалы и представления указанного эпизодического уровня концентрации глюкозы в виде входных данных для расчета болюса;
глюкометр (112) для непрерывного измерения для непрерывного измерения уровня глюкозы у пациента через дискретные и, как правило, равномерные временные интервалы и представления концентрации глюкозы для каждого интервала в виде данных измерения глюкозы, которые можно использовать для расчета болюса;
инфузионный инсулиновый насос (102) для доставки инсулина в организм пациента;
микроконтроллер (104), соединенный с насосом (102), глюкометром и датчиком глюкозы, причем микроконтроллер выполнен с возможностью
обеспечения рекомендации болюса для пациента,
оценки, отличается ли фактический болюс, доставленный насосом, от рекомендации болюса;
в случае отличия доставленного фактического болюса от рекомендации болюса определения тенденции к понижению или к повышению скорости изменения уровня глюкозы в течение определенного периода времени после доставки болюса по отношению к предварительно заданному порогу тенденции к понижению или предварительно заданному порогу тенденции к повышению, и информирования пользователя о тенденции к понижению или повышению значений наряду с фактическим болюсом, доставленным в организм, и рекомендацией болюса.
2. Система по п. 1, в которой порог тенденции к понижению значений включает снижение скорости изменений концентрации глюкозы на приблизительно 20 мг/дл за каждые тридцать минут, а порог тенденции к повышению значений включает повышение скорости изменений концентрации глюкозы на 20 мг/дл за каждые тридцать минут.
| WO 2011104517 A2, 01.09.2011 | |||
| US 6852104 В2, 08.02.2005 | |||
| US 2010262434 A1, 14.10.2010 | |||
| US 2012059237 A1, 08.03.2012 | |||
| US 2005027463 A1, 03.02.2005 | |||
| US 2010168660 A1, 01.07.2010 | |||
| КАНЮЛЯ И УСТРОЙСТВО ДЛЯ ВВЕДЕНИЯ | 2007 |
|
RU2468828C2 |
Авторы
Даты
2019-05-15—Публикация
2014-11-18—Подача