Область техники, к которому относится настоящее изобретение
Изобретение относится к медицине и фармацевтической промышленности, а точнее к средствам для ингибирования и/или предотвращения роста микробиопленок и может быть использовано в качестве лекарственного или профилактического средства у людей, в частности в стоматологии и в лечении и профилактике состояний слизистых оболочек.
Предшествующий уровень техники настоящего изобретения
В настоящее время растет интерес к использованию новых нетрадиционных антимикробных средств и, в частности, пептидов, что привело к широкому кругу проводимых исследований в этой области в последние десятилетия. В результате было исследовано и предложено к использованию много типов антимикробных пептидов.
Здесь следует отметить, что указанные антимикробные пептиды вырабатываются всеми формами жизни: от растений до млекопитающих и человека, и по функциональным признакам как раз предназначены самой природой для самозащиты указанных форм жизни от посторонних микроорганизмов. Антимикробные пептиды непосредственно взаимодействуют с бактериями и убивают их. Их называют антимикробными, поскольку они обладают необычайно широким спектром активности, в том числе способностью убивать или нейтрализовать грамотрицательные и грамположительные бактерии, вирусы, имеющие оболочки, такие как ВИЧ и вирус герпеса, грибки и т.д. В общем случае указанные пептиды отличаются строением и составом, начиная с 12 аминокислот, и до молекул, содержащих более 200 аминокислотных остатков. Особенно активно исследуются гликопротеины и, в частности, лактоферрины. [1]
(см. И.М. Макеева, Т.Н. Смирнова и др.: Применение лактоферринов в комплексном лечении стоматологических заболеваний (Обзор литературы). Стоматология, т. 91, 4'2012, с. 66-71.
Преимущества использования антимикробных пептидов включают в себя: биосовместимость, вовлечение компонентов в метаболизм, что обеспечивает снижение аллергических реакций на препарат. Проведенные исследования выявили существенные преимущества применения препаратов на основе антимикробных пептидов по сравнению с традиционными средствами. Также эти исследования показали, что терапия и профилактика с помощью антимикробных пептидов является несколько более дорогостоящей по сравнению с традиционными средствами из-за дополнительных затрат на получение активного вещества и сравнительно больших его потерь в лечебном или профилактическом процессе. Таким образом, создание экономичных и эффективных антимикробных композиций на основе пептидов, а также технологий получения их лекарственных форм является актуальной задачей.
Из уровня техники известна противогрибковая композиция на основе сложных среднемолекулярных пептидов, состоящих из по меньшей мере 200 аминокислотных остатков, Полипептиды по настоящему изобретению имеют предпочтительно по меньшей мере 100% антимикробную активность полипептида, состоящего из последовательности аминокислот, показанной в виде аминокислот с 1 по 40 любой из последовательностей с SEQ ID NO: 3 по SEQ ID NO: 225 или любой из последовательностей с SEQ ID NO: 226 по SEQ ID NO: 251, или любой из последовательностей с SEQ ID NO: 252 по SEQ ID NO: 274. [2] (См. патент РФ на изобретение №2415150
«Полипептиды, обладающие антимикробной активностью, и полинуклеотиды, кодирующие их», опубл. 2011 г)
Из уровня техники известен также синтетический полипептид с антибактериальной активностью следующей формулы: U=XN, где XN- Ser или любой из остатков аминокислот Glu, Thr, Arg, Pro, Val, Leu, Asn; Arg; Leu; Phe; Lys; Ile; Gln; Gly; Ser; Ala в различных сочетаниях, где N достигает значений до 41, например пептид SE-41, являющийся ретропоследовательностью С-концевой части белка САР 18, обладающий антимикробной активностью и имеющий следующий аминокислотный состав SEQ ID NO: 1: SETRPVLNRLFDKIRQVIRKFEKGIKEKSKRFFDGLLAFRK, а также фрагменты пептида SE-41, имеющие в своем составе от 16 до 40 аминокислот. Лекарственный препарат для профилактики или лечения бактериальной инфекции человека, включает вышеуказанный полипептид, один или несколько фармацевтически приемлемых носителей, вспомогательных веществ или дополнительных противобактериальных средств. [3] (См. патент РФ на изобретение №2434880 С2 «Полипептид, имеющий антибактериальную активность и пригодный для получения лекарственных средств для лечения бактериальных инфекций человека», опубл. 2011 г.)
Известна также противогрибковая композиция на основе противомикробных пептидов, содержащих аргинин- и лизинсодержащий мотив общей формулы (I): ((X)I(Y)m)n, где пептид содержит от 3 до 200 аминокислот и где 1, m и п представляют собой целые числа от 0 до 10; X и Y, которые могут быть одинаковыми или разными и представляют собой катионные аминокислоты, выбранные из аргинина и лизина, в изготовлении
лекарственных средств для лечения грибковой инфекции. Композиция содержит фармацевтически эффективное количество одного или более пептидов или их фармацевтически приемлемых солей и фармацевтически приемлемый носитель, эксципиент или разбавитель, где эксципиент или разбавитель выбран из группы кислот: уксусной, лимонной, борной, молочной, пропионовой, фосфорной, бензойной, масляной, малоновой, яблочной, щавелевой, янтарной и винной или диметил сульфона, N-(2-меркаптопропионил) глицина, 2-н-нонил-1,3-диоксолана и этилового спирта. (См. патент РФ на изобретение №2396273 «Противомикробные пептиды, содержащие аргинин- и лизинсодержащий мотив», опубл. 2010 г.)
Из уровня техники известна также стоматологическая композиция для снижения или предотвращения роста бактериальных бляшек на зубной эмали, содержащая от примерно 100 мг до примерно 1000 мг молочного остеопонтина на 1 кг композиции. Способ предотвращения или ингибирования роста бактериальных бляшек на зубной эмали, включает введение в рот эффективного количества молочного остеопонтина. При этом стоматологическая композиция представляет собой зубной порошок, зубной гель, зубной эликсир, спрей для полости рта или жевательную резинку.[4] (См. патент РФ на изобретение №2385162 «Применение остеопонтина в стоматологических композициях», опубл. 2006 г.)
Известен также антибактериальный, антиоксидантный, детоксицирующий, иммуномодулирующий и антиканцерогенный препарат. Препарат содержит человеческий лактоферрин в качестве активного вещества и фармацевтически приемлемые добавки в соотношении лактоферрин/фармацевтически приемлемые добавки 10-90/90-10 и при содержании действующего вещества в лекарственных средствах от 0,01 до 1,0%. Лекарственные средства, содержащие препарат и фармацевтически приемлемые носители представляют собой растворы для внутривенного введения, для внутриполостного или внутрипузырного введения, для перорального введения, для обработки раневых поверхностей, для интраназального применения или в форме глазных капель, мази, болюсы для перорального применения, суппозитории для ректального или интравагинального применения, таблетки. [5] (См. патент РФ на изобретение №2165769 «антибактериальный, антриоксидантный, иммунномодулирующий и антиканцерогенный препарат и способ его применения», опубл. 2001 г).
Наиболее близким техническим решением к заявляемому антимикробному средству является антимикробное средство «гигиенический ополаскиватель «Неолактоферрин-дента» для ополаскивания полости рта, представляющий собой водный раствор ЛФ (комплекс белков ЛФ человека (90%) и ЛФ козы (10%) - получен из молока коз-продуцентов). (См. Бабина К.С. «Оценка влияния гигиенического ополаскивателя «Неолактоферрин-дента» на формирование и рост биопленки. // Материалы X международной научно-практической конференции «Современные достижения в науке», том 2, Прага, 2014, с. 65-72.)
Указанное средство, как это и следует из названия, предназначено и используют для снижения или предотвращения роста бактериальных бляшек на зубной эмали. Компоненты средства взяты в следующих соотношениях (мас): ЛФ 0,1 г/вода 100 г(мл).
Недостатки данного средства обусловлены необходимостью постоянного использования этого гигиенического средства.
Постановка задачи и раскрытие изобретения
Техническим результатом, на достижение которого направлено заявляемое изобретение, является повышение антибактериальной активности, а также увеличение ассортимента средств для лечения бактериального вагиноза и грибковых инфекций за счет расширения диапазона лечебного воздействия.
Указанный технический результат достигается тем, что антимикробное средство, содержащее лактоферрин дополнительно содержит моно[(2-диметиламино)этиловые] эфиры карбоновых кислот общей формулы R-О-(Et)-N(Me)2, где R-карбоновая кислота, выбранная из ряда: фумаровая, янтарная, малеиновая, α-кетоглутаровая, щавелевая, D,L-яблочная, пировиноградная, Et - этил и Me - метил, при этом соотношение(мас.) лактоферрин/эфиры карбоновых кислот составляет от 1/1 до 1/3. В заявляемом изобретении под лактоферрином (ЛФ) понимаются лактоферрины различного происхождения: ЛФ из молока коз-продуцентов - неолактоферрин, представляющий собой комплекс белков ЛФ человека (90%) и ЛФ козы (10%), ЛФ из коровьего молока и др.
Антимикробное средство может дополнительно содержать фармацевтически приемлемые добавки, а также бионейтральные компоненты, в качестве которых используют носители, загустители, антиоксиданты, количественное содержание которых в композиции определяется лекарственной формой и способом применения средства.
Лекарственная форма заявляемого антимикробного средства может быть выполнена в виде жидкого раствора, таблетки или пленки, для буккального применения, в виде жевательной резинки или в виде суппозитория для ректального или вагинального введения.
Содержание активного вещества в заявляемом антимикробном средстве может составлять 0,01-1,0% мас. Оптимальное содержание составляет 0,05-0,15% мае, или 0,5-1,5 мг/мл или мг/г. В суппозитории для одноразового ректального или вагинального введения содержание активного вещества может составлять 5,0-10,0 мг/г в дозе 10-30 мг.
В качестве эфиров оксокислот используют моно[(2-диметиламино)этиловые] эфиры фумаровой, янтарной, малеиновой, α-кетоглутаровой, щавелевой, D- или L-яблочной или пировиноградной кислоты. При этом указанные эфиры могут быть использованы порознь или в различных сочетаниях (смеси). Заявляемые эфиры могут быть получены (произведены) различными путями, например взаимодействием ангидридов вышеупомянутых кислот с 2-диметиламиноэтанолом. Авторы подтверждают это примером синтеза моно[(2-диметиламино)этилового] эфира янтарной кислоты: взаимодействием янтарного ангидрида с 2-диметиламиноэтанолом в ацетоне.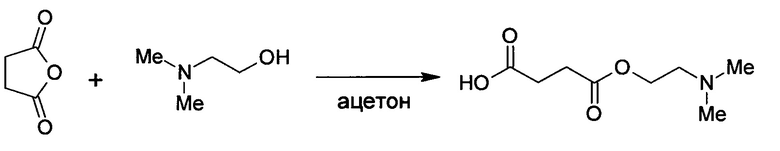
К раствору 10 г (0,1 М) янтарного ангидрида в 100 мл сухого ацетона добавляют 10 г (0,11 М) 2-диметиламиноэтанола. Смесь кипятят 1 час с обратным холодильником, отфильтровывают нерастворимый осадок, упаривают и охлаждают фильтрат. Выпавшие бесцветные кристаллы рекристаллизуют из ацетона. Выход 90%, Т. пл. 74-75°С. [1Н ЯМР (500 МГц, ДМСО-d6): 2.19 (с, 6Н), 2.41-2.53 (м, 6Н), 4.09 (т, j=5.6 Гц, 2Н), 4.5 (шс). 13С ЯМР (125 МГц, ДМСО-d6): 28.77, 28.81, 44.97, 56.85, 61.54, 172.03, 173.38.]
Авторы обнаружили неожиданный эффект. При добавлении в водный раствор ЛФ моно[(2-диметиламино)этиловых] эфиров карбоновых кислот в количестве от 1 до 3 масс от массы ЛФ установлено резкое возрастание бактерицидного эффекта против кишечной палочки, бацилл, сальмонелл, стрептококков, стафилококков, а также широкого круга специфических возбудителей (патогенных микроорганизмов, таких как, например, Staphylococcus aureus, Lactobacillus spp., Leuconostoc spp., и, дрожжевых грибков, например, Candida albicans.
Также следует отметить, что вышеуказанные производные оксокислот могут быть использованы порознь или в различных сочетаниях в виде смесей двух или более различных соединений рассматриваемого класса.
Характерной особенностью заявляемых эфиров является то, что они распадаются на вещества, представляющие собой метаболиты, экскретируемые из организма человека. Соответственно, и, следовательно, при употреблении заявляемых веществ вовнутрь они при распаде полностью и безопасно удаляются из организма. Признаки, приведенные в настоящем описании изобретения и в пунктах формулы изобретения, являются материалом для реализации настоящего изобретения в различных его формах, как отдельно, так и в любой их комбинации.
Технических решений, совпадающих с совокупностью существенных признаков заявляемого изобретения, не выявлено, что позволяет сделать вывод о соответствии заявляемого изобретения такому условию патентоспособности, как «новизна».
Заявляемые существенные признаки, предопределяющие получение указанного технического результата, явным образом не следуют из уровня техники, что позволяет сделать вывод о соответствии заявляемого изобретения такому условию патентоспособности, как «изобретательский уровень».
Условие патентоспособности «промышленная применимость» подтверждено на примерах конкретного применения.
Заявляемое изобретение может быть проиллюстрировано, но не исчерпано следующими примерами его конкретного осуществления.
Пример 1.
Методика определения влияния заявляемого антимикробного средства на формирование и рост биопленки позаимствована и результаты сопоставлены с результатами, опубликованными в
(Бабина К.С.Оценка влияния гигиенического ополаскивателя «Неолактоферрин-дента» на формирование и рост биопленки. // Материалы X международной научно-практической конференции «Современные достижения в науке», том 2, Прага, 2014, с. 65-72.) (в Таблицах ПР-1).
Примечание: При исследовании эффективности заявляемого средства в профилактике и
лечении стоматологических заболеваний оценку гигиенического состояния ротовой полости осуществляют по индексу Quigley-Hein в модификации Turesky (S. Tureskyetal., 1970), согласно которому по категориям:
- 0 категория - когда не выявлен зубной налет;
- 1 категория - зубной налет присутствует частично;
- 2 категория - присутствует бляшка у края десны;
- 3 категория - окрашивается треть поверхности коронки зуба;
- 4 категория - окрашивается две трети поверхности коронки зуба;
- 5 категория - окрашивается вся поверхность коронки зуба.
Готовят 3 образца ополаскивателя зубов: водный раствор моно[(2-диметиламино)этилового] эфира малеиновой кислоты (I) с концентрацией 0,1% мае, водный раствор неолактоферрина (НЛФ) с концентрацией 0,1% мас. (М) и водный раствор смеси равных количеств НЛФ и моно[(2-диметиламино)этилового] эфира малеиновой кислоты (III) с общей концентрацией 0,1%. Добровольцев-участников исследования (60 чел. без различия пола)разделяют по случайному признаку на 5 равных групп (дизайн исследования «splitmouth»):
1-я группа: чистка 2 и 3 квадрантов (левая верхняя и нижняя половины челюстей) зубной пастой, 1 и 4 квадранты (правая верхняя и нижняя половины челюстей) - не очищать в течение 3 дней;
2 группа: не использовать зубную пасту в течение 3 дней, а применять аппликации ополаскивателя (I) на 1 и 4 квадрантах;
3 группа: в течение 3-х дней очищать 2 и 3 квадранты зубной пастой, на 1 и 4 квадрантах - применять аппликации раствора ополаскивателя (I);
4 группа: не использовать зубную пасту в течение 3 дней, на 1 и 4 квадрантах применять ватные валики, смоченные водой;
5 группа: очищать 2 и 3 квадранты зубной пастой, на 1 и 4квадрантах -применять ватные валики, смоченные водой.
Соответственно ополаскиватели (II) и (III) испытывали аналогичным образом. Результаты испытаний представлены в Таблице 1
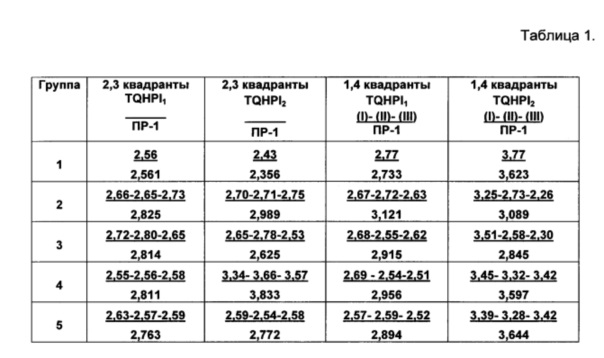
Среднее отклонение в пределах ~ 0,12
Пример 2
Влияние ополаскивателя на основе заявляемого антимикробного средства на формирование и рост биопленки определяют как в Примере 1, за исключением того, что в качестве ЛФ используют ЛФ из грудного молока и в качестве эфира - моно[(2-диметиламино)этиловый] эфир фумаровой кислоты. Готовят 3 образца ополаскивателя: водный раствор моно[(2-диметиламино)этилового] эфира фумаровой кислоты (IV) с концентрацией 0,1% мае, водный раствор ЛФ из грудного молока с концентрацией 0,1% мае. (V) и водный раствор смеси равных количеств ЛФ из грудного молока и моно[(2-диметиламино)этилового] эфира фумаровой кислоты (VI) с концентрацией 0,1%.
Результаты испытаний представлены в Таблице 2.
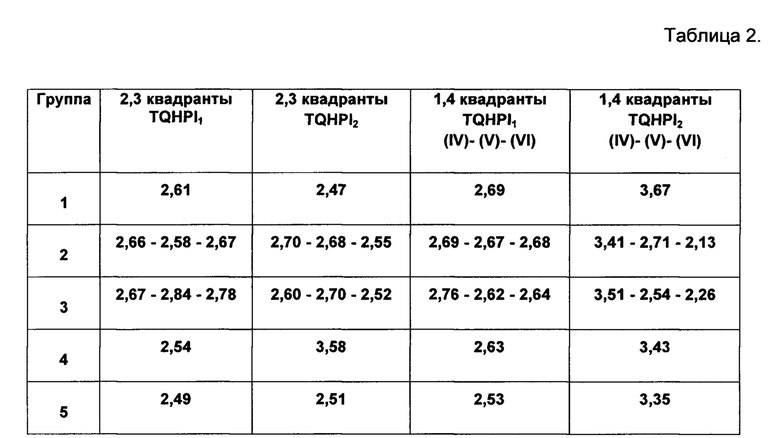
Среднее отклонение в пределах ~ 0,1
Пример 3
Влияние ополаскивателя на основе заявляемого антимикробного средства на формирование и рост биопленки определяют как в Примере 1, за исключением того, что готовят 3 образца ополаскивателя: водный раствор смеси моно[(2-диметиламино)этилового] эфира фумаровой кислоты и моно[(2-диметиламино)этилового] эфира янтарной кислоты в
соотношении 1/1 (VII) с концентрацией 0,1% мае, водный раствор рекомбинантного ЛФ концентрацией 0,1% мае. (VIII) и водный раствор смеси равных количеств рекомбинантного ЛФ и смеси моно[(2-диметиламино)этилового] эфира фумаровой кислоты и моно[(2-диметиламино)этилового] эфира янтарной кислоты в соотношении 1/1 (IX) с концентрацией 0,1%. Результаты испытаний представлены в Таблице 3.
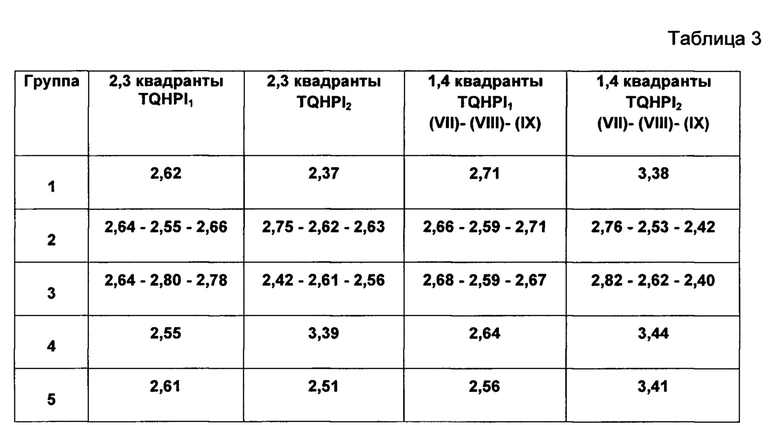
Среднее отклонение в пределах ~ 0,1
Пример 4.
Оценку заметного антимикробного действия заявляемого средства проводят как в Примере1, за исключением того, что испытуемых разделяют на две равные группы по 12 чел., из которых 1 группа не использует зубную пасту в течение 3 дней, а применяет аппликации ополаскивателя на 1 и 4 квадрантах; 2-я группа в течение 3-х дней очищает 2 и 3 квадранты зубной пастой и на 1 и 4 квадрантах - применяет аппликации раствора ополаскивателя. При этом средство готовят в виде водного раствора с соотношением (мас.): ЛФ/эфир 1/1,5 при концентрациях водного раствора средства (% мас.): 0,01 - 0,025 - 0,05-0,075 - 0,1 - 0,15 - 0,2 и 0,25. Результаты испытаний представлены в Таблице 4.
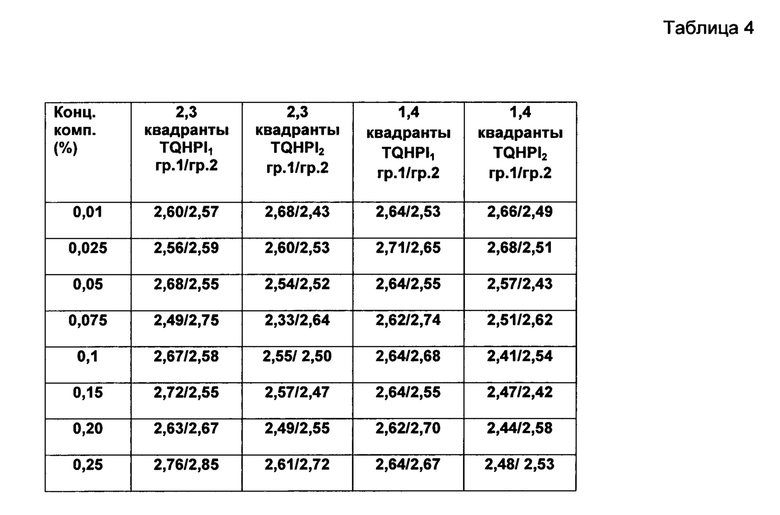
Из Таблицы 4 следует, что антимикробное действие заявляемого средства заметно проявляется при концентрации 0,05 %, достигает максимума при концентрации 0,15% и при дальнейшем увеличении концентрации (до 0,20 или 0,25% мае.) остается практически неизменным. Пример 5.
Оценка общего антимикробного действия композиции.
Примечание Оценку общего антимикробного действия заявляемого антимикробного средства осуществляют при помощи классического бактериологического метода. При определении степени воздействия заявляемого антимикробного средства на микроорганизмы, культивирование последних осуществляют в соответствии с ГОСТ 26670-91 - «Методы культивирования микроорганизмов», а отбор и подготовку проб в соответствии с ГОСТ 26668-85 и ГОСТ 26669-85. При посевах тестовой культуры микроорганизмов используют глубинный метод посева в плотные среды (вкол), поверхностный посев в плотные среды, а также посев в жидкие среды. В настоящем изобретении в качестве питательных сред используют официально зарегистрированные и разрешенные к использованию питательные среды, которые разработаны, зарегистрированы по РУ ФСР и произведены Федеральным государственным учреждением науки «Государственный научный центр прикладной микробиологии и биотехнологии Федеральной Службы по надзору в сфере защиты прав потребителя и благополучия человека».
Подготовка образцов
Готовят водные растворы ЛФ + эфиры оксикислот концентрации 0,05 и 0,1% мас. При этом эфиры оксикислот используют порознь или в виде смеси в различных сочетаниях. В качестве ЛФ используют рекомбинантный человеческий лактоферрин (РЛФ) и неолактоферрин (НЛФ).Получают 3 образца антимикробного средства в виде растворов определенного состава и концентрации (см. Таблицу 5).
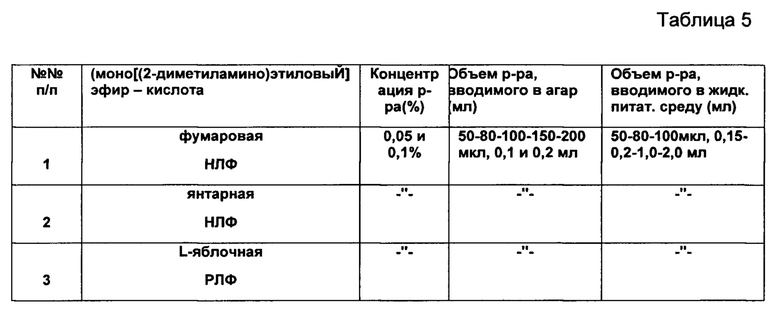
Посев тест-штаммов на агар в чашках Петри (чашки диаметром 100 мм, выстой 15 мм, ГОСТ 25336-82) ведут поверхностным способом (0,15 мл) и глубинным способом - вкол в агар (1,0 мл). Степень разведения продуктов для посева выдерживают в соответствии с ГОСТ 26670-91 как для бактерий, так и для плесеней и грибков.
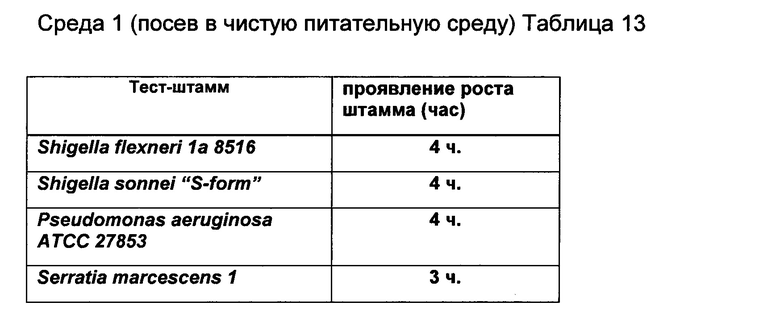
В качестве среды для культивирования энтеробактерий, псевдомонад, стафилококков используют «АгарХоттингера», для которого тест-штаммами являются Shigella flexneri 1а 8516, Shigella sonnei "S-form", Pseudomonas aeruginosa ATCC 27853, Serratia marcescens 1. (Среда 1).
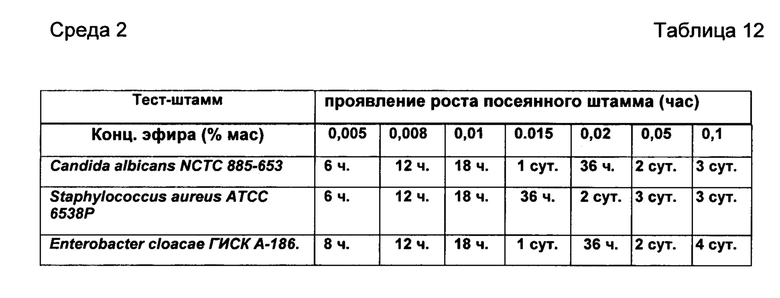
В качестве среды для культивирования дрожжеподобных и плесневых грибов используют «агар «САБУРО-МАЛЬТОЗА», для которого тест-штаммами являются Candida albicans NCTC 885-653, Staphylococcus aureus АТСС 6538P, Enterobacter cloacae ГИСКА-186. (РУ № ФСР 2009/05625).
Посев тест-штаммов на агар в чашках Петри ведут поверхностным способом (0,15 мл). (Среда 2).
В качестве среды для первичной идентификации энтеробактерий используют среду «РЕССЕЛЯ-ГРМ» для которой тест-штаммами являются Shigella flexneri 1а 8516, Salmonella paratifi А-225, Alcaligenesfaecalis 415, Escherichiacoli 339 (055:K 59).(РУ № ФСР 2008/02818). Посев тест-штаммов ведут в жидкую среду - до 50 мл. (Среда 3).
В процессе приготовления питательных сред в них вводят раствор заявляемого антимикробного средства (Таблица 5) в количестве 0,005 - 0,008 - 0,01 - 0,015 - 0,02 - 0,05 - 0,1% по отношению к массе агара (в пересчете объемов на концентрацию средства в агаре или жидкости). При посеве в жидкую среду раствор композиции вводят в том же количестве.
Для каждой питательной среды готовят контрольные образцы с посевами тест-штаммов с ЛФ и с эфиром, которые вводят в количестве 0,005 - 0,008 - 0,01 - 0,015 - 0,02 - 0,05 - 0,1% (в пересчете объемов на концентрацию композиции в агаре или жидкости) по отношению к массе агара.
Одновременно, для каждой питательной среды готовят контрольные образцы с посевами тест-штаммов без ЛФ и эфиров.
Далее готовые образцы с посевами тест-штаммов - чашки Петри (плотная среда) и пробирки (стекло, объем 150 мл) - жидкая среда, помещают в термостат, в котором поддерживают следующие параметры: 38°С, аэробная среда, 7 суток. Обсемененность образцов микроорганизмами осуществляют путем подсчета числа колоний, выросших в чашке Петри, в жидких средах - путем определения изменения цвета (окраски) среды. Контроль роста микроорганизмов осуществляют в следующей последовательности: через 1, 3, 6 и 12 часов первых суток, и далее каждые 6 часов последующих суток. Результаты тестов представлены в Таблицах 6, 7 и 8.
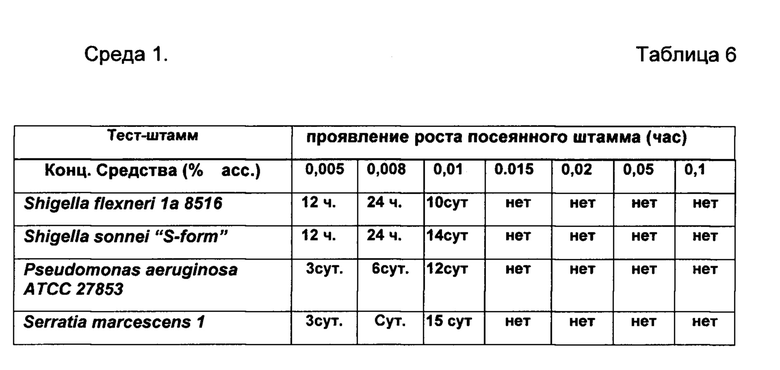
Примечание: выдержку в термостате продлили до 21 сут.
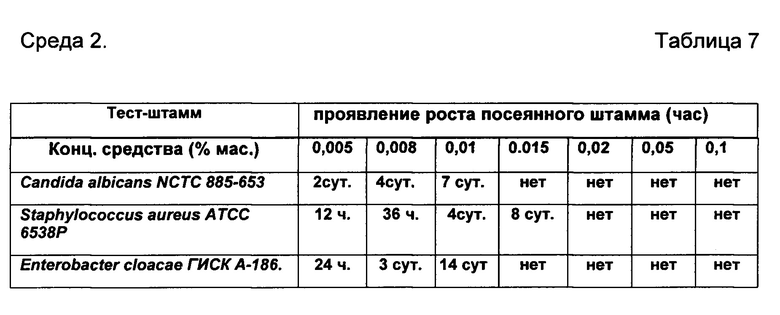
Примечание: выдержку в термостате продлили до 21 сут.
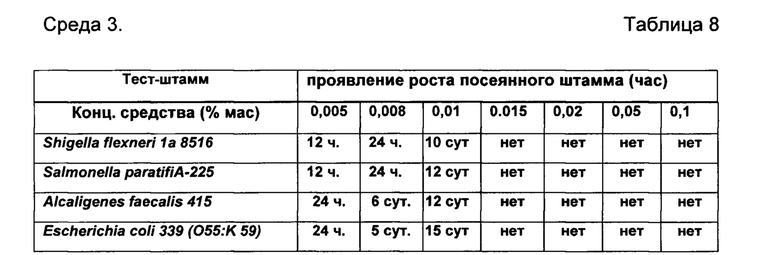
Примечание: выдержку в термостате продлили до 21 сут.
Результаты сравнительных и контрольных посевов в питательную среду 1 и среду 2(ЛФ и эфиры по отдельности) и посев в чистую питательную среду представлены в Таблицах 9-14 соответственно.
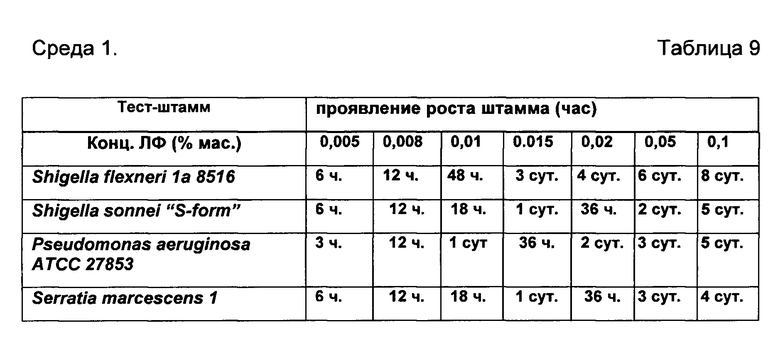
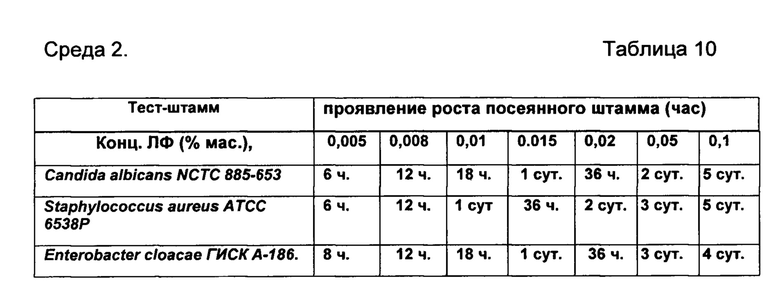
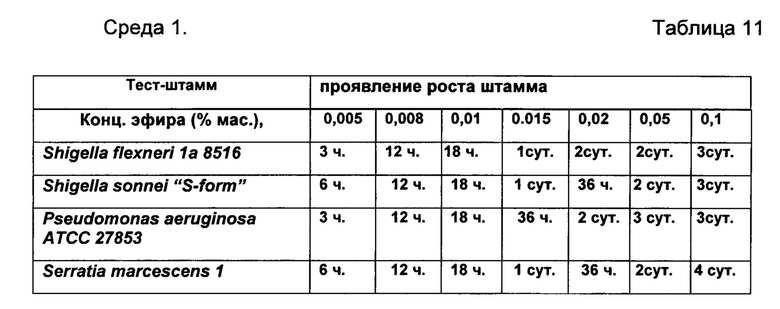

Пример 6.
Оценка фунгицидного воздействия заявляемого антимикробного средства.
Пациентка М*, 36 лет, жалобы на дискомфортное состояние слизистой вагины. Посев мазка поверхностным способом на «агар«САБУРО-МАЛЬТОЗА» показал наличие грибка Candida albicans.
Готовят суппозитории (вагинальные капсулы) на основе витепсола Х-19 и антимикробного средства состава (мае): РЛФ/ моно[(2-диметиламино)этиловый] эфир фумаровой кислоты - 2/5 при общем содержании композиции в суппозитории 30 мг, масса суппозитория ~4,0 г. Применяют капсулы по схеме 1 капсула ежевечерне. Побочных явлений не наблюдается. Контрольные мазки берут каждое утро. Результаты представлены в Таблице 15.

Для сравнения: рекомендуемые процедуры лечения проблем слизистой вагины
(молочница) - вагинальные таблетки Неотризол (состав: миконазол, неомицин, орнидазол, преднизолон) по 1 табл.1 раз в сутки на ночь 8-16 дней или Флуконазол по 150 мг внутрь на 1, 4, 7 день, далее по 1 капсуле в неделю в течение 6 мес.Отмечено, что указанные средства могут и вызывают крапивницу, сыпь, эритему, жжение, зуд, местное раздражение. (Взято из Интернета - ru.wikipedia.org/wiki/Кандидоз) Пример 7.
Оценка лечебного воздействия заявляемого антимикробного средства при стоматологических заболеваниях.
Пациент Ф**, 41 год, жалоба на боль десен, воспаление десен. Осмотр полости рта подтвердил наличие воспаления десен. Диагноз - гингивит. Предложено лечение - жевательная резинка (состав НЛФ/моно[(2-диметиламино)этиловый] эфир пировиноградной кислоты - 1/3 при общем содержании средства в жевательной резинке 25 мг, масса пластинки резинки - 2,5 г. Состав 30% мас. натурального каучука, 50% ксилита (Е967), 19,5% кленового сиропа и 0,5% ароматизатора (лимонен). Схема применения: 1 резинка утром и 1 вечером. Ежедневный контроль состояния полости рта установил: на четвертый день отек краевой части десны и межзубных сосочков исчез, на пятый день воспаления не наблюдалось, болевые ощущения отсутствовали.
Для сравнения: Лечение гингивита - полоскания 0,05% раствором хлоргексидина аппликации «Холисал-гелем» Курс лечения составляет 10 дней; обработка десен проводится 2 раза в день - утром и на ночь перед сном.(взято из Интернета 24stoma.ru)
Пример 8.
Оценка лечебного воздействия заявляемой антимикробной композиции при стоматологических заболеваниях (формирование и рост биопленки на зубах - профилактика и лечение).
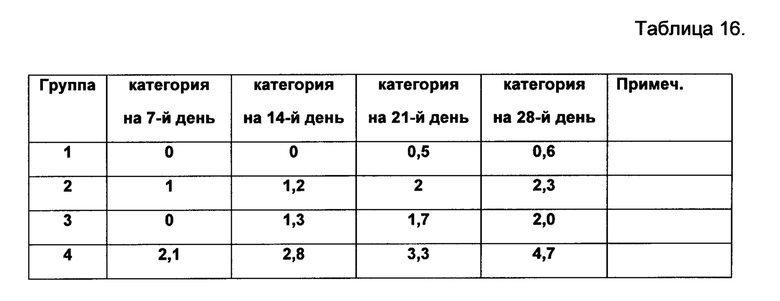
Готовят лечебную водорастворимую пленку-подложку (пластырь) для буккального применения в полости рта. Основа пластыря - поливинилпирролидон, лечебное вещество (композиция) - РЛФ/моно[(2-диметиламино)этиловый] эфир фумаровой кислоты 2/5 при общем содержании средства в пластыре 12-15 мг, масса пластыря ~1,0 г, габариты - 7X35 мм, толщина 2 мм. Пленка растворяется в воде при Т=36-37°С в течение ~3,5-4,0 ч. Применение: пластырь наклеивают на зубы правой и левой стороны со стороны щек верхней челюсти перед сном. Определяют формирование и рост биопленки на зубах как результат профилактики и лечения. (См. Пример 1) Исследуют четыре группы пациентов по 10 чел. Подготовка пациентов: ультразвуковая очистка зубов от налета и отложений, полировка зубов.
Первая группа - ежедневная чистка зубов пастой и применение пластыря (ежедневно течение 4 дней, далее на каждый третий день) по вышеприведенной схеме.
Вторая группа - ежедневная чистка зубов пастой без применения пластыря.
Третья группа - применение пластыря (ежедневно течение 4 дней, далее на каждый третий день) по вышеприведенной схеме без чистки зубов пастой.
Четвертая группа - зубы без ухода: ни чистки зубов пастой, ни применения пластыря.
Результаты представлены в Таблице 16.
Таким образом, анализ конкретных примеров использования антимикробного средства по заявляемому техническому решению, а также сопоставление результатов тестов с таковыми у известных технических решений, позволяет утверждать, что заявляемое антимикробное средство обладает высокими антисептическими свойствами в отношении подавляющего большинства грамположительных и грамотрицательных бактерий, фунгицидными свойствами в отношении грибов и обеспечивает эффективную профилактику и лечение заболеваний слизистой оболочки рта и других стоматологических заболеваний. Также заявляемое антимикробное средство является достаточно доступным по экономическим соображениям.
Источники информации, принятые во внимание при составлении заявки.
1. И.М. Макеева, Т.Н. Смирнова и др.: Применение лактоферринов в комплексном лечении стоматологических заболеваний (Обзор литературы). Стоматология, т. 91, 4'2012, с. 66-71.
2. Патент РФ на изобретение №2415150, опубл. 2011 г
3. Патент РФ на изобретение №2434880 С2, опубл. 2011 г.
4 Патент РФ на изобретение №2385162, опубл. 2006 г.
5. Патент РФ на изобретение №2165769, опубл. 2001 г.
6. Патент РФ на изобретение №2396273, опубл. 2010 г.
7. Патент РФ на изобретение №2579661, опубл. 2015 г.
8. Бабина К.С. «Оценка влияния гигиенического ополаскивателя «Неолактоферрин-дента» на формирование и рост биопленки. // Материалы X международной научно-практической конференции «Современные достижения в науке», том 2, Прага, 2014, с. 65-72 - прототип.
9. Взято из Интернета - ru.wikipedia.org/wiki/Кандидоз.
10. Взято из Интернета 24stoma.ru.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОПОЛАСКИВАТЕЛЬ ДЛЯ ПОЛОСТИ РТА | 2006 |
|
RU2312657C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ОЧИСТКИ | 2009 |
|
RU2441641C1 |
| АНТИМИКРОБНЫЕ КОМПОЗИЦИИ | 2013 |
|
RU2694758C2 |
| Композиция активной стоматологической основы для средств по уходу за ротовой полостью, стимулирующая восстановительные и репаративные процессы в тканях полости рта, и композиция для гигиены ротовой полости на ее основе (варианты) | 2023 |
|
RU2822421C1 |
| КОМПОЗИЦИИ ДЛЯ УХОДА ЗА ПОЛОСТЬЮ РТА, СОДЕРЖАЩИЕ ЧЕТВЕРТИЧНЫЕ АММОНИЕВЫЕ АНТИМИКРОБНЫЕ РЕАГЕНТЫ С ПОВЫШЕННЫМИ УРОВНЯМИ БИОЛОГИЧЕСКОЙ ДОСТУПНОСТИ | 2005 |
|
RU2325899C2 |
| Фитокомпозиция для гигиены полости рта | 2016 |
|
RU2635509C1 |
| Эмульсии для полоскания полости рта | 2013 |
|
RU2648461C2 |
| ПРОДУКТ ДЛЯ УХОДА ЗА ПОЛОСТЬЮ РТА И СПОСОБЫ ЕГО ПРИМЕНЕНИЯ И ИЗГОТОВЛЕНИЯ | 2010 |
|
RU2597159C2 |
| ИНГИБИРОВАНИЕ ОРГАНИЗМОВ БИОПЛЕНКИ | 2010 |
|
RU2548786C2 |
| Детская присыпка на основе лактоферрина | 2020 |
|
RU2743558C1 |
Изобретение относится к области медицины и предназначено для ингибирования и/или предотвращения роста микробиопленок. Антимикробное средство содержит лактоферрин, фармацевтически приемлемые добавки и моно[(2-диметиламино)этиловые] эфиры карбоновых кислот общей формулы R-О-(Et)-N(Me)2, где R - карбоновая кислота, выбранная из ряда: фумаровая, янтарная, малеиновая, α-кетоглутаровая, щавелевая, D,L-яблочная, пировиноградная, Et - этил и Me – метил. При этом соотношение (мас.) лактоферрин/эфиры карбоновых кислот составляет от 1/1 до 1/3. Использование изобретения позволяет повысить антисептические свойства в отношении подавляющего большинства грамположительных и грамотрицательных бактерий, фунгицидные свойства в отношении грибков, а также обеспечивает эффективную профилактику и лечение состояний слизистых оболочек и стоматологических заболеваний. 1 з.п. ф-лы, 16 табл., 8 пр.
1. Антимикробное средство на основе лактоферрина и фармацевтически приемлемых добавок и/или носителей, отличающееся тем, что оно дополнительно содержит моно[(2-диметиламино)этиловые] эфиры карбоновых кислот общей формулы R-О-(Et)-N(Me)2, где R - карбоновая кислота, выбранная из ряда: фумаровая, янтарная, малеиновая, α-кетоглутаровая, щавелевая, D,L-яблочная, пировиноградная, Et - этил и Me - метил, при этом соотношение (мас.) лактоферрин/эфиры карбоновых кислот составляет от 1/1 до 1/3.
2. Антимикробное средство по п. 1, отличающееся тем, что в качестве фармацевтически приемлемых носителей она содержит водорастворимые полимеры или растворители, или натуральный или синтетический каучук, или загустители.
| БАБИНА К.С | |||
| Оценка влияния гигиенического ополаскивателя "Неолактоферрин-дента" на формирование и рост биопленки | |||
| Материалы X международной научно-практической конференции "Современные достижения в науке", Прага, 2004, том 2, с | |||
| Разборное приспособление для накатки на рельсы сошедших с них колес подвижного состава | 1920 |
|
SU65A1 |
| СПОСОБ КОНСЕРВАЦИИ ПИЩЕВЫХ ПРОДУКТОВ | 2015 |
|
RU2631903C2 |
| 2000 |
|
RU2165769C1 | |
| CN 107496971 A, 22.12.2017 | |||
| МАКЕЕВА И.М | |||
| и др | |||
| Применение лактоферрина в комплексном лечении стоматологических заболеваний | |||
| Стоматология, 2012, т.91, no.4, с.66-71. | |||
Авторы
Даты
2019-05-17—Публикация
2018-03-02—Подача