Изобретение относится к области медицины, онкологии, к способам прогнозирования сроков ответа на андроген-депривационную терапию у больных раком предстательной железы и может быть использовано для определения тактики лечения пациентов с данной нозологией.
Рак предстательной железы (РПЖ) является одной из актуальных проблем современной онкологии. Это обусловлено высокими показателями прироста заболеваемости и отсутствием персонифицированных подходов к лечению, а соответственно, его недостаточной эффективностью. Согласно современным рекомендациям, андроген-депривационная терапия (АДТ) является стандартом в лечении пациентов с местно - распространенным и метастатическим РПЖ. Ответ опухоли на проводимую терапию регистрируется более чем у 90% пациентов. Однако длительность ответа при этом, составляет в среднем 12-36 мес, в дальнейшем наблюдается прогрессирование заболевания с развитием кастрационно-резистентной формы [1, 2].
На сегодняшний день рак предстательной железы представляет собой опухоль, использующую для своего развития различные механизмы. Андрогензависимый путь для данной патологии реализуется посредством активации андрогеновых рецепторов (AR) [3, 4], под воздействием дегидротестостерона и образующийся комплекс транслоцируется в ядро, взаимодействуя с ключевыми транскрипционными факторами и ДНК.
При андрогеннезависимом раке, в большей мере принимают участие ростовые и транскрипционные факторы [5]. Известно, что в ацинарных структурах нормальной ткани предстательной железы рецепторный статус характеризуется высоким содержанием AR и низким эстрогеновых рецепторов (ER). При развитии опухолевого процесса отмечается значимое увеличение экспрессии ER вместе с AR. Показано, что в процессах перехода простатической интраэпителиальной неоплазии в рак играют важную роль ERα и ERβ [6]. В настоящее время существует представление о наличии тонких взаимосвязей между AR и ER, что, в значительной мере, определяет развитие и прогрессирование РПЖ [7]. Считается, что ERα способны активировать пролиферацию опухолевых клеток при наличии мутации фосфатазы PTEN [8], стимулируя сигнальные пути AKT/m-TOR, МАРК. ERβ чаще рассматривается в качестве онкосупрессора [9, 10]. Таким образом, именно молекулярные характеристики опухоли и определяют ее биологическое поведение, ответ на терапию и исход заболевания.
В настоящее время предпринимаются попытки прогнозировать риск прогрессировала рака предстательной железы на фоне андроген-депривационной терапии.
Наиболее близким к заявляемому способу является метод прогнозирования развития ответа на андроген-депривационную терапию на основании анализа полиморфных вариантов гена HSD3B1 (1245А>С) в крови, который кодирует изоформу фермента, увеличивающего синтез дигидротестостерона из негонадных предшественников. Аллель HSD3B1 (1245С) связан с развитием резистентности к андроген-депривационной терапии (АДТ) у больных раком предстательной железы [11].
Данный подход позволяет предполагать ожидаемый ответ на лечение и выделить пациентов, у которых возможно развитие ранней резистентности к АДТ. Однако исследование генетического полиморфизма HSD3B1 (1245А>С) не отражает биологические характеристики опухоли, так как свидетельствует только о риске развития резистентности к проводимому лечению. Также данный способ не позволяет прогнозировать продолжительность ответа на АДТ.
В связи с этим необходимо решение новой технической задачи, направленной на повышение информативности предсказания ожидаемого риска раннего прогрессирования рака предстательной железы на фоне АДТ. Для этого целесообразно исследовать показатели, характеризующие молекулярные особенности опухоли.
Новый технический результат - повышение точности и информативности способа. Для достижения нового технического результата в способе прогнозирования сроков ответа на андроген-депривационную терапию (АДТ) у больных раком предстательной железы (РПЖ), путем исследования ткани опухоли, определяют экспрессии AR, ERα а так же учитывают возраст пациента, уровнь тестостерона и простат-специфического антигена (ПСА) крови, рассчитывают значения дискриминантных функций Yl, Y2 по уравнениям: Y1=-33,37+1,0⋅Х1+0,01⋅Х2+0,01⋅Х3+1,08⋅Х4-0,0004 Х5 (раннее рецидивирование РПЖ с эффектом АДТ в течение 12 месяцев);
Y2=-59,27+1,75⋅Х1+0,03⋅Х2+0,23⋅Х3-4,02⋅Х4+0,007 Х5 (отсроченное рецидивирование РПЖ с эффектом АДТ более 12 месяцев);
где X1 - возраст пациента, годы;
Х2 - экспрессия AR в опухоли, УЕ;
Х3 - экспрессия ERα в опухоли, УЕ;
Х4 - содержание тестостерона в сыворотке крови, нмоль/л;
Х5 - содержание простат-специфического антигена (ПСА) в сыворотке крови, нг/мл;
и при Y1>Y2 - прогнозируют ответ на андроген-депривационную терапию в сроки менее 12 месяцев, а при Y1<Y2 в сроки более 12 месяцев от начала лечения.
Способ осуществляют следующим образом:
Для прогнозирования времени ответа на АДТ у пациентов с РПЖ выполняют следующие манипуляции: определяют уровень простат-специфического антигена (ПСА), тестостерона в сыворотке крови, в опухолевой ткани, полученной при выполнении диагностической биопсии, проводят определение экспрессии AR, ERα.
Для исследования экспрессии молекулярных показателей и выделения мРНК образцы тканей помещают в раствор RNAlater (Ambion, USA) и сохраняют при температуре -80°С (после 24-часовой инкубации при +4°С). РНК выделяют с помощью набора RNeasyminiKit, содержащего ДНК-азу I (Qiagen, Germany). Для оценки количества выделенной РНК на спектрофотометре NanoDrop-2000 (ThermoScientific, USA) оценивают концентрацию и чистоту выделения РНК. Концентрация РНК составляет от 80 до 250 нг/мкл, А260/А280=1.95-2.05; А260/А230=1.90-2.31. Целостность РНК оценивают при помощи капиллярного электрофореза на приборе TapeStation (AgilentTechnologies, USA) и набора R6K ScreenTape (AgilentTechnologies, USA). RIN составляет 5.6-7.8.
Уровень экспрессии генов оценивают при помощи количественной обратно-транскриптазной ПЦР в режиме реального времени (RT-qPCR) с использованием красителя SYBR Green на амплификаторе iCycler (Bio-Rad, USA). Для получения кДНК на матрице РНК проводят реакцию обратной транскрипции с помощью набора OTm-MuLV-RH (БиоЛабмикс, Россия) со случайными гексануклеотидными праймерами в соответствии с инструкцией к набору. ПЦР ставят в трех репликах в объеме 25 мкл, содержащем 12,5 МклБиоМастерHS-qPCRSYBRBlue (БиоЛабмикс, Россия), 300 нМ прямого и обратного праймеров и 50 нгкДНК. Двухшаговая программа амплификации включает 1 цикл - 94°С, 10 мин - предварительная денатурация; 40 циклов - 1 шаг 94°С, 10 сек и 2 шаг 20 сек - при температуре 60°С. Праймеры подбирают с использованием программы VectorNTI Advance 11.5 и базы данных NCBI (http://www.ncbi.nlm. nih.gov/nuccore) (таблица 2). В качестве референсного гена используют ген «домашнего хозяйства» фермента GAPDH (glyceraldehydes-3-phosphate dehydrogenase), и уровень экспрессии каждого целевого гена нормализуют по отношению к экспрессии GAPDH.
Определяют экспрессии AR, ERα, а так же учитывают возраст пациента, уровень тестостерона и простат-специфического антигена (ПСА) крови, рассчитывают значения дискриминантных функций Y1, Y2 по уравнениям:
Y1=-33,37+1,0⋅Х1+0,01⋅Х2+0,01⋅Х3+1,08⋅Х4-0,0004 Х5 (раннее рецидивирование РПЖ с эффектом АДТ в течение 12 месяцев);
Y2=-59,27+1,75⋅Х1+0,03⋅Х2+0,23⋅Х3-4,02⋅Х4+0,007 X5 (отсроченное рецидивирование РПЖ с эффектом АДТ более 12 месяцев);
где X1 - возраст пациента, годы;
Х2 - экспрессия AR в опухоли, УЕ;
Х3-экспрессия ERα в опухоли, УЕ;
Х4 - содержание тестостерона в сыворотке крови, нмоль/л;
Х5 - содержание простат-специфического антигена (ПСА) в сыворотке крови, нг/мл;
и при Y1>Y2 - прогнозируют ответ на андроген-депривационную терапию в сроки менее 12 месяцев, а при Y1<Y2 в сроки более 12 месяцев от начала лечения.
Способ основан на результатах анализа данных лабораторных и клинических исследований. Информативность отобранных критериев подтверждают наличием связи экспрессии рецепторов андрогенов, эстрогенов с эффектом на андроген-депривационную терапию.
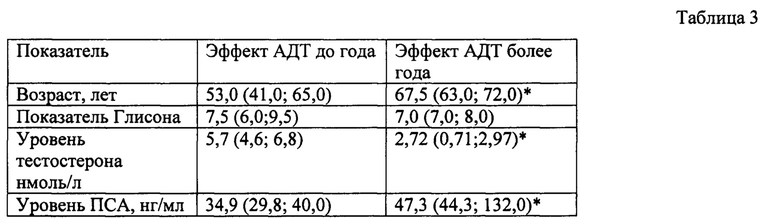
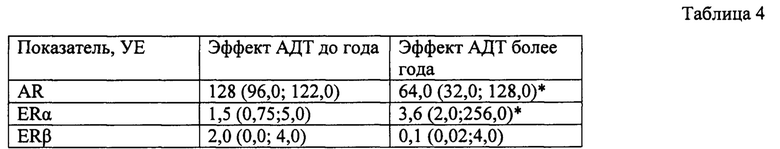
В исследование было включено 28 больных местно-распространенным и метастатическим раком предстательной железы. Всем пациентам было проведено комбинированное лечение, включающее в себя АДТ до достижения кастрационного уровня на тестостерона до 0,2 нмоль/л. В дальнейшем, при появлении у них признаков прогрессирования заболевания (рост ПСА более 4 нг/мл на фоне содержания тестостерона 0,2 нмоль/л) назначалась системная таксансодержащая полихимиотерапия. Основные клинико-морфологические параметры представлены в таблице 3. Отмечено, что пациенты в группах различались по возрасту, уровню тестостерона и содержанию ПСА. Так, больные с ответом на АДТ менее 12 месяцев и ранним рецидивированием были в 1,3 раза моложе, имели более высокий исходный уровень тестостерона (в 2 раза) и сниженное содержание ПСА (в 1,35 раза) по сравнению с больными, у которых наблюдался более длительный ответ на АДТ. При изучении молекулярных характеристик опухоли у пациентов с наличием эффекта на АДТ менее 12 месяцев выявлена высокая экспрессия AR и низкая экспрессия ERα (таблица 4).
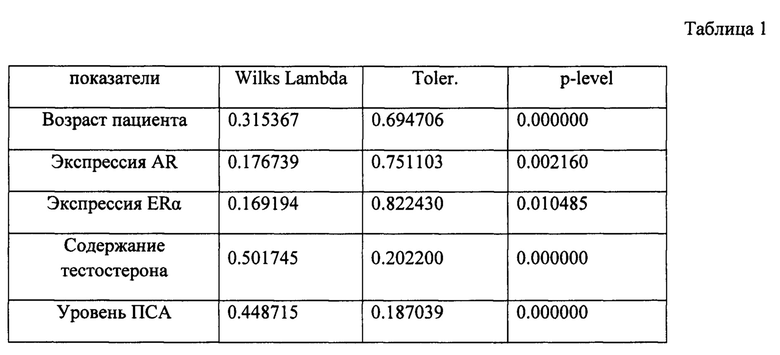
Информативность полученных функций оценивали у 12 пациентов, не включенных в основную выборку, у которых в ткани опухоли исследовали биологически активные молекулы с определением экспрессии AR, ERα и с учетом возраста пациента, уровня тестостерона, ПСА и рассчитывают значения дискриминантных функций Y1, Y2. При Y1>Y2 прогнозируют ответ на андроген-депривационную терапию в сроки менее 12 месяцев от начала лечения, а при Y1<Y2 - ответ на АДТ составит более 12 месяцев от начала лечения. (Таблица 1).Чувствительность и специфичность полученной дискриминантной модели по оценке продолжительности эффекта на АДТ и прогнозирования раннего рецидивирования составила, соответственно, 99,5% и 91,7%, диагностическая точность -95,6%.
Таким образом, выявлена совокупность параметров, позволяющая прогнозировать сроки рецидивирования заболевания больных РПЖ на фоне АДТ. Показано, что высокая экспрессия AR на фоне низкой экспрессии ERα свойственна для пациентов, у которых эффективность АДТ продолжалась менее 12 месяцев, что характеризуется развитием прогрессированием заболевания. Выявленные факты позволяют рассматривать эти параметры в качестве дополнительных информативных маркеров, позволяющих прогнозировать ожидаемые эффекты лечения. Клинические примеры:
Пример 1.
Больной К., 41 год, на фоне полного благополучия отметил дискомфорт в области промежности, эпизоды задержки мочеиспускания. Пациент обратился в НИИ онкологии г. Томска. При дообследовании выявлено повышение цифр ПСА крови до 44 нг/мл, по результатам остеосцинтиграфии (ОСГ) определялись множественные очаги деструкции костной ткани более вероятно метастатического характера. Данных за наличие висцеральных метастазов получено не было. Выполнена промежностная, мультифокальная биопсия предстательной железы под ТРУЗИ-контролем (взято по 6 фрагментов из каждой доли). Гистологическое исследование: в обеих долях предстательной железы определяется ацинарная аденокарцинома, Глисон 9 (4+5). Было проведено исследование опухолевой ткани, полученной при выполнении диагностической биопсии согласно предлагаемому способу с целью определения прогноза эффективности лечения РПЖ, результаты которого показали, что уровни экспрессии рецепторов AR и ERα: они составили 192 и 0,75 УЕ соответственно. При расчете дискриминантных функций выявлено, что Y1=14,5955 и Y2=-0,1211; Y1>Y2, что свидетельствует о возможном ранней резистентности к АДТ и рецидивирования рака предстательной железы, при котором ответ на лечение будет сохраняться не более 12 месяцев. Ответ опухоли на АДТ продолжался в течении 6 месяцев. Через 6 месяцев был отмечен рост ПСА крови на фоне проводимого лечения и кастрационных значений тестостерона. Прирост показателя фиксировался каждые 2 недели, среднее значение его составило 35,1 нг/мл. Таким образом, предлагаемый способ позволил с учетом признаков прогрессирования заболевания и формирования кастрационной резистентности своевременно перевести пациента через 6 месяцев на химиотерапию препаратами таксанового ряда.
Пример 2.
В НИИ онкологии г. Томска обратился пациент М, 60 лет с жалобами на боли в костях скелета, дискомфорт и болезненность в области промежности, эпизодическую задержку мочеиспускания. При дообследовании выявлено повышение цифр ПСА крови до 55 нг/мл, по результатам ОСГ определялись множественные очаги деструкции костной ткани, более вероятно метастатического характера. Данных за висцеральные метастазы получено не было. Выполнена промежностная мультифокальная биопсия предстательной железы под ТРУЗИ-контролем. Гистологическое исследование: в обеих долях предстательной железы определялась микроацинарная светлоклеточная аденокарцинома умеренной степени дифференцировки. Глисон 5 (3+2). Было проведено исследование опухолевой ткани, полученной при выполнении диагностической биопсии согласно предлагаемому способу с целью определения прогноза эффективности лечения РПЖ, результаты которого показали, что уровни экспрессии рецепторов AR, ERα, которые составили 51 и 68 УЕ соответственно. При расчете дискриминантных функций выявлено, что Y1=31,254 и Y2=50,421; YKY2, что свидетельствовало о возможном более длительном эффекте АДТ (отсроченная резистентность к АДТ и прогрессирование РПЖ в сроки более 12 месяцев от начала проведения терапии). Ответ опухоли на АДТ регистрировался на протяжении 25 месяцев. Однако, через 2 года был отмечен рост ПСА крови на фоне проводимого лечения и кастрационных значений тестостерона (0,25 нмоль/л). Прирост показателя фиксировался каждые 2 недели, среднее его значение составило 25,7 нг/мл. По данным ОСГ были зафиксированы признаки множественного очагового поражения скелета, что свидетельствует о прогрессировании процесса. Следовательно, предлагаемый способ позволил проводить АДТ в течении 25 месяцев до прогрессирования заболевания и формирования кастрационной резистентности с дальнейшим переводом пациента на химиотерапию препаратами таксанового ряда.
Таким образом, применение предлагаемого способа может быть использовано для оценки эффективности лечения РПЖ посредством прогнозирования времени ответа на андроген-депривационную терапию у пациентов с РПЖ.
Источники информации, принятые во внимание при составлении описания:
1. Маркова АС, Поликарпова СБ, Камолов БШ, Гриднева ЯВ, Калинин СА, Петерс MB, Матвеев ВБ. Факторы прогноза общей выживаемости больных метастатическим кастрационно-резистентным раком предстательной железы. // Онкоурология. 2015; 11(2): 77-84. [MarkovaA.S., PolikarpovaS.B., KamolovB.S., GridnevaY.V., Kalinin S.A., Peters M.V., Matveev V.B. Predictors of overall survival in patients with metastatic castration-resistant prostate cancer. Cancer Urology. 2015; 11 (2):77-84. (In Russ.) DOI: 10.17650/1726-9776-2015-11-2-77-84]
2. Amiya Y, Yamada Y, Sugiura M, Sasaki M, Shima T, Suzuki N, Nakatsu H, Murakami S, Shimazaki J. Treatment of locally advanced prostate cancer (Stage T3). Jpn J ClinOncol. 2017; 47(3):257-261. doi: 10.1093/jjco/hywl86.
3. Wang Y, Kreisberg JI, Ghosh PM. Cross-talk between the androgen receptor and the phosphatidylinositol 3-kinase/Akt pathway in prostate cancer. CurrCancerDrugTargets. 2007 Sep; 7(6):591-604. Review.
4.  AV, Moul J, Carroll PR, Sun L, Lubeck D, Chen MH. Prostate specific antigen doubling time as a surrogate end point for prostate cancer specific mortality following radical prostatectomy or radiation therapy. J Urol. 2004; 172(5 Pt 2):42-46.
AV, Moul J, Carroll PR, Sun L, Lubeck D, Chen MH. Prostate specific antigen doubling time as a surrogate end point for prostate cancer specific mortality following radical prostatectomy or radiation therapy. J Urol. 2004; 172(5 Pt 2):42-46.
5. Lonergan PE, Tindall DJ. Androgen receptor signaling in prostate cancer development and progression. J Carcinog. 2011;10:20. doi: 10.4103/1477-3163.83937. Epub 2011 Aug 23.
6. Al-MaghrabiJA, HassanTM, Abdel-MeguidTA, MosliHA. Original article Expression of Estrogen Alpha and Beta Receptors in Prostate Cancer and Hyperplasia: Immunohistochemical Analysis African Journal of Urology 1110-5704 Vol. 16, No. 3, 2010 79 79-87
7. Karamouzis MV, Papavassiliou KA, Adamopoulos C, Papavassiliou AG. Targeting Androgen/Estrogen Receptors Crosstalk in Cancer. Trends Cancer. 2016 Jan; 2(1):35-48. doi: 10.1016/j.trecan.2015.12.001. Epub 2015 Dec 31. Review
8. Takizawa I, Lawrence MG, Balanathan P, Rebello R, Pearson HB, Garg E, Pedersen J, Pouliot N, Nadon R, Watt MJ, Taylor RA, Humbert P, Topisirovic I, Larsson O, Risbridger GP, Furic L. Estrogen receptor alpha drives proliferation in PTEN-deficient prostate carcinoma by stimulating survival signaling, MYC expression and altering glucose sensitivity. Oncotarget. 2015 Jan 20; 6(2):604-16.
9. Ahmad N, Kumar R. Steroid hormone receptors in cancer development: A target for cancer therapeutics.Cancer Letters. 2011; 300:1-9.
10. Nelson AW, Tilley WD, Neal DE, Carroll JS. Estrogen receptor beta in prostate cancer: friend or foe? EndocrRelat Cancer. 2014; 21 (4):T219-34. doi: 10.1530/ERC-13-0508.
11. Hearn JWD, AbuAli G, Reichard CA, Reddy CA, Magi-Galluzzi C, Chang KH, Carlson R, Rangel L, Reagan K, Davis BJ, Karnes RJ, Kohli M, Tindall D, Klein EA, Sharifi N. HSD3B1 and resistance to androgen-deprivation therapy in prostate cancer: a retrospective, multicohort study. LancetOncol. 2016 Oct; 17(10):1435-1444. doi: 10.1016/S1470-2045(16)30227-3.
ПРИЛОЖЕНИЕ
Таблица 1. Показатели, включенные в дискриминантную модель прогнозирования раннего рецидивирования больных раком предстательной железы на фоне андроген-депривационной терапии
Таблица 2. Последовательность праймеров проб исследованных генов.
Примечание: NM - номер последовательности РНК в NCBI Nucleotide Database (http://www.ncbi.nlm.nih.gov/nuccore); F - прямой праймер; R - обратный праймер
Таблица 3. Клинико-морфологические характеристики пациентов с РПЖ в зависимости от эффекта АДТ
Примечание: * - значимость различий, р<0,05;
Таблица 4. Экспрессия AR, ERα, ERβ у пациентов с РПЖ в зависимости от эффекта АДТ Примечание: * - значимость различий, р<0,05;

Примечание: * - значимость различий, р<0,05;
Примечание: * - значимость различий, р<0,05;
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ С НАЛИЧИЕМ МЕТАСТАЗОВ В ЛИМФАТИЧЕСКИХ УЗЛАХ И ОЛИГОМЕТАСТАЗОВ В КОСТЯХ СКЕЛЕТА ПРИ РАКЕ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2018 |
|
RU2695348C2 |
| СПОСОБ КОМПЛЕКСНОГО ГОРМОНОХИМИОЛУЧЕВОГО ЛЕЧЕНИЯ ЛОКАЛИЗОВАННОГО ИЛИ МЕСТНО-РАСПРОСТРАНЕННОГО РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ ВЫСОКОГО И ОЧЕНЬ ВЫСОКОГО РИСКА ПРОГРЕССИРОВАНИЯ | 2019 |
|
RU2716942C2 |
| Способ лечения первичного метастатического рака предстательной железы | 2022 |
|
RU2796395C1 |
| СПОСОБ ЛЕЧЕНИЯ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ С ИСПОЛЬЗОВАНИЕМ ПРОЛОНГИРОВАННОЙ ДЕПО ФОРМЫ ОКТРЕОТИДА НА ФОНЕ ХИРУРГИЧЕСКОЙ ИЛИ МЕДИКАМЕНТОЗНОЙ КАСТРАЦИИ | 2013 |
|
RU2541810C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ БИОХИМИЧЕСКОГО РЕЦИДИВА У БОЛЬНЫХ РАКОМ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ ПОСЛЕ ГОРМОНОЛУЧЕВОЙ ТЕРАПИИ | 2015 |
|
RU2605838C1 |
| НОВАЯ ВСПОМОГАТЕЛЬНАЯ ТЕРАПИЯ ДЛЯ ПРИМЕНЕНИЯ В СПОСОБЕ ЛЕЧЕНИЯ РАКА ПРОСТАТЫ | 2018 |
|
RU2758386C2 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ И ДОБРОКАЧЕСТВЕННОЙ ГИПЕРПЛАЗИИ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2016 |
|
RU2647433C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ И ДОБРОКАЧЕСТВЕННОЙ ГИПЕРПЛАЗИЕЙ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2016 |
|
RU2646790C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ АГРЕССИВНЫХ ФОРМ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ У БОЛЬНЫХ ГРУППЫ ПРОМЕЖУТОЧНОГО И ВЫСОКОГО РИСКА | 2021 |
|
RU2768477C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ РАКОМ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ С ЛИМФОГЕННЫМ ПРОГРЕССИРОВАНИЕМ ПОСЛЕ РАДИКАЛЬНЫХ МЕТОДОВ ТЕРАПИИ | 2017 |
|
RU2681139C2 |
Изобретение относится к области медицины, а именно - онкологии, и может быть использовано для прогнозирования сроков ответа на андроген-депривационную терапию (АДТ) у больных раком предстательной железы (РПЖ). Способ включает исследование биологически активных молекул ткани опухоли с определением экспрессии AR, ERα, также учитывают возраст пациента, уровень тестостерона и простат-специфического антигена (ПСА) и рассчитывают значения дискриминантных функций Yl, Y2 по уравнениям: Y1=-33,37+1,0⋅Х1+0,01⋅Х2+0,01⋅Х3+1,08⋅Х4-0,0004 Х5 (раннее рецидивирование РПЖ с эффектом АДТ в течение 12 месяцев), Y2=-59,27+1,75⋅Х1+0,03⋅Х2+0,23⋅Х3-4,02⋅Х4+0,007 Х5 (отсроченное рецидивирование РПЖ с эффектом АДТ более 12 месяцев), где X1 - возраст пациента, годы, Х2 - экспрессия AR в опухоли, УЕ, Х3-экспрессия ERα в опухоли, УЕ, Х4 - содержание тестостерона в сыворотке крови, нмоль/л, Х5 - содержание простат-специфического антигена (ПСА) в сыворотке крови, нг/мл. При Y1>Y2 - прогнозируют ответ на АДТ в сроки менее 12 месяцев от начала лечения, а при Y1<Y2 - более 12 месяцев от начала лечения. Использование изобретения позволяет прогнозировать сроки рецидивирования заболевания на фоне АДТ, прогнозировать ожидаемые эффекты лечения и оценить его эффективность, повысить точность и информативность диагностики. 4 табл., 2 пр.
Способ прогнозирования сроков ответа на андроген-депривационную терапию (АДТ) у больных раком предстательной железы (РПЖ), путем исследования ткани опухоли, отличающийся тем, что исследуют биологически активные молекулы с определением экспрессии AR, ERα и с учитывают возраст пациента, уровень тестостерона и простат-специфического антигена (ПСА) и рассчитывают значения дискриминантных функций Y1, Y2 по уравнениям:
Y1=-33,37+1,0⋅Х1+0,01⋅Х2+0,01⋅Х3+1,08⋅Х4-0,0004 Х5 (раннее рецидивирование РПЖ с эффектом АДТ в течение 12 месяцев);
Y2=-59,27+1,75⋅Х1+0,03⋅Х2+0,23⋅Х3-4,02⋅Х4+0,007 Х5 (отсроченное рецидивирование РПЖ с эффектом АДТ более 12 месяцев);
где X1 - возраст пациента, годы;
Х2 - экспрессия AR в опухоли, УЕ;
Х3 - экспрессия ERα в опухоли, УЕ;
Х4 - содержание тестостерона в сыворотке крови, нмоль/л;
Х5 - содержание простат-специфического антигена (ПСА) в сыворотке крови, нг/мл;
и при Y1>Y2 - прогнозируют ответ на андрогендепривационную терапию в сроки менее 12 месяцев от начала лечения, а при Y1<Y2 - более 12 месяцев от начала лечения.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЛОКАЛЬНОГО РЕЦИДИВА ОПУХОЛИ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ ПОСЛЕ РАДИКАЛЬНОЙ ПРОСТАТЭКТОМИИ | 2004 |
|
RU2275861C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПРОДОЛЖИТЕЛЬНОСТИ ЖИЗНИ БОЛЬНЫХ МЕТАСТАТИЧЕСКИМ РАКОМ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2007 |
|
RU2340286C1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| ПЕШКОВ М | |||
| Н | |||
| Постгеномные технологии в диагностике рака предстательной железы//Клиническая лабораторная диагностика | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| - С | |||
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
| КОГАН Е | |||
| А | |||
| и др | |||
| Молекулярные маркеры в диагностике и прогнозировании рака предстательной железы (иммуногистохимическое исследование)//Вопросы биологической, медицинской и фармацевтической химии | |||
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| - С | |||
| Насос | 1917 |
|
SU13A1 |
Авторы
Даты
2019-05-21—Публикация
2019-01-10—Подача