ОБЛАСТЬ ТЕХНИЧЕСКОГО ПРИМЕНЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к области ветеринарии, в частности к лечению заболеваний у животных и, более конкретно, к профилактике или лечению репродуктивно-респираторного синдрома свиней (PRRS), свиной эпидемической диареи (PED), синдрома белых пятен у креветок, коровьего мастита, инфекций у свиней, вызванных бактерией Actinobacillus pleuropneumoniae, кокцидиоза у птиц и интоксикаций, вызванных грибными токсинами, путем введения концентрированной композиции иммуноглобулинов птичьего происхождения, полученной из желтков яиц от кур, ранее иммунизированных эмульгированной вакцинной композицией, содержащей антигены, легкое минеральное масло и дисперсный адъювант, состоящий из биодеградируемых полимерных частиц.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Здоровье животных является основным ключом к получению здоровой и качественной пищи. Таким образом, контроль заболеваний и использование всех имеющихся инструментов контроля имеет первостепенное значение. Вакцинация является одним из всех тех инструментов, которые повседневно используются в фермерских хозяйствах. Существуют другие инструменты, используемые в качестве мер биобезопасности для предупреждения проникновения патогенов из других источников, применение гигиенических стандартов и управление животными для уменьшения распространения заболеваний среди животных одинакового использования, строгий контроль питания или создание комфортной среды для животных на ферме.
Несмотря на это, на сегодняшний день существуют заболевания, контроль которых не выполняется надлежащим образом. К числу этих заболеваний относятся заболевания, вызываемые вирусами, как например, вирус репродуктивно-респираторного синдрома свиней, который является серьезным заболеванием свиней, он был зарегистрирован в Соединенных Штатах в 1987 году и позже идентифицирован в ряде европейских странах. В 1991 году в Голландии было сообщение об изоляции этиологического агента, который назвали вирусом Лелистада, и по симптоматике, наблюдаемой у свиней, он был назван респираторным и/или эпидемическим абортом у свиней.
Другим вирусным заболеванием, которое не поддается контролю, является свиная эпидемическая диарея (PED), представляющая собой вирусное заболевание исключительно у свиней, очень заразное и в большинстве случаев приводящее к смерти. Это заболевание действует на пищеварительную систему, и молочные поросята погибают в течение 3-5 дней из-за диареи и обезвоживания.
Другим заболеванием является заболевание, вызываемое вирусом синдрома белых пятен (WSSV), основным патогеном креветок и ответственным за большие потери производства и доходов в фермерской индустрии во всем мире. На сегодняшний день нет эффективного лечения, с помощью которого можно контролировать инфекцию.
Актуальным является и лечение заболеваний, вызываемых коровьим коронавирусом и ротавирусом.
Более того, мы обнаруживаем заболевания, вызываемые бактериями, как например коровий мастит, который приводит к воспалению молочной железы и ее секретирующих тканей, тем самым уменьшая объем молока и изменяя его состав, и даже его аромат, вдобавок увеличивая его нормальную бактериальную нагрузку. По продолжительности заболевания можно классифицировать как острое или хроническое. Что касается клинического проявления, оно может быть клиническим или субклиническим. Это заболевание приводит к серьезным экономическим потерям в молочной промышленности.
Мы также находим, что заболевания, вызываемые Actinobacillus pleuropneumoniae, бактериями, ответственными за респираторные расстройства у свиней, распространенные во всем мире, стали известны 50 лет назад, и число случаев этих заболеваний возросло с 80-х годов, часто в откормочных хозяйствах. Эти бактерии являются главной причиной плевропневмонии у свиней, а также отвечают за агента, который непосредственно вовлечен в респираторный комплекс у свиней. Это заболевание отличается широкой распространенностью, очень заразное и во многих случаях летальное для свиней от отъема до убоя. Оно вызывает фибринозный плеврит с очень характерными реберными спайками у 30-50% свиней и приводит к повышенной смертности в острых случаях, с высокой задержкой роста в хронических случаях. Кроме того, было установлено, что бактерии Actinobacillus pleuropneumoniae вовлечены в случаи среднего отита, артрита и остеомиелита.
Лечение заболеваний, вызванных Е. coli, Salmonella spp и Clostridium perfringens, также относится к здоровью животных.
Кроме того, существует кокцидиоз (coccidiosis), который является инфекционным заболеванием, вызванным жестокими внутриклеточными живыми паразитами рода Eimeria spp. и Isospora spp. Кокцидии (coccidias) вездесущи, поскольку есть в большинстве скотоводческих предприятий во всем мире. Эти паразиты могут инфицировать самых разнообразных животных, включая людей, домашнюю птицу, жвачных животных, свиней, собак, кошек и других домашних животных, несмотря на это в большинстве случаев кокцидии являются специфическими видами.
Кроме того, другие проблемы здоровья, с которыми сталкивается индустрия крупного рогатого скота, вызваны трихотеценами, которые являются токсинами, продуцируемыми несколькими грибами Fusarium, в частности Fusarium graminearum и Fusarium sporotrichioides. Они вырабатываются в сельскохозяйственных культурах и поступают в пищу через загрязненные ингредиенты. Трихотецены являются подтвержденными тканевыми раздражителями, и их проникновение внутрь в основном связано с поражениями ротовой полости, дерматитом и раздражением кишечника. Основной физиологической реакцией на эти микотоксины является потеря аппетита. Трихотецены - это сильные подавляющие микотоксины, влияющие на клеточный иммунный ответ, непосредственно воздействуя на костный мозг, селезенку, лимфоидные ткани, тимус и слизистую оболочку кишечника, где активно делящиеся клетки повреждаются.
Для профилактического контроля всех вышеуказанных заболеваний существуют в основном две формы защиты. Они могут подвергаться воздействию антигенов, полученных из инфекционного агента, для стимуляции защитной иммунной реакции, или они могут вводиться с предварительно сформированным антителом, полученным от иммунного субъекта.
Первая форма защиты достигается при помощи вакцин, которые могут быть разных классов: живые микроорганизмы, лиофилизированные или мертвые в масляных эмульсиях, и недавно созданные клонированные и рекомбинантные вакцины. Каждая из них имеет свои преимущества и недостатки с точки зрения защиты, иммунного ответа и продолжительности защиты. Тем не менее, было обнаружено, что в некоторых случаях возникают нежелательные повреждения в организме-носителе в результате вакцинного вируса (Tizard, I.R. 1998. Vacunacion у vacunas In: Inmunologia Veterinaria. 5th. Edition, Mc. Graw-Hill. Pp. 285-305).
Вторая форма защиты также называется пассивным иммунитетом и предполагает передачу специфических антител к инфекционным агентам хозяину.
Традиционно, на исследовательском уровне, антитела продуцируются главным образом у млекопитающих и реже у домашней птицы. Типы антител, которые регулярно продуцируются у млекопитающих, являются моноклональными и поликлональными типами, и поликлональными у домашней птицы (Larsson, et al., 1993. Chicken antibodies: taking advantage of evolution. A review Poultry Sci. 72: 1807-1812).
В случае домашней птицы, вид Gallus gallus domesticus (петухи и курицы) является единственным видом, от которого антитела получают более доступным способом и с высокой степенью определенности. Основным антителом к сыворотке, которое присутствует в указанном виде, является IgG, хотя IgG переносится в яйцо аналогично транспорту IgG млекопитающего через плаценту.
В яйце иммуноглобулин Y (IgY) также присутствует в более высокой концентрации в яичном желтке, однако, в яичном белке также имеются небольшие количества IgY. Было даже установлено, что количество IgY в яичном желтке выше, чем в сыворотке курицы (Larsson, et al 1993. Chicken antibodies: taking advantage of evolution. A review Poultry Sc. 72: 1807-1212).
Чтобы получить представление о количестве антител, продуцируемых курами, достаточно заметить, что курица-несушка производит приблизительно 5-6 яиц в неделю с приблизительным объемом яичного желтка 15 мл, таким образом, в течение недели курица может продуцировать антитела яичного желтка, эквивалентные 90-100 мл сыворотки или 180-200 цельной крови. Это, если сравнивать с 20 мл цельной крови, которую дает иммунизированный кролик в неделю, позволяет четко отметить эффективную продуктивность антител в яичном желтке. Ясно, что если используются более крупные животные, такие как лошади или коровы, количество сыворотки и антител будет выше, чем в яйце, но эта процедура дорогостоящая и, кроме того, более болезненная для животных.
Среди преимуществ антител ячного желтка следующие:
1. Они не связывают комплемент.
2. Они не связываются с А белком из Staphilococcus aureus.
3. Они не реагируют на ревматоидный фактор.
4. Из-за их филогенетического различия с антителами млекопитающих IgY не обнаруживают перекрестной реакции с антителами млекопитающих.
5. Низкая себестоимость производства.
В последние годы антитела яичного желтка (иммуноглобулины) использовались в качестве средств диагностики и терапии (Schmidt et al., 1989). Таким образом, благодаря преимуществу их филогенетического различия с антителами млекопитающих, иммуноглобулины продемонстрировали ряд преимуществ при использовании в иммунодиагностике. Например, иммуноглобулины яичного желтка использовали для обнаружения нескольких вирусов с помощью методов ELISA, иммунодиффузии, иммунофлюоресценции и фиксации комплемента. Из-за низкой изоэлектрической точки по сравнению с Ig человека они использовались в анализах электрофореза для количественного определения иммуноглобулинов в сыворотке различных животных (Altschuh, D. et al. 1984. Determination of IgG and IgM levels in serum by Rocket Immunoelectrophoresis using yolk antibodies from immunized chickens. J. Immunolog. Methods. 69: 1-7; Larsson, A. et al. 1988. Chicken antibodies: a tool to avoid false positive results by rheumatoid factor in latex fixation tests. J. Immunol. Methods. 108: 205-208; Larsson, A. et al. 1992. Chicken antibodies: a tool to avoid interference by complement activation in ELISA. J. Immunol. Methods. 156: 79-83.; Larsson, et al 1993. Chicken antibodies: taking advantage of evolution. A review Poultry Sci.72: 1807-1812; Schade, R. et al 1996. The production of avian (Egg yolk) antibodies: IgY. Atla. 24: 925-934).
Что касается терапевтического применения, IgY использовались в качестве иммунотерапии в различных областях науки, например, пероральное введение иммуноглобулинов яичного желтка предотвратило ротавирусные инфекции у мышей, бычков и свиней и т.д. (Ikemori, Y. et al. 1992 Protection ofneonatal calves against fatal enteric colibacillosis by administration of egg yolk powder from hens immunized with l<99-pillated enterotoxigenic Escherichia coli. Am.J.Vet.Res.53: 2005-2008; Kuroki, M. et al 1994. Passive protection against bovine rotavirus in calves by specific immunoglobulins from chicken egg yolk. Arch. Virol. 138: 143-148; Marquart, R. 1998. Antibody-loaded eggs for piglets: prevention of baby pigs from diarrhea. Proc. 2nd international Symposium on Egg Nutrition and Newly Emerging Ovo-Technologies. Alberta, Canada).
Иммуноглобулины яичного желтка IgY использовались даже в качестве антивенинов против змей и скорпионов, которые могут инъецироваться для нейтрализации токсинов без риска общих анафилактических реакций, обнаруженных в антивенинах, полученных от лошади (Larsson, et al 1993. Chicken antibodies: taking advantage of evolution. A review Poultry Sci. 72: 1807-1812). Другим применением было предотвращение кариеса у людей, вызванное Streptococcus mutans (Hatta, Н. et al. 1997. Passive immunization Against Dental Plaque Formation in Humans: Effect of a Mouth Rinse containing Egg Yolk Antibodies (IgY) Specific to Streptococcus mutans. Caries. Res. 31: 268-274).
В случае вышеупомянутых заболеваний у животных с течением времени были разработаны определенные меры контроля и профилактики в связи с расширением и экономическими последствиями указанных заболеваний. Среди стратегий борьбы с такими заболеваниями - инактивированные вакцины и живые вирусные вакцины. Однако ни одна из этих стратегий не была эффективной на 100%.
В конкретном случае РНК-вирусов, таких как вирус PRRS или вирус PED, отсутствие контроля в значительной степени обусловлено его высоким индексом частоты мутаций. Это общая особенность РНК-вирусов, вытекающая из недостатка коррекционной активности РНК-полимеразы. Таким образом, эта особенность наряду с быстрой кинетикой репликации вируса увеличивает риск мутации и появления квазивидов (Manreetpal Singh Brar, Mang Shi, Raymond Kin-Hi Hui and Frederick Chi-Ching (2014) Leung mail Genomic Evolution of Porcine Reproductive and Respiratory Syndrome Virus (PRRSV) Isolates Revealed by Deep Sequencing. PLOS one). Сообщается, что генетическая вариабельность вируса PRRS составляет от 0,48 до 1,32% (Murtaugh М., (2012) Use and interpretation of sequencing inf PRRSV control programs. Allen D. Leman Swaine Conference. Veterinary Continuing Education). Эти особенности вируса PRRS объясняют несоответствующую защиту, получаемую с помощью вакцин.
Одна из стратегий, используемых для предупреждения заболеваний, вызываемых этими вирусами, представляет собой аутовакцина, что подразумевает разработку вакцин не только по стране, но и по регионам, и наоборот, профилактика с помощью этих средств оказывается неудовлетворительной.
Также было замечено, что в случае вируса, вызывающего PRRS, он нейтрализуется путем использования иммуноглобулинов, извлеченных из сыворотки млекопитающих (US 5,489,805). Эти результаты показывают, что иммуноглобулины являются альтернативой для лечения вирусов, антитела нежизнеспособны.
Применение иммуноглобулинов, полученных из яичного желтка (IgY), уже использовалось в нескольких применениях защиты здоровья и профилактики животных, а также у людей. Исследования Akita и Nakai (Akita, Е., Nakai, S. (2000). Egg nutrition and biotechnology, CAB International, New York, p.301), показывают, что защитная роль IgY против инфекционных агентов в основном объясняется их способностью предотвращать колонизацию токсинов или нейтрализовать токсины.
Таким образом, целью настоящего изобретения является получение концентрированных композиций иммуноглобулинов IgY птичьего происхождения, эффективных и надежных против определенных агентов, которые инфицируют животных, включая, например, вирус PRRS, вирус свиной эпидемической диареи (PED), бакуловирусный комплекс синдрома белого пятна (White Spot Syndrome Baculovirus Complex), бактерии, вызывающие мастит у коров, бактерии Actinobacillus pleuropneumoniae и кокцидиоз, а также интоксикации, вызываемые трихотеценами, поскольку их применимость может непосредственно влиять на значительное снижение расходов, связанных со способами вакцинации, и, что более важно, значительно снижать производственные потери, связанные с указанными заболеваниями.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Для достижения целей настоящего изобретения экспериментально оценивали способность композиции, содержащей концентрированные иммуноглобулины IgY, специфические для нейтрализации вируса PRRS и полученные из яичного желтка от кур, которые были ранее иммунизированы эмульгированной вакцинной композицией, содержащей антигены, извлеченные из одного или нескольких штаммов вируса PRRS, легкое минеральное масло и дисперсный адъювант, состоящий из биоразлагаемых полимерных частиц, микрочастиц или наночастиц.
Авторы настоящей заявки успешно достигли целей настоящего изобретения и неожиданно обнаружили, что с помощью антигенов одного или нескольких различных штаммов вируса PRRS, тщательно отобранных, можно получить ожидаемую перекрестную защиту от других штаммов того же вируса, а также индуцировать продуцирование иммуноглобулинов, которые способны нейтрализовать большее количество вирусов PRRS, циркулирующих в поле. Кроме того, эмульгированная вакцинная композиция должна включать легкое минеральное масло, например, Marcol, и дисперсный адъювант, состоящий из биоразлагаемых полимерных частиц, микрочастиц или наночастиц, чтобы усилить вакцинацию, предпочтительно с использованием линейного полисахарида, состоящего из случайно распределенных цепей β-(1-4)D-глюкозамина (деацетилированные звенья) и N-ацетил-D-глюкозамина (ацетилированные звенья), такие как хитозан.
Полученной таким образом эмульгированной вакцинной композицией иммунизируют несушек домашней птицы, чтобы получить, через яичный желток, иммуноглобулины IgY, нейтрализующие инфекционные агенты или токсины, и после выполнения способа экстракции, обезжиривания и концентрирования, при использовании минимальных количеств, наконец, получают концентрированную композицию указанных иммуноглобулинов IgY, способную обеспечить неожиданную защиту вплоть до приблизительно 100%, и, помимо этого, регуляцию уровня S/P на зараженных фермах.
Изобретение обладает дополнительным преимуществом, заключающемся в стабилизации гурта, стада или больших групп, что уменьшает циркуляцию инфекционных агентов. Кроме того, при применении концентрированной композиции птичьего происхождения в соответствии с изобретениемпо программе сокращается генерация материнских субпопуляций и сероконверсия животных на откорме задерживается при отъеме.
В настоящее время оцениваемые иммуноглобулины получены из сыворотки млекопитающего, и они прошли испытания только на экспериментальной модели, зараженной тем же штаммом вируса, которым они были вакцинированы. Это означает, что, в отличие от настоящего изобретения, вакцины предшествующего уровня техники были протестированы только на защиту гомолога (WO 02/067985).
Кроме того, концентрированная композиция птичьего происхождения в соответствии с изобретением, содержащая концентрированные иммуноглобулины IgG, может быть использована на любой репродуктивной стадии животных без побочных или нежелательных эффектов.
Концентрированная композиция птичьего происхождения в соответствии с изобретением имеет высокую концентрацию и защищает от высокой вероятности контрольного заражения инфекционным агентом или токсинами. Имеются доказательства защиты от контрольных заражений, с 10 по 7 (10000000), что значительно выше того, что уже известно из предшествующего уровня техники (WO 2007/061281 А2).
Кроме того, с помощью способов в соответствии с настоящим изобретением получают такую концентрацию иммуноглобулинов (IgY), нейтрализующих инфекционные агенты, циркулирующие в поле, или токсины, что в виде концентрата вводится только 1 мл или 3 мл на дозу, тогда как при введении вакцин и продуктов предшествующего уровня техники вплоть до 5 мл и даже до 10 мл, и даже более, чем 10 мл (WO 2007/061281 А2).
Уменьшение объема введения полезно во многих отношениях. Во-первых, потому что введение упрощается, во-вторых, потому что производственные затраты снижаются и в-третьих, потому что транспортировка в разные районы занимает меньше места.
Дозы в 1 мл или вплоть до 3 мл, которые могут быть достигнуты благодаря композиции концентрированных иммуноглобулинов (IgY) в соответствии с настоящим изобретением, зависящие, безусловно, от степени тяжести заболевания, соответствуют программе иммунизации и даже тогда, когда они не являются вакциной как таковой, они могут работать как вакцина и контролировать зараженных животных. Концентрированная композиция птичьего происхождения в соответствии с изобретением попадает в область пассивного иммунитета, так как она содержит иммуноглобулины, нейтрализующие инфекционные агенты или токсины.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
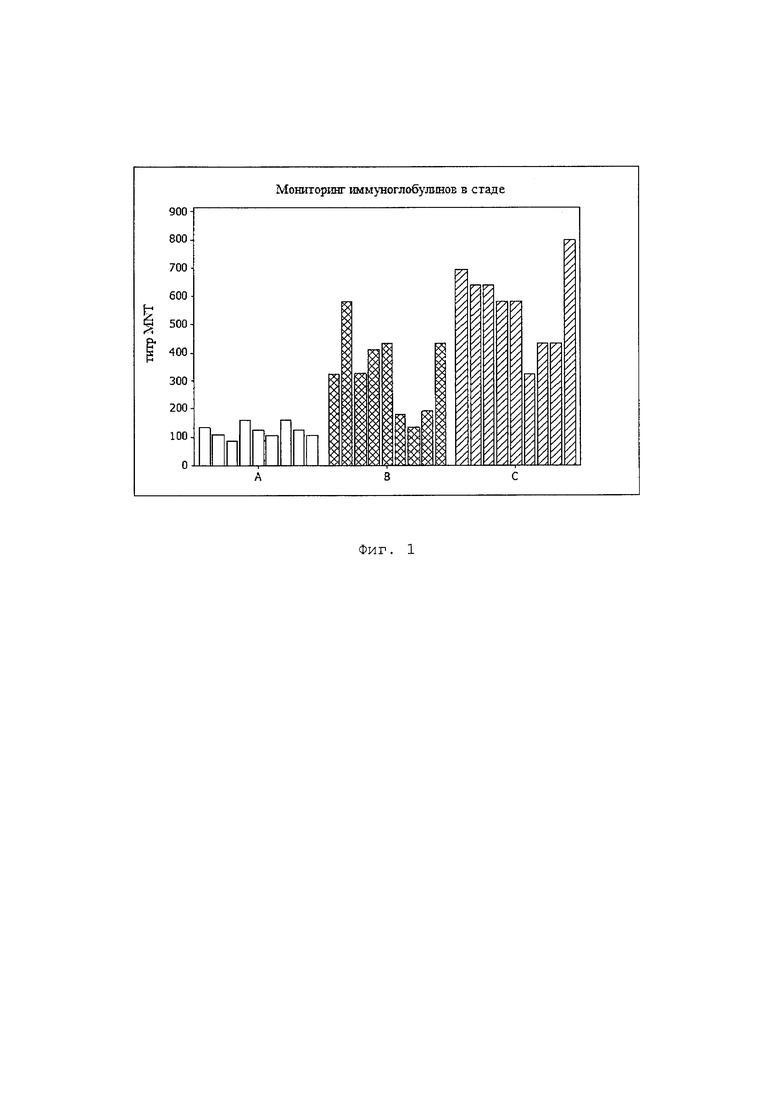
На Фиг. 1 показаны результаты MNT-титрования различных образцов яиц, собранных от домашней птицы, иммунизированной различными вакцинами. Группа А была вакцинирована 2 вакцинами, приготовленными с минеральным маслом, каждая из которых содержала 3 штамма вируса PRRS, применялись поочередно на ежемесячной основе. Группа B была вакцинирована одной вакциной, приготовленной с минеральным маслом и хитозаном, которая содержала 6 различных штаммов вируса PRRS и применялась раз в месяц. Группа C была вакцинирована с помощью вакцины, приготовленной с marcol и хитозаном, содержала 6 различных штаммов вируса PRRS, применялась раз в месяц.
Эти результаты указывают на то, что титры антител IgY, продуцируемые вакциной, содержащей шесть штаммов вируса PRRS, и при использовании композиции с marcol и хитозаном представляют собой титры, которые индуцируют наибольшее количество антител против репродуктивного и респираторного синдрома свиней.
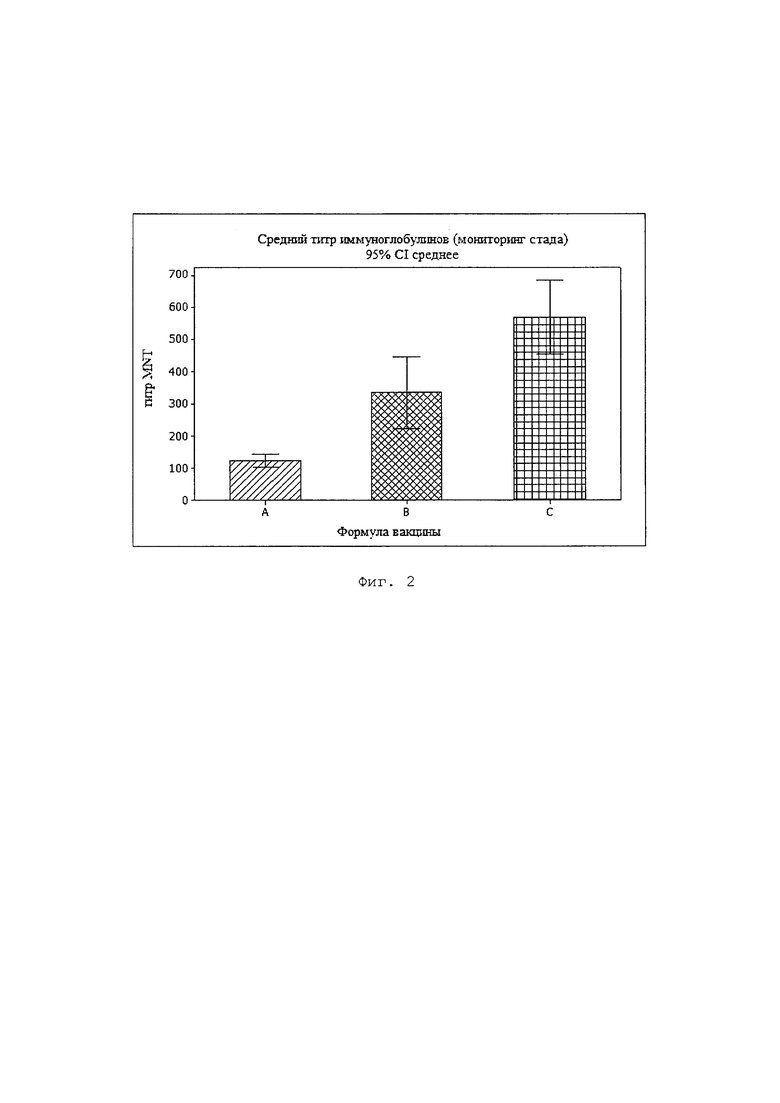
На Фиг. 2 показан титр антител IgY в желтке при использовании трех видов вакцинных композиций. Группа А была вакцинирована 2 вакцинами, приготовленными с минеральным маслом, каждая из которых содержала 3 штамма вируса PRRS, применялись поочередно и на ежемесячной основе. Группа В была вакцинирована одной вакциной, приготовленной с минеральным маслом и хитозаном, которая содержит 6 различных штаммов вируса PRRS, применялась раз в месяц. Группа С была вакцинирована вакциной, приготовленной с маслом marcol и хитозаном, которая содержит 6 различных штаммов вируса PRRS, применялась раз в месяц.
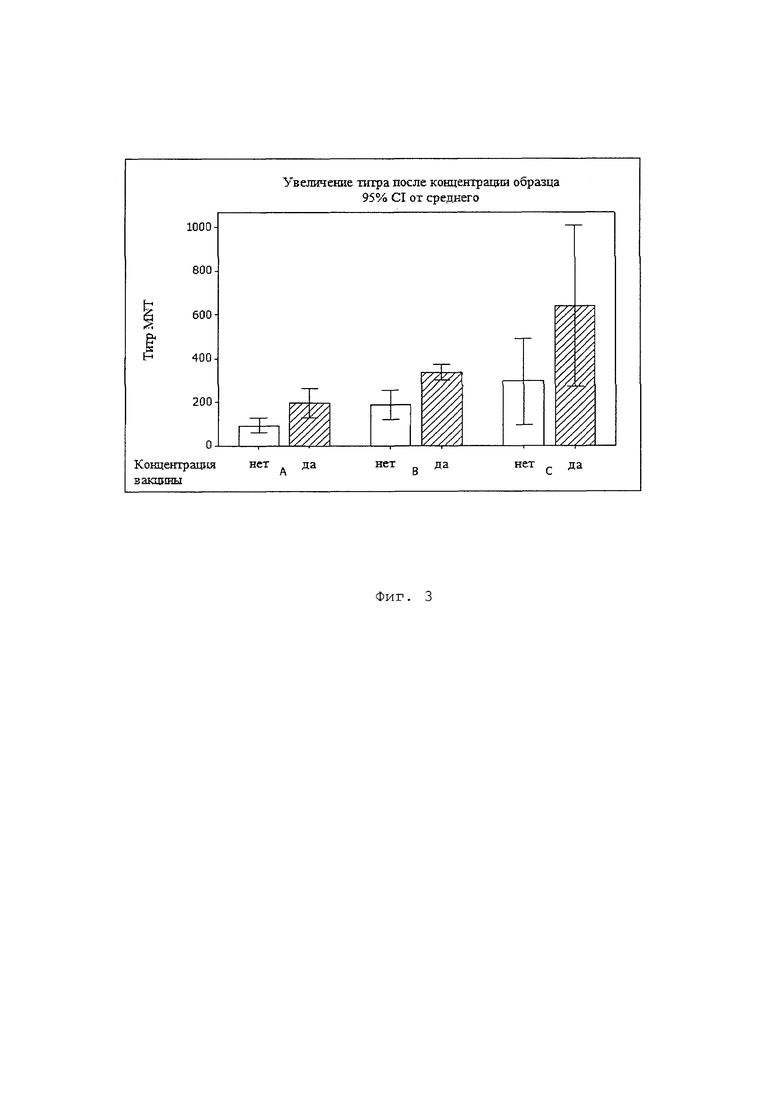
На Фиг. 3 показано увеличение титра иммуноглобулинов после применения способа концентрирования. Желточные иммуноглобулины извлекли, одну часть определили количественно с помощью MNT-метода, а остальные подвергли концентрированию. Группа А была вакцинирована 2 вакцинами, приготовленными с минеральным маслом, каждая из которых содержала 3 штамма вируса PRRS, применялись поочередно на ежемесячной основе. Группа B была вакцинирована одной вакциной, приготовленной с минеральным маслом и хитозаном, содержала 6 различных штаммов вируса PRRS и применялась раз в месяц. Группа C была вакцинирована вакциной, приготовленной с marcol и хитозаном, содержала 5 различных штаммов вируса PRRS и применялась раз в месяц.
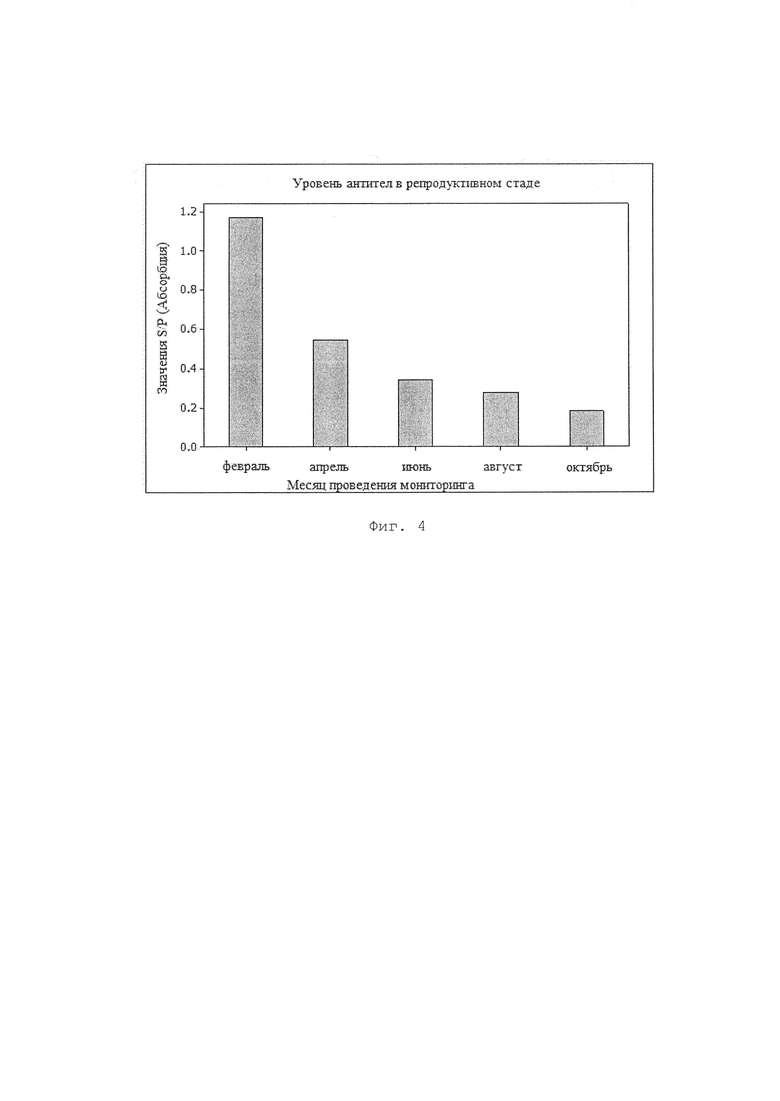
На Фиг. 4 показано постепенное снижение уровней антител у самок репродуктивного стада после получения концентрированной композиции.
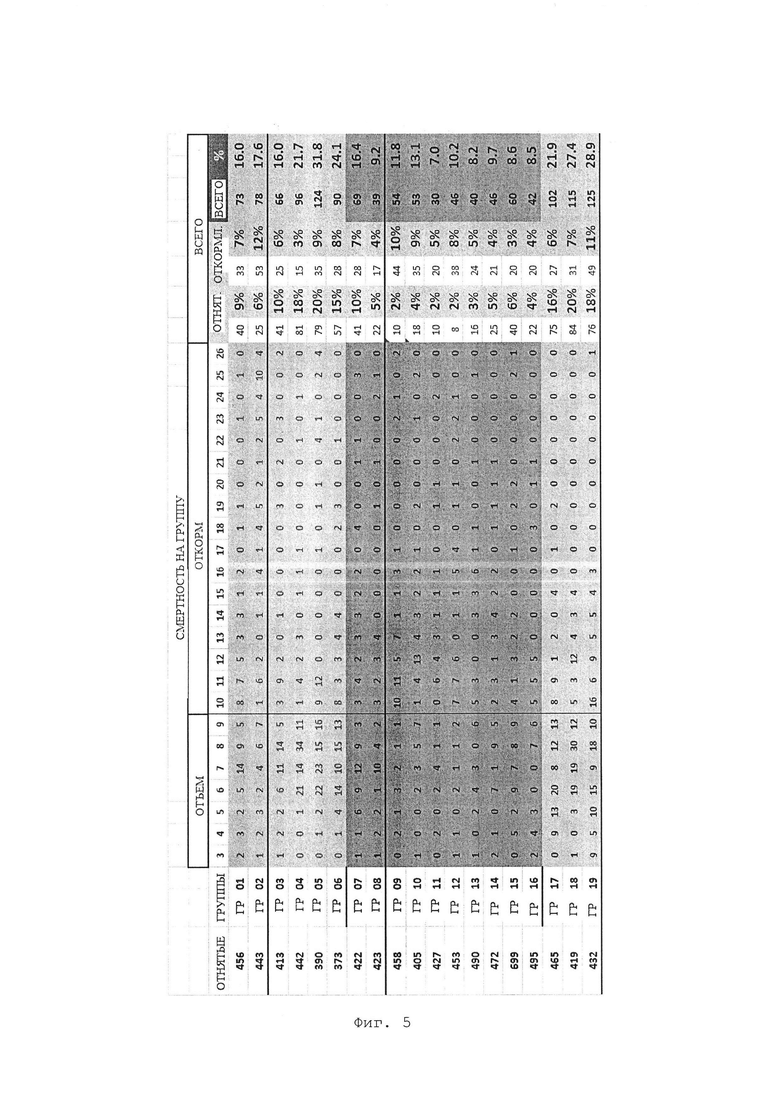
На Фиг. 5 показан мониторинг смертности с 3 по 26 недели. Группы, которых лечили концентрированной композицией иммуноглобулинов IgY птичьего происхождения по изобретению, выделены блоком более интенсивного синего цвета (группы с 7 по 16).
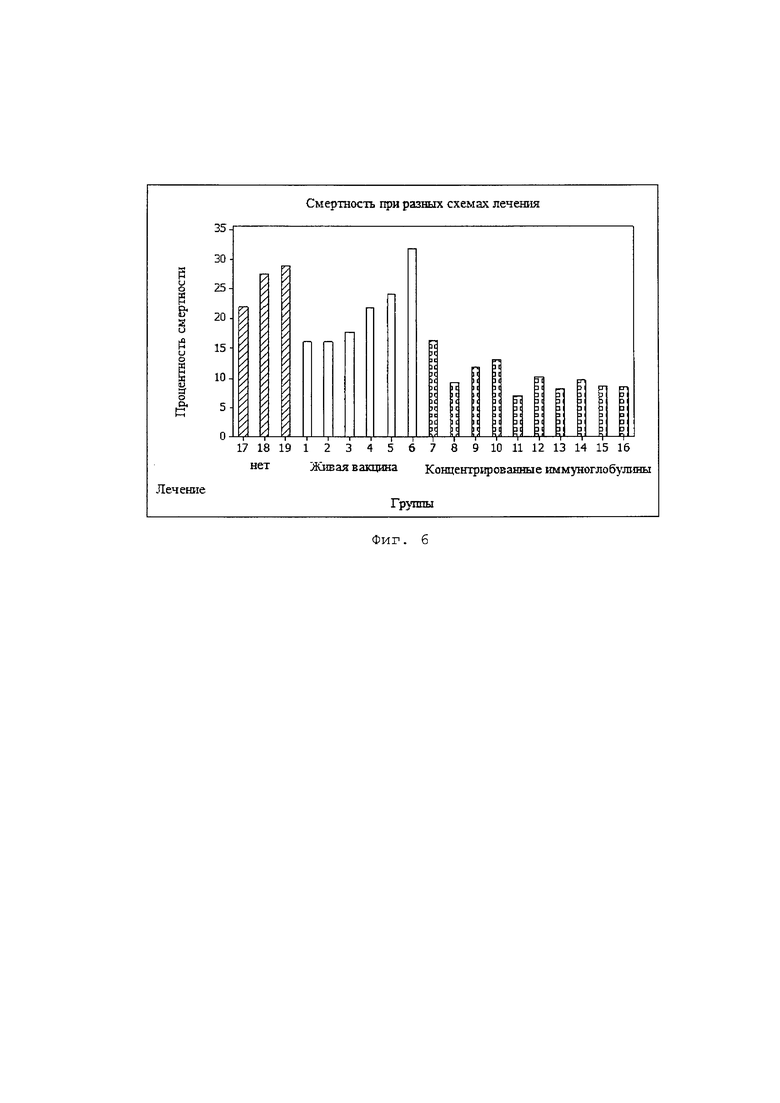
На Фиг. 6 показана диаграмма с указанием процента смертности в каждой оцениваемой группе, в которой выделены группы, которых лечили концентрированной композицией птичьего происхождения в соответствии с изобретением.
ПОДРОБНОЕ ОПИСАНИЕ
Иммунизация несушек домашней птицы с целью получения иммуноглобулинов (IgY), нейтрализующих инфекционные агенты или токсины
Получают эмульгированную вакцину, состоящую из антигенов для продуцирования нейтрализующих антител, и не только против одного штамма определенного инфекционного агента или токсина, а против нескольких штаммов, циркулирующих в поле (эпидемиологический надзор), или токсинов.
Вышеизложенное относится к случаю с вирусами, вызывающих острый некроз сетчатки, так как на основании данного исследования было замечено, что не все штаммы циркулирующего вируса могут нейтрализоваться антителами, полученными из антигенов специфического штамма. То же самое происходит с вакцинами против вируса, так как, если вакцинация выполняется гетерологичным штаммом, обеспечивается частичная защита.
В случае с микроорганизмами, штаммы были отобраны путем перекрестных тестов MNT (микронейтрализация). Этот тест заключается в тестировании уровня нейтрализации иммуноглобулинов, полученных с использованием вакцин с определенными штаммами, против новой изоляции инфекционного агента. В нашей работе в лаборатории мы определили, что если новая изоляция имеет титры ниже 1:160 в МНТ, тогда указанный штамм рассматривается как кандидат на включение в новую вакцину. Таким образом, на сегодняшний день наша вакцина содержит некоторые штаммы, которые обеспечивают широкий спектр нейтрализации против штаммов инфекционных агентов, циркулирующих в Мексике. Однако это не ограничивает изобретение и не следует понимать, что изобретение относится к вакцине, включающей только выбранные штаммы, поскольку штаммы инфекционного агента могут варьироваться по мере выполнения мониторинга циркуляции в поле новых штаммов, которые могут быть включены позже в вакцину для поддержания защиты у животных. Спектр нейтрализации в соответствии с настоящим изобретением также может быть расширен и приспособлен против других штаммов инфекционных агентов, циркулирующих в других странах или в других регионах.
Штаммы инфекционного агента могут быть полевыми изоляциями, полученными из сыворотки или ткани больного животного. Основанием для отбора, как указано выше, является тест перекрестной микронейтрализации между различными изолированными штаммами с Ig, содержащимися в продукте и генерируемыми из отобранных штаммов.
В случае вируса PRRS, клеточная линия MARC-145 может быть реплицирована, и выполняются не более пяти проходов рабочего посева для предотвращения ослабления. Отобранные антигены инактивируются с помощью 0,01% формалина или любым другим способом, описанным в предыдущем уровне техники. В нашей лаборатории мы определили, что каждая смесь антигенов должна иметь минимальный титр DIE50% 104/мл.
Принимая во внимание вышесказанное, для усиления вакцинации эмульгированная вакцинная композиция для иммунизации домашней птицы, кроме того, содержит антигены из одного или нескольких тщательно отобранных штаммов, легкое минеральное масло и дисперсный адъювант, состоящий из биоразлагаемых полимерных частиц, микрочастиц или наночастиц, в частности, линейный полисахарид, состоящий из случайно распределенных цепей β-(1-4)D-глюкозамина (деацетилированные звенья) и N-ацетил-D-глюкозамина (ацетилированные звенья), такие как хитозан, является предпочтительным.
Композиция вакцины водно-жирового типа может содержать примерно от 50% до 70% и предпочтительно примерно от 60% до 67% масла Marcol, примерно 20%-40% и предпочтительно примерно 28%-35% воды с антигенами вируса PRRS; примерно 5-15% каждого из штаммов вируса PRRS, отобранных согласно вышеприведенным критериям, примерно 2%-5% полиоксиэтиленмоноолеат сорбитана (Tween 80), примерно 2-8% сорбитанмоноолеат сорбитана (Span 80) и адъювант, как например линейный полисахарид, состоящий из случайно распределенных цепей β-(1-4)D-глюкозамина (деацетилированные звенья) и N-ацетил-D-глюкозамина (ацетилированные звенья), в частности от 4% до 6% хитозана. Для приготовления вакцины каждый компонент добавляют один за другим по системе перемешивания в течение от 1 до 5 минут с добавлением в конце хитозана.
Вакцина вводится несушкам домашней птицы без патогенов, в объеме 0,5 мл один раз в месяц, подкожно, начиная с 8-й недели и до 60-й недели, чтобы в конечном итоге получить композицию нейтрализующих инфекционные агенты или токсины иммуноглобулинов (IgY) из яичного желтка.
В частности, уровень антител для каждого из штаммов инфекционного агента оценивается с помощью микронейтрализации (MNT) образцов яичных желтков, собранных от вакцинированного стада. Минимальный титр сыворотки должен соответствовать критериям 1:160.
После иммунизации яйца собирают от иммунизированной домашней птицы и подвергают способу экстракции, обезжиривания и концентрирования иммуноглобулинов из яичного желтка.
Способ экстракции, обезжиривания и концентрирования иммуноглобулинов IgY
Для экстракции и концентрирования иммуноглобулинов IgY, нейтрализующих инфекционные агенты или токсины, из яичного желтка выполняются следующие этапы.
Яичный желток разбавляют 1:4 или 1:8 (без яичного белка) 0,01% азидом натрия и хранят в холодильнике, по меньшей мере, весь день, предпочтительно от 12 до 24 часов. Затем супернатант отделяют и добавляют от 1 до 15% фталата гидроксипропилметилцеллюлозы (НРМСР) в соотношении 0,25 мл на каждые 100 мл воды. Оставляют в покое по меньшей мере на 24 часа. Слой липидов, образованный в верхней части раствора, отделяют и водную часть фильтруют, затем добавляют PEG, предпочтительно 8000, в соотношении 5-30% P/V, смешивают и оставляют в покое по меньшей мере на 4 часа, но предпочтительно оставляют в покое на ночь при 4°C. Затем центрифугируют в течение 20-30 минут и супернатант удаляют. Полученную таблетку солюбилизируют буфером PBS IX или TRIS в объеме, эквивалентном 10% от исходного объема.
Лечение с помощью концентрированной композиции иммуноглобулинов IgY в соответствии с изобретением
Композиция, полученная в результате выполнения способа экстракции, обезжиривания и концентрирования иммуноглобулинов IgY, нейтрализующих инфекционные агенты или токсины, полученных из яичного желтка от кур, ранее иммунизированных с помощью эмульгированной вакцины, содержащей антигены, легкое минеральное масло и дисперсный адъювант, состоящий из биоразлагаемых полимерных частиц, как например линейный полисахарид, состоящий из случайно распределенных цепей β-(1-4) D-глюкозамина (деацетилированные звенья) и N-ацетил-D-глюкозамина (ацетилированные звенья) (хитозан), может содержать: примерно 0,8%-5% концентрированных иммуноглобулинов IgY против патогенов или токсинов в соответствии с изобретением, предпочтительно примерно 1% концентрированных иммуноглобулинов, примерно 80-90% воды и примерно 0,001%-0,03% консервантов. Лечебная доза концентрированной композиции в соответствии с изобретением может составлять 1 мл и не более 3 мл, что обеспечивает нейтрализацию полевых разновидностей инфекционных агентов или токсинов по изобретению, неожиданно обеспечивая защиту вплоть до 100% у животных и вдобавок регулируя уровень S/P на зараженных фермах, как показано ниже.
С учетом вышесказанного, в первом варианте осуществления настоящее изобретение относится к эмульгированной вакцинной композиции, содержащей антигены, легкое минеральное масло, предпочтительно Marcol, и дисперсный адъювант, состоящий из биоразлагаемых полимерных частиц, как например линейный полисахарид, состоящий из случайно распределенных цепей β-(1-4)D-глюкозамина (деацетилированные звенья) и N-ацетил-D-глюкозамина (ацетилированные звенья), предпочтительно хитозан. Кроме того, вакцинная композиция в соответствии с настоящим изобретением содержит один или несколько эмульгаторов, как например полиоксиэтиленмоноолеат сорбитан (Tween 80), сорбитанмоноолеат сорбитан (Span 80) или их смесь.
Антигены могут происходить от одного или нескольких различных штаммов от одного или нескольких инфекционных агентов или токсинов, как например вирусы, бактерии или простейшие, в частности от вируса PRRS, вируса PED, вируса комплекса бакуловируса синдрома белого пятна, Rotavirus spp.или Coronavirus spp., и, более конкретно, от вирусов PRRS, имеющих нуклеотидную последовательность гена ORF5, выбранную из группы, состоящей из SEQ. ID. NO: 1, SEQ. ID. NO: 2, SEQ. ID. NO: 3, SEQ. ID. NO: 4, SEQ. ID. NO: 5, SEQ. ID. NO: 6 и SEQ. ID. NO: 7, а также от вируса свиной эпидемической диареи (PED). Кроме того, антигены могут происходить от одной или нескольких бактерий, таких как Salmonella spp., от выбранных из группы, состоящей из: Staphylococcus aureus, Streptococcus agalactiae, Escherichia coli, Corynebacterium pyogenes и Mycoplasma bovis, или также от Actinobacillus pleuropneumoniae. Антигены могут дополнительно происходить от одного или нескольких простейших, выбранных из группы, состоящей из: Eimeria tenella, Eimeria acervulina и Eimeria maxima, или от токсинов, продуцируемых грибами, как например трихотецены и, более конкретно, от 4-дезоксиниваленола (DON). Более того, антигены могут происходить от одного или нескольких различных штаммов одного или нескольких вирусов, одной или нескольких бактерий, или одного или нескольких простейших, как например, от антигенов, извлеченных из Eschericihia coli, Salmonella spp., Clostridium perfringens, Rotavirus spp. и Coronavirus spp. В частности, антигены могут также происходить от группы, состоящей из Escherichia coli, Rotavirus spp. и Coronavirus spp.
Эмульгированная вакцинная композиция в соответствии с изобретением может содержать вирусные штаммы, отобранные по сывороточному титру ниже 1:160, оцененные с помощью перекрестной микронейтрализации при использовании пула иммуноглобулинов, полученных с помощью существующей вакцины.
Аналогично, эмульгированная вакцинная композиция в соответствии с изобретением может содержать смесь антигенов с титрами выше, чем DIE50% 104/мл.
Согласно выбранному антигену или антигенам, настоящее изобретение также относится к применению эмульгированной вакцинной композиции при получении концентрированной композиции иммуноглобулинов IgY, пригодной для лечения репродуктивно-респираторного синдрома свиней (PRRS), лечения свиной эпидемической диареи (PED), лечения синдрома белых пятен у креветок, лечения коровьего мастита, лечения инфекций, вызванных Actinobacillus pleuropneumoniae у свиней, лечения кокцидиоза у домашней птицы, лечения интоксикаций, вызванных трикотеценами, в частности, когда трикотецен представляет собой 4-дезоксиниваленол (DON), соответственно; причем эмульгированная вакцинная композиция вводится подкожно несушкам домашней птицы.
В другом варианте осуществления настоящее изобретение относится к способу экстракции и концентрирования иммуноглобулинов из яичного желтка от кур, ранее иммунизированных вакцинной композицией в соответствии с настоящим изобретением, характеризующемуся следующими этапами:
a) Желток разбавляют 1:4 или 1:8 (без яичного белка) 0,01% азидом натрия и хранят в холодильнике в течение по меньшей мере 24 часов.
b) Супернатант отделяют и добавляют фталат гидроксипропилметилцеллюлозы (НРМСР) 1-15% в 0,25 мл на каждые 100 мл соотношения желтка. Оставляют в покое в течение как минимум 24 часов.
c) Липидный слой, образованный в верхней части, отделяют от раствора и водную часть фильтруют.
d) Добавляют PEG, предпочтительно PEG 8000, в соотношении 5-30% P/V, смешивают и оставляют в покое в течение по меньшей мере 4-12 часов при 4°C.
e) Центрифугируют в течение 20-30 мин и супернатант удаляют.
f) Полученную таблетку солюбилизируют буфером PBS IX или TRIS в объеме, эквивалентном 10% от первоначального объема, поддерживая pH на уровне 7.
В дополнительном варианте осуществления, целью настоящего изобретения является концентрированная композиция иммуноглобулинов IgY птичьего происхождения, полученная путем экстракции, обезжиривания и концентрирования иммуноглобулинов из яичного желтка от кур, ранее гипериммунизированных с помощью эмульгированной вакцины по изобретению. Указанная концентрированная композиция птичьего происхождения по изобретению может дополнительно содержать примерно 70-85% воды и/или примерно 0,001-0,03% консервантов. В частности, концентрированная композиция иммуноглобулинов IgY характеризуется тем, что она содержит 0,8-5% концентрированных иммуноглобулинов IgY, нейтрализующих вирус, вызывающий PRRS.
Кроме того, в зависимости от выбранного антигена или антигенов настоящее изобретение также относится к применению концентрированной композиции иммуноглобулинов IgY птичьего происхождения в соответствии с изобретением при получении лекарственного средства для лечения репродуктивно-респираторного синдрома свиней (PRRS), свиной эпидемической диареи (PED), синдрома белого пятна у креветок, коровьего мастита, инфекций, вызванных Actinobacillus pleuropneumoniae у свиней, кокцидиоза у домашней птицы, интоксикаций, вызванных триптотеками, в частности, вызванных такими трикотеценами, как 4-дезоксиниваленол (DON), причем лекарственное средство может вводиться парентерально, предпочтительно внутримышечно или перорально и с пищей, если это применимо.
В следующих примерах показаны результаты применения концентрированной композиции по изобретению у свиней. Несмотря на это, указанные примеры представлены только в качестве иллюстрации и не должны рассматриваться как ограничения.
ПРИМЕР 1
Приготовили две вакцины, каждая из которых содержала три штамма вируса PRRS, с использованием композиции без Marcol и хитозана. Эти вакцины вводились раз в месяц и поочередно домашней птице; это означает, что одну вакцину вводили один месяц, а другую - в следующем месяце, и так далее.
После иммунизации яйца иммунизированной домашней птицы собирали и подвергали способу экстракции иммуноглобулина из яичного желтка, как описано выше.
В результате вышеуказанной иммунизации была получена композиция с иммуноглобулинами IgY, нейтрализующими вирус PRRS, но с низкой концентрацией.
На Фиг. 1 показаны результаты этого эксперимента (группа А), в которых можно отметить низкую эффективность иммуноглобулинов IgY, нейтрализующих вирус PRRS, ранее полученной композиции, неспособной обеспечить эффективное лечение свиней, страдающих репродуктивным и респираторным синдромом свиней, так как требуется использование объемов более 5 мл, которые защищают 104 титров. Кроме того, этот эксперимент оказался сложным и проблематичным из-за работы с двумя вакцинами.
ПРИМЕР 2
Приготовили одну вакцину, содержащую шесть различных штаммов вируса PRRS, с использованием композиции без масла Marcol и хитозана, которую вводили домашней птице по программе ежемесячной иммунизации.
После иммунизации яйца иммунизированной домашней птицы собирали и подвергали способу экстракции иммуноглобулина из яичного желтка, как описано выше.
В результате вышеупомянутой иммунизации эффективность по сравнению с экспериментом из Примера 1 была улучшена, но не была достаточной (см. Фиг. 1, группа В).
В результате этого эксперимента установили, что иммуноглобулины IgY, нейтрализующие работу вируса PRRS, не подходят для эффективного лечения свиней, страдающих репродуктивно-респираторным синдромом.
ПРИМЕР 3
Снова была составлена одна вакцина, но теперь с использованием Marcol в качестве легкого минерального масла и хитозана в качестве дисперсного адъюванта. На этот раз в одну единственную вакцину были включены антигены 6 штаммов вируса PRRS.
После иммунизации яйца иммунизированной домашней птицы собирали и подвергали способу экстракции иммуноглобулина из яичного желтка, как описано выше.
Результаты показывают, что титры антител увеличиваются вдвое по сравнению с результатами, полученными с композицией из эксперимента, приведенного в Примере 2 (см. Фиг. 2, группа С).
На Фигурах 1 и 2 показаны результаты этого эксперимента, в которых можно отметить, что эффективность иммуноглобулинов IgY, нейтрализующих вирус PRRS, соответственно увеличивается при использовании композиции с Marcol и хитозаном, что подходит для эффективного лечения свиней, страдающих репродуктивно-респираторным синдромом.
ПРИМЕР 4
В этом примере проанализировали конечный продукт иммуноглобулинов. Провели иммунизацию несушек домашней птицы, яйца иммунизированной домашней птицы собирали и яичные желтки подвергали способу экстракции и концентрировании иммуноглобулинов, как описано выше. Вакцины, используемые для иммунизации стада, были такими же, как в примерах 1-3, но в этом случае размер партии был увеличен до 10000 яиц на стадо.
Результаты показывают, что описанный выше способ концентрирования увеличивает титры антител по сравнению с полученными титрами без применения указанного способа. Увеличение концентрации составляет от 1,6 до 2,1 раза (Фиг. 3). В результате этого эксперимента авторами было установлено, что эффективность иммуноглобулинов IgY, нейтрализующих вирус PRRS, подходит для выполнения эффективного лечения свиней, страдающих репродуктивным и респираторным синдромом, при использовании меньшего объема для достижения защиты.
ПРИМЕР 5
Применение иммуноглобулинов (тип IgY) у самок племенного стада
Продольный мониторинг наличия антител против вируса PRRS проводился путем оценки сывороток от 30 случайно выбранных свиноматок с фермы полного цикла с 500 свиноматками, расположенной в Западной Мексике. Эта ферма производит молочных поросят, которые отрицательны к вирусу PRRS и заражены на протяжении всей продуктивной жизни.
Племенное стадо обрабатывали путем введения 1 мл концентрированной композиции иммуноглобулинов IgY птичьего происхождения в соответствии с изобретением внутримышечно, раз в 4 месяца и одно повторение в течение 15 дней. Затем еженедельно вводили в дни 70 и 85 беременности.
С целью определения вирусного движения раз в два месяца проводился мониторинг племенных свиноматок. Образцы крови брали у тех же 30 изначально отобранных животных. Для оценки использовали метод ELISA (IDEXX, PRRS Х3), который является косвенным способом измерения эффективности лечения с помощью концентрированных IgY. С помощью набора измеряются уровни антител типа IgG, продуцируемых свиньей в ответ на виремию. Таким образом, если свинья инфицирована, она будет продуцировать антитела типа IgG в качестве ответа, и будут получены значения S/P выше, чем точка отсечки, но, если виремия отсутствует, набор будет выдавать значения S/P ниже, чем точка отсечки. Точка отсечки для ELISA составила 0,4 S/P.
На Фигуре 4 показано, что при лечении, примененном к стаду, уровни антител постепенно снижаются по результатам двухмесячного мониторинга и, таким образом, видно, что вирус PRRS нейтрализован введенными иммуноглобулинами (тип IgY), тем самым ограничивая инфекцию. Стоит отметить, что, как ни удивительно, предлагаемый продукт нейтрализовал вирус таким образом, что через 6 месяцев повторное заражение вирусом PRRS не было зафиксировано. Это показывает существенную разницу между продуктивными параметрами отрицательных и положительных хозяйств.
ПРИМЕР 6
Применение концентрированных иммуноглобулинов (IgY) у молочных поросят
В этом примере приводятся результаты оценки снижения виремии у молочных поросят с клиническими признаками вируса PRRS. У молочных поросят не проявлялась виремия в течение периода материнства (первые 3 недели). Тем не менее, наблюдались клинические признаки виремии в возрасте примерно 6-8 недель. Это было подтверждено методом ПЦР в реальном времени, в котором было получено 5 пулов сывороток от виремических животных; каждый пул содержал сыворотку 5 различных свиней (всего оценивали 25 свиней). Как видно из таблицы, вирусная нагрузка достигала титров от 6,16×105 до 2,24×107.
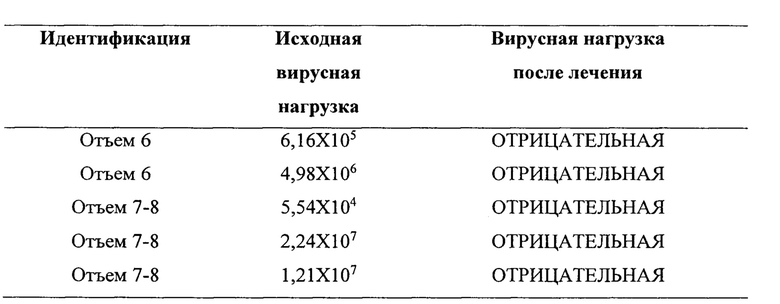
После подтверждения виремии поросятам вводили концентрированную композицию птичьего происхождения для лечения в соответствии с изобретением. 3-мл дозу вводили внутримышечно. Для оценки эффективности лечения наблюдали клинические данные и определяли количество циркулирующего вируса у свиней.
Результаты мониторинга через 10 дней после введения концентрированной композиции с иммуноглобулинами IgY птичьего происхождения согласно изобретению показали, что 100% образцов дали отрицательный результат на наличие генетического материала вируса PRRS в сыворотке.
Полученные результаты показывают, что применение иммуноглобулинов, согласно программе, в племенном стаде предотвращает циркуляцию вируса и может нейтрализовать виремию у отъемных молочных поросят при нагрузках 107 вирусных частиц на мл.
ПРИМЕР 7
Применение концентрированных иммуноглобулинов IgY снижает смертность молочных поросят
Концентрированную композицию с иммуноглобулинами IgY птичьего происхождения в соответствии с изобретением вводили отнятым и предназначенным для откорма свиньям. В течение всего производственного времени смертность регистрировалась при различных системах лечения.
Ферма, на которой проводились исследования, расположена в регионе Среднего Запада Мексики и имеет в репродуктивном стаде 1100 свиноматок и еженедельное производство 500 молочных поросят. Ферма имеет историю эндемичной инфекции PRRS даже при наличии нескольких стратегий контроля. Имеется система автоматической замены, которая предполагает введение свиноматок каждые четыре месяца. Племенное стадо включает введение модифицированной живой вирусной вакцины против PRRS каждые три месяца.
В этом примере проводился еженедельный мониторинг, и процент смертности рассчитывался как при отъеме (с 3 по 9 неделю), так и при откорме (с 10 по 26 неделю).
Сравнивались два вида лечения. Один базировался на живой вакцине, а другой - на концентрированных композициях иммуноглобулинов IgY птичьего происхождения в соответствии с изобретением, кроме того, рассматривался также не подвергавшийся иммунизации контрольный блок. Каждый вид лечения включал разные группы, которые оценивались независимо; группы 01-06 соответствуют молочным поросятам, которых лечили традиционно (живой вакциной), группы 07-16 представляли собой группы, которые получали две дозы концентрированной композиции иммуноглобулинов IgY птичьего происхождения в соответствии с изобретением, а группы 17, 18 и 19 не получали лечения.


На Фигуре 5 показан мониторинг смертности, начиная с 3 недели и до 26 недели. Группы, которые получали лечение концентрированной композицией иммуноглобулинов IgY птичьего происхождения в соответствии с изобретением, выделены блоком более интенсивного синего цвета (группы 07-16).
Средняя смертность в контрольных группах в процентах была самой высокой (25,06), далее следуют группы, которые получали традиционное лечение (в среднем 21,2%); лучшим лечением было лечение концентрированной композицией иммуноглобулинов IgY птичьего происхождения в соответствии с настоящим изобретением, где средняя смертность составила 10,27%. Это означает, что при использовании иммуноглобулинов IgY по изобретению достигается выживаемость почти 90% животных, подвергавшихся лечению, что представляет 10% от выживаемости, достигнутой методом вакцинации.
На Фигуре 6 показана диаграмма суммарной смертности в процентах для каждой оцениваемой группы, на которой выделены группы, подвергавшиеся лечению концентрированной композицией птичьего происхождения в соответствии с изобретением.
Результаты применения концентрированных иммуноглобулинов типа Ig показывают значительное снижение показателей смертности, связанных с вирусом PRRS. Кроме того, было отмечено, что состояние здоровья и продуктивность этих животных также улучшились, в отличие от групп, которые получали вакцину. Важно отметить, что это первый случай, когда доказано применение иммуноглобулинов птиц в лечении молочных поросят.
Эти результаты очень важны, так как программа с концентрированной композицией иммуноглобулинов IgY птичьего происхождения в соответствии с изобретением не только снижает показатели смертности, но также дает возможность дальнейшего улучшения параметров производства.
Таким образом, следует понимать, что, хотя конкретные варианты осуществления настоящего изобретения были описаны здесь в целях иллюстрации, могут быть выполнены различные модификации без отхода от сущности и объема изобретения. Соответственно, изобретение ограничивается только прилагаемой патентной формулой.




Группа изобретений относится к ветеринарии и касается вакцинных композиций. Предложены: эмульгированная вакцинная композиция для иммунизации птиц к вирусу репродуктивно-респираторного синдрома свиней (PRRS), содержащая: (i) антигены вируса PRRS, (ii) легкое минеральное масло Marcol и (iii) дисперсный адъювант, выбранный из группы, состоящей из биоразлагаемых полимерных частиц, микрочастиц или наночастиц, представляющий собой хитозан, причем антигены имеют титр выше, чем DIE50% 104/мл, её применение при приготовлении концентрированной композиции иммуноглобулинов IgY для лечения PRRS; концентрированная композиция иммуноглобулинов IgY, нейтрализующих вирус, вызывающий PRRS, способ её получения и её применение для производста лекарственного средства для лечения PRRS. Технический результат: повышенные титры антител IgY к вирусу PRRS, повышенная эффективность иммуноглобулинов IgY, нейтрализующих вирус PRRS, отсутствие повторных заражений молочных поросят указанным вирусом в течение 6 месяцев и снижение их смертности. 5 н. и 15 з.п. ф-лы, 6 ил., 2 табл., 7 пр.
1. Эмульгированная вакцинная композиция для иммунизации птиц к вирусу репродуктивно-респираторного синдрома свиней (PRRS), содержащая: (i) антигены вируса репродуктивно-респираторного синдрома свиней (PRRS), (ii) легкое минеральное масло и (iii) дисперсный адъювант, выбранный из группы, состоящей из биоразлагаемых полимерных частиц, микрочастиц или наночастиц, причем дисперсный адъювант представляет собой хитозан, а минеральное масло представляет собой Marcol, и причем антигены имеют титр выше, чем DIE50% 104/мл.
2. Эмульгированная вакцинная композиция по п. 1, отличающаяся тем, что антигены выделены из одного или нескольких различных изолированных штаммов одного или нескольких вирусов, включая вирус PRRS.
3. Эмульгированная вакцинная композиция по п. 2, отличающаяся тем, что изолированные штаммы вируса PRRS имеют нуклеотидную последовательность гена ORF5, выбранную из группы, состоящей из SEQ. ID. NO: 1, SEQ. ID. NO: 2, SEQ. ID. NO: 3, SEQ. ID. NO: 4, SEQ. ID. NO: 5, SEQ. ID. NO: 6 и SEQ. ID. NO: 7.
4. Эмульгированная вакцинная композиция по любому из пп. 1-3, отличающаяся тем, что антигены, выделенные из штаммов вируса репродуктивно-респираторного синдрома свиней (PRRS), выбраны с титром сыворотки ниже 1:160, оценены с помощью перекрестной микронейтрализации с использованием пула иммуноглобулинов, полученного с помощью существующей вакцины.
5. Эмульгированная вакцинная композиция по любому из пп. 1-4, дополнительно содержащая эмульгирующий агент.
6. Эмульгированная вакцинная композиция по п. 5, отличающаяся тем, что эмульгирующий агент выбирают из группы, состоящей из: полиоксиэтиленмоноолеата сорбитана (Tween 80), сорбитанмоноолеата сорбитана (Span 80) или их смеси.
7. Применение эмульгированной вакцинной композиции по любому из пп. 1-6 при приготовлении концентрированной композиции иммуноглобулинов IgY, пригодной для лечения репродуктивно-респираторного синдрома свиней (PRRS).
8. Применение по п. 7, отличающееся тем, что эмульгированная вакцинная композиция может вводиться подкожно птицам-несушкам.
9. Способ экстракции, обезжиривания и концентрирования иммуноглобулинов из яичных желтков от кур, гипериммунизированных эмульгированной вакцинной композицией по пп. 1-6, отличающийся тем, что он включает следующие этапы:
a) Желток разбавляют 1:4 или 1:8 (без яичного белка) 0,01% азидом натрия и хранят в холодильнике в течение по меньшей мере 24 часов;
b) Супернатант отделяют и добавляют фталат гидроксипропил метилцеллюлозы (НРМСР) в количестве 1-15% в 0,25 мл на каждые 100 мл желтка. Оставляют в покое в течение по меньшей мере 24 часов;
c) Липидный слой, образованный в верхней части, отделяют от раствора и водную часть фильтруют;
d) Добавляют PEG в соотношении 5-30% об., смешивают и оставляют в покое в течение по меньшей мере 4-12 часов при 4°С;
e) Центрифугируют в течение 20-30 мин и супернатант удаляют;
f) Полученную таблетку солюбилизируют буфером PBS 1X или TRIS в объеме, эквивалентном 10% от исходного объема.
10. Способ экстракции, обезжиривания и концентрирования иммуноглобулинов по п. 9, отличающийся тем, что яичный желток, разбавленный 1:4 или 1:8 (без яичного белка) 0,01% азидом натрия на этапе (а), хранят в холодильнике в течение 12-24 часов.
11. Способ экстракции, обезжиривания и концентрирования иммуноглобулинов по п. 9, отличающийся тем, что на этапе (d) добавляют PEG8000 в соотношении 5-30% об., смешивают и оставляют в покое в течение по меньшей мере 4-12 часов при 4°С.
12. Концентрированная композиция иммуноглобулинов IgY птичьего происхождения, полученная с помощью способа по любому из пп. 9-11.
13. Концентрированная композиция иммуноглобулинов IgY птичьего происхождения по п. 12, отличающаяся тем, что содержит от 0,8% до 5% иммуноглобулинов IgY, нейтрализующих вирус, вызывающий PRRS.
14. Концентрированная композиция иммуноглобулинов IgY птичьего происхождения по п. 13, отличающаяся тем, что содержит 1% иммуноглобулинов IgY, нейтрализующих вирус, вызывающий PRRS.
15. Концентрированная композиция иммуноглобулинов IgY птичьего происхождения по любому из пп. 12-14, дополнительно содержащая от 70 до 85% воды.
16. Концентрированная композиция иммуноглобулинов IgY птичьего происхождения по любому из пп. 12-15, дополнительно содержащая от 0,001 до 0,03% консервантов.
17. Применение концентрированной композиции иммуноглобулинов IgY птичьего происхождения по любому из пп. 12-15 при приготовлении лекарственного средства для лечения репродуктивного и респираторного синдрома свиней (PRRS).
18. Применение по п. 17, отличающееся тем, что лекарственное средство пригодно для парентерального введения.
19. Применение по п. 18, отличающееся тем, что лекарственное средство пригодно для внутримышечного введения.
20. Применение по п. 17, отличающееся тем, что лекарственное средство пригодно для перорального введения и с пищей.
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| CN 101428145 A, 13.05.2009 | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| ШТАММ "ВНИВИП-ДЕП" ДЛЯ ПОЛУЧЕНИЯ ВАКЦИНЫ ПРОТИВ РЕОВИРУСНОГО ТЕНОСИНОВИТА КУР | 1998 |
|
RU2158304C2 |
| PAULY D | |||
| et al | |||
| IgY technology: extraction of chicken antibodies from egg yolk by polyethylene glycol (PEG) precipitation | |||
| J.Vis.Exp | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
Авторы
Даты
2019-05-28—Публикация
2014-08-22—Подача