ОБЛАСТЬ ТЕХНИКИ
[0001]
Настоящее изобретение относится к новым антителам к TSLP-рецептору человека.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[0002]
Тимусный стромальный лимфопоэтин (TSLP) является цитокином, продуцируемым эпителиальными клетками в ответ на провоспалительные стимулы. В основном, TSLP усиливает аллергический воспалительный ответ посредством активации дендритных клеток и тучных клеток. Дендритные клетки экспрессируют TSLP-рецептор и α-цепь IL-7-рецептора, которые являются членами семейства гемопоэтических рецепторов, и TSLP связывается с гетеродимером, состоящим из TSLP-рецептора и α-цепи IL-7-рецептора, тем самым активируя дендритные клетки. Дендритные клетки, активированные TSLP, экспрессируют воспалительные хемокины, такие как регулируемый тимусом и активацией хемокин (TARC (CCL17)), хемокин макрофагального происхождения (MDC (CCL22)) и им подобные белки (Nat. Immunol., 2002, Vol. 7, p. 673-680). Известно, что TARC и MDC являются Th2-хемокинами и связываются с Th2-клетками в месте воспаления (Int. Immunol., 1999, Vol. 11, p. 81-88). Далее, дендритные клетки, активированные TSLP, индуцируют дифференцировку наивных T-клеток в Тh2-клетки, а Тh2-клетки продуцируют IL-4, IL-5, IL-13 и TNF, и вызывают воспалительную реакцию (Nat. Immunol., 2002, Vol. 7, p. 673 to 680).
[0003]
Сообщалось о том, что активация дендритных клеток посредством TSLP через такие TSLP-рецепторы участвует в патологии заболеваний, включая такие аллергические воспалительные заболевания, как астма и системный склероз.
[0004]
Что касается астмы, то ранее сообщалось, что в трансгенных мышах, в которых экспрессия TSLP усилена специфично в легких, вызванный воспалительный ответ в дыхательных путях сопровождается увеличением количества IgE и Th2-цитокинов в легких, и это ведет к астматической патологии (Nat. Immunol., 2005, Vol. 6, p. 1047-1053). Кроме того, в мышах нокаутных по TSLP-рецептору или в модели астмы, в которой вводятся антитела к TSLP-рецептору, наблюдалось снижение продукции Th2-цитокинов и IgE в крови и улучшение респираторных функций ((J. Exp. Med., 2005, Vol. 202, p. 829-839 и Clin. Immunol., 2008, Vol. 129. p. 202-210). В дополнение, сообщалось, что у пациентов, страдающих астмой, экспрессия TSLP, TARC и MDC увеличивалась в астматических дыхательных путях, коррелируя с тяжестью заболевания (J. Immunol., 2005, Vol. 174, p. 8183-8190 и J. Immunol., 2008, Vol. 181, p. 2790-2798).
[0005]
В отношении системного склероза сообщалось, что TSLP сверхэкспрессирован в коже у пациентов с системным склерозом (Arthritis Rheum., 2013, Vol. 65, p. 1335-1346), и что экспрессия IL-13 и IL-17 в воспаленном участке кожи была почти полностью подавлена, а доля коллагена в гистопатологии была значительно улучшена в блеомицин-индуцированной модели склеродермы с использованием мышей нокаутных по TSLP-рецептору (Ann. Rheum. Dis., 2013, Vol. 72, p. 2018-2023).
[0006]
Соответственно, когда может быть разработано моноклональное антитело, которое специфично связывается с TSLP-рецептором человека и ингибирует действие TSLP человека через TSLP-рецептор, ожидается, что такое антитело будет полезным для профилактики и лечения различных заболеваний, при которых TSLP человека и TSLP-рецептор человека вовлечены в патологию болезни.
[0007]
В качестве антител к TSLP-рецептору человека, для которых исследования уже ведутся, опубликованы 13H5 как мышиное моноклональное антитело и hu13H5 как его гуманизированное антитело (патентный документ 1), 1D6.C9 как мышиное моноклональное антитело и Nv115-3B-IgG1 и NV115-3B-IgG4 как его химерные антитела (патентный документ 1), NV164-2 и NV163-1 как полностью человеческие антитела (патентный документ 3), и TSLPR-012_141 как гуманизированное моноклональное антитело, полученное в хомяке.
[0008]
В 13H5, нейтрализующая активность подтверждена в методе анализа TSLP-индуцированной пролиферации с использованием клеток линии Ba/F3, стабильно экспрессирующих TSLP-рецептор, но нейтрализующая активность hu13H5 до сих пор не подтверждена (патентный документ 1). Дополнительно, основываясь на описании патентных документов 2-4, из антител, описанных в этих документах, TSLPR-4_8 имеет наивысшую нейтрализующую активность (патентные документы 2-4). TSLPR-012_012 было оценено с помощью различных тестов на нейтрализующую активность. Например, в методе анализа TSLP-индуцированной пролиферации с использованием клеток Ba/F3, стабильно экспрессирующих TSLP-рецептор, в методе анализа TSLP-индуцированной продукции TARC, MDC и IL-8 с использованием полученных из периферической крови дендритных клеток человека, в методе анализа TSLP-индуцированной продукции Th2-цитокинов с использованием полученных из периферической крови дендритных клеток человека и в системах совместного культивирования с наивными T-клетками и т.п. было подтверждено, что TSLPR-141_141 демонстрируют нейтрализующую активность (патентный документ 2). Однако в качестве лекарственного антитела желательно использовать антитело с наивысшей нейтрализующей активностью.
[0009]
Основные факторы, определяющие эффективную дозировку препарата антитела включают в себя связывающую активность и нейтрализующую активность антитела против антигена, а также количество антигена, которое присутствует в организме. Увеличение связывающей активности и нейтрализующей активности приводит к снижению дозировки, и, как следствие, приводит к сокращению финансового бремени и медицинских расходов пациентов, являясь крайне полезными улучшениями.
[0010]
Таким образом, для профилактики и лечения различных заболеваний необходимо получить антитело к TSLP-рецептору человека, которое превосходит по активности обычные антитела к TSLP-рецептору человека.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
ПАТЕНТНЫЙ ДОКУМЕНТ
[0011]
[Патентный документ 1] WO с 2009/100324
[Патентный документ 2] WO с 2007/112146
[Патентный документ 3] WO с 2008/155365
[Патентный документ 4] WO с 2012/007495
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ПРОБЛЕМЫ, РЕШАЕМЫЕ С ПОМОЩЬЮ ИЗОБРЕТЕНИЯ
[0012]
Задачей настоящего изобретения является создание антитела к TSLP-рецептору человека, которое специфично связывается с TSLP-рецептором человека и ингибирует действие TSLP человека через TSLP-рецептор человека.
СРЕДСТВА РЕШЕНИЯ ПРОБЛЕМ
[0013]
В результате интенсивных исследований авторов настоящего изобретения по получению антитела к TSLP-рецептору человека, было предложено антитело к TSLP-рецептору человека, содержащее вариабельную область тяжелой цепи, состоящую из аминокислотной последовательности с номерами аминокислот 1-118 из SEQ ID NO: 1, и вариабельную область легкой цепи, состоящую из аминокислотной последовательности с номерами аминокислот 1-108 из SEQ ID NO: 3. Было выявлено, что антитело к TSLP-рецептору человека ингибирует экспрессию мРНК TARC и продукцию белка MDC, индуцированную TSLP (примеры 5 и 6), и подавляет аллергическую реакцию в модели сенсибилизации к аскаридному антигену у обезьян (пример 7), посредством чего настоящее изобретение было выпонено.
[0014]
А именно, настоящее изобретение включает в себя следующие материалы или способы, которые являются полезными в медицине или промышленности:
(1) Антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент, содержащие вариабельную область тяжелой цепи, состоящую из аминокислотной последовательности с номерами аминокислот 1-118 из SEQ ID NO: 1, и вариабельную область легкой цепи, состоящую из аминокислотной последовательности с номерами аминокислот 1-108 из SEQ ID NO: 3.
(2) Антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент по п.(1) выше, где константная область тяжелой цепи антитела представляет собой константную область Igγ1 человека.
(3) Антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент по п.(1) выше, где константная область легкой цепи антитела представляет собой константную область Igκ человека.
(4) Антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент по п.(1) выше, где константная область тяжелой цепи антитела представляет собой константную область Igγ1 человека, и константная область легкой цепи антитела представляет собой константную область Igκ человека.
(5) Антигенсвязывающий фрагмент по любому одному из пп.(1)-(4) выше, где антигенсвязывающий фрагмент представляет собой одноцепочечный фрагмент вариабельной области, Fab, Fab’ или F(ab’)2.
(6) Антитело к TSLP-рецептору человека по п.(1) выше, содержащее тяжелую цепь, состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 1, и легкую цепь, состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 3.
(7) Антитело к TSLP-рецептору человека по п.(1) выше, содержащее тяжелую цепь, состоящую из аминокислотной последовательности с номерами аминокислот 1-447 из SEQ ID NO: 1, и легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 3.
(8) Полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи антитела по п.(1) выше.
(9) Полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область легкой цепи антитела по п.(1) выше.
(10) Экспрессионный вектор, содержащий полинуклеотид по п.(8) и/или (9) выше.
(11) Клетка-хозяин, трансформированная экспрессионным вектором по п.(10) выше, которая выбрана из группы, состоящей из пп.(a)-(d):
(a) Клетка-хозяин, трансформированная экспрессионным вектором, содержащим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи антитела к TSLP-рецептору человека по п.(1) выше, и полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область легкой цепи этого антитела;
(b) Клетка-хозяин, трансформированная экспрессионным вектором, содержащим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи антитела к TSLP-рецептору человека по п.(1) выше, и экспрессионным вектором, содержащим нуклеотидную последовательность, кодирующую вариабельную область легкой цепи этого антитела;
(c) Клетка-хозяин, трансформированная экспрессионным вектором, содержащим полинуклеотид, содержащий нуклеотидную последовательность вариабельной области тяжелой цепи антитела к TSLP-рецептору человека по п.(1) выше; и
(d) Клетка-хозяин, трансформированная экспрессионным вектором, содержащим полинуклеотид, содержащий нуклеотидную последовательность вариабельной области легкой цепи антитела к TSLP-рецептору человека по п.(1) выше.
(12) Клетка-хозяин, трансформированная экспрессионным вектором из (10) выше, которые были отобраны из группы состоящей из (a) до (d):
(a) Клетка-хозяин, трансформированная экспрессионным вектором, содержащим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи антитела к TSLP-рецептору человека по п.(6) выше, и полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область легкой цепи этого антитела;
(b) Клетка-хозяин, трансформированная экспрессионным вектором, содержащим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи антитела к TSLP-рецептору человека по п.(6) выше, и экспрессионным вектором, содержащим полинуклиотид, содержащий нуклеотидную последовательность, кодирующую легкую цепь этого антитела;
(c) Клетка-хозяин, трансформированная экспрессионным вектором, содержащим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую тяжелую цепь антитела к TSLP-рецептору человека по п.(6) выше; и
(d) Клетка-хозяин, трансформированная экспрессионным вектором, содержащим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую легкую цепь антитела к TSLP-рецептору человека по п.(6) выше.
(13) Способ получения антитела к TSLP-рецептору человека или его антигенсвязывающего фрагмента, который включает культивирование клеток-хозяев по п.(11) выше для экспрессии антитела к TSLP-рецептору человека или его антигенсвязывающего фрагмента.
(14) Способ получения антител к TSLP-рецептору человека, который включает культивирование клетки-хозяина по п.(12) выше для экспрессии антитела к TSLP-рецептору человека.
(15) Антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент, получаемые способом по п.(13) выше.
(16) Антитело к TSLP-рецептору человека, получаемое способом по п.(14) выше.
(17) Фармацевтическая композиция, содержащая антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент по любому одному из пп.(1)-(7), (15) и (16) выше и фармацевтически приемлемый наполнитель.
(18) Фармацевтическая композиция по п.(17) выше, которая представляет собой фармацевтическую композицию для профилактики или лечения астмы.
(19) Способ профилактики или лечения астмы, который включает введение терапевтически эффективного количества антитела к TSLP-рецептору человека или его антигенсвязывающего фрагмента по любому одному из пп.(1)-(7), (15) и (16) выше.
(20) Антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент по любому одному из пп.(1)-(7), (15) и (16) выше для применения при профилактики или лечении астмы.
(21) Антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент по любому одному из пп.(1)-(7), (15) и (16) выше для производства фармацевтической композиции для профилактики или лечения астмы.
Антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент по пп.(1)-(7), (15) и (16) выше включающий в себя слитый белок антитела или его антигенсвязывающего фрагмента с другим пептидом или белком и модификации, включающие модифицирующий агент, связанный с ними.
ЭФФЕКТЫ ИЗОБРЕТЕНИЯ
[0015]
Антитело к TSLP-рецептору человека по настоящему изобретению связывается с TSLP-рецептором человека, обладает нейтрализующей активностью в отношении действия TSLP человека через рецептор TSLP человека и может использоваться в качестве агента для профилактики и лечения аллергических воспалительных заболеваний, таких как астма или системный склероз.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0016]
[Фиг. 1] На фиг.1 показана ингибирующая активность полностью человеческого антитела T7-27 на концентрацию IgE, специфичных к аскаридному антигену, в модели сенсибилизации аскаридным антигеном у обезьян. Вертикальная ось представляет относительную плазматическую концентрацию IgE, специфичных к аскаридному антигену, для соответствующих образцов, когда плазматическая концентрация IgE, специфичных к аскаридному антигену, на 22-й день от одного индивидуума из группы носителя принята за 2000 Ед./мл. Показаны концентрация IgE в 1-й день в группе носителя и группе, которой вводили антитело (до введения жидкого аскаридного антигена, ресуспендированного в алюминий-гидроксидном геле), концентрация IgE на 22-й день в группе носителя и концентрация IgE на 22-й день в группе, которой вводили антитело.
[Фиг. 2] На фиг.2 показано ингибирующее действие полностью человеческого T7-27 специфичную на аскаридный антиген кожную реакцию в модели сенсибилизации аскаридным антигеном у обезьян. Показаны результаты введения фосфатно-солевого буфера (PBS) и 100 мкг/мл раствора аскаридного антигена на 22-й день. Вертикальная ось представляет величину (дельту в мм), являющуюся результатом вычитания диаметра кожной реакции, вызванной PBS из диаметра кожной реакции, вызванной раствором аскаридного антигена.
[Фиг. 3] На фиг. 3 показано ингибирующее действие антитела к TSLP-рецептору на реакцию гиперреактивности дыхательных путей в мышиной модели астмы. Вертикальная ось представляет значение PenH, используемое в качестве показателя функции дыхания (**p<0,01, *p<0,05, ##p<0,01, #p<0,05).
[Фиг. 4] На фиг. 4 показано ингибирующее действие антитела к TSLP-рецептору на инфильтрацию эозинофилов в мышиной модели астмы. Вертикальная ось представляет количество эозинофилов в клеточной суспензии BALF (**p<0,01).
[Фиг. 5] На фиг. 5 показано ингибирующее действие антитела к TSLP-рецептору на экспрессию мРНК TARC в мышиной модели астмы. Вертикальная ось представляет уровень экспрессии мРНК TARC.
Варианты осуществления изобретения
[0017]
Далее, настоящее изобретение будет описано более подробно.
[0018]
Существует пять классов антител: IgG, IgM, IgA, IgD и IgE, и базовая структура молекулы антитела состоит из тяжелых цепей с молекулярной массой от 50000 до 70000 и легких цепей с молекулярной массой от 20000 до 30000 в общем для каждого класса. Тяжелая цепь, которая обычно состоит из полипептидной цепи, содержащей 440 аминокислотных остатков, имеет характерную структуру для каждого из классов, и называется Igγ, Igμ, Igα, Igδ и Igε по аналогии с IgG, IgM, IgA, IgD и IgE, соответственно. Дополнительно, IgG включает четыре подкласса IgG1, IgG2, IgG3, и IgG4, и их тяжелые цепи соответственно называются Igγ1, Igγ2, Igγ3 и Igγ4. Легкая цепь обычно содержит 220 аминокислотных остатков, среди которых известно два типа, тип L и тип K, и они называются Igλ и Igκ. В белковой конфигурации базовой структуры молекул антител две гомологичные тяжелые цепи и две гомологичные легкие цепи связаны дисульфидными (S-S связи) и нековалентными связями, и их молекулярный вес составляет от 150000 до 190000. Два типа легких цепей могут быть связаны с любой тяжелой цепью. Соответствующие молекулы антитела, как правило, состоят из двух идентичных легких цепей и двух идентичных тяжелых цепей.
[0019]
Касательно внутренних S-S связей, в тяжелой цепи присутствуют четыре S-S связи (пять в Igμ и Igε), и две из них присутствуют в легкой цепи; одна петля образуется на 100-110 аминокислотных остатков, и данная пространственная структура сходна у всех петель и называется структурной единицей или доменом. Домен, расположенный на аминоконцевой (N-концевой) стороне обоих тяжелой и легкой цепи, аминокислотная последовательность которого не постоянна даже в случае представителей одного класса (подкласса) из одного и того же животного, называется вариабельной областью, и соответствующие домены называются вариабельной областью тяжелой цепи (VH) и вариабельной областью легкой цепи (VL). Аминокислотная последовательность с карбоксильной (C-концевой) стороны от вариабельной области почти неизменна для каждого класса или подкласса и называется константной областью (каждый из доменов называется CH1, CH2, CH3 и CL, соответственно).
[0020]
Участок распознавания антигена в антителе состоит из VH и VL, и его специфичность связывания зависит от аминокислотной последовательности в данном участке. С другой стороны, такие виды биологической активности, как связывание с системой комплемента и различными клетками, отражают различия в структурах константных обрастей среди разных классов Ig. Известно, что изменчивость вариабельных областей легких и тяжелых цепей в основном лимитирована тремя небольшими гипервариабельными областями, присутствующими в обоих цепях, и эти области называются определяющими комплементарность областями (CDR: CDR1, CDR2 и CDR3 начиная с N-конца). Остальной участок вариабельной области называется каркасной областью (FR) и является относительно постоянной.
[0021]
Кроме того, различные виды антигенсвязывающих фрагментов, содержащих VH и VL антитела, имеют антигенсвязывающую активность. Например, одноцепочечный фрагмент вариабельной области (scFv), Fab, Fab’ и F(ab’)2 приведены в качестве примеров типичных антигенсвязывающих фрагментов. Fab является моновалентным антигенсвязывающим фрагментом, который образован легкой цепью и фрагментом тяжелой цепи, включающим в себя VH, CH1 и участок шарнирной области. Fab’ является моновалентным антигенсвязывающим фрагментом, который образован легкой цепью и фрагментом тяжелой цепи, включающим в себя VH, CH1 и участок шарнирной области, и остатки цистеина, образующие S-S связи между тяжелыми цепями, включены в участок шарнирной области. F(ab’)2 является бивалентным антигенсвязывающим фрагментом, имеющим димерную структуру, в которой два Fab’-фрагмента связаны друг с другом посредством S-S связей в шарнирной области. scFv является моновалентным антигенсвязывающим фрагментом, который состоит из VH и VL, соединенных при помощи линкерного пептида.
[0022]
<Антитело к TSLP-рецептору человека по настоящему изобретению>
Антитело к TSLP-рецептору человека или его антигесвязывающий фрагмент по настоящему изобретению представляет собой антитело к TSLP-рецептору человека или его антигесвязывающий фрагмент, имеющие следующие характеристики.
Антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент, содержащие вариабельную область тяжелой цепи, состоящую из аминокислотной последовательности с номерами аминокислот 1-118 из SEQ ID NO: 1, и вариабельную область легкой цепи, состоящую из аминокислотной последовательности с номерами аминокислот 1-108 из SEQ ID NO: 3.
[0023]
Предпочтительно, чтобы антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент по настоящему изобретению имели вышеописанные характеристики и дополнительно содержали константную область тяжелой цепи и константную область легкой цепи. В качестве константной области могут быть выбраны любые подклассы константных областей (например, константная область Igγ1, Igγ2, Igγ3 или Igγ4 в качестве константной области тяжелой цепи и константные области Igλ или Igκ в качестве константных областей легкой цепи), но предпочтительна константная область Igγ1 человека в качестве константной области тяжелой цепи и константная область Igκ человека в качестве константной области легкой цепи.
[0024]
Константная область Igγ1 человека включает в себя, например, константную область Igγ1 человека, состоящую из аминокислотной последовательности с номерами аминокислот 119-448 из SEQ ID NO:1.
[0025]
Константная область Igκ человека включает в себя, например, константную область Igκ человека, состоящую из аминокислотной последовательности с номерами аминокислот 109-214 из SEQ ID NO:3.
[0026]
Кроме того, в качестве антитела к TSLP-рецептору человека или его антигенсвязывающего фрагмента по настоящему изобретению, предпочтительным является антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент, содержащие описанную выше вариабельную область тяжелой цепи и вариабельную область легкой цепи, в которых константной областью тяжелой цепи является константная область Igγ1 человека, а константной областью легкой цепи является константная область Igκ человека.
[0027]
В одном варианте осуществления антигенсвязывающим фрагментом по настоящему изобретению является scFv, Fab, Fab’, или F(аb’)2.
[0028]
Любой специалист в данной области может сконструировать антитело или его антигенсвязывающий фрагмент, слитые с другим пептидом или белком, а так же может сконструировать модификацию, имеющую связанный с ней модифицирующий агент, используя известные в данной области способы. Антитело или его антигенсвязывающий фрагмент по настоящему изобретению включает антитело или его антигенсвязывающий фрагмент в форме такого слитого белка или модификации. Например, антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент, содержащие вариабельную область тяжелой цепи, состоящую из аминокислотной последовательности с номерами аминокислот 1-118 из SEQ ID NO: 1, и вариабельную область легкой цепи, состоящую из аминокислотной последовательности с номерами аминокислот 1-108 из SEQ ID NO: 3, включает антитело или его антигенсвязывающий фрагмент, слитые с другим пептидом или белком, и модификацию, при которой модифицирующий агент связан с ними. Другой пептид или белок, используемый для слияния, конкретно не ограничен, при условии, что он не снижает связывающую активность антитела или его антигенсвязывающего фрагмента; их примеры включают сывороточный альбумин человека, различные тэговые пептиды, искусственный пептиды со спиральными мотивами, мальтозосвязывающие белки, глутатион-S-трансферазу, различные токсины, другие пептиды или белки, способные содействовать мультимеризации, и т.п. Модифицирующий агент, используемый для модификации, конкретно не ограничен, при условии, что он не снижает связывающую активность антитела или его антигенсвязывающего фрагмента; их примеры включают полиэтиленгликоль, цепи сахаров, фосфолипиды, липосомы, низкомолекулярные соединения и т.п.
[0029]
В одном варианте осуществления антитело к TSLP-рецептору человека по настоящему изобретению является антителом к TSLP-рецептору человека, имеющим следующие характеристики.
Антитело к TSLP-рецептору человека, содержащее тяжелую цепь, состоящую из аминокислотной последовательности, представленной в в SEQ ID NO: 1, и легкую цепь, состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 3.
[0030]
В случае, когда антитело экспрессируется в клетках, известно, что антитело модифицируется после трансляции. Примеры посттрансляционной модификации включают в себя удаление лизина с С-конца тяжелой цепи посредством карбоксипептидазы, модификацию глутаминовой кислоты или глутамина на N-конце тяжелой цепи в пироглутаминовую кислоту посредством пироглутаминирования и т.п. Известно, что лизин на C-конце тяжелой цепи удален, и большая часть глутамина на N-конце тяжелой цепи модифицирована в пироглутаминовую кислоту (Journal of Pharmaceutical Sciences, 2008, Vol. 97, p. 2426). Кроме того, также известно, что модификация после трансляции не влияет на активность антитела в данной области (Analytical Biochemistry, 2006, Vol. 348, p. 24-39).
[0031]
Антитело по настоящему изобретению включает в себя антитело, модифицированное после трансляции во время экспрессии в клетках, такое как антитело, содержащее удаленный с C-конца тяжелой цепи лизин, антитело, в котором глутамин или глутаминовая кислота на N-конце тяжелой цепи модифицированы в пироглутаминовую кислоты посредством пироглутаминирования, и т.п. в дополнении к актителу, содержащему полноразмерную тяжелую цепь. Дополнительно, антигенсвязывающий фрагмент по настоящему изобретению включает в себя антигенсвязывающий фрагмент, модифицированный после трансляции во время экспрессии в клетках, такой как антигенсвязывающий фрагмент, в котором глутамин или глутаминовая кислота на N-конце тяжелой цепи модифицированы в пироглутаминовую кислоты посредством пироглутаминирования.
[0032]
Например, антитело к TSLP-рецептору человека по изобретению включает в себя антитело к TSLP-рецептору человека, описанное ниже.
Антитело к TSLP-рецептору человека, содержащее тяжелую цепь, состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 1, в которой глутаминовая кислота в позиции 1 в SEQ ID NO: 1 модифицирована в пироглутаминовую кислоту и/или удален лизин с аминокислотным номером 448 в SEQ ID NO: 1, и легкую цепь, состояющу из аминокислотной последовательности, представленной в SEQ ID NO: 3.
[0033]
Настоящее изобретение включает антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент, имеющее следующие характеристики.
Антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент, содержащие вариабельную область тяжелой цепи, содержащую CDR1, состоящую из аминокислотной последовательности с номерами аминокислот 31-35 из SEQ ID NO: 1, CDR2, состоящую из аминокислотной последовательности с номерами аминокислот 50-66 из SEQ ID NO: 1, и CDR3, состоящую из аминокислотной последовательности с номерами аминокислот 99-107 из SEQ ID NO:1, и вариабельную область легкой цепи, содержащую CDR1, состоящую из аминокислотной последовательности с номерами аминокислот 24-34 из SEQ ID NO: 3, CDR2, состоящую из аминокислотной последовательности с номерами аминокислот 50-56 из SEQ ID NO: 3, и CDR3, состоящую из аминокислотной последовательности с номерами аминокислот 89-97 из SEQ ID NO:3.
[0034]
Антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент по настоящему изобретению связывается с TSLP-рецептором человека. Как для антитела, так и для его антигенсвязывающего фрагмента, связывание с TSLP-рецептором человека подтверждают с использованием способа измерения активности связывания в данной области. Примеры способов измерения активности связывания включают способ твердофазный иммуноферментный анализ (ELISA) или способ поверхностного плазмонного резонанса (SPR). В случае использования ELISA, в использованном для примера способе, слитый белок TSLP-рецептора и Fc человека (слитый белок TSLP-рецептор человека-Fc человека (кодируется нуклеотидной последовательностью SEQ ID NO: 5)) иммобилизуется на ELISA-планшете, а исследуемое антитело добавляются к нему для прохождения реакции. После реакции, проводят взаимодействие с вторичным антителом, таким как анти-IgG антитело и т.п., меченным ферментом, таким как пероксидаза хрена (HRP), и отмывают его, после чего можно подтвердить, связывается ли исследуемое антитело с TSLP-рецептором человека с помощью измерения активности с использованием реагента для обнаружения активности (например, в случае мечения HRP - BM-хемилюсцентного ELISA-субстрата (POD) (Roche Diagnostics. Inc.)). В случае использования SPR, например, возможно использование Biacore (зарегистрированная торговая марка) 2000 (GE Healthcare Japan Corporation). В использованном для примера способе, исследуемое антитело иммобилизовано на поверхности сенсорного чипа, а слитый белок TSLP-рецептора человека и мышиного Fc (слитый белок TSLP-рецептор человека-Fc мыши (кодируется нуклеотидной последовательностью SEQ ID NO: 6)) добавляется в поток. Подтвердить, связывается ли тестируемое антитело с TSLP-рецептором человека, можно, анализируя константу скорости связывания (ka), константу скорости диссоциации (kd), и константу диссоциации (KD) между антителом и TSLP-рецептором человека.
[0035]
Дополнительно, антитело или его антигенсвязывающий фрагмент по настоящему изобретению включают антитело или его антигенсвязывающий фрагмент, связывающиеся с TSLP-рецептором, полученным из других животных (например, TSLP-рецептором обезьяны) и связывающая активность с этими рецепторов может быть измерена с использованием этих же способов.
[0036]
Предпочтительно, чтобы антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент по настоящему изобретению связывались с TSLP-рецептором человека и имели нейтрализующую активность в отношении TSLP-рецептора человека. Нейтрализующая активность в отношении TSLP-рецептора человека означает активность, ингибирующую любую биологическую активность TSLP путем связывания с TSLP-рецептором человека, и может быть оценена на основе одной или нескольких биологических активностей TSLP человека через TSLP-рецептор человека в качестве показателя. Примеры такой нейтрализующей активности включают ингибирующую активность в отношении TSLP-индуцированной экспрессии мРНК TARC и ингибирующую активность в отношении TSLP-индуцированной продукции белка MDC с использованием мононуклеарных клеток периферической крови человека (PBMC), а способы, описанные в примерах 5 и 6 ниже, могут быть использованы в качестве специфичных способов оценки.
[0037]
Для более детальной оценки эффектов антитела к TSLP-рецептору человека или его антигенсвязывающего фрагмента по настоящему изобретению можно использовать исследования in vivo. Например, в примере 7, приведенном ниже, описано, что можно оценить эффекты антитела к TSLP-рецептору человека in vivo с помощью теста на подавление аллергической реакции с использованием модели сенсибилизации аскаридным антигеном у обезьян.
[0038]
Антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент по изобретению могут быть легко получены специалистом в данной области с использованием известного способа в данной области на основе информации о последовательности вариабельной области тяжелой цепи и вариабельной области легкой цепи антитела к TSLP-рецептору человека по изобретению, описанного в настоящей спецификации. Антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент по настоящему изобретению конкретно не ограничены, но они могут быть получены в соответствии со способом, описанным в разделе <Способ получения антитела к TSLP-рецептору человека по изобретению>, приведенном ниже.
[0039]
Антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент по настоящему изобретению дополнительно очищают при необходимости и вводят в рецептуру в соответствии с обычным способом. Они могут быть использованы для профилактики или лечения заболеваний, при которых TSLP человека и TSLP-рецептор человека участвуют в патологии заболевания, включающего аллергические воспалительные заболевания, такие как астма и системный склероз.
[0040]
<Полинуклеотид по настоящему изобретению>
Полинуклеотид по настоящему изобретению включает полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи антитела к TSLP-рецептору человека по настоящему изобретению, и полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область легкой цепи антитела к TSLP-рецептору человека по настоящему изобретению.
[0041]
В одном варианте осуществления полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи антитела к TSLP-рецептору человека по настоящему изобретению, представляет собой полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи, состоящую из аминокислотной последовательности с номерами аминокислот 1-118 из SEQ ID NO: 1.
[0042]
Полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи, представленную аминокислотной последовательностью с номерами аминокислот 1-118 из SEQ ID NO: 1, включает, например, полинуклеотид, содержащий нуклеотидную последовательность с номерами оснований 1-354 из SEQ ID NO: 2.
[0043]
В предпочтительном варианте осуществления полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи антитела к TSLP-рецептору человека по настоящему изобретению, представляет собой полинуклеотид, содержащий нуклеотидную последовательность, кодирующую тяжелую цепь, состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 1.
[0044]
Полинуклеотид, содержащий нуклеотидную последовательность, кодирующую тяжелую цепь, состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 1, включает, например, полинуклеотид, содержащий нуклеотидную последовательность, представленную в SEQ ID NO: 2.
[0045]
В одном варианте осуществления полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область легкой цепи антитела к TSLP-рецептору человека по настоящему изобретению, представляет собой полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область легкой цепи, состоящую из аминокислотной последовательности с номерами аминокислот 1-108 из SEQ ID NO: 3.
[0046]
Полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область легкой цепи, состоящую из аминокислотной последовательности с номерами аминокислот 1-108 из SEQ ID NO: 3, включает, например, полинуклеотид, содержащий нуклеотидную последовательность с номерами оснований 1-324 из SEQ ID NO: 4.
[0047]
В предпочтительном варианте осуществления полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область легкой цепи антитела к TSLP-рецептору человека по настоящему изобретению, представляет собой полинуклеотид, содержащий нуклеотидную последовательность, кодирующую легкую цепь, состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 3.
[0048]
Полинуклеотид, содержащий нуклеотидную последовательность, кодирующую легкую цепь, состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 3, включает, например, полинуклеотид, содержащий нуклеотидную последовательность, представленную в SEQ ID NO: 4.
[0049]
Полинуклеотид по настоящему изобретению может быть легко получен специалистом в данной области с использованием известного способа в данной области на основании нуклеотидной последовательности. Например, полинуклеотид по настоящему изобретению может быть синтезирован с использованием известного способа синтеза генов в данной области. Способы синтеза генов, включают, например, различные способы, известные специалистам в данной области, такие как способ синтеза генов антител, описанный в WO90/07861.
[0050]
<Экспрессионный вектор по настоящему изобретению, трансформированная клетка-хозяин по настоящему изобретению, способ получения антитела к TSLP-рецептору человека по настоящему изобретению и полученное этим способом антитело к TSLP-рецептору человека>
Экспрессионный вектор по настоящему изобретению включает экспрессионный вектор, включающий полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи антитела к TSLP-рецептору человека по настоящему изобретению, и/или полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область легкой цепи антитела к TSLP-рецептору человека по настоящему изобретению.
[0051]
Предпочтительные экспрессионные векторы по настоящему изобретению, включают экспрессионный вектор, содержащий полинуклеотид, содержащий нуклеотидную последовательность, кодирующую тяжелую цепь антитела к TSLP-рецептору человека по настоящему изобретению, экспрессионный вектор, содержащий полинуклеотид, содержащий нуклеотидную последовательность, кодирующую легкую цепь антитела к TSLP-рецептору человека по настоящему изобретению, или экспрессионный вектор, содержащий полинуклеотид, содержащий нуклеотидную последовательность, кодирующую тяжелую цепь антитела к TSLP-рецептору человека по настоящему изобретению, и полинуклеотид, содержащий нуклеотидную последовательность, кодирующую легкую цепь этого антитела.
[0052]
Экспрессионный вектор, используемый для экспрессии полинуклеотида по настоящему изобретению, конкретно не ограничен, при условии что полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи антитела к TSLP-рецептору человека по настоящему изобретению, и/или полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область легкой цепи антитела к TSLP-рецептору человека по настоящему изобретению, могут быть проэкспрессированы в различных эукариотических клетках-хозяевах (например, клетках животных, клетках насекомых, клетках растений и дрожжей) и/или прокариотических клетках-хозяевах (например, Escherichia coli), и могут быть получены кодируемые ими полипептиды. Примеры экспрессионных векторов включают плазмидные векторы, вирусные векторы (например, аденовирусные или ретровирусные) и т.п. Предпочтительно использование pEE6.4 или pEE12.4 (Lonza, Inc.). Кроме того, гены антител могут быть проэкспрессированы путем переноса фрагмента гена вариабельной области в экспрессионные векторы, уже содержащие константные области генов Ig человека, такие как AG-γ1 или AG-κ (например, см WO94/20632).
[0053]
Экспрессионный вектор по настоящему изобретению может включать промотор, который функционально связан с полинуклеотидом по настоящему изобретению. Примеры промотора для экспрессии полинуклеотида по изобретению в клетках животных включают полученные из вирусов промоторы, такие как CMV, RSV, или SV40, промотор актина, промотор EF1α (фактора элонгации 1α) и промотор белка теплового шока. Примеры промоторов для экспрессии в бактериях (например, в Escherichia) включают в себя Trp-промотор, lac-промотор, λPL-промотор и tac-промотор. Кроме того, примеры промоторов для экспрессии в дрожжах включают GAL1-промотор, GAL10-промотор, PH05-промотор, PGK-промотор, GAP-промотор и ADH-промотор.
[0054]
Трансформированная клетка-хозяин по настоящему изобретению включает в себя клетку-хозяина, трансформированную экспрессионным вектором по настоящему изобретению, которая выбрана из группы, состоящей из следующих пп.(а)-(d):
(а) клетка-хозяин, трансформированная экспрессионным вектором, включающим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи антитела к TSLP-рецептору человека по настоящему изобретению, и полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область легкой цепи этого антитела;
(b) клетка-хозяин, трансформированная экспрессионным вектором, включающим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи антитела к TSLP-рецептору человека по настоящему изобретению, и экспрессионным вектором, включающим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область легкой цепи этого антитела;
(c) клетка-хозяин, трансформированная экспрессионным вектором, включающим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи антитела к TSLP-рецептору человека по настоящему изобретению; и
(d) клетка-хозяин, трансформированная экспрессионным вектором, включающим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую вариабельную область легкой цепи антитела к TSLP-рецептору человека по настоящему изобретению.
[0055]
В одном варианте осуществления трансформированная клетка-хозяин по настоящему изобретению представляет собой клетку-хозяина, трансформированную экспрессионным вектором по настоящему изобретению, которая выбрана из группы, состоящей из следующих пп.(а)-(d):
(a) клетка-хозяин, трансформированная экспрессионным вектором, включающим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую тяжелую цепь антитела к TSLP-рецептору человека по настоящему изобретению, и полинуклеотид, содержащий нуклеотидную последовательность, кодирующую легкую цепь этого антитела;
(b) клетка-хозяин, трансформированная экспрессионным вектором, включающим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую тяжелую цепь антитела к TSLP-рецептору человека по настоящему изобретению, и экспрессионным вектором, включающим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую легкую цепь этого антитела;
(c) клетка-хозяин, трансформированная экспрессионным вектором, включающим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую тяжелую цепь антитела к TSLP-рецептору человека по настоящему изобретению; и
(d) клетка-хозяин, трансформированная экспрессионным вектором, включающим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую легкую цепь антитела к TSLP-рецептору человека по настоящему изобретению.
[0056]
В случае использования клетки животного, клетки насекомого, или дрожжей в качестве клетки-хозяина, экспрессионный вектор по настоящему изобретению может содержать кодон инициации и кодон терминации. В этом случае экспрессионный вектор по настоящему изобретению может содержать энхансерную последовательность, нетранслируемую область на 5'-стороне и 3'-стороне генов, кодирующих антитело по настоящему изобретению или вариабельную область тяжелой цепи или вариабельную область легкой цепи, секреторную сигнальную последовательность, сплайсинговое соединение, сайт полиаденилирования или репликон. При использовании Escherichia coli в качестве клетки-хозяина, экспрессионный вектор по настоящему изобретению может содержать кодон инициации, кодон терминации, терминаторную область и репликон. В этом случае экспрессионный вектор по данному изобретению может содержать селективный маркер (например, гены устойчивости к тетрациклину, гены устойчивости к ампициллину, гены устойчивости к канамицину, гены устойчивости к неомицину или гены дигидрофолатредуктазы), который обычно используется при необходимости.
[0057]
Предпочтительные примеры трансформированной клетки-хозяина по настоящему изобретению включают в себя клетку-хозяина, трансформированную экспрессионным вектором, включающим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую тяжелую цепь антитела к TSLP-рецептору человека по настоящему изобретению, и полинуклеотид, содержащий нуклеотидную последовательность, кодирующую легкую цепь этого антитела, и клетку-хозяина, трансформированную экспрессионным вектором, включающим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую тяжелую цепь антитела к TSLP-рецептору человека по настоящему изобретению, и экспрессионным вектором, включающим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую легкую цепь этого антитела.
[0058]
Трансформированная клетка-хозяин особо не ограничена, при условии что клетка-хозяин подходит для используемого экспрессионного вектора, трансформирована экспрессионным вектором и может экспрессировать антитело. Примеры трансформированной клетки-хозяина включают различные клетки, такие как природные клетки или искусственно созданные клетки, которые обычно используются в области настоящего изобретения (например, клетки животных (например, клетки СНО-K1SV), клетки насекомых (например, Sf9), бактерии (например, Escherichia), дрожжи (например, Saccharomyces или Pichia) и т.п.). Предпочтительно использовать культивируемые клетки, такие как клетки СНО-K1SV, клетки СНО-DG 44, клетки 293 или клетки NS0.
[0059]
Способ трансформации клетки-хозяина конкретно не ограничен, но, например, можно использовать кальций-фосфатный способ или электропорационный способ.
[0060]
Способы получения антитела к TSLP-рецептору человека или его антигенсвязывающего фрагмента по настоящему изобретению включают в себя способ получения антитела к TSLP-рецептору человека или его антигенсвязывающего фрагмента, который включает культивирование трансформированной клетки-хозяина по настоящему изобретению для экспрессии антитела к TSLP-рецептору человека или его антигенсвязывающего фрагмента.
[0061]
Антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент по настоящему изобретению включает антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент, полученные способом получения антитела к TSLP-рецептору человека или его антигенсвязывающего фрагмента по настоящему изобретению.
[0062]
Способ получения антитела к TSLP-рецептору человека или его антигенсвязывающего фрагмента по настоящему изобретению конкретно не ограничен, при условии что способ включает культивирование трансформированной клетки-хозяина по настоящему изобретению для экспрессии антитела к TSLP-рецептору человека или его антигенсвязывающего фрагмента. Предпочтительная клетка-хозяин, используемая в способе, включает в качестве предпочтительного примера трансформированную клетку-хозяина по настоящему изобретению, которая описано выше.
[0063]
Трансформированные клетки-хозяева можно культивировать с помощью известных способов. Условия культивирования, например, температуру, рН культуральной среды и время культивирования, выбирают соответственно. В случае, когда клетка-хозяин представляет собой животную клетку, примеры культуральной среды включают культуральную среду MEM, содержащую приблизительно от 5% до 20% фетальной бычьей сыворотки (Science, 1959, Vol. 130, No. 3373, p. 432-7), культуральную среду DMEM (Virology, 1959, Vol. 8, p. 396), а также культуральную среду RPMI 1640 (J. Am. Med. Assoc., 1967, Vol. 199, p. 519) и культуральную среду 199 (Exp. Biol. Med., 1950, Vol. 73, p. 1-8). Значение рН культуральной среды, предпочтительно, составляет приблизительно от 6 до 8, а культивирование обычно проводят при температуре приблизительно 30°C-40°C в течение приблизительно 15-72 часов при вентиляции воздухом и перемешивании при необходимости. В случае, когда клетка-хозяин представляет собой клетку насекомого, в качестве культуральной среды, например, может использоваться культуральная среда Грейса (Proc. Natl. Acad. Sci. USA, 1985, Vol. 82, p. 8404), дополненная фетальной бычьей сывороткой. Значение рН культуральной среды, предпочтительно, составляет приблизительно о5-8, а культивирование обычно проводят при температуре приблизительно 20°C-40°C в течение приблизительно 15-100 часов при вентиляции воздухом и перемешивании при необходимости. В случае, когда клетка-хозяин представляет собой Escherichia coli или дрожжи, в качестве культуральной среды, например, подходит жидкая культуральная среда, содержащая источник питательных веществ. Предпочтительно, чтобы питательная культуральная среда включала источник углерода, неорганический источник азота или органический источник азота, необходимые для роста трансформированной клетки-хозяина. Примеры источника углерода включают глюкозу, декстран, растворимый крахмал, сахарозу, а примеры неорганического источника азота или органического источника азота включают соли аммония, нитратные соли, аминокислоты, жидкий кукурузный экстракт, пептон, казеин, мясной экстракт, соевый жмых и картофельный экстракт. Другие питательные вещества (например, неорганические соли (например, хлорид кальция, дигидрофосфат натрия и хлорид магния), витамины и антибиотики (например, тетрациклин, неомицин, ампициллин и канамицин)) могут быть включены по желанию. Значение рН культуральной среды, предпочтительно, составляет приблизительно от 5 до 8. В случае, когда клетка-хозяин представляет собой Escherichia coli, предпочтительные примеры культуральной среды включают культуральную среду LB и культуральную среду M9 (Mol. Clo., Cold Spring Harbor Laboratory, Vol. 3, A2.2). Культивирование обычно проводят при температуре приблизительно 14°C-43°C в течение приблизительно 3-24 часов при вентиляции воздухом и перемешивании при необходимости. В случае, когда клетка-хозяин представляет дрожжи, в качестве культуральной среды, например, может быть использована минимальная среда Беркхолдера (Proc. Natl. Acad, Sci, USA, 1980, Vol. 77, p. 4505). Культивирование обычно проводят при температуре приблизительно 20°C-35°C в течение приблизительно 14-144 часов при вентиляции воздухом и перемешивании при необходимости. При проведении культивирования вышеописанным способом можно экспрессировать антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент по настоящему изобретению.
[0064]
В дополнение к культивированию трансформированных клеток-хозяев по настоящему изобретению для экспрессии антитела к TSLP-рецептору человека или его антигенсвязывающего фрагмента способ получения антитела к TSLP-рецептору человека или его антигенсвязывающего фрагмента по настоящему изобретению может включать в себя выделение, предпочтительно экстракцию или очистку, антитела к TSLP-рецептору человека или его антигенсвязывающего фрагмента из трансформированных клеток-хозяев. Примеры способа выделения или очистки включают способы, в которых используется растворимость, такие как высаливание и способ осаждения растворителем; способы, в которых используется различие в молекулярной массе, такие как диализ, ультрафильтрация, гель-фильтрация; способы, в которых используется электрический заряд, такие как ионообменная хроматография и гидроксилапатитная хроматография; способы, в которых используется специфическое сродство, такие как аффинная хроматография; способы, в которых используется различие в гидрофобности, такие как обращеннофазовая высокоэффективная жидкостная хроматография; и способы, в которых используются отличия в изоэлектрических точках, такие как изоэлектрофокусирующий форез. Предпочтительно, чтобы антитела, накапливающиеся в культуральном супернатанте, можно было очищать с помощью различных хроматографических методов, например, колоночной хроматографией с использованием колонки с белком A или колонки с белком G.
[0065]
<Фармацевтическая композиция по настоящему изобретению>
Фармацевтические композиции по настоящему изобретению включают в себя фармацевтическую композицию, содержащую антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент по настоящему изобретению и фармацевтически приемлемые вспомогательные вещества. Фармацевтическая композиция по настоящему изобретению может быть получена обычно используемым способом с вспомогательными веществами, а именно, с вспомогательными веществами для медицины или с носителями для медицины, обычно используемыми в данной области. Примеры лекарственных форм фармацевтических композиций включают парентеральные препараты, такие как препараты для инъекций и препараты для капельного вливания, и они могут быть введены внутривенно, подкожно или аналогичным путем. При получении лекарственных препаратов, вспомогательные вещества, носители и добавки в соответствии с лекарственной формой могут быть использованы в фармацевтически приемлемом диапазоне.
[0066]
Фармацевтические композиции по настоящему изобретению могут включать в себя множество видов антител к TSLP-рецептору человека или их антигенсвязывающих фрагментов по настоящему изобретению. Например, настоящее изобретение включает фармацевтическую композицию, содержащую антитело, в котором удален лизин на C-конце тяжелой цепи, антитело или его антигенсвязывающий фрагмент с посттрансляционной модификацией на N-конце, антитело, в котором удален лизин на C-конце тяжелой цепи и проведена посттрансляционная модификация на N-конце, и/или антитело, которое имеет лизин на С-конце тяжелой цепи и не имеет посттрансляционной модификации на N-конце.
[0067]
Например, фармацевтическая композиция по настоящему изобретению, содержащая антитело к TSLP-рецептору человека по настоящему изобретению, включает в себя фармацевтическую композицию, содержащую два или несколько видов антитела к TSLP-рецептору человека по пп.(1)-(4) ниже.
(1) Антитело к TSLP-рецептору человека, включающее тяжелую цепь, состоящую из аминокислотной последовательности с номерами аминокислот 1-447 из SEQ ID NO: 1, и легкую цепь, состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 3.
(2) Антитело к TSLP-рецептору человека, включающее тяжелую цепь, которая состоит из аминокислотной последовательности, представленной в SEQ ID NO: 1, в которой глутаминовая кислота с аминокислотным номером 1 модифицирована в пироглутаминовую кислоту, и легкую цепь, состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 3.
(3) Антитело к TSLP-рецептору человека, включающее тяжелую цепь, которая состоит из аминокислотной последовательности с номерами аминокислот 1-447 из SEQ ID NO: 1, в которой глутаминовая кислота с аминокислотным номером 1 модифицирована в пироглутаминовую кислоту, и легкую цепь, состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 3.
(4) Антитело к TSLP-рецептору человека, включающее тяжелую цепь, состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 1, и легкую цепь, состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 3.
[0068]
Количество антитела к TSLP-рецептору или его антигенсвязывающего фрагмента по настоящему изобретению, добавляемое в лекарственный препарат, варьирует в зависимости от степени выраженности симптомов пациента, возраста пациента, используемой лекарственной формы препарата, титра связывания антитела и т.п., и, например, может быть использовано добавляемое количество со приблизительно от 0,001 мг/кг до 100 мг/кг.
[0069]
Фармацевтическая композиция по настоящему изобретению может быть использована в качестве фармацевтической композиции для профилактики или лечения заболеваний, при которых TSLP человека и TSLP-рецептор человека участвуют в патологии заболевания, таких как астма.
[0070]
Настоящее изобретение включает фармацевтическую композицию для профилактики или лечения астмы, содержащую антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент по настоящему изобретению. Кроме того, настоящее изобретение включает способ профилактики или лечения астмы, включающий введение терапевтически эффективного количества антитела к TSLP-рецептору человека или его антигенсвязывающего фрагмента по настоящему изобретению. Дополнительно, настоящее изобретение включает антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент по настоящему изобретению для применения в профилактике или лечении астмы. Дополнительно, настоящее изобретение включает использование антитела к TSLP-рецептору человека или его антигенсвязывающего фрагмента по настоящему изобретению для производства фармацевтической композиции для профилактики или лечения астмы.
[0071]
Настоящее изобретение было описано в общем смысле, а для лучшего понимания будут приведены конкретные примеры, на которые дается ссылка, но они являются только примерами и не ограничивают настоящее изобретение.
[Примеры]
[0072]
В отношении частей, в которых используются коммерчески доступные наборы или реактивы, тесты проводятся в соответствии с прилагаемым протоколом, если не указано иное. Кроме того, для удобства, концентрация моль/л выражена как М. Например, 1 М водный раствор гидроксида натрия означает 1 моль/л водного раствора гидроксида натрия.
[0073]
(Пример 1: получение слитого белка TSLP-рецептор-Fc)
Для оценки связывающей активности антитела были получены слитый белок TSLP-рецептора человека и Fc человека (слитый белок TSLP-рецептор человека-Fc человека), слитый белок TSLP-рецептор человека и Fc мыши (слитый белок TSLP-рецептор человека-Fc мыши) и слитый белок TSLP-рецептора обезьяны и Fc человека (слитый белок TSLP-рецептор обезьяны-Fc человека). Ген слитого белка TSLP-рецептора человека-Fc человека (SEQ ID NO: 5), ген слитого белка TSLP-рецептора человека-Fc мыши (SEQ ID NO: 6) и ген слитого белка TSLP-рецептора обезьяны-Fc человека (SEQ ID NO: 7), соответственно, рекомбинировали с вектором для экспрессии в клетках млекопитающих, GS-вектором pEE12.4 (Lonza, Inc.). Полученными векторами трансфецировали клетки FreeStyle 293 (Life Technologies, Inc.) с использованием трансфекционного реагента 293fectin (Life Technologies, Inc.), и клетки культивировали в бессывороточной культуральной системе использованием экспрессионной среды FREESTYLE 293 (Life Technologies, Inc.) в течение одной недели, а затем, соответственно, были получены супернатанты, содержащие слитый белок TSLP-рецептора человека-Fc человека, слитый белок TSLP-рецептора человека-Fc мыши и слитый белок TSLP-рецептора обезьяны-Fc человека. Соответствующие слитые белки TSLP-рецептор-Fc очищали с использованием колонки для очистки белков - колонки с белком G (GE Healthcare Corporation Japan) из полученных культуральных супернатантов.
[0074]
(Пример 2: получение мутированных белков TSLP с Flag-тегом)
Для оценки нейтрализующей активности антитела были получены мутированный белок TSLP человека с Flag-тегом (мутированный TSLP человека-Flag) и мутированный белок TSLP обезьяны с Flag-тегом (мутированный TSLP обезьяны-Flag). Ген мутированного TSLP человека или обезьяны с Flag-тегом (SEQ ID NO: 8 или 9 (которые, соответственно, кодируют аминокислотные последовательности TSLP дикого типа человека или обезьяны, в которые для предупреждения потери активности вследствие расщепления фуриновой протеазой была внесена мутация в сайт расщепления), соответственно, рекомбинировали с GS-вектором pEE12.4. Полученными векторами трансфицировали клетки FreeStyle 293 с использованием 293fectin, и клетки культивировали в бессывороточной культуральной системе с использованием экспрессионной среды FreeStyle 293 в течение одной недели, а затем, соответственно, получали культуральные супернатанты, содержащие мутированный белок TSLP человека с Flag-тегом или мутированный белок TSLP обезьяны с Flag-тегом. Соответствующие мутированные белки TSLP с Flag-тегом очищали из полученных культуральных супернатантов с помощью аффинного геля с анти-FLAG антителом M2 (Sigma, Inc.).
[0075]
(Пример 3: получение полностью человеческого антитела к TSLP-рецептору человека)
Мышь из технологии получения моноклональных антител человека, "VelocImmune" (технология получения антител VelocImmune, Regeneron, Inc. (патент США № 6596541)) иммунизировали адъювантом для стимуляции иммунного ответа, TSLP рецептором человека-Fc (R & D, Inc.) и экспрессирующими TSLP-рецептор человека клетками Ba/F3 (полученными путем переноса векторов, кодирующих ген TSLP-рецептора человека (SEQ ID NO: 10) и ген α-цепи IL-7-рецептора человека (SEQ ID NO: 11), в мышиные клетки Ba/F3 (RIKEN: RCB0805)). В соответствии с обычным способом выделяли селезенку или лимфатический узел иммунизированной мыши, собирали лимфоциты и сливали с клетками мышиной миеломы SP2/0 (ATCC CRL-1581), таким образом получая гибридомы. Гибридомы моноклонизировали, а затем культивировали в гибридомной культуральной среде CD (Life Technologies, Inc.), которая является бессывороточной средой. Антитела очищали из полученных культуральных супернатантов с использованием набора для очистки антител Protein G Purification kit (Proteus, Inc.).
[0076] Для оценки связывающей активности антител, соответственно проводили ELISA с использованием слитого белка TSLP-рецептора человека-Fc человека и слитого белка TSLP-рецептора обезьяны-Fc человека, полученных в примере 1. Кроме того, для оценки нейтрализующей активности антител, проводили анализ ингибирования роста клеток на клетках Ba/F3, экспрессирующих TSLP-рецептор человека, при стимуляции мутированными белками TSLP обезьяны с Flag-тегом, полученными в примере 2, и проводили анализ ингибирования продукции белка MDC на цельной крови обезьяны при стимуляции мутированными белками TSLP обезьяны с Flag-тегом, полученными в примере 2.
[0077]
С помощью описанных выше тестов было выявлено, что антитело (химерное антитело), именуемое T7-27, имело связывающую активность и нейтрализующую активность в отношении TSLP-рецепторов человека и обезьяны. Гены, кодирующие тяжелую цепь и легкую цепь антитела из гибридомы, продуцирующей T7-27, были клонированы, и была определена их последовательность.
[0078]
В вышеописанном антителе вариабельная область получена от человека, а константная область получена от мыши. По этой причине, экспрессионные векторы, содержащие гены тяжелой цепи и легкой цепи были сконструированы с помощью GS-векторов, и было получено полностью человеческое антитело. Более конкретно, гены, кодирующие сигнальные последовательности (Nigel Whittle et al., Protein Engineering 1987; 1(6): 499 to 505.) были соединены с 5'стороной генов вариабельной области тяжелой цепи антитела T7-27, а гены константной области (состоящие из нуклеотидной последовательности с номерами оснований 355-1344 из SEQ ID NO: 2) Igγ1 человека были соединены с их 3'-стороной, а затем гены тяжелой цепи были вставлены в GS-вектор pEE6.4. Кроме того, гены, кодирующие сигнальные последовательности (Nigel Whittle et al., указано выше) были соединены с 5'-стороной генов вариабельной области легкой цепи антитела, а гены константной области (состоящие из нуклеотидной последовательности с номерами оснований 325-642 из SEQ ID NO: 4) Igκ человека были соединены с их 3'-стороной, а затем гены легкой цепи были вставлены в GS-вектор pEE12.4.
[0079]
Нуклеотидная последовательность, кодирующая тяжелую цепь полностью человеческого антитела из полученного T7-27 (полностью человеческое T7-27) показана в SEQ ID NO: 2, кодируемая ей аминокислотная последовательность показана в SEQ ID NO: 1, и нуклеотидная последовательность, кодирующая легкую цепь антитела показана в SEQ ID NO: 4, а кодируемая ей аминокислотная последовательность показано в SEQ ID NO: 3. Вариабельная область тяжелой цепи полностью человеческого T7-27 состоит из аминокислотной последовательности с номерами аминокислот 1-118 в SEQ ID NO: 1, а CDR1, CDR2 и CDR3 тяжелой цепи, соответственно, состоят из аминокислотных последовательностей с номерами аминокислот 31-35, 50-66 и 99-107 в SEQ ID NO: 1. Вариабельная область легкой цепи полностью человеческого T7-27 состоит из аминокислотной последовательности с номерами аминокислот 1-108 в SEQ ID NO: 3, а CDR1, CDR2 и CDR 3 легкой цепи, соответственно, состоят из аминокислотных последовательностей с номерами аминокислот 24-34, 50-56 и 89-97 в SEQ ID NO: 3.
[0080]
Антитело было проэкспрессировано с использованием двух вариантов способов транзиентной экспрессии и конститутивной экспрессии с описанными выше GS-векторами, в которой гены тяжелой цепи и легкой цепи антитела были, соответственно, вставлены. В случае транзиентной экспрессии, экспрессионные векторы обеих тяжелой и легкой цепей трансфицировали с использованием 293fectin в клетки FreeStyle 293, культивируемые в количестве примерно 1000000 клеток/мл в экспрессионной среде FreeStyle 293, и затем культивировали в течение 7 дней. В альтернативном варианте, экспрессионные векторы обеих тяжелой и легкой цепей, описанных выше, трансфицировали с использованием метода электропорации в примерно 10000000 клеток СНО-K1SV (Lonza, Inc.), а затем культивировали в среде CD-CHO (Life Technologies, Inc.) в течение 7 дней. Культуральные супернатанты очищали с использованием колонки с белком А или колонки с белком G (GE Healthcare Corporation Japan), и таким образом получали очищенное полностью человеческое антитело. В случае конститутивной экспрессии, GS-векторы, в которые гены тяжелой цепи и легкой цепи антитела были, соответственно, вставлены, разрезали рестриктазой по сайтам NotI и PvuI и проводили лигирование с использованием набора для лигирования Ligation-Convenience Kit (NIPPONGENE, Inc.) или лигирующего реагента Ligation-high (TOYOBO, Inc.), а затем были сконструированы GS векторы, в которые были вставлены оба гена тяжелой цепи и легкой цепи. Экспрессионные векторы кодировали полноразмерную тяжелую цепь и легкую цепь, и антитело было проэкспрессировано путем трансфекции в клетки СНО-K1SV. Культуральные супернатанты очищали с использованием колонки с белком А или колонки с белком G (GE Healthcare Corporation Japan), и таким образом получали очищенное полностью человеческое антитело. В результате анализа аминокислотной модификации очищенного полностью человеческого T7-27 было показано, что в значительной части очищенного антитела произошло удаление лизина на С-конце тяжелой цепи.
[0081]
(Пример 4: оценка связывающей активности с помощью SPR-анализа)
Для более точного измерения связывающей активности полностью человеческого T7-27 проводили SPR-анализ. В настоящем примере в качестве сравнительного антитела было использовано антитело к TSLP-рецептору человека, TSLPR-012_141 (патентный документ 4).
[0082]
В SPR-анализе, анализ проводили с использованием Biacore (зарегистрированная торговая марка) 2000 (GE Healthcare Japan Corporation). Соответствующие антитела к TSLP-рецептору человека иммобилизовали на поверхности сенсорного чипа CM5 с использованием наборов Human Antibody Capture Kit и Amine Coupling Kit (GE Healthcare Japan Corporation). Полученный в примере 1 слитый белок TSLP-рецептора человека с мышиным Fc серийно разводили раствором HBS-EP (GE Healthcare Corporation Japan), и 100 мкл раствора добавляли в поток, имеющий скорость потока 50 мкл/ мин. С помощью этой системы измерения были вычислены константа скорости связывания (ka), константа скорости диссоциации (kd) и константа диссоциации (KD) слитого белка TSLP-рецептора человека-Fc мыши и антитела к TSLP-рецептору человека с использованием программного обеспечения для анализа данных ((BIA Evaluation) (таблица 1).
Активность связывания TSLP-рецептора человека с помощью SPR-анализа
[0083]
В результате, стало ясно, что полностью человеческое T7-27 имело примерно в 3 раза более сильную связывающую активность по сравнению с TSLPR-012_141.
[0084]
(Пример 5: оценка ингибирования индуцированной TSLP экспрессии мРНК TARC с использованием РВМС человека)
Для оценки нейтрализующей активности полностью человеческого T7-27, проводили оценку ингибирования индуцированной TSLP экспрессии мРНК TARC в мононуклеарных клетках периферической крови (РВМС) человека. Поскольку РВМС человека включают дендритные клетки, экспрессирующие TSLP-рецептор, РВМС человека могут быть использованы для оценки антитела к TSLP-рецептору. В качестве сравнительного антитела использовали TSLPR-012_141. Поскольку по результатам испытательного примера 1, описанного ниже, была обнаружена корреляция между улучшением патологии в модели астмы и ингибированием в крови экспрессии мРНК TARC с использованием антитела к TSLP-рецептору, данная система оценки представляет собой систему оценки, указывающую на эффективность в отношении патологии.
[0085]
Высевали 200000 клеток РВМС человека (AllCells, Inc.) на лунку в 96-луночных планшетах (Gleiner, Inc.) в 160 мкл культуральной среды PRMI1640 (Life Technologies, Inc.). Готовили серии разведений (7 точек с конечной концентрацией в диапазоне от 0,1 нг/мл до 100 нг/мл) мутированного белка TSLP человека с Flag-тегом, полученного в примере 2, в культуральной среде RPMI164, и по 20 мкл этих разведений добавляли в культуру, а затем инкубировали в течение 24 часов в CO2-инкубаторе с установленной температурой 37°C. Затем получали соответствующие антитела к TSLP-рецептору человека в среде RPMI1640, так что конечная концентрация составляла 0,3 мкг/мл, добавляли в культуру в количестве 20 мкл и дополнительно инкубировали в течение 72 часов. В качестве контрольных образцов, соответственно, подготавливали лунку, в которую добавляли культуральную среду RPMI1640 вместо мутированного белка TSLP человека с Flag-тегом, и лунку, в которую добавляли культуральную среду RPMI1640 вместо антител. Удаляли 200 мкл культуральной жидкости, а затем общую РНК выделяли в 30 мкл воды с использованием набора RNeasy 96 (Qiagen, Inc.) для очистки РНК. Впоследствии, 10 мкл РНК использовали для реакции обратной транскрипции с использованием набора для обратной транскрипции, High Capacity cDNA Reverse Transcription Kit (Life Technologies, Inc.). Затем уровень экспрессии мРНК TARC измеряли ПЦР-способом TaqMan с использованием TaqMan-зонда для TARC (Ccl17, Hs00171074, Life technologies, Inc), TaqMan-зонда для β-актина (Actb, Hs99999903, Life Technologies, Inc.), смеси Express qPCR SuperMix (A10313, Life Technologies, Inc.) и 2 мкл кДНК. Эксперимент проводили в двух повторах для соответствующих антител, и результаты измерения были проанализированы с использованием метода сравнения СТ, а затем рассчитывали уровень экспрессии мРНК TARC. После чего была рассчитана степень ингибирования антителами при каждой концентрации TSLP. Степень ингибирования для лунки, в которую была добавлена культуральная среда RPMI1640 вместо мутированного белка TSLP человека с Flag-тегом была принята как 100%, а среднее значение для лунок, в которые были, соответственно, были добавлены 30 нг/мл и 100 нг/мл мутированного белка TSLP человека с Flag-тегом, принимали как степень ингибирования 0%. Проводили анализ рассчитанной степени ингибирования и вычисляли концентрацию TSLP, имеющую 50% степени ингибирования антителом 0,3 мкг/мл (таблица 2) путем аппроксимации трехпараметрической логарифмической кривой. Поскольку эта концентрация TSLP становится выше, нейтрализующая активность по отношению к TSLP испытуемого антитела становится сильнее.
Активность ингибирования TSLP-индуцированной экспрессии мРНК TARC с использованием РВМС
[0086]
В результате, было выяснено, что полностью человеческое антитело T7-27 имело приблизительно в 12 раз более высокую активность ингибирования индуцированной TSLP человека экспрессии мРНК TARC человека по сравнению с TSLPR-012_141.
[0087]
(Пример 6: Оценка ингибирования TSLP-индуцированной продукции белка MDC производства с использованием РВМС человека)
Проводили оценку ингибирования TSLP-индуцированной продукции белка MDC в РВМС человека для исследования нейтрализующей активности полностью человеческого антитела T7-27. В качестве сравнительного антитела использовали TSLPR-012_141.
[0088]
Кровь человека разводили равным объемом PBS и наслаивали на на такой же объем Ficoll-Paque PLUS (GE Healthcare Японии Corporation), а затем центрифугировали в течение 30 минут при комнатной температуре и 400×g, таким образом получая РВМС человека. Высевали приблизительно 300000 клеток РВМС человека на лунку в 96-луночные планшеты (Gleiner, Inc.) в 100 мкл культуральной среды PRMI1640 (Life Technologies, Inc.). Мутированный белок TSLP человека с Flag-тегом, полученный в примере 2, разводили в культуральной среде RPMI1640 таким образом, чтобы его конечная концентрация стала 5 нг/мл, и добавляли в культуру клеток в количестве 10 мкл с последующей инкубацией в течение 24 ч в CO2-инкубаторе, температура которого была установлена на 37°C. Затем подготавливали серийные разведения (5 точек с конечной концентрацией в диапазоне от 0,1 нг/мл до 10 мкг/мл) соответствующего антитела к TSLP-рецептору человека в культуральной среде RPMI164 и добавляли по 10 мкл в культуру клеток с последующей инкубацией в течение 5 дней. В качестве контрольного образца, соответственно, подготавливали лунку, в которую добавляли культуральную среду RPMI1640 вместо мутированного белка TSLP человека с Flag-тегом, и лунку, в которую добавляли культуральную среду RPMI1640 вместо антитела. Впоследствии собирали культуральные супернатанты и количество продуцируемого MDC оценивали с помощью набора Human CCL22/MDC Quantikine Kit (ELISA R&D, Inc.) с использованием супернатантов, разбавленных PBS в 20 раз (Life Technologies, Inc.). Эксперимент проводили в двух повторах для соответствующих антител и рассчитывали степень ингибирования для каждой концентрации антитела. Степень ингибирования для лунки, в которую была добавлена культуральная среда RPMI1640 вместо мутированного белка TSLP человека с Flag-тегом, была принята за 100%, а степень ингибирования в лунке, в котороую была добавлена культуральная среда RPMI1640 вместо антител, была принята за 0%. Концентрацию антитела, дающую 50% степени ингибирования, рассчитывали как IC 50 (таблица 3) путем аппроксимации трехпараметрической логарифмической кривой.
Оценка ингибирования TSLP-индуцированной продукции белка MDC с использованием РВМС человека
[0089]
В результате было выяснено, что полностью человеческое антитело T7-27 имело примерно в 9 раз более высокую активность ингибирования TSLP-индуцированной продукции белка MDC по сравнению с TSLPR-012_141.
[0090]
(Пример 7: оценка полностью человеческого T7-27 в модели сенсибилизации аскаридным антигеном обезьян)
Появление специфичных к аскаридному антигену IgE индуцируется при сенсибилизации обезьян аскаридным антигеном, а реакция кожи вызывается аллергической реакцией.
Жидкий аскаридный антиген (DNP-Ascaris (LSL, Inc.)), ресуспендированный в алюминий-гидроксидном геле (далее именуемом квасцами) (0,5 мг/мл DNP-Ascaris, ресуспендированного в PBS с концентрацией квасцов 50 мг/мл, далее именуется жидкий аскаридный антиген в квасцах) вводили в 1 день, 8-й день и 15-й день самцам яванского макака в количестве 3,6 мл/кг внутрибрюшинно и количестве 0,4 мл/кг внутримышечно для сенсибилизации. Кроме того, аналогично обработанным группам были организованы нормальная группа (необработанная группа, n=2), группа носителя (группа, которой водили растворитель (20 мМ буферный раствор цитрата натрия/120 мМ NaCl (рН 6,0)) внутривенно за один день до сенсибилизации, n=3) и группа введения антитела (группа, которой вводили 10 мг/кг полностью человеческого антитела T7-27 (разбавленного растворителем) внутривенно за один день до сенсибилизации, n=3).
Кроме того, квасцы были приготовлены следующим способом.
Сульфат алюминия (14-18-гидраты) (Wako, Inc.) растворяли в сверхчистой воде для приготовления 1М раствора, и раствор фильтровали через фильтр 0,22 мкм, а затем к нему добавляли 1М раствор гидроксида натрия (Nacalai Tesque) до тех пора, пока не выпадал белый осадок. Удаляли надосадочную жидкость, осадок промывали сверхчистой водой 5 раз, а затем дополнительно промывали PBS (WAKO, Inc.) три раза. Промытый осадок белого цвета мелко измельчали в гомогенизаторе (CH-6010, KINEMATICA, Inc.) при охлаждении льдом, с последующим центрифугированием в течение 5 минут при 2000 об./мин. и температуре 4°C с использованием центрифуги (himac CR21, Hitachi, Ltd.). Затем удаляли надосадочную жидкость, и осадок два раза промывали PBS. Полученный осадок ресуспендировали в PBS, чтобы получить квасцы.
[0091] Измерение плазматических IgE, специфичных к аскаридному антигену
Кровь последовательно собирали у вышеописанных макаков в 1-й день (до введения жидкого аскаридного антигена в квасцах), 8-й день, 15-й день и 22-й день, и плазму отбирали после центрифугирования (1800×g, 4°C, 10 минут). Концентрацию специфичных к аскаридному антигену IgE в плазме измеряли, используя следующий способ.
DNP-Ascaris подготавливали в PBS таким образом, чтобы его концентрация составляла 100 мкг/мл, и добавляли в 96-луночные неразборные планшеты Nunc-Immuno™ MicroWell™ (Nunc Inc.) в количестве 100 мкл, а затем иммобилизовали при комнатной температуре в течение ночи. Блокирующий агент (Blocking One, Nacalai Tesque) добавляли в количестве 200 мкл и оставляли на 30 минут, после чего раствор удаляли. Далее, соответственно, добавляли в количестве 100 мкл выделенную плазму и образец калибровочной кривой. В качестве образца калибровочной кривой, концентрация плазматических IgE, специфичных к аскаридному антигену от одного животного из группы, которой вводили носитель, на 22-й день была принята как 2000 Ед/мл, и были приготовлены и использованы серийные разведения (2000 мЕд/мл - 16 мЕд/мл) в растворе для разведения (5% Blocking One в PBS). Инкубацию проводили при комнатной температуре в течение 1 часа, с последующим 5-кратным промыванием в Т-PBS (0,05% Tween-20 в PBS), а затем добавляли 100 мкл HRP-меченного антитела для детекции IgE (A80-108P, Bethyl Inc.), разведенного в 10000 раз в растворе для разведения. После чего инкубацию проводили при комнатной температуре в течение 1 часа с последующим 5-кратным промыванием Т-PBS. В конце, измерения проводили с использованием набора для цветовой детекции пероксидазы (ML-1120T, Sumilon Inc.). Оптическую плотность измеряли на Spectramax (Molecular Devices, Inc.). Результаты для 1-го и 22-го дня показаны на фиг. 1.
[0092]
Кожный тест
На 22-й день, PBS, 1, 10 и 100 мкг/мл раствора аскаридного антигена (раствора, в котором DNP-Ascaris ресуспендирован в PBS) вводили внутрикожно в двух точках, соответственно (всего 8 точек на одно животное) на выбритом животе каждого индивидуума в группе, получавшей носитель, и в группе, который вводили антитело, в количестве 100 мкл. В нормальной группе, внутрикожно вводили PBS и 100 мкг/мл раствора аскаридного антигена в 4-х точках, соответственно (всего 8 точек на одно животное), на выбритом животе каждого животного в количестве 100 мкл. Через 20 минут после сенсибилизации кожи, кожную реакцию фиксировали путем измерения диаметра с помощью нониусного штангенциркуля. Для каждого животного величина, в которой диаметр кожной реакции на введение PBS был вычтен из диаметра кожной реакции на введение аскаридного антигена, приведена как разница (дельта) в мм. Результаты при введении аскаридного антигена в концентрации 100 мкг/мл показаны на фиг. 2. Следует отметить, что в случае введения раствора аскаридного антигена в концентрации 1 и 10 мкг/мл не развивалась кожная реакция, достаточная для оценки исследуемого антитела.
[0093]
Вычисляли среднее значение и стандартную ошибку для каждой группы и вычисляли степень ингибирования, принимая значение в 1-й день (значение перед введением жидкого аскаридного антигена в квасцах) за 100% и значение в группе носителя на 22-й день за 0% в измерении плазматических IgE, специфичных к аскаридному антигену.
[0094]
Как показано на фиг. 1, полностью человеческое антитело T7-27 снижало (97%-е ингибирование) концентрацию IgE, специфичных к аскаридному антигену, в модели сенсибилизации аскаридным антигеном обезьян по сравнению с группой носителя.
[0095]
Как показано на фиг. 2, полностью человеческое антитело T7-27 снижало кожную реакцию на аскаридный антиген при введении 100 мкг/мл раствора аскаридного антигена в модели сенсибилизации аскаридным антигеном обезьян по сравнению с группой носителя.
[0096]
Из результатов, описанных выше, было выяснено, что полностью человеческое антитело T7-27 подавляло аллергическую реакцию, вызванную IgE, специфичными к аскаридному антигену, в модели сенсибилизации аскаридным антигеном обезьян.
[0097]
(Испытательный пример 1: оценка антитела к TSLP-рецептору в мышиной модели астмы при сенсибилизации клещевым антигеном)
Мышиная модель сенсибилизации клещевым антигеном известна как модель астмы, и патологическое состояние включает повышение реактивности дыхательных путей и инфильтрацию эозинофилов в бронхоальвеолярный лаваж.
Сенсибилизацию проводили путем внутрибрюшинного введения мышам NC/Nga (Charles River, Inc.) клещевого антигена (Dp) (LSL, Inc.) в дозировке 100 мкг Dp на 0,5 мл физиологического раствора на мышь в 0-й день (точка начала сенсибилизации) и 5-й день. Воспаление дыхательных путей вызывали назальным введением клещевого антигена с дозировкой 100 мкг DP на 50 мкл физиологического раствора на мышь на 12-й день и 19-й день. Антитело против мышиного TSLP-рецептора (WAKO, Inc.), растворенное в PBS (WAKO, Inc.), вводили группе введения антитела подкожно в дозировке (0,1, 1, 10 мг/кг) в -1-й день, 2-й день, 5-й день, 8-й день, 11-й день, 14-й день и 18-й день (дни введения антитела) один раз в день. В качестве положительной контрольной группы создавали группу введения дексаметазона (группа Dex). Дексаметазон, растворенный в PBS, вводили группе Dex внутрибрюшинно в дозировке 3 мг/кг с 12-го по 19-й день один раз в день. Набор обработанных групп был следующим.
[Экспериментальные группы]
Нормальная группа (n=10):
Необработанные животные
Группа физиологического раствора (n=6):
Клещевой антиген вводили внутрибрюшинно в 0-й день и 5-й день, физиологический раствор вводили интраназально в 12-й день и 19-й день, и PBS вводили подкожно в день введения антитела.
Группа PBS (n=10):
Клещевой антиген вводили внутрибрюшинно в 0-й день и 5-й день, клещевой антиген вводили интраназально в 12-й день и 19-й день, и PBS вводили подкожно в день введения антитела.
Группа введения антитела (0,1, 1, 10 мг/кг) (n=10 для каждой дозировки):
Клещевой антиген вводили внутрибрюшинно в 0-й день и 5-й день, клещевой антиген вводили интраназально в 12-й день и 19-й день, и антитело вводили подкожно в день введения антитела.
Группа Dex (n=10):
Клещевой антиген вводили внутрибрюшинно в 0-й день и 5-й день, клещевой антиген вводили интраназально в 12-й день и 19-й день, и дексаметазон вводили внутрибрюшинно с 12-го дня до 19-го дня.
[0098]
Мышь помещали в не ограничивающую движения камеру только для мышей на 20-й день. Датчик, в котором использовался пневмотахограф, был прикреплен к камере и подключен к анализатору дыхательной функции BioSystem XA (Buxco, Inc.), и изменение давления внутри камеры относительно атмосферного давления детектировали с помощью датчика. Концентрацию хлорида ацетил-β-метил холина (Sigma, Inc.) (0,25, 0,5, 1, 2, 4 мг/мл), растворенного в физиологическом растворе, последовательно повышали, и затем вводили через дыхательное отверстие при помощи небулайзера для изучения реактивности дыхательных путей. PenH, автоматически рассчитанный по изменению давления во внутренней части камеры, использовали в качестве показателя дыхательной функции. Результаты измерений показаны на фиг. 3.
[0099]
Далее, после сбора крови у мышей из полой вены брюшной полости, их умерщвляли путем обескровливания. Канюлю интубировали в трахею, и бронхоальвеолярный лаваж осуществляли 0,1%-м раствором фетальной бычьей сывороткой (BioWest, Inc.) в PBS, а затем собирали жидкость после бронхоальвеолярного лаважа (BALF). BALF центрифугировали, удаляли супернатант, осадок ресуспендировали в 500 мкл физиологического раствора, и получали суспензию BALF-клеток. Количество эозинофилов в BALF-клеточной суспензии измеряли с использованием мультипозиционнного автоматического анализатора клеток крови XT-2000i (Sysmex, Inc.). Результаты измерений показаны на фиг. 4.
[0100]
Полученную кровь разводили в 10 раз культуральной средой RPMI1640 (Life Technologies, Inc.). Разбавленную кровь высевали в количестве 1 мл на планшет (IWAKI Co. Ltd.). Мышиный TSLP (R&D, Inc.) разводили в PBS так, чтобы его конечная концентрация составляла 0 или 10 нг/мл, и добавляли по 100 мкл этих растворов. Инкубацию проводили при 37°C в течение 24 часов в атмосфере 5% CO2, а общую РНК выделяли в 30 мкл воды с использованием набора RNeasy 96 Kit (Qiagen, Inc.). Далее, 10 мкл РНК использовали в реакции обратной транскрипции с использованием набора High Capacity cDNA Reverse Transcription Kit (Life Technologies, Inc.). Далее, уровень экспрессии мРНК TARC измеряли с помощью ПЦР-способа TaqMan с использованием TaqMan-зонда для TARC (Ccl17, Mn01244826 g1, Life technologies, Inc.), TaqMan-зонда для β-актина (Actb, Mm00607939 s1, Life technologies, Inc.), смеси Express qPCR SuperMix (A10313, Life Technologies, Inc.) и 2 мкл кДНК. Уровень экспрессии был рассчитан путем анализа результатов измерения с использованием метода сравнения СТ. Результаты при 10 нг/мл TSLP показаны на фиг. 5.
[0101]
Были вычислены средние значения и стандартные ошибки для соответствующих групп. Тест Стьюдента использовали для определения достоверного различия между группой PBS и нормальной группой, группы PBS и группой Dex, соответственно. Для определения достоверного различия между группой PBS и группой введения антитела использовали множественное сравнение Даннета. В обоих случаях, достоверное различие присутствовало в случае р<0,05.
[0102]
Как показано на фиг. 3, в группе, которой вводили антитело, ингибирующее действие на гиперреактивность дыхательных путей, индуцированную 1 мг/мл хлорида ацетил-β-метил холина, было найдено в мышиной модели астмы по сравнению с группой PBS. Стало ясно, что антитело к TSLP-рецептору улучшает дыхательную функцию в модели астмы.
[0103]
Как показано на фиг. 4, в группе, которой вводили антитело, ингибирующее действие на инфильтрацию эозинофилов в бронхоальвеолярный лаваж было обнаружено в сравнении с группой PBS.
[0104]
Как показано на фиг. 5, в группе, которой вводили антитело, ингибирующее действие на экспрессию мРНК TARC было найдено в сравнении с группой PBS.
[0105]
Результаты, представленные на фиг. 3 и 4, подтверждали, что антитело к TSLP-рецептору улучшало патологическое состояние в модели астмы. Кроме того на основании результатов, представленных на фиг. 3-5, была обнаружена корреляция между улучшением патологического состояния и ингибированием экспрессии мРНК TARC после введения антитела к рецептору анти-TSLP, и стало очевидно, что положительное воздействие на патологическое состояние может быть оценено по ингибирующему эффекту на экспрессию мРНК TARC качестве показателя.
Промышленная применимость
[0106]
Антитело к TSLP-рецептору человека по настоящему изобретению является полезным для профилактики и лечения различных заболеваний, в которых TSLP человека и TSLP-рецептор человека участвуют в патологии заболевания. Кроме того, способы получения полинуклеотидов, экспрессионных векторов и клеток-хозяев по настоящему изобретению могут использоваться для получения антитела к TSLP-рецептору человека.
[Свободный текст списка последовательностей]
[0107]
В ряде заголовков <223> в списке последовательностей приведено описание «Искусственная последовательность». В частности, нуклеотидными последовательностями, приведенными в SEQ ID NO: 2 и SEQ ID NO: 4 из списка последовательностей, являются нуклеотидные последовательности тяжелой цепи и легкой цепи полностью человеческого антитела T7-27, соответственно, а аминокислотными последовательностями, приведенными в SEQ ID NO: 1 и SEQ ID NO: 3, являются аминокислотные последовательности тяжелой цепи и легкой цепи, кодируемые SEQ ID NO: 2 и SEQ ID NO: 4, соответственно. Нуклеотидными последовательностями, приведенными в SEQ ID NO: 5, 6, 7, 8, и 9 из списка последовательностей, являются нуклеотидные последовательности, кодирующие слитый белок TSLP-рецептора человека с Fc человека, слитый белок TSLP-рецептора человека с Fc мыши, слитый белок TSLP-рецептора обезьяны с Fc человека, мутированный белок TSLP человека с Flag-тегом и мутированный белок TSLP обезьяны с Flag-тегом, соответственно.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛО К CD73 ЧЕЛОВЕКА | 2017 |
|
RU2754058C2 |
| ТЕРАПЕВТИЧЕСКИЕ СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2002 |
|
RU2328506C2 |
| АНТИ-СD3-АНТИТЕЛО И МОЛЕКУЛА, СОДЕРЖАЩАЯ ЭТО АНТИТЕЛО | 2017 |
|
RU2790326C2 |
| МОНОКЛОНАЛЬНОЕ АНТИТЕЛО К IL-5Rα | 2017 |
|
RU2698048C2 |
| АНТИТЕЛА К РЕЦЕПТОРУ ТИМУСНОГО СТРОМАЛЬНОГО ЛИМФОПОЭТИНА | 2007 |
|
RU2486202C2 |
| Рекомбинантный дрожжевой трансформант и способ получения с его использованием Fc-фрагмента иммуноглобулина | 2014 |
|
RU2664862C2 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2694412C2 |
| ГУМАНИЗИРОВАННЫЕ МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА К СЕА С СОЗРЕВШЕЙ АФФИННОСТЬЮ | 2010 |
|
RU2570554C2 |
| Моноклональные антитела, которые специфически связываются с участком бета цепи семейства TRBV-9 Т-клеточного рецептора человека, и способы их применения | 2018 |
|
RU2711871C1 |
| СКОНСТРУИРОВАННОЕ АНТИТЕЛО ПРОТИВ TSLP | 2010 |
|
RU2575039C2 |
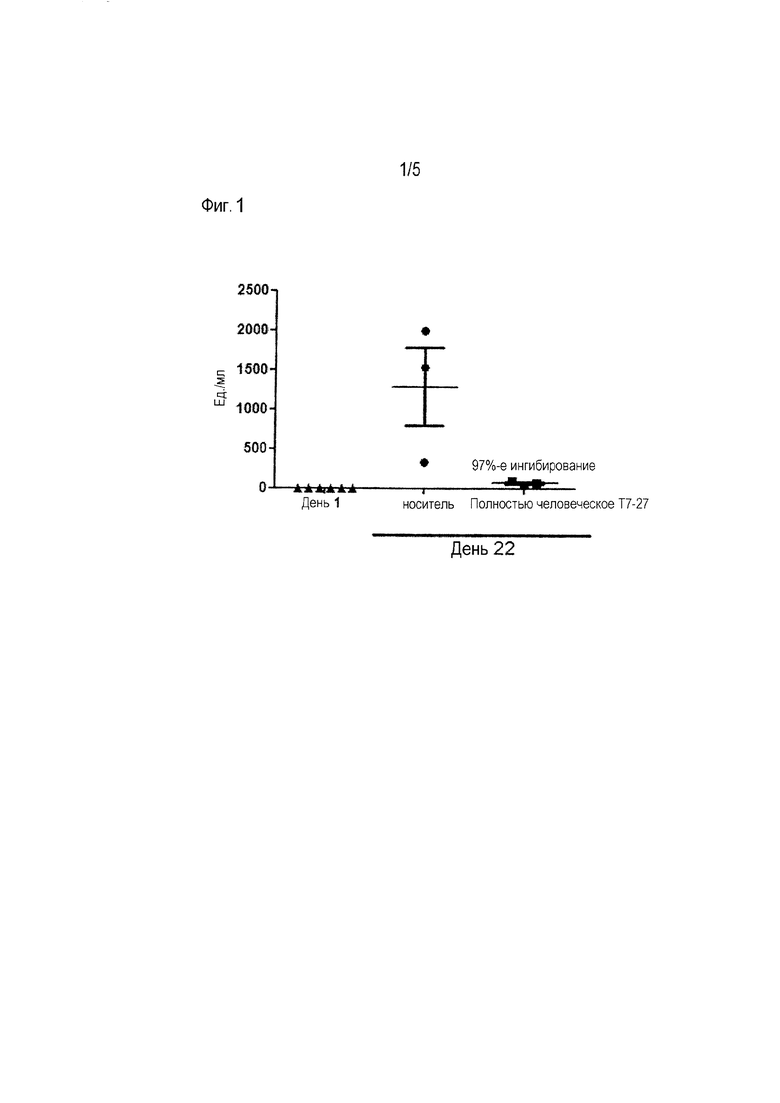
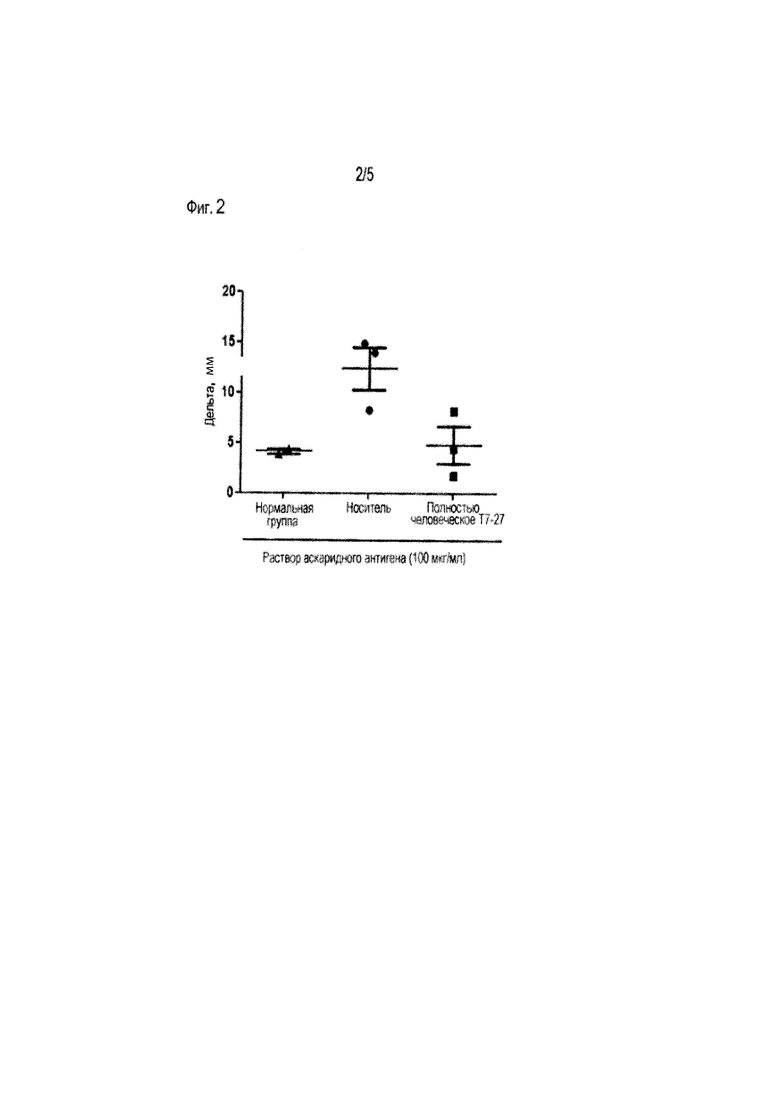
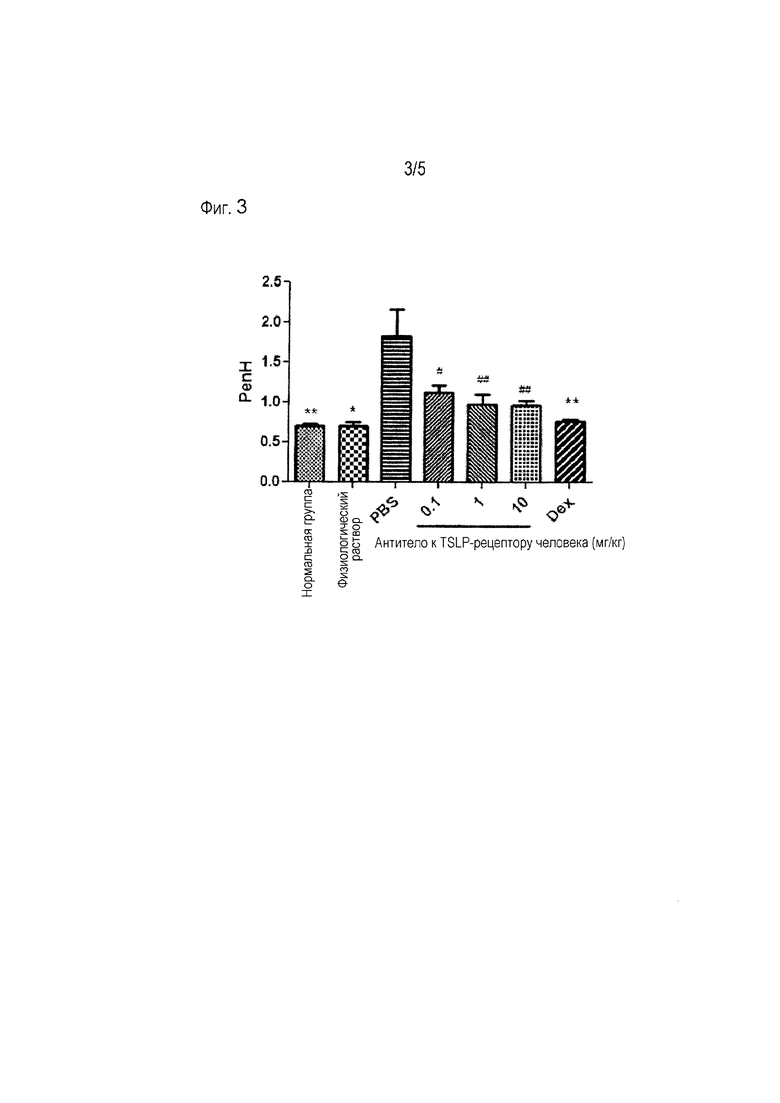
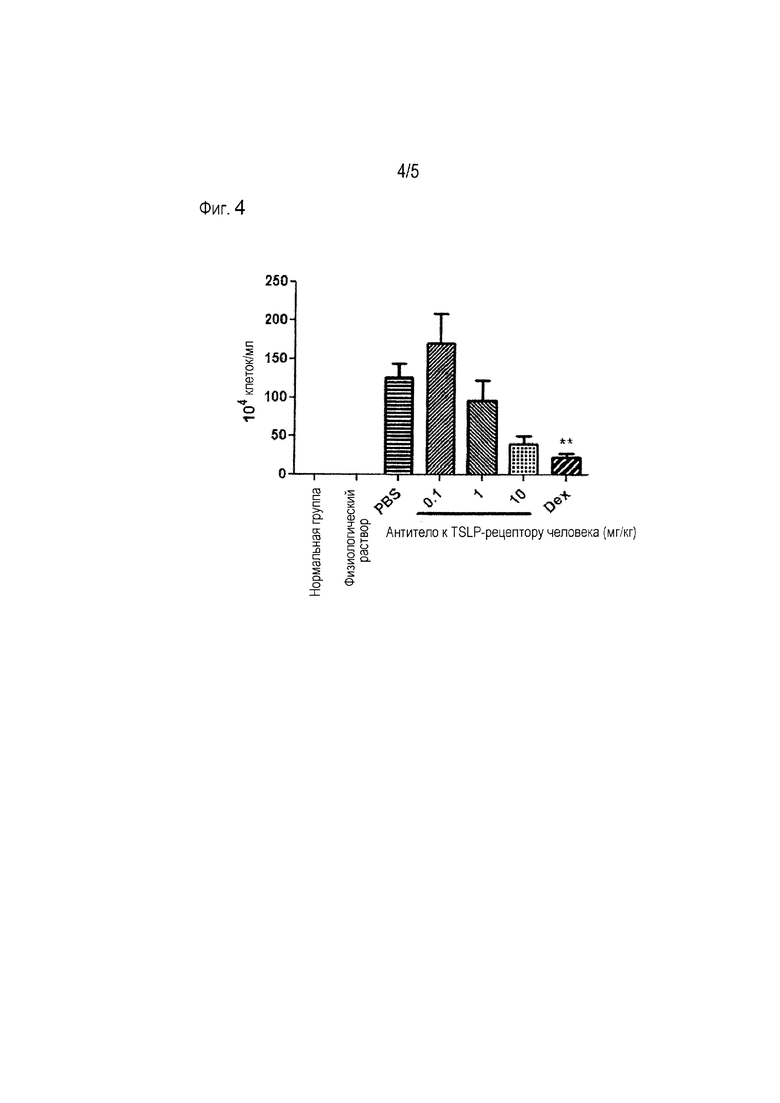
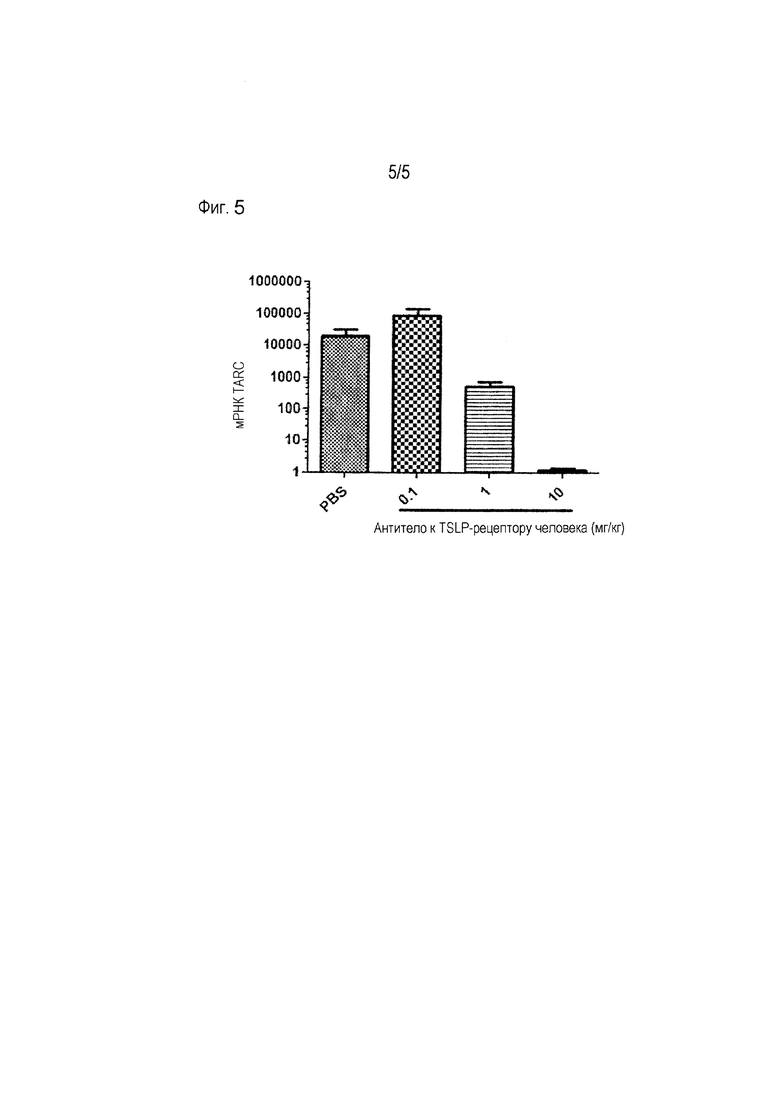
Изобретение относится к области биохимии, в частности к антителу к TSLP-рецептору. Также раскрыты экспрессионный вектор, клетка-хозяин для получения указанного антитела. Раскрыт способ получения указанного антитела. Изобретение обладает способностью эффективно лечить заболевания, ассоциированные с TSLP-рецептором. 4 н. и 4 з.п. ф-лы, 7 пр., 5 ил., 3 табл.
1. Антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент, содержащие вариабельную область тяжелой цепи, содержащую CDR1, состоящую из аминокислотной последовательности с номерами аминокислот 31-35 последовательности SEQ ID NO: 1, CDR2, состоящую из аминокислотной последовательности с номерами аминокислот 50-66 последовательности SEQ ID NO: 1, и CDR3, состоящую из аминокислотной последовательности с номерами аминокислот 99-107 последовательности SEQ ID NO: 1, и вариабельную область легкой цепи, содержащую CDR1, состоящую из аминокислотной последовательности с номерами аминокислот 24-34 последовательности SEQ ID NO: 3, CDR2, состоящую из аминокислотной последовательности с номерами аминокислот 50-56 последовательности SEQ ID NO: 3, и CDR3, состоящую из аминокислотной последовательности с номерами аминокислот 89-97 последовательности SEQ ID NO: 3.
2. Антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент по п.1, выбранные из (1) или (2) ниже:
(1) антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент, содержащие вариабельную область тяжелой цепи, состоящую из аминокислотной последовательности с номерами аминокислот 1-118 последовательности SEQ ID NO: 1, и вариабельную область легкой цепи, состоящую из аминокислотной последовательности с номерами аминокислот 1-108 последовательности SEQ ID NO: 3;
(2) антитело к TSLP-рецептору человека или его антигенсвязывающий фрагмент, где глутаминовая кислота N-конца тяжелой цепи антитела или его антигенсвязывающего фрагмента согласно (1) модифицирована на пироглутаминовую кислоту.
3. Антитело к TSLP-рецептору человека по п.2, выбранное из (1) или (2) ниже:
(1) антитело к TSLP-рецептору человека, содержащее тяжелую цепь, состоящую из аминокислотной последовательности, представленной последовательностью SEQ ID NO: 1, и легкую цепь, состоящую из аминокислотной последовательности, представленной последовательностью SEQ ID NO: 3;
(2) антитело к TSLP-рецептору человека, содержащее тяжелую цепь, состоящую из аминокислотной последовательности, представленной последовательностью SEQ ID NO: 1, где глутаминовая кислота под аминокислотным номером 1 последовательности SEQ ID NO: 1 модифицирована на пироглутаминовую кислоту, и/или лизин под аминокислотным номером 448 последовательности SEQ ID NO: 1 делетирован, и легкую цепь, состоящую из аминокислотной последовательности, представленной последовательностью SEQ ID NO: 3.
4. Антитело к TSLP-рецептору человека по п.3, содержащее тяжелую цепь, состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 1, и легкую цепь, состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 3.
5. Антитело к TSLP-рецептору человека по п.3, содержащее тяжелую цепь, состоящую из аминокислотной последовательности с номерами аминокислот 1-447 последовательности SEQ ID NO: 1, и легкую цепь, состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 3.
6. Экспрессионный вектор, содержащий:
(i) полинуклеотид, содержащий нуклеотидную последовательность, кодирующую тяжелую цепь антитела по п. 4, и/или
(ii) полинуклеотид, содержащий нуклеотидную последовательность, кодирующую легкую цепь антитела по п. 4.
7. Клетка-хозяин для получения антитела, где клетку выбирают из группы, состоящей из следующих пп. (a)-(d):
(а) клетка-хозяин, трансформированная экспрессионным вектором, включающим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую тяжелую цепь антитела к TSLP-рецептору человека по п.4, и полинуклеотид, содержащий нуклеотидную последовательность, кодирующую легкую цепь этого антитела;
(b) клетка-хозяин, трансформированная экспрессионным вектором, включающим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую тяжелую цепь антитела к TSLP-рецептору человека по п.4, и экспрессионным вектором, включающим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую легкую цепь этого антитела;
(c) клетка-хозяин, трансформированная экспрессионным вектором, включающим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую тяжелую цепь антитела к TSLP-рецептору человека по п.4; и
(d) клетка-хозяин, трансформированная экспрессионным вектором, включающим полинуклеотид, содержащий нуклеотидную последовательность, кодирующую легкую цепь антитела к TSLP-рецептору человека по п.4.
8. Способ получения антитела к TSLP-рецептору человека, который включает культивирование клетки-хозяина по п.7 для экспрессии антитела к TSLP-рецептору человека.
| АНТИТЕЛА К РЕЦЕПТОРУ ТИМУСНОГО СТРОМАЛЬНОГО ЛИМФОПОЭТИНА | 2007 |
|
RU2486202C2 |
| WO 2013067051 A1, 10.05.2013 | |||
| УСТРОЙСТВО ДЛЯ ЛОКАЛЬНОГО ОХЛАЖДЕНИЯ | 1993 |
|
RU2077279C1 |
| US 20120020960 A1, 26.01.2012 | |||
| US 8076456 B2, 13.12.2011. | |||
Авторы
Даты
2019-05-28—Публикация
2014-08-08—Подача