Настоящее изобретение относится к способам лечения воспалительных заболеваний кишечника, таких как, например, болезнь Крона и язвенный колит, и всех заболеваний кишечника инфекционного происхождения, и в особенности оно относится к веществу для применения при лечении воспаления у больных с воспалительным заболеванием кишечника.
Болезнь Крона (CD), язвенный колит (UC) и различные IBD инфекционного происхождения, представляют собой многофакторные заболевания часто неясной этиологии. Нарушение регуляции врожденной и адаптивной иммунной систем, направленное против внутрикишечных бактерий или их продуктов, и ненадлежащие иммунные ответы на организмы в кишечнике, которые в норме не вызывают ответа, представляют собой иммунные факторы, характерные для CD, UC и других IBD.
В соответствии с современным пониманием, микроорганизмы пользуются преимуществами ослабленного слоя слизистых оболочек пациентов, страдающих от воспалительных заболеваний кишечника, и невозможностью очистить от бактерий стенки кишечника, тем самым вызывая симптомы заболеваний.
Некоторые исследования показали, что адгезивно-инвазивная Escherichia coli (AIEC), значительно более распространена у пациентов с CD, чем в контрольной группе.
Другие исследования, такие как опубликованные Nicolas Barnich, Arlette Darfeuille-Michaud в работе «Adherent-Invasive Escherichia coli and Crohn's Disease» в Curr Opin Gastroenterol. 2007; 23(1): 16-20, показали, что поскольку инфекционный цикл адгезивно-инвазивной Е.coli может зависеть от способности AIEC колонизировать желудочно-кишечный тракт пациентов с генетической предрасположенностью к болезни Крона, антибиотики, которые могли бы уничтожить бактерии, или пробиотики, которые могли бы заменить их в желудочно-кишечном тракте, могли бы иметь терапевтическую ценность при болезни Крона в подвздошной кишке.
Адгезивно-инвазивная Escherichia coli охватывает подгруппу Е.coli spp., названную так по их характерной способности прикрепляться к клеткам кишечника, вторгаться в инфицированные эукариотические клетки и реплицироваться в эпителиальных клетках и макрофагах, вызывая кишечные заболевания у людей. LF82, штамм Е.coli (серологический тип O83:Н1) первоначально выделенный от пациента с болезнью Крона, представляет собой прототип штамма AIEC, как описано в работе Darfeuille-Michaud А., Neut С., Barnich N., Lederman E., Di Martino P., Desreumaux P. et al. «Presence of adherent Escherichia coli strains in ileal mucosa of patients with Crohn's disease» Gastroenterology, 115 (1998), pp. 1405-1413.
Лактоферрин (Lf), член семейства трансферринов представляющих собой железо-связывающие гликопротеины, - это одна из основных противомикробных систем в молоке и в других экзокринных секретах. Известные биологические свойства Lf включают противомикробную активность в отношении широкого спектра патогенных бактерий, грибов, простейших и вирусов, а также противовоспалительные, противоопухолевые и иммуномодулирующие, активности, как описано в работах Steijns, J.M. and Van Hooijdonk, A.C.M. «Occurrence, structure, biochemical properties and technological characteristics of lactoferrin», Br J Nutr 2000; 84, 511-517; и Superti, F.; Berlutti, F.; Paesano, R.; Valenti, P. «Structure and activity of lactoferrin - A multi functional protective agent for human health», Iron Metabolism and Disease; Fuchs, H., Ed.; Research Signpost: Kerala, India, 2008; pp. 1-32.
Как правило, лечение острых состояний воспалительных заболеваний кишечника включает применение лекарственных препаратов, например, антибиотиков, для лечения любой инфекции, и противовоспалительных лекарственных препаратов и кортикостероидов для снижения воспаления. Однако длительное применение антибиотиков, противовоспалительных лекарственных препаратов и кортикостероидов имеет значительные побочные эффекты, так что следует его избегать.
Следовательно, цель настоящего изобретения заключается в обеспечении вещества для применения при лечении пациентов, страдающих от воспалительных заболеваний кишечника, вызванных бактериальной инфекцией, которое не вызывает каких-либо существенных побочных эффектов.
Эта цель была достигнута с помощью лактоферрина для применения в соответствии с первым пунктом формулы изобретения, и композиций с модифицированным высвобождением, включающих лактоферрин, для применения в соответствии с пунктом 4 формулы изобретения, в то время как другие признаки были раскрыты в остальных пунктах формулы изобретения.
В соответствии с настоящим изобретением, было обнаружено, что лактоферрин, в особенности бычий лактоферрин, оказывает сильное ингибирующее действие на инвазию AIEC в эпителиальные клетки кишечника и может быть применен при лечении воспалительных заболеваний кишечника, таких, например, как и болезнь Крона и язвенный колит, и для поддержания ремиссии у пациентов, несущих патогенные AIEC, колонизирующие ранние и хронические очаги поражения подвздошной кишки.
В действительности, проведенные авторами изобретения испытания показывают, что пепсиновый гидролизат лактоферрина способен предотвратить адгезию и интернализацию AIEC в клетки кишечника, в то же время он не в состоянии снизить воспаление. Напротив, лактоферрин, как ни удивительно, сильно ингибирует инвазию клеток кишечника AIEC и снижает воспаление.
В соответствии с изобретением дополнительно было установлено, что, в нецитотоксической и в небактерицидной концентрации, лечение лактоферрином не оказывало никакого влияния на адгезию бактерий, в то же время он был в состоянии предотвратить инвазию клеток кишечника прототипом штамма AIEC LF82 зависимым от дозы образом.
Следовательно, композиции с модифицированным высвобождением, включающие лактоферрин, могут быть применены при лечении хронических воспалительных состояний, вызванных бактериальной инфекцией, в особенности инвазией AIEC и любым другим микроорганизмом, связанным с воспалительными заболеваниями кишечника.
В особенности bLf, свободный от негативных побочных эффектов, может быть применен при лечении болезни Крона и других воспалительных заболеваний кишечника и для поддержания состояния ремиссии у пациентов.
В соответствии с указанными выше результатами, композиции с модифицированным высвобождением, включающие лактоферрин или, предпочтительно, бычий лактоферрин в соответствии с настоящим изобретением, были получены путем тщательной и целенаправленной селекции известных систем с модифицированным высвобождением и примененных в них веществ.
В действительности, композиции лактоферрина с модифицированным высвобождением в соответствии с настоящим изобретением обладают локализованной активностью в различных отделах желудочно-кишечного тракта или системной активностью, и контролируемым высвобождением, начиная с ранних стадий введения. Кроме того, обеспечивают однородность высвобождения во времени и, в тоже время, допускается, что, поскольку только часть активного вещества стала доступна, то оно сразу же становиться активным или местно, или на системном уровне, из-за его состояния в виде микроэмульсии, солюбилизации или комплексообразования.
В соответствии с настоящим изобретением, для применения при лечении воспалительных заболеваний кишечника обеспечивают вещество, указанное вещество представляет собой лактоферрин и, предпочтительно, бычий лактоферрин.
В особенности лактоферрин обеспечивают для применения при лечении заболеваний кишечника, вызванных инвазией Escherichia coli, в особенности для применения при лечении заболеваний кишечника, вызванных инвазией адгезивно-инвазивной Escherichia coli.
Лактоферрин для применения в соответствии с настоящим изобретением может быть введен в любом ежедневном количестве, которое приводит к снижению симптомов воспалительных заболеваний кишечника. Предпочтительно, лактоферрин для применения в соответствии с настоящим изобретением может быть введен в количестве, равном от 50 мг до 250 мг в день; более предпочтительно, указанное суточное количество включает от 100 мг до 200 мг в день.
Так или иначе, обычные специалисты имеют возможность отрегулировать величины дозы и режим приема посредством наблюдения за эффективностью лечения. Соответственно, предполагается, что диапазон дозировки для применения может быть на несколько порядков выше или ниже, чем приведенный выше оптимум. Несмотря на то, что предпочтительный способ введения представляет собой пероральное введение, специалистам в данной области техники будет очевидно, что другие пути также подходят в соответствии с изобретением, включая подкожное введение, внутримышечное, внутривенное введение и тому подобное.
В соответствии с другим аспектом настоящего изобретения, обеспечивают пероральную композицию для лекарственной формы с модифицированным высвобождением, включающую лактоферрин для применения при лечении воспалительных заболеваний кишечника, таких как болезнь Крона, язвенный колит, в особенности для применения при лечении заболеваний кишечника, вызванных инвазией Escherichia coli, в особенности для применения при лечении воспалительных заболеваний кишечника, вызванных инвазией Escherichia coli LF82.
В особенности лекарственная форма с модифицированным высвобождением означает замедленное высвобождение, которое позволяет получить преимущество сниженной частоты введения и сниженного высвобождения активного вещества в определенных участках желудочно-кишечного тракта.
Пероральная композиция для лекарственной формы с модифицированным высвобождением для применения в соответствии с настоящим изобретением включает лактоферрин, растворенный и/или диспергированный и/или погруженный в матрицу, и наружное покрытие, в которой указанная матрица включает:
- вещества, выбранные из группы, состоящей из липидных вещества, гидрофильных веществ, амфифильных веществ и их смесей; и
- необязательно, фармацевтически приемлемые вспомогательные вещества, предназначены для облегчения выполнения фармацевтической формы.
В качестве лактоферрина в пероральной композиции в соответствии с настоящим изобретением может быть применен бычий лактоферрин. Количество лактоферрина в пероральных композициях в соответствии с настоящим изобретением предпочтительно подходит для обеспечения введения лактоферрина в суточной дозе, равной от 50 мг до 250 мг; предпочтительно от 100 мг до 200 мг, в одном или нескольких ежедневных введениях.
Указанное наружное покрытие предпочтительно выполнено из материалов, обеспеченных свойством растворяться под действием желудочного сока или свойством устойчивости к действию желудочного сока и/или свойством высвобождаться при специфическом рН кишечника (свойством рН-зависимого высвобождения) или свойством не зависимого от рН замедленного высвобождения.
Подходящие вещества для указанного наружного покрытия пероральных композиций в соответствии с настоящим изобретением включают ацетат-фталат целлюлозы, метакриловой ацетат, полимеры метакриловой кислоты, шеллак, этилцеллюлозу, альгиновые кислоты и их комбинации; предпочтительно, могут быть упомянуты устойчивые к действию желудочного сока средства для покрытия, которые выбирают из группы, состоящей из шеллака, полиметакрилатов, ацетофталата целлюлозы, производных альгината. Предпочтительно может быть применен водный шеллак (например, изделие Aquagold® от компании Натке) и его комбинации, или комбинация этилцеллюлозы и солей альгиновой кислоты, представленная на рынке в виде питательной энтеросолюбильной системы покрытия Nutrateric® от компании Colorcon Inc., Westpoint, Pa.
Липидные вещества, которые могут быть применены в матрице пероральной композиции в соответствии с изобретением, включают жирные спирты, жирные кислоты, триглицериды, воски. Предпочтительно, указанные липидные вещества выбирают из группы, состоящей из пальмитиновой кислоты, цетилового спирта, цетостеарилового спирта, карнаубского воска, стеариновой кислоты.
Гидрофильные вещества, которые могут быть применены в матрице пероральных композиций в соответствии с изобретением, включают гидрогели, то есть вещества, которые переходят от безводного к гидратированному состоянию, демонстрируя явление молекулярной релаксации, которое характеризуется значительным увеличением объема системы за счет увеличения размера и веса после координации большого количества молекул воды полярными группами, присутствующими в полимерной цепи. Гидрогели, которые могут быть применены в соответствии с изобретением, выбирают из группы, состоящей из полимеров или сополимеров акриловой или метакриловой кислоты, полимеров алкилвиниловых эфиров, гидроксиалкилцеллюлоз, карбоксиалкилцеллюлоз, полисахаридов, альгинатов, пектинов, крахмалов, натуральных и синтетических смол, поликарбофила и их смесей. Предпочтительно, указанные гидрофильных веществ включают гидроксипропилметилцеллюлозу (например, продаваемую под торговыми названиями Methocel® K4M, K15M, K100M, 100LV), карбоксиметилцеллюлозу (например, продаваемую под торговым названием Blanose®), гидроксипропилцеллюлозу (например, продаваемую под торговыми названиями Klucel® EF, LF, JF, GF, MF, HF), микрокристаллическую целлюлозу, крахмалы, такие как кукурузный крахмал и лактозу.
Амфифильные вещества матрицы, которые может быть применено в композиции в соответствии с изобретением, включают лецитин, фосфатидилхолин, фосфатидилэтаноламин, простые алкиловые эфиры гликолей, такие как моноэтиловый эфир диэтиленгликоля, макроголглицериды, полиэтиленгликоля гидроксистеараты, воска, лаурилсульфат натрия, додецилсульфат натрия, полисорбаты, холевую кислоту, полоксамер, сульфосукцинат натрия, лауроилсаркозинат натрия и их смеси. Предпочтительно, указанные амфифильные вещества включают лауроилполиоксиглицериды (например, изделия, представленные на рынке под торговым названием Gelucire® 44/14 или Labrafil®M2130Cs), гидрогенизированное кокосовое масло, сложные эфиры PEG 1500, стеароилполиоксиглицериды (например, изделие, представленное на рынке под торговым названием Gelucire® 50/13), гидрогенизированное пальмовое масло, лецитин (например, изделия, представленные на рынке под торговым названием Epikuron®, Phosal®, Phospholipon® 100 Н, Lipoid®).
Указанные фармацевтически приемлемые вспомогательные вещества, которые предназначены для облегчения выполнения фармацевтической формы, могут быть выбраны из средств для облегчения скольжения, разбавителей, антиадгезивных средств, смазочных веществ, разрыхлителей, противослеживающих средств, стабилизаторов.
В соответствии с альтернативным воплощением, пероральная композиция в соответствии с изобретением выполнена в форме системы резервуара, в которой лактоферрин растворен и/или диспергирован и/или погружен в сердцевину резервуара, покрытого полупроницаемыми для воды целлюлозными мембранами, предпочтительно, этилцеллюлозными мембранами.
Сердцевины резервуара можно рассматривать как емкости для лактоферрина, которые надлежащим образом покрыты полупроницаемыми мембранами, изготовленными из производных целлюлозы, таких как этилцеллюлоза, метилцеллюлоза, метилэтилцеллюлоза, гидроксипропилметилцеллюлоза.
Другие необязательные компоненты пероральных композиций в соответствии с настоящим изобретением, представляющие собой пленкообразующие вспомогательные вещества и гранулирующие вспомогательные вещества, могут в свою очередь быть выбраны из числа растворимых в желудочном соке средств для покрытия, устойчивых к действию желудочного сока средства для покрытия, зависимых от рН средств для покрытия, независимых от рН средств для покрытия, обладающих свойствами высвобождаться в определенных участках, и могут включать целлюлозы ацетат фталат, полимеры метакриловой кислоты, шеллак, этилцеллюлозу, альгиновые кислоты.
Кроме того, композиции в соответствии с настоящим изобретением могут включать другие активные вещества, такие как противовоспалительные лекарственные препараты, мезаламин, производные мезаламина, кортикостероиды, азатиоприн, циклоспорин, моноклональные антитела.
Пероральные композиции в соответствии с настоящим изобретением могут быть получены с помощью производственных процессов, выбранный среди тех, которые обычно применяют в фармацевтических областях производства, таких как способ прямого прессования, способ влажного гранулирования, способ уплотнения/сухого гранулирования и способ, включающий гранулирование плавлением и загрузку/совместное размалывание и заключительное заполнение порошка.
В особенности пероральные композиции в соответствии с изобретением могут быть получены с помощью способа, состоящего из следующих этапов:
a) смешивание просеянного лактоферрина с веществом матрицы, выбранного из липидных вещества, гидрофильных веществ, амфифильных веществ;
b) необязательно, добавление любых других активных веществ;
c) проведение стадии, которую выбирают из группы, состоящей из влажного гранулирования, сухого гранулирования, прямого заполнения, совместного размалывания, гранулирования из расплава;
d) необязательно, добавление другие фармацевтически приемлемых вспомогательных веществ предназначенных для облегчения выполнимости лекарственной формы, такие как средства для облегчения скольжения, разбавители, антиадгезивные средства, смазочные вещества, разрыхлители, для получения твердой формы в виде порошка и/или гранул и/или мини-таблеток и/или микрогранул с хорошими характеристиками сыпучести и сжимаемости;
е) покрытие пленкой посредством растворимых в желудке или устойчивых к действию желудочного сока вспомогательных веществ или зависимых от рН и/или рН-независимых вспомогательных веществ, способный задерживать высвобождение лактоферрина, для того чтобы получить внешнее покрытие, обеспечивающее высвобождение в определенном участке желудочно-кишечного тракта.
В соответствии с изобретением, для изготовления монолитной матричной системы получают липидную или амфифильную или гидрофильную матрицу, содержащую лактоферрин, затем добавляют различные функциональные вспомогательные вещества для разведения и для того, чтобы изделие можно было обрабатывать подходящими фармацевтическими способами. Отношение между количеством лекарственного препарата и вещества матрицы по отношению к вспомогательным веществам, которые добавляют на данной стадии, как правило, не превышает 1:4; оптимальное количество лекарственного препарата и вещества матрицы равно от 0,1% до 20% по массе от количества вспомогательных веществ.
К данной смеси можно добавить разбавители в количестве вплоть до 50% по массе, смазочные вещества в количестве, равном 0,5-3% по массе, средства для облегчения скольжения в количестве, равном 0,5-3% по массе, и разрыхлители в количестве, равном 0,1-40% по массе, все проценты отнесены к конечной массе стандартной лекарственной формы.
Альтернативная фармацевтическая форма лактоферрина заключается в резервуарных системах. Для получения резервуарной системы с лактоферрином, сердцевину, содержащую фармацевтический лактоферрин, представленный множеством обособленных частиц, или монолитный лактоферрин, получают путем загрузки лактоферрина в инертные вспомогательные вещества, такие как разбавители, средства для облегчения скольжения, смазочные вещества. Массовое отношение между лактоферрином и средствами-разбавителями может быть равно, например, 1:1; массовое отношение между лактоферрином и средствами для облегчения скольжения может быть равно, например, 1:0,5; массовое отношение между лактоферрином и смазочными веществами может быть равно, например, 1:0,5. Полученную сердцевину затем покрывают полупроницаемой мембраной, которая регулирует время задержки и время высвобождения. Мембрана может быть выполнена из полимеров целлюлозы и их производных, и покрытие обеспечивает увеличение массы системы от 0,5% до 30%.
С точки зрения характеристик растворения, контакт данных композиций с водой или водными растворами приводит к модифицированному и/или отложенному и/или замедленному высвобождению активного вещества и/или высвобождению в определенном участке активного вещества, которое сразу же диспергируется, солюбилизируется в составленной таким способом системе. Вспомогательные вещества и полимеры, присутствующие в структуре, управляют смачиваемостью системы и гомогенностью солюбилизации лактоферрина в узком диапазоне высвобождения, таким путем, благоприятствуя его локализованной активности и/или непрерывной и постепенной абсорбции или постепенному местному высвобождению в желудочно-кишечном тракте.
Дополнительные преимущества и отличительные признаки композиций лактоферрина для применения в соответствии с настоящим изобретением станут понятны специалистам в этой области техники из следующих примеров с отсылкой на прилагаемые чертежи, в которых:
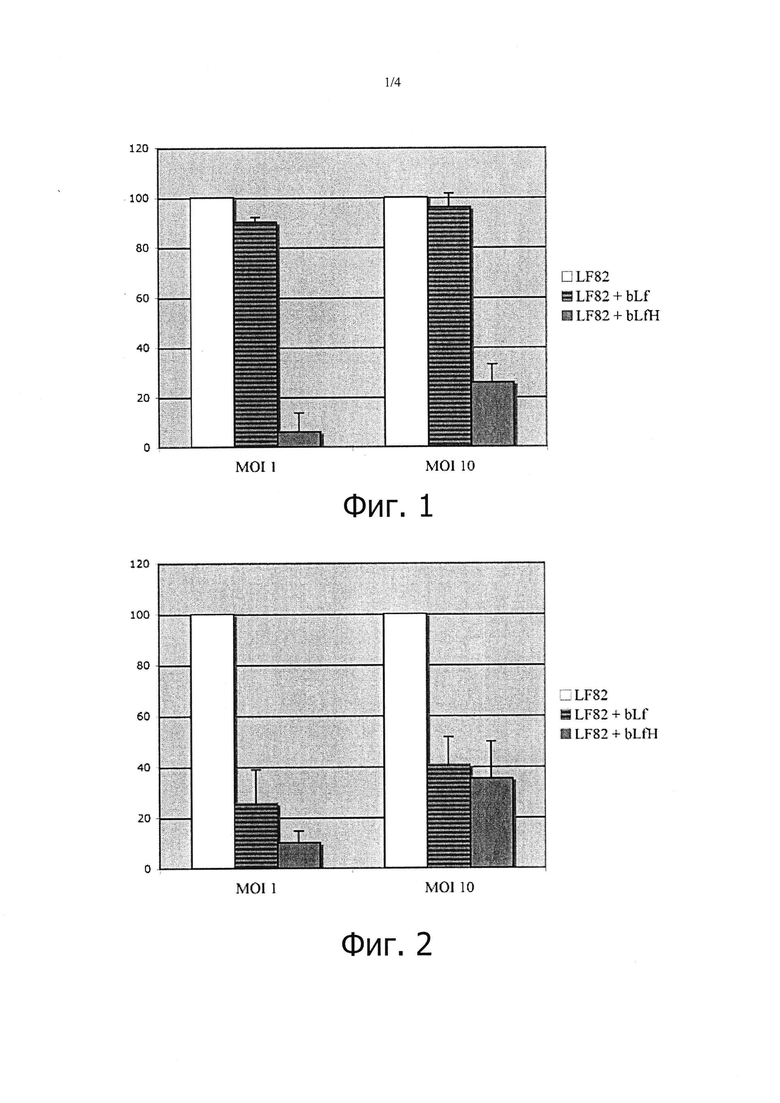
- фигура 1 представляет собой график, показывающий влияние bLf и bLfH (1 мг/мл) на способность к адгезии LF82 к эпителиальным клеткам;
- фигура 2 представляет собой график, показывающий влияние bLf и bLfH (1 мг/мл) на способность к инвазии LF82 в эпителиальные клетки;
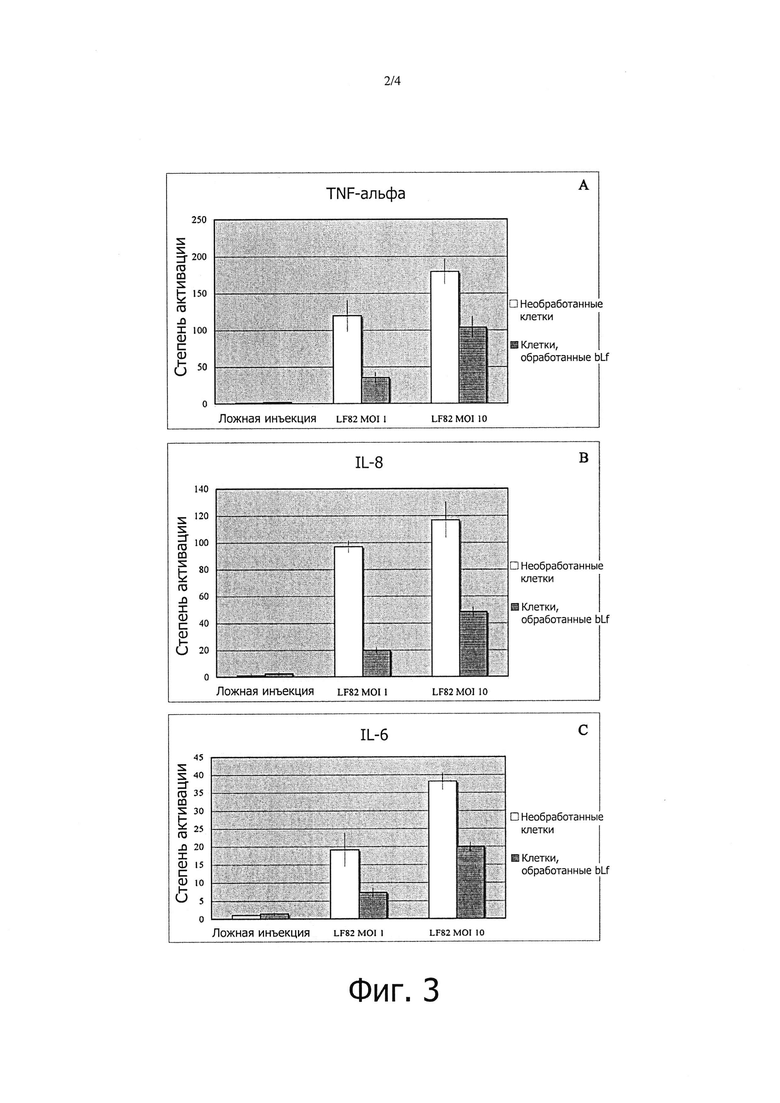
- фигуры 3 А, В и С представляют собой графики, показывающие влияние bLf (1 мг/мл) на экспрессию мРНК TNF-альфа, IL 8 и IL6 в эпителиальных клетках;
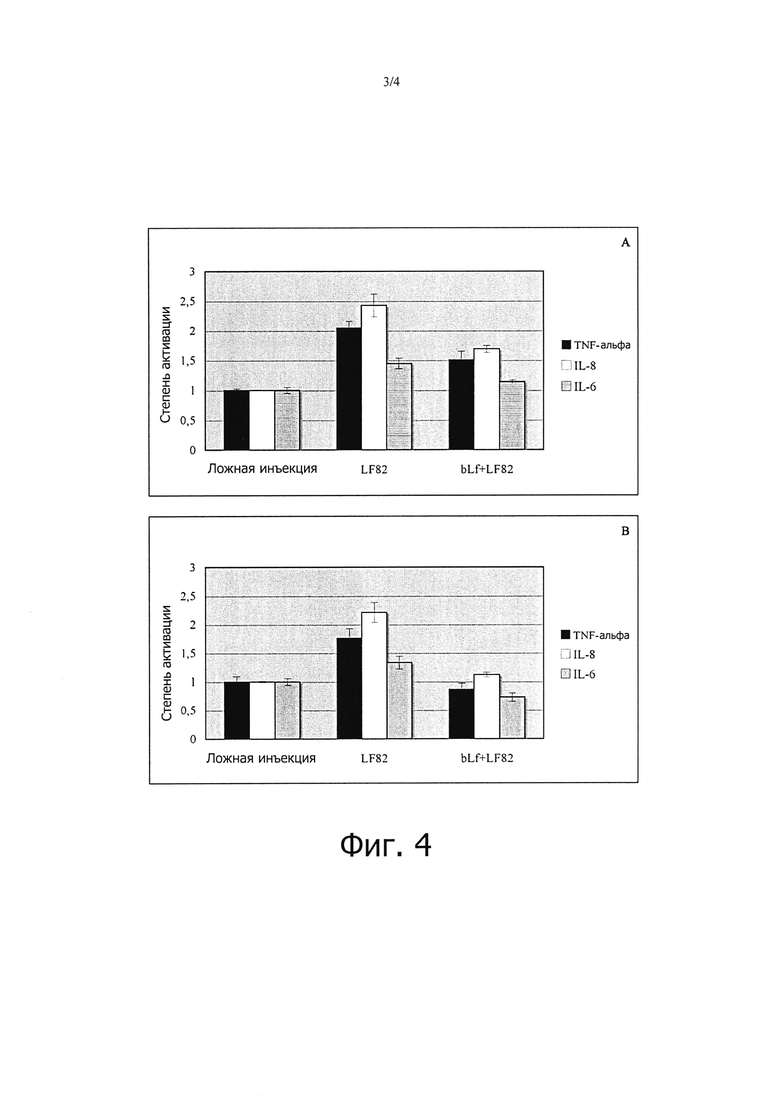
- фигуры 4 А и В представляют собой графики, показывающие влияние bLf на экспрессию мРНК TNF-альфа, IL-8 и IL-6 в культуре эксплантов слизистых оболочек, инфицированных LF82 в течение 6-ти часов (А) и 24-х часов (В); и
- фигура 5 представляет собой график, показывающий влияние добавления bLf на экспрессию мРНК провоспалительного цитокина, в особенности TNF-альфа, в клетках, обработанных INF-гамма.
Материалы и способы
Адгезивно-инвазивный штаммы Е.coli, примененные в данном исследовании, представлял собой штамм LF82 (штамм Крона из подвздошной кишки, любезно предоставленный Arlette Darfeuille-Michaud, Университет Клермона, Университет Оверни, Клермон-Ферран, Франция).
LF82 культивировали в чашках с агаром МакКонки в течение 24-х часов при 37°С и затем пересеивали в Лурия Бертани бульон (LB, Oxoid) и инкубировали в течение ночи на воздухе при 37°С. Перед инфицированием клеток, бактерии промывали и ресуспендировали в подходящих концентрациях в среде для культивирования клеток.
Культивирование клеточных линий
Клетки Сасо-2 (колоректальная аденокарцинома человека) получали из Американской коллекции типовых культур (АТСС, Rockville, MA). Клетки растили при 37°С в увлажненной атмосфере с 5% СО2 в минимальной поддерживающей среде Дульбекко (DMEM, Gibco), дополненной 10%-ной инактивированной фетальной телячьей сывороткой (FCS, Euroclone) и 2 мМ L-глутамином.
Органная культура
Исследование было одобрено комитетом по этике университетской больницы Умберто I, в которую были госпитализированы пациенты. Для каждого пациента было получено информированное согласие от родителей. После письменного согласия, макроскопическим способом от субъекта с CD получали биопсии из тканей кишечника, не вовлеченных в хронические воспалительные процессы. Для органной культуры, образцы немедленно помещали в среду Trowell Т8 и обрабатывали, как описано ниже.
Образцы биопсии слизистой оболочки помещали на железные сетки, слизистой оболочкой вверх, в центральную лунку чашки с органной культурой («Falcon», Becton Dickinson, NJ, США), содержавшую среду Trowell Т8 и среду NCTC-135 (в отношении 3:1) (Biowest, Miami, FL, США), дополненную 10%-ной FCS (Euroclone). Чашки помещали в камеру модульного инкубатора (MP Biomedicals, Aurora, Ohio, США) при высокой насыщенности кислородом (95%) и инкубировали при 37°С.
Химические реагенты
Бычий лактоферрин (bLf) и его пепсиновый гидролизат (bLfH), производства Morinaga Milk Industry Co., Ltd., растворяли в PBS в концентрации 80 мг/мл.
Анализ цитотоксичности
Для того чтобы установить максимальную нецитотоксичную дозу bLf или bLf-гидролизата, серийные разведения каждого препарата инкубировали при 37°C с различными клеточными линиями, выращенными в различных средах роста при 37°С в увлажненной инкубаторе с 5% СО2. Через 24, 48 и 72 часа, оценивали следующие параметры: число, морфологию и жизнеспособность клеток после диспергирования на индивидуальные клетки с помощью трипсина.
Антибактериальная активность
Минимальную ингибирующую концентрацию (MIC) bLf и bLfh определяли с помощью способов микроразведения в среде. Тесты выполняли с клетками LF82, которые предварительно выращивали вплоть до экспоненциальной фазы роста в среде Мюллера-Хинтона в конечной концентрации, равной 5×105 КОЕ/мл.
Сто микролитров бактерий добавляли в лунки 96-луночного планшета со 100 мкл разных концентраций bLf или bLfH (серийные двукратные разведения в интервале от 0,08 до 40 мг/мл). MIC определяли как наименьшую концентрацию белка или гидролизата, которая вызывала полное ингибирование бактериального роста через 24 часа инкубации при 37°С.
Для определения минимальной бактерицидной концентрации (МВС), из лунок, где не был обнаружен рост, отбирали объем, равный 100 мкл, распределяли на чашках TSA и инкубировали при 37°С в течение 24-х часов. МВС определяли как концентрацию, при которой число жизнеспособных клеток снижалось >99,9% (3 порядка).
Ингибирование адгезии LF82 к клеткам Сасо-2
Монослои клеток Сасо-2 получали в 24-луночных планшетах для культуры ткани («Falcon»).
Перед тестом на адгезию, клетки инкубировали при 37°С в DMEM, дополненной 10%-ной FCS в присутствии или в отсутствии bLf или bLfH (1 мг/мл). Через 2 часа, клетки инфицировали LF82 при множественности заражения (MOI), равной 1 или 10 бактерии на клетку. Через 3 часа инкубация при 37°С, клетки отмывали 3 раза и лизировали 0,1%-ным TritonX-100 и число КОЕ определяли путем посева на чашку. Бактериальную адгезию в различных экспериментальных условиях определяли как процент прикрепленных бактерии в сравнении с адгезией необработанных бактерий, которую принимали за 100%. Все анализы выполняли в трех повторностях.
Ингибирование инвазии LF82 в клетки Сасо-2
Для определения бактериальной инвазии, монослои клеток Сасо-2 инфицировали 1 или 10 бактериями на клетку. Через 3 часа инкубация при 37°С, клетки отмывали 3 раза и инкубировали в течение дополнительных 2-х часов в среде, дополненной 0,1 мг/мл гентамицина для уничтожения внеклеточных бактерий. Ингибирующую активность, равную 1 мг/мл bLf или bLfH, оценивали путем инкубирования клеток за 2 часа перед инфекцией и в процессе инфекции, в присутствии или отсутствии белков. Затем монослои отмывали и лизировали добавлением деионизированной воды, содержавшей 0,1%-ный Triton Х-100, в течение 5 мин для высвобождения интернализированных бактерий. Все анализы выполняли в трех повторностях. Бактериальную инвазию в различных экспериментальных условиях определяли как процент внутриклеточных бактерии, которые сохранили способность к культивированию после обработки гентамицином и лизиса клеток, в сравнении с необработанными бактериями, которые принимали за 100%.
Анализ цитокинов в инфицированных клетках Сасо-2
Клетки Сасо-2 инкубировали в отсутствии или в присутствии bLf bLfH в течение 2-х часов перед инфекцией и в процессе инфекции (3 часа при 37°С) с LF82 (MOI 1 или 10). В ходе инфекции, собирали культуральные супернатанты, очищенные от каких-либо клеток и патогенов центрифугированием, и хранили в замороженном виде при -80°С до применения. Супернатанты и клеточные экстракты обрабатывали для определения цитокинов (IL-6, IL-8 и TNF-альфа) с помощью количественной ПЦР в реальном времени.
Анализ цитокинов в инфицированных органных культурах
Органные культуры инкубировали в отсутствии или в присутствии bLf перед (2 часа при 37°С) и в процессе инфекции LF82 (108 КОЕ/мл). Чашки затем помещали в камеру модульного инкубатора (MP Biomedicals, Aurora, ОН) при высокой насыщенности кислородом (95%) и инкубировали при 37°С. Через 6 и 24 часов, собирали биопсии и экстрагировали суммарную РНК для анализа с помощью ПЦР с обратной транскрипции (ОТ-ПЦР).
Индукция цитокинов в клетках Сасо-2
Индукцию провоспалительных цитокинов проводили путем обработки клеток Сасо-2, в отсутствии или в присутствии bLf, с 5 нг/мл интерферона-гамма в течение 6-ти часов. Супернатанты и клеточные экстракты обрабатывали для определения цитокинов (IL-6, IL-8 и TNF-альфа) с помощью количественной ПЦР в реальном времени.
ПЦР в режиме реального времени
Экспрессию TNF-альфа, IL-8 и IL-6 детектировали с помощью ПЦР в режиме реального времени. Праймеры конструировали к нерезервированным последовательностям с помощью программы Primer Express V3.0 (Applied Biosystems, Foster City, Калифорния, Соединенные Штаты).
Праймеры:
TNF-альфа:
прямой 5'-TCTGGCCCAGGCAGTCAGATC-3';
обратный 5'-CAGTGATGTTGGGGATAAAGAGC-3';
IL-8
прямой 5'-ATGACTTCCAAGCTGGCCGTGGCT-3';
обратный 5'-TCTCAGCCCTCTTCAAAAACTTCTC-3';
IL-6:
прямой 5'-AGGGCTCTTCGGCAAATGTA3';
обратный 5'-GAAGGAATGCCCATTAACAACAA-3'.
Суммарную РНК (1 мкг) обратно транскрибировали в кДНК, применив набор High Capacity cDNA Reverse Transcription (Applied Biosystems). Амплификация с помощью ПЦР в режиме реального времени была проведена в системе обнаружения последовательностей ABI®PRISM 7300, с помощью набора SYBR®Green (Applied Biosystems). Относительные уровни транскриптов определяли, применяя ГАФД в качестве гена эндогенного контроля: примененные праймеры:
5'-TCATCAATGGAAATCCCATCA-3 и 5'-GCCAGCATCGCCCCACTT-3'.
Результаты
Влияние лактоферрина и его пепсинового гидролизата на адгезию LF82 к клеткам Сасо-2
Предварительную серию экспериментов проводили для того, чтобы определить максимальную нецитотоксическую и небактерицидную концентрацию лактоферрина и его пепсинового гидролизата. Для этой цели, 2-кратные серийные разведения белков из 4 мг/мл в MEM инкубировали с клетками Сасо-2 в течение 24-х часов при 37°С. В таких условиях, белки, в концентрации вплоть до 4 мг/мл, не влияли на какие-либо из параметров цитотоксичности (данные не показаны). Затем исследовали антибактериальную активность лактоферрина и его пепсинового гидролизата, и полученные результаты показали, что оба белка, вплоть до 40 мг/мл, не влияли на жизнеспособность бактериальных клеток. Затем протестировали влияние белков в концентрации 1 мг/мл на адгезию LF82 к клеткам Сасо-2.
Как показано на фигуре 1, bLf существенно не влиял на прикрепление LF82 к мембранам клеток Сасо-2, в то время как обработка bLfH ингибировала бактериальную адгезию приблизительно на 95 и 75% с MOI 1 и MOI 10, соответственно.
Влияние лактоферрина и его пепсинового гидролизата на инвазию LF82 в клетки Сасо-2
Затем протестировали влияние bLf и bLfH на инвазию LF82. Как показано на фигуре 2, как bLf, так и bLfH LF82 значительно ингибировали интернализацию в клетках Сасо-2, при этом bLfH был более активен по сравнению с bLf. Фактически обработка bLfH привела к ингибированию бактериальной инвазии приблизительно на 90 и 65% с MOI 1 и MOI 10, соответственно, в то время как, в тех же экспериментальных условиях, bLf снижал вход LF82 приблизительно на 75 и 60%.
Влияние bLf и bLfH на экспрессию провоспалительного цитокина
Для того чтобы понять, могут ли bLf и bLfH повлиять на продукцию провоспалительных цитокинов и, таким образом, модулировать воспаление, анализировали экспрессию мРНК фактора некроза опухолей-альфа (TNF-альфа), интерлейкина 8 (IL-8) и интерлейкина 6 (IL-6) в клетках Сасо-2, инфицированных или неинфицированных LF82. Инфицирование монослоев проводили в отсутствии или в присутствии bLf или bLfH как описано в тесте на адгезию. В данных экспериментальных условиях, отсутствие антибактериальной активности bLf и bLfH было важным для исключения возможности того, что экспрессия мРНК разных цитокинов может быть связана с различным числом жизнеспособных прикрепившихся бактерий. Полученные результаты показали, что добавление bLf не влияет на экспрессию мРНК провоспалительных цитокинов в ложно-инфицированных клетках, в то время как значительно снижает экспрессию мРНК TNF-альфа, IL-8, и IL-6 в клетках, инфицированных LF82 (фигура 3). Это влияние не было результатом прямого действия на бактериальную инвазию как в случае с bLfH, и хотя оно и было способно предотвратить интернализацию бактерий, но не было способно подавить экспрессию мРНК провоспалительных цитокинов (данные не показаны).
Влияние bLf на экспрессию мРНК TNF-альфа, IL-8 и IL-6 в культуре эксплантов слизистых оболочек, инфицированных LF82
Для моделирования условий in vivo, влияние bLf на экспрессию мРНК провоспалительных цитокинов также проанализировали на биопсиях, взятых у двух субъектов с CD, как описано в разделе «Материалы и способы», которые инфицировали LF82 и культивировали в течение 6-ти и 24-х часов как описано в разделе «Материалы и способы». Аналогично экспериментам in vitro, полученные результаты показали, что добавление bLf снижало экспрессию мРНК TNF-альфа, IL-8, и IL-6 в культуре эксплантов слизистых оболочек, инфицированных LF82, данное ингибирование было лучше выражено через 24 часа (фигура 4).
Влияние bLf на экспрессию мРНК провоспалительных цитокинов в клетках Сасо-2, обработанных INF-гамма
Экспрессия лактоферрина стимулируется в ответ на воспалительные стимулы. Противовоспалительная активность проявляется посредством ингибирования связывания липополисахарида эндотоксина воспалительными клетки, а также путем взаимодействия с эпителиальными клетками в локальных участках воспаления для ингибирования продукции воспалительных цитокинов (Conneely ОМ. Antiinflammatory activities of lactoferrin. J Am Coll Nutr. 2001 20: 389S-395S). Для оценки возможного прямого влияния bLf на синтез провоспалительного цитокина, клетки Сасо-2 обрабатывали INF-гамма в течение 6-ти часов в присутствии или в отсутствии bLf. Полученные результаты показали, что добавления bLf снижало экспрессию мРНК провоспалительных цитокинов, в особенности TNF-альфа, в обработанных INF-гамма клетках (фигура 5).
Следующие неограничивающие примеры предназначены для более подробного объяснения изобретения.
ПРИМЕР 1
200 г бычьего лактоферрина загружали в смеситель с большими сдвиговыми усилиями, оборудованный нагревательной рубашкой, и замешивали с 50 г цетилового спирта, предварительно нагретого до температуры размягчения.
Затем, смесь гранулировали с водной суспензией, содержавшей 15 г поливинилпирролидона до получения гомогенного гранулированного продукта.
5 г поливинилпирролидона и 80 г гидроксипропилметилцеллюлозы гидрофильной матрицы добавляли в тот же смеситель с большими сдвиговыми усилиями.
Компоненты перемешивали до получения гомогенной дисперсии матриц. Затем 100 г микрокристаллической целлюлозы, 5 г стеарата магния, 5 г талька и 10 г коллоидного диоксида кремния добавляли в порядке упоминания.
Смесь прессовали так, чтобы получить конечную унитарную массу, равную 470 мг/таблетка, подходящую для обеспечения 200 мг активного ингредиента для каждой таблетки.
Полученные таблетки затем покрывали пленочной оболочкой из гидроксипропилметилцеллюлозы и пластификаторов.
Таблетки, подвергнутые тесту на растворение в желудочном соке и в моделированной кишечной среде в соответствии с действующей редакцией Европейской Фармакопеи, показали следующий профиль высвобождения: через 60 минут менее чем 30%, через 180 минут менее чем 60%, через 5 часов менее чем 80%.
ПРИМЕР 2
20 г бычьего лактоферрина загружали в гранулятор/гомогенизатор и добавляли 10 г воска карнаубы и 45 г цетилового спирта. Смесь нагревали до температуры размягчения и получали гомогенную смесь.
155 г гидроксипропилметилцеллюлозы гидрофильной матрицы и 50 мг поликарбофила добавляли в тот же смеситель.
Компоненты перемешивали до получения гомогенной дисперсии матрицы. Затем, 210 г фосфата кальция, 5 г стеарата магния и 5 г коллоидного диоксида кремния добавляли в порядке упоминания.
Смесь прессовали вплоть до конечной унитарной массы, равной 500 мг/таблетка, подходящей для обеспечения 20 мг активного ингредиента для каждой таблетки.
Полученные таблетки затем покрывали пленочной оболочкой гидроксипропилметилцеллюлозы и пластификаторов.
Таблетки, протестированные на растворение в желудочном соке и в моделированной кишечной среде в соответствии с действующей редакцией Европейской Фармакопеи, показали следующий профиль высвобождения: через 60 минут менее чем 25%, через 180 минут менее чем 50%, через 5 часов менее чем 70%.
ПРИМЕР 3
300 г микрогранул, изготовленных из микрокристаллической целлюлозы и кукурузного крахмала, загружали в систему Wuster с псевдоожиженным слоем; 100 г бычьего лактоферрина с 20 г поливинилпирролидона суспендировали одновременно путем загрузки поверх микрогранул.
Затем для получения гомогенных микрогранул выполняли покрытие пленкой с помощью водного раствора, содержавшего 50 г поливинилпирролидона и 50 г этилцеллюлозы.
Затем капсулы размером 0 заполняли смесью до конечной унитарной массы, равной 520 мг/капсула с получением 100 мг активного ингредиента на одну капсулу.
Капсулы, протестированные на растворение в желудочном соке и в моделированной кишечной среде в соответствии с действующей редакцией Европейской Фармакопеи, показали следующий профиль высвобождения: в желудочном соке через 120 минут 0%, в кишечном соке через 60 минут менее чем 25%, через 180 минут менее чем 50%, через 6 часов менее чем 80%.
ПРИМЕР 4
200 г микрокристаллической целлюлозы со 100 г кукурузного крахмала загружали в псевдоожиженный слой с 200 г бычьего лактоферрина.
Смесь гранулировали с водный раствором, содержащим 50 г поливинилпирролидона, и получали гомогенное гранулированное изделие.
Затем, 150 г гидроксипропилметилцеллюлозы, 5 г стеарата магния и 5 г коллоидного диоксида кремния добавляли.
Смесь затем прессовали до конечную унитарной массы 710 мг/таблетка для обеспечения 200 мг активного ингредиента, содержащегося в одной таблетке.
Полученные таблетки затем покрывали пленочной оболочкой из полиметакрилатов и пластификаторов для обеспечения устойчивости к желудочному соку и предупреждения высвобождения активного ингредиента в желудке.
Таблетки, протестированные на растворение в желудочном соке и в моделированной кишечной среде, показали следующий профиль высвобождения: в желудочном соке 0% через 120 минут, в кишечном соке через 60 минут менее чем 25%, через 180 минут менее чем 50%, через 6 часов менее чем 80%.
ПРИМЕР 5
800 г бычьего лактоферрина загружали в гранулятор/гомогенизатор, и добавляли 400 г гидроксипропилметилцеллюлозы, 480 г маннитола, 252 г микрокристаллической целлюлозы.
Смесь перемешивали в течение 15 минут.
20 г стеариновой кислоты, 8 г кроскармеллозы, 20 г лецитина, 40 г коллоидного диоксида кремния и 20 г стеарата магния добавляли в порядке упоминания.
Смесь прессовали до конечной унитарной массы, равной 510 мг/таблетка для обеспечения одной таблетки, содержавшей каждая 200 мг активного ингредиента.
Полученные таблетки покрывали 500 г шеллака (aquagold 25%), 50 г гидроксипропилметилцеллюлозы и 25 г глицерина для получения 50 мг таблетки с кишечнорастворимым пленочным покрытием.
Покрытые таблетки протестировали на растворение в желудочном соке и в моделированной кишечной среде в соответствии с действующей редакцией Европейской Фармакопеи. Тесты показали следующий профиль высвобождения: в желудочном соке через 120 минут 0%, в кишечном соке через 60 минут менее чем 25%, через 180 минут менее чем 50% через 8 часов не менее 80%, через 12 часов >80%.
ПРИМЕР 6
800 г бычьего лактоферрина загружали в смеситель/гомогенизатор, затем добавляли 400 г гидроксипропилметилцеллюлозы, 480 г маннитола, 252 г микрокристаллической целлюлозы.
Смесь перемешивали в течение 15-ти минут для получения гомогенной смеси.
Добавление осуществляли в следующем порядке: 20 г стеариновой кислоты, 8 г кроскармеллозы, 20 г лецитина, 40 г коллоидного диоксида кремния и 20 г стеарата магния.
Смесь прессовали до конечной унитарной массы, равной 510 мг/таблетка, для обеспечения таблетки, содержавшей 200 мг активного ингредиента в одной таблетке.
Полученные таблетки покрывали водным раствором, содержавшим 40 г гидроксипропилметилцеллюлозы и 8 г талька, для получения 12 мг покрытой оболочкой таблетки.
Таблетки, протестированные на растворение в желудочном соке и в моделированной кишечной среде в соответствии с действующей редакцией Европейской Фармакопеи, показали следующий профиль высвобождения: через 60 минут менее чем 25%, через 180 минут менее чем 60%, через 8 часов менее чем 80.
ПРИМЕР 7
800 г бычьего лактоферрина загружали в смеситель/гомогенизатор и добавляли 416 г микрокристаллической целлюлозы, 496 г маннитола.
Смесь перемешивали в течение 15-ти минут.
20 г стеариновой кислоты, 160 мг поперечно-сшитого ПВП, 60 г кроскармеллозы, 20 г лецитина, 40 г коллоидного диоксида кремния и 20 г стеарата магния добавляли в указанном порядке.
Смесь прессовали вплоть до конечной унитарной массы, равной 510 мг/таблетка, для обеспечения таблетки, содержавшей 200 мг активного ингредиента в одной таблетке.
Полученные таблетки покрывали 480 г шеллака (aquagold 25%), 48 г гидроксипропилметилцеллюлозы, 24 г глицерина для получения 50 мг покрытой кишечнорастворимой пленкой таблетки.
Покрытые таблетки, протестированные на растворение в желудочном соке и в моделированной кишечной среде в соответствии с действующей редакцией Европейской Фармакопеи, показали следующий профиль высвобождения: в желудочном соке через 120 минут 0%, в кишечном соке через 60 минут менее чем 25%, через 180 минут >70%, через 300 минут >80%.
ПРИМЕР 8
200 г бычьего лактоферрина загружали в смеситель с большими сдвиговыми усилиями с нагревательной рубашкой и замешивали с 50 г лауроилполиоксиглицеридов, предварительно доведенных до температуры размягчения.
Смесь далее гранулировали с раствором/водной суспензией, содержавшей 15 г поливинилпирролидона до получения гомогенного гранулята.
5 г кросповидона и 80 г гидроксипропилметилцеллюлозы добавляли в тот же смеситель.
Компоненты перемешивали до получения гомогенной дисперсии матриц. Затем, 100 г микрокристаллической целлюлозы, 5 г стеарата магния, 5 г талька и 10 г коллоидного диоксида кремния добавляли в порядке упоминания.
Смесь прессовали вплоть до конечной унитарной массы, равной 470 мг/срr, что подходит для введения 200 мг активного ингредиента для каждой таблетки.
Полученные таблетки затем покрывали пленочной оболочкой из гидроксипропилметилцеллюлозы и пластификаторов.
Таблетки, протестированные на растворение в желудочном соке и в моделированной кишечной среде в соответствии с действующей редакцией Европейской Фармакопеи, показали следующий профиль высвобождения: через 60 минут не более чем 30%, через 180 минут не более чем 60%, через 5 часов не более чем 80%.
ПРИМЕР 9
20 г бычьего лактоферрина загружали в гранулятор/гомогенизатор и затем добавляли 55 г стеароилглицеридов. Смесь гранулировали вплоть до температуры размягчения и получали гомогенную смесь. Затем в тот же смеситель добавляли 205 г гидроксипропилметилцеллюлозы.
Компоненты смешивали до получения гомогенной дисперсии матриц и затем 210 г фосфата кальция, 5 г стеарата магния и 5 г коллоидного диоксида кремния добавляли в порядке упоминания.
Смесь прессовали вплоть до конечной унитарной массы, равной 500 мг/срr, подходящей для введения 20 мг активного ингредиента для каждой таблетки.
Полученные таблетки затем покрывали пленочной оболочкой из гидроксипропилметилцеллюлозы и пластификаторов.
Таблетки, протестированные на растворение в желудочном соке и в моделированной кишечной среде в соответствии с действующей редакцией Европейской Фармакопеи, показали следующий профиль высвобождение: через 60 минут не более чем 25%, через 180 минут не более чем 50%, через 5 часов не более чем 70%.

Изобретение относится к фармации и медицине. Предложена пероральная композиция c отложенным и/или замедленным высвобождением для лечения воспалительных заболеваний кишечника, вызванных инвазией адгезивно-инвазивной Escherichia coli (AIEC), включающая лактоферрин, погруженный в сердцевину резервуара, покрытого полупроницаемой пленкой, или растворенный, и/или диспергированный, и/или включенный в матрицу, содержащую липиды, гидрофильные, амфифильные вещества и их смеси, и внешнее покрытие включает устойчивые к действию желудочного сока средства для покрытия (шеллак, полиметакрилаты, производные целлюлозы), или полупроницаемая пленка включает производные целлюлозы. Технический результат состоит в снижении адгезии AIEC к клеткам кишечника Сасо-2 и в снижении их инвазии в указанные клетки. 6 з.п. ф-лы, 5 ил., 9 пр.
1. Пероральная композиция c отложенным и/или замедленным высвобождением для лечения воспалительных заболеваний кишечника, вызванных инвазией адгезивно-инвазивной Escherichia coli (AIEC), включающая лактоферрин, погруженный в сердцевину резервуара, покрытого полупроницаемой пленкой, или лактоферрин, растворенный, и/или диспергированный, и/или включенный в матрицу, и внешнее покрытие, где указанная матрица включает вещества, выбранные из группы, состоящей из липидных веществ, гидрофильных веществ, амфифильных веществ и их смесей, и внешнее покрытие включает устойчивые к действию желудочного сока средства для покрытия, которые выбирают из группы, состоящей из шеллака, полиметакрилатов, ацетофталата целлюлозы и производных альгината, или полупроницаемая пленка включает производные целлюлозы, которые выбирают из группы, состоящей из этилцеллюлозы, метилцеллюлозы, метилэтилцеллюлозы и гидроксипропилметилцеллюлозы.
2. Пероральная композиция по п. 1, в которой указанные воспалительные заболевания кишечника представляют собой болезнь Крона.
3. Пероральная композиция по п. 1, в которой указанные липидные вещества выбирают из группы, состоящей из жирных спиртов, жирных кислот, триглицеридов, восков.
4. Пероральная композиция по п. 1, в которой указанные гидрофильные вещества выбирают из группы, состоящей из полимеров или сополимеров акриловой или метакриловой кислоты, полимеров алкилвинилового эфира, гидроксиалкилцеллюлоз, карбоксиалкилцеллюлоз, полисахаридов, альгинатов, пектинов, крахмалов, натуральных и синтетических смол, поликарбофила и их смесей.
5. Пероральная композиция по п. 1, в которой указанные амфифильные вещества выбирают из группы, состоящей из лецитина, фосфатидилхолина, фосфатидилэтаноламина, простых алкиловых эфиров гликолей, таких как моноэтиловый эфир диэтиленгликоля, макроголглицеридов, полиэтиленгликоля гидроксистеараты, восков, лаурилсульфата натрия, додецилсульфата натрия, полисорбатов, желчных кислот, полоксамера, сульфосукцината натрия, лауроилсаркозината натрия и их смесей.
6. Пероральная композиция по п. 1, в которой количество лактоферрина составляет от 50 мг до 250 мг.
7. Пероральная композиция по п. 1, которая дополнительно включает фармацевтически приемлемые эксципиенты.
| FLORES-VILLASENOR H et al | |||
| Соломорезка | 1918 |
|
SU157A1 |
| Biochem | |||
| Cell Biol | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Устройство для моделирования движения селевых потоков | 1986 |
|
SU1350519A1 |
| SUZUKI N | |||
| et al | |||
| Effects of enteric-coated lactoferrin tablets containing Lactobacillus brevis subsp | |||
| coagulans on fecal properties, defecation frequency and intestinal microbiota of Japanese women with tendency for constipation: a randomized placebo-controlled crossover study | |||
| Biosci | |||
| Microbiota Food Health | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| JP 2006111558 A, 27.04.2006 | |||
| СПОСОБ ПОЛУЧЕНИЯ БАКТЕРИАЛЬНОГО ЛАКТОФЕРРИНА | 2008 |
|
RU2418071C2 |
Авторы
Даты
2019-05-30—Публикация
2014-09-04—Подача