Ссылка на перечень последовательностей
Данная заявка содержит перечень последовательностей в машиночитаемой форме, который включен в данный документ с помощью ссылки.
Область изобретения
Настоящее изобретение относится к применению полипептида, обладающего дезоксирибонуклеазной (ДНКазной) активностью, для предотвращения или уменьшения повторного осаждения грязи на изделии в ходе процесса последующей чистки или стирки. Изобретение относится также к моющей композиции, содержащей полипептид, обладающий дезоксирибонуклеазной активностью (ДНКаза), и способу предотвращения или уменьшения повторного осаждения грязи на изделии в ходе процесса последующей чистки или стирки.
Предпосылки изобретения
Как правило, микроорганизмы живут прикрепленными к поверхностям во многих природных, промышленных и медицинских средах, инкапсулированными внеклеточными веществами, в том числе биополимерами и макромолекулами. Полученный в результате слой инкапсулированного в слизи микроорганизма называют биопленкой. Биопленки представляют собой преобладающую форму роста бактерий в природной среде, и бактерии, растущие в биопленках, проявляют различные физиологические свойства. По сравнению с их планктонно растущими эквивалентами, бактерии в биопленке являются более устойчивыми к воздействию антибиотиков, УФ-облучению, моющим средствам и иммунному ответу хозяина.
На протяжении многих лет известна проблема, заключающаяся в том, что с течением времени подлежащие стирке изделия, такие как рубашки и блузки, становятся все более и более серыми. Для обычной дневной одежды, а также одежды для активного отдыха пот и возникающий в результате запах представляет собой непростую задачу. Как правило, такие пятна состоят из большого количества различных компонентов, прилипающих к ткани одежды, и могут быть труднорастворимыми и трудноудаляемыми. Если используются такие подлежащие стирке изделия, как футболки или одежда для активного отдыха, то они контактируют с потом и бактериями тела пользователя, а также прочими видами загрязнения из остальной окружающей среды, в которой их применяют. Некоторые из таких бактерий способны прилипать к подлежащему стирке изделию и образовывать на данном изделии биопленку. Присутствие бактерий подразумевает, что подлежащие стирке изделия становятся липкими, и следовательно грязь прилипает к липким областям. Такая грязь оказывается трудноудаляемой с помощью коммерчески доступных моющих композиций. Кроме того, если сильно загрязненные подлежащие стирке изделия стирают вместе с менее загрязненными подлежащими стирке изделиями, то загрязнение, присутствующее в моющей жидкости, обычно прилипает к биопленке. В результате этого подлежащее стирке изделие является более "грязным" и более серым после стирки, чем перед стиркой.
Одежда для активного отдыха является хорошим примером, потому что часто грязь, глина и дорожное загрязнение бывают на одежде, выстиранной вместе с очень потными рубашками. От стирки до стирки предметы одежды становятся все более и более серыми, и в конце концов это проявляется в виде хорошо заметных пятен. Такой вид грязи является одной из причин, почему люди отказываются от предметов своей одежды. Несмотря на то, что данная проблема является хорошо известной для большинства видов одежды, такая проблема является очень выраженной для меланжевых тканей. Что касается стирки, то в Европе существует политическое требование беречь природные ресурсы, что привело в ЕС к принятию закона о маркировке для стиральных машин с целью исключения машин с высоким потреблением энергии. Это означает, что холодная вода для стирки гораздо более распространена в странах ЕС, и, таким образом, условия стирки во всех остальных странах мира становится более похожими. Тем не менее, экономия энергии с помощью стирки при более низкой температуре может приводить к тому, что потребители отказываются от предметов одежды и приобретают новую, потому что пятна пота как следует не удаляются. Существует настоятельная необходимость в решении проблемы эффективного удаления пятен пота.
Международная заявка на патент WO 2011/098579 касается соединений бактериальной дезоксирибонуклеазы и способов разрушения и предотвращения образования биопленки.
Краткое описание настоящего изобретения
Настоящее изобретение относится к применению полипептида, обладающего ДНКазной активностью, для предотвращения или уменьшения повторного осаждения грязи на изделии в ходе процесса последующей чистки или стирки. Изобретение относится также к моющей композиции, содержащей полипептид с дезоксирибонуклеазной (ДНКазной) активностью. Далее заявляется способ предотвращения или уменьшения повторного осаждения грязи на изделии в ходе процесса последующей чистки или стирки, включающий стадии:
а) приведение изделия в контакт с композицией в соответствии с настоящим изобретением или с жидким раствором, содержащими полипептид, обладающий ДНКазной активностью; и
b) необязательно полоскание изделия,
где изделие представляет собой текстильное изделие или твердую поверхность.
Определения
Термин алкил означает углеводородную группу, которая является прямой или разветвленной, насыщенной или ненасыщенной. Если не указано иное, алкильные группы являются предпочтительно насыщенными или ненасыщенными двойными связями, предпочтительно одной или двумя двойными связями. В термин "алкил" включена алкильная часть ацильных групп.
Термин "композиция для автоматизированного мытья посуды" относится к композициям, предназначенным для чистки посуды, такой как тарелки, чашки, стаканы, миски, столовых приборов, таких как ложки, ножи, вилки, сервировочные принадлежности, керамики, пластмассы, металлов, фарфора, стекла и акрила в посудомоечной машине. Термины охватывают любые материалы/соединения, выбранные для бытовых или промышленных применений для стирки, и форма продукта может представлять собой жидкость, порошок или гранулят. В дополнение к липазе, композиция для автоматизированного мытья посуды содержит моющие компоненты, такие как полимеры, отбеливающие системы, активаторы отбелки, катализаторы отбелки, силикаты, красители и средства по уходу за металлом.
Аллельный вариант. Термин "аллельный вариант" означает любую из двух или более альтернативных форм гена, занимающих один и тот же хромосомный локус. Аллельное разнообразие возникает в естественных условиях вследствие мутации и может приводить к полиморфизму в пределах популяций. Генные мутации могут быть молчащими (никаких изменений в кодируемом полипептиде) или могут кодировать полипептиды, имеющие измененные аминокислотные последовательности. Аллельный вариант полипептида представляет собой полипептид, кодируемый аллельным вариантом гена.
Бактериальный. В контексте настоящего изобретения термин "бактериальный" в отношении полипептида (такого как фермент, например, ДНКаза) относится к полипептиду, кодируемому геномом бактерий и, таким образом, непосредственно получаемому из данного генома, при этом такие бактерии не были генетически модифицированы для кодирования указанного полипептида, например, введением кодирующей последовательности в геном с помощью методики рекомбинантной ДНК. В контексте настоящего изобретения термины "бактериальная ДНКаза", или "полипептид, обладающий ДНКазной активностью, полученный из бактериального источника", или "полипептид бактериального происхождения", таким образом, относится к ДНКазе, кодируемой геномом видов бактерий, и, таким образом, непосредственно получаемой из данного генома, где виды бактерий не подвергались генетической модификации с введением рекомбинантной ДНК, кодирующей указанную ДНКазу. Таким образом, нуклеотидная последовательность, кодирующая бактериальный полипептид, обладающий ДНКазной активностью, представляет собой последовательность, в естественных условиях находящуюся в генетическом окружении видов бактерий. Бактериальный полипептид, обладающий ДНКазной активностью, кодируемый такой последовательностью, может также относиться к ДНКазе дикого типа (исходной ДНКазе). В следующем аспекте в настоящем изобретении предусматриваются полипептиды, обладающие ДНКазной активностью, где указанные полипептиды, по сути, гомологичны бактериальной ДНКазе. В контексте настоящего изобретения термин "по сути, гомологичный" обозначает полипептид, обладающий ДНКазной активностью, который по меньшей мере на 80%, предпочтительно по меньшей мере на 85%, более предпочтительно по меньшей мере на 90%, более предпочтительно по меньшей мере на 95%, еще более предпочтительно по меньшей мере на 96%, 97%, 98% и наиболее предпочтительно по меньшей мере на 99% идентичен аминокислотной последовательности выбранной бактериальной ДНКазы.
Биопленка. Биопленка представляет собой любую группу микроорганизмов, в которой клетки прилипают друг к другу или прилипают к поверхности, такой как текстильное изделие, посуда, или твердая поверхность, или другой вид поверхности. Данные прилипшие клетки часто встроены внутрь самопродуцируемой матрицы внеклеточного полимерного вещества (EPS). Биопленка EPS представляет собой полимерный конгломерат, как правило состоящий из внеклеточной ДНК, белков и полисахаридов. Биопленки могут образовываться на живых или неживых поверхностях. Микробные клетки, растущие в биопленке, физиологически отличается от планктонных клеток того же организма, которые, напротив, представляют собой отдельные клетки, которые могут держаться на поверхности или плавать в жидкой среде.
Бактерии, живущие в биопленке, обычно характеризуются свойствами, которые значительно отличаются от свойств планктонных бактерий того же вида, поскольку густая и защищенная среда пленки позволяет им объединяться и взаимодействовать различными способами. Одним преимуществом такой среды для микроорганизмов является повышенная устойчивость к моющим средствам и антибиотикам, поскольку плотная внеклеточная матрица и наружный слой клеток защищают внутреннюю часть сообщества.
На подлежащих стирке изделиях бактерии, образующие биопленку, могут быть обнаружены среди следующих видов: Acinetobacter sp., Aeromicrobium sp., Brevundimonas sp., Microbacterium sp., Micrococcus luteus, Pseudomonas sp., Staphylococcus epidermidis и Stenotrophomonas sp. На твердых поверхностях бактерии, образующие биопленку, могут быть найдены среди следующих видов: Acinetobacter sp., Aeromicrobium sp., Brevundimonas sp., Microbacterium sp., Micrococcus luteus, Pseudomonas sp., Staphylococcus epidermidis и Stenotrophomonas sp. В одном варианте осуществления штаммом, образующим биопленку, является Brevundimonas sp. В одном варианте осуществления штаммом, образующим биопленку, является Pseudomonas alcaliphila или Pseudomonas fluorescens.
кДНК. Термин "кДНК" означает молекулу ДНК, которую можно получить с помощью обратной транскрипции из зрелой сплайсированной молекулы мРНК, полученной из эукариотической или прокариотической клетки. В кДНК отсутствуют интронные последовательности, которые могут присутствовать в соответствующей геномной ДНК. Исходный, первичный РНК-транскрипт является предшественником мРНК, который подвергается процессингу в ходе ряда стадий, включая сплайсинг, перед тем как станет зрелой сплайсированной мРНК.
Кодирующая последовательность. Термин "кодирующая последовательность" означает полинуклеотид, который непосредственно определяет аминокислотную последовательность полипептида. Пределы кодирующей последовательности обычно определяются открытой рамкой считывания, которая начинается со стартового кодона, такого как ATG, GTG или TTG, и заканчивается стоп-кодоном, таким как TAA, TAG или TGA. Кодирующая последовательность может представлять собой геномную ДНК, кДНК, синтетическую ДНК или их комбинацию.
Цветовое различие (L-значение). Цветовое пространство Lab представляет собой цветоппонентное пространство с величиной L для обозначения яркости. L-значение, L* обозначает самый темный черный при L*=0 и самый светлый белый при L*=100. В контексте настоящего изобретения L-значение также называют цветовым различием. Способ цветового различия используется в разделе примеров настоящей заявки на патент.
Контрольные последовательности. Термин "контрольные последовательности" означает последовательности нуклеиновых кислот, необходимые для экспрессии полинуклеотида, кодирующего зрелый полипептид по настоящему изобретению. Каждая контрольная последовательность может быть нативной (т. е. из того же гена) или чужеродной (т. е. из другого гена) по отношению к кодирующему полипептид полинуклеотиду или нативной или чужеродной по отношению друг к другу. Такие контрольные последовательности включают в себя без ограничения лидерную последовательность, последовательность полиаденилирования, пропептидную последовательность, промотор, последовательность сигнального пептида и терминатор транскрипции. Как минимум, контрольные последовательности включают в себя промотор и сигналы остановки транскрипции и трансляции. Контрольные последовательности могут быть снабжены линкерами с целью введения специфических сайтов рестрикции, способствующих лигированию контрольных последовательностей с кодирующим участком полинуклеотида, кодирующего полипептид.
Под термином "глубокая чистка" подразумевается разрушение, уменьшение или устранение биопленки или компонентов биопленки, таких как полисахариды, белки, ДНК, грязь или другие компоненты, присутствующие в биопленке. Любая чистка, которая не разрушает, не уменьшает или не удаляет биопленку, не является глубокой чисткой.
Моющие компоненты. Термин ʺмоющие компонентыʺ в данном документе определен как означающий типы химических веществ, которые могут использоваться в моющих композициях. Примерами моющих компонентов являются поверхностно-активные вещества, гидротропы, моющие компоненты, дополнительные моющие компоненты, комплексообразователи или хелатирующие средства, отбеливающая система или отбеливающие компоненты, полимеры, окрашивающие средства для тканей, кондиционеры для тканей, пенообразователи, подавители образования мыльной пены, диспергирующие средства, ингибиторы переноса красителей, флуоресцентные отбеливающие средства, отдушка, оптические отбеливатели, бактерициды, фунгициды, средства, суспендирующие грязь, грязеотталкивающие полимеры, средства против повторного осаждения, ингибиторы или стабилизаторы ферментов, активаторы ферментов, антиоксиданты и солюбилизаторы.
Моющая композиция. Термин "моющая композиция" относится к композициям, которые находят применение в удалении нежелательных соединений с изделий, подлежащих очистке, таких как текстильные изделия. Моющую композицию можно применять, например, для чистки текстильных изделий, как для чистки в домашних условиях, так и для промышленной чистки. Термины охватывают любые материалы/соединения, выбранные для конкретного типа желаемой композиции для чистки, и форму продукта (например, жидкость, гель, порошок, гранулят, паста или композиции для распыления) и включает без ограничения моющие композиции (например, жидкие и/или твердые моющие средства для стирки белья и моющие средства для тонких тканей; освежители тканей; мягчители тканей; а также средства для предварительного замачивания/предварительной обработки для текстильных изделий и белья для стирки). В дополнение к содержащемуся ферменту по настоящему изобретению, моющий состав может содержать один или несколько дополнительных ферментов (например, протеазы, амилазы, липазы, кутиназы, целлюлазы, эндоглюканазы, ксилоглюканазы, пектиназы, пектин-лиазы, ксантаназы, пероксидазы, галогенпероксигеназы, каталазы и маннаназы или любую их смесь) и/или моющих добавочных ингредиентов, таких как поверхностно-активные вещества, моющие компоненты, комплексообразователи или хелатирующие средства, отбеливающую систему или отбеливающие компоненты, полимеры, кондиционеры для тканей, пенообразователи, подавители образования мыльной пены, красители, отдушку, ингибиторы потускнения, оптические отбеливатели, бактерициды, фунгициды, средства, суспендирующие грязь, антикоррозионные средства, ингибиторы или стабилизаторы ферментов, активаторы ферментов, трансферазу(трансферазы), гидролитические ферменты, оксидоредуктазы, виды синьки и флуоресцентные красители, антиоксиданты и солюбилизаторы.
Посуда. Термин "посуда" предназначен для любой формы кухонной посуды, набора посуды или столовой посуды, такой как без ограничения сковородки, гончарная посуда, столовые приборы, такие как тарелки, чашки, ножи, вилки, ложки, фарфор и т. д.
Композиция для мытья посуды. Термин "композиция для мытья посуды" относится к композициям, содержащим моющие компоненты, композиция которых является подходящей и предназначенной для чистки посуды, столовой посуды, гончарной посуды, кастрюль, сковородок, столовых приборов. В одном варианте осуществления настоящего изобретения композицию для мытья посуды можно использовать для чистки областей твердых поверхностей на кухнях. Настоящее изобретение не ограничивается каким-либо конкретным типом композиции для мытья посуды или каким-либо конкретным моющим средством.
ДНКаза (дезоксирибонуклеаза). Термин "ДНКаза" означает полипептид с ДНКазной активностью, который катализирует гидролитическое расщепление связей на основе сложного фосфодиэфира в каркасе ДНК, разрушая таким образом ДНК. Для целей настоящего изобретения ДНКазную активность определяют в соответствии с процедурой, описанной в анализе I. В одном аспекте полипептиды по настоящему изобретению характеризуются по меньшей мере 20%, например, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 100% ДНКазной активности зрелого полипептида под SEQ ID NO: 2. Для целей настоящего изобретения ДНКазную активность можно определять в соответствии с процедурой, описанной в анализе I. В одном варианте осуществления по настоящему изобретению ДНКазная активность полипептида характеризуется по меньшей мере 105%, например, по меньшей мере 110%, по меньшей мере 120%, по меньшей мере 130%, по меньшей мере 140%, по меньшей мере 160%, по меньшей мере 170%, по меньшей мере 180% или по меньшей мере 200% ДНКазной активности зрелого полипептида под SEQ ID NO: 2, полинуклеотида, содержащего или состоящего из последовательности, изложенной под SEQ ID NO: 3, полинуклеотида, содержащего или состоящего из последовательности, изложенной под SEQ ID NO: 5, полинуклеотида, содержащего или состоящего из зрелого полипептида под SEQ ID NO: 6, полинуклеотида, содержащего или состоящего из зрелого полипептида под SEQ ID NO: 7, полинуклеотида, содержащего или состоящего из зрелого полипептида под SEQ ID NO: 8.
Преимущество моющего средства с ферментами. Термин "преимущество моющего средства с ферментами" в данном документе определяют как полезный эффект, который фермент может придавать моющем средству, по сравнению с таким же моющим средством без такого фермента. Важными преимуществами моющих средств, которые могут обеспечиваться ферментами, являются устранение пятен без видимой грязи или с очень небольшим ее количеством после стирки и/или чистки, предотвращение или уменьшение повторного осаждения видов грязи, высвободившейся в процессе мытья (эффект, который также называется препятствованием повторному осаждению), полное или частичное восстановление белизны текстильных изделий, которые изначально были белыми, однако после многократного использования и стирки приобрели сероватый или желтоватый вид (эффект, который также называется отбеливанием). Преимущества, связанные с уходом за текстильными изделиями, которые непосредственно не относятся к каталитическому устранению пятен или предотвращению повторного осаждения видов грязи, также являются важными преимуществами моющего средства с ферментами. Примерами таких преимуществ, связанных с уходом за текстильными изделиями, являются предотвращение или уменьшение переноса красителя с одной ткани на другую ткань или другую часть той же ткани (эффект, который также называется ингибированием переноса красителя или препятствованием переотложению красителя), устранение выступающих или порванных волокон с поверхности ткани для уменьшения склонности к скатыванию волокна в узелки или устранения уже существующих узелков или взлохмачивания (эффект, который также называется препятствованием скатыванию волокна в узелки), улучшение мягкости ткани, осветление цвета ткани и устранение загрязнений в форме мелких частиц, которые захвачены волокнами ткани или предметами одежды. Ферментная отбелка представляет собой дополнительное преимущество моющего средства с ферментами, где каталитическая активность, как правило, используется для катализа образования отбеливающих компонентов, таких как пероксид водорода или другие пероксиды.
Экспрессия. Термин "экспрессия" предусматривает любую стадию, связанную с образованием полипептида, в том числе без ограничения транскрипцию, посттранскрипционную модификацию, трансляцию, посттрансляционную модификацию и секрецию.
Вектор экспрессии. Термин "вектор экспрессии" означает линейную или кольцевую молекулу ДНК, которая содержит полинуклеотид, кодирующий полипептид, и функционально связана с контрольными последовательностями, которые предусмотрены для ее экспрессии.
Фрагмент. Термин "фрагмент" означает полипептид, содержащий один или несколько (например, некоторое количество) аминокислот с амино и/или карбоксильного конца зрелого полипептида или домена; где фрагмент обладает ДНКазной активностью. В одном аспекте фрагмент содержит по меньшей мере 206 аминокислотных остатков (например, аминокислоты с 1 по 206 последовательности под SEQ ID NO: 2), по меньшей мере 205 аминокислотных остатков (например, аминокислоты 2-206 последовательности под SEQ ID NO: 2) или по меньшей мере 204 аминокислотных остатка (например, аминокислоты 3-206 последовательности под SEQ ID NO: 2). В одном аспекте фрагмент содержит по меньшей мере 139 аминокислотных остатков (например, аминокислоты 50-188 последовательности под SEQ ID NO: 5), или по меньшей мере 188 аминокислотных остатков (например, аминокислоты 1-188 последовательности под SEQ ID NO: 5).
Грибной. В контексте настоящего изобретения термин "грибной" относительно полипептида (такого как фермент, например, ДНКаза) относится к полипептиду, кодируемому геномом гриба и, таким образом, непосредственно получаемому из данного генома гриба, при этом такой гриб не был генетически модифицированным для кодирования указанного полипептида, например, путем введения кодирующей последовательности в геном с помощью методики рекомбинантной ДНК. В контексте настоящего изобретения термин "грибная ДНКаза", или "полипептид, обладающий ДНКазной активностью, полученной из грибного источника", или "полипептид грибного происхождения", таким образом, относится к ДНКазе, кодируемой геномом видов грибов и, таким образом, непосредственно получаемой из них, где виды грибов не подвергались генетической модификации с введением рекомбинантной ДНК, кодирующей указанную ДНКазу. Таким образом, нуклеотидная последовательность, кодирующая грибной полипептид, который обладает ДНКазной активностью, представляет собой последовательность, в естественных условиях находящуюся в генетическом окружении видов грибов. Грибной полипептид, обладающий ДНКазной активностью, который кодируется такой последовательностью, может относится также к ДНКазе дикого типа (или исходной ДНКазе). В следующем аспекте в настоящем изобретении предусматриваются полипептиды, обладающие ДНКазной активностью, где указанные полипептиды, по сути, гомологичны грибной ДНКазе. В контексте настоящего изобретения термин "по сути, гомологичный" обозначает полипептид, обладающий ДНКазной активностью, который по меньшей мере на 80%, предпочтительно по меньшей мере на 85%, более предпочтительно по меньшей мере на 90%, более предпочтительно по меньшей мере на 95%, еще более предпочтительно по меньшей мере на 96%, 97%, 98%, и наиболее предпочтительно по меньшей мере на 99% идентичен аминокислотной последовательности выбранной грибной ДНКазы.
Твердая поверхность. Термин «твердая поверхность» в данном документе определяется как поверхность, которая не поглощает воду. В частности, термин «твердая поверхность» не охватывает текстильное изделие или ткань.
Поэтому изделия, имеющие твердую поверхность и подпадающие под предполагаемое значение термина, следовательно, включают бытовые поверхности, поверхности в больницах/учреждениях и наружные поверхности, такие как полы, стены, крыши и т. д., а также поверхности твердых объектов, таких как автомобили (мойка автомобилей), столы и прочая мебель, а также посуда. Посуда включает без ограничения гончарную посуду, такую как тарелки, чашки, стаканы, миски, столовые приборы, такие как ложки, ножи, вилки, сервировочные принадлежности и другие изделия, изготовленные из керамики, пластмасс, металлов, фарфора, стекла, и акрилов, и т. д.
Моющая композиция для твердых поверхностей. Термин "моющая композиция для твердых поверхностей" относится к композициям, содержащим моющие компоненты, композиция которых является подходящей и предназначенной для чистки областей твердых поверхностей. Настоящее изобретение не ограничивается каким-либо конкретным типом композиции для чистки твердых поверхностей или каким-либо конкретным моющим средством.
Клетка-хозяин. Термин «клетка-хозяин» означает любой тип клеток, который является восприимчивым к трансформации, трансфекции, трансдукции или подобным процедурам при помощи конструкции нуклеиновой кислоты или вектора экспрессии, содержащих полинуклеотид по настоящему изобретению. Термин "клетка-хозяин" охватывает любого потомка исходной клетки, который не является идентичным исходной клетке вследствие мутаций, происходящих в ходе репликации.
Выделенный. Термин "выделенный" означает вещество в форме или среде, которые не встречаются в естественных условиях. Неограничивающие примеры выделенных веществ включают: (1) любое не встречающееся в естественных условиях вещество; (2) любое вещество, в том числе без ограничения любой фермент, вариант, нуклеиновую кислоту, белок, пептид или кофактор, которые по меньшей мере частично отделены от одного, или нескольких, или всех встречающихся в естественных условиях составляющих, с которыми они связаны в естественных условиях; (3) любое вещество, модифицированное человеком, по сравнению с таким веществом, встречающимся в природе; или (4) любое вещество, модифицированное с помощью увеличения количества вещества по сравнению с другими компонентами, с которыми оно связано в естественных условиях (например, рекомбинантное получение в клетке-хозяине; несколько копий гена, кодирующего вещество; а также применение более сильного промотора, чем промотор, в естественных условиях связанный с геном, кодирующим вещество). Выделенное вещество может присутствовать в образце ферментативного бульона; например, клетка-хозяин может быть генетически модифицирована для экспрессии полипептида по настоящему изобретению. Ферментативный бульон из такой клетки-хозяина будет содержать выделенный полипептид.
Стирка. Термин "стирка" относится как к стирке в домашних условиях, так и к промышленной стирке и означает способ обработки текстильных изделий раствором, содержащим чистящую или моющую композицию по настоящему изобретению. Например, процесс стирки можно осуществлять с применением, например, домашней или промышленной стиральной машины или можно осуществлять вручную.
Под термином "неприятный запах" понимают запах, который не является желательным на чистых изделиях. Очищенное изделие должно иметь свежий и чистый аромат, без неприятных запахов, оставшихся на изделии. Одним примером неприятного запаха являются соединения с неприятным запахом, которые могут быть образованы микроорганизмами. Другим примером являются неприятные запахи, которые могут представлять собой запах пота или запах тела, оставшиеся на изделии, которое контактировало с телом человека или животного. Другим примером неприятного запаха может быть запах пряностей, который остается на изделиях, например, карри или другие экзотические пряности, которые сильно пахнут. Одним способом измерения способности изделия поглощать неприятный запах является применение анализа II, описанного в примерах 5 и 6.
Зрелый полипептид. Термин "зрелый полипептид" означает полипептид в его конечной форме, после трансляции и любых посттрансляционных модификаций, таких как процессинг N-концевой части, усечение C-концевой части, гликозилирование, фосфорилирование и т. д. В одном аспекте зрелый полипептид представляет собой аминокислоты с 1 по 206 последовательности под SEQ ID NO: 2, и аминокислоты от -37 до -16 последовательности под SEQ ID NO: 2 представляют собой сигнальный полипептид, а аминокислоты от -15 до -1 последовательности под SEQ ID NO: 2 представляют собой пропептид. В одном аспекте зрелый полипептид представляет собой аминокислоты 1-188 последовательности под SEQ ID NO: 5, и аминокислоты от -17 до -1 последовательности под SEQ ID NO: 2 представляют собой сигнальный пептид. В одном аспекте зрелый полипептид представляет собой аминокислоты с 1 по 110 последовательности под SEQ ID NO: 6, зрелый полипептид представляет собой аминокислоты 1-109 последовательности под SEQ ID NO: 7, или зрелый полипептид представляет собой аминокислоты с 1 по 206 последовательности под SEQ ID NO: 8. Из уровня техники известно, что клетка-хозяин может вырабатывать смесь из двух или более различных зрелых полипептидов (т. е. с другой C-концевой и/или N-концевой аминокислотой), экспрессируемых одним и тем же полинуклеотидом. Из уровня техники также известно, что в различных клетках-хозяевах процессинг полипептидов осуществляется различным образом, и таким образом одна клетка-хозяин, экспрессирующая полинуклеотид, может вырабатывать другой зрелый полипептид (например, с другой C-концевой и/или N-концевой аминокислотой) по сравнению с другой клеткой-хозяином, экспрессирующей один и тот же полинуклеотид. В одном аспекте зрелые полипептиды содержат не более 206 аминокислотных остатков последовательности под SEQ ID NO: 2, SEQ ID NO: 3 или SEQ ID NO: 8 (например, аминокислоты с 1 по 206 последовательности под SEQ ID NO: 2), или не более 204 аминокислотных остатка (например, аминокислоты 3-206 последовательности под SEQ ID NO: 2).
Последовательность, кодирующая зрелый полипептид. Термин "последовательность, кодирующая зрелый полипептид" означает полинуклеотид, который кодирует зрелый полипептид, обладающий ДНКазной активностью. В одном аспекте последовательность, кодирующая зрелый полипептид, представляет собой нуклеотиды 1-242, 309-494, 556-714 и 766-907 последовательности под SEQ ID NO: 1. В одном аспекте кодирующая последовательность зрелого полипептида представляет собой нуклеотиды 52-864 последовательности под SEQ ID NO: 4, где три интрона предполагаются в последовательности аминокислот в положениях 76-164, 289-362 и 520-615 последовательности под SEQ ID NO: 4. Сигнал секреции присутствует в аминокислотах в положениях 1-51 последовательности под SEQ ID NO: 4.
Конструкция нуклеиновой кислоты. Термин "конструкция нуклеиновой кислоты" означает либо одно-, либо двухцепочечную молекулу нуклеиновой кислоты, выделенную из встречающегося в естественных условиях гена или модифицированную с тем, чтобы она содержала сегменты нуклеиновых кислот в таком порядке, который в иных случаях не мог бы существовать в естественных условиях, или которая является синтетической, содержащей одну или несколько контрольных последовательностей.
Функционально связанный. Термин "функционально связанный" означает конфигурацию, при которой контрольная последовательность размещена в соответствующем положении относительно кодирующей последовательности полинуклеотида так, что контрольная последовательность управляет экспрессией кодирующей последовательности.
Идентичность последовательностей. Родство между двумя аминокислотными последовательностями или между двумя нуклеотидными последовательностями описывается параметром "идентичность последовательностей". В целях настоящего изобретения идентичность последовательностей между двумя аминокислотными последовательностями может быть определена с использованием алгоритма Нидлмана-Вунша (Needleman and Wunsch, 1970, J. Mol. Biol. 48: 443-453), который реализован в программе Needle из пакета программ EMBOSS (EMBOSS: The European Molecular Biology Open Software Suite, Rice et al., 2000, Trends Genet. 16: 276-277), предпочтительно версии 5.0.0 или более поздней. Применяемыми параметрами являются штраф за открытие гэпа, составляющий 10, штраф за продление гэпа, составляющий 0,5, и матрица замен EBLOSUM62 (версия BLOSUM62 для EMBOSS). Выводимые данные в Needle, помеченные как "наиболее длинная идентичность" (полученные с применением опции - nobrief), применяют в качестве процента идентичности и рассчитывают следующим образом:
(идентичные остатки x 100)/(длина выравниваемого участка - общее число гэпов в выравниваемом участке).
В целях настоящего изобретения идентичность последовательностей для двух дезоксирибонуклеотидных последовательностей может быть определена с использованием алгоритма Нидлмана-Вунша (Needleman and Wunsch, 1970, выше), который реализован в программе Needle из пакета программ EMBOSS (EM-BOSS: The European Molecular Biology Open Software Suite, Rice et al., 2000, выше), предпочтительно версии 5.0.0 или более поздней. Применяемыми параметрами являются штраф за открытие гэпа, составляющий 10, штраф за продление гэпа, составляющий 0,5, и матрица замен EDNAFULL (версия NCBI NUC4.4 для EMBOSS). Выводимые данные в Needle, помеченные как "наиболее длинная идентичность" (полученные с применением опции - nobrief), применяют в качестве процента идентичности и рассчитывают следующим образом:
(идентичные дезоксирибонуклеотиды x 100)/(длина выравниваемого участка - общее число гэпов в выравниваемом участке).
Условия жесткости. Термин "условия очень низкой жесткости" означает для зондов длиной по меньшей мере 100 нуклеотидов предварительную гибридизацию и гибридизацию при 42°C в 5X SSPE, 0,3% SDS, 200 микрограммах/мл разрезанной и денатурированной ДНК из молок лососевых и 25% формамиде после стандартных процедур Саузерн-блоттинга в течение 12-24 часов. В конце материал-носитель промывают три раза, каждый раз в течение 15 минут, с применением 2X SSC, 0,2% SDS при 45°C.
Термин "условия низкой жесткости" означает для зондов длиной по меньшей мере 100 нуклеотидов предварительную гибридизацию и гибридизацию при 42°C в 5X SSPE, 0,3% SDS, 200 микрограммах/мл разрезанной и денатурированной ДНК из молок лососевых и 25% формамиде после стандартных процедур Саузерн-блоттинга в течение 12-24 часов. В конце материал-носитель промывают три раза, каждый раз в течение 15 минут, с применением 2X SSC, 0,2% SDS при 50°C.
Термин "условия умеренной жесткости" означает для зондов длиной по меньшей мере 100 нуклеотидов предварительную гибридизацию и гибридизацию при 42°C в 5X SSPE, 0,3% SDS, 200 микрограммах/мл разрезанной и денатурированной ДНК из молок лососевых и 35% формамиде после стандартных процедур Саузерн-блоттинга в течение 12-24 часов. В конце материал-носитель промывают три раза, каждый раз в течение 15 минут, с применением 2X SSC, 0,2% SDS при 55°C.
Термин "условия умеренно высокой жесткости" означает для зондов длиной по меньшей мере 100 нуклеотидов предварительную гибридизацию и гибридизацию при 42°C в 5X SSPE, 0,3% SDS, 200 микрограммах/мл разрезанной и денатурированной ДНК из молок лососевых и 35% формамиде после стандартных процедур Саузерн-блоттинга в течение 12-24 часов. В конце материал-носитель промывают три раза, каждый раз в течение 15 минут, с применением 2X SSC, 0,2% SDS при 60°C.
Термин "условия высокой жесткости" означает для зондов длиной по меньшей мере 100 нуклеотидов предварительную гибридизацию и гибридизацию при 42°C в 5X SSPE, 0,3% SDS, 200 микрограммах/мл разрезанной и денатурированной ДНК из молок лососевых и 50% формамиде после стандартных процедур Саузерн-блоттинга в течение 12-24 часов. В конце материал-носитель промывают три раза, каждый раз в течение 15 минут, с применением 2X SSC, 0,2% SDS при 65°C.
Термин "условия очень высокой жесткости" означает для зондов длиной по меньшей мере 100 нуклеотидов предварительную гибридизацию и гибридизацию при 42°C в 5X SSPE, 0,3% SDS, 200 микрограммах/мл разрезанной и денатурированной ДНК из молок лососевых и 50% формамиде после стандартных процедур Саузерн-блоттинга в течение 12-24 часов. В конце материал-носитель промывают три раза, каждый раз в течение 15 минут, с применением 2X SSC, 0,2% SDS при 70°C.
Подпоследовательность. Термин "подпоследовательность" означает полинуклеотид, у которого отсутствуют один или несколько (например, некоторое количество) нуклеотидов с 5'- и/или 3'-конца последовательности, кодирующей зрелый полипептид; причем подпоследовательность кодирует фрагмент, обладающий ДНКазной активностью. В одном аспекте подпоследовательность содержит по меньшей мере 796 нуклеотидов (например, нуклеотиды 112-907 последовательности под SEQ ID NO: 1), по меньшей мере 793 нуклеотида (например, нуклеотиды 115-907 последовательности под SEQ ID NO: 1), по меньшей мере 790 нуклеотидов (например, нуклеотиды 118-907 последовательности под SEQ ID NO: 1). В одном аспекте подпоследовательность содержит по меньшей мере 587 нуклеотидов (например, нуклеотиды 278-864 последовательности под SEQ ID NO: 4), по меньшей мере 650 нуклеотидов (например, нуклеотиды 215-864 последовательности под SEQ ID NO: 4), по меньшей мере 816 нуклеотидов (например, нуклеотиды 52-864 последовательности под SEQ ID NO: 4).
Текстильное изделие. Термин ʺтекстильное изделиеʺ означает любой текстильный материал, в том числе пряжу, промежуточные продукты из пряжи, волокна, нетканые материалы, природные материалы, синтетические материалы и любой другой текстильный материал, ткани, изготовленные из этих материалов, и продукты, изготовленные из тканей (например, виды одежды и другие изделия). Текстильное изделие или ткань может быть в форме трикотажа, тканых изделий, изделий из грубой хлопчатобумажной ткани, нетканых изделий, войлочных изделий, пряжи и ткани для полотенец. Текстильное изделие может быть на основе целлюлозы, например, природные целлюлозные полимеры, в том числе хлопок, волокна льна/льняное полотно, джутовая ткань, волокна рами, сизаль или кокосовые волокна, или созданные человеком целлюлозные полимеры (например, полученные из древесной пульпы), в том числе вискоза/искусственный шелк, волокна из ацетата целлюлозы (триацетатные), лиоцелл или их смеси. Текстильное изделие или ткань могут быть также отличными от целлюлозных, например, природные полиамиды, в том числе шерсть, верблюжья шерсть, кашемир, мохер, кроличья шерсть и шелк, или синтетические полимеры, такие как нейлон, арамид, синтетический сложный полиэфир, полимер на основе акрилонитрила, полипропилен и спандекс/эластан, или их смеси, а также смеси волокон на основе целлюлозы и волокон, отличных от целлюлозных. Примерами смесей являются смеси хлопка и/или искусственного шелка/вискозы с одним или несколькими дополнительными материалами, такими как шерсть, синтетическое волокно (например, полиамидное волокно, акриловое волокно, полиэфирное волокно, поливинилхлоридное волокно, полиуретановое волокно, полимочевинное волокно, арамидное волокно) и/или целлюлозосодержащее волокно (например, искусственный шелк/вискоза, волокна рами, волокна льна/льняное полотно, джутовая ткань, волокно из ацетата целлюлозы, лиоцелл). Ткань может представлять собой белье, пригодное для обычной стирки, например, загрязненное белье для домашнего обихода. При использовании термина ткань или предмет одежды предусматривается, что он предназначен также для охватывания более общего термина текстильные изделия.
Вариант. Термин "вариант" означает полипептид, обладающий такой же активностью, как и исходный фермент, содержащий изменение, т. е. замену, вставку и/или делецию в одном или нескольких (например, некоторых) положениях. Замена означает замещение аминокислоты, занимающей определенное положение, другой аминокислотой; делеция означает устранение аминокислоты, занимающей определенное положение; а вставка означает добавление аминокислоты рядом с и непосредственно после аминокислоты, занимающей определенное положение. В контексте настоящего изобретения вариант идентифицированной ДНКазы обладает ферментативной активностью исходной, т. е. способностью катализировать гидролитическое расщепление связей сложного фосфодиэфира в каркасе ДНК (дезоксирибонуклеазная активность). В одном варианте осуществления дезоксирибонуклеазная активность варианта является повышенной относительно исходной ДНКазы, например, зрелый полипептид под SEQ ID NO: 2.
Цикл стирки. Термин "цикл стирки" в данном документе определяют как моющую операцию, где текстильные изделия погружают в моющую жидкость, к текстильному изделию применяют механическое воздействие некоторого вида с целью избавления от пятен и облегчения перетекания моющей жидкости внутрь и наружу из текстильного изделия, а также конечного устранения избыточной моющей жидкости. После одного или нескольких циклов стирки текстильное изделие, как правило, прополаскивают и высушивают.
Моющая жидкость. Термин «моющая жидкость» относится к раствору или смеси воды и моющих средств, в том числе необязательно ферментам, используемым для стирки текстильных изделий, для чистки твердых поверхностей или для мытья посуды.
Подробное описание настоящего изобретения
Как описано выше, на протяжении многих лет известна проблема, заключающаяся в том, что с течением времени подлежащие стирке изделия, такие как рубашки и блузки, утрачивают белизну или становятся все более и более серыми. Считается, что часть данной проблемы обусловлена повторным осаждением грязи во время стирки, так что если очень грязные подлежащие стирке изделия стирают вместе с менее грязными подлежащими стирке изделиями, то присутствующее в моющей жидкости загрязнение проявляет тенденцию прилипать к подлежащим стирке изделиям. В результате подлежащее стирке изделие является более "загрязненным" и более серым после стирки, чем оно было перед стиркой. Авторы настоящего изобретения неожиданно обнаружили, что применение полипептидов, обладающих ДНКазной активностью, может быть использовано для предотвращения или уменьшения такого повторного осаждения грязи в ходе процесса последующей чистки или стирки. Изделие может быть с текстильной или твердой поверхностью, например, посуда.
Авторы настоящего изобретения обнаружили, что при приведении изделия, такого как подлежащее стирке изделие, в контакт с полипептидом, обладающим ДНКазой активностью, подлежащее стирке изделие является более чистым и менее серым после последующей стирки без присутствия ДНКазы, чем аналогичное подлежащее стирке изделие, которое не контактировало с полипептидом, обладающим ДНКазной активностью, см., например, примеры 1 и 2. Авторы настоящего изобретения обнаружили, что полипептид, обладающий ДНКазой активностью, может быть использован для поддержания или улучшения белизны изделия, см. например, примеры 1 и 2.
Кроме того, настоящее изобретение относится к применению полипептида, обладающего ДНКазной активностью, для предотвращения или уменьшения прилипания грязи и/или запаха к изделию в ходе процесса последующей чистки или стирки, где ДНКазу не применяют, см. примеры 1-7.
Авторы настоящего изобретения обнаружили, что применение полипептида, обладающего ДНКазной активностью, может предотвращать или уменьшать неприятный запах, исходящий от изделия, такого как текстильное изделие (см. примеры 3-7), твердых поверхностей, например, посуды. В одном варианте осуществления настоящего изобретения неприятный запах вызван E-2-ноненалем.
В обычных способах стирки неприятный запах может сохраняться даже в процессе стирки и процессе сушки. Это приводит к эффекту, что неприятный запах может ощущаться при использовании текстильного изделия. Для пользователя текстильного изделия это не очень приятно, т. е. при носке одежды для активного отдыха, которая пахнет еще до начала спортивной активности. Для пользователя текстильного изделия это может быть смущающим, и он выберет купить новую одежду для активного отдыха вместо плохо пахнущей одежды. С помощью настоящего изобретения этого избегают, и, таким образом, окружающая среда сохраняется в отношении ограниченных ресурсов, таких как сырьевой материал для новых текстильных изделий, вода, энергия и загрязнение окружающей среды. В одном варианте осуществления настоящего изобретения количество Е-2-ноненаля присутствует на сухом изделии после того, как после стирки он устранен, содержание его снижено или он удален.
Одно из преимуществ по настоящему изобретению состоит в том, что данный неприятный запах не появляется от влажных изделий, подлежащих стирке, т. е. при открытии стиральной машины. Это делает процесс стирки более привлекательным как в бытовых, так и в промышленных применениях.
Еще одно преимущество по настоящему изобретению заключается в том, что при выемке мокрого белья непосредственно из стиральной машины или моющей жидкости подлежащие стирке изделия не имеют неприятного запаха и воспринимаются как чистые. При этом сохраняются время, деньги и энергия на ненужные вторую или даже третью стирки. Это огромное преимущество для окружающей среды.
В одном варианте осуществления настоящего изобретения изделие контактирует с полипептидом, обладающим ДНКазной активностью. Полипептид, обладающий ДНКазной активностью, может, например, быть распыленным на изделие. Осаждение грязи и/или запаха может быть, таким образом, уменьшено или устранено с помощью распыления полипептида, например, на ковры, полы или простыни.
Другой способ предотвращения или уменьшения повторного осаждения заключается в приведении изделия в контакт с жидким раствором, который содержит полипептид, обладающий ДНКазной активностью. Изделие можно приводить в контакт с жидким раствором, например, с помощью погружения изделия в жидкий раствор. Жидкий раствор может быть моющей жидкостью, и изделие может быть в то же время выстирано. Данный вариант осуществления изобретения является предпочтительным для текстильных изделий, таких как текстильные изделия для стирки, которые могут быть в то же время выстираны. В одном варианте осуществления настоящего изобретения текстильное изделие является недавно изготовленным и предварительно обработанным промыванием, погружением или пропитыванием текстильного изделия полипептидом, обладающим ДНКазной активностью, после изготовления текстильного изделия. С помощью пропитывания изделия, например, текстильный элемент, может быть более устойчивым к осаждению грязи и/или запаха на данном изделии.
Моющая жидкость может использоваться также для мытья полов или других твердых поверхностей, которые нуждаются в обработке против повторного осаждения.
Жидкий раствор может быть также пропитывающей жидкостью, которая предотвращает накапливание загрязнения на изделии в ходе процесса последующей чистки или стирки. Жидкий раствор для пропитки может служить в качестве моющего средства и в то же время раствора против повторного осаждения.
В одном варианте осуществления настоящего изобретения полипептид, обладающий ДНКазной активностью, применяется для чистки или стирки изделия по меньшей мере один раз перед процессом последующей чистки или стирки, где последующий процесс стирки мог бы не включать в себя применение ДНКазы. В одном варианте осуществления полипептид, обладающий ДНКазной активностью, в процессе последующей чистки или стирки не используется.
В одном варианте осуществления полипептид, обладающий ДНКазной активностью, используется для чистки или стирки изделия по меньшей мере два раза, три раза, четыре раза, пять раз, шесть раз, семь раз, восемь раз, девять раз или десять раз перед процессом последующей чистки или стирки. В одном варианте осуществления полипептид, обладающий ДНКазной активностью, используется для чистки или стирки изделия по меньшей мере два раза, три раза, четыре раза, пять раз, шесть раз, семь раз, восемь раз, девять раз или десять раз перед процессом последующей чистки или стирки, где полипептид, обладающий ДНКазной активностью, не используется.
Кроме того, изобретение относится к моющей композиции, содержащей полипептид, обладающий дезоксирибонуклеазной активностью (ДНКаза), и поверхностно-активное вещество, где композиция соответствует по меньшей мере одному из а) или b):
а) композиция дополнительно содержит средство для контроля запаха и/или
b) поверхностно-активное вещество не является катионным поверхностно-активным веществом.
Средство для контроля запаха выбрано из группы, состоящей из циклодекстринов и их смесей, блокаторов запаха, реакционноспособных альдегидов, флаваноидов, солей металлов, цеолитов, активированного угля, гидрофобно модифицированных полимеров для контроля неприятного запаха (НМР), производных изотиазолинона, таких как бензизотиазолинон, и/или летучих альдегидов.
В одном варианте осуществления настоящего изобретения композиция содержит бензизотиазолинон и используется для предотвращения образования, уменьшения или удаления биопленки, для уменьшения неприятного запаха, для улучшения белизны и/или для уменьшения повторного осаждения. Бензизотиазолинон представляет собой широко используемый биоцид и принадлежит к группе изотиазолинонов.
В одном варианте осуществления настоящего изобретения поверхностно-активное вещество представляет собой неионное поверхностно-активное вещество, анионное поверхностно-активное вещество, цвиттерионное поверхностно-активное вещество или полуполярное поверхностно-активное вещество.
Поверхностно-активное вещество может быть анионным поверхностно-активным веществом, выбранным из группы, состоящей из: сульфатов и сульфонатов, таких как линейные алкилбензолсульфонаты (LAS), изомеры LAS, разветвленные алкилбензолсульфонаты (BABS), фенилалкансульфонаты, альфа-олефинсульфонаты (AOS), олефинсульфонаты, алкенсульфонаты, алкан-2,3-диилбис(сульфаты), гидроксиалкансульфонаты и дисульфонаты, алкилсульфатов (AS), таких как додецилсульфат натрия (SDS), сульфаты жирных спиртов (FAS), сульфаты первичных спиртов (PAS), эфирсульфаты спиртов (AES или AEOS, или FES, также известные как этоксисульфаты спиртов или эфирсульфаты жирных спиртов), вторичные алкансульфонаты (SAS), сульфонаты парафина (PS), сульфонаты сложных эфиров, сложные эфиры глицерина и сульфонированных жирных кислот, метиловые сложные эфиры жирных альфа-сульфокислот (альфа-SFMe или SES), в том числе сульфонат сложного метилового эфира (MES), алкил- или алкенилянтарная кислота, додеценил/тетрадеценил янтарная кислота (DTSA), жирнокислотные производные аминокислот, сложные диэфиры и моноэфиры сульфоянтарной кислоты или соли жирной кислоты (мыло), и их комбинаций.
Количество анионного поверхностно-активного вещества составляет от приблизительно 1% до приблизительно 40% по весу, например, от приблизительно 5% до приблизительно 30%, включая от приблизительно 5% до приблизительно 15%, или от приблизительно 15% до приблизительно 20%, или от приблизительно 20% до приблизительно 25%.
Поверхностно-активное вещество может быть неионным поверхностно-активным веществом, выбранным из группы, состоящей из этоксилатов спирта (AE или AEO), пропоксилатов спирта, пропоксилированных жирных спиртов (PFA), алкоксилированных алкиловых сложных эфиров жирных кислот, таких как этоксилированные и/или пропоксилированные алкиловые сложные эфиры жирных кислот, алкилфенолэтоксилаты (APE), нонилфенолэтоксилаты (NPE), алкилполигликозиды (APG), алкоксилированные амины, моноэтаноламиды жирных кислот (FAM), диэтаноламиды жирных кислот (FADA), этоксилированные моноэтаноламиды жирных кислот (EFAM), пропоксилированные моноэтаноламиды жирных кислот (PFAM), амиды жирных полигидроксиалкилкислот или N-ацил-N-алкил-производные глюкозамина (глюкамиды, GA, или глюкамиды жирных кислот, FAGA), SPAN™, TWEEN™, и их комбинаций.
Количество неионного поверхностно-активного вещества составляет от приблизительно 0,2% до приблизительно 40% по весу неионного поверхностно-активного вещества, например, от приблизительно 0,5% до приблизительно 30%, в частности, от приблизительно 1% до приблизительно 20%, от приблизительно 3% до приблизительно 10%, например, от приблизительно 3% до приблизительно 5%, от приблизительно 8% до приблизительно 12% или от приблизительно 10% до приблизительно 12%.
Поверхностно-активное вещество может быть полуполярным поверхностно-активным веществом, выбранным из группы, состоящей из аминоксидов (AO), таких как алкилдиметиламиноксид, N-(кокоалкил)-N,N-диметиламиноксид и N-(таллоу-алкил)-N,N-бис(2-гидроксиэтил)аминоксид и их комбинаций.
Поверхностно-активное вещество может быть цвиттерионным поверхностно-активным веществом, выбранным из группы, состоящей из бетаинов, таких как алкилдиметилбетаины, сульфобетаины.
В одном варианте осуществления поверхностно-активное вещество выбрано из группы, состоящей из этоксисульфата натрия на основе спирта, линейного алкилбензолсульфоната, натриевой соли жирной кислоты, алкилсульфата натрия, лаураминоксида, линейного алкилбензолсульфоната (MEA соль), линейного алкилбензолсульфоната (натриевая соль), этоксилата спирта.
Моющая композиция по настоящему изобретению может быть использована для предотвращения или уменьшения повторного осаждения грязи на изделии во ходе процесса последующей чистки или стирки и для предотвращения или уменьшения неприятного запаха.
Композиция может дополнительно включать моющие компоненты, флокулирующее вспомогательное средство, хелатирующие средства, ингибиторы переноса красителей, ферменты, стабилизаторы ферментов, ингибиторы ферментов, каталитические материалы, активаторы отбелки, пероксид водорода, источники пероксида водорода, предварительно образованные перкислоты, полимерные диспергирующие средства, средства для устранения/средства против повторного осаждения глинистой грязи, отбеливатели, подавители образования мыльной пены, красители, отдушки, средства, обеспечивающие эластичность, мягчители тканей, носители, гидротропы, моющие компоненты и дополнительные моющие компоненты, окрашивающие средства для тканей, противовспенивающие средства, диспергирующие средства, технологические добавки и/или пигменты.
Композиция может содержать один или несколько ферментов, выбранных из группы, состоящей из протеаз, липаз, кутиназ, амилаз, карбогидраз, целлюлаз, пектиназ, маннаназ, арабиназ, галактаназ, ксиланаз и оксидаз.
Композиция может быть моющей композицией, подходящей для стирки, мытья посуды или чистки твердых поверхностей.
Настоящее изобретение дополнительно относится к жидкой моющей композиции, содержащей поверхностно-активное вещество и моющее средство, а также моющий компонент с общей концентрацией по меньшей мере 3% по весу, и микрокапсулу, содержащую моющий фермент, где мембрана микрокапсулы получена с помощью сшивания полиразветвленного полиамина с молекулярным весом более 1 кДа. Авторами настоящего изобретения было обнаружено, что при инкапсулировании ферментов в микрокапсуле с полупроницаемой мембраной, и при наличии более высокой активности воды внутри данных капсул (перед добавлением в жидкое моющее средство), чем в жидком моющем средстве, капсулы будут подвергаться (частично) разрушению при добавлении в моющее средство (вода вытекает наружу), при этом более концентрированный и более вязкий фермент остается внутри капсул. Разрушение мембраны также может приводить к уменьшенной проницаемости. Это также может быть дополнительно использовано с помощью добавления стабилизаторов/полимеров, в частности таких, которые не проникают через мембрану. Разрушение и полученное в результате повышение вязкости будет уменьшать/препятствовать диффузии нежелательных компонентов (например, поверхностно-активных веществ или секвестрантов) в капсулы и, таким образом, повышать стабильность при хранении фермента в жидком моющем средстве. Компоненты в жидком моющем средстве, которые чувствительны к действию фермента (например, компоненты, которые выступают в качестве субстрата для фермента), также защищены от распада, вызванного ферментом. Во время стирки жидкое моющее средство разводят водой, повышая таким образом активность воды. После этого вода диффундирует внутрь капсул (осмос). Капсулы будут набухать и мембрана будет либо становится проницаемой для фермента, так что он будет выходить из капсул, либо просто прорываться и таким способом высвобождать фермент. Концепция является очень эффективной для стабилизации ферментов против нежелательных компонентов в жидком моющем средстве и, наоборот, также защищает чувствительные к действию фермента компоненты в жидком моющем средстве от воздействия ферментов.
Примеры моющих компонентов, которые чувствительны к действию ферментов и могут распадаться под их действием, включают (используемый фермент в скобках): ксантановую камедь (ксантаназа), полимеры со сложноэфирными связями (липаза), гидрогенизированное касторовое масло (липаза), отдушку (липаза), поверхностно-активные вещества на основе сульфонатов сложных метиловых эфиров (липаза), целлюлозу и производные целлюлозы (например, CMC) (целлюлаза), а также декстрин и циклодекстрин (амилаза).
Кроме того, чувствительные моющие ингредиенты могут быть инкапсулированы и, таким образом, стабилизированы, в микрокапсулах. Чувствительные моющие ингредиенты при хранении склонны к распаду. Такие моющие ингредиенты включают соединения для отбелки, активаторы отбелки, отдушки, полимеры, моющие компоненты, поверхностно-активные вещества и т. д.
Как правило, микрокапсулы можно использовать для разделения несовместимых компонентов/соединений в моющих средствах.
Добавление микрокапсул в моющие средства можно применять для воздействия на внешний вид моющего продукта, такой как эффект непрозрачности (небольшие микрокапсулы) или эффект отчетливо видимых частиц (крупные микрокапсулы). Микрокапсулы также могут быть окрашены.
Микрокапсулы можно применять для уменьшения уровней ферментной пыли в течение обработки и переработки ферментных продуктов.
Если не указано иное, все процентные содержания приведены в виде процента по весу (% вес./вес.) по всей данной заявке.
Микрокапсула. Микрокапсулы обычно получают с помощью образования капель воды в сплошной среде, которая является несмешиваемой с водой - т. е., обычно, с помощью приготовления эмульсии вода-в-масле и последующего образования мембраны с помощью межфазной полимеризации посредством добавления сшивающего средства. После возможного отверждения капсулы можно собирать и далее прополаскивать и составлять с помощью способов, известных из уровня техники. Затем состав капсул добавляют в моющее средство.
Нагрузка, основные составляющие мембраны и возможный дополнительный компонент, которые подлежат инкапсулированию, обнаружены в водной фазе. В сплошной среде обнаружены компоненты, которые стабилизируют капли воды с целью коалесценции (эмульгаторы, стабилизаторы эмульсий, поверхностно-активные вещества и т. д.), и через сплошную среду добавляют также сшивающее средство.
Эмульсию можно получать с помощью любых способов, известных из уровня техники, например, с помощью механического перемешивания, способов стекания каплями, эмульгирования мембраны, микроструйной методики, обработки ультразвуком и т. д. В некоторых случаях простое смешивание фаз будет в результате автоматически обеспечивать эмульсию, что часто называется самоэмульгированием. Применение способов, обеспечивающих получение в результате узкого распределения размеров частиц, является преимуществом.
Затем сшивающее средство(средства) обычно добавляют в эмульсию либо непосредственно, либо (более часто) с помощью получения раствора сшивающего средства в растворителе, который растворим в непрерывной фазе. Эмульсию и сшивающее средство или его раствор можно смешивать с помощью обычных способов, применяемых в данной области техники, например, с помощью простого смешивания или с помощью тщательного контроля потоков эмульсии и раствора сшивающего средства через встроенный смеситель.
В некоторых случаях отверждение капсул необходимо для завершения образования мембраны. Отверждение зачастую представляет собой простое перемешивание капсул в течение некоторого времени для обеспечения завершения реакции межфазной полимеризации. В других случаях образование мембраны можно остановить с помощью добавления гасителя реакции.
Впоследствии капсулы могут быть модифицированы, например, с помощью осуществления реакции компонентов на мембране для препятствования или устранения слипания частиц в моющем средстве, как описано в WO 99/01534.
Полученные капсулы могут быть выделены или концентрированы с помощью способов, известных в данной области техники, например, с помощью фильтрации, центрифугирования, дистилляции или отстаивания дисперсии капсул.
Полученные в результате капсулы могут быть дополнительно составлены, например, с помощью добавления поверхностно-активных веществ с получением продукта с необходимыми свойствами для хранения, транспортировки и последующей обработки и добавления в моющее средство. Другие средства для состава микрокапсул включают средства, модифицирующие реологические свойства, биоциды (например, Proxel), кислоту/основание для регулирования pH (которые также будут регулировать внутреннюю часть микрокапсул) и воду для регулирования активности воды.
Способ образования капсул может включать следующие стадии:
- получение исходной воды и масляной фазы(фаз),
- образование эмульсии вода-в-масле,
- образование мембраны с помощью межфазной полимеризации,
- необязательная модификация после реакции,
- необязательное выделение и/или составление,
- добавление в моющее средство.
Способ может быть либо периодическим способом, либо непрерывным или полунепрерывным способом.
Микрокапсула по настоящему изобретению представляет собой небольшую водную сферу с однородной мембраной вокруг нее. Материал внутри микрокапсулы называют ядром, внутренней фазой или наполнением, тогда как мембрану иногда называют оболочкой, покрытием или стенкой. Микрокапсулы имеют диаметры от 0,5 мкм до 2 миллиметров. Предпочтительно средний диаметр микрокапсул находится в диапазоне от 1 мкм до 1000 мкм, более предпочтительно в диапазоне от 5 мкм до 500 мкм, еще более предпочтительно в диапазоне от 10 мкм до 500 мкм, еще более предпочтительно в диапазоне от 50 мкм до 500 мкм и наиболее предпочтительно в диапазоне от 50 мкм до 200 мкм. Альтернативно, диаметр микрокапсул находится в диапазоне от 0,5 мкм до 30 мкм; или в диапазоне от 1 мкм до 25 мкм. Диаметр микрокапсулы измеряют в масляной фазе после завершения полимеризации. Диаметр капсулы может изменяться в зависимости от активности воды окружающей химической среды.
Микроинкапсулирование ферментов, применяемое в настоящем изобретении, можно осуществлять с помощью межфазной полимеризации, где два реагента в реакции полимеризации контактируют на межфазной границе и быстро реагируют. Основой данного способа является реакция полиамина с производным кислоты, обычно с галогенангидридом, которое выступает в качестве сшивающего средства. Полиамин предпочтительно, по сути, растворим в воде (если находится в форме свободного основания). В соответствующих условиях на поверхности быстро образуются тонкие гибкие мембраны. Одним способом осуществления полимеризации является применение водного раствора фермента и полиамина, которые эмульгируются неводным растворителем (и эмульгатором), и добавление раствора, содержащего производное кислоты. Щелочное средство может присутствовать в растворе фермента для нейтрализации кислоты, образованной в ходе реакции. Полимерные (полиамидные) мембраны мгновенно образуются на поверхности капель эмульсии. Полимерная мембрана микрокапсулы обычно имеет катионную природу и, таким образом, связывается/образует комплекс с соединениями анионной природы.
Диаметр микрокапсул определяют по размеру капель эмульсии, который контролируют, например, с помощью скорости перемешивания.
Эмульсия. Эмульсия представляет собой временную или постоянную дисперсию одной жидкой фазы во второй жидкой фазе. Вторую жидкость обычно называют непрерывной фазой. Поверхностно-активные вещества обычно применяют для облегчения образования и стабилизации эмульсий. Не все поверхностно-активные вещества в равной степени способны стабилизировать эмульсию. Тип и количество поверхностно-активного вещества необходимо выбирать из оптимального применения эмульсии, в частности относительно получения и физической стабильности эмульсии и стабильности при разбавлении и дальнейшей переработке. Физическая стабильность относится к поддержанию эмульсией формы дисперсии. Процессы, такие как коалесценция, агрегация, поглощение стенками контейнера, осаждение и отстаивание, представляют собой формы физической нестабильности, и их следует избегать. Примеры подходящих поверхностно-активных веществ описаны в WO 97/24177, стр. 19-21; и в WO 99/01534.
Эмульсии могут быть дополнительно классифицированы либо как простые эмульсии, где диспергированная жидкая фаза представляет собой гомогенную жидкость, либо как более сложная эмульсия, где диспергированная жидкая фаза представляет собой гетерогенную комбинацию жидких или твердых фаз, например, двойная эмульсия или множественная эмульсия. Например, могут быть образованы двойная эмульсия вода-в-масле или многофазная эмульсия, где водная фаза сама по себе дополнительно содержит эмульгированную масляную фазу; данный тип эмульсии может быть определен как эмульсия масло-в-воде-в масле (o/w/o). Альтернативно, может быть образована эмульсия вода-в-масле, где водная фаза содержит диспергированную твердую фазу, которую часто называют суспензия-эмульсия. Могут быть описаны другие, более сложные эмульсии. Вследствие характерной сложности описания таких систем, термин эмульсия применяют для описания как простых, так и более сложных эмульсий без необходимого ограничения формы эмульсии или типа и числа присутствующих фаз.
Полиамин. Жесткость/гибкость и проницаемость мембраны в основном зависит от выбора полиамина. Полиамин по настоящему изобретению представляет собой полиразветвленный полиамин.
Каждая ветвь предпочтительно заканчивающаяся группой первичного амина, выступает в качестве точки связывания в сетке мембраны, обеспечивая таким образом благоприятные свойства. Полиразветвленный полиамин в соответствии с настоящим изобретением представляет собой полиамин, имеющий более двух точек разветвления и более двух реакционноспособных аминогрупп (способных вступать в реакцию со связывающим средством, т. е. группами первичного и вторичного аминов). Полиразветвленный полиамин применяют в качестве исходного материала, если получают эмульсию - ее не образовывают in situ из других исходных материалов. Для получения приемлемых свойств полиразветвленная структура полиамина должна присутствовать в качестве исходного материала.
Существует тесная связь между числом точек разветвления и числом первичных аминов, поскольку первичные амины всегда будут располагаться на конце ветви: линейный амин может содержать только два первичных амина. Для каждой точки разветвления, гипотетически введенной в такой линейный диамин, будет обеспечиваться один или несколько первичных аминов для введения в конец введенной ветви(ветвей). В данном контексте группу первичных аминов понимают как часть ветви, т. е. конечную точку ветви. Например, авторы настоящего изобретения трис(2-аминоэтил)амин и 1,2,3-пропантриамин рассматривают как молекулы с одной точкой разветвления. Для настоящего изобретения полиамин имеет по меньшей мере четыре первичных амина. Точки разветвления могут быть введены из цепи алифатического углеводорода, как в ранее приведенных примерах, или из ненасыщенных углеродных связей, как, например, в 3,3'-диаминобензидине, или из групп третичных аминов, как в N,N,N',N'-тетракис-(2-аминоэтил)этилендиамине.
Помимо числа точек разветвления было обнаружено, что компактность реакционноспособных аминогрупп имеет большое значение. Вещество, такое как, например, N,N,N',N'-тетракис-(12-аминододецил)этилендиамин, не является подходящим. Также для образования мембраны не является подходящим пептид или белок, такой как фермент. Таким образом, полиразветвленный полиамин не является пептидом или белком.
В одном варианте осуществления реакционноспособные аминогруппы составляют по меньшей мере 15% молекулярного веса полиразветвленного полиамина, например, более 20% или более 25%. Предпочтительно молекулярный вес полиразветвленного полиамина составляет по меньшей мере 1 кДа; более предпочтительно молекулярный вес полиразветвленного полиамина составляет по меньшей мере 1,3 кДа.
В предпочтительном варианте осуществления полиразветвленный полиамин представляет собой полиэтиленимин (PEI) и его модификации, имеющие более двух точек разветвления и более двух реакционноспособных аминогрупп; где реакционноспособные аминогруппы составляют по меньшей мере 15% молекулярного веса PEI, например, более 20% или более 25%. Предпочтительно молекулярный вес PEI составляет по меньшей мере 1 кДа.
Комбинации различных полиразветвленных полиаминов можно применять для получения микрокапсулы по настоящему изобретению.
Полезные свойства (например, стабильность фермента при хранении, уменьшение вытекания фермента, уменьшение притока моющих ингредиентов) микрокапсулы могут быть улучшены с помощью добавления одного или нескольких небольших аминов с молекулярным весом менее 1 кДа. Низкомолекулярный амин предпочтительно, по сути, растворим в воде (если находится в форме свободного основания) и может представлять собой материал, такой как этилендиамин, гексаметилендиамин, гександиамин, диэтилентетрамин, этилентетрамин, диаминобензол, пиперазин, тетраметиленпентамин или предпочтительно диэтилентриамин (DETA). Низкомолекулярные амины можно добавлять в количестве не более 50%, предпочтительно не более 40%, не более 30%, не более 20%, не более 10% или не более 5% по весу от общего содержания низкомолекулярного амина и полиразветвленного полиамина при получении микрокапсулы.
Сшивающее средство. Сшивающее средство, применяемое в настоящем изобретении, представляет собой молекулу, имеющую по меньшей мере две группы/сайта, способные вступать в реакцию с аминами с образованием ковалентных связей.
Сшивающее средство предпочтительно является растворимым в масле и может находиться в форме ангидрида кислоты или галогенангидрида, предпочтительно хлорангидрида. Например, это может быть адипоилхлорид, себакоилхлорид, хлорангидрид додекандиоевой кислоты, хлорангидрид фталевой кислоты, терефталоилхлорид, изофталоилхлорид или тримезоилхлорид; однако, предпочтительно сшивающий агент представляет собой терефталоилхлорид или тримезоилхлорид. Настоящее ее изобретение также относится к способу предотвращения или уменьшения повторного осаждения грязи на изделии в ходе процесса последующей чистки или стирки, включающему стадии:
а) приведение изделия в контакт с композицией по любому из пунктов 26-52 формулы изобретения или с жидким раствором, содержащими полипептид, обладающий ДНКазной активностью; и
b) необязательно полоскание изделия,
где изделие представляет собой текстильное изделие, посуду или твердую поверхность.
Композиция или полипептид, обладающий ДНКазной активностью, могут быть приведены в контакт с изделием, например, с помощью распыления, нанесения покрытия, пропитывания, стирки или погружения изделия с композицией или жидким раствором. Изделие можно приводить в контакт с изделием в течение короткого периода времени, например, 1-60 секунд, или в течение более длительного периода времени, например, 1-60 минут, или еще более длительного, например, 1-12 часов.
В одном варианте осуществления настоящего изобретения композиция или полипептид согласно стадии а) используется для чистки или стирки изделия по меньшей мере один раз перед процессом последующей чистки или стирки.
В одном варианте осуществления композиция или полипептид согласно стадии а) используется для чистки или стирки изделия по меньшей мере два раза, три раза, четыре раза, пять раз, шесть раз, семь раз, восемь раз, девять раз или десять раз перед процессом последующей чистки или стирки.
Жидкий раствор может дополнительно включать поверхностно-активные вещества, моющие компоненты, флокулирующее вспомогательное средство, хелатирующие средства, ингибиторы переноса красителей, ферменты, стабилизаторы ферментов, ингибиторы ферментов, каталитические материалы, активаторы отбелки, пероксид водорода, источники пероксида водорода, предварительно образованные перкислоты, полимерные диспергирующие средства, средства для устранения/средства против повторного осаждения глинистой грязи, отбеливатели, подавители образования мыльной пены, красители, отдушки, средства, обеспечивающие эластичность, мягчители тканей, носители, гидротропы, моющие компоненты и дополнительные моющие компоненты, окрашивающие средства для тканей, противовспенивающие средства, диспергирующие средства, технологические добавки и/или пигменты.
В одном варианте осуществления жидкий раствор может дополнительно содержать один или несколько ферментов, выбранных из группы, состоящей из протеаз, липаз, кутиназ, амилаз, карбогидраз, целлюлаз, пектиназ, маннаназ, арабиназ, галактаназ, ксиланаз и оксидаз.
Значение pH жидкого раствора находится в диапазоне от 1 до 11, например, в диапазоне от 5,5 до 11, например, в диапазоне от 7 до 9, в диапазоне от 7 до 8 или в диапазоне от 7 до 8,5.
Температура жидкого раствора может находиться в диапазоне от 5°C до 95°C, или в диапазоне от 10°C до 80°C, в диапазоне от 10°C до 70°C, в диапазоне от 10°C до 60°C, в диапазоне от 10°C до 50°C, в диапазоне от 15°C до 40°C или в диапазоне от 20°C до 30°C. В одном варианте осуществления температура жидкого раствора составляет 30°C.
В одном варианте осуществления изделие после приведения в контакт с жидким раствором прополаскивают. Изделие можно полоскать водой или водой, содержащей кондиционер.
Концентрация ДНКазы обычно находится в диапазоне от 0,00004 до 100 ppm белка-фермента, например, в диапазоне от 0,00008 до 100, в диапазоне от 0,0001 до 100, в диапазоне от 0,0002 до 100, в диапазоне от 0,0004 до 100, в диапазоне от 0,0008 до 100, в диапазоне от 0,001 до 100 ppm белка-фермента, 0,01-100 ppm белка-фермента, предпочтительно 0,05-50 ppm белка-фермента, более предпочтительно 0,1-50 ppm белка-фермента, более предпочтительно 0,1-30 ppm белка-фермента, более предпочтительно 0,5-20 ppm белка-фермента и наиболее предпочтительно 0,5-10 ppm белка-фермента.
ДНКазу по настоящему изобретению можно добавлять в моющую композицию в количестве, соответствующем по меньшей мере 0,002 мг белка ДНКазы, например, по меньшей мере 0,004 мг белка ДНКазы, по меньшей мере 0,006 мг белка ДНКазы, по меньшей мере 0,008 мг белка ДНКазы, по меньшей мере 0,01 мг белка ДНКазы, по меньшей мере 0,1 мг белка, предпочтительно по меньшей мере 1 мг белка, более предпочтительно по меньшей мере 10 мг белка, еще более предпочтительно по меньшей мере 15 мг белка, наиболее предпочтительно по меньшей мере 20 мг белка и еще более предпочтительно по меньшей мере 25 мг белка. Таким образом, моющая композиция может содержать по меньшей мере 0,00008% белка ДНКазы, предпочтительно по меньшей мере 0,002%, 0,003%, 0,004%, 0,005%, 0,006%, 0,008%, 0,01%, 0,02%, 0,03%, 0,05%, 0,1%, 0,2%, 0,3%, 0,4%, 0,6%, 0,7%, 0,8%, 0,9% или 1,0% белка ДНКазы.
Полипептид, обладающий ДНКазой активностью, может быть животного, растительного или микробного происхождения. В одном варианте осуществления полипептид характеризуется человеческим или бычьим происхождением. В одном варианте осуществления полипептид получен из растения, такого как фасоль золотистая. В одном варианте осуществления полипептид характеризуется бактериальным или грибным происхождением.
Полипептид грибного происхождения может быть выбран из группы, состоящей из:
a. полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 2, полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 3, или полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 5 или полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 8;
b. полипептида, кодируемого полинуклеотидом, который гибридизируется в условиях низкой жесткости с
i. последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 1 или последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 4
ii. ее последовательностью кДНК или
iii. последовательностью полной длины, комплементарной (i) или (ii);
c. полипептида, кодируемого полинуклеотидом, характеризующимся по меньшей мере 60% идентичностью последовательности, кодирующей зрелый полипептид, под SEQ ID NO: 1, или его последовательности кДНК, или полипептида, кодируемого полинуклеотидом, характеризующегося по меньшей мере 60% идентичностью последовательности, кодирующей зрелый полипептид, под SEQ ID NO: 4 или ее последовательности кДНК;
d. варианта зрелого полипептида под SEQ ID NO: 2, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях, варианта зрелого полипептида под SEQ ID NO: 3, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях, или варианта зрелого полипептида под SEQ ID NO: 5, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях, или варианта зрелого полипептида под SEQ ID NO: 8, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях; и
e. фрагмента полипептида (a), (b), (c) или (d), который обладает ДНКазной активностью.
В заявке на Европейский патент №14164424.5 в примерах с 1 по 3 раскрывается, как образуется полипептид под SEQ ID NO: 2, SEQ ID NO: 3 и SEQ ID NO: 8. В заявке на Европейский патент №14164429.4 в примерах с 1 по 2 раскрывается, как образуется полипептид под SEQ ID NO: 5.
Полипептид бактериального происхождения может быть выбран из группы, состоящей из:
a. полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 6, или полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 7;
b. варианта зрелого полипептида под SEQ ID NO: 6, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях, или варианта зрелого полипептида под SEQ ID NO: 7, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях; и
c. фрагмента полипептида (a), (b), (c) или (d), который обладает ДНКазной активностью.
Полипептид может характеризоваться по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100% идентичностью последовательности зрелого полипептида под SEQ ID NO: 2, зрелого полипептида под SEQ ID NO: 3, или зрелого полипептида под SEQ ID NO: 5, или зрелого полипептида под SEQ ID NO: 6, или зрелого полипептида под SEQ ID NO: 7.
В Международной заявке на патент, опубликованной под № WO2011098579, в примере 3 раскрывается как клонировать и экспрессировать полипептид под SEQ ID NO: 6.
Полипептид может содержать или состоять из последовательности под SEQ ID NO: 2 или зрелого полипептида под SEQ ID NO: 2, полипептид содержит или состоит из последовательности под SEQ ID NO: 3 или зрелого полипептида под SEQ ID NO: 3, полипептид содержит или состоит из последовательности под SEQ ID NO: 5 или зрелого полипептида под SEQ ID NO: 5, полипептид содержит или состоит из последовательности под SEQ ID NO: 6 или зрелого полипептида под SEQ ID NO: 6, полипептид содержит или состоит из последовательности под SEQ ID NO: 7 или зрелого полипептида под SEQ ID NO: 7, или полипептид содержит или состоит из последовательности под SEQ ID NO: 8 или зрелого полипептида под SEQ ID NO: 8.
Зрелый полипептид может содержать аминокислоты с 1 по 206 из последовательности под SEQ ID NO: 2 или аминокислоты с 1 по 206 последовательности под SEQ ID NO: 3, аминокислоты с 1 по 188 последовательности под SEQ ID NO: 5, аминокислоты с 1 по 110 последовательности под SEQ ID NO: 6, аминокислоты 1-109 последовательности под SEQ ID NO: 7 или аминокислоты с 1 по 206 последовательности под SEQ ID NO: 8.
Полипептид может быть вариантом зрелого полипептида под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 или SEQ ID NO: 8, где вариант характеризуется заменой, делецией и/или вставкой в одном или нескольких положениях, или вариантом зрелого полипептида под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 или SEQ ID NO: 8, который характеризуется заменой, делецией и/или вставкой в одном или нескольких положениях.
Полипептид может быть фрагментом SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 или SEQ ID NO: 8, где фрагмент обладает ДНКазной активностью.
Полипептид, обладающий ДНКазной активностью, может быть получен из Aspergillus, например, из Aspergillus oryzae.
В одном варианте осуществления настоящее изобретение относится к полипептидам, характеризующимся идентичностью последовательности зрелого полипептида под SEQ ID NO: 2, который обладает ДНКазной активностью, составляющей по меньшей мере 60%, например, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100%. В одном аспекте полипептиды отличаются не более 10 аминокислотами, например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, от зрелого полипептида под SEQ ID NO: 2.
В одном варианте осуществления настоящее изобретение относится к полипептидам, характеризующимся идентичностью последовательности зрелого полипептида под SEQ ID NO: 3, который обладает ДНКазной активностью, составляющей по меньшей мере 60%, например, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100%. В одном аспекте полипептиды отличаются не более 10 аминокислотами, например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, от зрелого полипептида под SEQ ID NO: 3.
В одном варианте осуществления настоящее изобретение относится к полипептидам, характеризующимся идентичностью последовательности зрелого полипептида под SEQ ID NO: 8, который обладает ДНКазной активностью, составляющей по меньшей мере 60%, например, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100%. В одном аспекте полипептиды отличаются не более 10 аминокислотами, например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, от зрелого полипептида под SEQ ID NO: 8.
В одном варианте осуществления полипептид был выделен. Полипептид по настоящему изобретению предпочтительно содержит, или состоит из аминокислотной последовательности под SEQ ID NO: 2 или ее аллельного варианта; или представляет собой ее фрагмент, обладающий ДНКазной активностью. В другом аспекте полипептид содержит или состоит из зрелого полипептида под SEQ ID NO: 2. В другом аспекте полипептид содержит или состоит из аминокислот с 1 по 206 последовательности под SEQ ID NO: 2.
В одном варианте осуществления полипептид был выделен. Полипептид по настоящему изобретению предпочтительно содержит, или состоит из аминокислотной последовательности под SEQ ID NO: 3 или ее аллельного варианта; или представляет собой ее фрагмент, обладающий ДНКазной активностью. В другом аспекте полипептид содержит или состоит из зрелого полипептида под SEQ ID NO: 3. В другом аспекте полипептид содержит или состоит из аминокислот с 1 по 206 последовательности под SEQ ID NO: 3.
В одном варианте осуществления полипептид был выделен. Полипептид по настоящему изобретению предпочтительно содержит, или состоит из аминокислотной последовательности под SEQ ID NO: 8 или ее аллельного варианта; или представляет собой ее фрагмент, обладающий ДНКазной активностью. В другом аспекте полипептид содержит или состоит из зрелого полипептида под SEQ ID NO: 8. В другом аспекте полипептид содержит или состоит из аминокислот с 1 по 206 последовательности под SEQ ID NO: 8.
В другом варианте осуществления настоящее изобретение относится к выделенному полипептиду, обладающему ДНКазной активностью, кодируемому полинуклеотидом, который гибридизируется в условиях низкой жесткости с (i) последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 1, (ii) ее последовательностью кДНК или (iii) последовательностью полной длины, комплементарной (i) или (ii) (Sambrook et al., 1989, Molecular Cloning, A Laboratory Manual, 2d edition, Cold Spring Harbor, New York). В одном варианте осуществления полипептид был выделен.
В другом варианте осуществления настоящее изобретение относится к полипептиду, обладающему ДНКазной активностью, кодируемому полинуклеотидом, характеризующимся идентичностью последовательности с последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 1 или ее последовательностью кДНК, составляющей по меньшей мере 60%, например, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100%. В дополнительном варианте осуществления полипептид был выделен.
В другом варианте осуществления настоящее изобретение относится к вариантам зрелого полипептида под SEQ ID NO: 2, характеризующегося заменой, делецией и/или вставкой в одном или нескольких (например, некоторых) положениях. В одном варианте осуществления количество аминокислотных замен, делеций и/или вставок, введенных в зрелый полипептид под SEQ ID NO: 2, составляет не более 10, например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10. Изменения аминокислот могут быть незначительными, то есть являться консервативными аминокислотными заменами или вставками, которые не оказывают значительного влияния на фолдинг и/или активность белка; небольшими делециями, как правило, размером 1-30 аминокислот; небольшими удлинениями на амино- или карбокси-конце, такими как амино-концевой метиониновый остаток; небольшим линкерным пептидом размером до 20-25 остатков; или небольшим удлинением, которое облегчает чистку с помощью изменения суммарного заряда, или другой функциональной группой, такой как полигистидиновый тракт, антигенный эпитоп или связывающий домен.
В другом варианте осуществления настоящее изобретение относится к вариантам зрелого полипептида под SEQ ID NO: 3, характеризующегося заменой, делецией и/или вставкой в одном или нескольких (например, некоторых) положениях. В одном варианте осуществления количество аминокислотных замен, делеций и/или вставок, введенных в зрелый полипептид под SEQ ID NO: 3, составляет не более 10, например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10. Изменения аминокислот могут быть незначительными, то есть являться консервативными аминокислотными заменами или вставками, которые не оказывают значительного влияния на фолдинг и/или активность белка; небольшими делециями, как правило, размером 1-30 аминокислот; небольшими удлинениями на амино- или карбокси-конце, такими как амино-концевой метиониновый остаток; небольшим линкерным пептидом размером до 20-25 остатков; или небольшим удлинением, которое облегчает чистку с помощью изменения суммарного заряда, или другой функциональной группой, такой как полигистидиновый тракт, антигенный эпитоп или связывающий домен.
Полипептид, обладающий ДНКазной активностью, может быть получен из Trichoderma, например, из Trichoderma harzianum. В одном варианте осуществления настоящее изобретение относится к полипептидам, характеризующимся идентичностью последовательности зрелого полипептида под SEQ ID NO: 5, который обладает ДНКазной активностью, составляющей по меньшей мере 60%, например, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100%. В одном аспекте полипептиды отличаются не более 10 аминокислотами, например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, от зрелого полипептида под SEQ ID NO: 5.
В одном варианте осуществления полипептид был выделен. Полипептид по настоящему изобретению предпочтительно содержит, или состоит из аминокислотной последовательности под SEQ ID NO: 5 или ее аллельного варианта; или представляет собой ее фрагмент, обладающий ДНКазной активностью. В другом аспекте полипептид содержит или состоит из зрелого полипептида под SEQ ID NO: 5. В другом аспекте полипептид содержит или состоит из аминокислот с 1 по 188 последовательности под SEQ ID NO: 5.
В другом варианте осуществления настоящее изобретение относится к выделенному полипептиду, обладающему ДНКазной активностью, кодируемому полинуклеотидом, который гибридизируется в условиях низкой жесткости с (i) последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 4, (ii) ее последовательностью кДНК или (iii) последовательностью полной длины, комплементарной (i) или (ii) (Sambrook et al., 1989, Molecular Cloning, A Laboratory Manual, 2d edition, Cold Spring Harbor, New York). В одном варианте осуществления полипептид был выделен.
Полинуклеотид под SEQ ID NO: 1 или SEQ ID NO: 4 или его подпоследовательность, а также полипептид под SEQ ID NO: 5, SEQ ID NO: 2, SEQ ID NO: 3 или его фрагмент можно применять для конструирования зондов на основе нуклеиновой кислоты для идентификации и клонирования ДНК, кодирующей полипептид, обладающий ДНКазной активностью, из штаммов разных родов или видов в соответствии со способами, хорошо известными из уровня техники.
В частности, такие зонды можно применять для гибридизации с геномной ДНК или кДНК представляющей интерес клетки после стандартных процедур Саузерн-блоттинга с целью идентификации и выделения их соответствующего гена. Такие зонды могут быть значительно короче полной последовательности, однако должны иметь в длину по меньшей мере 15, например, по меньшей мере 25, по меньшей мере 35 или по меньшей мере 70 нуклеотидов. Зонд на основе нуклеиновой кислоты предпочтительно имеет длину по меньшей мере 100 нуклеотидов, например, имеет в длину по меньшей мере 200 нуклеотидов, по меньшей мере 300 нуклеотидов, по меньшей мере 400 нуклеотидов, по меньшей мере 500 нуклеотидов, по меньшей мере 600 нуклеотидов, по меньшей мере 700 нуклеотидов, по меньшей мере 800 нуклеотидов или по меньшей мере 900 нуклеотидов. Можно применять как ДНК-, так и РНК-зонды. Как правило, зонды метят для выявления соответствующего гена (например, с помощью 32P, 3H, 35S, биотина или авидина). Такие зонды охватываются настоящим изобретением.
Библиотеку геномной ДНК или кДНК, полученную из других таких штаммов, можно подвергать скринингу в отношении ДНК, которая гибридизируется с описанными выше зондами и кодирует полипептид, обладающий ДНКазной активностью. Геномную или другую ДНК из других таких штаммов можно разделять с помощью электрофореза в агарозном или полиакриламидном геле или других методик разделения. ДНК из библиотек или разделенную ДНК можно переносить и иммобилизировать на нитроцеллюлозе или другом подходящем материале-носителе. С целью идентификации клона или ДНК, которые гибридизируются с SEQ ID NO: 4 или ее подпоследовательностью, материал-носитель применяется в Саузерн-блоттинге.
В контексте настоящего изобретения гибридизация указывает на то, что полинуклеотид гибридизируется с меченым зондом на основе нуклеиновой кислоты, соответствующим (i) SEQ ID NO: 1 или SEQ ID NO: 4; (ii) последовательности, кодирующей зрелый полипептид, под SEQ ID NO: 1 или SEQ ID NO: 4; (iii) последовательности ее кДНК, (iv) комплементарной ей последовательности полной длины; или (v) ее подпоследовательности; в условиях жесткости, от очень низкой до очень высокой. Молекулы, с которыми в данных условиях гибридизируется зонд на основе нуклеиновой кислоты, можно выявлять с помощью, например, пленки для рентгенографии или любых других средств для выявления, известных из уровня техники.
В другом варианте осуществления настоящее изобретение относится к полипептиду, обладающему ДНКазной активностью, кодируемому полинуклеотидом, характеризующимся идентичностью последовательности с последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 1 или SEQ ID NO: 4 или ее последовательностью кДНК, составляющей по меньшей мере 60%, например, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100%. В дополнительном варианте осуществления полипептид был выделен.
В другом варианте осуществления настоящее изобретение относится к вариантам зрелого полипептида под SEQ ID NO: 2, SEQ ID NO: 3 или SEQ ID NO: 5, характеризующегося заменой, делецией и/или вставкой в одном или нескольких (например, некоторых) положениях. В одном варианте осуществления количество аминокислотных замен, делеций и/или вставок, введенных в зрелый полипептид под SEQ ID NO: 2, SEQ ID NO: 3 или SEQ ID NO: 5, составляет не более 10, например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10. Изменения аминокислот могут быть незначительными, то есть являться консервативными аминокислотными заменами или вставками, которые не оказывают значительного влияния на фолдинг и/или активность белка; небольшими делециями, как правило, размером 1-30 аминокислот; небольшими удлинениями на амино- или карбокси-конце, такими как амино-концевой метиониновый остаток; небольшим линкерным пептидом размером до 20-25 остатков; или небольшим удлинением, которое облегчает чистку с помощью изменения суммарного заряда, или другой функциональной группой, такой как полигистидиновый тракт, антигенный эпитоп или связывающий домен.
Полипептид, обладающий ДНКазной активностью, может быть получен из Bacillus, например, из Bacillus substilis или Bacillus licheniformis.
В одном варианте осуществления настоящее изобретение относится к полипептидам, характеризующимся идентичностью последовательности зрелого полипептида под SEQ ID NO: 6 или SEQ ID NO: 7, который обладает ДНКазной активностью, составляющей по меньшей мере 60%, например, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100%. В одном аспекте полипептиды отличаются не более 10 аминокислотами, например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, от зрелого полипептида под SEQ ID NO: 6 или SEQ ID NO: 7.
В одном варианте осуществления полипептид был выделен. Полипептид по настоящему изобретению предпочтительно содержит, или состоит из аминокислотной последовательности под SEQ ID NO: 6, SEQ ID NO: 7 или ее аллельного варианта; или представляет собой ее фрагмент, обладающий ДНКазной активностью. В другом аспекте полипептид содержит или состоит из зрелого полипептида под SEQ ID NO: 6 или SEQ ID NO: 7. В другом аспекте полипептид содержит или состоит из аминокислот с 1 по 110 последовательности под SEQ ID NO: 6 или аминокислот с 1 по 109 последовательности под SEQ ID NO: 7.
В другом варианте осуществления настоящее изобретение относится к полипептиду, обладающему ДНКазной активностью, кодируемому полинуклеотидом, характеризующимся идентичностью последовательности с последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 6, SEQ ID NO: 7 или ее последовательностью кДНК, составляющей по меньшей мере 60%, например, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100%. В дополнительном варианте осуществления полипептид был выделен.
В другом варианте осуществления настоящее изобретение относится к полипептиду, обладающему ДНКазной активностью, кодируемому полинуклеотидом, характеризующимся идентичностью последовательности с последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 6, SEQ ID NO: 7 или их последовательностью кДНК, составляющей по меньшей мере 60%, например, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100%, и где полипептид используется для предупреждения или уменьшения повторного осаждения грязи на изделии в ходе процесса последующей чистки или стирки.
В другом варианте осуществления настоящее изобретение относится к вариантам зрелого полипептида под SEQ ID NO: 6 или SEQ ID NO: 7, характеризующегося заменой, делецией и/или вставкой в одном или нескольких (например, некоторых) положениях. В одном варианте осуществления количество аминокислотных замен, делеций и/или вставок, введенных в зрелый полипептид под SEQ ID NO: 6 или SEQ ID NO: 7, составляет не более 10, например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10. Изменения аминокислот могут быть незначительными, то есть являться консервативными аминокислотными заменами или вставками, которые не оказывают значительного влияния на фолдинг и/или активность белка; небольшими делециями, как правило, размером 1-30 аминокислот; небольшими удлинениями на амино- или карбокси-конце, такими как амино-концевой метиониновый остаток; небольшим линкерным пептидом размером до 20-25 остатков; или небольшим удлинением, которое облегчает чистку с помощью изменения суммарного заряда, или другой функциональной группой, такой как полигистидиновый тракт, антигенный эпитоп или связывающий домен.
Примерами консервативных замен являются замены в пределах групп основных аминокислот (аргинин, лизин и гистидин), кислых аминокислот (глутаминовая кислота и аспарагиновая кислота), полярных аминокислот (глутамин и аспарагин), гидрофобных аминокислот (лейцин, изолейцин и валин), ароматических аминокислот (фенилаланин, триптофан и тирозин) и малых аминокислот (глицин, аланин, серин, треонин и метионин). Аминокислотные замены, которые в целом не изменяют специфическую активность, известны из уровня техники и описаны, например, в H. Neurath и R.L. Hill, 1979, в The Proteins, Academic Press, New York. Обычные замены представляют собой Ala/Ser, Val/Ile, Asp/Glu, Thr/Ser, Ala/Gly, Ala/Thr, Ser/Asn, Ala/Val, Ser/Gly, Tyr/Phe, Ala/Pro, Lys/Arg, Asp/Asn, Leu/Ile, Leu/Val, Ala/Glu и Asp/Gly.
Альтернативно, изменения аминокислот имеют такой характер, что физико-химические свойства полипептидов изменяются. Например, изменения аминокислот могут улучшать термоустойчивость полипептида, изменять субстратную специфичность, изменять оптимальное значение pH и т. п.
Незаменимые аминокислоты в полипептиде можно идентифицировать в соответствии с процедурами, известными из уровня техники, такими как сайт-направленный мутагенез или аланин-сканирующий мутагенез (Cunningham and Wells, 1989, Science 244: 1081-1085). В последней методике отдельные мутации, заключающиеся в замене на аланин, вводят в каждый остаток в молекуле и полученные в результате мутантные молекулы исследуют в отношении ДНКазной активности для идентификации аминокислотных остатков, которые являются определяющими для активности молекулы. См. также Hilton et al., 1996, J. Biol. Chem. 271: 4699-4708. Активный сайт для ферментативного или другого биологического взаимодействия можно также определять с помощью физического анализа структуры, которую определяют с помощью таких методик, как ядерный магнитный резонанс, кристаллография, дифракция электронов или фотоаффинное мечение в сочетании с мутацией аминокислот предполагаемого контактирующего сайта. См., например, de Vos et al., 1992, Science 255: 306-312; Smith et al., 1992, J. Mol. Biol. 224: 899-904; Wlodaver et al., 1992, FEBS Lett. 309: 59-64. Об идентичности незаменимых аминокислот можно также сделать заключение на основании выравнивания с родственным полипептидом.
Одну или несколько аминокислотных замен, делеций и/или вставок можно осуществлять и исследовать с помощью известных способов мутагенеза, рекомбинации и/или шаффлинга с последующей соответствующей процедурой скрининга, например, таких, как раскрыты в Reidhaar-Olson and Sauer, 1988, Science 241: 53-57; Bowie and Sauer, 1989, Proc. Natl. Acad. Sci. USA 86: 2152-2156; WO 95/17413 или WO 95/22625. Другие способы, которые можно применять, включают ПЦР пониженной точности, фаговый дисплей (например, Lowman et al., 1991, Biochemistry 30: 10832-10837; патент США № 5223409; WO 92/06204) и мутагенез, направленный на участок (Derbyshire et al., 1986, Gene 46: 145; Ner et al., 1988, DNA 7: 127).
Способы мутагенеза/шаффлинга можно объединять со способами автоматизированного скрининга с высокой пропускной способностью для выявления активности клонированных, подвергнутых мутагенезу полипептидов, экспрессируемых клетками-хозяевами (Ness et al., 1999, Nature Biotechnology 17: 893-896). Подвергнутые мутагенезу молекулы ДНК, которые кодируют активные полипептиды, можно извлекать из клеток-хозяев и быстро секвенировать с применением стандартных способов из уровня техники. Такие способы предусматривают возможность быстрого определения важности отдельных аминокислотных остатков в полипептиде.
Полипептид может представлять собой гибридный полипептид, в котором участок одного полипептида слит с N-концом или C-концом участка другого полипептида.
Полипептид может представлять собой слитый полипептид или расщепляемый слитый полипептид, в котором другой полипептид слит с N-концом или C-концом полипептида по настоящему изобретению. Слитый полипептид получают с помощью слияния полинуклеотида, кодирующего другой полипептид, с полинуклеотидом по настоящему изобретению. Методики получения слитых полипептидов известны из уровня техники и включают лигирование кодирующих последовательностей, кодирующих полипептиды, с тем, чтобы они находились в рамке и чтобы экспрессия слитого полипептида находилась под контролем одних и тех же промотора(промоторов) и терминатора. Слитые полипептиды можно также конструировать с применением интеиновой технологии, в которой слитые полипептиды создаются посттрансляционно (Cooper et al., 1993, EMBO J. 12: 2575-2583; Dawson et al., 1994, Science 266: 776-779).
Слитый полипептид может дополнительно содержать сайт расщепления между двумя полипептидами. После секреции слитого белка сайт расщепляется с высвобождением двух полипептидов. Примеры сайтов расщепления включают без ограничения сайты, раскрытые в Martin et al., 2003, J. Ind. Microbiol. Biotechnol. 3: 568-576; Svetina et al., 2000, J. Biotechnol. 76: 245-251; Rasmussen-Wilson et al., 1997, Appl. Environ. Microbiol. 63: 3488-3493; Ward et al., 1995, Biotechnology 13: 498-503; и Contreras et al., 1991, Biotechnology 9: 378-381; Eaton et al., 1986, Biochemistry 25: 505-512; Collins-Racie et al., 1995, Biotechnology 13: 982-987; Carter et al., 1989, Proteins: Structure, Function, and Genetics 6: 240-248; и Stevens, 2003, Drug Discovery World 4: 35-48.
Дезоксирибонуклеаза (ДНКаза)
Полипептид, обладающий ДНКазной активностью, или дезоксирибонуклеаза (ДНКаза), представляет собой любой фермент, который катализирует гидролитическое расщепление связей сложного фосфодиэфира в каркасе ДНК, разрушая таким образом ДНК. Два термина, - полипептид, обладающий ДНКазной активностью, и ДНКаза, - применяют взаимозаменяемо.
В соответствии с настоящим изобретением предпочтительной является ДНКаза, получаемая из гриба; в частности, предпочтительной является ДНКаза, которую можно получать из Aspergillus; в частности, предпочтительной является ДНКаза, которую можно получать из Aspergillus oryzae. В одном варианте осуществления настоящего изобретения полипептид, обладающий дезоксирибонуклеазной активностью, не является S1 нуклеазой из Aspergillus oryzae.
ДНКаза, применяемая в настоящем изобретении, предпочтительно включает в себя зрелый полипептид под SEQ ID NO: 2, показанный как аминокислоты с 1 по 206 последовательности под SEQ ID NO: 2, который получают из Aspergillus oryzae. Полипептид, обладающий ДНКазной активностью, может быть получен из Aspergillus, например, из Aspergillus oryzae. В одном варианте осуществления настоящего изобретения полипептид, обладающий ДНКазной активностью, представляет собой заявленный полипептид.
Один аспект настоящего изобретения относится к выделенным полипептидам, характеризующимся идентичностью последовательности зрелого полипептида под SEQ ID NO: 2, который обладает ДНКазной активностью, составляющей по меньшей мере 60%, например, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100%. В одном аспекте полипептиды отличаются не более 10 аминокислотами, например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, от зрелого полипептида под SEQ ID NO: 2.
В одном варианте осуществления настоящее изобретение относится к выделенным полипептидам, характеризующимся идентичностью последовательности зрелого полипептида под SEQ ID NO: 3, который обладает ДНКазной активностью, составляющей по меньшей мере 60%, например, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100%. В одном аспекте полипептиды отличаются не более 10 аминокислотами, например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, от зрелого полипептида под SEQ ID NO: 3.
Один вариант осуществления настоящего изобретения относится к выделенным полипептидам, характеризующимся идентичностью последовательности под SEQ ID NO: 8, которая обладает ДНКазной активностью, составляющей по меньшей мере 60%, например, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100%. В одном аспекте полипептиды отличаются не более 10 аминокислотами, например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, от зрелого полипептида под SEQ ID NO: 8.
Полипептид по настоящему изобретению предпочтительно содержит, или состоит из аминокислотной последовательности под SEQ ID NO: 2 или ее аллельного варианта; или представляет собой ее фрагмент, обладающий ДНКазной активностью. В другом аспекте полипептид содержит или состоит из зрелого полипептида под SEQ ID NO: 2. В другом аспекте полипептид содержит или состоит из аминокислот с 1 по 206 последовательности под SEQ ID NO: 2.
В одном варианте осуществления полипептид был выделен. Полипептид по настоящему изобретению предпочтительно содержит, или состоит из аминокислотной последовательности под SEQ ID NO: 3 или ее аллельного варианта; или представляет собой ее фрагмент, обладающий ДНКазной активностью. В другом аспекте полипептид содержит или состоит из зрелого полипептида под SEQ ID NO: 3. В другом аспекте полипептид содержит или состоит из аминокислот с 1 по 204 последовательности под SEQ ID NO: 3. Один аспект настоящего изобретения относится к композиции, содержащей или состоящей из полипептида, который состоит из аминокислотной последовательности под SEQ ID NO: 8, и полипептида по настоящему изобретению, состоящего из аминокислотной последовательности под SEQ ID NO: 3.
В другом варианте осуществления настоящее изобретение относится к выделенному полипептиду, обладающему ДНКазной активностью, кодируемому полинуклеотидом, который гибридизируется в условиях низкой жесткости с (i) последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 1, (ii) ее последовательностью кДНК или (iii) последовательностью полной длины, комплементарной (i) или (ii) (Sambrook et al., 1989, Molecular Cloning, A Laboratory Manual, 2d edition, Cold Spring Harbor, New York). В одном варианте осуществления полипептид был выделен.
В другом варианте осуществления настоящее изобретение относится к выделенному полипептиду, обладающему ДНКазной активностью, кодируемому полинуклеотидом, который гибридизируется в условиях умеренно низкой жесткости с (i) последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 1, с (ii) ее последовательностью кДНК или (iii) последовательностью полной длины, комплементарной (i) или (ii). В одном варианте осуществления полипептид был выделен.
В другом варианте осуществления настоящее изобретение относится к выделенному полипептиду, обладающему ДНКазной активностью, кодируемому полинуклеотидом, который гибридизируется в условиях умеренной жесткости с (i) последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 1, с (ii) ее последовательностью кДНК или (iii) последовательностью полной длины, комплементарной (i) или (ii). В одном варианте осуществления полипептид был выделен.
В другом варианте осуществления настоящее изобретение относится к выделенному полипептиду, обладающему ДНКазной активностью, кодируемому полинуклеотидом, который гибридизируется в условиях умеренно высокой жесткости с (i) последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 1, с (ii) ее последовательностью кДНК или (iii) последовательностью полной длины, комплементарной (i) или (ii). В одном варианте осуществления полипептид был выделен.
В другом варианте осуществления настоящее изобретение относится к выделенному полипептиду, обладающему ДНКазной активностью, кодируемому полинуклеотидом, который гибридизируется в условиях высокой жесткости с (i) последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 1, с (ii) ее последовательностью кДНК или (iii) последовательностью полной длины, комплементарной (i) или (ii). В одном варианте осуществления полипептид был выделен.
В другом варианте осуществления настоящее изобретение относится к выделенному полипептиду, обладающему ДНКазной активностью, кодируемому полинуклеотидом, который гибридизируется в условиях очень высокой жесткости с (i) последовательностью, кодирующей зрелый полипептид под SEQ ID NO: 1, с (ii) ее последовательностью кДНК или (iii) последовательностью полной длины, комплементарной (i) или (ii). В одном варианте осуществления полипептид был выделен.
В другом варианте осуществления настоящее изобретение относится к полипептиду, обладающему ДНКазной активностью, кодируемому полинуклеотидом, характеризующимся идентичностью последовательности с последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 1 или ее последовательностью кДНК, составляющей по меньшей мере 60%, например, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100%. В дополнительном варианте осуществления полипептид был выделен.
В другом варианте осуществления настоящее изобретение относится к вариантам зрелого полипептида под SEQ ID NO: 2, характеризующегося заменой, делецией и/или вставкой в одном или нескольких (например, некоторых) положениях. В одном варианте осуществления количество аминокислотных замен, делеций и/или вставок, введенных в зрелый полипептид под SEQ ID NO: 2, составляет не более 10, например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10. Изменения аминокислот могут быть незначительными, то есть являться консервативными аминокислотными заменами или вставками, которые не оказывают значительного влияния на фолдинг и/или активность белка; небольшими делециями, как правило, размером 1-30 аминокислот; небольшими удлинениями на амино- или карбокси-конце, такими как амино-концевой метиониновый остаток; небольшим линкерным пептидом размером до 20-25 остатков; или небольшим удлинением, которое облегчает чистку с помощью изменения суммарного заряда, или другой функциональной группой, такой как полигистидиновый тракт, антигенный эпитоп или связывающий домен.
В другом варианте осуществления настоящее изобретение относится к вариантам зрелого полипептида под SEQ ID NO: 3, характеризующегося заменой, делецией и/или вставкой в одном или нескольких (например, некоторых) положениях. В одном варианте осуществления количество аминокислотных замен, делеций и/или вставок, введенных в зрелый полипептид под SEQ ID NO: 3, составляет не более 10, например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10. Изменения аминокислот могут быть незначительными, то есть являться консервативными аминокислотными заменами или вставками, которые не оказывают значительного влияния на фолдинг и/или активность белка; небольшими делециями, как правило, размером 1-30 аминокислот; небольшими удлинениями на амино- или карбокси-конце, такими как амино-концевой метиониновый остаток; небольшим линкерным пептидом размером до 20-25 остатков; или небольшим удлинением, которое облегчает чистку с помощью изменения суммарного заряда, или другой функциональной группой, такой как полигистидиновый тракт, антигенный эпитоп или связывающий домен.
Фермент ДНКаза может содержать или состоять из аминокислотной последовательности, показанной как аминокислоты от -37 до 206 последовательности под SEQ ID NO: 2 или ее фрагмента, который обладает ДНКазной активностью, такого, как зрелый полипептид. Или фермент ДНКаза может содержать или состоять из фрагмента аминокислот с -37 по 206 последовательности под SEQ ID NO: 2 или аминокислот с 1 по 206 последовательности под SEQ ID NO: 2, для которого одну или несколько аминокислот фрагмента удаляют c амино- и/или карбоксильного конца последовательности под SEQ ID NO: 2.
Фермент ДНКаза может содержать или состоять из аминокислотной последовательности, показанной как аминокислоты с 1 по 206 последовательности под SEQ ID NO: 3 или ее фрагмента, который обладает ДНКазной активностью, такого, как зрелый полипептид. Или фермент ДНКаза может содержать или состоять из фрагмента аминокислот с 1 по 206 последовательности под SEQ ID NO: 3 или аминокислот с 1 по 206 последовательности под SEQ ID NO: 3, для которого одну или несколько аминокислот фрагмента удаляют c амино- и/или карбоксильного конца последовательности под SEQ ID NO: 3.
Фермент ДНКаза может содержать или состоять из аминокислотной последовательности, показанной как аминокислоты с 1 по 206 последовательности под SEQ ID NO: 8 или ее фрагмента, который обладает ДНКазной активностью, такого, как зрелый полипептид. Или фермент ДНКаза может содержать или состоять из фрагмента аминокислот с 1 по 206 последовательности под SEQ ID NO: 8 или аминокислот с 1 по 206 последовательности под SEQ ID NO: 8, для которого одну или несколько аминокислот фрагмента удаляют c амино- и/или карбоксильного конца последовательности под SEQ ID NO: 8.
В настоящем изобретении также представлены полипептиды ДНКазы, которые, по сути, гомологичны вышеприведенным полипептидам и их видовым гомологам (паралогам или ортологам). Термин "по сути, гомологичный" в данном документе применяют для обозначения полипептидов, которые по меньшей мере на 80%, предпочтительно по меньшей мере на 85%, более предпочтительно по меньшей мере на 90%, более предпочтительно по меньшей мере на 95%, еще более предпочтительно по меньшей мере на 97% идентичны и наиболее предпочтительно по меньшей мере на 99% или более идентичны аминокислотной последовательности под SEQ ID NO: 2, или аминокислотной последовательности под SEQ ID NO: 3, или ее фрагменту, который обладает ДНКазной активностью, или ее ортологам или паралогам.
В другом варианте осуществления ДНКаза под SEQ ID NO: 2 характеризуется заменой, делецией и/или вставкой в одном или нескольких (например, некоторых) положениях. В другом варианте осуществления ДНКаза под SEQ ID NO: 3 характеризуется заменой, делецией и/или вставкой в одном или нескольких (например, некоторых) положениях. В одном варианте осуществления количество аминокислотных замен, делеций и/или вставок, введенных в зрелый полипептид под SEQ ID NO: 2 или в зрелый полипептид под SEQ ID NO: 3, составляет не более 10, например, 1, 2, 3, 4, 5, 6, 7, 8 или 9. Изменения аминокислот могут быть незначительными, то есть являться консервативными аминокислотными заменами или вставками, которые не оказывают значительного влияния на фолдинг и/или активность белка; небольшими делециями, как правило, размером 1-30 аминокислот; небольшими удлинениями на амино- или карбокси-конце, такими как амино-концевой метиониновый остаток; небольшим линкерным пептидом размером до 20-25 остатков; или небольшим удлинением, которое облегчает чистку с помощью изменения суммарного заряда, или другой функциональной группой, такой как полигистидиновый тракт, антигенный эпитоп или связывающий домен.
В соответствии с настоящим изобретением предпочтительной является ДНКаза, получаемая из гриба; в частности, предпочтительной является ДНКаза, которую можно получать из Trichoderma; в частности, предпочтительной является ДНКаза, которую можно получать из Trichoderma harzianum.
ДНКаза, применяемая в настоящем изобретении, включает зрелый полипептид под SEQ ID NO: 5, показанный как аминокислоты с 1 по 188 последовательности под SEQ ID NO: 5, которую получают из Trichoderma harzianum.
Фермент ДНКаза может содержать или состоять из аминокислотной последовательности, показанной как аминокислоты с 17 по 188 последовательности под SEQ ID NO: 5 или ее фрагмента, который обладает ДНКазной активностью, такого, как зрелый полипептид. Или фермент ДНКаза может содержать или состоять из фрагмента аминокислот с -17 по 188 последовательности под SEQ ID NO: 5 или аминокислот с 1 по 188 последовательности под SEQ ID NO: 5, для которого одну или несколько аминокислот фрагмента удаляют c амино- и/или карбоксильного конца последовательности под SEQ ID NO: 5.
В настоящем изобретении также представлены полипептиды ДНКазы, которые, по сути, гомологичны вышеприведенным полипептидам и их видовым гомологам (паралогам или ортологам). Термин "по сути, гомологичный" в данном документе применяют для обозначения полипептидов, которые по меньшей мере на 80%, предпочтительно по меньшей мере на 85%, более предпочтительно по меньшей мере на 90%, более предпочтительно по меньшей мере на 95%, еще более предпочтительно по меньшей мере на 97% идентичны и наиболее предпочтительно по меньшей мере на 99% или более идентичны аминокислотной последовательности под SEQ ID NO: 5, или ее фрагменту, который обладает ДНКазной активностью, или ее ортологам или паралогам.
В соответствии с настоящим изобретением предпочтительной является ДНКаза, получаемая из гриба; в частности, предпочтительной является ДНКаза, которую можно получать из Bacillus; в частности, предпочтительной является ДНКаза, которую можно получать из Bacillus subtilis или Bacillus licheniformis.
ДНКаза, применяемая в настоящем изобретении, включает зрелый полипептид под SEQ ID NO: 6, показанный как аминокислоты с 1 по 110 последовательности под SEQ ID NO: 6, полученный из Bacillus subtilis; или зрелый полипептид под SEQ ID NO: 7, показанный как аминокислоты с 1 по 109 последовательности под SEQ ID NO: 7, полученный из Bacillus licheniformis.
Фермент ДНКаза может содержать или состоять из аминокислотной последовательности, показанной как аминокислоты с -26 по 110 последовательности под SEQ ID NO: 6 или аминокислоты с -33 по 109 последовательности под SEQ ID NO: 7, или ее фрагмента, который обладает ДНКазной активностью, такого, как зрелый полипептид. Фрагмент из аминокислот с -26 по 110 последовательности под SEQ ID NO: 6 или аминокислот с 1 по 110 последовательности под SEQ ID NO: 6 представляет собой полипептид, одна или несколько аминокислот которого удалены c амино- и/или карбоксильного конца последовательности под SEQ ID NO: 6. Фрагмент из аминокислот с -33 по 109 последовательности под SEQ ID NO: 7 или с 1 по 109 последовательности под SEQ ID NO: 7 представляет собой полипептид, одна или несколько аминокислот которого удалены c амино- и/или карбоксильного конца последовательности под SEQ ID NO: 7.
В настоящем изобретении также представлены полипептиды ДНКазы, которые, по сути, гомологичны вышеприведенным полипептидам и их видовым гомологам (паралогам или ортологам). Термин "по сути, гомологичный" в данном документе применяют для обозначения полипептидов, которые по меньшей мере на 80%, предпочтительно по меньшей мере на 85%, более предпочтительно по меньшей мере на 90%, более предпочтительно по меньшей мере на 95%, еще более предпочтительно по меньшей мере на 97% идентичны и наиболее предпочтительно по меньшей мере на 99% или более идентичны аминокислотной последовательности под SEQ ID NO: 6 или SEQ ID NO: 7, или ее фрагменту, который обладает ДНКазной активностью, или ее ортологам или паралогам.
Примерами консервативных замен являются замены в пределах групп основных аминокислот (аргинин, лизин и гистидин), кислых аминокислот (глутаминовая кислота и аспарагиновая кислота), полярных аминокислот (глутамин и аспарагин), гидрофобных аминокислот (лейцин, изолейцин и валин), ароматических аминокислот (фенилаланин, триптофан и тирозин) и малых аминокислот (глицин, аланин, серин, треонин и метионин). Аминокислотные замены, которые в целом не изменяют специфическую активность, известны из уровня техники и описаны, например, в H. Neurath и R.L. Hill, 1979, в The Proteins, Academic Press, New York. Обычные замены представляют собой Ala/Ser, Val/Ile, Asp/Glu, Thr/Ser, Ala/Gly, Ala/Thr, Ser/Asn, Ala/Val, Ser/Gly, Tyr/Phe, Ala/Pro, Lys/Arg, Asp/Asn, Leu/Ile, Leu/Val, Ala/Glu и Asp/Gly.
Альтернативно, изменения аминокислот имеют такой характер, что физико-химические свойства полипептидов изменяются. Например, изменения аминокислот могут улучшать термоустойчивость полипептида, изменять субстратную специфичность, изменять оптимальное значение pH и т. п.
Незаменимые аминокислоты в полипептиде можно идентифицировать в соответствии с процедурами, известными из уровня техники, такими как сайт-направленный мутагенез или аланин-сканирующий мутагенез (Cunningham and Wells, 1989, Science 244: 1081-1085). В последней методике отдельные мутации, заключающиеся в замене на аланин, вводят в каждый остаток в молекуле и полученные в результате мутантные молекулы исследуют в отношении ДНКазной активности для идентификации аминокислотных остатков, которые являются определяющими для активности молекулы. См. также Hilton et al., 1996, J. Biol. Chem. 271: 4699-4708. Активный сайт для ферментативного или другого биологического взаимодействия можно определять также с помощью физического анализа структуры, которую определяют с помощью таких методик, как ядерный магнитный резонанс, кристаллография, дифракция электронов или фотоаффинное мечение в сочетании с мутацией аминокислот предполагаемого контактирующего сайта. См., например, de Vos et al., 1992, Science 255: 306-312; Smith et al., 1992, J. Mol. Biol. 224: 899-904; Wlodaver et al., 1992, FEBS Lett. 309: 59-64. Об идентичности незаменимых аминокислот можно также сделать заключение на основании выравнивания с родственным полипептидом.
Одну или несколько аминокислотных замен, делеций и/или вставок можно осуществлять и исследовать с помощью известных способов мутагенеза, рекомбинации и/или шаффлинга с последующей соответствующей процедурой скрининга, например, таких, как раскрыты в Reidhaar-Olson and Sauer, 1988, Science 241: 53-57; Bowie and Sauer, 1989, Proc. Natl. Acad. Sci. USA 86: 2152-2156; WO 95/17413 или WO 95/22625. Другие способы, которые можно применять, включают ПЦР пониженной точности, фаговый дисплей (например, Lowman et al., 1991, Biochemistry 30: 10832-10837; патент США № 5223409; WO 92/06204) и мутагенез, направленный на участок (Derbyshire et al., 1986, Gene 46: 145; Ner et al., 1988, DNA 7: 127).
Способы мутагенеза/шаффлинга можно объединять со способами автоматизированного скрининга с высокой пропускной способностью для выявления активности клонированных, подвергнутых мутагенезу полипептидов, экспрессируемых клетками-хозяевами (Ness et al., 1999, Nature Biotechnology 17: 893-896). Подвергнутые мутагенезу молекулы ДНК, которые кодируют активные полипептиды, можно извлекать из клеток-хозяев и быстро секвенировать с применением стандартных способов из уровня техники. Такие способы предусматривают возможность быстрого определения важности отдельных аминокислотных остатков в полипептиде.
Полипептид может представлять собой гибридный полипептид, в котором участок одного полипептида слит с N-концом или C-концом участка другого полипептида.
Полипептид может представлять собой слитый полипептид или расщепляемый слитый полипептид, в котором другой полипептид слит с N-концом или C-концом полипептида по настоящему изобретению. Слитый полипептид получают с помощью слияния полинуклеотида, кодирующего другой полипептид, с полинуклеотидом по настоящему изобретению. Методики получения слитых полипептидов известны из уровня техники и включают лигирование кодирующих последовательностей, кодирующих полипептиды, с тем, чтобы они находились в рамке и чтобы экспрессия слитого полипептида находилась под контролем одного и того же промотора(промоторов) и терминатора. Слитые полипептиды можно также конструировать с применением интеиновой технологии, в которой слитые полипептиды создаются посттрансляционно (Cooper et al., 1993, EMBO J. 12: 2575-2583; Dawson et al., 1994, Science 266: 776-779).
Слитый полипептид может дополнительно содержать сайт расщепления между двумя полипептидами. После секреции слитого белка сайт расщепляется с высвобождением двух полипептидов. Примеры сайтов расщепления включают без ограничения сайты, раскрытые в Martin et al., 2003, J. Ind. Microbiol. Biotechnol. 3: 568-576; Svetina et al., 2000, J. Biotechnol. 76: 245-251; Rasmussen-Wilson et al., 1997, Appl. Environ. Microbiol. 63: 3488-3493; Ward et al., 1995, Biotechnology 13: 498-503; и Contreras et al., 1991, Biotechnology 9: 378-381; Eaton et al., 1986, Biochemistry 25: 505-512; Collins-Racie et al., 1995, Biotechnology 13: 982-987; Carter et al., 1989, Proteins: Structure, Function, and Genetics 6: 240-248; и Stevens, 2003, Drug Discovery World 4: 35-48.
Концентрация ДНКазы обычно находится в диапазоне от 0,00004 до 100 ppm белка-фермента, например, в диапазоне от 0,00008 до 100, в диапазоне от 0,0001 до 100, в диапазоне от 0,0002 до 100, в диапазоне от 0,0004 до 100, в диапазоне от 0,0008 до 100, в диапазоне от 0,001 до 100 ppm белка-фермента, 0,01-100 ppm белка-фермента, предпочтительно 0,05-50 ppm белка-фермента, более предпочтительно 0,1-50 ppm белка-фермента, более предпочтительно 0,1-30 ppm белка-фермента, более предпочтительно 0,5-20 ppm белка-фермента и наиболее предпочтительно 0,5-10 ppm белка-фермента.
ДНКазу по настоящему изобретению можно добавлять в моющую композицию в количестве, соответствующем по меньшей мере 0,002 мг белка ДНКазы, например, по меньшей мере 0,004 мг белка ДНКазы, по меньшей мере 0,006 мг белка ДНКазы, по меньшей мере 0,008 мг белка ДНКазы, по меньшей мере 0,01 мг белка ДНКазы, по меньшей мере 0,1 мг белка, предпочтительно по меньшей мере 1 мг белка, более предпочтительно по меньшей мере 10 мг белка, еще более предпочтительно по меньшей мере 15 мг белка, наиболее предпочтительно по меньшей мере 20 мг белка и еще более предпочтительно по меньшей мере 25 мг белка. Таким образом, моющая композиция может содержать по меньшей мере 0,00008% белка ДНКазы, предпочтительно по меньшей мере 0,002%, 0,003%, 0,004%, 0,005%, 0,006%, 0,008%, 0,01%, 0,02%, 0,03%, 0,05%, 0,1%, 0,2%, 0,3%, 0,4%, 0,6%, 0,7%, 0,8%, 0,9% или 1,0% белка ДНКазы. ДНКазу в моющей композиции по настоящему изобретению можно стабилизировать с применением общепринятых стабилизирующих средств, например, полиола, такого как пропиленгликоль или глицерин, сахара или сахароспирта, молочной кислоты, борной кислоты или производного борной кислоты, например, ароматического сложного эфира борной кислоты или производного фенилбороновой кислоты, например, 4-формилфенилбороновой кислоты, и при этом композицию можно составить, как описано, например, в WO 92/19709 и WO 92/19708.
Полипептид по настоящему изобретению также может быть включен в составы моющих средств, раскрытых в WO 97/07202, которая включена в данный документ с помощью ссылки.
Моющие композиции
В одном варианте осуществления настоящее изобретение направлено на моющие композиции, содержащие фермент по настоящему изобретению в комбинации с одним или несколькими дополнительными компонентами композиции для чистки. Выбор дополнительных компонентов находится в компетенции специалиста в данной области и предусматривает общепринятые ингредиенты, в том числе иллюстративные неограничивающие компоненты, изложенные ниже.
Средства для контроля запаха
Средства для контроля запаха представляют собой средства, которые уменьшают неприятный запах, исходящий от изделия, при этом средства для контроля запаха представляют собой средства, которые снижают, нейтрализуют или устраняют неприятный запах, исходящий от изделия, если средство для контроля запаха используется во время мытья или стирки изделия. Средство для контроля запаха отличается от ДНКазы.
Средства для контроля запаха по настоящему изобретению могут включать без ограничения HMP, летучие альдегиды, или циклодекстрины, или их смеси.
В общем, настоящие композиции для контроля неприятного запаха будут содержать одно или несколько средств для контроля запаха на уровне от приблизительно 0,001% до приблизительно 99, 99%, предпочтительно от приблизительно 0,002% до приблизительно 99,9% и более предпочтительно от приблизительно 0,005% до приблизительно 99% по весу композиции для контроля неприятного запаха. Если композиции представляют собой водные жидкие композиции (особенно неаэрозольные композиции) для распыления на поверхности, такие как ткани, то композиции будут предпочтительно содержать менее чем приблизительно 20%, предпочтительно менее чем приблизительно 10%, более предпочтительно менее чем приблизительно 5% по весу композиции средства для контроля запаха. Средство для контроля запаха служит для уменьшения или устранения неприятного запаха с поверхностей или объектов, обработанных композициями по настоящему изобретению. Средство для контроля запаха предпочтительно выбрано из группы, состоящей из незакомплексованных циклодекстринов; блокаторов запаха; реакционноспособных альдегидов; флаваноидов; цеолитов; активированного угля; а также их смесей.
Незакомплексованный циклодекстрин
Используемый в данном документе термин "незакомплексованный циклодекстрин" включает в себя любой из известных циклодекстринов в незакомплексованной форме, такой как незамещенные циклодекстрины, содержащие от шести до двенадцати глюкозных звеньев, в частности, альфа-циклодекстрин, бета-циклодекстрин, гамма-циклодекстрин и/или их производные, и/или их смеси. Альфа-циклодекстрин состоит из шести глюкозных звеньев, бета-циклодекстрин состоит из семи глюкозных звеньев, а гамма-циклодекстрин состоит из восьми глюкозных звеньев, расположенных в кольцах тороидальной формы. Конкретное связывание и конформация глюкозных звеньев придают циклодекстринам жесткую коническую молекулярную структуру с полыми внутренними пространствами определенного объема. "Подкладка" каждой внутренней полости образована атомами водорода и гликозидными мостиковыми атомами кислорода; таким образом, данная поверхность достаточно гидрофобна. Уникальная форма и физико-химические свойства данной полости обеспечивают молекулам циклодекстрина возможность поглощать (формировать комплексы включения с) органические молекулы или части органических молекул, которые могут поместиться в данную полость. В такую полость могут помещаться молекулы многих пахучих веществ, в том числе многие молекулы с неприятным запахом и молекулы ароматизирующих веществ. Таким образом, циклодекстрины, и особенно смеси циклодекстринов с полостями различных размеров, могут быть использованы для контроля запахов, вызванных широким спектром пахучих органических материалов, которые могут содержать или не содержать реакционноспособные функциональные группы. Комплексообразование между циклодекстрином и молекулами пахучих веществ происходит быстро, в присутствии воды. Тем не менее, степень образования комплекса зависит также от полярности абсорбированных молекул. В водном растворе сильно гидрофильные молекулы (те, которые являются в высокой степени растворимыми в воде) поглощаются лишь частично, если вообще поглощаются. Таким образом, циклодекстрин эффективно не образует комплекс с несколькими органическими аминами и кислотами с очень низким молекулярным весом, если они присутствуют на поверхностях при низких уровнях содержания. Полости внутри циклодекстрина в дезодорирующей композиции по настоящему изобретению при пребывании в растворе должны оставаться по существу незаполненными (циклодекстрин остается незакомплексованным) с тем, чтобы обеспечить возможность циклодекстрину абсорбировать различные молекулы запахов, когда раствор наносят на поверхность. Недериватизированный (нормальный) бета-циклодекстрин может присутствовать на уровне вплоть до предела его растворимости от приблизительно 1,85% (приблизительно 1,85 г в 100 г воды) в условиях эксплуатации при комнатной температуре. Предпочтительно применяемый в настоящем изобретении циклодекстрин является высокорастворимым в воде, например, альфа-циклодекстрин и/или его производные, гамма-циклодекстрин и/или его производные, производные бета-циклодекстринов и/или их смеси. Производные циклодекстрина состоят в основном из молекул, в которых некоторые из ОН-групп преобразуются в OR-группы. Производные циклодекстрина включают в себя например, производные, имеющие алкильные группы с короткой цепью, такие как метилированные циклодекстрины и этилированные циклодекстрины, где R представляет собой метильную или этильную группу; производные с гидроксиалкилзамещенными группами, такие как гидроксипропилциклодекстрины и/или гидроксиэтилциклодекстрины, где R представляет собой -CH2-CH-(OH)-CH3 или -CH2CH2-OH группу; разветвленные циклодекстрины, такие как мальтоза-связанные циклодекстрины; катионные циклодекстрины, такие как те, которые содержат 2-гидрокси-3-(диметиламино) пропиловый эфир, где R представляет собой CH2-CH (OH)-CH2-N-(CH3)2, который является катионным при низком значении рН; четвертичный аммоний, например, группы хлорида 2-гидрокси-3-(триметиламмоний) пропилового эфира, где R представляет собой CH2-CH-(OH)-CH2-N+(CH3) 3Cl-; анионные циклодекстрины, такие как карбоксиметилциклодекстрины, циклодекстринсульфаты и циклодекстринсукцинилаты; амфотерные циклодекстрины, такие как карбоксиметил/четвертичные аммониевые циклодекстрины; циклодекстрины, где по меньшей мере одно глюкопиранозное звено имеет 3-6-ангидро-цикломальто-структуру, например, моно-3-6-ангидроциклодекстрины, как описано в "Optimal Performances with Minimal Chemical Modification of Cyclodextrins", F. Diedaini-Pilard and B. Perly, The 7th International Cyclodextrin Symposium Abstracts, апрель 1994 г., стр. 49; и их смеси. Другие производные циклодекстрина описаны в патентах США №№: 3426011, Parmerter et al., выданном 4 февраля 1969 г.; 3453257; 3453258; 3453259; а также 3453260, все под именем Parmerter et al. и все выданы 1 июля 1969 г.; 3459731, Gramera et al., выданном 5 августа 1969 г.; 3553191, Parmerter et al., выданном 5 января 1971 г.; 3565887, Parmerter et al., выданном 23 февраля 1971 г.; 4535152, Szejtli et al., выданном 13 августа 1985 г.; 4616008, Hirai et al., выданном 7 октября 1986 г.; 4678598, Ogino et al., выданном 7 июля 1987 г.; 4638058, Brandt et al., выданном 20 января 1987 г.; а также 4746734, Tsuchiyama et al., выданном 24 мая 1988 г. Другие подходящие для использования в настоящем изобретении производные циклодекстрина включают описанные в V. T. D'Souza and K. B. Lipkowitz, CHEMICAL REVIEWS: CYCLODEXTRINS, том. 98, № 5 (Американское химическое общество, июль/август 1998 г.).
Высокорастворимыми в воде циклодекстринами являются те, которые характеризуются растворимостью в воде по меньшей мере приблизительно 10 г в 100 мл воды при комнатной температуре, предпочтительно по меньшей мере приблизительно 20 г в 100 мл воды, более предпочтительно по меньшей мере приблизительно 25 г в 100 мл воды при комнатной температуре. При нанесении на поверхности, особенно ковровые поверхности, солюбилизированный, растворимый в воде циклодекстрин может проявлять более эффективную способность контролировать запах, чем нерастворимый в воде циклодекстрин.
Примерами предпочтительных водорастворимых производных циклодекстрина, пригодных для использования в настоящем изобретении, являются гидроксипропил-альфа-циклодекстрин, метилированный альфа-циклодекстрин, метилированный бета-циклодекстрин, гидроксиэтил бета-циклодекстрин и гидроксипропил бета-циклодекстрин. Производные гидроксиалкилциклодекстрина предпочтительно характеризуются степенью замещения от приблизительно 1 до приблизительно 14, более предпочтительно от приблизительно 1,5 до приблизительно 7, где общее количество OR-групп на циклодекстрин определяется как степень замещения. Производные метилированного циклодекстрина обычно характеризуются степенью замещения от приблизительно 1 до приблизительно 18, предпочтительно от приблизительно 3 до приблизительно 16. Известный метилированный бета-циклодекстрин представляет собой гептакис-2,6-ди-О-метил-циклодекстрин, широко известный как DIMEB, в котором каждое глюкозное звено имеет приблизительно 2 метильные группы со степенью замещения приблизительно 14. Предпочтительным, более коммерчески доступным метилированным бета-циклодекстрином является произвольно метилированный бета-циклодекстрин, общеизвестный как RAMEB, характеризующийся различными степенями замещения, как правило, приблизительно 12,6. RAMEB является более предпочтительным, чем DIMEB, поскольку DIMEB влияет на поверхностную активность предпочтительных поверхностно-активных веществ больше, чем RAMEB. Предпочтительные циклодекстрины доступны, например, от Cerestar USA, Inc. и Wacker Chemicals (США), Inc.
Кроме того, предпочтительно использовать смесь циклодекстринов. Такие смеси абсорбируют запахи более широко, путем комплексообразования с более широким диапазоном пахучих молекул, имеющих более широкий диапазон размеров молекул. Предпочтительно по меньшей мере часть циклодекстрина представляет собой альфа-циклодекстрин и его производные, гамма-циклодекстрин и его производные и/или дериватизированный бета-циклодекстрин, более предпочтительно представляет собой смесь альфа-циклодекстрина или производного альфа-циклодекстрина и дериватизированного бета-циклодекстрина, еще более предпочтительно представляет собой смесь дериватизированного альфа-циклодекстрина и дериватизированного бета-циклодекстрина, наиболее предпочтительно представляет собой смесь гидроксипропил-альфа-циклодекстрина и гидроксипропил-бета-циклодекстрина и/или смесь метилированного альфа-циклодекстрина и метилированного бета-циклодекстрина. Поскольку циклодекстрин, особенно в водных композициях, может быть главной питательной средой для некоторых микроорганизмов, то предпочтительно включать в состав описанный ниже водорастворимый консервант, который является эффективным для ингибирования и/или регулирования роста микроорганизмов с целью увеличения стабильности при хранении абсорбирующих запах водных растворов, содержащих водорастворимый циклодекстрин.
В качестве средства для контроля запаха для смягчения эффектов неприятных запахов могут быть использованы блокаторы запаха "Odor blockers".
В целях эффективности блокаторы запаха в норме должны присутствовать всегда. Если блокатор запаха испаряется до того, как источник запаха устранен, то вероятность контролировать запах уменьшается. Кроме того, блокаторы запаха могут проявлять склонность оказывать отрицательный эффект на эстетику, блокируя желаемые запахи, такие как отдушки. Неограничивающие примеры блокаторов запаха, пригодных в качестве средств для контроля запаха в композициях по настоящему изобретению, включают 4-циклогексил-4-метил-2-пентанон, 4-этилциклогексил метил кетон, 4-изопропилциклогексил метил кетон, циклогексил метил кетон, 3-метилциклогексил метил кетон, 4-трет-бутилциклогексил метил кетон, 2-метил-4-трет-бутилциклогексил метил кетон, 2-метил-5-изопропилциклогексил метил кетон, 4-метилциклогексил-изопропилкетон, 4-метилциклогексил-втор-бутилкетон, 4-метилциклогексил-изобутилкетон, 2,4-диметилциклогексил метил кетон, 2,3-диметилциклогексил метил кетон, 2,2-диметилциклогексил метил кетон, 3,3-диметилциклогексил метил кетон, 4,4-диметилциклогексил метил кетон, 3,3,5-триметилциклогексил метил кетон, 2,2,6-триметилциклогексил метил кетон, 1-циклогексил-L-этилформиат, 1-циклогексил-L-этилацетат, 1-циклогексил-L-этил-пропионат, 1-циклогексил-1-этил-изобутират, 1-циклогексил-L-этил-н-бутират, 1-циклогексил-L-пропилацетат, 1-циклогексил-L-пропил-н-бутират, L-циклогексил-2-метил-1-пропилацетат, 2-циклогексил-2-пропилацетат, 2-циклогексил-2-пропил-пропионат, 2-циклогексил-2-пропил-изобутират, 2-циклогексил-2-пропил-н-бутират, 5,5-диметил-1,3-циклогександион (димедон), 2,2-диметил-1,3-диоксан-4,6-дион (кислота Мельдрума), спиро [4. 5]-6,10-диокса-7,9-диоксодекан, спиро-[5. 5]-1,5-диокса-2,4-диоксоундекан, 2,2-гидроксиметил-1,3-диоксан-4,6-дион и 1,3-циклогексадион. Блокаторы запаха более подробно раскрыты в патентах США №№ 4009253; 4187251; 4719105; 5441727 и 5861371.
Реакционноспособные альдегиды
В качестве необязательного средства для контроля запаха могут быть использованы реакционноспособные альдегиды, как средство для контроля запаха с целью смягчения эффектов неприятных запахов. Неограничивающие примеры подходящих реакционноспособных альдегидов включают альдегиды класса I, альдегиды класса II и их смеси. Неограничивающие примеры альдегидов класса I включают анисовый альдегид, о-аллил-ванилин, бензальдегид, куминовый альдегид, этил-аубепин, этилванилин, гелиотропин, толилальдегид и ванилин. Неограничивающие примеры альдегидов класса II включают 3-(4'-трет-бутилфенил)пропаналь, 2-метил-3-(4'-трет-бутилфенил)пропаналь, 2-метил-3-(4'-изопропилфенил)пропаналь, 2,2-диметил-3-(4-этилфенил)пропаналь, коричный альдегид, а-амилкоричный альдегид, а-гексил-коричный альдегид. Данные реакционноспособные альдегиды более подробно описаны в патенте США №5676163.
Реакционноспособные альдегиды при их применении могут включать в себя комбинацию по меньшей мере двух альдегидов, с одним альдегидом, выбираемым из ациклических алифатических альдегидов, нетерпеновых алифатических альдегидов, нетерпеновых алициклических альдегидов, терпеновых альдегидов, алифатических альдегидов, замещенных ароматической группой, и бифункциональных альдегидов; а второй альдегид выбирают из альдегидов, обладающих альфа-ненасыщенностью в отношении альдегидной функции, конъюгированныхс ароматическим кольцом, а также альдегидов, в которых альдегидная группа расположена на ароматическом кольце. Такое сочетание
по меньшей мере двух альдегидов более подробно описывается в публикации Международной заявки на патент № WO 00/49120.
Термин "реакционноспособные альдегиды", используемый в данном документе, дополнительно охватывает дезодорирующие материалы, которые являются продуктами реакции (i) альдегида со спиртом, (ii) кетона со спиртом или (iii) альдегида с теми же или другими альдегидами. Такие дезодорирующие материалы могут представлять собой: (a) ацеталь или полуацеталь, полученные посредством взаимодействия альдегида с карбинолом; (b) кеталь или полукеталь, полученные посредством взаимодействия кетона с карбинолом; (c) циклический триацеталь или смешанный циклический триацеталь по меньшей мере двух альдегидов или смесь любых из данных ацеталей, полуацеталей, кеталей, полукеталей или циклических триацеталей. Такие дезодорирующие парфюмерные материалы описаны более подробно в публикации Международной заявки на патент № WO 01/07095.
Флаваноиды
В качестве средства для контроля запаха также могут быть использованы флаваноиды. Флаваноиды представляют собой соединения, основанные на Ca Q Q; каркасе флавана. Флаваноиды можно найти в типичных эфирных маслах. Такие масла включают эфирные масла, добываемые сухой перегонкой из хвойных деревьев и трав, таких как кедр, японский кипарис, кипарис японский, эвкалипт, сосна густоцветная, одуванчик, горец японский и герань, и могут содержать терпеновые материалы, такие как альфа-пинен, бета-пинен, мирцен, фенкон и камфен. Также включены экстракты из чайного листа. Описания таких материалов можно найти в JP 02284997 и JP 04030855.
Соли металлов
Средство для контроля запаха по настоящему изобретению может содержать соли металлов для обеспечения преимуществ контроля неприятного запаха. Соли металлов выбраны из группы, состоящей из солей меди, солей цинка и их смесей.
Предпочтительные соли цинка обладают свойствами для контроля неприятного запаха. Чаще всего применяется цинк из-за его свойства улучшать неприятный запах, например, в продуктах для ополаскивания рта, как это раскрыто в патентах США №№ 4325939 и 4469674. Высоко ионизованные и растворимые соли цинка, такие как хлорид цинка, обеспечивают лучший источник ионов цинка. Предпочтительные соли цинка выбирают из группы, состоящей из бората цинка, каприлата цинка, хлорида цинка, рицинолеата цинка, гептагидрата сульфата цинка, ундецилената цинка и их смесей.
Предпочтительно соли металлов представляют собой водорастворимые соли цинка, соли меди или их смеси и более предпочтительно соли цинка, особенно ZnC12. Такие соли предпочтительно присутствуют в настоящем изобретении в качестве средства для контроля запаха прежде всего, чтобы абсорбировать амин- и серосодержащие соединения. Серосодержащие материалы с низким молекулярным весом, например, сульфиды и меркаптаны, являются компонентами неприятных запахов многих типов, например, пищевых запахов (чеснок, лук), запаха тела/пота, запаха изо рта и т. д. Амины с низким молекулярным весом также являются компонентами многих неприятных запахов, например, пищевых запахов, запахов тела, мочи и т. д.
Соли цинка, если они применяются, можно объединять с анионным поверхностно-активным веществом, имеющим формулу R-(O-СН2-СН2)-Х-О-CH2COO-, где R представляет собой заместитель, являющийся жирным спиртом, или заместитель, являющийся алкиларилом, и Х составляет по меньшей мере 2. Такие анионные поверхностно-активные вещества могут выступать в качестве средства для контролируемого высвобождения солей цинка с целью улучшения свойств контроля неприятного запаха композиции. Такое сочетание солей цинка и анионного поверхностно-активного вещества более подробно описано в патенте США №6358469.
Соли цинка, если они используются, можно также объединять с карбонатом и/или бикарбонатом для улучшения свойств контроля неприятного запаха у композиции. Когда соли цинка объединяют с карбонатом и/или бикарбонатом, композиция предпочтительно дополнительно содержит стабилизирующий анион, выбранный из фосфатов, имеющих более одной (Р=O)-группы, и органических кислот, имеющих более чем одну кислотную функциональную группу. Такое сочетание солей цинка, карбоната и/или бикарбоната и стабилизирующих анионов более подробно описано в патенте США № 6015547.
Соли меди обладают некоторыми способностями для контроля неприятного запаха. См. патент США №3172817, Leupold, et al., в котором описаны дезодорирующие композиции для обработки одноразовых изделий, содержащие по меньшей мере практически нерастворимые в воде соли ацилацетона, в том числе соли меди и соли цинка. Если соли металлов добавляют в композицию по настоящему изобретению, то в качестве средства для контроля запаха они, как правило, присутствуют на уровне от приблизительно 0,001% до эффективного количества с тем, чтобы обеспечить насыщенный раствор соли, предпочтительно от приблизительно 0,002% до приблизительно 25%, более предпочтительно от приблизительно 0, 003% до приблизительно 8%, еще более предпочтительно от приблизительно 0,1% до приблизительно 5% по весу композиции.
Цеолиты
В данном документе средства для контроля запаха могут быть также цеолитами. Предпочтительный класс цеолитов характеризуется как "промежуточные" силикат/алюминат-цеолиты. Промежуточные цеолиты характеризуются мольным соотношением SiOx/A10z менее чем приблизительно 10. Предпочтительно мольное соотношение Si02/A102 находится в диапазоне от приблизительно 2 до приблизительно 10. Промежуточные цеолиты могут иметь преимущество перед "высшими" цеолитами. Промежуточные цеолиты имеют более высокое сродство к запахам аминного типа, они являются более эффективными по весу для абсорбции запаха, так как они имеют большую площадь поверхности, а также они более влаговыносливы и сохраняют больше способности абсорбировать запах в воде, чем высшие цеолиты. Широкое разнообразие промежуточных цеолитов, пригодных для использования в данном изобретении, являются коммерчески доступными как Valfor® CP301-68, Valfor® 300-63, Valfor® CP300-35 и Valfor®CP300-56, доступные от PQ Corporation, а также серии цеолитов CBV100® от Conteka.
Также предпочтительными являются цеолитные материалы, продаваемые под торговой маркой Absents® и Smellrite®, доступные от The Union Carbide Corporation и UOP. Такие материалы являются предпочтительными по сравнению с промежуточными цеолитами для контроля серосодержащих запахов, например, тиолов, меркаптанов. Если цеолиты используются в качестве средств для контроля запаха в композициях, которые должны распыляться на поверхностях, то цеолитный материал предпочтительно характеризуется размером частиц менее чем приблизительно 10 микрон и присутствует в композиции на уровне менее чем приблизительно 1% по весу композиции.
Активированный уголь
Активированный уголь представляет собой еще одно подходящее средство для контроля запаха для включения в композиции по настоящему изобретению. Углеродный материал, пригодный для использования в настоящем изобретении, представляет собой материал, хорошо известный в коммерческой практике в качестве абсорбента для органических молекул и/или для очистки воздуха. Часто такой углеродный материал называют "активированным" углем или "активированным" древесным углем.
Такой углерод доступен из коммерческих источников под торговыми названиями, такими как Calgon-Type CPG®; Type PCB®; Type SGL®; Type CAL® и Type OL®.
Если активированный уголь используют в качестве средства для контроля запаха в композициях, которые должны распыляться на поверхностях, то активированный уголь предпочтительно характеризуется размером частиц менее чем приблизительно 10 микрон и присутствует в композиции на уровне менее чем приблизительно 1% по весу композиции.
В тех случаях, когда какой-либо описанный в данном документе материал в качестве средства для контроля запаха мог быть классифицирован также как еще один описанный в данном документе компонент для целей настоящего изобретения, такой материал должен быть классифицирован в качестве средства для контроля запаха.
Гидрофобно модифицированные полимеры для контроля неприятного запаха (НМР)
Средство для контроля запаха может представлять собой гидрофобно модифицированные полимеры для контроля неприятного запаха, как описано в WO 2012/097034.
Композиция по настоящему изобретению включает в себя гидрофобно модифицированный полимер для контроля неприятного запаха (HMP). НМР образован из полиаминополимера, имеющего первичную, вторичную и/или третичную аминогруппу, которая модифицирована гидрофобной группой, такой как алкил, алкенил, алкоксид или амид. Хотя аминогруппа была модифицирована, HMP имеет по крайней мере одну свободную и немодифицированную первичную, вторичную и/или третичную аминогруппу для вступления в реакцию с компонентами неприятных запахов. Не желая быть связанными теорией, гидрофобная модификация может увеличивать сродство с полимером в отношении гидрофобных запахов, что делает возможным взаимодействие между молекулами запахов и активными аминными участками. В свою очередь, HMP может улучшать широту эффективности устранения неприятного запаха.
НМР по настоящему изобретению имеет общую формулу (I):
P(R)x (I),
где:
Р представляет собой полиаминополимер;
R представляет собой гидрофобную группу С2-С26; и
х представляет собой общую степень замещения, которая составляет меньше чем 100% аминных участков на полимере.
1. Полиаминополимер
HMP может содержать полиаминополимерный каркас, который может быть либо линейным, либо циклическим. HMP может также содержать разветвленные полиаминовые цепи. Полиаминополимер имеет общую формулу (I1):
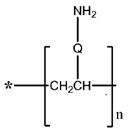 (I1),
(I1),
где Q представляет собой целое число, имеющее значения между 0 и 3.
Неограничивающие примеры полиаминполимеров включают поливиниламины (PVam), полиэтиленимины (PEIS), которые являются линейными или разветвленными, полиамидоамины (PAMam), полиаллиамины (PAam), полиэфирамины (PEam) или другие азотосодержащие полимеры, такие как лизин, или смеси таких азотосодержащих полимеров.
a. PVam
В одном варианте осуществления НМР включает в себя каркас PVam. PVam представляет собой линейный полимер с подвешенными первичными аминогруппами, непосредственно связанными с основной цепью чередующихся атомов углерода. PVam изготовлены в результате гидролиза поли(N-винилформамида) (PVNF), который приводит к отсутствию con-групп, как описывается следующей формулой (I1a):
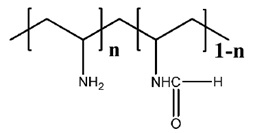 (I1a),
(I1a),
где n обозначает число от 0,1 до 0,99, в зависимости от степени гидролиза. Например, в 95% гидролизованном PVam n будет составлять 0,95, в то время как 5% полимера будет иметь винилформамидные звенья. PVam могут быть частично гидролизованными, это означает, что гидролизуется от 1% до 99%, альтернативно, от 30% до 99%, альтернативно, от 50% до 99%, альтернативно, от 70% до 99%, альтернативно, от 80% до 99%, альтернативно, от 85% до 99%, альтернативно, от 90% до 99%, альтернативно, от 95% до 99%, альтернативно, от 97% до 99%, альтернативно, 99% PVam. Было установлено, что высокая степень гидролиза PVam увеличивает способность образующегося полимера смягчать неприятные запахи. PVam, которые могут быть гидролизованы, могут иметь средний молекулярный вес (ММ) от 5000 до 350000. Подходящие гидролизованные PVam коммерчески доступны от BASF. Некоторые примеры включают Lupamin(TM) 9095, 9030, 5095 и 1595.
Такие гидролизованные PVam могут затем быть гидрофобно модифицированы. Гидрофобная модификация, как описано ниже, может дополнительно улучшать эффективность устранения неприятного запаха.
b. Полиалкиленимин/PEI
В другом варианте осуществления НМР включает в себя полиалкилениминовый каркас. Полиалкиленимины включают в себя PEI и полипропиленимины, а также алкиленимины C4-C12. PEI представляет собой подходящий полиалкиленимин. Химическая структура PEI следует простому принципу: одна функциональная аминогруппа и два атома углерода. PEI имеют следующую общую формулу (l1b):
-(CH2-CH2-NH)n- (l1b),
где n=10-105
PEI составляют большое семейство водорастворимых полиаминов с различным молекулярным весом, структурой и степенью модификации. Они могут действовать как слабые основания и могут проявлять катионный характер, в зависимости от степени протонирования, обусловленной значением рН.
PEI получают с помощью катионной полимеризации этиленимина с раскрытием цикла, как показано ниже.
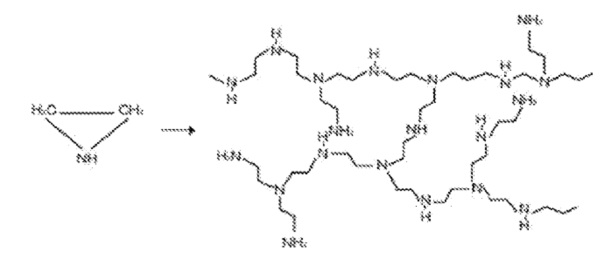
Как полагают, PEI должны быть сильно разветвленными, содержащими первичные, вторичные и третичные аминогруппы в соотношении приблизительно 1:2:1. PEI могут включать в себя первичные амины в диапазоне от приблизительно 30% до приблизительно 40%, альтернативно, от приблизительно 32% до приблизительно 38%, альтернативно, от приблизительно 34% до приблизительно 36%. PEI могут включать в себя вторичные амины в диапазоне от приблизительно 30% до приблизительно 40%, альтернативно, от приблизительно 32% до приблизительно 38%, альтернативно, от приблизительно 34% до приблизительно 36%. PEI могут включать в себя третичные амины в диапазоне от приблизительно 25% до приблизительно 35%, альтернативно, от приблизительно 27% до приблизительно 33%, альтернативно, от приблизительно 29% до приблизительно 31%.
Другие пути синтеза могут приводить к продуктам со структурой с модифицированными разветвленными цепями или даже к PEI с линейными цепями. Линейные PEI содержат аминные участки в основной цепи, в то время как разветвленные PEI содержат амины на основных и боковых цепях. Ниже приведен пример линейного PEI:
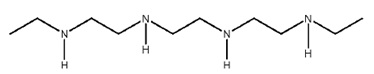
Композиция по настоящему изобретению может содержать PEI, имеющие MW от приблизительно 800 до приблизительно 2000000, альтернативно, от приблизительно 1000 до приблизительно 2000000, альтернативно, от приблизительно 1200 до приблизительно 25000, альтернативно, от приблизительно 1300 до приблизительно 25000, альтернативно, приблизительно 2000 до приблизительно 25000, альтернативно, от приблизительно 10000 до приблизительно 2000000, альтернативно, от приблизительно 25000 до приблизительно 2000000, альтернативно, приблизительно 25000.
В одном варианте осуществления PEI может иметь удельный вес 1,05 и/или аминовое число 18 (ммоль/г, твердое вещество). Для ясности, такой удельный вес и/или аминовое число PEI описывает PEI до того, как он модифицирован или добавлен как часть водной композиции. Специалистам в данной области техники будет понятно, что, например, первичные и вторичные аминогруппы могут вступать в реакцию с другими компонентами композиции.
Типичные PEI включают те, которые коммерчески доступны под торговым названием Lupasol® от BASF или торговым названием Epomine™ от Nippon Shokubia.
В некоторых вариантах осуществления менее чем 100% активных аминных участков замещены гидрофобными функциональными группами, альтернативно, от приблизительно 0,5% до приблизительно 90%, альтернативно, от приблизительно 0,5% до приблизительно 80%, альтернативно, от приблизительно 0,5% до приблизительно 70%, альтернативно, от приблизительно 0,5% до приблизительно 60%, альтернативно, от приблизительно 0,5% до приблизительно 50%, альтернативно, от приблизительно 0,5% до приблизительно 40%, альтернативно, от приблизительно 0,5% до приблизительно 35%, альтернативно, от приблизительно 0,5% до приблизительно 30%, альтернативно, от приблизительно 1% до приблизительно 30%, альтернативно, от приблизительно 1% до приблизительно 25%, альтернативно, от приблизительно 1% до приблизительно 20%, альтернативно, от приблизительно 5% до приблизительно 20%, альтернативно, от приблизительно 10% до приблизительно 30%, альтернативно, от приблизительно 20% до приблизительно 30%, альтернативно, приблизительно 20% активных аминных участков замещены гидрофобными функциональными группами. Если PEI имеет активные аминные участки, которые полностью замещены гидрофобными функциональными группами, то такой гидрофобно модифицированный PEI может не обладать активностью для контроля неприятного запаха.
c. PAMam
В другом варианте осуществления НМР включает в себя каркас PAMam. PAMam представляют собой полимеры, основная цепь которых содержит как аминофункциональные группы (NH), так и амидные функциональные группы (NH-, -C(O)). PAMam содержат также первичные аминогруппы и/или карбоксильные группы на концах полимерной цепи. Общая структура PAMam приведена ниже (l1e):
 (l1e).
(l1e).
d. PAam
В другом варианте осуществления НМР включает в себя каркас PAam. PAam получают в результате полимеризации аллиламина C3H5NH2. В отличие от PEI, они содержат только первичные аминогруппы, которые для PAAm показаны ниже (l1d):
 (l1d).
(l1d).
e. PEam
В еще одном варианте осуществления НМР включает в себя каркас PEam. PEam содержат первичные аминогруппы, прикрепленные к концу полиэфирного каркаса. Полиэфирный каркас может быть на основе оксида пропилена (PO), оксида этилена (ЕО) или смешанным PO/EO. Общая формула для PEam показана ниже (l1e):
 (I1e),
(I1e),
R=H для (EO) или CH3 для (PO).
Эти так называемые моноамины, М-серии, коммерчески доступны от Hunstman под торговым наименованием моноамины Jeffamine®. В другом варианте осуществления НМР включает в себя каркас PEam, имеющий диамины, как показано ниже (I1f):
Диамины коммерчески доступны от Hunstman под торговым наименованием диамины Jeffamine <(R)> (например, серии D, ED и EDR). HMP может также включать в себя каркас PEam, имеющий триамины (например, триамин T-серии Jeffamine®).
2. Другие полимерные звенья
HMP могут включать в себя сополимер азотсодержащих полимеров, имеющих формулу (I2):
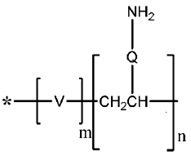 (I2),
(I2),
где Q представляет собой целое число, имеющее значения между 0 и 3, и V представляет собой сомономер. Неограничивающие примеры (I2) немодифицированных полимеров включают виниламиды, винилпирролидон, винилимидазол, сложные виниловые эфиры, виниловые спирты и их смеси.
3. Гидрофобные группы
Гидрофобная группа HMP может быть линейной, разветвленной или представлять собой циклический алкил, гидроксиалкил, алкенил, гидроксиалкенил, алкилкарбоксил, алкилоксид, алкандиил, амид или арил. В некоторых вариантах осуществления гидрофобная группа представляет собой С2-С26, альтернативно, C2-С12, альтернативно, C2-C10, альтернативно, C4-C10, альтернативно, С16-С26, альтернативно, С6. Там, где циклодекстрин включен в состав, может быть желательным использовать HMP, который был модифицирован С2-C10 алкильной группой, альтернативно, С16-С26 алкильной группой, альтернативно, C6 алкильной группой, поскольку такие алкильные группы являются совместимыми с циклодекстринами.
4. Гидрофобная модификация
Полиаминовые каркасы гидрофобно модифицированы таким образом, что по меньшей мере один атом азота полиаминовой цепи, альтернативно, каждый атом азота, в дальнейшем описан в отношении звена, которое является замещенным, кватернизованным, окисленным, или их комбинации.
Существует много способов гидрофобно модифицировать полиаминополимеры. Как правило, модификация является однонаправленной на первичные, вторичные и/или третичные амины полимера. С помощью осуществления реакции каркаса немодифицированного полиамина с соответствующими реагентами, его можно приводить в состояние гидрофобного полиаминополимера, увеличивая таким образом эффективность устранения неприятного запаха. Ниже приведены неограничивающие примеры способов получения HMP, раскрытых в данном документе.
а. Алкоксилирование
Реакция полиаминополимера с эпоксидом, содержащим углеводороды (R), приводит к замене одного или нескольких азотных фрагментов на полимере:
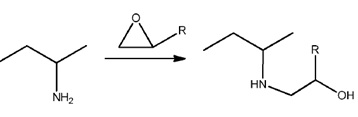
где R > C2.
Неограничивающие примеры таких углеводородов включают цепь С2-С26, которая является замещенной или незамещенной, разветвленной или неразветвленной. Например, в результате реакции додеценоксида с полимером PEI получают раскрытый в данном документе С6-HMP, имеющий структуру, показанную ниже:
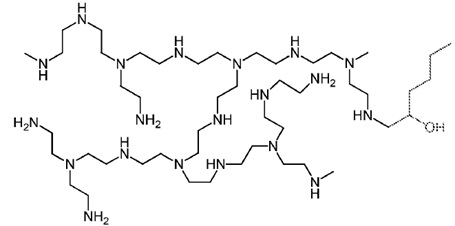
Альтернативно, можно модифицировать основной полимер с помощью осуществления реакции вначале с ЕО, а затем закончить алкилированием. Дополнительные модификации могут включать также покрытие модифицированного полимера ЕО группами, если растворимость в воде является более желательной. Альтернативно, гидроксильные группы могут быть в дальнейшем замещены с помощью осуществления реакции алкоксилированных полимеров, как описано в подпункте c ниже.
b. Амидирование
Реакция полиаминовых полимеров с амид-образующими реагентами, такими как ангидриды, лактоны, изоцианаты или карбоновые кислоты, приводит к замещению одного или нескольких фрагментов азота на полимере, придавая гидрофобный характер. До начала амидирования можно начинать с частичного замещения аминных участков на EO или PO, а затем осуществлять амидирование на остальных аминных фрагментах. Реакция ангидридов с полиаминополимерами приводит к образованию амидных звеньев полимера с помощью частичного замещения участков первичных/вторичных аминов. Неограничивающие примеры включают нециклические ангидриды карбоновых кислот, такие как уксусный ангидрид, или циклические ангидриды карбоновых кислот, такие как малеиновый ангидрид, янтарный ангидрид или фталевый ангидрид. Например, взаимодействие полиамина с уксусным ангидридом вводит в полимер амидные звенья:
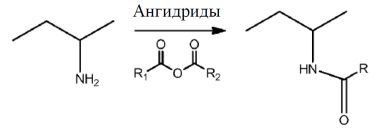
где R > C2.
С другой стороны, реакция полиаминополимера с циклическими ангидридами вводит в полимер звенья амидных кислот.
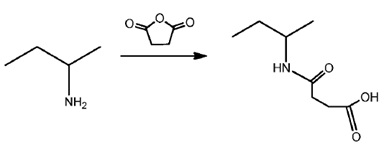
Большее количество гидрофобно модифицированных производных могут быть получены с помощью циклических ангидридов, таких как алкиленянтарные ангидриды, додеценилянтарные ангидриды или полиизобутанянтарные ангидриды:
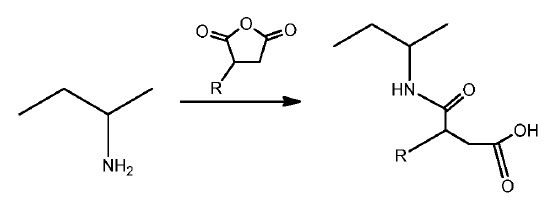
где R > C2.
Полиаминополимеры, содержащие гидроксил-концевые полиамидные звенья, могут быть получены с помощью осуществления реакции полимеров с лактонами. Использование более гидрофобных алкилзамещенных лактонов может придавать больше гидрофобности. Необязательно, гидроксил-концевые группы могут быть дополнительно замещены функциональными группами, как описано в подпункте с ниже.
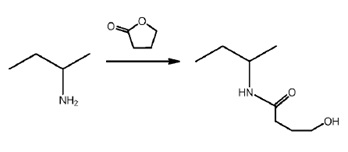
Взаимодействия изоцианата с полиаминополимерами приводят к образованию производных мочевины, показанных ниже:
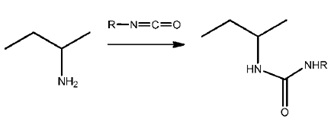
где R > C2.
с. Алкоксилирование с последующим замещением гидроксильных групп
Дополнительные функциональные группы могут быть ковалентно связаны с ОН-группой на алкоксилированных полиаминополимерах ("х" в формуле (I)). Это может быть достигнуто с помощью последующего осуществления реакции алкоксилированных полимеров с бифункциональными соединениями, такими как эпигалоидогидрины, такие как эпихлоргидрин, галиды 2-гало-кислоты, изоцианаты или диизоцианаты, такие как триметилгексан-диизоцианат или циклические ангидриды карбоновых кислот, такие как малеиновый ангидрид или фталевый ангидрид. Например, реакция алкоксилированного PEI с изоцианатам и приводит к получению:
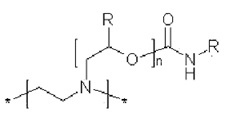
где R > C2.
Продукты реакции алкоксилированного PEI и производного алк(ен)илянтарных ангидридов:
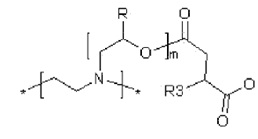
где R > C2.
Все такие HMP, раскрытые в данном документе, могут быть дополнительно ограничены гидрофильными группами, такими как EO, для придания растворимости в воде, при необходимости.
В некоторых вариантах осуществления от приблизительно 0,5% до приблизительно 90% аминогрупп во всем немодифицированном полиаминополимере могут быть замещены гидрофобной группой, альтернативно, от приблизительно 0,5% до приблизительно 80%, альтернативно, от приблизительно 0,5% до приблизительно 70%, альтернативно, от приблизительно 0,5% до приблизительно 60%, альтернативно, от приблизительно 0,5% до приблизительно 50%, альтернативно, от приблизительно 0,5% до приблизительно 40%, альтернативно, от приблизительно 0,5% до приблизительно 35%, альтернативно, от приблизительно 0,5% до приблизительно 30%, альтернативно, от приблизительно 1% до приблизительно 30%, альтернативно, от приблизительно 1% до приблизительно 25%, альтернативно, от приблизительно 1% до приблизительно 20%, альтернативно, от приблизительно 5% до приблизительно 20%, альтернативно, от приблизительно 10% до приблизительно 30%, альтернативно, от приблизительно 20% до приблизительно 30%, альтернативно, приблизительно 20% аминогрупп во всем немодифицированном полиаминополимере могут быть замещены гидрофобной группой. Уровень замещения аминных звеньев может быть ниже чем 0,01 мольного процента от теоретического максимума, где были заменены все первичные, вторичные и/или третичные аминные звенья. HMP для использования в настоящем изобретении могут иметь MW от приблизительно 150 до приблизительно 2*106, альтернативно, от приблизительно 400 до приблизительно 106, альтернативно от приблизительно 5000 до приблизительно 106. Полимеры для контроля неприятного запаха, пригодные для использования в настоящем изобретении, являются водорастворимыми или диспергируемыми. В некоторых вариантах осуществления первичные, вторичные и/или третичные амины полиаминных цепей частично замещены, придавая гидрофобность, при сохранении желаемой растворимости в воде. Минимальный коэффициент растворимости HMP может составлять приблизительно 2% (т. е. 2 г/100 мл воды). Подходящий НМР для водного состава освежителя тканей может характеризоваться процентом растворимости в воде, большим чем от приблизительно 0,5% до 100%, альтернативно, большим чем приблизительно 5%, альтернативно, большим чем приблизительно 10%, альтернативно, большим чем приблизительно 20%. Коэффициент растворимости в воде может быть определен с помощью теста на растворимость в воде на стр.13 WO 2012/097034.
Летучие альдегиды
Композиция для контроля неприятного запаха содержит летучие альдегиды, которые нейтрализуют неприятные запахи в паровой и/или жидкой фазе посредством химических реакций. Альдегиды, которые являются частично летучими, можно считать летучим альдегидом, используемым в данном документе. Летучие альдегиды могут вступать в реакцию с молекулами запахов на основе аминов, следуя пути образования основания шиффа. Летучие альдегиды могут также вступать в реакцию с молекулами запахов на основе серы, образуя тиоловые ацетали, гемитиоацетали и сложные тиоловые эфиры в паровой и/или жидкой фазе. Для данных летучих альдегидов в паровой и/или жидкой фазе может быть желательным, чтобы они не имели практически никакого негативного влияния на желаемый парфюмерный характер продукта.
Подходящие летучие альдегиды могут характеризоваться давлением паров (VP) в диапазоне от приблизительно 0,0001 торр до 100 торр, альтернативно, от приблизительно 0,0001 торр до приблизительно 10 торр, альтернативно, от приблизительно 0,001 торр до приблизительно 50 торр, альтернативно, от приблизительно 0,001 торр до приблизительно 20 торр, альтернативно, от приблизительно 0,001 торр до приблизительно 0,100 торр, альтернативно, от приблизительно 0,001 торр до 0,06 торр, альтернативно, от приблизительно 0,001 торр до 0,03 торр, альтернативно, от приблизительно 0,005 торр до приблизительно 20 торр, альтернативно, от приблизительно 0,01 торр до приблизительно 20 торр, альтернативно, от приблизительно 0,01 торр до приблизительно 15 торр, альтернативно, от приблизительно 0,01 торр до приблизительно 10 торр, альтернативно, от приблизительно 0,05 торр до приблизительно 10 торр, измеренным при 25°C. Летучие альдегиды могут также характеризоваться определенной температурой кипения (B.P.) и коэффициентом распределения октанол/вода (P). В.Р., упоминаемый в данном документе, измеряется при нормальном стандартном давлении 760 мм рт. ст. В.Р. многих летучих альдегидов приведены при стандартных 760 мм рт.ст., например, "Perfume and Flavor Chemicals (Aroma Chemicals)", написанный и опубликованный Steffen Arctander, 1969 г.
Коэффициент распределения октанол/вода летучего альдегида представляет собой соотношение между его равновесной концентрацией в октаноле и в воде. Коэффициенты распределения летучих альдегидов, используемых в композиции для контроля неприятного запаха, для большего удобства могут быть приведены в виде их десятичного логарифма, logP. Значения logP многих летучих альдегидов опубликованы. См., например, базу данных Pomona92, доступную от Daylight Chemical Information Systems, Inc. (Daylight CIS), Ирвин, Калифорния. Однако значения logP наиболее удобно рассчитывать с помощью программы "CLOGP", также доступной от Daylight CIS. Данная программа также регистрирует экспериментальные значения logP, если они доступны в базе данных Pomona92. "Рассчитанные logP" (ClogP) определяются с помощью фрагментного подхода Хэнш и Лео (ср. A. Leo, in Comprehensive Medicinal Chemistry, Vol. 4, C. Hansch, P. G. Sammens, J. B. Taylor and C. A. Ramsden, Eds., p. 295, Pergamon Press, 1990). Фрагментный подход основан на химической структуре каждого летучего альдегида и учитывает количества и типы атомов, связность атомов и химическое связывание. Значения ClogP, которые являются наиболее надежными и широко используемыми оценками для данного физико-химического свойства, предпочтительно используют вместо экспериментальных значений logP при выборе летучих альдегидов для композиции для контроля неприятного запаха.
Значения ClogP могут быть определены в четыре группы, и летучие альдегиды могут быть выбраны из одной или нескольких таких групп. Первая группа содержит летучие альдегиды, которые характеризуются В.Р. приблизительно 250°C или менее и ClogP приблизительно 3 или менее. Вторая группа содержит летучие альдегиды, которые характеризуются В.Р. 250°C или менее и ClogP 3,0 или более. Третья группа содержит летучие альдегиды, которые характеризуются В.Р. 250°C или более и ClogP 3,0 или менее. Четвертая группа содержит летучие альдегиды, которые характеризуются В.Р. 250°C или более и ClogP 3,0 или более. Композиция для контроля неприятного запаха может содержать любую комбинацию летучих альдегидов из одной или нескольких групп ClogP.
В некоторых вариантах осуществления компонент для контроля неприятного запаха может содержать, по весу компонента для контроля неприятного запаха, от приблизительно 0% до приблизительно 30% летучих альдегидов из группы 1, альтернативно, приблизительно 25%; и/или от приблизительно 0% до приблизительно 10% летучих альдегидов из группы 2, альтернативно, приблизительно 10%; и/или от приблизительно 10% до приблизительно 30% летучих альдегидов из группы 3, альтернативно, приблизительно 30%; и/или от приблизительно 35% до приблизительно 60% летучих альдегидов из группы 4, альтернативно, приблизительно 35%.
Количество летучих альдегидов, которые могут быть составлены в освежающую композицию, может составлять от приблизительно 0,015% до приблизительно 1%, альтернативно, от приблизительно 0,01% до приблизительно 0,5%, альтернативно, от приблизительно 0,015% до приблизительно 0,3% по весу освежающей композиции.
Типичные летучие альдегиды, которые могут быть использованы в качестве компонента для контроля неприятного запаха, включают без ограничения адоксаль (2,6,10-триметил-9-ундеценаль), бургеональ (4-трет-бутилбензолпропиональдегид), лилестралис 33 (2-метил-4-трет-бутилфенил)пропанол), коричный альдегид, коричный альдегид (фенилпропеналь, 3-фенил-2-пропеналь), цитраль, гераниаль, нераль (диметилоктадиеналь, 3,7-диметил-2,6-октадиен-l-аль), циклаль С (2,4-диметил-3-циклогексен-l-карбальдегид), флоргидраль (3-(3-изопропилфенил)-бутиральдегид), цитронеллаль (3,7-диметил 6-октеналь), цималь, цикламенальдегид, циклозаль, лаймовый альдегид (альфа-метил-п-изопропилфенилпропилальдегид), метилнонилацетальдегид, альдегид С12 МНА (2-метил-l-ундеканаль), гидроксицитронеллаль, цитронеллальгидрат (7-гидрокси-3,7-диметил октан-l-аль), гелиональ (альфа-метил-3,4-(метилендиокси)-гидрокоричный альдегид, гидрокоричный альдегид (3-фенилпропаналь, 3-фенилпропиональдегид), интрелевен альдегид (ундец-10-ен-л-аль), лигустраль, триверталь (2,4-диметил-3-циклогексен-l-карбоксальдегид), жасморанж, сатинальдегид (2-метил-3-толилпропиональдегид, 4-диметилбензолпропаналь), лираль (4-(4-гидрокси-4-метилпентил)-3-циклогексен-l-карбоксальдегид), мелональ (2,6-диметил-5-гептеналь), метоксимелональ (6-метокси-2,6-диметилгептаналь), метоксициннамальдегид (транс-4-метоксициннамальдегид), мирак-альдегид изогексенил циклогексенил-карбоксальдегид, триферналь ((3-метил-4-фенилпропаналь, 3-фенилбутаналь), лилиаль, P.T. буциналь, лисмераль, бензолпропаналь (4-трет-бутил-альфа-метил-гидрокоричный альдегид), дупикаль, трициклодецилиденбутаналь (4-трицикло5210-2,6-децилиден-8-бутаналь), метафлер (1,2,3,4,5,6,7,8-октагидро-8,8-диметил-2-нафтальдегид), метилоктилацетальдегид, альдегид C-l l MOA (2-метилдека-l-аль), оницидаль (2,6,10-триметил-5,9-ундекадиен-l-аль), цитронеллилоксиацетальдегид, альдегид ландыша 50 ((3,7-диметил-6-октенил) оксиацетальдегид), фенилацетальдегид, мефраналь (3-метил-5-фенилпентаналь), триплаль, вертоцитраль диметил тетрагидробензол альдегид (2,4-диметил-3-циклогексен-l-карбоксальдегид), 2-фенилпропиональдегид, гидротропальдегид, кантоксал, анизилпропаналь 4-метокси-альфа-метил бензолпропаналь (2-анизилиденпропаналь), циклемон А (1,2,3,4,5,6,7,8-октагидро-8,8-диметил-2-нафтальдегид) и прециклемон В (1-циклогексен-l-карбоксальдегид).
Кроме того, другие типичные альдегиды включают без ограничения ацетальдегид (этаналь), пентаналь, валеральдегид, амилальдегид, сцентеналь (октагидро-5-метокси-4,7-метан-lH-инден-2-карбоксальдегид), пропиональдегид (пропаналь), циклоцитраль, бета-циклоцитраль, (2,6,6-триметил-l-циклогексен-l-ацетальдегид), изоциклоцитраль (2,4,6-триметил-3-циклогексен-l-карбоксальдегид), изобутиральдегид, бутиральдегид, изовалериановый альдегид (3-метилбутиральдегид), метилбутиральдегид (2-метилбутиральдегид, 2-метилбутаналь), дигидроцитронеллаль (3,7-диметилоктан-l-аль), 2-этилбутиральдегид, 3-метил-2-бутеналь, 2-метилпентаналь, 2-метилвалеральдегид, гексеналь (2-гексеналь, транс-2-гексеналь), гептаналь, октаналь, нонаналь, деканаль, лауриновый альдегид, тридеканаль, 2-додеканаль, метилтиобутаналь, глутаральдегид, пентандиаль, глутаровый альдегид, гептеналь, цис- или транс-гептеналь, ундеценаль (2-,10-),2,4-октадиеналь, ноненаль (2-,6-), деценаль (2-,4-), 2,4-гексадиеналь, 2,4-декадиеналь, 2,6-нонадиеналь, октеналь, 2,6-диметил-5-гептеналь, 2-изопропил-5-метил-2-гексеналь, триферналь, бета-метилбензолпропаналь, 2,6,6-триметил-l-циклогексен-l-ацетальдегид, фенил-бутеналь (2-фенил-2-бутеналь), 2-метил-3-(п-изопропилфенил)-пропиональдегид, 3-(p-изопропилфенил)-пропиональдегид, п-толилацетальдегид (4-метилфенилацетальдегид), анисовый альдегид (п-метоксибензолальдегид), бензальдегид, вернальдегид (l-метил-4-(4-метилпентил)-3-циклогексенкарбальдегид), гелиотропин (пиперональ) 3,4-метилендиоксибензальдегид, альфа-амилкоричный альдегид, 2-пентил-3-фенилпропеноевый альдегид, ванилин (4-метокси-3-гидроксибензальдегид), этилванилин (3-этокси-4-гидроксибензальдегид), гексилкоричный альдегид, жасминальдегид Н (альфа-н-гексилкоричный альдегид), флоралозон (альфа, альфа-диметил-п-этилфенилпропаналь), азалия (п-метил-альфа-пентилциннамальдегид), метилциннамальдегид, альфа-метилциннамальдегид (2-метил-3-фенилпропеналь), альфа-гексилциннамальдегид (2-гексил-3-фенилпропеналь), салицилальдегид (2-гидроксибензальдегид), 4-этилбензальдегид, куминальдегид (4-изопропилбензальдегид), этоксибензальдегид, 2,4-диметилбензальдегид, вератральдегид (3,4-диметоксибензальдегид), сирингальдегид (3,5-диметокси-4-гидроксибензальдегид), катехальдегид (3,4-дигидроксибензальдегид), сафраналь (2,6,6-триметил-3-диен-метаналь), миртеналь (пин-2-ен-l-карбальдегид), периллальдегид l-4 (l-метилэтенил)-l-циклогексен-l-карбоксальдегид), 2,4-диметил-3-циклогексенкарбоксальдегид, 2-метил-2-пентеналь, 2-метилпентеналь, пирувальдегид, формилтрициклодекан, мандариновый альдегид, циклемакс, пиноацетальдегид, Corps Iris, мацеаль и Corps 4322.
В одном варианте осуществления компонент для контроля неприятного запаха включает смесь двух или более летучих альдегидов, выбранных из группы, состоящей из 2-этоксибензальдегида, 2-изопропил-5-метил-2-гексеналя, 5-метилфурфураля, 5-метилтиофенкарбоксальдегида, адоксаля, п-анисового альдегида, бензилальдегида, бургеналя, коричного альдегида, цималя, децилальдегида, цветочного супер (4,8-диметилдека-4,9-диеналя), флоргидраля, гелионаля, лауринового альдегида, лигустраля, лираля, мелоналя, о-анисового альдегида, пиноацетальдегида, P.T. буциналя, тиофенкарбоксальдегида, транс-4-деценаля, транс-транс-2,4-нонадиеналя, ундецилальдегида, а также их смесей.
Поверхностно-активные вещества
Моющая композиция может содержать одно или несколько поверхностно-активных веществ, которые могут быть анионными, и/или неионными, и/или полуполярными, и/или цвиттерионными, или их смесью. В конкретном варианте осуществления моющая композиция включает смесь одного или нескольких неионных поверхностно-активных веществ и одного или нескольких анионных поверхностно-активных веществ. Поверхностно-активное вещество(вещества) обычно присутствует в количестве от приблизительно 0,1% до 60% по весу, например, от приблизительно 1% до приблизительно 40%, или от приблизительно 3% до приблизительно 20%, или от приблизительно 3% до приблизительно 10%. Поверхностно-активное вещество(вещества) выбирают, исходя из необходимого применения для чистки, и при этом может предусматриваться любое общепринятое поверхностно-активное вещество(вещества), известное(известные) из уровня техники.
При их включении моющее средство обычно будет содержать от приблизительно 1% до приблизительно 40% по весу анионного поверхностно-активного вещества, например, от приблизительно 5% до приблизительно 30%, включая от приблизительно 5% до приблизительно 15%, или от приблизительно 15% до приблизительно 20%, или от приблизительно 20% до приблизительно 25% анионного поверхностно-активного вещества. Неограничивающие примеры анионных поверхностно-активных веществ включают сульфаты и сульфонаты, в частности, линейные алкилбензолсульфонаты (LAS), изомеры LAS, разветвленные алкилбензолсульфонаты (BABS), фенилалкансульфонаты, альфа-олефинсульфонаты (AOS), олефинсульфонаты, алкенсульфонаты, алкан-2,3-диилбис(сульфаты), гидроксиалкансульфонаты и дисульфонаты, алкилсульфаты (AS), такие как додецилсульфат натрия (SDS), сульфаты жирных спиртов (FAS), сульфаты первичных спиртов (PAS), эфирсульфаты спиртов (AES, или AEOS, или FES, также известные как этоксисульфаты спиртов или эфирсульфаты жирных спиртов); вторичные алкансульфонаты (SAS), сульфонаты парафина (PS), сульфонаты сложных эфиров, сложные эфиры глицерина и сульфонированных жирных кислот, метиловые сложные эфиры жирных альфа-сульфокислот (альфа-SFMe или SES), включая сульфонат сложного метилового эфира (MES), алкил- или алкенилянтарную кислоту, додеценил/тетрадеценилянтарную кислоту (DTSA), жирнокислотные производные аминокислот, сложные диэфиры и моноэфиры сульфоянтарной кислоты или соль жирных кислот (мыло) и их комбинации.
При их включении моющее средство обычно будет содержать от приблизительно 0,2% до приблизительно 40% по весу неионного поверхностно-активного вещества, например, от приблизительно 0,5% до приблизительно 30%, в частности, от приблизительно 1% до приблизительно 20%, от приблизительно 3% до приблизительно 10%, например, от приблизительно 3% до приблизительно 5%, от приблизительно 8% до приблизительно 12% или от приблизительно 10% до приблизительно 12%. Неограничивающие примеры неионных поверхностно-активных веществ включают этоксилаты спирта (AE или AEO), пропоксилаты спирта, пропоксилированные жирные спирты (PFA), алкоксилированные алкиловые сложные эфиры жирных кислот, например, этоксилированные и/или пропоксилированные алкиловые сложные эфиры жирных кислот, алкилфенолэтоксилаты (APE), нонилфенолэтоксилаты (NPE), алкилполигликозиды (APG), алкоксилированные амины, моноэтаноламиды жирных кислот (FAM), диэтаноламиды жирных кислот (FADA), этоксилированные моноэтаноламиды жирных кислот (EFAM), пропоксилированные моноэтаноламиды жирных кислот (PFAM), амиды жирных полигидроксиалкилкислот или N-ацил-N-алкил-производные глюкозамина (глюкамиды, GA или глюкамиды жирных кислот, FAGA), а также продукты, доступные под торговыми названиями SPAN и TWEEN и их комбинации.
При их включении моющее средство обычно будет содержать от приблизительно 0% до приблизительно 40% по весу полуполярного поверхностно-активного вещества. Неограничивающие примеры полуполярных поверхностно-активных веществ включают аминоксиды (AO), такие как алкилдиметиламиноксид, N-(кокоалкил)-N,N-диметиламиноксид и N-(таллоу-алкил)-N,N-бис(2-гидроксиэтил)аминоксид и их комбинации.
При их включении моющее средство обычно будет содержать от приблизительно 0% до приблизительно 40% по весу цвиттерионного поверхностно-активного вещества. Неограничивающие примеры цвиттерионных поверхностно-активных веществ включают бетаины, такие как алкилдиметилбетаины, сульфобетаины, и их комбинации.
Гидротропы
Гидротроп представляет собой соединение, которое солюбилизирует гидрофобные соединения в водных растворах (или, в противоположном случае, полярные соединения в неполярной среде). Как правило, гидротропы имеют как гидрофильный, так и гидрофобный характер (так называемые амфифильные свойства, которые известны у поверхностно-активных веществ), тем не менее, молекулярная структура гидротропов обычно не способствует спонтанной аутоагрегации, см., например, обзор Hodgdon and Kaler (2007), Current Opinion in Colloid & Interface Science 12: 121-128. Гидротропы не проявляют критическую концентрацию, выше которой происходит аутоагрегация, которая обнаруживается у поверхностно-активных веществ и липидов, образующих мицеллярные, ламеллярные или другие хорошо определенные мезофазы. Между тем, у многих гидротропов наблюдают процесс агрегации непрерывного типа, при этом размеры агрегатов растут по мере увеличения концентрации. Тем не менее, многие гидротропы изменяют фазовое поведение, устойчивость и коллоидные свойства систем, содержащих вещества полярного и неполярного характера, в том числе смеси воды, масла, поверхностно-активных веществ и полимеров. Гидротропы обычно применяют в отраслях, начиная от фармацевтики, личной гигиены, пищевой промышленности и заканчивая применениями в технике. Применение гидротропов в моющих композициях обеспечивает получение, например, более концентрированных составов поверхностно-активных веществ (например, в процессе компактизации жидких моющих средств с помощью устранения воды), не вызывая нежелательные явления, такие как разделение фаз или высокая вязкость.
Моющее средство может содержать 0-10% по весу, например, 0-5% по весу, например, от приблизительно 0,5 до приблизительно 5% или от приблизительно 3% до приблизительно 5% гидротропа. В моющих средствах можно применять любой гидротроп, известный из уровня техники. Неограничивающие примеры гидротропов включают бензолсульфонат натрия, п-толуолсульфонат натрия (STS), ксилолсульфонат натрия (SXS), кумолсульфонат натрия (SCS), цимолсульфонат натрия, аминоксиды, спирты и полигликолевые эфиры, гидроксинафтоат натрия, гидроксинафталинсульфонат натрия, этилгексилсульфат натрия и их комбинации.
Моющие компоненты и дополнительные моющие компоненты
Моющая композиция может содержать приблизительно 0-65% по весу, например, от приблизительно 5% до приблизительно 50% моющего компонента, или дополнительного моющего компонента, или их смеси в моющем средстве. Моющий компонент и/или дополнительный моющий компонент могут представлять собой, в частности, хелатирующее средство, которое образует растворимые в воде комплексы с Ca и Mg. Можно применять любой моющий компонент и/или дополнительный моющий компонент, известные из уровня техники. Неограничивающие примеры моющих компонентов включают цеолиты, дифосфаты (пирофосфаты), трифосфаты, такие как трифосфат натрия (STP или STPP), карбонаты, такие как карбонат натрия, растворимые силикаты, такие как метасиликат натрия, слоистые силикаты (например, SKS-6 от Hoechst), этаноламины, такие как 2-аминоэтан-1-ол (MEA), диэтаноламин (DEA, также известный как 2,2'-иминодиэтан-1-ол), триэтаноламин (TEA, также известный как 2,2',2"-нитрилoтриэтан-1-ол) и (карбоксиметил)инулин (CMI), а также их комбинации.
Моющая композиция также может содержать 0-50% по весу, например, от приблизительно 5% до приблизительно 30%, дополнительного моющего компонента моющего средства. Композиция моющего средства может включать дополнительный моющий компонент отдельно или в сочетании с моющим компонентом, например, моющим компонентом на основе цеолита. Неограничивающие примеры дополнительных компонентов моющих средств включают гомополимеры полиакрилатов или их сополимеры, такие как поли(акриловая кислота) (PAA) или сополимер акриловой кислоты/малеиновой кислоты (PAA/PMA). Дополнительные неограничивающие примеры включают цитрат, комплексообразователи, такие как аминокарбоксилаты, аминополикарбоксилаты, а также фосфонаты и алкил- или алкенилянтарную кислоту. Дополнительные конкретные примеры включают 2,2',2"-нитрилотриуксусную кислоту (NTA), этилендиаминтетрауксусную кислоту (EDTA), диэтилентриаминпентауксусную кислоту (DTPA), иминодиянтарную кислоту (IDS), этилендиамин-N,N'-диянтарную кислоту (EDDS), метилглициндиуксусную кислоту (MGDA), глутаминовую кислоту-N,N-диуксусную кислоту (GLDA), 1-гидроксиэтан-1,1-дифосфоновую кислоту (HEDP), этилендиаминтетра(метиленфосфоновую кислоту) (EDTMPA), диэтилентриаминпентакис(метиленфосфоновую кислоту) (DTMPA или DTPMPA), N-(2-гидроксиэтил)иминодиуксусную кислоту (EDG), аспарагиновую кислоту-N-моноуксусную кислоту (ASMA), аспарагиновую кислоту-N,N-диуксусную кислоту (ASDA), аспарагиновую кислоту-N-монопропионовую кислоту (ASMP), иминодиянтарную кислоту (IDA), N-(2-сульфометил)-аспарагиновую кислоту (SMAS), N-(2-сульфоэтил)-аспарагиновую кислоту (SEAS), N-(2-сульфометил)-глутаминовую кислоту (SMGL), N-(2-сульфоэтил)-глутаминовую кислоту (SEGL), N-метилиминодиуксусную кислоту (MIDA), α-аланин-N,N-диуксусную кислоту (α-ALDA), серин-N,N-диуксусную кислоту (SEDA), изосерин-N,N-диуксусную кислоту (ISDA), фенилаланин-N,N-диуксусную кислоту (PHDA), антраниловую кислоту-N,N-диуксусную кислоту (ANDA), сульфаниловую кислоту-N,N-диуксусную кислоту (SLDA), таурин-N,N-диуксусную кислоту (TUDA) и сульфометил-N,N-диуксусную кислоту (SMDA), N-(2-гидроксиэтил)-этилендиамин-N, N',N'-триуксусную кислоту (HEDTA), диэтанолглицин (DEG), диэтилентриамин-пента(метиленфосфоновую кислоту) (DTPMP), аминотрис(метиленфосфоновую кислоту) (ATMP), а также их комбинации и соли. Дополнительные типичные моющие компоненты и/или дополнительные моющие компоненты описаны, например, в WO 09/102854, US 5977053.
Отбеливающие системы
Моющее средство может содержать 0-30% по весу, например, от приблизительно 1% до приблизительно 20% отбеливающей системы. Для использования в моющих средствах можно применять любую отбеливающую систему, известную из уровня техники. Компоненты подходящей отбеливающей системы включают катализаторы отбелки, фотоотбеливатели, активаторы отбелки, источники пероксида водорода, такие как перкарбонат натрия, пербораты натрия и пероксид водорода-мочевина (1:1), предварительно образованные перкислоты и их смеси. Подходящие предварительно образованные перкислоты включают без ограничения пероксикарбоновые кислоты и соли, дипероксидикарбоновые кислоты, перимидные кислоты и соли, пероксимоносерные кислоты и соли, например, Oxone (R), и их смеси. Неограничивающие примеры отбеливающих систем включают отбеливающие системы на основе пероксида, которые могут содержать, например, неорганическую соль, в том числе соли щелочных металлов, такие как натриевые соли пербората (обычно моно- или тетрагидраты), перкарбоната, персульфата, перфосфата, персиликатные соли в комбинации с активатором отбелки, образующим перкислоту. Под выражением "активатор отбелки" в данном документе понимают соединение, которое реагирует с пероксидом водорода с образованием перкислоты посредством пергидролиза. Перкислота, полученная таким образом, представляет собой активированное отбеливающее вещество. Подходящие активаторы отбелки для применения согласно данному документу включают активаторы, принадлежащие к классу сложных эфиров, амидов, имидов или ангидридов. Подходящие примеры представляют собой тетраацетилэтилендиамин (TAED), натрия 4-[(3,5,5-триметилгексаноил)окси]бензол-1-сульфонат (ISONOBS), 4-(додеканоилокси)бензол-1-сульфонат (LOBS), 4-(деканоилокси)бензол-1-сульфонат, 4-(деканоилокси)бензоат (DOBS или DOBA), 4-(нонаноилокси)бензол-1-сульфонат (NOBS) и/или раскрытые в WO98/17767. Конкретное семейство активаторов отбелки, которое представляет интерес, раскрыто в EP624154, и наиболее предпочтительным в этом семействе является ацетилтриэтилцитрат (ATC). ATC или короткоцепочечный триглицерид, такой как триацетин, имеет преимущество, которое заключается в том, он является экологически безопасным. Кроме того, ацетилтриэтилцитрат и триацетин обладают хорошей гидролитической стабильностью в продукте при хранении и являются эффективными активаторами отбелки. Наконец, ATC является многофункциональным, поскольку цитрат, высвобождаемый при реакции пергидролиза, может действовать в качестве моющего компонента. Альтернативно, отбеливающая система может содержать пероксикислоты, например, амидного, имидного или сульфонового типа. Отбеливающая система может дополнительно содержать перкислоты, такие как 6-(фталимидо)пероксигексановая кислота (PAP). Отбеливающая система может дополнительно включать катализатор отбелки. В некоторых вариантах осуществления отбеливающий компонент может представлять собой органический катализатор, выбранный из группы, состоящей из органических катализаторов со следующими формулами:
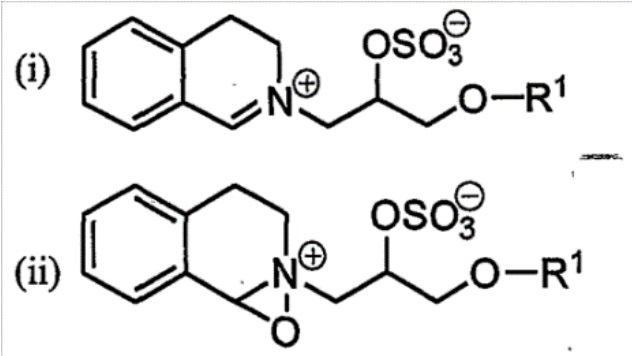
(iii) и их смесей;
где каждый R1 независимо представляет собой разветвленную алкильную группу, содержащую от 9 до 24 атомов углерода, или линейную алкильную группу, содержащую от 11 до 24 атомов углерода, предпочтительно каждый R1 независимо представляет собой разветвленную алкильную группу, содержащую от 9 до 18 атомов углерода, или линейную алкильную группу, содержащую от 11 до 18 атомов углерода, более предпочтительно каждый R1 независимо выбран из группы, состоящей из 2-пропилгептила, 2-бутилоктила, 2-пентилнонила, 2-гексилдецила, додецила, тетрадецила, гексадецила, октадецила, изононила, изодецила, изотридецила и изопентадецила. Другие иллюстративные отбеливающие системы описаны, например, в WO2007/087258, WO2007/087244, WO2007/087259, EP1867708 (витамин K) и WO2007/087242. Подходящие фотоотбеливатели могут, например, представлять собой сульфонированный цинк или фталоцианины алюминия.
Предпочтительно отбеливающий компонент содержит источник перкислоты в дополнение к катализатору отбелки, в частности, органическому катализатору отбелки. Источник перкислоты может быть выбран из (a) предварительно образованной перкислоты; (b) перкарбонатной, перборатной или персульфатной соли (источника пероксида водорода), предпочтительно в комбинации с активатором отбелки; и (c) фермента пергидролазы и сложного эфира для образования перкислоты in situ в присутствии воды на стадии обработки текстильного изделия.
Полимеры
Моющее средство может содержать 0-10% по весу, как например, 0,5-5%, 2-5%, 0,5-2% или 0,2-1% полимера. Для применения в моющих средствах можно использовать любой полимер, известный из уровня техники. Полимер может выполнять функцию дополнительного моющего компонента, который упомянут выше, или может препятствовать повторному осаждению, обеспечивать защиту волокон, отталкивание грязи, ингибирование переноса красителя, чистку от жира и/или антивспенивающие свойства. Некоторые полимеры могут иметь более чем одно из вышеупомянутых свойств и/или более чем один из нижеприведенных мотивов. Иллюстративные полимеры включают (карбоксиметил)целлюлозу (CMC), поли(виниловый спирт) (PVA), поли(винилпирролидон) (PVP), поли(этиленгликоль) или поли(этиленоксид) (PEG), этоксилированный поли(этиленимин), карбоксиметилинулин (CMI) и поликарбоксилаты, такие как PAA, PAA/PMA, полиаспарагиновую кислоту и сополимеры лаурилметакрилата/акриловой кислоты, гидрофобно модифицированную CMC (HM-CMC) и кремнийогранические соединения, сополимеры терефталевой кислоты и олигомерные гликоли, сополимеры поли(этилентерефталата) и поли(оксиэтилентерефталата) (PET-POET), PVP, поли(винилимидазол) (PVI), поли(винилпиридин-N-оксид) (PVPO или PVPNO) и поливинилпирролидон-винилимидазол (PVPVI). Дополнительные иллюстративные полимеры включают сульфированные поликарбоксилаты, полиэтиленоксид и полипропиленоксид (PEO-PPO) и этоксисульфат дикватерния. Другие иллюстративные полимеры раскрыты, например, в WO 2006/130575. Также предусматриваются соли вышеупомянутых полимеров.
Окрашивающие средства для тканей
Композиции моющего средства по настоящему изобретению могут также включать окрашивающие средства для тканей, такие как красители или пигменты, которые при введении в состав композиции моющего средства могут откладываться на ткани, при контакте указанной ткани с моющей жидкостью, содержащей указанные композиции моющего средства, и, следовательно, они изменяют тон указанной ткани с помощью поглощения/отражения видимого света. Флуоресцентные отбеливающие средства излучают по меньшей мере некоторое количество видимого света. Напротив, окрашивающие средства для тканей изменяют тон поверхности, поскольку они поглощают по меньшей мере часть видимой части спектра. Подходящие окрашивающие средства для тканей включают красители и конъюгаты краситель-глина, а также они могут включать пигменты. Подходящие красители включают низкомолекулярные красители и полимерные красители. Подходящие низкомолекулярные красители включают низкомолекулярные красители, выбранные из группы, состоящей из красителей, относящихся при классификации по цветовому индексу (C.I.) к Direct Blue, Direct Red, Direct Violet, Acid Blue, Acid Red, Acid Violet, Basic Blue, Basic Violet и Basic Red или их смеси, например, как описано в WO2005/03274, WO2005/03275, WO2005/03276 и EP1876226 (включены в данный документ с помощью ссылки). Моющая композиция предпочтительно содержит от приблизительно 0,00003 вес. % до приблизительно 0,2 вес. %, от приблизительно 0,00008 вес. % до приблизительно 0,05 вес. % или даже от приблизительно 0,0001 вес. % до приблизительно 0,04 вес. % окрашивающего средства для тканей. Композиция может содержать от 0,0001 вес. % до 0,2 вес. % окрашивающего средства для тканей, причем может быть особенно предпочтительным, если композиция присутствует в форме пакета с единичной дозой. Подходящие окрашивающие средства также раскрыты, например, в WO 2007/087257 и WO 2007/087243.
Ферменты
Моющая добавка, а также моющая композиция могут содержать один или несколько дополнительных ферментов, таких как протеаза, липаза, кутиназа, амилаза, карбогидраза, целлюлаза, пектиназа, маннаназа, арабиназа, галактаназа, ксиланаза, оксидаза, например, лакказа и/или пероксидаза.
В целом, свойства выбранного фермента(ферментов) должны быть совместимыми с выбранным моющим средством (т. е. оптимум pH, совместимость с другими ферментативными и неферментативными ингредиентами и т. д.), при этом фермент(ферменты) должен присутствовать в эффективных количествах.
Целлюлазы
Подходящие целлюлазы включают таковые бактериального или грибного происхождения. Предусматриваются химически модифицированные или полученные с помощью белковой инженерии мутанты. Подходящие целлюлазы включают целлюлазы из родов Bacillus, Pseudomonas, Humicola, Fusarium, Thielavia, Acremonium, например, грибные целлюлазы, полученные из Humicola insolens, Myceliophthora thermophila и Fusarium оксиsporum, раскрытые в US 4435307, US 5648263, US 5691178, US 5776757 и WO 89/09259.
Особенно подходящими целлюлазами являются щелочные или нейтральные целлюлазы, обладающие положительными эффектами сохранения цвета. Примерами таких целлюлаз являются целлюлазы, описанные в EP 0495257, EP 0531372, WO 96/11262, WO 96/29397, WO 98/08940. Другими примерами являются такие варианты целлюлаз, как описанные в WO 94/07998, EP 0531315, US 5457046, US 5686593, US 5763254, WO 95/24471, WO 98/12307 и WO99/001544.
Другими целлюлазами являются фермент ендо-бета-1,4-глюканаза, характеризующийся по меньшей мере 97% идентичностью аминокислотной последовательности, от положения 1 до положения 773, под SEQ ID NO:2 из WO 2002/099091, или семейство 44 ксилоглюканаз, в котором фермент ксилоглюканаза характеризуется по меньшей мере 60% идентичностью положениям 40-559 последовательности под SEQ ID NO: 2 из WO 2001/062903.
Коммерчески доступные целлюлазы включают Celluzyme™ и Carezyme™ (Novozymes A/S), Carezyme Premium™ (Novozymes A/S), Celluclean (Novozymes A/S), Celluclean Classic™ (Novozymes A/S), Cellusoft™ (Novozymes A/S), Whitezyme™ (Novozymes A/S), Clazinase™, и Puradax HA™ (Genencor International Inc.), и KAC-500(B)™ (Kao Corporation).
Протеазы
Подходящие протеазы включают протеазы бактериального, грибного, растительного, вирусного или животного происхождения, например, растительного или микробного происхождения. Микробное происхождение является предпочтительным. Предусматриваются химически модифицированные или полученные с помощью белковой инженерии мутанты. Это может быть щелочная протеаза, например, серин-протеаза или металлопротеаза. Серин-протеаза может быть, например, представителем семейства S1, таким как трипсин, или семейства S8, таким как субтилизин. Протеазы, относящиеся к металлопротеазам, могут, например, представлять собой термолизин, например, из семейства M4, или другую металлопротеазу, например, из семейств M5, M7 или M8.
Термин "субтилазы" относится к подгруппе серин-протеазы в соответствии с Siezen et al., Protein Engng. 4 (1991) 719-737 и Siezen et al. Protein Science 6 (1997) 501-523. Серин-протеазы представляют собой подгруппу протеаз, которая характеризуется наличием серина в активном сайте, который образует ковалентный аддукт с субстратом. Субтилазы могут быть разделены на 6 подразделов, т. е. семейство субтилизина, семейство термитазы, семейство протеиназы K, семейство пептидазы-лантибиотика, семейство кексина и семейство пиролизина.
Примерами субтилаз являются субтилазы, полученные из Bacillus, например, Bacillus lentus, B. alkalophilus, B. subtilis, B. amyloliquefaciens, Bacillus pumilus и Bacillus gibsonii, описанные в US7262042 и WO09/021867, и субтилизин lentus, субтилизин Novo, субтилизин Carlsberg, Bacillus licheniformis, субтилизин BPN', субтилизин 309, субтилизин 147 и субтилизин 168, описанные в WO89/06279, и протеаза PD138, описанная в (WO93/18140). Другими подходящими протеазами могут быть протеазы, описанные в WO 92/175177, WO 01/016285, WO 02/026024 и WO 02/016547. Примерами трипсин-подобных протеаз являются трипсин (например, свиного или бычьего происхождения) и протеаза Fusarium, описанная в WO 89/06270, WO 94/25583 и WO 05/040372, и химотрипсиновые протеазы, полученные из Cellumonas, описанные в WO 05/052161 и WO 05/052146.
Следующей предпочтительной протеазой является щелочная протеаза из Bacillus lentus DSM 5483, описанная, например, в WO 95/23221, и ее варианты, которые описаны в WO 92/21760, WO 95/23221, EP 1921147 и EP 1921148.
Примерами металлопротеаз являются нейтральная металлопротеаза, описанная в WO 07/044993 (Genencor Int.), например, металлопротеазы, полученные из Bacillus amyloliquefaciens.
Примерами пригодных протеаз являются варианты, описанные в WO 92/19729, WO 96/034946, WO 98/20115, WO 98/20116, WO 99/011768, WO 01/44452, WO 03/006602, WO 04/03186, WO 04/041979, WO 07/006305, WO 11/036263, WO 11/036264, в частности, варианты с заменами в одном или нескольких из следующих положений: 3, 4, 9, 15, 27, 36, 57, 68, 76, 87, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 106, 118, 120, 123, 128, 129, 130, 160, 167, 170, 194, 195, 199, 205, 206, 217, 218, 222, 224, 232, 235, 236, 245, 248, 252 и 274, при использовании BPN'-нумерации. Более предпочтительно варианты субтилазы могут содержать следующие мутации: S3T, V4I, S9R, A15T, K27R, *36D, V68A, N76D, N87S,R, *97E, A98S, S99G,D,A, S99AD, S101G,M,R S103A, V104I,Y,N, S106A, G118V,R, H120D,N, N123S, S128L, P129Q, S130A, G160D, Y167A, R170S, A194P, G195E, V199M, V205I, L217D, N218D, M222S, A232V, K235L, Q236H, Q245R, N252K, T274A (при использовании BPN'-нумерации).
Подходящие коммерчески доступные ферменты-протеазы включают в себя продаваемые под торговыми названиями Alcalase®, DuralaseTm, DurazymTm, Relase®, Relase® Ultra, Savinase®, Savinase® Ultra, Primase®, Polarzyme®, Kannase®, Liquanase®, Liquanase® Ultra, Ovozyme®, Coronase®, Coronase® Ultra, Neutrase®, Everlase® и Esperase® (Novozymes A/S), продаваемые под торговым названием Maxatase®, Maxacal®, Maxapem®, Purafect®, Purafect Prime®, Preferenzm, Purafect MA®, Purafect Ox®, Purafect OxP®, Puramax®, Properase®, EffectenzTm, FN2®, FN3®, FN4®, Excellase®, Opticlean® и Optimase® (Danisco/DuPont), Axapem™ (Gist-Brocases N.V.), BLAP (последовательность, представленная на фигуре 29 в US 5352604) и их варианты (Henkel AG) и KAP (субтилизин Bacillus alkalophilus) от Kao.
Липазы и кутиназы
Подходящие липазы и кутиназы включают таковые бактериального или грибного происхождения. Предусматриваются химически модифицированные или полученные с применением белковой инженерии мутантные ферменты. Примеры включают липазу из Thermomyces, например, из T. lanuginosus (ранее называемый Humicola lanuginosa), которая описана в EP 258068 и EP 305216, кутиназу из Humicola, например, H. insolens (WO 96/13580), липазу из штаммов Pseudomonas (некоторые из них сейчас переименованы в Burkholderia), например, P. alcaligenes или P. pseudoalcaligenes (EP 218272), P. cepacia (EP 331376), P. sp. штамм SD705 (WO 95/06720 и WO 96/27002), P. wisconsinensis (WO 96/12012), липазы GDSL-типа Streptomyces (WO 10/065455), кутиназу из Magnaporthe grisea (WO 10/107560), кутиназу из Pseudomonas mendocina (US 5389536), липазу из Thermobifida fusca (WO 11/084412), липазу Geobacillus stearothermophilus (WO 11/084417), липазу из Bacillus subtilis (WO 11/084599) и липазу из Streptomyces griseus (WO 11/150157) и S. pristinaespiralis (WO 12/137147).
Другими примерами являются варианты липаз, такие как описанные в EP 407225, WO 92/05249, WO 94/01541, WO 94/25578, WO 95/14783, WO 95/30744, WO 95/35381, WO 95/22615, WO 96/00292, WO 97/04079, WO 97/07202, WO 00/34450, WO 00/60063, WO 01/92502, WO 07/87508 и WO 09/109500.
Предпочтительные коммерческие продукты на основе липаз включают Lipolase™, Lipex™; Lipolex™ и Lipoclean™ (Novozymes A/S), Lumafast (первоначально от Genencor) и Lipomax (первоначально от Gist-Brocades).
Другими примерами являются липазы, иногда называемые ацилтрансферазами или пергидролазами, например, ацилтрансферазы с гомологией липазе А Candida antarctica (WO 10/111143), ацилтрансферазы из Mycobacterium smegmatis (WO 05/56782), пергидролазы из семейства CE 7 (WO 09/67279) и варианты пергидролазы M. smegmatis, в частности, вариант S54V, используемый в коммерческом продукте Gentle Power Bleach от Huntsman Textile Effects Pte Ltd (WO 10/100028).
Амилазы
Подходящие амилазы, которые можно применять совместно с ферментом по настоящему изобретению, могут представлять собой альфа-амилазу или глюкоамилазу и могут быть бактериального или грибного происхождения. Предусматриваются химически модифицированные или полученные с помощью белковой инженерии мутанты. Амилазы предусматривают, например, альфа-амилазы, полученные из Bacillus, например, специального штамма Bacillus licheniformis, описанного более детально в GB 1296839.
Подходящие амилазы включают амилазы под SEQ ID NO: 2 в WO 95/10603 или их варианты, обладающие 90% идентичностью последовательности под SEQ ID NO: 3. Предпочтительные варианты описаны в WO 94/02597, WO 94/18314, WO 97/43424 и SEQ ID NO: 4 из WO 99/019467, например, варианты с заменами в одном или нескольких из следующих положений: 15, 23, 105, 106, 124, 128, 133, 154, 156, 178, 179, 181, 188, 190, 197, 201, 202, 207, 208, 209, 211, 243, 264, 304, 305, 391, 408 и 444.
Различные подходящие амилазы включают амилазы под SEQ ID NO: 6 из WO 02/010355 или их варианты, характеризующиеся 90% идентичностью последовательности под SEQ ID NO: 6. Предпочтительными вариантами последовательности под SEQ ID NO: 6 являются варианты, характеризующиеся делецией в положениях 181 и 182 и замену в положении 193.
Другие амилазы, которые являются подходящими, представляют собой гибридную альфа-амилазу, содержащую остатки 1-33 альфа-амилазы, полученной из B. amyloliquefaciens, приведенные в SEQ ID NO: 6 из WO 2006/066594, и остатки 36-483 альфа-амилазы B. licheniformis, приведенные в SEQ ID NO: 4 из WO 2006/066594, или варианты, обладающие 90% идентичностью их последовательности. Предпочтительными вариантами данной гибридной альфа-амилазы являются варианты, имеющие замену, делецию или вставку в одном или нескольких из следующих положений: G48, T49, G107, H156, A181, N190, M197, I201, A209 и Q264. Наиболее предпочтительные варианты гибридной альфа-амилазы, содержащие остатки 1-33 альфа-амилазы, полученной из B. amyloliquefaciens, приведены под SEQ ID NO: 6 из WO 2006/066594, и остатки 36-483 из последовательности под SEQ ID NO: 4 представляют собой варианты, имеющие следующие замены:
M197T;
H156Y+A181T+N190F+A209V+Q264S или
G48A+T49I+G107A+H156Y+A181T+N190F+I201F+A209V+Q264S.
Следующие амилазы, которые являются подходящими, представляют собой амилазы под SEQ ID NO: 6 из WO 99/019467 или их варианты, характеризующиеся 90% идентичностью последовательности под SEQ ID NO: 6. Предпочтительными вариантами последовательности под SEQ ID NO: 6 являются варианты, имеющие замену, делецию или вставку в одном или нескольких из следующих положений: R181, G182, H183, G184, N195, I206, E212, E216 и K269. Особенно предпочтительными амилазами являются амилазы, имеющие делецию в положениях R181 и G182 или положениях H183 и G184.
Дополнительными амилазами, которые можно применять, являются амилазы под SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 2 или SEQ ID NO: 7 из WO 96/023873 или их варианты, обладающие 90% идентичностью последовательностям под SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3 или SEQ ID NO: 7. Предпочтительными вариантами последовательностей под SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3 или SEQ ID NO: 7 являются варианты, имеющие замену, делецию или вставку в одном или нескольких из следующих положений: 140, 181, 182, 183, 184, 195, 206, 212, 243, 260, 269, 304 и 476, с применением SEQ ID 2 из WO 96/023873 для нумерации. Более предпочтительными являются варианты которые характеризуются делецией в двух положениях, выбранных из 181, 182, 183 и 184, такие как 181 и 182, 182 и 183, или положения 183 и 184. Наиболее предпочтительными вариантами амилазы под SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 7 являются варианты, характеризуются делецией в положениях 183 и 184 и замену в одном или нескольких из положений 140, 195, 206, 243, 260, 304 и 476.
Другие амилазы, которые можно применять, представляют собой амилазы под SEQ ID NO: 2 из WO 08/153815, SEQ ID NO: 10 из WO 01/66712 или их варианты, характеризующиеся 90% идентичностью последовательности под SEQ ID NO: 2 из WO 08/153815 или характеризующиеся 90% идентичностью последовательности под SEQ ID NO: 10 из WO 01/66712. Предпочтительными вариантами последовательности под SEQ ID NO: 10 из WO 01/66712 являются варианты, имеющие замену, делецию или вставку в одном или нескольких из следующих положений: 176, 177, 178, 179, 190, 201, 207, 211 и 264.
Следующими подходящими амилазами являются амилазы из последовательности под SEQ ID NO: 2 из WO 09/061380 или их варианты, обладающие 90% идентичностью последовательности под SEQ ID NO: 2. Предпочтительными вариантами последовательности под SEQ ID NO: 2 являются варианты, имеющие усечение C-конца и/или замену, делецию или вставку в одном или нескольких из следующих положений: Q87, Q98, S125, N128, T131, T165, K178, R180, S181, T182, G183, M201, F202, N225, S243, N272, N282, Y305, R309, D319, Q320, Q359, K444 и G475. Более предпочтительными вариантами под SEQ ID NO: 2 являются варианты, имеющие замену в одном или нескольких из следующих положений: Q87E,R, Q98R, S125A, N128C, T131I, T165I, K178L, T182G, M201L, F202Y, N225E,R, N272E,R, S243Q,A,E,D, Y305R, R309A, Q320R, Q359E, K444E и G475K, и/или делецию в положении R180, и/или S181, или T182, и/или G183. Наиболее предпочтительными вариантами амилазы под SEQ ID NO: 2 являются варианты, имеющие следующие замены:
N128C+K178L+T182G+Y305R+G475K;
N128C+K178L+T182G+F202Y+Y305R+D319T+G475K;
S125A+N128C+K178L+T182G+Y305R+G475K или
S125A+N128C+T131I+T165I+K178L+T182G+Y305R+G475K, где варианты усечены по C-концу и необязательно дополнительно содержат замену в положении 243 и/или характеризуются делецией в положении 180 и/или положении 181.
Другие подходящие амилазы представляют собой альфа-амилазу под SEQ ID NO: 12 из WO 01/66712 или вариант, обладающий 90% идентичностью последовательности под SEQ ID NO: 12. Предпочтительными вариантами амилазы являются варианты, характеризующиеся заменой, делецией или вставкой в одном или нескольких из следующих положений последовательности под SEQ ID NO: 12 из WO 01/66712: R28, R118, N174; R181, G182, D183, G184, G186, W189, N195, M202, Y298, N299, K302, S303, N306, R310, N314; R320, H324, E345, Y396, R400, W439, R444, N445, K446, Q449, R458, N471, N484. Особенно предпочтительные амилазы включают варианты, характеризующиеся делецией в D183 и G184 и имеющие замены в R118K, N195F, R320K и R458K, и вариант, дополнительно имеющий замены в одном или нескольких положениях, выбранных из группы следующих: M9, G149, G182, G186, M202, T257, Y295, N299, M323, E345 и A339, причем наиболее предпочтительным является вариант, который дополнительно имеет замены во всех данных положениях.
Другими примерами являются варианты амилазы, например, варианты, описанные в WO 2011/098531, WO 2013/001078 и WO 2013/001087.
Имеющиеся в продаже амилазы представляют собой Duramyl™, Termamyl™, Fungamyl™, Stainzyme™, Stainzyme Plus™, Natalase™, Liquozyme X, и BAN™ (от Novozymes A/S), и Rapidase™, Purastar™/Effectenz™, Powerase и Preferenz S100 (от Genencor International Inc./DuPont).
Пероксидазы/оксидазы
Пероксидаза по настоящему изобретению представляет собой фермент пероксидазу, включенный в классификацию ферментов EC 1.11.1.7, как изложено Номенклатурным комитетом Международного союза биохимии и молекулярной биологии (IUBMB), или любой фрагмент, полученный из него, проявляющий пероксидазную активность.
Подходящие пероксидазы включают пероксидазы растительного, бактериологического или грибного происхождения. Предусматриваются химически модифицированные или полученные с помощью белковой инженерии мутанты. Примеры пригодных пероксидаз включают пероксидазы из Coprinopsis, например, из C. cinerea (EP 179,486), и их варианты, описанные в WO 93/24618, WO 95/10602 и WO 98/15257.
Пероксидаза по настоящему изобретению также включает фермент галогенпероксидазу, например, хлорпероксидазу, бромпероксидазу и соединения, проявляющие хлорпероксидазную или бромпероксидазную активность. Галогенпероксидазы классифицируют в соответствии с их специфичностью относительно ионов галогена. Хлорпероксидазы (E.C. 1.11.1.10) катализируют образование гипохлорита из хлорид-ионов.
В одном варианте осуществления галогенпероксидаза по настоящему изобретению представляет собой хлорпероксидазу. Предпочтительно галогенпероксидаза представляет собой ванадиевую галогенпероксидазу, т.е. содержащую ванадат галогенпероксидазу. В предпочтительном способе по настоящему изобретению содержащая ванадат галогенпероксидаза объединена с источником хлорид-иона.
Галогенпероксидазы были выделены из множества различных грибов, в частности, из группы грибов гифомицетов, таких как Caldariomyces, например, C. fumago, Alternaria, Curvularia, например, C. verruculosa, и C. inaequalis, Drechslera, Ulocladium и Botrytis.
Галогенпероксидазы также были выделены из бактерий, таких как Pseudomonas, например, P. pyrrocinia, и Streptomyces, например, S. aureofaciens.
В предпочтительном варианте осуществления галопероксидазу можно получать из Curvularia sp., в частности Curvularia verruculosa или Curvularia inaequalis, например C. inaequalis CBS 102.42, как описано в WO 95/27046; или C. verruculosa CBS 147.63, или C. verruculosa CBS 444.70, как описано в WO 97/04102; или из Drechslera hartlebii, как описано в WO 01/79459, Dendryphiella salina, как описано в WO 01/79458, Phaeotrichoconis crotalarie, как описано в WO 01/79461, или Geniculosporium sp., как описано в WO 01/79460.
Оксидаза по настоящему изобретению включает, в частности, любой фермент лакказу, включенный в классификацию ферментов EC 1.10.3.2, или любой фрагмент, полученный из него, проявляющий лакказную активность, или соединение, проявляющее подобную активность, например, катехолоксидазу (EC 1.10.3.1), o-аминофенолоксидазу (EC 1.10.3.4) или билирубиноксидазу (EC 1.3.3.5).
Предпочтительные ферменты лакказы представляют собой ферменты микробного происхождения. Ферменты могут быть получены из растений, бактерий или грибов (в том числе мицелиальных грибов и дрожжей).
Подходящие примеры ферментов из грибов включают лакказу, которую можно получить из штамма Aspergillus, Neurospora, например, N. crassa, Podospora, Botrytis, Collybia, Fomes, Lentinus, Pleurotus, Trametes, например, T. villosa и T. versicolor, Rhizoctonia, например, R. solani, Coprinopsis, например, C. cinerea, C. comatus, C. friesii и C. plicatilis, Psathyrella, например, P. condelleana, Panaeolus, например, P. papilionaceus, Myceliophthora, например, M. thermophila, Schytalidium, например, S. thermophilum, Polyporus, например, P. pinsitus, Phlebia, например, P. radiata (WO 92/01046), или Coriolus, например, C. hirsutus (JP 2238885).
Подходящие примеры ферментов из бактерий включают лакказу, которую можно получить из штамма Bacillus.
Лакказа, полученная из Coprinopsis или Myceliophthora, является предпочтительной; в частности, лакказа, полученная из Coprinopsis cinerea, как раскрыто в WO 97/08325; или из Myceliophthora thermophila, как раскрыто в WO 95/33836.
Фермент(ферменты) в моющем средстве может быть включен(включены) в моющую композицию с помощью добавления отдельных добавок, содержащих один или несколько ферментов, или с помощью добавления комбинированной добавки, содержащей все эти ферменты. Моющую добавку по данному изобретению, т. е. отдельную добавку или комбинированную добавку, можно составить, например, в виде гранулята, жидкости, взвеси и т. д. Предпочтительные составы моющих добавок представляют собой грануляты, в частности, непылящие грануляты, жидкости, в частности, стабилизированные жидкости, или взвеси.
Непылящие грануляты можно получать, например, как раскрыто в US 4106991 и 4661452, и на них можно наносить покрытие с применением способов, известных из уровня техники. Примерами восковидных покрывающих материалов являются поли(этиленоксидные) продукты (полиэтиленгликоль, PEG) со средним молярным весом 1000-20000; этоксилированные нонилфенолы, содержащие 16-50 этиленоксидных звеньев; этоксилированные жирные спирты, в которых спирт содержит от 12 до 20 атомов углерода и в которых присутствует от 15 до 80 этиленоксидных звеньев; жирные спирты; жирные кислоты; а также моно-, и ди-, и триглицериды жирных кислот. Примеры пленкообразующих покрывающих материалов, подходящих для нанесения с помощью методик с применением псевдоожиженного слоя, приведены в GB 1483591. Жидкие ферментные препараты можно, например, стабилизировать с помощью добавления полиола, такого как пропиленгликоль, сахара или сахароспирта, молочной кислоты или борной кислоты в соответствии с общепризнанными способами. Защищенные ферменты можно получать в соответствии со способом, раскрытым в EP 238216.
Другие материалы
Также в моющих средствах можно применять любые моющие компоненты, известные из уровня техники. Другие необязательные моющие компоненты включают антикоррозионные средства, средства, препятствующие усадке, средства, препятствующие повторному осаждению грязи, средства, препятствующие сминанию, бактерициды, связующие, ингибиторы коррозии, разрыхлители/разрыхляющие средства, красители, стабилизаторы ферментов (в том числе борная кислота, бораты, CMC и/или полиолы, например, пропиленгликоль), кондиционеры для тканей, в том числе глины, наполнители/технологические добавки, флуоресцентные отбеливающие средства/оптические отбеливатели, пенообразователи, регуляторы пенообразования (образования мыльной пены), отдушки, средства, суспендирующие грязь, смягчители, подавители образования мыльной пены, ингибиторы потускнения и средства, способствующие впитыванию влаги, либо отдельно, либо в комбинации. В моющих средствах можно применять любой ингредиент, известный из уровня техники. Выбор таких ингредиентов находится в компетенции специалиста в данной области.
Диспергирующие средства
Композиции моющего средства по настоящему изобретению могут также содержать диспергирующие средства. В частности, порошкообразные моющие средства могут содержать диспергирующие средства. Подходящие растворимые в воде органические материалы включают гомо- или сополимерные кислоты или их соли, в которых поликарбоновая кислота содержит по меньшей мере два карбоксильных радикала, отделенных друг от друга не более чем двумя атомами углерода. Подходящими диспергирующими средствами являются, например, описанные в Powdered Detergents, Surfactant science series volume 71, Marcel Dekker, Inc.
Средства, ингибирующие перенос красителя
Композиции моющего средства по настоящему изобретению могут также включать одно или несколько средств, ингибирующих перенос красителя. Подходящие полимерные средства, ингибирующие перенос красителя, включают без ограничения полимеры поливинилпирролидона, полимеры полиамин-N-оксида, сополимеры N-винилпирролидона и N-винилимидазола, поливинилоксазолидоны и поливинилимидазолы или их смеси. Если они присутствуют в представленной композиции, средства, ингибирующие перенос красителя, могут присутствовать при уровнях от приблизительно 0,0001% до приблизительно 10%, от приблизительно 0,01% до приблизительно 5% или даже от приблизительно 0,1% до приблизительно 3% по весу композиции.
Флуоресцентное отбеливающее средство
Моющие композиции по настоящему изобретению предпочтительно будут также содержать дополнительные компоненты, которые могут придавать очищаемому изделию цветовой оттенок, такие как флуоресцентное отбеливающее средство или оптические отбеливатели. Если он присутствует, то содержание отбеливателя предпочтительно составляет от приблизительно 0,01% до приблизительно 0,5%. В композиции по настоящему изобретению может применяться любое флуоресцентное отбеливающее средство, подходящее для применения в композиции моющего средства для стирки. Наиболее часто применяемые флуоресцентные отбеливающие средства представляют собой таковые, относящиеся к классам производных диаминостильбен-сульфоновой кислоты, диарилпиразолиновых производных и бисфенилдистириловых производных. Примеры флуоресцентных отбеливающих средств типа производных диаминостильбен-сульфоновой кислоты включают натриевые соли: 4,4'-бис-(2-диэтаноламино-4-анилино-s-триазин-6-иламино)стильбен-2,2'-дисульфонат, 4,4'-бис-(2,4-дианилино-s-триазин-6-иламино)стильбен-2.2'-дисульфонат, 4,4'-бис-(2-анилино-4-(N-метил-N-2-гидрокси-этиламино)-s-триазин-6-иламино)стильбен-2,2'-дисульфонат, 4,4'-бис-(4-фенил-1,2,3-триазол-2-ил)стильбен-2,2'-дисульфонат и натрия 5-(2H-нафто[1,2-d][1,2,3]триазол-2-ил)-2-[(E)-2-фенилвинил]бензолсульфонат. Предпочтительные флуоресцентные отбеливающие средства представляют собой Tinopal DMS и Tinopal CBS, поставляемые компанией Ciba-Geigy AG, Базель, Швейцария. Tinopal DMS представляет собой динатриевую соль 4,4'-бис-(2-морфолино-4 анилино-s-триазин-6-иламино)стильбен-2,2'-дисульфоната. Tinopal CBS представляет собой динатриевую соль 2,2'-бис-(фенил-стирил)дисульфоната. Предпочтительными также являются флуоресцентные отбеливающие средства, коммерчески доступные в виде Parawhite KX, поставляемого Paramount Minerals and Chemicals, Мумбай, Индия. Другие флуоресцентные вещества, подходящие для применения в настоящем изобретении, включают 1-3-диарилпиразолины и 7-алкиламинокумарины.
Количества подходящего флуоресцентного отбеливателя включают нижние значения количества от приблизительно 0,01, от 0,05, от приблизительно 0,1 или даже от приблизительно 0,2 вес. % до верхних значений количества 0,5 или даже 0,75 вес. %.
Грязеотталкивающие полимеры
Моющие композиции по настоящему изобретению могут также включать один или несколько грязеотталкивающих полимеров, которые способствуют устранению загрязнений с тканей, таких как хлопок и ткани на основе синтетического сложного полиэфира, в частности, для устранения гидрофобных загрязнений с тканей на основе сложного полиэфира. Грязеотталкивающими полимерами могут, например, являться неионные или анионные полимеры на основе терефталата, поливинилкапролактам и родственные сополимеры, виниловые привитые сополимеры, сложный полиэфир-полиамиды, см., например, главу 7 в Powdered Detergents, Surfactant science series volume 71, Marcel Dekker, Inc. Другим типом грязеотталкивающих полимеров являются амфифильные алкоксилированные полимеры для чистки от жира, содержащие сердцевинную структуру и множество алкоксилатных групп, прикрепленных к этой сердцевинной структуре. Сердцевинная структура может содержать полиалкилениминную структуру или полиалканоламинную структуру, которые подробно описаны в WO 2009/087523 (тем самым включены с помощью ссылки). Более того, случайные привитые сополимеры являются подходящими грязеотталкивающими полимерами. Подходящие привитые сополимеры более подробно описаны в WO 2007/138054, WO 2006/108856 и WO 2006/113314 (включенные в данный документ с помощью ссылки). Другими грязеотталкивающими полимерами являются замещенные полисахаридные структуры, особенно замещенные целлюлозные производные, такие как модифицированные производные целлюлозы, такие как описанные в EP 1867808 или WO 2003/040279 (обе из которых включены в данный документ с помощью ссылки). Подходящие целлюлозные полимеры включают целлюлозу, эфиры целлюлозы, сложные эфиры целлюлозы, амиды целлюлозы и их смеси. Подходящие целлюлозные полимеры включают анионно-модифицированную целлюлозу, неионно-модифицированную целлюлозу, катионно-модифицированную целлюлозу, цвиттерионно-модифицированную целлюлозу и их смеси. Подходящие целлюлозные полимеры включают метилцеллюлозу, карбоксиметилцеллюлозу, этилцеллюлозу, гидроксиэтилцеллюлозу, гидроксипропилметилцеллюлозу, сложный эфир карбоксиметилцеллюлозы и их смеси. Грязеотталкивающий полимер отличается от ДНКазы.
Средства против повторного осаждения
Моющие композиции по настоящему изобретению могут также включать одно или несколько средств против повторного осаждения, таких как карбоксиметилцеллюлоза (CMC), поливиниловый спирт (PVA), поливинилпирролидон (PVP), полиоксиэтилен и/или полиэтиленгликоль (PEG), гомополимеры акриловой кислоты, сополимеры акриловой кислоты и малеиновой кислоты и этоксилированные полиэтиленимины. Полимеры на основе целлюлозы, описанные как грязеотталкивающие полимеры выше, могут также функционировать в качестве средств против повторного осаждения. Полимер против повторного осаждения отличается от ДНКазы.
Средства, модифицирующие реологические свойства
Моющие композиции по настоящему изобретению также могут включать один или несколько средств, модифицирующих реологические свойства, структурообразующих средств или загустителей, в отличие от средств, уменьшающих вязкость. Средства, модифицирующие реологические свойства, выбраны из группы, состоящей из неполимерного кристаллического материала, гидрокси-функционализированных материалов, полимерных средств, модифицирующих реологические свойства, которые предусматривают характеристики истончения сдвига для водной жидкой матрицы жидкой моющей композиции. Реологические свойства и вязкость моющего средства можно модифицировать и регулировать с помощью способов, известных из предыдущего уровня техники, например, как показано в EP 2169040.
Другие подходящие вспомагательные материалы включают без ограничения средства, препятствующие усадке, средства, препятствующие сминанию, бактерициды, связующие средства, носители, красители, стабилизаторы ферментов, мягчители тканей, наполнители, регуляторы пенообразования, гидротропы, отдушки, пигменты, подавители образования мыльной пены, растворители и структурообразующие средства для жидких моющих средств и/или средства, обеспечивающие эластичность структуры.
Состав моющих продуктов
Моющая композиция по настоящему изобретению может быть представлена в любой удобной форме, например, бруска, гомогенной таблетки, таблетки с двумя или более слоями, пакета с одним или несколькими отделениями, обычного или уплотненного порошка, гранулы, пасты, геля или обычной, уплотненной или концентрированной жидкости.
Пакеты могут быть выполнены как с одним, так и с множеством отделений. Они могут иметь любую форму, вид и материал, который является подходящим для удерживания композиции, например, без возможности высвобождения композиции из пакета до контакта с водой. Пакет изготовлен из водорастворимой пленки, которая охватывает внутренний объем. Указанный внутренний объем может быть разделен на отделения пакета. Предпочтительными пленками являются полимерные материалы, предпочтительно полимеры, которые имеют форму пленки или листа. Предпочтительные полимеры, сополимеры или их производные выбраны из полиакрилатов и водорастворимых coполимеров акрилата, метилцеллюлозы, карбоксиметилцеллюлозы, декстрина натрия, этилцеллюлозы, гидроксиэтилцеллюлозы, гидроксипропилметилцеллюлозы, мальтодекстрина, полиметакрилатов, наиболее предпочтительно coполимеров поливинилового спирта и гидроксипропилметилцеллюлозы (HPMC). Предпочтительно количество полимера в пленке, например, PVA, составляет по меньшей мере приблизительно 60%. Предпочтительный средний молекулярный вес обычно составляет от приблизительно 20000 до приблизительно 150000. Пленки также могут состоять из смешанных композиций, содержащих гидролитически разлагаемые и водорастворимые смеси полимеров, например, полилактида и поливинилового спирта (известных под торговым названием M8630, продаваемых MonoSol LLC, Индиана, США), с пластификаторами, такими как глицерин, этиленглицерин, пропиленгликоль, сорбит и их смеси. Пакеты могут содержать твердую композицию для чистки белья путем стирки или часть компонентов и/или жидкую композицию для чистки или часть компонентов, разделенные водорастворимой пленкой. Отделение для жидких компонентов может отличаться по составу от отделений, содержащих твердые вещества: US 2009/0011970 A1.
Ингредиенты моющего средства могут быть отделены физически один от другого с помощью отделений в водорастворимых пакетах или в различных слоях таблеток. Таким образом можно избежать негативного взаимодействия между компонентами при хранении. Различные профили растворимости каждого из отделений также могут обеспечивать задержку растворения выбранных компонентов в моющем растворе.
Моющее средство в виде жидкости или геля, которое не является единичной дозой, может быть водным, как правило, содержащим от по меньшей мере 20% по весу и до 95% воды, например, до приблизительно 70% воды, до приблизительно 65% воды, до приблизительно 55% воды, до приблизительно 45% воды, до приблизительно 35% воды. Другие типы жидкостей, в том числе без ограничения алканолы, амины, диолы, эфиры и полиолы, могут быть включены в водную жидкость или гель. Моющее средство в виде водной жидкости или геля может содержать 0-30% органического растворителя.
Моющее средство в виде жидкости или геля может быть неводным.
Бруски мыла для стирки
ДНКазу по настоящему изобретению можно добавлять в бруски мыла для стирки и их можно применять для ручной стирки белья, тканей и/или текстильных изделий. Термин брусок мыла для стирки охватывает бруски средства для стирки, бруски мыла, бруски c комбинацией средств, бруски синтетического моющего средства и бруски моющего средства. Типы бруска обычно отличаются по типу поверхностно-активного вещества, которое они содержат, и при этом термин брусок мыла для стирки охватывает бруски, содержащие мыла из жирных кислот и/или синтетические мыла. Брусок мыла для стирки характеризуется физической формой, которая при комнатной температуре. представляет собой твердое вещество, а не жидкость, гель или порошок. Термин твердое вещество определяется как физическая форма, которая со временем не подвергается значительным изменениям, т. е. если твердый объект (например, брусок мыла для стирки) поместить в контейнер, этот твердый объект не изменяет форму с тем, чтобы заполнить контейнер, в который он помещен. Брусок представляет собой твердое вещество, как правило, в форме прямоугольного бруска, но может представлять собой твердое вещество другой формы, например, круглой или овальной.
Брусок мыла для стирки может содержать один или несколько дополнительных ферментов, ингибиторы протеазы, например, пептиды, содержащие альдегидные группы (или гидросульфитный аддукт, или полуацетальный аддукт), борную кислоту, борат, буру и/или производные фенилбороновой кислоты, например, 4-формилфенилбороновую кислоту, одно или несколько мыл или синтетических поверхностно-активных веществ, полиолы, например, глицерин, соединения для регулирования pH, например, жирные кислоты, лимонную кислоту, уксусную кислоту, и/или муравьиную кислоту, и/или соль одновалентного катиона и органического аниона, где одновалентный катион может представлять собой, например, Na+, K+ или NH4+, и при этом органический анион может представлять собой, например, формиат, ацетат, цитрат или лактат, таким образом, соль одновалентного катиона и органического аниона может представлять собой, например, формиат натрия.
Брусок мыла для стирки также может содержать комплексообразующие вещества, такие как EDTA и HEDP, отдушки и/или другой тип наполнителей, поверхностно-активные вещества, например, анионные синтетические поверхностно-активные вещества, моющие компоненты, полимерные грязеотталкивающие средства, комплексообразователи моющего средства, стабилизирующие средства, наполнители, красители, красящие вещества, ингибиторы переноса красителя, алкоксилированные поликарбонаты, подавители образования мыльной пены, структурообразующие средства, связующие средства, средства для выщелачивания, активаторы отбелки, средства для устранения глинистой грязи, средства против повторного осаждения, полимерные диспергирующие средства, отбеливатели, мягчители тканей, отдушки и/или другие соединения, известные из уровня техники.
Брусок мыла для стирки можно обрабатывать с помощью обычного оборудования для изготовления брусков мыла для стирки, например, без ограничения мешалок, шнек-прессов, например, двухступенчатого вакуумного шнек-пресса, экструдеров, устройств для резки, устройств для клеймения, туннельных охладителей и упаковочных устройств. Настоящее изобретение не ограничивается получением брусков мыла для стирки с помощью какого-либо одного способа. Предварительно полученную смесь по настоящему изобретению можно добавлять к мылу на различных стадиях способа. Например, можно получать предварительно полученную смесь, содержащую мыло, ДНКазу, необязательно один или несколько дополнительных ферментов, ингибитор протеазы и соль одновалентного катиона и органического аниона, и затем смесь обрабатывать с помощью шнек-пресса. ДНКазу и необязательные дополнительные ферменты можно добавлять одновременно с ингибитором протеазы, например, в жидкой форме. Кроме стадии смешивания и стадии обработки с помощью шнек-пресса, способ дополнительно может включать стадии размалывания, экструдирования, разрезания, штампования, охлаждения и/или упаковывания.
Состав фермента в комбинированной грануле
ДНКаза может быть составлена в виде гранулы, например, в виде комбинированной гранулы, которая объединяет один или несколько ферментов. Тогда каждый фермент будет присутствовать в большем количестве гранул, обеспечивая более однородное распределение ферментов в моющем средстве. Это также уменьшает физическое разделение различных ферментов в связи с различными размерами частиц. Способы получения многоферментных комбинированных гранулятов для производства моющих средств раскрыты в раскрытии IP.com IPCOM000200739D.
Другой пример состава ферментов для применения в комбинированных гранулятах раскрыт в WO 2013/188331, который относится к моющей композиции, содержащей (a) комбинированную гранулу с несколькими ферментами; (b) менее 10 вес. % цеолита (безводное основание); и (c) менее 10 вес. % фосфатной соли (безводное основание), где указанная комбинированная гранула с ферментом содержит от 10 до 98 вес. % увлажняющего компонента и композиция дополнительно содержит от 20 до 80 вес. % моющего увлажняющего компонента. WO 2013/188331 также относится к способу обработки и/или чистки поверхности, предпочтительно тканевой поверхности, включающему стадии (i) приведения указанной поверхности в контакт с моющей композицией, как заявляется и описано в данном документе в водном моющей жидкости, (ii) полоскания и/или высушивания поверхности.
Комбинированная гранула с несколькими ферментами может содержать ДНКазу и (a) один или несколько ферментов, выбранных из группы, состоящей из липаз для первой стирки, очищающих целлюлаз, ксилоглюканазы, пергидролаз, пероксидаз, липоксигеназ, лакказ и из смесей; и (b) один или несколько ферментов, выбранных из группы, состоящей из гемицеллюлаз, протеаз, целлюлаз для ухода, целлобиоздегидрогеназ, ксиланаз, фосфолипаз, эстераз, кутиназ, пектиназ, маннаназ, пектат-лиаз, кератиназ, редуктаз, оксидаз, фенолоксидаз, лигниназ, пуллуланаз, танназ, пентозаназ, лихеназ, глюканаз, арабинозидаз, гиалуронидаз, хондроитиназ, амилаз и их смесей.
Настоящее изобретение дополнительно кратко изложено в следующих пунктах.
1. Применение полипептида, обладающего ДНКазной активностью, для предотвращения или уменьшения повторного осаждения грязи и/или запаха на изделии в ходе процесса последующей чистки или стирки.
2. Применение по пункту 1, где полипептид, обладающий ДНКазной активностью, не присутствует в ходе процесса последующей чистки или стирки.
3. Применение по любому из предыдущих пунктов 1-2, где изделие представляет собой текстильное изделие или твердую поверхность.
4. Применение по любому из предыдущих пунктов для предотвращения или уменьшения прилипания грязи к изделию.
5. Применение по любому из предыдущих пунктов для поддержания или улучшения белизны изделия.
6. Применение по любому из предыдущих пунктов для предотвращения или уменьшения неприятного запаха, исходящего от изделия.
7. Применение по пункту 6, где неприятный запах вызван E-2-ноненалем.
8. Применение по любому из пунктов 6-7, где присутствие количества E-2-ноненаля на мокром изделии предотвращается, уменьшается или удаляется.
9. Применение по любому из пунктов 6-7, присутствие количества E-2-ноненаля на сухом изделии предотвращается, уменьшается или удаляется.
10. Применение по любому из предыдущих пунктов, где изделие приводят в контакт с жидким раствором, который содержит полипептид, обладающий ДНКазной активностью.
11. Применение по любому из предыдущих пунктов, где полипептид, обладающий ДНКазной активностью, распыляется на изделие.
12. Применение по пункту 10, где жидкий раствор представляет собой моющую жидкость.
13. Применение по любому из предыдущих пунктов, где полипептид, обладающий ДНКазной активностью, применяется для пропитывания изделия.
14. Применение по любому из предыдущих пунктов, где полипептид, обладающий ДНКазной активностью, применяется для чистки или стирки изделия по меньшей мере один раз перед процессом последующей чистки или стирки.
15. Применение по любому из предыдущих пунктов, где полипептид, обладающий ДНКазной активностью, применяется для чистки или стирки изделия по меньшей мере два раза, три раза, четыре раза, пять раз, шесть раз, семь раз, восемь раз, девять раз или десять раз перед процессом последующей чистки или стирки.
16. Применение по любому из предыдущих пунктов, где полипептид, обладающий ДНКазной активностью, представляет собой полипептид животного, растительного или микробного происхождения.
17. Применение по пункту 16, где полипептид характеризуется человеческим или животным происхождением.
18. Применение по пункту 16, где полипептид получен из фасоли золотистой.
19. Применение по пункту 16, где полипептид характеризуется бактериальным или грибным происхождением.
20. Применение по пункту 19, где полипептид характеризуется грибным происхождением или полипептид выбран из группы, состоящей из:
a) полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 2, полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 3, полипептида, характеризующегося по меньшей мере на 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 5, или полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 8;
b) полипептида, кодируемого полинуклеотидом, который гибридизируется в условиях низкой жесткости с
i. последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 1 или последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 4,
ii. ее последовательностью кДНК или
iii. последовательностью полной длины, комплементарной (i) или (ii);
c) полипептида, кодируемого полинуклеотидом, характеризующимся по меньшей мере 60% идентичностью последовательности, кодирующей зрелый полипептид, под SEQ ID NO: 1, или его последовательности кДНК, или полипептида, кодируемого полинуклеотидом, характеризующегося по меньшей мере 60% идентичностью последовательности, кодирующей зрелый полипептид, под SEQ ID NO: 4 или ее последовательности кДНК;
d) варианта зрелого полипептида под SEQ ID NO: 2, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях, варианта зрелого полипептида под SEQ ID NO: 3, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях, варианта зрелого полипептида под SEQ ID NO: 5, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях, или варианта зрелого полипептида под SEQ ID NO: 8, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях; и
e) фрагмента полипептида (a), (b), (c) или (d), который обладает ДНКазной активностью.
21. Применение по пункту 19, где полипептид характеризуется бактериальным происхождением и полипептид выбран из группы, состоящей из:
a) полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 6, или полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 7;
b) варианта зрелого полипептида под SEQ ID NO: 6, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях, или варианта зрелого полипептида под SEQ ID NO: 7, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях; и
c) фрагмента полипептида (a), (b), (c) или (d), который обладает ДНКазной активностью.
22. Применение по любому из пунктов 19-21, где полинуклеотид характеризуется по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100% идентичностью последовательности зрелого полипептида под SEQ ID NO: 2, зрелого полипептида под SEQ ID NO: 3, зрелого полипептида под SEQ ID NO: 5, зрелого полипептида под SEQ ID NO: 6, зрелого полипептида под SEQ ID NO: 7 или зрелого полипептида под SEQ ID NO: 8.
23. Полипептид по любому из пунктов 19-22, где полинуклеотид содержит или состоит из последовательности под SEQ ID NO: 2 или зрелого полипептида под SEQ ID NO: 2, полипептид содержит или состоит из последовательности под SEQ ID NO: 3 или зрелого полипептида под SEQ ID NO: 3, полипептид содержит или состоит из последовательности под SEQ ID NO: 5 или зрелого полипептида под SEQ ID NO: 5, полипептид содержит или состоит из последовательности под SEQ ID NO: 6 или зрелого полипептида под SEQ ID NO: 6, полипептид содержит или состоит из последовательности под SEQ ID NO: 7 или зрелого полипептида под SEQ ID NO: 7 или полипептид содержит или состоит из последовательности под SEQ ID NO: 8 или зрелого полипептида под SEQ ID NO: 8.
24. Применение по любому из пунктов 19-23, где зрелый полипептид представляет собой аминокислоты с 1 по 206 последовательности под SEQ ID NO: 2, аминокислоты с 1 по 206 последовательности под SEQ ID NO: 3, аминокислоты с 1 по 188 последовательности под SEQ ID NO: 5, аминокислоты с 1 по 110 последовательности под SEQ ID NO: 6 или аминокислоты с 1 по 109 последовательности под SEQ ID NO: 7 или аминокислоты с 1 по 206 последовательности под SEQ ID NO: 8.
25. Применение по любому из пунктов 19-24, где полипептид представляет собой вариант зрелого полипептида под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 6 или SEQ ID NO: 7, где вариант характеризуется заменой, делецией и/или вставкой в одном или нескольких положениях, или вариант зрелого полипептида под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 или SEQ ID NO: 8, который характеризуется заменой, делецией и/или вставкой в одном или нескольких положениях.
26. Применение по любому из пунктов 19-25, где полипептид представляет собой фрагмент последовательности под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 или SEQ ID NO: 8, где фрагмент обладает ДНКазной активностью.
27. Моющая композиция, содержащая полипептид, обладающий дезоксирибонуклеазной (ДНКазной) активностью, и поверхностно-активное вещество, где композиция соответствует по меньшей мере одному из а) или b):
а) композиция дополнительно содержит средство для контроля запаха и/или
b) поверхностно-активное вещество не является катионным поверхностно-активным веществом.
28. Композиция по пункту 27, где средство для контроля запаха выбрано из группы, состоящей из циклодекстринов и их смесей, блокаторов запаха, реакционноспособных альдегидов, флавоноидов, солей металлов, цеолитов, активированного угля, гидрофобно-модифицированных полимеров для контроля неприятного запаха (НМР), производных изотиазолинона, таких как бензизотиазолинон, и/или летучих альдегидов.
29. Композиция по любому из пунктов 27-28, где поверхностно-активное вещество представляет собой неионное поверхностно-активное вещество, анионное поверхностно-активное вещество, цвиттерионное поверхностно-активное вещество или полуполярное поверхностно-активное вещество.
30. Композиция по пункту 29, где поверхностно-активное вещество представляет собой анионное поверхностно-активное вещество, выбранное из группы, состоящей из сульфатов и сульфонатов, таких как линейные алкилбензолсульфонаты (LAS), изомеры LAS, разветвленные алкилбензолсульфонаты (BABS), фенилалкансульфонаты, альфа-олефинсульфонаты (AOS), олефинсульфонаты, алкенсульфонаты, алкан-2,3-диилбис(сульфаты), гидроксиалкансульфонаты и дисульфонаты, алкилсульфатов (AS), таких как додецилсульфат натрия (SDS), сульфаты жирных спиртов (FAS), сульфаты первичных спиртов (PAS), эфирсульфаты спиртов (AES или AEOS, или FES, также известные как этоксисульфаты спиртов или эфирсульфаты жирных спиртов), вторичных алкансульфонатов (SAS), сульфонатов парафина (PS), сульфонатов сложных эфиров, сложных эфиров глицерина и сульфонированных жирных кислот, метиловых сложных эфиров жирных альфа-сульфокислот (альфа-SFMe или SES), в том числе сульфоната сложного метилового эфира (MES), алкил- или алкенилянтарной кислоты, додеценил/тетрадеценил янтарной кислоты (DTSA), жирнокислотных производных аминокислот, сложных диэфиров и моноэфиров сульфоянтарной кислоты или солей жирных кислот (мыло), и их комбинаций.
31. Композиция по пункту 30, где количество анионного поверхностно-активного вещества составляет от приблизительно 1% до приблизительно 40% по весу, например, от приблизительно 5% до приблизительно 30%, включая от приблизительно 5% до приблизительно 15%, или от приблизительно 15% до приблизительно 20%, или от приблизительно 20% до приблизительно 25%.
32. Композиция по любому из пунктов 27-29, где поверхностно-активное вещество представляет собой неионное поверхностно-активное вещество, выбранное из группы, состоящей из этоксилатов спирта (AE или AEO), пропоксилатов спирта, пропоксилированных жирных спиртов (PFA), алкоксилированных алкиловых сложных эфиров жирных кислот, таких как этоксилированные и/или пропоксилированные алкиловые сложные эфиры жирных кислот, алкилфенолэтоксилаты (APE), нонилфенолэтоксилаты (NPE), алкилполигликозиды (APG), алкоксилированные амины, моноэтаноламиды жирных кислот (FAM), диэтаноламиды жирных кислот (FADA), этоксилированные моноэтаноламиды жирных кислот (EFAM), пропоксилированные моноэтаноламиды жирных кислот (PFAM), амиды жирных полигидроксиалкилкислот или N-ацил-N-алкил-производные глюкозамина (глюкамиды, GA или глюкамиды жирных кислот, FAGA), SPAN™, TWEEN™, и их комбинаций.
33. Композиция по пункту 32, где количество неионного поверхностно-активного вещества составляет от приблизительно 0,2% до приблизительно 40% по весу неионного поверхностно-активного вещества, например, от приблизительно 0,5% до приблизительно 30%, в частности, от приблизительно 1% до приблизительно 20%, от приблизительно 3% до приблизительно 10%, например, от приблизительно 3% до приблизительно 5%, от приблизительно 8% до приблизительно 12% или от приблизительно 10% до приблизительно 12%.
34. Композиция по пункту 29, где поверхностно-активное вещество представляет собой полуполярное поверхностно-активное вещество, выбранное из группы, состоящей из аминоксидов (AO), таких как алкилдиметиламиноксид, N-(кокоалкил)-N,N-диметиламиноксид и N-(таллоу-алкил)-N,N-бис(2-гидроксиэтил)аминоксид, и их комбинаций.
35. Композиция по пункту 29, где поверхностно-активное вещество представляет собой цвиттерионное поверхностно-активное вещество, выбранное из группы, состоящей из бетаинов, таких как алкилдиметилбетаины, сульфобетаины.
36. Композиция по любому из предыдущих пунктов, относящихся к композиции, где поверхностно-активное вещество выбрано из группы, состоящей из этоксисульфата натрия на основе спирта, линейного алкилбензолсульфоната, натриевой соли жирной кислоты, алкилсульфата натрия, лаураминоксида, линейного алкилбензолсульфоната (MEA соль), линейного алкилбензолсульфоната (натриевая соль), этоксилата спирта.
37. Композиция по любому из предыдущих пунктов, относящихся к композиции, для предотвращения или уменьшения повторного осаждения грязи и/или запаха на изделии в ходе процесса последующей чистки или стирки.
38. Композиция по любому из предыдущих пунктов, относящихся к композиции, для предотвращения или уменьшения повторного осаждения грязи и/или запаха на изделии в ходе процесса последующей чистки или стирки, где полипептид, обладающий ДНКазной активностью, не применяется в ходе процесса последующей чистки или стирки.
39. Композиция по любому из предыдущих пунктов для предотвращения или уменьшения неприятного запаха.
40. Композиция по любому из предыдущих пунктов, относящихся к композиции, где композиция дополнительно включает моющие компоненты, флокулирующее вспомогательное средство, хелатирующие средства, ингибиторы переноса красителей, ферменты, стабилизаторы ферментов, ингибиторы ферментов, каталитические материалы, активаторы отбелки, пероксид водорода, источники пероксида водорода, предварительно образованные перкислоты, полимерные диспергирующие средства, средства для устранения/средства против повторного осаждения глинистой грязи, отбеливатели, подавители образования мыльной пены, красители, отдушки, средства, обеспечивающие эластичность, мягчители тканей, носители, гидротропы, моющие компоненты и дополнительные моющие компоненты, окрашивающие средства для тканей, противовспенивающие средства, диспергирующие средства, технологические добавки и/или пигменты.
41. Композиция по любому из предыдущих пунктов, относящихся к композиции, где композиция дополнительно содержит один или несколько ферментов, выбранных из группы, состоящей из протеаз, липаз, кутиназ, амилаз, карбогидраз, целлюлаз, пектиназ, маннаназ, арабиназ, галактаназ, ксиланаз и оксидаз.
42. Композиция по любому из предыдущих пунктов, относящихся к композиции, где полипептид, обладающий ДНКазной активностью, представляет собой полипептид животного, растительного или микробного происхождения.
43. Композиция по любому из предыдущих пунктов, относящихся к композиции, где полипептид характеризуется человеческим происхождением.
44. Композиция по любому из предыдущих пунктов, относящихся к композиции, где полипептид получен из фасоли золотистой.
45. Композиция по любому из предыдущих пунктов, относящихся к композиции, где полипептид характеризуется бактериальным или грибным происхождением.
46. Композиция по пункту 45, где полипептид характеризуется грибным происхождением и полипептид выбран из группы, состоящей из:
a) полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 2, полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 3, полипептида, характеризующегося по меньшей мере на 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 5, или полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 8;
b) полипептида, кодируемого полинуклеотидом, который гибридизируется в условиях низкой жесткости с
i. последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 1 или последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 4,
ii. ее последовательностью кДНК или
iii. последовательностью полной длины, комплементарной (i) или (ii);
c) полипептида, кодируемого полинуклеотидом, характеризующимся по меньшей мере 60% идентичностью последовательности, кодирующей зрелый полипептид, под SEQ ID NO: 1, или его последовательности кДНК, или полипептида, кодируемого полинуклеотидом, характеризующегося по меньшей мере 60% идентичностью последовательности, кодирующей зрелый полипептид, под SEQ ID NO: 4 или ее последовательности кДНК;
d) варианта зрелого полипептида под SEQ ID NO: 2, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях, варианта зрелого полипептида под SEQ ID NO: 3, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях, варианта зрелого полипептида под SEQ ID NO: 5, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях, или варианта зрелого полипептида под SEQ ID NO: 8, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях; и
e) фрагмента полипептида (a), (b), (c) или (d), который обладает ДНКазной активностью.
47. Композиция по пункту 45, где полипептид характеризуется бактериальным происхождением и полипептид выбран из группы, состоящей из:
a) полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 6, или полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 7;
b) варианта зрелого полипептида под SEQ ID NO: 6, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях, или варианта зрелого полипептида под SEQ ID NO: 7, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях; и
c) фрагмента полипептида (a), (b), (c) или (d), который обладает ДНКазной активностью.
48. Композиция по любому из пунктов 46-47, где полинуклеотид характеризуется по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100% идентичностью последовательности зрелого полипептида под SEQ ID NO: 2, зрелого полипептида под SEQ ID NO: 3, зрелого полипептида под SEQ ID NO: 5, зрелого полипептида под SEQ ID NO: 6, зрелого полипептида под SEQ ID NO: 7 или зрелого полипептида под SEQ ID NO: 8.
49. Композиция по любому из пунктов 46-48, где полинуклеотид содержит или состоит из SEQ ID NO: 2 или зрелого полипептида под SEQ ID NO: 2, полипептид содержит или состоит из последовательности под SEQ ID NO: 3 или зрелого полипептида под SEQ ID NO: 3, полипептид содержит или состоит из последовательности под SEQ ID NO: 5 или зрелого полипептида под SEQ ID NO: 5, полипептид содержит или состоит из последовательности под SEQ ID NO: 6 или зрелого полипептида под SEQ ID NO: 6, полипептид содержит или состоит из SEQ ID NO: 7 или зрелого полипептида под SEQ ID NO: 7 или полипептид содержит или состоит из последовательности под SEQ ID NO: 8 или зрелого полипептида под SEQ ID NO: 8.
50. Композиция по любому из пунктов 46-49, где зрелый полипептид представляет собой аминокислоты с 1 по 206 последовательности под SEQ ID NO: 2, аминокислоты с 1 по 206 последовательности под SEQ ID NO: 3, аминокислоты с 1 по 188 последовательности под SEQ ID NO: 5, аминокислоты с 1 по 110 последовательности под SEQ ID NO: 6, аминокислоты с 1 по 109 последовательности под SEQ ID NO: 7 или аминокислоты с 1 по 206 последовательности под SEQ ID NO: 8.
51. Композиция по любому из пунктов 46-50, где зрелый полипептид представляет собой вариант зрелого полипептида под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 или SEQ ID NO: 8, где вариант характеризуется заменой, делецией и/или вставкой в одном или нескольких положениях, или вариант зрелого полипептида под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 6, или SEQ ID NO: 7, или SEQ ID NO: 8, который характеризуется заменой, делецией и/или вставкой в одном или нескольких положениях.
52. Композиция по любому из пунктов 46-51, где полипептид представляет собой фрагмент последовательности под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 или SEQ ID NO: 8, где фрагмент обладает ДНКазной активностью.
53. Композиция по любому из предыдущих пунктов, относящихся к композиции, где композиция представляет собой брусок, гомогенную таблетку, таблетку с двумя или более слоями, пакет с одним или несколькими отделениями, обычный или уплотненный порошок, гранулу, пасту, гель или обычную, уплотненную или концентрированную жидкость.
54. Композиция по любому из предыдущих пунктов, относящихся к композиции, где композиция представляет собой жидкое моющее средство, моющее средство в форме порошка или моющее средство в форме гранул.
55. Способ предотвращения или уменьшения повторного осаждения грязи на изделии в ходе процесса последующей чистки или стирки, включающий стадии:
а) приведение изделия в контакт с композицией по любому из пунктов 27-54 и пунктов 82-96, или с жидким раствором, содержащим полипептид, обладающий ДНКазной активностью; и
b) необязательно полоскание изделия,
где изделие представляет собой текстильное изделие или твердую поверхность.
56. Способ по пункту 55, где процесс последующей чистки или стирки не включает применение полипептида, обладающего ДНКазной активностью.
57. Способ по любому из пунктов 55-56, где приведение в контакт согласно стадии а) осуществляется с помощью пропитывания изделия или при мытье изделия.
58. Способ по пункту 55, где жидкий раствор представляет собой моющую жидкость или раствор для пропитывания изделия.
59. Способ по любому из предыдущих пунктов, где приведение в контакт согласно стадии а) осуществляется с помощью распыления композиции или жидкого раствора на изделие.
60. Способ по любому из предыдущих пунктов, относящихся к способу, где композиция или полипептид согласно стадии а) применяется для чистки или стирки изделия по меньшей мере один раз перед процессом последующей чистки или стирки.
61. Способ по пункту 60, где композицию или полипептид согласно стадии а) применяют для чистки или стирки изделия по меньшей мере два раза, три раза, четыре раза, пять раз, шесть раз, семь раз, восемь раз, девять раз или десять раз перед процессом последующей чистки или стирки.
62. Способ по любому из предыдущих пунктов, относящихся к способу, где жидкий раствор дополнительно включает поверхностно-активные вещества, моющие компоненты, флокулирующее вспомогательное средство, хелатирующие средства, ингибиторы переноса красителей, ферменты, стабилизаторы ферментов, ингибиторы ферментов, каталитические материалы, активаторы отбелки, пероксид водорода, источники пероксида водорода, предварительно образованные перкислоты, полимерные диспергирующие средства, средства для устранения/средства против повторного осаждения глинистой грязи, отбеливатели, подавители образования мыльной пены, красители, отдушки, средства, обеспечивающие эластичность, мягчители тканей, носители, гидротропы, моющие компоненты и дополнительные моющие компоненты, окрашивающие средства для тканей, противовспенивающие средства, диспергирующие средства, технологические добавки и/или пигменты.
63. Способ по любому из предыдущих пунктов, относящихся к способу, где жидкий раствор дополнительно содержит один или несколько ферментов, выбранных из группы, состоящей из протеаз, липаз, кутиназ, амилаз, карбогидраз, целлюлаз, пектиназ, маннаназ, арабиназ, галактаназ, ксиланаз и оксидаз.
64. Способ по любому из предыдущих пунктов, относящихся к способу, где значение pH жидкого раствора находится в диапазоне от 1 до 11.
65. Способ по любому из предыдущих пунктов, относящихся к способу, где значение pH жидкого раствора находится в диапазоне от 5,5 до 11, например, в диапазоне от 7 до 9, в диапазоне от 7 до 8 или в диапазоне от 7 до 8,5.
66. Способ по любому из предыдущих пунктов, относящихся к способу, где температура жидкого раствора находится в диапазоне от 5°C до 95°C или в диапазоне от 10°C до 80°C, в диапазоне от 10°C до 70°C, в диапазоне от 10°C до 60°C, в диапазоне от 10°C до 50°C, в диапазоне от 15°C до 40°C или в диапазоне от 20°C до 30°C.
67. Способ по любому из предыдущих пунктов, относящихся к способу, где температура жидкого раствора составляет 30°C.
68. Способ по любому из предыдущих пунктов, относящихся к способу, где изделие прополаскивают после приведения в контакт с композицией или полипептидом согласно стадии а).
69. Способ по любому из предыдущих пунктов, относящихся к способу, где изделие прополаскивают водой или водой, содержащей кондиционер.
70. Способ по любому из предыдущих пунктов, относящихся к способу, где полипептид, обладающий ДНКазной активностью, представляет собой полипептид животного, растительного или микробного происхождения.
71. Способ по пункту 70, где полипептид характеризуется человеческим происхождением.
72. Способ по пункту 70, где полипептид получают из фасоли золотистой.
73. Способ по пункту 70, где полипептид характеризуется бактериальным или грибным происхождением.
74. Способ по пункту 73, где полипептид характеризуется грибным происхождением и полипептид выбран из группы, состоящей из:
a) полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 2, полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 3, полипептида, характеризующегося по меньшей мере на 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 5, или полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 8;
b) полипептида, кодируемого полинуклеотидом, который гибридизируется в условиях низкой жесткости с
i. последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 1 или последовательностью, кодирующей зрелый полипептид, под SEQ ID NO: 4,
ii. ее последовательностью кДНК или
iii. последовательностью полной длины, комплементарной (i) или (ii);
c) полипептида, кодируемого полинуклеотидом, характеризующимся по меньшей мере 60% идентичностью последовательности, кодирующей зрелый полипептид, под SEQ ID NO: 1, или его последовательности кДНК, или полипептида, кодируемого полинуклеотидом, характеризующегося по меньшей мере 60% идентичностью последовательности, кодирующей зрелый полипептид, под SEQ ID NO: 4 или ее последовательности кДНК;
d) варианта зрелого полипептида под SEQ ID NO: 2, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях, варианта зрелого полипептида под SEQ ID NO: 3, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях, варианта зрелого полипептида под SEQ ID NO: 5, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях, или варианта зрелого полипептида под SEQ ID NO: 8, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях; и
e) фрагмента полипептида (a), (b), (c) или (d), который обладает ДНКазной активностью.
75. Способ по пункту 73, где полипептид характеризуется бактериальным происхождением и полипептид выбран из группы, состоящей из:
a) полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 6, или полипептида, характеризующегося по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 7;
b) варианта зрелого полипептида под SEQ ID NO: 6, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях, или варианта зрелого полипептида под SEQ ID NO: 7, характеризующегося заменой, делецией и/или вставкой в одном или нескольких положениях; и
c) фрагмента полипептида (a), (b), (c) или (d), который обладает ДНКазной активностью.
76. Способ по любому из пунктов 74-75, где полипептид характеризуется по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100% идентичностью последовательности зрелого полипептида под SEQ ID NO: 2, зрелого полипептида под SEQ ID NO: 3, зрелого полипептида под SEQ ID NO: 5, зрелого полипептида под SEQ ID NO: 6, зрелого полипептида под SEQ ID NO: 7 или зрелого полипептида под SEQ ID NO: 8.
77. Способ по любому из пунктов 74-76, где полипептид содержит или состоит из последовательности под SEQ ID NO: 2 или зрелого полипептида под SEQ ID NO: 2, полипептид содержит или состоит из последовательности под SEQ ID NO: 3 или зрелого полипептида под SEQ ID NO: 3, полипептид содержит или состоит из последовательности под SEQ ID NO: 5 или зрелого полипептида под SEQ ID NO: 5, полипептид содержит или состоит из последовательности под SEQ ID NO: 6 или зрелого полипептида под SEQ ID NO: 6, полипептид содержит или состоит из SEQ ID NO: 7 или зрелого полипептида под SEQ ID NO: 7, или полипептид содержит или состоит из последовательности под SEQ ID NO: 8 или зрелого полипептида под SEQ ID NO: 8.
78. Способ по любому из пунктов 74-77, где зрелый полипептид представляет собой аминокислоты c 1 по 206 в последовательности под SEQ ID NO: 2, аминокислоты с 1 по 206 последовательности под SEQ ID NO: 3, аминокислоты с 1 по 188 последовательности под SEQ ID NO: 5, аминокислоты с 1 по 110 последовательности под SEQ ID NO: 6, или аминокислоты с 1 по 109 последовательности под SEQ ID NO: 7, или аминокислоты с 1 по 206 последовательности под SEQ ID NO: 8.
79. Способ по любому из пунктов 74-78, где полипептид представляет собой вариант зрелого полипептида под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 или SEQ ID NO: 8, где вариант характеризуется заменой, делецией и/или вставкой в одном или нескольких положениях, или вариант зрелого полипептида под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 или SEQ ID NO: 8, который характеризуется заменой, делецией и/или вставкой в одном или нескольких положениях.
80. Способ по любому из пунктов 74-79, где полипептид представляет собой фрагмент последовательности под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 или SEQ ID NO: 8, где фрагмент обладает ДНКазной активностью.
81. Способ по любому из предыдущих пунктов, относящихся к способу, где концентрация полипептида в моющей жидкости находится в диапазоне от 0,00004 до 100 ppm белка-фермента, например, в диапазоне от 0,00008 до 100, в диапазоне от 0,0001 до 100, в диапазоне от 0,0002 до 100, в диапазоне от 0,0004 до 100, в диапазоне от 0,0008 до 100, в диапазоне от 0,001 до 100 ppm белка-фермента, в диапазоне от 0,01 до 100 ppm белка-фермента, в диапазоне от 0,05 до 50 ppm белка-фермента, в диапазоне от 0,1 до 50 ppm белка-фермента, в диапазоне от 0,1 до 30 ppm белка-фермента, в диапазоне от 0,5 до 20 ppm белка-фермента или в диапазоне от 0,5 до 10 ppm белка-фермента.
82. Моющая композиция по пункту 27, где композиция представляет собой жидкую моющую композицию, содержащую поверхностно-активное вещество и моющий компонент моющего средства, в общей концентрации по меньшей мере 3% по весу, и моющий фермент, содержащий микрокапсулу, где мембрана микрокапсулы получена путем сшивания полиразветвленного полиамина с молекулярным весом более 1 кДа.
83. Моющая композиция по пункту 82, где реакционноспособные аминогруппы полиразветвленного полиамина составляют по меньшей мере 15% молекулярного веса.
84. Моющая композиция по любому из пунктов 82-83, где микрокапсулу получают при использовании хлорангидрида в качестве сшивающего средства.
85. Моющая композиция по любому из пунктов 82-84, где диаметр микрокапсулы составляет по меньшей мере 50 микрометров или больше.
86. Моющая композиция по любому из пунктов 82-85, где микрокапсула содержит по меньшей мере 1% по весу активного фермента.
87. Моющая композиция по любому из пунктов 82-86, которая дополнительно включает спирт, такой как полиол.
88. Моющая композиция по любому из пунктов 82-87, где поверхностно-активное вещество представляет собой анионное поверхностно-активное вещество.
89. Моющая композиция по любому из пунктов 82-88, которая представляет собой жидкую композицию для стирки или композицию для автоматизированного мытья посуды.
90. Моющая композиция по любому из пунктов 82-89, которая содержит менее 90% по весу воды.
91. Моющая композиция по любому из пунктов 82-90, где моющий фермент представляет собой полипептид, обладающий ДНКазной активностью, протеазу, амилазу, липазу, целлюлазу, маннаназу, пектиназу или оксидоредуктазу.
92. Моющая композиция по любому из пунктов 82-91, где протеаза представляет собой металлопротеазу или щелочную серин-протеазу, такую как субтилизин.
93. Моющая композиция по любому из пунктов 82-92, где полипептид, обладающий ДНКазной активностью, представляет собой полипептид, характеризующийся по меньшей мере 60% идентичностью последовательности под SEQ ID NO: 2, полипептид, характеризующийся по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 3, полипептид, характеризующийся по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 5, или полипептид, характеризующийся по меньшей мере 60% идентичностью последовательности зрелого полипептида под SEQ ID NO: 8.
94. Моющая композиция по любому из пунктов 82-93, где микрокапсула получена путем поверхностной полимеризации с использованием хлорангидрида в качестве сшивающего средства.
95. Моющая композиция по любому из пунктов 82-94, где полиразветвленный полиамин представляет собой полиэтиленимин.
96. Моющая композиция по любому из пунктов 82-95, где микрокапсула содержит источник ионов Mg2+, Ca2+ или Zn2+, такой как слаборастворимая соль Mg2+, Ca2+ или Zn2+.
97. Изделие, обработанное или пропитанное полипептидом, обладающим ДНКазной активностью.
98. Изделие по пункту 97, где изделие представляет собой текстильное изделие.
Анализы и моющие композиции
Моющие композиции
Упомянутую ниже моющую композицию можно применять в комбинации с полипептидом по настоящему изобретению для предотвращения или уменьшения статического электричества.
Biotex Black (жидкость)
5-15% анионных поверхностно-активных веществ, <5% неионных поверхностно-активных веществ, отдушка, ферменты, DMDM и гидантоин.
Композиция Ariel Sensitive White & Color, жидкая моющая композиция
Вода, этоксисульфат спирта, этоксилат спирта, аминоксид, лимонная кислота, C12-18 высшая жирная пальмоядровая кислота, протеаза, гликозидаза, амилаза, этанол, 1,2-пропандиол, формиат натрия, хлорид кальция, гидроксид натрия, эмульсия на основе силикона, транс-сульфатированый EHDQ (ингредиенты перечислены в порядке убывания).
Композиция моющего средства-модели WFK IEC-A (порошок)
Ингредиенты: линейный алкилбензолсульфонат натрия- 8,8%, этоксилированный жирный спирт C12-18 (7 EO) - 4,7%, натриевое мыло - 3,2%, противовспенивающее средство DC2-4248S - 3,9%, алюмосиликат натрия - цеолит 4A - 28,3%, карбонат натрия - 11,6%, натриевая соль сополимера акриловой и малеиновой кислоты (Sokalan CP5) - 2,4%, силикат натрия - 3,0%, карбоксиметилцеллюлоза - 1,2%, Dequest 2066-2,8%, оптический осветлитель - 0,2%, сульфат натрия - 6,5%, протеаза - 0,4%.
Композиция моющего средства-модели A (жидкость)
Ингредиенты: 12% LAS, 11% AEO Biosoft N25-7 (NI), 7% AEOS (SLES), 6% MPG (монопропиленгликоля), 3% этанола, 3% TEA, 2,75% кокосового мыла, 2,75% соевого мыла, 2% глицерина, 2% гидроксида натрия, 2% цитрата натрия, 1% формиата натрия, 0,2% DTMPA и 0,2% PCA (все процентные содержания приведены в вес./вес.).
Композиция Ariel Actilift (жидкость)
Ингредиенты: 5-15% анионных поверхностно-активных веществ; <5% неионных поверхностно-активных веществ, фосфонаты, мыло; ферменты, оптические отбеливатели, бензизотиазолинон, метилизотиазолинон, отдушки, альфа-изометил ионон, цитронеллол, гераниол, линалоол.
Композиция Ariel Actilift Colour&Style (жидкость)
Ингредиенты: 5-15% анионных поверхностно-активных веществ; <5% неионных поверхностно-активных веществ, фосфонаты, мыло; ферменты, отдушки, бензизотиазолинон, метилизотиазолинон, альфа-изометил ионон, бутилфенилметилпропиональ, цитронеллол, гераниол, линалоол.
Композиция Ariel Actilift Colour & Style
Вода, додецилбензолсульфонат натрия, С14-С15 парет-7, цитрат натрия, пропиленгликоль, пальмкернелат натрия, лауретсульфат натрия, MEA додецилбензолсульфонат, сульфатированный этоксилированный кватернизованный гексаметилендиамин, куменсульфонат натрия, отдушка, сополимер PEG/винилацетата, формиат натрия, гидрогенизированное касторовое масло, диэтилентриаминпентаметиленфосфонат натрия, пропилгептиловый эфир PEG/PPG-10/2, бутиофенилметилпропиональ, поливинилпиридин-N-оксид, сорбит, глицерин, этаноламин, гидроксид натрия, альфа-изометилионон, протеаза, хлорид кальция, гераниол, линалоол, цитронеллол, трипропиленгликоль, глюкозидаза, бензизотиазолинон, диметикон, гликозидаза, ацетат натрия, целлюлаза, красящее вещество, глицерилстеарат, гидроксиэтилцеллюлоза, кремнезем.
Композиция Ariel Actilift Colour & Style, новая упаковка
Ингредиенты: вода, лауретсульфат натрия, пропиленгликоль, С14-С15 парет-7, цитрат натрия, пальмкернелат натрия, спирт, формиат натрия, сульфатированный этоксилированный кватернизованный гексаметилендиамин, гидроксид натрия, отдушка, поливинилпиридин-N-оксид, сорбит, хлорид кальция, протеаза, глицерин, глюкозидаза, гликозидаза, ацетат натрия, красящее вещество, целлюлаза.
Композиция Ariel Actilift Whites & Colours Coolclean, новая упаковка
Ингредиенты: вода, лауретсульфат натрия, пропиленгликоль, С14-С15 парет-7, цитрат натрия, пальмкернелат натрия, спирт, формиат натрия, сульфатированный этоксилированный кватернизованный гексаметилендиамин, гидроксид натрия, отдушка, сорбит, хлорид кальция, протеаза, глицерин, глюкозидаза, гликозидаза, ацетат натрия, красящее вещество, целлюлаза.
Композиция Ariel Sensitive White & Color
Ингредиенты: вода, лауретсульфат натрия, пропиленгликоль, С14-С15 парет-7, цитрат натрия, пальмкернелат натрия, спирт, формиат натрия, сульфатированный этоксилированный кватернизованный гексаметилендиамин, гидроксид натрия, сорбит, хлорид кальция, протеаза, глицерин, гликозидаза, ацетат натрия, целлюлаза, кремнезем.
Композиция Ariel Actilift, обычная
Вода, додецилбензолсульфонат натрия, С14-С15 парет-7, цитрат натрия, пропиленгликоль, пальмкернелат натрия, лауретсульфат натрия, MEA додецилбензолсульфонат, сульфатированный этоксилированный кватернизованный гексаметилендиамин, куменсульфонат натрия, отдушка, сополимер PEG/винилацетата, формиат натрия, С12-С14 парет-7, гидрогенизированное касторовое масло, диэтилентриаминпентаметиленфосфонат натрия, пропилгептиловый эфир PEG/PPG-10/2, бутиофенилметилпропиональ, флуоресцентный отбеливатель 9, сорбит, глицерин, этаноламин, гидроксид натрия, альфа-изометилионон, протеаза, хлорид кальция, гераниол, линалоол, цитронеллол, трипропиленгликоль, хлорид натрия, глюкозидаза, бензизотиазолинон, диметикон, гликозидаза, ацетат натрия, целлюлаза, красящее вещество, глицерилстеарат, гидроксиэтилцеллюлоза, кремнезем.
Композиция Persil Small & Mighty (жидкость)
Ингредиенты: 15-30% анионных поверхностно-активных веществ, неионные поверхностно-активные вещества, 5-15% мыла, < 5% поликарбоксилатов, отдушка, фосфаты, оптические отбеливатели.
Persil 2 in1 with Comfort Passion Flower Powder
Сульфат натрия, карбонат натрия, додецилбензолсульфонат натрия, бентонит, перкарбонат натрия, силикат натрия, цеолит, вода, лимонная кислота, TAED, C12-15 парет-7, стеариновая кислота, отдушка, натриевая соль акриловой кислоты/сополимер MA, целлюлозная камедь, модифицированный кукурузный крахмал, хлорид натрия, тетранатрия этидронат, кальция-натрия EDTMP, динатрия анилиноморфолинотриазинил-аминостильбенсульфонат, бикарбонат натрия, фенилпропилэтилметикон, бутилфенилметилпропиональ, глицерилстеараты, карбонат кальция, полиакрилат натрия, альфа-изометил ионон, дистиролбифенилдисульфонат динатрия, целлюлоза, протеаза, лимонен, PEG-75, диоксид титана, декстрин, сахароза, полиарилсульфонат натрия, CI 12490, CI 45100, CI 42090, тиосульфат натрия, CI 61585.
Persil Biological Powder
Сахароза, сорбит, силикат алюминия, полиоксиметилен меламин, полиарилсульфонат натрия, CI 61585, CI 45100, липаза, амилаза, ксантановая камедь, гидроксипропилметилцеллюлоза, CI 12490, динатрия дистирилбифенил дисульфонат, тиосульфат натрия, CI 42090, маннаназа, CI 11680, этидроновая кислота, тетранатрия EDTA.
Persil Biological Tablets
Карбонат натрия, перкарбонат натрия, бикарбонат натрия, цеолит, вода, силикат натрия, лаурилсульфат натрия, целлюлоза, TAED, додецилбензолсульфонат натрия, гемицеллюлоза, лигнин, лаурилглюкозид, натриевая соль акриловой кислоты/сополимер MA, бентонит, хлорид натрия, отдушка, тетранатрия этидронат, сульфат натрия, полиакрилат натрия, диметикон, анилиноморфолинотриазиниламиностильбенсульфонат динатрия, додецилбензолсульфоновая кислота, триметилсилоксисиликат, карбонат кальция, целлюлоза, PEG-75, диоксид титана, декстрин, протеаза, модиифцированный кукурузный крахмал, сахароза, CI 12490, полиарилсульфонат натрия, тиосульфат натрия, амилаза, каолин.
Persil Colour Care Biological Powder
Субтилизин, имидазолинон, гексилциннамаль, сахароза, сорбит, силикат алюминия, полиоксиметилен меламин, CI 61585, CI 45100, липаза, амилаза, ксантановая камедь, гидроксипропилметилцеллюлоза, CI 12490, динатрия дистирилбифенил дисульфонат, тиосульфат натрия, CI 42090, маннаназа, CI 11680, этидроновая кислота, тетранатрия EDTA.
Persil Colour Care Biological Tablets
Бикарбонат натрия, карбонат натрия, цеолит, вода, силикат натрия, лаурилсульфат натрия, целлюлозная камедь, додецилбензолсульфонат натрия, лаурилглюкозид, хлорид натрия, натриевая соль акриловой кислоты/сополимер MA, отдушка, тиогликолат натрия, PVP, сульфат натрия, тетранатрия этидронат, полиакрилат натрия, диметикон, бентонит, додецилбензолсульфоновая кислота, триметилсилоксисиликат, карбонат кальция, целлюлоза, PEG-75, диоксид титана, декстрин, протеаза, модифицированный кукурузный крахмал, сахароза, тиосульфат натрия, амилаза, CI 74160, каолин.
Persil Dual Action Capsules Bio
MEA-додецилбензолсульфонат, MEA-гидрогенизированный кокоат, C12-15 парет-7, дипропиленгликоль, вода, тетранатрия этидронат, поливиниловый спирт, глицерин, азиридин, этоксилированный гомополимер, пропиленгликоль, отдушка, диэтилентриаминпентаметиленфосфонат натрия, сорбит, MEA-сульфат, этаноламин, субтилизин, гликоль, бутилфенилметилпропиональ, бороновая кислота, (4-формилфенил), гексилциннамаль, лимонен, линалоол, динатрия дистирилбифенил дисульфонат, альфа-изометил ионон, гераниол, амилаза, полимерный синий краситель, полимерный желтый краситель, тальк, хлорид натрия, бензизотиазолинон, маннаназа, денатониум бензоат.
Persil 2 in1 with Comfort Sunshiny Days Powder
Сульфат натрия, карбонат натрия, додецилбензолсульфонат натрия, бентонит, перкарбонат натрия, силикат натрия, цеолит, вода, лимонная кислота, TAED, C12-15 парет-7, отдушка, стеариновая кислота, натриевая кислота акриловой кислоты/сополимер MA, целлюлозная камедь, модифицированный кукурузный крахмал, хлорид натрия, тетранатрия этидронат, кальция-натрия EDTMP, динатрия анилиноморфолинотриазинил-аминостильбенсульфонат, бикарбонат натрия, фенилпропилэтилметикон, бутилфенилметилпропиональ, глицерилстеараты, карбонат кальция, полиакрилат натрия, гераниол, динатрия дистирилбифенил дисульфонат, целлюлоза, протеаза, PEG-75, диоксид титана, декстрин, сахароза, полиарилсульфонат натрия, CI 12490, CI 45100, CI 42090, тиосульфат натрия, CI 61585.
Persil Small & Mighty 2 in 1 with Comfort Sunshiny Days
Вода, C12-15 парет-7, додецилбензолсульфонат натрия, пропиленгликоль, гидрогенизированный кокоат натрия, триэтаноламин, глицерин, TEA-гидрогенизированный кокоат, отдушка, хлорид натрия, поликватерний-10, PVP, полимерный розовый краситель, сульфат натрия, динатрия дистирилбифенил дисульфонат, бутилфенилметилпропиональ, сополимер стирола/акрилатов, гексилциннамаль, цитронеллол, евгенол, поливиниловый спирт, ацетат натрия, изопропиловый спирт, полимерный желтый краситель, лаурилсульфат натрия.
Persil Small & Mighty Bio
Вода, MEA-додецилбензолсульфонат, пропиленгликоль, лауретсульфат натрия, C12-15 парет-7, TEA-гидрогенизированный кокоат, MEA-цитрат, этоксилированный гомополимер азиридина, MEA-этидронат, триэтаноламин, отдушка, сополимер акилатов, сорбит, MEA-сульфат, сульфит натрия, динатрия дистирилбифенил дисульфонат, бутилфенилметилпропиональ, сополимер стирола/акрилатов, цитронеллол, сульфат натрия, пептиды, соли, сахара из (процесса) ферментации, субтилизин, глицерин, бороновая кислота, (4-формилфенил), гераниол, пектат-лиаза, амилаза, лаурилсульфат натрия, маннаназа, CI 42051.
Persil Small & Mighty Capsules Biological
MEA-додецилбензолсульфонат, MEA-гидрогенизированный кокоат, C12-15 парет-7, дипропиленгликоль, вода, глицерин, поливиниловый спирт, отдушка, этоксилированный гомополимер азиридина, диэтилентриаминпентаметиленфосфонат натрия, пропиленгликоль, сорбит, MEA-сульфат, этаноламин, субтилизин, гликоль, бутилфенилметилпропиональ, гексилциннамаль, крахмал, бороновая кислота, (4-формилфенил), лимонен, линалоол, динатрия дистирилбифенил дисульфонат, альфа-изометил ионон, гераниол, амилаза, тальк, полимерный синий краситель, хлорид натрия, бензизотиазолинон, денатониум бензоат, полимерный желтый краситель, маннаназа.
Persil Small & Mighty Capsules Colour Care
MEA-додецилбензолсульфонат, MEA-гидрогенизированный кокоат, C12-15 парет-7, дипропиленгликоль, вода, глицерин, поливиниловый спирт, отдушка, этоксилированный гомополимер азиридина, диэтилентриаминпентаметиленфосфонат натрия, пропиленгликоль, MEA-сульфат, этаноламин, PVP, сорбит, бутилфенилметилпропиональ, субтилизин, гексилциннамаль, крахмал, лимонен, линалоол, бороновая кислота, (4-формилфенил), альфа-изометил ионон, гераниол, тальк, полимерный синий краситель, денатониум бензоат, полимерный желтый краситель.
Persil Small & Mighty Colour Care
Вода, MEA-додецилбензолсульфонат, пропиленгликоль, лауретсульфат натрия, C12-15 парет-7, TEA-гидрогенизированный кокоат, MEA-цитрат, этоксилированный гомополимер азиридина, MEA-этидронат, триэтаноламин, отдушка, сополимер, сорбит, MEA-сульфат, сульфит натрия, глицерин, бутилфенилметилпропиональ, цитронеллол, сульфат натрия, пептиды, соли, сахара из (процесса) ферментации,сополимер стирола/акрилатов, субтилизин, бороновая кислота, (4-формилфенил), гераниол, пектат-лиаза, амилаза, лаурилсульфат натрия, маннаназа, CI 61585, CI 45100.
Композиция Fairy Non Bio (жидкость)
Ингредиенты: 15-30% анионных поверхностно-активных веществ, 5-15% неионных поверхностно-активных веществ, мыло, бензизотиазолинон, метилизотиазолинон, отдушки.
Композиция моющего средства-модели T (порошок)
Ингредиенты: 11% LAS, 2% AS/AEOS, 2% мыла, 3% AEO, 15,15% карбоната натрия, 3% силиката натрия, 18,75% цеолита, 0,15% хелатирующего агента, 2% цитрата натрия, 1,65% сополимера AA/MA, 2,5% CMC и 0,5% SRP (все процентные содержания приведены в вес./вес.).
Композиция моющего средства-модели X (порошок)
Ингредиенты: 16,5% LAS, 15% цеолита, 12% дисиликата натрия, 20% карбоната натрия, 1% Sokalan, 35,5% сульфата натрия (все процентные содержания приведены в вес./вес.).
Композиция Ariel Actilift Colour & Style (порошок)
Ингредиенты: 15-30% анионных поверхностно-активных веществ, <5% неионных поверхностно-активных веществ, фосфонаты, поликарбоксилаты, цеолиты; ферменты, отдушки, гексилциннамаль.
Композиция Ariel Actilift (порошок)
Ингредиенты: 5-15% анионных поверхностно-активных веществ, отбеливающие вещества на основе кислорода, <5% неионных поверхностно-активных веществ, фосфонатов, поликарбоксилатов, цеолиты, оптические отбеливатели, ферменты, отдушки, бутилфенилметилпропиональ, кумарин, гексилциннамаль.
Композиция Persil Megaperls (порошок)
Ингредиенты: 15-30% следующего: анионные поверхностно-активные вещества, отбеливающее вещество на основе кислорода и цеолиты, менее 5% следующего: неионные поверхностно-активные вещества, фосфонаты, поликарбоксилаты, мыло, дополнительные ингредиенты: отдушки, гексилциннамаль, бензилсалицилат, линалоол, оптические отбеливатели, ферменты и цитронеллол.
Gain Liquid, Original
Ингредиенты: вода, этоксисульфат спирта, диэтиленгликоль, этоксилат спирта, этаноламин, линейный алкилбензолсульфонат, натриевые соли жирных кислот, полиэтиленимин этоксилат, лимонная кислота, бура, натрия куменсульфонат, пропиленгликоль, DTPA, динатрия диаминостильбен дисульфонат, дипропилэтил тетрамин, гидроксид натрия, формиат натрия, формиат кальция, диметикон, амилаза, протеаза, Liquitint™, гидрогенизированное касторовое масло, ароматизатор.
Tide Liquid, Original
Ингредиенты: линейный алкилбензолсульфонат, пропиленгликоль, лимонная кислота, гидроксид натрия, бура, этаноламин, этанол, сульфатный спирт, полиэтилениминэтоксилат, натриевые соли жирных кислот, дикватерний этоксисульфат, протеаза, диэтиленгликоль, лаурет-9, алкилдиметиламин оксид, ароматизатор, амилаза, динатрия диаминостильбен дисульфонат, DTPA, формиат натрия, формиат кальция, полиэтиленгликоль 4000, маннаназа, Liquitint™ синий, диметикон.
Liquid Tide, Free and Gentle: вода, этоксисульфат натрия на основе спирта, пропиленгликоль, бура, этанол, линейный алкилбензолсульфонат натрия, соль, полиэтиленимин этоксилат, диэтиленгликоль, транс-сульфатированный и этоксилированный гексаметилендиамин, этоксилат спирта, линейный алкилбензолсульфонат, соль MEA, формиат натрия, натрия алкилсульфат, DTPA, аминоксид, формиат кальция, динатрия диаминостильбен, дисульфонат, амилаза, протеаза, диметикон, бензизотиазолинон.
Tide Coldwater Liquid, Fresh Scent: вода, этоксисульфат натрия на основе спирта, линейный алкилбензолсульфонат, диэтиленгликоль, пропиленгликоль, этаноламин, лимонная кислота, бура, сульфат спирта, гидроксид натрия, полиэтиленимин, этоксилат, натриевые соли жирных кислот, этанол, протеаза, лаурет-9, дикватерний этоксисульфат, лаураминоксид, кумен натрия, сульфонат, ароматизатор, DTPA, амилаза, динатрия диаминостильбен, дисульфонат, формиат натрия, динатрия дистирилбифенил дисульфонат, формиат кальция, полиэтиленгликоль 4000, маннаназа, пектиназа, Liquitint™ синий, диметикон.
Tide TOTALCARE™ Liquid, Cool Cotton: вода, этоксисульфат спирта, пропиленгликоль, натриевые соли жирных кислот, лауртримонийхлорид, этанол, гидроксид натрия, натрия куменсульфонат, лимонная кислота, этаноламин, диэтиленгликоль, силиконовый полиэфир, бура, ароматизатор, полиэтиленимин этоксилат, протеаза, лаурет-9,
DTPA, полиакриламид кватернийхлорид, динатрия диаминостильбен дисульфонат, формиат натрия, Liquitint™ оранжевый, дипропилэтилтетраамин, диметикон, целлюлаза.
Liquid Tide Plus Bleach Alternative™, Vivid White and Bright, Original and Clean Breeze:
вода, этоксисульфат натрия на основе спирта, алкилсульфат натрия, цитрат MEA, линейный алкилбензолсульфонат, соль MEA, пропиленгликоль, диэтиленгликоль, полиэтиленимин этоксилат, этанол, натриевые соли жирных кислот, этаноламин, лаураминоксид, бура, лаурет-9, DTPA, натрия куменсульфонат, формиат натрия, формиат кальция, линейный алкилбензолсульфонат, натриевая соль, сульфат спирта, гидроксид натрия, дикватерний этоксисульфат, ароматизатор, амилаза, протеаза, маннаназа, пектиназа, динатрия диаминостильбен дисульфонат, бензизотиазолинон, Liquitint™ синий, диметикон, дипропилэтилтетраамин.
Liquid Tide HE, Original Scent: вода, этоксисульфат натрия на основе спирта, цитрат MEA, алкилсульфат натрия, этоксилат спирта, линейный алкилбензолсульфонат, соль MEA, натриевые соли жирных кислот, полиэтилениминэтоксилат, диэтиленгликоль, пропиленгликоль, дикватерний этоксисульфат, бура, полиэтиленимин, этоксилат пропоксилат, этанол, натрия куменсульфонат, ароматизатор, DTPA, динатрия диаминостильбен дисульфонат, маннаназа, целлюлаза, амилаза, формиат натрия, формиат кальция, лаураминоксид, Liquitint™ синий, диметикон/полидиметилсиликон.
Tide TOTALCARE HE Liquid, renewing Rain: вода, этоксисульфат спирта, линейный алкилбензолсульфонат, этоксилат спирта, лимонная кислота, этаноламин, натриевые соли жирных кислот, диэтиленгликоль, пропиленгликоль, гидроксид натрия, бура, полиэтилениминэтоксилат, силиконовый полиэфир, этанол, протеаза, куменсульфонат натрия, дикватерний-этоксисульфат, лаурет-9, ароматизатор, амилаза, DTPA, динатрия диаминостильбен дисульфонат, динатрия дистирилбифенил дисульфонат, формиат натрия, формиат кальция, маннаназа, Liquitint™ оранжевый, диметикон, полиакриламид кватерний-хлорид, целлюлаза, дипропилэтилтетраамин.
Tide liquid HE Free: вода, этоксисульфат спирта, диэтиленгликоль, моноэтаноламинцитрат, формиат натрия, пропиленгликоль, линейные алкилбензолсульфонаты, этаноламин, этанол, полиэтиленимин этоксилат, амилаза, бензизотиазолин, бура, формиат кальция, лимонная кислота, диэтилентриамин пентаацетат натрия, диметикон, дикватерний этоксисульфат, динатрия диаминостильбен дисульфонат, лаурет-9, маннаназа, протеаза, натрия куменсульфонат, натриевые соли жирных кислот.
Tide Coldwater HE Liquid, Fresh Scent: вода, этоксисульфат спирта, цитрат MEA, сульфат спирта, этоксилат спирта, линейный алкилбензолсульфонат MEA, натриевые соли жирных кислот, полиэтиленимин этоксилат, диэтиленгликоль, пропиленгликоль, дикватерний этоксисульфат, бура, полиэтиленимин этоксилат пропоксилат, этанол, натрия куменсульфонат, ароматизатор, DTPA, динатрия диаминостильбен дисульфонат, протеаза, маннаназа, целлюлаза, амилаза, формиат натрия, формиат кальция, лаураминоксид, Liquitint™ синий, диметикон.
Tide for Coldwater HE Free Liquid: вода, этоксисульфат натрия на основе спирта, цитрат MEA, линейный алкилбензолсульфонат: натриевая соль, этоксилат спирта, линейный алкилбензолсульфонат: Соль MEA, натриевые соли жирных кислот, полиэтиленимин этоксилат, диэтиленгликоль, пропиленгликоль, дикватерний этоксисульфат, бура, протеаза, полиэтиленимин этоксилат пропоксилат, этанол, натрия куменсульфонат, амилаза, лимонная кислота, DTPA, динатрия диаминостильбен дисульфонат, формиат натрия, формиат кальция, диметикон.
Tide Simply Clean & Fresh: вода, этоксилатсульфат спирта, линейный алкилбензолсульфонат натрия/соли Mea, пропиленгликоль, диэтиленгликоль, формиат натрия, этанол, бура, натриевые соли жирных кислот, ароматизатор, лаураминоксид, DTPA, полиэтилен амин этоксилат, формиат кальция, динатрия диаминостильбен дисульфонат, диметикон, тетрамин, Liquitint™ синий.
Tide Pods, Ocean Mist, Mystic Forest, Spring Meadow: линейные алкилбензолсульфонаты, C12-16 парет-9, пропиленгликоль, этоксисульфат спирта, вода, полиэтилениминэтоксилат, глицерин, соли жирных кислот, PEG-136 поливинилацетат, соль этилендиаминдиянтарной кислоты, моноэтаноламинцитрат, бисульфит натрия, диэтилентриаминпентаацетат натрия, динатрия дистирилбифенил дисульфонат, формиат кальция, маннаназа, эксилоглюканаза, формиат натрия, гидрогенизированное касторовое масло, наталаза, красители, термамил, субтилизин, бензизотиазолин, отдушка.
Tide to Go: деионизованная вода, бутиловый эфир дипропиленгликоля, алкилсульфат натрия, пероксид водорода, этанол, сульфат магния, алкилдиметиламинооксид, лимонная кислота, гидроксид натрия, триметоксибензойная кислота, ароматизатор.
Tide Stain Release Liquid: вода, алкилэтоксилат, линейный алкилбензолсульфонат, пероксид водорода, дикватерний этоксисульфат, этаноламин, динатрия дистирилбифенил дисульфонат, тетрабутил этилиденбисфенол, F&DC желтый 3, ароматизатор.
Tide Stain Release Powder: натрия перкарбонат, сульфат натрия, карбонат натрия, алюмосиликат натрия, нонаноилокси бензолсульфонат, полиакрилат натрия, вода, натрия алкилбензолсульфонат, DTPA, полиэтиленгликоль, пальмитат натрия, амилаза, протеаза, модифицированный крахмал, FD&C синий 1, ароматизатор.
Tide Stain Release, Pre Treater Spray:
вода, алкилэтоксилат, борат MEA, линейный алкилбензолсульфонат, пропиленгликоль, дикватерний этоксисульфат, кальция хлоридфермент, протеаза, этаноламин, бензoизотиазолинон, амилаза, цитрат натрия, гидроксид натрия, ароматизатор.
Tide to Go Stain Eraser: вода, алкиламиноксид, фениловый эфир дипропиленгликоля, пероксид водорода, лимонная кислота, натриевая соль этилендиаминдиянтарной кислоты, алкилсульфат натрия, ароматизатор.
Tide boost with Oxi:
бикарбонат натрия, карбонат натрия, перкарбонат натрия, этоксилат спирта, хлорид натрия, малеиновый/акриловый сополимер, нонаноилоксибензолсульфонат, сульфат натрия, красящее вещество, натриевая соль диэтилентриаминпентаацетата, гидратированный алюмосиликат (цеолит), полиэтиленгликоль, натрия алкилбензолсульфонат, пальмитат натрия, крахмал, вода, ароматизатор.
Tide Stain Release boost Duo Pac:
пленка для пакета на основе поливинилового спирта, в которую упакована жидкая часть и порошкообразная часть.
Жидкие ингредиенты: дипропиленгликоль, дикватерний этоксисульфат, вода, глицерин, LiquitintTM оранжевый. Порошкообразные ингредиенты: Перкарбонат натрия, нонаноилоксибензолсульфонат, карбонат натрия, сульфат натрия, алюмосиликат натрия, полиакрилат натрия, алкилбензолсульфонат натрия, малеиновый/акриловый сополимер, вода, амилаза, полиэтиленгликоль, пальмитат натрия, модифицированный крахмал, протеаза, глицерин, DTPA, ароматизатор.
Tide Ultra Stain Release: вода, этоксисульфат спирта натрия, линейный алкилбензолсульфонат, соли натрия/MEA, цитрат MEA, пропиленгликоль, полиэтилениминэтоксилат, этанол, диэтиленгликоль, полиэтиленимин пропоксиэтоксилат, натриевые соли жирных кислот, протеаза, бура, куменсульфонат натрия, DTPA, ароматизатор, амилаза, диаминостильбен-дисульфонат динатрия, формиат кальция, формиат натрия, глюконаза, диметикон, Liquitint™ синий, маннаназа.
Ultra Tide with a Touch of Downy® Powdered Detergent, April Fresh/Clean Breeze/April Essence: карбонат натрия, алюмосиликат натрия, сульфат натрия, линейный алкилбензолсульфонат, бентонит, вода, перкарбонат натрия, полиакрилат натрия, силикат, алкилсульфат, нонаноилоксибензолсульфонат, DTPA, полиэтиленгликоль 4000, силикон, этоксилат, ароматизатор, полиэтиленоксид, пальмитиновая кислота, диаминостильбен-дисульфонат динатрия, протеаза, Liquitint™ красный, FD&C синий 1, целлюлаза.
Ultra Tide with a Touch of Downy Clean Breeze: вода, этоксисульфат натрия на основе спирта, цитрат MEA, линейный алкилбензолсульфонат: соли натрия/MEA, пропиленгликоль, полиэтилениминэтоксилат, этанол, диэтиленгликоль, полиэтиленимин, пропоксиэтоксилат, дикватерний-этоксисульфат, сульфат спирта, диметикон, ароматизатор, бура, натриевые соли жирных кислот, DTPA, протеаза, бисульфит натрия, диаминостильбен-дисульфонат динатрия, амилаза, глюконаза, касторовое масло, формиат кальция, MEA, сополимер стирола/акрилата, формиат натрия, Liquitint™ синий.
Ultra Tide with Downy Sun Blossom: вода, этоксисульфат натрия на основе спирта, цитрат MEA, линейный алкилбензолсульфонат: соли натрия/MEA, пропиленгликоль, этанол, диэтиленгликоль, полиэтиленимин пропоксиэтоксилат, полиэтиленимин этоксилат, сульфат спирта, диметикон, ароматизатор, бура, натриевые соли жирных кислот, DTPA, протеаза, бисульфит натрия, динатрия диаминостильбен дисульфонат, амилаза, касторовое масло, формиат кальция, MEA, стирол акрилат сополимер, пропанаминия пропанамид, глюконаза, формиат натрия, Liquitint™ синий.
Ultra Tide with Downy April Fresh/Sweet Dreams: вода, этоксисульфат натрия на основе спирта, цитрат MEA, линейный алкилбензолсульфонат: соли натрия/MEA, пропиленгликоль, полиэтиленимин этоксилат, этанол, диэтиленгликоль, полиэтиленимин пропоксиэтоксилат, дикватерний этоксисульфат, сульфат спирта, диметикон, ароматизатор, бура, натриевые соли жирных кислот, DTPA, протеаза, бисульфит натрия, динатрия диаминостильбен дисульфонат, амилаза, глюконаза, касторовое масло, формиат кальция, MEA, стирол акрилат сополимер, пропанаминия пропанамид, формиат натрия, Liquitint™ синий.
Ultra Tide Free Powdered Detergent: карбонат натрия, алюмосиликат натрия, алкилсульфат, сульфат натрия, линейный алкилбензолсульфонат, вода, полиакрилат натрия, силикат, этоксилат, перкарбонат натрия, полиэтиленгликоль 4000, протеаза, динатрия диаминостильбен дисульфонат, силикон, целлюлаза.
Ultra Tide Powdered Detergent, Clean Breeze/Spring Lavender/mountain Spring: карбонат натрия, алюмосиликат натрия, сульфат натрия, линейный алкилбензолсульфонат, алкилсульфат, перкарбонат натрия, вода, полиакрилат натрия, силикат, нонаноилоксибензолсульфонат, этоксилат, полиэтиленгликоль 4000, ароматизатор, DTPA, динатрия диаминостильбен дисульфонат, пальмитиновая кислота, протеаза, силикон, целлюлаза.
Ultra Tide HE (high Efficiency) Pwdered Detergent, Clean Breeze: карбонат натрия, алюмосиликат натрия, сульфат натрия, линейный алкилбензолсульфонат, вода, нонаноилоксибензолсульфонат, алкилсульфат, полиакрилат натрия, силикат, перкарбонат натрия, этоксилат, полиэтиленгликоль 4000, ароматизатор, DTPA, пальмитиновая кислота, динатрия диаминостильбен дисульфонат, протеаза, силикон, целлюлаза.
Ultra Tide Coldwater Powdered Detergent, Fresh Scent: карбонат натрия, алюмосиликат натрия, сульфат натрия, перкарбонат натрия, алкилсульфат, линейный алкилбензолсульфонат, вода, нонаноилоксибензолсульфонат, полиакрилат натрия, силикат, этоксилат, полиэтиленгликоль 4000, DTPA, ароматизатор, Natalase, пальмитиновая кислота, протеаза, динатрий, диаминостильбен дисульфонат, FD&C синий 1, силикон, целлюлаза, алкилэфирсульфат.
Ultra Tide with bleach Powdered Detergent, Clean Breeze: карбонат натрия, алюмосиликат натрия, сульфат натрия, линейный алкилбензолсульфонат, перкарбонат натрия, нонаноилоксибензолсульфонат, алкил сульфат, вода, силикат, полиакрилат натрия, этоксилат, полиэтиленгликоль 4000, ароматизатор, DTPA, пальмитиновая кислота, протеаза, динатрия диаминостильбен дисульфонат, силикон, FD&C синий 1, целлюлаза, алкилэфирсульфат.
Ultra Tide with Febreeze Freshness™ Powdered Detergent, Spring Renewal:
карбонат натрия, алюмосиликат натрия, сульфат натрия, линейный алкилбензолсульфонат, перкарбонат натрия, алкил сульфат, вода, полиакрилат натрия, силикат, нонаноилоксибензолсульфонат, этоксилат, полиэтиленгликоль 4000, DTPA, ароматизатор, целлюлаза, протеаза, динатрия диаминостильбен дисульфонат, силикон, FD&C синий 1.
Жидкость Tide Plus with Febreeze Freshness - Sport HE Active Fresh:
вода, этоксисульфат натрия на основе спирта, цитрат MEA, линейный алкилбензолсульфонат, натриевая соль, линейный алкилбензолсульфонат: соль MEA, этоксилат спирта, натриевые соли жирных кислот, пропиленгликоль, диэтиленгликоль, полиэтиленимин этоксилат пропоксилат, дикватерний этоксисульфат, этанол, натрия куменсульфонат, бура, ароматизатор, DTPA, бисульфат натрия, динатрия диаминостильбен дисульфонат, маннаназа, целлюлаза, амилаза, формиат натрия, формиат кальция, лаураминоксид, Liquitint™ синий, диметикон/полидиметилсиликон.
Tide Plus Febreeze Freshness Spring & Renewal:
вода, этоксисульфат натрия на основе спирта, линейный алкилбензолсульфонат: соли натрия/MEA, цитрат MEA, пропиленгликоль, полиэтилениминэтоксилат, ароматизатор, этанол, диэтиленгликоль, полиэтиленимин пропоксиэтоксилат, протеаза, сульфат спирта, бура, натриевые соли жирных кислот, DTPA, динатрия диаминостильбен дисульфонат, MEA, маннаназа, глюконаза, формиат натрия, диметикон, Liquitint™ синий, тетрамин.
Liquid Tide Plus with Febreeze Freshness, Sport HE Victory Fresh: вода, этоксисульфат натрия на основе спирта, цитрат MEA, линейный алкилбензолсульфонат, натриевая соль, линейный алкилбензолсульфонат: соль MEA, этоксилат спирта, натриевые соли жирных кислот, пропиленгликоль, диэтиленгликоль, полиэтиленимин этоксилат пропоксилат, дикватерний-этоксисульфат, этанол, куменсульфонат натрия, бура, ароматизатор, DTPA, бисульфат натрия, динатрия диаминостильбен дисульфонат, маннаназа, целлюлаза, амилаза, формиат натрия, формиат кальция, лаураминоксид, Liquitint™ синий, диметикон/полидиметилсиликон.
Tide Vivid White+Bright Powder, Original:
карбонат натрия, алюмосиликат натрия, сульфат натрия, линейный алкилбензолсульфонат, перкарбонат натрия, нонаноилоксибензолсульфонат, алкил сульфат, вода, силикат, полиакрилат натрия этоксилат, полиэтиленгликоль 4000, ароматизатор, DTPA, пальмитиновая кислота, протеаза, динатрия диаминостильбен дисульфонат, силикон, FD&C синий 1, целлюлаза, алкилэфирсульфат.
Моющее средство HEY SPORT TEX WASH
Вода, додецилбензолсульфокислота, лаурет-11, пег-75 ланолин, пропиленгликоль, денат. спирт, соят калия, гидроксид калия, динатрия кокоамфодиацетат, этилендиаминтриацетат кокосалкилацетамид, отдушка, рицинолеат цинка, хлорид натрия, бензизотиазолинон, метилизотиазолинон, ci 16255, бензиловый спирт.
Продукты под названиями Tide, Ariel, Gain и Fairy являются коммерчески доступными продуктами, поставляемыми Procter & Gamble. Продукты под названием Persil являются коммерчески доступными продуктами, поставляемыми Unilever и Henkel. Продукты под названием Hey Sport являются коммерчески доступными продуктами, поставляемыми Hey Sport.
40%) по весу содержащего группу сульфовой кисоты мономера (B); и где средний молекулярный вес составляет от приблизительно 23000 до приблизительно 50000, предпочтительно
в диапазоне от приблизительно 25000 до приблизительно 38000, как описано в WO2014032269.
40 вес. %
обладающая ферментной активностью от приблизительно 10 мг до приблизительно 50 мг активного фермента/г)
от приблизительно 10 мг до приблизительно 50 мг активного фермента/г)
содержащий отдушку цеолит и любая их комбинация)
Все уровни ферментов выражены в виде приблизительного количества активного белка-фермента на 100 г моющей композиции. Ингредиенты, выступающие в качестве поверхностно-активных веществ, могут быть получены из BASF, Людвигсхафен, Германия (Lutensol(R)); Shell Chemicals, Лондон, Великобритания; Stepan, Норфилд, III, США; Huntsman, Huntsman, Солт-Лейк-Сити, Юта, США; Clariant, Зульцбах, Германия (Praepagen(R)).
Натрия триполифосфат может быть получен от Rhodia, Париж, Франция.
Цеолит может быть получен от Industrial Zeolite (Великобритания) Ltd, Грейс, Эссекс, Великобритания. Лимонная кислота и цитрат натрия могут быть получены от Jungbunzlauer, Базель, Швейцария.
NOBS представляет собой нонаноилоксибензолсульфонат натрия, поставляемый Eastman, Бейтсвил, Арканзас, США.
TAED означает тетраацетилэтилендиамин, поставляемый под торговым названием Peractive(R) от Clariant GmbH, Зульцбах, Германия.
Карбонат натрия и бикарбонат натрия могут быть получены от Solvay, Брюссель, Бельгия.
Полиакрилат, сополимеры полиакрилата/малеата могут быть получены от BASF, Людвигсхафен, Германия.
Repel-O-Tex(R) могут быть получены от Rhodia, Париж, Франция.
Texcare(R) может быть получен от Clariant, Зульцбах, Германия. Перкарбонат натрия и карбонат натрия могут быть получены от Solvay, Хьюстон, Техас, США.
Соль Na изомера этилендиамин-N,N'-диянтарной кислоты, (S,S) (EDDS) поставляется Octel, Элсмир-Порт, Великобритания.
Гидроксиэтандифосфонат (HEDP) поставляется Dow Chemical, Мидланд, Мичиган,
США.
Ферменты Savinase(R), Savinase(R) Ultra, Stainzyme(R) Plus, Lipex(R), Lipolex(R), Lipoclean(R), Celluclean(R), Carezyme(R), Natalase(R), Stainzyme(R), Stainzyme(R) Plus, Termamyl(R), Termamyl(R) ultra и Mannaway(R) могут быть получены от Novozymes, Багсверд, Дания.
Ферменты Purafect(R), FN3, FN4 и Optisize могут быть получены от Genencor International
Inc., Пало-Альто, Калифорния, США.
Красители Direct violet 9 и 99 могут быть получены от BASF DE, Людвигсхафен, Германия. Краситель Solvent violet 13 может быть получен от Ningbo Lixing Chemical Co., Ltd. Нинбо, Чжэцзян, Китай. Отбеливатели могут быть получены от Ciba Specialty Chemicals, Базель, Швейцария.
Все процентные содержания и отношения рассчитаны по весу, если не указано иное. Все процентные содержания и отношения рассчитаны на основании общей композиции, если не указано иное. Следует понимать, что каждое максимальное количественное ограничение, приведенное по всему данному описанию, включает каждое более низкое количественное ограничение, как если бы такие более низкие количественные ограничения были явно описаны в данном документе. Каждое минимальное количественное ограничение, приведенное по всему данному описанию, будет включать каждое более высокое количественное ограничение, как если бы такие более высокие количественные ограничения были явно описаны в данном документе. Каждая область числовых значений, приведенная по всему данному описанию, будет включать каждую более узкую область числовых значений, которая входит в данную более широкую область числовых значений, как если бы такие более узкие области числовых значений были явно описаны в данном документе.
Анализы стирки
Система-модель для стирки Launder-O-Meter (LOM)
Launder-O-Meter (LOM) представляет собой систему-модель для стирки среднего масштаба, которую можно применять для исследования не более 20 различных условий стирки одновременно. LOM, по сути, представляет собой большую терморегулируемую водяную баню с 20 закрытыми металлическими лабораторными стаканами, вращающимися внутри нее. Каждый лабораторный стакан представляет собой одну небольшую стиральную машину, и при этом в ходе эксперимента каждая из них содержит раствор конкретной системы моющее средство/фермент, исследование которой предусматривается, вместе с загрязненными и незагрязненными тканями, с использованием которых проводится ее исследование. Механическое воздействие достигается за счет вращения лабораторных стаканов на водяной бане и помещения металлических шариков в лабораторный стакан.
Система-модель для стирки LOM главным образом используется для исследования моющих средств и ферментов в среднем масштабе при условиях стирки, характерных для Европы. В эксперименте с LOM такие факторы, как отношение балласта к грязи и отношение ткани к моющей жидкости могут варьироваться. Следовательно, LOM предусматривает связь между экспериментами малого масштаба, такими как AMSA и стирка в малом масштабе, и более затратными по времени полномасштабными экспериментами в стиральных машинах с фронтальной загрузкой.
Система-модель для стирки Mini Launder-O-Meter (MiniLOM)
MiniLOM представляет собой модифицированную систему стирки в малом масштабе Launder-O-Meter (LOM), которая представляет собой систему-модель для стирки среднего масштаба, которую можно применять для исследования не более 20 различных условий стирки одновременно. LOM по сути представляет собой большую терморегулируемую водяную баню с 20 закрытыми металлическими лабораторными стаканами, вращающимися внутри нее. Каждый лабораторный стакан представляет собой одну небольшую стиральную машину, и при этом в ходе эксперимента каждая из них содержит раствор конкретной системы моющее средство/фермент, исследование которой предусматривается, вместе с загрязненными и незагрязненными тканями, с использованием которых проводится ее исследование. Механическое воздействие достигается за счет вращения лабораторных стаканов на водяной бане и помещения металлических шариков в лабораторный стакан.
Система-модель для стирки LOM главным образом используется для исследования моющих средств и ферментов в среднем масштабе при условиях стирки, характерных для Европы. В эксперименте с LOM такие факторы, как отношение балласта к грязи и отношение ткани к моющей жидкости могут варьироваться. Следовательно, LOM предусматривает связь между экспериментами малого масштаба, такими как AMSA и стирка в малом масштабе, и более затратными по времени полномасштабными экспериментами в стиральных машинах с фронтальной загрузкой.
В системе MiniLOM все стирки осуществляли в пробирках объемом 50 мл, помещенных в ротатор Stuart.
Анализ стирки Terg-O-tometer (TOM)
Tergo-To-Meter (TOM) представляет собой систему-модель для стирки среднего масштаба, которую можно применять для исследования 12 различных условий стирки одновременно. По существу, TOM представляет собой большую терморегулируемую водяную баню с не более чем 12 открытыми металлическими лабораторными стаканами, погруженными в нее. Каждый лабораторный стакан представляет собой одну небольшую стиральную машину с вертикальной загрузкой, и при этом в течение эксперимента каждая из них содержит раствор конкретной системы моющее средство/фермент и загрязненные и незагрязненные ткани, с использованием которых проводится исследование ее эффективности. Механическое воздействие достигается за счет вращения лопасти мешалки, которая перемешивает жидкость в каждом лабораторном стакане. Поскольку у лабораторных стаканов в TOM нет крышки, возможно извлекать образцы в течение эксперимента и анализа TOM для оперативного получения информации в процессе стирки.
Система-модель для стирки TOM главным образом используется для исследования моющих средств и ферментов в среднем масштабе при условиях стирки, характерных для США или LA/AP. В эксперименте TOM такие факторы, как отношение балласта к грязи и отношение ткани к моющей жидкости, могут варьироваться. Следовательно, TOM предусматривает связь между экспериментами малого масштаба, такими как AMSA и стирка в малом масштабе, и более затратными по времени полномасштабными экспериментами в стиральных машинах с вертикальной загрузкой.
Оборудование: водяная баня с 12 стальными лабораторными стаканами и 1 вращающейся лопастью на лабораторный стакан с вместимостью 500 или 1200 мл моющей жидкости. Температура находится в диапазоне от 5 до 80°C. Водяную баню следует заполнять деионизированной водой. Скорость вращения может быть установлена на 70-120 об./мин.
Устанавливают температуру в Terg-O-Tometer и начинают вращение на водяной бане. Ожидают до выравнивания температуры (допустимое отклонение составляет +/- 0,5°C). Все лабораторные стаканы должны быть очищены и не должны содержать следов предыдущего исследуемого материала.
Моющий раствор с необходимым количеством моющего средства, температурой и жесткостью воды готовят в сосуде. Обеспечивают возможность растворения моющего средства в течение магнитного перемешивания в течение 10 мин. Моющий раствор следует применять в течение 30-60 мин. после получения.
800 мл моющего раствора добавляют в лабораторный стакан TOM. Моющий раствор перемешивают со скоростью 120 об./мин. и в лабораторный стакан добавляют необязательно один или несколько ферментов. В лабораторный стакан высыпают образцы, а затем балластную загрузку. Измерение времени начинают, когда образцы и балласт добавляют в лабораторный стакан. Образцы промывают в течение 20 минут, после чего перемешивание завершают. Моющую загрузку затем переносят из лабораторного стакана TOM на сито и прополаскивают холодной водопроводной водой. Твердые образцы отделяют от балластной загрузки. Образцы грязи переносят в лабораторный стакан на 5 л с холодной водопроводной водой под проточной водой в течение 5 минут. Балластную загрузку выдерживают отдельно для следующей инактивации. Воду осторожно выжимают из образцов рукой и их помещают в поддон, покрытый бумагой. Другой лист бумаги помещают поверх образцов. Обеспечивают высушивание образцов в течение ночи перед проведением анализа образцов, такого как определение устранения запаха, как описано в примере 7.
Полномасштабная стирка
Данная стирка представляет собой метод исследования эффективности ДНКазы при полномасштабной стирке при условиях ЕС (стирка в стиральной машине с фронтальной загрузкой).
При каждой стирке добавляют реальные изделия (футболки) и балласт, вместе с моющим средством и ферментом. После стирки реальные изделия (футболки) сушат. После сушки вырезают круглые образцы и промывают моющим средством при добавлении грязи (загрязняющее моющее средство) в miniLOM. Цветовое различие измеряют на спектрофотометре MacBeth Color Eye.
Ферменты добавляют на основе весовых процентов дозировки моющего средства в каждой промывке.
Применяемое оборудование:
• стиральная машина: Miele Softtronic W2445;
• счетчики воды и система автоматического сбора данных;
• спектрофотометр MacBeth Color Eye.
Для получения и регулирования жесткости воды необходимы следующие ингредиенты:
• хлорид кальция (CaCl2⋅2H2O);
• хлорид магния (MgCL2⋅6H2O);
• гидрокарбонат натрия (NaHCO3).
Балласт:
балласт состоит из чистой белой ткани, изготовленной из хлопка, синтетического сложного полиэфира или хлопка/синтетического сложного полиэфира, без оптического осветлителя. Состав балласта представляет собой смесь различных изделий при соотношении хлопок/синтетический сложный полиэфир 65/35, в зависимости от веса. Вес балласта, сухость и состав изделий должны быть одинаковыми в каждой стирке.
После каждой стирки балласт инактивируют в промышленной стиральной машине при 85°C/15 мин. или при стирке при 95°C (машина ЕС) без моющего средства.
Пример балласта (состав балласта, стандарт ЕС, итого 3 кг):
• 3 футболки (100% хлопка);
• 10 рубашек с короткими рукавами (55% хлопка, 45% синтетического сложного полиэфира);
• 4 наволочек (35% хлопка, 65% синтетического сложного полиэфира),110×75 см;
• 1 небольшая простыня размером 100×75 см (100% хлопка);
• 3 чайных полотенца (100% хлопка);
• носки (80% хлопка, 20% синтетического сложного полиэфира) в качестве баланса.
Условия стирки:
• температура: 30°C;
• программа стирки: нормальная стирка хлопка без предварительной стирки: хлопчатобумажная ткань;
• уровень воды 13-14 л с "water plus";
• жесткость воды: стандартные условия ЕС: 15°dH, Ca2+:Mg2+:HCO3=4:1:7,5;
• доза ДНКазы: 1 ppm.
Подробные стадии проведения полномасштабной испытательной стирки
1. Выбирают программу стирки согласно плану исследования.
2. Моющее средство и ДНКазу помещают в стиральный барабан в "стирочный шар" (моющие средства, как жидкие, так и в форме порошка). Его помещают в нижнюю часть.
3. Реальные изделия (футболки) и балласт помещают в стиральный барабан.
4. Запускают цифровой счетчик воды
5. Запускают стиральную машину, нажимая на кнопку СТАРТ
6. После стирки реальные изделия (футболки) и балласт достают, помещая реальные изделия в сушильную комнату.
Процедура сушки
Изделия кладут на поддон или развешивают на веревке и сушат при комнатной температуре. В комнате имеется де-увлажнитель воздуха работающий в течение 24 ч в день, чтобы поддерживать комнату сухой.
Оценка
Круглые образцы из футболок (подмышки, лицевая сторона, спина и край) вырезают и промывают в miniLOM с загрязняющим моющим средством, добавляющим грязь. Образцы оценивают с помощью измерения цветового различия (L-значения), измеренного с использованием Color Eye (отражательный спектрофотометр Macbeth Color Eye 7000). Измерения осуществляли без УФ-излучения в отраженном свете и L-значение выделяли из цветового пространства CIE Lab.
Ферментные анализы
Анализ I
Анализ I: исследование ДНКазной активности
ДНКазную активность определяли на агаре для теста на ДНКазу с метиловым зеленым (BD, Франклин Лейкс, Нью-Джерси, США), который готовили в соответствии с инструкцией производителя. Вкратце, 21 г агара растворяли в 500 мл воды и затем автоклавировали в течение 15 мин. при 121°C. Температуру автоклавированного агара доводили до 48°C на водяной бане, и 20 мл агара выливали в чашки Петри, и обеспечивали отверждение при инкубации в течение ночи при комнатной температуре. В планшеты с отвержденным агаром добавляли 5 мкл растворов фермента, и ДНКазную активность наблюдали в виде бесцветных зон вокруг точечных растворов фермента.
Анализ II
Анализ E-2-ноненаля на текстильном изделии с использованием электронного анализатора запахов.
Один из способов исследования присутствия неприятного запаха на текстильных изделиях состоит в использовании E-2-ноненаля в качестве маркера для неприятного запаха, поскольку данное соединение вызывает неприятный запах при стирке.
Раствор E-2-ноненаля добавляли на текстильный образец 5 см x 5 см и образец помещали в стеклянный флакон для анализа GC на 20 мл, и закупоривали флакон. Анализировали 5 мл свободного пространства над образцом из закупоренных флаконов в электронном анализаторе запахов Heracles II от Alpha M.O.S., Франция (хроматографический газовый анализатор с двойной колонкой с 2 FID, колонка 1: MXT5 и колонка 2: MXT1701) после 20 минут инкубации при 40°C.
Примеры
Пример 1
Обнаружение эффектов глубокой очистки на футболках для бега
Две белые футболки для бега, изготовленные из 100% синтетического сложного полиэфира, предварительно стирали (полномасштабная стирка) в стиральной машине с использованием 3,33 г/л моющего средства-модели A.
Две футболки носились испытуемым (мужчиной), одна футболка за раз. Испытуемый носил каждую из футболок во время физической активности в течение одного часа. После ношения одну футболку стирали в стиральной машине с использованием 3,33 г/л моющего средства-модели A с ДНКазой под SEQ ID NO: 7 (1 ppm), тогда как вторую футболку стирали в стиральной машине с использованием 3,33 г/л моющего средства-модели A без ДНКазы (0 ppm). Футболки стирали, как описано для полномасштабной стирки, описанной выше, и для стирки применяли 15 л водопроводной воды. Обе футболки носили во время физической активности, а затем стирали. Такой цикл ношения и стирки повторяли 10 раз.
Для оценки эффекта очистки (эффекта глубокой очистки) пять круглых образцов (диаметром 2 см) вырезали из подмышки, спины (верхняя часть спины, между лопатками), лицевой стороны (грудь) и нижнего переднего края футболок. Пять образцов, соответственно подмышек, спины, лицевой стороны и края, смешивали с пятью стерильными образцами из синтетического сложного полиэфира WFK30A в пробирке объемом 50 мл и добавляли 10 мл моющей жидкости, полученной с помощью добавления в воду 3,33 г/л моющего средства-модели A, добавляли 0,7 г/л грязи (Pigmentschmutz, 09V, wfk, Крефельд, Германия). Пробирки помещали в ротатор Stuart (miniLOM) в течение 1 часа при 30°С и промывали в соответствии с вышеописанным miniLOM. Образцы дважды прополаскивали 10 мл водопроводной воды и сушили на фильтровальной бумаге в течение ночи.
Цветовое различие (L-значение) измеряли с использованием Color Eye (отражательного спектрофотометра Macbeth Color Eye 7000). Измерения осуществляли без УФ-излучения в отраженном свете и L-значение выделяли из цветового пространства CIE Lab. Белое текстильное изделие характеризуется высоким L-значением. Таким образом, чем ΔL выше, тем текстильное изделие белее.
Результат ниже показывает, что стирка с ДНКазой на протяжении 10 стирок предотвращает оседание грязи в последующем процессе стирки. Кроме того, результаты показывают, что стирка с ДНКазой на протяжении 10 стирок улучшает белизну текстильного изделия.
Пример 2
Эффективность глубокого очищения в жидком моющем средстве после 2 стирок
Один штамм Brevundimonas sp., выделенный из белья для стирки, применяли в настоящем примере. Brevundimonas sp. предварительно выращивали в соевой среде на триптон-соевом агаре (TSA) (pH 7,3) (CM0131; Oxoid Ltd, Бейзингстоук, Великобритания) в течение 2-5 дней при 30°C. Из одной колонии целую петлю переносили в 10 мл TSB (триптон-соевый бульон, Oxoid) и инкубировали в течение 16 часов при 30°C со встряхиванием (240 об./мин.). После культивирования Brevundimonas sp. осаждали с помощью центрифугирования (Sigma Laboratory Centrifuge 6K15) (3000 g при 21°C в течение 7 мин.) и повторно суспендировали в 10 мл TSB, дважды разбавленного водой качества Milli-Q. Оптическую плотность (OD) при 600 нм измеряли с использованием спектрофотометра (POLARstar Omega (BMG Labtech, Ортенберг, Германия). Свежеполученный TSB, дважды разбавленный стерильной водой качества Milli-Q, инокулировали Brevundimonas sp. до OD600 нм 0,03 и 1,6 мл добавляли в каждую лунку 12-луночного полистирольного микропланшета с плоским дном (3512; Corning Incorporated, Корнинг, Нью-Йорк, США), в который помещали круглый образец (диаметр 2 см) стерильного синтетического сложного полиэфира WFK30A. Соответственно, через 24 ч и 72 ч инкубации при 15°C при встряхивании (100 об./мин.) питательную среду удаляли и образцы дважды прополаскивали 0,9% (вес./об.) NaCl.
При стирке 1 пять прополосканных образцов с Brevundimonas sp., полученных выше (донорских образцов), смешивали с пятью образцами стерильного синтетического сложного полиэфира WFK30A (меченные образцы) в пробирке объемом 50 мл и добавляли 10 мл моющей жидкости, полученной с помощью добавления в воду 3,33 г/л моющего средства-модели A и ДНКазы под SEQ ID NO: 2 (0,04 ppm). Стирки с моющим средством-моделью A без добавления ДНКазы проводили параллельно. Пробирки помещали в ротатор Stuart (miniLOM) в течение 1 часа при 30°С и промывали в соответствии с вышеописанным miniLOM. Образцы дважды прополаскивали водопроводной водой и сушили на фильтровальной бумаге в течение ночи.
При стирке 2 пять высушенных донорских и меченных образцов из стирки 1 стирали в пробирке объемом 50 мл, добавляли 10 мл моющей жидкости, полученной с помощью добавления в воду 3,33 г/л моющего средства-модели A и 0,7 г/л грязи (Pigmentschmutz, 09V, wfk, Крефельд, Германия). Пробирки помещали в ротатор Stuart в течение 1 часа при 30°С и промывали в соответствии с вышеописанным miniLOM. Образцы дважды прополаскивали водопроводной водой и сушили на фильтровальной бумаге в течение ночи.
Цветовое различие (L-значения) измеряли с использованием Color Eye (отражательного спектрофотометра Macbeth Color Eye 7000). Измерения осуществляли без УФ-излучения в отраженном свете и L-значение выделяли из цветового пространства CIE Lab. Белое текстильное изделие характеризуется высоким L-значением. Таким образом, чем ΔL выше, тем текстильное изделие белее.
Результаты, представленные в таблице ниже, показывают, что L-значения измеряли после стирки 2. Результаты показывают, что стирка с ДНКазой при стирке 1 предотвращает оседание грязи в последующем процессе стирки без присутствия ДНКазы. Кроме того, результаты показывают, что стирка с ДНКазой на протяжении 10 стирок улучшает белизну текстильного изделия.
Пример 3
Определение запаха пота на футболках для бега
Две белые футболки для бега, изготовленные из 100% синтетического сложного полиэфира, предварительно стирали в стиральной машине (полномасштабная стирка) с использованием 3,33 г/л моющего средства-модели A.
Две футболки носились испытуемым (мужчиной), одна футболка за раз. Испытуемый носил каждую из футболок во время физической активности в течение одного часа. После ношения одну футболку стирали в стиральной машине с использованием 3,33 г/л моющего средства-модели A с ДНКазой под SEQ ID NO: 7 (1 ppm), тогда как вторую футболку стирали в стиральной машине с использованием 3,33 г/л моющего средства-модели A без ДНКазы (0 ppm). Футболки стирали, как описано для полномасштабной стирки, описанной выше, и для стирки применяли 15 л водопроводной воды. Обе футболки носили во время физической активности, а затем стирали. Этот цикл ношения и стирки повторяли 10 раз.
Для оценки запаха тренированный испытуемый перед применением исследовал футболки в отношении запаха пота (неприятного запаха) путем оценки запаха футболок. Если обнаруживался запах пота, то в таблице ниже добавляли отметку (X). Наблюдения ниже показывают, что стирка с ДНКазой на протяжении 10 стирок предотвращает накопление запаха в последующем процессе стирки, где ДНКазу не применяли.
Таблица 1
с ДНКазой
Пример 4
Эксперимент стирки осуществляли на коллекции одежды для бега (свитера и футболки для бега), которые носили во время тренировочных упражнений по меньшей мере 50 раз. Во время тренировочных упражнений предметы одежды для бега становились сырыми от пота, но в целом не загрязнялась. Предметы одежды для бега предварительно стирали в Miele Softtronic W5825 при 30°C (низкое заполнение машины) с использованием BioTex Black (Unilever) в рекомендованной стандартной дозе.
Перед проведением настоящего эксперимента свитер и футболку для бега (100% синтеического сложного полиэфира) оценивались подготовленным членом группы оценки запаха, который обнаружил выраженный запах кислого пота (неприятный запах), в частности, присутствующий в подмышечных областях на предметах одежды. Неприятный запах присутствовал после стирки предметов одежды с использованием BioTex Black и неприятный запах накапливался с числом применений предметов одежды для бега.
Одежду для бега стирали в Miele Softtronic W5825 при 30°C (низкое заполнение машины) с использованием стандартной дозы BioTex Black и дозы ДНКазы A. oryzae (0,4 ppm).
После каждого тренировочного упражнения предметы одежды для бега подвергали другому кругу оценивания участником группы оценки запаха. Участник группы оценки запаха обнаруживал, что неприятный запах значительно уменьшался и его было трудно определить после 1-3 циклов стирки в присутствии ДНКазы A. oryzae по настоящему изобретению. В расширенном исследовании предметы одежды для бега стирали в присутствии ДНКазы A. oryzae по настоящему изобретению каждый раз, когда одежду стирали. Участник группы оценки запаха обнаружил, что если предметы одежды для бега стирали в присутствии ДНКазы A. oryzae, ее можно носить по меньшей мере два тренировочных упражнения (обеспечивая высыхание предметов одежды без стирки предметов одежды между тренировочными упражнениями) до того, как неприятный запах становился четко определяемым.
Пример 5
Устранение запаха ДНКазой (электронный анализатор запахов)
Получение образцов ДНК с E-2-ноненалем
Хромосомную ДНК из Pseudomonas sp. выделяли с помощью QIAamp DNA Blood Mini Kit, следуя инструкциям производителя (Qiagen, Хильден, Германия). Образцы синтетического сложного полиэфира (WFK30A) (2 см в диаметре) стерилизовали в автоклаве Holm & Halby Systec DB-23 в течение 60 минут при 121°C. 100 мкл очищенной ДНК Pseudomonas sp., разбавленной до конечной концентрации 1 нг/мкл, добавляли к каждому из автоклавированных образцов и образцы высушивали в стеллаже с постоянным ламинарным потоком воздуха в течение 2 часов. После высушивания 10 образцов с ДНК помещали в стерильную пробирку NUNC объемом 25 мл (364238; Thermo Scientific) и добавляли 10 мл 0,2 мМ E-2-ноненаля (255653; Sigma-Aldrich) (анализ II). Пробирку помещали в ротатор Stuart (miniLOM) (20 об./мин. при комнатной температуре в течение 20 мин.). 10 образцов переносили в центрифужную пробирку 50.000 MWCO (VS203, Vivaspin 20, Satorius). Пробирки центрифугировали с 3000 g при 21°C в течение 1 мин. и 10 образцов разделяли между 2 стерильными пробирками NUNC (364238; Thermo Scientific) по 5 образцов в каждой пробирке. Кроме того, 5 стерильных образцов синтетического сложного полиэфира (WFK30A) (2 см в диаметре) без ДНК и E-2-ноненаля добавляли в каждую из данных пробирок. Образцы без ДНК отмечали, обеспечивая возможность отличия от образцов с ДНК/E-2-ноненалем.
Процедура стирки образцов ДНК с E-2-ноненалем
Моющую жидкость порошка Ariel Actilift powder Style&Color и порошка Ariel Actilift powder White готовили путем растворения 5,0 г моющего средства в 1000 мл стерильной воды качества Milli-Q с жесткостью 15 dH (условия ЕС). Моющую жидкость Tide Pods готовили путем растворения 1,8 г белой фазы моющего средства в 1000 мл стерильной воды качества Milli-Q с жесткостью 6 dH. Моющие жидкости оставляли на магнитной мешалке в течение 20 мин. перед применением.
Моющую жидкость (10 мл) добавляли в каждую из двух идентичных пробирок с 5 образцами ДНК с E-2-ноненалем и в одну из пробирок добавляли 5 стерильных образцов, 10 мкл ДНКазы Apergillus oryzae по настоящему изобретению, полученной в результате в конечной концентрации 5 ppm. Пробирки помещали в ротатор Stuart (20 об./мин. при 30°C в течение 60 мин.). Моющую жидкость выливали и образцы дважды прополаскивали 20 мл стерильной воды качества Milli-Q с жесткостью 15°dH. Образцы из каждой пробирки переносили в центрифужную пробирку 50.000 MWCO (VS203, Vivaspin 20, Satorius) и центрифугировали при 3000 g при 21°C в течение 1 мин. Каждый образец с E-2-ноненалем затем переносили в GC-флакон для хроматографирования на 20 мл с использованием чистых стерильных пинцетов для помещения каждого образца в каждый флакон. Затем их анализировали в электронном анализаторе запахов Alpha MOS HERACLES Flash Gas Chromatography, оснащенном капиллярной колонкой Restek MXT-5 с автоматическим пробоотборником HS100 и детектором FID.
Таблица 2. Интенсивность E-2-ноненаля, измеренная с помощью электронного анализатора запахов
(без ДНКазы)
(с ДНКазой)
Вывод: захваченный ДНК запах на текстильном изделии может быть устранен с помощью ДНКазы Apergillus oryzae, приводя таким образом к уменьшению запаха.
Пример 6
Устранение запаха с помощью ДНКазы (сенсорный анализ)
Образцы синтетического сложного полиэфира и хлопка (2 см в диаметре) загрязняли ДНК Pseudomonas sp. и 0,5 мМ E-2-ноненаля (255653; Sigma Aldrich) (см. пример 5 относительно подробностей получения образцов ДНК) и стирали в ротаторе Stuart (miniLOM) в течение 60 мин. при 30°C в моющем средстве-модели A (полученном с помощью растворения 3,33 г в 1 литре воды качества Milli-Q с жесткостью 15°dH) в присутствии или в отсутствие ДНКазы Apergillus oryzae по настоящему изобретению (5 ppm). После стирки образцы дважды прополаскивали в 20 мл воды качества Milli-Q с жесткостью 15°dH. Образцы оценивали в отношении предполагаемой интенсивности E-2-ноненаля четырьмя участниками группы оценки запаха (образцы были замаскированы). Для оценки предполагаемой интенсивности применяли шкалу от 0 до 9. 0 обозначал отсутствие предполагаемой интенсивности E-2-ноненаля, тогда как 9 указывало на наивысшую предполагаемую интенсивность E-2-ноненаля. Результаты продемонстрировали согласованность между всеми четырьмя участниками группы оценки запаха.
Таблица 3
Захваченный ДНК запах на текстильном изделии может быть устранен с помощью ДНКазы Apergillus oryzae, приводя, таким образом, к уменьшению запаха.
Пример 7
Анализ визуального определения устранения запаха
Brevundimonas sp. предварительно выращивали в соевой среде с агаром Tryptone (TSA) (pH 7,3) (CM0131; Oxoid Ltd, Бейзингстоук, Великобритания) в течение 2-5 дней при 30°C. Из одной колонии целые петли переносили в 10 мл TSB и инкубировали в течение 20 часов при 30°C со встряхиванием (240 об./мин.). После культивирования, Brevundimonas sp. осаждали с помощью центрифугирования (Sigma Laboratory Centrifuge 6K15) (3000 g при 21°C в течение 7 мин.) и повторно суспендировали в 10 мл TSB, дважды разбавленном водой. Оптическую плотность (OD) при 600 нм измеряли с использованием спектрофотометра (POLARstar Omega (BMG Labtech, Ортенберг, Германия). Свежеприготовленный TSB, дважды разбавленный водой, инокулировали до OD 600 нм 0,03 и добавляли 20 мл в чашку Петри, в которую помещали образец стерильного синтетического сложного полиэфира WFK30A 5 см x 5 см. После инкубации (24 ч при 15°C при встряхивании (75 об./мин.) образцы дважды прополаскивали 0,9% (вес./об.) NaCl. Образцы стирали в TOM либо непосредственно после полоскания, либо после высушивания в течение 24 часов в стеллаже LAF.
Средство для визуального определения феноловый красный в растворе получали путем растворения 0,1 г в 100 мл 99% этанола. Индикаторный раствор (50 мкл) добавляли на фильтровальную бумагу (диаметр 2 см) и высушивали в течение ночи в вытяжном шкафу с образованием захватывающего запах средства, содержащего средство для визуального определения (феноловый красный). Четыре выстиранных образца помещали на дно стеклянного контейнера (один контейнер на каждый образец) и добавляли 500 мкл 17% TSB. В качестве контроля выстиранное чистое текстильное изделие из синтетического сложного полиэфира помещали на дно другого стеклянного контейнера и добавляли 500 мкл 17% TSB. Контейнеры с образцами инкубировали при 37°C. Контейнеры изучали до 48 часов для определения изменения цвета меченного феноловым красным образца.
Таблица 4. Результаты инкубации
Часы в таблице указывают на моменты времени для обнаруженного изменения цвета.










| название | год | авторы | номер документа |
|---|---|---|---|
| МОЮЩАЯ КОМПОЗИЦИЯ | 2015 |
|
RU2737535C2 |
| Чистящие композиции, содержащие варианты амилазы в соответствии с перечнем последовательностей | 2012 |
|
RU2617954C2 |
| ВАРИАНТЫ ПРОТЕАЗЫ И КОДИРУЮЩИЕ ИХ ПОЛИНУКЛЕОТИДЫ | 2014 |
|
RU2670946C9 |
| ПОЛИПЕПТИДЫ С ЛИЗОЦИМНОЙ АКТИВНОСТЬЮ И ПОЛИНУКЛЕОТИДЫ, КОДИРУЮЩИЕ ИХ | 2012 |
|
RU2619051C2 |
| ВАРИАНТЫ СУБТИЛАЗЫ И КОДИРУЮЩИЕ ИХ ПОЛИНУКЛЕОТИДЫ | 2015 |
|
RU2710720C2 |
| ВАРИАНТЫ ЛИПАЗЫ И КОМПОЗИЦИИ В ВИДЕ МИКРОКАПСУЛ, СОДЕРЖАЩИЕ ТАКИЕ ВАРИАНТЫ ЛИПАЗЫ | 2018 |
|
RU2779301C2 |
| Способы и композиции, содержащие варианты сериновой протеазы | 2012 |
|
RU2663114C2 |
| МОЮЩАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ВАРИАНТ КСИЛОГЛЮКАНАЗЫ СЕМЕЙСТВА 44 | 2009 |
|
RU2525669C2 |
| ПРИМЕНЕНИЕ ВАРИАНТОВ ПРОТЕАЗЫ | 2010 |
|
RU2639534C2 |
| МОЮЩИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ЛИПАЗЫ | 2018 |
|
RU2775700C2 |
Настоящее изобретение относится к применению полипептида, обладающего дезоксирибонуклеазной (ДНКазной) активностью, для предотвращения или уменьшения повторного осаждения грязи на изделии в ходе процесса последующей чистки или стирки. Описано применение полипептида, обладающего ДНКазной активностью, для предотвращения или уменьшения повторного осаждения грязи или запаха на изделии в ходе процесса стирки, где изделие представляет собой текстильное изделие. Изобретение относится также к моющей композиции, содержащей полипептид, обладающий дезоксирибонуклеазной активностью (ДНКаза), и способу предотвращения или уменьшения повторного осаждения грязи на изделии в ходе процесса последующей чистки или стирки. Технический результат - эффективное удаление пятен и глубокая очистка ткани. 4 н. и 11 з.п. ф-лы, 4 табл., 7 пр.
1. Применение полипептида, обладающего ДНКазной активностью, для предотвращения или уменьшения повторного осаждения грязи или запаха на изделии в ходе процесса стирки, где изделие представляет собой текстильное изделие.
2. Применение по п. 1, где полипептид, обладающий ДНКазной активностью, не присутствует в ходе процесса последующей чистки или стирки.
3. Применение по любому из пп. 1, 2 для предотвращения или уменьшения прилипания грязи и/или запаха к изделию.
4. Применение по любому из пп. 1-3 для поддержания или улучшения белизны изделия.
5. Применение по любому из пп. 1-4 для предотвращения или уменьшения неприятного запаха, исходящего от изделия.
6. Применение по любому из пп. 1-5, где полипептид, обладающий ДНКазной активностью, применяется для чистки или стирки изделия по меньшей мере один раз перед процессом последующей чистки или стирки.
7. Применение по любому из пп. 1-6, где полипептид, обладающий ДНКазной активностью, применяется для чистки или стирки изделия по меньшей мере два раза, три раза, четыре раза, пять раз, шесть раз, семь раз, восемь раз, девять раз или десять раз перед процессом последующей чистки или стирки.
8. Моющая композиция, содержащая полипептид, обладающий дезоксирибонуклеазной (ДНКазной) активностью, и поверхностно-активное вещество, где композиция соответствует по меньшей мере одному из а) или b):
а) композиция дополнительно содержит средство для контроля запаха; и/или
b) поверхностно-активное вещество не является катионным поверхностно-активным веществом.
9. Композиция по п. 8, где средство для контроля запаха выбрано из группы, состоящей из циклодекстринов и их смесей, блокаторов запаха, реакционноспособных альдегидов, флавоноидов, солей металлов, цеолитов, активированного угля, гидрофобно-модифицированных полимеров для контроля неприятного запаха (НМР), производных изотиазолинона, таких как бензизотиазолинон, и/или летучих альдегидов.
10. Способ предотвращения или уменьшения повторного осаждения грязи на изделии в ходе процесса последующей чистки или стирки, включающий стадии:
а) приведение изделия в контакт с композицией по п. 9 или с жидким раствором, содержащим полипептид, обладающий ДНКазной активностью; и
b) необязательно полоскание изделия,
где изделие представляет собой текстильное изделие или твердую поверхность.
11. Способ по п. 10, где приведение в контакт согласно стадии а) осуществляют с помощью пропитывания изделия или при мытье изделия.
12. Способ по любому из пп. 10, 11, где жидкий раствор представляет собой моющую жидкость или раствор для пропитывания изделия.
13. Способ по любому из пп. 10-12, где композицию или полипептид согласно стадии а) применяют для чистки или стирки изделия по меньшей мере один раз перед процессом последующей чистки или стирки.
14. Изделие, обработанное или пропитанное полипептидом, обладающим ДНКазной активностью.
15. Изделие по п. 14, где изделие представляет собой текстильное изделие.
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| WO 2011084574 A1, 14.07.2011 | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| КОМПОЗИЦИИ МОЮЩИХ СРЕДСТВ | 2007 |
|
RU2479627C2 |
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
Авторы
Даты
2019-06-05—Публикация
2015-05-28—Подача