Область техники
Настоящее изобретение относится к способу изготовления подложек с покрытием на основе хрома - оксида хрома и к полученным таким способом подложкам с покрытием на основе хрома - оксида хрома. Кроме того, настоящее изобретение относится к применению подложек с покрытием на основе хрома - оксида хрома в упаковочных применениях.
Уровень техники
Электроосаждение является процессом осаждения металлического покрытия на подложку путем пропускания электрического тока через раствор электролита, который содержит металл, подлежащий осаждению.
Традиционно электроосаждение хрома осуществляют путем пропускания электрического тока через раствор электролита, содержащий шестивалентный хром (Cr(VI)). Однако использование растворов электролита с Cr(VI) скоро будет запрещено ввиду токсичности и канцерогенной природы соединений Cr(VI). Поэтому в последние годы исследования сфокусированы на поисках подходящих альтернатив электролитам на основе Cr(VI). Одной альтернативой является создание электролита на основе трехвалентного хрома, поскольку такие электролиты по своей природе менее токсичны и позволяют получить хромовые покрытия, подобные к осаждаемым из растворов электролитов на основе Cr(VI).
Несмотря на использование электролитов на основе трехвалентного хрома, одной основной проблемой является возможное окисление трехвалентного хрома на аноде до шестивалентного хрома. Дополнительно на аноде может случайно окислиться некоторое количество Cr(III) до Cr(VI), поскольку электродные потенциалы окисления воды до кислорода и окисления Cr(III) до Cr(VI) очень близки.
US2010/0108532 раскрывает процесс электроосаждения хрома из гальванической ванны (ванны для нанесения гальванических покрытий) трехвалентного хрома. Согласно US2010/0108532, электролит содержит металлический хром, добавленный в виде основного сульфата хрома, сульфат натрия, борную кислоту и малеиновую кислоту. Дополнительно электролит содержит ионы марганца для снижения образования чрезмерного количества шестивалентного хрома. Хотя образование чрезмерного количества шестивалентного хрома предотвращается, шестивалентный хром, тем не менее, все же образуется.
В отличие от US2010/0108532, EP0747510 описывается способ осаждения оксидов хрома из раствора трехвалентного хрома, который не содержит добавленный буфер. Из-за отсутствия буфера в катодной пленке повышается pH, что, в свою очередь, обеспечивает возможность непосредственного образования оксида хрома на катоде. Согласно EP0747510, образование шестивалентного хрома на аноде можно предотвратить или уменьшить выбором подходящего анода, например, платины, платинированного титана, никель-хрома или углерода и применением деполяризатора, такого как бромид калия. Однако раствор электролита на основе трехвалентного хрома, применяемый в EP0747510, содержит также хлорид калия, который в процессе электроосаждения превращается в хлор. Газообразный хлор потенциально опасен для окружающей среды и работников и поэтому нежелателен.
Согласно US6004448, для получения стали с электролитическим покрытием хромом (ECCS) с использованием химии трехвалентного Cr требуется два разных электролита. Металлический Cr осаждают из первого электролита с буфером из борной кислоты, после чего осаждают оксид Cr из второго электролита без буфера из борной кислоты. Согласно этой патентной заявке, в высокопроизводительной непрерывной линии возникает проблема, что борная кислота из первого электролита будет все больше попадать во второй электролит из-за уноса из резервуара, содержащего первый электролит, в резервуар, содержащий второй электролит, и в результате повышается осаждение металлического Cr и снижается или даже прекращается осаждение оксида Cr. Эта проблема решается добавлением во второй электролит комплексообразующего агента, который нейтрализует введенный буфер.
Подробное описание изобретения
Одной целью настоящего изобретения является обеспечение способа осаждения на подложку покрытия из раствора трехвалентного хрома, при котором избегают образования шестивалентного хрома.
Другой целью настоящего изобретения является обеспечение способа осаждения на подложку покрытия из раствора трехвалентного хрома, при котором избегают образования газообразного хлора.
Дополнительной целью настоящего изобретения является обеспечение слоя на основе хрома – оксида хрома (Cr-CrOx) на стальной подложке, предпочтительно в один этап, при высокой скорости осаждения из простого электролита без буфера, с использованием химии трехвалентного Cr.
Первый аспект изобретения относится к способу изготовления подложки с покрытием на основе металлического хрома - оксида хрома путем электролитического осаждения покрытия на основе металлического хрома - оксида хрома на электропроводящую подложку из раствора электролита, который содержит соединение трехвалентного хрома и хелатообразующий агент, причем раствор электролита не содержит хлорид-ионов и буферного агента в виде борной кислоты, причем электропроводящая подложка действует как катод, а для снижения или исключения окисления ионов Cr(III) до ионов Cr(VI) выбирают анод, содержащий каталитическое покрытие из оксида иридия или смешанного оксида металлов.
Авторы изобретения обнаружили, что независимо от материала каталитического покрытия (платина, оксид иридия или смешанный оксид металлов), на аноде образовывался токсичный газообразный хлор, если покрытие на основе хрома – оксида хрома осаждали электролитически из хлоридсодержащего электролита на основе трехвалентного хрома. Хотя было обнаружено, что деполяризатор, такой как бромид, существенно подавляет эту вредную побочную реакцию, образование газообразного хлора не может быть полностью предотвращено. Чтобы предотвратить выделение газообразного хлора на аноде, из электролита на основе трехвалентного хрома были исключены хлоридсодержащие соединения, например, повышающие проводимость соли, такие как хлорид калия.
Буферный агент в виде борной кислоты с самого начала не включали в состав электролита на основе трехвалентного хрома с тем, чтобы на катоде образовывался преимущественно оксид хрома, т.е. вместо металлического хрома. Эффектом отсутствия буферного агента в виде борной кислоты в электролите является то, что анод становится очень кислым:
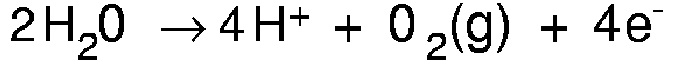
Понятно, что в результате приведенной выше реакции окисление Cr(III) до Cr(VI) предотвращается или по меньшей мере подавляется:

Однако, когда электроосаждение покрытия на основе хрома - оксида хрома проводили в присутствии электролита по изобретению, т.е. электролита без хлорид-ионов и без буферного агента в виде борной кислоты, но с повышающей проводимость сульфатсодержащей солью и с анодом, содержащим каталитическое покрытие из платины, на аноде наблюдалось значительное количество шестивалентного хрома. Неожиданно было обнаружено, что образование шестивалентного хрома предотвращалось, когда каталитическое покрытие из платины было заменено каталитическим покрытием из оксида иридия или смешанного оксида металлов. Однако, если в вышеуказанный, не содержащий хлорида электролит на основе трехвалентного хрома снова вводили буферный агент в виде борной кислоты, на аноде опять образовывалось значительное количество шестивалентного хрома, даже если анод содержал каталитическое покрытие из оксида иридия или смешанного оксида металлов.
Исключение борной кислоты из электролита и выбор покрытого оксидом иридия или смешанным оксидом металлов анода имеет дополнительное преимущество в том, что не нужно обеспечивать электролит добавками, например, ионами Mn2+, чтобы подавить или устранить образование шестивалентного хрома.
В предпочтительном варианте осуществления электролит содержит повышающую проводимость соль, предпочтительно сульфат щелочного металла, более предпочтительно сульфат калия. Авторы изобретения обнаружили, что повышающие проводимость соли на основе сульфатов щелочных металлов были подходящими заменами повышающим проводимость солям на основе хлоридов в том смысле, что все еще достигается хорошая электропроводность электролита, пусть даже и в меньшей степени. Дополнительным преимуществом является то, что применение таких электролитов в комбинации с анодом с покрытием из оксида иридия или смешанного оксида металлов предотвращает образование опасных побочных продуктов, таких как шестивалентный хром и хлор. Было обнаружено, что электролиты, которые содержат сульфат калия в качестве повышающей проводимость соли, очень хорошо подходили для повышения проводимости электролита. Не содержащие хлорида соли лития, натрия или аммония также очень хорошо подходят для повышения проводимости электролита. Особенно предпочтителен сульфат натрия, поскольку растворимость сульфата натрия намного выше, чем растворимость сульфата калия. Более высокая концентрация соли повышает кинематическую вязкость электролита и позволяет использовать более низкие токи для осаждения покрытий на основе хрома – оксида хрома. При снижении плотности тока снижается риск нежелательных побочных реакций, например, окисления Cr3+ в Cr6+, и может быть продлен срок службы каталитического покрытия.
В предпочтительном варианте осуществления хелатообразующий агент содержит катион щелочного металла и карбоксилат. Выгода от использования катиона щелочного металла заключается в том, что в его присутствии сильно повышается электропроводность электролита. Для этой цели особенно предпочтительны катионы калия, поскольку по сравнению с катионами других щелочных металлов они обеспечивают наибольшее повышение проводимости. Для улучшения характеристик покрытия на основе хрома - оксида хрома использовали хелатообразующие агенты, содержащие карбоксилатные анионы, предпочтительно имеющие от 1 до 6 атомов углерода. Подходящие карбоксилатные анионы включают оксалат, малат, ацетат и формиат, причем наиболее предпочтителен формиат, поскольку получаются очень хорошие характеристики покрытия. Вышеуказанные карбоксилатные анионы являются слабыми хелатообразующими агентами и могут использоваться сами по себе или в комбинации. Эти слабые хелатообразующие агенты дестабилизируют очень стабильный шестиводный комплекс, где L означает хелатный лиганд:

Когда электролит содержит сульфат натрия, предпочтительно использовать формиат натрия, например, вместо формиата калия, поскольку это упрощает состав электролита.
В предпочтительном варианте осуществления раствор электролита не содержит буферного агента. Было обнаружено, что отсутствие буферного агента в электролите обеспечивает возможность более предпочтительно осаждать оксид хрома, чем металлический хром. Дополнительно, исключение из состава электролита буферного агента в виде борной кислоты означает, что предотвращается или по меньшей мере подавляется окисление Cr(III) до Cr(VI), когда электролит содержит сульфат щелочного металла в качестве повышающей проводимость соли. При исключении буфера из электролита, pH у поверхности катода повышается до 6,5-11,5, так что в дополнение к металлическому хрому будет осаждаться оксид хрома.
Авторы настоящего изобретения обнаружили также, что для получения ECCS с использованием химии трехвалентного Cr требуется всего один простой электролит без буфера. Даже хотя этот простой электролит не содержит буфера, авторами настоящего изобретения было обнаружено, что из этого электролита неожиданно осаждается также и металлический Cr вследствие частичного восстановления оксида Cr до металлического Cr. Это открытие чрезвычайно упрощает производство ECCS в целом, поскольку для осаждения металлического Cr не нужен электролит с буфером, как это ошибочно предполагалось в US6004488, а требуется только один простой электролит без буфера, что решает также проблему загрязнения этого электролита буфером.
В предпочтительном варианте осуществления соединение трехвалентного хрома содержит основный сульфат хрома(III). Основный сульфат хрома очень подходит как альтернатива хлоридсодержащим соединениям хрома, таким как хлорид хрома(III). При использовании основного сульфата хрома в электролите вместо хлоридсодержащего соединения хрома можно избежать риска образования газообразного хлора на аноде. Другие предпочтительные соли трехвалентного хрома включают формиат хрома(III), оксалат хрома(III), ацетат хрома(III), оксалат калия-хрома(III) и нитрат хрома(III). Вышеуказанные соли, в том числе основный сульфат хрома(III), можно добавлять по отдельности или в комбинации.
В предпочтительном варианте осуществления смешанный оксид металлов содержит оксиды иридия и тантала. Типично анод снабжен электрокаталитическим покрытием на основе платины. Однако авторы изобретения обнаружили, что если анод этого типа был приведен в контакт с не содержащим хлорида электролитом на основе трехвалентного хрома, будет образовываться шестивалентный хром. Было обнаружено, что электрокаталитические покрытия, содержащие смесь оксида иридия и оксида тантала, не вызывают образования шестивалентного хрома на аноде при погружении анода в не содержащий хлорида электролит на основе трехвалентного хрома.
В предпочтительном варианте осуществления раствор электролита не содержит деполяризатора, предпочтительно бромида калия. Согласно EP0747510, присутствие такого деполяризатора, как бромид, в электролите на основе трехвалентного хрома подавляет окисление Cr(III) до Cr(VI). Однако авторы изобретения обнаружили, что, несмотря на отсутствие деполяризатора в электролите, если электролит был хлоридсодержащим электролитом на основе трехвалентного хрома, на аноде (покрытом платиной) не образовывалось никакого шестивалентного хрома. Напротив, было обнаружено, что деполяризатор подавляет образование хлора. Авторы изобретения обнаружили также, что когда электролит на основе трехвалентного хрома по изобретению содержал деполяризатор и повышающую проводимость соль на основе сульфата, на покрытом платиной аноде образовывалось значительное количество шестивалентного хрома. Кроме того, было обнаружено, что когда деполяризатор содержал бромид калия, образовывался газообразный бром. Газообразный бром потенциально опасен для окружающей среды и рабочих и поэтому нежелателен. Авторы изобретения открыли, что для того чтобы избежать образования шестивалентного хрома, не нужно добавлять деполяризатор, например, бромид калия, если электроосаждение проводится в присутствии электролита на основе трехвалентного хрома, содержащего повышающую проводимость соль на основе сульфата, и с покрытым смешанным оксидом металлов анодом. На анодах, покрытых оксидом иридия, если деполяризатор отсутствует, из электролита на основе трехвалентного хрома шестивалентный хром также не образуется.
В предпочтительном варианте осуществления pH раствора электролита устанавливают на от pH 2,6 до pH 3,4, предпочтительно от pH 2,8 до pH 3,0. Было обнаружено, что pH электролита влияет на состав, внешний вид поверхности, например, цвет, и на морфологию поверхности покрытия на основе хрома - оксида хрома. Что касается влияния pH на состав покрытия на основе хрома - оксида хрома, было обнаружено, что количество металлического хрома, осажденного на катод, можно увеличить при использовании электролита на основе трехвалентного хрома с pH от 2,6 до 3,0. С другой стороны, если pH электролита установить выше pH 3,0, более предпочтительно будет осаждаться оксид хрома, а не металлический хром.
Также понятно, что pH у поверхности влияет на внешний вид поверхности осажденного покрытия. В связи с этим наблюдалось, что внешний вид поверхности покрытия на основе хрома - оксида хрома изменялся от серого до коричневатого цвета по мере повышения pH электролита. Это объяснялось составом покрытия на основе хрома - оксида хрома, содержащего больше металлического хрома (серый) при низком pH и больше оксида хрома (коричневый) при более высоком pH. Что касается внешнего вида поверхности, предпочтительно обеспечить электролит с pH от 2,6 до 3,0, чтобы получить покрытие на основе хрома - оксида хрома с преобладанием серого цвета.
pH электролита также имеет непосредственное влияние на морфологию поверхности покрытия на основе хрома - оксида хрома. В этой связи использование электролита с pH выше 3,0, приводило к покрытию на основе хрома - оксида хрома, имеющему относительно открытую и грубую структуру. Напротив, при pH от 2,6 до 3,0, предпочтительно от 2,8 до 3,0, полученное покрытие на основе хрома - оксида хрома характеризовалось более плотной структурой покрытия, проявляющей меньшую пористость по сравнению с покрытиями, осажденными при pH выше 3,0. С точки зрения морфологии поверхности предпочтительно обеспечить электролит с pH от 2,8 до 3,0, поскольку можно получить более значительное улучшение пассивирующих свойств покрытия с учетом уменьшенной пористости таких покрытий.
Было также обнаружено, что pH электролита влияет на скорость, с которой покрытие на основе хрома - оксида хрома осаждается на подложку. Это можно понять, рассмотрев механизм осаждения оксида хрома. Осаждение оксида хрома на катоде происходит при pH от 6,5 до 11,5 и обуславливается восстановлением H+ (H3O+) до H2(г). Согласно этому механизму, использование электролита с кислым pH будет увеличивать время электролиза, которое необходимо для осаждения покрытия на основе хрома - оксида хрома, поскольку для повышения pH у поверхности до значения от 6,5 до 11,5, чтобы осаждался оксид хрома, необходимо восстановить больше H+. Поскольку увеличение времени электролиза приведет к более затратному процессу изготовления, предпочтительно обеспечить электролит с pH по меньшей мере 3,4. Однако, с учетом вышеупомянутых эффектов в отношении состава, внешнего вида и морфологии осажденного покрытия на основе хрома - оксида хрома, предпочтителен электролит с pH по меньшей мере 2,8.
Было обнаружено, что температура раствора электролита также влияет на реакцию осаждения и внешний вид поверхности покрытия на основе хрома - оксида хрома. Было обнаружено, что для осаждения покрытия на основе хрома - оксида хрома с хорошим внешним видом поверхности очень хорошо подходит раствор электролита с температурой от 30°C до 70°C. Предпочтительно температура раствора электролита составляет от 40°C до 60°C, поскольку это ведет к более эффективной реакции осаждения. В этом диапазоне температур раствор электролита демонстрирует хорошую электропроводность, так что требуется меньше энергии для осаждения покрытия на основе хрома - оксида хрома.
В предпочтительном варианте осуществления электропроводящую подложку снабжают путем электролитического осаждения оловянным покрытием на одной или обеих сторонах стальной подложки и покрытую оловом (луженую) сталь подвергают обработке диффузионным отжигом с образованием железо-оловянного сплава на стали.
Предпочтительно стальная подложка содержит рекристаллизационно-отожженную сталь однократной прокатки или сталь двойной прокатки, которая была подвергнута обработке рекристаллизационным отжигом между обработкой первой прокаткой и обработкой второй прокаткой. Оловянное покрытие может быть обеспечено на одной или обеих сторонах стальной подложки на этапе гальванического лужения, причем масса оловянного покрытия составляет не более 1000 мг/м2, а предпочтительно по меньшей мере 100 и/или не более 600 мг/м2 поверхности подложки. При диффузионном отжиге луженой подложки при температуре по меньшей мере 513°C в восстановительной атмосфере слой олова превращается в железо-оловянный сплав, который содержит по меньшей мере 80 процентов по массе (мас.%) FeSn (50 ат.% железа и 50 ат.% олова). Затем эту подложку можно быстро охладить в инертной, неокисляющей охлаждающей среде, удерживая подложку с покрытием в восстановительной атмосфере или атмосфере инертного газа до охлаждения с тем, чтобы получить устойчивый стабильный оксид на поверхности. Слой сплава FeSn обеспечивает защиту от коррозии нижележащей стальной подложке. Отчасти это достигается экранированием подложки, поскольку слой сплава FeSn является очень плотным и имеет очень низкую пористость. Кроме того, сплав FeSn по своей природе сам очень устойчив к коррозии.
В предпочтительном варианте осуществления электропроводящая подложка содержит черную жесть или белую жесть. Было обнаружено, что способ по изобретению очень хорошо подходит для осаждения покрытия на основе хрома - оксида хрома на черную жесть (известную также как сталь без покрытия) и белую жесть, которые обе широко применяются в упаковочной промышленности.
В предпочтительном варианте осуществления на одной или обеих сторонах подложки с покрытием на основе металлического хрома - оксида хрома предусмотрено органическое покрытие. Было обнаружено, что органические покрытия можно легко нанести на покрытие на основе хрома - оксида хрома, которое само действует как пассивирующий слой для защиты электропроводящей подложки. В случае белой жести или стальной подложки, снабженной слоем FeSn, покрытие на основе хрома - оксида хрома предусматривается для пассивации оловянной поверхности, чтобы предотвратить или по меньшей мере уменьшить рост оксидов олова, которые со временем могут вызвать отслоение нанесенного органического покрытия от подложки. Покрытие на основе хрома - оксида хрома также демонстрирует хорошую адгезию к электропроводящей подложке и к наносимому последовательно органическому покрытию. Органическое покрытие может быть обеспечено в виде лакового покрытия или в виде термопластичного полимерного покрытия. Предпочтительно термопластичное полимерное покрытие является системой полимерных покрытий, которая содержит один или более слоев с использованием термопластов, таких как сложные полиэфиры или полиолефины, но которое может также включать акриловые смолы, полиамиды, поливинилхлорид, фторуглеродные смолы, поликарбонаты, смолы стирольного типа, АБС-пластики, хлорированные простые полиэфиры, иономеры, уретановые смолы и функционализованные полимеры. Для ясности:
- Сложный полиэфир представляет собой полимер, состоящий из дикарбоновой кислоты и гликоля. Примеры подходящих дикарбоновых кислот включают терефталевую кислоту, изофталевую кислоту, нафталиндикарбоновую кислоту и циклогександикарбоновую кислоту. Примеры подходящих гликолей включают этиленгликоль, пропандиол, бутандиол, гександиол, циклогександиол, циклогександиметанол, неопентилгликоль и т.д. Можно использовать одновременно более двух видов дикарбоновых кислот или гликолей.
- Полиолефины включают, например, полимеры или сополимеры этилена, пропилена, 1-бутена, 1-пентена, 1-гексена или 1-октена.
- Акриловые смолы включают, например, полимеры или сополимеры акриловой кислоты, метакриловой кислоты, сложного эфира акриловой кислоты, сложного эфира метакриловой кислоты или акриламида.
- Полиамидные смолы включают, например, так называемый Нейлон 6, Нейлон 66, Нейлон 46, Нейлон 610 и Нейлон 11.
- Поливинилхлорид включает гомополимеры и сополимеры, например, с этиленом или винилацетатом.
- Фторуглеродные смолы включают, например, тетрафторированный полиэтилен, трифторированный монохлорированный полиэтилен, гексафторированную этилен-пропиленовую смолу, поливинилфторид и поливинилиденфторид.
- Функционализованные полимеры, например, функционализованные прививанием малеинового ангидрида, включают, например, модифицированные полиэтилены, модифицированные полипропилены, модифицированные сополимеры этилена-акрилата и модифицированные этиленвинилацетаты.
Можно использовать смеси двух или более смол. Дополнительно, смолу можно смешать с антиоксидантом, термостабилизатором, УФ-поглотителем, пластификатором, пигментом, зародышеобразователем, антистатиком, антиадгезивом, добавкой от слеживания и т.д. Было показано, что использование таких систем термопластичных полимерных покрытий обеспечивает отличные характеристики при изготовлении жестяных банок и использовании банок, например, высокий срок годности.
Второй аспект изобретения относится к подложке с покрытием на основе металлического хрома - оксида хрома, полученной согласно первому аспекту изобретения. Преимущества одного или более вариантов осуществления, описанные в связи с первым аспектом изобретения, подобным образом применимы ко второму аспекту изобретения.
Карбид хрома присутствовал в покрытии на основе хрома – оксида хрома в слое на основе металлического хрома, смежного с катодом (но не был обнаружен в слое на основе оксида хрома). Понятно, что источником карбида может быть анион хелатообразующего агента, например, формиат. Полагают, что присутствие карбида хрома в металлическом хроме способствует росту в направлении вверх от подложки.
Органический углерод был обнаружен преимущественно в слое на основе оксида хрома, но также обнаружен и в слое на основе металлического хрома, более конкретно между зернами металлического хрома в слое на основе металлического хрома. Карбид хрома можно было обнаружить на границах этих зерен.
В покрытии на основе хрома - оксида хрома был также обнаружен сульфат хрома. Более конкретно, сульфат присутствовал в слое на основе оксида хрома, что указывает, что сера внедряется (связывается) в слой на основе оксида хрома во время его образования.
Третий аспект изобретения относится к применению подложки с покрытием на основе металлического хрома - оксида хрома в упаковочных применениях.
Теперь изобретение будет пояснено на некоторых примерах. Предполагается, что эти примеры позволят специалистам в данной области осуществить изобретение на практике, но они никоим образом не ограничивают объем изобретения, который определен формулой изобретения.
Образец упаковочной стали (состоящей из обычно используемой марки низкоуглеродистой отпущенной стали) очищали в промышленном растворе для щелочной чистки (Chela Clean KC-25, поставляемый Foster Chemicals), промывали в деионизированной воде, протравливали в 5%-ном растворе серной кислоты при 25°C в течение 10 с и снова промывали. На образец электроосаждением наносили оловянное покрытие (600 мг/м2) из ванны метансульфокислоты (MSA), которая широко используется для получения белой жести в линиях непрерывного нанесения гальванических покрытий. На 1 с прикладывали ток плотностью 10 А/дм2.
Для формирования железо-оловянного сплава на стали образец белой жести отжигали в атмосфере восстановительного газа, используя смесь азота и водорода, содержащую 5% H2(г). Затем образец нагревали от комнатной температуры до 600°C при скорости нагрева 100 °C/сек. Сразу после того, как образец достиг своей пиковой температуры 600°C, образец охлаждали за 1 с до температуры 80°C путем закалки в воде. Образованный слой железо-оловянного сплава содержал более 90% фазы сплава FeSn.
Образец стали со слоем сплава FeSn помещали в прямоугольную электролитную ванну с желобками вдоль боковых стенок для удержания образца и анодов. Покрытие на основе хрома - оксида хрома осаждали из электролита, содержащего 120 г/л основного сульфата хрома, 80 г/л сульфата калия и 51 г/л формиата калия. Этот раствор электролита не содержал хлоридов, буферного агента, например, борной кислоты, и деполяризатора, такого, как бромид калия. pH этого электролита составляла приблизительно 3,85. Температура раствора электролита была 50°C.
Чтобы определить влияние pH на время электролиза, плотность тока и цвет при осаждении покрытий на основе хрома - оксида хрома, pH электролита пошагово устанавливали от pH 3,85 до 3,4, 3,2, 3,0, 2,8 и 2,6 соответственно, добавляя серную кислоту (98 мас.%). При каждом pH определяли время электролиза для осаждения полной массы покрытия Cr ~60 мг/м2, как определено рентгенофлуоресцентным анализом (XRF) с использованием спектрометра SPECTRO XEPOS XRF с кремниевым дрейфовым детектором.
Аналогично, плотность тока определяли при фиксированном времени электролиза 1 с. Используя спектрофотометр Minolta CM-2002, в каждом из этих экспериментов определяли цвет покрытия на основе хрома - оксида хрома в соответствии с хорошо известной системой CIELab. Система CIELab использует три цветовых компонента L*, a* и b* для описания цветов, которые вычисляют из так называемых цветовых компонент X, Y и Z. L* означает яркость цвета (L*=0 указывает на черный, а L*=100 указывает на размытый белый). Компонент a* означает положение на хроматической оси "красный-зеленый" в цветовом пространстве CIELab. Компонент b* означает положение на хроматической оси "синий-желтый". Результаты экспериментов по осаждению и результаты цветовых измерений приведены в таблице 1.
Эти результаты показали, что когда электролит становится более кислым, для осаждения такого же количества хрома требуется или большее время электролиза, или более высокая плотность тока. Из результатов цветовых измерений можно также видеть, что по мере повышения pH цвет осажденного слоя на основе хрома - оксида хрома изменяется от чисто серого на коричневатый цвет. Из вышеуказанных экспериментов следует, что наилучший компромисс между скоростью осаждения и внешним видом получается при использовании электролита с pH приблизительно 3,0. Следовательно, в приложениях, где внешний вид покрытия не так важен, pH электролита можно повысить в сторону более основного pH, чтобы уменьшить время электролиза или плотность тока. При этом будет достигнута более высокая рентабельность производственного процесса.
Были проведены также эксперименты для изучения влияния pH на морфологию поверхности с использованием прибора Zeiss-Ultra 55 FEG-SEM (автоэмиссионная пушка – сканирующий электронный микроскоп). Для оптимального разрешения изображений к внешней поверхности образцов прикладывали низкое ускоряющее напряжение, 1 кВ, в комбинации с коротким рабочим расстоянием и небольшой апертурой.
После установления pH электролита наблюдалось изменение в морфологии поверхности покрытия на основе хрома – оксида хрома. При этом относительно открытая и грубая структура покрытия получалась, когда pH электролита устанавливали выше 3,0. Напротив, когда pH электролита устанавливали от 2,6 до 3,0, получали довольно плотное непористое покрытие, демонстрирующее хорошие пассивирующие свойства.
Для получения информации о химических свойствах этих образцов проводили энергорассеивающий рентгеновский анализ (EDX) со стандартным ускоряющим напряжением 15 кВ, стандартными рабочим расстоянием и апертурой. Эти установки привели к времени задержки 0-35%. Для всех образцов средний EDX-спектр снимали на площади 1000 мкм × 750 мкм в течение 50 с.
Полученные EDX-спектры показали, что количество кислорода в покрытии на основе хрома - оксида хрома увеличилось с увеличением pH, что указывает, что осаждается оксид хрома предпочтительно по сравнению с металлическим хромом по мере того, как электролит становится менее кислым. EDX-спектры выявили также присутствие сульфата хрома в покрытии на основе хрома - оксида хрома.
Для определения характеристик образцов (таблица 2) использовалась также рентгеновская фотоэлектронная спектроскопия (РФЭС). Спектры РФЭС и профили распределения по глубине записывали на приборе Kratos Axis Ultra с использованием рентгеновского излучения Mg Kα с энергией 1253,6 эВ. Размер пятна измерений составлял 700 мкм × 300 мкм. Профили распределения по глубине записывали с использованием ионов Ar+ с энергией 4 кэВ, создающие кратер распыления 3 мм × 3 мм. Скорость распыления калибровали по стандарту BCR 30-ти нм Ta2O5 на Ta, и она составляла 2,15 нм/мин. Ожидаемая скорость распыления соединений Cr была подобна Ta2O5.
В соответствии с анализом СЭМ/EDX, количество осажденного оксида хрома значительно повышается, когда pH электролита составляет выше pH 3,0. РФЭС-измерения также показали, что при более высоком pH сильнее увеличение количества осажденного оксида хрома при использовании неизменной плотности тока по сравнению со случаем, когда плотность тока меняется, а продолжительность электролиза сохраняется постоянной. Эти же тенденции были отмечены при анализе содержания сульфата в осажденном покрытии, и при этом сульфат присутствовал во всем слое на основе оксида хрома, что указывает на то, что сульфат связывается с оксидом хрома, а не просто диспергируется в нем. Это было подтверждено, когда образцы затем промывали в деионизированной воде, а никакого значительного снижения содержания сульфата не наблюдалось. Было также обнаружено, что оксид хрома образуется в процессе осаждения, а не после него, когда образцы подвергаются воздействию атмосферы, т.е. при окислении металлического хрома воздухом.
Можно было также видеть, что и металлический хром, и карбид хрома осаждались совместно, и что содержание металлического хрома снижалось по мере того, как pH становился менее кислым, в частности, при pH выше 3,0. Дополнительно, карбид хрома был найден преимущественно в слое на основе металлического хрома, смежным с железо-оловянным сплавом. Если хелатообразующий агент исключался из электролита, в слое на основе хрома не наблюдалось никакого карбида хрома, что указывает на то, что источником карбида является хелатообразующий агент, в данном случае формиат калия. В слое на основе оксида хрома обнаружили органический углерод, т.е. углерод не в форме карбида.
Измеряли также пористость покрытий путем суммирования атомной процентной доли (определенной методом РФЭС) Sn+Fe/Cr на самых внешних 3,2 нм покрытия. Каждое покрытие, за исключением выброса при pH 2,6, продемонстрировало пористость менее 3,0%.
Проводили также исследование, чтобы понять, при каких условиях на аноде образовывались шестивалентный хром и/или другие вредные побочные продукты. Каждый электролит содержал 120 г/л основного сульфата хрома. Площадь электрически активной поверхности анода составляла 122 мм × 10 мм. Анодная плотность тока была 60 А/дм2. Окружающий воздух над раствором анализировали с помощью трубок Drager® для хлора 0,2/a. Концентрацию Cr(VI) в электролите на основе Cr(III) анализировали методом дифференциальной импульсной полярографии (DPP). Результаты исследований после 5 ч электролиза приведены в таблице 3 ниже.
Результаты показывают, что когда электролит содержит хлорид-ионы (опыт №1 и №2), на аноде образуется газообразный хлор, и что присутствие деполяризатора, такого как бромид, в электролите сильно подавляет, но не устраняет эти вредные побочные реакции (опыт №1). Результаты показывают также, что когда электролит содержит хлорид-ионы, присутствие бромида в электролите не играет никакой роли в предотвращении образования шестивалентного хрома на аноде (см. также опыт №1 и опыт №2).
Когда повышающая проводимость соль содержит сульфаты вместо хлоридов, на аноде образуются значительные количества шестивалентного хрома, если анод содержит каталитическое покрытие из платины (см. также опыты №3 и №4). Можно видеть, что присутствие бромида в сульфатсодержащем электролите даже повышает образование шестивалентного хрома. Однако если заменить каталитическое покрытие из платины каталитическим покрытием из смешанного оксида металлов из оксида тантала и оксида иридия, на аноде не образуется никакого шестивалентного хрома (опыты №5 и №6). Присутствие бромида калия в электролите (опыт №5), по-видимому, не играет никакой роли в предотвращении образования шестивалентного хрома. Образование шестивалентного хрома на аноде также предотвращалось, когда анод содержал каталитическое покрытие из оксида иридия (опыты №7 и №8). Однако если не содержащий хлорида электролит включал сульфаты и борную кислоту, на аноде снова был обнаружен шестивалентный хром (опыт №9). Эти результаты означают, что если электролит не содержит хлорид-ионов (с тем, чтобы избежать образования хлора на аноде), а в качестве повышающей проводимость соли используется сульфат щелочного металла, электролит не должен содержать буферного агента в виде борной кислоты, а анод не должен содержать каталитического покрытия из платины или на основе платины (с тем, чтобы избежать образования шестивалентного хрома на аноде).
Проводились также эксперименты для исследования состава покрытий на основе хрома – оксида хрома, которые были (i) осаждены в соответствии со способом по настоящему изобретению (одностадийный способ) или (ii) осаждены в соответствии со способом по EP0747510 (двухстадийный способ). Было обнаружено, что применение одностадийного или двухстадийного процесса осаждения влияло на состав осажденного покрытия на основе хрома - оксида хрома. В частности, покрытия на основе хрома - оксида хрома, полученные двухстадийным процессом, содержали меньше оксида хрома, чем покрытия на основе хрома - оксида хрома, полученные одностадийным процессом. Кроме того, когда использовался двухстадийный процесс осаждения, у поверхности покрытия на основе хрома - оксида хрома концентрировалась большая доля оксида хрома, тогда как оксид хрома был более равномерно распределен по всему покрытию на основе хрома - оксида хрома, полученном одностадийным процессом осаждения. Было также обнаружено, что содержание карбида хрома было значительно выше для покрытий на основе хрома - оксида хрома, полученных двухстадийным процессом, по сравнению с покрытиями, полученными одностадийным способом.
или Br2(г)
Изобретение относится к области гальванотехники и может быть использовано для упаковочных применений. Способ изготовления подложки с покрытием на основе металлического хрома - оксида хрома включает электролитическое осаждение покрытия на основе металлического хрома - оксида хрома на электропроводящую подложку в одну стадию из раствора электролита, который содержит соединение трехвалентного хрома и хелатообразующий агент, причем раствор электролита не содержит хлорид-ионов и буферного агента, причем электропроводящую подложку используют в качестве катода, а для снижения или исключения окисления ионов Cr(III) до ионов Cr(VI) выбирают анод, содержащий каталитическое покрытие из оксида иридия или смеси оксидов иридия и тантала. Технический результат: обеспечение осаждения покрытия из раствора трехвалентного хрома, при котором избегают образования шестивалентного хрома и газообразного хлора, предпочтительно в один этап, при высокой скорости осаждения из простого электролита без буфера. 3 н. и 11 з.п. ф-лы, 3 табл.
1. Способ изготовления подложки с покрытием на основе металлического хрома - оксида хрома путем электролитического осаждения покрытия на основе металлического хрома - оксида хрома на электропроводящую подложку в одну стадию из раствора электролита, который содержит соединение трехвалентного хрома и хелатообразующий агент, при этом раствор электролита не содержит хлорид-ионов и буферного агента, причем электропроводящую подложку используют в качестве катода, а для снижения или исключения окисления ионов Cr(III) до ионов Cr(VI) выбирают анод, содержащий каталитическое покрытие из оксида иридия или смеси оксидов иридия и тантала.
2. Способ по п.1, в котором электролит содержит повышающую проводимость соль, предпочтительно сульфат щелочного металла, более предпочтительно сульфат калия или сульфат натрия.
3. Способ по п.1 или 2, в котором хелатообразующий агент содержит карбоксилат щелочного металла, предпочтительно формиат калия или формиат натрия.
4. Способ по п.1 или 2, в котором соединение трехвалентного хрома содержит основный сульфат хрома (III).
5. Способ по п.1 или 2, в котором раствор электролита не содержит деполяризатор, предпочтительно бромид калия.
6. Способ по п.1 или 2, в котором pH раствора электролита устанавливают от 2,6 до 3,4, предпочтительно от 2,8 до 3,0.
7. Способ по п.1 или 2, в котором в качестве электропроводящей подложки используют стальную подложку с оловянным покрытием, полученную путем электролитического осаждения оловянного покрытия на одной или обеих сторонах стальной подложки, которая подвергнута диффузионному отжигу.
8. Способ по п.1 или 2, в котором в качестве электропроводящей подложки используют подложку из черной жести или белой жести.
9. Способ по п.1 или 2, в котором на одной или обеих сторонах электропроводящей подложки с покрытием на основе металлического хрома - оксида хрома предусмотрено органическое покрытие.
10. Подложка с покрытием на основе металлического хрома - оксида хрома, отличающаяся тем, что она получена способом по любому из пп. 1-9.
11. Подложка по п.10, в которой покрытие дополнительно содержит карбид хрома.
12. Подложка по п.10 или 11, в которой покрытие дополнительно содержит органический углерод.
13. Подложка по любому из пп.10-12, в которой покрытие дополнительно содержит сульфат хрома.
14. Применение подложки с покрытием на основе металлического хрома - оксида хрома по любому из пп.10-13 в качестве подложки для упаковочных применений.
| Способ автоматического управления процессом регенерации ионообменного фильтра | 1978 |
|
SU747510A1 |
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| СПОСОБ ПОВЕРХНОСТНОГО УПРОЧНЕНИЯ ИЗДЕЛИЙ ИЗ СТАЛИ | 2004 |
|
RU2251594C1 |
Авторы
Даты
2019-06-25—Публикация
2014-05-21—Подача