Область техники
Настоящее изобретение относится к новому пептиду и, более конкретно, к новому пептиду и его применению.
Уровень техники
Виды рака (или опухоли) возникают в результате неконтролируемой пролиферации клеток в живых тканях. Раковые клетки проникают в окружающие ткани или распространяются на другие органы, что часто приводит к летальному исходу.
Способы лечения такого рака включают хирургическую операцию, лучевую терапию, химиотерапию, иммунотерапию и т.д., и при этом продолжается исследование таких пептидов, которые проявляют противораковые эффекты (публикация международной заявки на патент № WO 2007/133033 A1).
[Перечень ссылок]
[Патентная литература]
(Патентный документ 1) публикация международной заявки на патент № WO 2007/133033 A1, 22 ноября 2007 г., реферат.
Раскрытие изобретения
Техническая задача
Соответственно, настоящее изобретение было создано с учетом вышеупомянутых задач из предшествующего уровня техники, и при этом настоящее изобретение предназначено для обеспечения нового пептида.
Кроме того, настоящее изобретение предназначено для обеспечения нового применения пептида.
Дополнительные технические задачи, которые не были указаны выше, будут полностью понятны специалистам в данной области техники из приведенного ниже описания.
Решение задачи
В настоящем изобретении предусматривают пептид, состоящий из аминокислотной последовательности (QLHLD) с SEQ ID NO: 1, или его фармацевтически приемлемую соль.
В аминокислотной последовательности Q обозначает глутамин (Gin), L обозначает лейцин (Leu), H обозначает гистидин (His) и D обозначает аспартат (Asp).
Аминокислоты, которые входят в состав пептида, включают L-, D- и DL-формы, все из которых включены в настоящее изобретение. Кроме того, будет понятно, что Asp может интерпретироваться как имеющий значение, включающее аспарагиновую кислоту, а также аспартат, в качестве аминокислоты.
Пептид включает его варианты, в которых часть структуры пептида в соответствии с настоящим изобретением варьирует из-за спонтанной мутации или искусственной мутации без изменения его основной активности.
Примеры фармацевтически приемлемой соли могут включать гидрохлорид, сульфат, фосфат, ацетат, цитрат, тартрат, сукцинат, лактат, малеат, фумарат, оксалат, метан сульфонат и пара-толуолсульфонат.
Кроме того, в настоящем изобретении предусматривают медицинское применение пептида в соответствии с настоящим изобретением или его фармацевтически приемлемой соли, предпочтительно для противоракового применения и более предпочтительно для предупреждения или лечения рака. При этом под термином «лечение» в полном объеме подразумевают снижение или облегчение связанных с раком симптомов, а термин «предупреждение» применяют во всеобъемлющем значении, включая подавление прогрессирования заболевания от бессимптомной стадии до заболевания.
Рак может представлять собой метастатический рак.
В настоящем изобретении противораковый эффект может проявляться путем подавления по меньшей мере одного явления, выбранного из инвазии и метастазирования раковых клеток.
Соответственно, в настоящем изобретении предусматривают противораковую композицию, содержащую пептид по настоящему изобретению или его фармацевтически приемлемую соль. Соответственно, в настоящем изобретении предусматривают композицию для применения при лечении или предупреждении рака, содержащую пептид по настоящему изобретению или его фармацевтически приемлемую соль. Лечение или предупреждение рака может достигаться путем подавления по меньшей мере одного явления, выбранного из инвазии и метастазирования раковых клеток. Композиция может представлять собой фармацевтическую композицию.
Фармацевтическая композиция в качестве активного ингредиента содержит пептид в соответствии с настоящим изобретением или его фармацевтически приемлемую соль.
Кроме того, фармацевтическая композиция дополнительно содержит фармацевтически приемлемую добавку и может, таким образом, состоять из пептида в соответствии с настоящим изобретением или его фармацевтически приемлемой соли и добавки.
Пептид в соответствии с настоящим изобретением можно получать с помощью способов, которые обычно применяют в области химии пептидов. Например, пептид можно получать с помощью способа, раскрытого Schroder и Lubke, «The Peptides» том 1, Academic Press, Нью-Йорк (1965), или с помощью способа, такого как синтез в растворе или твердофазный синтез.
Примеры способов образования пептидных связей могут включать ацилазидный способ, ацилгалогенидный способ, ацилимидазольный способ, карбодиимидный способ, способ с применением фосфония, ангидридный способ, смешанный ангидридный способ, окислительно-восстановительный способ и применение K-реагента Вудворда.
Перед проведением реакции конденсации карбоксильную группу, аминогруппу или т.п., которые не участвуют в реакции, можно защитить, и карбоксильную группу, которая участвует в реакции конденсации, можно активировать с помощью способов, известных из уровня техники.
Примеры функциональных групп для защиты карбоксильной группы могут включать группы, образующие сложный эфир, а именно метил, трет-бутил, арил, пентафторфенил, бензил, параметоксибензил и метоксиэтоксиметил.
Примеры функциональных групп для защиты аминогруппы могут включать тритилкарбонил, арилоксикарбонил, циклогексилоксикарбонил, трихлорэтилоксикарбонил, бензилоксикарбонил, трет-бутоксикарбонил и/или 9-флуоренилметилоксикарбонил.
Примеры активных форм карбоксильной группы могут включать смешанный ангидрид, азид, ацилхлорид и активный сложный эфир [сложный эфир со спиртом (например, пентахлорфенол, 2,4-динитрофенол, цианометиловый спирт, п-нитрофенол, N-гидрокси-5-норборнен-2,3-дикарбоксимид, N-гидроксисукцинимид, N-гидроксифталамид или 1-гидроксибензотриазол)].
Растворитель, применимый в реакции конденсации с образованием пептидных связей, может включать бензол, толуол, гексан, ацетон, нитрометан, циклогексан, эфир, хлороформ, дихлорметан, этилацетат, N,N-диметилформамид, диметилсульфоксид, пиридин, диоксан, тетрагидрофуран, воду, метанол и этанол, которые можно применять отдельно или в комбинации.
Температура реакции варьируется от приблизительно -70 до 100°C и предпочтительно от -30 до 30°C.
Реакцию снятия защиты для удаления защитной группы пептида можно осуществлять с применением кислотного соединения, основного соединения или переходного металла, способного удалять защитную группу, не воздействуя на пептидную связь, в зависимости от вида защитной группы.
Реакцию снятия защиты можно выполнять посредством обработки кислотой с применением, например, хлороводорода, бромоводорода, фторводорода, уксусной кислоты, метансульфоновой кислоты, трифторметансульфоновой кислоты, трифторуксусной кислоты, триметилхлорсилана или их смесей.
При осуществлении реакции снятия защиты посредством обработки кислотой, ее можно стимулировать путем добавления вспомогательного вещества, такого как анизол, фенол или тиоанизол.
В качестве альтернативы, реакцию снятия защиты можно выполнять посредством обработки основным соединением, например, аммиаком, диэтиламином, гидразином, морфолином, N-метилпирролидином, пиперидином, карбонатом натрия или их смесями.
В качестве альтернативы, реакцию снятия защиты можно выполнять посредством обработки переходным металлом с применением, например, цинка, ртути, палладия/водорода и т.д.
После завершения реакции пептид можно очищать с применением традиционного способа очистки, такого как экстрагирование, разделение слоев, осаждение твердых частиц, перекристаллизация или колоночная хроматография.
Более того, пептид в соответствии с настоящим изобретением можно превратить в его вариант или его фармацевтически приемлемую соль с применением традиционного способа.
Пептид в соответствии с настоящим изобретением можно синтезировать с применением автоматизированного синтезатора пептидов или можно получить с помощью генной инженерии. Например, слитый ген, кодирующий слитый белок, содержащий партнера по слиянию и пептид в соответствии с настоящим изобретением, получают с помощью генной инженерии, а затем применяют для трансформации микроорганизма-хозяина, в результате чего слитый белок экспрессируется в микроорганизме-хозяине, после чего пептид в соответствии с настоящим изобретением расщепляется или отделяется от слитого белка с применением протеолитического фермента или соединения, с получением таким образом желаемого пептида.
Пептид или его фармацевтически приемлемую соль вводят парентерально в количестве от 200 до 500 мг/день и предпочтительно от 267 до 400 мг/день. Вводимый пептид или его фармацевтически приемлемая соль могут предназначаться для взрослых (приблизительно 60 кг). При пероральном введении его количество превышает в 2-5 раз количество при парентеральном введении. Пептид в соответствии с настоящим изобретением может в основном вводиться посредством парентеральных путей, например, местной инъекции, внутривенной или подкожной инъекции, интрацеребрального или интраспинального введения или назального или ректального введения. В некоторых случаях возможно пероральное введение.
Пептид или композиция в соответствии с настоящим изобретением могут быть составлены в форме инъекции, суппозитория, порошка, назальных капель, гранулы или таблетки, вместе с фармацевтически приемлемой добавкой.
Фармацевтически приемлемую добавку можно использовать в зависимости от различных факторов, хорошо известных специалистам в данной области техники, включая, например, определенный биоактивный материал, его концентрацию, стабильность и предполагаемую биодоступность; нарушения и заболевания, подлежащие лечению, или состояния, ассоциированные с ними; индивидуумы, подлежащие лечению, их возраст, размер и общее состояние здоровья; и пути введения композиции, например, назальный, пероральный, глазной, местный, дермальный и внутримышечный пути, однако, настоящее изобретение не ограничивается ими. Фармацевтически приемлемая добавка, которую применяют для введения биоактивного материала, в дополнение к пероральному пути введения, может включать водный раствор, включающий D5W (5% глюкозы в воде), декстрозу и физиологическую соль в количестве, находящемся в пределах 5% от ее объема. В случае местной инъекции, вводимой внутрь пораженных тканей, для усиления терапевтических эффектов и увеличения их продолжительности могут использоваться любые инъецируемые гидрогели. Фармацевтически приемлемая добавка может содержать дополнительные компоненты для улучшения стабильности активных компонентов, такие как консерванты и антиоксиданты. Пептид или композицию в соответствии с настоящим изобретением можно получать с помощью подходящих способов из смежной области техники, и, например, предпочтительно составлять как подходящую для каждого заболевания или компонента с помощью способа, раскрытого в Remington's Pharmaceutical Science, Mack Publishing Company, Easton PA (последнее издание).
Пептид по настоящему изобретению может храниться в солевом растворе или может лиофилизироваться в ампуле после добавления маннита или сорбита и может вводиться после растворения в солевом растворе.
Кроме того, в настоящем изобретении предусматривают способ лечения или предупреждения рака, включающий введение пептида или его фармацевтически приемлемой соли по настоящему изобретению млекопитающим, в том числе людям, нуждающимся во введении. Кроме того, в настоящем изобретении предусматривают применение пептида или его фармацевтически приемлемой соли по настоящему изобретению при изготовлении противоракового лекарственного препарата и предпочтительно при изготовлении лекарственного препарата для применения при лечении или предупреждении рака. Лечение или предупреждение рака может достигаться путем подавления по меньшей мере одного явления, выбранного из инвазии и метастазирования раковых клеток. Вводимые пептид или его фармацевтически приемлемая соль могут представлять собой пептид или его фармацевтически приемлемую соль в эффективном количестве.
Если не указано иное, признаки, описанные в связи с пептидом или его фармацевтически приемлемой солью, применением, композицией и способом в соответствии с настоящим изобретением являются применимыми друг к другу в пределах идентичности, если они не противоречат друг другу.
Полезные эффекты изобретения
В соответствии с настоящим изобретением можно осуществлять эффективное лечение или предупреждение рака.
Краткое описание графических материалов
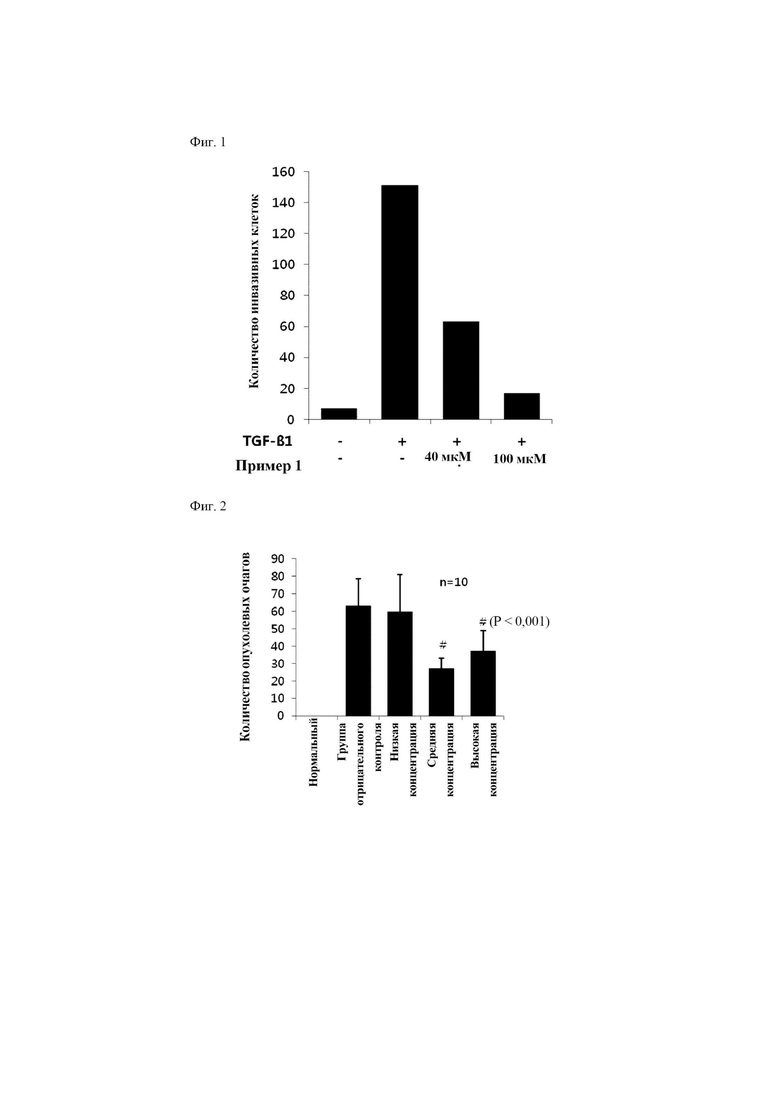
На фиг. 1 представлен график, иллюстрирующий эффекты варианта осуществления настоящего изобретения в отношении инвазии раковых клеток.
На фиг. 2 представлен график, иллюстрирующий эффекты варианта осуществления настоящего изобретения в отношении метастазирования раковых клеток.
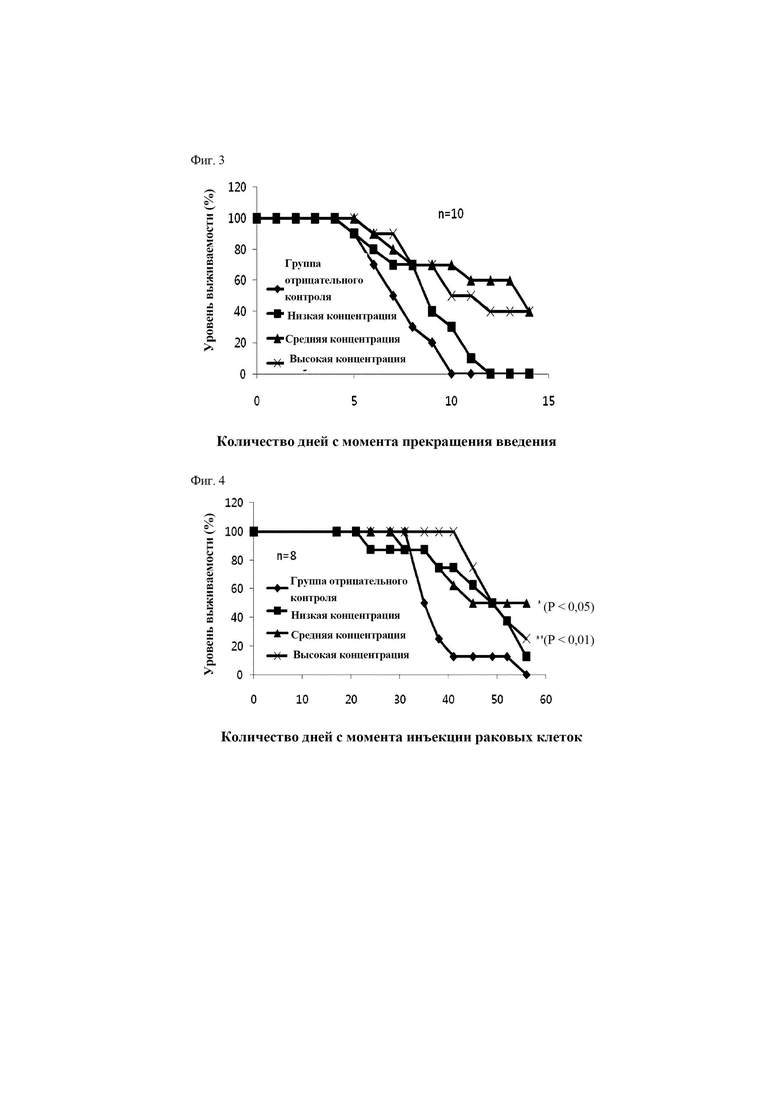
На фигурах 3 и 4 представлены графики, иллюстрирующие противораковые эффекты в соответствии с вариантом осуществления настоящего изобретения.
Вариант изобретения
Лучшего понимания настоящего изобретения можно достичь с помощью следующих примеров и примера получения, которые изложены исключительно для иллюстрации и не должны быть истолкованы как ограничивающие настоящее изобретение.
Термин «противораковый» относится к способности обеспечивать лечение или предупреждение рака, и, в частности, противораковый эффект может проявляться путем подавления по меньшей мере одного явления, выбранного из инвазии и метастазирования раковых клеток.
Реактивы, используемые в указанных ниже примерах, являются коммерчески доступными и лучшими продуктами, приобретенными у Sigma-Aldrich, если не указано иное.
<Пример 1> Получение пептида
Пептид (QLHLD: SEQ ID NO: 1), состоящий из аминокислотной последовательности с SEQ ID NO: 1, получали в AnyGen Co., Ltd., Корея. В частности, его синтезировали с помощью твердофазного способа с применением химических свойств Fmoc (9-флуоренилметоксикарбонила). Более конкретно, C-конец пептида связывали с 0,55 ммоль/г твердой смолы (смола Ванга; Sigma-Aldrich). Связывание аминокислоты Fmoc-Phe-OH осуществляли вместе с O-бензотриазол-N,N,N',N'-тетраметилуроний гексафторфосфатом (HBTU). Боковая цепь аминокислоты была защищена трет-бутилом и трет-бутилоксикарбонилом. Снятие защиты и отделение смолы выполняли при комнатной температуре в течение 3 ч. с применением смешанного раствора, содержащего трифторуксусную кислоту и воду в соотношении 95:5 (об./об.). Неочищенный пептид несколько раз промывали диэтиловым эфиром, высушивали под вакуумом, а затем очищали с помощью обращенно-фазовой высокоэффективной жидкостной хроматографии (RP-HPLC) с применением колонки Shimadzu 5 мкм Shimpak ODS C18 (20×250 мм). Очищенный пептид идентифицировали с помощью аналитической RP-HPLC с применением колонки Shimpak 5 мкм ODS C18 (4,6×250 мм). Молекулярную массу синтезированного пептида измеряли с применением масс-спектрометра с матрично-активированной лазерной десорбцией/ионизацией (MALDI) (Axima CFR, Kratos Analytical, Манчестер, Великобритания).
<Пример 2> Оценка ингибирующего эффекта в отношении инвазии раковых клеток
Экспериментально оценивали, была ли инвазия раковых клеток подавлена пептидом из примера 1. В частности, для оценки эффекта пептида из примера 1 в отношении подавления инвазии раковых клеток, выполняли анализ инвазии Transwell. Matrigel cо сниженным содержанием факторов роста (BD Biosciences, Франклин-Лейкс, Нью-Джерси, США) разбавляли 1:1 средой {среда RPMI 1640 (Welgene Inc., Корея)} и 70 мкл ее добавляли в верхнюю камеру вкладышей Transwell (Corning, № по кат. 3422, Тьюксбери, Массачусетс, США), с последующим нанесением покрытия в течение 1 ч. в CО2-инкубаторе при 37°C. 500 мкл среды {среда RPMI 1640 (Welgene Inc., Корея)}, содержащей 10% эмбриональную бычью сыворотку (FBS, Cellgro, № по кат. 35-015-CV, США), добавляли в нижнюю камеру, после чего в тестируемую группу добавляли 10 нг/мл TGF-бета-1 (PromoKine, Германия). Покрытую верхнюю камеру устанавливали на нижнюю камеру и в верхнюю камеру добавляли 100 мкл среды RPMI 1640, содержащей 0,5% FBS с 20000 клеток рака щитовидной железы SNU-790 (корейский банк клеточных линий). Таким образом, были получены группа отрицательного контроля и две тестируемые группы. Соответствующие тестируемые группы обрабатывали пептидом из примера 1 в количествах 40 мкМ и 100 мкМ, а группу отрицательного контроля не обрабатывали пептидом из примера 1. Кроме того, контрольную группу получали таким же образом, как и группу отрицательного контроля, за исключением того, что не добавляли TGF-бета-1 (трансформирующий фактор роста-бета-1).
Тестируемые группы, контрольную группу и группу отрицательного контроля культивировали в CО2-инкубаторе в течение 2 дней при 37°C. После завершения культивирования клетки, оставшиеся в верхней камере, полностью удаляли с использованием ватного тампона. Клетки, которые прикреплялись к наружной поверхности верхней камеры, промывали с помощью DPBS (фосфатно-солевой буферный раствор Дульбекко) в течение 5 мин., фиксировали в 100% метаноле при -20°C в течение 5 мин., а затем окрашивали в течение 15 мин. в растворе гематоксилина Майера (Sigma-Aldrich), с последующим промыванием водопроводной водой в течение 5 мин., фиксацией в 100% этаноле в течение 5 мин., а затем окрашивали в течение 15 мин. в растворе эозина Y. В конечном итоге, выполняли промывание 100% этанолом, и лезвием обрезали мембрану, к которой прикреплялись клетки, помещали ее на предметное стекло и исследовали под микроскопом. Фотографировали четыре случайно выбранных участка и подсчитывали количество клеток в этих участках, усредняли и изображали на графике. На фиг. 1 представлен график, демонстрирующий описанные выше результаты, нанесенные на ось x, на которой представлена каждая группа, и ось y, на которой представлено количество инвазивных клеток. Как показано на фиг. 1, инвазию раковых клеток, которая повышалась под воздействием TGF-бета-1, подавляли зависимым от концентрации способом с помощью пептида из примера 1.
Следовательно, пептид в соответствии с настоящим изобретением был эффективным в отношении подавления инвазии раковых клеток, за счет чего проявлялись противораковые эффекты.
<Пример 3> Оценка ингибирующего эффекта в отношении метастазирования раковых клеток in vivo
Экспериментально оценивали, было ли метастазирование раковых клеток подавлено пептидом из примера 1. В частности, для оценки ингибирующего эффекта пептида из примера 1 на метастазирование раковых клеток, выполняли тестирование с применением модели легочного метастазирования с клетками рака молочной железы мыши 4T1 (ATCC CRL-2539, США). Пептид из примера 1 инъецировали в хвостовую вену хвоста самок мышей BALB/c (SPF, SLC/Япония). Тестируемую группу разделяли на три группы в соответствии с вводимой концентрацией; низкая концентрация {40 мкг/особь}, средняя концентрация {80 мкг/особь} и высокая концентрация {120 мкг/особь}. Группу отрицательного контроля обрабатывали таким же образом, как и тестируемую группу, за исключением того, что не вводили пептид из примера 1. В день после первого введения клетки 4T1 (l,5×104 клеток/особь) инъецировали в хвостовую вену хвоста мыши. Спустя 1 ч. повторно вводили пептид из примера 1. Введение пептида выполняли три раза в неделю (понедельник, среда и пятница), в общем в течение трех недель, начиная со второго дня введения и заканчивая последним днем введения. Вес мыши измеряли два раза в неделю и вскрытие выполняли на 21-й день после инъекции раковых клеток. Вырезали ткань легкого, окрашивали раствором Боуина и фиксировали, а затем подсчитывали количество очагов метастатической опухоли. Кроме того, группу (нормальную группу), обработанную таким же образом, как и тестируемую группу, получали как контрольную группу, за исключением того, что не добавляли ни пептид из примера 1, ни клетки 4T1. Результаты показаны на фиг. 2. График на фиг. 2 нанесен с осью x, на которой представлена каждая группа, и осью y, на которой представлено количество опухолевых очагов. Таким образом, n обозначает количество индивидуумов в каждой группе, а P обозначает вероятность значимости. Как проиллюстрировано на фиг. 2, в тестируемой группе, в которой пептид из примера 1 вводили в средней концентрации и высокой концентрации, значимо уменьшалось количество опухолевых очагов (P<0,001). В частности, ингибирующий эффект в отношении метастазирования рака был наиболее высоким в тестируемой группе, в которой пептид вводили в средней концентрации.
Следовательно, пептид по настоящему изобретению является эффективным при подавлении метастазирования раковых клеток, за счет чего проявляются противораковые эффекты.
<Пример 4> Оценка противоракового эффекта I
Противораковый эффект пептида из примера 1 оценивали экспериментально. В частности, для оценки эффекта пептида из примера 1 на выживание индивидуумов, страдающих раком, уровень выживаемости измеряли с применением животной модели, полученной таким же образом, как и в примере 3.
Группу отрицательного контроля и тестируемую группу получали таким же образом, как и в примере 3, за исключением вскрытия и последующей обработки. Для измерения уровня выживаемости наблюдали и регистрировали уровень выживаемости для каждой группы. Результаты показаны на фиг. 3. На графике на фиг. 3 показан уровень выживаемости, при этом на оси x представлено количество дней с момента прекращения введения, и на оси y представлен уровень выживаемости (%). Кроме того, n представляет собой количество индивидуумов в каждой группе. Как проиллюстрировано на фиг. 3, в тестируемых группах, в которых пептид из примера 1 вводили в средней и высокой концентрациях, некоторые индивидуумы выживали даже после гибели особей в группе отрицательного контроля. В частности, уровень выживаемости был наиболее высоким в тестируемой группе, в которой пептид вводили в средней концентрации.
Следовательно, можно обнаружить, что пептид по настоящему изобретению проявляет противораковые эффекты.
<Пример 5> Оценка противоракового эффекта II
Противораковый эффект пептида из примера 1 оценивали экспериментально. В частности, для оценки эффекта пептида из примера 1 на выживание индивидуумов, страдающих раком, уровень выживаемости измеряли с применением животной модели с клетками меланомы мыши B16-BL6 (корейский банк клеточных линий, Корея).
Клетки B16-BL6 {1×105 клеток/особь} подкожно инъецировали 7-недельным самцам мышей C57BL/6J (Orientbio Inc., Корея). Через одну неделю внутрибрюшинно вводили пептид из примера 1. Тестируемую группу разделяли на три группы в соответствии с вводимой концентрацией; низкая концентрация {40 мкг/особь}, средняя концентрация {80 мкг/особь} и высокая концентрация {120 мкг/особь}. Группу отрицательного контроля обрабатывали таким же образом, как и тестируемую группу, за исключением того, что не вводили пептид из примера 1. Введение повторяли дважды в неделю в течение двух недель от первого дня введения, а затем раз в неделю в течение дополнительных четырех недель, и в общем пептид вводили восемь раз. Для измерения уровня выживаемости наблюдали и регистрировали уровень выживаемости для каждой группы. Результаты показаны на фиг. 4. На графике на фиг. 4 показан уровень выживаемости, на при этом оси x представлено количество дней с момента инъекции раковых клеток, и на оси y представлен уровень выживаемости (%). Кроме того, n представляет собой количество индивидуумов в каждой группе, а P представляет собой вероятность значимости. Как проиллюстрировано на фиг. 4, в тестируемых группах, в которых вводили пептид из примера 1, некоторые индивидуумы выживали даже после гибели особей в группе отрицательного контроля. В частности, уровень выживаемости был наиболее высоким в тестируемой группе, в которой пептид вводили в средней концентрации.
Следовательно, можно обнаружить, что пептид в соответствии с настоящим изобретением проявляет противораковые эффекты.
<Пример получения 1> Получение лекарственной формы для инъекции
500 мг пептида, полученного таким же образом как и в примере 1, растворяли в солевом растворе с получением 10 мл раствора. Этим раствором заполняли ампулу для инъекции, с получением лекарственной формы для инъекции.
Промышленная применимость
Настоящее изобретение обеспечивает эффективное лечение или предупреждение рака и является, таким образом, промышленно применимым.

Изобретение относится к пептиду, состоящему из аминокислотной последовательности GlnLeuHisLeuAsp (SEQ ID NO: 1), или его фармацевтически приемлемой соли и к их применению для лечение рака. 3 н. и 2 з.п. ф-лы, 4 ил., 5 пр.
1. Пептид, состоящий из аминокислотной последовательности с SEQ ID NO: 1, или его фармацевтически приемлемая соль.
2. Фармацевтическая композиция для применения при лечении или предупреждении рака, где рак выбирают из рака щитовидной железы, рака молочной железы и меланомы, содержащая пептид или его фармацевтически приемлемую соль по п. 1.
3. Фармацевтическая композиция по п. 2, где лечение или предупреждение рака достигается путем подавления по меньшей мере одного явления, выбранного из инвазии и метастазирования раковых клеток.
4. Применение пептида или его фармацевтически приемлемой соли по п. 1 при изготовлении лекарственного препарата для применения при лечении или предупреждении рака, где рак выбирают из рака щитовидной железы, рака молочной железы и меланомы.
5. Применение по п. 4, где лечение или предупреждение рака достигается путем подавления по меньшей мере одного явления, выбранного из инвазии и метастазирования раковых клеток.
| СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОГО ПРЕПАРАТА ИММУНОМОДУЛЯТОРА ДЛЯ ЛЕЧЕНИЯ ТЯЖЕЛЫХ ФОРМ ГНОЙНО-СЕПТИЧЕСКИХ И АУТОИММУННЫХ ЗАБОЛЕВАНИЙ | 2012 |
|
RU2491944C1 |
| СИСТЕМА И СПОСОБ ПОДАЧИ ПОТОКА, МАШИНА ДЛЯ ПРИГОТОВЛЕНИЯ НАПИТКА, А ТАКЖЕ НОСИТЕЛЬ ДАННЫХ, НА КОТОРОМ ХРАНИТСЯ КОМПЬЮТЕРНАЯ ПРОГРАММА ДЛЯ РЕАЛИЗАЦИИ СПОСОБА | 2020 |
|
RU2807180C1 |
| НОВЫЙ ПЕПТИД И ЕГО ПРИМЕНЕНИЕ | 2011 |
|
RU2525913C1 |
| WO 2006084016 A1, 10.08.2006. | |||
Авторы
Даты
2019-07-03—Публикация
2016-07-22—Подача