Изобретение относится к медицине, в частности, к фармакологии и касается средства для лечения диабета.
Сахарный диабет занимает 3-е место среди основных причин смертности населения в большинстве стран мира. Темпы нарастания распространенности этого заболевания носят угрожающий характер. По данным Международной федерации диабета (IDF) в настоящее время более 422 млн. человек в мире больны этим заболеванием, а к 2040 году их количество возрастет до 642 млн. По числу больных диабетом Россия занимает 5-ое место в мире.
Терапия сахарного диабета 2-го типа (СД 2) затруднена недостаточной эффективностью применяемых средств и наличием побочных эффектов: для производных сульфонилмочевины характерно развитие вторичной резистентности, для бигуанидов - гепатотоксичность [L.M. Forman, D.A. Simmons, R.H. Diamond Hepatic failure in a patient taking rosiglitazone // Ann Intern Med. 2000. V. 132 (2): 118-121] и повышение риска развития кардиоваскулярной патологии [A. Rohatgi, D.K. McGuire Effects of the thiazolidinedione medications on micro- and macrovascular complications in patients with diabetes - update 2008 // Cardiovasc Drugs Ther. 2008. V. 22 (3): 233-240], для ингибиторов дипептидил-пептидазы-IV (ДПП-4) - повышение риска развития панкреатита и рака поджелудочной железы [М. Elashoff, A.V. Matveyenko, В. Gier et al. Pancreatitis, pancreatic, and thyroid cancer with glucagon-like peptide-1-based therapies // Gastroenterology. 2011. V. 141 (1): 150-156; E.A. Шестакова, Г.Р. Галстян. Ингибиторы ДПП-4: сравнительный анализ представителей группы // Проблемы эндокринологии. 2012. №1: 61-66]. Для многих антидиабетических веществ характерно развитие гипогликемии [С.Е. Leonard, X. Han, С.М. Brensinger et al. Comparative risk of serious hypoglycemia with oral antidiabetic monotherapy: A retrospective cohort study // Pharmacoepidemiol Drug Saf. 2017. 1-10]. Вышеизложенные факторы определяют необходимость продолжения активного поиска новых высокоэффективных, безопасных противодиабетических препаратов. Известно, что диабет повышает риск развития депрессии, и что основным фактором сопряженности этих двух заболеваний (коморбидности) является недостаточность нейротрофического фактора BDNF [J. Wang, X. Zhao, М. Не Is BDNF biological link between depression and type 2 diabetes mellitus? // Med Hypotheses. 2012. V. 79 (2): 255-258]. Классические антидепрессанты (трициклические антидепрессанты, ингибиторы обратного захвата серотонина и др.) не только не ослабляют проявления диабета, но и могут повысить вероятность его развития [К. Barnard, R.C Peveler, RI.G. Holt Antidepressant medication as a risk factor for type 2 diabetes and impaired glucose regulation: systematic review // Diabetes Care. 2013. V. 36 (10): 3337-3345].
Среди новых терапевтических стратегий, отвечающих требованиям высокой эффективности и безопасности, привлекает внимание стратегия, направленная на сохранение инсулин-продуцирующей функции β-клеток поджелудочной железы за счет нейротрофических воздействий. Известно, что BDNF при экзогенном введении положительно влияет на морфогенез β-клеток и их инсулинопродуцирующую функцию [Е.Е. Noble, C.J. Billington, С.М. Kotz et al. The lighter side of BDNF // Am J Physiol Regul Integr Comp Physiol. 2011. V. 300 (5): 1053-1069]. Синергический эффект BDNF и инсулиноподобного фактора роста ведет к усилению транскрипции генов, способствующих выживанию β-клеток и ослаблению активности систем клеточной гибели [Т. Nakagawa, Y. Ogawa, К. Ebihara et al. Anti-obesity and anti-diabetic effects of brain-derived neurotrophic factor in rodent models of leptin resistance // Int J Obes Relat Disord. 2003. V. 27 (5): 557-565]. В экспериментах in vitro показано, что введение диабетогенного токсина стрептозотоцина (СТЗ) снижает выживаемость клеток инсулиномы RIN5F, тогда как BDNF, внесенный в среду в диапазоне концентраций 10-100 нг/мл, восстанавливает нарушенную диабетогенным токсином выживаемость β-клеток, их инсулин-продуцирующую функцию и активность антиоксидантной системы [S. Bathina, N. Srinivas, U.N. Das BDNF protects pancreatic β cells (RIN5F) against cytotoxic action of alloxan, streptozotocin, doxorubicin and benzo(a)pyrene in vitro // Metabolism. 2016. V. 65 (5): 667-684]. Способность BDNF поддерживать жизнеспособность и функционирование β-клеток, а также стимулировать секрецию инсулина определяют возможный терапевтический потенциал BDNF для лечения СД и его осложнений. Однако применение нативной молекулы BDNF в клинике ограничено широким спектром фармакокинетических особенностей, таких как недостаточная биологическая стабильность молекулы и низкая способность проникать через клеточные барьеры. Антидиабетических препаратов с BDNF-подобным механизмом действия ранее не описано.
В ФГБНУ «НИИ фармакологии имени В.В. Закусова» создано низкомолекулярное соединение, имитирующие эффекты BDNF: на основе структуры β-изгиба 1-й петли BDNF синтезирован димерный дипептидный миметик ГСБ-214 (гептаметилендиамид бис-(N-моносукцинил-L-метионил-L-серина)) [С.Б. Середенин, Т.А. Гудашева Дипептидные миметики нейротрофинов NGF и BDNF: Патент РФ №2410392 // Б.И. 2011. №3; Т.А. Гудашева, А.В. Тарасюк, С.В. Помогайбо и др. Дизайн и синтез дипептидных миметиков мозгового нейротрофического фактора // Биоорганическая химия, 2012. Т. 38 (3): 280-290]. Методом Вестер-блот анализа с использованием моноклональных антител показано, что соединение ГСБ-214 подобно нативной молекуле действует через TrkB рецепторы [Т.А. Гудашева, И.О. Логвинов, П.Ю. Поварнина и др. Анализ зависимости антидепрессивного действия лигандов рецепторов TtrkB от активации МАР-киназного пути // Доклады Академии Наук. 2015. Т. 460 (3): 346-348]. В экспериментах in vitro на модели окислительного стресса на культуре клеток НТ-22 [Т.А. Гудашева, А.В. Тарасюк, С.В. Помогайбо и др. Дизайн и синтез дипептидных миметиков мозгового нейротрофического фактора // Биоорганическая химия. 2012. Т. 38 (3): 280-290] и in vivo на модели окклюзии среднемозговой артерии [Т.А. Gudasheva, P.Y. Povarnina, I.O. Logvinov et al. Mimetics of brain-derived neurotrophic factor loops 1 and 4 are active in a model of ischemic stroke in rats // Drug Des. Devel. Ther. 2016. V. 10: 3545-3553] показано, что соединение ГСБ-214 обладает нейропротективной активностью.
Задачей настоящего изобретения является разработка средства для лечения сахарного диабета 2-го типа, способного замедлять прогрессирование заболевания и предотвращать развитие сопутствующей диабету депрессии.
Техническим результатом изобретения является расширение арсенала антидиабетических средств, замедляющих развитие диабета 2-го типа, и при этом не проявляющих гипогликемического эффекта, и обладающих антидепрессивной активностью.
Решение поставленной задачи достигалось путем применения в качестве антидиабетического средства, ослабляющего также проявления депрессии, сопутствующей диабету, соединения ГСБ-214 (гептаметилендиамид бис-(N-моносукцинил-L-метионил-L-серина)) - оригинального димерного дипептида, созданного на основе структуры 1-й петли BDNF.
Изобретение иллюстрируют следующие примеры:
Пример 1. Эффект комбинированного (профилактического и лечебного) введения соединения ГСБ-214 на модели стрептозотоцинового диабета
Исследование выполнено на самцах мышей линий С57Вl/6 (общим количеством n=66) массой 23-28 г. Экспериментальные животные были получены из Центрального питомника лабораторных животных «Столбовая» (Московская область). Мыши содержались в стандартных условиях вивария при свободном доступе к пище (за исключением 16 часов, предшествующих введению стрептозотоцина) и воде. Животные содержались в пластмассовых клетках с решетчатыми крышками из нержавеющей стали, с подстилкой из деревянной стружки по 10-13 особей в каждой клетке. Использовался полный рацион экструдированного брикетированного корма (ГОСТ на корм Р 50258-92). Содержание животных соответствовало правилам лабораторной практики при проведении доклинических исследований в РФ (ГОСТ 351.000.3-96 и 51000.4-96), Приказу МЗ и CP РФ от 23 августа 2010 г. №708н «Об утверждении Правил лабораторной практики». Эксперименты проводили с 10 до 16 часов.
Стрептозотоциновый (СТЗ) диабет является общепринятой экспериментальной моделью сахарного диабета. При введении этого токсина постепенно развивается как дисфункция β-клеток поджелудочной железы, так и связанные с диабетом метаболические и поведенческие нарушения.
Введение СТЗ в дозе 100 мг/кг в/б мышам С57Вl/6 вызывает СД 2. Экспериментальные животные были разделены на три группы. Животным группы пассивного контроля (Контроль) ежедневно вводили дистиллированную воду (ДВ) в течение 29 дней. Животным группы активного контроля (СТЗ) в течение 14 дней вводили ДВ, затем однократно СТЗ (Sigma) в дозе 100 мг/кг, растворенный в цитратном буфере (рН 4,5), далее продолжалось введение ДВ в течение последующих 14 дней. Животным опытной группы (СТЗ + ГСБ-214) профилактически ежедневно вводили ГСБ-214 в дозе 0,1 или 0,5 мг/кг, растворенный ex tempore в ДВ, затем однократно был введен СТЗ, и далее в течение 14 дней продолжали введение ГСБ-214 в той же дозе.
Определение фонового уровня глюкозы в крови, взятой из хвостовой вены мышей, проводили при помощи глюкометра One Touch Ultra (USA) до введения СТЗ и после введения СТЗ на разные сроки: на 5-е, 12-е, 20-е, 30-е и 60-е сутки. Измерение массы тела животных проводилось каждые 3-4 дня.
Статистическую обработку результатов проводили с помощью программы Statistica 8.0. Для оценки статистической значимости различий между группами по исследуемым параметрам использовали непараметрический метод - критерий Манна-Уитни (Mann-Whitney U test). Результаты считали достоверными при р≤0,05. Экспериментальные данные представлены в виде средних значений по группе с указанием стандартной ошибки среднего (М±SEM).
Для характеристики динамики эффекта исследуемого соединения был рассчитан относительный показатель антигипергликемической активности (Аг) по формуле:
Аг=гл. СТЗ-гл. (СТЗ + В-во) / Гл. СТЗ - гл. ДВ х 100%,
где, гл. СТЗ - уровень глюкозы в крови в группе активного контроля,
гл. СТЗ + В-во - уровень глюкозы крови в опытной группе,
гл. ДВ - уровень глюкозы в крови в группе пассивного контроля.
1.1. Влияние ГСБ-214 в дозе 0,1 мг/кг на уровень гликемии на модели диабета 2-го типа
Профилактическое введение ГСБ-214 в дозе 0,1 мг/кг в течение 14 дней не вызывало изменений уровня глюкозы в крови; показатель гликемии в группе, леченной соединением ГСБ-214, не отличались от пассивного контроля (таблица 1).
СТЗ вызывал достоверное повышение уровня глюкозы в крови у животных группы активного контроля. В опытной группе мышей, которым вводили ГСБ-214, отмечалось ослабление гипергликемии, наибольший эффект наблюдался на 12-е сутки после введения СТЗ, показатель антигипергликемической активности (Аг) на этот срок составлял 86,8% (таблица 1). В отдаленных сроках (на 60-е сутки) после введения токсина, эффект соединения не наблюдался.
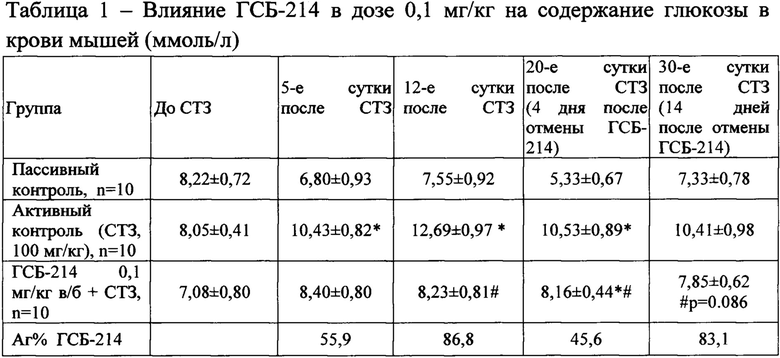
Примечание: достоверные отличия при Р<0,05: * - относительно группы пассивного контроля (Mann-Whitney U test); # - относительно группы активного контроля (СТЗ) (Mann-Whitney U test); Аг - относительный показатель антигипергликемической активности.
1.2. Влияние ГСБ-214 в дозе 0,5 мг/кг на уровень гликемии и массу тела на модели диабета 2-го типа
Профилактическое введение соединения ГСБ-214 в дозе 0,5 мг/кг в течение 14 дней не приводило к изменениям уровня глюкозы в крови мышей С57Вl/6, по сравнению с группой пассивного контроля.
Введение диабетогенного токсина СТЗ в дозе 100 мг/кг вызывало гипергликемию - выраженное повышение уровня глюкозы в крови у животных группы активного контроля до 17-24 ммоль/л, которое сохранялось на протяжении всего эксперимента (60 дней)1. (1 Причиной различного уровня гипергликемии (и изменения динамики веса) в группе активного контроля в пунктах А и Б может явиться разное содержание более активного α-изомера в различных пробах СТЗ, поставляемых фирмой Sigma [de la Garza-Rodea A.S., 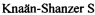 ., den Hartigh J.D., Verhaegen A.P., van Bekkum D.W. Anomer-equilibrated streptozotocin solution for the induction of experimental diabetes in mice (Mus musculus) J Am Assoc Lab Anim Sci. 2010, 49(1): 40-44].).
., den Hartigh J.D., Verhaegen A.P., van Bekkum D.W. Anomer-equilibrated streptozotocin solution for the induction of experimental diabetes in mice (Mus musculus) J Am Assoc Lab Anim Sci. 2010, 49(1): 40-44].).
В опытной группе мышей, которым вводили ГСБ-214, уже с 5-х суток после введения СТЗ отмечалось выраженное ослабление гипергликемии до значений, близких к показателям группы пассивного контроля. При этом антигиперглимеческий эффект соединения не только проявлялся во время терапии, но и сохранялся длительное время после ее отмены - на 44-е сутки после отмены (Таблица 2). Этому соответствует динамика показателя Аг, составляющего 80, 56, 65, 72 и 84% через 5, 12, 20, 30 и 60 дней после введения СТЗ, соответственно.
Примечание: достоверные отличия при Р<0,05: * - относительно группы пассивного контроля (Mann-Whitney U test); # - относительно группы активного контроля (СТЗ) (Mann-Whitney U test); Аг - относительный показатель антигипергликемической активности.
Важным показателем выраженного диабетогенного эффекта СТЗ также является потеря массы тела или замедление ее прибавки. В то время как в группе пассивного контроля наблюдалось постепенное нарастание массы тела, которое к концу эксперимента составило 15% (по отношению к исходной массе), в группе нелеченных диабетических мышей имело место первоначальное уменьшение веса, а затем медленная прибавка массы, которая к концу эксперимента составляла лишь 7%. В группе диабетических мышей, которым вводили ГСБ-214, наблюдалось нарастание массы тела на 16%, т.е имело место полное восстановление массы тела до уровня группы пассивного контроля (Таблица 3).

Примечание - за день «-1» принят день накануне введения СТЗ; достоверные отличия при Р<0,05: * - относительно группы пассивного контроля (Mann-Whitney U test); # -относительно группы активного контроля (СТЗ) (Mann-Whitney U test)
Пример 2. Эффект комбинированного (профилактического и лечебного) введения соединения ГСБ-214 на выраженность депрессивноподобного состояния, вызванного введением СТЗ
Известно, что недостаточность BDNF является важным патогенетическим фактором сопряженности депрессии и диабета [J. Wang, X. Zhao, М. Не Is BDNF biological link between depression and type 2 diabetes mellitus? // Med Hypotheses. 2012. V. 79 (2): 255-258].
Оценка влияния соединения ГСБ-214 в дозах 0,1 и 0,5 мг/кг на выраженность депрессивноподобного состояния осуществлялась в тесте Порсолта в отдаленные сроки после введения СТЗ (61-е и 62-е сутки эксперимента, т.е. на 45-е и 46-е сутки после отмены терапии), поскольку в литературе имеются данные о большой длительности депрессивноподобных проявлений на модели диабета [Y.W. Chen, P.Y. Lin, K.Y. Tu et al. Significantly lower nerve growth factor levels in patients with major depressive disorder than in healthy subjects: a meta-analysis and systematic review // Neuropsychiatric Disease and Treatment. 2015. V. 11: 925-933].
Мышей помещали в сосуды цилиндрической формы диаметром 10 см и высотой 30 см (ООО «НПК Открытая наука»), которые наполняли водой на высоту 20 см (23-25°С). В первый день мышей опускали в сосуд на 10 минут, при этом со 2-й по 6-ю минуту проводили видеорегистрирацию поведения [R.D. Porsolt, A. Bertin, М. Jalfre "Behavioural despair" in rats and mice: strain differences and the effects of imipramine // Eur. J. Pharmacol. 1978. V. 51 (3): 291-294]. Через 24 часа проводили повторное тестирование в течение 6 минут [М.Т. Perona, S. Waters, F.S. Hall et al. Animal models of depression in dopamine, serotonin, and norepinephrine transporter knockout mice: prominent effects of dopamine transporter deletions // Behav. Pharmacol. 2008. V. 19 (5-6): 566-574]. Длительность периодов активного плавания и иммобилизации в обоих сеансах определяли с помощью компьютерной программы «RealTimer». За активное плавание принимали периоды движения передних лап вверх вдоль стенок цилиндра, а за иммобилизацию - полную неподвижность животного, или совершение незначительных движений для поддержания головы над поверхностью воды.
2.1. Влияние ГСБ-214 в дозе 0,1 мг/кг на уровень депрессивноподобного состояния на модели диабета 2-го типа
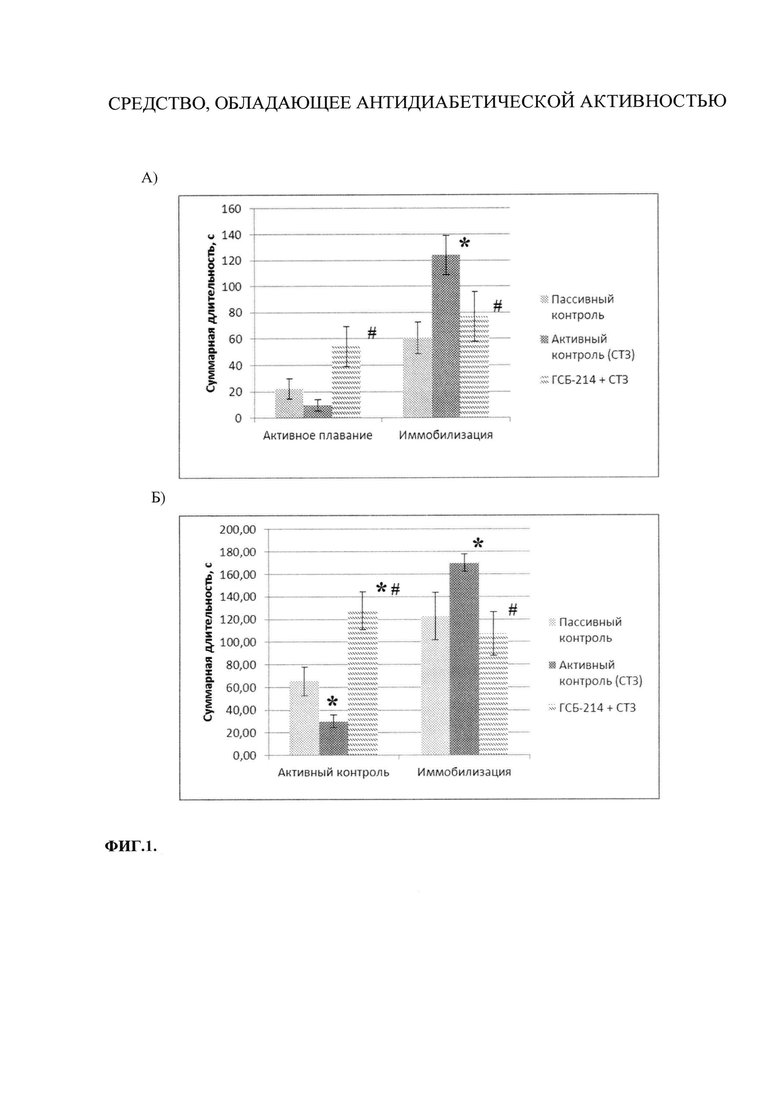
Сравнение показателей активного плавания и времени иммобилизации по группам позволило выявить нарастание в 2 раза суммарного времени иммобилизации у мышей группы активного контроля по сравнению с группой пассивного контроля (с длительностью иммобилизации 60,6 с в группе пассивного контроля до 123,9 с в группе активного контроля). Соединение ГСБ-214 вызывало снижение времени иммобилизации мышей до 76,8 с. На фоне действия соединения также отмечалось увеличение времени активного плавания по сравнению с группой пассивного контроля (рисунок 1 А).
На второй день эксперимента у мышей группы активного контроля тоже было отмечено увеличение времени иммобилизации (с длительности 122,8 с в группе пассивного контроля до 170,0 с в группе активного контроля), а также уменьшение времени активного плавания (с длительности 65,4 с в группе пассивного контроля до 30,4 с в группе активного контроля). Соединение ГСБ-214 вызывало ослабление степени депрессии (с 170,0 с в группе активного контроля до 107,4 в опытной группе), и повышало время активного плавания даже выше уровня пассивного контроля (рисунок 1 Б).
2.2. Влияние ГСБ-214 в дозе 0,5 мг/кг на уровень депрессивноподобного состояния на модели диабета 2-го типа
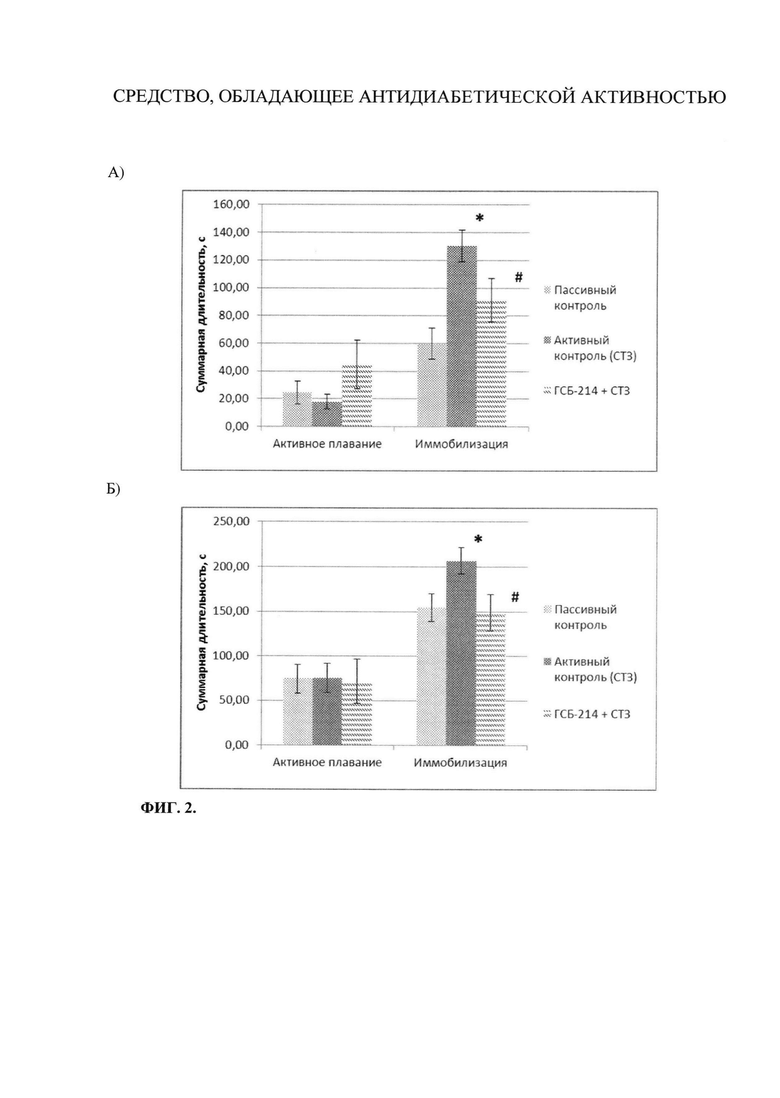
В первый день эксперимента у мышей в группе активного контроля наблюдалось нарастание суммарного времени иммобилизации (с 59,9 с в группе пассивного контроля до 130,5 с в группе активного контроля), соединение ГСБ-214 вызывало снижение времени иммобилизации до 91,4 с (рисунок 2 А).
На второй день эксперимента у мышей группы активного контроля тоже было отмечено увеличение времени иммобилизации (с 154,7 с в группе пассивного контроля до 206,9 с в группе активного контроля), соединение ГСБ-214 вызывало снижение времени иммобилизации до 149,2 с, что свидетельствует об ослаблении степени депрессии (рисунок 2 Б).
Таким образом, показано, что низкомолекулярный димерный миметик мозгового нейротрофического фактора BDNF соединение ГСБ-214 при введении в дозах 0,1 и 0,5 мг/кг в течение 28 дней оказывает антидиабетический эффект и ослабляет выраженность депрессии, сопутствующей диабету, проявляющиеся в снижении уровня гипергликемии и уменьшении иммобилизации на модели депрессивноподобного состояния. Выявлено сохранение эффектов после отмены введения соединения. Установлено отсутствие гипогликемического эффекта у здоровых животных.
Краткое описание чертежей.
На фиг. 1 (Влияние ГСБ-214 в дозе 0,1 мг/кг на показатели депрессивноподобного состояния на модели диабета 2-го типа на 61-е (А) и 62-е (Б) сутки после введения СТЗ) показано влияние ГСБ-214 в дозе 0,1 мг/кг на показатели депрессивноподобного поведения (суммарное время активного плавания и иммобилизации) в отдаленные сроки после введения СТЗ. Ось абсцисс - показатели депрессивноподобного состояния; ось ординат - суммарная длительность (с). Данные представлены в виде средних значений по группе с указанием стандартной ошибки среднего (М±SEM).
* - р<0,05 по сравнению с группой «Пассивный контроль» (U тест Манна-Уитни); # - р<0,05 по сравнению с группой «Активный контроль (СТЗ)» (U тест Манна-Уитни).
На фиг. 2 (Влияние ГСБ-214 в дозе 0,5 мг/кг на показатели депрессивноподобного состояния на модели диабета 2-го типа на 61-е (А) и 62-е (Б) сутки после введения СТЗ) показано влияние ГСБ-214 в дозе 0,5 мг/кг на показатели депрессивноподобного поведения (суммарное время активного плавания и иммобилизации) в отдаленные сроки после введения СТЗ. Ось абсцисс - показатели депрессивноподобного состояния; ось ординат - суммарная длительность (с). Данные представлены в виде средних значений по группе с указанием стандартной ошибки среднего (М±SEM).
* - р<0,05 по сравнению с группой «Пассивный контроль» (U тест Манна-Уитни); # - р<0,05 по сравнению с группой «Активный контроль (СТЗ)» (U тест Манна-Уитни).
| название | год | авторы | номер документа |
|---|---|---|---|
| Фармацевтическая композиция на основе гексаметилендиамида бис-(N-моносукцинил-L-серил-L-лизина) (ГСБ-106) | 2018 |
|
RU2697254C1 |
| СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ДИАБЕТА | 2013 |
|
RU2597848C2 |
| ДИМЕРНЫЙ ДИПЕПТИДНЫЙ МИМЕТИК BDNF КАК СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ОПИОИДНОЙ ЗАВИСИМОСТИ | 2023 |
|
RU2823374C1 |
| ДИМЕРНЫЕ ДИПЕПТИДНЫЕ МИМЕТИКИ НЕЙРОТРОФИНА-3 | 2022 |
|
RU2800369C1 |
| Малые молекулы с NGF-подобной активностью, обладающие антидиабетическими свойствами | 2013 |
|
RU2613314C2 |
| Низкомолекулярный миметик BDNF как средство для лечения опиоидной зависимости | 2019 |
|
RU2707301C1 |
| СРЕДСТВО ДЛЯ ПРЕДУПРЕЖДЕНИЯ И КОРРЕКЦИИ ПРОЯВЛЕНИЙ ДИАБЕТА | 2012 |
|
RU2563234C2 |
| Низкомолекулярный миметик нейротрофина-3 в качестве средства для снижения болевой реакции и восстановления чувствительности при периферической нейропатии | 2024 |
|
RU2828668C1 |
| СПОСОБ КОРРЕКЦИИ ДЕПРЕССИВНЫХ РАССТРОЙСТВ ПРОИЗВОДНЫМИ ТИЕТАН-1,1-ДИОКСИДА В ЭКСПЕРИМЕНТЕ | 2010 |
|
RU2424799C1 |
| Применение производных N,N"-замещенных 3,7-диазабицикло[3.3.1]нонанов для терапии депрессии | 2019 |
|
RU2726313C1 |
Изобретение относится к фармакологии, а именно к применению димерного дипептида ГСБ-214 (гептаметилендиамид бис-(N-моносукцинил-L-метионил-L-серина)) в качестве средства, обладающего антидиабетической активностью и ослабляющего проявление депрессии, сопутствующей диабету. Изобретение расширяет арсенал антидиабетических средств, замедляющих развитие диабета 2-го типа и при этом не проявляющих гипогликемического эффекта, и обладающих антидепрессивной активностью. 2 ил., 3 табл., 2 пр.
Применение димерного дипептида ГСБ-214 (гептаметилендиамид бис-(N-моносукцинил-L-метионил-L-серина)) в качестве средства, обладающего антидиабетической активностью и ослабляющего проявление депрессии, сопутствующей диабету.
| ДИПЕПТИДНЫЕ МИМЕТИКИ НЕЙРОТРОФИНОВ NGF И BDNF | 2009 |
|
RU2410392C2 |
| ОСТРОВСКАЯ Р | |||
| У | |||
| и др | |||
| Эффективность Ноопепта на стрептозотоциновой модели диабета у крыс //Бюллетень экспериментальной биологии и медицины | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| - Т | |||
| Способ приготовления кирпичей для футеровки печей, служащих для получения сернистого натрия из серно-натриевой соли | 1921 |
|
SU154A1 |
| - No | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| - С | |||
| Приспособление для обрезывания караваев теста | 1921 |
|
SU317A1 |
| US 6391312 B1, 21.05.2002 | |||
| DIEMEL L | |||
| T | |||
| et al | |||
| Expression of neuropeptides in experimental diabetes; effects of treatment with nerve growth factor or brain-derived neurotrophic factor //Molecular brain research | |||
| Прибор для охлаждения жидкостей в зимнее время | 1921 |
|
SU1994A1 |
| - Т | |||
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
| - No | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| - С | |||
| Аппарат для передачи изображений на расстояние | 1920 |
|
SU171A1 |
Авторы
Даты
2019-07-03—Публикация
2017-11-20—Подача