Область техники, к которой относится изобретение
Изобретение относится к области фармакогенетики и персонализированной медицины и касается способа определения генетических маркеров, которые обуславливают индивидуальную чувствительность к статинам (симвастатин, аторвастатин, правастатин, розувастатин), с использованием полимеразной цепной реакции (ПЦР) и последующей гибридизацией с олигонуклеотидным биологическим микрочипом (биочипом).
Полиморфные варианты генов SLCO1B1, АРОЕ и АВСВ1 являются одной из причин межиндивидуальных различий в ответе на статины. Генетическое тестирование SLCO1B1 при назначении этих препаратов включено в Рекомендации экспертов Консорциума по внедрению клинической фармакогенетики (CPIC, США) (Wilke RA, Ramsey LB, Johnson SG et al; The clinical pharmacogenomics implementation consortium: CPIC guideline for SLCO1B1 and simvastatin-induced myopathy. Clin Pharmacol Ther. 2012 Jul; 92(1): 112-7), а также в Практические рекомендации экспертов Европейского научного фонда по применению фармакогенетического тестирования (Becquemont L, Alfirevic А, Amstutz U, Brauch Н et. al. Pharmacogenomics. Practical recommendations for pharmacogenomics-based prescription: 2010 ESF-UB Conference on Pharmacogenetics and Pharmacogenomics. 2010; 12(1):113-24).
Применение фармакогенетического тестирования с использованием настоящего изобретения позволит персонализировать терапию статинами, в том числе снизить риск нежелательных лекарственных реакций (в частности, статин-индуцированной миопатии).
Уровень техники
В настоящее время существует ряд методов анализа полиморфизма генома человека, в том числе и для анализа маркеров в генах SLCO1B1, АРОЕ и АВСВ1. Большинство современных методов основано на проведении ПЦР с различными вариациями, при этом дизайн реакций и способы детекции результата существенно варьируются, и зависят от конкретных задач.
Наиболее распространенными методами анализа полиморфизма генома являются:
1. Секвенирование по Сенгеру:
Метод является достаточно информативным. Он предоставляет полную информацию о последовательности ДНК в исследуемом локусе. Однако он характеризуется низкой производительностью, высокой стоимостью проведения анализа, время- и трудозатратен. Часто этот метод используется для подтверждения результатов, полученных с помощью других методов [Fesenko DO, Avdonina MA, Gukasyan LG, Surzhikov SA, Chudinov AV, Zasedatelev AS, Nasedkina TV. Multiplex Genotyping of Allelic Variants of Genes Involved in Metabolizing Antileukemic Drugs. Mol Biol (Mosk). 2018; 52(2):238-245.].
2. Аллель-специфичный рестрикционный анализ (ПДРФ, полиморфизм длин рестрикционных фрагментов):
Данный метод требует постановки ПЦР и реакции рестрикции, что делает его трудоемким и повышает вероятность ошибки, не подлежит автоматизации. Однако данный метод не требует высокой квалификации персонала и дорогостоящего оборудования [Su J, Yu Q, Zhu H, Li X, Cui H, Du W, Ji L, Tong M, Zheng Y, Xu H, Zhang J, Zhu Y, Xia Y, Liu T, Yao Q, Yang J, Chen X, Yu J. The risk of clopidogrel resistance is associated with ABCB1 polymorphisms but not promoter methylation in a Chinese Han population. PLoS One. 2017 Mar 30; 12(3):e0174511.;  The role of CYP2D6 and ABCB1 pharmacogenetics in
The role of CYP2D6 and ABCB1 pharmacogenetics in  patients with first-episode schizophrenia treated with risperidone. Eur J Clin Pharmacol. 2010 Nov; 66(11):1109-17.].
patients with first-episode schizophrenia treated with risperidone. Eur J Clin Pharmacol. 2010 Nov; 66(11):1109-17.].
3. Аллель-специфичная ПЦР (AS-PCR)
Метод распространен достаточно широко, однако требует постановки независимых параллельных ПЦР-реакций, соответствующих количеству анализируемых однонуклеотидных замен, что снижает его ценность для широкомасштабного генотипирования. Детекция осуществляется в режиме реального времени или по конечной точке реакции с последующим разделением продуктов с помощью электрофореза [Op den Buijsch RA, Wijnen PA, van Dieijen-Visser MP, de Vries JE, Bekers O. Rapid genotyping of the OATP1B1 polymorphisms A388G and T521C with real-time PCR FRET assays. Pharmacogenomics. 2005 Jun;6(4):393-7.;  Barczak W, Gryczka R,
Barczak W, Gryczka R,  Jagielski P, Czernikiewicz A,
Jagielski P, Czernikiewicz A,  Wojewoda A, Perz K,
Wojewoda A, Perz K,  Morze K, Kanduta Z, Lisiak N, Mrozikiewicz PM, Grodecka-Gazdecka S,
Morze K, Kanduta Z, Lisiak N, Mrozikiewicz PM, Grodecka-Gazdecka S,  Study of ABCB1 polymorphism frequency in breast cancer patients from Poland. Pharmacol Rep. 2012; 64(6): 1560-6.].
Study of ABCB1 polymorphism frequency in breast cancer patients from Poland. Pharmacol Rep. 2012; 64(6): 1560-6.].
4. ПЦР в реальном времени с TaqMan-зондами:
Метод является достаточно быстрым и удобным. Требует оборудования для ПЦР в реальном времени. Возможен анализ нескольких локусов в одной пробирке. [Thompson J F, Man M, Johnson К J, Wood L S, Lira M E, Lloyd D B, Banerjee P, Milos P M, Myrand S P, Paulauskis J, Milad M A, Sasiela W J. An association study of 43 SNPs in 16 candidate genes with atorvastatin response. The pharmacogenomics journal. 2005.; Baldissera VD, de Mattos AA, Coral GP, de Araujo FB, Marroni CA, de Mello  AB, Ott Fontes PR, Schmidt Cerski CT, Hartmann AA, Kretzmann Filho NA. Evaluation of the C3435T polymorphism in the MDR1 gene in patients with hepatocellular carcinoma. Ann Hepatol. 2012 Nov-Dec; 11(6):899-906.].
AB, Ott Fontes PR, Schmidt Cerski CT, Hartmann AA, Kretzmann Filho NA. Evaluation of the C3435T polymorphism in the MDR1 gene in patients with hepatocellular carcinoma. Ann Hepatol. 2012 Nov-Dec; 11(6):899-906.].
5. Анализ кривых плавления высокого разрешения:
Метод 5 является достаточно простым методом скрининга, однако для анализа некоторых последовательностей данный метод не подходит. HRM анализ может быть выполнен только на приборе с специальным каналом для HRM и специальным программным обеспечением. Кроме того, он также требует постановки нескольких параллельных реакций для каждого пациента по числу анализируемых локусов [Kaewboonlert N, Thitisopee W, Sirintronsopon W, Porntadavity S, Jeenduang N. Lack of association between SLCO1B1 polymorphisms and lipid-lowering response to simvastatin therapy in Thai hypercholesterolaemic patients. J Clin Pharm Ther. 2018 Oct; 43(5):647-655.; Yang H, Wang Q, Zheng L, Lin M, Zheng XB, Lin F, Yang LY. Multiple Genetic Modifiers of Bilirubin Metabolism Involvement in Significant Neonatal Hyperbilirubinemia in Patients of Chinese Descent. PLoS One. 2015 Jul 6; 10(7):e0132034.].
6. Высокопроизводительное секвенирование (next generation sequencing, NGS):
Метод является высокоинформативным. Однако из-за высокой стоимости оборудования, расходных материалов и необходимости высокой квалификации персонала его применение в рутинной лабораторной диагностике ограничено. Используется для поиска ассоциаций [Thompson John F, Hyde Craig L, Wood Linda S, Paciga Sara A, Hinds David A, Cox David R, Hovingh G Kees, Kastelein John J P. Comprehensive whole-genome and candidate gene analysis for response to statin therapy in the Treating to New Targets (TNT) cohort. Circulation. Cardiovascular genetics. 2009.; Calandra S, Tarugi P, Bertolini S. Impact of rare variants in autosomal dominant hypercholesterolemia causing genes. Curr Opin Lipidol. 2017 Jun; 28(3):267-272.].
Запатентовано большое количество методов анализа полиморфных генетических маркеров для определения индивидуальной чувствительности к статинам, в том числе те, которые позволяют анализировать генетические варианты генов SLCO1B1, АРОЕ и АВСВ1.
В китайском патенте CN 105803099 A от 2016-05-16 описан метод одновременного обнаружения мутаций SLCO1B1, АРОЕ и LDLR, однако полиморфизм гена АВСВ1 не включен в данный анализ. В китайском патенте CN 106434940 A от 2016-10-20 праймеры для обнаружения локуса rs17238540 гена HMGCR, rs7412 гена АРОЕ, rs429358 гена АРОЕ и rs4149056 гена SLCO1B1, однако метод не позволяет анализировать аллели гена АВСВ1. В китайском патенте CN 107099602 A от 2017-05-27 представлен анализ полиморфизма генов АРОЕ, SLCO1B1, СЕТР, АВСВ1 и MTHFR. Данная панель генетических маркеров широка и информативна, однако для проведения анализа требуется оборудование для ПЦР в реальном времени, которым располагают не все диагностические лаборатории.
Раскрытие сущности изобретения
Задача настоящего изобретения состоит в создании способа определения генетических маркеров, которые обуславливают индивидуальную чувствительность к статинам. Панель маркеров включает наиболее информативные генетические маркеры, определение которых позволяет персонализировать терапию статинами, снизить риск нежелательных лекарственных реакций (в частности, статин-индуцированной миопатии).
Сущность изобретения заключается в обеспечении способа анализа однонуклеотидного полиморфизма (SNP, Single nucleotide polymorphism) генов SLCO1B1, АРОЕ, АВСВ1, продукты которых обуславливают индивидуальную чувствительность к статинам (симвастатин, аторвастатин, правастатин, розувастатин). Данный способ позволяет выявлять следующие полиморфные маркеры в генах: SLCO1B1 (rs4149056, rs4149015), АРОЕ (rs7412), АВСВ1 (rs2032582).
Основными признаками данного изобретения являются мультиплексная одноэтапная ПЦР и последующая гибридизация продуктов на биочипе, содержащем набор иммобилизованных олигонуклеотидных зондов.
Первый важный признак изобретения - набор праймеров для амплификации анализируемых локусов, который используется для получения флуоресцентно меченных продуктов в необходимом количестве для гибридизации на биочипе. Один из пары праймеров для каждого локуса имеет часть, комплементарную участку гена (на 3'-конце) и часть с универсальной последовательностью (на 5'-конце), соответствующей универсальному праймеру. Последовательности праймеров для проведения ПЦР приведены в Перечне последовательностей 1 (последовательности SEQ ID NO: 1-9).
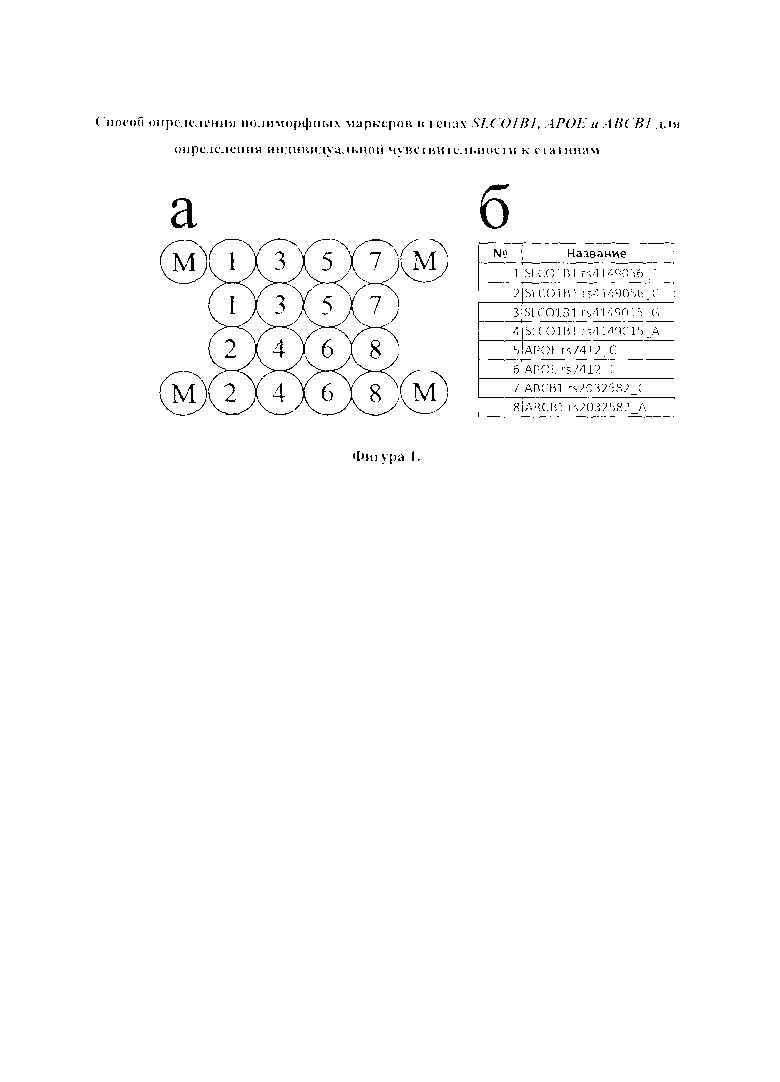
Второй важный признак изобретения - биочип, содержащий набор иммобилизованных олигонуклеотидных зондов, последовательности которых приведены в Перечне последовательностей 2 (последовательности SEQ ID NO: 10-17). Олигонуклеотидные зонды иммобилизуются в ячейках гидрогелевого микрочипа, как описано в патенте RU 2206575 (дата публикации 2003-06-20) в концентрации 2000 мкМ. Схема расположения зондов в ячейках биочипа приведена на Фигуре 1.
Набор праймеров для ПЦР используется при проведении одноэтапной ПЦР, результатом которой является флюоресцентно меченный продукт, полученный за два раунда, для последующей гибридизации на биочипе. Далее проводится гибридизация флуоресцентно меченных фрагментов ДНК с иммобилизованными в ячейках биочипа олигонуклеотидными зондами, расположенными на пластиковой подложке. После проведения гибридизации и отмывки биочипа проводится анализ полученной флуоресцентной картины, на основании которой делается отчет о генотипе исследуемого образца. Пример картины гибридизации приведен на Фигуре 2.
Краткое описание таблиц и фигур
Фигура 1. Схема расположения зондов в ячейках биочипа для анализа полиморфных маркеров в генах SLCO1B1, АРОЕ и АВСВ1 для определения индивидуальной чувствительности к статинам. (а) расположение ячеек на биочипе; (б) расшифровка условных обозначений. (М) - ячейки, содержащие флуоресцентный краситель Су5, светящийся перманентно, для ориентировки и контроля интенсивности свечения.
Фигура 2. Гибридизационная картина анализа полиморфных маркеров в генах SLCO1B1, АРОЕ и АВСВ1 для определения индивидуальной чувствительности к статинам (пациент №1), полученная на биочипе.
Осуществление изобретения
Для обеспечения оптимальных условий мультиплексной ПЦР необходимо использовать праймеры, обеспечивающие специфичный и эффективный отжиг на мишени при одинаковой температуре (для одного этапа), и они не должны образовывать при этой температуре вторичные структуры, в том числе и в условиях мультиплексной ПЦР. Для оптимальной (стабильной и специфичной) наработки необходимого для гибридизации на биочипе количества флюоресцентно меченного ПЦР-продукта должны быть подобраны такие параметры как концентрации реагентов в реакционной смеси и температурно-временной режим реакции. В результате проведенной работы были подобраны праймеры и условия для проведения ПЦР, которые позволяют осуществлять эффективную наработку исследуемых локусов ДНК в условиях мультиплексной ПЦР.
Для иммобилизации на биочипе подбираются олигонуклеотидные зонды, позволяющие идентифицировать все выбранные для анализа участки генов.
Олигонуклеотидные зонды должны быть подобраны в соответствии со следующими критериями:
1) Олигонуклеотидный зонд должен обладать высокой специфичностью к анализируемому локусу.
2) Предпочтительно расположение вариабельного нуклеотида в серединной области зонда, так как такая конструкция зонда позволяет добиться лучшей дискриминации между совершенными и несовершенными дуплексами.
3) Олигонуклеотидный зонд в условиях, при которых проводится гибридизация не должен образовывать стабильных вторичных структур, наличие которых может приводить к снижению эффективности гибридизации.
Для анализа полиморфных маркеров в генах SLCO1B1, АРОЕ и АВСВ1 для определения индивидуальной чувствительности к статинам на биочипе было иммобилизовано 10 высокоспецифичных дифференцирующих олигонуклеотидных зондов (Перечень последовательностей 2, последовательности SEQ ID NO: 10-17), структура которых обеспечивает высокоспецифичное связывание с полностью комплементарными ДНК-мишенями. Яркий флюоресцентный сигнал наблюдается только в ячейках, в которых при гибридизации образовался совершенный дуплекс между олигонуклеотидным зондом и флюоресцентно меченным ПЦР-продуктом.
Приведем последовательность анализа с использованием данного метода. Амплификация ПЦР-продуктов для последующей гибридизации на биочипе проводится посредством мультиплексной одноэтапной ПЦР, при этом в качестве матрицы для проведения реакции используют образец ДНК, выделенный из крови или соскоба буккального эпителия любым известным исследователю методом (фенол-хлороформная экстракция, выделение на колонках, выделение на сорбенте и т.д.).
ПЦР может быть проведена с использованием любого вида термостабильной полимеразы (Taq-полимераза, Taq-полимераза с горячим стартом, Tth-полимераза, Tfl-полимераза, Pfu-полимераза, Vent-полимераза, DeepVent-полимераза и другие коммерчески доступные ферменты, выделенные из термофилов), работающей в соответствующем буфере. Для построения новой цепи в буфер добавляется смесь дНТФ (дАТФ, дГТФ, дЦТФ, дТТФ). Для проведения ПЦР могут быть использованы готовые коммерчески доступные наборы, содержащие все необходимые компоненты за исключением праймеров.
В ходе мультиплексной одноэтапной ПЦР осуществляется наработка преимущественно одноцепочечных продуктов (за счет добавления в реакцию избытка универсального праймера), и их флюоресцентное маркирование с использованием дУТФ-Су5, который способен включаться в растущую цепь ДНК. В качестве флуоресцентной метки также может быть использован любой флуорохром без ограничения (например, FITC, Texas red, Су-3 и т.д.), а также биотин.
Синтез праймеров и олигонуклеотидных зондов осуществляется с помощью таких химических подходов как фосфодиэфирный метод, гидрофосфорильный метод и т.д. Для синтеза праймеров используются автоматические ДНК/РНК синтезаторы, например, производства фирмы «Applied Biosystems» (США). Для иммобилизации в гидрогелевых ячейках биочипа, к 5'- или 3'-концу олигонуклеотидных зондов добавляется активная группа (например на 3'-конец может быть добавлена свободная аминогруппа с помощью 3'-Amino-Modifier С7 CPG 500, «Glen Research)), США).
Для проведения ПЦР используют праймеры SEQ ID NO: 1-8 в концентрации 1 пикомоль/мкл, и универсальный праймер SEQ ID NO: 9 в концентрации 50 пикомоль/мкл. Последовательности праймеров приведены в Перечне последовательностей 1.
Далее проводится гибридизация флуоресцентно - меченых фрагментов ДНК, полученных после проведения ПЦР, с иммобилизованными в ячейках геля олигонуклеотидными зондами, последовательности которых представляют собой участки, комплементарные последовательностям мажорного или минорного аллеля по исследуемым локусам.
Гибридизация ПЦР-продукта с олигонуклеотидными зондами на биочипе может быть проведена в любом гибридизационном буфере, например, в SSPE-буфере с формамидом или буфере с гуанидином. Перед постановкой гибридизации ПЦР-продукт прогревают при 95°C в течение 5 минут, затем охлаждают на льду в течение 2 минут, после чего наносят гибридизационную смесь на биочип. Гибридизация проводят 12-14 ч при 37°C. Отмывка биочипа после проведения гибридизации может быть проведена в любом известном в данной области техники буфере (SSC, SSPE и т.п.) или в дистиллированной воде.
Анализируемый фрагмент ДНК в условиях (состав реакции, температура и время гибридизации), при которых осуществляется гибридизация, образует совершенные дуплексы только с полностью комплементарными ему олигонуклеотидными зондами. Сигнал флюоресценции детектируется только в ячейках, в которых образовался совершенный дуплекс. В случае, если дуплекс несовершенный (присутствует хотя бы один не спаренный нуклеотид), то сигнал флюоресценции отсутствует.
Далее проводится визуализация результатов гибридизации с помощью любой детектирующей системы, способной возбуждать флюоресценцию и распознавать флуоресцентный сигнал (например, портативный анализатор биочипов, снабженный ПЗС-камерой и специальным программным обеспечением, производства ООО «БИОЧИП-ИМБ» (Москва, Россия)).
Изготовление биочипов может осуществляться посредством последовательного нанесения на поверхность подложки из стекла ячеек акриламидного геля, активации ячеек и иммобилизации в ячейках модифицированных олигонуклеотидов [Analysis of SNPs and other genomic variations usins sel-based chips / A. Kolchinsky, A. Mirzabekov // Hum Mutat. - 2002. - Vol. 19. - P. 343-360. Review]. В качестве подложки кроме стекла может быть использован любой материал, в том числе металл, гибкие мембраны и пластик (Патент RU 2309959, опубликован 2007-11-10). Биочипы также могут быть изготовлены и другими известными способами [Arrays of immobilized oligonucleotides-contributions to nucleic acids technology / H. Seliger, M. Hinz, E. Happ // Curr Pharm Biotechnol. - 2003. - Vol. 4. - P. 379-395].
Для изготовления биочипа в настоящем изобретении используется набор олигонуклеотидных зондов SEQ ID NO: 10-17, приведенный в Перечне последовательностей 2. Расположение конкретных олигонуклеотидных зондов на биочипе может варьироваться в зависимости от удобства интерпретации результатов.
Далее приведены примеры, иллюстрирующие возможности применения способа анализа полиморфных маркеров в генах SLCO1B1, АРОЕ и АВСВ1 для определения индивидуальной чувствительности к статинам. Варианты и модификации осуществления изобретения, которые могут быть воспроизведены, не отходя от общей концепции настоящего изобретения и без привлечения собственной изобретательской деятельности, также будут входить в объем притязаний настоящего изобретения.
Пример 1. Амплификация участков генов SLCO1B1, АРОЕ и ABCB1 с целью получения флуоресцентно меченного ПЦР-продукта в необходимом количестве.
Из крови пациента больного выделяли ДНК с помощью набора QIAamp DNA Blood Mini Kit (Qiagen, США).
Наработку участков анализируемых генов проводили методом одноэтапной мультиплексной ПЦР. ПЦР проводилась в одной реакции для каждого образца. ПЦР-смесь общим объемом 25 мкл включала в себя: 0.5 ед. акт. Taq-полимеразы («СибЭнзим», Россия), ПЦР-буфер (70 мМ Трис-HCl (рН 8.3), 16.6 мМ (NH4)SO4, 2.5 мМ MgCl2, 200 мкМ каждого дНТФ («СибЭнзим», Россия), 10 нг ДНК, по 1 пмоль каждого праймера SEQ ID NO: 1-14, 50 пмоль универсального праймера SEQ ID NO: 9, 8 мкМ флуоресцентно меченного дУТФ-Су5. Амплификацию проводили по следующей схеме: 40 циклов (94°C 30 с, 65°C 30 с, 67°C 30 с, 69°C 30 с, 72°C 20 с), далее 40 циклов (94°C 30 с, 56°C 10 с, 72°C 30 с), на приборе Т100 («Bio-Rad», США).
Пример 2. Олигонуклеотидный биочип для анализа полиморфных маркеров в генах SLCO1B1, АРОЕ и АВСВ1.
Олигонуклеотидные зонды для иммобилизации на микрочипе синтезировали на автоматическом синтезаторе 394 DNA/RNA Synthesizer («Applied Biosystems», США) с использованием стандартной фосфоамидитной процедуры. В 3'-конец олигонуклеотидов вводят спейсер со свободной аминогруппой, используя метод 3'-Amino-Modifier С7 CPG 500 («Glen Research», США).
Биочип изготовляют методом сополимеризации олигонуклеотида в акриламидном геле (патент RU 2309959, опубликованный 2007-11-10 и RU 2175972, опубликованный 2001-11-20). Биочип содержит 8 иммобилизованных олигонуклеотидных зондов (SEQ ID NO: 10-29), список которых представлен также в Перечне последовательностей 2. Ячейки наносят согласно схеме на Фигуре 1.
Пример 3. Гибридизация меченного продукта на биочипе
Реакционную смесь, полученную после проведения второго этапа ПЦР, описанного в Примере 1, использовали для гибридизации на биочипе. 10 мкл формамида ("Serva", США), 10 мкл 20*SSPE ("Promega", США) и 20 мкл амплификата. Гибридизационную смесь денатурировали при 95°C 5 минут, охлаждали во льду 2 минуты, наносили на биочип и оставляли на 12 часов при 37°C. После проведения гибридизации биочип отмывали в 1x SSPE в течение 10 минут при комнатной температуре.
Пример 4. Регистрация и интерпретация результатов гибридизации
Регистрацию гибридизационной картины производили с помощью портативного анализатора биочипов, снабженного ПЗС-камерой, производимого ООО «Биочип-ИМБ». По полученной гибридизационной картине, представленной на Фигуре 2. определяли генотип образца
Генотип образца:
SLCO1B1 rs4149056_T/T
SLCO1B1 rs4149015_G/G
АРОЕ rs7412_C/G
ABCB1 rs2032582_C/A



Изобретение относится к области фармакогенетики и персонализированной медицины. Предложен способ анализа полиморфных маркеров в генах SLCO1B1, АРОЕ и АВСВ1 для определения индивидуальной чувствительности к статинам, предусматривающий следующие стадии: амплификацию с помощью мультиплексной одноэтапной ПЦР, обеспечение биочипа, гибридизацию флуоресцентно меченного ПЦР-продукта на биочипе и регистрацию и интерпретацию результатов гибридизации. Изобретение обеспечивает выявление следующих полиморфных маркеров: SLCO1B1 (rs4149056, rs4149015), АРОЕ (rs7412), АВСВ1 (rs2032582). 1 з.п. ф-лы, 2 ил., 2 табл., 4 пр.
1. Способ анализа полиморфных маркеров в генах SLCO1B1, АРОЕ и АВСВ1 для определения индивидуальной чувствительности к статинам, предусматривающий следующие стадии:
(а) амплификацию фрагментов генов SLCO1B1, АРОЕ и АВСВ1 с помощью мультиплексной одноэтапной ПЦР, в которой в качестве матрицы для амплификации используется ДНК, выделенная из крови или другого биоматериала, полученного от пациента, и праймеры, представленные последовательностями SEQ ID NO: 1-9;
(б) обеспечение биочипа для анализа и идентификации полиморфных маркеров в генах SLCO1B1, АРОЕ и АВСВ1 для определения индивидуальной чувствительности к статинам, набором олигонуклеотидных зондов, представленных последовательностями SEQ ID NO: 10-17;
(в) гибридизацию флуоресцентно меченного ПЦР-продукта, полученного на стадии (а), на биочипе, полученном на стадии (б);
(г) регистрацию и интерпретацию результатов гибридизации на биочипе, проведенной на стадии (в).
2. Способ по п. 1, в котором для идентификации полиморфных маркеров в генах SLCO1B1, АРОЕ и АВСВ1, амплифицированных с помощью набора праймеров, охарактеризованных в п. 1, используется биочип, представляющий собой подложку с набором иммобилизованных на ней олигонуклеотидных зондов с последовательностями, представленными в SEQ ID NO: 10-17.
| КАЗАКОВ Р.Е | |||
| и др | |||
| Значение генетических факторов в прогнозировании побочного действия статинов | |||
| Международный журнал прикладных и фундаментальных исследований | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| CN 105803099 A, 27.07.2016 | |||
| CN 107099602 A, 29.08.2017. | |||
Авторы
Даты
2019-07-26—Публикация
2018-12-28—Подача