Область техники, к которой относится изобретение
Изобретение относится к области генетики, молекулярной биологии и медицины, и может быть использовано для определения генетической предрасположенности к болезни Альцгеймера посредством анализа полиморфизма в генах АроЕ, ApoJ и GAB2 в российских популяциях.
Уровень техники
Известно большое количество способов определения генетического полиморфизма в которых используются различные инструменты для анализа уникальной нуклеотидной последовательности ДНК человека. Условно среди них можно выделить шесть групп:
1) Ферментативные подходы:
полиморфизм длин амплифицированных фрагментов (AFLP);
полиморфизм длин рестрикционных фрагментов (RFLP);
расщепление клевазой (CFLP);
расщепление резольвазой (EMD);
анализ, основанный на лигазной реакции (LDR, LCR);
инвазивное расщепление олигонуклеотидов;
случайная амплификация полиморфной ДНК (RAPD, AP-PCR);
ПЦР с прямой терминацией синтеза (DT-PCR);
аллель-специфическая ПЦР (AS-PCR, PCR-SSP).
2) Химические методы:
химическое расщепление гетеродуплексов;
химическое лигирование.
3) Методы, основанные на различной электрофоретической подвижности полиморфных участков ДНК:
анализ конформации одноцепочечных фрагментов (SSCP);
гетеродуплексный анализ (НА);
секвенирование.
4) Детекция на твердой фазе:
гибридизация на олигонуклеотидных матрицах;
оптико-волоконный ДНК-гибридизационный анализ;
элонгация иммобилизованных праймеров (минисеквенирование);
пиросеквенирование.
5) Хроматографические методы:
высокоэффективная жидкостная хроматография (HPLC).
6) Физические методы:
масс-спектрометрия;
резонансное тушение флуоресценции (FRET);
люминесценция, зависящая от локального окружения.
Наиболее распространенными из представленных методов являются:
1. Анализ полиморфизма длин рестрикционных фрагментов ДНК (RFLP-анализ).
Определение полиморфного сайта рестрикции методом RFLP (restriction fragment length polymorphism) заключается в ПЦР-амплификации интересующего фрагмента и его последующем расщеплении соответствующим ферментом рестрикции. Далее проводится визуализация результатов рестрикции для оценки распределения фрагментов по длине различными методами, в том числе с помощью блот-гибридизации. Преимуществами метода являются простота и надежность, недостатками -длительность проведения анализа, трудоемкость, а также возможность детекции только известных полиморфных замен, при этом одновременно можно выявлять не более двух SNPs.
[Garcia AN, Silva HA, Silva RC, Leal EM, Rodrigues L, Silva VC, Dellalibera E, Freitas EM, Ataide L Jr, Muniz MT. APOE-epsilon4 polymorphism and cognitive deficit among the elderly population of Fernando de Noronha. Arq Neuropsiquiatr. 2008 Jun; 66(2B):298-302]
[Rihn BH, Berrahmoune S, Jouma M, Chamaa S, Marcocci L, Le Faou A. APOE genotyping: comparison of three methods. Clin Exp Med. 2009 Mar; 9(J):61-5]
2. Секвенирование амплифицированных фрагментов ДНК.
Секвенирование является самым точным методом анализа генетических вариаций. Преимуществами метода являются высокая точность и чувствительность, недостатками - высокая стоимость оборудования, что исключает широкое внедрение метода в клиническую практику. Существует несколько модификаций реакции сиквенса, снижающих ее стоимость. Например, можно секвенировать сразу обе цепи в одной реакции используя два различно меченых праймера. Другой способ - использование SSR (single sequencing reaction), когда для терминации синтеза используется только один из четырех ddNTP. Активно разрабатываются способы совмещения ПЦР-амплификации и секвенирования в одной пробирке сразу для нескольких локусов.
[Rihn ВН, Berrahmoune S, Jouma М, Chamaa S, Marcocci L, Le Faou A. APOE genotyping: comparison of three methods. Clin Exp Med. 2009 Mar; 9(l):61-5]
[Yang L, Lu R, Jiang L, Liu Z, Peng Y. Expression and genetic analysis of tumor necrosis factor-alpha (TNF-alpha) G-308A polymorphism in sporadic Alzheimer's disease in a Southern China population. Brain Res. 2009 Jan 9; 1247:178-81}
3. Аллель-специфичная ПЦР (AS-PCR).
Для проведения ПЦР с высокой эффективностью 3′-концевой нуклеотид праймера должен быть комплементарен соответствующему нуклеотиду матричной ДНК. В противном случае эффективность удлинения праймера во время ПЦР резко снижается и при определенных сочетаниях ошибочно спаренных нуклеотидов может отсутствовать вообще. Именно эта особенность ПЦР и лежит в основе метода обнаружения мутаций и однонуклеотидного полиморфизма с помощью аллель-специфичной ПЦР, иначе называемой аллель-специфической элонгацией праймера. Преимуществом метода является высокая скорость, так как при правильно подобранных условиях анализ SNPs занимает всего 3-4 часа. К недостаткам метода можно отнести точность (большое количество ложноположительных результатов), трудоемкость (для каждого нового SNP необходимо корректировать условия реакции и тщательно подбирать последовательности праймеров), а также невозможность одновременной детекции большого числа SNP в одном анализе.
[Lin GF, Ma QW, Zhang DS, Zha YL, Lou KJ, Shen JH. Polymorphism of alpha-estrogen receptor and aryl hydrocarbon receptor genes in dementia patients in Shanghai suburb. Acta Pharmacol Sin. 2003 Jul; 24(7):651-6]
4. Анализ конформации одноцепочечных фрагментов ДНК (SSCP). SSCP-анализ включает денатурацию ПЦР-продуктов и разделение их в неденатурирующем геле. Электрофоретическая подвижность одноцепочечных фрагментов ДНК зависит от их нуклеотидной последовательности, определяющей характер вторичных и третичных структур, и меняется даже при отличии в один нуклеотид. Преимуществами метода являются простота, чувствительность, относительно невысокая стоимость, возможность использования флуоресцентной метки и капиллярного электрофореза, что позволяет легко автоматизировать процесс и анализировать одновременно большое количество локусов. К недостаткам метода можно отнести низкую воспроизводимость результатов, особенно при обнаружении de novo мутаций, и невозможность анализа ряда SNP, особенно групп полиморфных замен, расположенных на близком расстоянии друг от друга.
[Kamruecha W, Chansirikarnjana S, Nimkulrat E, Udommongkol C, Wongmek W, Thangnipon W. Rapid detection of apolipoprotein E genotypes in Alzheimer′s disease using polymerase chain reaction-single strand conformation polymorphism. Southeast Asian J Trop Med Public Health. 2006 Jul; 3 7(4): 793-7]
[Ezquerra M, Carnero C, Blesa R, Oliva R. A novel presenilin 1 mutation (Leu166Arg) associated with early-onset Alzheimer disease. Arch Neurol. 2000 Apr;57(4):485-8]
5. Гетеродуплексный анализ (НА).
При использовании данного метода денатурированные контрольный и анализируемый ПЦР-продукты не разделяют в геле, а сначала позволяют им ренатурировать. Одноцепочечные фрагменты образуют дуплексы. Если последовательности двух цепей полностью комплементарны, то будут образовываться гомодуплексы, если они отличаются хотя бы на один нуклеотид - гетеродуплексы. Гомо- и гетеродуплексы имеют разную электрофоретическую подвижность и могут быть разделены в неденатурирующем геле. В лабораторных исследованиях меченые Су5 красителем ПЦР-продукты с известным нуклеотидом в исследуемой позиции SNP смешивают с анализируемыми ПЦР-продуктами, после чего проводят детекцию. Преимуществом метода является простота визуализации результатов в обычном полиакриламидном геле. Недостатками метода являются низкая чувствительность (~80%), при этом для более эффективного разделения гомо- и гетеродуплексов требуется использование дорогостоящих вариантов гелей, а также невозможность определения точной локализации SNP внутри исследуемого фрагмента.
[Ezquerra M, Carnero С, Blesa R, Oliva R. A novel presenilin 1 mutation (Leu166Arg) associated with early-onset Alzheimer disease. Arch Neurol. 2000 Apr; 57(4):485-8]
[Ben-Avi L, Durst R, Shpitzen S, Leitersdorf E, Meiner V. Apolipoprotein E genotyping: accurate, simple, high throughput method using ABI Prism SNaPshot Multiplex System. J Alzheimers Dis. 2004 Oct; 6(5):497-501]
6. Масс-спектрометрия.
Метод заключается в том, что ионизированные молекулы ДНК (чаще всего специально подготовленные продукты ПЦР) отрываются от подложки методами MALDI (matrix-assisted laser desorption/ionisation) и ESI (electrospray ionisation). Они разгоняются в электрическом поле и направляются через вакуумную камеру к детектору. Время движения регистрируется. Время обратно пропорционально скорости молекулы, которая, в свою очередь, прямо пропорциональна отношению массы летящей молекулы к ее заряду. Поскольку отношение массы к заряду является уникальной величиной для каждой молекулы, основными преимуществами метода являются чувствительность и специфичность, а также минимально необходимое количество образца для проведения анализа. Недостатками метода являются трудоемкость, высокая стоимость оборудования, необходимость высококвалифицированных сотрудников и сложность использования вне крупных медицинских центров мегаполисов.
[Yu JT, Мао СХ, Zhang HW, Zhang Q, Wu ZC, Yu NN, Zhang N, Li Y, Tan L. Genetic association of rs11610206 SNP on chromosome 12q13 with late-onset Alzheimer's disease in a Han Chinese population. Clin Chim Acta. 2011 Jan 14; 412(1-2):148-51]
7. Анализ, основанный на лигазной реакции (LDR).
Метод основан на высокой чувствительности к субстрату лигаз из термофильных организмов: они не способны делать сшивку в случае, если фланкирующие нуклеотиды некомплементарны матрице. Как правило, 3′-концевые мисматчи лучше дискриминируются, чем 5′-концевые. В реакции лигазной детекции (LDR, Ligase detection Reaction) используются три олигонуклеотида, два из которых флуоресцентно меченые аллель-специфичные (различаются только меткой и 3′-нуклеотидом, соответствующим позиции SNP), а третий располагается с 5′-конца от SNP и непосредственно примыкает к аллель-специфичному праймеру. Полученные лигированные фрагменты детектируются с помощью электрофореза. Преимуществом метода является возможность одновременного проведения большого числа параллельных реакций и, следовательно, параллельной детекции большого количества возможных SNP. К недостаткам метода можно отнести трудоемкость ввиду необходимости синтеза индивидуальных проб для каждого анализируемого SNP.
[Kay DM, Stevens CF, Hamza TH, Montimurro JS, Zabetian CP, Factor SA, Samii A, Griffith A, Roberts JW, Molho ES, Higgins DS, Gancher S, Moses L, Zareparsi S, Poorkaj P, Bird T, Nutt J, Schellenberg GD, Payami H. A comprehensive analysis of deletions, multiplications, and copy number variations in PARK2. Neurology. 2010 Sep 28; 75(13):1189-94]
8. Гибридизация на олигонуклеотидных матрицах (биочипы или микроматрицы).
Микроматрица - это твердый носитель небольшого размера (например, стекло, нейлон или металлическая пластина) с прикрепленными к нему в определенном порядке короткими олигонуклеотидами (8-80 нуклеотидов) или фрагментами ДНК (размером более 100 нуклеотидов). Прикрепление одного из компонентов реакции к подложке позволяет проводить множество реакций одновременно посредством детекции пространственно разделенных отдельных однонуклеотидных замен (SNPs). Иммобилизованной может быть как контрольная ДНК с известной последовательностью, так и анализируемая ДНК с неизвестным нуклеотидом в вариабельной позиции. Микроматрицы могут применяться как для мутационного скрининга, так и для детекции известных аллелей. Иммобилизованная ДНК может непосредственно гибридизоваться с неизвестной последовательностью, и тогда эффективность гибридизации служит сигналом наличия/отсутствия мутации либо присутствующая в растворе ДНК может являться матрицей для синтеза ДНК с иммобилизованного праймера для определения прилежащего к нему нуклеотида. Преимуществами метода являются простота, низкая стоимость и возможность использования флуоресцентной метки, что позволяет легко автоматизировать процесс. К недостаткам метода можно отнести невозможность анализа тандемных повторов, а также высокую стоимость оборудования в некоторых модификациях метода.
[Ducray F, Honnorat J, Lachuer J. DNA microarray technology: principles and applications to the study of neurological disorder. Rev Neurol (Paris). 2007 Apr; 163(4):409-20}
[Lemos RR, Castelletti CH, Lima Filho JL, Marques ET Oliveira JR In silico identification of new genetic variations as potential risk factors for Alzheimer's disease in a microarray-oriented simulation. J Mol Neurosci. 2009 Sep; 39(l-2):242-7}
9. Минисеквенирование на олигонуклеотидном микрочипе.
Гибридизующийся зонд используют в качестве матрицы для синтеза ДНК с иммобилизованного олигонуклеотида. Вместо dNTP можно добавлять в реакцию меченые ddNTP одновременно для терминации реакции синтеза и мечения получающегося продукта. Таким образом, можно получить информацию о следующем за праймером нуклеотиде, соответствующем позиции SNP. В отличие от чипов, используемых для гибридизационного анализа (the Affymetrix «Gene Chip»; «Affymetrix», США, в этом случае олигонуклеотиды иммобилизуются на поверхности за 5′-конец, оставляя 3′-конец свободным для элонгации. Существует множество вариаций этой методики и сама реакция может заключаться как в непосредственной элонгации праймера (если праймер располагается вплотную к SNP), так и в элонгации, определяемой праймером (если 3′-концевой нуклеотид праймера соответствует одному из аллельных состояний гена и эффективность элонгации праймера зависит от того, комплементарен этот нуклеотид матрице или нет). Метод позволяет с высокой точностью определять генотипы и проводить одновременный анализ более 20 SNPs, однако является достаточно дорогостоящим и не подходит для анализа повторов и некартированных делеций и дупликаций.
[Ben-Avi L, Durst R, Shpitzen S, Leitersdorf E, Meiner V. Apolipoprotein E genotyping: accurate, simple, high throughput method using ABI Prism SNaPshot Multiplex System. J Alzheimers Dis. 2004 Oct; 6(5):497-501]
[Podder M, Welch WJ, Zamar RH, Tebbutt SJ. Dynamic variable selection in SNP genotype autocalling from APEX microarray data. BMC Bioinformatics. 2006 Nov 30; 7:521]
Таким образом, в настоящее время существует множество подходов для определения аллелей генов-кандидатов, ассоциированных с нейродегенеративными заболеваниями, в том числе с развитием болезни Альцгеймера. Данные подходы различаются набором маркеров (генотипируемые полиморфные локусы) и методами их определения. Так, например, в патенте US 2010035266 представлен способ определения генетической предрасположенности к болезни Альцгеймера путем определения однонуклеотидных замен в генах, продукты которых участвуют в биосинтезе стероидов. Анализ проводится с использованием метода раздельной амплификации исследуемых полиморфных локусов с помощью специфичных праймеров с дальнейшим секвенированием наработанных фрагментов на автоматическом секвенаторе «ABI 3730 XL DNA analyzer» (п. 2, метод секвенирования амплифицированных фрагментов ДНК).
Следует отметить, что в полигенных заболеваниях, таких как спорадическая форма болезни Альцгеймера, зачастую наблюдается этническая гетерогенность генетических маркеров, ассоциированных с риском развития данных заболеваний. В данном патенте предлагается определять полиморфизм генов, показавших наиболее значимую ассоциацию с риском развития спорадической формы болезни Альцгеймера в российских популяциях.
В патенте СА 2718392 предлагается определение полиморфизма 17 различных генов, ассоциированных с развитием болезни Альцгеймера, посредством ДНК-микрочипов фирмы «Affymetrix» (п. 8, метод гибридизации на олигонуклеотидных матрицах). Показано, что достоверность полученных результатов составляет около 90%. Кроме того, для многих из анализируемых генов, в частности для предшественника интегрина α2, циклина D3 и интерлейкина 3, ассоциация с заболеванием показана лишь на единичных популяциях и не подтверждена на других выборках. Кроме того, использование таких ДНК-микрочипов требует дорогостоящего оборудования и высокой квалификации персонала. Все это делает невозможным применение подобной тест-системы в клинических условиях.
Ближайшим аналогом настоящего изобретения является метод, описанный в п. 8. Поскольку все имеющиеся в настоящее время методы определения полиморфизма в генах-кандидатах развития нейродегенеративных заболеваний обладают теми или иными недостатками, существует реальная потребность в создании простого, недорогого и специфичного метода для выявления функционально значимых полиморфных локусов, ассоциированных с развитием болезни Альцгеймера, с целью дальнейшего внедрения в любую стандартную клиническую лабораторию.
Такой способ обеспечивается настоящим изобретением.
Раскрытие изобретения
Сущность изобретения заключается в обеспечении способа определения генетического полиморфизма, ассоциированного с риском развития спорадической формы болезни Альцгеймера в российских популяциях. Способ основан на проведении анализа полиморфизма генов, наиболее значимо ассоциированных с риском развития спорадической формы болезни Альцгеймера в российских популяциях - АроЕ, ApoJ и GAB2 (Низамутдинов, 2013).
Потенциальные механизмы влияния полиморфизма генов АроЕ (rs429358, rs7412), ApoJ (rs11136000) и GAB2 (rs2373115) на возникновение нейродегенеративных заболеваний, в том числе на развитие болезни Альцгеймера, представлены в Табл. 1.
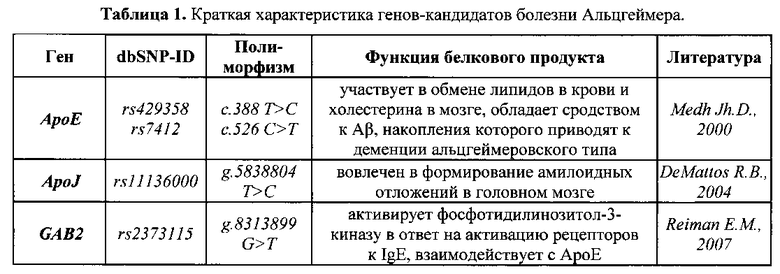
Литература
1. Низамутдинов И.И., Андреева Т.В., Степанов В.А., Марусин А.В., Рогаев Е.И., Заседателев А.С, Наседкина Т.В. Биочип для выявления генетических маркеров риска развития спорадической формы болезни Альцгеймера у славянского населения России. Молекулярная биология. 2013 47(6).949-958.
2. DeMattos RB. Apolipoprotein Е dose-dependent modulation of beta-amyloid deposition in a transgenic mouse model of Alzheimer's disease. J Mol Neurosci. 2004;23(3):255-62.
3. Medh JD, Fry GL, Bowen SL, Ruben S, Wong H, Chappell DA. Lipoprotein lipase- and hepatic triglyceride lipase- promoted very low density lipoprotein degradation proceeds via an apolipoprotein E-dependent mechanism. J Lipid Res. 2000 Nov; 41(11):1858-71.
4. Reiman EM, Webster J A, Myers AJ, Hardy J, Dunckley T, Zismann VL, Joshipura KD, Pearson JV, Hu-Lince D, Huentelman MJ, Craig DW, Coon KD, Liang WS, Herbert RH, Beach T, Rohrer КС, Zhao AS, Leung D, Bryden L, Marlowe L, Kaleem M, Mastroeni D, Grover A, Heward CB, Ravid R, Rogers J, Hutton ML, Melquist S, Petersen RC, Alexander GE, Caselli RJ, Kukull W, Papassotiropoulos A, Stephan DA. GAB2 alleles modify Alzheimer′s risk in APOE epsilon4 carriers. Neuron. 2007 Jun 7; 54(5):713-20.
Основным аспектом данного изобретения является набор иммобилизованных дифференцирующих олигонуклеотидов, последовательности которых приведены в Табл. 2 и Перечне последовательностей (SEQ ID NO: 1-8). Дифференцирующие олигонуклеотиды (SEQ ID NO: 1-8) могут быть иммобилизованы в ячейках гидогелевого микрочипа, как описано в патенте [Мирзабеков А.Д., Рубина А.Ю., Паньков С. В., Перов А.Н., Чупеева В.В. (2003). Композиция для иммобилизации биологических макромолекул в гидрогелях, способ приготовления композиции, биочип, способ проведения ПЦР на биочипе. Патент RU 2206575 С2], в концентрации 2000-4000 пкмоль на 1 мкл геля. Схема расположения ячеек, содержащих олигонуклеотидные зонды для анализа генетической предрасположенности к болезни Альцгеймера, приведена на Фиг. 1. Проведение анализа с использованием предлагаемого изобретения выполняется аналогично способу, описанному в патенте [Заседателев А.С., Наседкина Т.В., Глотов А.С.(2007) Способ анализа генетического полиморфизма, определяющего предрасположенность к онкологическим заболеваниям и индивидуальную чувствительность к фармацевтическим препаратам, с использованием олигонуклеотидного биологического микрочипа (биочипа). Патент RU 2303634].
Другим аспектом изобретения являются праймеры для амплификации полиморфных ДНК-локусов исследуемых генов, набор которых используется для получения изучаемых флуоресцентно меченых фрагментов ДНК в требуемом количестве. Последовательности праймеров приведены в Табл. 3 и Перечне последовательностей (SEQ ID NO: 9-20).
Набор праймеров используется на стадии предварительной амплификации полиморфных ДНК-локусов посредством проведения двухэтапной «гнездовой» ПЦР для подготовки ДНК-мишени к гибридизации на биочипе. На первом этапе проходит амплификация фрагмента геномной ДНК, на втором этапе с амплифицированного фрагмента нарабатывается одноцепочечная ДНК с одновременным введением флуоресцентной метки. Далее проводится гибридизация флуоресцентно меченых фрагментов ДНК, полученных после проведения второго этапа ПЦР, с иммобилизованными в ячейках геля олигонуклеотидами, расположенными на пластиковой подложке. После проведения гибридизации и отмывки биочипа проводится анализ полученной флуоресцентной картины, на основании которого делается вывод о генотипе в исследуемом образце. Пример гибридизационной картины приведен на Фиг. 2.
Осуществление изобретения
Задача настоящего изобретения состоит в создании способа экспресс-анализа, позволяющего проводить генотипирование по четырем полиморфным ДНК-локусам генов АроЕ (rs429358, rs7412), ApoJ (rs11136000) и GAB2 (rs2373115).
Дифференцирующие олигонуклеотиды для определения генетической предрасположенности к болезни Альцгеймера подбираются таким образом, чтобы идентифицировать все выбранные для анализа вариабельные позиции в генах АроЕ, ApoJ, и GAB2.
Олигонуклеотиды должны соответствовать следующим критериям:
1. Дискриминирующий зонд должен обладать высокой специфичностью к выбранному для анализа полиморфному локусу, который представляет собой участок гена, амплифицированный с помощью ПЦР, с включенной флуоресцентной меткой.
2. Вариабельный нуклеотид должен находиться в серединной области зонда, поскольку такое положение позволяет добиться большей дискриминации между совершенными и несовершенными дуплексами.
3. Выбранные олигонуклеотиды не должны содержать высокостабильных вторичных структур, наличие которых может приводить к снижению эффективности гибридизации.
Для идентификации каждого однонуклеотидного полиморфизма используются два специфичных дискриминирующих олигонуклеотида. При гибридизации с гомозиготной пробой один из них образовывает с пробой совершенный, а другой - несовершенный дуплекс. При одновременном анализе двух полиморфных сайтов в гене АроЕ количество специфических пар олигонуклеотидов соответствует количеству анализируемых сайтов, что позволяет определять наличие аллелей ε2 (сочетание rs429358 (Т), rs7412 (Т)), ε3 (сочетание rs429358 (Т), rs7412 (С)) и ε4 (сочетание rs429358 (С), rs7412 (С)).
Для определения генетической предрасположенности к болезни Альцгеймера используется 8 иммобилизованных высокоспецифичных дифференцирующих олигонуклеотидных зондов (Табл. 2 и Перечень последовательностей (SEQ ID NO: 1-8)), структура которых обеспечивает связывание только с полностью комплементарными ДНК-мишенями, что, в свою очередь, обуславливает яркий флуоресцентный сигнал и дает наиболее четкие картины распределения гибридизационных сигналов. Неспецифическое связывание сведено к минимуму, что практически исключает ложноположительное «срабатывание» ячеек.
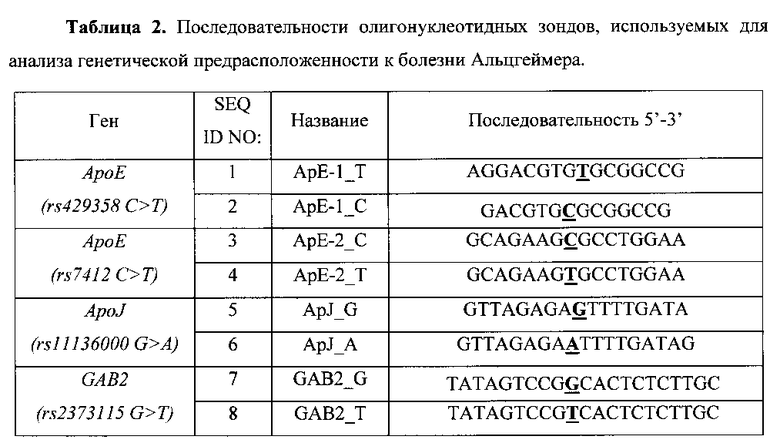
Для обеспечения оптимального состава и структуры ПЦР-праймеров, используемых в протоколе мультиплексной ПЦР, необходимы такие праймеры, которые не образуют между собой высокоэнергетических внутренних структур (шпильки и дуплексы), обеспечивают специфичную амплификацию необходимого количества продукта и при этом подобраны таким образом, чтобы их отжиг на мишени происходил при одинаковой для всех температуре (60-64°С). Для обеспечения сбалансированной эффективной амплификации исследуемых образцов также должны быть оптимизированы такие параметры, как концентрация MgCl2 и ПЦР-праймеров в ПЦР-смеси, соотношение прямых и обратных праймеров, количество циклов амплификации на обоих этапах, время элонгации, денатурации и отжига праймеров, температура отжига праймеров на каждом этапе. В результате проведенной работы подобраны праймеры 1 и 2 этапа, которые позволяют осуществлять эффективную наработку фрагментов геномной ДНК, содержащих выбранные функционально значимые полиморфные локусы генов-кандидатов развития спорадической формы болезни Альцгеймера АроЕ, ApoJ и GAB2.
Приведем последовательность анализа с использованием данного метода. Наработка ПЦР-продуктов для последующей гибридизации с олигонуклеотидными зондами, представленными в Табл. 2, проводится посредством «гнездовой» мультиплексной ПЦР в два этапа, при этом в качестве матрицы для проведения реакции используют образец ДНК. ПЦР может быть проведена с использованием любого вида термостабильной полимеразы (Taq-полимераза, Tth-полимераза, Tfl-полимераза, Pfu-полимераза, Vent-полимераза, DeepVent-полимераза и т.п. коммерчески доступные ферменты, выделенные из термофилов), работающей в соответствующем буфере. Для построения новой цепи в буфер добавляется смесь дНТФ (дАТФ, дГТФ, дЦТФ, дТТФ) в принятых концентрациях, при этом вместо дТТФ может быть использован дУТФ. Для проведения ПЦР могут быть использованы готовые коммерчески доступные наборы, содержащие все необходимые компоненты за исключением праймеров.
На первом этапе проходит амплификация полиморфных ДНК-локусов генов-кандидатов развития спорадической формы болезни Альцгеймера АроЕ, ApoJ и GAB2. Продукт первого этапа ПЦР используют в качестве матрицы на втором этапе, который проводят в реакционной смеси того же состава, но добавляют избыток одного из праймеров для обеспечения избытка флуоресцентно меченого одноцепочечного ПЦР-продукта. Это позволяет получать одноцепочечный ампликон, способный к гибридизации с аллель-специфичными ДНК-зондами на биочипе. Флуоресцентное мечение проводят на втором этапе ПЦР одновременно с амплификацией одноцепочечных фрагментов ДНК посредством введения флуоресцентной метки. В качестве флуоресцентной метки используется дезоксинуклеотидтрифосфат, а именно Су5-дУТФ, встраивающийся de novo в синтезируемую ДНК-цепь. В качестве флуоресцентной метки также может быть использован любой флуорохром без ограничения (например, FITC, Texas red, Су-3 и т.д.), а также биотин.
Праймеры и олигонуклеотидные зонды синтезируют с использованием различных химических подходов, таких как фосфодиэфирный метод, гидрофосфорильный метод и т.д., при этом наиболее распространенным в настоящее время является фосфоамидитный метод синтеза. Синтез праймеров осуществляют, используя автоматические ДНК/РНК синтезаторы, например производства фирмы «Applied Biosystems» (США).
Для иммобилизации могут быть использованы олигонуклеотиды, несущие по 5′- или 3′-концу активную группу. Модификация олигонуклеотида для введения активной группы может быть осуществлена как в автоматическом режиме при синтезе с использованием широкого спектра коммерчески доступных модификаторов, так и постсинтетически в ручном режиме. Например, при синтезе олигонуклеотидных зондов с помощью 3′-Amino-Modifier С7 CPG 500 («Glen Research)), США) на 3′-конец олигонуклеотидов вводится спейсер со свободной аминогруппой, используемый для последующей иммобилизации олигонуклеотида на подложке.
В качестве праймеров для проведения мультиплексной «гнездовой» двухэтапной ПЦР используют праймеры SEQ ID NO: 9-20, приведенные в Перечне последовательностей и в Табл. 3.
В мультиплексной реакции I этапа используют праймеры: 9, 10, 13, 14, 17, 18;
В мультиплексной реакции II этапа используют праймеры: 11, 12, 15, 16, 19, 20;
Далее проводится гибридизация флуоресцентно меченых фрагментов ДНК, полученных после проведения второго этапа ПЦР, с иммобилизованными в ячейках геля олигонуклеотидами, которые представляют собой полиморфные участки генов и являются комплементарными как последовательности «дикого типа» (предковый аллельный вариант), так и вариабельной последовательности (производный аллель).

Перед постановкой гибридизации ампликон денатурируют путем прогрева готовой гибридизационной смеси при 95°С в течение 5 мин с последующим быстрым охлаждением на льду. Гибридизация может быть проведена в любом известном специалисту в данной области гибридизационном буфере, например в гуанидиновом или SSPE-буфере. Типичное время гибридизации составляет 12-14 ч при 37°С. Анализ генотипов и аллелей в исследуемом образце проводится с учетом расположения олигонуклеотидных зондов на биочипе, схема которого позволяет определить, какие варианты присутствуют в том или ином образце.
Анализируемый фрагмент ДНК образует совершенные гибридизационные дуплексы только с соответствующими полностью комплементарными ему олигонуклеотидами. Если последовательность анализируемой ДНК полностью комплементарна последовательности зонда, то образуется стабильный совершенный дуплекс (детектируется сигнал флуоресценции). В случае если искомого фрагмента нет или в нем находится некомплементарное основание, то стабильного дуплекса не образуется (сигнал флуоресценции отсутствует). Дискриминацию совершенных и несовершенных дуплексов проводят после отмывки биочипа, сравнивая интенсивности сигналов флуоресценции, соответствующих различным олигонуклеотидным зондам. Отмывка может быть проведена в любом известном в данной области техники буфере с добавлением соли (SSC, SSPE и т.п.) или в деионизованной воде, но за более короткое время [Sambrook J.F. & D.W. Russell (2001) "Molecular cloning: a laboratory manual" Cold Spring Harbor Laboratory Press].
После проведения гибридизации и отмывки проводится визуализация результатов гибридизации с помощью возбуждения флуоресценции меченого ПЦР-продукта второго этапа ПЦР, на основании которой делается вывод о генотипе в исследуемом образце. Регистрация гибридизационной картины может быть произведена с помощью любой детектирующей системы, распознающей флуоресцентный сигнал (флуоресцентный микроскоп с ПЗС-камерой, лазерный сканер, портативный анализатор биочипов и т.п. коммерчески доступные флуоресцентные анализаторы, например портативный анализатор биочипов, снабженный ПЗС-камерой и специальным программным обеспечением, производства ООО «БИОЧИП-ИМБ» (Россия)).
Иммобилизация олигонуклеотидных зондов осуществляется посредством нанесения на поверхность подложки матрицы из ячеек акриламидного геля, активации ячеек и ковалентной иммобилизации в ячейках модифицированных олигонуклеотидов, несущих активные группы [Kolchinsky A, Mirzabekov A. Analysis of SNPs and other genomic variations using gel-based chips. Hum Mutat. 2002 Apr; 19(4):343-60. Review]. В качестве материала подложки может быть использовано стекло, металл, гибкие мембраны и пластик [Паньков С.В., Крейндлин Э.Я., Сомова О.Г., Моисеева О.В., Барский В.Е., Заседателев А.С.(2007) Применение немодифицированных полимерных материалов для изготовления подложки биочипов, биочип на их основе и способ его изготовления, способ иммобилизации гидрогелей на немодифицированных полимерных материалах. Патент RU 2309959]. Подложки также могут быть изготовлены любыми другими известными специалисту в данной области способами [Seliger Н, Hinz М, Нарр Е. Arrays of immobilized oligonucleotides-contributions to nucleic acids technology. Curr Pharm Biotechnol. 2003 Dec; 4(6):379-95].
Для иммобилизации в настоящем изобретении используется набор олигонуклеотидов SEQ ID NO: 1-8, приведенных в Перечне последовательностей, а также в Табл. 2. В качестве контроля прохождения гибридизации в настоящем изобретении используют образец контрольной ДНК. Расположение конкретных олигонуклеотидных зондов на биочипе может варьироваться и определяется только удобством интерпретации результатов гибридизации.
Далее приводятся примеры, которые показывают применение способа анализа однонуклеотидного полиморфизма для определения генетической предрасположенности к спорадической форме болезни Альцгеймера. Следует понимать, что приводимые примеры служат исключительно для иллюстрации и не предназначены для ограничения объема притязаний, выраженных в формуле изобретения. На основании настоящего описания специалист в данной области сможет легко предложить свои варианты и модификации осуществления изобретения, не отходя от общей концепции настоящего изобретения и без привлечения собственной изобретательской деятельности, так что должно быть понятно, что такие варианты и модификации также будут входить в объем притязаний настоящего изобретения.
Пример 1. Амплификация фрагментов генов АроЕ, ApoJ и GAB2 методом двухэтапной «гнездовой» мультиплексной ПЦР с целью получения флуоресцентно меченого полиморфного ДНК-локуса гена в необходимом количестве.
Из слюны испытуемых была выделена ДНК набором Oragene™ DNA Self-Collection Kit («DNA Genotek», Канада). Для мультиплексной наработки всех анализируемых генов использовали ПЦР-праймеры SEQ ID NO: 9, 10, 13, 14, 17 и 18. Первый этап ПЦР проводили на приборе MiniCycler («MJ Research, Inc.», США) в объеме 25 мкл реакционной смеси, составом: 1×ПЦР-буфер (67 мМ Трис-HCl, рН 8,6, 166 мМ (NH4)2SO4), 1,5 мМ MgCl2, 0,2 мМ каждого из dNTP («Силекс», Россия), по 5 рМ каждого праймера (SEQ ID NO: 9, 10, 13, 14, 17 и 18), 1 мкл геномной ДНК и 1,5 ед. акт.Taq-полимеразы («Силекс», Россия). ДНК денатурировали 5 мин при 94°С и проводили 40 циклов амплификации (94°С - 30 с, 65°С - 30 с, 72°С - 30 с), затем 10 мин при 72°С. Смесь второго этапа ПЦР отличалась составом и концентрацией праймеров: прямые праймеры (SEQ ID NO: 11, 15 и 19) брали в концентрации 5 пкмоль/мкл, обратные праймеры (SEQ ID NO: 12, 16 и 20) - 50 пкмоль/мкл. В смесь добавляли 2 мкл продукта из первого этапа и проводили амплификацию по схеме: 5 мин 94°С, 40 циклов (94°С - 30 с, 60°С - 30 с, 72°С - 30 с), 10 мин при 72°С. Также на втором этапе одновременно с проведением преимущественной амплификации одноцепочечного фрагмента ДНК проводили флуоресцентное мечение посредством добавления в ПЦР-смесь дезоксиуридинтрифосфата, меченого флуоресцентным красителем Су-5 (Су5-дУТФ), в количестве 0,2 нмоль на реакцию.
Пример 2. Иммобилизация дифференцирующих олигонуклеотидных зондов для определения генетического полиморфизма в генах-кандидатах предрасположенности к спорадической форме болезни Альцгеймера АроЕ, ApoJ и GAB2.
Олигонуклеотиды для иммобилизации синтезируют на автоматическом синтезаторе 394 DNA/RNA Synthesizer («Applied Biosystems», США) с использованием стандартной фосфоамидитной процедуры. 5′ или 3′-конец олигонуклеотидов содержит спейсер со свободной аминогруппой, который вводят в состав олигонуклеотида при синтезе путем использования 3′-Amino-Modifier С7 CPG 500 («Glen Research)), США). Присоединение флуоресцентной метки к олигонуклеотидам по свободной аминогруппе осуществляют в соответствии с рекомендациями производителя. Олигонуклеотиды, меченые цианиновым красителем Су-3, очищают методом ВЭЖХ от олигонуклеотидов, не включивших флуоресцентный краситель, на колонке «Hypersil ODS» 5 мкм, 4,6×250 мм» («Sypelco Int», США).
Проводят сополимеризацию олигонуклеотидов в акриламидном геле, как описано ранее [Паньков С.В., Крейндлин Э.Я., Сомова О.Т., Моисеева О.В., Барский В.Е., Заседателев А.С. (2007) Применение немодифицированных полимерных материалов для изготовления подложки биочипов, биочип на их основе и способ его изготовления, способ иммобилизации гидрогелей на немодифицированных полимерных материалах. Патент RU 2309959], [Мирзабеков А.Д., Рубина А.Ю., Паньков СВ., Чернов Б.К. (2001) Способ иммобилизации олигонуклеотидов, содержащих непредельные группы, в полимерных гидрогелях при формировании микрочипа. Патент RU 2175972]. После нанесения на подложку проводится контроль качества нанесения, который включает в себя визуальный контроль физических размеров гелевых ячеек при помощи светового микроскопа в отраженном свете и контроль концентрации иммобилизованных олигонуклеотидов с помощью красителя Су-3 (ООО «Биочип-ИМБ», Россия). Подложка содержит 8 иммобилизованных олигонуклеотидных зондов (SEQ ID NO: 1-8), список которых представлен также в Табл. 2. Ячейки наносят согласно схеме на Фиг. 1.
Пример 3. Гибридизация меченого продукта на биочипе
Реакционную смесь, полученную после проведения II этапа ПЦР, описанного в Примере 1, используют для гибридизации на подложке, описанной в Примере 2, в буфере следующего состава: 25% формамид («Sigma», США), 5х SSPE («Promega», США). Готовую гибридизационную смесь перед гибридизацией денатурируют при 95°С в течение 5 мин, охлаждают во льду 2 мин и наносят в гибридизационную камеру объемом 40 мкл (ООО «Биочип-ИМБ», Россия). Гибридизацию проводят в течение 12-14 ч при температуре 37°С. После завершения инкубации гибридизационную камеру удаляют вместе с непрореагировавшей гибридизационной смесью и проводят отмывку в 1x SSPE буфере («Promega», США) при комнатной температуре в течение 10 мин.
Пример 4. Регистрация и интерпретация результатов гибридизации
Регистрацию гибридизационной картины производят с помощью портативного анализатора, снабженного ПЗС-камерой, производимого ООО «БИОЧИП-ИМБ». Описание алгоритма автоматического анализа изображения с помощью программы ImageWare™ выходит за рамки настоящего изобретения.
Определим генотип по гибридизационной картине, представленной на Фиг. 2. Полиморфный участок гена АроЕ: положительный сигнал наблюдается в двух верхних ячейках первого столбца и двух нижних ячейках второго столбца, соответственно, генотип образца rs429358 (Т/Т), rs7412 (Т/Т), что соответствует аллелю ε2 в гомозиготном состоянии.
Аналогично определяем генотипы по остальным точкам: ApoJ (rs1136000 G/T) и GAB2 (rs2373115 G/G).
Последовательности олигонуклеотидных зондов, используемых для анализа генетической предрасположенности к болезни Альцгеймера.
(rs429358 C>T)
(rs7412 C>T)
(rs11136000 G>A)
(rs2373115 G>T)
Последовательности праймеров I и II этапа для проведения мультиплексных ПЦР с последующим анализом методом гибридизации на биочипе для определения генетической предрасположенности к спорадической форме болезни Альцгеймера.
ID NO:
10
ApE_R1
18
63,5
12
ApE_R2
GGGCCCCGGCCTG
13
58,1
14
ApJ_R1
25
63,1
16
ApJ_R2
20
60,2
18
GAB_R1
ATGCAGGGCAGTTATTATGTAGGCA
25
64,4
20
GAB_R2
AAAGCTAGAATTGATTATGAAGTAGTTTTA
30
58,5
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения полиморфных маркеров в генах SLCO1B1, APOE и ABCB1 для определения индивидуальной чувствительности к статинам | 2018 |
|
RU2695783C1 |
| БИОЛОГИЧЕСКИЙ МИКРОЧИП С НАБОРОМ ПРАЙМЕРОВ ДЛЯ АНАЛИЗА ПОЛИМОРФИЗМА В ГЕНАХ AB0, HLA-DQA1, AMEL, DARC, NAT2 | 2014 |
|
RU2582216C2 |
| Способ анализа полиморфных маркеров в генах VKORC1, CYP4F2, CYP2C9, CYP2C19, ABCB1, ITGB3 для определения индивидуальной чувствительности к противосвертывающим препаратам | 2018 |
|
RU2689400C1 |
| Способ анализа полиморфных маркеров в генах метаболизма лекарственных препаратов и генах иммунного ответа при терапии острых лейкозов у детей | 2016 |
|
RU2643333C1 |
| СПОСОБ АНАЛИЗА ГЕНЕТИЧЕСКОГО ПОЛИМОРФИЗМА, ОПРЕДЕЛЯЮЩЕГО ПРЕДРАСПОЛОЖЕННОСТЬ К ОНКОЛОГИЧЕСКИМ ЗАБОЛЕВАНИЯМ И ИНДИВИДУАЛЬНУЮ ЧУВСТВИТЕЛЬНОСТЬ К ФАРМАЦЕВТИЧЕСКИМ ПРЕПАРАТАМ С ИСПОЛЬЗОВАНИЕМ ОЛИГОНУКЛЕОТИДНОГО БИОЛОГИЧЕСКОГО МИКРОЧИПА (БИОЧИПА) | 2005 |
|
RU2303634C2 |
| Способ определения полиморфных маркеров в генах CYP2C19 и CYP2D6 для определения индивидуальной чувствительности к антидепрессантам | 2018 |
|
RU2716589C1 |
| СПОСОБ АНАЛИЗА ГЕНЕТИЧЕСКОГО ПОЛИМОРФИЗМА ДЛЯ ОПРЕДЕЛЕНИЯ ПРЕДРАСПОЛОЖЕННОСТИ К ШИЗОФРЕНИИ И АЛКОГОЛИЗМУ | 2012 |
|
RU2565036C2 |
| Способ идентификации генетических полиморфизмов, влияющих на метаболизм противоопухолевых препаратов, с использованием биологических микрочипов | 2018 |
|
RU2697096C1 |
| Способ анализа соматических мутаций в генах GNAQ и GNA11 с использованием LNA-блокирующей мультиплексной ПЦР и последующей гибридизацией с олигонуклеотидным биологическим микрочипом (биочипом) | 2017 |
|
RU2674687C1 |
| СПОСОБ ВЫЯВЛЕНИЯ ГЕНЕТИЧЕСКИХ ФАКТОРОВ РИСКА РАЗВИТИЯ ДЕМЕНЦИЙ АЛЬЦГЕЙМЕРОВСКОГО ТИПА НА ОСНОВЕ ГИДРОГЕЛЕВОГО МАТРИЧНОГО БИОЧИПА | 2022 |
|
RU2795795C1 |


Изобретения относятся к области генетики, молекулярной биологии и медицины и касаются способа для анализа генетического полиморфизма в локусах ДНК ApoE, ApoJ и GAB2 и набора олигонуклеотидных праймеров и зондов. Охарактеризованный способ включает стадии: (а) амплификация полиморфных фрагментов генов АроЕ, ApoJ и GAB2 с помощью мультиплексной «гнездной» двухэтапной ПЦР, в которой в качестве матрицы для амплификации используется образец ДНК; при проведении I этапа ПЦР используется набор праймеров с последовательностями, представленными в SEQ ID NO: 9, 10, 13, 14, 17, 18; при проведении II этапа ПЦР используется набор праймеров с последовательностями, представленными в SEQ ID NO: 11, 12, 15, 16, 19, 20, и дезоксиуридинтрифосфат, меченый флуоресцентным красителем Су-5, в результате чего образуется флуоресцентно меченый ПЦР-продукт; (б) иммобилизация олигонуклеотидных зондов, последовательности которых представлены в SEQ ID NO: 1-8, на твердой подложке; (в) гибридизация меченого ПЦР-продукта с иммобилизованными олигонуклеотидами, представленными в SEQ ID NO: 1-8; (г) регистрация и интерпретация результатов гибридизации. Изобретения обеспечивают возможность определения нуклеотидного состава в четырех полиморфных позициях: ApoE (rs429358, rs7412), ApoJ (rs11136000) и GAB2 (rs2373115), что, в свою очередь, позволяет определить предрасположенность к спорадической форме болезни Альцгеймера у представителей российских популяций. 2 н.п. ф-лы, 2 ил., 3 табл., 4 пр.
1. Способ для анализа генетического полиморфизма в локусах ДНК АроЕ (rs429358, rs7412), ApoJ (rs11136000) и GAB2 (rs2373115), предусматривающего следующие стадии:
а) амплификация полиморфных фрагментов генов АроЕ, ApoJ и GAB2 с помощью мультиплексной «гнездной» двухэтапной ПЦР, в которой в качестве матрицы для амплификации используется образец ДНК; при проведении I этапа ПЦР используется набор праймеров с последовательностями, представленными в SEQ ID NO: 9, 10, 13, 14, 17, 18; при проведении II этапа ПЦР используется набор праймеров с последовательностями, представленными в SEQ ID NO: 11, 12, 15, 16, 19, 20, и дезоксиуридинтрифосфат, меченый флуоресцентным красителем Су-5, в результате чего образуется флуоресцентно меченый ПЦР-продукт;
б) иммобилизация олигонуклеотидных зондов, последовательности которых представлены в SEQ ID NO: 1-8, на твердой подложке;
в) гибридизация меченого ПЦР-продукта с иммобилизованными олигонуклеотидами, представленными в SEQ ID NO: 1-8;
г) регистрация и интерпретация результатов гибридизации.
2. Набор олигонуклеотидных праймеров и зондов для анализа генетического полиморфизма в локусах ДНК АроЕ (rs429358, rs7412), ApoJ (rs11136000) и GAB2 (rs2373115), включающий (а) праймеры с последовательностями, представленными в SEQ ID NO: 9-20 для проведения двухэтапной «гнездовой» мультиплексной амплификации и получения флуоресцентно меченого ПЦР-продукта по п. 1, и (б) олигонуклеотидные зонды для идентификации полиморфных маркеров в указанных генах с последовательностями, представленными в SEQ ID NO: 1-8.
| NIZAMUTDINOV I.I | |||
| ET AL., Biochip for Determination of Genetic Markers of Sporadic Alzheimer’?s Disease Risk in the Russian Slavic Population, Molecular Biology, 2013, v | |||
| Способ очищения сернокислого глинозема от железа | 1920 |
|
SU47A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Литая рама для паровозов | 1923 |
|
SU827A1 |
| KAMEL A | |||
| ABD-ELSALAM, Bioinformatic tools and guideline for PCR primer design, African Journal of Biotechnology, 2003, v | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Огнетушитель | 0 |
|
SU91A1 |
| СПОСОБ АНАЛИЗА ГЕНЕТИЧЕСКОГО ПОЛИМОРФИЗМА, ОПРЕДЕЛЯЮЩЕГО ПРЕДРАСПОЛОЖЕННОСТЬ К ОНКОЛОГИЧЕСКИМ ЗАБОЛЕВАНИЯМ И ИНДИВИДУАЛЬНУЮ ЧУВСТВИТЕЛЬНОСТЬ К ФАРМАЦЕВТИЧЕСКИМ ПРЕПАРАТАМ С ИСПОЛЬЗОВАНИЕМ ОЛИГОНУКЛЕОТИДНОГО БИОЛОГИЧЕСКОГО МИКРОЧИПА (БИОЧИПА) | 2005 |
|
RU2303634C2 |
Авторы
Даты
2016-10-27—Публикация
2014-04-09—Подача