Изобретение относится к способам получения лекарственных препаратов в капсулах с контролируемым и последовательным высвобождением.
Изобретение предназначено для получения лекарственных препаратов пептидной природы с контролируемым и последовательным высвобождением биологически активного вещества в виде матричной структуры.
Фармакологически активная субстанция препаратов содержит клеточные экстракты, выделенные из гетерологичных (ксеногенных) и гомологичных (аллогенных) органов и тканей северных оленей и других животных, обладающих генетической и биологической чистотой вследствие их травоядности.
Изготавливается способом щадящего лизиса в результате действия кислотного пара под вакуумом из лиофилизированного сухого порошка органов и тканей эмбрионов (до 3-х месяцев), фетальных (от 3-х до 9 месяцев) и ювенильных (новорожденные до полового созревания), только от здоровых животных.
Клеточные экстракты представляют собой набор водорастворимых олиго-, полипептидных фракций вплоть до их мономерных субъединиц и обладают олиго-полипептид класс-эффектом.
Известны способы получения биологически разлагаемых капсул, способных высвобождать терапевтический препарат контролируемым образом.
Известен способ получения многокомпонентной модифицированной композиции с контролируемым высвобождением по патенту US 6228398, публикация 08.05.2001, МПК А61К 9/14. Композиция включает компонент немедленного высвобождения и компонент с модифицированным высвобождением. Компонент немедленного высвобождения, содержащий первую популяцию частиц, содержащих активный ингредиент, и компонент с модифицированным высвобождением, содержащий вторую популяцию частиц активного ингредиента, покрытых покрытием с контролируемым высвобождением; в котором комбинация компонентов быстрого высвобождения и модифицированного высвобождения в процессе работы доставляет активный ингредиент импульсным или бимодальным способом.
Известен способ получения многокомпонентной пульсирующей системы доставки лекарств по патенту US 5260068, публикация 09.11.1993, МПК А61К-009/22. Капсула или таблетка состоит из большого количества гранул и содержит терапевтический препарат и растворимый в воде осмотический агент, включающий водонерастворимый полимер. Пленочное покрытие каждой популяции гранул отличается от покрытия другой популяции гранул тем, что вода растворяет покрытие с разной скоростью. Осмотический агент растворяется в воде, заставляя гранулы разбухать и регулировать скорость диффузии лекарственного средства в окружающую среду. Поскольку каждая популяция гранул последовательно выдает свои лекарственные средства в окружающую среду, эффект заключается в обеспечении серии пульсирующих введений лекарственного средства из разовой лекарственной формы.
Наиболее близким решением является биоразлагаемая композиция микросфер, подходящая для контролируемого высвобождения пептида и способ ее получения по заявке KR20080094616, публикация 23.10.2008, МПК А61К 09/14.
Биологически разлагаемые микросферы способны высвобождать регулирующий глюкозу пептид контролируемым образом и содержат биодеградируемый полимерный носитель с инкапсулированным в него глюкоза-регулирующим пептидом. Микросферы обеспечивают высвобождение лекарственного средства нулевого порядка в течение длительного периода времени, таким образом улучшая терапевтический эффект лекарственного средства.
Для применения препаратов пептидной природы характерно что эффект кумуляции пептидов носит кратковременный характер и развивается сразу после применения в течение одного часа независимо от способа введения. В дальнейшем концентрация падает за счет трансформации пептидов и включения их в биохимические реакции.
Однако известно, например, и установлено, что периодически необходимо повторение курса лечения. Однако принятая дозировка от миллиграмм до грамм приводит к иммунологической сенсибилизации, аллергическим реакциям и снижению эффективности воздействия, особенно при проведении повторных курсов лечения.
Техническим результатом, достигаемым в заявляемом способе, является создание препаратов пептидной природы, обеспечивающих достижение максимального терапевтического эффекта в течение длительного времени при достижении иммунной толерантности по отношению к клеточным экстрактам, без потери терапевтической эффективности.
Способ получения лекарственного препарата пептидной природы с контролируемым и последовательным высвобождением характеризуется тем, что изготавливают ряд видов микросфер набора олиго-, полипептидов в смеси с агентом контролируемого высвобождения с различной концентрацией D6 -10-6 г/л, D4 -10-4 г/л, D2 -10-2 г/л. После чего покрывают микросферы пленочной оболочкой, обеспечивающей растворимость пленки с различной скоростью: D6 - 10-30 минут; D4 - 2-4 часов; D2 - 5-7 часов. И объединяют покрытые пленочной оболочкой микросферы в единую матричную структуру.
В одном частном случае выполнения ряд видов микросфер содержит один и тот же набор олиго-, полипептидов.
В другом частном случае выполнения ряд видов микросфер содержит разные наборы олиго-, полипептидов.
В частности, объединяют микросферы в единую матричную структуру в необходимой пропорции для получения препарата с необходимым терапевтическим эффектом.
Кроме того, в качестве агента контролируемого высвобождения используют производные целлюлозы с различным замещением.
Помимо этого, в качестве пленочной оболочки используют производные целлюлозы с различным замещением.
В частности, при покрытии микросфер пленочной оболочкой добавляют в покрытие цветовой пигмент в зависимости от концентрации олиго-, полипептидов.
В частности, единая матричная структура выполнена в виде капсулы.
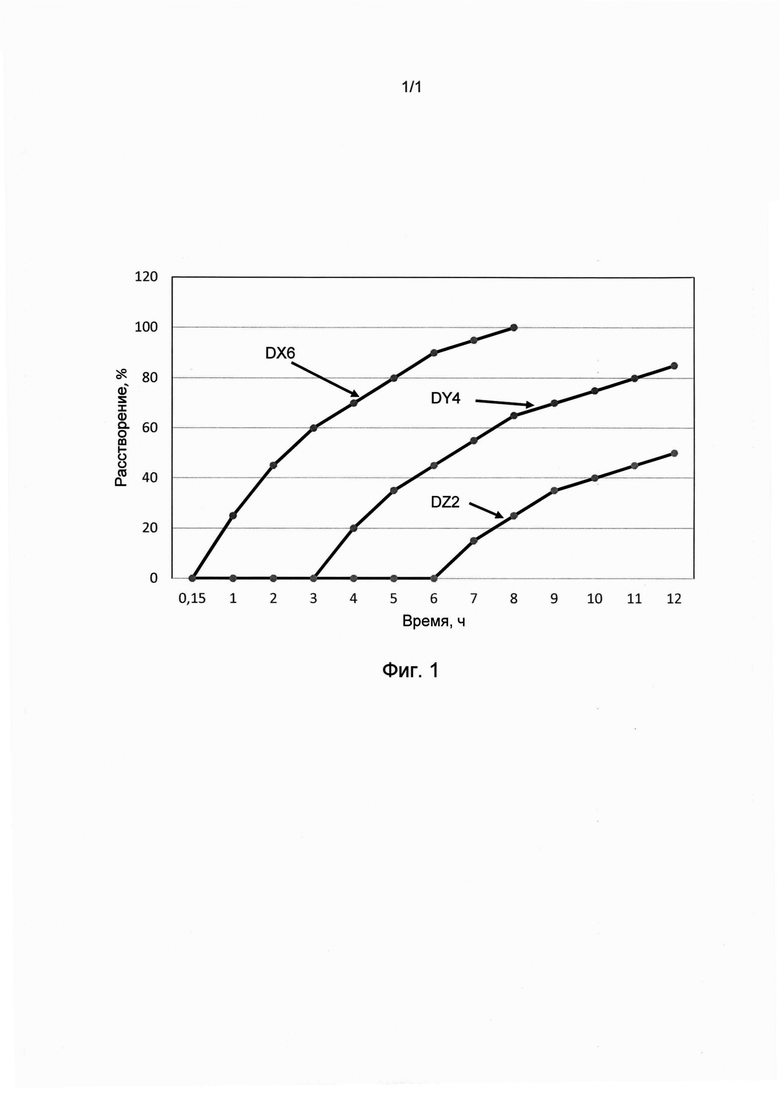
На рисунке, Фиг. 1 приведена диаграмма растворения компонентов многокомпонентного лекарственного препарата.
Способ выполняется следующим образом.
Первоначально изготавливают ряд видов микросфер олиго-, полипептидов в смеси с агентом контролируемого высвобождения с различной концентрацией D6 -10-6 г/л, D4-10-4 г/л, D2 - 10-2 г/л.
Получение микросфер разных концентраций биологически активного вещества состоит из стадий, объединенных в каскад: грануляция, экструзия-пеллетирование, вакуумная сушка влажных микросфер, покрытие кишечнорастворимой оболочкой.
В данной схеме при работе в периодическом режиме несколько высокоскоростных смесителей грануляторов, экструдеров-пеллетизереров, вакуумных сушек, объединяются в каскад. Каскадный принцип используется для получения монопрепаратов или многокомпонентых препаратов с разной концентрацией разведений биологически активной субстанции D6, D4, D2 на стадии смешения грануляции.
Обозначение D6, D4, D2 указывает на различную концентрацию препарата X, Y, Z (D6 - 10-6 г/л, D4 - 10-4 г/л, D2 - 10-2 г/л), так и на различную скорость высвобождения препарата X, Y Z (D6 -10-30 минут; D4 - 2-4 часов; D2 - 5-7 часов).
Данным способом могут быть получены монопрепараты DX6÷DX4÷DX2 или многокомпонентные препараты с разной концентрацией, например, DX6÷DY4÷DZ2, так и необходимой концентрацией DX4÷DY4÷DZ4 на каждой стадии высвобождения.
В качестве фармакологически активной субстанции клеточных экстрактов могут использоваться, в частности, биомолекулы клеток фетальных и ювенильных органов северного оленя и других животных, обладающих генетической и биологической чистотой вследствие их травоядности.
Например, X - клеточный экстракт эпифиза, Y - клеточный экстракт гипофиза, Z - клеточный экстракт гипоталамуса или X - клеточный экстракт яичников, Y - клеточный экстракт желтого тела, Z - клеточный экстракт молочной железы и др. в зависимости от фармакологической направленности.
Смешение и грануляция производится на высокоскоростном смесителе-грануляторе. Агент контролируемого высвобождения загружается в гранулятор-смеситель, с помощью перистальтического насоса через форсунку подается фармакологически активная субстанция клеточного экстракта. В качестве агента контролируемого высвобождения используются производные целлюлозы, в частности гидроксипропилметилцеллюлоза (гипромеллоза) высокой вязкости производные целлюлозы.
Контролируемое высвобождение регулируется вязкостью и типом замещения агента контролируемого высвобождения. В линии D6 концентрация экстракта равна 10-6 г/л по сухому веществу. Пример: в смеситель-гранулятор загружают 3500 г 60SH гипромеллозы, через форсунку подается 3500 мл клеточного экстракта с концентрацией олиго-, полипептидов 10-6 г/л. При такой загрузке получается 3500 г микросфер или 10000 капсул по 350 мг. Соответственно концентрация клеточного экстракта в первой линии D6 должна быть 0,01 г/л сухого вещества, во второй линии D4 -1 г/л и в третьей линии каскада D2 - 100 г/л, то есть на одну капсулу (350 мг) получается для D6 (0,01/10000=0,000001 г); для D4 (1/10000=0,0001 г) и для D2 (100/10000=0,01 г).
С помощью роторно-передаточного экструдера образуется экструдат, который на второй стадии обкатывается в пелетизере до сферической формы и удаляется из аппарата. Пластина пелетизера вращается, при этом плотно прилегает к стенкам аппарата. Таким образом, образуются микросферы сферической формы и достигается распределение частиц по размерам. Экструдат обкатывается до сферической формы под действием центробежных сил и сил трения. Оптимизация процесса достигается путем выбора времени цикла вращения, скорости вращения пластины, загрузки продукта и регулирования потока воздуха по периферии вращающейся пластины. Предварительно сформированные экструдаты подаются на вращающийся диск для пелетирования. За счет вращения диска, потока поступающего продукта и струи подающегося через щель в боковой стенке воздуха создается упорядоченное движение продукта по спиральной траектории у стенки емкости. Благодаря интенсивному перекатыванию поверхность частиц сглаживается, образуя микросферы. Образующиеся при этом частицы пыли снова захватываются полученными микросферами непосредственно в ходе технологического процесса.
Влажные микросферы подают на вакуумную сушку, где происходит доведение их до необходимой остаточной влажности.
Далее покрывают микросферы пленочной оболочкой, обеспечивающей растворимость пленки с различной скоростью: D6 - 10-30 минут; D4 - 2-4 часов; D2 - 5-7 часов. Покрытие производится на машине покрытия пленочной оболочкой с использованием кишечнорастворимого компонента и цветового пигмента для различных концентраций матричной структуры (D6 (красный), D4 (желтый), D2 (зеленый). Различная цветовая схема матрицы используется для идентификации концентраций и исключения перепутывания микросфер в процессе производства. В качестве покрытия может применятся покрытие на основе гипромеллозы фталат (гидроксипропилметилцеллюлозы фталат или другие производные целлюлозы. Цветовым пигментом могут служить пищевые красители: кармин, ликопин - D6 (красный); куркумин, рибофлавин - D4 (желтый); хлорофилла - D2 (зеленый) и другие разрешенные пищевые добавки.
Полученные микросферы объединяются в единую матричную структуру.
Капсулы и размер капсул единой матричной структуры выбираются в соответствии с государственными фармакопеями XI, вып. 2, с. 143 в зависимости от вместимости и изготавливаются стандартных восьми номеров (капсула №1 вмещает 350 мг микросфер размером 1 мм). Размер микросфер также может выбираться в зависимости от задач 0,5 мм, 1,0 мм, 1,5 мм.
Пример единой матричной структуры, когда используются микросферы одного и того же набора олиго-, полипептидов, клеточных экстрактов гипофиза, в пропорции D6 (1000 пг)÷D4 (100 мкг)÷D2 (10 мг).
Примером многокомпонентного препарата, микросферы объединяются в единую матричную структуру в пропорции DX6(1000 пг)÷DY4(100 мкг)÷DZ2(10 мг), где X - клеточный экстракт эпифиза, Y - клеточный экстракт гипофиза, Z -клеточный экстракт гипоталамуса или X - клеточный экстракт яичников, Y -клеточный экстракт желтого тела, Z - клеточный экстракт молочной железы и др. в зависимости от фармакологической направленности.
В частности, микросферы для многокомпонентного препарата могут смешиваться, в следующей пропорции: 33:33:33 штуки или по 116 мг в капсуле.
На диаграмме, Фиг. 1 показана динамика растворения приведенного примера многокомпонентного лекарственного препарата с тремя клеточными экстрактами, DX6÷DY4÷DZ2. Видно, что сначала, примерно после 15 минут после приема препарата начинает поступать в организм клеточный экстракт эпифиза концентрацией 1000 пг, примерно через три часа начинает поступать в организм клеточный экстракт гипофиза концентрацией 100 мкг и через примерно шесть часов начинает поступать в организм клеточный экстракт гипоталамуса с концентрацией 10 мг. Таким образом удается последовательно высвобождать три разные субстанции в разные временные промежутки времени.
Лекарственными препаратами пептидной природы в виде набора олиго-, полипептидов с контролируемым и последовательным высвобождением биологически активного вещества в виде матричной структуры реализуется возможность последовательно высвобождать, адресно и «точечно» воздействовать на гомологичные органы человека, а именно стимулировать фармакологические мишени.
Результат, который получается при использовании данного способа, характеризуется следующими преимуществами:
Достигается максимальный терапевтический эффект лекарственных препаратов пептидной природы в виде набора олиго-, полипептидов в течение длительного времени.
Достигается специфическая иммунная толерантность по отношению к клеточным экстрактам пептидной природы без потери терапевтической эффективности.
Получение микросфер с разной скоростью высвобождения активной субстанции, путем объединения их в одну матричную структуру (капсулу).
Возможность пролонгирования действия одной субстанции, либо последовательно высвобождать до трех разных субстанций в разные временные промежутки времени.
Возможность пролонгирования действия клеточных экстрактов пептидной природы за счет высвобождения второй и третьей фазы действующего вещества, либо последовательного стимулирования фармакологических мишеней разными субстанциями.
Способ обеспечивает получение лекарственных препаратов, позволяющих осуществлять процессы высвобождения и регулировать фармакинетику клеточных экстрактов в виде набора олиго-, полипептидов с селективным тропизмом к органам и тканям, проводить фармакологическую коррекцию различных заболеваний, в том числе в персонализированной медицине за счет контролируемого и последовательного высвобождения монопрепаратов различных концентраций, многокомпонентных препаратов для последовательного воздействия на разные фармакологические мишени.
Способ может быть промышленно реализован с использованием существующего оборудования.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПЕПТИДНОГО ГИДРОЛИЗАТА КОЛЛАГЕНА ИЗ РОГОВ | 2020 |
|
RU2752943C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИЗКОЭТЕРИФИЦИРОВАННОГО ПЕКТИНА | 2020 |
|
RU2737540C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ СЕРДЕЧНО-СОСУДИСТЫХ ЗАБОЛЕВАНИЙ | 2011 |
|
RU2491070C2 |
| Пероральная система доставки вещества белковой природы (варианты), защитная оболочка системы доставки (варианты) | 2014 |
|
RU2665367C2 |
| ВЕКТОРЫ И УСИЛИТЕЛИ ТРАНСЦИТОЗА ДЛЯ ДОСТАВКИ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ | 1996 |
|
RU2169010C2 |
| СРЕДСТВО МЕСТНОГО ДЕЙСТВИЯ, ОКАЗЫВАЮЩЕЕ СТИМУЛИРУЮЩЕЕ ВЛИЯНИЕ НА ПРОЦЕССЫ ВОССТАНОВЛЕНИЯ КЛЕТОК | 2002 |
|
RU2229872C1 |
| ЛЕКАРСТВЕННАЯ ФОРМА С МОДИФИЦИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ 6-МЕТИЛ-2-ЭТИЛ-3-ГИДРОКСИПИРИДИНА СУКЦИНАТА | 2008 |
|
RU2411035C2 |
| МАТРИЧНАЯ ТАБЛЕТКА С ОСНОВОЙ ДЛЯ ПРОЛОНГИРОВАННОГО ВЫСВОБОЖДЕНИЯ ТРИМЕТАЗИДИНА И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2010 |
|
RU2445958C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С ПРОЛОНГИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ С АНТИПСИХОТИЧЕСКОЙ АКТИВНОСТЬЮ И СПОСОБЫ ЕЁ ПОЛУЧЕНИЯ | 2012 |
|
RU2584653C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ТРАНСДЕРМАЛЬНОГО ПРИМЕНЕНИЯ ДЛЯ УВЕЛИЧЕНИЯ АКТИВНОСТИ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ И СНИЖЕНИЯ ИХ ПОБОЧНЫХ ЭФФЕКТОВ | 2010 |
|
RU2469706C2 |
Изобретение относится к способам получения лекарственных препаратов в капсулах с контролируемым и последовательным высвобождением. Способ получения лекарственного препарата пептидной природы с контролируемым и последовательным высвобождением включает изготовление ряда видов микросфер клеточных экстрактов в виде набора олиго-, полипептидов в смеси с агентом контролируемого высвобождения с различной концентрацией D6 - 10-6 г/л, D4 - 10-4 г/л, D2 - 10-2 г/л, покрытие микросферы пленочной оболочкой, обеспечивающей растворимость пленки с различной скоростью: D6 - 10-30 минут; D4 - 2-4 часов; D2 - 5-7 часов, и объединение покрытых пленочной оболочкой микросфер в единую матричную структуру. 7 з.п. ф-лы, 1 ил.
1. Способ получения лекарственного препарата пептидной природы с контролируемым и последовательным высвобождением, характеризующийся тем, что изготавливают ряд видов микросфер набора олиго-, полипептидов в смеси с агентом контролируемого высвобождения с различной концентрацией D6 - 10-6 г/л, D4 - 10-4 г/л, D2 - 10-2 г/л, после чего покрывают микросферы пленочной оболочкой, обеспечивающей растворимость пленки с различной скоростью: D6 - 10-30 минут; D4 - 2-4 часов; D2 - 5-7 часов, и объединяют покрытые пленочной оболочкой микросферы в единую матричную структуру.
2. Способ по п. 1, характеризующийся тем, что ряд видов микросфер содержит один и тот же набор олиго-, полипептидов.
3. Способ по п. 1, характеризующийся тем, что ряд видов микросфер содержит разные наборы олиго-, полипептидов.
4. Способ по п. 1, характеризующийся тем, что объединяют микросферы в единую матричную структуру в необходимой пропорции для получения препарата с необходимым терапевтическим эффектом.
5. Способ по п. 1, характеризующийся тем, что в качестве агента контролируемого высвобождения используют производные целлюлозы с различным замещением.
6. Способ по п. 1, характеризующийся тем, что в качестве пленочной оболочки используют производные целлюлозы с различным замещением.
7. Способ по п. 1, характеризующийся тем, что при покрытии микросфер пленочной оболочкой добавляют в покрытие цветовой пигмент в зависимости от концентрации олиго-, полипептидов.
8. Способ по п. 1, характеризующийся тем, что единая матричная структура выполнена в виде капсулы.
| KR 20080094616 A, 23.10.2008 | |||
| М.В | |||
| ГРИГОРЬЕВА | |||
| ПОЛИМЕРНЫЕ СИСТЕМЫ С КОНТРОЛИРУЕМЫМ ВЫСВОБОЖДЕНИЕМ БИОЛОГИЧЕСКИ АКТИВНЫХ СОЕДИНЕНИЙ / БИОТЕХНОЛОГИЯ, 2011, т | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| WO 2013109635 A1, 25.07.2013 | |||
| Е.В.Иванникова и др | |||
| Исследование фармакокинетики и биодоступности в создании новых оригинальных лекарственных средств пептидной структуры и их оптимальных лекарственных форм / Фармакокинетика и фармакодинамика, 2013, N2, стр | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2019-08-06—Публикация
2018-08-13—Подача