Настоящее изобретение относится к новому применению соединений, разрушающих IL-1β-лиганд/IL-1-рецептор (называемых в настоящем изобретении «соединениями IL-1бета»); такие низкомолекулярные соединения, разрушающие взаимодействие IL-1β-лиганд - IL-1-рецептор, антитела против IL-1β или антитела против рецептора IL-1, например, IL-1β-связывающие молекулы, описанные в настоящем изобретении, например, антитела, описанные в настоящем изобретении, например, IL-1β-связывающие соединения или IL-1-рецептор-связывающие соединения, и/или соединения РНК, снижающие уровни белков, либо IL-1β-лигандов, либо IL-1-рецептора, при лечении и/или предупреждении синдромов аутоиммунного воспаления, например, ювенильного ревматоидного артрита или ревматоидного артрита взрослых, и к способам лечения и/или предупреждения синдромов аутоиммунного воспаления, например, ювенильного ревматоидного артрита или ревматоидного артрита взрослых, у млекопитающих, особенно людей.
Интерлейкин-1β (также обозначается «IL-1бета», или «IL-1β», или «Интерлейкин-1β») является мощным иммуномодулятором, который опосредует широкий круг иммунных и воспалительных ответов. Непомерная или несоответствующая выработка IL-1β связана с патологией различных заболеваний и расстройств, например, с сепсисом, септическим или эндотоксическим шоком, аллергией, астмой, остеопорозом, ишемией, ударом, травматическим повреждением мозга, ревматоидным артритом и другими воспалительными расстройствами. Антитела к IL-1β были предусмотрены для применения в лечении IL-1-опосредованных заболеваний и расстройств; см., например, WO 95/01997 и обсуждение во введении, и WO 02/16436, содержание которых включено в настоящее изобретение в виде ссылок. При работе над настоящим изобретением неожиданно было обнаружено, что соединения IL-1бета применимы для предупреждения и лечения синдромов аутоиммунного воспаления у пациентов, например млекопитающих, особенно людей. Синдромы аутоиммунного воспаления по настоящему изобретению, например, является синдромы из группы наследственных расстройств, отличающихся случаями рецидивирующего воспаления, которые в отличие от аутоиммунных заболеваний утратили высокие титры антител или специфичных по антигену Т-клеток. Кроме того, синдромы аутоиммунного воспаления по настоящему изобретению показывают повышенную секрецию IL-1бета (утрата отрицательной регуляторной роли пирина, который предположительно изменяется при указанных заболеваниях), активацию ядерного фактора NFkB и повышенный апоптоз лейкоцитов. Синдромами аутоиммунного воспаления по настоящему изобретению являются синдромы Макл-Уэлса (Muckle-Wells syndromes - MWS), латентный аутоиммунный диабет взрослых (LADA - Latent Autoimmune Diabetes in Adults), семейный холодовый аутовоспалительный синдром/семейная холодовая крапивница (familial cold autoinflammmatory syndrome - FCAS), криопиринассоциированный воспалительный синдром (Cryopyrin-associated periodic syndromes - CAPS), мультисистемная воспалительная болезнь с неонатальным началом (neonatal-onset mutlisystem inflammatory syndrome - NOMID), хронический инфантильный неврологический, кожный, суставной синдром (chronic infantile neurological, cutaneous, articular - CINCA), семейная средиземноморская лихорадка (familial mediterranean fever -FMF) и/или определенные формы ювенильного артрита, например, ювенильный идиопатический артрит с системным началом (systemic onset juvenile idiopathic arthritis - SJIA), определенные формы ювенильного ревматоидного артрита, например, ювенильный идиопатический артрит с системным началом, и/или определенные формы ревматоидного артрита взрослых. Соединения IL-1бета также могут применяться при лечении диабета второго типа, при котором клинические и доклинические исследования показывают улучшенное функционирование островков за счет блокирования IL-1. Соединения IL-1бета также полезны для лечения различных патологий, связанных с диабетом, например, ретинопатии, заживления ран, сосудистых заболеваний (включая артериальный рестеноз после установки стента или ангиопластики), дисфункции почек, хронической болезни почек, метаболического синдрома и ожирения. Соединения IL-1бета также могут применяться для лечения мигрени, синовита, подагры, псевдоподагры / подагрического артрита или хондрокальциноза, хронической обструктивной болезни легких (chronic obstructive pulmonary disease - COPD), поражения легких, вызванного искусственной вентиляцией, различных болевых состояний, например, устойчивой к морфину боли, нейропатической боли, боли, связанной с преждевременными родами, боли, связанной со смещением межпозвоночных дисков, боли, связанной с воспалением, головной боли или мигрени. IL-1бета вовлечен в восприятие боли и увеличение нейрогенальных признаков. Кроме того, соединения IL-1бета по настоящему изобретению применяют в лечении атеросклероза, острой почечной колики, печеночной колики и боли, связанной с этими расстройствами.
Соединения IL-1бета могут применяться для лечения возвратной лихорадки: семейной средиземноморской лихорадки (familial Mediterranean fever - FMF), периодического синдрома, ассоциированного с рецептором фактора некроза опухоли (Tumor Necrosis Factor Receptor Associated Periodic Syndrome - TRAPS), rHnep-IgD-синдрома (hyperimmunoglobulin D syndrome - HIDS), также называемого гипериммуноглобулинемией D с приступами лихорадки или синдромом периодической лихорадки, ассоциированной с мевалонаткиназой, семейного холодового аутовоспалительного синдрома и синдрома периодической лихорадки, афтозного стоматита, фарингита, аденита (periodic fever, aphthous-stomatitis, pharyngitis, adenitis - PFAPA), при которых доминирующим цитокином является IL-1бета. К другим заболеваниям, при которых IL-1бета является доминантным цитокином, и которые можно лечить соединениями IL-1бета по настоящему изобретению, относятся антисинтетазный синдром, синдром активации макрофагов (Macrophage activation syndrome -MAS), Болезнь Бехчета, синдром Блау, синдром PAPA, синдром Шнитцлера, синдром Свита. Блокирование IL-1бета лиганда - рецептора и соединения IL-1бета по настоящему изобретению могут также применяться для лечения васкулита; гигантоклеточного артериита giant-cell arteritis - GCA), пурпуры Геноха-Шенлейна, первичного системного васкулита, болезни Кавасаки (синдрома кожнослизистых лимфоузлов), артериита Такаясу, нодозного полиартрита, выраженного криоглобулинемического васкулита, микроскопического полиартрита (microscopic polyangiitis - МРА) и синдрома Чержда-Стросса (Churg-Strauss syndrome - CSS), уртикарного васкулита. Кроме того, соединения IL-1бета по настоящему изобретению могут применяться для лечения аутоиммунных заболеваний типа саркоидоза, пемфигуса, анкилозирующего спондилоартрита, болезни Альцгеймера, амилоидоза, вторичного амилоидоза и синдрома Стилла у взрослых (adult onset Still disease -AOSD).
Соединения IL-1бета по настоящему изобретению могут применяться для лечения заболеваний, связанных с HLA-B27, к которым относятся, но которыми не перечень не ограничивается, псориаз, анкилозирующий спондилит, болезнь Рейтера и энтеропатический артрит.Соединения IL-1бета по настоящему изобретению могут применяться для лечения ревматической атаки, полимиалгии ревматической и гигантоклеточного артериита. Кроме того, соединения IL-1бета по настоящему изобретению могут быть применены для лечения инфекций, в частности бактериальных инфекций и вирусных инфекций, более предпочтительно бактериальных инфекций, связанных с симптомами артрита, к которым, например, относятся, но ими перечень не ограничивается, кроветворный остеомиелит, инфекционный артрит, туберкулезный артрит.
Предпочтительно соединения IL-1бета применимы для предупреждения и лечения ювенильного ревматоидного артрита и ревматоидного артрита взрослых и/или синдрома Макл-Уэлса.
В соответствии с определенными находками, сделанными в настоящем изобретении, в нем предусмотрены следующие варианты осуществления:
Настоящее изобретение также относится к композициям и способам для предупреждения и лечения синдромов аутоиммунного воспаления у млекопитающих, включая людей. Соответственно, соединения IL-1бета также применимы для приготовления лекарственных средств для лечения синдромов аутоиммунного воспаления. Согласно одному из объектов настоящего изобретения такие лекарственные средства включают терапевтически эффективное количество соединений IL-1бетас фармацевтически приемлемым носителем.
В другом варианте осуществления настоящего изобретения предусмотрено применение антитела, которое специфически связывается с каким-либо из выше или ниже описанных полипептидов, например, 1b-IL-1β-лигандом или IL-1β-рецептором, предпочтительно IL-1β-лигандом, для предупреждения и/или лечения ювенильного ревматоидного артрита, или синдрома ревматоидного артрита взрослых, и/или других синдромов аутоиммунного воспаления, и/или синдрома Макл-Уэлса. Необязательно антитело является моноклональным, гуманизированным антителом, фрагментом антитела или одноцепочечным антителом. Один из объектов настоящего изобретения касается выделенного антитела, которое связывает IL-1β-лиганд. В другом объекте настоящего изобретения антитело ингибирует или нейтрализует действие IL-1β-лиганда (антитело-антагонист). В другом объекте настоящего изобретения антитело является моноклональным антителом, которое содержит остатки комплементарно детерминируемой области (CDR) или человека, или другого вида, и остатки каркасного участка человека (framework region - FR). На антитело может быть нанесена метка, и оно может быть иммобилизовано на твердой основе. В другом объекте настоящего изобретения антитело является фрагментом антитела, моноклональным антителом, одноцепочечным антителом или анти-идиотипическим антителом. В еще одном из вариантов осуществления настоящего изобретения предусмотрена композиция, включающая антитело против IL-1β-лиганда или IL-1β-рецептора, предпочтительно антитело против IL-1β-лиганда в смеси с фармацевтически приемлемым носителем. В другом варианте композиция включает терапевтически эффективное количество антитела. Предпочтительно композиция стерильна. Композиция может вводиться в форме жидкого фармацевтического состава, который может сохраняться для длительного стабильного хранения. В другом варианте антитело является моноклональным антителом, фрагментом антитела, гуманизированным антителом или одноцепочечным антителом.
В другом варианте осуществления настоящего изобретения предусмотрено применение соединений IL-1бета, например, антитела против IL-1бета, способных прерывать положительную петлю обратной связи IL-1бета in vivo, для предупреждения и/или лечения ювенильного ревматоидного артрита, или ревматоидного артрита взрослых, и/или других синдромов аутоиммунного воспаления, и/или синдрома Макл-Уэлса. Такая положительная обратная связь in vivo приводит к самоподдерживающейся выработке IL-1b у таких пациентов.
В другом варианте осуществления настоящего изобретения предусматривают применение соединений IL-1бета, например, антител против IL-1бета, при заболеваниях с мутацией в гене MEFV, расположенном на хромосоме 16р13 и кодирующем белок пирин (также называемый маренострином). Пирин экспрессируется в гранулоцитах, моноцитах и синовиальных фибробластах. Пирин участвует в процессинга IL-1бета.
В другом варианте осуществления настоящее изобретение относится к получаемому объекту, который включает: (а) композицию материала, содержащую антитело против IL-1бета-лиганда или антитело против IL-1бета-рецептора, предпочтительно антитело против IL-1бета-лиганда, (б) контейнер, включающий указанную композицию, и (в) этикетку, прикрепленную к указанному контейнеру, или вкладыш, упакованный в указанный контейнер, касающийся применения указанного антитела против IL-1бета-лиганда или антитела против IL-1бета-рецептора, предпочтительно антитела против IL-1бета-лиганда, для лечения ювенильного ревматоидного артрита, или ревматоидного артрита взрослых, и/или других синдромов аутоиммунного воспаления, и/или синдрома Макл-Уэлса. Композиция может включать терапевтически эффективное количество антитела против IL-1бета-лиганда или антитела против IL-1бета-рецептора, предпочтительно антитела против IL-1бета-лиганда.
В еще одном из вариантов осуществления настоящее изобретение предусматривает способ или применение, согласно указанному выше, включающее совместное введение терапевтически эффективного количества соединений IL-1бета в свободной форме или в форме соли, предпочтительно в фармацевтически приемлемой форме доставки, например, внутривенной или подкожной, и второго лекарственного вещества, которое является противовоспалительным соединением в свободной форме или в форме соли.
В другом варианте осуществления настоящего изобретения используют соединения IL-1бета по настоящему изобретению, которые представляют IL-1бета связывающую молекулу, включающую сайт связывания антигена, содержащий по меньшей мере один вариабельный домен тяжелой цепи (VH) иммуноглобулина, который включает последовательно гипервариабельные области CDR1, CDR2 и CDR3, причем указанная область CDR1 имеет аминокислотную последовательность Val-Tyr-Gly-Met-Asn, указанная область CDR2 имеет аминокислотную последовательность Ile-Ile-Trp-Tyr-Asp-Gly-Asp-Asn-Gln-Tyr-Tyr-Ala-Asp-Ser-Val-Lys-Gly, и указанная область CDR3 имеет аминокислотную последовательность Asp-Leu-Arg-Thr-Gly-Pro, и соответствующие эквиваленты.
В еще одном из вариантов осуществления настоящего изобретения используемое соединение IL-1бета по настоящему изобретению является IL-1бета связывающей молекулой, которая включает по меньшей мере один вариабельный домен (VL) легкой цепи иммуноглобулина, который включает последовательно гипервариабельные области CDR1', CDR2' и CDR3', причем указанная область CDR1' имеет аминокислотную последовательность Arg-Ala-Ser-Gln-Ser-Ile-Gly-Ser-Ser-Leu-His, указанная область CDR2' имеет аминокислотную последовательность Ala-Ser-Gln-Ser-Phe-Ser и указанная область CDR3' имеет аминокислотную последовательность His-Gln-Ser-Ser-Ser-Leu-Pro, и соответствующие эквиваленты.
В еще одном из вариантов осуществления настоящего изобретения соединение IL-1бета, используемое по настоящему изобретению, является однодоменной IL-1бета-связывающей молекулой, включающей выделенную тяжелую цепь иммуноглобулина, включающую вариабельный домен тяжелой цепи (VH) согласно описанному выше, например, для получения лекарственного средства для лечения ювенильного ревматоидного артрита, или синдрома ревматоидного артрита взрослых, и/или других синдромов аутоиммунного воспаления, предпочтительно ювенильного ревматоидного артрита, или ревматоидного артрита взрослых, и/или синдрома Макл-Уэлса.
В еще одном из вариантов осуществления настоящего изобретения соединение IL-1бета, используемое по настоящему изобретению, является Перевязывающей молекулой, включающей вариабельные домены и тяжелой (VH), и легкой цепи (VL), причем указанная IL-1β-связывающая молекула включает по меньшей мере один сайт связывания антигена, включающий:
а) вариабельный домен тяжелой цепи иммуноглобулина (VH), который включает последовательно гипервариабельные области CDR1, CDR2 и CDR3, причем указанная область CDR1 имеет аминокислотную последовательность Val-Tyr-Gly-Met-Asn, указанная область CDR2 имеет аминокислотную последовательность Ile-Ile-Trp-Tyr-Asp-Gly-Asp-Asn-Gln-Tyr-Tyr-Ala-Asp-Ser-Val-Lys-Gly, и указанная область CDR3 имеет аминокислотную последовательность Asp-Leu-Arg-Thr-Gly-Pro, и
б) вариабельный домен легкой цепи иммуноглобулина (VL), который включает последовательно гипервариабельные области CDR1', CDR2' и CDR3', причем указанная область CDR1' имеет аминокислотную последовательность Arg-Ala-Ser-Gln-Ser-Ile-Gly-Ser-Ser-Leu-His, указанная область CDR2' имеет аминокислотную последовательность Ala-Ser-Gln-Ser-Phe-Ser и указанная область CDR3' имеет аминокислотную последовательность His-Gln-Ser-Ser-Ser-Leu-Pro,
и соответствующие эквиваленты.
Если не указано иначе, какая-либо полипептидная цепь, описанная в настоящем изобретении в качестве имеющей аминокислотную последовательность, начинающуюся с N-конца и заканчивающуюся на С-конце. Если сайт связывания антигена включает оба домена, VH и VL, они могут быть расположены в той же молекуле полипептида или, предпочтительно, каждый из доменов может быть в разных цепях, домен VH является частью тяжелой цепи иммуноглобулина или его фрагмента, и VL является частью легкой цепи иммуноглобулина или его фрагмента.
Понятие «IL-1β-связывающая молекула» означает какую-либо молекулу, способную связываться или только с одним IL-1β-лигандом, или в его соединении с другими молекулами. Реакция связывания может быть продемонстрирована стандартными методами (качественные исследования), включая, например, биоисследование для определения подавления связывания IL-1β с его рецептором или какой-либо тип исследования связывания при сопоставлении с отрицательным контролем, в котором используют антитело со специфичностью иного рода, но того же типа, например, анти-CD25 антитело. Преимущественно связывание IL-1β-связывающих молекул по настоящему изобретению с IL-1β может быть показано в анализе конкурентного связывания.
Примерами антигенсвязывающих молекул являются антитела, вырабатываемые В-клетками или гибридомами, и химерные, с пересаженными областями CDR антителами или антителами человека, или каким-либо их фрагментами, например, F(ab')2 и Fab фрагментами, а также одноцепочечными или однодоменными антителами.
Одноцепочечное антитело состоит из вариабельных доменов тяжелых и легких цепей антитела, ковалентно связанных пептидным линкером, обычно состоящим из 10-30 аминокислот, предпочтительно 15-25 аминокислот. Таким образом, такая структура не содержит константной части тяжелых и легких цепей, и предполагают, что малый пептидный спейсер должен быть менее антигенным по сравнению с целой константной частью. Понятие «химерное антитело» означает антитело, в котором константные области тяжелых или легких цепей, или и тех и других, происходят от человека, но вариабельные домены и тяжелых и легких цепей не происходят от человека (например, происходят от грызуна), или они происходят от человека, но от разных антител человека. Понятие «антитело с пересаженной областью CDR» означает антитело, в котором гипервариабельные области (CDR) производны от антитела-донора, например, антитела, происходящего не от человека (например, антитела грызунов), или другого антитела человека, хотя все или почти все другие части иммуноглобулина, например, константные области и в высокой степени консервативные части вариабельных доменов, т.е. каркасные участки, производны от акцепторного антитела, например, антитела, происходящего от человека. Антитело с пересаженной областью CDR тем не менее может содержать несколько аминокислот последовательности-донора в каркасных участках, например, в частях каркасных участков, присоединенных к гипервариабельным областям. Понятие «антитело человека» означает антитело, в котором обе области, константная и вариабельная, и тяжелой, и легкой цепей, все происходят от человека, или практически идентичны последовательностям, происходящим от человека, не обязательно от того же антитела, и включает антитела, вырабатываемые мышами, в которых гены вариабельной и константной частей иммуноглобулина грызунов были замещены на их аналоги от человека, например, описанные в общепринятых терминах в ЕР 0546073 В1, USP 5545806, USP 5569825, USP 5625126, USP 5633425, USP 5661016, USP 5770429, ЕР 0 438474 В1 и ЕР 0 463151 В1.
Понятие «прямые эквиваленты» охватывает какие-либо молекулы, антитела или их функциональные фрагменты, имеющие свойства IL-1бета-связывающей молекулы по настоящему изобретению согласно описанию, в том числе антитела разных видов и изотипов, фрагменты Fab2, Fab и scFv, а также мутанты, включающие 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более точечных мутаций в областях CDR или за пределами областей CDR последовательностей SEQ ID No 1 и 2.
Особенно предпочтительными IL-1β-связывающими молекулами по настоящему изобретению являются антитела человека, особенно антитело ACZ 885, описанное ниже в примерах и в WO 02/16436.
Таким образом, в предпочтительных антителах по настоящему изобретению вариабельные домены и тяжелых, и легких цепей, происходят от человека, например, домены антитела ACZ 885, представленные в виде
последовательностей SEQ ID NO:1 и SEQ ID NO:2. Домены константной области предпочтительно также включают соответствующие домены константной области человека, например, описанные Kabat Е.А. и др. в кн.: «Sequences of Proteins of Immunological Interest)), Министерство здравоохранения и социального обеспечения США, Национальный институт здоровья.
Гипервариабельные области могут быть связаны с каркасными участками какого-либо типа, причем все-таки предпочтительно происходящими от человека. Соответствующие каркасные участки описаны в приведенной выше работе Kabat Е.А. и др. Предпочтительным каркасным участком тяжелой цепи является каркасный участок тяжелой цепи человека, например, в антителе ACZ 885, который представлен в виде последовательности SEQ ID NO:1. Он последовательно содержит каркасные участки FR1, FR2, FR3 и FR4. Сходным образом последовательность SEQ ID NO:2 представляет собой каркасный участок легкой цепи предпочтительного антитела ACZ 885, который последовательно содержит каркасные участки FR1', FR2', FR3' и FR4'.
Таким образом, настоящее изобретение также предусматривает IL-1β-связывающую молекулу, которая включает по меньшей мере один сайт связывания антигена, включающий либо первый домен, имеющий аминокислотную последовательность, в существенной степени идентичную последовательности, показанной в виде SEQ ID NO:1, начинающуюся с аминокислоты в положении 1 и заканчивающуюся аминокислотой в положении 118, или первый домен, описанный выше, и второй домен с аминокислотной последовательностью, в существенной степени идентичной последовательности, показанной в виде последовательности SEQ ID NO:2, начинающейся с аминокислоты в положении 1 и заканчивающейся аминокислотой в положении 107.
Моноклональные антитела, индуцированные против белка, который естественным образом имеется у всех людей, обычно формируются в системе, которой не является человек, например, в мышах, и поэтому обычно они не являются белками человека. В качестве прямого следствия ксеногенное антитело, вырабатываемое гибридомой, при введении людям вызывает нежелательный иммунный ответ, который преимущественно опосредуется константной частью ксеногенного иммуноглобулина. Это очевидно ограничивает применение таких антител, поскольку они не могут вводиться на протяжении пролонгированного периода времени. Следовательно, особенно предпочтительно использовать одноцепочечные, однодоменные, химерные, с пересаженными областями CDR антитела или особенно антитела человека, которые предположительно не вызывают сильный аллогенный ответ при введении людям.
С учетом вышесказанного более предпочтительно IL-1β-связывающая молекула по настоящему изобретению является выбранной из антител человека против IL-1β и включает по меньшей мере:
а) тяжелую цепь иммуноглобулина, или ее фрагмент, которая включает (i) вариабельный домен, включающий в последовательности гипервариабельные области CDR1, CDR2 и CDR3 и (ii) константную часть или ее фрагмент тяжелой цепи человека; указанная область CDR1 имеет аминокислотную последовательность Val-Tyr-Gly-Met-Asn, указанная область CDR2 имеет аминокислотную последовательность Ile-Ile-Trp-Tyr-Asp-Gly-Asp-Asn-Gln-Tyr-Tyr-Ala-Asp-Ser-Val-Lys-Gly, и указанная область CDR3 имеет аминокислотную последовательность Asp-Leu-Arg-Thr-Gly-Pro, и
б) легкую цепь иммуноглобулина, или ее фрагмент, которая включает (i) вариабельный домен, включающий в последовательности гипервариабельные области и необязательно также CDR1', CDR2', и CDR3' гипервариабельные области и (ii) константную часть, или ее фрагмент, легкой цепи человека; указанная область CDR1' имеет аминокислотную последовательность Arg-Ala-Ser-Gln-Ser-Ile-Gly-Ser-Ser-Leu-His, указанная область CDR2' имеет аминокислотную последовательность Ala-Ser-Gln-Ser-Phe-Ser, и указанная область CDR3' имеет аминокислотную последовательность His-Gln-Ser-Ser-Ser-Leu-Pro;
и соответствующие эквиваленты.
В другом варианте IL-1β-связывающая молекула по настоящему изобретению может быть выбрана из одноцепочечной связывающей молекулы, которая включает сайт связывания антигена, содержащий:
а) первый домен, включающий последовательно гипервариабельные области CDR1, CDR2 и CDR3, причем указанная область CDR1 имеет аминокислотную последовательность Val-Tyr-Gly-Met-Asn, указанная область CDR2 имеет аминокислотную последовательность Ile-Ile-Trp-Tyr-Asp-Gly-Asp-Asn-Gln-Tyr-Tyr-Ala-Asp-Ser-Val-Lys-Gly, и указанная область CDR3 имеет аминокислотную последовательность Asp-Leu-Arg-Thr-Gly-Pro,
б) второй домен, включающий гипервариабельные области CDR11, CDR2' и CDR3', причем указанная область CDR1' имеет аминокислотную последовательность Arg-Ala-Ser-Gln-Ser-Ile-Gly-Ser-Ser-Leu-His, указанная область CDR2' имеет аминокислотную последовательность Ala-Ser-Gln-Ser-Phe-Ser, и указанная область CDR3' имеет аминокислотную последовательность His-Gln-Ser-Ser-Ser-Leu-Pro, и
в) пептидный линкер, который связан с N-концевым краем первого домена и с С-концевым краем второго домена, или с С-концевым краем первого домена и с N-концевым краем второго домена;
и соответствующие эквиваленты.
Известно, что минимальные изменения аминокислотной последовательности, например, делеции, вставки или замещения одной, нескольких или даже некоторого большего количества аминокислот может привести к аллельной форме исходного белка, которая имеет в значительной степени идентичные свойства.
Таким образом, понятие «соответствующие эквиваленты» означает или какую-либо однодоменную IL-1β-связывающую молекулу (молекулу X):
(i) в которой гипервариабельные области CDR1, CDR2 и CDR3 в совокупности по меньшей мере на 80% гомологичны, предпочтительно по меньшей мере на 90% гомологичны, более предпочтительно по меньшей мере на 95% гомологичны гипервариабельным областям, указанным выше, и
(ii) которая способна ингибировать связывание IL-1β с его рецептором практически в той же степени, что и контрольная молекула, имеющая каркасные участки, идентичные каркасным участкам молекулы X, но имеющая гипервариабельные области CDR1, CDR2 и CDR3, идентичные гипервариабельным областям, указанным выше,
или какую-либо IL-1β-связывающую молекулу, имеющую по меньшей мере два домена на сайт связывания (молекулу X')
(i) в которой гипервариабельные области CDR1, CDR2, CDR3, CDR1', CDR2' и CDR3' в совокупности по меньшей мере на 80% гомологичны, предпочтительно по меньшей мере на 90% гомологичны, более предпочтительно по меньшей мере на 95, 98 или 99% гомологичны гипервариабельным областям, указанным выше, и
(ii) которая способна ингибировать связывание IL-1β с его рецептором практически в той же степени, что и контрольная молекула, имеющая каркасные участки и константные части, идентичные молекуле X', но имеющая гипервариабельные области CDR1, CDR2, CDR3, CDR1', CDR2' и CDR3', идентичные гипервариабельным областям, указанным выше.
В другом объекте настоящего изобретения также предусматривают IL-1бета-связывающую молекулу, включающую вариабельные домены и тяжелой (VH), и легкой (VL) цепи, причем указанная IL-1бета-связывающая молекула включает по меньшей мере один сайт связывания антигена, содержащий:
а) вариабельный домен тяжелой цепи иммуноглобулина (VH), который включает последовательно гипервариабельные области CDR1, CDR2 и CDR3, причем указанная область CDR1 имеет аминокислотную последовательность Ser-Tyr-Trp-Ile-Gly, указанная область CDR2 имеет аминокислотную последовательность Ile-Ile-Tyr-Pro-Ser-Asp-Ser-Asp-Thr-Arg-Tyr-Ser-Pro-Ser-Phe-Gln-Gly, и указанная область CDR3 имеет аминокислотную последовательность Tyr-Thr-Asn-Trp-Asp-Ala-Phe-Asp-Ile, и
б) вариабельный домен легкой цепи иммуноглобулина (VL), который включает гипервариабельную область CDR3', имеющую аминокислотную последовательность Gln-Gln-Arg-Ser-Asn-Trp-Met-Phe-Pro;
и соответствующие эквиваленты.
В другом объекте настоящего изобретения также предусматривается IL-1бета-связывающая молекула, включающая вариабельные домены и тяжелой (VH), и легкой цепи (VL), причем указанная IL-1бета-связывающая молекула включает по меньшей мере один сайт связывания антигена, содержащий:
а) вариабельный домен тяжелой цепи иммуноглобулина (VH), который последовательно включает гипервариабельные области CDR1, CDR2 и CDR3, указанная область CDR1 имеющую аминокислотную последовательность Ser-Tyr-Trp-Ile-Gly, указанная область CDR2 имеющую аминокислотную последовательность Ile-Ile-Tyr-Pro-Ser-Asp-Ser-Asp-Thr-Arg-Tyr-Ser-Pro-Ser-Phe-Gln-Gly, и указанная область CDR3 имеющую аминокислотную последовательность Tyr-Thr-Asn-Trp-Asp-Ala-Phe-Asp-Ile, и
б) вариабельный домен легкой цепи иммуноглобулина (VL), который последовательно включает гипервариабельные области CDR1', CDR2' и CDR3', указанная область CDR1' Arg-Ala-Ser-Gln-Ser-Val-Ser-Ser-Tyr-Leu Ala, указанная область CDR2' имеющую аминокислотную последовательность Asp-Ala-Ser-Asn-Arg-Ala-Thr, и указанная область CDR3' имеющую аминокислотную последовательность Gln-Gln-Arg-Ser-Asn-Trp-Met-Phe-Pro;
и соответствующие эквиваленты.
В настоящем изобретении аминокислотные последовательности по меньшей мере на 80% гомологичны друг другу, если они содержат по меньшей мере на 80% идентичные аминокислотные остатки в таком положении, в котором они совпадают оптимально, причем гэпы и инсерции в аминокислотных последовательностях учитывают в качестве неидентичных остатков.
Подавление связывания IL-1β с его рецептором может быть легко исследовано в различных анализах, включая анализы, описанные в WO 02/16436. Понятие «в той же степени» означает, что контрольная и эквивалентная молекулы статистически проявляют по существу идентичные кривые подавления связывания IL-1β в одном из исследований, указанных выше. Например, у IL-1P-связывающих молекул по настоящему изобретению обычно величины IC50 по подавлению связывания IL-1β с его рецептором находятся в пределах величины +/-x5 от соответствующего показателя, предпочтительно в существенной степени такие же, что и величины IC50 соответствующей контрольной молекулы при описанном выше исследовании.
Например, применяемое исследование может быть исследованием конкурентного подавления связывания IL-1β растворимыми рецепторами IL-1 и IL-1β-связывающими молекулами по настоящему изобретению.
Наиболее предпочтительно IL-1β-связывающая молекула для применения по настоящему изобретению является антителом человека IL-1, которое по меньшей мере включает:
а) одну тяжелую цепь, которая включает вариабельный домен, имеющий аминокислотную последовательность, в существенной степени идентичную последовательности, представленной в виде SEQ ID NO:1, начиная с аминокислоты в положении 1 и заканчивая аминокислотой по положению 118, и константную часть тяжелой цепи человека; и
б) одну легкую цепь, которая включает вариабельный домен, имеющий аминокислотную последовательность, в существенной степени идентичную последовательности, представленной в виде SEQ ID NO:2, начиная с аминокислоты в положении 1 и заканчивая аминокислотой по положению 107, и константную часть легкой цепи человека.
Наиболее предпочтительно IL-1β-связывающей молекулой для применения по настоящему изобретению является антитело ACZ885 (см. пример).
Константная часть тяжелой цепи человека может быть типа γ1, γ2, γ3, γ4, μ, α1, α2, δ или ε типа, предпочтительно γ типа, более предпочтительно типа γ1 , причем константная часть легкой цепи человека может быть типа κ или λ (которые включают подтипы λ1, λ2, 2 и λ3), но предпочтительно типа к. Аминокислотные последовательности всех константных частей приведены в цитируемой выше работе Kabat и др.
IL-1β-связывающая молекула по настоящему изобретению может быть получена методами рекомбинации ДНК, например, описанными в W0 02/16436.
В еще одном из вариантов осуществления настоящего изобретения соединения IL-1бета могут быть антителами, обладающими специфичностью связывания в отношении антигенного эпитопа IL-1β человека, который включает петлю, содержащую остаток Glu 64 зрелого IL-1β человека (остаток Glu 64 зрелого IL-1β человека соответствует остатку 180 предшественника IL-1β человека). Этот эпитоп расположен вне сайта распознавания IL-1бета-рецептора и поэтому наиболее поразительно, что антитела к этому эпитопу, например, антитело ACZ 885, способны ингибировать связывание IL-1β с его рецептором. Таким образом, применение таких антител для лечения ювенильного ревматоидного артрита и ревматоидного артрита взрослых, и/или синдромов аутоиммунного воспаления, и/или синдрома Макл-Уэлса является новым и включено в рамки охвата настоящего изобретения.
Таким образом, другой объект настоящего изобретения включает применение антитела к IL-1β, которое обладает специфичностью связывания антигена в отношении антигенного эпитопа IL-1β человека, который включает петлю, содержащую остаток Glu 64 зрелого IL-1β человека, и которое способно ингибировать связывание IL-1β с его рецептором для лечения ювенильного ревматоидного артрита или ревматоидного артрита взрослых, и/или синдромов аутоиммунного воспаления, и/или синдрома Макл-Уэлса.
Другие объекты настоящего изобретения включают:
i) применение антитела к IL-1β, которое обладает антигенсвязывающей специфичностью в отношении антигенного эпитопа зрелого IL-1β человека, который включает петлю, содержащую Glu 64, и которое может ингибировать связывание IL-1β с его рецептором, для предупреждения и/или лечения ювенильного ревматоидного артрита, или ревматоидного артрита взрослых, и/или синдромов аутоиммунного воспаления, и/или синдрома Макл-Уэллса;
ii) способ предупреждения и/или лечения ювенильного ревматоидного артрита, или ревматоидного артрита взрослых, и/или синдромов аутоиммунного воспаления, и/или синдрома Макл-Уэллса у пациента, который включает введение пациенту эффективного количества антитела к IL-1β, обладающего антигенной специфичностью в отношении антигенного эпитопа зрелого IL-1β человека, который включает петлю, содержащую Glu 64, и которое может ингибировать связывание IL-1β с его рецептором;
iii) фармацевтического композиция, включающая антитело к IL-1β, которое обладает антигенсвязывающей специфичностью в отношении антигенного эпитопа зрелого IL-1β, который включает петлю, содержащую Glu 64, и которое способно ингибировать связывание IL-1β с его рецептором, в комбинации с фармацевтически приемлемым эксципиентом, растворителем или носителем; для лечения ювенильного ревматоидного артрита, или ревматоидного артрита взрослых, и/или синдромов аутоиммунного воспаления, и/или синдрома Макл-Уэлса.
iv) применение антитела к IL-1β, которое обладает антигенсвязывающей специфичностью в отношении антигенного эпитопа зрелого IL-1β человека, который включает петлю, содержащую Glu 64, и которое способно ингибировать связывание IL-1β с его рецептором, для получения лекарственного средства для лечения ювенильного ревматоидного артрита, или ревматоидного артрита взрослых, и/или синдромов аутоиммунного воспаления, и/или синдрома Макл-Уэлса.
Для целей настоящего изобретения антитело «способно ингибировать связывание IL-1β», если антитело способно ингибировать связывание IL-1β с его рецептором практически в той же степени, что и антитело ACZ 885, т.е. обладает константой уравнения диссоциации (KD), измеренной, например, с помощью стандартного анализа BIAcore по описанию в примере 10 нМ или меньше, например, 1 нМ или меньше, предпочтительно 100 пМ или меньше, более предпочтительно 50 пМ или меньше.
Таким образом, еще один объект настоящего изобретения предусматривает применение антитела к IL-1β, у которого величина Ко по связыванию с IL-1β примерно составляет 10 нМ, 1 нМ, предпочтительно 100 пМ, более предпочтительно 50 пМ или менее для лечения ювенильного ревматоидного артрита, или ревматоидного артрита взрослых, и/или синдромов аутоиммунного воспаления. Этот объект настоящего изобретения также включает способы применения и композиции для таких антител с высоким сродством, согласно описанному выше для антител к IL-1β, имеют связывающую специфичность в отношении антигенного детерминанта зрелого IL-1β человека, который включает петлю, содержащую Glu 64.
В настоящем изобретении фраза «ювенильный ревматоидный артрит, или ревматоидный артрит взрослых, и/или синдромы аутоиммунного воспаления» охватывает все заболевания и медицинские состояния, которые являются частью ювенильного ревматоидного артрита, или ревматоидного артрита взрослых, и/или синдромов аутоиммунного воспаления, прямо или косвенно, в заболевании или медицинском состоянии, включая этиологию, развитие, прогрессирование, персистенцию или патологию заболевания или состояния.
В настоящем изобретении фраза «синдрома Макл-Уэлса (Muckle Wells Syndrome - MWS)» охватывает все заболевания и медицинские состояния, которые являются частью «синдрома Макл-Уэллса», прямо или косвенно, в заболевании или медицинском состоянии, включая этиологию, развитие, прогрессирование, персистенцию или патологию заболевания или состояния.
Соединения формулы I могут вводиться в качестве единственного действующего ингредиента или совместно, например, в качестве адъюванта, с другими лекарственными средствами, например, с иммуносупрессивными или иммуномодулирующими агентами, или другими противовоспалительными агентами, например, для лечения или предупреждения острого или хронического отторжения аллотрансплантата или ксенотрансплантата, или воспалительного или аутоиммунного расстройства, или с химиотерапевтическим агентом, например, агентом против пролиферации злокачественных клеток. Например, могут применяться антитела по настоящему изобретению в комбинации с ингибитором кальциневрина, например, циклоспорином А или FK 506; ингибитором mTOR, например, рапамицином, 40-О-(2-гидроксиэтил)рапамицином, CCI779, АВТ578, АР23573, АР23464, АР23675, АР23841, TAFA-93, биолимусом-7 или биолимусом-9; аскомицином с иммуносупрессивными свойствами, например, АВТ-281, ASM981, и др.; кортикостериодами; циклофосфамидом; азатиопреном; метотрексатом; лефлуномидом; мизорибином; микофеноловой кислотой или солью; микофенолятом мофетила; 15-дезоксиспергуалином или иммуносупрессивным гомологом, аналогом или их производным; ингибитором РКС, например, описанным в WO 02/38561 или WO 03/82859, например, соединением из примера 56 или 70; ингибитором JAK3 киназы, например, N-бензил-3,4-дигидрокси-бензилиден-цианоацетамид-□-циано-(3,4-дигидрокси)-]N-бензилциннамамидом (тирфостином AG 490), продигиозином 25-С (PNU156804), [4-(4'-гидроксифенил)амино-6,7-диметоксихиназолином] (WHI-P131), [4-(3'-бром-4'-гидроксифенил)-амино-6,7-диметоксихиназолином] (WHI-P154), [4-(3',5'-дибром-4'-гидроксифенил)-амино-6,7-диметоксихиназолином] WHI-P97, KRX-211, 3-{(3R,4R)-4-метил-3-[метил-(7H-пирроло[2,3-d]пиримидин-4-ил)-амино]-пиперидин-1-ил}-3-оксо-пропионитрилом, в свободной форме или в форме фармацевтически приемлемой соли, например, моноцитрата (также называемого СР-690550), или соединением, описанным в WO 04/052359 или WO 05/066156; иммуносупрессивными моноклональными антителами, например, моноклональными антителами к рецепторам лейкоцитов, например, МНС, CD2, CD3, CD4, CD7, CD8, CD25, CD28, CD40, CD45, CD52, CD58, CD80, CD86 или их лигандами; другими иммуномодулирующими соединениями, например, рекомбинанатными связывающими молекулами, имеющими по меньшей мере часть внеклеточного домена CTLA4 или его мутанта, например, по меньшей мере внеклеточную часть CTLA4 или его мутанта, соединенного с последовательностью белка, не являющегося CTLA4, например, CTLA4Ig (например, обозначенного АТСС 68629) или его мутанта, например, LEA29Y; ингибиторами адгезии молекул, например, антагонистами LFA-1, антагонистами ICAM-1 или -3, антагонистами VCAM-4 или антагонистами VLA-4; или химиотерапевтическим агентом, например, паклитакселом, гемцитабином, цисплатином, доксорубицином или 5-фторурацилом; или противоинфекционным агентом. Иммуномодулирующие лекарственные средства, которые могут применяться в комбинации с соединением по настоящему изобретению включают, например,
- медиаторы, например, ингибиторы действия mTOR, включая рапамицин формулы

и производные рапамицина, например, включающие
производные 40-О-алкилрапамицина, например, производные 40-О-гидроксиалкилрапвмицина, например, 40-О-(2-гидрокси)этилрапомицин (эверолимус),
производные 32-дезоксирапамицина и производные 32-гидроксирапамицина, например, 32-дезоксирапамицин,
производные 16-О-замещенного рапамицина, например, 16-пент-2-инилокси-32-дезоксирапамицин, 16-реп1-2-инилокси-32(8 или R)-дигидрорапамицин, 16-пент-2-инилокси-32(8 или К)-дигидро-40-О-(2-гидроксиэтил)-рапамицин,
производные рапамицина, которые ацилированы по кислородной группе в положении 40, например, 40-[3-гидрокси-2-(гидроксиметил)-2-метилпропаноат]-рапамицин (также обозначаемое CCI779),
производные рапамицина, которые замещены по положению 40 гетероциклическим соединением, например, 40-эпи-(тетразолил)-рапамицином (также обозначаемое АВТ578),
так называемые рапалоги, например, описанные в WO 9802441, WO 0114387 и WO 0364383, например, АР 23573, и
соединения под названием TAFA-93 и биолимус (биолимус А9).
Соединения IL-1бета по настоящему изобретению могут быть введены в качестве единственного действующего ингредиента, или в соединении с бисфофсонатами, последовательно, одновременно или комбинированно в одном составе. Бисфосфанаты, применяемые в соединении с молекулами IL-1бета по настоящему изобретению, включают этидронат, клодронат, тилудронат, памидронат, неридронат, олпадронат, алендронат, ибандронат, ризедронат, золедронат и какие-либо их полиморфы или производные в виде соли, кислоты.
Соединения IL-1бета по настоящему изобретению могут преимущественно комбинироваться с ингибиторами протеинкиназы С и/или супрессорами активации Т-клеток, в частности производными индолилмалеимида, например, сотрастаурином (3-(1.Н.-индол-3-ил)-4-[2-(4-метилпиперазин-1-ил)-хиназолин-4-ил]-пиррол-2,5-дионом), например, для подавления адаптивной иммунной системы и за счет этого дополнительно повышая терапевтическое воздействие соединений IL-1бета.
Соединения IL-1бета по настоящему изобретению могут также преимущественно комбинироваться с антицитокинами и/или антиинтерлейкинами, в частности IL-17-связывающими соединениями, описанными в WO 2006/013107, необязательно в комбинации с сотрастаурином.
Соединения IL-1бета по настоящему изобретению могут также преимущественно комбинироваться с анти-ТИРальфа соединениями, например, этанерсептом, адалимумабом, инфликсимабом, например, при лечении RA и других аутоиммунных заболеваний.
В настоящем описании понятия «лечение» или «лечить» относятся и к профилактике, и к превентивному лечению, а также к целебному или модифицирующему болезнь лечению, включая лечение пациентов с риском развития заболевания или предположительно уже заболевших, а также пациентов, которые больны или у которых было диагностировано заболевание или медицинское состояние, включают подавление клинического рецидива. Успешное лечение по настоящему изобретению также включает ремиссии всех излечиваемых симптомов, но не ремиссии симптомов, не поддающихся лечению. Например, одним из симптомов Макл-Уэлса является прогрессирование глухоты, которое обычно не поддается излечению и, следовательно, не следует ожидать, что этот симптом может быть излечен. Однако другие симптомы синдрома Макл-Уэлса, поддающиеся излечению, например, сыпь, боль в мышцах, лихорадка, утомляемость и конъюнктивит могут быть полностью преодолены благодаря успешному лечению по настоящему изобретению. Другое определение успешного лечения представляет снижение релевантных биомаркеров синдромов аутоиммунного воспаления, например, синдрома Макл-Уэлса, т.е. снижение сывороточного амилоидного белка (serum amyloid protein -SAA) и с-реактивного белка (c-reactive protein - CRP) до нормального уровня, т.е. <10 мг/л сыворотки у пациентов.
В описании настоящего изобретения заболевание «синдрома Макл-Уэлса Muckle-Wells» находится среди других (молекулярно патологических) заболеваний, определенных по клиническим симптомам, которые представляют эпизоды острого воспаления с лихорадкой при артрите и крапивнице, прогрессирующей глухоте и необязательно длительном амилоидозе многих органов (примерно 25% случаев). Молекулярная патология, вызванная одной или несколькими мутациями в гене MEFV, локализованном на хромосоме 16р 13, который кодирует белок, называемый пирином.
IL-1β-связывающие молекулы, указанные выше, в частности, IL-1β-связывающие молекулы по первому и второму объектам - антитела настоящего изобретения, обладающие связывающей специфичностью в отношении антигенного эпитопа зрелого IL-1β человека, который включает петлю, содержащую Glu 64, в определенных антителах, способных ингибировать связывание IL-1β с его рецептором; и антитела к IL-1β, которые имеют величину Ко для связывания с IL-1β примерно составляющую 10 нМ, 1 нМ, предпочтительно 100 пМ, более предпочтительно 50 пМ или меньше, в настоящем изобретении также относятся к антителам по настоящему изобретению.
В другом варианте осуществления настоящего изобретения дополнительными применениями соединений IL-1бета, например, антител по настоящему изобретению, являются следующие: предупреждение и лечение воспалительной болезни кишечника (ВБК), ювенильного артрита, реактивного артрита, анкилозирующего спондилита, дистрофии миокарда, артериального рестеноза, муковисцидоза, болезни Альцгеймера, множественной миеломы, артериосклероза, фиброза легких, синдрома Макл-Уэллса и хронического обструктивного заболевания легких (ХОЗЛ).
Для всех показаний, описанных в настоящем изобретении (показаний по настоящему изобретению), соответствующие дозы могут, безусловно, варьировать, например, в зависимости от определенных соединений IL-1бета, например, применяемого антитела по настоящему изобретению, хозяина, способа введения, природы и тяжести подвергаемого лечению состояния. Однако при профилактике удовлетворительные результаты обычно получают в дозах примерно от 0,05 мг до примерно 10 мг на кг массы тела, чаще примерно от 0,1 мг до примерно 5 мг на кг массы тела. Антитела по настоящему изобретению удобно вводить парентерально, внутривенно, например, в локтевую или другую периферическую вену, внутримышечно или подкожно.
В еще одном из вариантов осуществления настоящее изобретение относится к непредвиденной частоте дозирования для терапевтического применения, т.е. схемы лечения соединениями IL-1бета, предпочтительно антителами против IL-1бета, более предпочтительно антителом ACZ885 (в обычной дозе, например, примерно от 0,1 мг до примерно 50 мг, более предпочтительно от 0,5 до 20 мг, еще более предпочтительно 1-10 мг антитела ACZ885 на кг массы тела пациента), которое может проводиться раз в неделю или реже, более предпочтительно один раз каждые две недели или реже, более предпочтительно один раз каждые три недели или реже, более предпочтительно один раз каждый месяц или реже, более предпочтительно один раз каждые 2 месяца или реже, более предпочтительно один раз каждые 3 месяца или реже, еще более предпочтительно один раз каждые 4 месяца или реже, еще более предпочтительно один раз каждые 5 месяцев или реже, или еще более предпочтительно один раз каждые 6 месяца или реже. Наиболее предпочтительно один раз каждый месяц.
Фармацевтические композиции настоящего изобретения могут быть получены традиционным способом. Композиция по настоящему изобретению предпочтительно предусмотрена в лиофилизированной форме. Для безотлагательного введения ее растворяют в соответствующем водном носителе, например, стерильной воде для инъекций или стерильном буферном физиологическом растворе. Если считают желательным приготовить раствор большего объема для введения путем инфузии, которое предпочтительнее болюсной инъекции, полезно включить сывороточный альбумин человека или гепаринизированную кровь самого пациента в раствор в момент его составления. Наличие избытка такого физиологически инертного белка предупреждает утрату антитела за счет адсорбции на стенках контейнера и шлангов, используемых для раствора для инфузии. При использовании альбумина соответствующая концентрация составляет от 0,5 до 4,5 мас.% в физиологическом растворе.
Настоящее изобретение дополнительно поясняется приводимыми ниже примерами.
Примеры
Пример 1. Антитело ACZ885
Структура и получение антитела ACZ885 описаны, например, в WO 02/16436. Вкратце, аминоконцевые последовательности вариабельных доменов последовательностей тяжелой и легкой цепи и соответствующие последовательности ДНК приведены ниже в виде последовательностей SEQ ID NO:1 и SEQ ID NO:2, в которых области CDR отмечены курсивом и тип подчеркнут.
Последовательность SEQ ID NO:1 вариабельной области тяжелой цепи антитела ACZ885
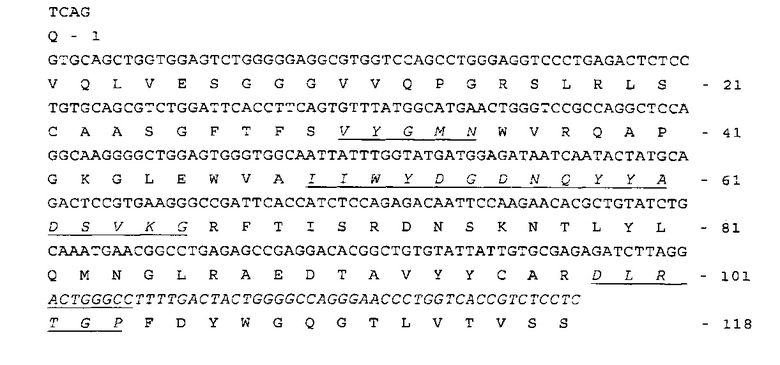
Последовательность SEQ ID NO:2 вариабельной области легкой цепи антитела ACZ885

Пример 2. Биохимические и биологические данные антитела ACZ885 Установлено, что моноклональное антитело ACZ 885 нейтрализует действие интерлейкина-1β in vitro. Моноклональное антитело дополнительно описывают по способности связываться с рекомбинантным IL-1β человека методом поверхностного плазмонного резонанса. Характер нейтрализации оценивают с помощью исследования конкурентного связывания с растворимыми рецепторами IL-1. Биологическое действие антитела ACZ 885 по отношению к рекомбинантному и природному вырабатываемому IL-1β определяют в первичных клетках человека, отвечающих на стимулирование с помощью IL-1β.
Определение константы уравнения диссоциации
Константы скорости ассоциации и диссоциации для связывания рекомбинантного IL-1бета человека с ACZ885 определяют методом плазмонного резонанса. ACZ885 иммобилизуют и связывание рекомбинантного IL-1бета в диапазоне концентраций 1-4 нМ измеряют методом поверхностного плазмонного резонанса. Выбранный формат представляет моновалентное взаимодействие и таким образом осуществляет воздействие на связывание IL-1бета с ACZ885 в стехиометрическом соотношении 1:1. Данные анализа обрабатывают, используя программное обеспечение BIAevaluation.

Заключение: антитело ACZ885 связывается с рекомбинантным IL-1бета человека с очень высокой степенью сродства.
Пример 3. Клиническое исследование с использованием антитела ACZ885
Для оценки применимости соединения IL-1бета, например, ACZ885, проводят открытое одноцентровое исследование дозы ACZ885 (моноконального антитела против IL-1бета человека) для оценки клинической эффективности, безопасности, фармакокинетики и фармакодинамики у пациентов с синдромом MW, характеризующемся мутациями NALP3.
Пациентам вводят инфузией одну дозу ACZ885 (10 мг/кг внутривенно). Клинический ответ определяют по улучшению симптомов (например, кожного высыпания, мышечной боли, лихорадки, утомляемости) и по снижению белков острой фазы - сывороточного амилоидного белка (serum amyloid protein - SAA) и с-реактивного белка (c-reactive protein - CRP). Кроме того, ответ на лечение оценивают по анализу иРНК, полученной из клеток периферической крови. Второе лечение (1 мг/кг внутривенно) проводят после возобновления проявления клинических симптомов. Результаты: клиническая ремиссия симптомов (лихорадки, сыпи, конъюнктивита) в течение 3 суток и снижение CRP и SAA до нормального уровня (<10 мг/л) у пациентов. Клиническая ремиссия симптомов после первой инфузии длится в течение по меньшей мере 134 суток, обычно от 160 до 200 суток. После второй обработки пониженной дозой пациенты отвечают улучшением симптомов и нормализацией белков острой фазы.
Анализ иРНК, полученной из периферических клеток крови, свидетельствует о снижении регуляции трансляции IL-1b- и IL-1b-индуцированных генов в течение 24 ч при лечении ACZ885. Это означает, что антитело ACZ885 может прервать петлю положительной обратной связи in vivo, которая приводит к самоподдерживающемуся сверхсинтезу IL-1b у этих пациентов. Такая связь также поддерживается первоначальной характеристикой воздействий PK/PD антитела ACZ885, которое проявляет блокирование выработки IL-1b при лечении антителом ACZ885 этих пациентов. Это свойство антитела ACZ885 может способствовать (быть причиной) долго длящегося клинического эффекта.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ ПОКАЗАНИЯ К ПРИМЕНЕНИЮ ПРИ ЛЕЧЕНИИ АНТИТЕЛАМИ ПРОТИВ IL-1-БЕТА | 2019 |
|
RU2834722C2 |
| НОВОЕ ПРИМЕНЕНИЕ СОЕДИНЕНИЙ ИЛ-1β | 2012 |
|
RU2571563C2 |
| НОВОЕ ПРИМЕНЕНИЕ СОЕДИНЕНИЙ ИЛ-1β | 2006 |
|
RU2468817C2 |
| АНТИТЕЛА К ЧЕЛОВЕЧЕСКОМУ IL-1БЕТА | 2001 |
|
RU2286351C2 |
| РЕКОМБИНАНТНОЕ АНТИТЕЛО К ЧЕЛОВЕЧЕСКОМУ ИНТЕРЛЕЙКИНУ 1β | 2001 |
|
RU2264413C2 |
| АНТИТЕЛА К ЧЕЛОВЕЧЕСКОМУ МСР-1 | 2001 |
|
RU2314316C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИСПЕЦИФИЧЕСКИХ АНТИТЕЛ, БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА И ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ ТАКИХ АНТИТЕЛ | 2018 |
|
RU2795240C2 |
| СОСТАВЫ, СОДЕРЖАЩИЕ АНТИТЕЛА | 2009 |
|
RU2745601C2 |
| ТЕРАПЕВТИЧЕСКИЕ СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2002 |
|
RU2328506C2 |
| ПРИМЕНЕНИЕ CD25-СВЯЗЫВАЮЩИХ МОЛЕКУЛ ДЛЯ ЛЕЧЕНИЯ ПАЦИЕНТОВ, УСТОЙЧИВЫХ К СТЕРОИДАМ | 2002 |
|
RU2318537C2 |
Группа изобретений относится к медицине, а именно к иммунологии, и может быть использована для лечения периодического синдрома, ассоциированного с рецептором фактора некроза опухоли (TRAPS). Для этого лекарственное средство включает IL-1 бета связывающее антитело человека, причем это антитело содержит: первый домен, имеющий аминокислотную последовательность SEQ ID NO:1, и второй домен, имеющий аминокислотную последовательность SEQ ID NO:2. Группа изобретений относится также к фармацевтической композиции, содержащей указанное антитело, и к способу лечения TRAPS. Использование данной группы изобретений позволяет использовать полученное лекарственно средство, содержащее IL-1 бета связывающее антитело человека, для лечения периодического синдрома, ассоциированного с рецептором фактора некроза опухоли. 3 н. и 16 з.п. ф-лы, 3 пр.
1. Лекарственное средство для лечения синдрома аутоиммунного воспаления у нуждающегося в этом пациента, где лекарственное средство включает IL-1 бета связывающее антитело человека, причем это антитело содержит:
первый домен, имеющий аминокислотную последовательность SEQ ID NO:1, и
второй домен, имеющий аминокислотную последовательность SEQ ID NO:2, и где указанный синдром аутоиммунного воспаления является периодическим синдромом, ассоциированным с рецептором фактора некроза опухоли (TRAPS).
2. Лекарственное средство по п. 1, где антитело представляет собой ACZ885.
3. Лекарственное средство по п. 1 или 2, где указанное лекарственное средство предназначено для парентерального введения и содержит дозу между 0,1-50 мг указанного антитела на кг веса пациента.
4. Лекарственное средство по п. 1 или 2, где указанное лекарственное средство содержит дозу между 0,5-20 мг указанного антитела на кг веса пациента.
5. Лекарственное средство по п. 1 или 2, где указанное лекарственное средство содержит дозу между 1-10 мг указанного антитела на кг веса пациента.
6. Лекарственное средство по п. 1 или 2, где указанное лекарственное средство предназначено для введения один раз каждую неделю или с меньшей частотой.
7. Лекарственное средство по п. 1 или 2, где указанное лекарственное средство предназначено для введения один раз каждый месяц или с меньшей частотой.
8. Лекарственное средство по п. 1, где указанное лекарственное средство предназначено для подкожного введения.
9. Лекарственное средство по п. 1, где указанное лекарственное средство предназначено для внутривенного введения.
10. Способ лечения периодического синдрома, ассоциированного с рецептором фактора некроза опухоли (TRAPS), включающий введение нуждающемуся в этом пациенту эффективного количества IL-1 бета связывающего антитела, как определено в п. 1 или 2.
11. Способ по п. 10, где указанное антитело вводят парентерально в дозе между 0,1-50 мг указанного антитела на кг веса пациента.
12. Способ по п. 10 или 11, где указанное антитело вводят в дозе между 0,5-20 мг указанного антитела на кг веса пациента.
13. Способ по п. 10 или 11, где указанное антитело вводят в дозе между 1-10 мг указанного антитела на кг веса пациента.
14. Способ по п. 13, где указанное антитело вводят один раз каждую неделю или с меньшей частотой.
15. Способ по п. 13, где указанное антитело вводят один раз каждый месяц или с меньшей частотой.
16. Способ по п. 13, где указанное антитело вводят пациенту подкожно.
17. Способ по п. 13, где указанное антитело вводят пациенту внутривенно.
18. Фармацевтическая композиция для лечения периодического синдрома, ассоциированного с рецептором фактора некроза опухоли (TRAPS), включающая IL-1 бета связывающее антитело человека, как определено в п. 1 или 2, и фармацевтически приемлемые эксципиент, растворитель или носитель.
19. Фармацевтическая композиция по п. 18, где антитело представляет собой ACZ885.
| WO2005117945 A1, 15.12.2005 | |||
| WO2007050607 A2, 03.05.2007 | |||
| SIMON A | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| SIMON A | |||
| et al | |||
| Pathogenesis of familial periodic fever syndromes or hereditary autoinflammatory syndromes // Am J Physiol Regul Integr Comp Physiol | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
Авторы
Даты
2019-08-23—Публикация
2014-01-15—Подача