Изобретение относится к медицине, а именно к магнитно-резонансной диагностике, и может быть использовано для диагностики аденокарциномы поджелудочной железы (ПЖ) и метастазов в ее паренхиму.
Заболеваемость опухолями поджелудочной железы в России по данным на 2014 г. составляет 11,4 человек на 100 тыс.населения (см. Под редакцией А.Д. Каприна, В.В. Старинского, Г.В. Петровой Состояние онкологической помощи населению России в 2014 году. М.: МНИОИ им. П.А. Герцена филиал ФГБУ «НМИРЦ» Минздрава России, 2015. илл. - 236 с. ISBN 978-5-85502-210-0).
Нестандартизированные показатели заболеваемости раком поджелудочной железы (РПЖ) в России в 2015 году составили среди мужчин - 12,96, среди женщин - 11,36 на 100 тысяч населения. Стандартизированные по возрасту показатели заболеваемости раком поджелудочной железы составили среди мужчин - 9,14, среди женщин - 5,16 на 100 тысяч населения. Прирост показателей заболеваемости раком поджелудочной железы среди мужчин за предшествующие 10 лет составил 9,39%, среди женщин - 14,95%. При этом отмечается ее неуклонный рост, который за последние 10 лет составил 21,6%. Среди всех злокачественных новообразований рак поджелудочной железы занимает 13-е место, а в структуре смертности от злокачественных новообразований стойко удерживает 4-е место на протяжении нескольких лет во всем мире (см. Siegel RL1, Miller KD, Jemal АСА Cancer J Clin. 2015 Jan-Feb; 65(1):5-29. doi: 10.3322/caac.21254. Epub 2015 Jan 5 Cancer statistics, 2015 CA Cancer J Clin. 2015 Jan-Feb; 65(1):5-29. doi: 10.3322/caac.21254. Epub 2015 Jan 5.Siegel RL1, Miller KD, Jemal А. и Torre LA1, Bray F, Siegel RL, Ferlay J, Lortet-Tieulent J, Jemal A. Global cancer statistics, 2012.CA Cancer J Clin. 2015 Mar; 65(2):87-108. doi: 10.3322/caac.21262. Epub 2015 Feb 4).
Результаты лечения рака поджелудочной железы, как и всех других опухолей, в значительной мере зависят от ранней диагностики. Агрессивность рака поджелудочной железы (ПЖ) и, как следствие, низкие показатели выживаемости больных как без, так и после хирургического лечения, требуют новых подходов к своевременной диагностике данного заболевания (см. American Cancer Society. Cancer Facts & Figures 2013. Atlanta: American Cancer Society; 2013.www.cancer.org).
Метастатическое поражение поджелудочной железы может выявляться при различных злокачественных новообразованиях. Как правило, метастазы в ПЖ диагностируются при диссеминации опухолевого процесса, когда радикальное лечение невозможно, и чаще всего в поджелудочную железу метастазирует рак почки (см. Tanis P.J., van der Gaag N.A., Busch O.R., van Gulik T.M. Gouma D.J. Systematic review of pancreatic surgery for metastatic renal cell carcinoma. Br J Surg 2009; 96: 579-592.).
Вторичные опухоли, поражающие поджелудочную железу, являются метастазами рака легкого, лимфомы, карциномы желудочно-кишечного тракта и карциномы молочной железы. Большая часть обнаружена только при аутопсии. Опухоли, возникающие в забрюшинном пространстве, близлежащих лимфатических узлах или желудочно-кишечной системе, могут инфильтрировать ткань поджелудочной железы.
Для дифференциальной диагностики заболеваний поджелудочной железы предложены разные методы обследования, такие как ультразвуковое исследование (УЗИ), компьютерная томография (КТ), магнитно-резонансная томография (МРТ) с различными последовательностями, Эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ), радиальносканирующая эндосонография, конвексная эндосонография с пункционной биопсией.
УЗИ просто в применении, неинвазивно, аппаратура повсеместно распространена, первый этап обследования пациентов с желтухой либо болью в животе. Однако, метод необъективен, зависим от личного опыта оператора и условий выполнения. Ожирение, асцит, метеоризм, неадекватная подготовка к исследованию, болевой синдром ухудшают визуализацию.
Точность обычной УЗИ-диагностики ограничена сложным расположением поджелудочной железы, наличия артефактов от прилежащих петель кишки и желудка. При чувствительности от 60% до 90% (см. Ueno N., Tomiyama Т., Tano S. et al. (1997) Color Doppler ultrasonography in the diagnosis of portal vein invasion in patients with pancreatic cancer. J Ultrasound Med., 16: 825-830; см. Casadei R., Ghigi G., Gullo L. et al. (1998) Role of color Doppler ultrasonography in the preoperative staging of pancreatic cancer. Pancreas., 16: 26-30; см. Minniti S., Bruno C., Biasiutti C. et al. (2003) Sonography versus helical CT in identification and staging of pancreatic ductal adenocarcinoma. J Clin Ultrasound., 31: 175-182) специфичность метода, по данным ряда мнению авторов, может превышать 90% (см. Morrin М.М., Kruskal J.B., Raptopoulos V. et al. (2001) State-of-the-art ultrasonography is as accurate as helical computed tomography and computed tomographic angiography for detecting unresectable periampullary cancer. J. Ultrasound Med., 20: 481-490).
Компьютерная томография позволяет неинвазивным способом получать изображение патологического очага в поджелудочной железе. Аппараты компьютерной томографии доступны, данные объективны. Методика обладает высокой чувствительностью (91%) и специфичностью (85%) при выявлении РПЖ, преимущественно в случае местно-распространенной опухоли (см. Bipat S., Phoa S.S., van Delden O.M. et al. (2005) Ultrasonography, computed tomography and magnetic resonance imaging for diagnosis and determining resectability of pancreatic adenocarcinoma: a meta-analysis. J Comput Assist Tomogr., 29: 438-445).
Однако в распознавании опухолевых поражений поджелудочной железы, определении их границ на фоне дистрофических и воспалительных изменений остаются неразрешенные проблемы. Это связано с отсутствием больших различий рентгенологической плотности между опухолевой тканью и паренхимой железы, когда приходится ориентироваться на изменение формы и контуров поджелудочной железы, состояние парапанкреатической клетчатки.
Применение компьютерной томографии ведет к лучевой нагрузке на организм пациента. Контрастирование повышает точность и специфичность но потенциально опасно за счет возможности аллергической реакции. Так же, остаются сложности в выявлении небольших размеров опухолевых и метастатических процессов в поджелудочной железе, менее 10-15 мм.
Анатомическое расположение поджелудочной железы определяет объективные трудности при получении материала для морфологической верификации диагноза.
Зачастую, опухоль развивается на фоне последствий воспалительных изменений паренхимы, что, в свою очередь, приводит к вторичному изменению окружающей паренхимы. Это обусловливает дополнительные трудности, искажая характерную эндосонографическую, КТ и МР-картину, изменяя и клиническое течение заболевания.
Наиболее близким к предлагаемому является способ диагностики опухолей поджелудочной железы посредством магнитно-резонансной томографии (МРТ), выбранный нами в качестве прототипа (см. Ly JN, Miller FH. MR imaging of the pancreas: A practical approach. Radiol Clin North Am. 2002; 40:1289-1306. и Lee NK, Kim S, Kim GH, et al. (2012) Diffusion-weighted imaging of biliopancreatic disorders: correlation with conventional magnetic resonance imaging. World J Gastroenterol 18:4102-4117). Он заключается в получении изображений опухолевых образований паренхиматозных органов, взвешенных по Т2 (продольная релаксация) и по Т1 (поперечная релаксация).
При МРТ карциному поджелудочной железы описывают как очаговое неоднородное образование неправильной формы, чаще пониженного в Т1 и изоинтенсивного паренхиме в Т2 и FATSAT сигнала, с нечеткими контурами и нарушением структур протоковой системы, повышенного сигнала в DWI. Традиционно, сканирование поджелудочной железы проводят в трех плоскостях - аксиальной, корональной и сагиттальной.
Анатомия поджелудочной железы, локализация опухолевого и метастатического процессов в любом из ее отделов и направления срезов рутинного исследования приводит к искажению целостной визуализации протоков и участков ткани железы в косых границах сред, получаемыми острыми углами между плоскостью аксиального среза и физиологическим наклоном железы. Так же, недостатком метода является потеря данных из участков, пересекаемых срезом главного панкреатического протока при его диагональном прохождении через объем вокселя, что математически усредняет сигнал в постпроцессинге за счет преобладания в вокселе паренхимы железы.
Эти особенности традиционной визуализации отражены на фигурах 1-3. Это явление относится к группе артефактов частичного объема. Изобретение посвящено сокращению их влияния на диагностический процесс.
Уменьшение объема вокселя приводит к падению сигнала и удлинению времени сбора данных. Изометрическая воксельная визуализация создает реконструируемое изображение, однако грубость итогового визуализационного паттерна не всегда обеспечивает оптимальную интерпретацию и диагностику, что в свою очередь приводит к большему числу эксплоративных лапаротомий, где интраоперационно обнаруживаются метастатические очаги в паренхиме различных отделов поджелудочной железы.
К сожалению, все известные способы не обладают высокой информативностью при диагностике опухолей поджелудочной железы, ее мелкоочагового лимфомного поражения и метастазов в ее паренхиму.
Техническим результатом предлагаемого способа является повышение информативности и точности дифференциальной диагностики опухолевых процессов поджелудочной железы, метастазов в ее паренхиму и состояния ее протоковой системы.
Технический результат достигается тем, что осуществляют транспанкреатическую Т2-взвешенную последовательность, срезы которой закладывают через поджелудочную железу параллельно расположению Вирсунгова протока, для этого используют косое - oblique - Т2-взвешенное изображение с ТЕ в диапазоне 80-90, TR 9400-9500, разрешение матрицы не ниже 320×192, при этом толщина среза - slice - должна составлять 3-4 мм, а расстояние - spacing - между срезами устанавливают 0 мм; используют функцию запуска сбора данных на совпадающих фазах дыхания - respiratory triggering либо задержку дыхания на выдохе, количество срезов должно быть достаточным для визуализации всей поджелудочной железы; получают Т2-взвешенное изображение ПЖ с протоковой системой, определяют наличие опухоли ПЖ, нарушающую проходимость протоковой системы с ее супрастенотическим расширением каудальнее опухоли, либо метастазов в ее паренхиму и их взаиморасположение с протоковой системой; затем аналогичным образом диагонально закладывают изовоксельную DWI-последовательность с b 0 и b 1000 параллельно Вирсунгову протоку, что сокращает количество артефактов и усредненных данных в постпроцессинге на границах сред тканей в перпендикулярных интересующим участкам плоскостях; далее получают суммационное - FUSION - изображение ПЖ с опухолью либо метастазами в ее паренхиму, используя ADC изовоксельной DWI-последовательности с b 0 и b 1000 и транспанкреатическую Т2-последовательность; при наличии гиперинтесивного MP-сигнала в DWI, ограничивающего диффузию до 0,0008-0,0014 мм2/с в опухоли, изогиперинтенсивного MP-сигнала в транспанкреатической Т2-последовательности с нарушением проходимости протоковой системы ПЖ диагностируют аденокарциному ПЖ или метастаз в ее паренхиму; при выявлении MP-картины аденокарциномы ПЖ или метастазов в ее паренхиму для улучшения визуализации границы опухолевого процесса, паренхимы и протоковой системы железы закладывают кросспанкреатическую Т2-взвешенную последовательность, плоскость которой перпендикулярно пересекает расположение Вирсунгова протока, для этого используют косое - oblique - Т2-взвешенное изображение с ТЕ 80-90, TR 9400-9500, разрешение матрицы не ниже 320×192 с расстоянием между срезами 0 мм; далее получают суммационное - FUSION - изображение ПЖ с опухолью либо метастазами, используя ADC изовоксельной DWI-последовательности с b 0 и b 1000 и кросспанкреатическую Т2-взвешенную последовательность.
Изобретение «Способ диагностики аденокарциномы поджелудочной железы (ПЖ) и метастазов в ее паренхиму» является промышленно применимым, так как может быть использовано в клинической онкологии для дифференциальной диагностики рака и метастатического поражения поджелудочной железы.
В предлагаемом описании изобретения используются следующие фигуры:
Фигура 1. Проблема визуализации поджелудочной железы в сагиттальной проекции (плоскости). На фигуре отражены проблемы визуализации:
а - участки поджелудочной железы, где сбор сигнала затруднен и недостоверен - в областях между срезами (вертикальные обесцвеченные области);
б - части поджелудочной железы, заполняющие объем среза частично и не позволяющие полноценно собрать истинный MP-сигнал от ткани, при сканировании в аксиальной плоскости (овалы с обесцвеченной тканью).
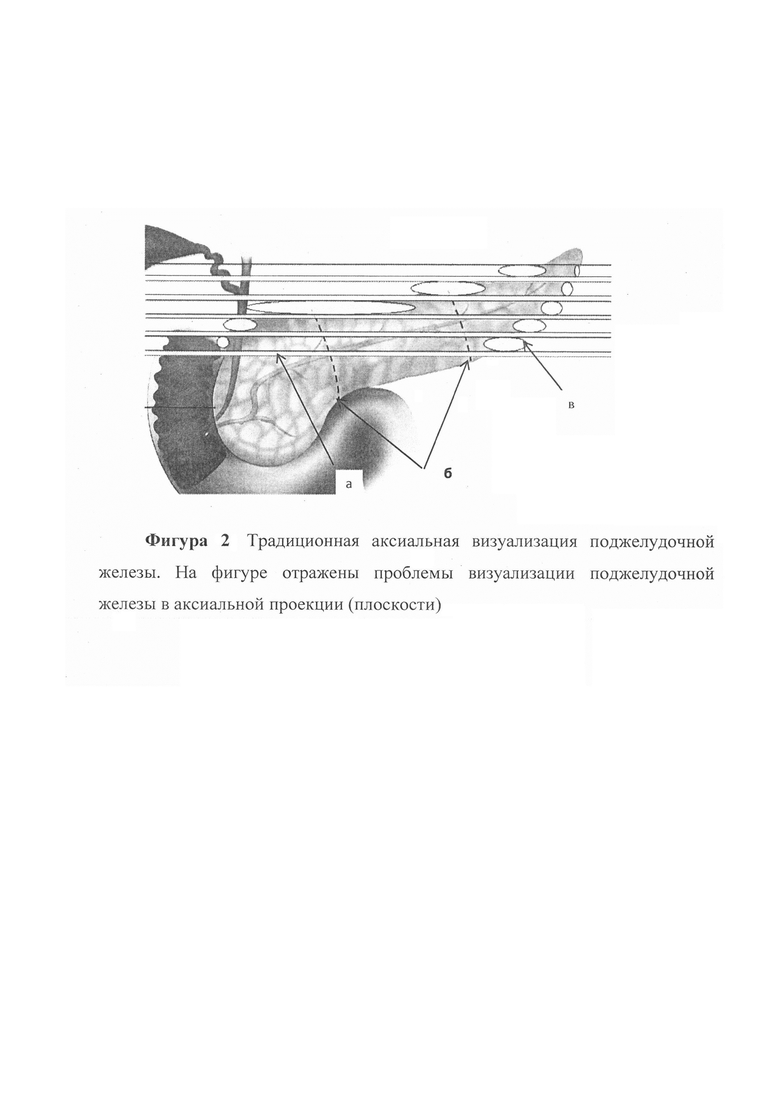
Фигура 2 - На фигуре отражены проблемы визуализации поджелудочной железы в аксиальной проекции:
а - участки поджелудочной железы, где сбор сигнала затруднен и недостоверен - в областях между срезами (горизонтальные обесцвеченные области);
б - границы головки, тела и хвоста поджелудочной железы (пунктирные линии);
в - части поджелудочной железы, заполняющие объем среза частично и не позволяющие полноценно собрать истинный MP-сигнал от ткани, при сканировании в аксиальной плоскости (овалы с обесцвеченной тканью).
Все эти участки создают дополнительные сложности при визуализации процесса традиционными аксиальными срезами.
Фигура 3. Проблема визуализации панкреас в корональной плоскости.
На фигуре отражены проблемы визуализации:
а - участки поджелудочной железы, где сбор сигнала затруднен и недостоверен - в областях между срезами (поперечные обесцвеченные области);
б - части поджелудочной железы, заполняющие объем среза частично, и не позволяющие полноценно собрать истинный MP-сигнал от ткани, при сканировании в аксиальной плоскости (овалы с обесцвеченной тканью).
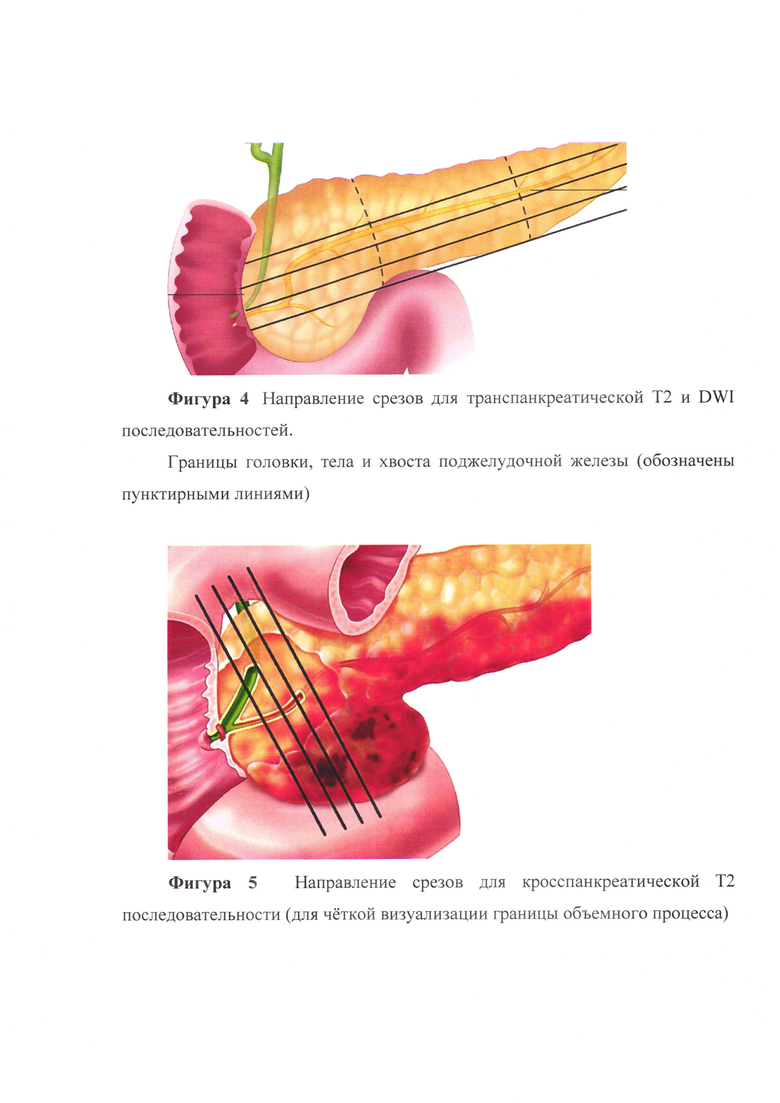
Фигура 4. Направление срезов для транспанкреатической Т2 и DWI последовательностей. Границы головки, тела и хвоста поджелудочной железы (обозначены пунктирными линиями).
Фигура 5. Направление срезов для кросспанкреатической Т2 последовательности (для четкой визуализации границы объемного процесса).
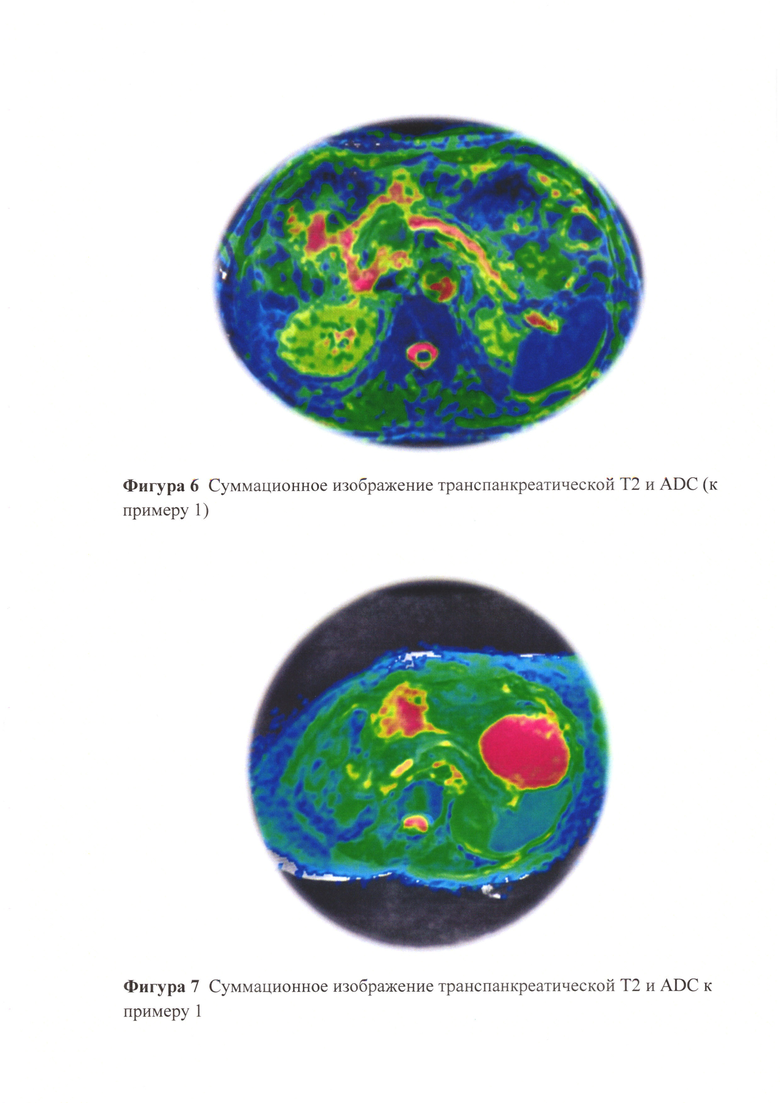
Фигура 6. Суммационное изображение транспанкреатической Т2 и ADC (к примеру 1).
Фигура 7. Суммационное изображение транспанкреатической Т2 и ADC (к примеру 1).
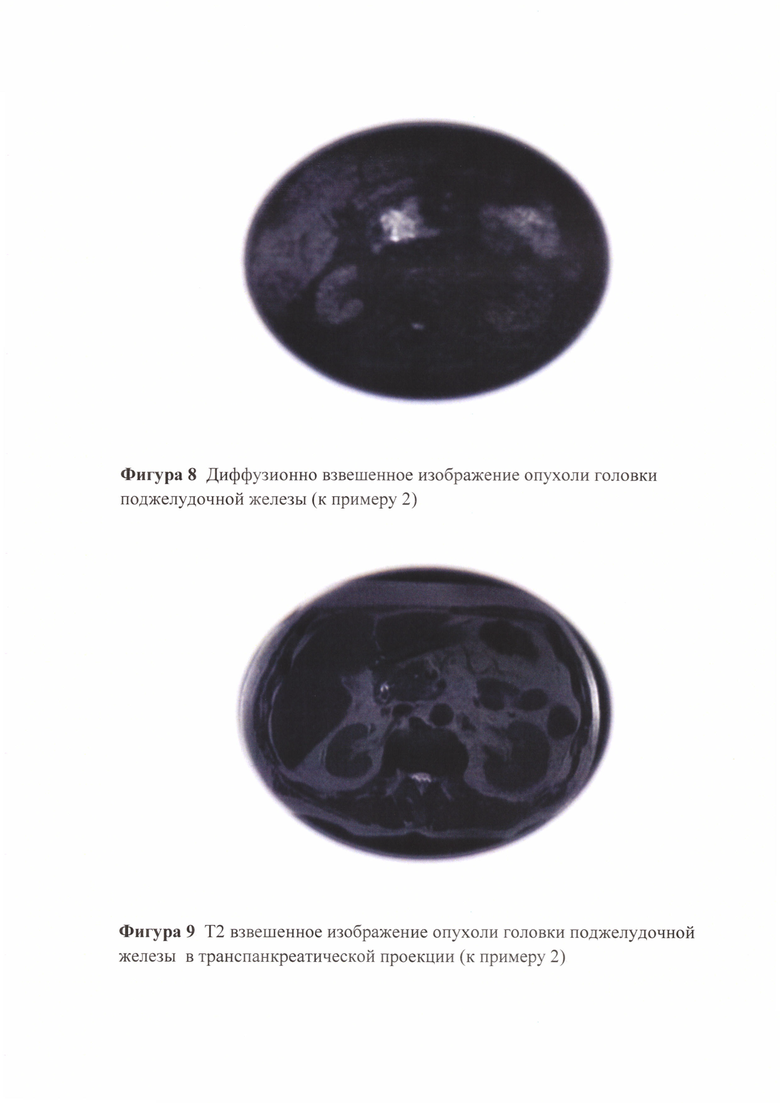
Фигура 8. Диффузионно взвешенное изображение опухоли головки поджелудочной железы (к примеру 2).
Фигура 9. Т2 взвешенное изображение опухоли головки поджелудочной железы в транспанкреатической проекции (к примеру 2).
Фигура 10. Суммационное изображение опухоли головки поджелудочной железы (к примеру 2).
Фигура 11. Суммационное изображение транспанкреатической Т2 и ADC (к примеру 3).
Фигура 12. Суммационное изображение транспанкреатической Т2 и ADC (к примеру 3).
Способ осуществляется следующим образом.
Укладываем пациента в аппарат МРТ в положении на спине головой к оператору (supine feet first) на поверхностной 8-канальной абдоминальной катушке. В руку пациента вкладываем пневматическую грушу для связи с оператором, на грудную клетку накладываем датчик дыхания на уровне нижних ребер. Разметку осуществляем на эпигастральном уровне. Проводим магнитно-резонансное исследование органов брюшной полости для позиционирования поджелудочной железы и визуализации общей анатомии в Т2 и DWI с расчетом ADC. Определяем направление хода панкреатического и общего желчного протоков. Для получения специализированной транспанкреатической Т2-взвешенной последовательности закладываем срезы через поджелудочную железу параллельно расположению Вирсунгова протока (главного панкреатического). Используем косое (oblique) Т2-взвешенное изображение ТЕ 80-90 мс, TR 9400-9500 мс, разрешение матрицы не ниже 320×192. При этом толщина среза (slice) должна составлять 3-4 мм, а расстояние (spacing) между срезами устанавливается 0 мм. Направление срезов для транспанкреатической Т2 и DWI последовательностей схематически показано (см. Фиг. 4).
Используем функцию запуска сбора данных на совпадающих фазах дыхания (respiratory triggering), либо задержку дыхания на выдохе.
Количество срезов должно быть достаточным для визуализации всей поджелудочной железы в зависимости от анатомических особенностей.
Получают Т2-взвешенное изображение протоковой системы, определяют наличие инфильтративного процесса, вовлекающего протоковую систему и супрастенотическое расширение каудальнее опухоли, либо метастатическое поражение паренхимы поджелудочной железы и его отношение к протоковой системе. Также диагонально закладываем изовоксельную DWI с b 0 и b 1000, параллельно Вирсунгову протоку, что сокращает количество артефактов и усредненных данных в постпроцессинге на границах сред тканей в максимально перпендикулярных плоскостях.
Далее получаем суммационное изображение поджелудочной железы и ADC/DWI. Используя изовоксельную DWI с b 0 и b 1000 и специализированной транспанкреатической Т2-взвешенной последовательности возможно получение суммационного (FUSION) изображения с характерным паттерном опухоли.
При наличии гиперинтесивного в DWI, ограничивающего диффузию до 0,0008-0,0014 мм2/с образования, изо-гиперинтенсивного в Т2 с нарушением проходимости протоковой системы поджелудочной железы в специализированной транспанкреатической Т2-взвешенной последовательности, можно указывать на наличие аденокарциномы поджелудочной железы.
При наличии MP-картины образования, для улучшения визуализации границы процесса и паренхимы железы, опухоли и протоковой системы, закладывается кросспанкреатическая Т2-взвешенная серия, плоскость которой перпендикулярно пересекает ход Вирсунгова протока (см. Фиг. 5). Используют косое (oblique) Т2-взвешенное изображение ТЕ 80-90 мс, TR 9400-9500 мс, разрешение матрицы не ниже 320×192, также с нулевым расстоянием между срезами. Далее получают суммационное изображение протоков и ADC/DWI. Используют изовоксельную DWI с b 0 и b 1000 и специализированной транспанкреатической Т2-взвешенной последовательности получают суммационное (FUSION) изображение с характерным паттерном опухоли либо метастаза. Направление срезов для кросспанкреатической Т2 последовательности показано на фигуре 5.
Этот дополнительный критерий визуализации (статус протока и паренхимы поджелудочной железы, FUSION-изображение) расширяет возможности MP-визуализации. Также визуализируют состояние воротной и селезеночной вен, чревного ствола, верхней брыжеечной артерии, парапанкреатической клетчатки, лимфоузлов, прилежащих к поджелудочной железе, двенадцатиперстной кишки.
Типичный паттерн представлен в практических примерах визуализации.
Новым является то, что визуализация осуществляется относительно хода протоковой системы органа, а не традиционных абстрактных плоскостей тела пациента.
Авторами в научно-медицинской и патентной литературе не обнаружено сведений об использовании комплекса данных отличительных признаков для оценки состояния поджелудочной железы в онкологической практике. Таким образом, заявляемое изобретение соответствует критерию «новизна».
Установлено, что наличие солидного образования с вовлечением панкреатического протока и наличие или отсутствие типичной дольчатой паренхимы панкреатического сосудистого и протокового рисунка в образовании являются характерными признаками, совокупность которых позволяет с высокой точностью неинвазивно дифференцировать очаговые поражения и рак поджелудочной железы.
Приводим клинические примеры применения способа.
Пример 1.
Пациент К. обратился в поликлиническое отделение РНИОИ с болевым синдромом в эпигастрии, жалобами на наличие «панкреатического» стула, потемнение мочи. По месту жительства лечился по поводу панкреатита, после КТ и ультрасонографии высказана диагностическая гипотеза о наличии объемного образования головки поджелудочной железы, требующая дифференциальной диагностики с псевдотуморозным панкреатитом.
На стандартном протоколе Т1 и Т2-взвешенные изображения не обеспечивали общей картины зон экстраорганной инвазии и не исключали наличия мелкоочагового поражения тела и хвоста поджелудочной железы на фоне атрофических и воспалительных изменений. Вовлечение стенки воротной вены также визуализировалось неоднозначно.
При исследовании пациента по предлагаемой методике визуализирована MP-картина солидной злокачественной опухоли головки и перешейка поджелудочной железы с вовлечением воротной вены.
Суммационные изображения представлены на фигуре 6 и 7.
Пример 2.
Пациент Б. обратилась в поликлиническое отделение РНИОИ с болевым синдромом в эпигастрии, жалобами на наличие тяжести в области желудка и снижение массы тела. По месту жительства лечилась по поводу панкреатита, холецистита, гастрита после КТ и ультрасонографии высказана диагностическая гипотеза о наличии образования головки поджелудочной железы. Для проведения дифференциальной диагностики с псевдотуморозным панкреатитом направлена в РНИОИ.
На стандартном протоколе Т1 и Т2-взвешенные изображения не обеспечивали общей картины зон экстраорганной инвазии и не исключали наличия мелкоочагового поражения тела и хвоста поджелудочной железы на фоне атрофических и воспалительных изменений.
При исследовании пациента по предлагаемой методике визуализирована MP-картина Tr головки и перешейка поджелудочной железы с множественными мтс-лимфоузлами по ходу воротной вены, в паракавальном коллекторе и одиночным мезентериальным мтс-лимфоузлом. Главный панкреатический проток в каудальной части и теле органа расширен до 5 мм, локально выше опухоли расширен до 10 мм.
Процесс верифицирован морфологически. Суммационное, диффузионно-взвешенное и транспанкреатическое Т2 изображения представлены на фигурах 8, 9 и 10.
Пример 3
При стандартном исследовании поджелудочной железы выявлена следующая MP-картина: локальное утолщение стенок двенадцатиперстной кишки на уровне Фатерова соска, фокус патологической инфильтрации в проекции головки поджелудочной железы. ADC 0,0012 мм 2/с. Холедох дренирован, без расширения внутрипеченочных желчных протоков. Поджелудочная железа в остальных отделах не увеличена, имеет ровные контуры, без очаговых изменений.
При выполнении расширенных серий в том числе транс- и кросс-панкреатической с DWI, при реконструкции выявлено метастатическое поражение тела и хвоста поджелудочной железы, что подтверждено интраоперационно.
Суммационные изображения представлены на фигурах 11 и 12.
Диагностические возможности предлагаемого способа были проверены при анализе результатов 10 пациентов.
Предлагаемый способ бесконтрастной дифференциальной диагностики опухолей поджелудочной железы, отличаясь простотой и кратковременностью проведения 30 мин, а также высокой информативностью, позволяет улучшить результаты постановки диагноза, а следовательно, и лечения данного контингента больных.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ РАКА ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2019 |
|
RU2742744C1 |
| СПОСОБ ДИАГНОСТИКИ ГИПЕРТЕНЗИИ ВИРСУНГОВА ПРОТОКА У БОЛЬНЫХ С ХРОНИЧЕСКИМ ПАНКРЕАТИТОМ | 2015 |
|
RU2616324C2 |
| Способ проведения магнитно-резонансной томографии предстательной железы у пациентов с металлоконструкциями тазобедренного сустава | 2021 |
|
RU2783002C1 |
| СПОСОБ ДИАГНОСТИКИ ИНФИЛЬТРАТИВНЫХ ОПУХОЛЕЙ ПОЧЕК | 2020 |
|
RU2726589C1 |
| СПОСОБ ИССЛЕДОВАНИЯ ОПУХОЛИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ, СПОСОБ ИССЛЕДОВАНИЯ РЕЗЕЦИРОВАННОГО ОРГАНОКОМПЛЕКСА И ЕГО ПРИМЕНЕНИЕ | 2014 |
|
RU2568766C2 |
| СПОСОБ ЛЕЧЕНИЯ НЕЙРОЭНДОКРИННЫХ ОПУХОЛЕЙ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ МАЛОГО РАЗМЕРА | 2019 |
|
RU2714034C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ РАКА ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ И ХРОНИЧЕСКОГО ПАНКРЕАТИТА | 2007 |
|
RU2353301C2 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ЛОЖНЫХ КИСТ ГОЛОВКИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ, СООБЩАЮЩИХСЯ С ГЛАВНЫМ ПАНКРЕАТИЧЕСКИМ ПРОТОКОМ | 2005 |
|
RU2277870C1 |
| Способ дифференциальной диагностики рака поджелудочной железы и хронического панкреатита | 2021 |
|
RU2785325C1 |
| СПОСОБ ДИАГНОСТИКИ ПАНКРЕАТИЧЕСКОЙ ГИПЕРТЕНЗИИ | 2013 |
|
RU2526917C1 |




Изобретение относится к медицине, а именно к магнитно-резонансной томографии, абдоминальной хирургии и гастроэнтерологии, и может быть использовано для диагностики аденокарциномы поджелудочной железы (ПЖ) и метастазов в ее паренхиму. Проводят магнитно-резонансное исследование органов брюшной полости в Т2- и DWI-взвешенных последовательностях с расчетом ADC для позиционирования поджелудочной железы, визуализации общей анатомии, определения направления хода панкреатического и общего желчного протоков. Осуществляют транспанкреатическую Т2-взвешенную последовательность, срезы которой закладывают через поджелудочную железу параллельно расположению Вирсунгова протока. Для этого используют косое – oblique – Т2-взвешенное изображение с ТЕ в диапазоне 80-90, TR – 9400-9500, разрешение матрицы не ниже 320×192. При этом толщина среза – slice – должна составлять 3-4 мм, а расстояние – spacing – между срезами устанавливают 0 мм. Используют функцию запуска сбора данных на совпадающих фазах дыхания – respiratory triggering либо задержку дыхания на выдохе. Количество срезов должно быть достаточным для визуализации всей поджелудочной железы. Получают Т2-взвешенное изображение ПЖ с протоковой системой. Определяют наличие опухоли ПЖ, нарушающей проходимость протоковой системы с ее супрастенотическим расширением каудальнее опухоли, либо метастазов в ее паренхиму и их взаиморасположение с протоковой системой. Затем аналогичным образом диагонально закладывают изовоксельную DWI-последовательность с b 0 и b 1000 параллельно Вирсунгову протоку, что сокращает количество артефактов и усредненных данных в постпроцессинге на границах сред тканей в перпендикулярных интересующим участкам плоскостях. Далее получают суммационное – FUSION – изображение ПЖ с опухолью либо метастазами в ее паренхиму, используя ADC изовоксельной DWI-последовательности с b 0 и b 1000 и транспанкреатическую Т2-последовательность. При наличии гиперинтесивного MP-сигнала в DWI, ограничивающего диффузию до 0,0008-0,0014 мм2/с в опухоли, изогиперинтенсивного MP-сигнала в транспанкреатической Т2-последовательности с нарушением проходимости протоковой системы ПЖ диагностируют аденокарциному ПЖ или метастаз в ее паренхиму. При выявлении MP-картины аденокарциномы ПЖ или метастазов в ее паренхиму для улучшения визуализации границы опухолевого процесса, паренхимы и протоковой системы железы может быть использовано закладывание кросспанкреатической Т2-взвешенной последовательности, плоскость которой перпендикулярно пересекает расположение Вирсунгова протока. Для этого используют косое – oblique – Т2-взвешенное изображение с ТЕ 80-90, TR 9400-9500, разрешение матрицы не ниже 320×192 с расстоянием между срезами 0 мм. Далее получают суммационное – FUSION – изображение ПЖ с опухолью либо метастазами, используя ADC изовоксельной DWI-последовательности с b 0 и b 1000 и кросспанкреатическую Т2-взвешенную последовательность. Способ обеспечивает повышение информативности и точности дифференциальной диагностики опухолевых процессов поджелудочной железы, метастазов в ее паренхиму и состояния ее протоковой системы. 1 з.п. ф-лы, 12 ил., 3 пр.
Способ диагностики аденокарциномы поджелудочной железы (ПЖ) и метастазов в ее паренхиму, включающий магнитно-резонансное исследование органов брюшной полости в Т2- и DWI-взвешенных последовательностях с расчетом ADC для позиционирования поджелудочной железы и визуализации общей анатомии, определения направления хода панкреатического и общего желчного протоков, отличающийся тем, что осуществляют транспанкреатическую Т2-взвешенную последовательность, срезы которой закладывают через поджелудочную железу параллельно расположению Вирсунгова протока, для этого используют косое - oblique -Т2-взвешенное изображение с ТЕ в диапазоне 80-90, TR 9400-9500, разрешение матрицы не ниже 320×192, при этом толщина среза - slice - должна составлять 3-4 мм, а расстояние - spacing - между срезами устанавливают 0 мм; используют функцию запуска сбора данных на совпадающих фазах дыхания - respiratory triggering - либо задержку дыхания на выдохе, количество срезов должно быть достаточным для визуализации всей поджелудочной железы; получают Т2-взвешенное изображение ПЖ с протоковой системой, определяют наличие опухоли ПЖ, нарушающей проходимость протоковой системы с ее супрастенотическим расширением каудальнее опухоли, либо метастазов в ее паренхиму и их взаиморасположение с протоковой системой; затем аналогичным образом диагонально закладывают изовоксельную DWI-последовательность с b 0 и b 1000 параллельно Вирсунгову протоку, что сокращает количество артефактов и усредненных данных в постпроцессинге на границах сред тканей в перпендикулярных интересующим участкам плоскостях; далее получают суммационное - FUSION - изображение ПЖ с опухолью либо метастазами в ее паренхиму, используя ADC изовоксельной DWI-последовательности с b 0 и b 1000 и транспанкреатическую Т2-последовательность; при наличии гиперинтесивного MP-сигнала в DWI, ограничивающего диффузию до 0,0008-0,0014 мм2/с в опухоли, изогиперинтенсивного MP-сигнала в транспанкреатической Т2-последовательности с нарушением проходимости протоковой системы ПЖ диагностируют аденокарциному ПЖ или метастаз в ее паренхиму.
2. Способ по п. 1, где при выявлении MP-картины аденокарциномы ПЖ или метастазов в ее паренхиму для улучшения визуализации границы опухолевого процесса, паренхимы и протоковой системы железы закладывают кросспанкреатическую Т2-взвешенную последовательность, плоскость которой перпендикулярно пересекает расположение Вирсунгова протока, для этого используют косое - oblique - Т2-взвешенное изображение с ТЕ 80-90, TR 9400-9500, разрешение матрицы не ниже 320×192 с расстоянием между срезами 0 мм; далее получают суммационное - FUSION - изображение ПЖ с опухолью либо метастазами, используя ADC изовоксельной DWI-последовательности с b 0 и b 1000 и кросспанкреатическую Т2-взвешенную последовательность.
| Gibbs P | |||
| et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| // Invest Radiol | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| СПОСОБ УЛЬТРАЗВУКОВОЙ ДИАГНОСТИКИ ПЕРВИЧНОЙ ЛОКАЛИЗАЦИИ ОПУХОЛЕЙ, ВЫЗЫВАЮЩИХ ОБСТРУКЦИЮ ДИСТАЛЬНОГО ОТДЕЛА ОБЩЕГО ЖЕЛЧНОГО ПРОТОКА | 1997 |
|
RU2119299C1 |
| Шима В | |||
| и др | |||
| Аденокарцинома поджелудочной железы: выявление, определение стадии и дифференциальная диагностика | |||
| // Медицинская визуализация | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Lee N.K.et al | |||
| Diffusion-weighted imaging of biliopancreatic disorders: correlation with conventional magnetic resonance imaging | |||
| // World J Gastroenterol | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Lee E.S | |||
| et al | |||
| Imaging diagnosis of pancreatic cancer: a state-of-the-art review | |||
| // World J Gastroenterol | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Zhang L | |||
| et al | |||
| Challenges in diagnosis of pancreatic cancer | |||
| // World J Gastroenterol | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Gurney-Champion O.J | |||
| et al | |||
| Comparison of six fit algorithms for the intra-voxel incoherent motion model of diffusion-weighted magnetic resonance imaging data of pancreatic cancer patients | |||
| // PLoS One | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
Авторы
Даты
2019-09-04—Публикация
2018-06-18—Подача