Ящур занимает первоочередное место в системе мер борьбы и профилактики вирусных болезней крупного рогатого скота во многих государствах. Данное заболевание представляет собой мировую проблему, которой особое внимание уделяют ветеринарные службы многих стран и международные организации (ФАО/МЭБ). По итогам 81-ой Генеральной сессии ФАО/МЭБ (2013 г.) была принята резолюция, согласно которой ящур, принадлежащий группе «трансграничных инфекций», признается глобальной проблемой, наносящей значительный ущерб для торговли и продовольственной безопасности всех стран [1, 2]. Вирус ящура легко распространяется, по этой причине данное заболевание может приобретать размах эпизоотий [3, 4]. В Российской Федерации применяется система мероприятий по борьбе и профилактике ящура, которая направлена на предупреждение заноса вируса в страну, систематическую иммунизацию крупного и мелкого рогатого скота в буферной зоне, а также проведение мониторинга иммунного статуса привитых животных. Для иммунизации животных должна применяться вакцина, изготовленная из вируса, гомологичного полевым изолятам [5, 6].
Недавние вспышки ящура демонстрируют, что эта крайне заразная вирусная инфекция парнокопытных животных продолжает оставаться значительной экономической проблемой во всем мире. Споры о наиболее эффективном способе реагирования на вспышки ящура в странах, свободных от болезни, по-прежнему сосредоточены на использовании вакцин. Экстренная вакцинация является одной из нескольких мер, которые могут быть применены для борьбы со вспышками ящура. Это может быть ценным дополнением к применению основных мер зоосанитарного контроля, которые должны включать быструю диагностику, отслеживание, контроль за передвижением и дезинфекцию и которые могут также включать убой инфицированных и контактирующих животных и их безопасное удаление [4, 7]. Критерии, которые определяют успешное применение экстренной вакцинации включают в себя доступ к вакцине, которая, во-первых, содержит штамм вируса достаточного антигенного родства в очаге; во-вторых, характеризуется приемлемой безвредностью и эффективностью; в-третьих, имеет соответствующий доступ, в том числе количество и своевременность поставок.
Планирование на случай непредвиденных обстоятельств должно включать обеспечение экстренной вакцинации и учитывать сложные решения не только о том, когда, где и как применять вакцину, но и ее экономические последствия [4, 6].
В литературных источниках указывают, что экстренная вакцинация крупного рогатого скота, овец и свиней вакцина может быть эффективной в профилактике заболевания в течение 4-5 дней после вакцинации [4, 8]. Эти исследования демонстрируют, что риск распространения инфекции уменьшается по мере увеличения интервала между вакцинацией и заражением вирусом и что вакцинация может уменьшить количество выделяемого вируса по сравнению с не вакцинированными животными [4, 5, 9].
В период с сентября 2017 г. по март 2018 г. было зарегистрировано около 30 вспышек ящура типа О у крупного рогатого скота, овец и коз в нескольких провинциях Монголии, территориально граничащей с Россией на севере и Китаем на юге. Постоянная возможность заноса возбудителя на территорию России диктует необходимость усиления противоящурных мероприятий, которые направлены на предупреждение заноса вируса в страну, проведение систематических мониторинговых исследований, а также осуществление поголовной вакцинации восприимчивых животных в буферной зоне [10, 11]. Из-за быстрого распространения инфекции меры контроля должны применяться сразу после вспышки, например, при использовании вакцин, которые вызывают быструю защиту. Вакцины за многие десятилетия их производства доказали свою неоспоримую пользу в борьбе с инфекционными заболеваниями. Для специфической профилактики ящура широко применяют моно- и поливалентные вакцины из инактивированного культурального вируса ящура [12]. Исследования по разработке вакцин для ранней защиты подтверждают, что при их использовании динамика нарастания иммунитета у восприимчивых животных в зоне вспышки служит барьером для вируса, приводит к сдерживанию инфекции и ее купированию в первичном очаге [13, 14].
Важной особенностью возбудителя ящура является антигенная изменчивость штаммов в пределах одного серотипа, возникающая в различные временные промежутки на разных территориях, и зависящая от видового состава восприимчивого поголовья животных, его иммунного статуса и множества других факторов. Преимущественно замены в аминокислотных последовательностях имеют место в полипептидах вирусных белках, составляющих капсид вириона. Возникающие антигенные изменения могут выражаться как в незначительных отличиях между штаммами, улавливаемых только с помощью тонких методов молекулярного анализа, так и в появлении совершенно отличающихся штаммов, требующих использования новых средств специфической профилактики вызываемой болезни [2, 3].
Изменения антигенного спектра, соответствующие обновлению структуры нового полевого изолята, могут варьировать от незначительных, детектируемых моноклональными антителами, до существенных, регистрируемых с помощью поликлональных иммуноглобулинов. Существенные генетические изменения природного изолята вызывают ослабление специфического иммунитета против ящура, индуцированного гетерологичным антигеном. В результате возникает необходимость создания новых средств диагностики и специфической иммунопрофилактики ящура.
Известны штаммы возбудителя ящура типа О, которые долгое время применяли в качестве производственных в России в течение последних 50 лет.
На территории РФ в ОПХ «Степное» села Элитное Уссурийского района Приморского края 13 апреля 2000 года от свиней выделен изолят вируса ящура типа О №1734/Приморский/2000. Сравнительный анализ нуклеотидных последовательностей штамма О №1734/Приморский/2000, показал, что данный вирус относится к генетической линии PanAsia типа О. Паназиатский вирус вызвал пандемию ящура в 1999-2000 годах в большинстве стран Азии, в том числе в Японии, Корее, Вьетнаме, Монголии, а также Армении и Грузии. Опустошительная эпизоотия ящура в Великобритании в 2001 году была также вызвана вирусом данной генетической линии. Штамм О №1734/Приморский/2000 имеет наиболее высокий уровень гомологии (98,74%) с изолятами О Вьетнам/99 и О Тайвань/99. При этом по антигенным характеристикам он отличается от всех выделенных ранее штаммов О1 №194 и О1 №1618/Чечено-Ингушский/66, используемых для изготовления средств диагностики и специфической профилактики [15].
В Восточно-Гобийском аймаке Монголии в феврале 2004 года от КРС выделили штамм О №1964/Монголия/2004, который используется для производства диагностических и вакцинных препаратов [16].
В странах Юго-Восточной Азии (Бутан, Монголия, Непал, Китай и др.) за 2015-2017 гг.по квартальным данным WRL FMD неоднократно выделяли изоляты вируса ящура, которые по результатам молекулярно-биологического анализа гена VP1, относятся к генетической линии O/ME-SA/Ind-01d. Следует отметить, что вирус ящура линии О Ind-2001 был выделен на территории Российской Федерации впервые.
Наиболее близкой предлагаемому изобретению по совокупности существенных признаков является вакцина инактивированная эмульсионная против ящура типа О, содержащая активное вещество в виде авирулентного и очищенного антигенного материала из гомологичного возбудителю инфекции штамма О №2147/Приморский/2012, полученного в чувствительной биологической системе, и целевые добавки в виде масляного адъюванта в соотношении, мкг/см3:
В качестве чувствительной биологической системы для репродукции вируса ящура используют перевиваемую суспензионную клеточную линию из почки новорожденного сирийского хомячка ВНК-21, в качестве поддерживающей среды применяют раствор Эрла без внесения сыворотки, с добавлением ферментативного гидролизата мышц сухого (ФГМС), гидролизата белков крови сухого (ГБКС) и антибиотиков при рН среды 7,4-7,6.
Для инактивации вируса используют аминоэтилэтиленимин (АЭЭИ). При изготовлении эмульсионной вакцины в качестве адъювантов служат Montanide ISA-206. Очистку вируссодержащей суспензии от балластных примесей осуществляют с применением полигексаметиленгуанидин гидрохлорид (ПГМГ).
Авирулентный и очищенный антигенный материал из штамма О №2147/Приморский/2012 представляет собой суспензию, состоящую преимущественно из 146S и 75S иммуногенных компонентов вируса ящура.
Существенный недостаток известных вакцин, в том числе и вакцины-прототипа, состоит в их недостаточной иммуногенной активности, что объясняется невысокой степенью защиты восприимчивых животных от эпизоотических изолятов вируса ящура типа О, циркулирующего в странах Центральной и Юго-Восточной Азии.
Для решения этой проблемы было создано настоящее изобретение, в которое входила разработка противоящурной инактивированной эмульсионной вакцины, обеспечивающей эффективную раннюю защиту восприимчивых животных против полевых изолятов вируса ящура типа О, распространенных на территории Центральной и Юго-Восточной Азии.
Технический результат от использования предлагаемого изобретения заключается в расширении арсенала вакцин для ранней защиты против ящура типа О инактивированных эмульсионных.
Указанный технический результат достигнут созданием вакцины для ранней защиты против ящура типа О инактивированной эмульсионной, охарактеризованной следующей совокупностью признаков.
Разработанная вакцина в 1 см3 препарата содержит следующие компоненты: активное вещество в виде авирулентного и очищенного антигенного материала из гомологичного возбудителю инфекции штамма О №2344/Монголия/2017 вируса ящура, репродуцированного предпочтительно в перевиваемой суспензионной клеточной линии ВНК-21, в количестве не менее 3,0 мкг и масляный адъювант Montanide ISA-206 предпочтительно в количестве 500000,0-575000,0 мкг, соответственно.
Изолят вируса ящура, послуживший источником для получения штамма вируса ящура типа О №2344/Монголия/2017, был выделен в ноябре 2017 года от больных ящуром КРС, находящихся на территории Монголии (экспертиза №2344). Производственный штамм вируса ящура типа О №2344/Монголия/ 2017 получен путем последовательных пассажей на чувствительных гетеро- и гомологичных культурах клеток.
Штамм вируса ящура типа О №2344/Монголия/2017 депонирован в Коллекцию штаммов микроорганизмов Федерального государственного бюджетного учреждения «Федеральный центр охраны здоровья животных» (ФГБУ «ВНИИЗЖ»), под регистрационным номером: №116 - деп / 19-6 - КШМ ФГБУ «ВНИИЗЖ».
Штамм адаптирован к первично-трипсинизированным клеткам свиной почки и перевиваемым клеточным линиям из почки новорожденного сирийского хомячка (ВНК-21), почки свиньи (IB-RS-2) и почки сибирского горного козерога (ПСГК-30).
Для изготовления вакцины в качестве чувствительной биологической системы используют предпочтительно перевиваемую суспензионную культуру клеток ВНК-21, а в качестве поддерживающей среды применяют раствор Эрла без внесения сыворотки с добавлением ФГМС, ГБКС и антибиотиков при рН среды 7,4-7,6. Инактивацию вируса проводят с использованием АЭЭИ с концентрацией 0,025-0,050% от объема вируссодержащей суспензии. По окончании процесса АЭЭИ нейтрализуют внесением в суспензию тиосульфата натрия [8]. Инактивированный антиген очищают от балластных примесей с помощью ПГМГ, который вносят в суспензию до концентрации 0,005-0,007% от общего объема [9].
Авирулентный и очищенный антигенный материал из штамма О №2344/Монголия/2017 представляет собой суспензию, содержащую преимущественно 146S иммуногенный компонент вируса ящура.
Содержание компонента в продукте оценивают с помощью количественного варианта реакции связывания комплемента (РСК) [10]. Для приготовления вакцины используют вирусный материал, содержащий в 1 см3 не менее 0,5 мкг 146S иммуногенного компонента вируса ящура. Необходимую концентрацию 146S компонента в вакцинном препарате обеспечивают благодаря концентрированию антигена методом проточной ультрафильтрации.
Эмульсионную инактивированную вакцину против ящура типа О получают путем диспергирования при помощи гомогенизатора концентрата ящурного антигена и масляного адъюванта в соотношении 1:1 по массе, соответственно. Для усиления иммунного ответа используют масляный адъювант производства фирмы «Seppic» Montanide ISA-206.
Полученная вакцина представляет собой молокоподобную жидкость, не растворимую в воде.
Предлагаемое изобретение включает следующую совокупность существенных признаков, обеспечивающих получение технического результата во всех случаях, на которые спрашивается правовая охрана:
1. Вакцина инактивированная эмульсионная против ящура типа О.
2. Активное вещество в виде авирулентного и очищенного антигенного материала из гомологичного возбудителю инфекции штамма О №2344/Монголия/2017 вируса ящура в эффективном количестве.
3. Целевые добавки.
Существенные отличительные признаки предлагаемой вакцины заключаются в том, что в качестве активного вещества она содержит авирулентный очищенный антигенный материал из штамма О №2344/Монголия/2017 в эффективном количестве.
Предлагаемое изобретение характеризуется также другими отличительными признаками, выражающими конкретные формы выполнения или особые условия его использования:
1. Авирулентный и очищенный антигенный материал из штамма О №2344/Монголия/2017 вируса ящура типа О, полученный предпочтительно в суспензионной перевиваемой культуре клеток ВНК-21 и представляющий собой суспензию, содержащую преимущественно 146S иммуногенный компонент вируса ящура в эффективном количестве.
2. Авирулентный и очищенный антигенный материал из штамма О №2344/Монголия/2017 вируса ящура типа О, полученный предпочтительно в суспензионной перевиваемой культуре клеток ВНК-21 и представляющий собой суспензию, содержащую преимущественно 146S иммуногенный компонент вируса ящура в количестве не менее 3,0 мкг в 1 см3 готового препарата.
3. Из целевых добавок вакцина содержит масляный адъювант.
4. Из целевых добавок вакцина содержит масляный адъювант Montanide ISA-206.
5. Вакцина содержит масляный адъювант Montanide ISA-206 в количестве 500000,0-575000,0 мкг в 1 см3 готового препарата.
6. Авирулентный и очищенный антигенный материал из штамма О №2344/Монголия/2017 вируса ящура, полученного предпочтительно в суспензионной перевиваемой культуре клеток BHK-21 и масляный адъювант Montanide ISA-206 в количестве, мкг/см готового препарата:
Предлагаемая вакцина обладает высокой иммуногенной активностью и обеспечивает надежную раннюю защиту против вируса ящура типа О, циркулирующего в странах Центральной и Юго-Восточной Азии.
Достижение технического результата от использования изобретения обеспечивается тем, что в состав предлагаемой противоящурной вакцины в качестве активного вещества введен антигенный материал из штамма О №2344/Монголия/2017, обладающий высокой иммуногенной активностью, создающий эффективную раннюю защиту восприимчивых животных против вируса ящура серотипа О, вызывающего в последние годы вспышки заболевания в странах Центральной и Юго-Восточной Азии.
Сущность изобретения представлена на дендрограмме, которая отражает филогенетическое взаимоотношение штамма О №2344/Монголия/2017 вируса ящура с эпизоотическими изолятами и вакцинными штаммами вируса ящура серологического типа О. Дендрограмма основана на сравнении полных нуклеотидных последовательностей гена VP1.
Сущность изобретения изложена в перечне последовательностей, в котором:
SEQ ID NO: 1 представляет последовательность нуклеотидов гена VP1 штамма О №2344/Монголия/2017 вируса ящура типа О;
SEQ ID NO: 2 отражает последовательность аминокислот белка VP1 штамма О №2344/Монголия/2017 вируса ящура типа О.
Штамм О №2344/Монголия/2017 вируса ящура типа О характеризуется следующими признаками и свойствами.
Морфологические признаки
Штамм вируса ящура О №2344/Монголия/2017 относится к семейству Picornaviridae, роду Aphtovirus, серотипу О и обладает морфологическими признаками, характерными для возбудителя ящура: форма вириона икосаэдрическая, размер 23-25 нм. Вирион состоит из молекулы РНК, заключенной в белковую оболочку. Белковая оболочка состоит из 32 капсомеров, расположенных в кубической симметрии.
Антигенные свойства
По своим антигенным свойствам штамм О №2344/Монголия/2017 вируса ящура относится к серотипу О. Вирус стабильно нейтрализуется гомологичной антисывороткой. Вирус не проявляет гемагглютинирующей активности (ГА-активности). У переболевших животных в сыворотке крови образуются типоспецифические антитела, выявляемые в иммуноферментном анализе (ИФА) и реакции микронейтрализации (РМН).
Методом нуклеотидного секвенирования была определена первичная структура гена VP1 штамма вируса ящура О №2344/Монголия/2017. Сравнительный анализ нуклеотидных последовательностей показал, что штамм О №2344/Монголия/2017 вируса ящура принадлежит к генетической линии Ind-2001 топотипа Ближний Восток - Южная Азия.
Антигенное родство штамма О №2344/Монголия/2017 с производственными штаммами вируса ящура O1 Manisa, О №1734/Приморский/2000, О PanAsia-2, О №2147/Приморский/2012 и О №2212/Приморский/2014 изучено в РМН. Результаты исследований в РМН представлены в таблице 1, из которой следует, что антигенное соответствие (r1) составило для O1 Manisa - 0,45; О №1734/Приморский/2000 - 0,46; О PanAsia2 - 0,47; О №2147/Приморский/2012 - 0,74 и 0№2212/ Приморский/2014 - 0,24.
При значении r1>0,3 полевой изолят и производственный штамм являются близкородственными, и вакцина из производственного штамма будет защищать от эпизоотического вируса, при значении r1<0,3 полевой изолят отличается от производственного штамма, и вакцина из данного штамма не защищает от эпизоотического вируса.
Биотехнологические характеристики
Штамм вируса ящура О №2344/Монголия/2017 репродуцируется в перевиваемых культурах клеток: почки сибирского горного козерога (ПСГК-30), почки свиньи (IB-RS-2), почки сирийского хомячка (ВНК-21). В течение 20-24 часов инкубирования урожай вируса в указанных культурах клеток достигает высоких значений от 5,70±0,25 до 6,25±0,25 lg ТЦД50/0,1 см3. Данный штамм сохраняет исходные характеристики при пассировании в клеточных культурах ПСГК-30 и IB-RS-2 на протяжении 3 последовательных пассажей (срок наблюдения). Кроме того, штамм О №2344/Монголия/2017 сохраняет исходные характеристики при пассировании в суспензионной клеточной линии ВНК-21 на протяжении 10 пассажей последовательных (срок наблюдения).
Гено- и хемотаксономическая характеристики
Штамм О №2344/Монголия/2017 вируса ящура принадлежит типу О, топотипу ME-SA генетической линии Ind-2001.
Возбудитель является РНК-содержащим вирусом с молекулярной массой 7,6×106Д. Нуклеиновая кислота представлена одноцепочной линейной молекулой молекулярной массой 2,8×106 Д. Вирион имеет белковую оболочку, состоящую из четырех основных белков VP1, VP2, VP3 и VP4. Липопротеидная оболочка отсутствует.
Основным антигенным белком является VP1. В вирионе содержится приблизительно 31,5% РНК и 68,5% белка. Вирионная РНК является инфекционной и участвует в образовании белков-предшественников в инфицированных клетках. Предшественники, в свою очередь, расщепляются с образованием более стабильных структурных и неструктурных полипептидов вируса. Из 8 неструктурных полипептидов, накапливающихся в инфицированных клетках, один (VP66a) является РНК-зависимой РНК-полимеразой, участвующей в репликации РНК новых вирионов.
Физические свойства
Масса вириона составляет 8,4×1018 г. Константа седиментации - 146S. Плавучая плотность в градиенте сахарозы - 1,45 г/см3.
Устойчивость к внешним факторам
Штамм вируса ящура О №2344/Монголия/2017 устойчив к эфиру, хлороформу, фреону, ацетону и другим органическим растворителям и детергентам. Наиболее стабилен при рН 7,4-7,6. Сдвиги показателя кислотности как в кислую, так и в щелочную сторону ведут к инактивации вируса. Чувствителен к формальдегиду, УФ-облучению, γ-облучению, воздействию высоких температур.
Дополнительные признаки и свойства
Реактогенность - реактогенными свойствами не обладает.
Патогенность - патогенен для парнокопытных животных, новорожденных мышат, морских свинок.
Вирулентность - вирулентен для естественно-восприимчивых животных при контактном, аэрозольном и парентеральном заражении.
Стабильность - сохраняет исходные биологические свойства при пассировании в чувствительных биологических системах в течение 3 пассажей на перевиваемой культуре клеток IB-RS-2 (срок наблюдения).
При испытании было проведено 3 последовательных пассажей штамма вируса ящура О №2344/Монголия/2017 в перевиваемой культуре клеток IB-RS-2. Для определения биологической активности проводили титрование вируса каждого пассажа в перевиваемой культуре клеток IB-RS-2.
Исходя из полученных данных, можно утверждать, что штамм О №2344/Монголия/2017 по антигенному и иммунологическому спектрам является оригинальным, в таксономическом отношении новым, ранее неизвестным вариантом вируса ящура типа О, обладает более высокой протективной и иммуногенной активностью.
Для снижения эпизоотической опасности ящура типа О и предотвращения возникновения новых очагов болезни важна своевременная вакцинопрофилактика, что требует разработки высокоиммуногенной вакцины.
Получена высокоиммуногенная инактивированная эмульсионная вакцина для ранней защиты против ящура типа О из штамма О №2344/Монголия/2017.
Сущность предлагаемого изобретения пояснена примерами его использования, которые не ограничивают объем изобретения.
Пример 1. Получение и исследование биологических свойств штамма О №2344/Монголия/2017 вируса ящура.
Штамм О №2344/Монголия/2017 вируса ящура типа О был изолирован из полевого материала, поступившего в ФГБУ «ВНИИЗЖ» в виде эпителия афт от КРС, подозреваемых в заболевании ящуром, при проведении лабораторной диагностики этого заболевания и дифференциации его от других везикулярных болезней. С целью проведения изоляции вируса использован комплекс биологических, вирусологических и биохимических методов.
Биологические и вирусологические методы включали выделение вируса в культуре первично-трипсинизированных клеток свиной почки (СП), перевиваемых линиях клеток ПСГК-30, IB-RS-2 с последующей адаптацией в течение 3 последовательных пассажей (таблица 2). Для постановки биопробы в первичных и перевиваемых культурах клеток их выращивали на соответствующих питательных средах, в стационарных условиях во флаконах с площадью поверхности 25 см2, отмывали от ростовой среды и заражали 10% суспензией афтозного материала (множественность заражения составляла 1-10 ТЦД50/клетка), приготовленной в растворе Хенкса с 0,5% гидролизата лактальбумина (ГЛА) и антибиотиками по стандартной рецептуре. Для удаления микрофлоры и балластных клеточных компонентов суспензию обрабатывали 10% хлороформа. После инкубации при температуре 37±1°С в течение 0,5 часа во флаконы вносили по 5 см поддерживающей среды и инкубировали при температуре 37±1°С до появления цитопатического действия (ЦПД) вируса, характеризующегося округлением клеток, дегенерацией и отделением клеток от стекла, повышением оптической плотности суспензии в видимом спектре света. После развития ЦПД флаконы подвергали процессу замораживания-оттаивания, очистке клеточной взвеси хлороформом и центрифугированию при 3000 об/мин (1200 g) в течение 0,25 ч. Полученный вирусосодержащий материал использовали для последующих пассажей и исследования в РСК для детекции вирусного антигена, при этом использовали коммерческие типоспецифические сыворотки, хранящихся в музее штаммов ФГБУ «ВНИИЗЖ». Возбудитель ящура считали адаптированным к культурам клеток, если в течение 18-24 часов клеточный монослой деструктировал под влиянием вируса на 90-100%.
Вирус, адаптированный к культуре клеток IB-RS-2, использовали для получения антигена для РСК.
Вирус, адаптированный к культуре клеток ПСГК-30, был использован для заражения суспензии клеток ВНК-21 с целью получения антигена для изготовления экспериментальной серии вакцины, а также для гипериммунизации морских свинок.
Результаты исследований представлены в таблице 3, данные которой свидетельствуют о высокой адаптационной активности штамма О №2344/Монголия/2017 вируса ящура типа О к использованным клеточным культурам.
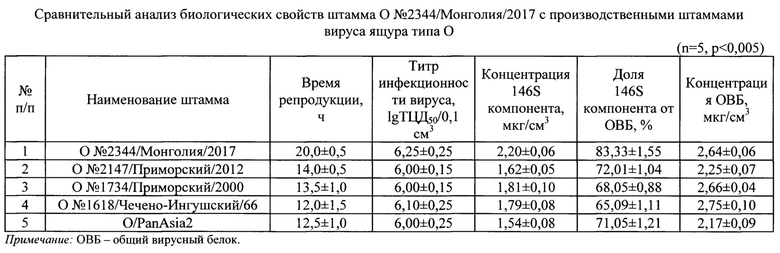
Пример 2. Сравнительный анализ биологических свойств штамма О №2344/Монголия/2017 с производственными штаммами вируса ящура типа О.
При изучении свойств штамма О №2344/Монголия/2017 вируса ящура выявлены значительные преимущества в сравнении с другими используемыми производственными штаммами О №2344/Монголия/2017, О №2147/Приморский/2012, О №1734/Приморский/2000, О №1618/Чечено-Ингушский/66, O/PanAsia2. В качестве тест-системы для заражения использовали суспензию клеток линии ВНК-21 с концентрацией 3,0-3,5 млн клеток/см3. Доза заражения составляла 0,005 ТЦД50/клетка.
В таблице 4 приведены результаты культивирования вируса ящура штаммов представленных штаммов из которой следует, что разрушение клеток ВНК-21 до 90-95% у штамма О №2344/Монголия/2017 наступает спустя 20,0±0,5 ч, при этом для штаммов О №2147/Приморский/2012, О №1734/Приморский/2000, О №1618/Чечено-Ингушский/66 и O/PanAsia2 это время снижено до 14,0±0,5, 13,5±1,0, 12,0±1,5, 12,5±1,0 ч, соответственно. При этом результаты репродукции вируса ящура указанных штаммов свидетельствуют о преимуществах О №2344/Монголия/2017, поскольку для него характерны более высокие значения титра инфекционной активности (6,25±0,25 lg ТЦД50/0,1 см3) по сравнению со штаммами О №2147/Приморский/2012, О №1734/Приморский/2000, О №1618/Чечено-Ингушский/66, O/PanAsia2 для которых значения титра инфекционности соответствовали показаниям 6,00±0,15, 6,00±0,15, 6,10±0,25, 6,00±0,25 lg ТЦД50/0,1 см3. По итогам сравнительного анализа выявлено, что накопление 146S иммуногенного компонента для полученного штамма О №2344/Монголия/2017 составляла 2,20±0,06 мкг/см3, что на 35,8, 21,55, 22,91, 42,86% выше по сравнению с репродукцией штаммов О №2147/Приморский/2012, О №1734/Приморский/2000, О №1618/Чечено-Ингушский/66, O/PanAsia2, соответственно. Следует также отметить, что при культивировании штамма О №2344/Монголия/2017 массовая доля 146S компонента от содержания общего вирусного белка составляет 83,33±1,55%, что на 11,32, 15,28, 18,24, 12,28% выше по сравнению со средними данными для штаммов О №2147/Приморский/2012, О №1734/Приморский/2000, О №1618/Чечено-Ингушский/66, O/PanAsia2, соответственно.
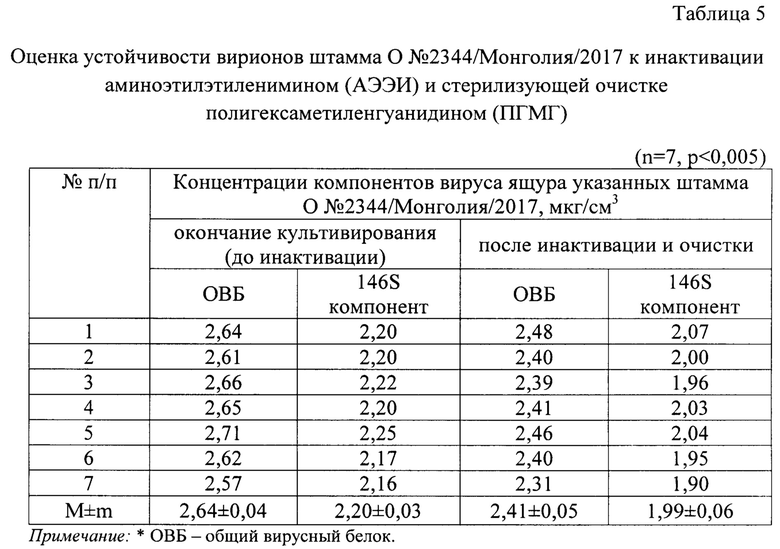
Пример 3. Получение инактивированного антигена и исследование влияния инактивации и очистки антигенного материала с помощью АЭЭИ и ПГМГ на количество 146S компонента вируса ящура штамма О №2344/Монголия/2017.
Инактивированную эмульсионную вакцину для ранней защиты против ящура типа О готовят из штамма О №2344/Монголия/2017 вируса ящура, выращенного в суспензионной перевиваемой клеточной линии ВНК-21. В качестве поддерживающей среды используют раствор Эрла без сыворотки с добавлением ФГМС, ГБКС и антибиотиков при рН среды 7,4-7,6. Культуру клеток заражают вирусом из расчета 0,005-0,100 ТЦД50/клетка.
Культивирование вируса осуществляют при температуре 35-37°С. Через 6-7 часов инкубирования оценивают концентрацию живых и мертвых клеток при их окрашивании трипановым синим. Если количество живых клеток составляет 15-20%, то экспозицию с вирусом продолжают еще 2-4 часа. При достижении цитопатического действия около 85-95% репродукцию вируса ящура прекращают, а полученную суспензию контролируют на стерильность и содержание 146S компонента. Концентрация 146S компонента вируса ящура в суспензии должна составлять не менее 0,5 мкг/см3. Сразу по окончании цикла репродукции вируса, не прекращая процесса термостатирования, в вируссодержащую суспензию добавляют 15-20%-ный раствор АЭЭИ, подкисленный ледяной уксусной кислотой до рН 8,2-8,5. Конечная концентрация АЭЭИ в вируссодержащей суспензии должна составлять 0,025-0,050%. Инактивацию инфекционности вируса проводят в течение 12 часов при температуре 36-37°С и рН 7,2-7,6 с перемешиванием через 5-6 часов в течение 3-5 минут. Для флокуляции балластных примесей и инактивации возможных контаминантов в теплую суспензию вносят 10%-ный раствор ПГМГ до концентрации 0,005-0,007%. Флокулированные балластные примеси подвергают седиментации с последующей декантацией.
Результаты исследований по изучению влияния инактивации и очистки антигенного материала с помощью АЭЭИ и ПГМГ на количество 146S компонента вируса ящура штамма О №2344/Монголия/2017 отражены в таблице 5. Из данных таблицы 5 видно, что до инактивации среднее значение концентрации общего вирусного белка составило 2,64±0,04 мкг/см3, 146S компонента - 2,20±0,03 мкг/см3. После процесса инактивации средние показатели снизились на 87,96-94,09%) и составили для общего вирусного белка 2,41±0,05 мкг/см3, для 146S компонента (вирионов) - 1,99±0,06 мкг/см. Таким образом, 146S иммуногенный компонент штамма О №2344/Монголия/2017 вируса ящура устойчив к инактивации и очистке.
Пример 4. Концентрирование антигена вируса ящура штамма О №2344/Монголия/2017 для получения вакцины.
Необходимую концентрацию 146S компонентов в прививной дозе эмульсионной вакцины из штамма О №2344/Монголия/2017 получают путем концентрирования антигена проточной ультрафильтрацией с применением ультрафильтров при давлением 1,5 атм. Полученный концентрат антигена хранят при температуре 4-6°С до момента использования. Получаемую вакцину расфасовывают в стеклянные или пластиковые флаконы и проводят контроль стерильности продукции в соответствии с ГОСТ 28085-89.
Пример 5. Процесс диспергирования антигена и адъюванта для получения инактивированной эмульсионной вакцины против ящура из штамма О №2344/Монголия/2017.
Инактивированную эмульсионную вакцину для ранней защиты против ящура типа О получают путем диспергирования на коллоидных мельницах концентрата антигена и масляного адъюванта. В качестве адъюванта применяют Montanide ISA-206 производства фирмы «Seppic» (Франция, стандарт ИСО 9001).
При изготовлении эмульсионной вакцины на основе Montanide ISA-206 адъювант и антиген подогревают до температуры 25-30°С и на гомогенизаторе проводят их диспергирование в соотношении 1:1.
В результате получают вакцину инактивированную эмульсионную против ящура из производственного штамма О №2344/Монголия/2017, которая представляет собой молокоподобную жидкость, нерастворимую в воде. Вакцина имеет жидкую консистенцию, легко рассасывается в месте введения, не вызывает образования абсцессов, общей реакции в виде повышения температуры. Обладает выраженной иммуногенной активностью для КРС и свиней в прививной дозе 2 см3 через 21 день после введения. В 1 см3 должно содержаться не менее 3 мкг 146S компонента вируса ящура. Оптимальный компонентный состав полученной вакцины представлен на странице 9.
Пример 6. Оценка авирулентности и безвредности инактивированной эмульсионной вакцины против ящура из штамма О №2344/Монголия/2017.
Для определения авирулентности вакцины на свиньях отобранную пробу вакцинного препарата вводили внутрикожно по 0,1 см3 в две точки венчика на каждой конечности. В исследовании использовали свиней массой 35-40 кг. В течение 10 суток наблюдения животные остались клинически здоровыми, и при патологоанатомическом исследовании не было обнаружено изменений, характерных для ящура. Это свидетельствовало об отсутствии вирулентных свойств разработанной вакцины.
Контроль безвредности продукта на свиньях проводили путем внутримышечного введения вакцины в область верхней трети шеи в дозе 6 см3. Срок наблюдения также составлял 10 суток. Следует отметить, что после инокуляции температура тела животного может повышаться до 41°С и удерживаться на этом уровне в течение 1-3 суток.
По результатам исследований вакцина была признана безвредной, все животные в период наблюдения оставались клинически здоровыми, при патологоанатомическом анализе некроза тканей на месте введения вакцины не обнаружено.
Пример 7. Оценка гуморального иммунитета у свиней при использовании противоящурной вакцины из штамма О №2344/Монголия/2017 против гомологичного штамма и гетерологичных штаммов O/PanAsia2 и О №2147/Приморский/2012.
Проведена оценка гуморального иммунитета у свиней, привитых инактивированной противоящурной эмульсионной вакциной из штамма О №2344/Монголия/2017 против гомологичного штамма и гетерологичных штаммов O/PanAsia2 и О №2147/Приморский/2012.
Проведены испытания эмульсионной вакцины против ящура типа О, изготовленной так, как описано в примерах 4, 5, 6 и содержащей, мкг в 4 см3:
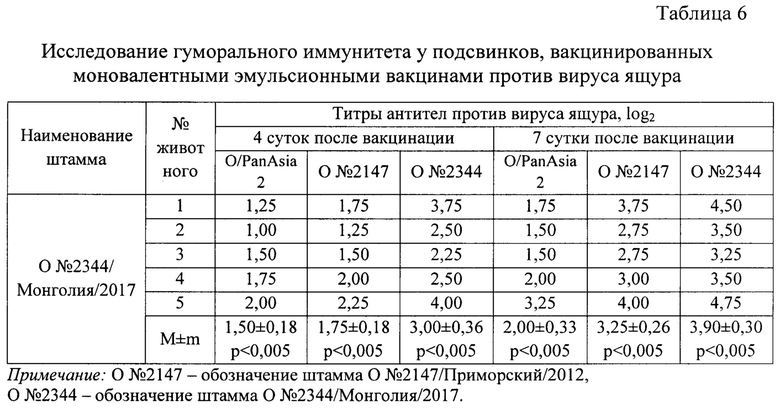
Испытание провели на 5 головах свиней. Эмульсионную вакцину вводили внутримышечно в дозе 4,0 см3. Результаты исследований представлены в таблице 6, из данных которой видно, что эмульсионная вакцина стимулировала у свиней выработку вируснейтрализующих антител (ВНА) против гомологичного штамма О №2344/Монголия/2017 на 4 сутки после вакцинации в количестве 3,00±0,36 log2, против гетерологичных штаммов O/PanAsia2 - 1,50±0,18 log2 и О №2147/Приморский/2012 - 1,75±0,18 log2. На 7 сутки после инокуляции титры антител против гомологичного штамма О №2344/Монголия/2017 составили 3,90±0,30 log2, против гетерологичных штаммов O/PanAsia2 - 2,00±0,33 log2 и О №2147/Приморский/2012 - 3,25±0,26 log2. Разница в титрах вируснейтрализующих антител является существенной и достоверной. Таким образом, моновалентная эмульсионная противоящурная вакцина из штамма О №2344/Монголия/2017 обеспечивает раннюю защиту подсвинков от гомологичного штамма и гетерологичных штаммов O/PanAsia2 и О №2147/Приморский/2012.
Пример 8. Оценка гуморального иммунитета у свиней при использовании противоящурной вакцины из штамма O/PanAsia2 против гомологичного штамма и гетерологичного штамма О №2344/Монголия/2017.
Проведена оценка гуморального иммунитета у свиней на 4 и 7 сутки после вакцинации, привитых инактивированной противоящурной эмульсионной вакциной из штамма O/PanAsia2, против гетерологичного штамма О №2344/Монголия/2017 вируса ящура.
Проведены испытания эмульсионной вакцины против ящура типа О, изготовленной так, как описано в примерах 4, 5, 6 и содержащей, мкг в 4 см3:
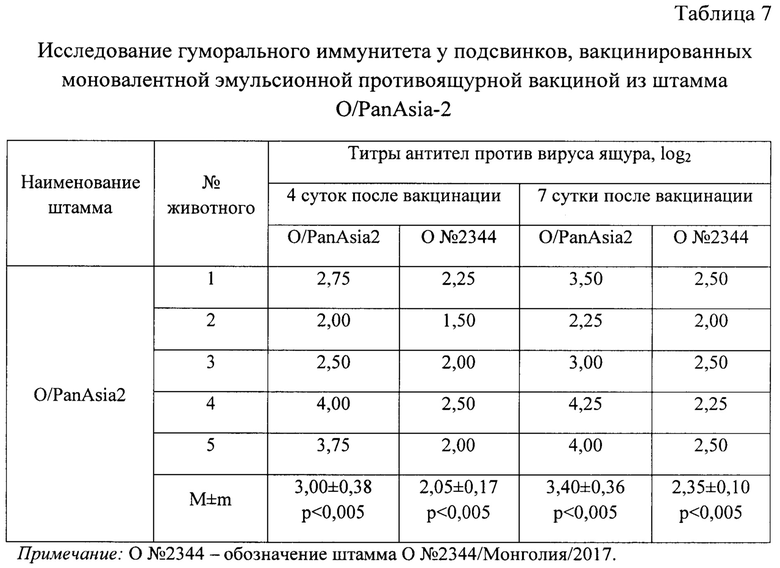
Испытание провели на 5 головах свиней. Эмульсионную вакцину вводили внутримышечно в дозе 4,0 см3. Результаты исследований представлены в таблице 7, из данных которой видно, что эмульсионная вакцина стимулировала у свиней выработку ВНА против гомологичного штамма O/PanAsia2 на 4 сутки после иммунизации в количестве 3,00±0,38 log2, против гетерологичного штамма О №2344/Монголия/2017 - 2,05±0,17 log2. На 7 сутки после инокуляции титры антител против гомологичного вируса ящура O/PanAsia2 соответствовали значению 3,40±0,36 log2, против гетерологичного штамма О №2344/Монголия/2017 - 2,35±0,31 log2. Разница в титрах вируснейтрализующих антител является существенной и достоверной. Из этого следует, что вакцина, изготовленная из производственного штамма O/PanAsia2 не создает гуморальный иммунитет для защиты животных от заражения гетерологичным штаммом вируса ящура О №2344/Монголия/2017.
Пример 9. Оценка гуморального иммунитета у свиней при использовании противоящурной вакцины из штамма
О №2147/Приморский/2012 против гомологичного штамма и гетерологичного штамма О №2344/Монголия/2017.
Проведена оценка гуморального иммунитета у свиней на 4 и 7 сутки после вакцинации, привитых инактивированной противоящурной эмульсионной вакциной из штамма О №2147/Приморский/2012, против гетерологичного штамма О №2344/Монголия/2017 вируса ящура.
Проведены испытания эмульсионной вакцины против ящура типа О, изготовленной так, как описано в примерах 4, 5, 6 и содержащей, мкг в 4 см3:
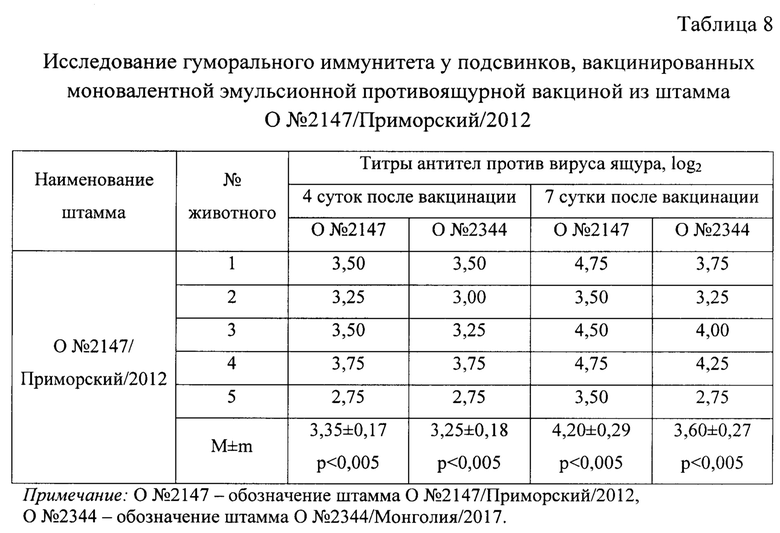
Испытание провели на 5 головах свиней. Эмульсионную вакцину вводили внутримышечно в дозе 4,0 см3. Результаты исследований представлены в таблице 8, из данных которой видно, что эмульсионная вакцина стимулировала у свиней выработку вируснейтрализующих антител против гомологичного штамма О №2147/Приморский/2012 на 4 сутки после иммунизации в количестве 3,35±0,17 log2, против гетерологичного штамма О №2344/Монголия/2017 - 3,25±0,18 log2. На 7 сутки после инокуляции титры антител против гомологичного штамма вируса ящура О №2147/Приморский/2012 составили 4,20±0,29 log2, против гетерологичного штамма О №2344/Монголия/2017 - 3,60±0,27 log2. Разница в титрах вируснейтрализующих антител является существенной и достоверной. Из этого следует, что вакцина, изготовленная из производственного штамма О №2147/Приморский/2017 не создает гуморальный иммунитет для защиты животных от заражения гетерологичным штаммом вируса ящура О №2344/Монголия/2017.
Пример 10. Оценка гуморального иммунитета у КРС при использовании противоящурной вакцины из штамма О №2344/Монголия/2017 против гомологичного штамма и гетерологичных штаммов O/PanAsia2 и О №2147/Приморский/2012.
Проведена оценка гуморального иммунитета у КРС, привитых инактивированной противоящурной эмульсионной вакциной из штамма О №2344/Монголия/2017 против гомологичного штамма и гетерологичных штаммов O/PanAsia2 и О №2147/Приморский/2012.
Проведены испытания эмульсионной вакцины против ящура типа О, изготовленной так, как описано в примерах 4, 5, 6 и содержащей, мкг в 4 см3:
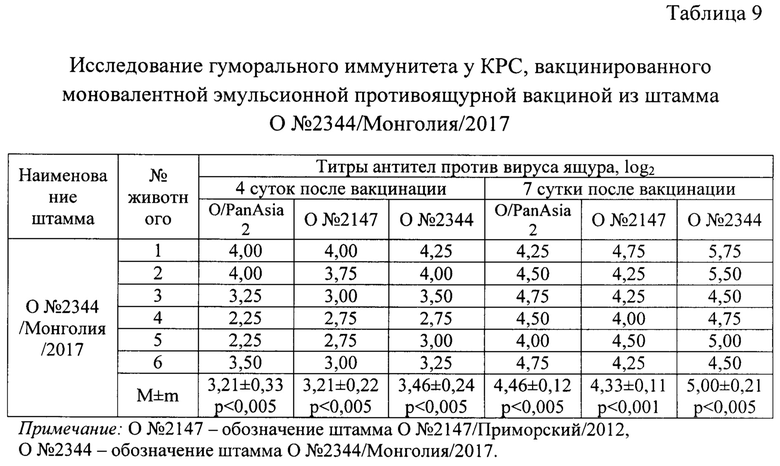
Испытание провели на 6 головах КРС. Эмульсионную вакцину вводили внутримышечно в дозе 4,0 см3. Результаты исследований представлены в таблице 9, из данных которой видно, что эмульсионная вакцина стимулировала у КРС выработку вируснейтрализующих антител против гомологичного штамма О №2344/Монголия/2017 на 4 сутки после вакцинации в количестве 3,46±0,24 log2, против гетерологичных штаммов O/PanAsia2 и О №2147/Приморский/2012 - 3,21±0,33 и 3,21±0,22 log2, соответственно. На 7 сутки после инокуляции титры антител против гомологичного штамма О №2344/Монголия/2017 составили 5,00±0,21 log2, а против гетерологичных штаммов O/PanAsia2 и О №2147/Приморский/2012 - 4,46±0,12 и 4,33±0,11 log2, соответственно. Разница в титрах вируснейтрализующих антител является существенной и достоверной. Иными словами, моновалентная эмульсионная противоящурная вакцина из штамма О №2344/Монголия/2017 обеспечивает раннюю защиту КРС от гомологичного штамма и гетерологичных штаммов O/PanAsia2 и О №2147/Приморский/2012.
Пример 11. Оценка гуморального иммунитета у крупного рогатого скота при использовании противоящурной вакцины из штамма O/PanAsia2 против гомологичного штамма и гетерологичного штамма О №2344/Монголия/2017.
Проведена оценка гуморального иммунитета у КРС на 4 и 7 сутки после вакцинации, привитых инактивированной эмульсионной противоящурной вакциной из штамма O/PanAsia2, против гетерологичного штамма О №2344/Монголия/2017 вируса ящура.
Проведены испытания эмульсионной вакцины против ящура типа О, изготовленной так, как описано в примерах 4, 5, 6 и содержащей, мкг в 4 см3:
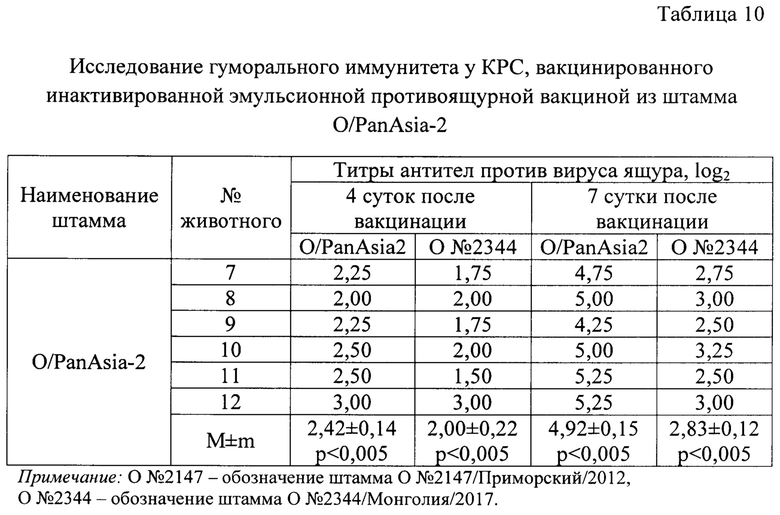
Испытание провели на 6 головах КРС. Эмульсионную вакцину вводили внутримышечно в дозе 4,0 см3. Результаты исследований представлены в таблице 10, из данных которой следует, что полученная вакцина стимулировала у КРС выработку вируснейтрализующих антител против гомологичного штамма O/PanAsia2 на 4 сутки после иммунизации в количестве 2,42±0,14 log2, против гетерологичного штамма О №2344/Монголия/2017 - 2,00±0,22 log2. На 7 сутки после инокуляции титры антител против гомологичного вируса ящура O/PanAsia2 составили 4,92±0,15 log2, против гетерологичного штамма О №2344/Монголия/2017 - 2,83±0,13 log2. Разница в титрах вируснейтрализующих антител является существенной и достоверной. Из этого следует, что инактивированная эмульсионная противоящурная вакцина, изготовленная из производственного штамма O/PanAsia2 не создает гуморальный иммунитет для защиты животных от заражения гетерологичным вирусом ящура О №2344/Монголия/2017.
Пример 12. Оценка гуморального иммунитета у КРС при использовании противоящурной вакцины из штамма О №2147/Приморский/2012 против гомологичного штамма и гетерологичного штамма О №2344/Монголия/2017.
Проведена оценка гуморального иммунитета у КРС на 4 и 7 сутки после вакцинации, привитых инактивированной эмульсионной противоящурной вакциной из штамма О №2147/Приморский/2012, против гетерологичного штамма О №2344/Монголия/2017 вируса ящура.
Проведены испытания эмульсионной вакцины против ящура типа О, изготовленной так, как описано в примерах 4, 5, 6 и содержащей, мкг в 4 см3:
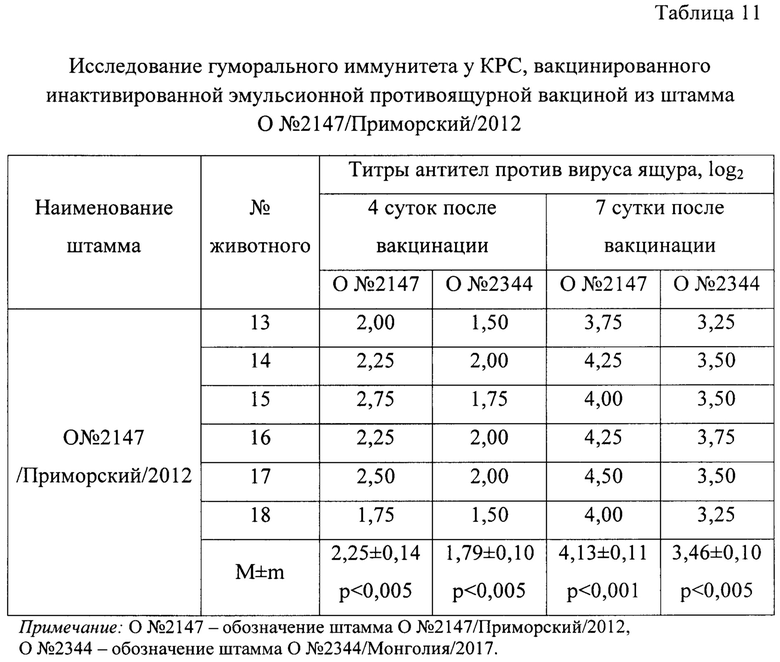
Испытание провели на 6 головах КРС. Эмульсионную вакцину вводили внутримышечно в дозе 4,0 см3. Результаты исследований представлены в таблице 11, из данных которой видно, что инактивированная эмульсионная противоящурная вакцина у свиней стимулировала выработку вируснейтрализующих антител против гомологичного штамма О №2147/Приморский/2012 на 4 сутки после иммунизации в количестве 2,25±0,14 log2, против гетерологичного штамма О №2344/Монголия/2017 - 1,79±0,10 log2. На 7 сутки после инокуляции титры антител составили против гомологичного вируса ящура О №2147/Приморский/2012 - 4,13±0,11 log2, против гетерологичного штамма О №2344/Монголия/2017 - 3,46±0,10 log2. Разница в титрах вируснейтрализующих антител является существенной и достоверной. Иными словами, что вакцина, изготовленная из производственного штамма О №2147/Приморский/2017 не создает гуморальный иммунитет для защиты животных от заражения гетерологичным штаммом вируса ящура О №2344/Монголия/2017.
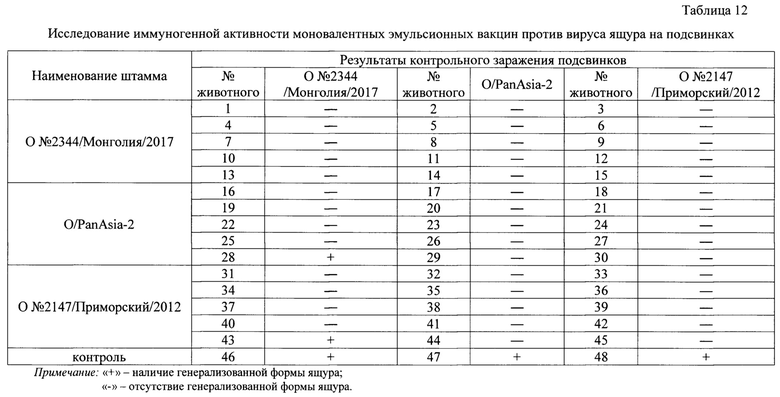
Пример 13. Оценка иммуногенной активности вакцин против ящура из штаммов О №2147/Приморский/2012 и O/PanAsia2 на естественно восприимчивых животных против гетерологичного штамма О №2344/Монголия/2017.
Проведены испытания эмульсионных вакцин против ящура типа О, изготовленной так, как описано в примерах 4, 5, 6 и содержащей, мкг в 4 см3:
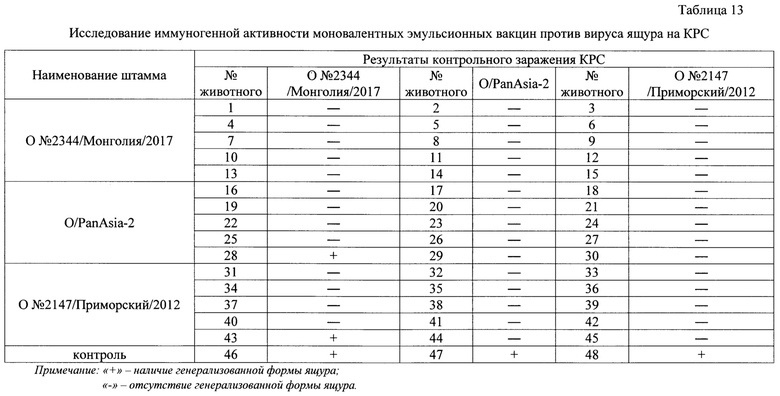
Испытания провели на 48 головах подсвинках и 48 головах КРС результаты исследований указаны в таблицах 12 и 13. Эмульсионные вакцины вводили в дозе 4 см3.
Из данных таблиц 12 и 13 следует, что разработанная инактивированная эмульсионная противоящурная вакцина для ранней защиты из штамма О №2344/Монголия/2017 по итогам контрольного заражения штаммами О №2344/Монголия/2017, O/PanAsia2 и О №2147/Приморский/2012 обеспечивает защиту против гомологичного и гетерологичных штаммов вируса ящура типа О.
Таким образом, приведенная выше информация свидетельствует о том, что вакцина инактивированная эмульсионная против ящура типа О, воплощающая предлагаемое изобретение, предназначена для использования в сельском хозяйстве, а именно в ветеринарной вирусологии и биотехнологии; подтверждена возможность осуществления представленного; вакцина, изготовленная из штамма О №2344/Монголия/2017 в соответствии с предлагаемым изобретением, обладает высокой иммуногенной активностью и способна обеспечить раннюю эффективную защиту восприимчивых животных против эпизоотического штамма вируса ящура типа О, циркулирующего в странах Центральной и Юго-Восточной Азии.
Источники информации, принятые во внимание при составлении описания изобретения к заявке на выдачу патента РФ на изобретение «Вакцина для ранней защиты против ящура типа О эмульсионная инактивированная»:
1. Annual OIE/FAO FMD Reference Laboratory Network Report / N. Ferris, N. Knowles [et al.]. - Pirbright, 2007. - URL: http://www.wrlfmd.org/ref_labs/fmd_ref_lab_reports.htm.
2. OIE. Manual of diagnostic tests and vaccines for terrestrial animals - 24th Ed. -, Paris, 2015 - Vol. 1, Chapter 2.1.5. - P. 166-169.
3. Бурдов A.H., Дудников А.И., Малярец П.В. и др. Ящур. - М.: Агропромиздат, 1990. - 320 с.
4. Пономарев А.П., Узюмов В.Л., Груздев К.Н. Вирус ящура: структура, биологические и физико-химические свойства. - Владимир: Фолиант, 2006. - 250 с.
5. Aspects of emergency vaccination against foot-and-mouth disease / P. Barnett, J.M/ Garland, R.P. Kitching [et.al.] // Comparative Immunology, Microbiology and Infectious Diseases. - October 2002. - V. 25. - P. 345-364.
6. Brown F. A brief history of FMD and its casual agent. FMD: Control Strateies: Proc. Jnt. Symp. 2-5. June 2002, Lyons, France. - Paris, 2003. - p. 13-21.
7. Pepep X. Ящур. - M., 1971. - 432 c.
8. Grubman M.J. Development of novel stategies to control FMD: marker vaccines and antivirals Biologicals. - 2005. - Vol. 33. №4. - P. 227-234.
9. Alexandersen, S., Zhang, Z., Donaldson, A.L. and Garland, A.J.M. (2003) The pathogenesis and diagnosis of foot and mouth disease. J. Compr. Pathol., V. 129. - p. 268-282.
10. Рахманов A.M. Современная эпизоотическая ситуация в мире по ящуру и меры ее контроля.//Ветеринарная медицина мiжвiд. тем. наук. Харкiв, 2013. - С. 37-38.
11. J.S. Salt, P.V. Barnett, P. Dani L. Williams. Emergency vaccination of pigs against foot-and-mouth disease: protection against disease and reduction in contact transmission / Vaccine. - 1998. - V. 16. - P. 746-754.
12. Михалишин Д.В., Лезова Т.Н., Ходакова Н.Н., Борисов А.В., Клюкина Н.Д., Стариков В.А., Михалишин В.В., Балашов А.Н. Динамика развития противоящурного гуморального иммунитета у крупного рогатого скота, иммунизированного трехвалентной сорбированной вакциной типов А, О, Азия-1 // Труды Федерального центра охраны здоровья животных. - Владимир, 2007. - Т. 5. - С. 75-82.
13. Aspects of emergency vaccination against foot-and-mouth disease / P. Barnett, J.M/ Garland, R.P. Kitching [et.al.] // Comparative Immunology, Microbiology and Infectious Diseases. - 2002. - V. 25. - P. 345-364.
14. Horsingtona J., Zhangb Z., Bittnerb H., Holeb K., Singanallura N.В., Alexandersenb S., Vosloo W.. Early protection in sheep against intratypic heterologous challengewith serotype О foot-and-mouth disease virus using high-potency, emergency vaccine // Vaccine. - 2015. - V.35. - P. 422-429.
15. Спирин В.К. Иммунобиологические свойства эпизоотического штамма вируса ящура типа О №1734 Приморский/2000 / В.К. Спирин, А.И. Егорова, С.Р. Кременчугская [и др.] // Тр. Федерального центра охраны здоровья ж-ных. - Владимир. - 2007. - Т. 5. - С. 52-58.
16. Фомина Т.А. Иммунобиологические свойства эпизоотического штамма вируса ящура типа О №1964/Монголия/2004 / Т.А. Фомина, В.К. Спирин, А.И. Егорова [и др.] // Труды Федерального центра охраны здоровья животных. - Владимир. - 2005. - Т. 3. - С. 94-104.


| название | год | авторы | номер документа |
|---|---|---|---|
| Вакцина инактивированная эмульсионная против ящура типа О | 2017 |
|
RU2665849C1 |
| Вакцина инактивированная эмульсионная против ящура типа О | 2017 |
|
RU2682876C1 |
| Штамм О N 2212/Приморский/2014 вируса ящура Aphtae epizooticae типа О для контроля антигенной и иммуногенной активности противоящурных вакцин и для изготовления биопрепаратов для диагностики и специфической профилактики ящура типа О | 2016 |
|
RU2650768C1 |
| Вакцина против ящура генотипа O/SEA/Mya-98 из штамма "О N2383/Приморский/2019" культуральная инактивированная эмульсионная | 2023 |
|
RU2804803C1 |
| ШТАММ О №2102/Забайкальский/2010 ВИРУСА ЯЩУРА Aphtae epizooticae ТИПА О ДЛЯ КОНТРОЛЯ АНТИГЕННОЙ И ИММУНОГЕННОЙ АКТИВНОСТИ ПРОТИВОЯЩУРНЫХ ВАКЦИН И ДЛЯ ИЗГОТОВЛЕНИЯ БИОПРЕПАРАТОВ ДЛЯ ДИАГНОСТИКИ И СПЕЦИФИЧЕСКОЙ ПРОФИЛАКТИКИ ЯЩУРА ТИПА О | 2014 |
|
RU2563522C1 |
| Вакцина против ящура генотипа О/ЕА-3 из штамма "О N2241/Эфиопия/2011" культуральная инактивированная эмульсионная | 2023 |
|
RU2816264C1 |
| Вакцина для ранней защиты против ящура типа Азия-1 инактивированная эмульсионная | 2020 |
|
RU2741639C1 |
| Вакцина против ящура серотипа О из штамма «O/ARRIAH/Mya-98» культуральная инактивированная эмульсионная | 2023 |
|
RU2816944C1 |
| Штамм О N 2311/Забайкальский/2016 вируса ящура Aphtae epizooticae типа О для изготовления биопрепаратов для диагностики и специфической профилактики ящура типа О | 2017 |
|
RU2658608C1 |
| Вакцина против ящура генотипа O/ME-SA/Ind-2001e из штамма "О N2620/Оренбургский/2021" культуральная инактивированная эмульсионная | 2023 |
|
RU2815537C1 |

Изобретение относится к области ветеринарной вирусологии и биотехнологии и представляет собой вакцину для ранней защиты против ящура типа О инактивированная эмульсионная, содержащая активное вещество и адъюванты, отличающаяся тем, что в качестве активного вещества она содержит авирулентный и очищенный антигенный материал из штамма вируса Aphtae epizooticae «О №2344/Монголия/2017», сем. Picornaviridae, рода Aphtovirus, типа О, депонированного в Коллекцию штаммов микроорганизмов ФГБУ «Федеральный центр охраны здоровья животных» (ФГБУ «ВНИИЗЖ»), под регистрационным номером: №116 - деп / 19-6 - КШМ ФГБУ «ВНИИЗЖ», в эффективном количестве. Изобретение обеспечивает высокую иммуногенность и способность обеспечить раннюю эффективную защиту от гомологичного возбудителя инфекции, циркулирующего в странах Центральной и Юго-Восточной Азии. 6 з.п. ф-лы, 1 ил., 13 табл., 13 пр.
1. Вакцина для ранней защиты против ящура типа О инактивированная эмульсионная, содержащая активное вещество и адъюванты, отличающаяся тем, что в качестве активного вещества она содержит авирулентный и очищенный антигенный материал из штамма вируса Aphtae epizooticae «О №2344/Монголия/2017», сем. Picornaviridae, рода Aphtovirus, типа О, депонированного в Коллекцию штаммов микроорганизмов ФГБУ «Федеральный центр охраны здоровья животных» (ФГБУ «ВНИИЗЖ»), под регистрационным номером: №116 - деп / 19-6 - КШМ ФГБУ «ВНИИЗЖ», в эффективном количестве.
2. Вакцина по п. 1, отличающаяся тем, что она содержит авирулентный и очищенный антигенный материал из гомологичного возбудителю инфекции штамма О №2344/Монголия/2017, полученный в чувствительной биологической системе и представляющий собой суспензию, содержащую преимущественно 146S иммуногенный компонент вируса ящура типа О.
3. Вакцина по п. 2, отличающаяся тем, что она содержит авирулентный и очищенный антигенный материал из гомологичного возбудителю инфекции штамма О №2344/Монголия/2017, полученный предпочтительно в перевиваемой культуре клеток ВНК-21 и представляющий собой суспензию, содержащую преимущественно 146S иммуногенный компонент вируса ящура типа О.
4. Вакцина по п. 3, отличающаяся тем, что она содержит авирулентный и очищенный антигенный материал из гомологичного возбудителю инфекции штамма О №2344/Монголия/2017, полученный предпочтительно в перевиваемой культуре клеток ВНК-21 и представляющий собой суспензию, содержащую преимущественно 146S иммуногенный компонент вируса ящура типа О в количестве не менее 3,0 мкг в 1 см3 готового препарата.
5. Вакцина по п. 1, отличающаяся тем, что в качестве адъюванта она содержит масляный адъювант Montanide ISA-206.
6. Вакцина по п. 5, отличающаяся тем, что она содержит масляный адъювант Montanide ISA-206 предпочтительно в количестве 500000,0-575000,0 мкг в 1 см3 готового препарата.
7. Вакцина по любому из пп. 1-6, отличающаяся тем, что она содержит авирулентный и очищенный антигенный материал из гомологичного возбудителю инфекции штамма О №2344/Монголия/2017, полученный предпочтительно в перевиваемой культуре клеток ВНК-21 и представляющий собой суспензию, содержащую преимущественно 146S иммуногенный компонент вируса ящура типа О, масляный адъювант Montanide ISA-206 в соотношении, мкг 1 см3 готового препарата:
| ВАКЦИНА ИНАКТИВИРОВАННАЯ ЭМУЛЬСИОННАЯ ПРОТИВ ЯЩУРА ТИПОВ А, О, АЗИЯ-1 | 2015 |
|
RU2593718C1 |
| Вакцина инактивированная эмульсионная против ящура типа О | 2017 |
|
RU2665849C1 |
| Вакцина инактивированная эмульсионная против ящура типа О | 2017 |
|
RU2682876C1 |
| CN 1966079 A, 23.05.2007 | |||
| US 4508708 A1, 02.04.1985 | |||
| CN 107266537 A, 20.10.2017. | |||
Авторы
Даты
2019-09-09—Публикация
2019-05-31—Подача