Изобретение относится к медицине, а именно к урологии, и может быть применимо для хирургического лечения болезни Пейрони у пациентов с искривлением полового члена.
Болезнь Пейрони (БП), или фибропластическая индурация полового члена - это заболевание, при котором в белочной оболочке полового члена возникают фибропластические бляшки, нарушающие ее эластичность и приводящие к деформации полового члена (ПЧ) во время эрекции. Клинические проявления БП представлены болью, деформацией, искривлением ПЧ при эрекции и наличием зон уплотнения белочной оболочки и межкавернозной перегородки, определяющихся при пальпации (Москалева Ю.С., Остапченко А.Ю., 2015). Частым осложнением БП становится эректильная дисфункция (ЭД), которая развивается как следствие непосредственной деформации ПЧ, делающей невозможным половой акт, так и по психологической причине, связанной с искривлением. Это значительно снижает качество жизни таких пациентов.
Частоту БП среди всех взрослых мужчин оценивают в диапазоне от 3 до 8% (Sommer F., Schwarzer U., Wassmer С, et al. 2002; La Pera G., Pescatori E.S., Calabrese M. et al. 2001; Щеплев П.А., Данилов И.А., Колотинский А.Б. и др. 2007). Показаниями к оперативному лечению являются искривление ПЧ, препятствующее коитусу, угол искривления более 45 градусов, наличие бляшек больших размеров, приводящих к девиации ПЧ.
Оперативные вмешательства при БП можно разделить на два вида: операции, укорачивающие ПЧ, и операции, удлиняющие его. Устранить искривление ПЧ без его укорочения позволяют пластические операции: заместительная корпоропластика или графтинг, когда дефект белочной оболочки после иссечения бляшки закрывают трансплантатом-графтом (Москалева Ю.С., Корнеев И.А. 2017; Королева С.В., Ковалев В.А., Лещев Н.В. и соавт., 2005; Carson СС, 1998). Графт (от англ. Graft - трансплантат), подразумевающий любой орган, ткань или часть тела, используемые для трансплантации (пересадки) с целью замены поврежденной части тела (https://dic.academic.ru/dic.nsf/medic/7581).
Процесс приживления графта продолжается около 96 часов и в данный промежуток времени происходит истинное восстановление его микроциркуляции. Процесс приживления связан как с природой ткани графта, так и с состоянием ложа, и обусловлен васкуляризацией последнего (Беломытцев С.В., 2012).
В качестве аутографтов используют аутовену, белочную или влагалищную оболочку яичка, слизистую щеки, фасциальный или кожный лоскут. К аллографтам относят трупный перикард, трупную широкую фасцию, трупную твердую мозговую оболочку. Ксенографтами могут быть подслизистая основа тонкой кишки свиньи, бычий перикард (ксеноперикард), дерма свиньи. Синтетические трансплантаты представлены гортексом, даксоном, силастиком (Калинина С.Н. и соавт., 2018).
Как и в любой хирургической практике, проблема минимизации хирургических осложнений является актуальной и для БП. Более того, профилактика осложнений в реконструктивной хирургии ПЧ является залогом успеха не только самого оперативного вмешательства, но и дальнейшей социально-психологической адаптации пациента, спокойствия его близких и окружающих, в том числе и врача.
Актуальным является поиск методик профилактики осложнений корпоропластики буккальным лоскутом, в частности аневризматического расширения белочной оболочки в области установки графта (так называемого грыжевого выпячивание). Данное осложнение изменяет геометрию ПЧ, создает психологический дискомфорт у пациента, что в дальнейшем приводит к возникновению или усугублению ЭД.
Из существующего уровня техники известен способ хирургического лечения БП (Патент РФ №2376943 от 27.12.2009), включающий разрез по венечной борозде ПЧ, мобилизацию покровных тканей к его основанию, иссечение фиброзной бляшки в пределах здоровых тканей, забор мышечного трансплантата с последующим закрытием им дефекта белочной оболочки и наложением шва на рану ПЧ, отличающийся тем, что после разреза по венечной борозде ПЧ и мобилизации покровных тканей к его основанию мобилизуют дорсальный сосудисто-нервный пучок ПЧ, через срединный разрез по передней брюшной стенке выполняют забор правой порции прямой мышцы живота с фрагментом ее влагалища на питающих сосудах, перемещают фрагмент мышцы под кожу полового члена, выполняют пластику дефекта белочной оболочки фрагментом прямой мышцы живота таким образом, что фрагмент фасции фиксируют к краям дефекта белочной оболочки, а мышцу - к латеральным поверхностям ПЧ с одной и другой стороны.
Недостатком данного технического решения является травматичность методики забора трансплантата, а также выполнение полного иссечения фиброзной бляшки, что повышает риск развития ЭД.
Известен способ корпоропластики при БП (Патент РФ №2640770 от 11.01.2018), заключающийся в устранении пенильной девиации путем удаления бляшки с пластикой образовавшегося дефекта, отличающийся тем, что бляшка удаляется по границе здоровой ткани, а образовавшийся дефект белочной оболочки укрывают моделированным графтом из децеллюляризированной артерии.
Недостатком данного способа является полное иссечение фиброзной бляшки, а также использование в качестве графта децеллюляризированной артерии, что имеет значительные риски при его заборе, необходимость привлечения к операции сосудистого хирурга, невозможность использования данного способа при больших дефектах белочной оболочки ввиду ограниченности материала и тонкости стенки данного графта.
Щеплев П.А. предложил замещать белочную оболочку фрагментом широчайшей фасции бедра (Щеплев П.А. / Реконструктивная и эстетическая хирургия полового члена: Дисс. и автореф. дис…др. мед. наук. М.: 1996).
Недостатком метода является необходимость дополнительных разрезов при заборе фасции бедра, травматичность и техническая сложность забора графта.
Наиболее близким к предлагаемому техническому решению является способ хирургического лечения БП (Патент РФ №2460473 от 10.09.2012), включающий скелетирование ПЧ, выделение участка фиброза белочной оболочки, иссечение его в пределах здоровой ткани и закрытие дефекта трансплантатом методом ротации кожного лоскута крайней плоти, отличающийся тем, что перед операцией предварительно вводят под листки крайней плоти 0,5%-ный раствор метиленового синего с новокаином в половинном разведении в объеме по 0,5 мл в обе латеральные зоны ПЧ, затем выкраивают два лоскута крайней плоти на сосудистой ножке, производят их деэпителизацию и встречную ротацию в сторону дефекта, листки проводят под сосудисто-нервным пучком, сшивают их между собой, замещая полученный дефект белочной оболочки, перемещенные листки фиксируют к кавернозным телам, швы накладывают в шахматном порядке.
Недостатком данного способа является необходимость полного иссечения фиброзной бляшки, а также использование в качестве графта кожного лоскута, который имеет наибольший риск сморщивания среди трансплантатов, что зачастую приводит к рецидиву искривления ПЧ.
Указанные недостатки прототипа устраняются в заявляемом техническом решении.
Задачей, на решение которой направлено заявляемое изобретение, является разработка более эффективного метода реконструкции дефекта белочной оболочки после ее рассечения и профилактики ее аневризматического расширения, так как при значительных деформациях полового члена при иссечении фиброзной ткани обычно создается большой дефект белочной оболочки.
Данная задача решается тем, что выкраивают буккальный графт из слизистой рта и вшивают, замещая полученный дефект белочной оболочки по периметру прямоугольника, после фиксации графта воспроизводят искусственную эрекцию, и производят прошивание латеральных краев белочной оболочки шовным материалом биосин 3/0 в поперечном к оси полового члена направлении, швами параллельными друг другу с частотой шага в 5 мм с протягиванием нити поверх графта с захватом ткани графта посередине и фиксацией данных нитей посередине графта; повторно создают искусственную эрекцию и нити затягивают дополнительным узлом до исчезновения аневризматической деформации и выравнивания графта по отношению к белочной оболочке.
Техническим результатом, обеспечиваемым приведенной совокупностью признаков, является профилактика возникновения аневризматической деформации графта (а значит и ПЧ) и снижение количества рецидивов за счет создания каркаса на буккальном графте по типу «гамака» и корректировки его натяжения путем создания искусственной эрекции. Данный каркас создается за счет прошиванием латеральных краев белочной оболочки в направлении перпендикулярно оси полового члена, параллельно друг другу с частотой шага в 5 мм, поверх графта с захватом ткани графта посередине и фиксацией к нему данной нитью. Повторно создают искусственную эрекцию, выявляют аневризматическую деформацию, после чего нити затягивают дополнительным узлом до равномерного выравнивания графта.
За счет этого создается стабилизация графта и тем самым уменьшается вероятность его аневризматической деформации. Созданием искусственной эрекции оценивается выпрямление полового члена в нескольких плоскостях, а также определение герметичности дефекта и оценка степени выпрямления полового члена, наличие и выраженность аневризматической деформации графта.
В связи с тем, что графт из слизистой щеки более эластичен по сравнению с белочной оболочкой ПЧ, при замещении дефекта больших размеров (более 2,5 см) при создании искусственной эрекции может развиваться аневризматическая деформация, что относится к осложнению данного оперативного вмешательства. При наличии значительной аневризматической деформации буккального графта, производится прошивание краев белочной оболочки параллельно друг другу - в направлении перпендикулярном оси ПЧ с захватом участков графта. За счет этого создается стабилизация графта и тем самым уменьшается аневризматическая деформация и, следовательно, визуальная деформация полового члена.
Использование графта слизистой щеки для хирургической коррекции искривления ПЧ является высокоэффективным методом, позволяющим добиться долгосрочных удовлетворительных результатов лечения. Трансплантат слизистой ротовой полости, наиболее простой и доступный материал для реконструктивной урологии, имеет различные многочисленные преимущества, такие как - его постоянное наличие, благоприятные иммунологические свойства, легкость забора, исключительные тканевые характеристики, простоту обработки, минимальное формирование контрактур и адаптация к влажной среде. Важным фактором является обеспечение механизма ангиогенеза и реваскуляризации ткани за счет проникновения кровеносных сосудов и нервных волокон от подслизистой основы в собственную пластинку (Duckett, J. W., 1995). Установлено, что корпоропластика с использованием графта слизистой щеки имеет низкую частоту интра- и послеоперационных осложнений (Юсуфов А.Г., 2018).
Используемый шовный материал биосин 3/0 обеспечивает сохранение примерно 75% прочности узла в первые 2 недели после операции и около 40% прочности сохраняется по истечению 3 недель после имплантации шовного материала. Процесс рассасывания начинается как потеря прочности без потери массы и заканчивается между 90 и 110 днем. Этого периода достаточно для стабилизации графта и возможности принятия им эластических свойств, схожих с белочной оболочкой ПЧ.
Заявляемый способ применим у пациентов с большим дефектом белочной оболочки после рассечения фиброзных бляшек кавернозных тел, где необходимо применение графтов больших размеров, что позволяет исключить осложнения типа аневризматической деформации буккального графта и профилактировать возникновение рецидивов.
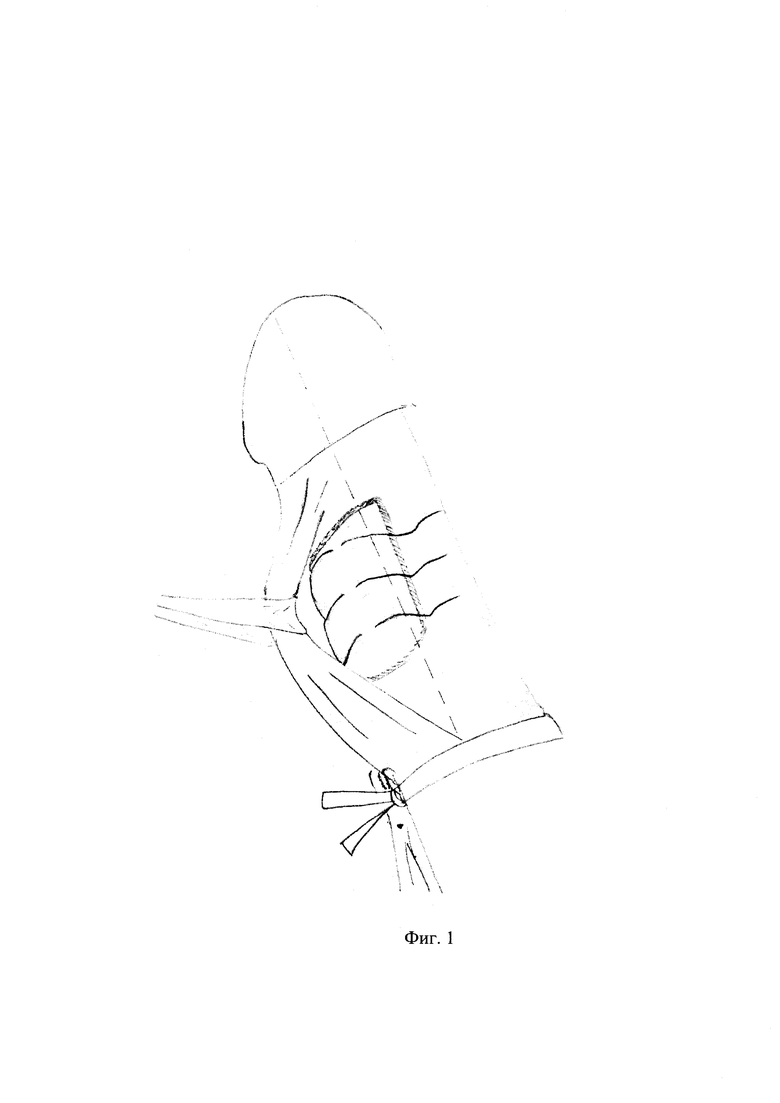
Изобретение иллюстрируется фиг. 1-2, на которых изображены заключительные этапы проведения операции.
Фиг. 1 - наложение параллельных нитей поверх графта перпендикулярно оси полового члена с захватом ткани графта посередине.
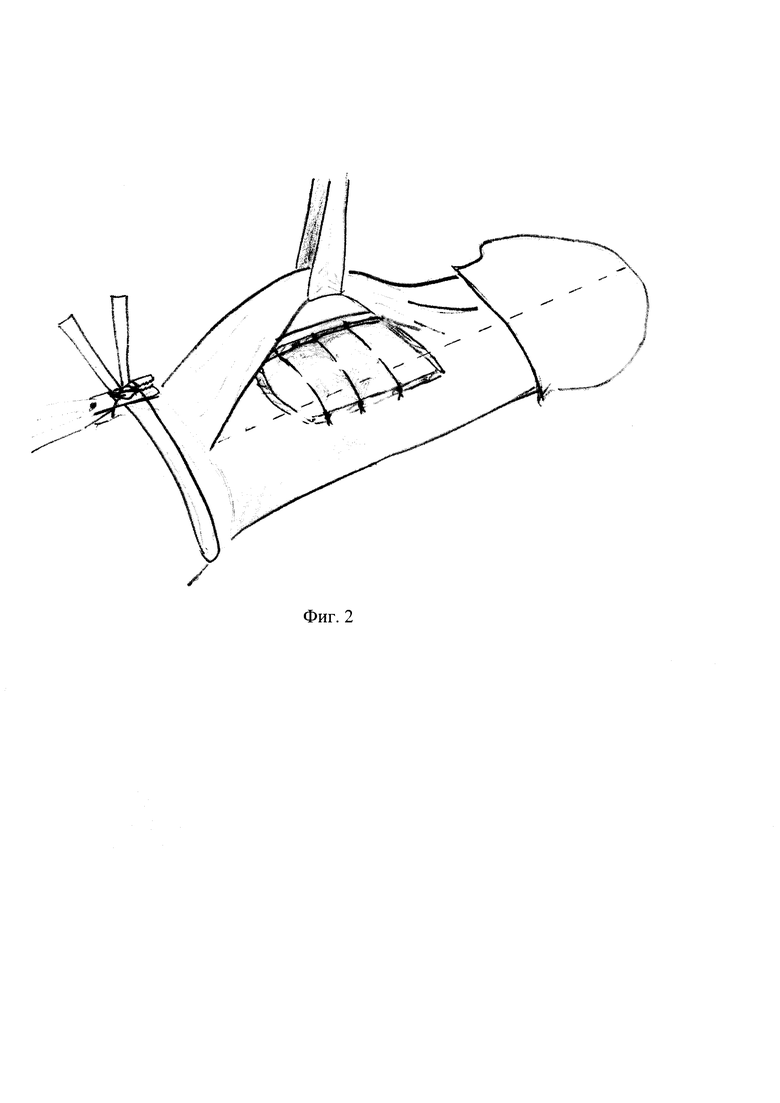
Фиг. 2 - затягивание нитей на графте при создании искусственной эрекции для устранения аневризматической деформации.
Подробное описание способа и примеры его клинического выполнения.
Способ осуществляется следующим образом. Вмешательство выполняется под эндотрахеальной анестезией. После циркумцизии и дегловации (скальпирования) ПЧ выполняется мобилизация дорзального пучка от белочной оболочки. На основание ПЧ накладывается турникет. Дистальнее наложенного турникета в боковую поверхность одного из кавернозных тел полового члена вводится периферический катетер 20G. С помощью шприца вводится стерильный физиологический раствор до достижения полной эрекции. После чего определяют угол искривления и длину полового члена, тем самым планируют линию разреза (инцизии) бляшки, с углами отклонения на боковых концах. Бляшка рассекается поперечно боковым поверхностям кавернозных тел под контролем искусственной эрекции. Производится частичное иссечение грубой фиброзной ткани для возможности прошивания белочной оболочки. Далее проводят тракцию члена и замеряют дефект белочной оболочки.
Следующим этапом получают трансплантант (графт). Производится забор буккального графта из ротовой полости соответствующего размера по общепринятой методике. Границы забора графта должны соответствовать размеру дефекта. Дистальным краем забора является 1,0-1,5 см до небных дужек. После получения графта приступают к его подготовке: тщательно очищают от жировой и мышечной ткани до собственной пластинки.
Третий этап - непосредственно заместительная корпоропластика, целью которого является имплантация и фиксация графта слизистой оболочки щеки. Используют непрерывный шов нитью монокрил 4/0 по периметру прямоугольника, что обеспечивает адекватное герметичное расположение трансплантанта. После фиксации графта повторно вызывают искусственную эрекцию для определения герметичности и оценки степени выпрямления полового члена. С целью предотвращения аневризматической деформации графта, которая изменяет геометрию полового члена, прошивают дополнительно поверх графта латеральные края белочной оболочки в перпендикулярном оси ПЧ направлении шовным материалом биосин 3/0, параллельно друг другу, с частотой шага в 5 мм и протягиванием нитей поверх графта с его прошиванием посередине. Повторно создают искусственную эрекцию и затягивают нити над графтом до полного исчезновения выпячивания, также исключая чрезмерное затягивание нитей. Нити завязывают в натяжении обычными одиночными узлами. Производится восстановление всех слоев полового члена с тщательным гемостазом и наложением тугой фиксирующей повязки.
Работоспособность заявляемого способа подтверждается следующими клиническими примерами.
Пример 1.
Больной Д-н, 49 лет, оперирован 12.03.18. Считает себя больным около двух лет, когда стал отмечать искривление ПЧ. При осмотре: на дорзальной стороне ПЧ проксимально в 10 мм от венечной борозды пальпируется фиброзная бляшка, размерами 2×2 см. Угол искривления по аутофотографическим данным составил 70 градусов. Выполненное физикальное обследование, УЗИ полового члена, что позволило установить следующий диагноз: Болезнь Пейрони, искривление полового члена с сохранной эректильной функцией.
Больному выполнена операция заявляемым способом. Под эндотрахеальной анестезией после циркумцизии и дегловации (скальпирования) ПЧ произведена мобилизация дорзального пучка от белочной оболочки. На основание ПЧ наложен турникет. Дистальнее наложенного турникета в боковую поверхность одного из кавернозных тел ПЧ введен периферический катетер 20G. С помощью шприца выполнено введение стерильного физиологического раствора до достижения полной эрекции. После индуцирования эрекции, мобилизации дорзального пучка определили угол искривления. С помощью маркера разметили линию разреза (инцизии) бляшки. Далее рассекли бляшку с выполнением Y-образных разрезов по краям. Для возможности прошивания выполнено частичное иссечение грубой фиброзной ткани краев бляшки. После тракции ПЧ установлен дефект белочной оболочки кавернозных тел 4,0×2,5 см.
Затем по общепринятой методике произведен забор буккального графта из ротовой полости соответствующего размера.
Далее выполнена заместительная корпоропластика. После фиксации графта и повторного создания искусственной эрекции для определения герметичности и оценки степени выпрямления ПЧ у данного пациента было отмечено наличие аневризматической деформации графта над окружающими тканями на 0,8 см. Аневризматическая деформация ликвидирована путем прошивания семью нитями латеральных краев белочной оболочки в направлении перпендикулярном оси ПЧ, швами параллельными друг другу с частотой шага 5 мм с протягиванием нитей поверх графта и фиксацией к нему данных нитей посередине графта. При выполнении искусственной эрекции в результате корректировки натяжения нитей над графтом, достигнуто сдавление и выравнивание графта по отношению к белочной оболочке.
Затем выполнено восстановление всех слоев полового члена с тщательным гемостазом и наложением тугой фиксирующей повязки.
При контрольном обследовании через 1, 3, 6 и 12 мес. - искривления полового члена, аневризматической деформации графта не выявлено. Пациент находится под динамическим наблюдением.
Пример 2.
Больной С-н, 52 года, оперирован 05.02.19. Искривление ПЧ стал отмечать в течение последнего года. При осмотре - на дорзальной стороне ПЧ, проксимально на 10 мм от венечной борозды, пальпируется фиброзная бляшка, размерами 2×1,5 см. Угол искривления по аутофотографическим данным составил 65 градусов. Выполненное УЗИ полового члена в совокупности с вышеуказанными данными позволило установить следующий диагноз - Болезнь Пейрони, искривление полового члена с сохранной эректильной функцией.
Больному выполнена операция заявляемым способом. Под эндотрахеальной анестезией после циркумцизии и дегловации ПЧ произведена мобилизация дорзального пучка от белочной оболочки. На основание ПЧ наложен турникет. Дистальнее наложенного турникета в боковую поверхность одного из кавернозных тел введен периферический катетер. С помощью шприца выполнено введение стерильного физиологического раствора до достижения полной эрекции. После индуцирования эрекции, мобилизации сосудисто-нервного пучка, определен угол искривления. Далее рассекли бляшку с выполнением продольных разрезов по краям. Для возможности прошивания выполнено частичное иссечение грубой фиброзной ткани краев бляшки. Создавшийся дефект белочной оболочки кавернозных тел составил 4,2×2,0 см. Выполнен забор графта из ротовой полости соответствующего размера.
После вшивания графта повторная искусственная эрекция определила герметичность и отсутствие искривления ПЧ, при этом отмечено значительное аневризматическое выбухание графта, изменяющее геометрию ПЧ. С помощью прошивания дополнительно поверх графта латеральных краев белочной оболочки шовным материалом биосин 3/0, параллельно друг другу, с частотой шага в 5 мм произвели стабилизацию графта. Это выполнено путем прошивания нитями латеральных краев белочной оболочки в направлении перпендикулярном оси ПЧ, швами параллельными друг другу с частотой шага 5 мм протягиванием нитей поверх графта и фиксацией к нему нитей посередине графта. При повторной искусственной эрекции достигнуто сдавление и выравнивание графта по отношению к белочной оболочке, в результате затягивания нитей над графтом. Далее выполнено восстановление всех слоев ПЧ с тщательным гемостазом и наложением тугой фиксирующей повязки.
При контрольном обследовании через 1, 3 мес. - искривления ПЧ, аневризматической деформации графта не выявлено. Пациент находится под наблюдением.
Преимущества заявляемого метода:
- профилактика возникновения аневризматической деформации графта (а значит и ПЧ) и снижение количества рецидивов;
- отсутствие аллергической реакции и отторжения, т.к. при данном методе применяются собственные ткани;
- возможность закрытия больших дефектов белочной оболочки ПЧ, что позволяет применять методику также при удлиняющих пластиках полового члена.
Заявляемый способ оперативного лечения болезни Пейрони, осложненной искривлением ПЧ, апробирован на достаточном клиническом материале, показал эффективность применения и может быть рекомендован к использованию в специализированных хирургических стационарах.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОРПОРОПЛАСТИКИ ПРИ БОЛЕЗНИ ПЕЙРОНИ | 2024 |
|
RU2817956C1 |
| Способ хирургического лечения протяженных стриктур бульбозного отдела уретры у мужчин | 2020 |
|
RU2723744C1 |
| Способ хирургического лечения протяженных стриктур и облитераций мочеточника и лоханочно-мочеточникового сегмента при его туберкулезном поражении | 2019 |
|
RU2711110C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ БОЛЕЗНИ ПЕЙРОНИ | 2010 |
|
RU2460473C2 |
| Способ ксенопластики при хирургическом лечении болезни Пейрони | 2020 |
|
RU2725837C1 |
| Способ хирургического лечения протяженных стриктур средней трети мочеточника с участком облитерации | 2024 |
|
RU2836988C1 |
| СПОСОБ ХИРУРГИЧЕСКОЙ КОРРЕКЦИИ ОРГАНИЧЕСКОЙ ФОРМЫ ЭРЕКТИЛЬНОЙ ДИСФУНКЦИИ, ОБУСЛОВЛЕННОЙ БОЛЕЗНЬЮ ПЕЙРОНИ | 1999 |
|
RU2179827C2 |
| Способ коррекции искривления полового члена с помощью свободного лоскута белочной оболочки яичка | 2023 |
|
RU2836015C1 |
| СПОСОБ КОРПОРОПЛАСТИКИ ПРИ БОЛЕЗНИ ПЕЙРОНИ | 2016 |
|
RU2640770C1 |
| СПОСОБ ХИРУРГИЧЕСКОЙ КОРРЕКЦИИ ЭРЕКТИЛЬНОЙ ДЕФОРМАЦИИ ПРИ БОЛЕЗНИ ПЕЙРОНИ | 2002 |
|
RU2234257C2 |
Изобретение относится к медицине, а именно к урологии, и может быть применимо для лечения болезни Пейрони, осложненной искривлением полового члена. В качестве трасплантата выкраивают буккальный графт из слизистой рта и вшивают, замещая полученный дефект белочной оболочки, по периметру прямоугольника. После фиксации графта воспроизводят искусственную эрекцию, и производят прошивание латеральных краев белочной оболочки шовным материалом биосин 3/0 в поперечном к оси полового члена направлении, швами, параллельными друг другу, с частотой шага в 5 мм, с протягиванием нити поверх графта с захватом ткани графта посередине. Повторно создают искусственную эрекцию и нити затягивают дополнительным узлом до исчезновения аневризматической деформации и выравнивания графта по отношению к белочной оболочке. Способ позволяет уменьшить риск рецидива. 2 ил.
Способ хирургического лечения болезни Пейрони, осложненной искривлением полового члена, включающий выделение участка фиброза белочной оболочки, его рассечение, удаление части фиброзной ткани и закрытие дефекта трансплантатом, отличающийся тем, что в качестве трасплантата выкраивают буккальный графт из слизистой рта и вшивают, замещая полученный дефект белочной оболочки, по периметру прямоугольника, после фиксации графта воспроизводят искусственную эрекцию, и производят прошивание латеральных краев белочной оболочки шовным материалом биосин 3/0 в поперечном к оси полового члена направлении, швами, параллельными друг другу, с частотой шага в 5 мм, с протягиванием нити поверх графта с захватом ткани графта посередине; повторно создают искусственную эрекцию и нити затягивают дополнительным узлом до исчезновения аневризматической деформации и выравнивания графта по отношению к белочной оболочке.
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ БОЛЕЗНИ ПЕЙРОНИ | 2010 |
|
RU2460473C2 |
| Устройство для получения токов низкой частоты методом биений | 1931 |
|
SU27413A1 |
| КАЛИНИНА С.Н | |||
| и др | |||
| Хирургическое лечение болезни Пейрони | |||
| Урологические ведомости, 2018, т.8, N 2, с.24-29 | |||
| GEORGIOS HATZICHRISTODOULOU et al | |||
| Peyronie`s graft surgery - tips and tricks from the masters in andrologic surgery | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
Авторы
Даты
2019-09-30—Публикация
2019-06-17—Подача