Изобретение относится к медицине, а именно к урологии, и может быть использовано для хирургического лечения пациентов с болезнью Пейрони.
Фибропластическая индурация полового члена или болезнь Пейрони (БП) — заболевание, проявляющееся неконтролируемым тканевым фиброзом белочной оболочки полового члена, которое приводит к укорочению полового члена за счѐт искривления и развитию эректильной дисфункции [Оперативные вмешательства при фибропластической индурации полового члена (болезни Пейрони): учебно-методическое пособие / С.В. Котов, А.Г. Юсуфов, М.С. Жилов. — Москва: РНИМУ им. Н.И. Пирогова, 2021. — с.]. Данное заболевание впервые было описано в 1743 году французским хирургом Франсуа Жиго де Ла Пейрони, однако, спустя более 280 лет фибропластическая индурация полового члена (ПЧ) остается актуальной проблемой в реконструктивной урологии.
По данным различных авторов встречаемость БП составляет от 0,4 до 20,3% [Eric Chung, Michael Gillman, Derren Rushton, Chris Love, Darren Katz. Prevalence of penile curvature: a population-based cross-sectional study in metropolitan and rural cities in Australia. BJU Int, 2018. 122 Suppl 5: 42. https://pubmed.ncbi.nlm.nih.gov/30387224/]. Современная научная литература указывает на заметные различия в частоте БП в зависимости от страны происхождения. Сообщается, что распространенность БП составляет от 0,7% до 11% мужчин в Соединенных Штатах [Stuntz, M., et al. The Prevalence of Peyronie's Disease in the United States: A Population-Based Study. PLoS One, 2016. 11: e0150157. https://pubmed.ncbi.nlm.nih.gov/26907743/]. По результатам исследования 2012 года, в Японии отмечен низкий уровень заболеваемости БП - 0,6% мужчин [Shiraishi K, Shimabukuro T, Matsuyama H. The prevalence of Peyronie’s disease in Japan: a study in men undergoing maintenance hemodialysis and routine health checks. J Sex Med. 2012;9:2716–2723]. Более высокий уровень БП - 7,1% был выявлен в ходе опроса итальянских мужчин [La Pera G, Pescatori ES, Calabrese M, et al.SIMONA Study Group Peyronie’s disease: prevalence and association with cigarette smoking. A multicenter population-based study in men aged 50–69 years. [Accessed March 10, 2015]; Eur Urol. 2001 40(5):525–530.]. По данным Stuntz и соавт. пик заболеваемости наблюдается у мужчин в возрасте 40-70 лет [Stuntz M, Perlaky A, Des Vignes F, Kyriakides T, Glass D. The prevalence of Peyronie’s disease in the United States: A population-based study. PLoS One 2016;11(2). doi:10.1371/journal.pone.015015].
На сегодняшний день этиология БП до конца не изучена. Наиболее распространѐнной теорией развития заболевания является травма полового члена, включая как последствия острой травмы, так и повторяющуюся микротравму. Факторами риска развития болезни Пейрони являются сахарный диабет, артериальная гипертензия, нарушения липидного обмена, ишемическая болезнь сердца, курение, злоупотребление алкоголем.
Основными симптомами заболевания являются боль в половом члене, искривление и укорочение полового члена, пальпируемая бляшка, эректильная дисфункция (ЭД), которая наблюдается в 22 – 54%. Во время естественного течения заболевания эрекция ухудшается у 40 – 52% пациентов [Paulis G., Romano G., Paulis A. Prevalence, psychological impact, and risk factors of erectile dysfunction in patients with Peyronie's disease: a retro- spective analysis of 309 cases // Res. Rep. Urol. 2016. Vol. 8. P. 95–103. doi: 10.2147/RRU.S109319].
Хирургическое лечение болезни Пейрони относится к наиболее сложным и актуальным разделам оперативной урологии. Варианты хирургического лечения обсуждаются после стабилизации, которая наступает через 6-18 месяцев от начала заболевания. У больных с углом искривления более 40º, крупной оссифицированной бляшкой, длиной полового члена менее 13 см, наличием сложной деформации полового члена ("песочные часы", по типу "винта" и др.) — «удлиняющие» операции являются методом выбора хирургического лечения. Основная идея данных операций заключается в рассечении бляшки с замещением дефекта белочной оболочки трансплантатом — графтом. В качестве трансплантата используют аутологичные (вена (vena saphena magna), оральная слизистая, внутренний листок крайней плоти), аллогенные (подслизистый слой тонкой кишки), ксеногенные и синтетические материалы.
На сегодняшний день идеальный графт для лечения болезни Пейрони еще не найден. Требования, предъявляемые к трансплантату, должны включать следующие свойства: широкую доступность, отсутствие иммунной реакции, определенные физические параметры. Более того, некоторые из специфических осложнений техники трансплантации включают контрактуру трансплантата, что приводит к повторному искривлению и снижению чувствительности головки полового члена [Павлов В.Н., Бакиров А.А., Казихинуров Р.А., Казихинуров А.А., Агавердиев М.А., Папоян А.О., Мазоров Б.З., Казихинуров Р.Р. Корпоропластика при болезни Пейрони: обзор литературы // Креативная хирургия и онкология, Том 11, № 3, 2021]. Согласно ряду исследований корпоропластика сопряжена с дополнительными рисками формирования ЭД de novo или усугублением имевшихся нарушений, которые могут достигать 67% [Terrier J.E., Tal R., Nelson C.J., Mulhall J.P. Penile sensory changes after plaque incision and grafting surgery for Peyronie’s disease. J Sex Med. 2018;15(10):1491–7. DOI: 10.1016/j.jsxm.2018.07.020].
Отсутствие патогенетического лечения, частое сочетание с эректильной дисфункцией и высокий риск рецидива после оперативного лечения обусловливают актуальность разработки новых способов корпоропластики при болезни Пейрони.
В качестве ближайшего аналога взят способ хирургического лечения болезни Пейрони, осложненной искривлением полового члена, заключающийся в том, что в качестве трасплантата выкраивают буккальный графт из слизистой рта и вшивают, замещая полученный дефект белочной оболочки, по периметру прямоугольника. После фиксации графта воспроизводят искусственную эрекцию, и производят прошивание латеральных краев белочной оболочки шовным материалом биосин 3/0 в поперечном к оси полового члена направлении, швами, параллельными друг другу, с частотой шага в 5 мм, с протягиванием нити поверх графта с захватом ткани графта посередине. Повторно создают искусственную эрекцию и нити затягивают дополнительным узлом до исчезновения аневризматической деформации и выравнивания графта по отношению к белочной оболочке [патент RU 2701575, 2019].
Недостатками прототипа являются:
1. Необходимость забора собственных тканей, что сопряжено с удлинением времени операции и анестезиологического пособия.
2. Осложнения, связанные с забором слизистой ротовой полости.
3. Физический дискомфорт пациента в донорской зоне.
4. Невозможность использования оральной слизистой при протезировании полового члена.
Процент рецидивов после корпоропластики с использованием различных трансплантатов может достигать 78,9%, а развитие эректильной дисфункции de novo 63% [European Association of Urology Guidelines on Sexual and Reproductive Health – 2023].
В доступной научно-медицинской и патентной литературе отсутствуют сведения по применению аллогенного трупного трансплантата перикарда Аллоплант® в качестве материала для корпоропластики для уменьшения послеоперационного риска развития эректильной дисфункции с использованием регенеративных технологий, особенно при одномоментном применении для профилактики эректильной дисфункции de novo.
Задачей изобретения является разработка способа корпоропластики с использованием аллогенного трупного трансплантата перикарда Аллоплант® и стромально-васкулярной фракции (СВФ), полученной из аутологичной жировой ткани, для стимуляции неоангиогенеза, обеспечивающего улучшение косметического эффекта и уменьшение послеоперационного риска развития эректильной дисфункции у больных с болезнью Пейрони.
Технический результат при использовании изобретения – улучшение функциональных результатов за счет достижения косметического результата и уменьшения послеоперационного риска развития эректильной дисфункции.
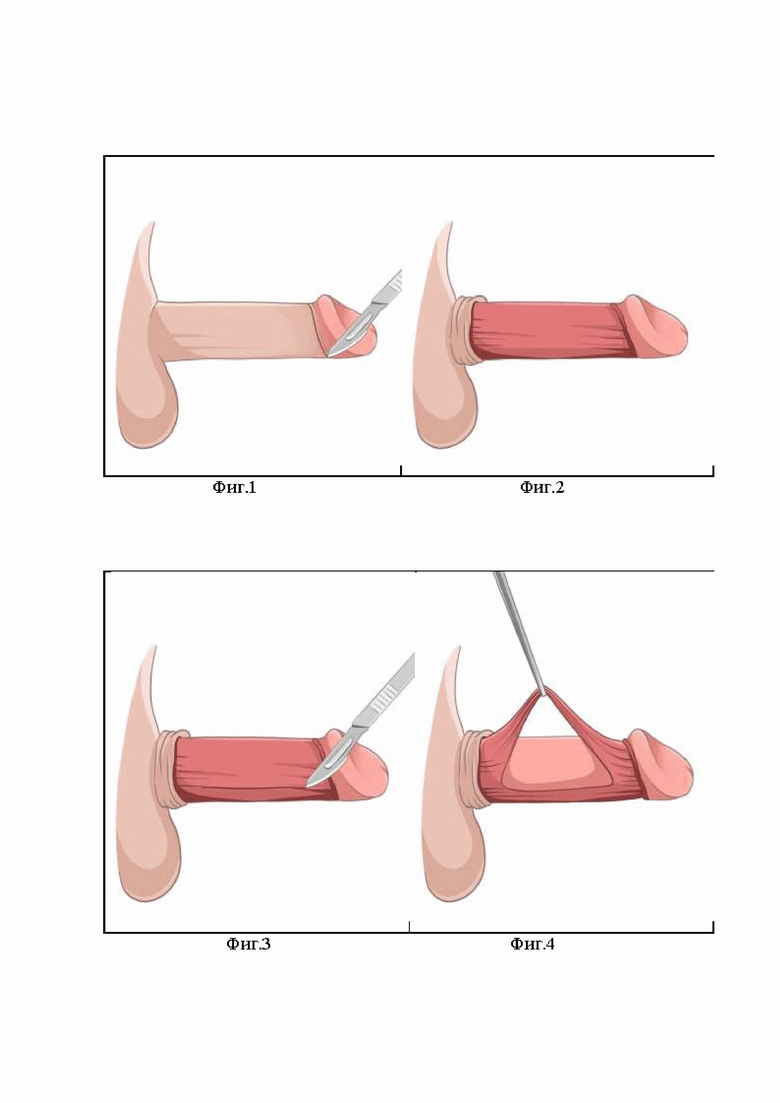
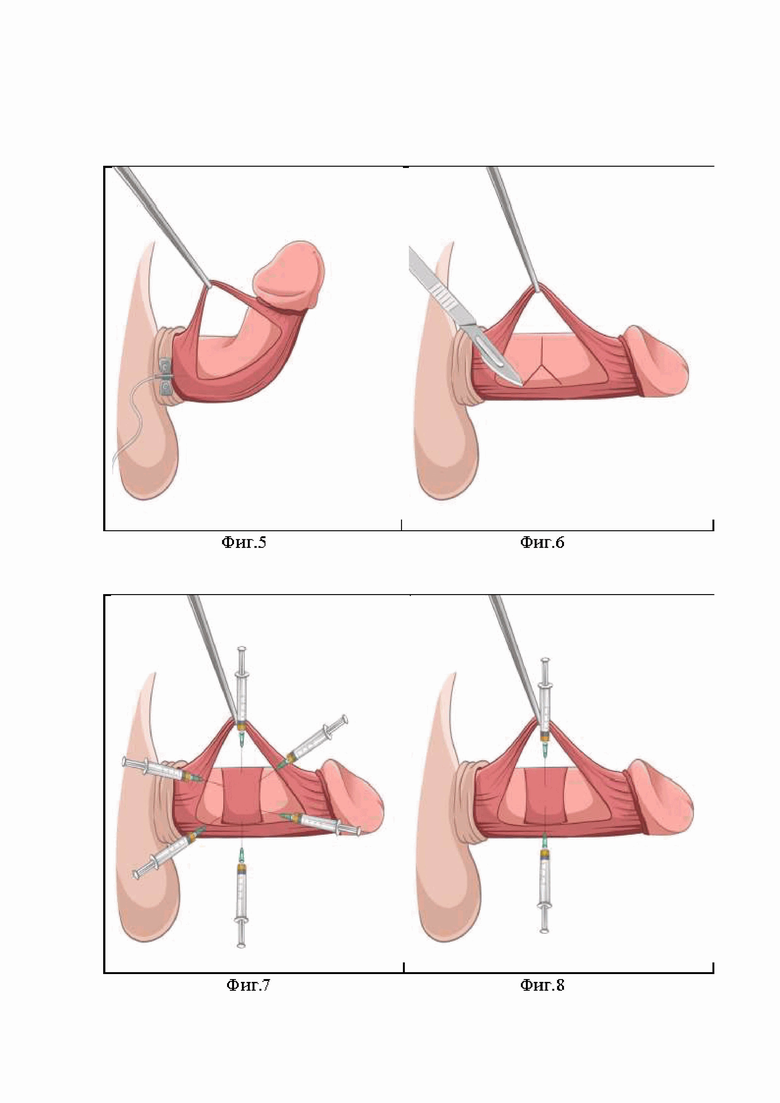
Изобретение иллюстрируется следующими фигурами: на фиг. 1 – циркулярный разрез полового члена; на фиг. 2 – скальпирование полового члена; на фиг. 3 – выделение сосудисто-нервного пучка; на фиг. 4 – мобилизованный сосудисто-нервный пучок взят на держалку; на фиг. 5 – определение положения бляшки; на фиг. 6 – поперечная Y – корпоротомия; на фиг. 7, 8 – введение СВФ в кавернозные тела по периметру и по площади; на фиг. 9, 10 – фиксация алогенного трупного трансплантата перикарда Аллоплант®.
Предлагаемый способ корпоропластики при болезни Пейрони осуществляется следующим образом. После трехкратной обработки операционного поля спиртовым раствором хлоргексидина, под спинальной анестезией, производят циркулярный разрез кожи полового члена, далее циркумцизию (фиг.1). Половой член скальпируют (фиг.2). Отступя от уретры на 0,5 см, выделяют сосудисто-нервный пучок справа и слева (фиг.3), берут на держалку (фиг.4), после чего проводят индукцию
тумесценции введением физиологического раствора NaСl 0,9% в кавернозные тела (фиг.5), определяют зону втяжения. Далее производят поперечное рассечение фиброзной бляшки в виде двойного Y-разреза в точке максимального искривления (фиг.6). В последующем, производят забор собственной подкожно-жировой клетчатки в объеме 100-150 мл для получения СВФ, которую вводят в кавернозные тела по периметру и по площади дефекта в объѐме 4-5 мл (фиг.7, 8).
Измеряют длину и ширину дефекта белочной оболочки, подбирают аллогенный трупный трансплантат перикарда Аллоплант® шириной на 30% больше ширины дефекта белочной оболочки, на углы для фиксации накладывают узловые швы плетенным синтетическим рассасывающимся шовным материалом (кополимер гликолид/лактид) толщиной 3/0, далее проводят ушивание на максимально растянутом половом члене по периметру узловыми швами тем же материалом (фиг. 9, 10). В последующем выполняют тест на герметичность и резидуальное искривление введением 0,9% физиологического раствора NaСl. Рану послойно ушивают. На кожу накладывают узловые швы. Асептическая повязка на половой член.
Аллоплант - это биоматериал, полученный от недавно умерших доноров, используемый в регенеративной хирургии и терапии. Многолетний опыт экспериментального и клинического исследования производимых биоматериалов Аллоплант является убедительным подтверждением их избирательного воздействия на процессы репаративной регенерации различных тканей и анатомических структур. Это исключительно перспективное направление открывает возможности лечения широко распространенных аутоиммунных, наследственных и сосудистых заболеваний. При использовании различных видов биоматериалов, Аллоплант может стимулировать регенерацию кровеносных и лимфатических сосудов, роговицы, склеры, кожных покровов, конъюнктивы, нервов, паренхимы печени, слизистой оболочки ЖКТ и т.д. Аллоплант широко применяется в офтальмологии, пластической хирургии, стоматологии, грудной хирургии, нейрохирургии, проктологии, ортопедии, травматологии, хирургии печени, гинекологии и т.д.
Министерство Здравоохранения России одобрило широкое клиническое применение пересадочного материала «Аллоплант» (Регистрационное удостоверение No 901 от 22.07.1987). Аллоплант включен в общую классификацию биологической продукции и разрешен к широкому клиническому применению. Спецификация No 42-2-537-93 (Министерство Здравоохранения России, регистрационный номер 056/003230 от 17.05.1993). Забор донорского трупного материала производится в соответствии с Законом Российской Федерации «О трансплантации органов и тканей» No 4181-1 от 22.11.1992.
Получение СВФ осуществляется в несколько этапов.
Первым этапом выполняют тумесцентную липосакцию. Параумбиликально выполняют кожный разрез 5 мм. После чего от центра к периферии выполняют инфильтрацию подкожно-жировой клетчатки с использованием тонкой канюли для инфильтрации длиной 250 мм, диаметром 3 мм и шприца Luer-Lock 50 мл.
После инфильтрации проводят экспозицию на протяжении 7 минут. Далее проводят липоаспирацию с использованием канюли для липосакции, диаметром 4 мм, длиной 300 мм, с одним центральным отверстием и двумя боковыми и коннектором для шприца на 60 мл. Возвратно - поступательными движениями выполняют забор жировой ткани в объеме 150 мл. Для выделения СВФ из жировой ткани используют специализированные двойные шприцы Arthrex ACP®, объемом 15 мл.
После проведения липосакции шприцы Arthrex ACP® в количестве 4 штук помещают в настольную центрифугу Rotofix 32 А с роторами-крестовинами со свободно подвешенными стаканами. Проводят центрифугирование при режиме 2500 оборотов/минуту на протяжении 4 минут. После однократного центрифугирования удаляют оставшуюся тумесцентную жидкость и выполняют перенос жировой ткани в шприц Luer - Lock 10 мл. Далее с использованием коннектора диаметром 1,4 мм и двух шприцов Luer - Lock 10 мл проводят последовательный перенос оставшейся жировой ткани из шприца в шприц через коннектор в количестве 30 раз с целью механической обработки. После чего обработанную ткань переносят в шприц Arthrex ACP для повторного центрифугирования при режиме 2500 оборотов/минуту на протяжении 4 минут. По результатам повторного центрифугирования происходит разделение жировой ткани на фракции. Заключительный этап включается в переносе СВФ с использованием коннектора диаметром 1,4 мм в шприц Luer - Lock объемом 5 мл. Таким образом, из 60 мл жировой ткани возможно получение 4-5 мл СВФ, в которой содержится 50 миллионов и более клеток [Ala Lozinski, MD, FRCPC, DABD, Nasim S. Huq, MD, FRCSC, MSc, FACS, CAQHS, DABPS, DOI:https://doi.org/10.1016/j.cps.2013.07.006].
Клеточный компонент СВФ гетерогенен и меняется в зависимости от места липосакции, пола и возраста донора, а также наличия хронических заболеваний. Основными клеточными фракциями, обладающими терапевтическим эффектом, являются мезенхимальные стволовые клетки (МСК), помимо которых СВФ содержит предшественники эндотелиальных клеток, перициты, моноциты/макрофаги, регуляторные Т-лимфоциты, предшественники гемопоэтических клеток. При этом данные литературы о поверхностных маркерах довольно противоречивы. Их описанию посвящено большое количество исследований. В целом считается, что для негемопоэтической (CD45–) популяции клеток СВФ характерна экспрессия маркеров МСК. Однако существуют сложности в идентификации субпопуляций СВФ. Также интересно, что культивирование способно влиять на процентное соотношение клеток СВФ с тенденцией к снижению содержания стромальных и прогениторных клеток [Ramakrishnan V.M., Boyd N.L. The Adipose Stromal Vascular Fraction as a Complex Cellular Source for Tissue Engineering Applications. Tissue Eng Part B Rev. 2018 Aug;24(4):289-299. doi: 10.1089/ten.TEB.2017.0061. Epub 2017 Apr 13.].
Основной механизм действия основан на сложной связи разнородной клеточной популяции СВФ с клетками реципиента, приводящей к стимуляции дифференцировки клеток, ангиогенезу, иммуномодулирующему, антиапоптотическому эффектам и соответственно восстановлению поврежденных клеток и тканей.
При этом возникает стимуляция компенсаторных возможностей микроциркуляторного русла за счет увеличения капиллярной сети, что достигается путем стимуляции неоангиогенеза и стимуляции регенеративных процессов в зоне проводимой корпоропластики и тканей рядом с ними, что в свою очередь снижает риск рецидива заболевания и развития ЭД.
Сущность изобретения поясняется следующими клиническими примерами.
Пример 1. Больной Б. 35 лет, поступил в клинику с жалобами на искривление и укорочение полового члена. Давность заболевания около 1-го года. В течение 3-х месяцев отмечает отсутствие дальнейшего искривления. При осмотре: состояние удовлетворительное. При пальпации полового члена на границе средней и праксимальной трети кавернозных тел, по дорсальной поверхности, определяется участок уплотнения размером 25х20 мм. Согласно опроснику МИЭФ-5 индекс эректильной функции составил 21 балл. При проведении ультразвукового исследования (УДС) полового члена с интракавернозной фармаконагрузкой (алпростадил, 10 мкг) выполнена фотофиксация, угол искривления составил 55°. Допплерографические признаки нарушения веноокклюзивного механизма. Выполнена корпоропластика с использованием алогенного трупного трансплантата перикарда Аллоплант® с введением СВФ.
Операция произведена следующим образом:
Положение пациента на операционном столе на спине. После трехкратной обработки операционного поля спиртовым раствором хлоргексидина, под спинальной анестезией, субкоронарным доступом произведен циркулярный разрез кожи полового члена, далее циркумцизия. Половой член скальпирован. Отступя от уретры на 0,5 см выделен сосудисто-нервный пучок справа и слева, взят на держалку. На основание полового члена наложен турникет, после чего проведена индукция тумесценции введением физиологического раствора NaСl 0,9% в кавернозные тела в объѐме 40 мл, определена зона втяжения. Далее произведено поперечное рассечение фиброзной бляшки в виде двойного Y-разреза в точке максимального искривления. В последующем произведен забор собственной подкожно-жировой клетчатки в объеме 100 мл для изготовления СВФ. Получено 4 мл СВФ, которая введена в кавернозные тела по периметру и по площади дефекта.
После измерения ширины и длины, дефект белочной оболочки составил 30×50 мм (ш×д), подобран алогенный трупный трансплантат перикард Аллоплант® шириною 39 мм, на углы для фиксации наложены узловые швы плетенным синтетическим рассасывающимся шовным материалом (кополимер гликолид/лактид) толщиной 3/0, далее проведено ушивание на максимально растянутом половом члене по периметру узловыми швами тем же материалом. В последующем выполнен тест на герметичность и резидуальное искривление введением 0,9% физиологического раствора NaСl в объѐме 40 мл. Рана послойно ушита. На кожу наложены узловые швы. Асептическая повязка на половой член.
Пациент выписан из клиники в удовлетворительном состоянии на 2-е сутки после операции. Оценка результатов операции проведена через 3, 6, 9, 12 месяцев – пациент удовлетворен достигнутым косметическим результатом, по данным опросника МИЭФ-5 эректильной дисфункции не наблюдается, резидуальная девиация не определяется.
Пример 2. Больной Б. 40 лет, поступил в клинику с жалобами на искривление и укорочение полового члена. Давность заболевания 8 месяцев. В течение 3-х месяцев отмечает отсутствие дальнейшего искривления. При осмотре: состояние удовлетворительное. При пальпации полового члена на границе средней и проксимальной трети кавернозных тел, по дорсальной поверхности, определяется участок уплотнения размером 25×20 мм. Согласно опроснику МИЭФ-5 индекс эректильной функции составил 22 балла. При проведении ультразвукового исследования (УДС) полового члена с интракавернозной фармаконагрузкой (алпростадил, 10 мкг) выполнена фотофиксация, угол искривления составил 57°. Выполнена корпоропластика с использованием алогенного трупного трансплантата перикарда Аллоплант® с введением СВФ. Операция произведена следующим образом:
Положение пациента на операционном столе на спине. После трехкратной обработки операционного поля спиртовым раствором хлоргексидина, под спинальной анестезией, субкоронарным доступом произведен циркулярный разрез кожи полового члена, далее циркумцизия. Половой член скальпирован. Отступя от уретры на 0,5 см выделен сосудисто-нервный пучок справа и слева, взят на держалку. На основание полового члена наложен турникет, после чего проведена индукция тумесценции введением физиологического раствора NaСl 0,9% в кавернозные тела в объѐме 45 мл, определена зона втяжения. Далее произведено поперечное рассечение фиброзной бляшки в виде двойного Y-разреза в точке максимального искривления. В последующем произведен забор собственной подкожно-жировой клетчатки в объеме 150 мл для изготовления СВФ. Получено 5 мл СВФ, которая введена в кавернозные тела по периметру и по площади дефекта.
После измерения ширины и длины, дефект белочной оболочки составил 33×50 мм (ш×д), подобран алогенный трупный трансплантат перикард Аллоплант® шириною 42,9 мм, на углы для фиксации наложены узловые швы плетенным синтетическим рассасывающимся шовным материалом (кополимер гликолид/лактид) толщиной 3/0, далее проведено ушивание на максимально растянутом половом члене по периметру узловыми швами тем же материалом. В последующем выполнен тест на герметичность и резидуальное искривление введением 0,9% физиологического раствора NaСl в объѐме 40 мл. Рана послойно ушита. На кожу наложены узловые швы. Асептическая повязка на половой член.
Пациент выписан из клиники в удовлетворительном состоянии на 2-е сутки после операции. Оценка результатов операции проведена через 3, 6, 9, 12 месяцев – пациент удовлетворен достигнутым косметическим результатом, по данным опросника МИЭФ-5 эректильной дисфункции не наблюдается, резидуальная девиация не определяется.
Указанным способом, при информированном согласии, пролечено 30 пациентов с болезнью Пейрони.
Преимуществами заявляемого способа являются доступность, простота применения, эффективность, отсутствие прогнозируемых значимых осложнений и побочных эффектов, что позволяет успешно применять его в урологии.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ хирургического лечения болезни Пейрони, осложненной искривлением полового члена | 2019 |
|
RU2701575C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ БОЛЕЗНИ ПЕЙРОНИ | 2010 |
|
RU2460473C2 |
| Способ ксенопластики при хирургическом лечении болезни Пейрони | 2020 |
|
RU2725837C1 |
| СПОСОБ ДОРСАЛЬНОЙ АУГМЕНТАЦИОННОЙ УРЕТРОПЛАСТИКИ ПРИ СТРИКТУРАХ УРЕТРЫ У МУЖЧИН | 2022 |
|
RU2798681C1 |
| СПОСОБ КОРПОРОПЛАСТИКИ ПРИ БОЛЕЗНИ ПЕЙРОНИ | 2016 |
|
RU2640770C1 |
| СПОСОБ ВЫБОРА ТАКТИКИ УДАРНО-ВОЛНОВОЙ ТЕРАПИИ ПРИ БОЛЕЗНИ ПЕЙРОНИ | 2003 |
|
RU2256405C1 |
| СПОСОБ ХИРУРГИЧЕСКОЙ КОРРЕКЦИИ ОРГАНИЧЕСКОЙ ФОРМЫ ЭРЕКТИЛЬНОЙ ДИСФУНКЦИИ, ОБУСЛОВЛЕННОЙ БОЛЕЗНЬЮ ПЕЙРОНИ | 1999 |
|
RU2179827C2 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЕЗНИ ПЕЙРОНИ И ЭРЕКТИЛЬНОЙ ДИСФУНКЦИИ | 2005 |
|
RU2303405C1 |
| СПОСОБ ХИРУРГИЧЕСКОЙ КОРРЕКЦИИ ЭРЕКТИЛЬНОЙ ДЕФОРМАЦИИ ПРИ БОЛЕЗНИ ПЕЙРОНИ | 2002 |
|
RU2234257C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ БОЛЕЗНИ ПЕЙРОНИ И ЭРЕКТИЛЬНОЙ ДИСФУНКЦИИ | 2008 |
|
RU2376942C1 |

Изобретение относится к медицине, а именно к корпоративной урологии. Производят циркулярный разрез кожи полового члена, далее циркумцизию. Половой член скальпируют. Проводят индукцию тумесценции введением физиологического раствора NaСl 0,9% в кавернозные тела, определяют зону втяжения. Далее производят поперечное рассечение фиброзной бляшки в виде двойного Y-разреза в точке максимального искривления. Производят забор собственной подкожно-жировой клетчатки в объеме 100-150 мл для получения СВФ, которую вводят в кавернозные тела по периметру и по площади дефекта в объѐме 4-5 мл. Измеряют длину и ширину дефекта белочной оболочки, подбирают аллогенный трупный трансплантат перикарда Аллоплант® шириной на 30% больше ширины дефекта белочной оболочки, на углы для фиксации накладывают узловые швы плетенным синтетическим рассасывающимся шовным материалом (кополимер гликолид/лактид) толщиной 3/0, далее проводят ушивание на максимально растянутом половом члене по периметру узловыми швами тем же материалом. Способ обеспечивает улучшение функциональных результатов за счет достижения косметического результата и уменьшение послеоперационного риска развития эректильной дисфункции. 10 ил., 2 пр.
Способ корпоропластики при болезни Пейрони, включающий циркумцизию, скальпирование полового члена, индукцию тумесценции введением 0,9% физиологического раствора NaCl в кавернозные тела, поперечное рассечение фиброзной бляшки, имплантацию и фиксацию трансплантата, отличающийся тем, что производят забор собственной подкожно-жировой клетчатки в объеме 100-150 мл для получения стромально-васкулярной фракции, которую вводят в кавернозные тела по периметру и по площади дефекта в объёме 4-5 мл, в качестве трансплантата используют аллогенный трупный трансплантат перикарда Аллоплант шириной на 30% больше ширины дефекта белочной оболочки.
| Способ хирургического лечения болезни Пейрони, осложненной искривлением полового члена | 2019 |
|
RU2701575C1 |
| Способ лечения протяженных стриктур передней уретры | 2020 |
|
RU2746827C1 |
| Способ лечения эректильной дисфункции | 2016 |
|
RU2622757C1 |
| ПАВЛОВ В.Н | |||
| и др | |||
| Корпоропластика при болезни Пейрони: обзор литературы | |||
| Креативная хирургия и онкология | |||
| Способ регенерирования сульфо-кислот, употребленных при гидролизе жиров | 1924 |
|
SU2021A1 |
| Парный рычажный домкрат | 1919 |
|
SU209A1 |
| ВАСЮТИН И.А | |||
| И др | |||
| Реконструкция уретры с помощью технологий тканевой инженерии | |||
| Вестник РАМН | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| MAJKEN HORUP | |||
Авторы
Даты
2024-04-23—Публикация
2024-01-31—Подача