Изобретение относится к способу получения силилоксиаминов общей формулы
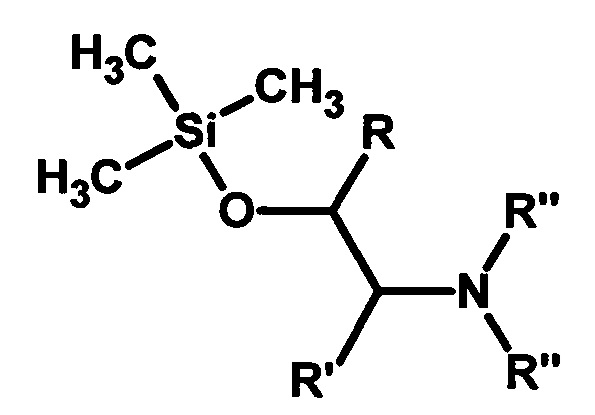
где R=CH2OAlk, R'=Н; R=R'=(СН2)4; R''=С2Н5, С3Н7, являющихся промежуточными продуктами в синтезе:
- противораковых агентов [Ekhato, I.V. Asymmetric synthesis of (R)-(+)-[[(2-bromoethyl)amino]methyl]-2-nitro-1H-imidazole[1-14C]-ethanol monohydrobromide / I.V. Ekhato // J. Label. Compd. Radiopharm - 1998. - V. 41. - №6. - P. 523-533],;
- биологически важных имидазолиловых спиртов [Jalil, М. А straightforward one-pot synthesis of biologically important imidazolyl alcohols via catalytic epoxide ring-opening reactions / M. Jalil, S. Masum // Tetrahedron Lett. - 2012. - V. 53. - №24. - P. 3049-3051];
- антидепрессантов [Kuwabe, S. Palladium-catalyzed intramolecular C-O bond formation / S. Kuwabe, K. Torraca, S. Buchwald // Journal of the American Chemical Society. - 2001. - V. 123. - №9. - P. 12202-12206];
- и ряда других соединений.
Известен способ получения силилоксиаминов взаимодействием N-триметилсилилимидазола с эпоксидными соединениями в присутствии 5 мольных % бромида лития при 20-60°С в течение 4-6 часов [Jalil, М.А straightforward one-pot synthesis of biologically important imidazolyl alcohols via catalytic epoxide ring-opening reactions / M. Jalil, S. Masum // Tetrahedron Lett. - 2012. - V. 53 - №24. - P. 3049-3051]. Недостатком данного метода является длительность процесса, необходимость нагревания, а также образование побочных продуктов из-за присоединения бромид-иона к интермедиату.
Известен способ получения силилоксиаминов взаимодействием аминосиланов с эпоксидными соединениями в среде дихлорметана в присутствии хлорида алюминия при комнатной температуре в течение 2 часов [Regiospecific Conversion of Oxiranes, Oxetanes, and Lactones into Difunctional Nitrogen Compounds / A. Papini, A. Ricci, M. Taddei, G. Seconi // J. Chem. Soc. Perkin Trans. 1: Org. and Bio-Organic Chem. - 1984. - №10. - P. 2261-2266]. Однако недостатком данного метода являются сравнительно низкие выходы целевых продуктов (41-68%), а также образование побочных продуктов за счет нуклеофильной атаки хлорид-иона.
Известен способ получения силилоксиаминов взаимодействием аминосиланов с эпоксидными соединениями в среде тетрагидрофурана в присутствии триметилсиланолята натрия. Взаимодействие проводят при температуре 95°С в течение 1,5 часов [Synthesis of the enantiomers of the dual function 2-nitroimidazole radiation sensitizer RB 6145 / A. Sercel, V. Beylin, M. Marlatt et al. // 2006. - V. 43. - №6. - P. 1597-1604]. Недостатками данного метода являются невысокие выходы целевых продуктов (61%).
Наиболее близким аналогом к предлагаемому техническому решению является способ получения силилоксиаминов взаимодействием аминосиланов с эпоксидными соединениями в среде диэтилового эфира в присутствии перхлората лития, в качестве катализатора, в течение 1 часа при комнатной температуре и избытке аминосилана в количестве 200 мол. %, [Ipaktschi, J. LiClO4-katalysierte nucleophile Addition an α-chirale Aldehyde, Aldimine und Oxirane / J. Ipaktschi, A. Heydari // Chemische Berichte. - 1993. - V. 126. - №8. - P. 1905-1912]. Целевые продукты при этом получают с выходами 93-98%. Однако недостатком данного метода является необходимость использования избытка аминосилана в количестве 200 мол. %, что приводит к избыточному расходу реагентов.
Техническим результатом предлагаемого способа является сокращение количеств используемых реагентов, а также времени получения конечного продукта.
Для достижения технического результата предлагается проводить взаимодействие аминосиланов с эпоксидными соединениями в среде толуола в присутствии 5 мол. % перхлората магния при использовании избытка аминосилана в количестве 10 мол. % при температуре 25-60°С в течение 20-40 минут по схеме:
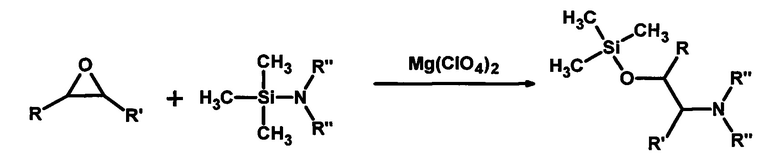
где R=CH2OAlk, R'=Н; R=R'=(СН2)4; R''=С2Н5, С3Н7.
Общими признаками предлагаемого способа и прототипа являются:
- использование аминосиланов и эпоксидов в качестве исходных соединений в среде растворителя;
- использование катализатора
- использование избытка аминосилана
Отличительными признаками являются:
- использование в качестве растворителя толуола;
- использование перхлората магния в качестве катализатора;
- использование избытка аминосилана в количестве 10 мол. %
- проведение взаимодействия при температуре 25-60°С в течение 20-40 мин.
Пример 1. Получение {3-(бутокси)-2-[(триметилсилил)окси]пропил}дипропиламина.
В вайл помещают 5,2 мг (0,05 ммоль) перхлората магния, 143 мкл (1 ммоль) глицидилового эфира бутанола-1, 251 мкл (1,1 ммоль) триметилсилилдипропиламина и 100 мкл толуола. Перемешивают при 25°С в течение 30 минут и очищают методом колоночной хроматографии. Получают 266,6 мг {3-(бутокси)-2-[(триметилсилил)окси]пропил}дипропиламина, выход 88%.
ЯМР 1Н δ 0.11 (s, 9Н, 3СН3), 0.84 (t, 6 Н, 2СН3, 3J=7.4 Гц), 0.89 (t, 3Н, СН3, 3J=7.3 Гц), 1.32-1.57 (m, 8 Н, 4СН2), 2.30-2.48 (m, 6 Н, 3СН2), 3.27-3.31 (d-d, Н, СН2, 2J=9.8 Гц, 3J=6.4 Гц), 3.40 (t, 2Н, СН2, 3J=6.6 Гц), 3.47-3.51 (d-d, Н, СН2, 2J=10.1 Гц, 3J=3.7 Гц), 3.81 (s, 1Н, СН);
ЯМР 13С δ 0.7, 12.0, 14.0, 19.4, 20.4, 31.9, 57.3, 58.3, 71.3, 71.5, 74.2;
ЯМР 29Si δ 17.1.
Пример 2. Получение {3-(2-этилгексилокси)-2-[(триметилсилил)окси]пропил}дипропиламина.
В вайл помещают 5,2 мг (0,05 ммоль) перхлората магния, 209 мкл (1 ммоль) глицидилового эфира 2-этил-1-гексанола, 251 мкл (1,1 ммоль) триметилсилилдипропиламина и 100 мкл толуола. Перемешивают при 25°С в течение 30 минут и очищают методом колоночной хроматографии. Получают 335,7 мг {3-(2-этилгексокси)-2-[(триметилсилил)окси]пропил}дипропиламина, выход 93%.
ЯМР 1Н δ 0.12 (s, 9Н, 3СН3), 0.83-0.89 (m, 12Н, 4СН3), 1.26-1.50 (m, 13 Н, 6СН2, СН), 2.34-2.52 (m, 4Н, 2СН2), 3.27-3.30 (m, 3Н, СН2, СН), 3.44-3.47 (d-d, Н, СН2, 2J=10.4 Гц, 3J=3.4 Гц) 3.81 (s, 1Н, СН);
ЯМР 13С δ 0.7, 11.4, 12.2, 14.4, 20.6, 23.4, 24.2, 29.4, 30.9, 40.0, 57.5, 58.7, 71.3,74.6, 74.7;
ЯМР 29Si δ 17.1.
Пример 3. Получение {3-(бутокси)-2-[(триметилсилил)окси]пропил}диэтиламина.
В вайл помещают 5,2 мг (0,05 ммоль) перхлората магния, 143 мкл (1 ммоль) глицидилового эфира бутанола-1, 189 мкл (1,1 ммоль) триметилсилилдиэтиламина и 100 мкл толуола. Перемешивают при 25°С в течение 40 минут и очищают методом колоночной хроматографии. Получают 259,0 мг {3-(бутокси)-2-[(триметилсилил)окси]пропил}диэтиламина, выход 94%.
ЯМР 1Н δ 0.11 (s, 9Н, 3СН3), 0.89 (t, 3Н, СН3, 3J=7.3 Гц), 0.97 (t, 6Н, 2СН3, 3J=7.1 Гц), 1.32-1.37 (m, 2Н, СН2), 1.50-1.55 (m, 2Н, СН2), 2.31-2.55 (m, 6Н, СН2), 3.27-3.31 (d-d, Н, СН2, 2J=9.9 Гц, 3J=6.2 Гц), 3.40 (t, 2Н, СН2, 3J-6.6 Гц), 3.45-3.49 (d-d, Н, СН2, 2J=9.8 Гц, 3J=3.9 Гц), 3.80-3.83 (m, 1Н, СН);
ЯМР 13С δ 0.4, 11.9, 13.9, 19.3, 31.8, 48.0, 56.9, 71.0, 71.2, 74.1;
ЯМР 29Si δ 17.1.
Пример 4. Получение {3-(2-этилгексилокси)-2-[(триметилсилил)окси]пропил}диэтиламина.
В вайл помещают 5,2 мг (0,05 ммоль) перхлората магния, 209 мкл (1 ммоль) глицидилового эфира 2-этил-1-гексанола, 189 мкл (1,1 ммоль) триметилсилилдиэтиламина и 100 мкл толуола. Перемешивают при 25°С в течение 30 минут и очищают методом колоночной хроматографии. Получают 325,8 мг {3-(2-этилгексилокси)-2-[(триметилсилил)окси]пропил}диэтиламина, выход 98%.
ЯМР 1Н δ 0.12 (s, 9Н, 3СН3), 0.83-0.89 (m, 6Н, 2СН3), 0.98 (t, 6Н, 2СН3, 3J=6.9 Гц), 1.24-1.50 (m, 9Н, 4СН2, СН), 2.32-2.57 (m, 6Н, 3СН2), 3.26-3.30 (m, 3Н, СН2, СН), 3.41-3.45 (d-d, Н, СН2, 2J=11.0 Гц, 3J=4.1 Гц), 3.82-3.84 (m, 1Н, СН);
ЯМР 13С δ 0.7, 11.4, 12.2, 14.4, 23.4, 24.1, 29.4, 30.9, 40.0, 48.3, 57.3, 71.3, 74.6, 74.7;
ЯМР 29Si δ 17.1
Пример 5. Получение диэтил{2-[(триметилсилил)окси]циклогексил}амина.
В вайл помещают 5,2 мг (0,05 ммоль) перхлората магния, 101 мкл (1 ммоль) циклогексеноксида, 189 мкл (1,1 ммоль) триметилсилилдиэтиламина и 100 мкл толуола. Перемешивают при 60°С в течение 30 минут и очищают методом колоночной хроматографии. Получают 224,7 мг диэтил{2-[(триметилсилил)окси]циклогексил}амина, выход 92%.
ЯМР 1Н δ 0.10 (s, 9Н, 3СН3), 1.01 (t, 6Н, 2СН3, 3J=7.1 Гц), 1.11-1.31 (m, 4Н, 2СН2), 1.59-1.73 (m, 3Н, 2СН2), 1.86-1.89 (m, 1Н, СН2), 2.40-2.46 (m, 1Н, СН), 2.52-2.68 (m, 4Н, 2СН2), 3.54-3.50 (m, 1H, СН);
ЯМР 13С δ 1.1, 15.2, 25.0, 25.9, 28.9, 36.6, 44.8, 65.5, 72.9;
ЯМР 29Si δ 14.4.
Пример 6. Получение {3-(бутокси)-2-[(триметилсилил)окси]пропил}дипропиламина.
В вайл помещают 5,2 мг (0,05 ммоль) перхлората магния, 143 мкл (1 ммоль) глицидилового эфира бутанола-1, 251 мкл (1,1 ммоль) триметилсилилдипропиламина и 100 мкл толуола. Перемешивают при 25°С в течение 20 минут. Выход по ГХМС составляет 93%.
Пример 7. Получение {3-(бутокси)-2-[(триметилсилил)окси]пропил}дипропиламина.
В вайл помещают 2,2 мг (0,01 ммоль) перхлората магния, 143 мкл (1 ммоль) глицидилового эфира бутанола-1, 251 мкл (1,1 ммоль) триметилсилилдипропиламина и 100 мкл толуола. Перемешивают при 25°С в течение 130 минут. Выход по ГХМС составляет 53%.
Пример 8. Получение {3-(бутокси)-2-[(триметилсилил)окси]пропил}дипропиламина.
В вайл помещают 21,9 мг (0,1 ммоль) перхлората магния, 143 мкл (1 ммоль) глицидилового эфира бутанола-1, 251 мкл (1,1 ммоль) триметилсилилдипропиламина и 100 мкл толуола. Перемешивают при 25°С в течение 30 минут и очищают методом колоночной хроматографии. Получают 268,4 мг {3-(бутокси)-2-[(триметилсилил)окси]пропил}дипропиламина, выход 88%.
Пример 9. Получение {3-(бутокси)-2-[(триметилсилил)окси]пропил}диэтиламина.
В вайл помещают 5,2 мг (0,05 ммоль) перхлората магния, 143 мкл (1 ммоль) глицидилового эфира бутанола-1, 206 мкл (1,2 ммоль) триметилсилилдиэтиламина и 100 мкл толуола. Перемешивают при 25°С в течение 40 минут и очищают методом колоночной хроматографии. Получают 261,6 мг {3-(бутокси)-2-[(триметилсилил)окси]пропил}диэтиламина, выход 95%.
ЯМР 1Н δ 0.11 (s, 9Н, 3СН3), 0.89 (t, 3Н, СН3, J=7.3 Гц), 0.97 (t, 6Н, 2СН3, 3J=7.1 Гц), 1.32-1.37 (m, 2Н, СН2), 1.50-1.55 (m, 2Н, СН2), 2.31-2.55 (m, 6Н, СН2), 3.27-3.31 (d-d, Н, СН2, 2J=9.9 Гц, 3J=6.2 Гц), 3.40 (t, 2Н, СН2, 3J-6.6 Гц), 3.45-3.49 (d-d, Н, СН2, 2J=9.8 Гц, 3J=3.9 Гц), 3.80-3.83 (m, 1Н, СН);
ЯМР 13С δ 0.4, 11.9, 13.9, 19.3,31.8,48.0, 56.9,71.0,71.2, 74.1;
ЯМР 29Si δ 17.1.

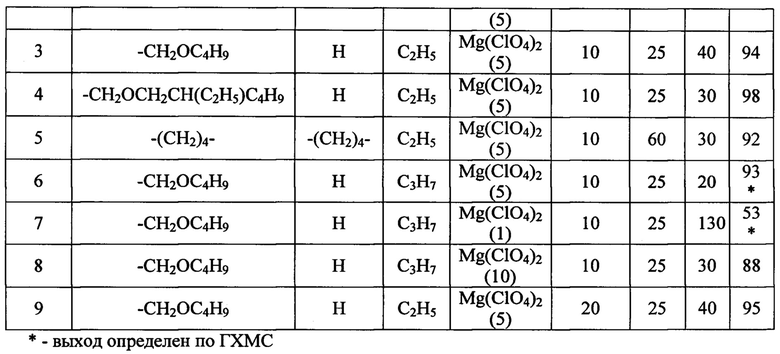
Как видно из приведенных примеров конкретного выполнения, при уменьшении количества катализатора реакция протекает значительно медленнее (пример 7), в то время как увеличение его количества не приводит к возрастанию выхода целевого продукта и уменьшению времени протекания реакции (пример 8). Увеличение избытка аминосилана до 20 мол. % не приводит к существенному увеличению выхода продукта (пример 9). Примеры 1-5 иллюстрируют возможность достижения технического результата для различных эпоксидов и диалкиламиносиланов, при взаимодействии от 20 до 40 минут и температуре 25-60°С.
Итак, время протекания реакции уменьшается в 1,5-3 раза, расход аминосилана значительно меньше.
На основании изложенного делаем вывод, что предлагаемое техническое решение является новым, обладает изобретательским уровнем и промышленно применимо, т.е. соответствует условиям патентоспособности, предъявляемым к изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| БЕТА-АДРЕНОБЛОКАТОРЫ НА ОСНОВЕ ПРОИЗВОДНЫХ ПИРИДОКСИНА | 2014 |
|
RU2569900C1 |
| СПОСОБ ОБРАЗОВАНИЯ ПОЛИГЕДРАЛЬНЫХ ОЛИГОМЕРНЫХ СИЛСЕСКВИОКСАНОВ (ВАРИАНТЫ) | 2000 |
|
RU2293745C2 |
| Производные пиридоксина и ацетона с противоопухолевой активностью | 2017 |
|
RU2639879C1 |
| ПРОИЗВОДНЫЕ ПИРИМИДИНА, ОБЛАДАЮЩИЕ МОДУЛЯТОРНОЙ АКТИВНОСТЬЮ ПО ОТНОШЕНИЮ К РЕЦЕПТОРАМ АМРА-ТИПА | 2019 |
|
RU2702751C1 |
| Четвертичные аммониевые соли на основе производных витамина В6 | 2015 |
|
RU2607522C1 |
| ЭФИРЫ КРЕМНИЯ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2005 |
|
RU2375370C2 |
| АНАЛОГ ПИРИДИНО[1,2-А]ПИРИМИДОНА, ИСПОЛЬЗУЕМЫЙ В КАЧЕСТВЕ ИНГИБИТОРА mTOR/PI3K | 2015 |
|
RU2658912C1 |
| 2, 5-ДИОКСОИМИДАЗОЛИДИН-4-ИЛ-МЕТИЛКАРБОНИЛЬНЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ, СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ИХ ПРИМЕНЕНИЕ В ИЗГОТОВЛЕНИИ ЛЕКАРСТВЕННОГО СРЕДСТВА | 2003 |
|
RU2326117C2 |
| ЛИГАНДЫ, ТРОПНЫЕ К ПРОСТАТИЧЕСКОМУ СПЕЦИФИЧЕСКОМУ МЕМБРАННОМУ АНТИГЕНУ И ИХ ПРИМЕНЕНИЕ ДЛЯ ПОЛУЧЕНИЯ ДВОЙНЫХ КОНЪЮГАТОВ С ТЕРАПЕВТИЧЕСКИМИ АГЕНТАМИ НА ИХ ОСНОВЕ ДЛЯ КОМБИНИРОВАННОЙ ТЕРАПИИ ПСМА ЭКСПРЕССИРУЮЩИХ ОПУХОЛЕЙ | 2023 |
|
RU2841078C1 |
| НОВЫЕ 2',5'-ДИАРИЛСПИРО[ИНДОЛ-3,3'-ПИРРОЛИДИН]-2(1Н)-ОНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2019 |
|
RU2730287C1 |
Изобретение относится к способу получения силилоксиаминов общей формулы (I), где R=CH2OAlk, R'=Н; R=R'=(СН2)4; R''=С2Н5, С3Н7. Предложен способ получения силилоксиаминов (I), включающий взаимодействие аминосиланов с эпоксидными соединениями в среде толуола в присутствии перхлората магния при использовании избытка аминосилана в количестве 10 мол. % при температуре 25-60°С в течение 20-40 минут. Технический результат – предложенный способ позволяет получать силилоксиамины (I) с высокими выходами при сокращении количеств используемых реагентов и времени получения конечного продукта. 1 табл., 9 пр.
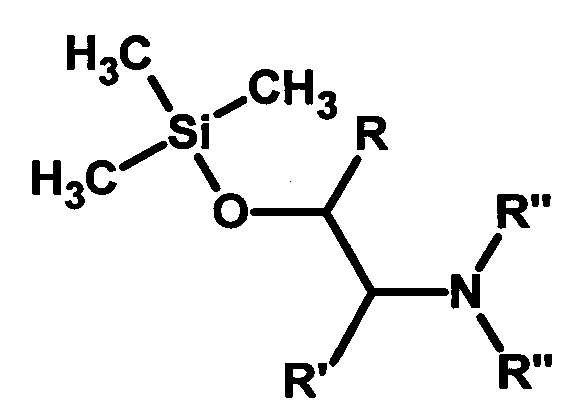 (I)
(I)
Способ получения силилоксиаминов общей формулы
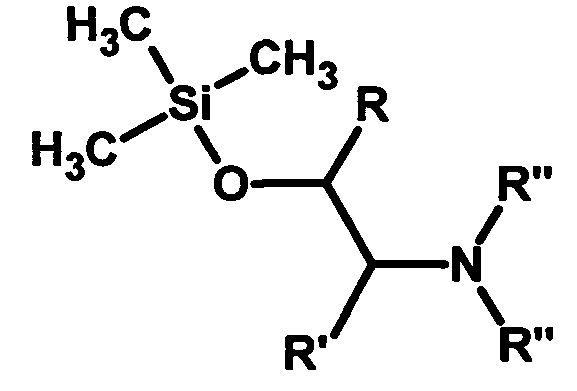
где R=CH2OAlk, R'=Н; R=R'=(СН2)4; R''=С2Н5, С3Н7,
включающий взаимодействие эпоксидных соединений с избытком аминосилана в среде органического растворителя в присутствии катализатора, отличающийся тем, что в качестве катализатора используют перхлорат магния, взаимодействие проводят в среде толуола при температуре 25-60°С в течение 20-40 мин, применяя избыток аминосилана в количестве 10 мол. %.
| Junes Ipaktschi, Akbar Heydari | |||
| Lithium perchlorate-catalyzed nucleophilic addition to α-chiral aldehydes, aldimines and oxiranes | |||
| Chem | |||
| Ber., 1993, 126(8), pp.1905-1912 | |||
| Abbas Ali Jafari, Moradgholi | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Способ получения кремнийорганических диаминов силоксанового ряда | 1970 |
|
SU303873A1 |
Авторы
Даты
2019-10-04—Публикация
2019-06-27—Подача