Область изобретения
Настоящее изобретение относится к методу обнаружения канцерогенеза в шейке матки. В частности, изобретение касается некоторых процедур диагностики рака шейки матки, которые интегрируют или замещают цитологические действия действиями из сферы молекулярной биологии, а также создания системы диагностики, прогнозирования и управления ВПЧ-индуцированных поражений шейки матки, в которой используются, в частности, аналитические методы вестерн-блоттинга и иммуноферментного теста (Sandwich ELISA) с целью выявления необратимых неопластических перерождений.
Предпосылки изобретения
Связь между вирусом папилломы человека (ВПЧ) и раком постоянно интересует исследователей. ВПЧ поражает базальные клетки плоского эпителия и вызывает образование доброкачественных поражений и/или, в некоторых случаях, инвазивных злокачественных опухолей. Вирион ВПЧ состоит из белковой оболочки (капсида), окружающей круговую двухцепочечную ДНК в кодирующих и некодирующих областях. В кодирующей области было обнаружено восемь ранних открытых рамок считывания (ОРС) (Е1-Е8) и две поздние ОРС (L1, L2). Ранние ОРС кодируют белки, участвующие в репликации вирусной ДНК в процессе пролиферации, регуляции экспрессии вирусного гена (Е2), сборке вируса (Е4), иммортализации и трансформации вируса (Е6 и Е7 только в ВПЧ с высоким риском). Поздние ОРС активируются только после дифференцировки клеток и кодируют вирусные белки капсида (L1 и L2). Промоутеры, усилители и другие регуляторные элементы расположены в некодирующей регуляторной области вирусного генома (URR).
Все типы ВПЧ развиваются и размножаются исключительно в кератиноцитах (или кератин-продуцирующих эпителиальных клетках), чья дифференцировка имеет решающее значение для развития вирусов. При прохождении через поражения в эпителиальных слоях ВПЧ достигает и поражает кератиноциты стволовых клеток, расположенных в базальном слое эпителия. Здесь вирус начинает репликацию с помощью механизмов клеточной репликации: клетка воспроизводит собственный геном несколько раз, сохраняя при этом низкий уровень вирусной нагрузки (до 50-300 копий). Когда базальные клетки пролиферируют и двигаются в направлении наружных слоев эпителия, вирусы также начинают двигаться и продолжают размножаться без дальнейшей амплификации генома, чтобы избежать обнаружения иммунной системой. Когда кератиноцит-хозяин достигает S-фазы дифференцировки (кератинизации), ВПЧ реплицирует свой геном примерно до 1000 копий. Фактически на данном этапе вирус выделяет белки Е6 и Е7, которые стимулируют переход клеток к S-фазе (Kadaja М, et al., Papillomavirus DNA replication - from initiation to genomic instability. Virology. 2009 Feb. 20; 384(2):360-8) (Кадажа M. и др., Репликация ДНК вируса папилломы - с начала до геномной нестабильности. Вирусология. 20 февраля 2009 г.; 384(2):360-8). И, наконец, когда кератиноцит достигает поверхностного эпителия и умирает, вирусный геном, переупакованный в капсид, выходит из клетки.
В промышленно развитых странах рак шейки матки - это тщательно контролируемая болезнь благодаря широкому применению мазка Папаниколау и особенно организованным программам скрининга. Фактически, это одно из немногих онкологических заболеваний, которые могут быть предотвращены путем раннего выявления и лечения преинвазивных поражений (интраэпителиальная неоплазия шейки матки, CIN). Путем цитологического исследования небольшого количества клеток, взятых из шейки матки, можно определить наличие аномалий в плоскоклеточном эпителии (SIL, плоскоклеточные интраэпителиальные поражения), которые классифицируются как ASC-US (атипичные клетки плоского эпителия неясного значения), ASC-H (атипичные клетки плоского эпителия - нельзя исключить высокодифференцированные плоскоклеточные интраэпителиальные поражения), LSIL (низкодифференцированные плоскоклеточные интраэпителиальные поражения), HSIL (высокодифференцированные плоскоклеточные интраэпителиальные поражения) и, наконец, «карцинома», когда раковые клетки уже присутствуют. Подсчитано, что мазок Папаниколау раз в три года в возрастной группе 35-65 лет может снизить риск развития инвазивного рака на 90% (IARC Working Group on the Evaluation of Cancer Preventive Strategies. IARC Handbooks of Cancer Prevention Vol. 10. Cervix Cancer Screening Lyon: IARC press, 2005) (Рабочая группа МАИР по оценке превентивных стратегий борьбы с раком. Справочники по профилактике рака МАИР, Том 10. Обследование для выявления рака шейки матки, Лион: IARC press, 2005 г.).
В последние десятилетия ВПЧ был признан необходимым, но не достаточным условием рака шейки матки (IARC Working Group 2005, loc. cit.) (Рабочая группа МАИР 2005 г., в цитированном отрывке). Рак может вызвать только хроническая инфекция ВПЧ, относящегося к типам высокого риска (Schiffman М., et al. Lancet. 2007; 370:890-907) (Шифман М. и др. Ланцет. 2007 г.; 370:890-907). Международное агентство по изучению рака (МАИР) недавно подтвердило свои заявления о канцерогенности некоторых типов ВПЧ (Straif KA, et al., on behalf of the WHO International Agency for Research on Cancer Monograph Working Group.Lancet Oncol, 2009; 10:321-322) (Страйф К.A. и др. от имени рабочей группы по монографиям Международного агентства ВОЗ по изучению рака. Ланцет, онкология, 2009 г.; 10: 321-322), и определили 12 типов высокого риска плюс один подозрительный тип, в то время как отношение к опухолям 12 других типов не определено. Этот важный шаг в изучении естественной истории болезни быстро привел к появлению двух новых профилактических средств: вакцины для предотвращения самой инфекции и теста для обнаружения ДНК штаммов ВПЧ с высоким онкогенным риском (тестирование на ДНК ВР-ВПЧ) для выявления женщин с риском развития или с возникшими преинвазивными поражениями. Тест на ДНК ВР-ВПЧ оказался более чувствительным, чем цитология при скрининге шейки матки (Arbyn J. et al. Vaccine. 2006; 24 Suppl 3: S3-78-89; Cuzick J. et al. Int J Cancer. 2006; 119:1095-1101) (Арбин Дж. и др. Вакцина. 2006 г.; 24 дополнение 3: S3-78-89; Кузик Дж. и др. Международный журнал по исследованию рака. 2006 г.; 119:1095-1101).
Тем не менее, неопластическое перерождение является редким осложнением инфекции ВПЧ высокого риска, которая в большинстве случаев является преходящим явлением. Кроме того, продемонстрировано, что низкодифферинцированные поражения (CTN 1, которые соответствуют LSIL в мазке Папаниколау), которые также связаны с ВПЧ-инфекцией, не могут рассматриваться как истинные преинвазивные поражения, поскольку в подавляющем большинстве случаев они спонтанно регрессируют (Schiffman М. et al. Lancet. 2007; 370:890-907) (Шифман М. и др. Ланцет. 2007 г.; 370:890-907). Следовательно, по этой причине тест на ДНК ВР-ВПЧ обладает низкой специфичностью (Cuzick J. et al. 2006, loc. cit.) (Кузик Дж. и др. 2006 г., в цитированном отрывке).
Рандомизированные контролируемые исследования показали эффективность тестов на ДНК ВР-ВПЧ в снижении смертности и заболеваемости раком шейки матки (Sankarana-rayanan R. et al. N Engl J Med. 2009; 360:1385-94; Bulkmans NW. et al. Lancet. 2007; 370:1764-7) (Санкарана-райанан П. и др. Медицинский журнал Новой Англии 2009 г.; 360:1385-94; Балкманс Н.В. и др. Ланцет. 2007 г.; 370:1764-7). Результаты этих исследований стимулировали проведение крупных доказательных исследований в Италии с использованием теста на ДНК ВР-ВПЧ в качестве основного скринингового исследования с последующим цитологическим исследованием положительных результатов (Confortini М. et al. J Med Screen. 2010; 17:79-86) (Конфортини M. и др. Журнал медицинских обследований 2010 г.; 17:79-86). Следует отметить, что регрессивными являются не только поражения CIN1; CIN2 и CIN3 (которые соответствуют HSIL в мазке Папаниколау) также часто регрессируют, особенно у молодых женщин (Schiffman М. et al. 2007, loc. cit.; Ronco G. et al. J Natl Cancer Inst, 2008; 100: 492-501) (Шифман M. и др. 2007 г., в цитированном отрывке; Ронко Г. и др. Журнал Национального института по изучению рака, 2008 г.; 100: 492-501).
Указанная особенность программ скрининга подразумевает, что некоторый процент гипердиагностики может объясняться самим скрининговым тестом; однако гипердиагностика, связанная с цитологическим скринингом раз в три года, считается приемлемой. Итальянское исследование NTCC (Новые технологии лечения рака шейки матки), начатое в 2004 году, показало, что тест на ДНК ВЧ-ВПЧ увеличивает как гипердиагностику, так и гиперлечение по сравнению с цитологией у женщин в возрасте до 35 лет, даже если цитологическая «сортировка» (т.е. «диагностическое исследование» положительных результатов теста на ДНК ВР-ВПЧ) проводится посредством мазка Папаниколау (Ronco G. et G. et al. 2008, loc. cit.; Ronco G. et al. Lancet Oncol, 2010 Jan18) (Ронко Г. и др. 2008 г., в цитированном отрывке; Ронко Г. и др. Ланцет, онкология 18 января 2010 г.). С другой стороны, продемонстрировано, что у женщин в возрасте старше 35 лет гипердиагноз, если таковой случается, имеет место редко, даже если не проводится отборочная цитология.
Вышеуказанные данные еще раз подчеркивают необходимость разработки конкретных биомаркеров для высокодифференцированной интраэпителиальной неоплазии шейки матки и рака, предназначенных для обнаружения молекулярных изменений, тесно связанных с трансформацией, а не простого обнаружения инфекций с ДНК ВР-ВПЧ. Избирательность еще более актуальна, когда группы женщин, вакцинированные против ВПЧ, проходят скрининг (Franco EL. et al. Vaccine. 2006; 24 Suppl 3:S171-7) (Франко Е.Л. и др. Вакцина. 2006 г.; 24 дополнение 3:S171-7).
В настоящее время единственными готовыми к использованию биомаркерами являются те, которые прямо или косвенно связаны с экспрессией вирусных генов Е6 и Е7, регулирующих репликацию ВПЧ. Гены Е6 и Е7, относящиеся к генотипам высокого риска, известны как онкогены, и их измененная транскрипционная регуляция, которая затрагивает почти все клеточные пути (Fehrmann F, Laimins LA. Oncogene. 2003; 22:5201-7) (Ферманн Ф., Лейминс Л.А. Онкоген. 2003 г.; 22:5201-7) и способствует нестабильности ДНК, выглядит необходимым шагом для трансформации клеток в злокачественные. Экспрессия онкогенов ВПЧ и ее влияние на клетку-хозяина можно непосредственно отследить путем выявления транскриптов мРНК вирусных Е6-Е7 (Lie AK, Kristensen G., Expert Rev Mol Diagn. 2008; 8:405-15) (Ли А.К., Кристенсен Г., Экспертная оценка молекулярной диагностики. 2008 г.; 8:405-15), или косвенно, путем обнаружения клеточного белка р16 (Carozzi F. et al., Lancet Oncol. 2008, 9:937-945; Benevolo M. et al. Am J Clin Pathol. 2008; 129:606-12) (Кароцци Ф. и др., Ланцет, онкология. 2008 г., 9:937-945; Беневоло М. и др. Американский журнал клинической патологии. 2008 г.; 129:606-12). Последний, как известно, является белком, участвующим в контроле клеточного цикла, который сверхэкспрессируется в цервикальных клетках, трансформированных ВПЧ. Фактически, как широко известно, экспрессия р16 стимулируется белком Е7 ВЧ-ВПЧ, и его повышающая регуляция в шейке матки в значительной степени связана с увеличением степени тяжести поражений (Benevolo М. et al., Mod Pathol. 2006 Mar;19(3):384-9) (Беневоло M. и др. Современная патология. Март 2006 г.;19(3):384-9).
Тем не менее иммуногистохимическая оценка р16 в настоящее время отличается ограниченной воспроизводимостью из-за отсутствия стандартных критериев для интерпретации иммунного окрашивания (Tsoumpou I., et al., p16(INK4a) immunostaining in cytological and histological specimens from the uterine cervix: a systematic review and metaanalysis, Cancer Treat Rev. 2009; 35:210-20) (Цумпу И. и др., р16 (INK4a) цитологических и гистологических образцов из шейки матки: систематический обзор и мета-анализ, Обзор лечения рака, ред. 2009 г.; 35:210-20). Что касается Е6-Е7, мРНК ВПЧ может быть перспективным биомаркером для выявления клинически значимых инфекций ДНК ВР-ВПЧ благодаря тесту полностью in vitro. Фактически, было замечено, что мРНК Е6-Е7 возрастает с увеличением тяжести заболевания шейки матки (Sotlar K. et al., J Med Virol. 2004; 74:107-16; Castle PE. et al., Clin Cancer Res. 2007; 13:2599-605) (Сотлар К. и др., Журнал медицинской вирусологии. 2004 г.; 74:107-16; Касл П.Е. и др., Клинические исследования рака. 2007 г.; 13:2599-605). Сообщалось, что оба теста - р16 и мРНК Е6-Е7 - являются немного менее чувствительными, чем ДНК ВЧ-ВПЧ, но гораздо более конкретными (Carozzi F. et al., Lancet Oncol. 2008, 9:937-945; Szarewski A. et al., Cancer Epidemiol Biomarkers Prev. 2008; 17:3033-4; Monsonego J. et al. EUROGIN 2010, Monaco. ES 4-4) (Кароцци Ф. и др., Ланцет, онкология. 2008 г., 9:937-945; Шаревски А. и др., Онкологическая эпидемиология, биомаркеры и профилактика. 2008 г.; 17:3033-4; Монсонего Дж. и др. EUROGIN 2010 г., Монако. ES 4-4).
Упомянутое выше направление исследования (обнаружение транскриптов мРНК вирусных Е6-Е7) включает, например, европейские патенты ЕР 1463839, ЕР 1718774 и ЕР 2267155 (Norchip A/S) и патент США US 7524631 (Patterson).
Однако до сих пор отсутствуют биологические маркеры, указывающие на необратимую трансформацию предраковых поражений в рак шейки матки (Koo YJ. et al., Dual immunostaining of cervical cytology specimens with atypical squamous cells for p16/Ki-67 does not exclude the existence of a high-grade squamous intraepithelial lesion. Virchows Arch. 2013 Oct 1; Pacchiarotti A. et al., Prognostic value of p16-INK4A protein in women with negative or CIN1 histology result: A follow-up study. Int J Cancer. 2014, 134, 897-904) (Коо Ю.Дж. и др., Двойное иммунное окрашивание цитологических образцов с атипичными плоскими клетками для p16/Ki-67 не исключает существование высокодифференцированного плоскоклеточного интраэпителиального поражения. Архив Вирхова. 1 октября 2013 г.; Паккиаротти А. и др., Прогностическое значение белка p16-INK4A у женщин с отрицательным гистологическим результатом или CIN1: Контрольное исследование. Международный журнал по исследованию рака. 2014 г., 134, 897-904).
Краткое изложение сущности изобретения
В рамках исследований, связанных с настоящим изобретением, рассматривалось взаимодействие двух вирусных онкогенов - Е6 и Е7 - с генами-онкосупрессорами р53 и pRB клетки-хозяина. Известно, что онкобелок Е6 связывается с онкосупрессивным белком р53 клетки-хозяина, вызывая его деградацию и разрушая активность, направленную на остановку роста и активацию апоптоза, типичную для этого онкосупрессора. Аналогичным образом, онкогенный белок Е7 образует комплексы и инактивирует pRb белка клетки-хозяина, тем самым угнетая его онкосупрессивную активность (Ishiji Т., Molecular mechanism of carcinogenesis by human papillomavirus-16. J Dermatol 2000, Feb; 27(2):73-86L; Buitrago-Perez A. et al., Molecular Signature of HPV-Induced Carcinogenesis; pRb, p53 and Gene Expression Profiling. Curr Genomics. 2009 Mar;10(1): 26-34; Shaikh F. et al., Molecular screening of compounds to the predicted Protein-Protein Interaction site of Rb1-E7 with p53-E6 in HPV. Bioinformation. 2012; 8(13): 607-12) (Ишижи Т., Молекулярный механизм канцерогенеза вируса папилломы человека-16. Дерматологический журнал. Февраль 2000 г.; 27(2):73-86L; Битраго-Перез А. и др., Молекулярные признаки канцерогенеза, вызванного ВПЧ; pRb, р53 и профилирование экспрессии генов. Современная геномика. Март 2009 г.; 10(1): 26-34; Шайх F. и др., Молекулярный скрининг соединений по отношению к прогнозируемому участку белок-белкового взаимодействия Rb1-E7 с р53-Е6 в ВПЧ. Биоинформация. 2012 г.; 8(13): 607-12).
В частности, экспрессия генов Е6 и Е7 и последующее образование родственных белков были бы необходимой причиной, вызывающей ВПЧ-индуцированный онкогенез, который характеризуется взаимодействием между белками Е6 и р53 и белками Е7 и pRb, соответственно. Е6 связывается с р53 в цитоплазме, а также задействует убиквитинлигазу Е6АР, что делает р53 мишенью для протеасомной деградации. Аналогично, Е7 связывается с pRb в цитоплазме и задействует убиквитинлигазу Cullin2, что, в свою очередь, способствует протеасомной деградации.
В соответствии с настоящим изобретением обнаружена возможность определения с помощью относительно простых исследований момента канцерогенеза путем обнаружения присутствия этих белков, которые, на основе взаимодействия вирусных онкогенов Е6 и Е7 с генами-супрессорами опухолей р53 и pRB клетки-хозяина, представляют индекс необратимого неопластического перерождения. Для выполнения функции отбора в случаях неопластического перерождения по сравнению с теми, в которых, несмотря на возникновение высокодифференцированных поражений, процесс канцерогенеза все еще обратим, предлагаемые в изобретении исследования должны проводиться в рамках диагностической процедуры программ скрининга или ранней диагностики рака шейки матки после положительного результата теста на ДНК ВР-ВПЧ и/или цитологической диагностики атипии плоских клеток (ASC) или худших показателей. Предлагаемый тест предпочтительно должен выполняться после теста на ДНК ВР-ВПЧ и мазка Папаниколау с положительными результатами.
Процедура, предложенная в соответствии с изобретением, модернизирует клиническое ведение женщин с диагнозом высокодифференцированных диспластических поражений шейки матки, связанных с ВПЧ-инфекцией. По существу, она сводится к использованию конкретных технологий для анализа белков, кодируемых вирусными онкогенами (Е6 и Е7), и белков, кодируемых генами-супрессорами клетки-хозяина (р53 и pRb), их категоризации и измерения в соответствии с фазами интеграции и/или взаимодействия генома вируса в клетке-хозяине. Как уже отмечалось, специфика предложенной процедуры заключается в определении статуса необратимости неопластического перерождения за счет взаимодействия вирусных белков с белками человека.
При осуществлении предложенного способа в соответствии с изобретением поиск белков, возникших в результате взаимодействия Е6 с р53 (в частности, белкового комплекса Е6/р53) и взаимодействия Е7 с pRb (в частности, белкового комплекса E7/pRB) может выполняться при помощи любого аналитического метода, который позволяет простым, но надежным способом выявить формирование одного или обоих указанных белковых комплексов в образце клеток, взятых из плоскоклеточного-цилиндроклеточного стыка эпителия шейки матки, полученном при обследовании пациентки. Более конкретно, используемый аналитический метод должен позволять обнаружение в образце белка Е6 или белка Е7 в сочетании с белковым комплексом, который содержит, соответственно, белок Е6 или белок Е7 вместе с белком р53 или pRB. На практике существуют два способа, наиболее подходящие для этой цели: А) аналитический метод вестерн-блоттинга и В) иммуноферментный анализ (Sandwich ELISA).
A) Вестерн-блоттинг: берется новый образец из шейки матки, который хранится в изотоническом растворе натрия хлорида при температуре 4-8°С. Затем он анализируется в соответствии с биохимическим методом, известным как Вестерн-блот (иммуноблот). Этот метод используется для обнаружения белка в образце гомогената ткани или клеточного экстракта. Он предусматривает центрифугирование образца с выделением супернатанта и, следовательно, разделение белков, ранее денатурированных на основе их молекулярной массы с помощью электрофореза в полиакриламидном геле в присутствии натрия додецилсульфата (SDS-PAGE). Затем белки переносятся из геля на мембрану, как правило, из нитроцеллюлозы, где они распознаются и связываются со специфическими антителами.
B) Sandwich ELISA: берется новый образец из шейки матки в жидкой фазе (ThinPrep -Hologic, Inc., Мальборо, штат Массачусетс, или SurePath - BD Diagnostics, Бурлингтон, Северная Каролина), если он еще не брался для предыдущих исследований; в противном случае используется остаточный образец. Образец анализировали посредством иммуноферментного анализа Sandwich ELISA. Это метод иммунологического анализа, используемый в биохимии для обнаружения присутствия вещества с помощью одного или более антител, с одним из которых связывается фермент: в зависимости от обнаружения интересующего белка, данный метод предполагает прямой перенос цервикального образца на должным образом подготовленную реакционную пластину со специфическими антителами к белку Е6 и белку Е7, а затем анализ с использованием других специфических антител-анти-р53-белков и анти-pRb-белков для обнаружения взаимодействия представляющих интерес белковых комплексов.
В соответствии с настоящим изобретением методы вестерн-блоттинга и Sandwich ELISA применяются с использованием специфических моноклональных антител - антител к белку Е6 и антител к белку Е7 из штаммов ВПЧ высокого онкогенного риска, антител анти-р53-белков, антител анти-pRb-белков, имеющихся на рынке. Эти методы дают возможность не только определить наличие четырех белков, представляющих интерес, но и выявить возможное взаимодействие между Е6 и р53 (Е6/р53), а также между Е7 и pRb (E7/pRB), которое представляет собой точку необратимого перерождения предраковых поражений в карциному шейки матки.
Поиск этих белков у женщин с диагнозом цитологической атипии плоских клеток (ASC) или худшим диагнозом, предлагаемый в соответствии с настоящим изобретением, позволяет повысить диагностическую точность теста на ДНК ВР-ВПЧ и отбора по мазку Папаниколау с увеличением общей чувствительности и специфичности скрининга. В частности, такой поиск приведет к увеличению прогностической ценности положительного результата скрининга (которая представляет собой соотношение истинно положительных субъектов и общего количества всех положительных субъектов, как истинных, так и ложных), и уменьшения гипердиагностики и гиперлечения.
Подробное описание изобретения
В соответствии с наиболее широким вариантом настоящее изобретение в частности относится к способу обнаружения неопластического перерождения клеток, вызываемого вирусом папилломы человека (ВПЧ) у женщин, проходящими скрининг на рак шейки матки, включающему обнаружение в образцах клеток, взятых из плоскоклеточного-цилиндроклеточного стыка эпителия шейки матки, белкового комплекса Е6/р53, формирующегося из белка Е6 и белка р53, и/или белкового комплекса E7/pRb, формирующегося из белка Е7 с белком pRb, согласно которому один из указанных двух белковых комплексов показывает, что у обследуемой пациентки канцерогенез перешел в необратимую форму; указанное обнаружение выполняется на основе комбинированного использования антител к белку Е6 и антител к белку Е7 и, предпочтительно, антител к белку р53 и антител к белку pRb, предпочтительно с использованием аналитических методов вестерн-блоттинга или Sandwich ELISA.
В соответствии с обычной методикой, процедура А) вестерн-блоттинга для обнаружения взаимодействия Е6/Е7 и p53/pRB состоит из следующих этапов: (а) подготовка образцов (например, гомогенизация/экстракция, центрифугирование и кипячение для денатурации белков в буфере для образцов); (b) гель-электрофореза; (с) перенос на мембрану; (d) блокирование неспецифических участков мембраны, как правило, бычьим альбумином (БСА) или молоком; (е) выявление искомого белка путем инкубации с антителами (одним первичным и одним распознающим антиген, за которым следует вторичное, конъюгированное с системой обнаружения, которая распознает первичное); (f) определение связывающего антитела-антигена, как правило, с помощью колориметрической реакции или хемилюминесценции.
Таким образом, настоящее изобретение, в частности, дополнительно относится к способу обнаружения неопластического перерождения клеток, вызванного вирусом папилломы человека (ВПЧ) у женщин, проходящих скрининг на рак шейки матки, включающему следующие операции в соответствии с методикой вестерн-блоттинг:
a) подготовка образца клеток, взятых из плоскоклеточного-цилиндроклеточного стыка эпителия шейки матки обследуемой пациентки и его помещение в физиологический раствор;
b) извлечение белков из указанного образца и денатурирование полученных белков;
c) обработка полученных таким образом денатурированных белков электрофорезом в полиакриламидном геле;
d) перенос белков, полученных во время предыдущей операции, на мембрану и нейтрализация свободных участков указанной мембраны;
e) идентификация указанных белков путем их инкубации по меньшей мере со следующими антителами:
первичным моноклональным антителом к белку Е6;
первичным моноклональным антителом к белку Е7;
с последующей инкубацией с вторичными антителами анти-IgG, конъюгированными с биотином или ферментом-посредником, таким как щелочная фосфатаза;
f) проведение колориметрического анализа или хемилюминесценции продуктов, полученных в результате предыдущей операции;
отличающейся тем, что результаты упомянутого анализа, демонстрирующие двойную полосу реакции по меньшей мере для одного из белков Е6 (с молекулярной массой 18 кДа) и Е7 (с молекулярной массой 16 кДа), где указанная двойная полоса содержит первую полосу, соответствующую молекулярной массе искомого белка, т.е. Е6 или Е7, а вторая полоса соответствует молекулярной массе, отличающейся и превышающей молекулярную массу соответствующего белка первой полосы, указанная молекулярная масса по существу равна 71 кД для белкового комплекса Е6/р53 и 115,5 кД для белкового комплекса E7/pRB, показывают, что канцерогенез обследуемой пациентки стал необратимым. Фактически, молекулярная масса, соответствующая второй полосе, которая проявляется в этих случаях, по существу равна сумме молекулярных масс р53 и Е6 или Е7 и pRb, что указывает на истинный характер и взаимодействие между двумя белками пары.
В предпочтительном варианте в соответствии с изобретением эти результаты упомянутого обнаружения в соответствии со стадией f), показывающие двойную полосу реакции, как описано выше, как для белка Е6, так и для белка Е7, рассматриваются, для большей безопасности, как свидетельство уже установленного канцерогенеза.
В соответствии с предпочтительным вариантом осуществления настоящего изобретения в фазе е) вышеуказанные белки также инкубировали со следующими антителами: первичным моноклональным антителом к белку р53; первичным моноклональным антителом к белку pRb;
дальнейшие операции аналогичны тем, которые проводились в случае инкубации с указанными первичными моноклональными антителами к белку Е6 и к белку Е7, в которых результаты упомянутого анализа, показывающие двойную полосу реакции по меньшей мере для одного из белков р53 и pRb, где указанная двойная полоса, содержащая первую полосу, соответствующую молекулярной массе искомого белка р53 или pRb, и вторая полоса, соответствующая молекулярной массе, отличающейся и более высокой, чем молекулярная масса соответствующего белка первой полосы, показывают, что у обследуемой пациентки канцерогенез стал необратимым. Молекулярная масса, соответствующая второй полосе, которая проявляется в этих случаях, также в этом случае примерно равна сумме молекулярных масс р53 и Е6 или Е7 и pRb, что указывает на истинное взаимодействие между двумя белками пары.
Как уже отмечалось, взаимодействие между белками Е6 и р53 и между белками Е7 и pRb вызывают де-факто деградацию р53 и pRb. Учитывая то, что р53 вызывает остановку клеточного цикла в фазе G1 или запускает механизмы апоптоза, что обеспечивает подавление клонов опухолевых клеток и стабильность генома, и pRb представляет собой белок, подавляющий активность, связанную с ростом клеток, понятно, как взаимодействие между Е6 и р53 и Е7 и pRb и последующая деградация де-факто приводят к прекращению нормальной регуляторной функции двух генов, что, вероятно, становится пусковым механизмом для неопластического перерождения клетки.
В соответствии со способом согласно изобретению, результаты упомянутого анализа в виде одной полосы реакции на белки Е6 и Е7 (где одна полоса соответствует молекулярной массе искомого белка Е6 или Е7) показывают, что у обследуемой пациентки канцерогенез еще не начался или еще не стал необратимым. Согласно тому же критерию, если результаты анализа не показывают какой-либо полосы реакции для белков Е6 и Е7, это означает, что у обследуемой пациентки отсутствует интеграция ДНК вируса с ДНК клеток.
В предпочтительном варианте в соответствии с изобретением вторичные антитела-анти-IgG указанной стадии е) конъюгированы с щелочной фосфатазой, а также анализ на стадии f) является колориметрическим или хемилюминесцентным анализом. Кроме того, в соответствии с предпочтительными вариантами осуществления изобретения, указанные выше первичные моноклональные антитела к белку Е6 и к белку Е7 являются мышиными моноклональными антителами, направленными против белка Е6 или белка Е7 вирусного типа HPV16 и HPV18.
Также в соответствии с предпочтительными вариантами осуществления изобретения, первичное моноклональное антитело к белку р53 представляет собой мышиное моноклональное антитело к белку р53 человека, и первичное моноклональное антитело к pRb-белку представляет собой мышиное моноклональное антитело к белку pRb человека.
Как было отмечено ранее, диагностический способ в соответствии с изобретением предпочтительно включается в скрининг женского населения на выявление рака шейки матки после получения положительного результата теста на ДНК ВР-ВПЧ и/или после цитологической диагностики атипии плоских клеток (ASC) или худшего диагноза.
В соответствии с конкретным вариантом осуществления способа изобретения, предлагаемый анализ предусматривает процесс получения эпителиальных клеток из плоскоклеточного-цилиндроклеточного стыка эпителия шейки матки предпочтительно с помощью инструмента, известного как «цитощетка» (одноразовый инструмент с щеткой на конце для взятия эндоцервикальных клеток для цитологического исследования, со щетинками, расположенными в радиальном винтообразном направлении вокруг собственной оси, сужающийся к концу и имеющий коническую общую форму). Образец, полученный таким образом, хранится в физиологическом растворе (1 мл) при 4°С и из него извлекают исследуемые белки и проводят анализ путем вестерн-блоттинга.
Клеточный осадок, полученный путем центрифугирования образца, дважды промывают раствором хлорида натрия 0,9% по весу. После центрифугирования при 5000 оборотах в минуту в течение 5 минут клетки собирают в буфере для лизиса, и после добавления ингибиторов протеазы выпускают при перемешивании в течение 30 минут при температуре 4°С. Лизат затем центрифугируют в течение 20 минут при 14000 оборотах в минуту при температуре 4°С, чтобы извлечь белки из супернатанта. Белки, полученные таким образом, анализируют с помощью электрофореза в полиакриламидном геле в присутствии додецилсульфата натрия (SDS-PAGE) после тепловой денатурации (при 95°С в течение 5 минут) в определенном буфере. Белки переносят на мембрану Poly Screen (DuPont NEN).
Восстановленный гель и мембрану погружают на 15 минут в два отдельных лотка с буфером для блоттинга, подготавливая «сэндвич» путем размещения компонентов в определенной последовательности. Для этой цели может быть использована система полусухого иммуноблоттинга или aicos-Denmark. Для подтверждения переноса мембрана предпочтительно окрашивается красной краской Panceau на платформе планшетного шейкера в течение 5 минут, затем промывается деионизированной водой.
Опять же, в соответствии с вышеупомянутым конкретным вариантом осуществления, выполняется нейтрализация свободных участков мембраны и последующий анализ исследуемых белков. Мембрану, подготовленную с использованием отмывочного буфера, содержащего 2% молоко, анализируют на содержание белка с использованием следующих моноклональных первичных антител в течение 90 минут при непрерывном перемешивании:
■ для белка Е6, мышиное первичное моноклональное антитело к белку Е6 (антитело HPV16 E6 + HPV18 Е6 [CIP5], Abcam);
■ для белка Е7, мышиное первичное моноклональное антитело к белку Е7 (антитело HPV16-E7 [№28-0006], Invitrogen Corporation);
■ для белка р53, мышиное первичное моноклональное антитело к белку р53 (антитело-анти-р55 [№ АНО0112], Invitrogen Corporation); и
■ для белка pRb, мышиное первичное моноклональное антитело к белку Rb (антитело к белку Rb человека [№554162], BD Biosciences).
Выполняется инкубация вторичных мышиных антител-анти-IgG; затем выполняется промывка и подготовка реакций с фосфатазой для обнаружения вирусных онкобелков Е6 и Е7 и их возможного взаимодействия соответственно с белками р53 и pRb, интерпретации результатов, как показано на рисунке.
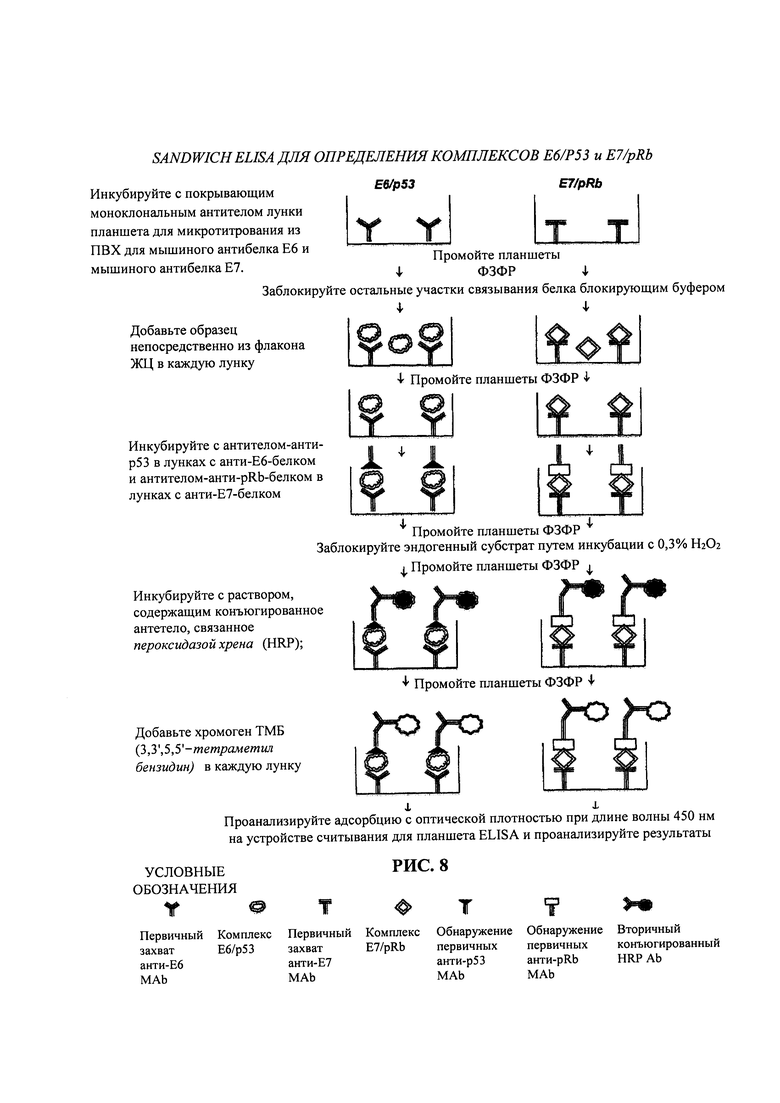
В соответствии с обычной методикой, процедура В), в которой используется метод Sandwich ELISA для обнаружения взаимодействий Е6/Е7 и p53/pRb, следуя научной концепции, относящейся к настоящему изобретению, уже указанной для метода А) вестерн-блоттинга, состоит из следующих этапов: (а) идентификация сохраненного образца в соответствии с используемым жидкофазным методом (ЖЦ); (b) адсорбция в разных лунках титрационного микропланшета иммобилизованных антител белков Е6 или Е7; (с) блокировка остальных участков связывания белков в лунке с помощью блокирующего буфера; (d) дозирование образца непосредственно из аппарата для ЖЦ в каждую лунку; (е) идентификация представляющих интерес белков путем инкубации с разведенными антителами-анти-р53-белками в лунках, адсорбированными с антителами к белку Е6, и разведенными антителами к белку Rb в лунках, адсорбированными с антителами-анти-Е7-белками; (f) блокировка эндогенного субстрата раствором 0,3% Н2О2 в метаноле; (g) инкубирование в соответствующих лунках антитела, конъюгированного с пероксидазой хрена (HRP); (h) дозирование раствора хромогена ТМБ (3,3',5,5'-тетраметилбензидин) в каждую лунку; (i) чтение результатов путем дискретизации голубоватого цвета в спектрофотометре при длине волны 450 нм.
Для подтверждения правильности результатов анализа вышеуказанные операции выполняются в двух отдельных лунках, которые различаются по типу первичного антитела, которое вводится вначале: одна лунка заполнена специфическим антителом к белку (Е6 или Е7), который должен быть идентифицирован, а другая - неспецифическим антителом. Чтобы анализ считался действительным, во-первых, результат во второй лунке должен быть отрицательным, и в том случае, когда анализируемый биологический образец фактически содержит искомое антитело, результат также должен быть положительным в другой лунке, насыщенной первичным антителом, специфичным для искомого белка.
Таким образом, настоящее изобретение, в частности, дополнительно относится к способу обнаружения неопластического перерождения клеток, вызванного вирусом папилломы человека (ВПЧ) у женщин, проходящих скрининг на рак шейки матки, включающему следующие операции в соответствии с методикой Sandwich ELISA:
a) идентификация образца клеток, полученных из плоскоклеточного-цилиндроклеточного стыка эпителия шейки матки обследуемой женщины, хранящегося в растворе в соответствии с используемым методом жидкостной цитологии (ЖЦ);
b) адсорбция в разных лунках микропланшета в ПВХ иммобилизованных антител белков Е6 и Е7 путем инкубации при 4°С в течение ночи и последующее промывание в фосфатном забуференном физиологическом растворе (ФЗФР);
c) блокирование остальных участков лунки, связывающих белки, с помощью блокирующего буфера, содержащего обезжиренное сухое молоко в ФЗФР с инкубацией по меньшей мере в течение 1-2 часов при комнатной температуре или в течение ночи при 4°С;
d) дозирование 100 мкл образца из бутылки с жидкой фазой цитологического образца непосредственно в каждую лунку с инкубацией при 37°С в течение 90 минут и удаление с дополнительной промывкой в ФЗФР;
e) идентификация искомых белков путем инкубации со 100 мкл разведенного антитела к белку р53 в лунках, адсорбированных с антителом к белку Е6, и 100 мкл разведенного антитела к белку pRb в лунках, адсорбированных с антителом к белку Е7, при комнатной температуре в течение 1-2 часов и удаление с последующей многократной промывкой в ФЗФР;
f) блокирование эндогенного субстрата путем инкубации при комнатной температуре в течение 20 минут с 0,3% раствором Н2О2 в метаноле;
g) инкубация в соответствующие лунки 100 мкл раствора, содержащего антитело, конъюгированное с пероксидазой хрена (HRP);
h) дозирование раствора хромогена ТМБ в каждую лунку в течение 20 минут (ферментативная реакция: Н2О2 + восстановленный субстрат ->2 Н2О + окисленный субстрат) и блокирование реакции путем добавления 2М раствора Н2О2;
i) продукт реакции на стадии h) изучается по интенсивности света, обнаруживаемого при длине волны 450 нм с помощью спектрофотометра,
при этом результаты, демонстрирующие окрашивание и подтвержденные положительной абсорбцией, показывают, что у обследуемой пациентки присутствует белковый комплекс Е6/р53 и/или E7/pRB, подтверждающий взаимодействие между белками вируса и человеческими белками, и, следовательно, наличие необратимого канцерогенеза.
Для подтверждения правильности результатов анализа вышеуказанные операции выполняются в двух отдельных лунках, которые различаются по типу первичного антитела, которое вводится вначале: одна лунка заполнена специфическим антителом к белку (Е6 или Е7), который должен быть идентифицирован, а другая - неспецифическим антителом. Анализ считается действительным, если он дает отрицательный результат в последнем блоке и положительный результат в блоке, насыщенном первичным антителом, специфичным для искомого белка.
В соответствии со способом, изложенным в изобретении, для стадий е), f), g) и h) можно использовать и другие имеющиеся на рынке системы, которые позволяют усилить хромогенный сигнал (например, с использованием антител-анти-р53 или белка pRb, биотинилированного и выделенного стрептавидином, конъюгированного с пероксидазой или другим ферментом).
В предпочтительном варианте в соответствии с изобретением результаты, которые с большей безопасностью считаются признаком уже установленного канцерогенеза это результаты указанного обнаружения в соответствии со стадией i), показывающие значения абсорбции, обнаруженные как для комплекса Е6/р53, так и для комплекса E7/pRb.
В соответствии со способом согласно изобретению, результаты этого обнаружения, демонстрирующие положительную реакцию для обоих белковых комплексов (Е6/р53 и E7/pRb) показывают, что у обследуемой пациентки канцерогенез уже начался и стал необратимым. В соответствии с тем же критерием, если результаты не показывают никакой положительной реакции (т.е. абсорбция сигнала отсутствует) для обоих белковых комплексов (Е6/р53 и E7/pRb), это означает, что у обследуемой пациентки отсутствует взаимодействие вирусной ДНК с ДНК клеток; однако это не исключает возможности взаимодействия вирусной ДНК с ДНК клеток, не диагностируемого на основе этой процедуры.
В предпочтительном варианте в соответствии с изобретением антитела на указанной стадии е) выявляются по реакции со специфическим антителом, конъюгированным с пероксидазой хрена, и обнаружение в фазах f), g) и h) является обнаружением колориметрического типа. Кроме того, в соответствии с предпочтительными вариантами осуществления изобретения, указанные выше первичные моноклональные антитела к белку Е6 и к белку Е7 являются мышиными моноклональными антителами, направленными против белка Е6 или белка Е7 вирусного типа HPV16 и HPV18.
Также в соответствии с предпочтительными вариантами осуществления изобретения, первичное моноклональное антитело к белку р53 представляет собой мышиное моноклональное антитело к р53-белку человека, и первичное моноклональное антитело к pRb-белку представляет собой мышиное моноклональное антитело к белку pRb человека.
Как было отмечено ранее, диагностический способ в соответствии с изобретением предпочтительно включается в скрининг женского населения на выявление рака шейки матки после получения положительного результата теста на ДНК ВР-ВПЧ и/или после цитологической диагностики атипии плоских клеток (ASC) или худшего диагноза.
В соответствии с конкретным вариантом осуществления метода по изобретению, предлагаемый анализ предусматривает процесс получения эпителиальных клеток плоскоклеточного-цилиндроклеточного стыка эпителия шейки матки предпочтительно с помощью инструмента, известного как «цитощетка». Образец, полученный таким образом, сохраняется в растворе для жидкостной цитологии, а затем выполняется анализ искомых белков по методу Sandwich ELISA.
Тем не менее, в соответствии с вышеприведенным конкретным вариантом осуществления, клетки, содержащиеся в образце для жидкостной цитологии, анализируются непосредственно, без экстракции белков, с помощью реакции антител типа «сандвич»: вирусное антитело к белку (Е6 или Е7), адсорбированное в планшете, искомый комплекс белков (Е6/Е7 или p53/pRb), присутствующий в образце, антибелок (р53 или pRb) человека. Метод обеспечивает абсолютную специфичность связывания и документальное подтверждение наличия белковых комплексов Е6/р53 и E7/pRb с использованием следующих первичных моноклональных антител:
■ для белка Е6, мышиное первичное моноклональное антитело к белку Е6 (антитело HPV16 E6 + HPV18 Е6 [CIP5], Abcam);
■ для белка Е7, мышиное первичное моноклональное антитело к белку Е7 (антитело HPV16-E7 [№28-0006], Invitrogen Corporation);
■ для белка р53, мышиное первичное моноклональное антитело к белку р53 (антитело-анти-р53 [№ АНО0112], Invitrogen Corporation); и
■ для белка pRb, мышиное первичное моноклональное антитело к белку Rb (антитело к белку Rb человека [№554162], BD Biosciences).
Последующая инкубация с мышиными антителами анти-IgG, конъюгированными с пероксидазой, и подготовка колориметрической реакции, документально подтвержденной спектрофотометрическими показателями, подтверждают положительные результаты исследований интересующего белкового комплекса с интерпретацией результатов, о которой говорилось выше.
В частности, настоящее изобретение предусматривает, в более общем смысле, модель диагностического метода для обнаружения любого опухолевого перерождения, индуцированного взаимодействием любого белка с онкогенным действием (например: BRAF, KRAS, NRAS, HER2 и т.д.) с другим белком, связанным с подавлением опухолевых клеток (например, р53, pRb, PTEN, BRCA, CD95 и т.д.), участвующим в работе различных органов и систем организма.
В частности, эти белки с онкогенным действием или белки, подавляющие опухолевый рост, идентифицируются с помощью специфичных моноклональных антител, и их взаимодействие доказывается посредством метода вестерн-блоттинга и/или ELISA Sandwich. Предпочтительно в соответствии с предлагаемыми способами также идентифицируется белковый комплекс (онкогенный белок/белок-супрессор опухолей), который взаимодействовал непосредственно со специфическими моноклональными антителами.
В целом, следовательно, изобретение позволяет предложить метод обнаружения любого неопластического перерождения клеток, вызванного взаимодействием любого белка с онкогенным действием с другим белком, связанным с клеточной активностью по подавлению роста опухоли, в соответствии с описанием выше; при этом указанный метод также используется в рамках диагностической программы и/или терапевтического лечения онкологических больных или пациентов с подозрением на рак с использованием целевой терапии, ингибирующей взаимодействие указанных белков.
Краткое описание рисунков
Конкретные элементы настоящего изобретения и его преимущества становятся более очевидными благодаря описанию экспериментальной работы, представленному исключительно в иллюстративных целях на следующих рисунках:
На Рис. 1 показана гистограмма с цитологической диагностикой 78 положительных случаев из 2500 женщин, проходивших скрининг с выполнением мазка Папаниколау.
На Рис. 2 показана гистограмма с результатами применения диагностического метода в соответствии с настоящим изобретением в 78 положительных случаях по результатам мазка Папаниколау из Рис. 1.
На Рис. 3-6 показаны результаты вестерн-блоттинга одного случая из результатов, полученных с использованием диагностического метода согласно настоящему изобретению, в котором присутствуют белки Е6 и Е7, и в котором присутствует взаимодействие между Е6/р53 и E7/pRb.
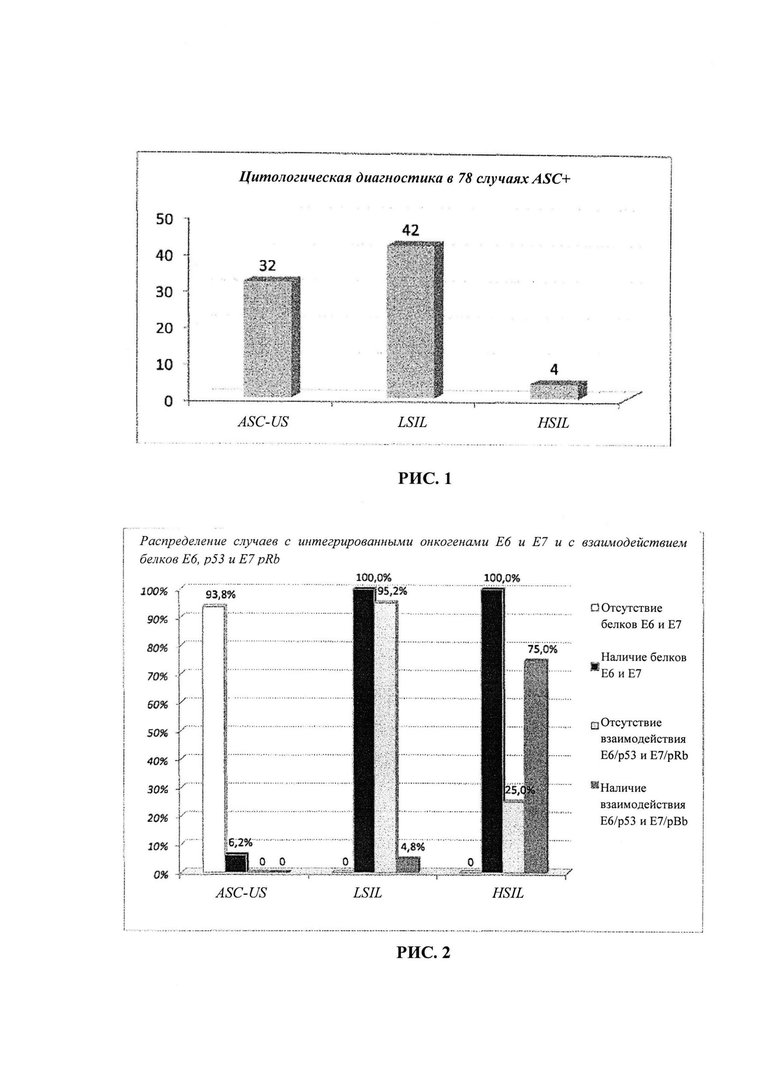
На Рис. 7 представлена блок-схема, иллюстрирующая показания для женщин с положительным результатом мазка Папаниколау и положительным результатом анализа на ДНК ВР-ВПЧ к применению диагностического способа согласно изобретению.
На Рис. 8 представлена блок-схема, иллюстрирующая применение метода Sandwich ELISA при использовании диагностического метода согласно изобретению.
Скрининговый анализ в популяции женщин, которым не делается мазок Папаниколау в качестве первичного обследования
В контексте настоящего изобретения было проведено исследование с целью выявления у женщин с клинически значимыми поражениями, у которых развились высокодифференцированные диспластические поражения или рак шейки матки. Исследование было проведено на 2500 цервикальных образцах женщин, полученных спонтанно в медицинских консультативных поликлиниках центров местного совета здравоохранения Caserta ASL. Исследование проводилось в период с июня по сентябрь 2012 года и включало предоставление информации женщинам и получение информированного согласия. В этой популяции проводились обычные мазки Папаниколау, которые анализировались в цитологической лаборатории Caserta ASL.
Из 2500 обследованных женщин в общей сложности у 78, то есть у 3,12%, диагноз был положительным, т.е. ASC (атипичные плоские клетки эпителия) + (атипия плоских клеток или хуже) по результатам мазка Папаниколау. Как показано на схеме на Рис. 1, цитологические диагнозы ASC + распределились следующим образом: 32 случая - ASC-US (атипичные клетки плоского эпителия неясного значения) (41%), 42 случая - LSIL (низкодифференцированные плоскоклеточные интраэпителиальные поражения) (54%), и 4 случая - HSIL (высокодифференцированные плоскоклеточные интраэпителиальные поражения) (5%).
96,88% результатов были отрицательными по плоскоклеточным интраэпителиальным поражениям или неопластическим перерождениям и относились к категории нормальных или доброкачественных воспалительных изменений, иногда с наличием микроорганизмов (бактерии, грибы или трихомонады).
78 женщин с положительным диагнозом были приглашены на дополнительное обследование в соответствии с методом по настоящему изобретению для получения второго образца с целью изучения интеграции/взаимодействия белков Е6/р53 и E7/pRb.
Образцы были взяты и проанализированы в соответствии с описанной выше процедурой для конкретного варианта осуществления метода в соответствии с изобретением в лаборатории молекулярной биологии больницы Marcianise.
Данные, полученные в результате анализа 78 положительных образцов мазков Папаниколау методом вестерн-блоттинга, показаны на Рис. 2. Гистограмма показывает, что во-первых, из 32 образцов цитологическим диагнозом ASC-US, только 2 (6,3%) оказались положительными на наличие белков Е6 и Е7, в то время как в остальных 30 (93,7%) белки не были найдены.
С другой стороны, во всех образцах с цитологическим диагнозом LSIL (42) и HSIL (4) доказано наличие белков Е6 и Е7. В целом, следовательно, из 78 случаев с положительным результатом мазка Папаниколау только 48 были положительными на белки Е6 и Е7 при использовании диагностического метода в соответствии с изобретением.
Из полученных данных ясно, что в большинстве ASC-US (93,7%) интеграция вирусного генома не происходила, и, следовательно, это может означать:
1) отсутствие ВПЧ: обнаруженные цитологические аномалии являются воспалительными по своей природе;
2) присутствие низкого риска ВПЧ: как правило, не может интегрироваться в геном, но ограничивается эписомальной формой;
3) присутствие высокого риска ВПЧ: находится на ранней стадии с очень недавней инфекцией и отсутствием интеграции.
Во всех случаях цитологического диагноза LSIL и HSIL были выявлены белки Е6 и Е7 и, следовательно, можно утверждать, что эти образцы свидетельствуют о высоком риске ВПЧ и давней инфекции, поскольку интеграция вирусного генома уже произошла.
Принимая во внимание 48 положительных случаев с наличием белков Е6 и Е7, как показано на Рис. 2, диагностический метод по настоящему изобретению показывает, что взаимодействие Е6/р53 и E7/pRb присутствует в 4,8% случаев LSIL и в 75,0% случаев HSIL и отсутствует в ASC-CIIIA при наличии белков Е6 и Е7.
Результаты, представленные на гистограмме на Рис. 2, также представлены в следующей таблице.
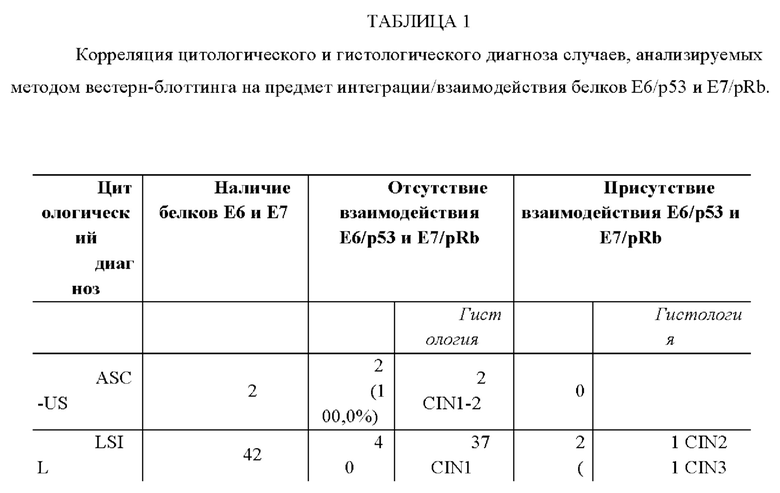
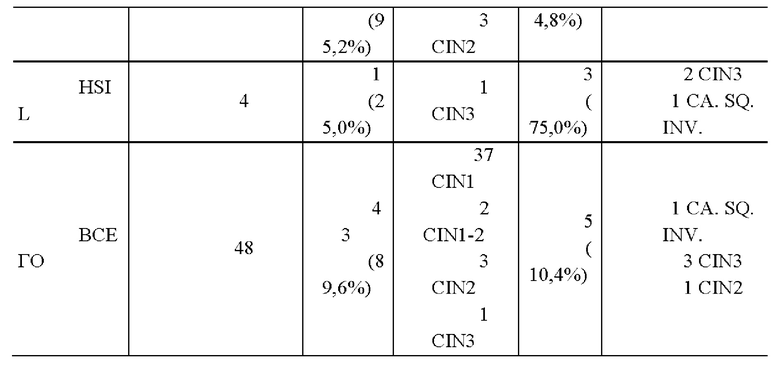
Приведенные выше данные показывают, что в 48,8% LSIL и 75,0% HSIL присутствует взаимодействие Е6/р53 и E7/PRB, а это означает, что процесс канцерогенеза находится на поздней стадии; в остальных случаях LSIL и HSIL, где взаимодействие отсутствует, можно предположить, что процесс канцерогенеза все еще находится в ранней стадии, и регрессия еще возможна.
Наиболее показательные примеры результатов, полученных по методу вестерн-блоттинга во время обсуждаемого исследования, показаны на прилагаемых Рис. 3, 4, 5 и 6 с результатами анализа по методу вестерн-блоттинга на образцах, в которых в дополнение к присутствию Е6 и Е7 было также установлено взаимодействие с р53 и pRb. Данные Рис. 3 и 4, соответственно, относящиеся к результатам вестерн-блоттинга с первичным моноклональным антителом к Е6-белку и к Е7-белку показывают двойные полосы реакции для каждого образца - 18 кД и 71 кД для белка Е6, 16 кД и 115,5 кД для белка Е7. Наличие дополнительных полос с гораздо большим молекулярным весом, чем Е6 и Е7, показывает, в соответствии с настоящим изобретением, наличие взаимодействия между Е6 и р53 и между Е7 и pRb.
Указанная гипотеза была подтверждена двумя дополнительными анализами по методу вестерн-блоттинга с первичными моноклональными антителами к белку рР53 и белку pRb, соответственно. На Рис. 5 и 6 показаны полученные результаты, подтверждающие данную гипотезу, поскольку полосы реакции точно соответствуют двум дополнительным полосам, наблюдавшимся ранее.
В образцах с белками Е6 и Е7, но без взаимодействия Е6/р53 и E7/pRb анализ методом вестерн-блоттинга с первичными моноклональными антителами к белку Е6 и к белку Е7 показали (для каждого образца) одну полосу реакции 18 кД для антитела к белку Е6 и 16 Кд к белку Е7, соответственно.
В образцах, где отсутствовали белки Е6 и Е7, оба анализа методом вестерн-блоттинга с первичными моноклональными антителами к белку Е6 и к белку Е7 не показали никакой полосы реакции, что доказывает отсутствие в этих образцах интеграции вирусной ДНК в клетку.
Согласно полученным результатам, во всех проанализированных случаях HSIL и в большинстве случаев LSIL присутствует интеграция вирусного генома в выработку белков Е6 и Е7. Тем не менее, 75,0% высокодиффузных поражений и лишь несколько низкодиффузных поражений (4,8%) продемонстрировали взаимодействие белков Е6/р53 и E7/pRb. Эти данные подтверждают, что взаимодействие является маркером канцерогенеза.
Таким образом, метод вестерн-блоттинга для оценки присутствия белков Е6 и Е7 и их возможного взаимодействия (Е6/р53 и E7/pRb) демонстрирует более высокую специфичность как теста на ДНК ВПЧ, так и цитологии, что позволяет выявлять пациентов с клинически значимыми поражениями (CIN2+). Гистологический контрольный анализ LSIL и HSTL подтвердил эту гипотезу. В частности (см. Таблицу 1), из четырех HSIL, в которых присутствовало взаимодействие белков Е6/р53 и E7/pRb, два были CTN 3 (тяжелая дисплазия - карцинома in situ) (50,0%) и один инвазивный плоскоклеточный рак (25,0%), и в четвертом случае без взаимодействия был поставлен диагноз CIN 3. Кроме того, случая два LSIL (4,8%) с взаимодействием белков Е6/р53 и E7/pRb представляют собой один CTN2 (умеренная дисплазия) (50,0%) и один CIN3 (50,0%). 40 LSIL (95,2%) без взаимодействия включали 37 CIN 1 (легкая дисплазия) (88,1%) и 3 CIN2 (7,1%).
Эти сведения подтверждают существование взаимосвязи между взаимодействием белков и канцерогенезом, однако еще предстоит понять биологические основы стадии перехода от интеграции к взаимодействию и карциноматозному перерождению. В основном только несколько интегрированных поражений со сверхэкспрессией белков Е6 и Е7 доходят до стадии полного канцерогенеза. Возникает гипотеза о существовании количественного порога вирусных белков, в течение которого происходит их взаимодействие. Согласно наиболее репрезентативным примерам, дальнейшие исследования могут подтвердить эту гипотезу.
Принимая во внимание тот факт, что вышеуказанные оценки считаются фундаментальными, в соответствии с методом изобретения мы предлагаем использовать вестерн-блоттинт или Sandwich ELISA для проведения теста на интеграцию/взаимодействие белков Е6/р53 и E7/pRb в рамках диагностики после получения положительного результата теста на ДНК ВР-ВПЧ и положительного результата мазка Папаниколау на поражения ASC+, в частности, согласно схеме, представленной на Рис. 7.
С помощью этой диагностической стратегии можно увеличить специфичность цитологической (ASC+) и молекулярной (положительный результат на ДНК ВР-ВПЧ) диагностики при скрининге на рак шейки матки, при этом на вторичное обследование будут приглашаться только женщины, у которых обнаружена интеграция/взаимодействие вирусного генома. Та же стратегия может быть применена при ВПЧ-индуцированных опухолевых поражениях в участках за пределами матки (анус-генитальной области, ротоглотке и т.д.).
Эффективная стратегия вакцинации в сочетании с организованным скринингом, адекватной чувствительностью и увеличением специфичности используемых тестов, подобно описанному в данном документе примеру, приведет к снижению количества случаев папилломавирусной инфекции, что позволит сократить последствия рака шейки матки для медицинских и социально-экономических институтов и общества и значительно снизить смертность, в том числе с помощью целевой терапии.
Еще одним возможным предпочтительным применением способа в соответствии с изобретением являются эксперименты на различных фазах развития болезни для изучения воздействия противораковых лекарственных средств и ингибирующей активности взаимодействия Е6/р53 и E7/pRb (Шейк Ф. и др. 2012 г., в цитированном отрывке) для разработки и тестирования лекарственного средства никандренон в целевой терапии.
Эти же методы предназначены для идентификации в клетках образцов, взятых при обследовании из любого анатомического участка, кроме шейки матки, любого пациента, белков, кодируемых онкогенными генами, включая не-вирусные, и белков, кодируемых генами-супрессорами опухолей, во время исследования клеток и определения с помощью вестерн-блоттинга и/или ELISA Sandwich возможного взаимодействия между ними.
Настоящее изобретение описано с конкретной ссылкой на некоторые конкретные варианты его осуществления, но следует понимать, что специалисты в данной области техники могут делать модификации и изменения, не выходя за пределы объема настоящего изобретения, как это определено в прилагаемой формуле изобретения.

Изобретение относится к медицине, а именно к онкодиагностике, и может быть использовано для обнаружения неопластического перерождения клеток, вызываемого вирусом папилломы человека (ВПЧ) у женщин, проходящих скрининг на рак шейки матки. Для этого проводят обнаружение в образцах клеток, взятых из плоскоклеточного-цилиндроклеточного стыка эпителия шейки матки обследуемой пациентки, белкового комплекса Е6/р53, состоящего из белка Е6 и белка p53, и белкового комплекса Е7/рRB, состоящего из белка Е7 и белка рRB. Причем обнаружение указанных двух белковых комплексов показывает, что у обследуемой пациентки канцерогенез стал необратимым, и указанное обнаружение выполняется при комбинированном использовании антител к белку Е6, антител к белку Е7, антител к белку p53 и антител к белку рRB. Изобретение обеспечивает диагностику рака шейки матки. 13 з.п. ф-лы, 8 ил., 1 табл.
1. Способ обнаружения неопластического перерождения клеток, вызываемого вирусом папилломы человека (ВПЧ) у женщин, проходящих скрининг на рак шейки матки, включающий обнаружение в образцах клеток, взятых из плоскоклеточного-цилиндроклеточного стыка эпителия шейки матки обследуемой пациентки, белкового комплекса Е6/р53, состоящего из белка Е6 и белка p53, и белкового комплекса Е7/рRB, состоящего из белка Е7 и белка рRB, причем обнаружение указанных двух белковых комплексов показывает, что у обследуемой пациентки канцерогенез стал необратимым, и указанное обнаружение выполняется при комбинированном использовании антител к белку Е6, антител кбелку Е7, антител к белку p53 и антител к белку рRB.
2. Способ по п.1, включающий следующие стадии в соответствии с методикой вестерн-блоттинга:
a) подготовка образца клеток, взятых из плоскоклеточного-цилиндроклеточного стыка эпителия шейки матки обследуемой пациентки, и помещение его в физиологический раствор;
b) извлечение белков из указанного образца и денатурирование полученных белков;
c) обработка полученных таким образом денатурированных белков электрофорезом в полиакриламидном геле;
d) перенос белков, полученных во время предыдущей стадии, на мембрану и нейтрализация свободных участков указанной мембраны;
e) идентификация указанных белков путем их инкубации по меньшей мере со следующими антителами:
первичным моноклональным антителом к белку Е6;
первичным моноклональным антителом к белку Е7;
первичным моноклональным антителом к белку р53;
первичным моноклональным антителом к белку рRB;
с последующей инкубацией с вторичными антителами анти-IgG, конъюгированными с биотином или ферментом-посредником, таким как щелочная фосфатаза;
f) проведение колориметрического анализа или анализа методом хемилюминесценции продуктов, полученных в результате предыдущей стадии;
где результаты указанного анализа, демонстрирующие двойную полосу реакции для белков Е6 и Е7, где указанная двойная полоса содержит первую полосу, соответствующую молекулярной массе искомого белка, т.е. Е6 или Е7, и вторую полосу, соответствующую молекулярной массе, отличающейся и превышающей молекулярную массу соответствующего белка первой полосы, и указанная молекулярная масса по существу равна 71 кД для белкового комплекса Е6/р53 и 115,5 кД для белкового комплекса E7/pRB, показывают, что канцерогенез обследуемой пациентки стал необратимым, и/или где результаты указанного анализа, демонстрирующие двойную полосу реакции по меньшей мере для одного из белков р53 и pRb, где указанная двойная полоса содержит первую полосу, соответствующую молекулярной массе искомого белка р53 или pRb, и вторую полосу, соответствующую молекулярной массе, отличающейся и более высокой, чем молекулярная масса соответствующего белка первой полосы, показывают, что у обследуемой пациентки канцерогенез стал необратимым.
3. Способ по п.2, отличающийся тем, что результаты указанного анализа, демонстрирующие одну полосу реакции для обоих белков Е6 и Е7, причем указанная одна полоса соответствует молекулярной массе искомого белка Е6 или Е7, показывают, что у обследуемой пациентки канцерогенез еще не начался или еще не стал необратимым.
4. Способ по п.3, отличающийся тем, что результаты анализа, не демонстрирующие какой-либо полосы реакции для белков Е6 и Е7, означают, что у обследуемой пациентки отсутствует интеграция ДНК вируса с ДНК клеток.
5. Способ по любому из пп.2-4, отличающийся тем, что вторичные антитела-анти-IgG указанной стадии e) конъюгированы с щелочной фосфатазой, и при этом указанный анализ на стадии f) представляет собой колориметрический анализ или анализ методом хемилюминесценции.
6. Способ по п.2, отличающийся тем, что указанное первичное моноклональное антитело к белку Е6 представляет собой мышиное антитело к белку E6 вирусного типа HPV16 и HPV18, а указанное первичное моноклональное антитело к белку Е7 представляет собой мышиное антитело к белку Е7 вирусного типа HPV16 и HPV18.
7. Способ по п.2, отличающийся тем, что указанное первичное моноклональное антитело к белку p53 представляет собой мышиное моноклональное антитело к белку р53 человека, и указанное первичное моноклональное антитело к белку pRb представляет собой мышиное моноклональное антитело к белку pRb человека.
8. Способ по п.1, включающий следующие стадии в соответствии с методом Sandwich ELISA:
a) идентификация изучаемого образца, хранящегося в соответствии с требованиями к жидкофазной цитологии;
b) адсорбция в разных лунках микропланшета антител к белку Е6 и к белку Е7 в качестве иммобилизованных антител вирусного белка Е6 или Е7;
c) блокировка остальных участков лунок, связывающих белки с помощью блокирующего буфера;
d) дозирование непосредственно в каждую лунку указанного клеточного образца для анализа;
e) идентификация искомых белков путем инкубации с разбавленным антителом к белку p53 в лунках с адсорбированным антителом к белку Е6 и разбавленным антителом к белку pRB в лунках с адсорбированным антителом к белку Е7;
f) блокировка эндогенного субстрата;
g) инкубация в соответствующие лунки антитела, конъюгированного с пероксидазой хрена (HRP);
h) дозирование раствора хромогена в каждую лунку;
i) продукт реакции на стадии h) изучается по интенсивности света, обнаруживаемого при длине волны 450 нм с помощью спектрофотометра, при этом результаты, демонстрирующие окрашивание и подтвержденные положительной абсорбцией, показывают, что у обследуемой пациентки присутствуют белковые комплексы Е6/р53 и/или E7/pRB, что подтверждает взаимодействие между белками вируса и человеческими белками, и, следовательно, указывает на то, что у обследуемой пациентки канцерогенез начался и стал необратимым.
9. Способ по п.8, в котором на стадиях e), f), g) и h) используются коммерчески доступные системы, позволяющие усиливать хромогенный сигнал, предпочтительно с использованием антител к белкам р53 и pRB, биотинилированных и выделенных стрептавидином, конъюгированным с пероксидазой или другим ферментом.
10. Способ по п.8, в котором в случае, если результаты анализа не показывают положительной реакции, и сигнал абсорбции при длине волны 450 нм отсутствует для обоих белковых комплексов E6/p53 и E7/pRB, результат указывает на то, что у обследуемой пациентки отсутствует интеграция вирусной ДНК с клеточной ДНК; не исключая возможности интеграции вирусной ДНК с клеточной ДНК.
11. Способ по п.8, отличающийся тем, что первичное моноклональное антитело к белку Е6 представляет собой мышиное моноклональное антитело к белку Е6 вирусных типов HPV16 и HPV18, указанное первичное моноклональное антитело к белку Е7 представляет собой мышиное моноклональное антитело к белку Е7 вирусного типа HPV16, указанное первичное моноклональное антитело к белку р53 представляет собой моноклональное мышиное антитело к белку р53 человека, указанное первичное моноклональное антитело к pRb-белку представляет собой моноклональное мышиное антитело к белку pRB человека.
12. Способ обнаружения неопластического перерождения клеток, вызываемого вирусом папилломы человека (ВПЧ) согласно любому из пп.2-5 и 8-11, в соответствии с которым указанный способ используется в рамках скрининговой программы для женского населения или в программе ранней диагностики для выявления рака шейки матки после цитологической диагностики атипичных клеток плоского эпителия (ASC) или худшего диагноза и последующего положительного результата теста на ДНК ВР-ВПЧ.
13. Способ обнаружения неопластического перерождения клеток, вызываемого вирусом папилломы человека (ВПЧ) согласно любому из пп.2-5 и 8-11, в соответствии с которым указанный способ используется в рамках скрининговой программы для женского населения или в программе ранней диагностики для выявления рака шейки матки после положительного результата теста на ДНК ВР-ВПЧ и последующей цитологической диагностики атипичных клеток плоского эпителия (ASC) или худшего диагноза.
14. Способ обнаружения неопластического перерождения клеток, вызываемого вирусом папилломы человека (ВПЧ) согласно любому из пп.2-5 и 8-11, в соответствии с которым указанный способ используется в рамках диагностических мер, скрининга или последующего наблюдения пациентов с неопластическими поражениями, вызванными ВПЧ или подозреваемыми в маточных и внематочных областях, таких как анус-генитальная область, ротоглотка.
| LU D.W | |||
| et al | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| WO 2011084598 A1, 14.07.2011 | |||
| SIMA N | |||
| et al | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| SIMA N | |||
| et al | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
Авторы
Даты
2019-10-08—Публикация
2015-05-07—Подача