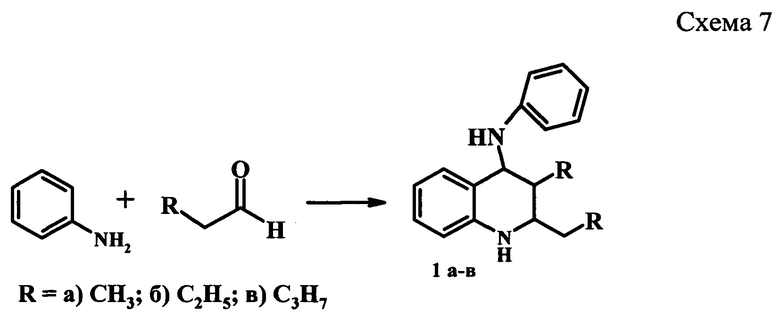
Предлагаемое изобретение относится к области органической химии, в частности, к способу получения 2,3-диалкил-N-фенил-1,2,3,4-тетрагидрохинолин-4-аминов общей формулы 1:
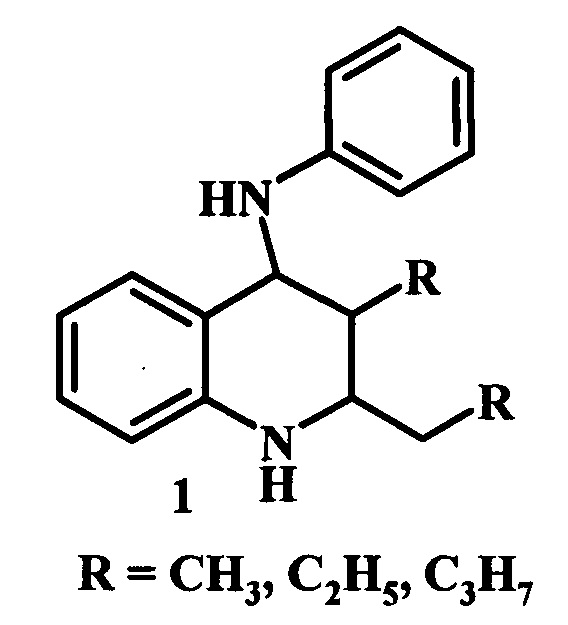
Производные тетрагидрохинолинов (ТГХ) относятся к классу N-гетероциклических соединений, обладающих широким спектром биологической активности. Они нашли применение в качестве антибиотиков [Omura, S.; Nakagawa, A. Tetruhedron Lett. 1981, 22, 2199-2202. Francis, С.L.; Ward, A.D. Aust. J. Chem 1994, 47, 2109-2117. Williamson, N.M.; March, D.R.; Ward, A.D. Tetrahedron Lrtt. 1995, 36, 7721-7724.], антидепрессантов [Buzas, A.; Ollivier, R.; El Ahmad, Y.; Laurent, E. // PCT Int. Appl. WO 93 16,057, 1993; Chem. Abstr. 1994, 120, 134523c], антигистаминных [Biller, S.A.; Misra, R.N. // U.S. Pat. US 4,843,082, 1989; Chem Abstr. 1989, 111, 232600j.], сердечно-сосудистых [Atwal, К. // Eur. Pat. EP 488, 616, 1992; Chem. Abstr. 1992, 117, 89978e], противоопухолевых [Lukevics, E.; Lapina, Т.; Segals, I.; Augustane, I.; Verovskii, V.N. // Khim.-Farm. Zh. 1988, 22, 947-951; Chem. Abstr. 1988, 109, 222016t.], противоязвенных [Uchida, M.; Chihiro, M.; Morita, S.; Yamashita, H.; Yamasaki, K.; Kanbe, Т.; Yabuuchi. Y.; Nakagawa, K. // Chem. Pharrm. Bull. 1990, 38, 1575-1586. Uchida, M.; Morita, S.; Chihiro, M. // Eur. Pat. EP 239, 129, 1987; Chem. Abstr. 1988, 108, 186740t] и других агентов. Помимо фармацевтической области применения, производные тетрагидрохинолина используются, как пестициды [Walter, Н. // Eur. Pat. 555, 183, 1993; Chem. Abstr. 1994, 120, 54551v. Ohsumi, Т.; Mito, N.; Oshio, H.; Itaya, N. // Nippon Noyaku Gokkuishi 1988, 13, 71-75; Chem. Abstr. 1988, 109, 88070a. Shmyreva, Zh. V.; Shikhaliev, Kh. S.; Shpanig, E.B. // Izv. Vyssh. Uchebn. Zaved, Khim. Khim. Tekhnol. 1988, 31, 45-48; Chem. Abstr. 1989, 111, 23363v. Tsushima, K.; Osumi, Т.; Matsuo, N.; Itaya, N. // Agric. Biol. Chem. 1989, 53, 2529-2530. Kurahashi, Y.; Shiokawa, K.; Goto, Т.; Kagabu, S.; Kamochi, A.; Moriya, K.; Hayakawa, H. // Eur. Pat. EP 198, 264, 1986; Chem. Abstr. 1987, 106, 98115w], антиоксиданты [Luzhkov, V.В.; Fentsov, D.V.; Kasaikina, О.T. Zh. Strukt. Khim. 1988, 29, 37-41. Chem. Abstr. 1989, 111, 22774t. Meier, H.R.; Evans, S. // Eur. Pat EP 273, 868, 1988; Chem Abstr. 1989, 110, 98598р. Fentsov, D.V.; Lobanova, Т.V.; Kassaikina, О.T. // Neftekhimiya 1990, 30, 103-108; Chem. Abstr. 1990, 112, 234619s. Evans, S. // Eur. Pat. EP 497, 735, 1992; Chem. Abstr. 1992, 117, 233868p], ингибиторы коррозии [Shikhaliev, Kh. S.; Shmyreva, Zh. V.; Gurova, E.M. // Izv. Vyssh. Uchebn. Zaved, Khim. Khim. Tekhnol. 1989, 32, 85-89; Chem. Abstr. 1990, 112, 216659a].
Одним из основных методов синтеза производных ТГХ является трехкомпонентная циклоконденсация (реакция Поварова) ариламина, альдегида и алкена, катализируемая солями переходных металлов [Kobayashi, S.; Ishitani, Н.; Nagayama, S. Chem. Lett. 1995, 423. Annunziata, R.; Cinquini, M.; Cozzi, F.; Molteni, V.; Schupp, O. Tetrahedron, 1997, 53, 9715.] (схема 1).
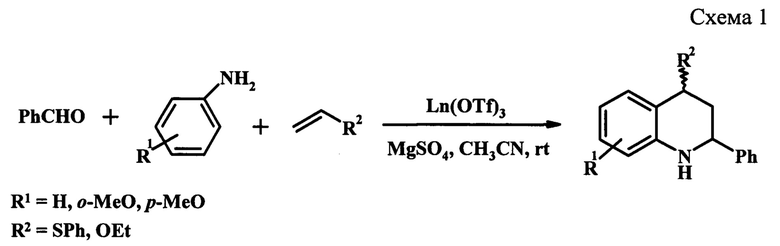
Существенным недостатком классических методов синтеза производных ТГХ в присутствии гомогенных кислотных катализаторов является необходимость проведения стадий нейтрализации и отмывки реакционной смеси, утилизация сточных вод, коррозия оборудования.
Авторами [Ishitani, Н.; Kobayashi, S. Tetrahedron Lett. 1996, 37, 7357] сообщается о получении производных ТГХ реакцией аза-Дильса-Альдера арилимина и алкена, катализируемую (10-20% мольных) хиральными комплексами иттербия (энантиомерный выход 70-91%) (схема 2) или в присутствии фосфорной кислоты, нанесенной на хиральную подложку (энантиомерный выход 87-98%) [Dagousset, G.; Zhu, J.P.; Masson, G.J Am Chem Soc 2011, 133, 14804. He, L.; Bekkaye, M.; Retailleau, P.; Masson, G. Org Lett 2012, 14, 3158].
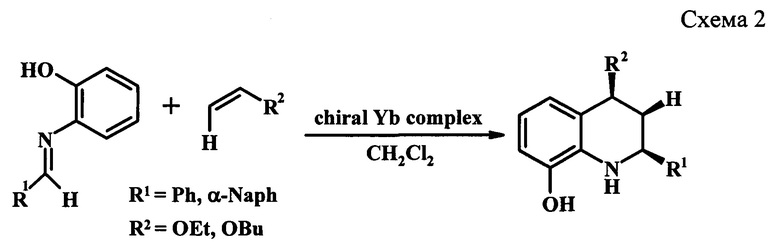
Недостатком данного метода является использование дорогостоящих труднодоступных хиральных комплексов. Кроме того, указанные выше методы приводят к получению 2,4-замещенных ТГХ.
Авторами [Т. Shao, Y. Yin, R. Lee, X. Zhao, G. Chai and Z. Jiang, Adv. Synth. Catal, 2018, 360, 1754. Z. Jiang, T. Shao, X. Zhao, Y. Liu, B. Qiao. Patent CN 108017580. Method for synthesis of 1,2,3,4-tetrahydroquinoline, 2018] разработан и запатентован метод синтеза 2,3-диалкил-N-фенил-1,2,3,4-тетрагидрохинолин-4-аминов (1) путем фотоиндуцируемого каскадного аэробного декарбоксилирования и окислительного дегидрирования N-ариламинокислоты (схема 3). Реакцию проводят при облучении 2×1 W синего света, в присутствии молекулярных сит 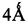 при 25°С в растворе хлороформа в течение 5-15 ч. В качестве хромофора используют дицианопиразиновое производное (0.4% мольных). Выход ТГХ (1) составляет 78%.
при 25°С в растворе хлороформа в течение 5-15 ч. В качестве хромофора используют дицианопиразиновое производное (0.4% мольных). Выход ТГХ (1) составляет 78%.
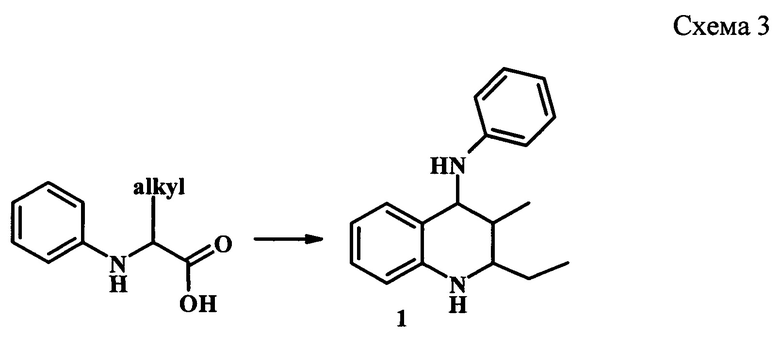
К недостаткам данного метода можно отнести использование специального оборудования для УФ-облучения, сложных в изготовлении и дорогостоящих N-ариламинокислот и хромофора, а также длительное время реакции.
В работе [Т. Job and N. Hagihara, J. Chem. Soc. Japan, 91, 378, 383 (1970); Chem. Abstr., 73,45,294,45,295(1971)] описано получение производных ТГХ (1) с выходом 78% взаимодействием основания Шиффа и метилвинилового эфира, катализируемого Ni(CO)4 (схема 4). Реакция проводится в инертной атмосфере в растворе ТГФ при 40-50°С в течение 6 ч.
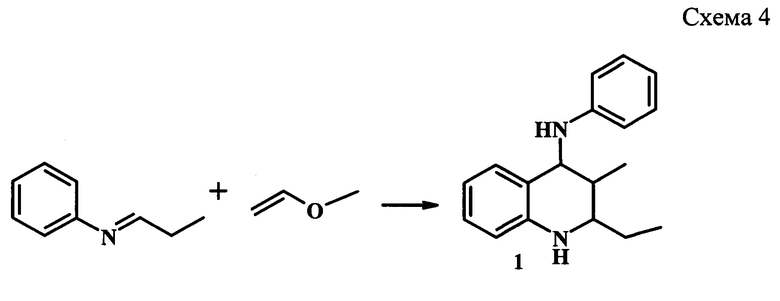
Недостатком данного способа является использование низкокипящих, гидролитически нестабильных виниловых эфиров, а также проведение синтеза во взрывоопасных эфирных растворителях.
Разработан метод синтеза ТГХ (1) из N-аллиланилина в присутствии Rh(I) катализаторов (схема 5) [М. Aresta, Е. Quaranta, S Treglia, J.A. Ibers. Organometallics, 1988, V7, №3, 577-583].
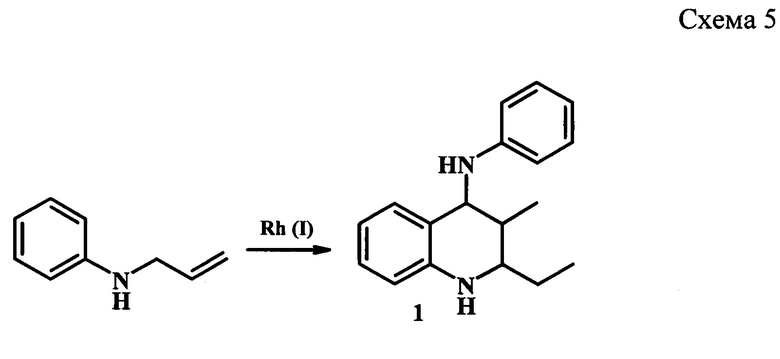
Реакцию проводили при мольном соотношении амин : катализатор=500:1 в растворе толуола/ тетрагидрофурана в инертной атмосфере в течение 2-72 ч. Выход ТГХ (1) не превышал 19%.
К недостаткам данного метода можно отнести низкий выход ТГХ (1) и использование сложных в изготовлении и дорогостоящих катализаторов, содержащих металлокомплексное соединение. Подобные каталитические системы требуют создания специальных условий использования, поскольку термически и гидролитически нестабильны.
Известен метод синтеза ТГХ (1) взаимодействием анилина с пропионовым альдегидом в «мягких условиях» [A.I.M. Ramos, J.S. Mecom, T.J. Kiesow, T.L. Graybill, G.D. Brown, N.V. Aiyar, E.A. Davenport, L.A. Kallal, B.A.K. Reed, P. Li, A.T. Londregan, D.M. Morrow, S. Senadhi, R.K. Thalji, S. Zhao, C.L.B. Kurtis, J.P. Marino. Bioorg. Med. Chem. Lett., 18 (2008), pp.6222-6226] (схема 6).
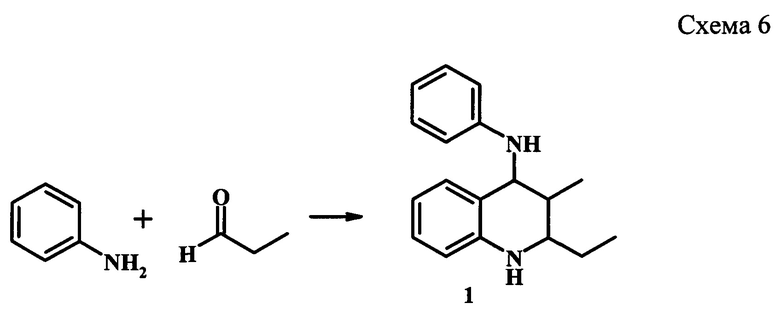
Реакция протекает без участия катализатора в этиловом спирте при 0°С с последующим увеличением температуры до комнатной в течение 14 ч, мольное соотношение анилин : альдегид = 1:1. Выход целевого продукта (1) составил 35%.
Авторами [VI Minkin, LE Nivorozhkin, AV Knyazev, Chem. Heterocycl. Comp, Vol. 2, No. 3, pp. 409-418, 1966] предложен аналогичный метод синтеза ТГХ (1), заключающийся в кислотно-катализируемой (ледяная уксусная кислота) конденсации ариламинов и пропионового альдегида, взятых в эквимольных количествах. Выход продукта (1) составляет 42%. Реакция протекает в метанольном растворе при комнатной температуре в течение 2-4 дней.
Недостатками данных методов является длительное время реакции, низкий выход ТГХ, а использование уксусной кислоты приводит к появлению дополнительных стадий нейтрализации и очистки реакционной массы, а также большого количества сточных вод.
В литературе отсутствует информация о получении производных ТГХ (1) взаимодействием анилина с альдегидами на цеолитных катализаторах.
Задачей настоящего изобретения является разработка селективного гетерогенно-каталитического способа синтеза 2,3-диалкил-N-фенил-1,2,3,4-тетрагидрохинолин-4-аминов.
Решение этой задачи достигается тем, что синтез 2,3-диалкилтетрагидрохинолинов (1) осуществляют реакцией анилина с алифатическими альдегидами (пропионовый, масляный, валерьяновый) в присутствии цеолита Y в Н-форме (H-Y).
Степень декатионирования (обмена катионов Na+ на Н+) цеолита H-Y составляет 60-95%. Реакцию проводят в проточном реакторе с неподвижным слоем катализатора (H-Y, 1 г) при 250-350°С, атмосферном давлении, объемной скорости подачи сырья (w) 2-10 ч-1, при мольном соотношении анилин : альдегид = 1:2. Конверсия анилина составляет 81-100%. Основным продуктом реакции являются 2,3-диалкилТГХ (1 а-в), образующиеся с селективностью 50-69% (схема 7). Кроме 2,3-диалкилТГХ (1 а-в), в реакционной массе содержатся другие промышленно важные N-содержащие производные (например, 2,3-диалкилхинолины, 2,3-диалкилдигидрохинолины) в количестве 31-50%.
Использование предлагаемого способа имеет следующие преимущества перед известными:
1. Гетерогенно-каталитические способы синтеза производных тетрагидрохинолина позволяют упростить и удешевить процесс их получения за счет уменьшения количества стадий и единиц оборудования.
2. Не требуется использование дорогостоящих и сложных в приготовлении катализаторов.
3. В способе отсутствуют сточные воды, кислоты и основания.
4. Не используются растворители.
Предлагаемый способ синтеза 2,3-диалкилпроизводных ТГХ (1 а-в) осуществляют следующим образом.
Используют анилин и карбонильные соединения: пропионовый, масляный, валерьяновый альдегиды.
В качестве катализатора используют цеолит Y (мольное соотношение SiO2/Al2O3=5.0), синтезированный в Na-форме по методу, приведенному в [Патент 2456238 RU // Б.И. 2012. №20]. Путем ионного обмена из раствора NH4NO3 цеолит NaY переводят в NH4-форму; последующей прокалкой при 540°С в течение 4 ч полученные образцы переводят в Н-форму с различной степенью ионного обмена - 0,6HNaY, 0,8HY и 0,95HY (цифры перед обозначением цеолита показывают степень обмена ионов Na+ на H+). В процессе ионного обмена с промежуточными термообработками аморфизация кристаллического каркаса цеолита не происходит.
Реакцию взаимодействия анилина и альдегидов (пропионовый, масляный, валерьяновый) проводят в проточном реакторе с неподвижным слоем катализатора H-Y при температуре 250-350°С, атмосферном давлении, с объемной скоростью подачи сырья (w) 2-10 ч-1, в токе азота, мольное соотношение анилин : альдегид = 1:2. Продукты собирают в охлаждаемый льдом приемник. Количественный анализ реакционной массы осуществляют методом газожидкостной хроматографии на хроматографе Shimadzu GC-9A с пламенно-ионизационным детектором, 3 м насадочная колонка, фаза SE-30, с программированным нагревом 50-250°С, газ-носитель гелий.
Идентификацию продуктов реакции осуществляли с помощью 1D и 2D методик ЯМР 1H и 13С спектроскопии, рентгеноструктурного анализа для соединения (1а), их брутто-состав подтвержден регистрацией пика молекулярного иона в ГХ-МС спектре.
Изобретение иллюстрируется следующим примером:
Пример 1. Смесь, содержащую 2,5 мл (28 ммоль) анилина и 4 мл (56 ммоль) пропионового альдегида, подают с помощью шприцевого микро-насоса в проточный реактор с неподвижным слоем цеолитного катализатора 0,6H-Y (SiO2/Al2O3=5.0) (1 г) при 250°C, атмосферном давлении, объемной скорости подачи сырья 7 ч-1, в токе азота. Продукты собирают в охлаждаемый льдом приемник, расположенный в нижней части установки. По окончании синтеза реактор продувают азотом в течение 30 минут, после чего продукты реакции анализируют методом газожидкостной хроматографии. Конверсия анилина составляет 97%, селективность образования 2,3-диалкилТГХ (1а) составляет 61%, т.пл. 104-106°С (лит. 103-104°С [Kozlov, N.S.; Zhurnal Obshchei Khimii 1966, V2(3), P. 461-463], 106-107°C [Joh, Takashi; Nippon Kagaku Zasshi 1970, V91(4), P. 378-383]).
Спектральные характеристики 2-этил-3-метил-N-фенил-1,2,3,4-тетрагидрохинолин-4-амина (1a): ЯМР 1H (500.17 М Гц, CDCl3, δ, м.д.): 1.01 (т, J=9.5 Гц, 3Н), 1.11 (д, J=8.5 Гц, 3Н), 1.61-1.67 (м, 2Н), 1.88-1.94 (м, 1Н), 3.14-3.18 (м, 1Н), 3.85 (м, 2Н), 4.34 (д, J=11.5 Гц, 1Н), 6.55 (д, J=10.0 Гц, 1Н), 6.62-6.77 (м, 4Н), 7.06 (т, J=8.8 Гц, 1H), 7.19-7.27 (м, 3Н). ЯМР 13С (125.78 МГц, CDCl3, δ, м.д.): 9.12, 15.76, 26.49, 37.39, 56.44, 57.86, 112.50, 113.25, 113.86, 116.85, 117.36, 123.38, 128.05, 128.31, 129.40, 129.45, 144.37, 148.76. Полученные данные соответствуют литературным [Aresta, М., Quaranta, Е., Treglia, S., & Ibers, J.А. (1988). Organometallics, 7(3), 577-583. doi:10.1021/om00093a001.A.I.M. Ramos, J.S. Mecom, T.J. Kiesow, T.L. Graybill, G.D. Brown, N.V. Aiyar, E.A. Davenport, L.A. Kallal, B.A.K. Reed, P. Li, A.T. L ondregan, D.M. Morrow, S. Senadhi, R.K. Thalji, S. Zhao, C.L.B. Kurtis, J.P. Mari no. Bioorg. Med. Chem. Lett., 18 (2008), pp. 6222-6226].
Пример 2. Сырье - смесь 2,5 мл (28 ммоль) анилина и 5,2 мл (56 ммоль) масляного альдегида - подают с помощью шприцевого микро-насоса в проточный реактор с неподвижным слоем цеолитного катализатора 0,6H-Y (SiO2/Al2O3=5.0) (1 г) при 250°С, атмосферном давлении, объемной скорости подачи сырья 7 ч-1, в токе азота. Продукты собирают в охлаждаемый льдом приемник, расположенный в нижней части установки. По окончании синтеза реактор продувают азотом в течение 30 минут, после чего продукты реакции анализируют методом газожидкостной хроматографии. Конверсия анилина составляет 91%, селективность образования 2,3-диалкилТГХ (1б) составляет 62%, т.пл. 90-92°С (лит. 91-92°С [Kozlov, N. S.; Zhurnal Obshchei Khimii 1966, V2(3), Р461-463]).
Спектральные характеристики 2-пропил-3-этил-N-фенил-1,2,3,4-тетрагидрохинолин-4-амина (1б): ЯМР 1Н (500.17 М Гц, CDCl3, δ, м.д.): 1.01 (т, J=7.5 Гц, 3Н), 1.07 (т, J=7.5 Гц, 3Н), 1.49-1.63 (м, 4Н), 1.92-2.00 (м, 3Н), 3.32-3.34 (м, 1Н), 3.96 (м, 2Н), 4.47 (д, J=9.5 Hz, 1Н), 6.59 (д, J=7.8 Гц, 1Н), 6.71-6.79 (м, 4Н), 7.12 (т, J=7.8 Гц, 1Н), 7.28-7.37 (м, 3Н). Спектр ЯМР 13С (125.78 МГц, CDCl3, δ, м.д.): 11.04, 14.14, 19.58, 23.58, 37.05, 41.67, 51.80, 53.24, 112.46, 113.34, 114.35, 116.87, 117.33, 122.30, 128.31, 129.44, 129.50, 129.92, 143.59, 148.05.
Пример 3. Сырье - смесь 2,5 мл (28 ммоль) анилина и 5,9 мл (56 ммоль) валерьянового альдегида - подают с помощью шприцевого микронасоса в проточный реактор с неподвижным слоем цеолитного катализатора 0,6H-Y (SiO2/Al2O3=5.0) (1 г) при 250°С, атмосферном давлении, объемной скорости подачи сырья 7 ч-1, в токе азота. Продукты собирают в охлаждаемый льдом приемник, расположенный в нижней части установки. По окончании синтеза реактор продувают азотом в течение 30 минут, после чего продукты реакции анализируют методом газожидкостной хроматографии. Конверсия анилина составляет 98%, селективность образования 2,3-диалкилТГХ (1в) составляет 50%, т.пл. 71-73°С.
Спектральные характеристики 2-бутил-3-пропил-N-фенил-1,2,3,4-тетрагидрохинолин-4-амина (1в): ЯМР 1Н (500.17 М Гц, CDCl3, δ, м.д.): 0.91-0.97 (м, 6Н), 1.27-1.48 (м, 10Н), 1.65-1.67 (м, 1Н), 3.24-3.27 (м, 1Н), 3.86 (м, 2Н), 4.39 (д, J=10.0 Hz, 1Н), 6.53-6.77 (м, 5Н), 7.07-7.26 (м, 4Н). Спектр ЯМР 13С (125.78 МГц, CDCl3, δ, м.д.): 14.02, 14.10, 22.63, 22.67, 29.32, 29.41, 35.09, 40.07, 52.62, 53.86, 112.47, 113.34, 114.35, 116.83, 117.23, 121.94, 127.94, 128.32, 129.39, 129.42, 143.44, 147.88.
Другие примеры (2, 3, 5-7) осуществления способа приведены в таблице.
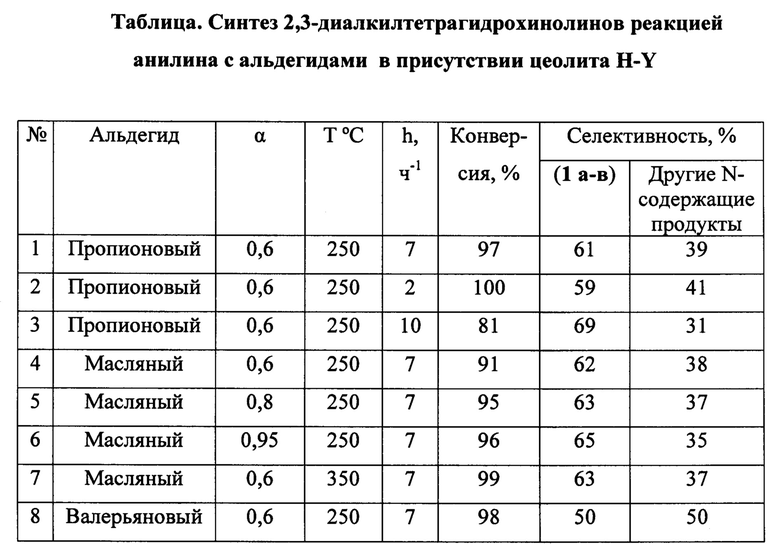
а - степень декатионирования, h - объемная скорость подачи сырья.
Реакцию проводят при 250-350°С, мольном соотношении анилин : альдегид = 1:2; объемной скорости подачи сырья h=2-10 ч-1.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 2,3-диалкил-N-фенил-1,2,3,4-тетрагидрохинолин-4-аминов | 2018 |
|
RU2697875C1 |
| Способ получения 2,3-диалкил-N-фенил-1,2,3,4-тетрагидрохинолин-4-аминов | 2018 |
|
RU2697876C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-МЕТИЛ-2-ЭТИЛ-N-ФЕНИЛ-1,2,3,4-ТЕТРАГИДРОХИНОЛИН-4-АМИНА | 2023 |
|
RU2808560C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛХИНОЛИНОВ | 2018 |
|
RU2688228C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛХИНОЛИНОВ | 2018 |
|
RU2687972C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛХИНОЛИНОВ | 2018 |
|
RU2688197C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛХИНОЛИНОВ | 2018 |
|
RU2688198C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛХИНОЛИНОВ | 2018 |
|
RU2687974C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛХИНОЛИНОВ | 2018 |
|
RU2690535C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2- И 2,3-ЗАМЕЩЕННЫХ ХИНОЛИНОВ | 2012 |
|
RU2504540C2 |
Изобретение относится к способу получения 2,3-диалкил-N-фенил-1,2,3,4-тетрагидрохинолин-4-аминов взаимодействием анилина с альдегидами в присутствии катализатора, отличающемуся тем, что в качестве катализатора используют цеолит Y в Н-форме, реакцию анилина с алифатическим альдегидом (пропионовый, масляный или валерьяновый) проводят в проточном реакторе с неподвижным слоем катализатора при 250-350°С, объемной скорости подачи сырья 2-10 ч-1, при атмосферном давлении, в токе азота и мольном соотношении анилин : альдегид 1:2. Технический результат: разработан новый упрощенный способ получения 2,3-диалкил-N-фенил-1,2,3,4-тетрагидрохинолин-4-аминов, позволяющий снизить энерго- и материалоемкость процесса гетероциклизации. 1 з.п. ф-лы, 1 табл., 3 пр.
1. Способ получения 2,3-диалкил-N-фенил-1,2,3,4-тетрагидрохинолин-4-аминов взаимодействием анилина с альдегидами в присутствии катализатора, отличающийся тем, что в качестве катализатора используют цеолит Y в Н-форме, реакцию анилина с алифатическим альдегидом (пропионовый, масляный или валерьяновый) проводят в проточном реакторе с неподвижным слоем катализатора при 250-350°С, объемной скорости подачи сырья 2-10 ч-1, при атмосферном давлении, в токе азота и мольном соотношении анилин : альдегид 1:2.
2. Способ по п. 1, в котором степень ионного обмена катионов Na+ на H+ в цеолите H-Y составляет 0,60-0,95.
| US 5700942 A1, 23.12.1997 | |||
| Vinu, Ajayan et al "Mesoporous aluminosilicate nanocage-catalyzed three-component coupling reaction: an expedient synthesis of α-aminophosphonates" Elsevier Ltd., Tetrahedron Letters (2009), 50(51), 7132-7136 | |||
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛХИНОЛИНОВ | 2006 |
|
RU2309952C1 |
Авторы
Даты
2019-10-08—Публикация
2018-12-14—Подача