Предлагаемое изобретение относится к способам получения гетероциклических соединений, конкретно к способу получения 2,3-диалкилхинолинов общей формулы

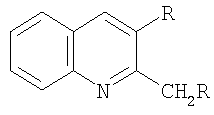
где R=C2H5, C3H7, C4H9
Хинолин и его производные используются при синтезе цианиновых красителей в качестве экстрагентов, сорбентов, а также ингибиторов коррозии.
Известен способ (Ф.А.Селимов, У.М.Джемилев, О.А.Пташко. Металлокомплексный катализ в синтезе пиридиновых оснований. - М.: Химия, 2003, с.223-233.) получения алкилпроизводных хинолина в реакции конденсации анилина с алифатическими альдегидами под действием трехкомпонентной системы LnCl3: PPh3: диметилформамид (ДМФА) при мольном соотношении, равном 0.4:1.2:13, и температуре реакции 100°С, в автоклаве, за 6 ч, в органических растворителях. В качестве лантанидов (Ln) применяли Pr, Nd, Sm, Dy, Yb, Gd, Eu, Ho, La, Er, Lu, Tm. Максимальная селективность по 2, 3-диалкилхинолину (91%) достигается при использовании PrCl3 и растворителя - этанола.
К недостаткам данного способа относятся большие энергозатраты (высокая температура, давление и длительность процесса), необходимость использования специального оборудования (автоклав) и лиганда активатора PPh3, а также высокая себестоимость безводных LnCl3 (малодоступных), что вызывает необходимость их предварительного получения (энергозатратный, трудоемкий синтез, в агрессивной среде).
Известен способ (патент РФ 2249476, опубликовано: 10.04.2005, Бюл. №10) получения 2,3-диалкилхинолинов в реакции конденсации анилина с алифатическими альдегидами в присутствии катализатора - комплекса [Sm(NO3)5]·[С5Н5NH]2. Реакцию проводят в автоклаве, при температуре 100°С, в бензоле, в течении 6 ч. Выход 2,3-диалкилхинолинов 51-66%.
К недостаткам данного способа относятся большие энергозатраты (высокая температура, давление и длительность процесса), необходимость использования специального оборудования (автоклав), низкий выход диалкилкилхинолинов, а также предварительный синтез [Sm(NO3)5]·[C5H5NH]2 (в агресивной среде - HNO3).
Предлагается новый способ получения 2,3-диалкилхинолинов. Сущность способа заключается во взаимодействии анилина с алифатическими альдегидами в присутствии катализатора Tb(NO3)3·6Н2O, взятыми в мольном соотношении 45:100:1.2. Реакция проводится при 20°С, атмосферном давлении, в течении 10 мин. В качестве растворителя применяли ДМФА. Реакция протекает по схеме.
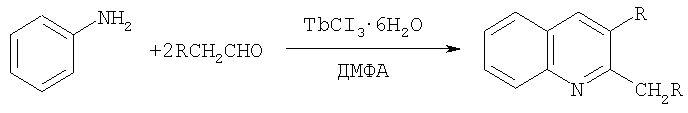
R=C2H5, С3Н7, С4H9.
При увеличении температуры раствора увеличивается содержание продуктов осмоления.
Существенные отличия предлагаемого способа
В предлагаемом способе в качестве катализатора используют коммерческий кристаллогидрат нитрат тербия Tb(NO3)3·6Н2О. Реакция идет при атмосферном давлении, при 20°С, в растворителе ДМФА, с более высоким выходом целевого продукта. В известных способах используют более дорогие соединения: безводные LnCl3 (малодоступные) или [Sm(NO3)5]·[C5H5NH]2 (не выпускаемый промышленностью) и требующие предварительного специального синтеза.
Предлагаемый способ обладает следующими преимуществами:
1. Способ не требует предварительного получения безводных солей LnCl3 или комплекса [Sm(NO3)5]·[C5H5NH]2 (трудоемкий, длительный синтез в агрессивной среде).
2. Способ позволяет за счет снижения температуры взаимодействия увеличить выход (90-94%) целевого продукта.
3. Способ позволяет значительно уменьшить температуру (от 100 до 20°С), время синтеза (от 6 ч до 10 мин), не требует специального оборудования (автоклава) и тем самым позволяет существенно упростить синтез и снизить себестоимость целевого продукта.
Способ поясняется следующими примерами:
ПРИМЕР 1. В стеклянную колбу объемом 50 мл, установленную на магнитной мешалке, помещают 8 мл ДМФА и 0.54 ммоль кристаллогидрата Tb(NO3)3·6Н2O. После полного растворения Tb(NO3)3·6Н2O (1-2 мин), при 20°С добавляют 20 ммоль анилина, 44 ммоль масляного альдегида и перемешивают 10 мин. Охлажденную реакционная массу трижды экстрагируют эфиром (3×50 мл), объеденные экстракты сушат над безводным MgSO4, растворитель отгоняют и остаток фракционируют в вакууме. Выход 2-пропил-3-этил хинолина составляет 94% (3.82 г.).
Другие примеры, подтверждающие способ, приведены в таблице.
Все опыты проводили в ДМФА при мольном соотношении C6H5NH2:RCH2CHO:Tb, равном 45:100:1.2.
Полученные соединения имеют следующие физико-химические характеристики:
2-Пропил-3-этилхинолин. Маслянистая жидкость, с характерным запахом. Ткип=118°С (1 мм рт.ст.). Найдено, %: С 84.64; N 7.01; Н 8.35. C14H17N. Вычислено, %: С 84.42; N 7.04; Н 8.54. Спектр ЯМР 1Н (CDCl3, δ, м.д.): 1,08 т (3Н, СН3); 1,23 т (3Н, СН3); 1,71 м (2Н, СН2); 2,68 к (2Н, СН2); 2,85 т (2Н, CH2); 7,3-8,1 м (5Н, аром.). Спектр ЯМР 13С (CDCl3, δ, м.д.): 13.91 к (С13); 14.0 к (С15); 23.4 т (С12); 24.7 т (С14); 37.22 т (С11); 125.05 с (С10); 125.15 д (С8); 126.48 д (С6); 127.0 д (С5); 128.1 д (С7); 133.2 д (С4); 134.7 с (С3); 146.07 с (С9); 161.33 с (С2).
2-Бутил-3-пропилхинолин. Маслянистая жидкость, с характерным запахом. Ткип=143°С (1 мм рт.ст.). Найдено, %: С 84,35; N 6.02; Н 9,63. C16H21N. Вычислено, %: С 84,58; N 6,17; Н 9,25. Спектр ЯМР 1Н (CDCl3, δ, м.д.): 1,1 т (3Н, СН3); 1,25 т (3Н, СН3); 1,68 м (2Н, СН2); 1,73 м (2Н, СН2); 1,82 т (2Н, СН2); 2,71 к (2Н, СН2); 7,28-8,07 м (5Н, аром.). Спектр ЯМР 13С (CDCl3, δ, м.д.): 13.80 к (С14); 13.90 к (С17); 22.80 т (С13); 23.20 т (С16); 31.10 т (С12); 33.70 т (С15); 35.00 т (С11); 125.10 д (С8); 126.20 д (С6); 126.80 с (С10); 128.10 д (С5); 128.15 д (С7); 133.10 д (С4); 134.20 с (С3); 145.80 с (С9); 161.10 с (С2).
2-Амил-3-бутилхинолин. Маслянистая жидкость, с характерным запахом. Ткип=156°С (1 мм рт.ст.). Найдено, %: С 85.5; N 5.2; Н 9.3. C18H25N. Вычислено, %: С 84.70; N 5.5; Н 9.8. Спектр ЯМР 1Н (CDCl3, δ, м.д.): 1.12 т (3Н, СН3); 1.27 т (3Н, СН3); 1.78 м (2Н, СН2); 1.86 м (2Н, СН2); 1.86 м (2Н, СН2); 1.97 м (2Н, СН2); 2.13 м (2Н, СН2); 2.38 м (2Н, СН2); 2.83 к (2Н, СН2); 2.97 т (2Н, СН2); 7.3-8.12 м (5Н, аром.). Спектр ЯМР 13С (CDCl3, δ, м.д.): 14.02 к (С15); 14.07 к (С19); 22.55 т (С14); 22.72 т (С18); 28.39 т (С13); 29.76 т (С17); 31.98 т (С12); 32.44 т (С16); 35.70 т (С11); 123.70 д (С8); 124.70 д (С6); 125.10 с (С10); 126.80 д (С5); 128.10 д (С7); 132.80 д (С4); 132.70 с (С3); 141.50 с (С9); 160.70 с (С2).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 2-ПРОПИЛ-3-ЭТИЛХИНОЛИНА | 2009 |
|
RU2409567C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛПРОИЗВОДНЫХ ХИНОЛИНА | 2005 |
|
RU2283836C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛ-7,8-БЕНЗО-1,6-НАФТИРИДИНОВ | 2006 |
|
RU2313526C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛПРОИЗВОДНЫХ ХИНОЛИНА | 2005 |
|
RU2283837C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛ-1,10-ФЕНАНТРОЛИНОВ | 2006 |
|
RU2313525C1 |
| КАТАЛИЗАТОР ДЛЯ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛ-1,10-ФЕНАНТРОЛИНОВ | 2003 |
|
RU2249478C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3,5-ТРИАЛКИЛПИРИДИНОВ | 2007 |
|
RU2334739C1 |
| КАТАЛИЗАТОР ДЛЯ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛХИНОЛИНОВ | 2003 |
|
RU2249476C2 |
| КАТАЛИЗАТОР ДЛЯ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛ-5,6-БЕНЗО-1,7 НАФТИРИДИНОВ | 2003 |
|
RU2249480C2 |
| КАТАЛИЗАТОР ДЛЯ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛ-1,10-ФЕНАНТРОЛИНОВ | 2003 |
|
RU2249479C2 |
Изобретение относится к области органического синтеза, конкретно к способу получения 2,3-диалкилхинолинов. Описывается способ получения 2,3-диалкилхинолинов общей формулы
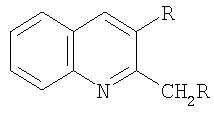
где R=С2Н5, С3Н7, С4Н9, путем взаимодействия анилина C6H5NH2 с алифатическими альдегидами общей формулы RCH2CHO (где R имеет указанные выше значения) в присутствии катализатора, отличающийся тем, что в качестве катализатора используют кристаллогидрат нитрат тербия Tb(NO3)3·6Н2O при мольном соотношении С6Н5NH2: RCH2CHO: Tb, равном 45:100:1.2, и реакцию проводят при атмосферном давлении 20°С в течение 10 минут в растворителе ДМФА. Технический результат - упрощение технологии получения целевого продукта. 1 табл.
Способ получения 2,3-диалкилхинолинов общей формулы
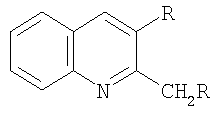
где R=C2H5, С3Н7, С4Н9,
путем взаимодействия анилина C6H5NH2 с алифатическими альдегидами общей формулы RCH2СНО (где R имеет указанные выше значения) в присутствии катализатора, отличающийся тем, что в качестве катализатора используют кристаллогидрат нитрат тербия Tb(NO3)3·6Н2O при мольном соотношении C6H5NH2 : RCH2СНО : Tb, равном 45:100:1,2, и реакцию проводят при атмосферном давлении 20°С, в течение 10 мин, в растворителе ДМФА.
| СЕЛИМОВ Ф.А | |||
| и др | |||
| Металлокомплексный катализ в синтезе пиридиновых оснований | |||
| - М.: Химия, 2003, с.223-233 | |||
| КАТАЛИЗАТОР ДЛЯ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛХИНОЛИНОВ | 2003 |
|
RU2249476C2 |
| У.М.ДЖЕМИЛЕВ и др | |||
| Синтез замещенных хинолинов конденсацией анилинов с алифатическими и ароматическими альдегидами под действием катализаторов на основе переходных и редкоземельных элементов | |||
| Изв | |||
| АН | |||
| Серия хим | |||
| Циркуль-угломер | 1920 |
|
SU1991A1 |
| Способ получения алкилпроизводных хинолина | 1990 |
|
SU1735287A1 |
| Способ получения алкилпроизводных хинолина | 1986 |
|
SU1416487A1 |
Авторы
Даты
2007-11-10—Публикация
2006-05-04—Подача