Предлагаемое изобретение относится к области органической химии, в частности к способу получения 2,3-диалкилхинолинов общей формулы:
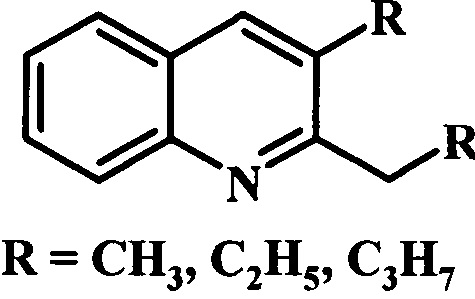
Хинолин и его производные обладают широким спектром биологической и фармацевтической активности. Производные хинолина входят в состав высокоэффективных противомалярийных [Larsen, R.D., Corley, Е.G., 1996. J. Org. Chem. 61, 3398. Chauhan, P.M.S., Srivastava, S.K., 2001. Curr. Med. Chem. 8, 1535], противоопухолевых [Myers, A.G., Tom, N.J., 1997. J. Am. Chem. Soc. 119, 6072. Comins, D.L., Hong, H., Saha, J.K., 1994. J. Org. Chem. 59, 5120], противовоспалительных [Roma, G., Braccio, M.D., 2000. Eur. J. Med. Chem. 35, 1021], противоастматических [Dube, D., Blouin, M., 1998. Bioorg. Med. Chem. Lett. 8, 1255], антигипертонических [Ferrarini, P.L., Mori, C, 2000. Eur. J. Med. Chem. 35, 815] и антибактериальных [Chen, Y.L., Fang, K.G., 2001. J. Med. Chem. 44, 2374] лекарственных препаратов, a также широко используются в качестве гербицидов и пестицидов [Larsen, R.D., Corley, Е.G., 1996. J. Org. Chem. 61, 3398. Chauhan, P.M.S., Srivastava, S.K., 2001. Curr. Med. Chem. 8, 1535]. Производные хинолина нашли применение в оптической электронике [Agarwal, А.K., Jenekhe, S.А., 1991. Macromolecules 24, 6806].
Классическими способами получения производных хинолина являются реакции Скраупа, Фридлендера, Дебнера-Миллера, Кнорра и Пфитцингера [Skraup, Z.Н., 1880. Ber. Dtsch. Chem. Ges.; Dobner, О., von Miller, W., 1881. Ber. Dtsch. Chem. Ges.; Gould, R.G., Jacobs, W.A. 1939. J. Am. Chem. Soc.]. Известно использование в качестве катализатора в данных реакциях органических кислот, металлорганических соединений, ионных жидкостей. Существенными недостатками способов синтеза производных хинолина с использованием традиционных каталитических систем являются образование большого количества отходов и побочных продуктов, высокая токсичность и коррозионная активность катализаторов.
В последнее время развиваются методы синтеза производных хинолина на гетерогенных катализаторах, в том числе на цеолитах и мезопористых алюмосиликатах.
В работе [Li В., Li Y., Zheng С, Gao D., Huang W. RSC Adv. 2016, 6, 38079] описано получение хинолина (1) методом Скраупа на цеолитном катализаторе Ni/H-Beta с мольным соотношением Si/Al=25 (схема 1).
Схема 1
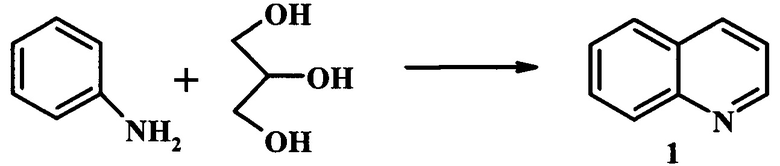
Реакцию проводят в проточном реакторе. Максимальный выход хинолина (1) (74,3%) получали при следующих условиях : объемная скорость = 0,13 ч-1, 470°С, мольное отношение анилин : глицерин = 1:4.
Недостатками данного метода является очень низкая объемная скорость подачи сырья, высокая температура реакции, большой избыток глицерина.
Известен [Guo Q., Liao L., Teng W., Ren S., Wang X., Lin Y., Meng F. Catalysis Today 2016, 263, 117] метод синтеза замещенных 2,3-диалкилхинолинов (2) с выходом 29-81% из ариламинов и альдегидов на катализаторе Cp2ZrCl2/MCM-41 (схема 2). Опыт проводили в реакторе периодического действия в растворе дихлорметана при мольном соотношении анилин : альдегид = 1:4 в атмосфере азота при 40°С в течение 4 ч.
Схема 2
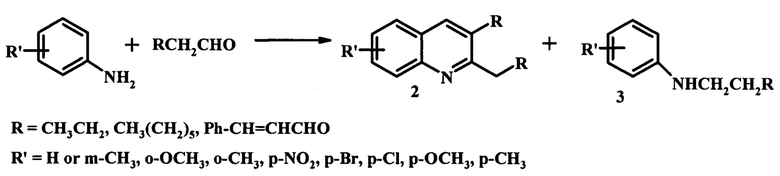
К недостаткам данного метода можно отнести использование сложного в изготовлении и дорогостоящего катализатора, содержащего металлокомплексное соединение. Подобные каталитические системы требуют создания специальных условий использования, поскольку термически и гидролитически нестабильны.
Запатентован [Mcateer, С.Н.; Davis, R.D., Sr.; Calvin, J.R., U.S. Patent 5 700 942, 1997] способ получения 8-метилхинолина (6) реакцией 2-метиланилина с формальдегидом и ацетальдегидом при 350°С в реакторе с псевдоожиженным слоем катализатора на основе цеолитов: H-ZSM-5, H-Beta, H-Y (схема 4). Мольное соотношение 2-метиланилин : формальдегид : ацетальдегид составляет 1:2:1. Выход 8-метилхинолина (6) - 50-55% при использовании цеолита H-Beta, 42-51% - на цеолите H-ZSM-5 и 29-53% на цеолите H-Y.
Схема 4
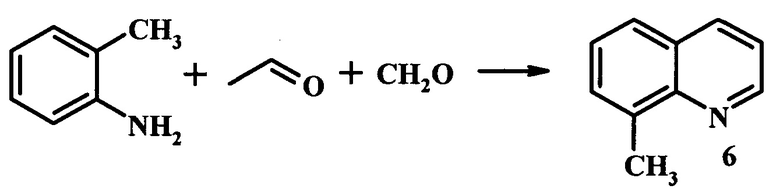
Недостатками данного способа является высокая температура реакции и получение в качестве основного продукта моноалкилхинолина, а не 2,3-диалкилхинолина.
Авторами [R. Brosius, D. Gammon, F. Van Laar, E. Van Steen, B. Sels, P. Jacobs, J. Catal., 2006, 239, 362] разработан метод синтеза 2-(4) и 4-метилхинолинов (5) реакцией анилина с ацетальдегидом на цеолите Н-Beta с мольным соотношением Si/Al=21,6 (схема 3). Реакцию проводили при 450°С, объемной скорости = 0,2 ч-1 и мольном соотношении анилин : ацетальдегид = 1:4 в течение 4,5 ч. Выход смеси метилхинолинов составил 83%.
Схема 3
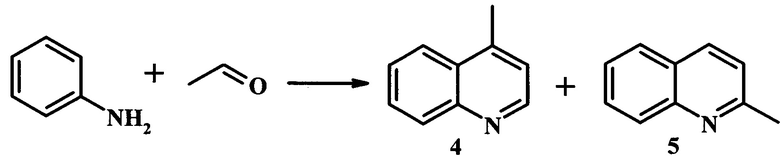
Недостатками данного метода является высокая температура реакции, большой избыток ацетальдегида, низкая объемная скорость подачи сырья и образование трудноразделимой смеси метилхинолинов. Кроме того, продуктами реакции являются моноалкилхинолины, а не 2,3-диалкилхинолины.
Задачей настоящего изобретения является разработка способа синтеза 2,3-диалкилхинолинов в более «мягких» условиях, более простого и селективного.
Решение этой задачи достигается тем, что синтез 2,3-диалкилхинолинов осуществляют реакцией анилина с алифатическими альдегидами (пропионовый, масляный, валерьяновый) в присутствии аморфного мезопористого алюмосиликата ASM.
Реакцию проводят в присутствии 5-20% мас. катализатора (ASM) при 120-180°С в растворе хлорбензола в течение 6 ч при мольном соотношении анилин : альдегид = 1:1-2. Конверсия анилина составляет 51-78%. Основным продуктом реакции являются 2,3-диалкилхинолины (7 а, б, в), образующиеся с селективностью 43-60% (схема 5). Кроме 2,3-диалкилхинолинов (7 а, б, в), в реакционной массе содержатся другие N-содержащие производные (например, 2,3-диалкил-N-фенил-1,2,3,4-тетрагидрохинолин-4-амины, 2,3-диалкил-дигидрохинолины) в количестве 40-57%.
Схема 5
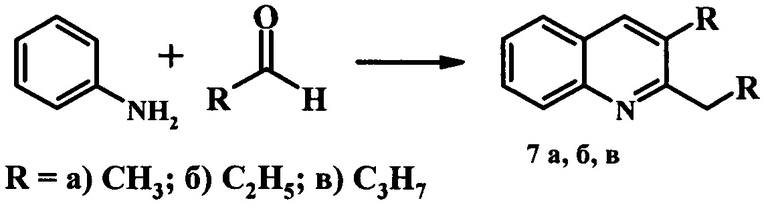
Мезопористый алюмосиликат ASM (Si/Al=40 и 100), получен двухстадийным золь-гель синтезом при переменном рН. Применение мезопористого алюмосиликата ASM в реакциях синтеза производных хинолина из анилина и альдегидов неизвестно.
Использование предлагаемого способа позволяет снизить энерго- и материалоемкость процесса гетероциклизации, поскольку:
1. Синтез 2,3-диалкилхинолинов проходит при более низкой температуре (120-180°С), чем в известных способах;
2. Используется мольное соотношение анилин : альдегид = 1:1-2, а не 1:4, как в описанных методиках.
Предлагаемый способ синтеза 2,3-диалкилхинолинов (7 а, б, в) осуществляют следующим образом.
Используют анилин и карбонильные соединения: пропионовый альдегид, масляный, валерьяновый альдегид.
В качестве катализатора используют аморфный мезопористый алюмосиликат ASM, синтезированный по методу, приведенному в [Аглиуллин М.Р., Григорьева Н.Г., Данилова И.Г., Магаев О.В., Водянкина О.В. // Кинетика и катализ. 2015. Т. 56. №4. С.507. Agliullin M.R., Danilova I.G., Faizullin A.V., Amarantov S.V., Bubennov S.V., Prosochkina T.R., Grigor'eva N.G., Paukshtis E.A., Kutepov B.I. // Micropor. Mesopor. Mat. 2016. V. 230. P. 118]. Образец ASM характеризуется узким распределением мезопор от 2 до 5 нм с объемом 0.70 см3/г.
Синтез 2,3-диалкилхинолинов проводят в металлическом автоклаве. В автоклав загружают анилин, альдегид (пропионовый, масляный, валерьяновый), катализатор и растворитель, герметично закрывают и помещают в термостатируемый шкаф, где автоклав непрерывно вращается при выбранной температуре. По окончании реакции реакционную массу охлаждают, отфильтровывают от нее катализатор. Состав продукта анализируют методом газожидкостной хроматографии. Условия ГЖХ-анализа: хроматограф Shimadzu GC-9A, пламенно-ионизационный детектор, 3 м насадочная колонка, фаза SE-30, программированный нагрев 50-250°С, газ-носитель гелий.
Структуру полученных 2,3-диалкилхинолинов (7 а, б, в) устанавливают на основании данных 1D и 2D ЯМР 1Н и 13С спектроскопии, их брутто-состав подтверждают регистрацией пика молекулярного иона в ГХ-МС спектре.
Изобретение иллюстрируется следующим примером:
Пример 1. В металлический автоклав загружают 0.25 мл (2.8 ммоль) анилина, затем 0.4 мл (5.6 ммоль) пропионового альдегида, 1 мл хлорбензола и 0.12 г (20% мас. в расчете на исходную смесь) мезопористого алюмосиликата ASM (Si/Al=40), автоклав герметично закрывают и помещают в термостатируемый шкаф. Реакцию проводят при температуре 160°С, 6 ч при непрерывном вращении автоклава. После окончания реакции реакционную массу охлаждают до комнатной температуры, отфильтровывают катализатор и хроматографируют на колонке (SiO2, элюент гексан → смесь гексан-этилацетат). Конверсия анилина 71%, селективность образования 2,3-диалкилхинолина (7а) 50%.
Пример 2. В металлический автоклав загружают 0.25 мл (2.8 ммоль) анилина, затем 0.52 мл (5.6 ммоль) масляного альдегида, 1 мл хлорбензола и 0.13 г (20% мас. в расчете на исходную смесь) мезопористого алюмосиликата ASM (Si/Al=40), автоклав герметично закрывают и помещают в термостатируемый шкаф. Реакцию проводят при температуре 160°С, 6 ч при непрерывном вращении автоклава. После окончания реакции реакционную массу охлаждают до комнатной температуры, отфильтровывают катализатор и хроматографируют на колонке (SiO2, элюент гексан → смесь гексан- этилацетат). Конверсия анилина 75%, селективность образования 2,3-диалкилхинолина (76) 44%.
Пример 3. В металлический автоклав загружают 0.25 мл (2.8 ммоль) анилина, затем 0.59 мл (5.6 ммоль) валерьянового альдегида, 1 мл хлорбензола и 0.15 г (20% мас. в расчете на исходную смесь) мезопористого алюмосиликата ASM (Si/Al=40), автоклав герметично закрывают и помещают в термостатируемый шкаф. Реакцию проводят при температуре 160°С, 6 ч при непрерывном вращении автоклава. После окончания реакции реакционную массу охлаждают до комнатной температуры, отфильтровывают катализатор и хроматографируют на колонке (SiO2, элюент гексан → смесь гексан-этилацетат). Конверсия анилина 78%, селективность образования 2,3-диалкилхинолина (7в) 43%.
Другие примеры (1,2,4-6) осуществления способа приведены в таблице.
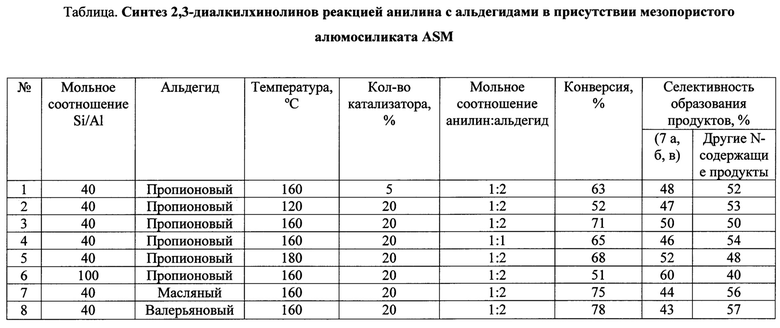
Реакцию проводят при 120-180°С, мольном соотношении анилин : альдегид = 1:1-2, 5-20% маc. катализатора, 6 ч, растворитель - хлорбензол.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛХИНОЛИНОВ | 2018 |
|
RU2688197C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛХИНОЛИНОВ | 2018 |
|
RU2688228C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛХИНОЛИНОВ | 2018 |
|
RU2690535C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛХИНОЛИНОВ | 2018 |
|
RU2687974C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛХИНОЛИНОВ | 2018 |
|
RU2688198C1 |
| Способ получения 2,3-диалкил-N-фенил-1,2,3,4-тетрагидрохинолин-4-аминов | 2018 |
|
RU2697875C1 |
| Способ получения 2,2,4-триалкил-2,3-дигидро-1Н-1,5-бензодиазепинов | 2019 |
|
RU2702359C1 |
| Способ получения 2,3-диалкил-N-фенил-1,2,3,4-тетрагидрохинолин-4-аминов | 2018 |
|
RU2697876C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-ПРОПИЛ-3-ЭТИЛХИНОЛИНА | 2009 |
|
RU2409567C2 |
| Способ получения 2,3-диалкил-N-фенил-1,2,3,4-тетрагидрохинолин-4-аминов | 2018 |
|
RU2702354C1 |
Изобретение относится к cпособу каталитического получения 2,3-диалкилхинолинов взаимодействием анилина с альдегидами, характеризующемуся тем, что в качестве катализатора используют аморфный мезопористый алюмосиликат ASM в количестве 5-20 мас.% по отношению к исходной смеси реагентов, реакцию проводят при мольном соотношении анилин : альдегид = 1:1-2 в автоклаве при 120-180°С в течение 6 ч в растворе хлорбензола. Способ позволяет упростить синтез производных хинолина и снизить энерго- и материалоемкость процесса гетероциклизации. 2 з.п. ф-лы, 3 пр., 1 табл.
1. Способ каталитического получения 2,3-диалкилхинолинов взаимодействием анилина с альдегидами, отличающийся тем, что в качестве катализатора используют аморфный мезопористый алюмосиликат ASM в количестве 5-20 мас.% по отношению к исходной смеси реагентов, реакцию проводят при мольном соотношении анилин : альдегид = 1:1-2 в автоклаве при 120-180°С в течение 6 ч в растворе хлорбензола.
2. Способ по п. 1, в котором аморфный мезопористый алюмосиликат ASM имеет мольное соотношение каркасных атомов Si/Al=40 и 100.
3. Способ по п. 1, в котором в качестве альдегидов используют пропионовый, масляный или валерьяновый альдегиды.
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛХИНОЛИНОВ | 2006 |
|
RU2309952C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2- И 2,3-ЗАМЕЩЕННЫХ ХИНОЛИНОВ | 2012 |
|
RU2504540C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛПРОИЗВОДНЫХ ХИНОЛИНА | 2005 |
|
RU2283836C1 |
| 2-(4-Пиридил)-3-этилхинолин в качестве ингибитора коррозии стали в водно-нефтяных средах | 1990 |
|
SU1759839A1 |
| Способ получения алкилпроизводных хинолина | 1986 |
|
SU1416487A1 |
| US 6103904 A1, 15.08.2000 | |||
| US 4180663 A1, 25.12.1979 | |||
| JP 10251233 A, 22.09.1998. | |||
Авторы
Даты
2019-05-17—Публикация
2018-11-30—Подача