РОДСТВЕННЫЕ ЗАЯВКИ НА ПАТЕНТЫ
Настоящая заявка испрашивает приоритет на основании заявки на патент Индии №3309/MUM/2013, поданной 22 октября 2013 года, полное содержание которой включено в настоящее описание посредством ссылки, как если бы оно было полностью переписано в настоящее описание.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к антибактериальным композициям и способам лечения или предотвращения бактериальных инфекций.
УРОВЕНЬ ТЕХНИКИ
Бактериальные инфекции продолжают оставаться одним из основных факторов, способствующих заболеваниям у людей. Одной из ключевых проблем при лечении бактериальных инфекций является способность бактерий вырабатывать с течением времени резистентность к одному или более антибактериальным агентам. Примеры таких бактерий, которые выработали резистентность к типичным антибактериальным агентам, включают резистентный к пенициллину Streptococcus pneumoniae, резистентные к ванкомицину Enterococci и резистентный к метициллину Staphylococcus aureus. Проблема возникновения резистентности к лекарственным средствам у бактерий часто решается за счет перехода на более новые антибактериальные агенты, которые могут быть более дорогими и иногда более токсичными. Кроме того, это не может быть постоянным решением, поскольку у бактерий часто с течением времени также развивается резистентность к более новым антибактериальным агентам. В целом, резистентность у бактерий развивается особенно эффективно, поскольку бактерии очень быстро размножаются и передают гены резистентности при репликации.
Лечение инфекций, вызванных резистентными бактериями, остается для врачебного сообщества ключевой проблемой. Одним из примеров такого сложного патогена является Acinetobacter baumannii (A. baumannii), лечение от которого становится все более сложной и затратной задачей для медицинских учреждений. Резистентность этого патогена ко множеству лекарств и его непредсказуемые схемы восприимчивости затрудняют поиск эмпирических и терапевтических решений. A. baumannii связан с инфекционными заболеваниями, такими как пневмония, бактериемия, раневые инфекции, инфекции мочевых путей и менингит.
Таким образом, существует необходимость разработки новых способов лечения инфекций, которые становятся резистентными к известным видам терапии и способам лечения. Неожиданно было обнаружено, что композиции, содержащие цефепим и некоторые азотсодержащие бициклические соединения (описанные в PCT/IB 2012/054290), проявляют неожиданную синергическую антибактериальную активность даже в отношении высокорезистентных штаммов бактерий.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Соответственно, предложены фармацевтические композиции, содержащие: (а) цефепим или его фармацевтически приемлемое производное и (b) соединение формулы (I), или его стереоизомер, или его фармацевтически приемлемое производное:
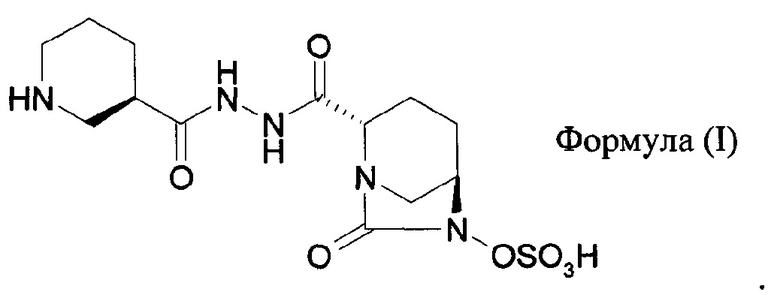
В одном общем аспекте настоящего изобретения предложены фармацевтические композиции, содержащие: (а) цефепим или его фармацевтически приемлемое производное и (b) соединение формулы (I), или его стереоизомер, или его фармацевтически приемлемое производное; причем указанное соединение формулы (I), или его стереоизомер, или его фармацевтически приемлемое производное присутствует в композиции в количестве от примерно 0,25 грамма до примерно 4 граммов на грамм цефепима или его фармацевтически приемлемого производного.
В еще одном общем аспекте настоящего изобретения предложены способы лечения или предотвращения бактериальной инфекции у субъекта, включающие введение указанному субъекту эффективного количества фармацевтической композиции, содержащей: (а) цефепим или его фармацевтически приемлемое производное; и (b) соединение формулы (I), или его стереоизомер, или его фармацевтически приемлемое производное.
В другом общем аспекте настоящего изобретения предложены способы лечения или предотвращения бактериальной инфекции у субъекта, включающие введение указанному субъекту эффективного количества фармацевтической композиции, содержащей: (а) цефепим или его фармацевтически приемлемое производное, и (b) соединение формулы (I), или его стереоизомер, или его фармацевтически приемлемое производное; причем указанное соединение формулы (I), или его стереоизомер, или его фармацевтически приемлемое производное присутствует в композиции в количестве от примерно 0,25 грамма до примерно 4 граммов на грамм цефепима или его фармацевтически приемлемого производного.
В еще одном общем аспекте настоящего изобретения предложены способы лечения или предотвращения бактериальной инфекции у субъекта, включающие введение указанному субъекту эффективного количества: (а) цефепима или его фармацевтически приемлемого производного; и (b) соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного.
В другом общем аспекте настоящего изобретения предложены способы лечения или предотвращения бактериальной инфекции у субъекта, включающие введение указанному субъекту эффективного количества: (а) цефепима или его фармацевтически приемлемого производного и (b) соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного; причем указанное соединение формулы (I), или его стереоизомер, или его фармацевтически приемлемое производное вводят в количестве от примерно 0,25 грамма до примерно 4 граммов на грамм цефепима или его фармацевтически приемлемого производного.
Подробности одного или более вариантов реализации настоящего изобретения изложены в приведенном ниже описании. Другие отличительные признаки, цели и преимущества настоящего изобретения станут очевидными из приведенного ниже описания, включая формулу изобретения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Далее будут приведены ссылки на иллюстративные варианты реализации настоящего изобретения, и для их описания в настоящем изобретении будет применяться специфическая терминология. Это ни в коей мере не следует понимать как ограничение объема настоящего изобретения. Вносимые изменения и дальнейшие модификации признаков настоящего изобретения, проиллюстрированных в данном документе, которые могут производиться специалистом в соответствующей области техники, ознакомившимся с настоящим описанием, следует рассматривать как находящиеся в рамках объема настоящего изобретения. Следует отметить, что в контексте настоящего описания и прилагаемой формулы изобретения неопределенные и определенные формы единственного числа включают формы множественного числа, если из содержания явным образом не следует иное. Содержание всех ссылок, включая патенты, патентные заявки и литературу, цитируемую в описании, специально полностью включено в настоящее описание посредством ссылки, как если бы оно было полностью переписано в настоящее описание.
Авторы настоящего изобретения неожиданно обнаружили, что фармацевтическая композиция, содержащая: (а) цефепим или его фармацевтически приемлемое производное и (b) соединение формулы (I), или его стереоизомер, или его фармацевтически приемлемое производное проявляет неожиданно улучшенную антибактериальную эффективность даже в отношении высокорезистентных бактерий, включая бактерии, продуцирующие ферменты бета-лактамазы расширенного спектра (БЛРС).
Термин «инфекция» или «бактериальная инфекция» в контексте настоящего описания включает присутствие бактерий в субъекте или на субъекте, в отношении которого в случае подавления роста бактерий обеспечивалась бы польза для субъекта. Таким образом, термин «инфекция» наряду с тем, что он относится к присутствию бактерий, также относится к присутствию других флор, которые являются нежелательными. Термин «инфекция» включает инфекцию, вызванную бактериями.
Термины «лечить», «проведение лечения» или «лечение» в контексте настоящего описания относятся к введению лекарственного средства, включая фармацевтическую композицию, либо одного или более фармацевтически активных ингредиентов, в профилактических и/или терапевтических целях. Термин «профилактическое лечение» относится к лечению субъекта, который еще не заражен, но который подвержен тем или иным образом риску получения инфекции (предотвращение бактериальной инфекции). Термин «терапевтическое лечение» относится к проведению лечения в отношении субъекта, который уже страдает от инфекции. Термины «проведение лечения» или «лечение» в контексте настоящего описания также относятся к введению композиций или одного или более фармацевтически активных ингредиентов, обсуждаемых в настоящем описании, совместно с дополнительными фармацевтически активными или инертными ингредиентами или без них, для того чтобы: (i) уменьшать или устранять либо бактериальную инфекцию, либо один или более симптомов бактериальной инфекции, или (ii) замедлять прогрессирование бактериальной инфекции или одного или более симптомов бактериальной инфекции, или (iii) уменьшать тяжесть бактериальной инфекции или одного или более симптомов бактериальной инфекции, или (iv) подавлять клинические проявления бактериальной инфекции, или (v) подавлять проявление неблагоприятных симптомов бактериальной инфекции.
Термины «фармацевтически эффективное количество» или «терапевтически эффективное количество» или «эффективное количество» в контексте настоящего описания относятся к количеству, которое оказывает лечебное действие или представляет собой такое количество, которое необходимо для получения терапевтического эффекта у субъекта. Например, «терапевтически эффективное количество» или «фармацевтически эффективное количество» или «эффективное количество» антибактериального агента или фармацевтической композиции представляет собой количество антибактериального агента или фармацевтической композиции, необходимой для получения желаемого терапевтического эффекта, о котором можно будет судить по результатам клинических испытаний, исследований на модели инфекции у животных и/или исследований in vitro (например, в среде с агаром или бульоном). Такое эффективное количество зависит от нескольких факторов, включая, но не ограничиваясь ими, вовлеченный микроорганизм (например, бактерию), характеристики субъекта (например, рост, вес, пол, возраст и историю болезни), тяжесть инфекции и конкретный тип применяемого бактерицидного агента. Для профилактического лечения профилактически эффективное количество представляет собой такое количество, которое было бы эффективным для предотвращения бактериальной инфекции.
Термин «введение» или «осуществление введения» означает и включает доставку композиции или одного или более фармацевтически активных ингредиентов субъекту, включая, например, любой подходящий способ, который служит для доставки композиции или ее активных ингредиентов или других фармацевтически активных ингредиентов к месту инфекции. Способ введения может изменяться в зависимости от различных факторов, таких как, например, компоненты фармацевтической композиции или тип/характер фармацевтически активных или инертных ингредиентов, место потенциальной или фактической инфекции, вовлеченный микроорганизм, тяжесть инфекции, возраст и физическое состояние пациента и тому подобное. Некоторые неограничивающие примеры способов введения пациенту композиции или фармацевтически активного ингредиента согласно настоящему изобретению включают пероральный, внутривенный, местный, внутриреспираторный, внутрибрюшинный, внутримышечный, парентеральный, сублингвальный, трансдермальный, интраназальный, аэрозольный, внутриглазной, внутритрахеальный, ректальный, вагинальный, посредством генной пушки, посредством кожного пластыря, с помощью глазных капель и жидкости для полоскания рта. В случае, когда фармацевтическая композиция содержит более одного ингредиента (активных или инертных), один из способов введения такой композиции представляет собой смешивание ингредиентов (например, в виде подходящей единичной дозированной формы, такой как таблетка, капсула, раствор, порошок или тому подобное), а затем введение лекарственной формы. В качестве альтернативы ингредиенты можно также вводить раздельно (одновременно или один за другим) до тех пор, пока эти ингредиенты не достигнут полезных терапевтических уровней, так что композиция как целое будет обеспечивать синергический и/или желаемый эффект.
Термин «рост» в контексте настоящего описания относится к росту одного или более микроорганизмов и включает репродукцию или расширение популяции микроорганизма (например, бактерии). Термин «рост» также включает поддержание текущих метаболических процессов микроорганизма, включая процессы, которые поддерживают микроорганизм в живом состоянии.
Термин «эффективность» в контексте настоящего описания относится к способности лечения, или композиции, или одного или более фармацевтически активного ингредиента вызывать желаемый биологический эффект у субъекта. Например, термин «антибактериальная эффективность» композиции или антибактериального агента относится к способности композиции или антибактериального агента предотвращать или лечить бактериальную инфекцию у субъекта.
Термин «синергический» или «синергия» в контексте настоящего описания относится к такому взаимодействию двух или более агентов, при котором их комбинированное действие больше, чем их индивидуальные действия.
Термин «антибактериальный агент» в контексте настоящего описания относится к любому веществу, соединению, комбинации веществ или комбинации соединений, способной к: (i) подавлению, уменьшению или предотвращению роста бактерий; (ii) подавлению или уменьшению способности бактерий служить источником инфекции у субъекта; или (iii) подавлению или снижению способности бактерий размножаться или оставаться заражающими в окружающей среде. Термин «антибактериальный агент» также относится к соединениям, способным к снижению инфицирующей способности или вирулентности бактерий.
Термин «бета-лактамный антибактериальный агент» в контексте настоящего описания относится к соединениям с антибактериальными свойствами, содержащими бета-лактамное ядро в своей молекулярной структуре.
Термин «бета-лактамаза» или «фермент бета-лактамаза» в контексте настоящего описания относится к любому ферменту или белку или любому другому веществу, которое разрывает бета-лактамное кольцо. Термин «бета-лактамаза» включает ферменты, которые вырабатываются бактериями и обладают способностью гидролизовать бета-лактамное кольцо в бета-лактамном соединении, либо частично, либо полностью.
Термин «бета-лактамаза расширенного спектра» (БЛРС) в контексте настоящего описания включает те ферменты бета-лактамазы, которые способны давать бактериям резистентность к различным бета-лактамным антибактериальным агентам, таким как пенициллины, цефалоспорины, азтреонам и тому подобное.
Термин «ингибитор бета-лактамазы» в контексте настоящего описания относится к соединению, способному ингибировать активность одного или более бета-лактамазных ферментов, либо частично, либо полностью.
Термин «колониеобразующие единицы» или «КОЕ» в контексте настоящего описания относится к оценке количества жизнеспособных бактериальных клеток на миллилитр образца. Как правило, «колония бактерий» относится к массе отдельных бактерий, растущих совместно.
Термин «фармацевтически инертный ингредиент», или «носитель», или «вспомогательное вещество» означает и включает соединения или материалы, применяемые для облегчения введения соединения, например, для повышения растворимости соединения. Типичные неограничивающие примеры твердых носителей включают крахмал, лактозу, дикальцийфосфат, сахарозу и каолин. Типичные неограничивающие примеры жидких носителей включают стерильную воду, физиологический раствор, буферы, неионные поверхностно-активные вещества и пищевые масла. Кроме того, также могут быть включены различные добавки, обычно применяемые в данной области техники. Эти и другие подобные соединения описаны в литературе, например, в Merck Index (Merck & Company, Rahway, N.J.). Соображения по включению различных компонентов в фармацевтические композиции описаны, например, в публикации Gilman et al. (Goodman and Gilman’s: The Pharmacological Basis of Therapeutics, 8th Ed., Pergamon Press., 1990), которая полностью включена в настоящее описание посредством ссылки.
Термин «субъект» в контексте настоящего описания относится к позвоночным или беспозвоночным, включая млекопитающих. Термин «субъект» включает людей, животных, птицу, рыбу или земноводное. Типичные неограничивающие примеры «субъекта» включают людей, кошек, собак, лошадей, овец, крупный рогатый скот, коров, свиней, ягнят, крыс, мышей и морских свинок.
Термин «фармацевтически приемлемое производное» в контексте настоящего описания означает и включает любую фармацевтически приемлемую соль, пролекарство, метаболит, сложный эфир, простой эфир, гидрат, полиморф, сольват, комплекс и аддукт описанного здесь соединения, которое при введении субъекту способно обеспечивать (прямо или косвенно) исходное соединение. Например, термин «антибактериальный агент или его фармацевтически приемлемое производное» включает все производные антибактериального агента (такие как соли, пролекарства, метаболиты, сложные эфиры, простые эфиры, гидраты, полиморфы, сольваты, комплексы и аддукты), которые в результате введения субъекту способны обеспечивать (прямо или косвенно) антибактериальный агент.
Термин «фармацевтически приемлемая соль» в контексте настоящего описания относится к одной или более соли данного соединения, которая обладает желаемой фармакологической активностью свободного соединения и которая не является нежелательной, ни биологически, ни иным образом. В общем, термин «фармацевтически приемлемая соль» относятся к солям, которые пригодны для применения для контакта с тканями человека и животных без чрезмерной токсичности, раздражения, аллергической реакции и тому подобного и соизмеримы с разумным соотношением польза/риск. Фармацевтически приемлемые соли хорошо известны в данной области техники. Например, в публикации S.М. Berge, et al. (J. Pharmaceutical Sciences, 66; 1-19, 1977), полностью включенной в настоящее описание посредством ссылки, детально описаны различные фармацевтически приемлемые соли.
Термин «стереоизомер» в контексте настоящего описания означает и включает изомерные молекулы, которые имеют одинаковую молекулярную формулу, но различаются по расположению атомов и/или функциональной группы в пространстве. Стереоизомеры могут быть дополнительно классифицированы как энантиомеры (где различные изомеры являются зеркальными образами каждого другого) и диастереомеры (где различные изомеры не являются зеркальными образами каждого другого). Диастереомеры включают изомеры, такие как конформеры, мезосоединения, цис-транс (Е-Z) изомеры, и неэнантиомерные оптические изомеры.
Специалисту в данной области техники будет понятно, что различные описанные в настоящем документе соединения (включая, например соединение формулы (I) и цефепим), могут существовать и часто применяться в качестве их фармацевтически приемлемых производных (например, солей, пролекарств, метаболитов, сложных эфиров, простых эфиров, гидратов, полиморфов, сольватов, комплексов и аддуктов).
В одном общем аспекте настоящего изобретения предложены фармацевтические композиции, содержащие: (а) цефепим или его фармацевтически приемлемое производное и (b) соединение формулы (I), или его стереоизомер, или его фармацевтически приемлемое производное:

Соединение формулы (I) согласно настоящему изобретению может быть применено в различных формах, включая в качестве таковых его стереоизомер или его фармацевтически приемлемое производное. Соединение формулы (I) (регистрационный номер CAS 1436861-97-0) также может быть известно под разными названиями, включая следующие: (а) транс-моно-[2-(N’-[(R)-пиперидин-3-карбонил]-гидразинокарбонил)-7-оксо-1,6-диазабицикло[3.2.1]окт-6-иловый] эфир серной кислоты; (b) (2S,5R)-моно-[2-(N’-[(R)-пиперидин-3-карбонил]-гидразинокарбонил)-7-оксо-1,6-диазабицикло[3.2.1]окт-6-иловый]эфир серной кислоты; или (с) "(1R,2S,5R)-1,6-диазабицикло[3.2.1]октан-2-карбоновая кислота, 7-оксо-6-(сульфоокси)-, 2-[2-[(3R)-3-пиперидинилкарбонил]гидразид]. Обозначение «соединение формулы (I)» предназначено для включения соединений, известных с точки зрения химии как: (а) транс-моно-[2-(N’-[(R)-пиперидин-3-карбонил]-гидразинокарбонил)-7-оксо-1,6-диаза-бицикло[3.2.1]окт-6-иловый] эфир серной кислоты; (b) (2S,5R)-моно-[2-(N’-[(R)-пиперидин-3-карбонил]-гидразинокарбонил)-7-оксо-1,6-диазабицикло[3.2.1]окт-6-иловый] эфир серной кислоты; или (с) (1R,2S,5R)-1,6-диазабицикло[3.2.1]октан-2-карбоновая кислота, 7-оксо-6-(сульфокси)-, 2-[2-[(3R)-3-пиперидинилкарбонил]гидразид].
Соединение формулы (I) также может быть применено в форме его стереоизомера или его фармацевтически приемлемого производного. Типичные неограничивающие примеры стереоизомерных форм соединения формулы (I) включают следующие:
(a) (1R,2S,5R)-1,6-диазабицикло[3.2.1]октан-2-карбоновую кислоту, 7-оксо-6-(сульфоокси)-, 2-[2-(3-пиперидинилкарбонил)гидразид];
(b) (2S,5R)-1,6-диазабицикло[3.2.1]октан-2-карбоновую кислоту, 7-оксо-6-(сульфоокси)-, 2-[2-[(3S)-3-пиперидинилкарбонил]гидразид];
(c) (2S,5R)-1,6-диазабицикло[3.2.1]октан-2-карбоновую кислоту, 7-оксо-6-(сульфоокси)-, 2-[2-(3-пиперидинилкарбонил)гидразид]; и
(d) (1R,2S,5R)-1,6-диазабицикло [3.2.1]октан-2-карбоновую кислоту, 7-оксо-6-(сульфоокси)-, 2- [2-[(3R)-3-пиперидинилкарбонил]гидразид].
Типичные неограничивающие примеры подходящих фармацевтически приемлемых производных соединения формулы (I) включают различные соли, такие как натриевая, калиевая и/или любая другая соль.
В другом общем аспекте настоящего изобретения предложены фармацевтические композиции, содержащие: (а) цефепим или его фармацевтически приемлемое производное и (b) соединение формулы (I), или его стереоизомер, или его фармацевтически приемлемое производное; причем указанное соединение формулы (I), или его стереоизомер, или его фармацевтически приемлемое производное присутствует в композиции в количестве от примерно 0,25 грамма до примерно 4 граммов на грамм цефепима или его фармацевтически приемлемого производного.
И цефепим, и соединение формулы (I) могут присутствовать в композиции в их свободных формах или в виде их фармацевтически приемлемых производных (таких как соли, про лекарства, метаболиты, сложные эфиры, простые эфиры, гидраты, полиморфы, сольваты, комплексы или аддукты).
Отдельные количества соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного и цефепима или его фармацевтически приемлемого производного в композиции может варьироваться в зависимости от клинических потребностей. В некоторых вариантах реализации настоящего изобретения соединение формулы (I), или его стереоизомер, или его фармацевтически приемлемое производное присутствует в композиции в количестве от примерно 0,01 грамма до примерно 10 граммов. В некоторых других вариантах реализации настоящего изобретения цефепим или его фармацевтически приемлемое производное присутствует в композиции в количестве от примерно 0,01 грамма до примерно 10 граммов.
В некоторых вариантах реализации настоящего изобретения фармацевтическая композиция согласно настоящему изобретению содержит примерно 1 грамм соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного и примерно 2 грамма цефепима или его фармацевтически приемлемого производного.
В некоторых других вариантах реализации настоящего изобретения фармацевтическая композиция согласно настоящему изобретению содержит примерно 2 грамма соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного и примерно 2 грамма цефепима или его фармацевтически приемлемого производного.
В некоторых вариантах реализации настоящего изобретения фармацевтическая композиция согласно настоящему изобретению содержит примерно 0,5 грамма соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного и примерно 2 грамма цефепима или его фармацевтически приемлемого производного.
В некоторых вариантах реализации настоящего изобретения фармацевтическая композиция согласно настоящему изобретению содержит примерно 0,25 грамма соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного и примерно 1 грамм цефепима или его фармацевтически приемлемого производного.
В некоторых других вариантах реализации настоящего изобретения фармацевтическая композиция согласно настоящему изобретению содержит примерно 0,5 грамма соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного и примерно 1 грамм цефепима или его фармацевтически приемлемого производного.
В некоторых вариантах реализации настоящего изобретения фармацевтическая композиция согласно настоящему изобретению содержит примерно 1 грамм соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного и примерно 1 грамм цефепима или его фармацевтически приемлемого производного.
В некоторых вариантах реализации настоящего изобретения фармацевтическая композиция согласно настоящему изобретению содержит примерно 2 грамма соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного и примерно 1 грамм цефепима или его фармацевтически приемлемого производного.
В некоторых вариантах реализации настоящего изобретения фармацевтическая композиция согласно настоящему изобретению содержит примерно 1 грамм соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного и примерно 0,5 грамм цефепима или его фармацевтически приемлемого производного.
Фармацевтические композиции согласно настоящему изобретению могут содержать один или более фармацевтически приемлемых носителей, или вспомогательных веществ, или тому подобное. Типичные неограничивающие примеры таких носителей или вспомогательных веществ включают маннитол, лактозу, крахмал, стеарат магния, сахарин натрия, тальк, целлюлозу, кроскармелозу натрия, глюкозу, желатин, сахарозу, карбонат магния, смачивающие агенты, эмульгирующие агенты, солюбилизирующие агенты, буферные агенты, смазывающие агенты, консерванты, стабилизирующие агенты, связывающие агенты и тому подобное.
Фармацевтические композиции, или активные ингредиенты согласно настоящему изобретению могут быть приготовлены в виде различных лекарственных форм, таких как твердые, полутвердые, жидкие и аэрозольные лекарственные формы. Типичные неограничивающие примеры некоторых лекарственных форм включают таблетки, капсулы, порошки, растворы, суспензии, суппозитории, аэрозоли, гранулы, эмульсии, сиропы, эликсиры и тому подобное.
В некоторых вариантах реализации настоящего изобретения фармацевтические композиции согласно настоящему изобретению представлены в виде порошка или раствора. В некоторых других вариантах реализации настоящего изобретения фармацевтические композиции согласно настоящему изобретению представлены в виде порошка или раствора, который может быть восстановлен путем добавления совместимого восстанавливающего разбавителя перед введением. В некоторых других вариантах реализации настоящего изобретения фармацевтические композиции согласно настоящему изобретению представлены в виде замороженной композиции, которая может быть разбавлена совместимым восстанавливающим разбавителем перед введением. Типичные неограничивающие примеры подходящего совместимого восстанавливающего разбавителя включают воду.
В некоторых других вариантах реализации настоящего изобретения фармацевтические композиции согласно настоящему изобретению находятся в форме, готовой к применению для парентерального введения.
Композиции согласно настоящему изобретению могут быть приготовлены в виде различных лекарственных форм, в которых активные ингредиенты и/или вспомогательные вещества могут присутствовать либо совместно (например, в качестве добавки), либо в виде отдельных компонентов. Когда различные ингредиенты в композиции готовят в виде смеси, такие композиции могут быть доставлены посредством введения такой смеси субъекту с помощью любого подходящего способа введения. В качестве альтернативы, фармацевтические композиции согласно настоящему изобретению также могут быть приготовлены в виде лекарственной формы, в которой один или более ингредиентов (таких, как активные или неактивные ингредиенты) присутствуют в виде отдельных компонентов. Такую композицию или лекарственную форму, в которой ингредиенты не присутствуют в виде смеси, а присутствуют в виде отдельных компонентов, можно вводить несколькими способами. В одном из возможных способов ингредиенты могут быть смешаны в нужных пропорциях, и смесь восстанавливают в подходящем восстанавливающем разбавителе и затем вводят по мере необходимости. В качестве альтернативы компоненты или ингредиенты (активные или инертные) можно вводить отдельно (одновременно или один за другим) в соответствующей пропорции таким образом, чтобы достичь того же или эквивалентного терапевтического уровня или действия, как было бы достигнуто путем введения эквивалентной смеси.
В некоторых вариантах реализации настоящего изобретения фармацевтические композиции согласно настоящему изобретению готовят в виде лекарственной формы, такой, что соединение формулы (I), или его стереоизомер, или его фармацевтически приемлемое производное и цефепим или его фармацевтически приемлемое производное присутствуют в композиции в виде смеси или в виде отдельных компонентов. В некоторых других вариантах реализации настоящего изобретения фармацевтические композиции согласно настоящему изобретению готовят в виде лекарственной формы, такой, что соединение формулы (I), или его стереоизомер, или его фармацевтически приемлемое производное и цефепим или его фармацевтически приемлемое производное присутствуют в композиции в виде отдельных компонентов.
В одном общем аспекте настоящего изобретения фармацевтические композиции согласно настоящему изобретению применяют для лечения или предотвращения бактериальной инфекции.
В другом общем аспекте настоящего изобретения предложены способы лечения или предотвращения бактериальной инфекции у субъекта, включающий введение указанному субъекту эффективного количества фармацевтической композиции согласно настоящему изобретению. В случае лекарственных форм, когда соединение формулы (I), или его стереоизомер, или его фармацевтически приемлемое производное и цефепим или его фармацевтически приемлемое производное присутствуют в композиции в виде отдельных компонентов, соединение формулы (I), или его стереоизомер, или его фармацевтически приемлемое производное можно вводить до, после или одновременно с введением цефепима или его фармацевтически приемлемого производного.
В еще одном общем аспекте настоящего изобретения предложены способы лечения или предотвращения бактериальных инфекций у субъекта, причем указанные способы включают введение указанному субъекту эффективного количества: (а) цефепима или его фармацевтически приемлемого производного и (b) соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного:

В другом общем аспекте настоящего изобретения предложены способы лечения или предотвращения бактериальных инфекций у субъекта, включающие введение указанному субъекту эффективного количества: (а) цефепима или его фармацевтически приемлемого производного и (b) соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного; причем количество вводимого соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного составляет от примерно 0,25 грамма до примерно 4 граммов на грамм цефепима или его фармацевтически приемлемого производного.
В некоторых вариантах реализации настоящего изобретения предложен способ лечения или предотвращения бактериальной инфекции у субъекта, включающий введение указанному субъекту: (а) цефепима или его фармацевтически приемлемого производного и (b) соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного в любом из следующих количеств:
(i) примерно 1 грамм соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного и примерно 2 грамма цефепима или его фармацевтически приемлемого производного;
(ii) примерно 2 грамма соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного и примерно 2 грамма цефепима или его фармацевтически приемлемого производного;
(iii) примерно 0,5 грамма соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного и примерно 2 грамма цефепима или его фармацевтически приемлемого производного;
(iv) примерно 0,25 грамма соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного и примерно 1 грамм цефепима или его фармацевтически приемлемого производного;
(v) примерно 0,5 грамма соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного и примерно 1 грамм цефепима или его фармацевтически приемлемого производного;
(vi) примерно 1 грамм соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного и примерно 1 грамм цефепима или его фармацевтически приемлемого производного;
(vii) примерно 2 грамма соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного и примерно 1 грамм цефепима или его фармацевтически приемлемого производного; или
(viii) примерно 1 грамм соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного и примерно 0,5 грамма цефепима или его фармацевтически приемлемого производного.
В некоторых вариантах реализации настоящего изобретения в способах согласно настоящему изобретению соединение формулы (I), или его стереоизомер, или его фармацевтически приемлемое производное вводят в количестве от примерно 0,01 грамма до примерно 10 граммов. В некоторых других вариантах реализации настоящего изобретения в способах согласно настоящему изобретению цефепим или его фармацевтически приемлемое производное вводят в количестве от примерно 0,01 грамма до примерно 10 граммов.
В некоторых вариантах реализации настоящего изобретения в способах согласно настоящему изобретению соединение формулы (I), или его стереоизомер, или его фармацевтически приемлемое производное вводят до, после или одновременно с введением цефепима или его фармацевтически приемлемого производного.
В способах согласно настоящему изобретению фармацевтическая композиция и/или другие фармацевтически активные ингредиенты, представленные в настоящем описании, могут быть введены любым подходящим способом, который служит для доставки композиции, или ее составных частей, или активных ингредиентов к нужному месту. Способ введения может меняться в зависимости от различных факторов, таких, как, например, компоненты фармацевтической композиции и природа активных ингредиентов, место потенциальной или фактической инфекции, вовлеченный микроорганизм (например, бактерия), тяжесть инфекции, возраст и физическое состояние субъекта. Некоторые неограничивающие примеры введения композиции субъекту согласно настоящему изобретению включают пероральное, внутривенное, местное, внутриреспираторное, внутрибрюшинное, внутримышечное, парентеральное, сублингвальное, трансдермальное, интраназальное, аэрозольное, внутриглазное, внутритрахеальное, ректальное, вагинальное, посредством генной пушки, кожного пластыря, глазных капель, ушных капель или жидкости для полоскания рта. В некоторых вариантах реализации настоящего изобретения композиции или один или более активных ингредиентов согласно настоящему изобретению вводят парентерально.
В некоторых вариантах реализации настоящего изобретения в композициях и способах согласно настоящему изобретению соединение формулы (I) представляет собой транс-моно-[2-(Н’-[(R)-пиперидин-3-карбонил]-гидразинокарбонил)-7-оксо-1,6-диазабицикло[3.2.1]окт-6-иловый]эфир серной кислоты. В некоторых других вариантах реализации в композициях и способах согласно настоящему изобретению соединение формулы (I) представляет собой "(1R,2S,5R)-1,6-диазабицикло[3.2.1]октан-2-карбоновую кислоту, 7-оксо-6-(сульфоокси)-, 2-[2-[(3R)-3-пиперидинилкарбонил]гидразид]". В некоторых вариантах реализации в композициях и способах согласно настоящему изобретению соединение формулы (I) представляет собой (2S,5R)-моно-[2-(N’-[(R)-пиперидин-3-карбонил]-гидразинокарбонил)-7-оксо-1,6-диазабицикло[3.2.1]октил-6-иловый] эфир серной кислоты. В некоторых вариантах реализации настоящего изобретения в композициях и способах согласно настоящему изобретению соединение формулы (I) присутствует в виде натриевой или калиевой соли (1R,2S,5R)-1,6-диазабицикло[3.2.1]октан-2-карбоновой кислоты, 7-оксо-6-(сульфоокси)-, 2-[2-[(3R)-3-пиперидинилкарбонил]гидразида].
В некоторых вариантах реализации настоящего изобретения предложен способ повышения антибактериальной эффективности цефепима или его фармацевтически приемлемого производного в отношении субъекта, включающий совместное введение цефепима или его фармацевтически приемлемый производного с соединением формулы (I), или его стереоизомером, или его фармацевтически приемлемым производным. В некоторых других вариантах реализации настоящего изобретения предложен способ повышения антибактериальной эффективности цефепима или его фармацевтически приемлемого производного в отношении субъекта, причем указанный способ включает совместное введение цефепима или его фармацевтически приемлемого производного с соединением формулы (I), или его стереоизомером, или его фармацевтически приемлемым производным, причем количество соединения формулы (I), или его стереоизомера, или его фармацевтически приемлемого производного составляет от примерно 0,25 грамма до примерно 4 граммов на грамм цефепима или его фармацевтически приемлемого производного.
С помощью композиций и способов согласно настоящему изобретению можно лечить или предотвращать широкое разнообразие бактериальных инфекций. Типичные неограничивающие примеры бактериальных инфекций, которые можно лечить или предотвращать с помощью способов и/или фармацевтических композиций согласно настоящему изобретению, включают инфекции Е. coli, Yersinia pestis (легочную чуму), стафилококковую инфекцию, микобактериальную инфекцию, бактериальную пневмонию, дизентерию Shigella, инфекции Serratia, инфекции Candida, инфекцию Cryptococcal, сибирскую язву, туберкулез или инфекции, вызванные Pseudomonas aeruginosa, Acinetobacter baumannii или устойчивым к метициллину Staphylococcus aureus (MRSA) и т.д.
Фармацевтические композиции и способы согласно настоящему изобретению полезны для лечения или предотвращения некоторых инфекций, включая, например, инфекции кожи и мягких тканей, фебрильную нейтропению, инфекцию мочевыводящих путей, интраабдоминальные инфекции, инфекции дыхательных путей, пневмонию (нозокомиальную), бактериальный менингит, хирургические инфекции и тому подобное.
В некоторых вариантах реализации настоящего изобретения фармацевтические композиции и способы согласно настоящему изобретению применяют для лечения или предотвращения инфекций, вызванных резистентными бактериями. В некоторых других вариантах реализации настоящего изобретения композиции и способы согласно настоящему изобретению применяют для лечения или предотвращения инфекций, вызванных бактериями, вырабатывающими один или более ферментов бета-лактамазы.
В общем, фармацевтические композиции и способы, описанные в настоящем документы, также эффективны для предотвращения или лечения инфекций, вызванных бактериями, которые считаются менее восприимчивыми или невосприимчивыми к одному или более из известных антибактериальных агентов или их известных композиций. Некоторые неограничивающие примеры таких бактерий, которые, как известно, выработали резистентность к различным антибактериальных агентам, включают Acinetobacter, Escherichia coli, Pseudomonas aeruginosa, Staphylococcus aureus, Enterobacter, Klebsiella, Citrobacter и тому подобные.
ПРИМЕРЫ
Следующие примеры иллюстрируют варианты реализации настоящего изобретения, которые в настоящее время наиболее известны. Тем не менее, следует понимать, что приведенная ниже информация приведена только в качестве примера или иллюстрации применения принципов настоящего изобретения. Многочисленные модификации и альтернативные композиции, способы и системы могут быть разработаны специалистами в данной области техники, не выходя за пределы сущности и объема настоящего изобретения. Прилагаемая формула изобретения предназначена для охвата таких модификаций и договоренностей. Таким образом, несмотря на то, что настоящее изобретение было подробно описано выше, в следующих примерах представлена дополнительная подробная информация в отношении того, что в настоящее время считается наиболее применимыми на практике вариантами реализации настоящего изобретения.
Исследовали антибактериальную активность комбинаций согласно настоящему изобретению в отношении различных штаммов бактерий. В типичном исследовании определяли минимальные ингибирующие концентрации (МИК) с использованием агара Мюллера-Хинтона (МНА) (BD, США) согласно рекомендациям Института клинических и лабораторных стандартов (Clinical and Laboratory Standards Institute (CLSI)), (Clinical and Laboratory Standards Institute (CLSI), Performance Standards for Antimicrobial Susceptibility Testing, 20th Informational Supplement, M 100-S20, Volume 30, No. 1, 2010). Вкратце, количество микроорганизмов в инокуляте доводили до примерно 104 колониеобразующих единиц (КОЕ) на лунку многолуночного инокулятора (Applied Quality Services, Соединенное Королевство). В планшеты вносили тестируемые комбинации согласно настоящему изобретению в МНА с двукратным увеличением их концентраций. Планшеты инокулировали и инкубировали при 35°C в течение 18 часов. За МИК принимали наименьшую концентрацию лекарственного средства, при которой достигалось полное ингибирование роста бактерий.
Синергический уничтожающий эффект, достигаемый комбинациями согласно настоящему изобретению, исследовали путем проведения обычных исследований уничтожения бактерий в определенном промежутке времени. Как правило, свежевыращенные культуры разводили до требуемой плотности клеток (исходный инокулят) в бульоне Мюллера-Хинтона с отрегулированным содержанием катионов (BD, США). Антибактериальные агенты при требуемых концентрациях добавляли в среду либо по отдельности, либо в комбинации. Образцы инкубировали в условиях встряхивания (120 оборотов в минуту) при 37°C. Подсчет количества жизнеспособных бактерий осуществляли каждые 2 часа путем разбавления в физиологическом растворе и высева на планшеты с триптон-соевым агаром (BD, США). Планшеты инкубировали в течение 24 часа с получением определенного количества жизнеспособных бактерий. Результаты выражали в виде Log КОЕ на мл. Уменьшение количества бактерий после введения комбинации согласно настоящему изобретению по сравнению с исходным количеством бактерий, составляющее 1 Log КОЕ/мл, соответствовало 90% уничтожения бактерий. Аналогичным образом, уменьшение, составляющее 2 Log КОЕ/мл, соответствовало 99% уничтожения бактерий, а уменьшение, составляющее 3 Log КОЕ/мл, соответствовало 99,9% уничтожения бактерий.
Пример 1
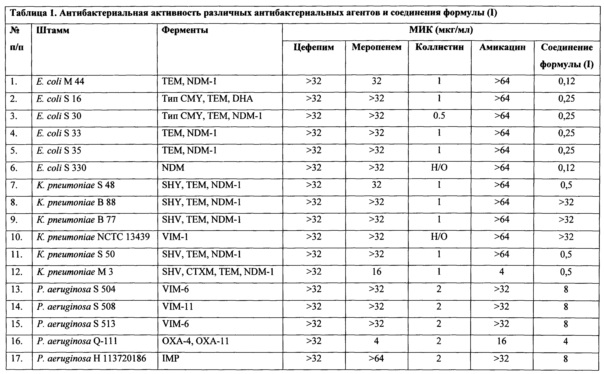
Результаты исследования антибактериальной активности цефепима, меропенема, колистина, амикацина и соединения формулы (I) в отношении высокорезистентных штаммов Е. coli, К. pneumonia и P. aeroginosa приведены в таблице 1. Как можно видеть, цефепим, меропенем и амикацин (МИК 16-64 мкг/мл) оказались неэффективными в отношении резистентных штаммов Е. coli, К. pneumonia и P. aeroginosa. Как можно видеть из представленных данных, выбранные для проведения исследований штаммы бактерий оказались высокорезистентными, и их подавление было возможно только посредством одного продаваемого лекарственного средства - колистина (МИК составила 0,5-2 мкг/мл). Однако было неожиданно обнаружено, что соединение формулы (I) проявляло значительную антибактериальную активность в отношении большинства штаммов Е. coli и К. pneumonia (МИК составила 0,1-0,5 мкг/мл). Соединение формулы (I) проявляло более высокую антибактериальную активность, чем колистин, в отношении большинства резистентных штаммов Е. coli и К. pneumonia. Также, по сравнению с цефепимом, меропонемом и амикацином, соединение формулы (I) проявляло повышенную антибактериальную активность в отношении резистентных штаммов P. aeroginosa.
Пример 2
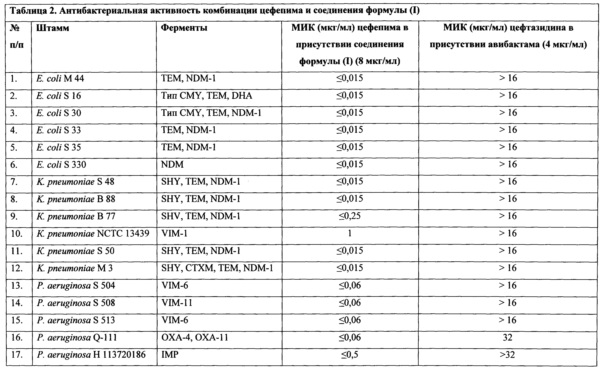
Результаты исследования антибактериальной активности комбинации цефепима и соединения формулы (I) в отношении резистентных штаммов Е. coli, К. pneumonia и Р. aeroginosa приведены в таблице 2. Как можно видеть из таблицы 2, значения МИК для цефепима были значительно снижены в присутствии соединения формулы (I) (8 мкг/мл). Значения МИК для цефепима снизились с 16-64 мкг/мл до примерно 0,015-1 мкг/мл в присутствии соединения формулы (I) (8 мкг/мл). Также определено значение МИК для цефтазидима в присутствии авибактама (4 мкг/мл), и, как можно видеть, значения МИК для цефтазидима были значительно выше (более 16 мкг/мл для большинства случаев). Меньшие значения МИК для комбинации цефепима и соединения формулы (I) продемонстрировали их высокую антибактериальную активность по сравнению с цефтазидимом и авибактамом.
Пример 3
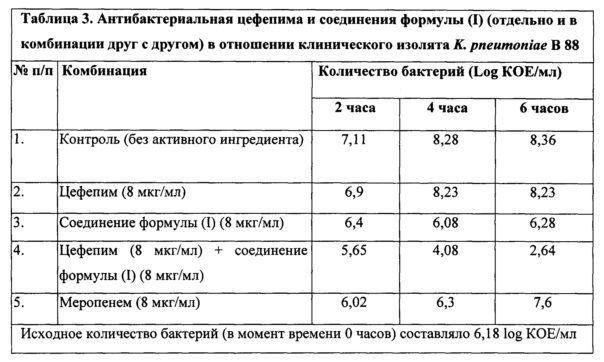
Результаты исследования антибактериальной активности цефепима и соединения формулы (I) (отдельно и в комбинации друг с другом) в отношении клинического изолята К. pneumonia В88, продуцирующего металло-бета-лактамазы [SHV, ТЕМ, NDM-1], приведены в таблице 3. Как можно видеть из таблицы 3, когда цефепим, меропенем и соединение формулы (I) использовали отдельно (в концентрации 8 мкг/мл), снижения количества бактерий не наблюдалось даже по истечении 6 часов. Однако комбинация цефепима и соединения формулы (I) (при концентрации каждого из них 8 мкг/мл) неожиданно позволила снизить количество бактерий с 6,18 до 2,64 Log КОЕ/мл по истечении 6 часов. Таким образом, комбинация цефепима и соединения формулы (I) проявила повышенную антибактериальную активность в отношении К. pneumonia В88.
Пример 4
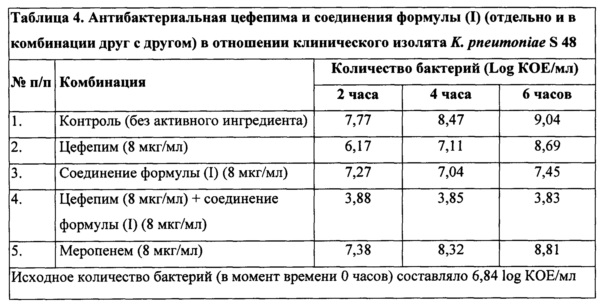
Результаты исследования антибактериальной активности цефепима и соединения формулы (I) (отдельно и в комбинации друг с другом) в отношении клинического изолята К. pneumonia S 48, продуцирующего металло-бета-лактамазы [SHV, ТЕМ, NDM-1], приведены в таблице 4. Как можно видеть из таблицы 4, когда цефепим, имипенем и соединение формулы (I) использовали отдельно (в концентрации 8 мкг/мл), по истечении 6 часов снижения количества бактерий не наблюдалось. Однако комбинация цефепима и соединения формулы (I) (при концентрации каждого из них 8 мкг/мл) неожиданно позволила снизить количество бактерий с 6,84 до 3,83 Log КОЕ/мл по истечении 6 часов. Таким образом, комбинация цефепима и соединения формулы (I) проявила повышенную антибактериальную активность в отношении К. pneumonia S 48.
Результаты, приведенные в таблицах 1-4 четко и неожиданно демонстрируют сильную антибактериальную активность комбинаций, содержащих цефепим и соединение формулы (I), в отношении высокорезистентных штаммов Е. coli, К. pneumonia и Р. aeroginosa. Таким образом, комбинация цефепима и соединения формулы (I) обладает колоссальным предпочтительным эффектом по подавлению высокорезистентных штаммов бактерий, демонстрируя заслуживающее внимание достижение в лечении инфекций, вызванных такими патогенами.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ 1,6-ДИАЗАБИЦИКЛО[3,2,1]ОКТАН-7-ОНА И ИХ ПРИМЕНЕНИЕ ПРИ ЛЕЧЕНИИ БАКТЕРИАЛЬНЫХ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ | 2012 |
|
RU2636147C1 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ АНТИБАКТЕРИАЛЬНЫЕ АГЕНТЫ | 2015 |
|
RU2705375C2 |
| ПРОИЗВОДНЫЕ 1,6-ДИАЗАБИЦИКЛО[3.2.1]ОКТАН-7-ОНА И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2013 |
|
RU2614418C2 |
| ПРОИЗВОДНЫЕ 1,6- ДИАЗАБИЦИКЛО [3,2,1] ОКТАН-7-ОНА И ИХ ПРИМЕНЕНИЕ ПРИ ЛЕЧЕНИИ БАКТЕРИАЛЬНЫХ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ | 2012 |
|
RU2578370C2 |
| АЗОТСОДЕРЖАЩИЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2012 |
|
RU2569307C1 |
| АНТИБАКТЕРИАЛЬНЫЕ КОМПОЗИЦИИ И СПОСОБЫ | 2017 |
|
RU2779346C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ СУЛБАКТАМ И ИНГИБИТОР БЕТА-ЛАКТАМАЗЫ | 2011 |
|
RU2560846C1 |
| ПРОИЗВОДНЫЕ 1,6-ДИАЗАБИЦИКЛО[3.2.1]ОКТАН-7-ОНА И ИХ ПРИМЕНЕНИЕ ПРИ ЛЕЧЕНИИ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2012 |
|
RU2570423C2 |
| АНТИБАКТЕРИАЛЬНЫЕ КОМПОЗИЦИИ | 2017 |
|
RU2813568C2 |
| КОМПОЗИЦИИ, ВКЛЮЧАЮЩИЕ АНТИБАКТЕРИАЛЬНОЕ СРЕДСТВО И ТАЗОБАКТАМ | 2011 |
|
RU2593363C2 |
Описаны фармацевтические композиции, содержащие цефепим или его фармацевтически приемлемое производное и соединение формулы (I)
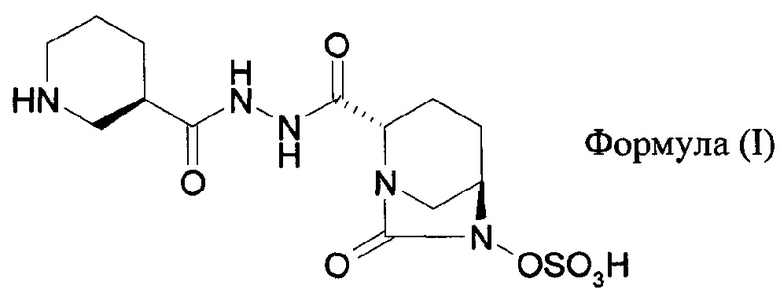
или его стереоизомер или его фармацевтически приемлемое производное. 4 н. и 4 з.п. ф-лы, 4 пр., 4 табл.
1. Фармацевтическая композиция для лечения бактериальной инфекции, содержащая: (a) цефепим или его фармацевтически приемлемую соль и (b) соединение формулы (I) или его фармацевтически приемлемую соль:
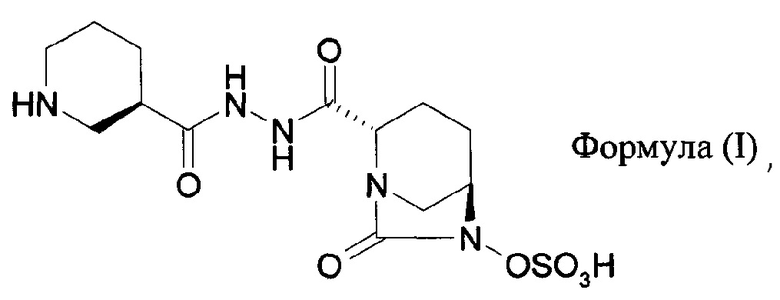
где указанная композиция отличается тем, что включает: (i) 2 г цефепима или его фармацевтически приемлемой соли и 1 г соединения формулы (I) или стереоизомера или его фармацевтически приемлемой соли, или (ii) 2 г цефепима или его фармацевтически приемлемой соли и 2 г соединения формулы (I) или стереоизомера или его фармацевтически приемлемой соли, или (iii) 2 г цефепима или его фармацевтически приемлемой соли и 0,5 г соединения формулы (I) или стереоизомера или его фармацевтически приемлемой соли.
2. Фармацевтическая композиция по п. 1, где соединение формулы (I) представляет собой транс-моно-[2-(N'-[(R)-пиперидин-3-карбонил]-гидразинокарбонил)-7-оксо-1,6-диазабицикло[3.2.1]окт-6-иловый] эфир серной кислоты, или (2S, 5R)- моно-[2-(N’-[(R)-пиперидин-3-карбонил]-гидразинокарбонил)-7-оксо-1,6-диазабицикло[3.2.1]окт-6-иловый] эфир серной кислоты, или (1R,2S,5R)-1,6-диазабицикло[3.2.1]октан-2-карбоновую кислоту, 7-оксо-6-(сульфоокси)-, 2-[2-[(3R)-3-пиперидинилкарбонил]гидразид], или натриевую или калиевую соль (1R,2S,5R)-1,6-диазабицикло[3.2.1]октан-2-карбоновой кислоты, 7-оксо-6-(сульфоокси)-, 2-[2-[(3R)-3-пиперидинилкарбонил]гидразида].
3. Фармацевтическая композиция по п. 1, где указанная композиция приготовлена в виде лекарственной формы, при этом соединение формулы (I) или его фармацевтически приемлемая соль и цефепим или его фармацевтически приемлемая соль присутствуют в композиции в виде смеси или в виде отдельных компонентов.
4. Фармацевтическая композиция по п. 1, где указанная композиция представлена в виде порошка или раствора.
5. Фармацевтическая композиция по п. 1, где указанная композиция представлена в виде порошка или раствора, который может быть восстановлен путем добавления совместимого восстанавливающего разбавителя для применения при парентеральном введении.
6. Способ лечения бактериальной инфекции у субъекта, включающий введение указанному субъекту эффективного количества фармацевтической композиции по п. 1.
7. Способ лечения бактериальной инфекции у субъекта, включающий введение указанному субъекту эффективного количества: (a) цефепима или его фармацевтически приемлемой соли и (b) соединения формулы (I) или его фармацевтически приемлемой соли:

где указанная композиция отличается тем, что включает: (i) 2 г цефепима или его фармацевтически приемлемой соли и 1 г соединения формулы (I) или стереоизомера или его фармацевтически приемлемой соли, или (ii) 2 г цефепима или его фармацевтически приемлемой соли и 2 г соединения формулы (I) или стереоизомера или его фармацевтически приемлемой соли, или (iii) 2 г цефепима или его фармацевтически приемлемой соли и 0,5 г соединения формулы (I) или стереоизомера или его фармацевтически приемлемой соли.
8. Способ повышения антибактериальной эффективности цефепима или его фармацевтически приемлемой соли у субъекта, включающий совместное введение цефепима или его фармацевтически приемлемой соли с соединением формулы (I)
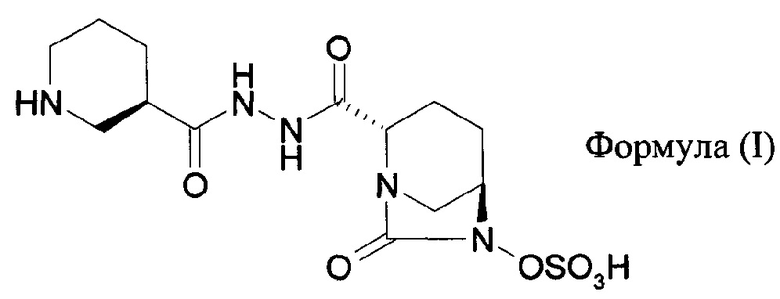
или его фармацевтически приемлемой солью,
где указанная композиция отличается тем, что включает: (i) 2 г цефепима или его фармацевтически приемлемой соли и 1 г соединения формулы (I) или стереоизомера или его фармацевтически приемлемой соли, или (ii) 2 г цефепима или его фармацевтически приемлемой соли и 2 г соединения формулы (I) или стереоизомера или его фармацевтически приемлемой соли, или (iii) 2 г цефепима или его фармацевтически приемлемой соли и 0,5 г соединения формулы (I) или стереоизомера или его фармацевтически приемлемой соли.
| WO 2013030733 A1, 07.03.2013 | |||
| US 2013225554 A1, 29.08.2013 | |||
| US 6465428 B1, 15.10.2002 | |||
| US 2009318378 A1, 24.12.2009 | |||
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ТЯЖЕЛЫХ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ И СМЕШАННЫХ ИНФЕКЦИЙ | 2008 |
|
RU2366450C1 |
Авторы
Даты
2019-10-08—Публикация
2014-10-22—Подача