Перекрестная ссылка на родственные заявки
[0001] Настоящая заявка заявляет приоритет предварительной заявки на патент США серийные №№ 62/098089, поданной 30 декабря 2014 года, 62/098097, поданной 30 декабря 2014 года, 62/255125 поданной 13 ноября 2015 года и 62/255131, поданной 13 ноября 2015 года, которые явным образом включены в настоящую заявку посредством ссылки.
Предпосылки и сущность изобретения
[0002] Фунгициды представляют собой соединения, природного или синтетического происхождения, которые действуют для защиты и/или лечения растений против повреждений, вызванных сельскохозяйственно-релевантными грибами. Как правило, нет ни одного фунгицида, полезного во всех ситуациях. Следовательно, продолжаются исследования для получения фунгицидов, которые могут иметь лучшие эксплуатационные характеристики, являются простыми в использовании и имеют меньшую стоимость.
[0003] Настоящее раскрытие относится к пиколинамидам и их использованию в качестве фунгицидов. Соединения по настоящему раскрытию могут предложить защиту от аскомицетов, базидиомицетов, дейтеромицетов и оомицетов.
[0004] Один вариант осуществления данного раскрытия может включать соединения формулы I:
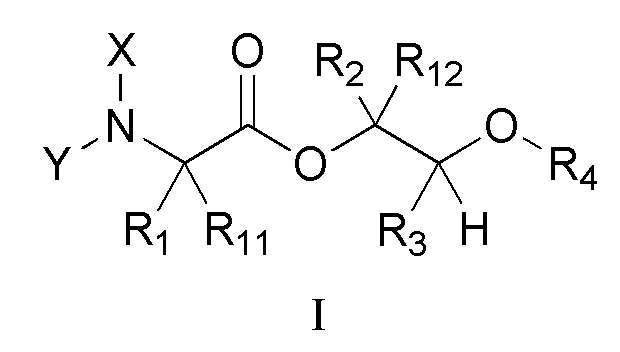
X представляет собой водород или C(О)R5;
Y представляет собой водород, C(О)R5 или
Q представляет собой
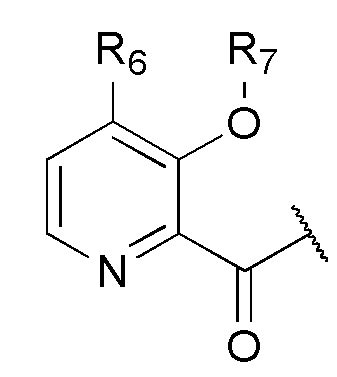 ;
;
R1 и R11 независимо выбраны из водорода или алкила, необязательно замещенного 0, 1 или несколькими заместителями R8;
альтернативно, R1 и R11 могут быть взяты вместе с образованием 3-6-членного насыщенного или частично насыщенного карбоциклического или гетероциклического кольца, необязательно замещенного 0, 1 или несколькими заместителями R8;
R2 и R12 независимо выбраны из водорода, алкила, арила или алкенила, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R8;
R3 представляет собой метил;
R4 выбран из алкила, арила или ацила, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R8;
R5 выбран из алкокси или бензилокси, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R8;
R6 выбран из водорода, алкокси или галогена, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R8;
R7 выбран из водорода, -C(О)R9 или -CH2OC(О)R9;
R8 выбран из водорода, алкила, арила, ацила, галогена, алкенила, алкокси или гетероциклила, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R10;
R9 выбран из алкила, алкокси или арила, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R8;
R10 выбран из водорода, алкила, арила, ацила, галогена, алкенила, алкокси или гетероциклила.
[0005] Другой вариант осуществления настоящего раскрытия может включать фунгицидную композицию для контроля или предотвращения поражения грибами, включающую описанные выше соединения и фитологически приемлемый материал-носитель.
[0006] Еще один вариант осуществления настоящего раскрытия может включать способ для контроля или предотвращения поражения грибами на растениях, при этом способ включает стадии нанесения фунгицидно эффективного количества одного или нескольких описанных выше соединений на по меньшей мере, один из грибов, растение и область, прилегающую к растению.
[0007] Специалистам в данной области техники будет понятно, что следующие термины могут включать общие "R"-группы в пределах их определений, например, "термин алкокси относится к -OR заместителю". Также понятно, что в определениях для следующих терминов, эти "R"-группы включены для иллюстрации и не должны истолковываться как ограничивающие или ограниченные заменами в формуле I.
[0008] Термин "алкил" относится к разветвленной, неразветвленной или насыщенной циклической углеродной цепи, включая, но не ограничиваясь этим, метил, этил, пропил, бутил, изопропил, изобутил, третичный бутил, пентил, гексил, циклопропил, циклобутил, циклопентил, циклогексил и подобные.
[0009] Термин "алкенил" относится к разветвленной, неразветвленной или циклической углеродной цепи, содержащей одну или несколько двойных связей, включая, но не ограничиваясь этим, этенил, пропенил, бутенил, изопропенил, изобутенил, циклобутенил, циклопентенил, циклогексенил и подобные.
[0010] Термин "алкинил" относится к разветвленной или неразветвленной углеродной цепи, содержащей одну или несколько тройных связей, включая, но не ограничиваясь этим, пропинил, бутинил и подобные.
[0011] Термины "арил" и "Ar" относятся к любому ароматическому кольцу, моно- или бициклическому, содержащему 0 гетероатомов.
[0012] Термин "гетероциклил" относится к любому ароматическому или неароматическому кольцу, моно- или бициклическому, содержащему один или несколько гетероатомов.
[0013] Термин "алкокси" относится к заместителю -OR.
[0014] Термин "ацилокси" относится к заместителю -OC(О)R.
[0015] Термин "циано" относится к заместителю -C≡N.
[0016] Термин "гидроксил" относится к заместителю -OH.
[0017] Термин "амино" относится к заместителю -N(R)2.
[0018] Термин "арилалкокси" относится к -О(CH2)nAr, где n представляет собой целое число, выбранное из 1, 2, 3, 4, 5 или 6.
[0019] Термин "галогеналкокси" относится к заместителю -OR-X, где X представляет собой Cl, F, Br или I или любую их комбинацию.
[0020] Термин "галогеналкил" относится к алкилу, который замещен при помощи Cl, F, I или Br или любой их комбинации.
[0021] Термин "галоген" или "гало" относится к одному или нескольким атомам галогена, определенным как F, Cl, Br и I.
[0022] Термин "нитро" относится к заместителю -NО2.
[0023] Термин тиоалкил относится к заместителю -SR.
[0024] На протяжении всего описания ссылки на соединения формулы I считаются, как включающие также все стереоизомеры, например, диастереомеры, энантиомеры и их смеси. В другом варианте осуществления, Формулу I следует рассматривать как включающую также их соли или гидраты. Иллюстративные соли включают, но не ограничиваются этим: гидрохлорид, гидробромид, гидройодид, трифторацетат и трифторметансульфонат.
[0025] Специалистам в данной области техники также будет понятно, что допускается дополнительное замещение, если не указано иное, при условии соблюдения правил химической связи и энергии деформации, и если продукт по-прежнему проявляет фунгицидную активность.
[0026] Другой вариант осуществления настоящего раскрытия представляет собой использование соединения формулы I, для защиты растения от атаки фитопатогенного организма или лечения растения, зараженного фитопатогенным организмом, включающее нанесение соединения формулы I или композиции, включающей соединение на почву, растение, часть растения, листья и/или корни.
[0027] Помимо этого, другой вариант осуществления настоящего раскрытия представляет собой композицию, полезную для защиты растения от атаки фитопатогенного организма и/или лечения растения, зараженного фитопатогенным организмом, включающую соединение формулы I и фитологически приемлемый материал-носитель.
Подробное описание изобретения
[0028] Соединения по настоящему раскрытию можно применять любым из множества известных способов, либо в виде соединений, либо в виде композиций, содержащих соединения. Например, соединения можно наносить на корни или листья растений для борьбы с различными грибами, не повреждая коммерческую ценность растений. Материалы могут применяться в форме любого из обычно используемых типов препаратов, например, в виде, растворов, дустов, смачивающихся порошков, жидких концентратов или эмульгируемых концентратов.
[0029] Предпочтительно, соединения по настоящему раскрытию применяют в виде состава, включающего одно или несколько соединений формулы I с фитологически приемлемым носителем. Концентрированные составы можно диспергировать в воде или других жидкостях, для нанесения, или составы могут быть могут быть пылевидными или гранулированными, которые затем можно применяться без дальнейшей обработки. Составы могут быть получены в соответствии с процедурами, которые являются обычными в области получения химикатов сельскохозяйственного назначения.
[0030] В настоящем описании рассматриваются все растворители, при помощи которых одно или несколько соединений могут быть сформулированы для доставки и использования в качестве фунгицида. Обычно, композиции применяют в виде водных суспензий или эмульсий. Такие суспензии или эмульсии можно получить из водорастворимых, водосуспендируемых или эмульгируемых композиций, которые представляют собой твердые вещества, обычно известные как смачивающиеся порошки; или жидкости, обычно известные как эмульгируемые концентраты, водные суспензии или суспензионные концентраты. Как легко понять, любой материал, к которому можно добавить эти соединения, может быть использован при условии, что он дает желаемую полезность без значительного вмешательства в активность этих соединений в качестве противогрибковых средств.
[0031] Смачивающиеся порошки, которые могут быть уплотнены с образованием воднодиспергируемых гранул, содержат однородную смесь одного или нескольких соединений формулы I, инертный носитель и поверхностно-активные вещества. Концентрация соединения в смачивающимся порошке может быть от около 10 процентов до около 90 процентов по массе от общей массы смачивающегося порошка, более предпочтительно около 25 массовых процентов до около 75 массовых процентов. При получении композиции смачивающегося порошка соединения можно смешать с любым тонкоизмельченным твердым веществом, таким как профиллит, тальк, мел, гипс, фуллерова глина, бентонит, аттапульгит, крахмал, казеин, глютен, монтмориллонитовые глины, диатомовые земли, очищенные силикаты или подобные. В таких операциях тонко измельченный носитель и поверхностно-активные вещества обычно смешивают с соединением (соединениями) и перемалывают.
[0032] Эмульгируемые концентраты соединений формулы I могут содержать удобную концентрацию, такую как от около 1 массового процента до около 50 массовых процентов соединения, в подходящей жидкости, в расчете на общую массу концентрата. Соединения можно растворить в инертном носителе, который является либо смешивающимся с водой растворителем, либо смесью несмешивающихся с водой органических растворителей и эмульгаторов. Концентраты могут быть разбавлены водой и маслом для образования смесей для опрыскивания в виде эмульсий масло-в-воде. Полезные органические растворители включают ароматические соединения, особенно высококипящие нафталиновые и олефиновые фракции нефти, такие как тяжелый лигроин, обогащенный ароматикой. Также могут быть использованы другие органические растворители, например, терпеновые растворители, включая производные канифоли, алифатические кетоны, такие как циклогексанон, и сложные спирты, такие как 2-этоксиэтанол.
[0033] Эмульгаторы, которые могут быть успешно использованы в настоящей заявке, могут быть легко определены специалистами в данной области и включают различные неионные, анионные, катионные и амфотерные эмульгаторы или смесь двух или более эмульгаторов. Примеры неионных эмульгаторов, полезных в получении эмульгируемых концентратов, включают полиалкиленгликолевые эфиры и продукты конденсации алкил- и арилфенолов, алифатических спиртов, алифатических аминов или жирных кислот с этиленоксидом, пропиленоксидами, такие как этоксилированные алкилфенолы и сложные эфиры карбоновых кислот, солюбилизированные с полиолом или полиоксиалкиленом. Катионные эмульгаторы включают четвертичные аммониевые соединения и соли жирных аминов. Анионные эмульгаторы включают растворимые в масле соли (например, кальция) алкиларилсульфоновых кислот, растворимые в масле соли или сульфатированные полигликолевые эфиры и подходящие соли фосфатированного полигликолевого эфира.
[0034] Типичные органические жидкости, которые можно использовать для получения эмульгируемых концентратов соединений по настоящему изобретению, представляют собой ароматические жидкости, такие как ксилол, пропилбензольные фракции; или смешанные нафталиновые фракции, минеральные масла, замещенные ароматические органические жидкости, такие как диоктилфталат; керосин; диалкиламиды различных жирных кислот, в частности диметиламиды жирных гликолей и производных гликоля, такие как н-бутиловый эфир, этиловый эфир или метиловый эфир диэтиленгликоля, метиловый эфир триэтиленгликоля, нефтяные фракции или углеводороды, такие как минеральное масло, ароматические растворители, парафиновые масла и тому подобные; растительные масла, такие как соевое масло, рапсовое масло, оливковое масло, касторовое масло, масло семян подсолнечника, кокосовое масло, кукурузное масло, хлопковое масло, льняное масло, пальмовое масло, арахисовое масло, сафлоровое масло, кунжутное масло, тунговое масло и тому подобные; эфиры вышеуказанных растительных масел; и подобные. Смеси двух или более органических жидкостей также можно использовать при получении эмульгируемого концентрата. Органические жидкости включают ксилольные и пропилбензольные фракции, при этом ксилол является наиболее предпочтительным в некоторых случаях. Поверхностно-активные диспергирующие агенты обычно используют в жидких композициях в количестве от 0,1 до 20 масс.% в расчете на общую массу диспергирующего агента с одним или несколькими соединениями. Композиции могут также содержать другие совместимые добавки, например регуляторы роста растений и другие биологически активные соединения, используемые в сельском хозяйстве.
[0035] Водные суспензии включают суспензии одного или нескольких нерастворимых в воде соединений формулы I, диспергированных в водном растворителе, в концентрации от примерно 1 до примерно 50 масс.% в расчете на общую массу водной суспензии. Суспензии получают путем тонкого измельчения одного или нескольких соединений и интенсивного смешивания исходного вещества с носителем, состоящим из воды и поверхностно-активных веществ, выбранных из тех же типов, которые обсуждались выше. Другие компоненты, такие как неорганические соли и синтетические или натуральные смолы, также могут быть добавлены для увеличения плотности и вязкости водного растворителя.
[0036] Соединения формулы I могут также применяться в виде гранулированных композиций, которые особенно полезны для нанесения на почву. Гранулированные композиции обычно содержат от примерно 0,5 до примерно 10 масс.%, в расчете на общую массу гранулированного состава, соединения (соединений), диспергированного в инертном носителе, который полностью или в значительной части состоит из грубо измельченного инертного материала, такого как аттапульгит, бентонит, диатомит, глина, или аналогичного недорогого вещества. Такие композиции обычно получают путем растворения соединения в подходящем растворителе и нанесения его на гранулированный носитель, который был получен с соответствующим размером частиц, в диапазоне от примерно 0,5 до примерно 3 мм. Подходящий растворитель представляет собой растворитель, в котором соединение растворимо в значительной степени или полностью. Такие композиции также можно получить путем приготовления густой массы или пасты носителя, соединения и растворителя, и измельчения и сушки с получением желаемой гранулированной частицы.
[0037] Дусты, содержащие соединения формулы I, могут быть получены путем тщательного смешивания одного или нескольких соединений в порошкообразной форме с подходящим порошковым сельскохозяйственным носителем, таким как, например, каолиновая глина, измельченная вулканическая порода и подобные. Дусты могут содержать от около 1 до около 10 масс.% соединений, в расчете на общую массу дуста.
[0038] Композиции могут дополнительно содержать адъювантные поверхностно-активные вещества для улучшения осаждения, смачивания и проникновения соединений на целевую культуру и организм. Эти адъювантные поверхностно-активные вещества необязательно можно использовать в качестве компонента композиции или в виде баковой смеси. Количество адъювантного поверхностно-активного вещества обычно будет варьироваться от 0,01 до 1,0 процента по объему, в расчете на распыляемый объем воды, предпочтительно от 0,05 до 0,5 об.%. Подходящие адъювантные поверхностно-активные вещества включают, но не ограничиваются этим, этоксилированные нонилфенолы, этоксилированные синтетические или натуральные спирты, соли сложных эфиров сульфоянтарных кислот, этоксилированные органосиликоны, этоксилированные жирные амины, смеси поверхностно-активных веществ с минеральными или растительными маслами, маслянистый концентрат, который снижает повреждение целевых культур (минеральное масло (85%)+эмульгаторы (15%)); этоксилат нонилфенола; четвертичную аммониевую соль бензилкокоалкилдиметила; смесь нефтяного углеводорода, алкиловых эфиров, органической кислоты и анионного поверхностно-активного вещества; C9-C11 алкилполигликозид; этоксилат фосфатированного спирта; этоксилат натурального первичного спирта (C12-C16); ди-втор-бутилфенол EO-PO блок-сополимер; полисилоксан с концевыми метильными группами; этоксилат нонилфенола+мочевино-аммониевый нитрат; эмульгированное метилированное растительное масло; этоксилат тридецилового спирта (синтетический) (8EO); этоксилат таллового амина (15 EO); PEG (400) диолеат-99. Композиции также могут включать эмульсии масло-в-воде, такие, которые описаны в заявке на патент США № 11/495228, раскрытие которой явно включено в настоящую заявку посредством ссылки.
[0039] Композиции необязательно могут включать комбинации, которые содержат другие пестицидные соединения. Такие дополнительные пестицидные соединения могут представлять собой фунгициды, инсектициды, гербициды, нематоциды, майтициды, артроподициды, бактерициды или их комбинации, которые совместимы с соединениями по настоящему изобретению в среде, выбранной для применения, и не являются антагонистичными по отношению к активности соединений по настоящему изобретению. Следовательно, в таких вариантах осуществления, другое пестицидное соединение используют в качестве дополнительного токсиканта для аналогичного или для другого применения в пестицидах. Соединения формулы I и пестицидное соединение в комбинации обычно могут присутствовать в массовом соотношении от 1:100 до 100:1.
[0040] Соединения по настоящему раскрытию также можно объединить с другими фунгицидами с образованием фунгицидных смесей и их синергических смесей. Фунгицидные соединения по настоящему раскрытию часто применяют в сочетании с одним или несколькими другими фунгицидами для борьбы с более широким спектром нежелательных заболеваний. При использовании в сочетании с другим(и) фунгицидом(фунгицидами), заявленные в настоящем изобретении соединения можно сформулировать с другим(и) фунгицидом(фунгицидами), смешать в баковую смесь с другим(и) фунгицидом(фунгицидами) или наносить последовательно с другим(и) фунгицидом (фунгицидами). Такие другие фунгициды могут включать 2-(тиоцианатометилтио)-бензотиазол, 2-фенилфенол, 8-гидроксихинолинсульфат, метоктрадин, амисульбром, антимицин, Ampelomyces quisqualis, азаконазол, азоксистробин, Bacillus subtilis, Bacillus subtilis штамм QST713, беналаксил, беномил, бентиаваликарб-изопропил, бензовиндифлупир, бензиламинобензол-сульфонатная (BABS) соль, бикарбонаты, бифенил, бисмертиазол, битертанол, биксафен, бластицидин-S, бура, смесь Бордо, боскалид, бромуконазол, бупиримат, полисульфид кальция, каптафол, каптан, карбендазим, карбоксин, карпропамид, карвон, Хлоазафенон, хлоронеб, хлороталонил, хлозолинат, Coniothyrium minitans, гидроксид меди, октаноат меди, оксихлорид меди, сульфат меди, сульфат меди (трехосновный), кумоксиксистробин, оксид меди, циазофамид, цифлуфенамид, цимоксанил, ципроконазол, ципродинил, дазомет, дебакарб, диаммоний этиленбис- (дитиокарбамат), дихлофлуанид, дихлорфен, диклоцимет, дикломезин, дихлоран, диэтофенкарб, дифеноконазол, дифензокват ион, дифлуметорим, диметоморф, димоксистробин, диниконазол, диниконазол-М, динобутон, динокап, дифениламин, дипиметитрон, дитианон, додеморф, додеморфацетат, додин, свободное основание додин, эдифенфос, энестробин, энестробурин, эноксастробин, эпоксиконазол, этабоксам, этиоксихин, этридиазол, фамоксадон, фенамидон, фенаминостробин, фенаримол, фенбуконазол, фенфурам, Фенхексимид, феноксанил, фенпиклонил, фенпропидин, фенпропиморф, фенпиразамин, фентин, фентин ацетат, фентин гидроксид, фербам, феримзон, флюазин, флудиоксонил, флуфеноксистробин, флуморф, флюопиколид, флюопирам, фтормид, флуоксастробин, флюквиназол, флюсилазол, флусульфамид, флутианил, флутоланил, флутриафол, флюсапироксад, фоллет, формальдегид, фосетил, фосетил-алюминий, фуберидазол, фуралаксил, фураметпир, гуазатин, гуазатин ацетат, GY-81, гексахлорбензол, гексаконазол, гимексазол, имазалил, имазалил сульфат, имибенконазол, иминоктадин, иминоктадинтриацетат, иминоктадин трис (альбезилат), иодокарб, ипконазол, ипфенпиразолон, ипробенфос, ипродион, ипроваликарб, изофетамид, изопротиолан, изопирамас, изоцианил, касугамицин, касугамицин гидрохлорид гидрат, крезоксим-метил, ламинарин, манкопер, манкозеб, мандестробин, мандипропамид, манеб, мефеноксам, мепапипирим, мепронил, мептилдинокап, хлористая ртуть, оксид ртути, хлорид ртути, металаксил, металаксил-М, метам, аммоний, метам-калий, метам-натрий, метконазол, метасульфокарб, метилйодид, метилизотиоцианат, метирам, метоминостробин, метрафенон, милдиомицин, миклобутанил, набам, нитротал-изопропил, нуаримол, октилинон, офурсал, олеиновая кислота (жирные кислоты), оризастробин, оксадиксил, оксатиапипролин, оксин-меди, оксоконазолфумарат, оксикарбоксин, пефуразоат, пенконазол, пенцикурон, пенфлуфен, пентахлорфенол, пентахлорфениллаурат, пентиопирад, фенилртуть ацетат, фосфоновая кислота, фталид, пикарбутразокс, пикоксистробин, полиоксин В, полиоксины, полиоксорим, бикарбонат калия, калий гидроксихинолинсульфат, пробеназол, прохлораз, процимидон, пропамокарб, пропамокарб гидрохлорид, пропиконазол, пропинеб, прокиназид, протиоконазол, пираклостробин, пираметростробин, пираоксистробин, пиразифлюмид, пиразофос, пирибенкарб, пирибутикарб, пирифенокс, пириметанил, пириофенон, пиризоксазол, пирокилон, хинокламин, хиноксифен, квинтозин, экстракт Reynoutria sachalinensis, седаксан, силтиофам, симеконазол, натрий 2-фенилфеноксид, бикарбонат натрия, пентахлорфеноксид натрия, спироксамин, сера, SYP-Z048, смолистые масла, тебуконазол, тебуфлоквин, текназен, тетраконазол, тиабендазол, тифлузамид, тиофанат-метил, тирам, тиадинил, толофос-метил, толкарб, толилфлуанид, триадимефон, триадименол, триазоксид, триклопирикарб, трициклазол, тридеморф, трифлоксиксистробин, трифлумизол, трифорин, тритиконазол, валидамицин, валифеналат, валифенал, винклозолин, зинеб, зирам, зоксамид, Candida oleophila, Fusarium оксиsporum, Gliocladium spp., Phlebiopsis gigantea, Streptomyces griseoviridis, Trichoderma spp., (RS)-N- (3,5-дихлорфенил)-2-(метоксиметил)сукцинимид, 1,2-дихлорпропан, 1,3-дихлор-1,1,3,3-тетрафторацетонгидрат, 1-хлор-2,4-динитронафталин, 1-хлор-2-нитропропан, 2-(2-гептадецил-2-имидазолин-1-ил) этанол, 2,3-дигидро-5-фенил-1,4-дитихин 1,1,4,4-тетраоксид, 2-метоксиэтилртутный ацетат, 2-метоксиэтилртутный хлорид, 2-метоксиэтилртутный силикат, 3-(4-хлорфенил)-5-метилраданин, 4-(2-нитропроп-1-енил) фенилтиоцианат, ампропилфос, анилазин, азитирам, полисульфид бария, Bayer 32394, бенноланил, бенхинокс, бентанурон, бензамакрил, бензамакрил-изобутил, бензаморф, бинапакрил, бис (метилртути) сульфат, бис (трибутилтин) оксид, бутиобат, кадмий кальций медь цинк хроматсульфат, карбаморф, CECA, хлобентиазон, хлораниформетан, хлорфеназол, хлорхинокс, климбазол, бис (3-фенилсалицилат)меди, медь цинк хромат, куфранеб, гидразиний сульфат меди, купробам, циклофурамид, ципендазол, ципрофурам, Декафентин, дихлон, дихлозолин, диклобутразол, диметиримол, динокон, динонсульфон, динотербон, дипиритион, диталимфос, додицин, дразоксолон, EBP, ESBP, этаконазол, этем, этирим, фенаминосульф, фенапанил, фениотпан, флюотримазол, фуркарбанил, фурконазол, фурконазол-цис, мехамекс, фурофанат, глиодин, гризеофульвин, галакринат, Hercules 3944, гексилтиофос, ICIA0858, Изопамфос, изоваледиол, мебенил, мекарбинзид, метазоклолон, метфлурок, метилртуть дициандиамид, метсульфовакс, милнеб, мукохлорный ангидрид, миклозолин, N-3,5-дихлорфенил-сукцинимид, N-3-нитрофенилитаконимид, натамицин, N-этилмеркурио-4-толуолсульфонанилид, никель-бис(диметилдитиокарбамат), OCH, фенилртуть диметилдитиокарбамат, нитрат фенилртути, фосдифен, протиокарб, протиокарб гидрохлорид, пиракарболид, пиридинитрил, пиоксихлор, пиоксифур, хинацетол, хинацетол сульфат, хиназамид, квинконазол, рабензазол, салициланилид, SSF-109, сультропен, текорам, тиадифтор, тициофен, тиохлорфенфим, тиофенат, тиохинокс, тиоксимид, триамифос, триаримол, триазбутил, трихломид, урбацид, зариламид и любые их комбинации.
[0041] Помимо этого, соединения, описанные в настоящей заявке можно объединить с другими пестицидами, включая инсектициды, нематоциды, майтициды, артроподициды, бактерициды или их комбинации, которые совместимы с соединениями по настоящему раскрытию, в среде, выбранной для применения и не антагонистической к активности соединений по настоящему изобретению, с образованием пестицидных смесей и их синергических смесей. Фунгицидные соединения по настоящему раскрытию можно применять в сочетании с одним или несколькими другими пестицидами для контроля более широкого круга нежелательных вредителей. При использовании в сочетании с другими пестицидами, заявленные в настоящем изобретении соединения можно сформулировать с другим(и) пестицидом(пестицидами), смешать в баковую смесь с другим(и) пестицидом(пестицидами) или наносить последовательно с другим(и) пестицидом(пестицидами). Типичные инсектициды включают, но не ограничиваются этим: 1,2-дихлорпропан, абамектин, ацефат, ацетамиприд, ацетион, ацетопрол, акринатрин, акрилонитрил, афидопиропен, аланикарб, альдикарб, альдоксикарб, альдрин, аллетрин, аллосамидин, аллилцикарб, альфа-циперметрин, альфа-экдизон, альфа-эндосульфан, амидитион, аминокарб, амитон, амитон оксалат, амитраз, анабасин, атидатион, азадирактин, азаметифос, азинфос-этил, азинфос-метил, азотоат, бария гексафторсиликат, бартрин, бендиокарб, бенфуракарб, бенсултап, бета-цифлутрин, бета-циперметрин, бифентрин, биоаллетрин, биоэтанометрин, биоперметрин, бистрифлурон, боракс, борная кислота, брофланилид, бромофенвинфос, бромоциклен, бром-ДДТ, бромофос, бромофос-этил, буфенкарб, бупрофензин, бутакарб, бутатиофос, бутокарбоксим, бутонат, бутоксикарбоксим, кадусафос, кальция арсенат, кальция полисульфид, камфехлор, карбанолат, карбарил, карбoфуран, дисульфид углерода, тетрахлорид углерода, карбoфенотион, карбoсульфан, картап, картап гидрохлорид, хлорантранилирол, хлорбициклен, хлордан, хлордекон, хлордимеформ, хлордимеформ гидрохлорид, хлорэтоксифос, хлорфенапир, хлорфенвинфос, хлорфлуазурон, хлормефос, хлороформ, хлоропикрин, хлорфоксим, хлоразофос, хлорпирифос, хлорпирифос-метил, хлортиофос, хромафенозид, цинерин I, цинерин II, цинерины, цисметрин, клацифос, клоэтокарб, клозантел, клотианидин, меди ацетоарсенит, меди арсенат, меди нафтенат, меди олеат, кумафос, кумитоат, кротамитон, кротоксифос, крумофат, криолит, цианофенфос, цианофос, циантоат, циантранилипрол, цикланилипрол, циклетрин, циклопротрин, цифлутрин, цигалотрин, циперметрин, цифенотрин, циромазин, цитиоат, ДДТ, декарбoфуран, дельтаметрин, демефион, демефион-O, демефион-S, деметон, деметон-метил, деметон-O, деметон-O-метил, деметон-S, деметон-S-метил, деметон-S-метилсульфон, диафентиурон, диалифос, диатомовая земля, диазинон, дикаптон, дихлофентион, дихлорвос, диклормезотиаз, дикрезил, дикротoфос, дицикланил, диелдрин, дифлубензурон, дилор, димефлутрин, димефокс, диметан, диметоат, диметрин, диметилвинфос, диметилан, динекс, динекс-диклексин, динопроп, диносам, динотефуран, диофенолан, диоксабензофос, диоксакарб, диоксатион, дисульфотон, дитикрофос, d-лимонен, DNOC, DNOC-аммоний, DNOC-калий, DNOC-натрий, дорамектин, экдистерон, эмамектин, эмамектин бензоат, EMPC, эмпентрин, эндосульфан, эндотион, эндрин, EPN, эпофенонан, эприномектин, эсдепаллетрин, эсфенвалерат, этафос, этиофенкарб, этион, этипрол, этоат-метил, этопрофос, этил формиат, этил-DDD, этилендибромид, этилендихлорид, этиленоксид, этофенпрокс, этримфос, EXD, фамфур, фенамифос, феназафлор, фенхлорфос, фенетакарб, фенфлутрин, фенитротион, фенoбукарб, феноксакрим, феноксикарб, фенпиритрин, фенпропaтрин, фенсульфотион, фентион, фентион-этил, фенвалерат, фипронил, флометохин, флоникамид, флубендиамид, флукофурон, флуциклоксурон, флуцитринат, флуфенерим, флуфеноксурон, флуфенпрокс, флуфипрол, флугексафон, флупирадифурон, флувалинат, фонофос, форметанат, форметанат гидрохлорид, формотион, формпаранат, формпаранат гидрохлорид, фосметилан, фоспират, фостиетан, фуратиокарб, фуретрин, гамма-цигалотрин, гамма-HCH, галфенпрокс, галогенфенозид, HCH, HEOD, гептахлор, гептафлутрин, гептенофос, гетерофос, гексафлумурон, HHDN, гидраметилнон, цианистый водород, гидропрен, гиквинкарб, имидаклоприд, имипротрин, индоксакарб, иодметан, IPSP, исазофос, изобензан, изокарбoфос, изодрин, изофенфос, изофенфос-метил, изопрокарб, изопротиолан, изотиоат, изоксатион, ивермектин, джасмолин I, джасмолин II, йодфенфос, ювенильный гормон I, ювенильный гормон II, ювенильный гормон III, каппа-бифентрин, каппа-тефлутрин, келеван, кинопрен, лямбда-цигалотрин, арсенат свинца, лепимектин, лептофос, линдан, лиримфос, луфенурон, лутидaтион, малатион, малонобен, мазидокс, meкарбам, мекарфон, меназон, мефосфолан, хлорид ртути, месулфенфос, метафлумизон, метакрифос, метамидофос, метидaтион, метиокарб, метокротoфос, метомил, метопрен, метоксихлор, метоксифенозид, метилбромид, метилизотиоцианат, метилхлороформ, метиленхлорид, метофлутрин, метолкарб, метоксадиазон, мевинфос, мексакарбат, милбемектин, милбемицин оксим, мипафокс, мирекс, молосултап, момфторотрин, монокротoфос, мономегипо, моносултап, морфотион, моксидектин, нафталофос, налед, нафталин, никотин, нифлуридид, нитенпирам, нитиазин, нитрилакарб, новалурон, новифлумурон, oметоат, оксамил, оксидеметон-метил, оксидепрофос, оксидисульфотон, пара-дихлорбензол, паратион, паратион-метил, пенфлурон, пентахлорфенол, перметрин, фенкаптон, фенотрин, фентоат, форат, фосалон, фосфолан, фосмет, фоснихлор, фосфамидон, фосфин, фоксим, фоксим-метил, пириметафос, пиримикарб, пиримифос-этил, пиримифос-метил, калия арсенит, калия тиоцианат, pp'-ДДТ, праллетрин, прекоцен I, прекоцен II, прекоцен III, примидофос, профенoфос, профлуралин, промацил, промекарб, пропaфос, пропeтамфос, пропоксур, протидaтион, протиофос, протоат, протрифенбут, пифлубумид, пираклофос, пирафлупрол, пиразофос, пиресметрин, пиретрин I, пиретрин II, пиретрины, пиридабен, пиридалил, пиридафентион, пирифлухиназон, пиримидифен, пириминостробин, пиримитат, пирипрол, пирипроксифен, кассия, хиналфос, хиналфос-метил, хинотион, рафоксанид, ресметрин, ротенон, риания, сабадилла, шрадан, селамектин, силафлуoфен, силикагель, натрия арсенит, натрия фторид, натрия гексафторсиликат, натрия тиоцианат, софамид, спинеторам, спиносад, спиромезифен, спиротетрамат, сулкофурон, сулкофурон-натрий, сулфлурамид, сульфотеп, сулфоксaфлор, сулфурилфторид, сулпрофос, тау-флувалинат, тазимкарб, TDE, тебуфенозид, тебуфенпирад, тебупиримфос, тефлубензурон, тефлутрин, темефос, TEPP, тераллетрин, тербуфос, тетрахлорэтан, тетрахлорвинфос, тетраметрин, тетраметилфлутрин, тетранилипрол, тета-циперметрин, тиаклоприд, тиаметоксам, тикрофос, тиокарбоксим, тиоциклам, тиоциклам оксалат, тиодикарб, тиофанокс, тиометон, тиосултап, тиосултап-динатрий, тиосултап-мононатрий, турингиенсин, тиоксазафен, толфенпирад, тралометрин, трансфлутрин, трансперметрин, триаратен, триазамат, триазофос, трихлорфон, трихлорметафос-3, трихлоронат, трифенoфос, трифлумезопирим, трифлумурон, триметакарб, трипрен, вамидотион, ваниллипрол, XMC, ксилилкарб, зета-циперметрин, золапрофос и любые их комбинации.
[0042] Кроме того, соединения, описанные в настоящей заявке, можно объединить с гербицидами, которые совместимы с соединениями по настоящему раскрытию в среде, выбранной для применения и не антагонистической к активности соединений по настоящему изобретению, с образованием пестицидных смесей и их синергических смесей. Фунгицидные соединения по настоящему раскрытию можно применять в сочетании с одним или несколькими гербицидами для контроля большого количества нежелательных растений. При использовании в сочетании с гербицидами, заявленные в настоящем изобретении соединения можно сформулировать с гербицидом(гербицидами), смешать в баковую смесь с гербицидом(гербицидами) или наносить последовательно с гербицидом(гербицидами). Типичные гербициды включают, но не ограничиваются этим: 4-CPA; 4-CPB; 4-CPP; 2,4-D; 3,4-DA; 2,4-DB; 3,4-DB; 2,4-DEB; 2,4-DEP; 3,4-DP; 2,3,6-TBA; 2,4,5-T; 2,4,5-TB; ацетохлор, ацифлуорфен, аклонифен, акролеин, алахлор, аллидохлор, аллоксидим, аллиловый спирт, алорак, аметридион, аметрин, амибузин, амикарбазон, амидосулфурон, аминоциклопирахлор, аминопиралид, амипрофос-метил, амитрол, аммония сулфамат, анилофос, анисурон, aсулам, атратон, атразин, азафенидин, азимсулфурон, азипротрин, барбан, BCPC, бефлубутамид, беназолин, бенкарбазон, бенфлуралин, бенфуресат, бенсулфурон, бенсулид, бентазон, бензaдокс, бензфендизон, бензипрам, бензобициклон, бензофенap, бензофлуор, бензоилпроп, бензтиазурон, бициклопирон, бифенокс, биланафос, биспирибак, боракс, бромацил, бромбонил, бромбутид, бромфеноксим, бромоксинил, бромпиразон, бутахлор, бутафенацил, бутамифос, бутенахлор, бутидазол, бутиурон, бутралин, бутооксидим, бутурон, бутилат, диметиларсиновая кислота, кафенстрол, кальция хлорат, кальция цианамид, камбендихлор, карбaсулам, карбетамид, карбоксазол, хлорпрокарб, карфентразон, CDEA, CEPC, клометоксифен, хлорамбен, хлоранокрил, хлоразифоп, хлоразин, хлорбромурон, хлорбуфам, хлоретурон, хлорфенac, хлорфенпроп, хлорфлуразол, хлорфлуренол, хлоридазон, хлоримурон, хлорнитрофен, хлоропон, хлорртолурон, хлороксурон, хлороксинил, хлорпрофам, хлорсулфурон, хлоротал, хлортиамид, цинидон-этил, цинметилин, циносулфурон, цисанилид, клетодим, клиодинат, клодинафоп, клофоп, кломазон, кломепроп, клопроп, клопроксидим, клопиралид, клорансулам, CMA, меди сульфат, CPMF, CPPC, кредазин, крезол, кумилурон, цианaтрин, цианазин, циклоат, циклопириморат, циклосулфамурон, циклоксидим, циклурон, цигалофоп, циперкват, ципразин, ципразол, ципромид, даимурон, далапон, дазомет, делахлор, десмедифам, десметрин, ди-аллат, дикамба, дихлобенил, дихлоралуреа, дихлормат, дихлорпроп, дихлорпроп-P, диклофоп, диклосулам, диетамкват, диетатил, дифенoпентен, дифеноксурон, дифензокват, дифлуфеникан, дифлуфензопир, димефурон, димепиперат, диметахлор, диметаметрин, диметенамид, диметенамид-P, димексано, димидазон, динитрамин, динофенат, динопроп, диносам, диносеб, динотерб, дифенамид, дипропeтрин, дикват, дисул, дитиопир, диурон, DMPA, DNOC, DSMA, EBEP, эглиназин, эндотал, эпроназ, EPTC, эрбон, эспрокарб, эталфлуралин, этаметсулфурон, этидимурон, этиолат, этофумесат, этоксифен, этоксисулфурон, этинофен, этнипромид, этобензанид, EXD, фенaсулам, фенoпроп, феноксапроп, феноксапроп-P, феноксасульфон, фенхинотрион, фентеракол, фентиапроп, фентразамид, фенурон, сульфат железа, флампроп, флампроп-M, флазасулфурон, флорaсулам, флуазифоп, флуазифоп-P, флуазолат, флукарбазон, флуцетосулфурон, флухлоралин, флуфенацет, флуфеникан, флуфенпир, флуметсулам, флумезин, флумиклорак, флумиоксазин, флумипропин, флуометурон, фтордифен, фторгликофен, фтормидин, фторнитрофен, флуoтиурон, флуpоксам, флупропацил, флупропанат, флупирсулфурон, флуридон, флурoхлоридон, флуроксипир, флуртамон, флутиацет, фомесафен, форамсулфурон, фосамин, фурилоксифен, глуфосинат, глуфосинат-P, глифосат, галауксифен, галосафен, галосулфурон, галоксидин, галоксифоп, галоксифоп-P, гексахлорацетон, гексафлурат, гексазинон, имазаметабенз, имазамox, имазапик, имазапир, имазахин, имазетапир, имазосулфурон, инданофан, индазифлам, иодбонил, иодметан, иодсулфурон, иофенсулфурон, иоксинил, ипазин, ипфенкарбазон, ипримидам, изокарбамид, изоцил, изометиозин, изонорурон, изополинат, изопропалин, изопротурон, изоурон, изоксабен, изоксахлортол, изоксафлутол, изоксапирифоп, карбутилат, кетоспирадокс, лактофен, ленацил, линурон, MAA, MAMA, MCPA, MCPA-тиоэтил, MCPB, мекопроп, мекопроп-P, мединотерб, мефенацет, мефлуидид, мезопразин, мезосулфурон, мезотнон, метам, метамифоп, метамитрон, метазахлор, метазосулфурон, метфлуразон, метабензтиазурон, металпропалин, метазол, метиобенкарб, метиозолин, метиурон, метометон, метопротрин, метилбромид, метилизотиоцианат, метилдимрон, метобензурон, метобромурон, метолахлор, метосулам, метоксурон, метрибузин, метсулфурон, молинат, моланид, монизоурон, монохлоруксусная кислота, монолинурон, монурон, морфамкват, MSMA, напроанилид, напропамид, напропамид-M, напталам, небурон, никосулфурон, нипираклофен, нитралин, нитрофен, нитрофлуорфен, норфлуразон, норурон, OCH, орбенкарб, орто-дихлорбензол, ортосулфамурон, оризалин, оксадиаргил, оксадиазон, оксапиразон, оксасулфурон, оксазикломефон, оксифлуорфен, парафлурон, паракват, пебулат, пеларгоновая кислота, пендиметалин, пенокссулам, пентахлорфенол, пентанoхлор, пентоксазон, перфлуидон, петоксамид, фенизофам, фенмедифам, фенмедифам-этил, фенобензурон, ацетат фенилтрути, пиклорам, пиколинaфен, пиноксаден, пиперофос, калия арсенит, калия азид, калия цианат, претилахлор, примисулфурон, проциазин, продиамин, профлуазол, профлуралин, профоксидим, проглиназин, прометон, прометрин, пропaхлор, пропанил, пропaхизафоп, пропазин, профам, пропизохлор, пропоксикарбазон, пропирисулфурон, пропизамид, просулфалин, просульфокарб, просулфурон, проксан, принахлор, пиданон, пираклонил, пирафлуфен, пирасульфотол, пиразолинат, пиразосулфурон, пиразоксифен, пирибензоксим, пирибутикарб, пириклор, пиридафол, пиридат, пирифталид, пириминобак, пиримисульфан, пиритиобак, пироксасульфон, пироксулам, хинклорак, хинмерак, хинокламин, хинонамид, хизалофоп, хизалофоп-P, родетанил, римсулфурон, сафлуфенацил, S-метолахлор, себутилазин, секбуметон, сетоксидим, сидурон, симазин, симетон, симетрин, SMA, натрия арсенит, натрия азид, натрия хлорат, сулкотрион, сулфаллат, сулфентразон, сульфометурон, сульфосульфурон, серная кислота, сулгликапин, свеп, TCA, тебутам, тебутиурон, тефурилтрион, темботрион, тепралоксидим, тербацил, тербукарб, тербухлор, тербуметон, тербутилазин, тербутрин, тетрафлурон, тенилхлор, тиазафлурон, тиазопир, тидиазимин, тидиазурон, тиенкарбазон-метил, тифенсулфурон, тиобенкарб, тиафенацил, тиокарбазил, тиоклопим, толпиралат, топрамезон, тралкоксидим, триaфамон, три-аллат, триaсулфурон, триазифлам, трибенурон, трикамба, триклопир, тридифан, триэтазин, трифлоксисулфурон, трифлудимоксазин, трифлуралин, трифлусулфурон, трифоп, трифопсим, тригидрокситриазин, триметурон, трипропиндаn, тритак, тритосулфурон, вернолат и ксилахлор.
[0043] Другой вариант осуществления настоящего раскрытия представляет способ для контроля или предотвращения поражения грибами. Этот способ включает нанесение на почву, растение, корни, листву или очаг гриба или на очаг, в котором необходимо предотвратить заражение (например, на зерновые или виноградные растения), фунгицидно эффективного количества одного или нескольких соединений формулы I. Соединения являются подходящими для лечения различных растений на фунгицидных уровнях, при этом они проявляют низкую фитотоксичность. Соединения могут быть полезны в качестве средства для защиты и/или уничтожения вредных организмов.
[0044] Было обнаружено, что соединения обладают значительным фунгицидным эффектом, особенно для сельскохозяйственного использования. Многие соединения особенно эффективны для использования с сельскохозяйственными культурами и садоводческими растениями.
[0045] Специалистам в данной области техники будет понятно, что эффективность соединений в отношении вышеперечисленных грибов доказывает общую полезность соединений в качестве фунгицидов.
[0046] Соединения имеют широкий диапазон активности против грибковых патогенов. Иллюстративные патогены могут включать, но не ограничиваются этим, патогены, вызывающее пятнистость листьев пшеницы (Zymoseptoria tritici), бурую ржавчину пшеницы (Puccinia triticina), желтую ржавчину пшеницы (Puccinia striiformis), паршу яблок (Venturia inaequalis), мучнистую росу виноградной лозы (Uncinula necator), ринхоспориоз ячменя (Rhynchosporium secalis), пирикуляриоз риса (Pyricularia oryzae), ржавчину сои (Phakopsora pachyrhizi), септориоз колоса пшеницы (Leptosphaeria nodorum), мучнистую росу пшеницы (Blumeria graminis f. sp.tritici), мучнистую росу ячменя (Blumeria graminis f. sp. hordei), мучнистую росу тыквенных культур (Erysiphe cichoracearum), антракноз тыквенных культур (Colletotrichum lagenarium), пятнистость листьев свеклы (Cercospora beticola), альтернариоз томатов (Alternaria solani) и гельминтоспориоз корней ячменя (Cochliobolus sativus). Точное количество активного вещества, необходимое для нанесения, зависит не только от конкретного применяемого активного вещества, но также от конкретного требуемого действия, вида грибка, который нужно контролировать, и стадии его роста, а также от части растения или другого продукта, который должен контактировать с соединением. Таким образом, все соединения и композиции, содержащие эти соединения, могут быть не одинаково эффективными при сходных концентрациях или против одних и тех же видов грибов.
[0047] Соединения эффективны при использовании для растений в ингибирующем заболевание и фитологически приемлемом количестве. Термин "ингибирующее заболевание и фитологически приемлемое количество" относится к количеству соединения, которое уничтожает или ингибирует заболевание растения, для которого требуется контроль, но не является значительно токсичным для растения. Это количество в основном будет в пределах от около 0,1 до около 1000 ч./млн (частей на миллион), предпочтительно от 1 до 500 ч./млн. Точная концентрация требуемого соединения зависит от контролируемого грибкового заболевания, типа применяемой композиции, способа нанесения, конкретных видов растений, климатических условий и тому подобного. Подходящая норма нанесения обычно находится в диапазоне от примерно 0,10 до примерно 4 фунтов/акр (от 0,01 до 0,45 г на квадратный метр, г/м2).
[0048] Любой диапазон или желаемое значение, приведенное в настоящей заявке, могут быть расширены или изменены без потери искомых эффектов, что очевидно для квалифицированного специалиста для понимания идей, изложенных в настоящей заявке.
[0049] Соединения формулы I могут быть получены с использованием известных химических процедур. Промежуточные вещества, не указанные конкретным образом в настоящем описании, являются либо коммерчески доступными, либо могут быть получены путями, раскрытыми в химической литературе, или могут быть легко синтезированы из коммерческих исходных материалов с использованием стандартных процедур.
Общие схемы
[0050] Следующие схемы иллюстрируют подходы к созданию пиколинамидных соединений формулы I. Следующие описания и примеры приведены для иллюстративных целей и не должны рассматриваться как ограничивающие, что касается заместителей или картин замещения.
[0051] Соединения формулы 1.2, где R8 является таким, как первоначально определено, можно получить способом, представленным на Схеме 1, стадия a. Соединение формулы 1.1 можно обработать основанием, таким как N-циклогексил-N-метилциклогексанамин, в присутствии ацетата трифенилвисмута(V) и ацетата меди(II) в растворителе, таком как толуол, при температуре от около 23°C до 40°C, с получением соединений формулы 1.2, где R8 такой, как определен ранее, как показано на стадии a. Альтернативно, соединения формулы 1.2, где R8 является таким, как первоначально определено, можно получить способом, представленным на Схеме 1, стадия b. Соединение формулы 1.1 можно обработать триарилвисмутовым(III) реагентом (получен в соответствии со способом, представленным в Synthetic Commun. 1996, 26 (24), 4569-4575), таким как трис(4-фтор-2-метилфенил)висмутан, в присутствии окислителя, такого как перуксуная кислота, и катализатора, такого как ацетат меди(II), в растворителе, таком как дихлорметан, при температуре от около 23°C до 40°C с получением соединений формулы 1.2, где R8 такой, как определен ранее, как показано на стадии b. Соединения формулы 1.3, где R8 является таким, как первоначально определено, можно получить способом, представленным на Схеме 1, стадия c. Соединение формулы 1.1 можно обработать при помощи катализатора, такого как трис(дибензилиденацетон)дипалладий(0) (Pd2(dba)3), и лиганда, такого как дифенилфосфиноферроцен (dppf), в присутствии аллилкарбоната, такого как (E)-трет-бутил (4,4,4-трифторбут-2-ен-1-ил)карбонат, в растворителе, таком как THF, при температуре от около 23°C до 80°C, с получением соединений формулы 1.3, где R8 такой, как определен ранее, как показано на стадии c. Соединения формулы 1.4, где R8 является таким, как первоначально определено, можно получить способом, представленным на Схеме 1, стадия d. Соединение формулы 1.1 можно обработать (бромметил)бензолом в присутствии оксида серебра(I) и йодида калия в растворителе, таком как дихлорметан (DCM), при температуре от около 23°C до температуры кипения с обратным холодильником, с получением соединений формулы 1.4, как показано на стадии d.
Схема 1
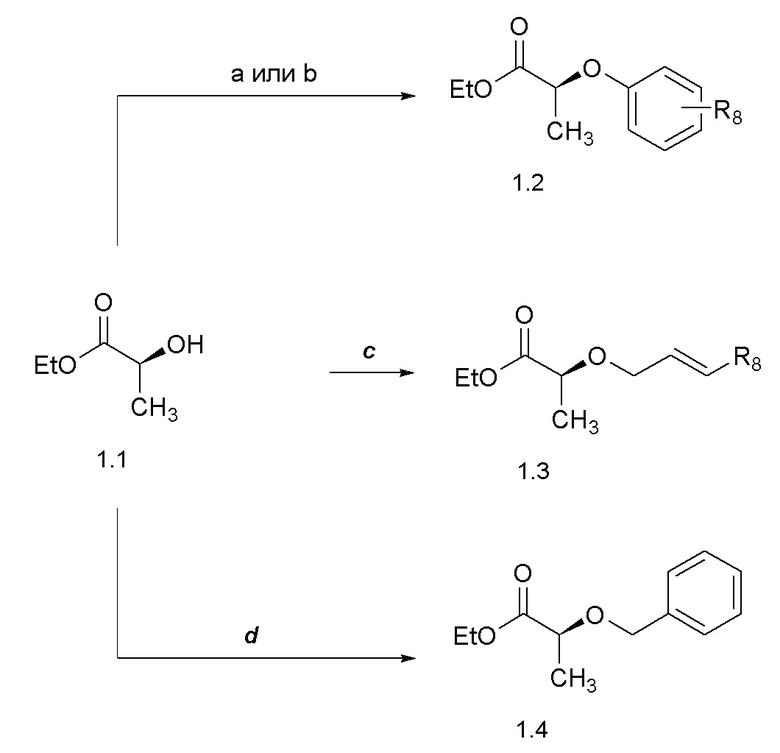
[0052] Соединения формулы 2.2 можно получить способом, представленным на Схеме 2, стадия a. Соединение формулы 2.1 можно обработать 4-метоксибензил 2,2,2-трихлорацетимидатом в присутствии камфорсульфоновой кислоты (CSA) в растворителе, таком как DCM, при температуре от около 23°C, с получением соединений формулы 2.2, как показано на стадии a. Соединение формулы 2.3, можно получить способом, представленным на Схеме 2, стадия b. Соединение формулы 2.3 можно обработать триизопропилсилилхлоридом в присутствии основания, такого как имидазол, в растворителе, таком как дихлорметан (DCM), при температуре от около 0°C, с получением соединений формулы 2.3, как показано на стадии b.
Схема 2
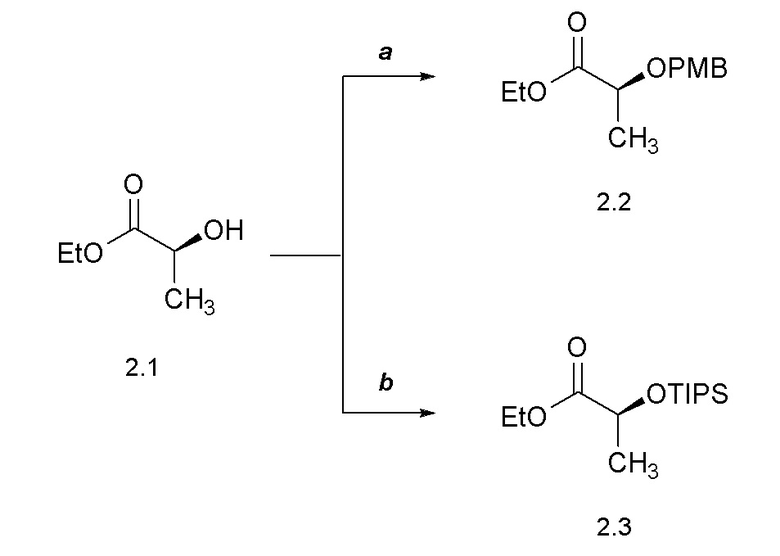
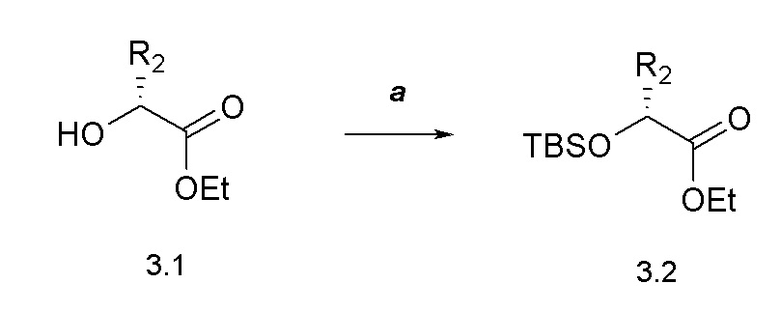
[0053] Соединение формулы 3.2, где R2 определен ранее, можно получить способом, представленным на Схеме 3, стадия a. Соединение формулы 3.1 можно обработать трет-бутилдиметилсилилхлоридом, в присутствии основания, такого как имидазол, в растворителе, таком как диметилформамид (DMF), при температуре от около 23°C, с получением соединений формулы 3.2, где R2 такой, как определен ранее, как показано на стадии a.
Схема 3
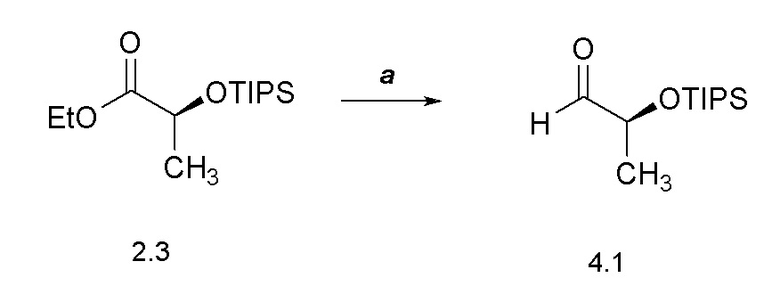
[0054] Соединения формулы 4.1 можно получить способом, представленным на Схеме 4, стадия a. Соединение формулы 2.3 можно обработать восстановителем, таким как диизобутилалюмогидрид (DIBAL), в растворителе, таком как DCM, при температуре от около -78°C, с получением соединений формулы 4.1, как показано на стадии a.
Схема 4
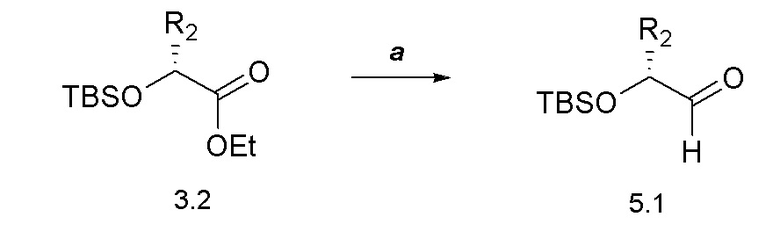
[0055] Соединения формулы 5.1, где R2 такой, как определен ранее, можно получить способом, представленным на Схеме 5, стадия a. Соединение формулы 3.2 можно обработать восстановителем, таким как диизобутилалюмогидрид (DIBAL), в растворителе, таком как DCM, при температуре от около -78°C, с получением соединений формулы 5.1, где R2 такой, как определен ранее, как показано на стадии a.
Схема 5
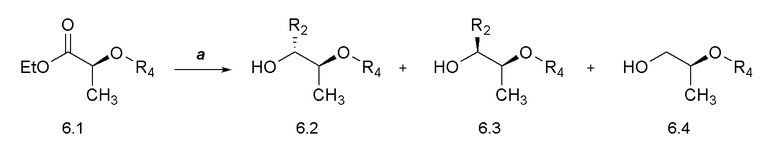
[0056] Соединения формулы 6.2, где R2 и R4 такие, как определены ранее, можно получить способом, представленным на Схеме 4, стадия a. Соединение формулы 6.1, где R4 такой, как определен ранее, можно обработать металлическим нуклеофилом, таким как R2-MgBr, и восстановителем, таким как литийборгидрид, в растворителе, таком как THF, при температуре от около 0°C до температуры окружающей среды, с получением соединений формулы 6.2, где R2 и R4 такие, как определены ранее, как показано на стадии a.
Схема 6
[0057] Соединения формулы 7.1, где R2 и R3 такие, как определены ранее, можно получить способом, представленным на Схеме 7, стадия a. Соединение формулы 4.1, где R3 такой, как определен ранее, можно обработать металлическим нуклеофилом, таким как R2-MgBr, в растворителе, таком как диэтиловый эфир, при температуре от около -78°C до температуры окружающей среды с получением соединений формулы 7.1, где R2 и R3 такие, как определены ранее, как показано на стадии a.
Схема 7
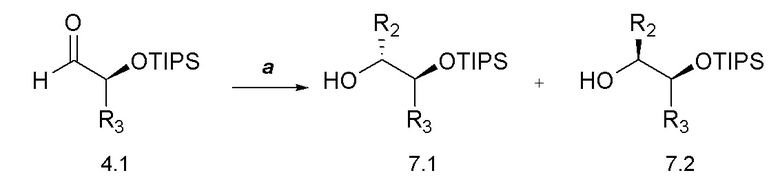
[0058] Соединения формулы 8.1, где R2 и R3 такие, как определены ранее, можно получить способом, представленным на Схеме 5, стадия a. Соединение формулы 5.1, где R2 такой, как определен ранее, можно обработать металлическим нуклеофилом, таким как R3-MgBr, в растворителе, таком как диэтиловый эфир, при температуре от около -78°C до температуры окружающей среды, с получением соединений формулы 8.1, где R2 и R3 такие, как определены ранее, как показано на стадии a.
Схема 8
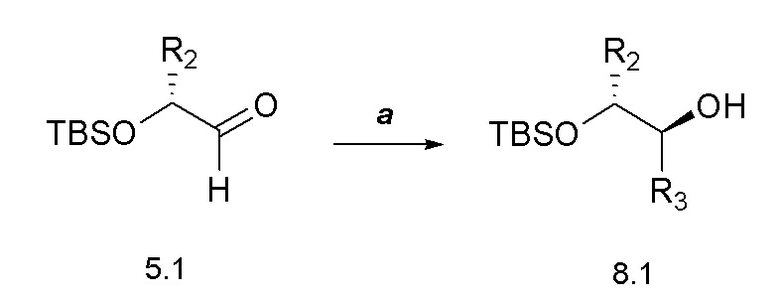
[0059] Соединения формулы 9.3, где R2 такой, как определен ранее, можно получить способом, представленным на Схеме 9, стадии a-b. Соединение формулы 9.1 можно обработать основанием, таким как гидрид натрия, и (бромметил)бензолом в растворителе, таком как DMF, при температуре от около 0°C до температуры окружающей среды, с получением соединений формулы 9.2, как показано на стадии a. Соединение формулы 9.2, где R2 такой, как определен ранее, можно обработать церий-аммоний нитратом в растворителе, таком как ацетонитрил, при температуре от около 0°C, с получением соединений формулы 9.3, где R2 такой, как определен ранее, как показано на стадии b.
Схема 9
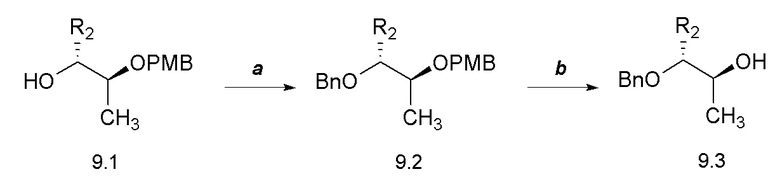
[0060] Соединения формулы 10.4, где R8 такой, как определен ранее, можно получить способом, представленным на Схеме 10, стадии a-c. Соединение формулы 10.1 можно обработать основанием, таким как гидрид натрия, и 4-метоксибензилбромидом в растворителе, таком как DMF, при температуре от около 0°C до температуры окружающей среды, с получением соединений формулы 10.2, как показано на стадии a. Соединение формулы 10.2, можно обработать тетрабутиламмонийфторидом в растворителе, таком как THF, при температуре от около 0°C до температуры окружающей среды, с получением соединений формулы 10.3, как показано на стадии b. Соединение формулы 10.3 можно обработать при помощи основания, такого как N-циклогексил-N-метилциклогексанамин, в присутствии ацетата трифенилвисмута(V) и ацетата меди(II) в растворителе, таком как толуол, при температуре от около 23°C до 40°C, с получением соединений формулы 10.4, где R8 такой, как определен ранее, как показано на стадии c.
Схема 10
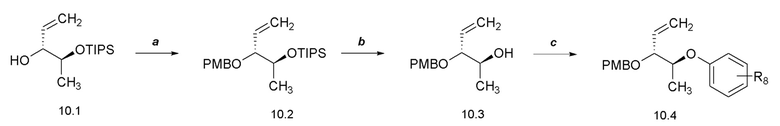
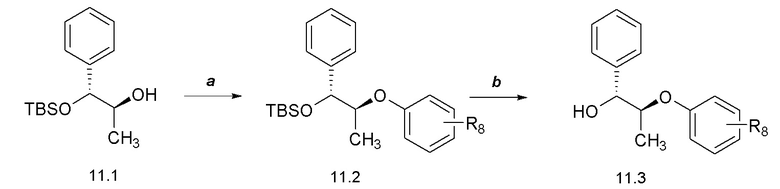
[0061] Соединения формулы 11.3, где R8 такой, как определен ранее, можно получить способом, представленным на Схеме 11, стадии a-b. Соединение формулы 11.1 можно обработать при помощи основания, такого как трет-бутоксид калия, в присутствии 1,2,4-трифторбензола в растворителе, таком как DMF, при температуре от около 23°C до 60°C, с получением соединений формулы 11.2, где R8 такой, как определен ранее, как показано на стадии a. Соединение формулы 11.2 можно обработать тетрабутиламмонийфторидом в растворителе, таком как THF, при температуре от около 0°C до температуры окружающей среды, с получением соединений формулы 11.3, где R8 такой, как определен ранее, как показано на стадии b.
Схема 11
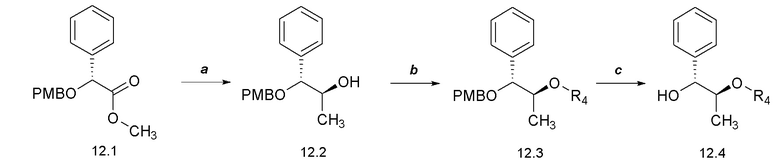
[0062] Соединения формулы 12.4, где R4 такой, как определен ранее, можно получить способом, представленным на Схеме 12, стадии a-c. Соединение формулы 12.1 можно обработать при помощи основания, такого как литийборгидрид, и метилирующего реагента, такого как метиллитий, в растворителе, таком как диэтиловый эфир, при температуре от около -78°C до температуры окружающей среды, с получением соединений формулы 12.2, как показано на стадии a. Соединение формулы 12.2 можно обработать при помощи основания, такого как гидрид натрия, катализатора, такого как тетрабутиламмониййодид (TBAI), и алкилбромида, такого как R4-Br, где R4 такой, как определен ранее, в растворителе, таком как THF, при температуре от около 23°C до температуры кипения с обратным холодильником, с получением соединений формулы 12.3, как показано на стадии b. Соединение формулы 12.3 можно обработать при помощи окислителя, такого как 2,3-дихлор-5,6-дициано-1,4-бензохинон (DDQ), в растворителе, таком как DCM, при температуре от около 0°C до температуры окружающей среды, с получением соединений формулы 12.4, как показано на стадии c.
Схема 12
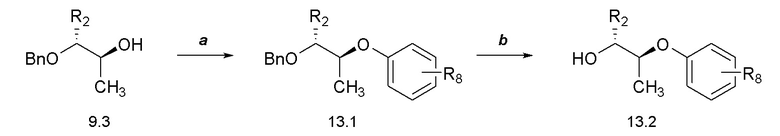
[0063] Соединения формулы 13.2, где R8 такой, как определен ранее, можно получить способом, представленным на Схеме 13, стадии a-b. Соединение формулы 9.3, где R2 такой, как определен ранее, можно обработать при помощи основания, такого как трет-бутоксид калия, в присутствии 1,2,4-трифторбензола в растворителе, таком как DMF, при температуре от около 23°C до 60°C, с получением соединений формулы 13.1, где R2 и R8 такие, как определены ранее, как показано на стадии a. Соединение формулы 13.1, где R2 и R8 такие, как определены ранее, можно обработать катализатором гидрирования, таким как палладий на углероде, в смеси растворителей, такой как 1:2 циклогексен:этанол, при температуре от приблизительно комнатной температуры до около 70°C, с получением соединений формулы 13.2, где R2 и R8 такие, как определены ранее, как показано на стадии b.
Схема 13
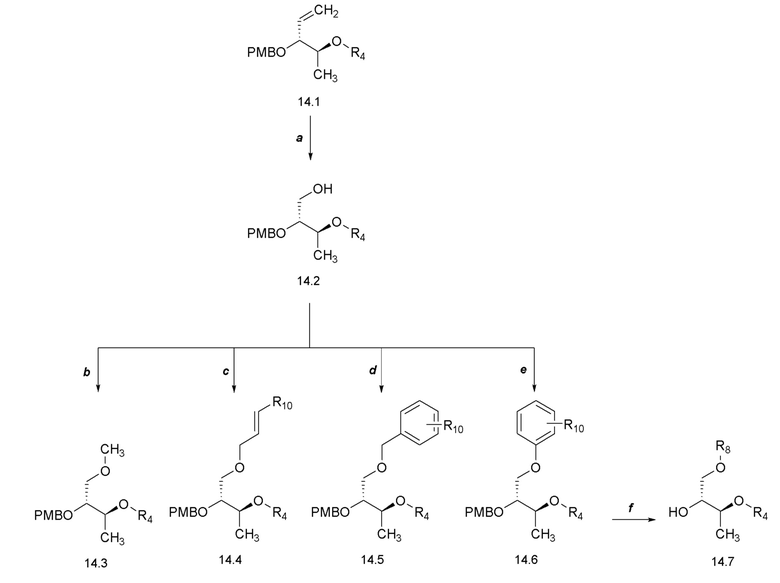
[0064] Соединения формулы 14.7. где R4 и R8 такие, как определены ранее, можно получить способом, представленным на Схеме 14, стадии a-f. Соединение формулы 14.1, где R4 такой, как определен ранее, можно обработать при помощи окислителя, такого как газообразный озон, в присутствии основания, такого как бикарбонат натрия, затем гидридом, таким как гидрид натрия, в смеси растворителей приблизительно от 1:32 метанол:дихлорметан до 1:3 метанол:дихлорметан, при температуре от около -78°C до температуры окружающей среды, с получением соединений формулы 14.2, где R4 такой, как определен ранее, как показано на стадии a. Соединение формулы 14.2, где R4 такой, как определен ранее, можно обработать метилирующим агентом, таким как триметилоксонийтетрафторборат, и акцептором протонов, таким как N1,N1,N8,N8-тетраметилнафталин-1,8-диамин, в растворителе, таком как дихлорметан, при температуре от около 23°C, с получением соединений формулы 14.3, где R4 такой, как определен ранее, как показано на стадии b. Альтернативно, соединение формулы 14.2, где R4 такой, как определен ранее, можно обработать аллильным реагентом, такие как аллилбромид, в присутствии основания, такого как гидрид натрия, и катализатора, такого как тетрабутиламмониййодид, в растворителе, таком как диметилформамид, при температуре от около 0°C до температуры окружающей среды, с получением соединений формулы 14.4, где R4 и R10 такие, как определены ранее, как показано на стадии c. Альтернативно, соединение формулы 14.2, где R4 такой, как определен ранее, можно обработать алкилирующим реагентом, таким как бензилбромид, в присутствии основания, такого как гидрид натрия, и катализатора, такого как тетрабутиламмоний йодид, в растворителе, таком как диметилформамид, при температуре от около 0°C до температуры окружающей среды, с получением соединений формулы 14.5, где R4 и R10 такие, как определены ранее, как показано на стадии d. Альтернативно, соединение формулы 14.2 можно обработать при помощи основания, такого как N-циклогексил-N-метилциклогексанамин, в присутствии ацетата трифенилвисмута(V) и ацетата меди(II) в растворителе, таком как толуол, при температуре от около 23°C до 40°C с получением соединений формулы 14.6, где R4 и R10 такие, как определены ранее, как показано на стадии e. Соединения формулы 14.3, 14.4, 14.5 и 14.6, где R4 и R10 такие, как определены ранее, можно обработать при помощи окислителя, такого как 2,3-дихлор-5,6-дициано-1,4-бензохинон (DDQ), в растворителе, таком как DCM, при температуре от около 0°C до температуры окружающей среды, с получением соединений формулы 14.7, где R4 и R8 такие, как определены ранее, как показано на стадии f.
Схема 14
[0065] Соединения формулы 15.3, где R4 такой, как определен ранее, можно получить способом, представленным на Схеме 15, стадии a-c. Соединение формулы 14.1, где R4 такой, как определен ранее, можно обработать при помощи окислителя, такого как газообразный озон, в присутствии основания, такого как бикарбонат натрия, после этого восстановителем, таким диметилсульфид, в смеси растворителей, такой как 1:10 метанол:дихлорметан, при температуре около -78°C, с получением соединений формулы 15.1, где R4 такой, как определен ранее, как показано на стадии a. Соединение формулы 15.1, где R4 такой, как определен ранее, можно обработать фторирующим агентом, таким как Deoxofluor®, в присутствии катализатора, такого как метанол, в растворителе, таком как дихлорметан, при температуре от около 0°C до температуры окружающей среды, с получением соединений формулы 15.2, где R4 такой, как определен ранее, как показано на стадии b. Соединение формулы 15.2, где R4 такой, как определен ранее, можно обработать при помощи окислителя, такого как 2,3-дихлор-5,6-дициано-1,4-бензохинон (DDQ), в растворителе, таком как DCM, при температуре от около 0°C до температуры окружающей среды, с получением соединений формулы 15.3, где R4 такой, как определен ранее, как показано на стадии c.
Схема 15
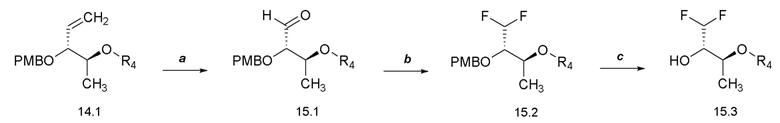
[0066] Соединения формулы 16.2, где R2 и R4 такие, как определены ранее, можно получить способом, представленным на Схеме 16, стадия a. Соединение формулы 16.1, где R2 и R4 такие, как определены ранее, можно обработать (трет-бутоксикарбонил)-1-аланином в присутствии реагента, используемого для образования пептидной связи, такого как 1-этил-3-(3-диметиламинопропил)карбодиимид (EDCI), и катализатора, такого как диметиламинопиридин (DMAP), в растворителе, таком как DCM, при температуре от около 0°C до температуры окружающей среды, с получением соединений формулы 16.2, где R2 и R4 такие, как определены ранее, как показано на стадии a.
Схема 16
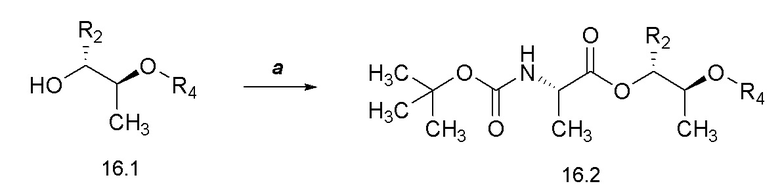
[0067] Соединения формулы 17.2, где R2 и R8 такие, как определены ранее, можно получить способом, представленным на Схеме 17, стадия a. Соединение формулы 17.1, где R2 и R8 такие, как определены ранее, можно обработать катализатором гидрирования, таким как палладий на углероде, в атмосфере водорода в растворителе, таком как этилацетат, при температуре около комнатной температуры с получением соединений формулы 17.2, где R2 и R8 такие, как определены ранее, как показано на стадии a.
Схема 17
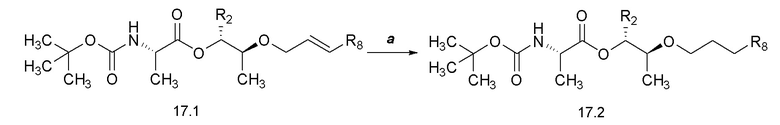
[0068] Соединения формулы 18.2, где R2 и R4 такие, как определены ранее, можно получить способом, представленным на Схеме 18, стадия a. Соединение формулы 18.1, где R2 и R4 такие, как определены ранее, можно обработать кислотой, такой как 4M раствор HCl в диоксане или трифторуксусной кислоте (TFA), в растворителе, таком как DCM, при температуре около комнатной, с получением соединений формулы 18.2, где R2 и R4 такие, как определены ранее, как показано на стадии a.
Схема 18
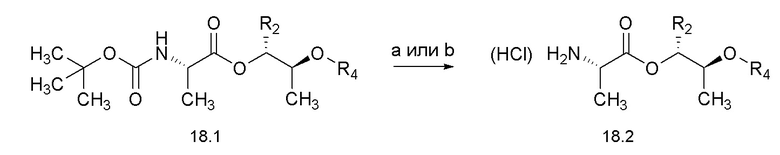
[0069] Соединения формулы 19.2, где R2, R4 и R6 такие, как определены ранее, можно получить способом, представленным на Схеме 19, стадия a. Соединение формулы 18.2, где R2 и R4 такие, как определены ранее, можно обработать при помощи соединения формулы 19.1, где R6 такой, как определен ранее, в присутствии основания, такого как диизопропилэтиламин (DIPEA), и реагента, используемого для образования пептидной связи, такого как гексафторфосфат бензотриазол-1-ил-окситрипирролидинофосфония (PyBOP), в галогенированном растворителе, таком как DCM, при температуре около комнатной, с получением соединений формулы 19.2, где R2, R4 и R6 такие, как определены ранее, как показано на стадии a.
Схема 19
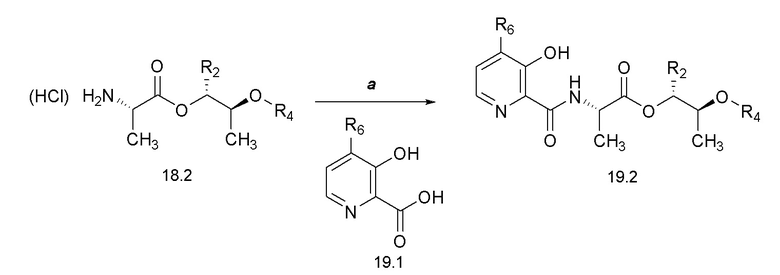
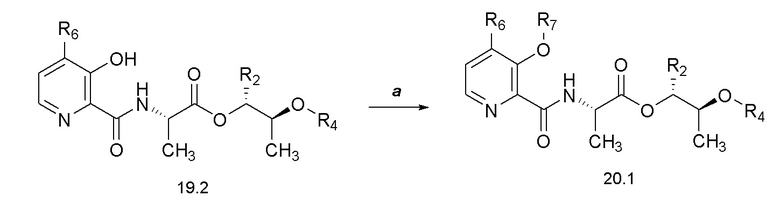
[0070] Соединения формулы 20.1, где R2, R4, R6 и R7 такие, как определены ранее, можно получить способом, представленным на Схеме 20, стадия a. Соединение формулы 19.2, где R2, R4 и R6 такие, как определены ранее, можно обработать подходящим алкилгалогенидом с или без реагента, такого как йодид натрия (NaI), и щелочного карбонатного основания, такого как карбонат натрия (Na2CО3) или карбонат калия (K2CO3), в растворителе, таком как ацетон, при температуре около 50°C, или путем обработки ацилгалогенидом в присутствии аминового основания, такого как пиридин, триэтиламин (Et3N), DMAP или их смесь, в апротонном растворителе, таком как DCM, при температуре от около 23°C, с получением соединений формулы 20.1, где R2, R4, R6 и R7 такие, как определены ранее, как показано на стадии a.
Схема 20
ПРИМЕРЫ
[0071] Химия в следующих примерах может быть осуществлена с использованием либо энантиомера 2-((трет-бутоксикарбонил)амино)пропановой кислоты (Boc-Ala-OH) либо защищенного (PMB или Bn) энантиомера этиллактата.
[0072] Пример 1A: Получение этил (S)-2-феноксипропаноата.
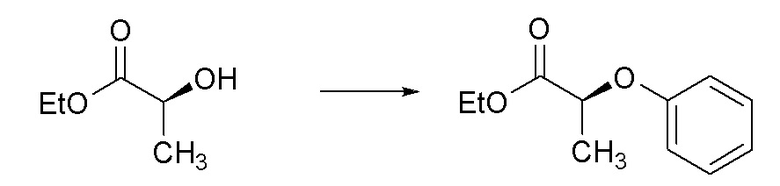
[0073] В круглодонную колбу объемом 250 мл загружали ацетат трифенилвисмута (V) (9,22 г, 16,51 ммоль) и ацетат меди(II) (0,231 г, 1,270 ммоль) и продували при помощи газообразного N2. Затем добавляли безводный толуол (85 мл), после этого (S)-этил 2-гидроксипропаноат (1,456 мл, 12,70 ммоль) и N-циклогексил-N-метилциклогексанамин (3,13 мл, 14,60 ммоль). Полученную сине-зеленую реакционную смесь затем нагревали до 40°C и перемешивали в течение 96 часов (час). Реакционную смесь охлаждали до комнатной температуры (кт) и фильтровали через слой Celite®. Фильтровальную лепешку промывали при помощи DCM и затем концентрировали с получением темно-желтого масла. Масло очищали при помощи колоночной флэш-хроматографии (силикагель (SiО2), 0→ 10% этилацетата в гексане) с получением указанного в заголовке соединения (2,43 г, 98%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 7,31-7,23 (м, 2H), 6,96 (тт, J=7,3, 1,1 Гц, 1H), 6,92-6,83 (м, 2H), 4,74 (кв., J=6,8 Гц, 1H), 4,21 (кв., J=7,1 Гц, 2H), 1,61 (д, J=6,8 Гц, 3H), 1,24 (т, J=7,1 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 172,24, 157,64, 129,51, 121,55, 115,16, 72,66, 61,23, 18,57, 14,12; ИК (тонкая пленка) 2986, 1753, 1733, 1494, 1239, 1134, 752 см-1.
[0074] Пример 1B: Получение (S)-этил 2-((триизопропилсилил)окси)пропаноата.
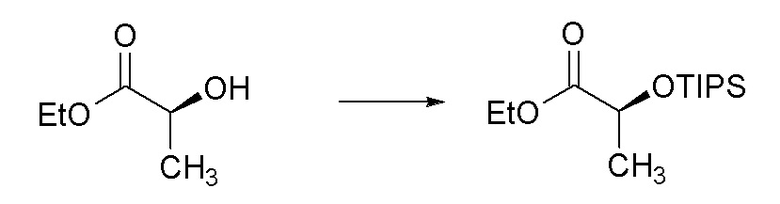
[0075] В круглодонной колбе объемом 500 мл, (S)-этил 2-гидроксипропаноат (9,71 мл, 85 ммоль) и имидазол (13,83 г, 203 ммоль) растворяли в DCM (220 мл) в атмосфере N2 и охлаждали до 0°C в бане лед/вода. Затем добавляли хлортриизопропилсилан (21,74 мл, 102 ммоль) при помощи шприца в течение 30 минут (мин). Реакционной смеси давали нагреться до комнатной температуры и перемешивали в течение ночи. Через 18 часов ТСХ указывала на расход исходного вещества. Реакционную смесь выливали в делительную воронку и промывали H2О (100 мл), насыщенным водным раствором NaHCО3 (100 мл), насыщенным солевым раствором (100 мл), 1M раствором HCl (100 мл) и затем в конце насыщенным солевым раствором (100 мл). Органический слой пропускали через фазовый сепаратор и концентрировали с получением чистого бесцветного масла. Масло очищали при помощи колоночной флэш-хроматографии (силикагель (SiО2), 0→10% этилацетата в гексане) с получением указанного в заголовке соединения (21,68 г, 93%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 4,41 (кв., J=6,7 Гц, 1H), 4,18 (кв.д, J=7,1, 2,7 Гц, 2H), 1,43 (д, J=6,7 Гц, 3H), 1,28 (т, J=7,1 Гц, 3H), 1,17-0,97 (м, 21H); 13C ЯМР (101 МГц, CDCl3) δ 174,23, 68,55, 60,66, 21,80, 17,85, 14,22, 12,16.
[0076] Пример 1C: Получение этил (S,E)-2-((4,4,4-трифторбут-2-ен-1-ил)окси)пропаноата.
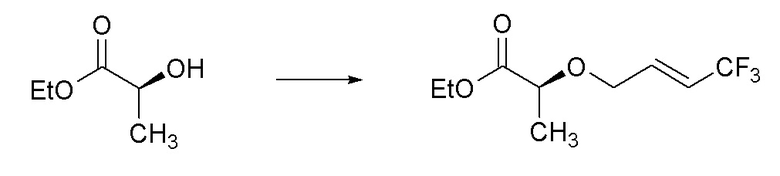
[0077] Этил (S)-2-гидроксипропаноат (0,971 мл, 8,47 ммоль) растворяли в безводном THF (42,3 мл). Добавляли Pd2(dba)3 (0,194 г, 0,212 ммоль) и dppf (0,235 г, 0,423 ммоль) и смесь нагревали до температуры кипения с обратным холодильником. Затем добавляли (E)-трет-бутил (4,4,4-трифторбут-2-ен-1-ил)карбонат (2,87 г, 12,70 ммоль) и реакцию контролировали до полного завершения при помощи ТСХ. Реакционную смесь охлаждали до комнатной температуры и тщательно концентрировали с получением масла. Масло очищали при помощи колоночной флэш-хроматографии (силикагель (SiО2), 0→10% MTBE в гексане) с получением указанного в заголовке соединения (1,59 г, 79%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 6,47-6,37 (м, 1H), 6,03-5,91 (м, 1H), 4,34-4,16 (м, 3H), 4,11-3,97 (м, 2H), 1,45 (д, J=6,8 Гц, 3H), 1,29 (т, J=7,1 Гц, 3H); 13C ЯМР (126 МГц, CDCl3) δ 172,67, 135,95 (кв., J=6,4 Гц), 123,01 (кв., J=269,2 Гц), 118,98 (кв., J=34,1 Гц), 75,01, 67,71, 61,08, 18,53, 14,20; ИК (тонкая пленка) 2988, 1742, 1686, 1302, 1264, 1202, 1112, 1087, 1018, 959 см-1.
[0078] Пример 1D: Получение метил этил (S)-2-((4-метоксибензил)окси)пропаноата.
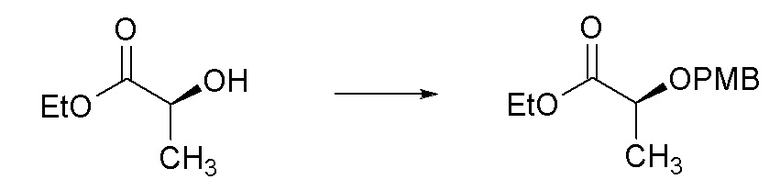
[0079] В круглодонной колбе объемом 500 мл получали раствор (S)-этил 2-гидроксипропаноата (10,15 мл, 89 ммоль) в DCM (89 мл). К этому раствору добавляли 4-метоксибензил 2,2,2-трихлорацетимидат (28,9 г, 102 ммоль), после этого камфорсульфоновую кислоту (2,065 г, 8,89 ммоль) и полученную оранжевую/коричневую реакционную смесь перемешивали при комнатной температуре в течение 72 часов. Добавляли гексан (100 мл) и реакционную смесь перемешивали в течение 30 минут. Осажденные твердые вещества фильтровали и фильтрат концентрировали с получением масла. Масло снова разбавляли смесью 200 мл DCM/Гексан (1:1). Смесь перемешивали при комнатной температуре в течение 30 минут. Твердые вещества фильтровали и фильтрат промывали насыщенным водным раствором NaHСО3 (100 мл), после этого насыщенным солевым раствором (100 мл). Органический слой сушили над Na2SO4, фильтровали и концентрировали с получением коричневого масла. Масло очищали при помощи колоночной флэш-хроматографии (силикагель (SiО2), 0→10% этилацетата в гексане) с получением указанного в заголовке соединения (11,96 г, 56%) в виде бледно-желтого масла: 1H ЯМР (400 МГц, CDCl3) δ 7,34-7,24 (м, 2H), 6,91-6,84 (м, 2H), 4,62 (д, J=11,3 Гц, 1H), 4,39 (д, J=11,2 Гц, 1H), 4,21 (кв.д, J=7,1, 2,4 Гц, 2H), 4,03 (кв., J=6,8 Гц, 1H), 3,80 (с, 3H), 1,41 (д, J=6,9 Гц, 3H), 1,29 (т, J=7,1 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 173,41, 159,37, 129,68, 113,83, 73,74, 71,66, 60,84, 55,31, 18,76, 14,28; ИК (тонкая пленка) 2984, 1730, 1513, 1247, 1198, 1031, 822 см-1.
[0080] Пример 1E: Получение этил (S)-2-(бензилокси)пропаноата.
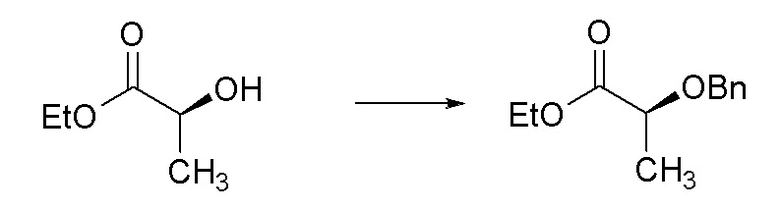
[0081] В круглодонной колбе объемом 500 мл получали раствор (S)-этил 2-гидроксипропаноата (11,65 мл, 102 ммоль) в безводном DCM (203 мл). К этому раствору добавляли (бромметил)бензол (18,12 мл, 152 ммоль), затем оксид серебра(I) (24,72 г, 107 ммоль) и йодид калия (1,686 г, 10,16 ммоль). Полученную черную реакционную смесь нагревали до температуры кипения с обратным холодильником и перемешивали в течение ночи. Через 24 часа ТСХ показала почти полный расход исходного вещества. Реакционную смесь фильтровали через слой Celite®, промывали при помощи DCM и концентрировали до масла. Масло очищали при помощи колоночной флэш-хроматографии (силикагель (SiО2), 0→5% этилацетата в гексане) с получением указанного в заголовке соединения (11,93 г, 56%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 7,48-7,14 (м, 5H), 4,69 (д, J=11,6 Гц, 1H), 4,45 (д, J=11,6 Гц, 1H), 4,21 (кв.д, J=7,1, 2,6 Гц, 2H), 4,05 (кв., J=6,9 Гц, 1H), 1,43 (д, J=6,9 Гц, 3H), 1,29 (т, J=7,1 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 173,27, 137,63, 128,43, 127,98, 127,84, 74,09, 72,00, 60,85, 18,74, 14,27; ИК (тонкая пленка) 2984, 1743, 1454, 1196, 1140, 1064, 1024, 736, 697 см-1.
[0082] Пример 1F, Стадия 1: Получение трис(4-фтор-2-метилфенил)висмутана.
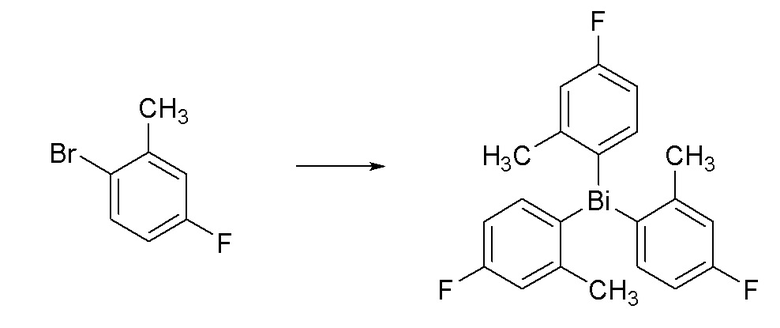
[0083] В круглодонной колбе объемом 250 мл получали раствор 1-бром-4-фтор-2-метилбензола (5,24 мл, 42,3 ммоль) в THF (171 мл) и охлаждали до -78°C в бане сухой лед/ацетон. Через ~10 минут добавляли по каплям при помощи шприца бутиллитий (2,5 M в гексане, 17,8 мл, 44,4 ммоль) и полученную чистую бесцветную реакционную смесь перемешивали в течение 1 часа. Через 1 час добавляли трихлорвисмутан (4,30 г, 13,63 ммоль) в виде раствора в THF (71 мл) при помощи шприца и реакционную смесь перемешивали при -78°C в течение 1 часа и затем нагревали до комнатной температуры и перемешивали в течение ночи. Через 18 часов реакционную смесь концентрировали и оставшийся остаток экстрагировали толуолом (200 мл) и желтовато-белое твердое вещество удаляли путем фильтрации. Фильтрат затем концентрировали досуха с получением указанного в заголовке соединения (7,25 г, 99%) в виде не совсем белого твердого вещества, которое использовали непосредственно на следующей стадии без дополнительной очистки: 1H ЯМР (400 МГц, CDCl3) δ 7,40 (дд, J=8,2, 6,7 Гц, 3H), 7,04 (дд, J=10,3, 2,7 Гц, 3H), 6,78 (тд, J=8,6, 2,7 Гц, 3H), 2,41 (с, 9H); 19F ЯМР (376 МГц, CDCl3) δ -113,91.
[0084] Пример 1F, Стадия 2: Получение этил (S)-2-(4-фтор-2-метилфенокси)пропаноата.
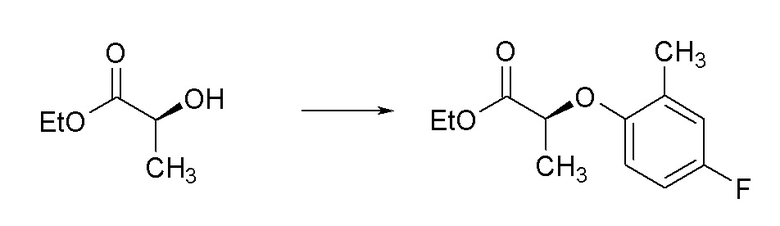
[0085] Раствор трис(4-фтор-2-метилфенил)висмутана (3,41 г, 6,35 ммоль) получали в DCM (21,16 мл) при комнатной температуре и затем медленно при помощи шприца добавляли перуксуную кислоту (1,225 мл, 7,20 ммоль) в течение 5 минут. Наблюдали образование пузырьков, и реакционная смесь становилась светло-оранжевого цвета. Полученной реакционной смесь давали смешаться при комнатной температуре в течение 30 минут. Через 30 минут добавляли этил (S)-2-гидроксипропаноат (0,485 мл, 4,23 ммоль) и ацетат меди(II) (0,154 г, 0,847 ммоль), колбу снабжали обратным холодильником и непрозрачную синюю/зеленую реакционную смесь нагревали до 45°C и перемешивали в течение ночи. Через 20 часов ТСХ показывала ~75% расход исходного вещества и преобразование в несколько более высоких Rf пятен. Реакционную смесь охлаждали до комнатной температуры и затем фильтровали через слой целита, фильтровали при помощи DCM (2×10 мл) и затем концентрировали с получением масла. Масло очищали при помощи колоночной флэш-хроматографии (силикагель (SiО2), 0→20% этилацетата в гексане) с получением указанного в заголовке соединения (318,8 мг, 33%) в виде бледно-желтого масла: 1H ЯМР (400 МГц, CDCl3) δ 6,85 (дд, J=9,0, 3,1 Гц, 1H), 6,76 (тд, J=8,5, 3,1 Гц, 1H), 6,63 (дд, J=8,9, 4,6 Гц, 1H), 4,66 (кв., J=6,8 Гц, 1H), 4,20 (кв.д, J=7,1, 1,4 Гц, 2H), 2,26 (с, 3H), 1,61 (д, J=6,8 Гц, 3H), 1,24 (т, J=7,1 Гц, 3H); 19F ЯМР (376 МГц, CDCl3) δ -123,28; 13C ЯМР (101 МГц, CDCl3) δ 172,18, 157,40 (д, J=239,0 Гц), 152,11 (д, J=2,3 Гц), 129,75 (д, J=7,7 Гц), 117,58 (д, J=22,8 Гц), 113,42 (д, J=8,5 Гц), 112,37 (д, J=22,8 Гц), 73,81, 61,19, 18,64, 16,40 (д, J=1,3 Гц), 14,12; ИК (тонкая пленка) 3350, 2987, 1750, 1496, 1191, 1134, 718 см-1; HRMS-ESI (m/z) рассчитано для [C12H16FO3]+, 227,1078; обнаружено, 227,1089.
[0086] Пример 2: Получение (S)-2-((триизопропилсилил)окси)пропаналя.
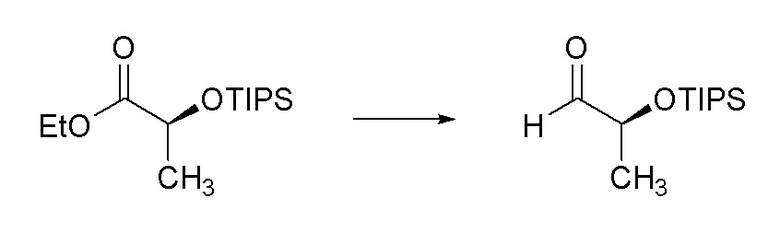
[0087] В круглодонной колбе объемом 1 л, (S)-этил 2-((триизопропилсилил)окси)пропаноат (21,68 г, 79 ммоль) растворяли в DCM (395 мл) в атмосфере N2 и охлаждали до -78°C в бане сухой лед/ацетон. Диизобутилалюмогидрид (1 M в гексане, 158 мл, 158 ммоль) добавляли при помощи шприца в течение 4 часов. Реакционную смесь перемешивали при -78°C еще дополнительно 30 минут. Через 30 минут добавляли этилацетат (75 мл), чтобы погасить реакцию, и реакционную смесь нагревали до 0°C в бане лед/вода. Добавляли насыщенный водный раствор калий натрий тартрата (~200 мл) и реакционную смесь тщательно перемешивали в течение ночи, медленно нагревая до комнатной температуры по мере таяния ледяной бани. Через 18 часов двухфазную смесь выливали в делительную воронку и слои разделяли. Водный слой экстрагировали при помощи DCM (3×150 мл). Объединенные органические слои пропускали через фазовый сепаратор и концентрировали с получением прозрачного бесцветного масла. Масло очищали при помощи колоночной флэш-хроматографии (силикагель (SiО2), 0→20% этилацетата в гексане) с получением указанного в заголовке соединения (15,85 г, 87%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 9,66 (д, J=1,7 Гц, 1H), 4,18 (кв.д, J=6,8, 1,7 Гц, 1H), 1,31 (д, J=6,8 Гц, 3H), 1,11-1,01 (м, 21H); 13C ЯМР (101 МГц, CDCl3) δ 204,54, 73,83, 18,95, 17,89, 12,14.
[0088] Пример 3A: Получение (3R,4,S)-2-метил-4-феноксипентан-3-ола.
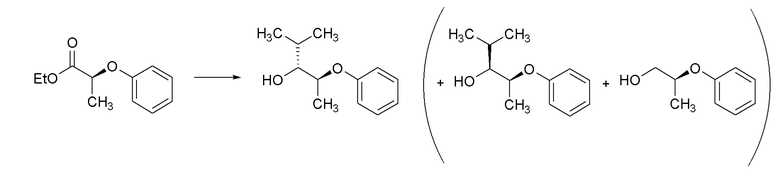
[0089] В колбе объемом 250 мл получали раствор изопропилмагнийбромида (2M в Et2О, 9,01 мл, 18,02 ммоль) и литийборгидрида (2M раствор в THF, 5,86 мл, 11,71 ммоль) в THF (33 мл). Реакционную смесь охлаждали до 0°C в ледяной бане. Через ~10 минут при помощи шприца добавляли по каплям этил (S)-2-феноксипропаноат (1,75 г, 9,01 ммоль) в виде раствора в THF (9 мл с промывками 2×1,5 мл) в течение 3 часов при помощи шприцевого насоса. Полученную бледно-желтую чистую реакционную смесь перемешивали в течение ночи, медленно нагревая до комнатной температуры по мере таяния ледяной бани. Реакционную смесь гасили водой (100 мл, осторожно, ВЫДЕЛЕНИЕ ГАЗА) и разбавляли при помощи Et2O (100 мл). Слои разделяли и водный слой экстрагировали при помощи Et2O (3×100 мл). Объединенные органические слои сушили над MgSO4, фильтровали и концентрировали с получением масла. Масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→30% этилацетата в гексане) с получением указанного в заголовке соединения (849 мг, 49%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 7,34-7,26 (м, 2H), 6,95 (тт, J=7,4, 1,1 Гц, 1H), 6,93-6,87 (м, 2H), 4,48 (кв.д, J=6,2, 3,8 Гц, 1H), 3,54 (дт, J=7,9, 3,4 Гц, 1H), 2,09 (д, J=3,1 Гц, 1H), 1,79 (дп, J=7,9, 6,7 Гц, 1H), 1,30 (д, J=6,3 Гц, 3H), 1,03 (д, J=6,6 Гц, 3H), 0,95 (д, J=6,8 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 157,39, 129,58, 121,08, 116,04, 78,00, 74,79, 29,87, 18,89, 18,71, 13,11; ИК (тонкая пленка) 3425, 2955, 1598, 1493, 1240, 1055, 752 см-1. Также выделяли (3S,4S)-2-метил-4-феноксипентан-3-ол (216 мг, 1,11 ммоль, 12% выход) в виде прозрачного бесцветного масла: 1H ЯМР (300 МГц, CDCl3) δ 7,34-7,21 (м, 2H), 7,00 6,86 (м, 3H), 4,38 (п, J=6,1 Гц, 1H), 3,36 (кв., J=5,1 Гц, 1H), 2,35 (д, J=5,1 Гц, 1H), 1,87 (пд, J=6,8, 5,0 Гц, 1H), 1,28 (д, J=6,2 Гц, 3H), 1,04-0,95 (м, 6H); 13C ЯМР (101 МГц, CDCl3) δ 157,73, 129,58, 121,18, 116,15, 79,40, 75,37, 30,07, 20,00, 16,60, 16,04; ИК (тонкая пленка) 3434, 2955, 1598, 1494, 1240, 1051, 752 см-1. Также выделяли (S)-2-феноксипропан-1-ол (44,4 мг, 0,292 ммоль, 3,2% выход) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 7,33-7,25 (м, 2H), 7,00-6,90 (м, 3H), 4,50 (пд, J=6,3, 3,8 Гц, 1H), 3,81-3,66 (м, 2H), 2,12 (с, 1H), 1,27 (д, J=6,3 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 157,73, 129,58, 121,22, 116,18, 74,77, 66,27, 15,84; ИК (тонкая пленка) 3381, 2932, 1598, 1493, 1240, 1051, 752 см-1.
[0090] Пример 3B: Получение (3R,4S)-4-((триизопропилсилил)окси)пент-1-ен-3-ола.
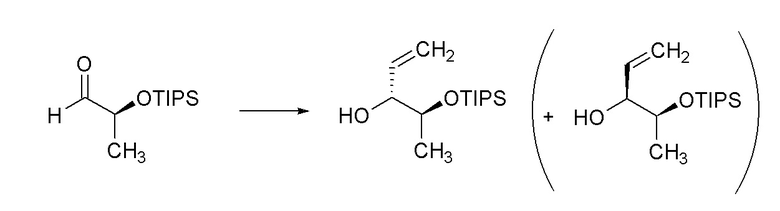
[0091] Раствор (S)-2-((триизопропилсилил)окси)пропаналя (5,0 г, 21,70 ммоль) в Et2О (108 мл) получали в круглодонной колбе объемом 250 мл и охлаждали до -78°C в бане сухой лед/ацетон в атмосфере N2. Затем при помощи шприца добавляли винилмагнийбромид (1,0 M раствор в THF, 23,87 мл, 23,87 ммоль) в течение 30 минут. Реакционную смесь перемешивали при -78°C в течение 30 минут и затем давали медленно нагреться до комнатной температуры в течение 2 часов. Реакционную смесь выливали в насыщенный водный раствор H4Cl (200 мл) и экстрагировали при помощи Et2О (3×100 мл). Объединенные органические слои сушили над MgSO4, фильтровали и концентрировали с получением бледно-желтого масла. Масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→20% этилацетата в гексане) с получением указанного в заголовке соединения (4,30 г, 77%, соотношение диастереомеров ~ 6:1) в виде прозрачного бесцветного масла: 1H ЯМР (300 МГц, CDCl3) δ 5,80 (ддд, J=17,0, 10,6, 6,0 Гц, 1H), 5,31 (дт, J=17,3, 1,7 Гц, 1H), 5,20 (дт, J=10,6, 1,6 Гц, 1H), 4,16 (дддт, J=6,4, 4,8, 3,2, 1,8 Гц, 1H), 4,00 (кв.д, J=6,4, 3,5 Гц, 1H), 2,45 (д, J=3,3 Гц, 1H), 1,12 (д, J=6,4 Гц, 3H), 1,08 (с, 21H); 13C ЯМР (101 МГц, CDCl3) δ 136,42, 116,31, 71,40, 60,35, 21,00, 18,02, 14,17, 12,38; ИК (неразбавленный) 3483, 2943, 2866, 1463, 676 см-1; HRMS-ESI (m/z) рассчитано для [C14H30NaO2Si]+, 281,1907; обнаружено, 281,1920.
[0092] Пример 3C: Получение (2S,3R)-2-((триизопропилсилил)окси)гекс-5-ен-3-ола.
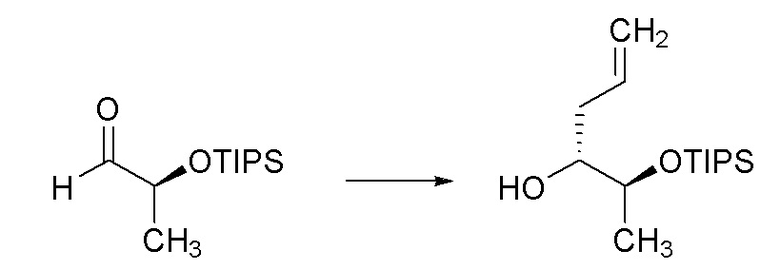
[0093] В круглодонную колбу объемом 500 мл загружали (+)-Ipc2-аллилборан (1M раствор в пентане, 25,0 мл, 25,00 ммоль) в атмосфере N2 и разбавляли при помощи Et2О (100 мл). Полученный чистый бесцветный раствор охлаждали до -78°C в бане ацетон/сухой лед. Добавляли при помощи шприца (S)-2-((триизопропилсилил)окси)пропаналь (4,61 г, 20,01 ммоль) в виде раствора в безводном Et2О (60 мл) в течение 1,5 часов. Прозрачную бесцветную реакционную смесь охлаждали дополнительно еще 1,5 часа при -78°C, после этого ТСХ указывала на расход исходного вещества. Затем добавляли MeOH (50 мл) и реакционную смесь перемешивали в течение 5 минут при -78°C. Добавляли pH 7 буфер (70 мл) и реакционную смесь нагревали до 0°C в бане лед/вода. Затем добавляли H2О2 (30%, 60 мл) и полученную двухфазную реакционную смесь тщательно перемешивали при 0°C в течение 2,5 часов и затем нагревали до комнатной температуры, пока плавился лед, и перемешивали в течение 30 часов. Слои разделяли и водную фазу экстрагировали при помощи Et2О (3×100 мл). Водный слой осторожно гасили насыщенным водным раствором Na2S2O3 на льду до тех пор, пока KI-крахмальная индикаторная бумага не показывала исчезновение остаточного количества H2О2. Объединенные органические слои сушили над MgSO4, фильтровали и концентрировали до чистого масла. Масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→15% этилацетата в гексане) с получением указанного в заголовке соединения (5,00 г, 92%) в виде прозрачного светло-розового масла: 1H ЯМР (400 МГц, CDCl3) δ 5,85 (ддт, J=17,2, 10,2, 7,0 Гц, 1H), 5,22-4,97 (м, 2H), 3,93 (кв.д, J=6,2, 3,3 Гц, 1H), 3,70 (ддт, J=8,3, 5,7, 2,9 Гц, 1H), 2,34 (д, J=2,6 Гц, 1H), 2,30-2,09 (м, 2H), 1,14 (д, J=6,3 Гц, 3H), 1,12-1,03 (м, 21H); 13C ЯМР (101 МГц, CDCl3) δ 134,91, 117,07, 74,48, 70,77, 36,72, 18,06, 16,59, 12,37; ИК (неразбавленный) 3480, 2943, 2866, 1463, 1067, 881 см-1; HRMS-ESI (m/z) рассчитано для [C15H33O2Si]+, 274,2270; обнаружено, 274,2274.
[0094] Пример 4A: Получение 1 -((((2S,3R)-3-(бензилокси)-4-метилпентан-2-ил)окси)метил)-4-метоксибензола.
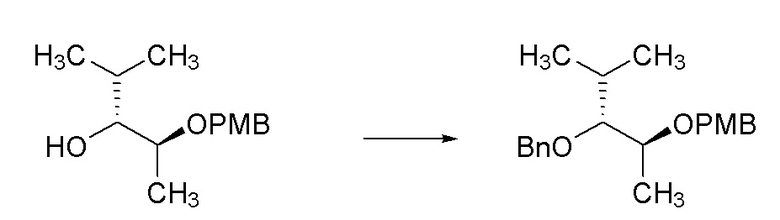
[0095] В круглодонной колбе объемом 250 мл получали суспензию гидрида натрия (0,329 г, 13,72 ммоль) в DMF (42,7 мл) в атмосфере N2 и охлаждали до 0°C в бане лед/вода. Через 5 минут при помощи шприца добавляли (2S,3R)-2-((4-метоксибензил)окси)-4-метилпентан-3-ол (1,868 г, 7,84 ммоль) в виде раствора в DMF (10 мл с промывками 2×5 мл). Полученную ярко-желтую реакционную смесь подогревали до комнатной температуры и перемешивали в течение 3 часов. Реакционную смесь охлаждали до 0°C и добавляли (бромметил)бензол (1,617 мл, 14,89 ммоль) одной порцией, с последующим добавлением тетрабутиламмониййодида (0,290 г, 0,784 ммоль). Реакционную смесь нагревали до 40°C и перемешивали в течение ночи. Реакционную смесь охлаждали до 0°C и при помощи шприца добавляли диэтиламин (2,433 мл, 23,51 ммоль) в течение 15 секунд. Бледно-желтую реакционную смесь нагревали до комнатной температуры и перемешивали в течение 1 часа, к этому моменту реакционная смесь становилась прозрачным желтым раствором. Через 1 час реакционную смесь гасили насыщенным водным раствором NH4Cl (200 мл) и экстрагировали при помощи Et2О (3×200 мл). Объединенные органические слои промывали насыщенным солевым раствором (200 мл), сушили над MgSO4, фильтровали и концентрировали с получением желтого масла. Масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→20% этилацетата в гексане) с получением указанного в заголовке соединения (1,73 г, 67%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 7,39-7,29 (м, 4H), 7,29-7,22 (м, 3H), 6,90-6,84 (м, 2H), 4,80 (д, J=11,3 Гц, 1H), 4,58 (д, J=11,3 Гц, 1H), 4,54 (д, J=11,4 Гц, 1H), 4,43 (д, J=11,4 Гц, 1H), 3,80 (с, 3H), 3,65 (кв.д, J=6,3, 4,5 Гц, 1H), 3,24 (дд, J=6,2, 4,4 Гц, 1H), 1,88 (дкв., J=13,4, 6,7 Гц, 1H), 1,26 (д, J=6,2 Гц, 3H), 0,96 (д, J=6,7 Гц, 3H), 0,92 (д, J=6,9 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 159,08, 139,27, 131,04, 129,09, 128,21, 127,81, 127,31, 113,77, 86,75, 76,06, 74,59, 70,33, 55,29, 30,11, 20,03, 18,44, 15,04; ИК (тонкая пленка) 2959, 2871, 1513, 1247, 1099, 1066, 1036 см-1.
[0096] Пример 4B: Получение триизопропил(((2S,3R)-3-((4-метоксибензил)окси)пент-4-ен-2-ил)окси)силана.
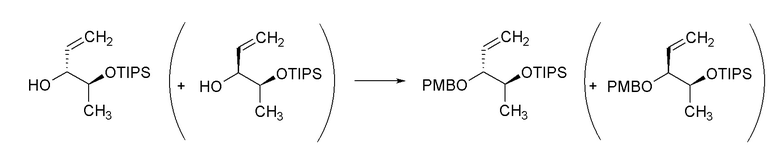
[0097] В круглодонной колбе объемом 250 мл получали суспензию гидрида натрия (1,165 г, 29,1 ммоль) в DMF (93 мл) в атмосфере N2 и охлаждали до 0°C в бане лед/вода. Через 5 минут добавляли при помощи шприца (3R,4,S)-4-((триизопропилсилил)окси)пент-1-ен-3-ол (4,301 г, 16,64 ммоль, соотношение диастереомеров ~6:1) в виде раствора в DMF (20 мл с промывками 2×10 мл). Полученную ярко-желтую реакционную смесь подогревали до комнатной температуры и перемешивали в течение 3 часов. Реакционную смесь охлаждали до 0°C и одной порцией добавляли 4-метоксибензилбромид (4,61 мл, 31,6 ммоль), с последующим добавлением тетрабутиламмониййодида (0,615 г, 1,664 ммоль), после этого реакционную смесь подверглись отчетливому изменению цвета до светло-оранжевого. Реакционную смесь нагревали до комнатной температуры и перемешивали в течение ночи. Через 20 часов ТСХ указывала на расход исходного вещества. Реакционную смесь охлаждали до 0°C и при помощи шприца добавляли диэтиламин (5,16 мл, 49,9 ммоль) в течение 15 секунд. Бледно-желтую реакционную смесь нагревали до комнатной температуры и перемешивали в течение 1 часа, к этому моменту реакционная смесь становилась прозрачным желтым раствором. Через 1 час реакционную смесь гасили насыщенным водным раствором NH4Cl (150 мл) и экстрагировали при помощи Et2О (3×150 мл). Объединенные органические слои промывали насыщенным солевым раствором (100 мл), сушили над MgSO4, фильтровали и концентрировали с получением желтого масла. Масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→15% MTBE в петролейном эфире) с получением указанного в заголовке соединения (4,063 г, 65%, соотношение диастереомеров ~6:1) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 7,34-7,19 (м, 2H), 6,92-6,79 (м, 2H), 5,84 (ддд, J=17,1, 10,5, 7,4 Гц, 1H), 5,43-5,08 (м, 2H), 4,55 (д, J=11,5 Гц, 1H), 4,38 (д, J=11,5 Гц, 1H), 3,98 (кв.д, J=6,3, 4,5 Гц, 1H), 3,80 (с, 3H), 3,63 (ддт, J=7,5, 4,4, 1,0 Гц, 1H), 1,19 (д, J=6,2 Гц, 3H), 1,10-0,98 (м, 21H); 13C ЯМР (101 МГц, CDCl3) δ 158,96, 136,47, 131,02, 129,29, 118,19, 113,62, 85,07, 71,35, 70,35, 55,26, 19,87, 18,15, 12,55; ИК (неразбавленный) 2942, 2865, 1513, 1246, 1039, 677 см-1; HRMS-ESI (m/z) рассчитано для [C22H38NaO3Si]+, 401,24824; обнаружено, 401,24711.
[0098] Пример 4C: Получение метил (R)-2-((трет-бутилдиметилсилил)окси)-2-фенилацетата.
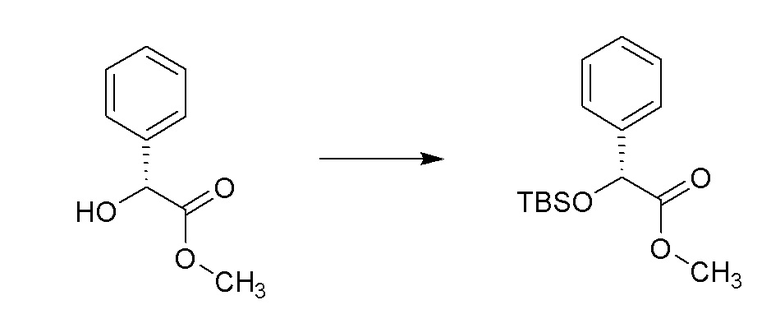
[0099] Раствор этил (R)-2-гидрокси-2-фенилацетата (5,00 г, 30,1 ммоль), TBSCl (6,80 г, 45,1 ммоль) и имидазола (4,10 г, 60,2 ммоль) получали в DMF (31,7 мл) и перемешивали в течение ночи при комнатной температуре. Через 20 часов раствор разбавляли Et2О и водой. Органическую фазу промывали насыщенным солевым раствором, сушили над Na2SO4 и концентрировали до масла. Масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→5% этилацетата в гексане) с получением указанного в заголовке соединения (7,53 г, 85%) в виде прозрачного бесцветного масла: 1H ЯМР (300 МГц, CDCl3) δ 7,42-7,31 (м, 2H), 7,28-7,17 (м, 3H), 5,13 (с, 1H), 3,57 (с, 3H), 0,81 (с, 9H), 0,00 (с, 3H), -0,07 (с, 3H); 13C ЯМР (126 МГц, CDCl3) δ 172,61, 139,11, 128,33, 128,09, 126,33, 74,39, 52,18, 25,71, 18,35, -5,09, -5,16; ИК (тонкая пленка) 2952, 2929, 2886, 2857, 1758, 1737, 1472, 1253, 1207, 1191, 1170, 1125, 861, 836, 778, 725, 696 см-1; HRMS-ESI (m/z) рассчитано для [C15H25O3Si]+, 281,1567; обнаружено, 281,1578.
[00100] Пример 5A: Получение (2S,3R)-3-(бензилокси)-4-метилпентан-2-ола.
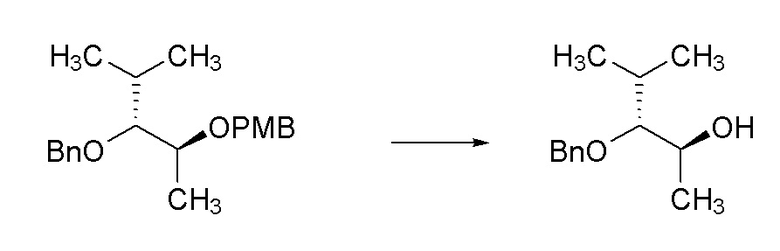
[00101] В колбе объемом 250 мл растворяли 1-((((2S,3R)-3-(бензилокси)-4-метилпентан-2-ил)окси)метил)-4-метоксибензол (1,7255 г, 5,25 ммоль) в ацетонитриле (96 мл) и H2О (9,55 мл) и охлаждали до 0°C в ледяной бане. Через ~5 минут добавляли церий-аммоний нитрат (14,40 г, 26,3 ммоль) и оранжевую реакционную смесь перемешивали при 0°C в течение 3 часов. Через 3 часа смесь гасили насыщенным водным раствором NaHСО3 (100 мл) и затем экстрагировали при помощи DCM (3 × 100 мл). Объединенные органические слои пропускали через фазовый сепаратор и концентрировали с получением прозрачного бесцветного масла. Масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→50% этилацетата в гексане) с получением указанного в заголовке соединения (401 мг, 37%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 7,39-7,22 (м, 5H), 4,66 (д, J=0,9 Гц, 2H), 3,93 (кв.д, J=6,4, 4,2 Гц, 1H), 3,13 (дд, J=6,4, 4,2 Гц, 1H), 1,92 (с, 1H), 1,86 (дкв., J=13,5, 6,8 Гц, 1H), 1,20 (д, J=6,5 Гц, 3H), 1,03 (д, J=6,7 Гц, 3H), 0,94 (д, J=6,9 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 138,91, 128,40, 127,60, 127,58, 88,50, 74,84, 68,43, 30,07, 19,94, 18,66, 18,08; ИК (тонкая пленка) 3406, 2962, 1454, 1093, 1063, 734, 697 см-1.
[00102] Пример 5B: Получение (2S,3R)-3-((4-метоксибензил)окси)пент-4-ен-2-ола.
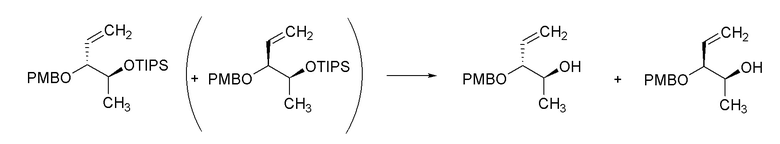
[00103] Раствор триизопропил(((2S,3R)-3-((4-метоксибензил)окси)пент-4-ен-2-ил)окси)силана (4,06 г, 10,7 ммоль, соотношение диастереомеров ~6:1) получали в круглодонной колбе объемом 250 мл в THF (53,7 мл) в атмосфере N2 и охлаждали до 0°C. Через 5 минут при помощи шприца добавляли по каплям TBAF (12,88 мл, 12,88 ммоль) в течение 2 минут. Реакционной смеси давали нагреться до комнатной температуры и перемешивали в течение 4 часов. Реакционную смесь гасили насыщенным водным раствором NH4Cl (100 мл) и экстрагировали при помощи Et2О (3×100 мл). Объединенные органические слои сушили над MgSO4, фильтровали и концентрировали с получением прозрачного бесцветного масла. Масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→30% этилацетата в гексане) с получением указанного в заголовке соединения (1,272 г, 53%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 7,25 (д, J=8,4 Гц, 2H), 6,88 (д, J=8,6 Гц, 2H), 5,82 (ддд, J=17,4, 10,4, 8,1 Гц, 1H), 5,40 (ддд, J=10,4, 1,9, 0,8 Гц, 1H), 5,30 (ддд, J=17,3, 1,9, 0,9 Гц, 1H), 4,57 (д, J=11,5 Гц, 1H), 4,31 (д, J=11,4 Гц, 1H), 3,92-3,78 (м, 4H), 3,71-3,62 (м, 1H), 2,21 (д, J=3,9 Гц, 1H), 1,13 (д, J=6,4 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 159,19, 134,66, 130,34, 129,39, 120,20, 113,80, 83,96, 69,95, 69,27, 55,27, 17,94; ИК (тонкая пленка) 3447, 2976, 2868, 1612, 1513, 1545, 1033, 819 см-1; HRMS-ESI (m/z) рассчитано для [C13H18NaO3]+, 245,11482; обнаружено, 245,1134. Также выделяли (2S,3S)-3-((4-метоксибензил)окси)пент-4-ен-2-ол (325 мг, 1,46 ммоль, 14% выход) в виде прозрачного бесцветного масла: 1H ЯМР (300 МГц, CDCl3) δ 7,31-7,21 (м, 2H), 6,94-6,85 (м, 2H), 5,79-5,62 (м, 1H), 5,45-5,15 (м, 1H), 4,57 (д, J=11,2 Гц, 1H), 4,28 (д, J=11,1 Гц, 1H), 3,81 (с, 3H), 3,74-3,64 (м, 1H), 3,50 (т, J=7,9 Гц, 1H), 2,83-2,69 (м, 1H), 1,18 (д, J=6,2 Гц, 1H), 1,12 (д, J=6,2 Гц, 3H); ИК (тонкая пленка) 3455, 2869, 1513, 1247, 1069, 1034, 820 см-1.
[00104] Пример 5C: Получение (1R,2S)-1-((4-метоксибензил)окси)-1-фенилпропан-2-ола.
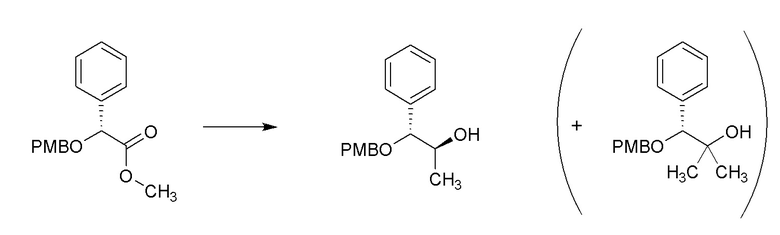
[00105] Раствор литийборгидрида (2M раствор в THF, 3,93 мл, 7,86 ммоль) и метиллития (1,6M раствор в THF, 3,93 мл, 6,29 ммоль) получали в Et2О (29,1 мл) и охлаждали до -78°C в бане сухой лед/ацетон. Через ~5 минут медленно добавляли раствор метил (R)-2-((4-метоксибензил)окси)-2-фенилацетата (1,5 г, 5,24 ммоль), растворенного в Et2О (9 мл), через капельную воронку. Реакционной смесь давали нагреться до комнатной температуры медленно в течение ночи. Через 20 часов реакционную смесь осторожно гасили насыщенным водным раствором NH4Cl и экстрагировали при помощи Et2О. Объединенные органические слои сушили над Na2SO4, фильтровали и концентрировали. Неочищенное вещество очищали при помощи колоночной флэш-хроматографии (SiО2, 0→15% этилацетата в гексане) с получением указанного в заголовке соединения (744 мг, 50%) в виде густого масла: 1H ЯМР (400 МГц, CDCl3) δ 7,43-7,29 (м, 5H), 7,25-7,18 (м, 2H), 6,90-6,85 (м, 2H), 4,48 (д, J=11,3 Гц, 1H), 4,26 (д, J=5,0 Гц, 1H), 4,23 (д, J=11,3 Гц, 1H), 4,01-3,91 (м, 1H), 3,81 (с, 3H), 1,93 (с, 1H), 1,11 (д, J=6,4 Гц, 3H); 13C ЯМР (126 МГц, CDCl3) δ 159,24, 138,27, 130,20, 129,45, 128,42, 128,02, 127,84, 113,82, 84,63, 70,82, 70,46, 55,28, 18,15; ИК (тонкая пленка) 3440, 2867, 2835, 1611, 1512, 1492, 1452, 1301, 1244, 1172, 1134, 1060, 1030, 952, 818, 755, 701 см-1; HRMS-ESI (m/z) рассчитано для [C17H20O3Na]+, 295,1305; обнаружено, 295,1300. Также выделяли (R)-1-((4-метоксибензил)окси)-2-метил-1-фенилпропан-2-ол (353 мг, 1,17 ммоль, 22% выход) в виде густого масла: 1H ЯМР (400 МГц, CDCl3) δ 7,40-7,29 (м, 5H), 7,25-7,19 (м, 2H), 6,93-6,85 (м, 2H), 4,45 (д, J=11,2 Гц, 1H), 4,23-4,15 (м, 2H), 3,81 (с, 3H), 2,53 (с, 1H), 1,16 (с, 3H), 1,09 (с, 3H); 13C ЯМР (126 МГц, CDCl3) δ 159,23, 138,13, 130,19, 129,47, 128,36, 128,03, 127,86, 113,79, 87,70, 72,85, 70,65, 55,28, 26,17, 24,38; ИК (тонкая пленка) 3418, 2973, 2933, 2866, 2835, 1611, 1512, 1452, 1370, 1351, 1244, 1170, 1085, 1062, 1028, 819, 742, 702 см-1; HRMS-ESI (m/z) рассчитано для [C18H22O3Na]+, 309,1461; обнаружено, 309,1462.
[00106] Пример 6A: Получение 1-метокси-4-((((3R,4S)-4-феноксипент-1-ен-3-ил)окси)метил)бензола.
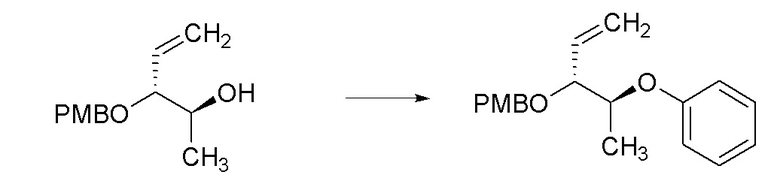
[00107] Раствор (2S,3R)-3-((4-метоксибензил)окси)пент-4-ен-2-ола (1,272 г, 5,72 ммоль), ацетата трифенилвисмута(V) (4,15 г, 7,44 ммоль) и ацетата меди(II) (0,104 г, 0,572 ммоль) получали в безводном толуоле (38,1 мл) в колбе объемом 100 мл в атмосфере N2. Затем добавляли при помощи шприца N-циклогексил-N-метилциклогексанамин (1,410 мл, 6,58 ммоль) одной порцией. Полученную сине-зеленую реакционную смесь нагревали до 40°C с получением бледно-сине-зеленой реакционной смеси. Смесь перемешивали при температуре в течение 96 часов. Реакционную смесь охлаждали до комнатной температуры и фильтровали через слой Celite®, промывали при помощи DCM и затем концентрировали с получением темно-желтого масла. Масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→20% этилацетата в гексане) с получением указанного в заголовке соединения (1,43 г, 84%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 7,31-7,20 (м, 4H), 6,96-6,81 (м, 5H), 5,87 (ддд, J=17,5, 10,0, 7,4 Гц, 1H), 5,35 (дт, J=2,6, 1,7 Гц, 1H), 5,33-5,30 (м, 1H), 4,60 (д, J=11,6 Гц, 1H), 4,44-4,35 (м, 2H), 3,91 (ддт, J=7,4, 4,7, 1,0 Гц, 1H), 3,79 (с, 3H), 1,32 (д, J=6,3 Гц, 3H); 13C ЯМР (126 МГц, CDCl3) δ 159,07, 157,93, 135,53, 130,48, 129,40, 129,32, 120,78, 118,99, 116,15, 113,69, 81,88, 76,17, 70,34, 55,25, 15,69; ИК (тонкая пленка) 2934, 1598, 1512, 1493, 1242, 1068, 753 см-1.
[00108] Пример 6B: Получение 1-(((2S,3R)-3-(бензилокси)-4-метилпентан-2-ил)окси)-2,4-дифторбензола.
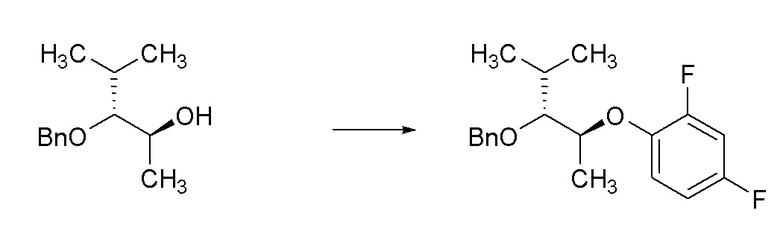
[00109] Раствор (2S,3R)-3-(бензилокси)-4-метилпентан-2-ола (91,5 мг, 0,439 ммоль) получали в DMF (1,76 мл) при комнатной температуре в небольшом сосуде. К этому раствору добавляли трет-бутоксид калия (71,5 мг, 0,637 ммоль), после этого 1,2,4-трифторбензол (138 мкл, 1,318 ммоль). Смесь перемешивали при 60°C в течение 72 часов. Реакционную смесь гасили при помощи AcOH (72 мкл) и затем разбавляли гексаном (1,76 мл). Смесь очищали при помощи колоночной флэш-хроматографии (SiО2, 0→20% этилацетата в гексане) с получением указанного в заголовке соединения (122,6 мг, 87%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 7,43-7,37 (м, 2H), 7,37-7,31 (м, 2H), 7,31-7,25 (м, 1H), 7,01 (ддд, J=10,7, 8,9, 5,4 Гц, 1H), 6,68 (ддд, J=9,8, 6,7, 3,0 Гц, 1H), 6,58 (ддт, J=8,9, 7,7, 3,1 Гц, 1H), 4,88 (д, J=11,1 Гц, 1H), 4,61 (д, J=11,1 Гц, 1H), 4,51 (кв.д, J=6,2, 3,8 Гц, 1H), 3,42 (дд, J=6,9, 3,8 Гц, 1H), 1,89 (г, J=6,8 Гц, 1H), 1,38 (д, J=6,3 Гц, 3H), 1,01 (д, J=6,7 Гц, 3H), 0,99 (д, J=6,8 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 158,73 (дд, J=242,0, 2,5 Гц), 149,83 (дд, J=241,2, 3,2 Гц), 146,37 (дд, J=12,5, 10,4 Гц), 138,86, 128,29, 127,99, 127,52, 116,51 (дд, J=21,2, 10,3 Гц), 106,87 (дд, J=23,9, 7,0 Гц), 104,17 (дд, J=27,0, 2,1 Гц), 86,00, 77,45, 74,87, 30,42, 19,66, 18,78, 14,46; 19F ЯМР (376 МГц, CDCl3) δ -116,80 (д, J=15,0 Гц), -138,81 (д, J=15,0 Гц); ИК (тонкая пленка) 2963, 1624, 1510, 1205, 1150, 1099, 698 см-1; HRMS-ESI (m/z) рассчитано для [C19H26F2NO2]+, 338,1926; обнаружено, 338,192.
[00110] Пример 6C: Получение 1-метокси-4-((((2R,3S)-3-((2-метилаллил)окси)-1-фенилбутан-2-ил)окси)метил)бензола.
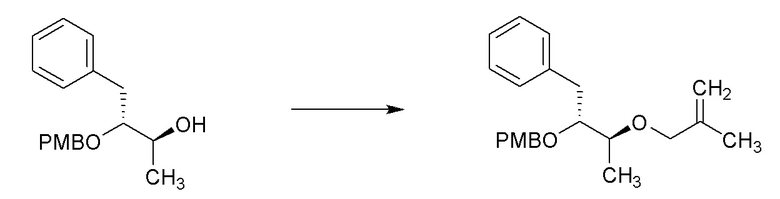
[00111] Раствор (2S,3R)-3-((4-метоксибензил)окси)-4-фенилбутан-2-ола (0,145 г, 0,506 ммоль) получали в THF (1,688 мл). Затем добавляли гидрид натрия (0,030 г, 0,760 ммоль) и TBAI (0,019 г, 0,051 ммоль). Одной порцией добавляли 3-бром-2-метилпроп-1-ен (0,153 мл, 1,519 ммоль) и реакционной смеси давали нагреться до температуры кипения с обратным холодильником. Реакционную смесь затем гасили водой и экстрагировали при помощи Et2О (2×), сушили над Na2SO4, фильтровали и концентрировали до масла. Неочищенное вещество очищали при помощи колоночной флэш-хроматографии (SiО2, 0→10% этилацетата в гексане) с получением указанного в заголовке соединения (144,1 мг, 79%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 7,33-7,18 (м, 5H), 7,12-7,01 (м, 2H), 6,83-6,77 (м, 2H), 5,01-4,92 (м, 1H), 4,89-4,80 (м, 1H), 4,47 (д, J=11,0 Гц, 1H), 4,26 (д, J=11,0 Гц, 1H), 3,94 (д, J=12,5 Гц, 1H), 3,89 3,80 (м, 1H), 3,78 (с, 3H), 3,63 (дт, J=8,5, 4,4 Гц, 1H), 3,46 (кв.д, J=6,3, 4,3 Гц, 1H), 2,89 (дд, J=13,9, 4,4 Гц, 1H), 2,79 (дд, J=13,9, 8,1 Гц, 1H), 1,74 (т, J=1,1 Гц, 3H), 1,24 (д, J=6,3 Гц, 3H); 13C ЯМР (126 МГц, CDCl3) δ 159,00, 142,65, 139,42, 130,77, 129,57, 129,49, 128,19, 126,01, 113,59, 111,73, 82,70, 76,66, 72,84, 72,64, 55,26, 37,96, 19,68, 15,29; ИК (тонкая пленка) 3027, 2932, 1612, 1512, 1495, 1453, 1301, 1246, 1172, 1081, 1035, 898, 820, 743, 699 см-1; HRMS-ESI (m/z) рассчитано для [C22H29O3]+, 341,2111; обнаружено, 341,2095.
[00112] Пример 7: Получение (2R,3S)-2-((4-метоксибензил)окси)-3-феноксибутан-1-ола.
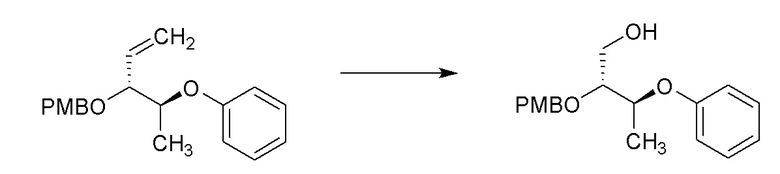
[00113] В колбе объемом 100 мл растворяли 1-метокси-4-((((3R,4S)-4-феноксипент-1-ен-3-ил)окси)метил)бензол (0,908 г, 3,04 ммоль) и бикарбонат натрия (0,026 г, 0,304 ммоль) в безводном DCM (29,5 мл) и безводном MeOH (0,928 мл). К этому раствору добавляли 5 капель 1% раствора DCM индикатора Судан III, получая светло-розовый раствор. Реакционную смесь охлаждали до -78°C в бане сухой лед/ацетон. Через ~5 минут через реакционную смесь О3 барботировали до исчезновения розовой окраски. Реакционную смесь затем продували газообразным N2 и добавляли дополнительное количество MeOH (9,28 мл) с последующим добавлением твердого боргидрида натрия (0,345 г, 9,13 ммоль) одной порцией. Раствору давали нагреться до комнатной температуры путем удаления бани сухой лед/ацетон, и реакционную смесь перемешивали в течение ночи. Через 18 часов ТСХ показывала преобразование в одно более низкое Rf пятно. Реакционную смесь гасили при помощи H2О (50 мл) и экстрагировали при помощи DCM (3×50 мл). Объединенные органические слои пропускали через фазовый сепаратор и концентрировали с получением бесцветного масла. Неочищенное масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→100% этилацетата в гексане) с получением указанного в заголовке соединения (893,7 мг, 97%) в виде прозрачного бесцветного масла: 1H ЯМР (300 МГц, CDCl3) δ 7,32-7,22 (м, 5H), 6,99-6,84 (м, 5H), 4,70 (д, J=11,2 Гц, 1H), 4,60 (д, J=11,2 Гц, 1H), 4,56-4,46 (м, 1H), 3,80 (с, 3H), 3,76 (дт, J=6,0, 4,6 Гц, 2H), 3,65 (тд, J=5,0, 4,4 Гц, 1H), 1,36 (д, J=6,3 Гц, 3H); 13C ЯМР (75 МГц, CDCl3) δ 159,41, 157,49, 130,15, 129,67, 129,59, 121,14, 115,99, 113,93, 81,20, 73,81, 72,66, 61,49, 55,29, 16,09; ИК (тонкая пленка) 3427, 2934, 1612, 1585, 1512, 1493, 1240, 1067, 1031, 752, 692 см-1; HRMS-ESI (m/z) рассчитано для [C18H22NaO4]+, 325,1410; обнаружено, 325,1396.
[00114] Пример 8A: Получение (((2R,3S)-2-((4-метоксибензил)окси)бутан-1,3-диил)бис(окси))дибензола.
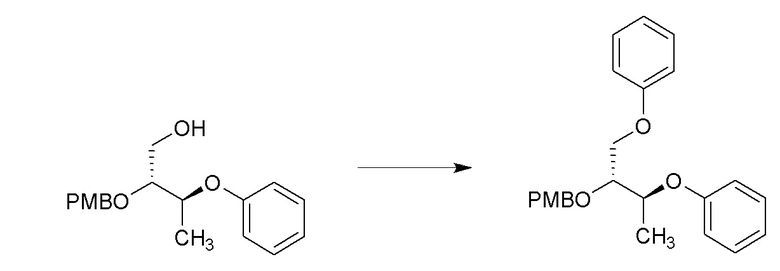
[00115] Раствор (2R,3S)-2-((4-метоксибензил)окси)-3-феноксибутан-1-ола (180 мг, 0,595 ммоль), ацетата трифенилвисмута(V) (499 мг, 0,893 ммоль) и ацетата меди(II) (16,22 мг, 0,089 ммоль) получали в безводном толуоле (3,97 мл) в 20 мл сосуде в атмосфере N2. Затем добавляли при помощи шприца N-циклогексил-N-метилциклогексанамин (166 мкл, 0,774 ммоль) одной порцией. Полученную сине-зеленую реакционную смесь нагревали до 40°C с получением бледно-сине-зеленой реакционной смеси и перемешивали в течение 48 часов. Через 48 часов ТСХ указывала на расход исходного вещества и преобразование в одно более высокое Rf пятно. Реакционную смесь охлаждали до комнатной температуры и фильтровали через слой Celite® при помощи DCM и органические вещества концентрировали с получением темно-желтого масла. Неочищенное масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→20% этилацетата в гексане) с получением указанного в заголовке соединения (208,5 мг, 93%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 7,33-7,20 (м, 6H), 6,98-6,82 (м, 8H), 4,71 (с, 2H), 4,68-4,60 (м, 1H), 4,17 (дд, J=10,0, 4,8 Гц, 1H), 4,10 (дд, J=10,0, 5,5 Гц, 1H), 3,98 (кв., J=5,1 Гц, 1H), 3,78 (с, 3H), 1,40 (д, J=6,2 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 159,31, 158,67, 157,61, 130,42, 129,66, 129,53, 129,45, 120,95, 120,92, 115,92, 114,62, 113,80, 78,80, 73,70, 73,03, 67,81, 55,26, 15,52; ИК (тонкая пленка) 2933, 1598, 1492, 1237, 1081, 1032, 751, 691 см-1; HRMS-ESI (m/z) рассчитано для [C24H26NaO4]+, 401,1723; обнаружено, 401,1725.
[00116] Пример 8B: Получение 1-метокси-4-((((2R,3,S)-1-метокси-3-феноксибутан-2-ил)окси)метил)бензола.
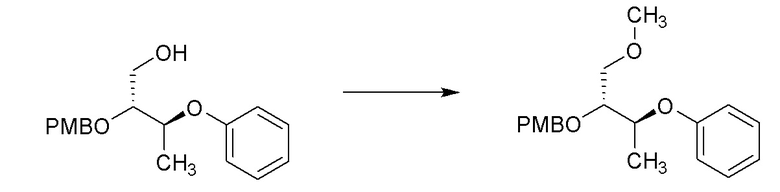
[00117] В небольшом сосуде (2R,3S)-2-((4-метоксибензил)окси)-3-феноксибутан-1-ол (150 мг, 0,496 ммоль) растворяли в DCM (2,48 мл) в атмосфере N2. N1,N1,N8,N8-тетраметилнафталин-1,8-диамин (319 мг, 1,488 ммоль) добавляли одной порцией, с последующим добавлением триметилоксоний тетрафторбората (110 мг, 0,744 ммоль). Полученный чистый бесцветный раствор перемешивали при комнатной температуре в течение ночи. Через 20 часов ТСХ показывала полный расход исходного вещества. Реакционную смесь осторожно гасили насыщенным водным раствором NaHСО3 (20 мл) и экстрагировали при помощи DCM (3×20 мл). Объединенные органические слои промывали 1N раствором HCl (2×20 мл), после этого насыщенным солевым раствором (20 мл). Органические слои фильтровали через фазовый сепаратор и концентрировали с получением бледно-желтого масла. Неочищенное масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→30% этилацетата в гексане) с получением указанного в заголовке соединения (117,5 мг, 75%) в виде бледно-желтого масла: 1H ЯМР (400 МГц, CDCl3) δ 7,31-7,22 (м, 4H), 6,97-6,81 (м, 5H), 4,65 (с, 2H), 4,54 (кв.д, J=6,2, 4,9 Гц, 1H), 3,79 (с, 3H), 3,74 (кв., J=5,0 Гц, 1H), 3,56 (дд, J=10,3, 4,6 Гц, 1H), 3,51 (дд, J=10,2, 5,3 Гц, 1H), 3,33 (с, 3H), 1,34 (д, J=6,3 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 159,20, 157,78, 130,71, 129,50, 129,48, 120,79, 115,91, 113,73, 79,30, 73,71, 72,64, 72,32, 59,22, 55,26, 15,44; ИК (тонкая пленка) 2894, 1598, 1513, 1493, 1240, 1083, 1034, 752, 692 см-1; HRMS-ESI (m/z) рассчитано для [C19H24NaO4]+, 339,1567; обнаружено, 339,1569.
[00118] Пример 8C: Получение 1-((((2R,3S)-1-(бензилокси)-3-феноксибутан-2-ил)окси)метил)-4-метоксибензола.
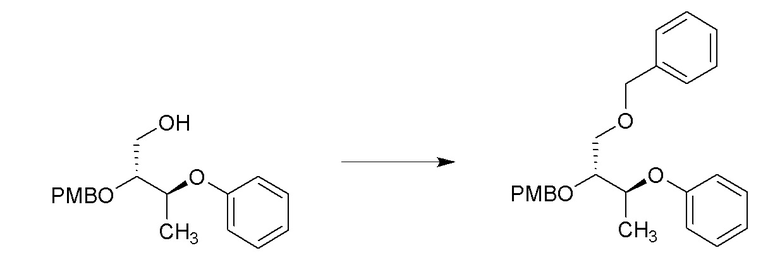
[00119] В 20 мл флаконе получали раствор (2R,3S)-2-((4-метоксибензил)окси)-3-феноксибутан-1-ола (145 мг, 0,480 ммоль) в DMF (3,84 мл) и охлаждали до 0°C в ледяной водяной бане. Через ~5 минут добавляли гидрид натрия (33,6 мг, 0,839 ммоль) и полученную реакционную смесь перемешивали в течение 2 часов, медленно нагревая до комнатной температуры. Через 2 часа реакционную смесь охлаждали до 0°C и добавляли (бромметил)бензол (99 мкл, 0,911 ммоль) одной порцией при помощи шприца, с последующим добавлением тетрабутиламмоний йодида (17,71 мг, 0,048 ммоль). Реакционную смесь оставляли перемешиваться в течение ночи, медленно нагревая до комнатной температуры по мере таяния ледяной бани. Через 18 часов ТСХ показывала полный расход исходного вещества. Реакционную смесь гасили насыщенным водным раствором NH4Cl (20 мл) и экстрагировали при помощи Et2О (3×20 мл). Объединенные органические слои промывали насыщенным солевым раствором (20 мл), сушили над MgSO4, фильтровали и концентрировали с получением желтого масла. Неочищенное масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→20% этилацетата в гексане) с получением указанного в заголовке соединения (148,4 мг, 79%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 7,34-7,20 (м, 9H), 6,96-6,87 (м, 3H), 6,87-6,82 (м, 2H), 4,65 (с, 2H), 4,63-4,55 (м, 1H), 4,51 (д, J=2,0 Гц, 2H), 3,82-3,74 (м, 4H), 3,68-3,57 (м, 2H), 1,34 (д, J=6,3 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 159,19, 157,76, 138,25, 130,69, 129,51, 129,48, 128,32, 127,58, 127,54, 120,75, 115,86, 113,72, 79,41, 73,65, 73,37, 72,67, 69,77, 55,25, 15,40; ИК (тонкая пленка) 3029, 2862, 1597, 1512, 1493, 1240, 1086, 1033, 751, 693 см-1; HRMS-ESI (m/z) рассчитано для [C25H28NaO4]+, 415,1880; обнаружено, 415,1876.
[00120] Пример 8D: Получение 1-((((2R,3S)-1-(аллилокси)-3-феноксибутан-2-ил)окси)метил)-4-метоксибензола.
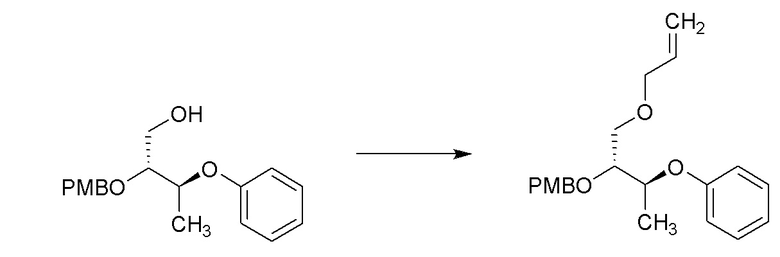
[00121] В 20 мл флаконе получали раствор (2R,3S)-2-((4-метоксибензил)окси)-3-феноксибутан-1-ола (145,4 мг, 0,481 ммоль) в DMF (3,85 мл) и охлаждали до 0°C в водной бане со льдом. Через ~5 минут добавляли гидрид натрия (33,7 мг, 0,842 ммоль) и полученную реакционную смесь перемешивали в течение 2 часов, медленно нагревая до комнатной температуры. Через 2 часа реакционную смесь охлаждали до 0°C и добавляли аллилбромид (79 мкл, 0,914 ммоль) одной порцией при помощи шприца, с последующим доавлением тетрабутиламмониййодида (17,76 мг, 0,048 ммоль). Реакционную смесь оставляли перемешиваться в течение ночи, медленно нагревая до комнатной температуры по мере таяния ледяной бани. Через 20 часов ТСХ указывала на расход исходного вещества. Реакционную смесь гасили насыщенным водным раствором NH4Cl (20 мл) и экстрагировали при помощи Et2О (3×20 мл). Объединенные органические слои промывали насыщенным солевым раствором (20 мл), сушили над MgSO4, фильтровали и концентрировали с получением желтого масла. Неочищенное масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→20% этилацетата в гексане) с получением указанного в заголовке соединения (145,4 мг, 88%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 7,31-7,20 (м, 4H), 6,96-6,82 (м, 5H), 5,87 (ддт, J=17,1, 10,8, 5,5 Гц, 1H), 5,25 (дкв., J=17,2, 1,7 Гц, 1H), 5,16 (дкв., J=10,4, 1,4 Гц, 1H), 4,66 (с, 2H), 4,56 (кв.д, J=6,2, 4,8 Гц, 1H), 3,97 (дт, J=5,5, 1,5 Гц, 2H), 3,85-3,73 (м, 4H), 3,62 (дд, J=10,2, 4,8 Гц, 1H), 3,56 (дд, J=10,2, 5,5 Гц, 1H), 1,35 (д, J=6,3 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 159,20, 157,78, 134,75, 130,74, 129,52, 129,47, 120,76, 116,81, 115,91, 113,73, 79,35, 73,77, 72,72, 72,30, 69,84, 55,26, 15,37; ИК (тонкая пленка) 2865, 1598, 1513, 1493, 1240, 1084, 1034, 752 см-1; HRMS-ESI (m/z) рассчитано для [C21H26NaO4]+, 365,1723; обнаружено, 365,1731.
[00122] Пример 9, Стадия 1: Получение (2S,3S)-2-((4-метоксибензил)окси)-3-феноксибутаналя.
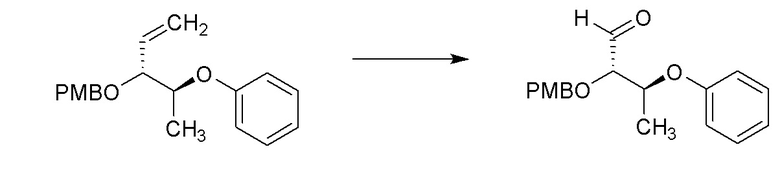
[00123] В колбе объемом 100 мл растворяли 1-метокси-4-((((3R,4S)-4-феноксипент-1-ен-3-ил)окси)метил)бензол (0,500 г, 1,676 ммоль) и бикарбонат натрия (0,014 г, 0,168 ммоль) в безводном DCM (15,23 мл) и безводном MeOH (1,523 мл). К этому раствору добавляли 5 капель 1% раствора DCM индикатора Судан III, получая светло-розовый раствор. Реакционную смесь охлаждали до -78°C в бане сухой лед/ацетон. Через ~5 минут О3 барботировали через реакционную смесь до исчезновения розовой окраски. Реакционную смесь затем продували газообразным азотом в течение ~5 минут и затем добавляли диметилсульфид (1,231 мл, 16,76 ммоль) одной порцией при помощи шприца. Полученному раствору давали нагреться до комнатной температуры путем удаления бани сухой лед/ацетон и реакционную смесь перемешивали в течение ночи. Через 18 часов ТСХ указывала на расход исходного вещества и преобразование в главный более низкий Rf продукт. Реакционную смесь гасили при помощи H2О (50 мл) и экстрагировали при помощи DCM (3×50 мл). Объединенные органические слои пропускали через фазовый сепаратор и концентрировали с получением бесцветного масла. Неочищенное масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→30% этилацетата в гексане) с получением указанного в заголовке соединения (385,2 мг, 77%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 9,69 (д, J=1,6 Гц, 1H), 7,34-7,21 (м, 4H), 7,00-6,81 (м, 5H), 4,81-4,55 (м, 3H), 4,00 (дд, J=3,9, 1,7 Гц, 1H), 3,80 (с, 3H), 1,36 (д, J=6,3 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 202,57, 159,62, 157,03, 129,86, 129,63, 129,20, 121,50, 116,02, 113,97, 84,11, 74,29, 73,09, 55,29, 15,70; ИК (тонкая пленка) 2934, 2836, 1731, 1513, 1491, 1232, 1087, 1031, 752 см-1; HRMS-ESI (m/z) рассчитано для [C18H24NO4]+, 318,1700; обнаружено, 318,1703.
[00124] Пример 9, Стадия 2: Получение 1-((((2S,3S)-1,1-дифтор-3-феноксибутан-2-ил)окси)метил)-4-метоксибензола.
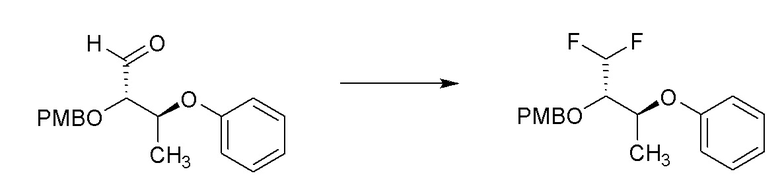
[00125] Раствор (2S,3S)-2-((4-метоксибензил)окси)-3-феноксибутаналя (0,361 г, 1,202 ммоль) получали в DCM (12,02 мл) и охлаждали до 0°C в бане лед/вода. Через ~5 минут добавляли одной порцией Deoxofluor (~50% в толуоле, 2,66 г, 6,01 ммоль), с последующим добавлением 1 капли MeOH. Раствор перемешивали в течение ночи, медленно нагревая до комнатной температуры по мере таяния льда. Через 18 часов ТСХ указывала на расход исходного вещества, и смесь концентрировали с получением оранжевого масла. Неочищенное масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→100% этилацетата в гексане) с получением указанного в заголовке соединения (342,1 мг, 88%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 7,32-7,23 (м, 4H), 7,01-6,94 (м, 1H), 6,92-6,83 (м, 4H), 5,91 (тд, J=55,0, 3,4 Гц, 1H), 4,77 (д, J=11,1 Гц, 1H), 4,69 (д, J=11,1 Гц, 1H), 4,56 (п, J=6,2 Гц, 1H), 3,85-3,74 (м, 4H), 1,37 (д, J=6,3 Гц, 3H); 19F ЯМР (376 МГц, CDCl3) δ -127,71 (дд, J=290,8, 2,1 Гц), -130,30 (дд, J=290,8, 4,0 Гц); ИК (тонкая пленка)2937, 1598, 1514, 1494, 1241, 1074, 1035, 754 см-1.
[00126] Пример 10A: Получение (2R,3S)-1-фенил-3-пропоксибутан-2-ола.
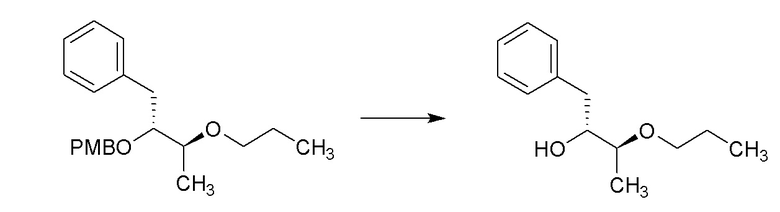
[00127] К смеси 1-метокси-4-((((2R,3,S)-1-фенил-3-пропоксибутан-2-ил)окси)метил)бензола (90 мг, 0,274 ммоль) в DCM (2466 мкл) и воде (274 мкл), перемешиваемой при помощи магнитной мешалки, добавляли DDQ (65,3 мг, 0,288 ммоль) и реакционную смесь перемешивали при 0°C в ледяной бане. Реакционной смеси давали постепенно нагреться до комнатной температуры и перемешивали в течение ночи. Реакционную смесь гасили при помощи NaOH (1N), экстрагировали при помощи DCM (3×). Объединенные органические слои пропускали через фазовый сепаратор и затем концентрировали. Неочищенное вещество очищали при помощи колоночной флэш-хроматографии (SiО2, 0→10% этилацетата в гексане). Продукт элюировали вместе с нежелательным пара- анисальдегидным побочным продуктом. Вещество разбавляли при помощи DCM (2 мл) и добавляли PS-TsNHNH2 (300 мг, твердая подложка) и смесь перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь фильтровали и фильтрат концентрировали с получением указанного в заголовке соединения (51,2 мг, 85%) в виде желтого масла: 1H ЯМР (400 МГц, CDCl3) δ 7,36-7,28 (м, 2H), 7,27-7,19 (м, 3H), 3,92 (дкв., J=8,3, 4,0 Гц, 1H), 3,48 (дт, J=9,1, 6,6 Гц, 1H), 3,42-3,32 (м, 2H), 2,80 (дд, J=13,9, 4,6 Гц, 1H), 2,72 (дд, J=13,9, 8,7 Гц, 1H), 2,01 (д, J=3,5 Гц, 1H), 1,64-1,52 (м, 3H), 1,20 (д, J=6,3 Гц, 3H), 0,92 (т, J=7,4 Гц, 3H); 13C ЯМР (126 МГц, CDCl3) δ 138,74, 129,24, 128,49, 126,32, 77,44, 74,26, 70,62, 38,86, 23,30, 13,98, 10,67; ИК (тонкая пленка) 3441, 2962, 2933, 2875, 1604, 1495, 1453, 1381, 1330, 1253, 1133, 1091, 1031, 984, 745, 699 см-1.
[00128] Пример 10B: Получение (1R,2S)-2-фенокси-1-фенилпропан-1-ола.
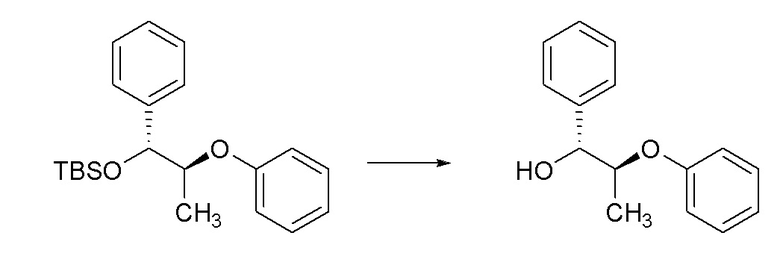
[00129] Раствор трет-бутилдиметил((1R,2S)-2-фенокси-1-фенилпропокси)силана (359,8 мг, 1,050 ммоль) получали в 20 мл емкости в THF (5,25 мл) в атмосфере N2 и охлаждали до 0°C. Через 5 минут добавляли по каплям при помощи шприца TBAF (1,05 мл, 1,050 ммоль) в течение 2 минут. Реакционной смеси давали нагреться до комнатной температуры и перемешивали в течение 4 часов. Реакционную смесь гасили насыщенным водным раствором NH4Cl (25 мл) и экстрагировали при помощи Et2О (3×25 мл). Объединенные органические слои сушили над MgSO4, фильтровали и концентрировали с получением прозрачного бесцветного масла. Масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→30% этилацетата в гексане) с получением указанного в заголовке соединения (96,0 мг, 40%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 7,40 (д, J=7,2 Гц, 2H), 7,34 (т, J=7,5 Гц, 2H), 7,27 (тд, J=7,1, 2,0 Гц, 3H), 7,00-6,88 (м, 3H), 5,02 (т, J=3,3 Гц, 1H), 4,55 (кв.д, J=6,3, 3,5 Гц, 1H), 2,63 (д, J=3,0 Гц, 1H), 1,17 (д, J=6,3 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 157,44, 140,15, 129,65, 128,34, 127,64, 126,39, 121,37, 116,31, 77,93, 75,12, 13,01; ИК (тонкая пленка) 3443, 2985, 1598, 1493, 1239, 1063, 752, 701 см-1.
[00130] Пример 10C: Получение 1-(((2S,3R)-3-(бензилокси)-4-метилпентан-2-ил)окси)-3-хлор-5-фторбензола.
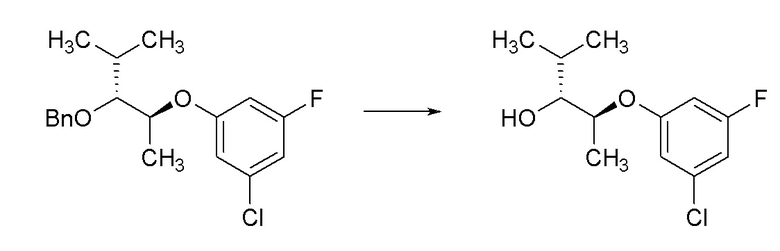
[00131] В небольшом сосуде растворяли 1-(((2S,3R)-3-(бензилокси)-4-метилпентан-2-ил)окси)-3-хлор-5-фторбензол (160,0 мг, 0,475 ммоль) в этаноле (1,58 мл) и циклогексене (0,79 мл). К этому раствору одной порцией добавляли палладий на углероде (5 масс.%, 50,6 мг, 0,024 ммоль) и полученную реакционную смесь нагревали до 70°C и перемешивали в течение ночи. Реакционную смесь охлаждали до комнатной температуры, фильтровали через слой Celite®, элюируя этилацетатом, и концентрировали до масла. Масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→50% ацетон в гексане) с получением указанного в заголовке соединения (114,0 мг, 97%) в виде желтого масла: 1H ЯМР (400 МГц, CDCl3) δ 6,69 (дп, J=4,2, 2,0 Гц, 2H), 6,51 (дт, J=10,5, 2,3 Гц, 1H), 4,40 (кв.д, J=6,2, 4,0 Гц, 1H), 3,52 (дд, J=7,5, 4,0 Гц, 1H), 2,02 (с, 1H), 1,80 (дкв., J=13,7, 6,9 Гц, 1H), 1,30 (д, J=6,2 Гц, 3H), 1,01 (д, J=6,6 Гц, 3H), 0,96 (д, J=6,9 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 163,45 (д, J=248,0 Гц), 159,06 (д, J=12,1 Гц), 135,54 (д, J=13,5 Гц), 112,29 (д, J=3,3 Гц), 108,95 (д, J=25,2 Гц), 102,10 (д, J=24,8 Гц), 77,96, 75,72, 29,85, 18,95, 18,38, 13,13; 19F ЯМР (376 МГц, CDCl3) δ -109,95; ИК (тонкая пленка) 3464, 2963, 1606, 1452, 1140, 1044, 917, 833 см-1.
[00132] Пример 11: Получение (2S,3R)-2-(3-хлор-5-фторфенокси)-4-метилпентан-3-ил(трет-бутоксикарбонил)-1-аланината.
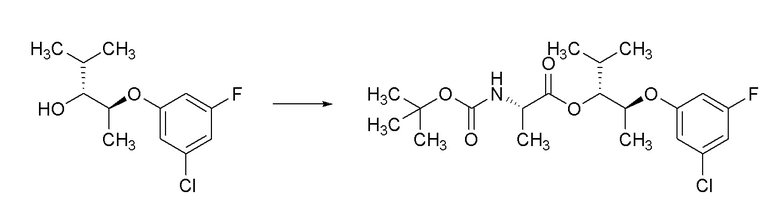
[00133] В небольшом сосуде растворяли (2S,3R)-2-(3-хлор-5-фторфенокси)-4-метилпентан-3-ол (114 мг, 0,462 ммоль), (трет-бутоксикарбонил)-1-аланин (109 мг, 0,578 ммоль) и DMAP (5,65 мг, 0,046 ммоль) в DCM (2,31 мл) в атмосфере N2 и охлаждали до 0°C в бане лед/вода. Через ~5 минут добавляли одной порцией EDCI (143 мг, 0,924 ммоль) и полученную бледно-желтую реакционную смесь перемешивали в течение ночи, медленно нагревая до комнатной температуры по мере таяния льда. Реакционную смесь концентрировали с получением масла. Масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→30% этилацетата в гексане) с получением указанного в заголовке соединения (171,0 мг, 89%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 6,72-6,63 (м, 2H), 6,49 (дт, J=10,5, 2,3 Гц, 1H), 5,04 (д, J=8,1 Гц, 1H), 5,00 (т, J=5,8 Гц, 1H), 4,45 (п, J=6,1 Гц, 1H), 4,35 (п, J=7,5 Гц, 1H), 2,05 (дкв., J=13,5, 6,7 Гц, 1H), 1,46 (с, 9H), 1,43 (д, J=7,2 Гц, 3H), 1,30 (д, J=6,2 Гц, 3H), 0,97 (д, J=6,9 Гц, 3H), 0,91 (д, J=6,7 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 172,97, 163,41 (д, J=248,0 Гц), 159,01 (д, J=12,3 Гц), 155,12, 135,49 (д, J=13,4 Гц), 112,14 (д, J=3,2 Гц), 109,04 (д, J=25,3 Гц), 102,09 (д, J=24,8 Гц), 79,89, 79,28, 73,49, 49,56, 28,78, 28,35, 19,22, 18,65, 17,34, 15,01; 19F ЯМР (376 МГц, CDCl3) δ -110,00; ИК (тонкая пленка) 3373, 2974, 1713, 1605, 1140, 1063 см-1; HRMS-ESI (m/z) рассчитано для [C20H29ClFNNaO5]+, 440,1611; обнаружено, 440,1611.
[00134] Пример 12A: Получение (3R,4S)-2-метил-4-пропоксипентан-3-ил (трет-бутоксикарбонил)-1-аланината.
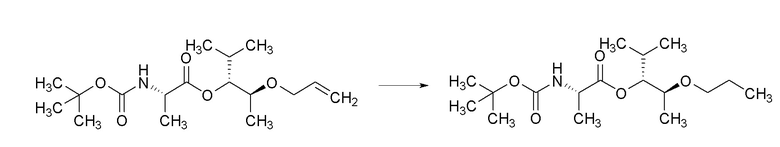
[00135] В емкость, содержащую (2S,3R)-2-(аллилокси)-4-метилпентан-3-ил (трет-бутоксикарбонил)-1-аланинат (0,1 г, 0,304 ммоль) и 5% палладий на углероде (0,097 г, 0,046 ммоль), добавляли EtOAc (1,52 мл) в атмосфере N2. Атмосферу затем заменяли водородом через баллон и реакционную смесь оставляли перемешиваться в течение ночи. Через 20 часов реакционную смесь затем фильтровали через Celite® и промывали при помощи EtOAc. Фильтрат затем концентрировали и неочищенное вещество анализировали при помощи ЯМР для подтверждения полной конверсии. Неочищенное вещество очищали при помощи колоночной флэш-хроматографии (SiО2, 0→20% этилацетата в гексане) с получением указанного в заголовке соединения (92,2 мг, 87%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 5,09 (д, J=7,8 Гц, 1H), 4,85 (т, J=5,9 Гц, 1H), 4,39-4,22 (м, 1H), 3,49 (п, J=6,2 Гц, 1H), 3,46-3,27 (м, 2H), 2,03 (г, J=6,7 Гц, 1H), 1,59-1,48 (м, 2H), 1,44 (с, 9H), 1,41 (д, J=7,2 Гц, 3H), 1,11 (д, J=6,2 Гц, 3H), 0,94-0,86 (м, 9H); 13C ЯМР (126 МГц, CDCl3) δ 172,97, 155,07, 79,86, 79,65, 74,27, 70,63, 49,53, 28,57, 28,33, 23,22, 19,34, 18,98, 17,32, 15,34, 10,66; ИК (тонкая пленка) 3359, 2967, 2936, 2877, 1716, 1502, 1455, 1366, 1340, 1248, 1167, 1107, 1066, 1021 см-1; HRMS-ESI (m/z) рассчитано для [C17H33NO5Na]+, 354,2251; обнаружено, 354,2251.
[00136] Пример 12B: Получение (2S,3R)-2-феноксигексан-3-ил (трет-бутоксикарбонил)-1-аланината.
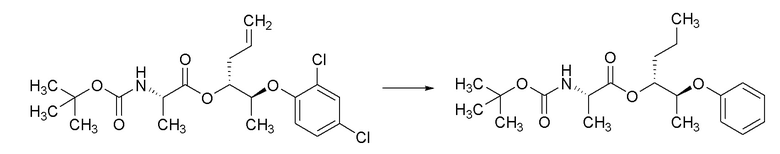
[00137] В 20 мл емкость, содержащую (5)-(2S,3R)-2-(2,4-дихлорфенокси)гекс-5-ен-3-ил 2-((трет-бутоксикарбонил)амино)пропаноат (166,7 мг, 0,386 ммоль) и палладий (5 масс.% на углероде, в расчете на сухое вещество, 82 мг, 0,039 ммоль) добавляли этилацетат (3,86 мл). Черную реакционную смесь продували газообразным H2 через балон. Полученную реакционную смесь перемешивали при комнатной температуре в течение ночи. Через 18 часов ТСХ и ВЭЖХ показывали расход исходного вещества. Реакционную смесь фильтровали через слой целита, элюируя при помощи EtOAc (2×10 мл). Полученный раствор концентрировали с получением желтого масла. Неочищенное вещество очищали при помощи колоночной флэш-хроматографии (SiО2, 0→40% этилацетата в гексане) с получением указанного в заголовке соединения (108,7 мг, 77%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 7,33-7,19 (м, 2H), 7,00-6,91 (м, 1H), 6,91-6,81 (м, 2H), 5,09 (дт, J=8,7, 4,2 Гц, 1H), 5,05-4,91 (м, 1H), 4,45 (кв.д, J=6,3, 4,3 Гц, 1H), 4,29 (т, J=7,6 Гц, 1H), 1,79-1,57 (м, 2H), 1,53-1,16 (м, 2H), 1,45 (с, 9H), 1,36 (д, J=7,2 Гц, 3H), 1,30 (д, J=6,3 Гц, 3H), 0,92 (т, J=7,4 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 172,96, 157,80, 155,05, 129,51, 121,19, 116,26, 115,59, 79,71, 76,45, 74,82, 49,49, 31,85, 28,32, 18,66, 15,64, 13,91; ИК (тонкая пленка) 3368, 2963, 1712, 1493, 1239, 1163, 1057, 752 см-1; HRMS-ESI (m/z) рассчитано для [C20H31NNaO5]+, 388,2097; обнаружено, 388,2077.
[00138] Пример 13A, Стадия 1: Получение (2S,3R)-2-(3-хлор-5-фторфенокси)-4-метилпентан-3-ил 1-аланинат гидрохлорида.
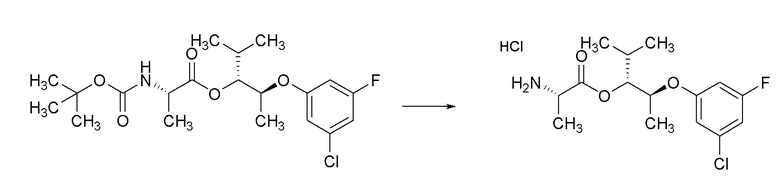
[00139] В небольшом сосуде (2S,3R)-2-(3-хлор-5-фторфенокси)-4-метилпентан-3-ил (трет-бутоксикарбонил)-1-аланинат (171,0 мг, 0,409 ммоль) растворяли в DCM (2 мл). Одной порцией добавляли хлорид водорода (4M раствор в диоксане, 1,534 мл, 6,14 ммоль) при помощи шприца. Полученную прозрачную бесцветную реакционную смесь перемешивали при комнатной температуре в течение 3 часов. Через 3 часа ТСХ показывала полный расход исходного вещества и преобразование в основной продукт. Реакционную смесь концентрировали в потоке N2 и сушили в вакуумной печи с получением указанного в заголовке соединения (145 мг, количественный выход) в виде прозрачного бесцветного масла, которое использовали непосредственно на следующей стадии: ESIMS m/z 318,2 [(M+H)+].
[00140] Пример 13A, Стадия 2: Получение (2S,3R)-2-(3-хлор-5-фторфенокси)-4-метилпентан-3-ил (3-гидрокси-4-метоксипиколиноил)-1-аланината.
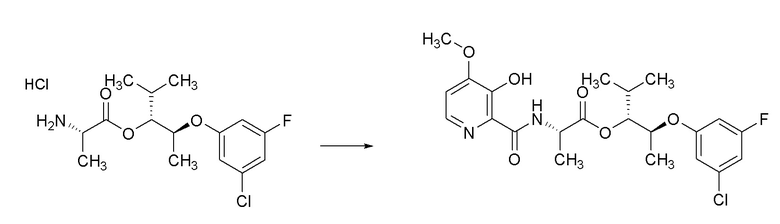
[00141] В емкость, содержащую (2S,3R)-2-(3-хлор-5-фторфенокси)-4-метилпентан-3-ил 1-аланинат гидрохлорид (145 мг, 0,409 ммоль), добавляли 3-гидрокси-4-метоксипиколиновую кислоту (90 мг, 0,532 ммоль) и ((1H-бензо[d][1,2,3]триазол-1-ил)окси)три(пирролидин-1-ил)фосфоний гексафторфосфат(V) (277 мг, 0,532 ммоль). Добавляли DCM (8,18 мл) с последующим добавлением по каплям N-этил-N-изопропилпропан-2-амина (428 мкл, 2,454 ммоль) в течение 45 секунд. Через 10 минут бóльшая часть твердых веществ растворялась, и полученную бледно-розовую реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь затем концентрировали при пониженном давлении с получением оранжевого масла. Масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→50% ацетон в гексане) с получением указанного в заголовке соединения (174,9 мг, 91% за две стадии) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 12,11 (с, 1H), 8,49 (д, J=7,9 Гц, 1H), 7,99 (д, J=5,2 Гц, 1H), 6,88 (д, J=5,2 Гц, 1H), 6,74-6,59 (м, 2H), 6,48 (дт, J=10,5, 2,3 Гц, 1H), 5,04 (т, J=5,8 Гц, 1H), 4,77 (п, J=7,3 Гц, 1H), 4,47 (п, J=6,1 Гц, 1H), 3,95 (с, 3H), 2,07 (дкв., J=13,4, 6,7 Гц, 1H), 1,61 (д, J=7,2 Гц, 3H), 1,30 (д, J=6,2 Гц, 3H), 0,98 (д, J=6,9 Гц, 3H), 0,92 (д, J=6,7 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 171,71, 168,87, 163,40 (д, J=248,1 Гц), 158,95 (д, J=12,2 Гц), 155,44, 148,84, 140,54, 135,51 (д, J=13,5 Гц), 130,46, 112,15 (д, J=3,2 Гц), 109,55, 109,10 (д, J=25,2 Гц), 102,06 (д, J=24,7 Гц), 79,77, 73,50, 56,09, 48,11, 28,76, 19,26, 18,31, 17,30, 15,05; 19F ЯМР (376 МГц, CDCl3) δ -109,89; ИК (тонкая пленка) 3370, 2968, 1743, 1605, 1527, 1438, 1139, 730 см-1; HRMS-ESI (m/z) рассчитано для [C22H27ClFN2O6]+, 469,1536; обнаружено, 469,1531.
[00142] Пример 13B, Стадия 1: Получение (3R,4S)-2-метил-4-((2-метилаллил)окси)пентан-3-ил 1-аланината.
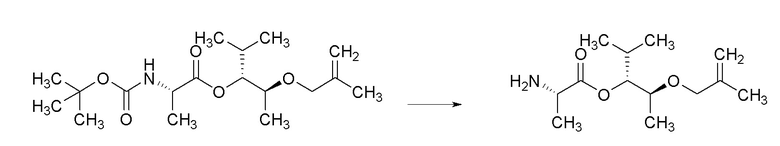
[00143] (3R,4S)-2-метил-4-((2-метилаллил)окси)пентан-3-ил (трет-бутоксикарбонил)-1-аланинат (0,155 г, 0,451 ммоль) растворяли в DCM (2,26 мл) и охлаждали до 0°C в ледяной бане. Через ~5 минут добавляли по каплям при помощи шприца TFA (0,522 мл, 6,77 ммоль) в течение 30 секунд. Реакционную смесь нагревали до комнатной температуры путем удаления ледяной водяной бани бани и давали перемешаться при комнатной температуре в течение 2 часов. Через 2 часа ТСХ указывала на расход исходного вещества. Реакционную смесь разбавляли при помощи DCM и промывали насыщенным водным раствором NaHСО3. Водный слой экстрагировали при помощи DCM (3×). Объединенные органические слои пропускали через фазовый сепаратор и концентрировали с получением неочищенного указанного в заголовке соединения в виде густого масла, которое использовали непосредственно на следующей стадии без дополнительной очистки: ИК (тонкая пленка) 3361, 2969, 1735, 1677, 1456, 1374, 1179, 1126, 1101, 907, 721 см-1; HRMS-ESI (m/z) рассчитано для [C13H26NO3]+, 244,1907; обнаружено, 244,1910.
[00144] Пример 13B, Стадия 2: Получение (3R,4S)-2-метил-4-((2-метилаллил)окси)пентан-3-ил (3-гидрокси-4-метоксипиколиноил)-1-аланината.
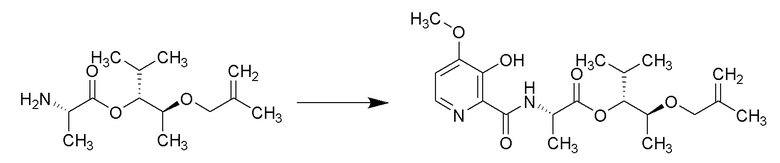
[00145] Неочищенный (3R,4S)-2-метил-4-((2-метилаллил)окси)пентан-3-ил 1-аланинат растворяли в безводном DCM (4,4 мл). Добавляли 3-гидрокси-4-метоксипиколиновую кислоту (0,084 г, 0,496 ммоль), PyBOP (0,258 г, 0,496 ммоль) и этил-N-изопропилпропан-2-амин (0,260 мл, 1,489 ммоль). Реакционную смесь затем перемешивали при комнатной температуре в течение 2 часов. Через 2 часа вещество концентрировали до масла. Масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→30% ацетона в гексане) с получением указанного в заголовке соединения (74,4 мг, 42% за 2 стадии) в виде густого бесцветного масла: 1H ЯМР (500 МГц, CDCl3) δ 12,18 (с, 1H), 8,54 (д, J=7,8 Гц, 1H), 7,99 (д, J=5,2 Гц, 1H), 6,87 (д, J=5,2 Гц, 1H), 4,96-4,91 (м, 2H), 4,88-,83 (м, 1H), 4,80-4,71 (м, 1H), 3,95 (с, 3H), 3,92 (д, J=12,4 Гц, 1H), 3,85 (д, J=12,3 Гц, 1H), 3,62-3,56 (м, 1H), 2,04 (дкв., J=13,4, 6,8 Гц, 1H), 1,72 (т, J=1,1 Гц, 3H), 1,60-1,57 (м, 3H), 1,14 (д, J=6,3 Гц, 3H), 0,92 (д, J=3,5 Гц, 3H), 0,91 (д, J=3,7 Гц, 3H); 13C ЯМР (126 МГц, CDCl3) δ 171,83, 168,69, 155,34, 148,73, 142,32, 140,46, 130,54, 112,11, 109,40, 80,21, 73,54, 72,68, 56,07, 48,13, 28,62, 19,59, 19,34, 18,53, 17,56, 15,09; ИК (тонкая пленка) 3370, 2968, 2939, 1739, 1649, 1576, 1527, 1481, 1438, 1366, 1330, 1280, 1263, 1212, 1182, 1150, 1101, 1060, 943, 849, 800 см-1; ESIMS m/z 395,3 [(M+H)+].
[00146] Пример 14A: Получение (3R,4S)-2-метил-4-феноксипентан-3-ил (3-ацетокси-4-метоксипиколиноил)-1-аланината.
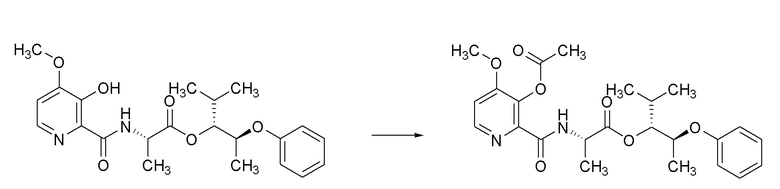
[00147] В небольшую емкость, содержащую (3R,4S)-2-метил-4-феноксипентан-3-ил (3-гидрокси-4-метоксипиколиноил)-1-аланинат (83,8 мг, 0,201 ммоль), добавляли пиридин (0,976 мл, 12,1 ммоль) с последующим добавлением уксусного ангидрида (0,951 мл, 10,1 ммоль) при помощи шприца. Полученную прозрачную и бесцветную реакционную смесь перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь концентрировали, разбавляли 5 мл толуола и повторно концентрировали с получением масла. Масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→50% ацетон в гексане) с получением указанного в заголовке соединения (78,1 мг, 85%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 8,57 (д, J=6,9 Гц, 1H), 8,32 (д, J=5,4 Гц, 1H), 7,30-7,21 (м, 2H), 7,00 (д, J=5,5 Гц, 1H), 6,93 (тт, J=7,3, 1,0 Гц, 1H), 6,90-6,80 (м, 2H), 5,06 (дд, J=6,3, 5,3 Гц, 1H), 4,76 (п, J=7,3 Гц, 1H), 4,50 (п, J=6,2 Гц, 1H), 3,90 (с, 3H), 2,40 (с, 3H), 2,16-2,09 (м, 1H), 1,56 (д, J=7,1 Гц, 3H), 1,28 (д, J=6,2 Гц, 3H), 0,96 (д, J=6,9 Гц, 3H), 0,91 (д, J=6,8 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 172,24, 168,88, 162,49, 159,50, 157,43, 146,68, 141,58, 137,55, 129,53, 121,09, 115,92, 109,79, 80,11, 72,60, 56,29, 48,28, 28,71, 20,73, 19,37, 18,72, 17,01, 15,52; ИК (тонкая пленка) 3383, 2967, 1771, 1677, 1507, 1198, 1174 см-1; HRMS-ESI (m/z) рассчитано для [C24H31N2O7]+, 459,2126; обнаружено, 459,2096.
[00148] Пример 14B: Получение (3R,4S)-2-метил-4-феноксипентан-3-ил (3-(ацетоксиметокси)-4-метоксипиколиноил)-1-аланината.
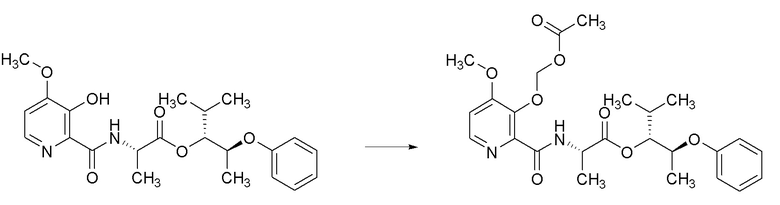
[00147] В небольшом сосуде растворяли (S)-(3R,4S)-2-метил-4-феноксипентан-3-ил 2-(3-гидрокси-4-метоксипиколинамидо)пропаноат (81,9 мг, 0,197 ммоль) в ацетоне (1,5 мл). К этому раствору добавляли карбонат калия (54,4 мг, 0,393 ммоль) одной порцией, после этого бромметилацетат (0,039 мл, 0,393 ммоль) одной порцией при помощи шприца. Полученный мутный белый раствор перемешивали при 50°C в течение 2 часов. Через 2 часа ТСХ показывала полный расход исходного вещества. Реакционную смесь затем концентрировали до белого масла в потоке N2. Масло очищали при помощи колоночной флэш-хроматографии (SiО2, 0→50% ацетона в гексане) с получением указанного в заголовке соединения (77,4 мг, 81%) в виде прозрачного бесцветного масла: 1H ЯМР (400 МГц, CDCl3) δ 8,40 (д, J=7,7 Гц, 1H), 8,28 (д, J=5,3 Гц, 1H), 7,31-7,20 (м, 2H), 6,99-6,84 (м, 4H), 5,80-5,71 (м, 2H), 5,07 (дд, J=6,4, 5,1 Гц, 1H), 4,80 (п, J=7,2 Гц, 1H), 4,50 (п, J=6,2 Гц, 1H), 3,91 (с, 3H), 2,21-2,09 (м, 1H), 2,07 (с, 3H), 1,58 (д, J=7,1 Гц, 3H), 1,30 (д, J=6,2 Гц, 3H), 0,97 (д, J=6,9 Гц, 3H), 0,92 (д, J=6,8 Гц, 3H); 13C ЯМР (101 МГц, CDCl3) δ 172,39, 170,27, 163,07, 160,32, 157,45, 145,73, 144,05, 142,58, 129,56, 121,11, 115,93, 109,61, 89,62, 80,12, 72,63, 56,20, 48,43, 28,72, 20,88, 19,42, 18,69, 16,98, 15,63; ИК (тонкая пленка) 3389, 2968, 1753, 1678, 1496, 1239, 1203, 1004 см-1; HRMS-ESI (m/z) рассчитано для [C25H33N2O8]+, 489,2231; обнаружено, 489,2212.
[00148] Пример A: Оценка фунгицидной активности: Пятнистость листьев пшеницы (Zymoseptoria tritici; Bayer код SEPTTR):
[00149] Технические сорта веществ растворяли в ацетоне, который затем смешивали с девятью объемами воды (H2О), содержащей 110 ч/млн Triton X-100. Фунгицидные растворы наносили на проростки пшеницы, используя автоматизированную камеру-распылитель. Все опрысканные растения подвергали сушке на воздухе до дальнейшей обработки. Все фунгициды оценивали с использованием вышеуказанного способа на их активность против всех целевых заболеваний, если не указано иное. Активность против пятнистости листьев пшеницы и бурой ржавчины также оценивали с использованием нанесения распыления по бороздам, в этом случае фунгициды формулировали как EC композиции, содержащие 0,1% Trycol 5941, в виде растворов для распыления.
[00150] Растения пшеницы (сорт Юма) выращивали из семян в теплице, в почвосмеси, состоящей из 50% минерализованной почвы Metro mix/50% почвы без Metro mix, до тех пор, пока полностью не появлялся первый лист, при 7-10 проростков на горшочек. Такие растения инокулировали водной суспензией спор грибка Zymoseptoria tritici либо перед обработкой фунгицидами, либо после нее. После инокуляции растения выдерживали при 100% относительной влажности (один день в темноте в орошаемой камере, с последующими двумя-тремя днями в освещенной орошаемой камере при 20°C), давая возможность спорам прорасти и инфицировать листья. Затем растения переносили в теплицу с установленной температурой 20°C для развития болезни. Когда симптомы болезни были полностью выражены на первых листьях необработанных растений, уровни инфекции оценивали по шкале от 0 до 100 процентов тяжести заболевания. Процент контроля заболевания рассчитывали с использованием отношения тяжести заболевания на обработанных растениях относительно необработанных растений.
[00151] Пример B: Оценка фунгицидной активности: Бурая ржавчина пшеницы (Puccinia triticina; Bayer код PUCCRT):
[00152] Растения пшеницы (сорт Юма) выращивали из семян в теплице, в почвосмеси, состоящей из 50% минерализованной почвы Metro mix/50% почвы без Metro mix, до тех пор, пока полностью не появлялся первый лист, при 7-10 проростков на горшочек. Такие растения инокулировали водной суспензией спор грибка Puccinia triticina либо перед обработкой фунгицидами, либо после нее. После инокуляции растения выдерживали в темной орошаемой камере при 22°C при 100% относительной влажности в течение ночи, давая возможность спорам прорасти и инфицировать листья. Затем растения переносили в теплицу с установленной температурой 24°C для развития болезни. Формулирование фунгицида, нанесение и оценку заболевания осуществляли следуя процедурам, описанным в Примере A.
[00153] Пример C: Оценка фунгицидной активности: Септориоз колоса пшеницы (Leptosphaeria nodorum; Bayer код LEPTNO):
[00154] Растения пшеницы (сорт Юма) выращивали из семян в теплице, в почвосмеси, состоящей из 50% минерализованной почвы Metro mix/50% почвы без Metro mix, до тех пор, пока полностью не появлялся первый лист, при 7-10 проростков на горшочек. Такие растения инокулировали водной суспензией спор грибка Leptosphaeria nodorum через 24 часа после обработки фунгицидами. После инокуляции растения выдерживали при 100% относительной влажности (один день в темноте в орошаемой камере, затем два дня в освещенной орошаемой камере при 20°C), давая возможность спорам прорасти и инфицировать листья. Затем растения переносили в теплицу с установленной температурой 20°C для развития болезни. Формулирование фунгицида, нанесение и оценку заболевания осуществляли следуя процедурам, описанным в Примере A.
[00155] Пример D: Оценка фунгицидной активности: парша яблок (Venturia inaequalis; Bayer код VENTIN):
[00156] Ростки яблонь (сорт Mcintosh) выращивали в почве без смеси Metro mix, с одним растением на горшочек. Проростки с двумя расширяющимися молодыми листьями наверху (старые листья внизу растений обрезали) использовали в испытании. Растения инокулировали суспензией спор грибка Venturia inaequalis через 24 часа после обработки фунгицидами и выдерживали при 22°C в темной орошаемой камере при 100% относительной влажности в течение 48 часов и затем переносили в теплицу с установленной температурой 20°C для развития болезни. Формулирование фунгицида, нанесение и оценку заболевания на опрысканных листьях осуществляли следуя процедурам, описанным в Примере A.
[00157] Пример E: Оценка фунгицидной активности: Пятнистость листьев сахарной свеклы (Cercospora beticola; Bayer код CERCBE):
[00158] Сахарную свеклу (сорт HH-88) выращивали в почве без смеси Metro mix и регулярно обрезали для поддержания одинакового размера растения перед испытанием. Растения инокулировали суспензией спор через 24 часа после обработки фунгицидами. Инокулированные растения выдерживали при 22°C в темной орошаемой камере в течение 48 часов, затем инкубировали в теплице с установленной температурой 24°C под прозрачным пластиковым колпаком с вентиляцией снизу до тех пор, пока симптомы болезни не были полностью выражены. Формулирование фунгицида, нанесение и оценку заболевания на опрысканных листьях осуществляли следуя процедурам, описанным в Примере A.
[00159] Пример F: Оценка фунгицидной активности: Азиатская ржавчина сои (Phakopsora pachyrhizi; Bayer код PHAKPA):
[00160] Технические сорта веществ растворяли в ацетоне, который затем смешивали с девятью объемами H2О, содержащей 0,011% Tween 20. Фунгицидные растворы наносили на проростки соевых бобов, используя автоматизированную камеру-распылитель. Все опрысканные растения подвергали сушке на воздухе до дальнейшей обработки.
[00161] Соевые растения (сорт Williams 82) выращивали в почве без смеси Metro mix, с одним растением на горшочек. Двухнедельные проростки использовали для исследования. Растения инокулировали либо за 3 дня до, либо через 1 день после обработки фунгицидами. Растения инкубировали в течение 24 часов в темной орошаемой камере при 22°C и 100% относительной влажности и затем переносили в теплицу с установленной температурой 23°C для развития болезни. Тяжесть заболевания оценивали на опрысканных листьях.
[00162] Пример G: Оценка фунгицидной активности: Ринхоспориоз ячменя (Rhyncosporium secalis; код Bayer RHYNSE):
[00163] Ростки ячменя (сорт Harrington) размножали в почве без смеси Metro mix, с 8-12 растениями в каждом горшочке, и использовали в испытании, когда полностью появился первый лист. Испытываемые растения инокулировали водной суспензией спор Rhyncosporium secalis через 24 часа после обработки фунгицидами. После инокуляции растения выдерживали при 22°C в темной орошаемой камере при 100% относительной влажности в течение 48 часов. Затем растения переносили в теплицу с установленной температурой 20°C для развития болезни. Формулирование фунгицида, нанесение и оценку заболевания на опрысканных листьях осуществляли следуя процедурам, описанным в Примере A.
[00164] Пример H: Оценка фунгицидной активности: Пирикуляриоз риса (Pyricularia oryzae; Bayer код PYRIOR):
[00165] Проростки риса (сорт Japonica) размножали в почве без смеси Metro mix, с 8-14 растениями в каждом горшочке, и использовали в испытании на 12-14 день. Испытываемые растения инокулировали водной суспензией спор Pyricularia oryzae через 24 часа после обработки фунгицидами. После инокуляции растения выдерживали при 22°C в темной орошаемой камере при 100% относительной влажности в течение 48 часов, давая возможность спорам прорасти и инфицировать листья. Затем растения переносили в теплицу с установленной температурой 24°C для развития болезни. Формулирование фунгицида, нанесение и оценку заболевания на опрысканных листьях осуществляли следуя процедурам, описанным в Примере A.
[00166] Пример I: Оценка фунгицидной активности: Альтернариоз томатов (Alternaria solani; Bayer код ALTESO):
[00167] Растения томатов (сорт Outdoor Girl) размножали в почве без смеси Metro mix, с одним растением в каждом горшочке, и использовали на 12-14 день. Испытываемые растения инокулировали водной суспензией спор Alternaria solani через 24 часа после обработки фунгицидами. После инокуляции растения выдерживали при 22°C при 100% относительной влажности в течение 48 часов, давая возможность спорам прорасти и инфицировать листья. Растения затем переносили в теплицу с установленной температурой 22°C для развития болезни. Формулирование фунгицида, нанесение и оценку заболевания на опрысканных листьях осуществляли следуя процедурам, описанным в Примере A.
[00168] Пример J: Оценка фунгицидной активности: Огуречный антракноз (Colletotrichum lagenarium; Bayer код COLLLA):
[00169] Ростки огурца (сорт Bush Pickle) размножали в почве без смеси Metro mix, с одним растением в каждом горшочке, и использовали в испытании на 12-14 день. Испытываемые растения инокулировали водной суспензией спор Colletotrichum lagenarium через 24 часа после обработки фунгицидами. После инокуляции растения помещали в темную орошаемую камеру при 22°C при 100% относительной влажности на 48 часов, давая возможность спорам прорасти и инфицировать листья. Растения затем переносили в теплицу с установленной температурой 22°C для развития болезни. Формулирование фунгицида, нанесение и оценку заболевания на опрысканных листьях осуществляли, следуя процедурам, описанным в Примере A.
Структура соединения, способ получения и физические свойства
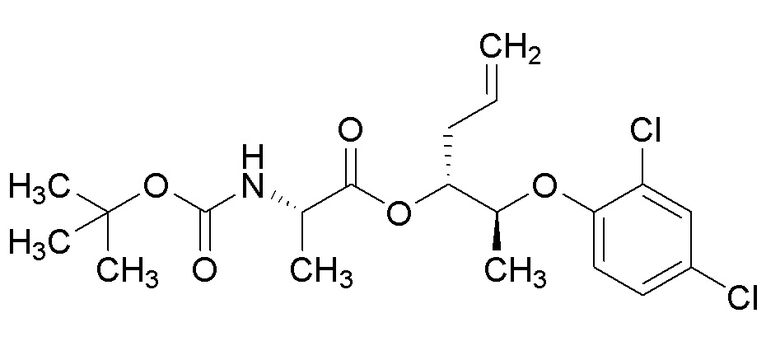
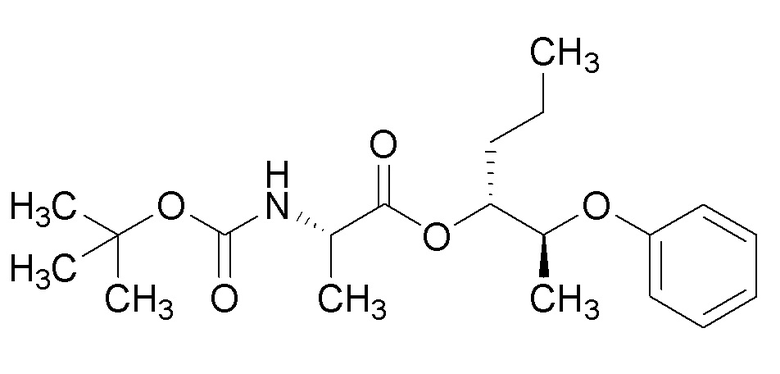
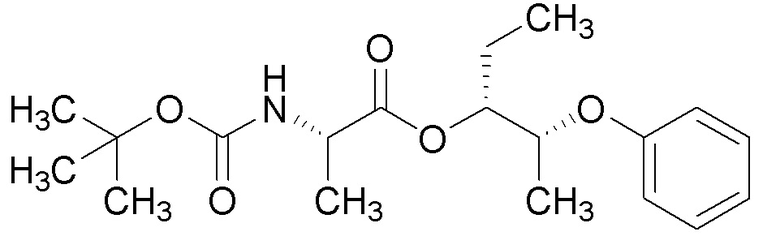
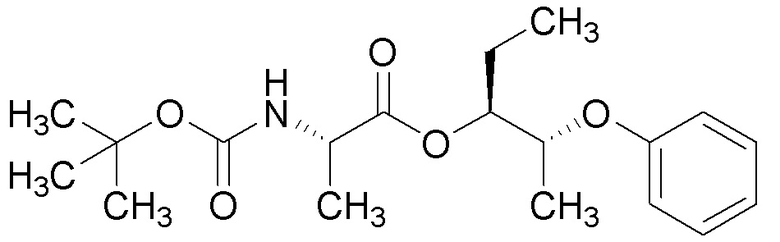
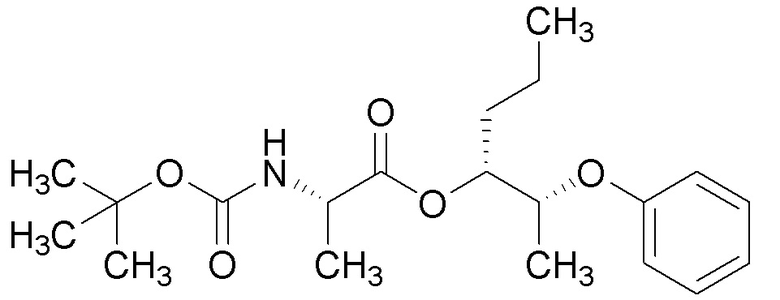
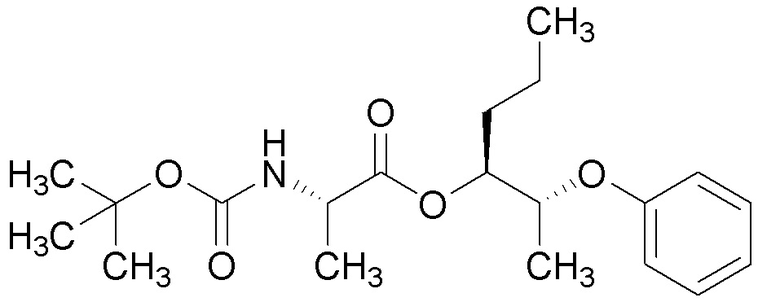
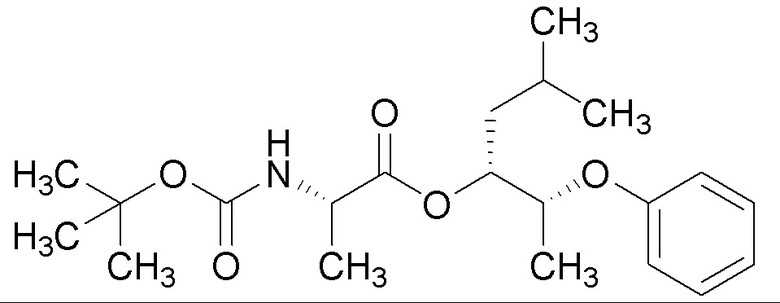
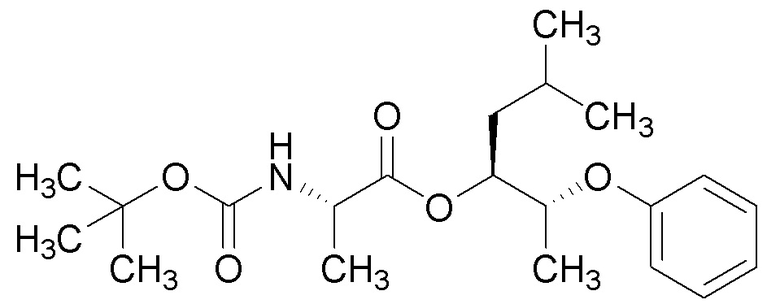
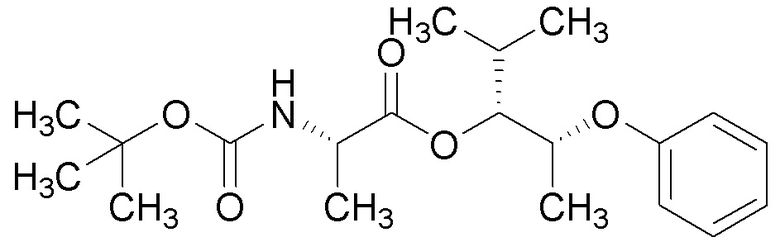
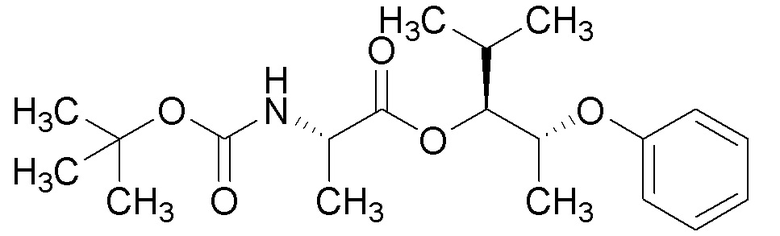
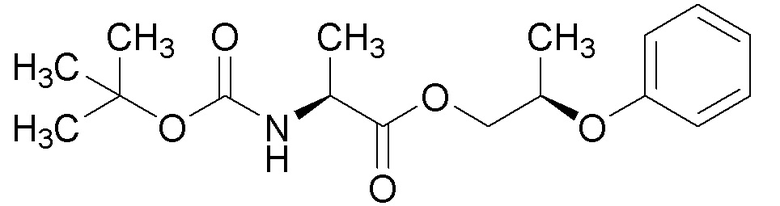
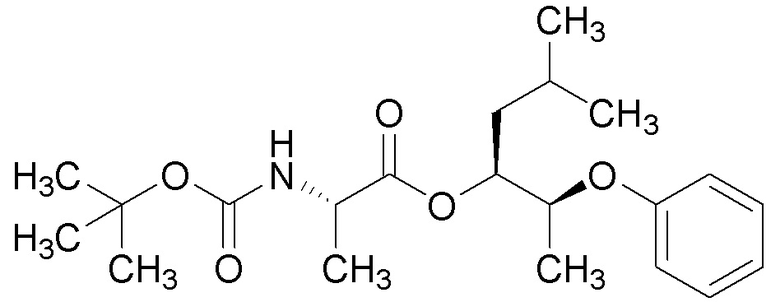
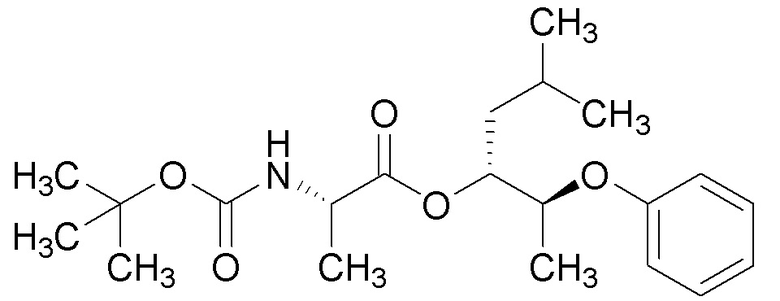
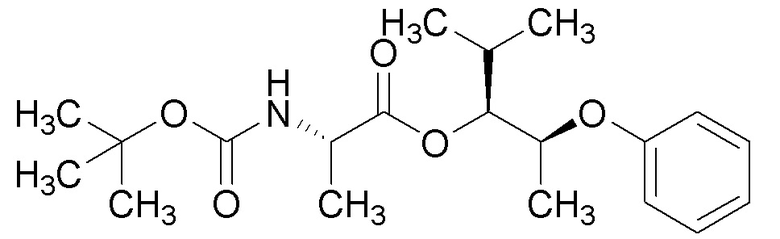
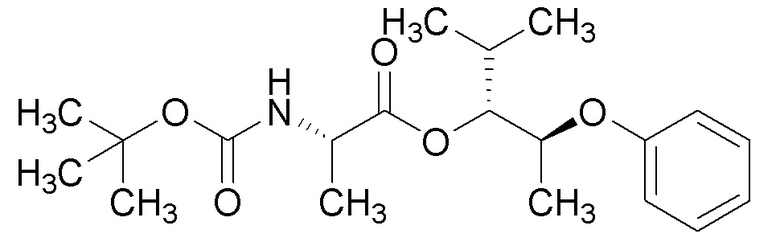
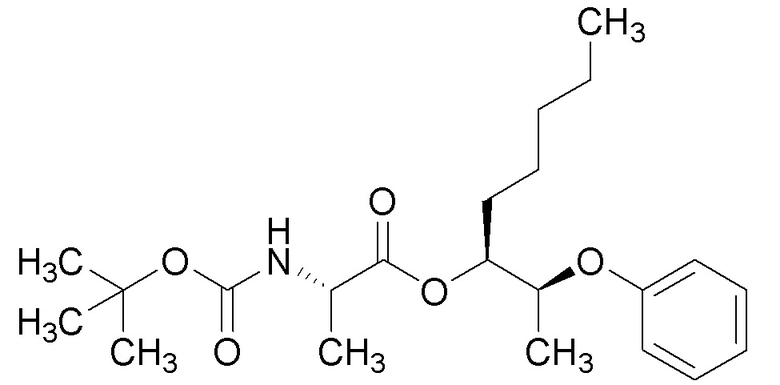
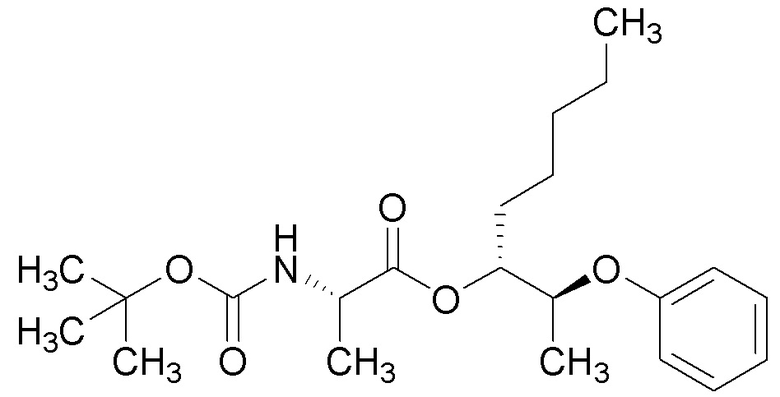
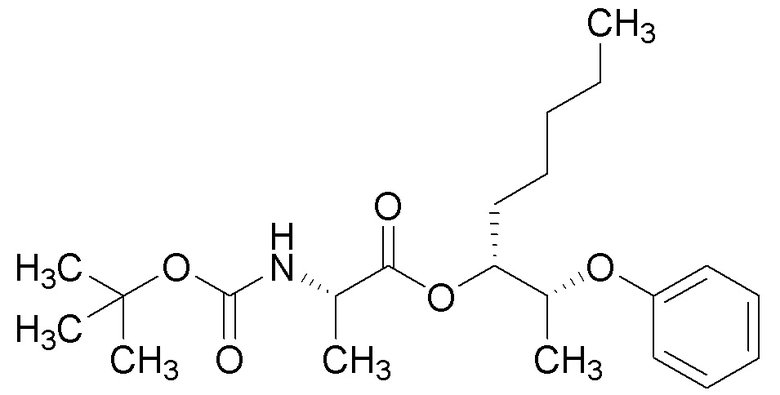
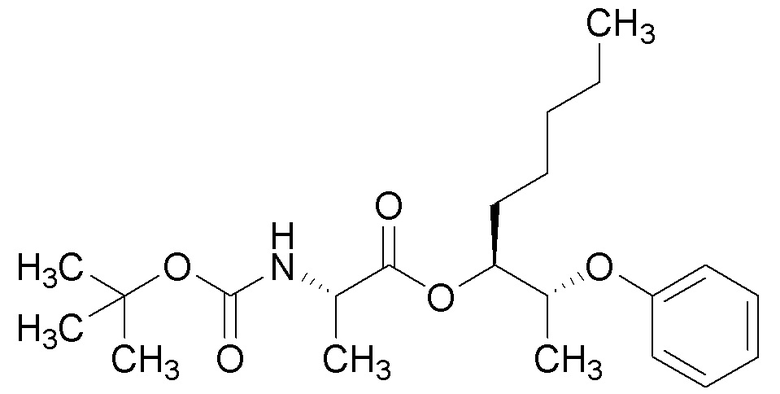
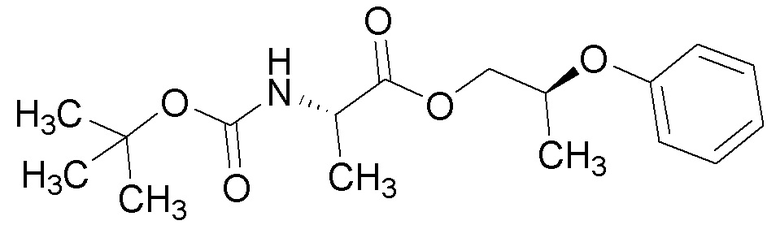
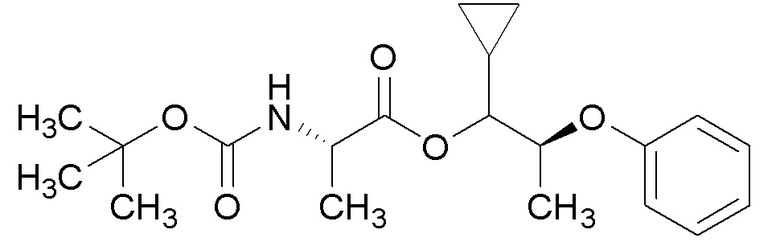
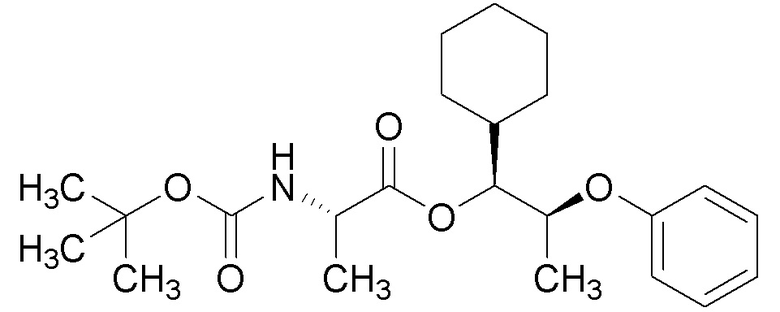
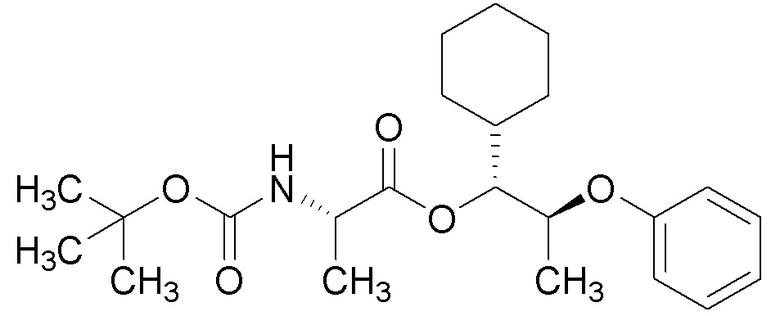
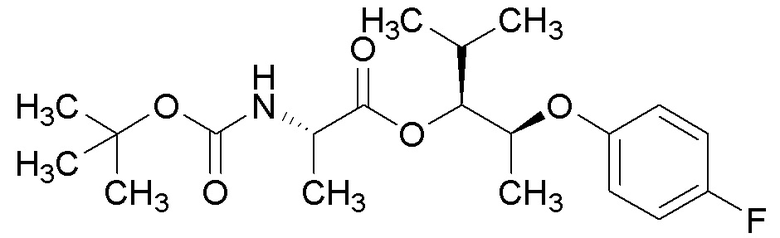
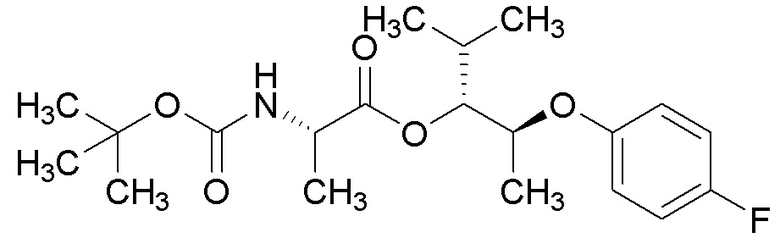
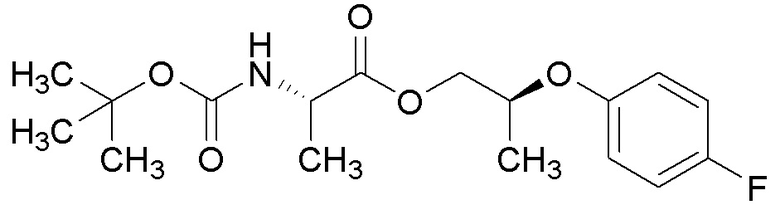
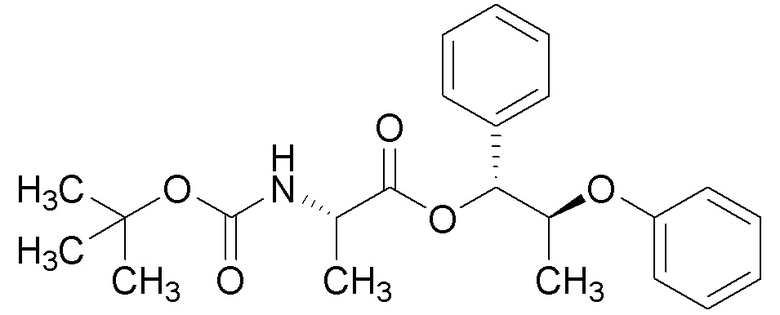
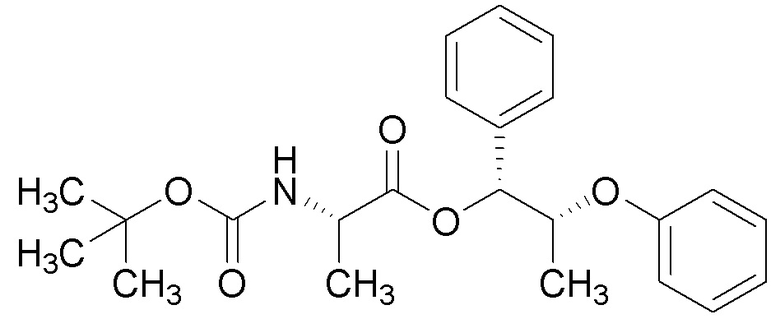
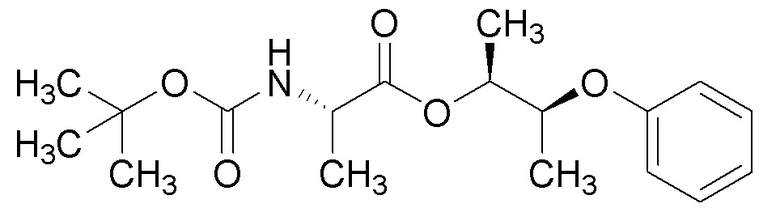
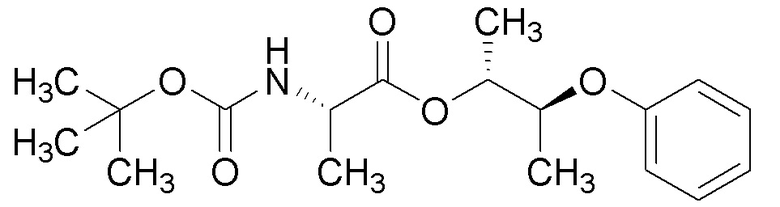
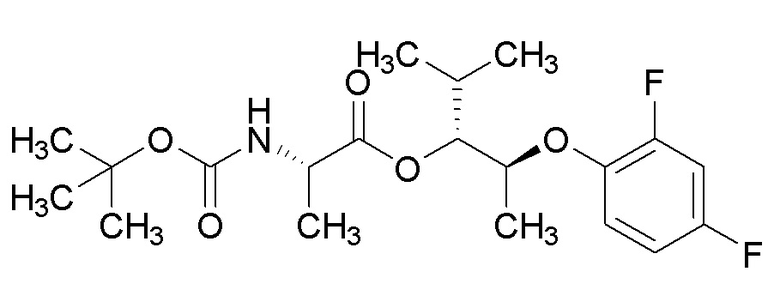
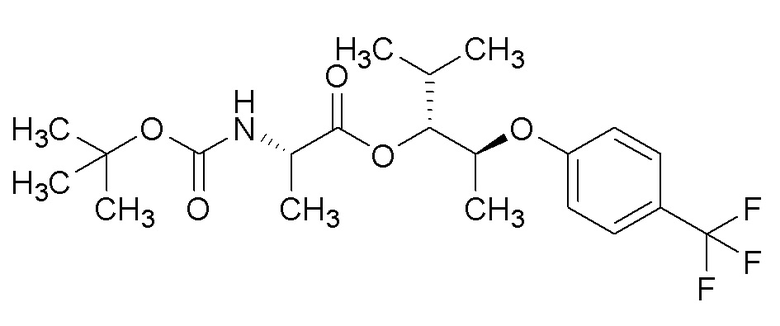
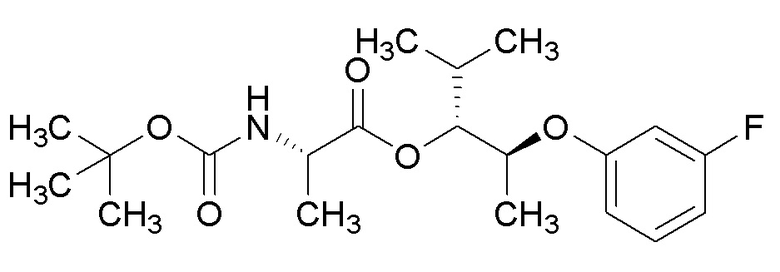
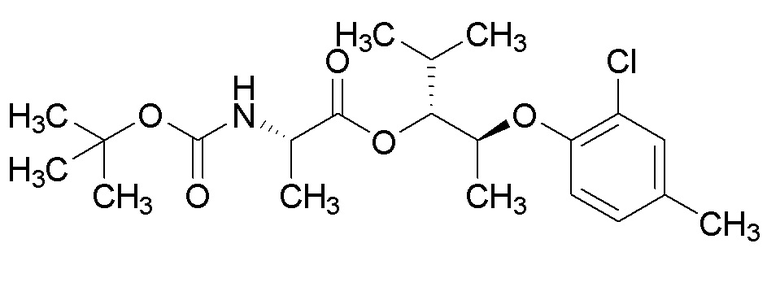
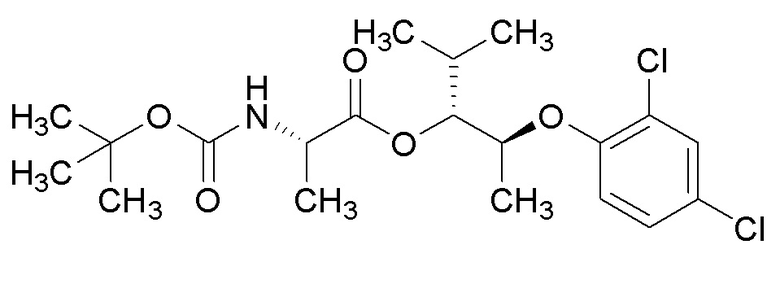
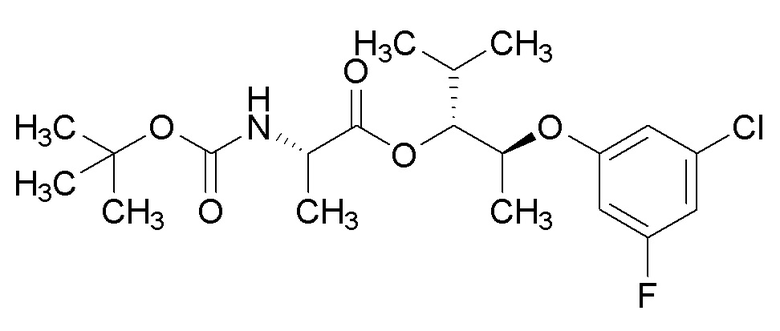
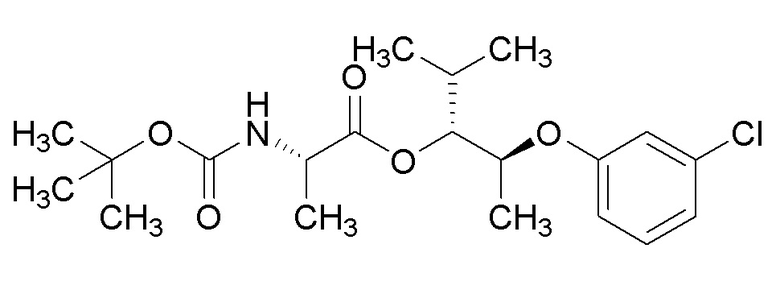
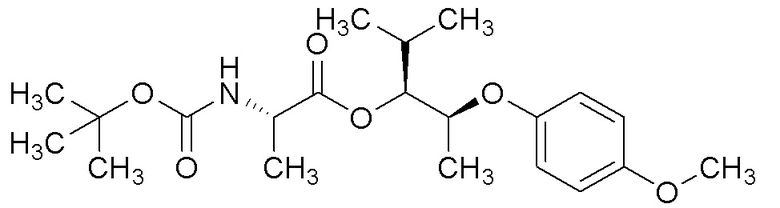
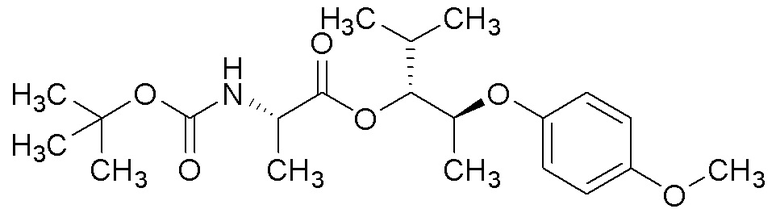
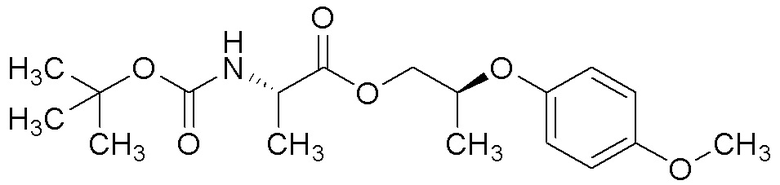
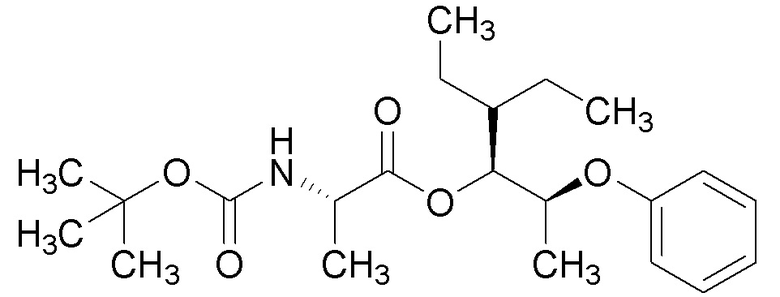
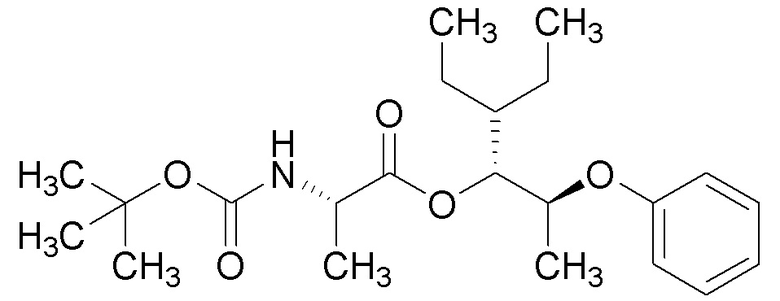
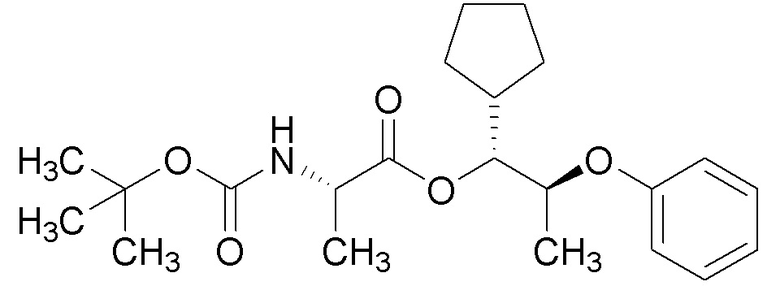
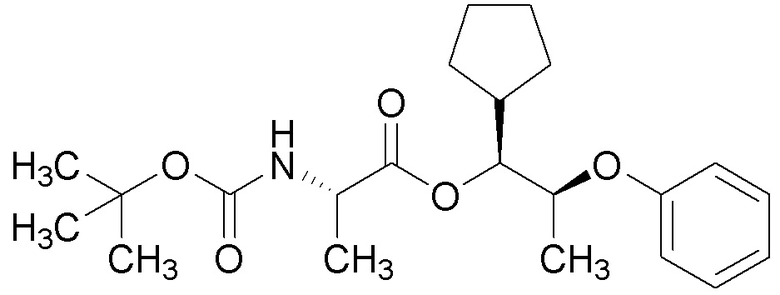
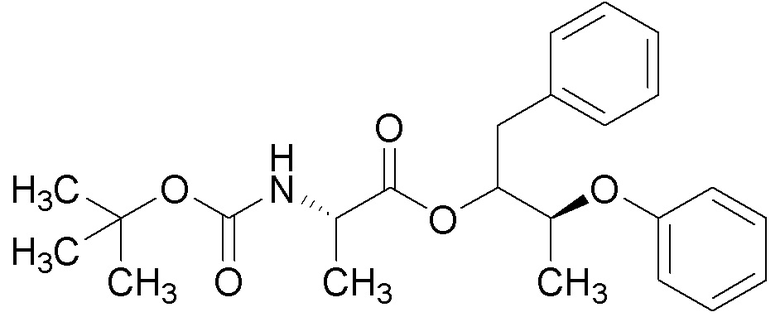
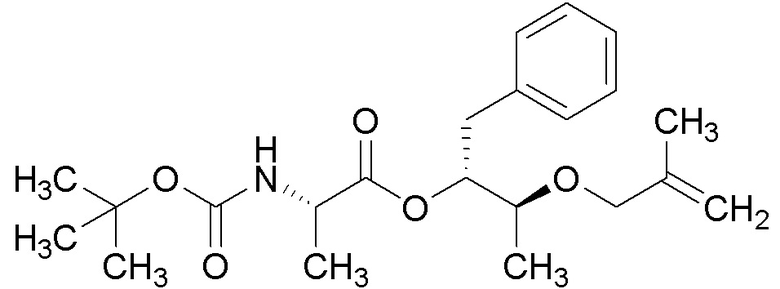
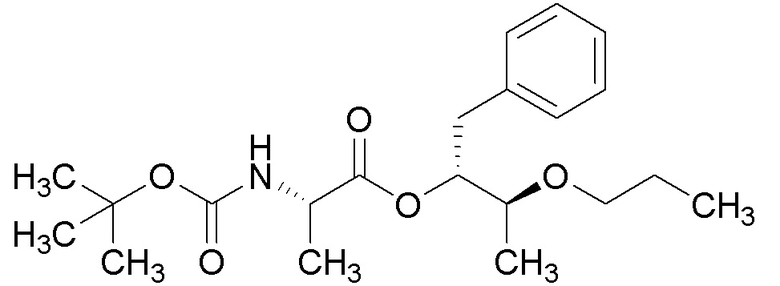
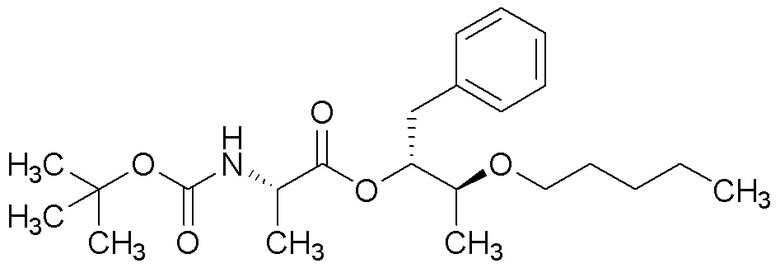
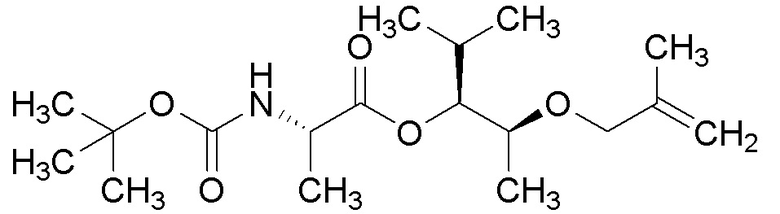
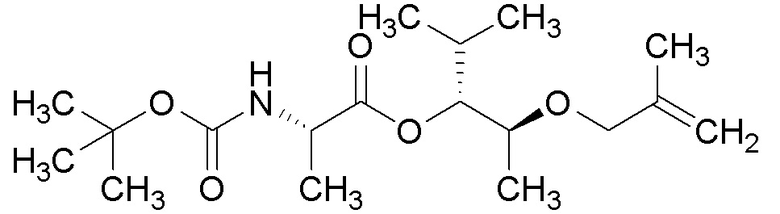
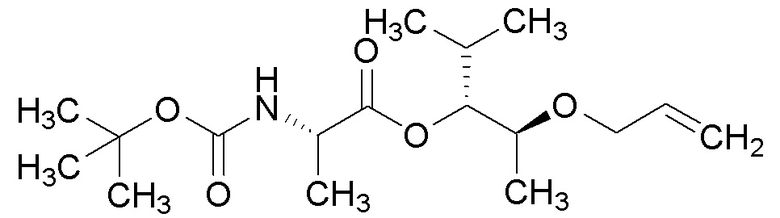
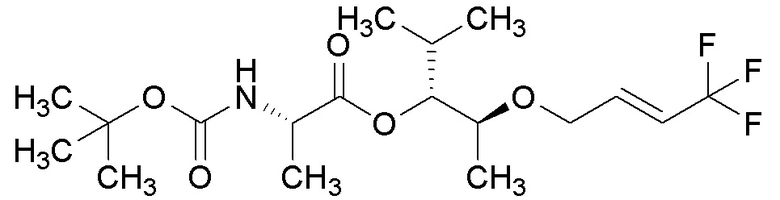
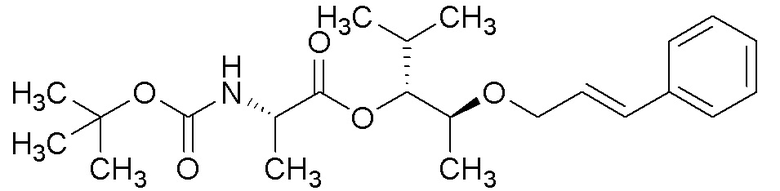
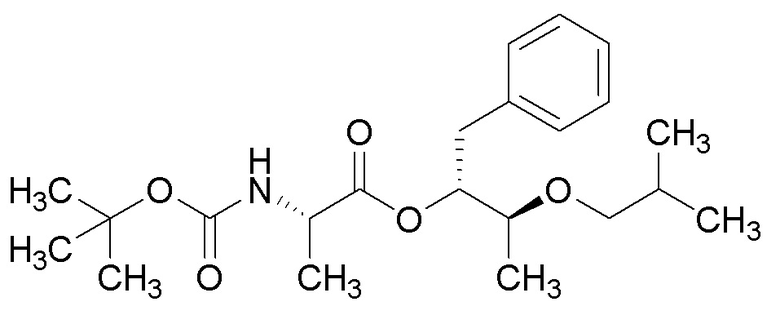
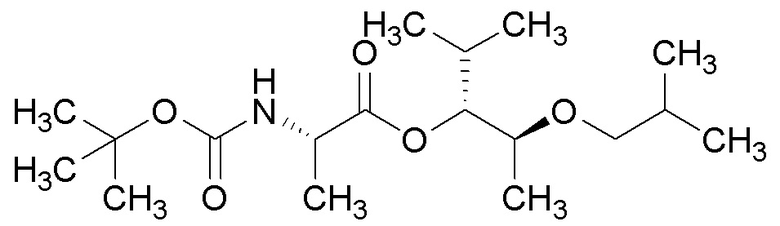
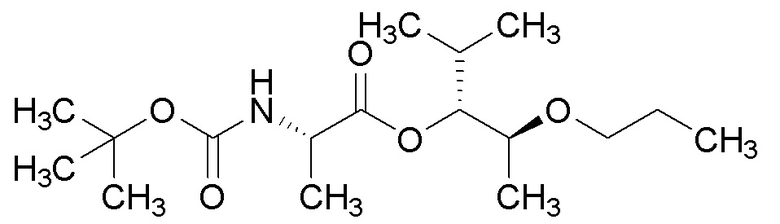
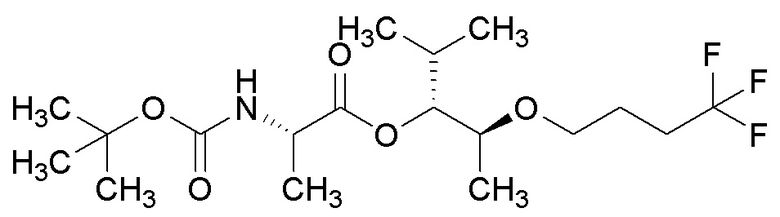
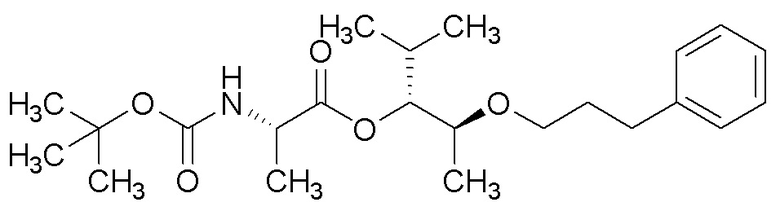
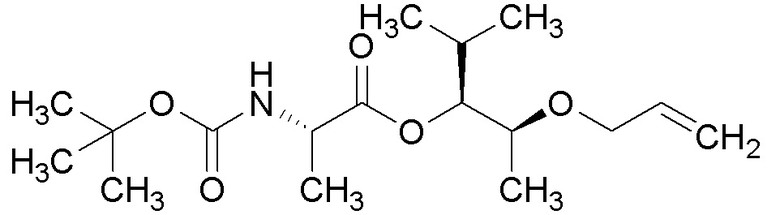
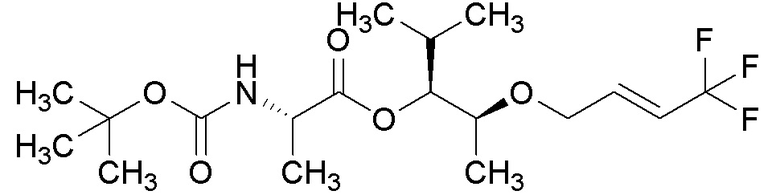
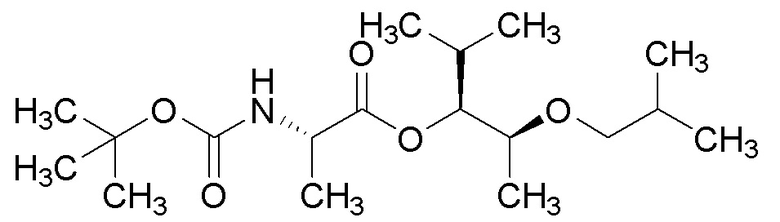
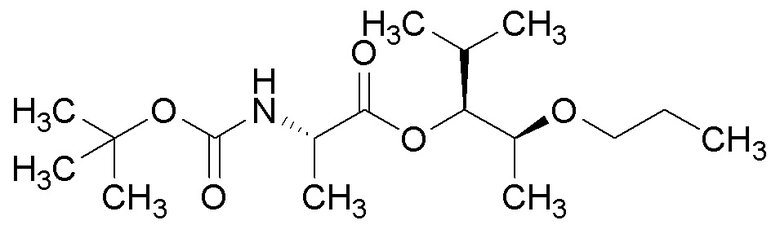
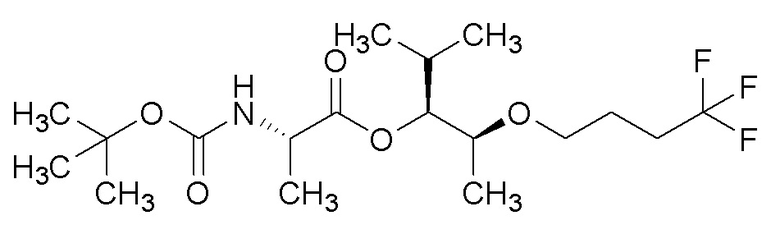
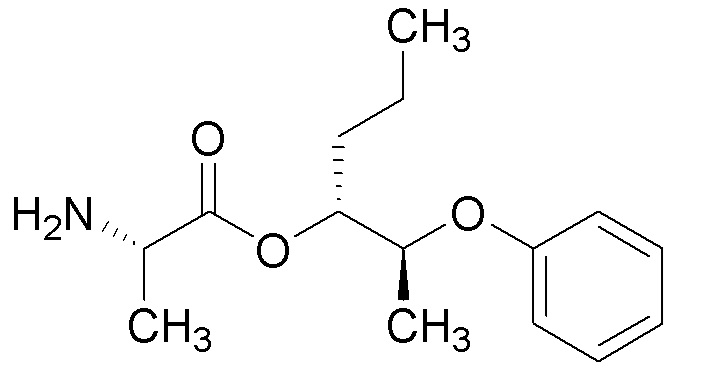
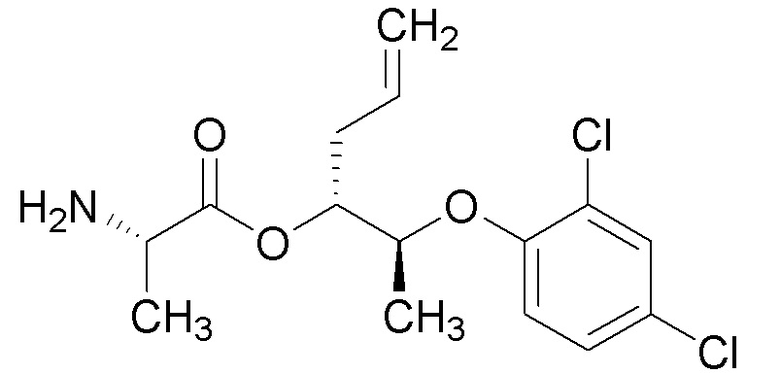
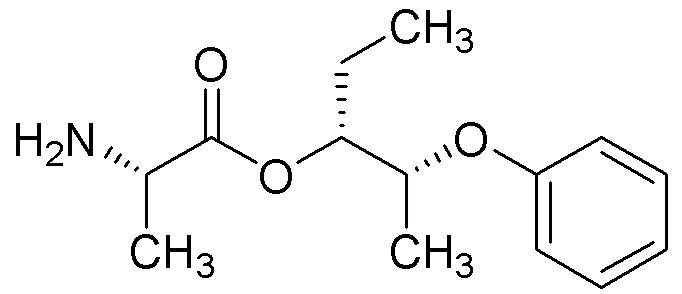
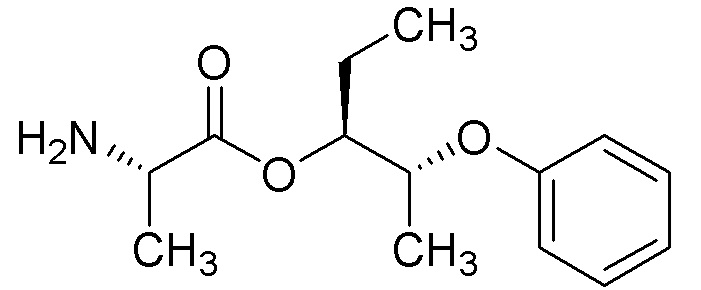
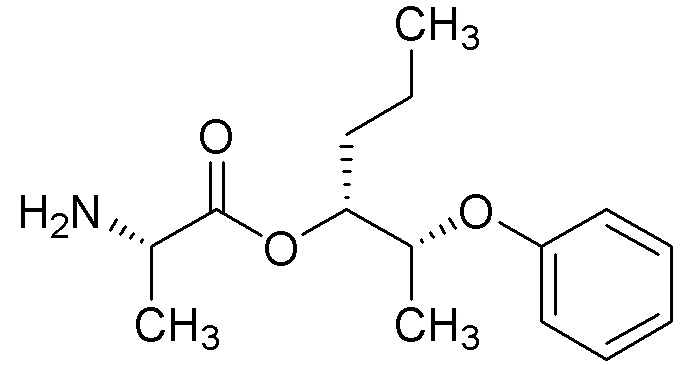
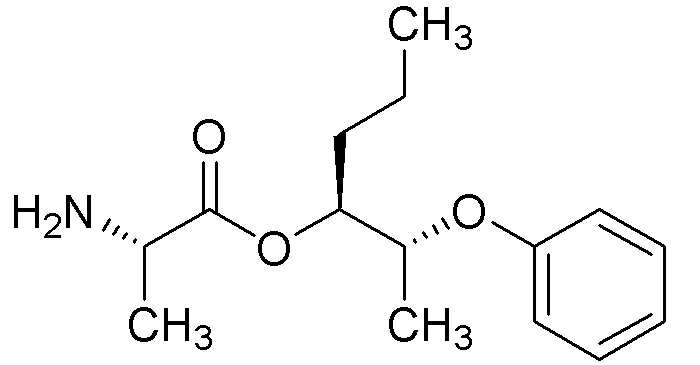
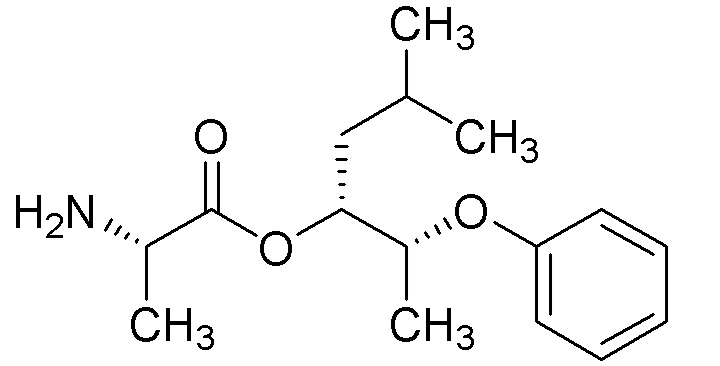
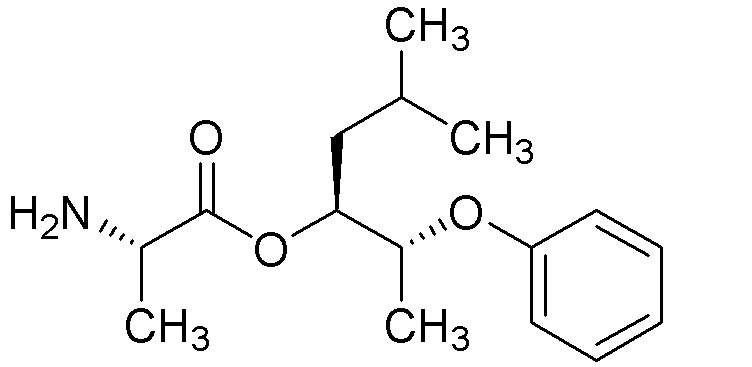
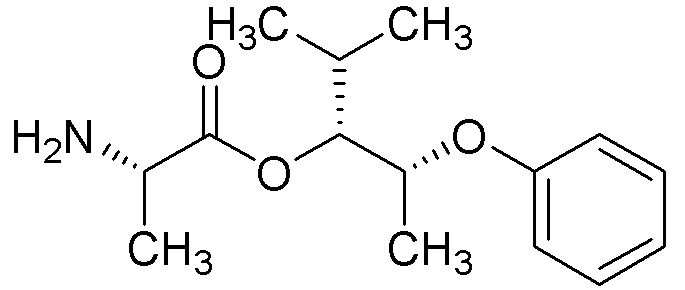
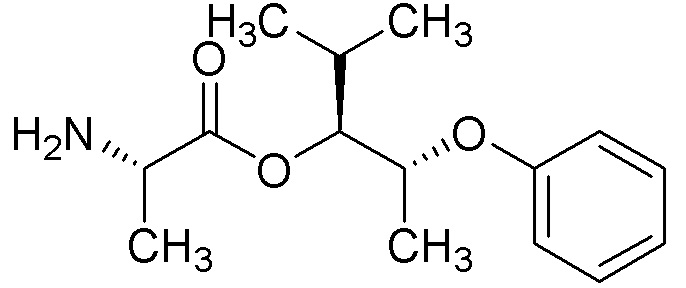
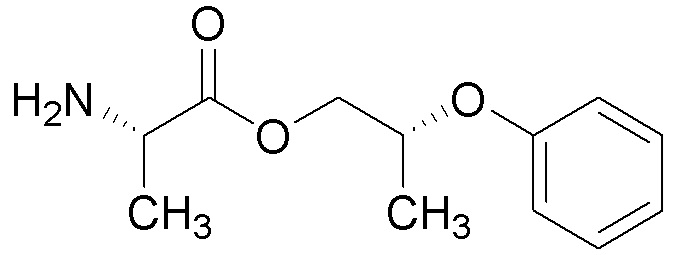
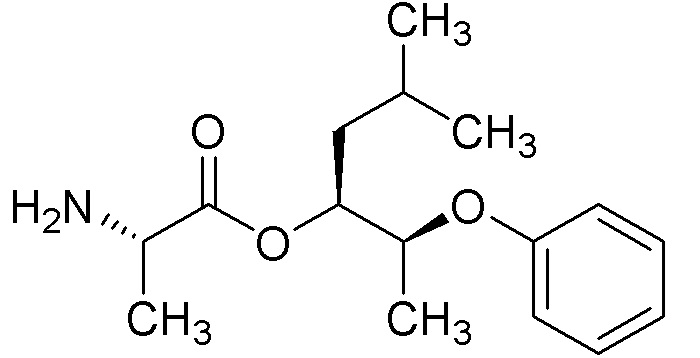
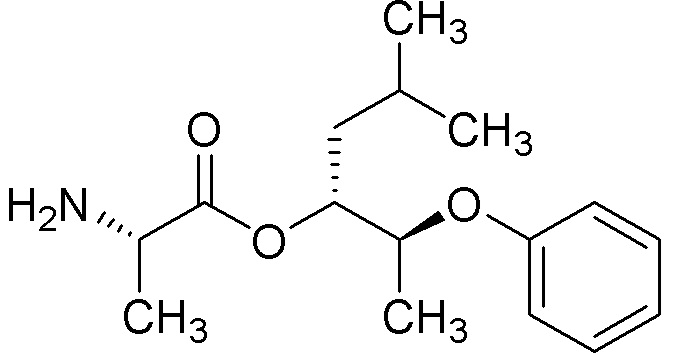
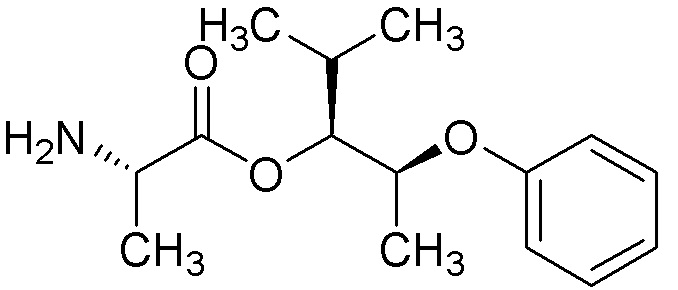
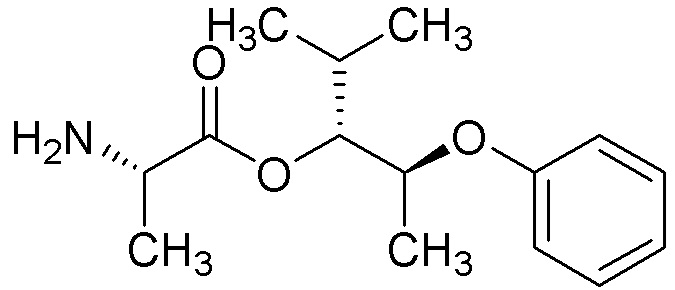
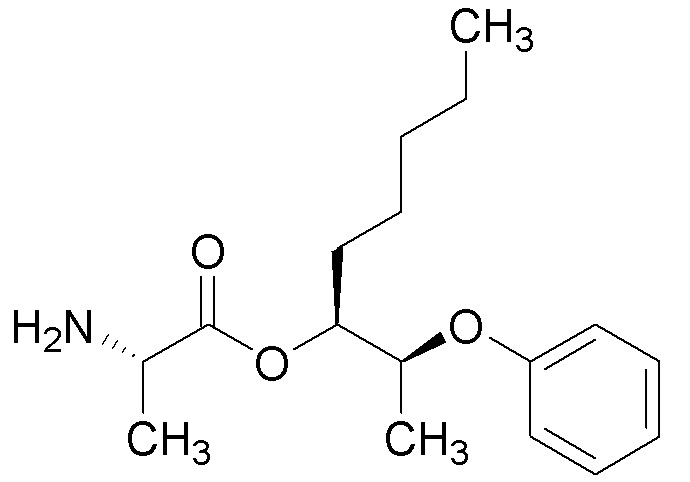
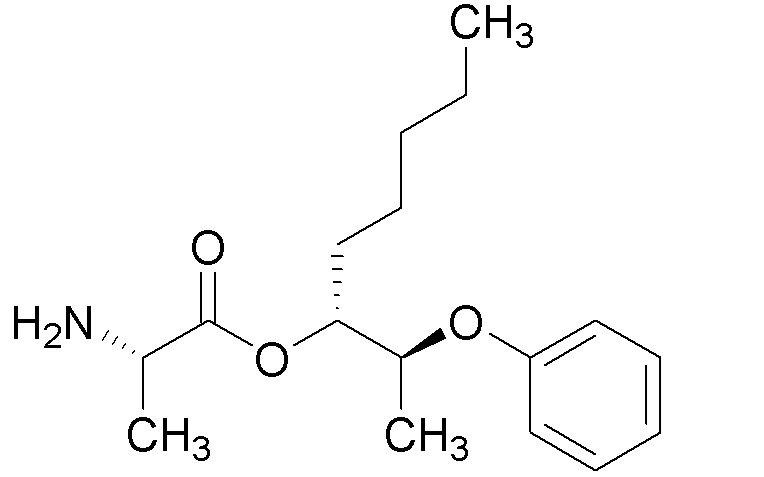
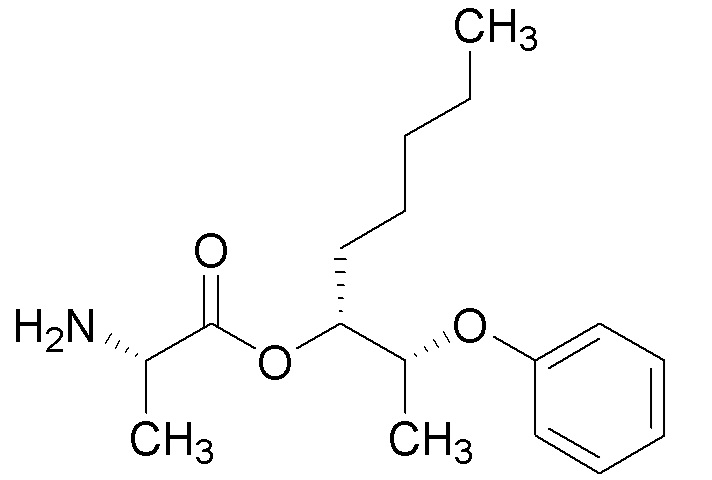
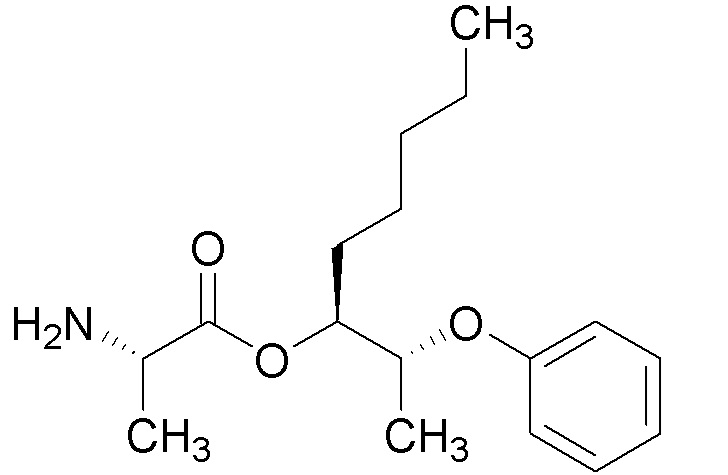
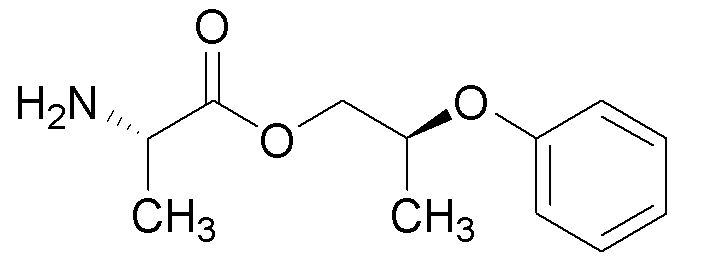
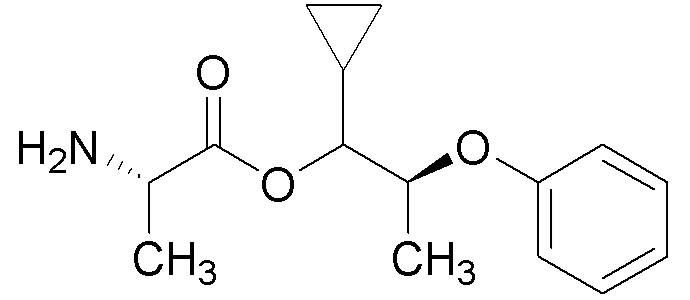
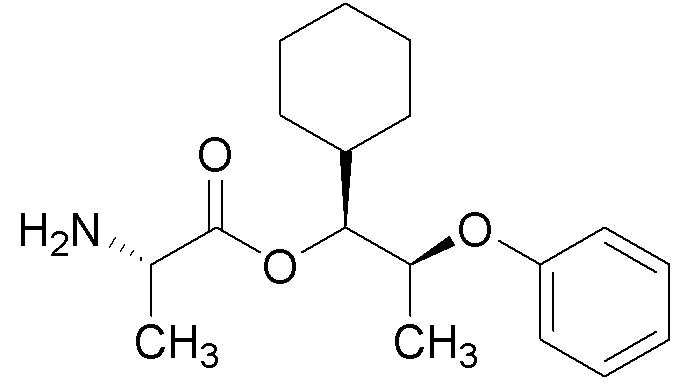
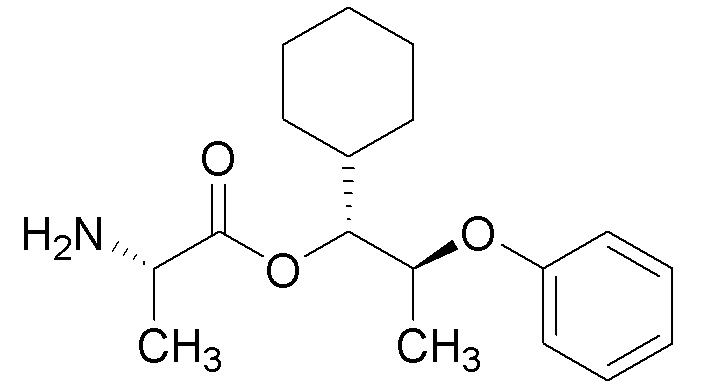
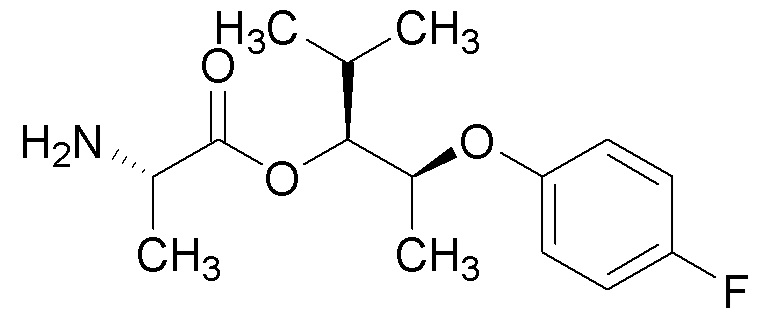
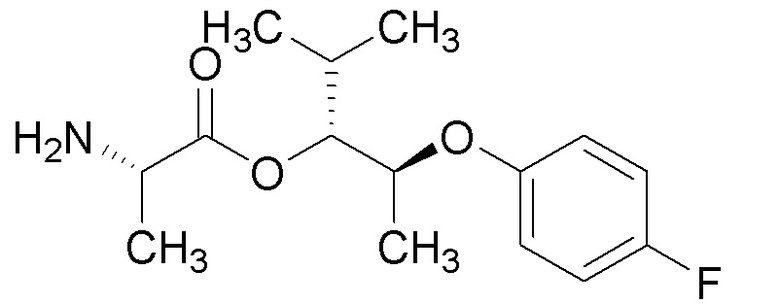
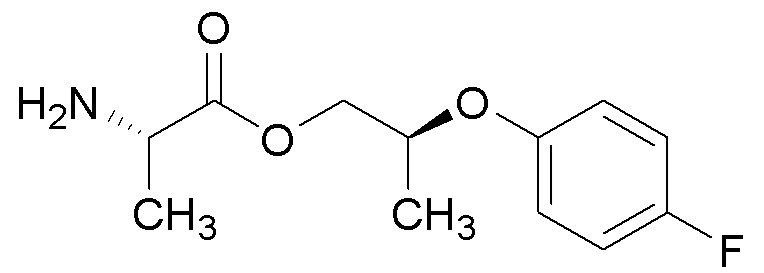
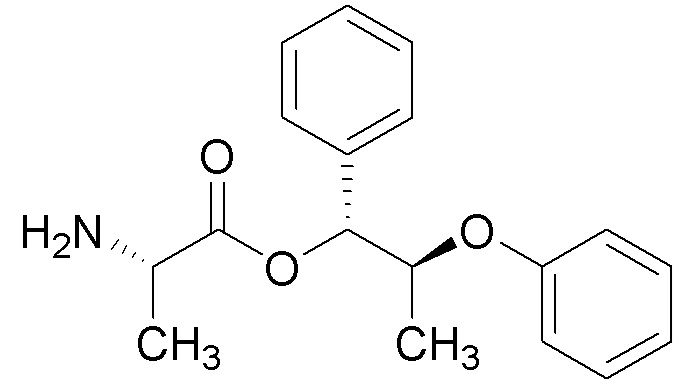
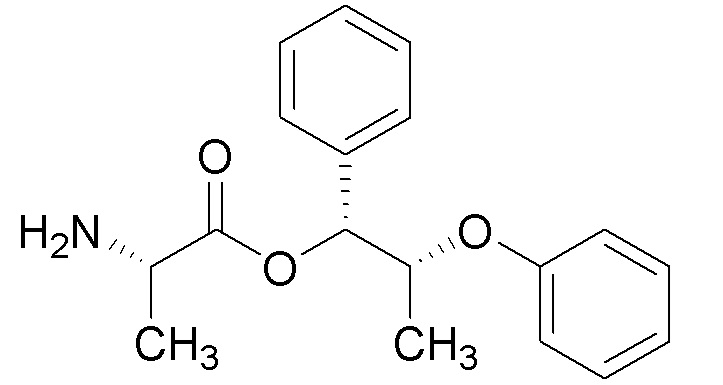
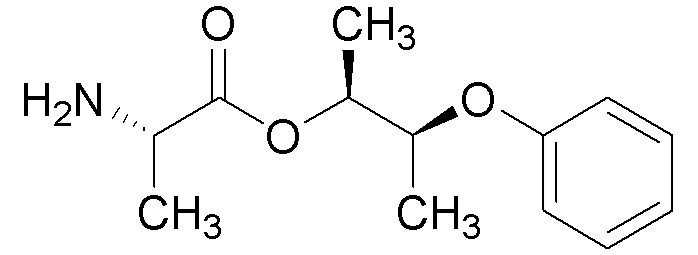
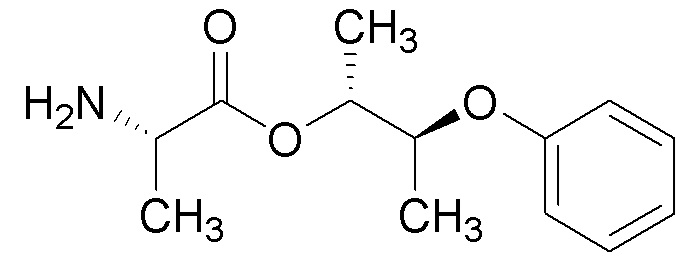
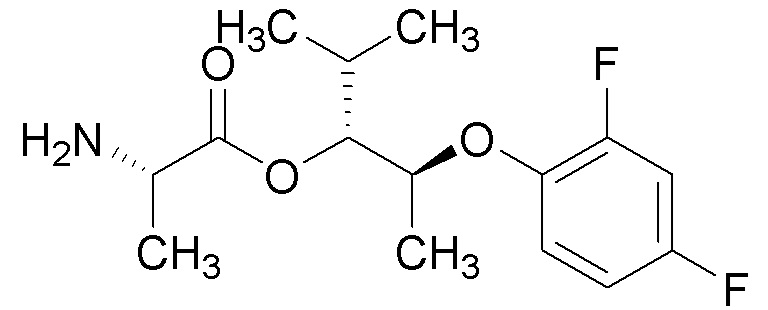
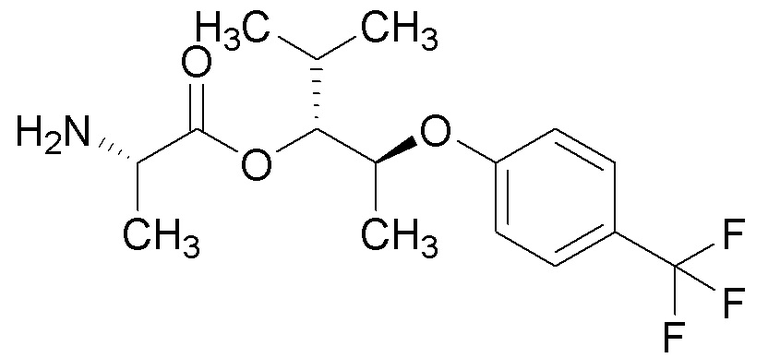
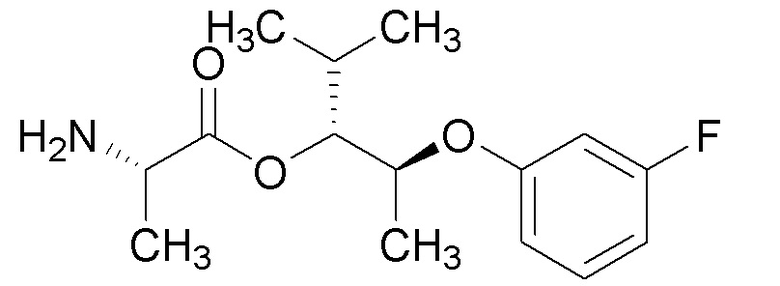
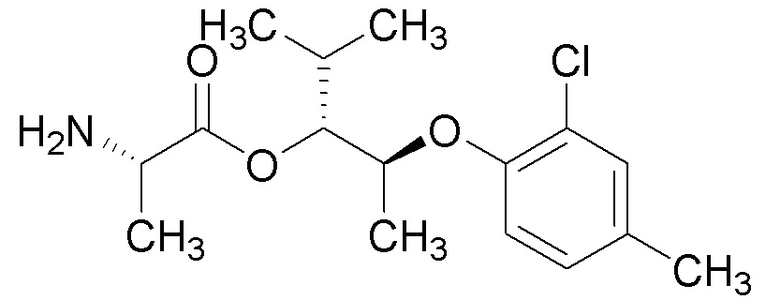
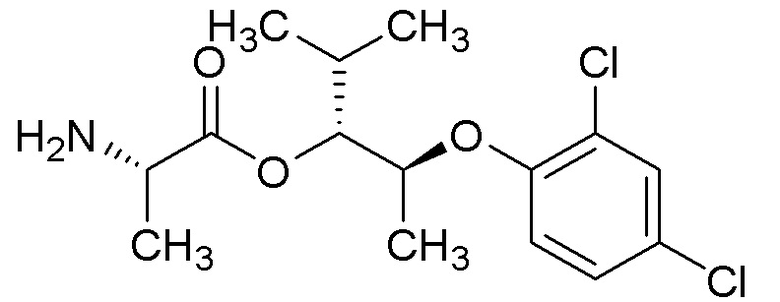
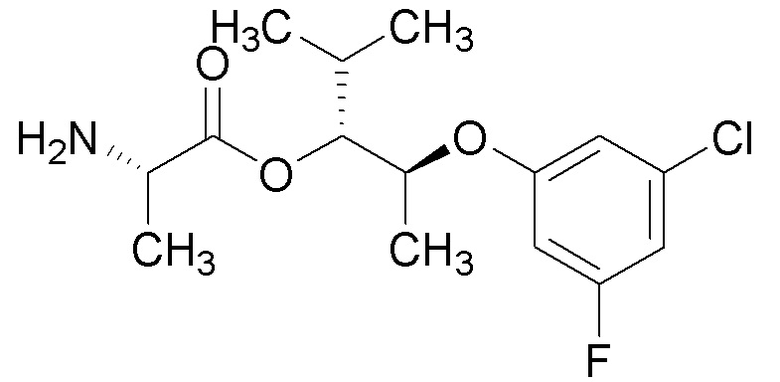
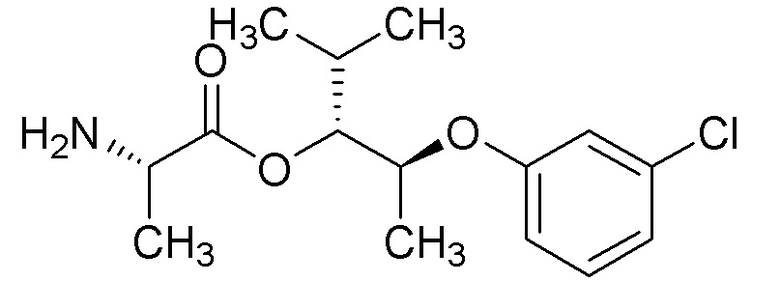
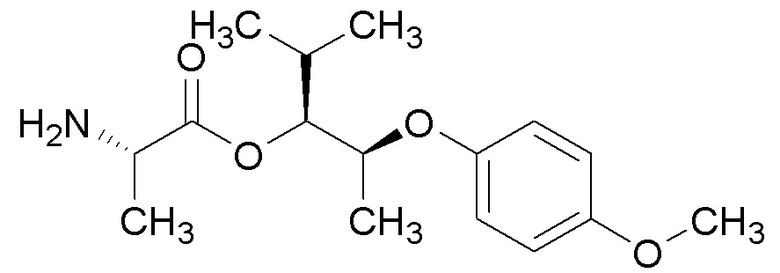
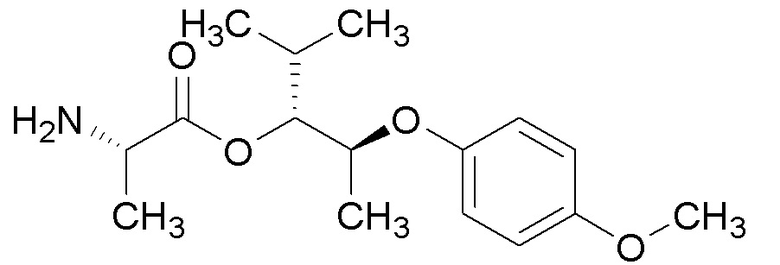
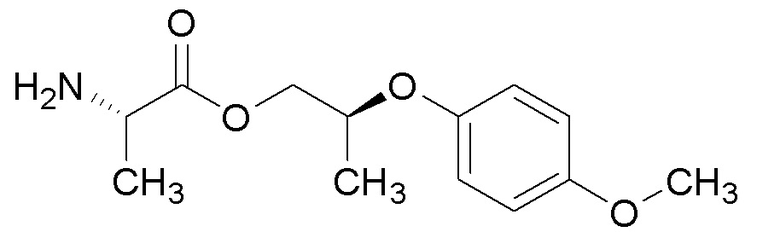
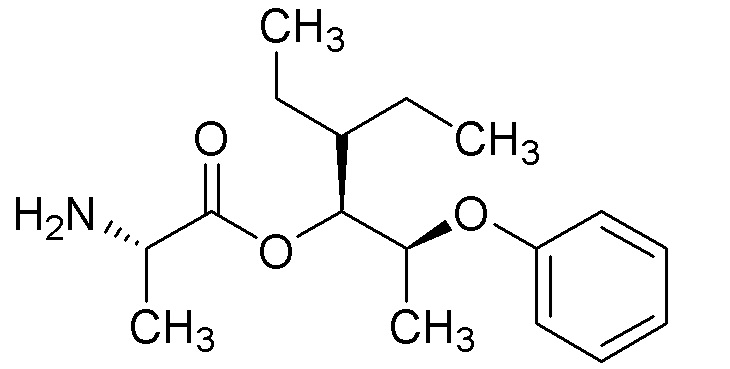
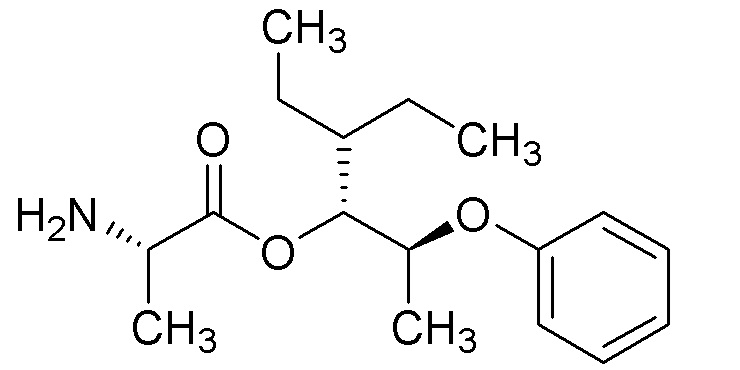
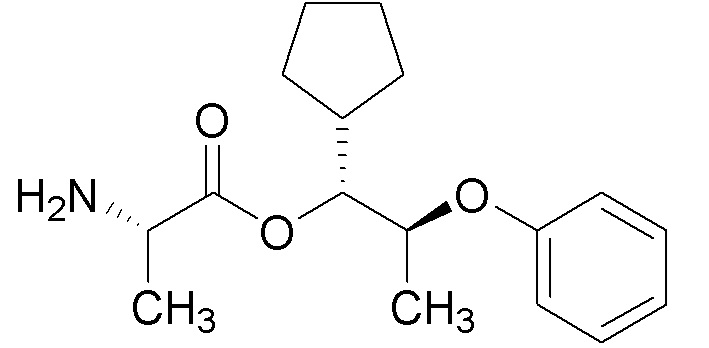
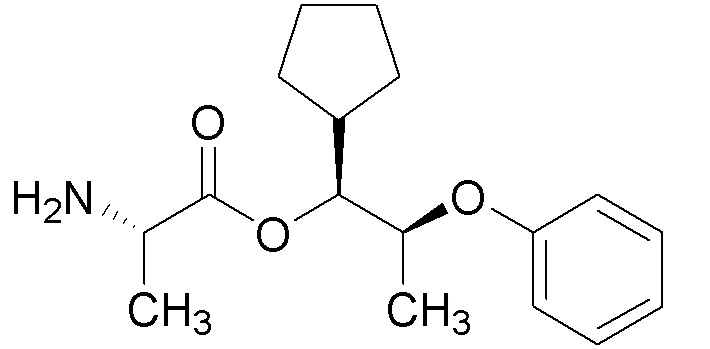
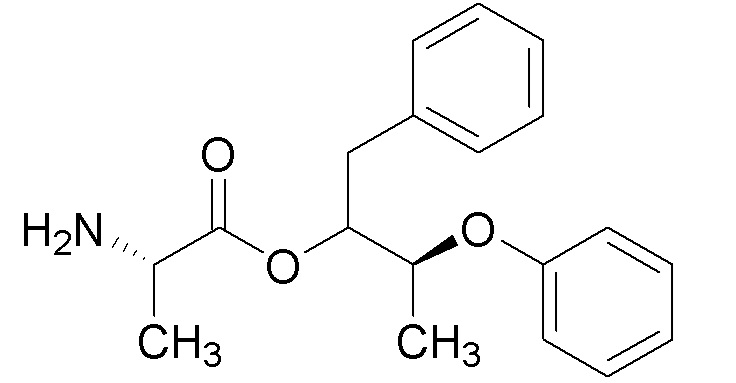
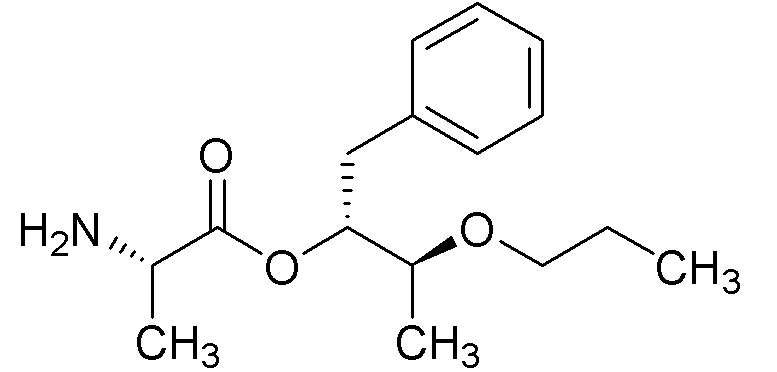
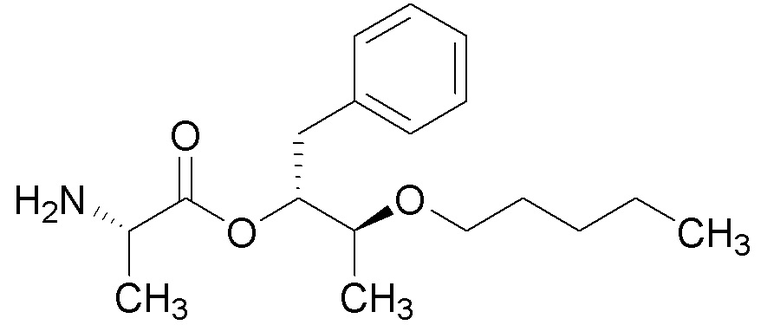
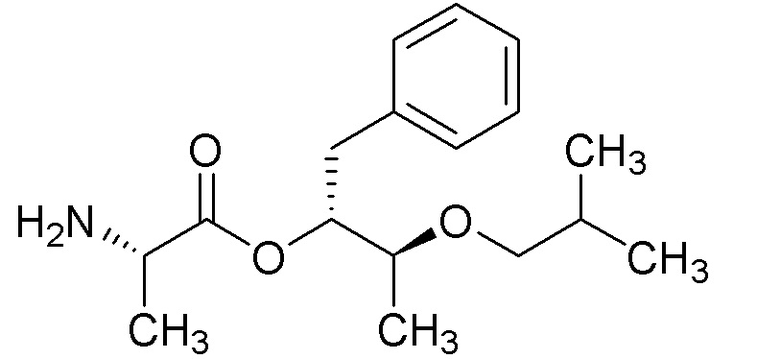
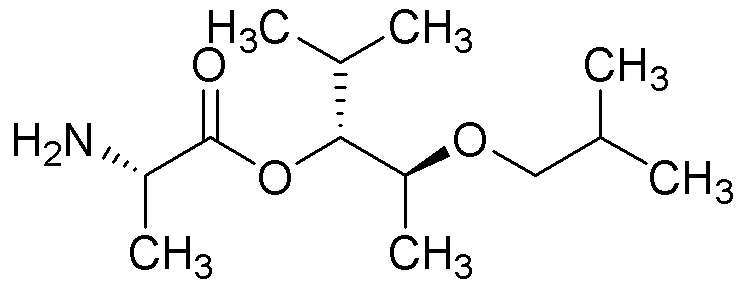
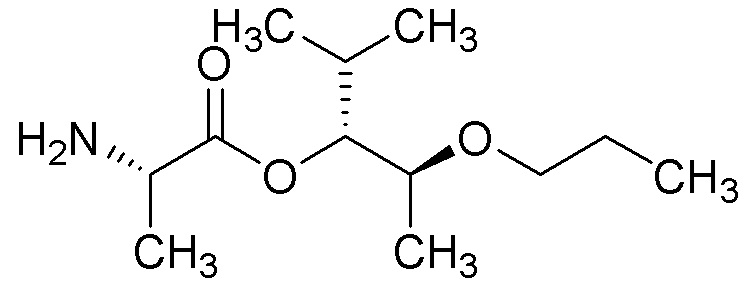
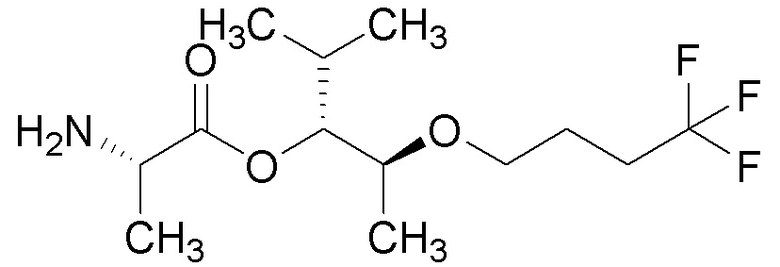
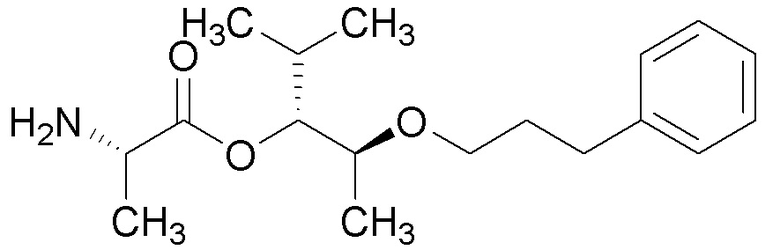
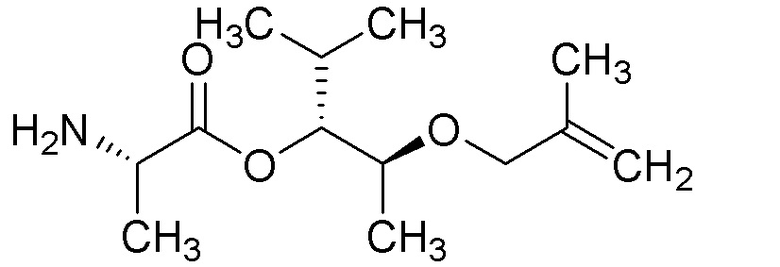
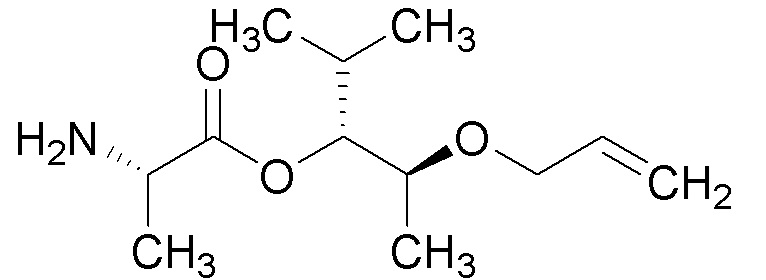
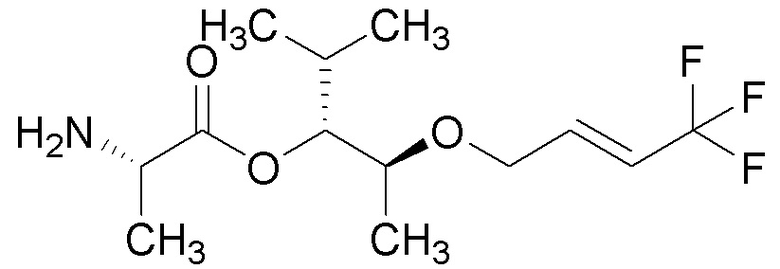
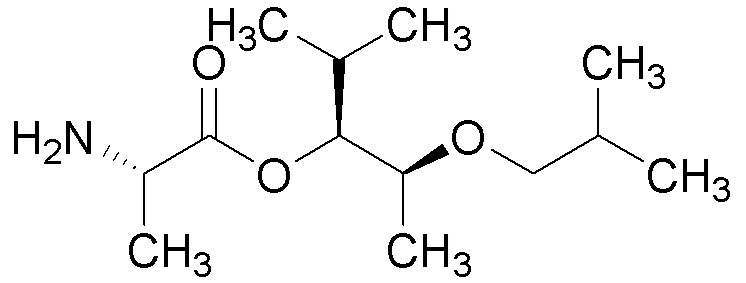
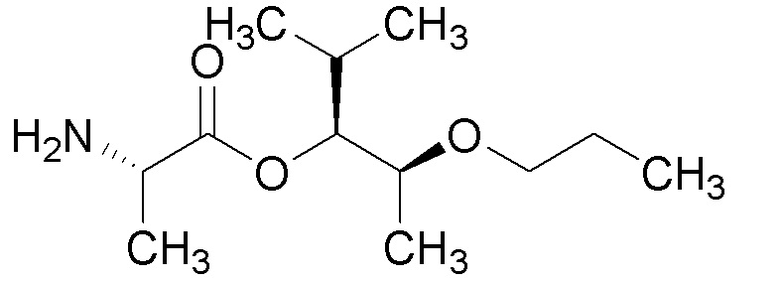
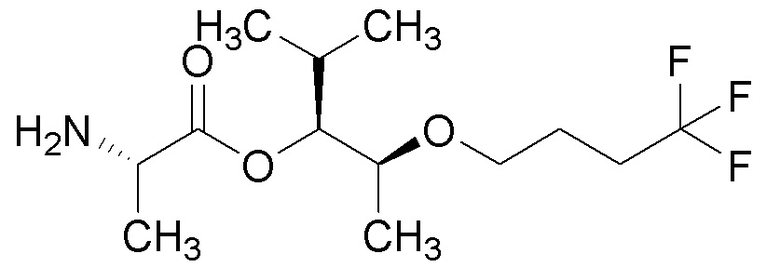
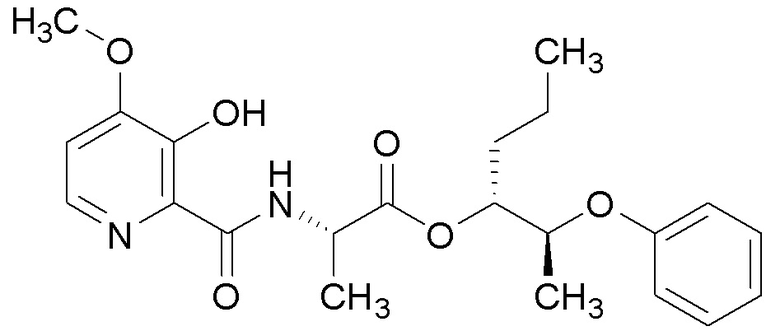
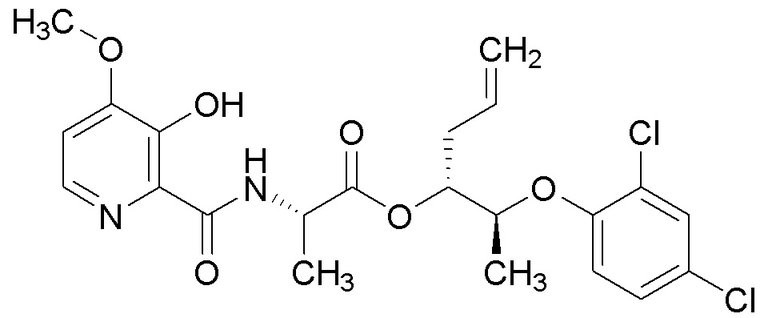
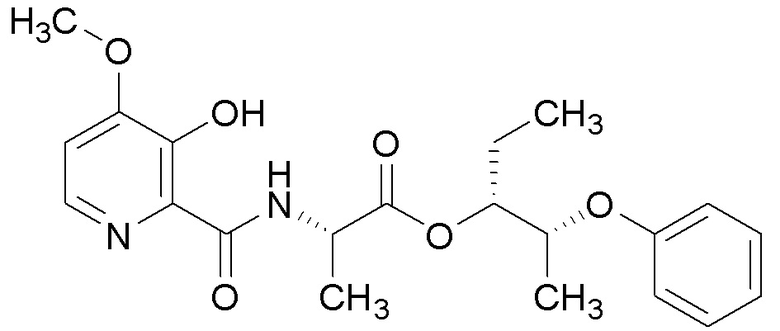
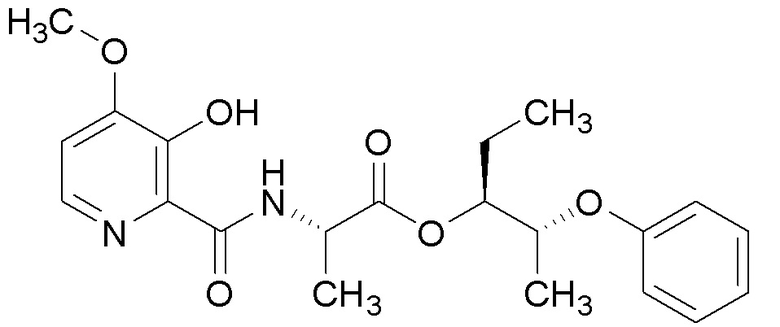
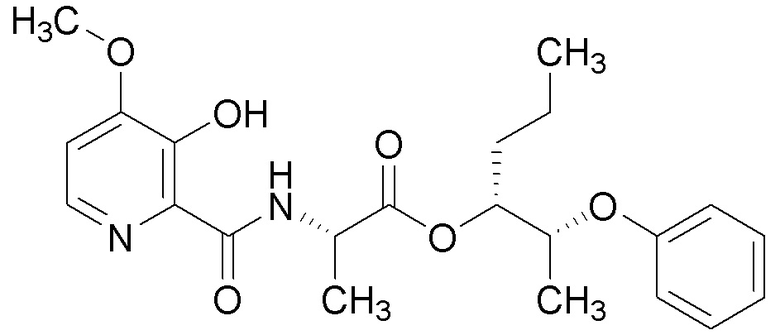
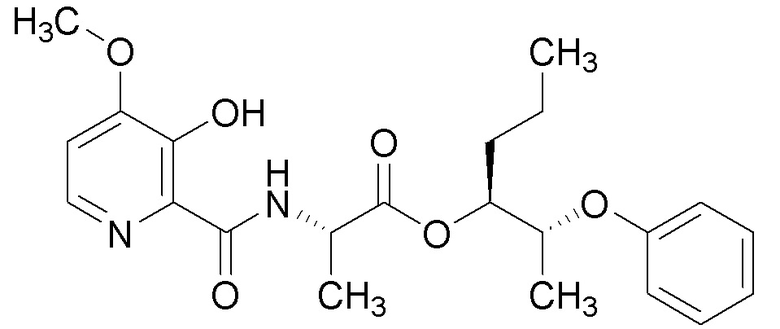
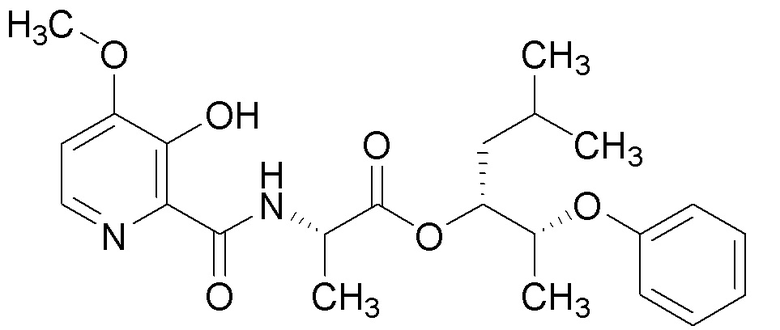
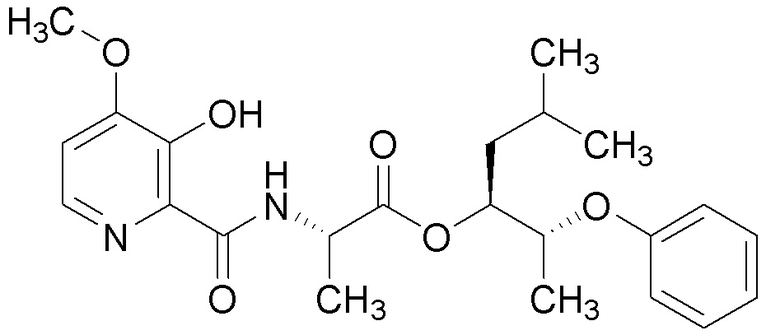
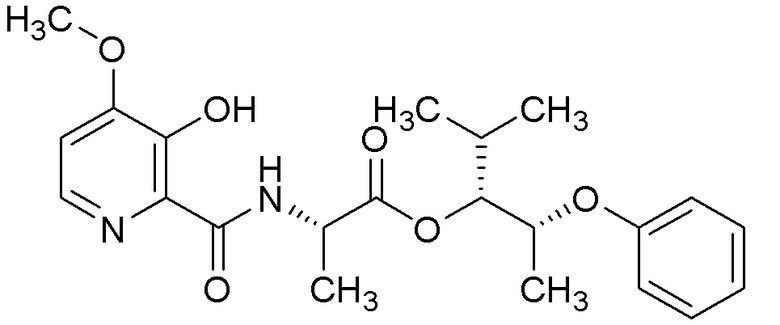
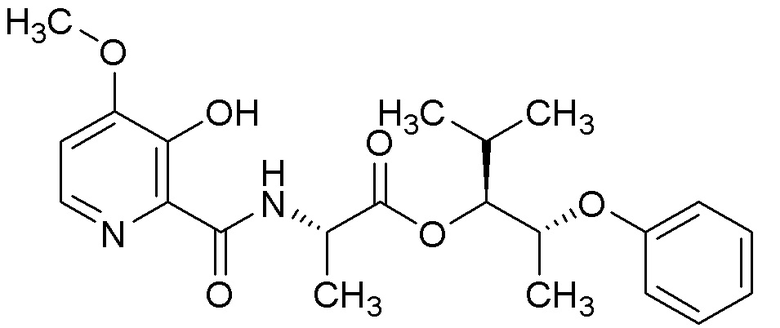
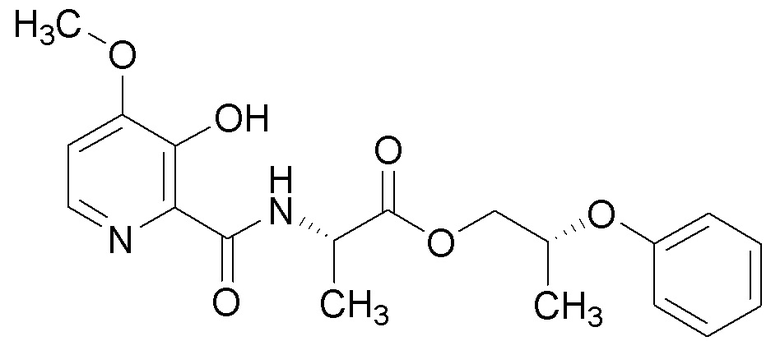
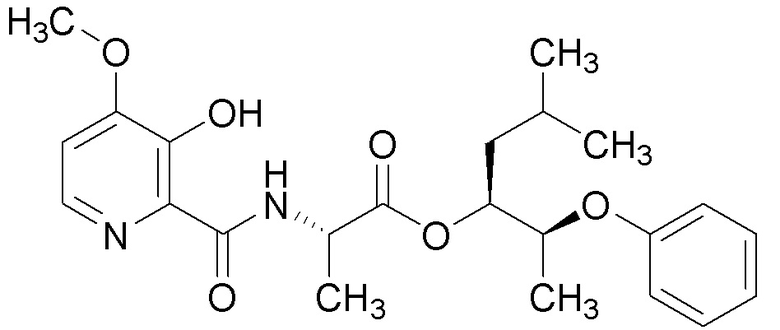
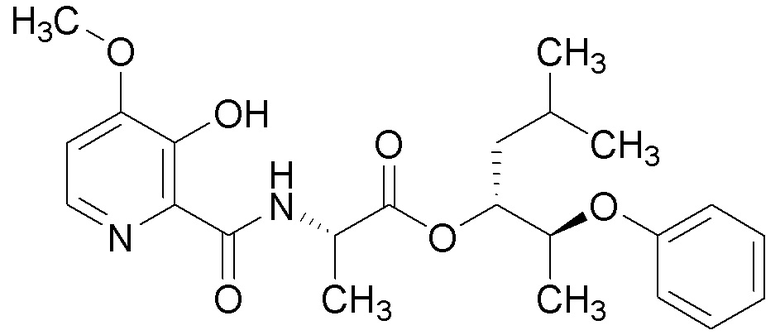
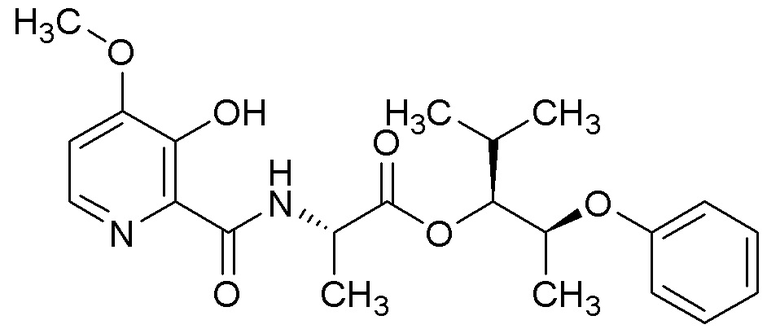
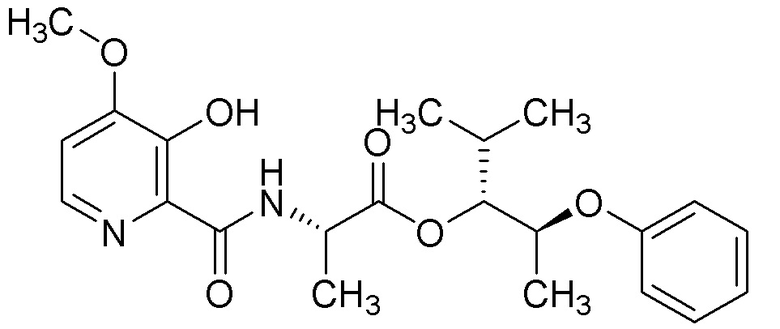
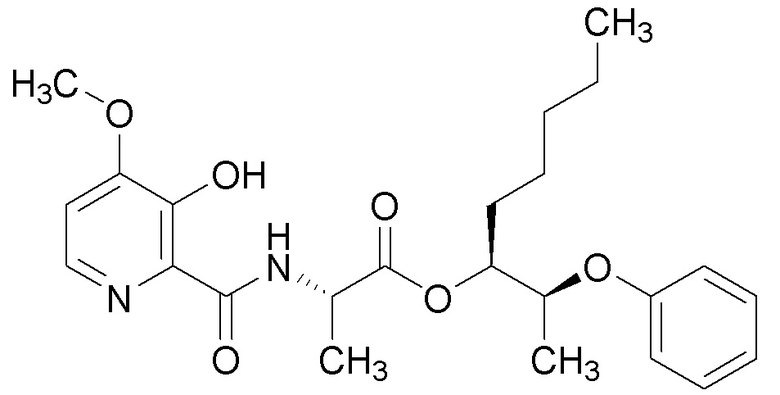
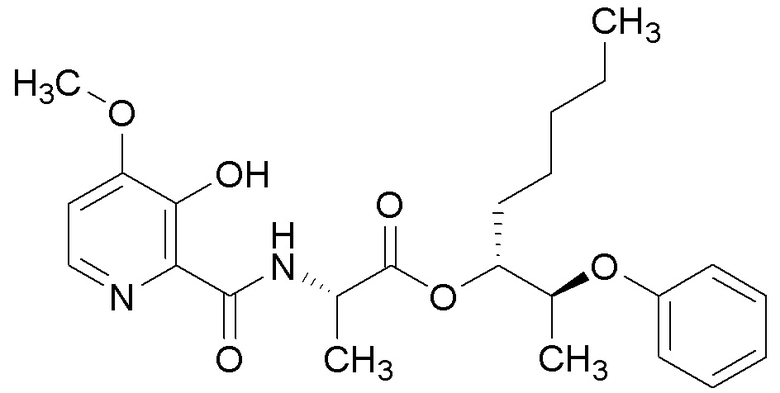
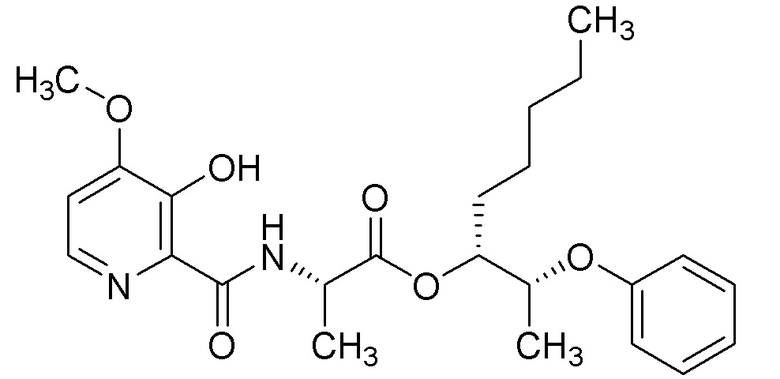
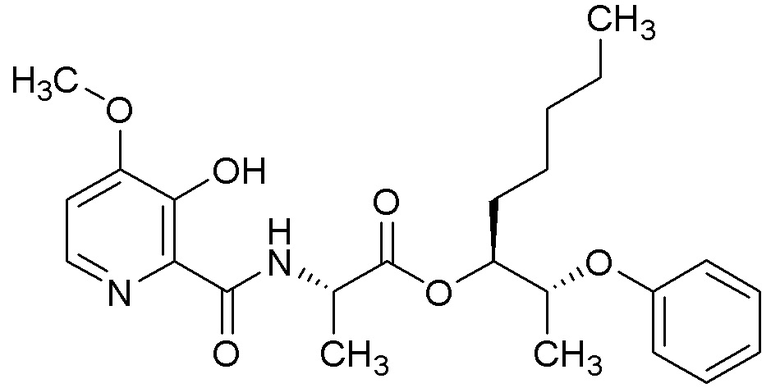
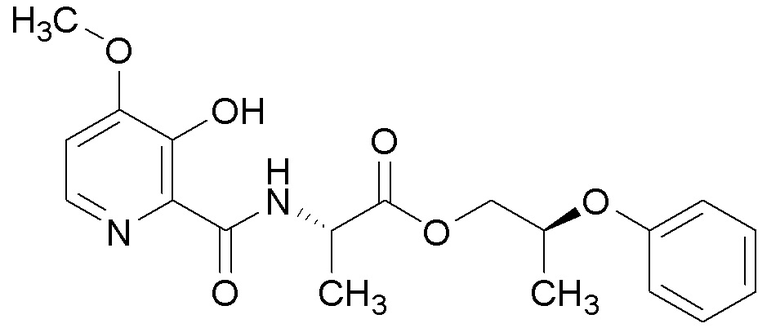
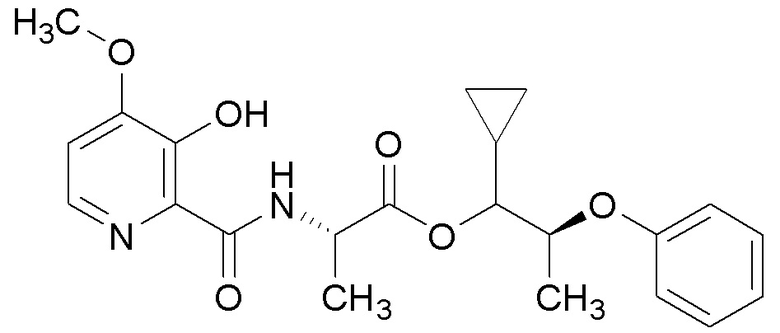
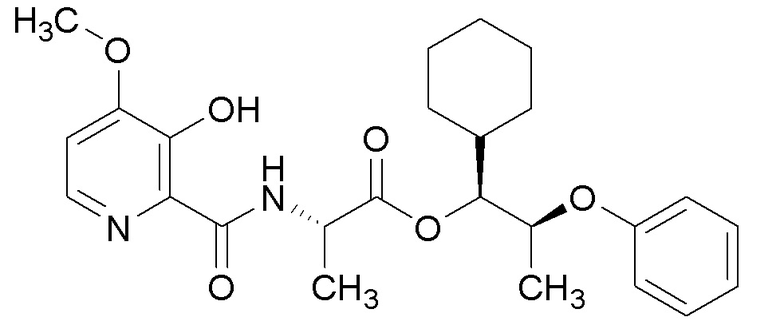
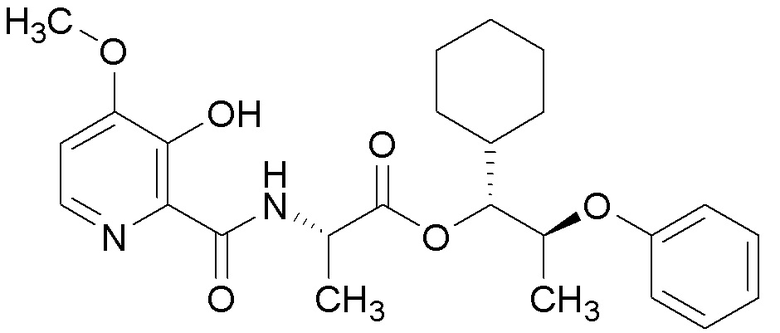
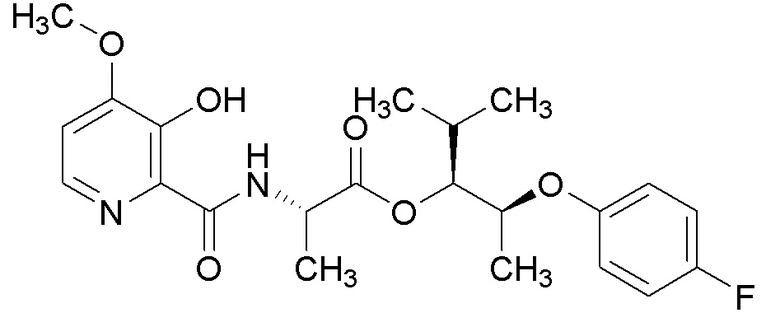
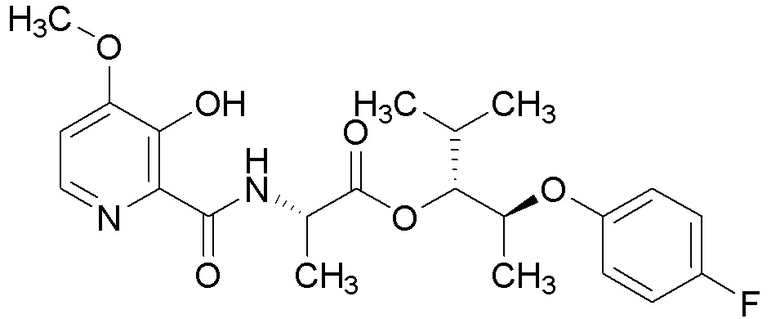
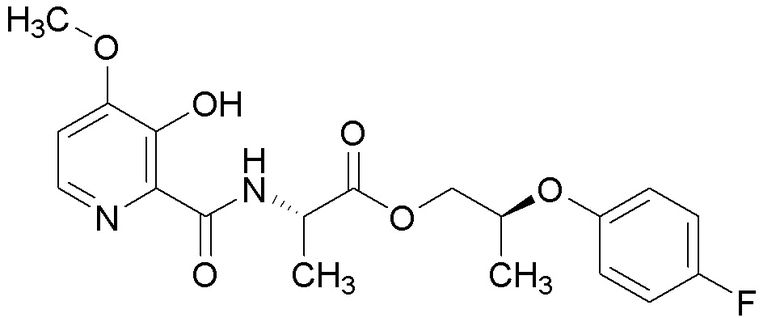
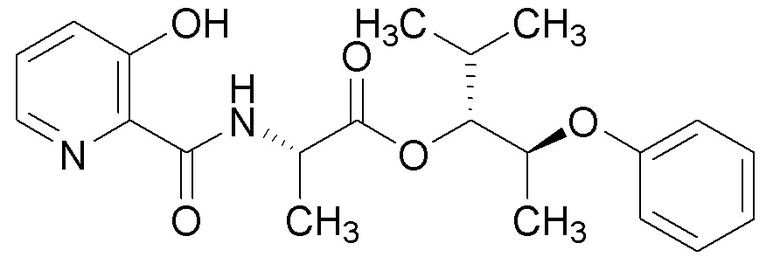
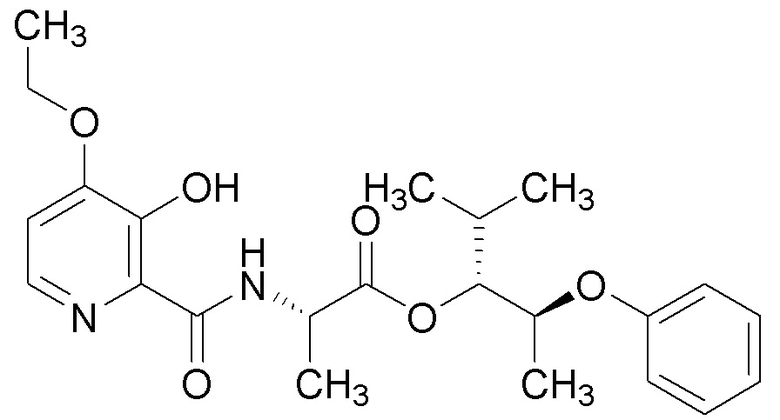
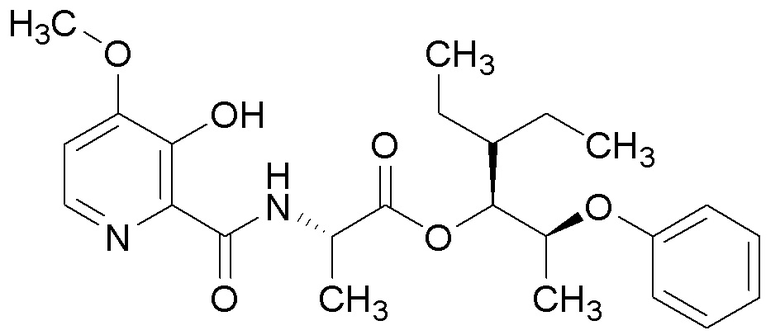
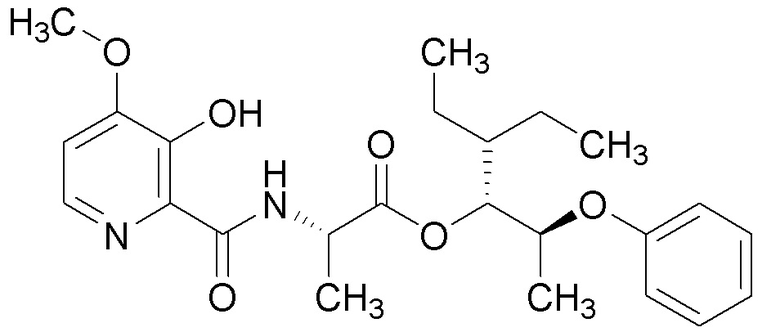
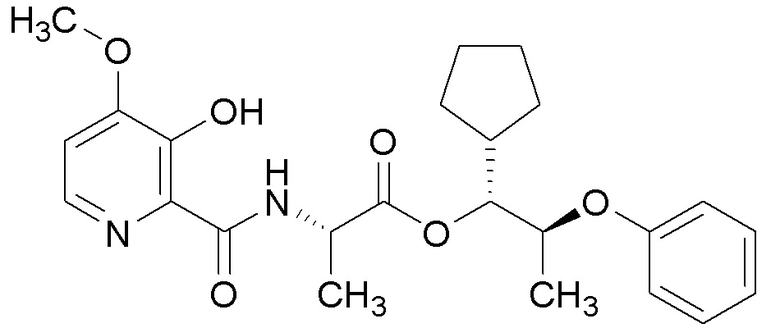
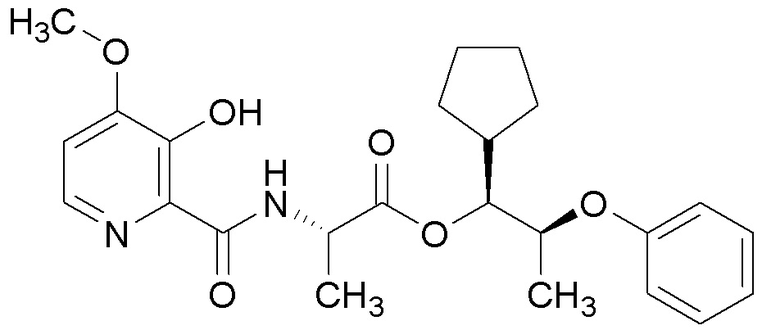
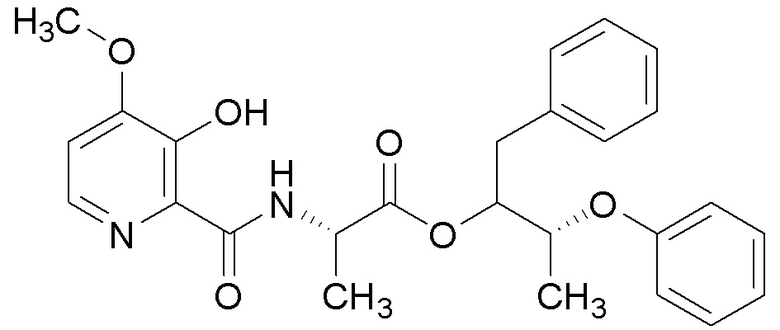
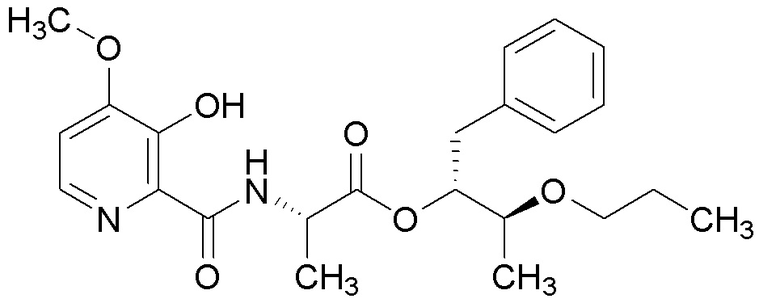
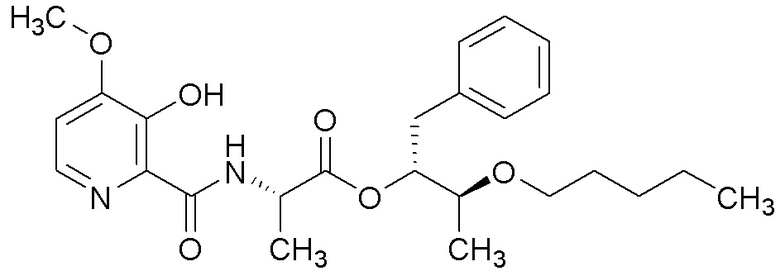
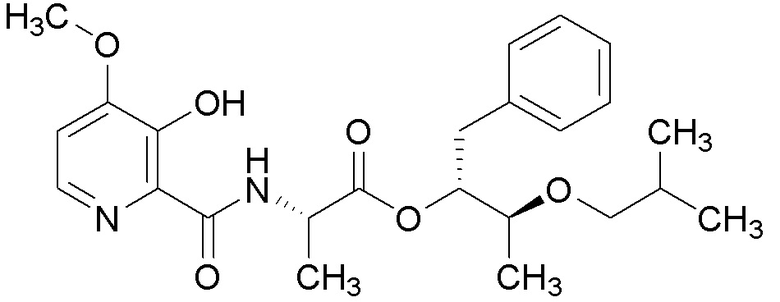
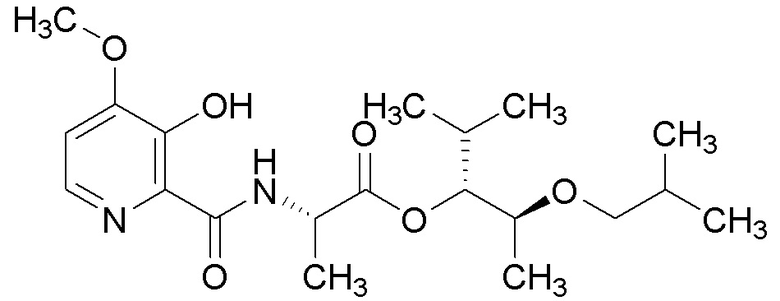
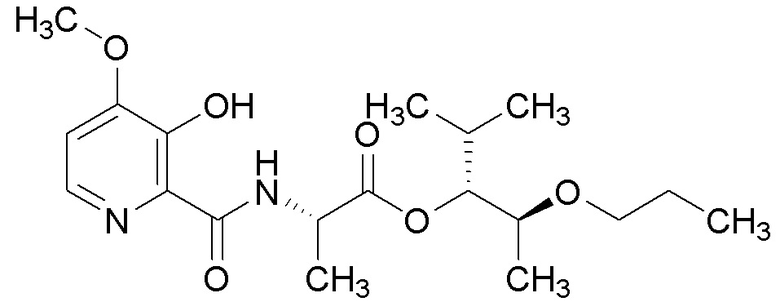
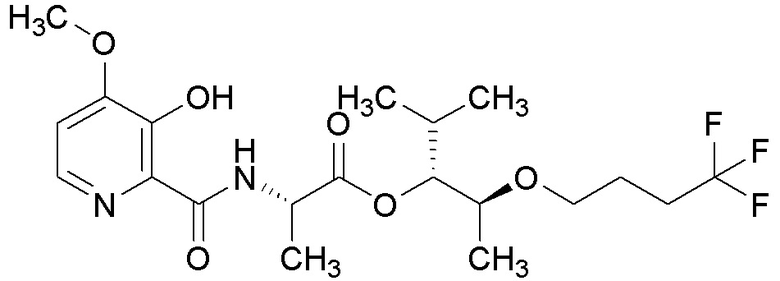
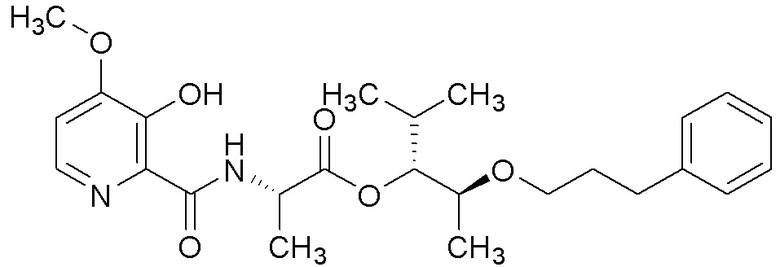
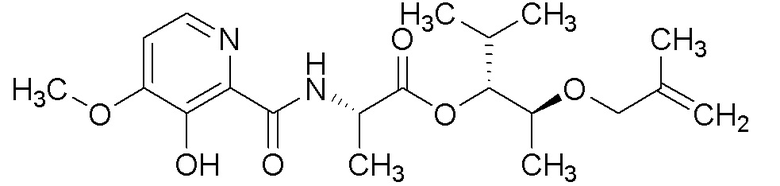
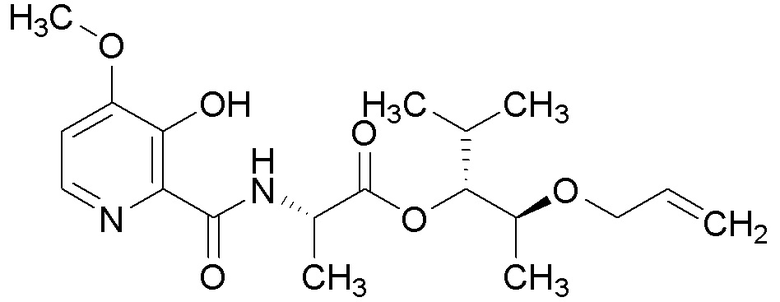
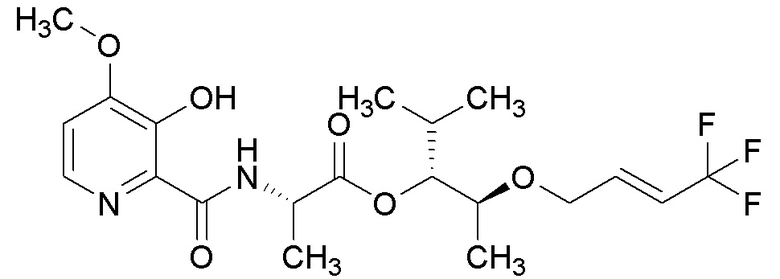
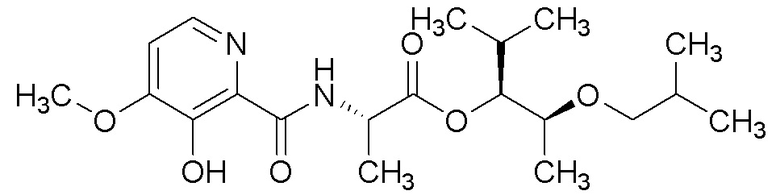
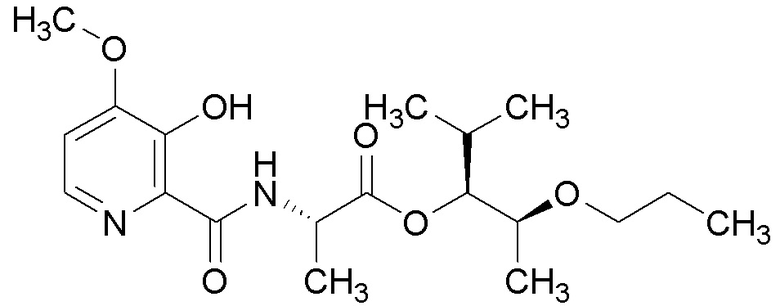
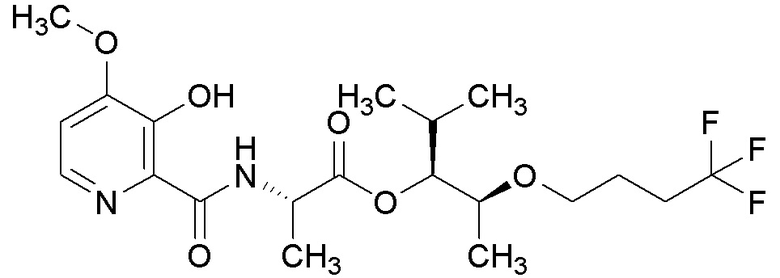
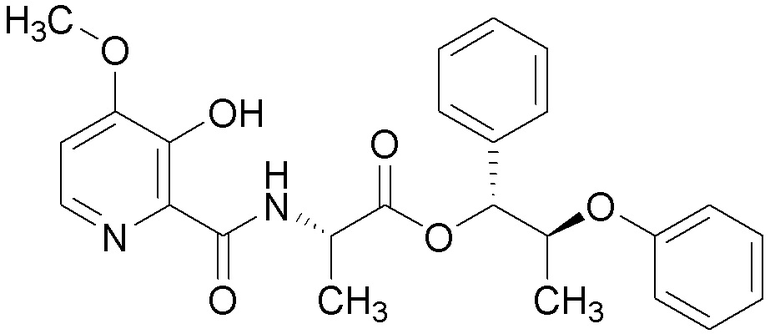
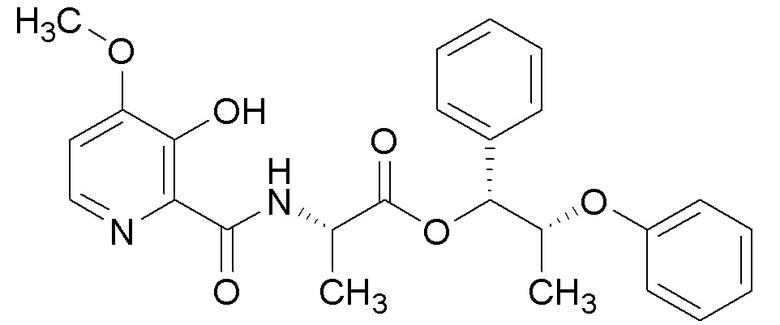
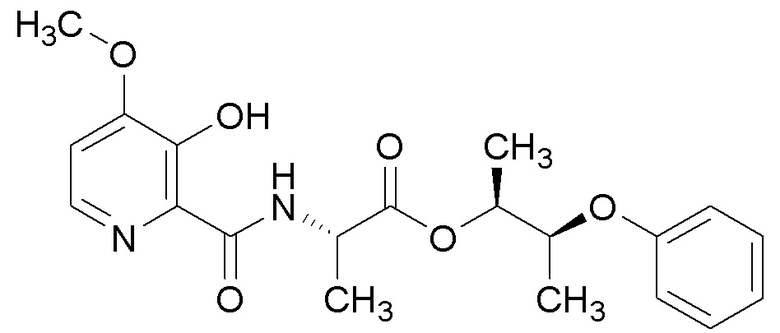
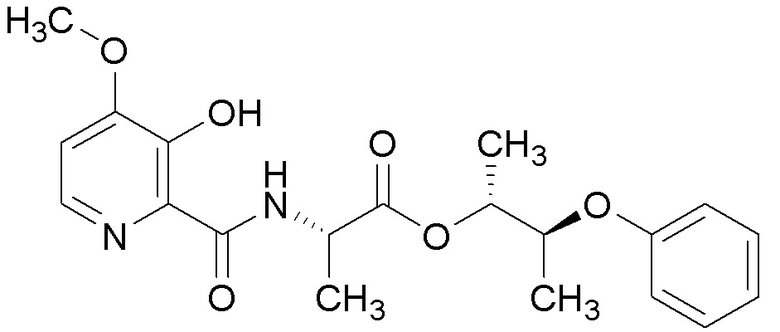
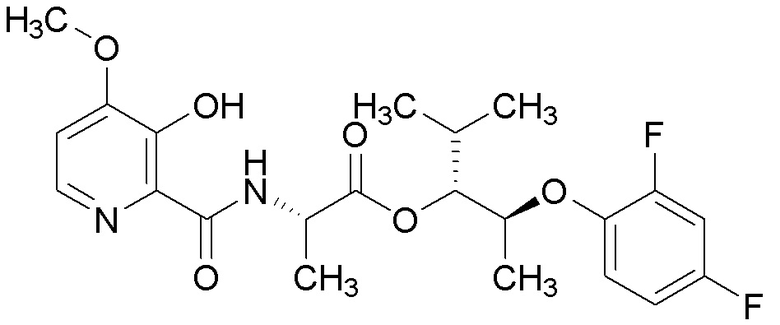
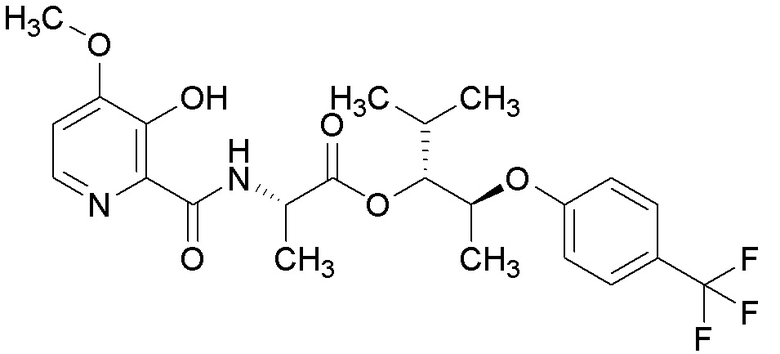
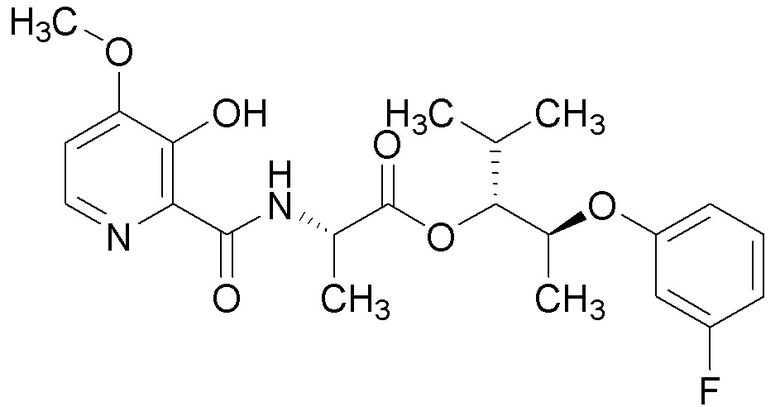
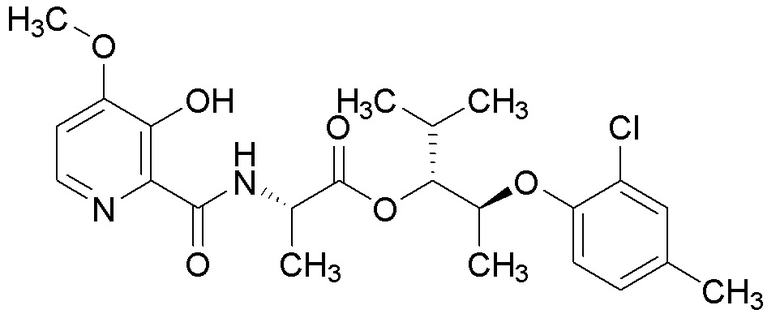
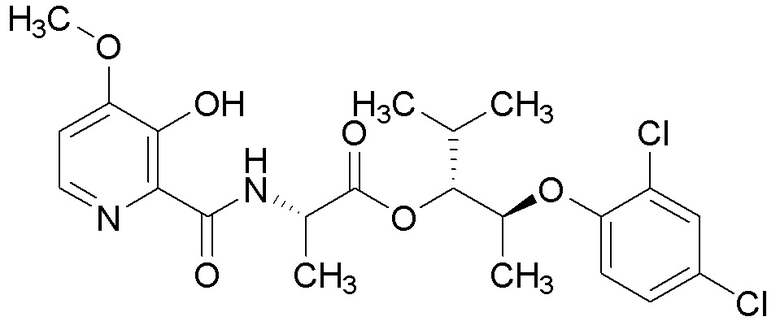
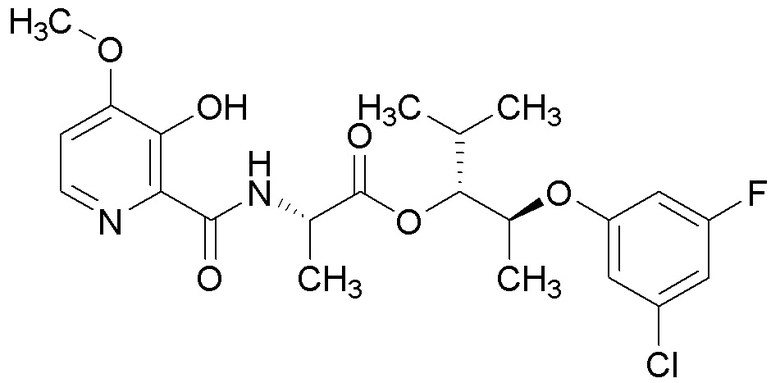
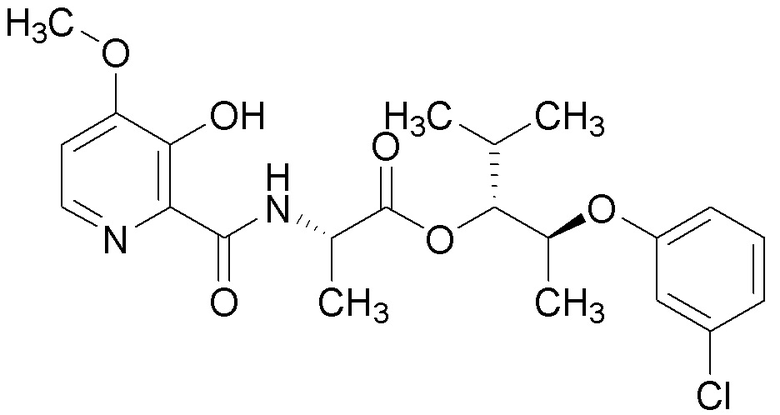
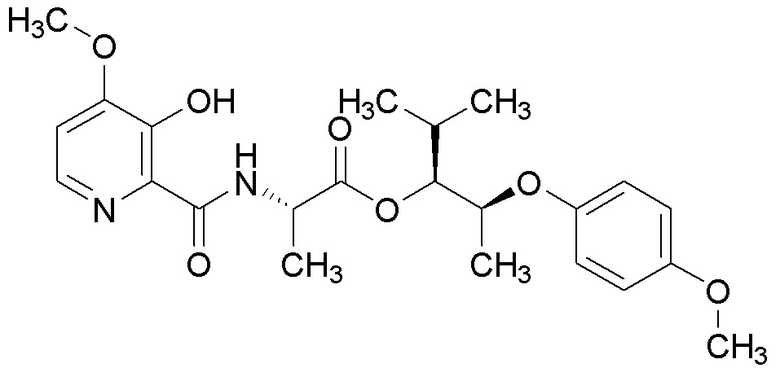
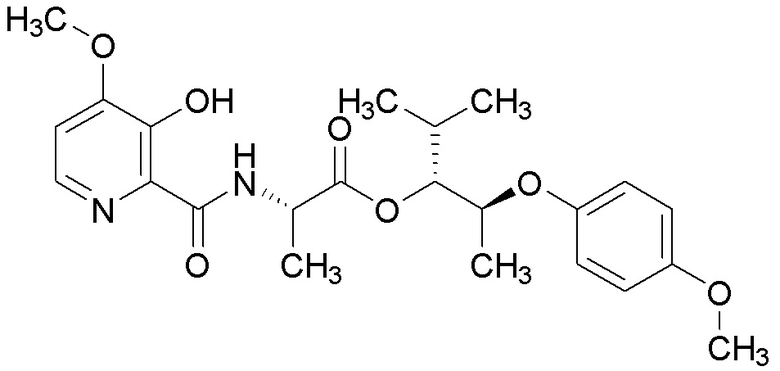
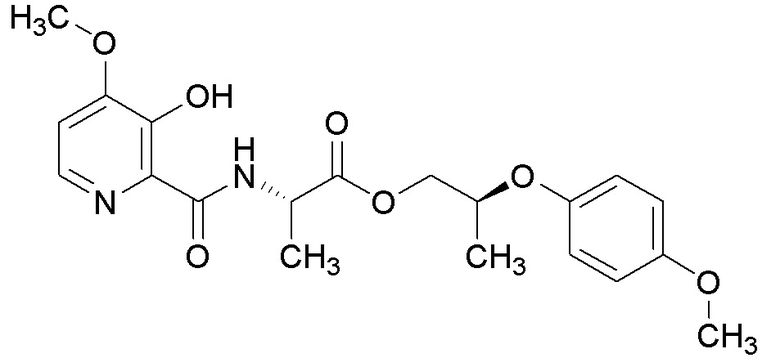
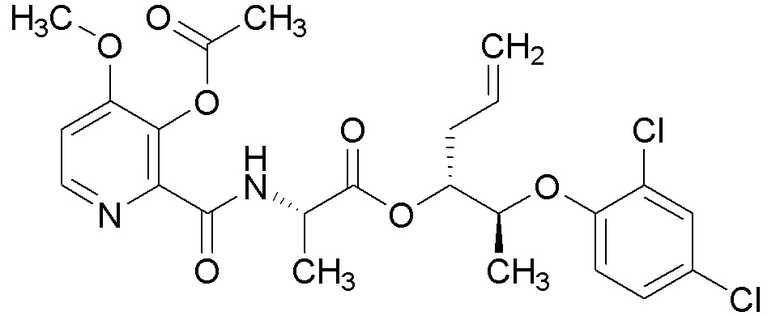
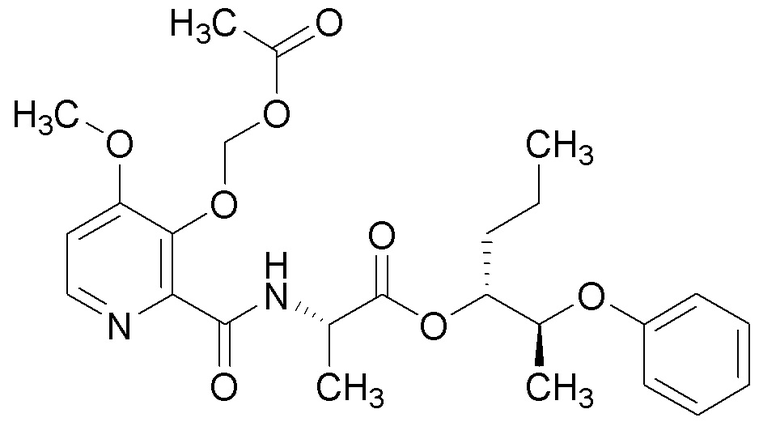
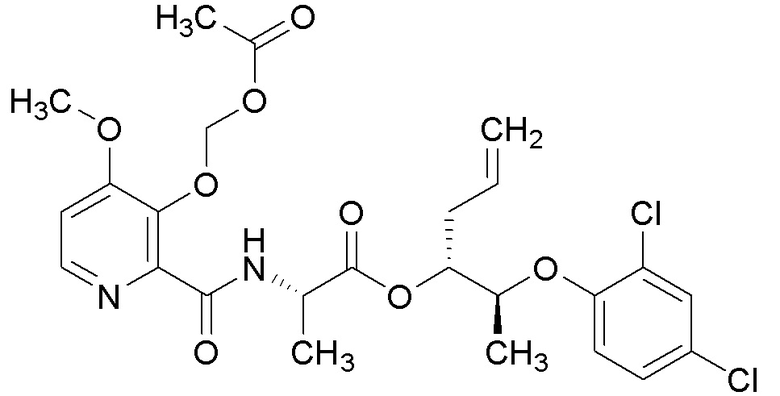
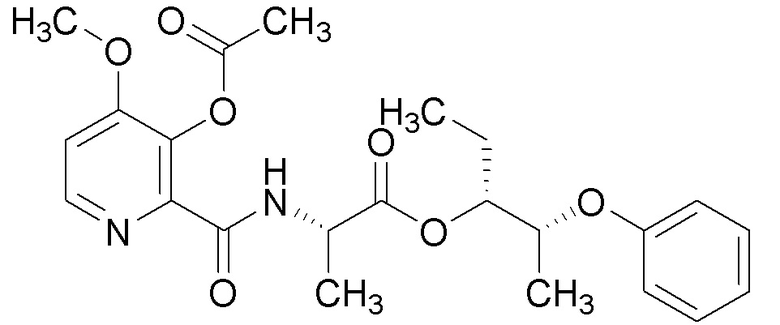
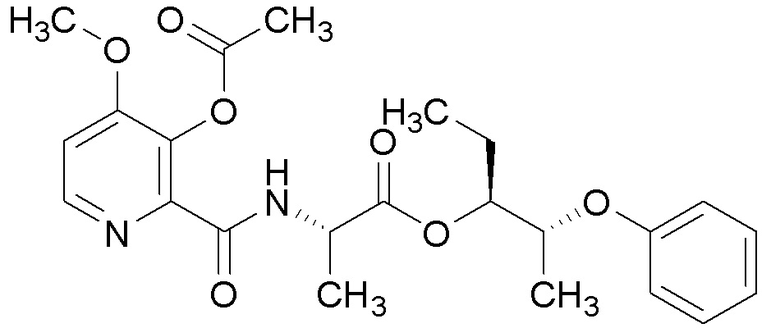
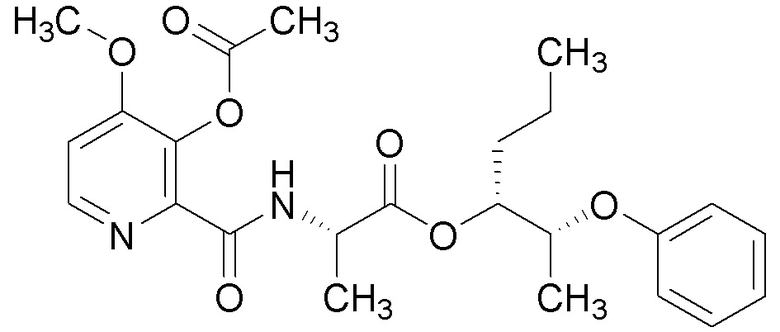
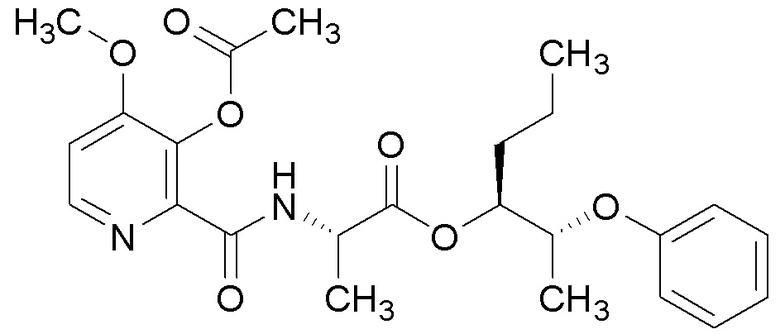
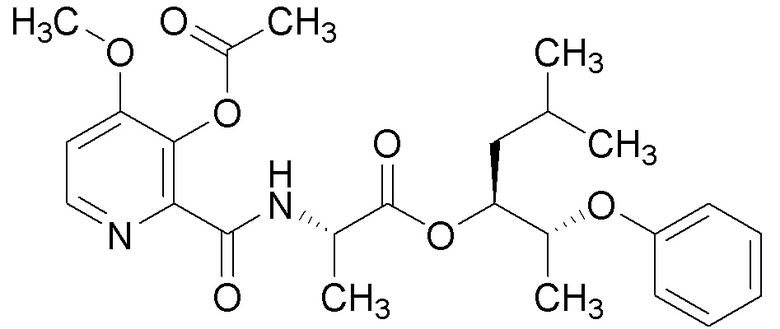
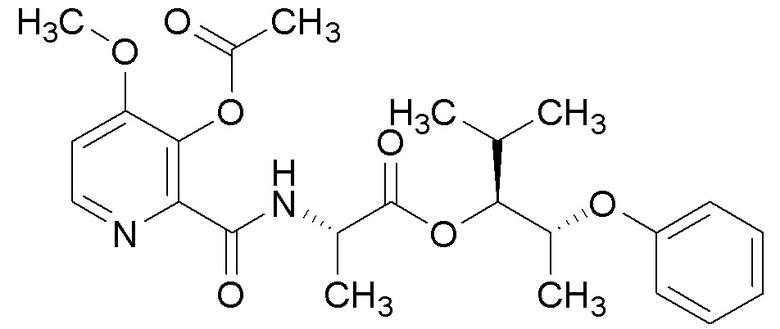
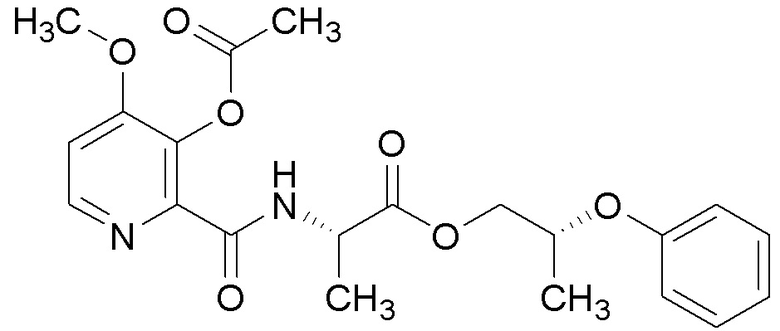
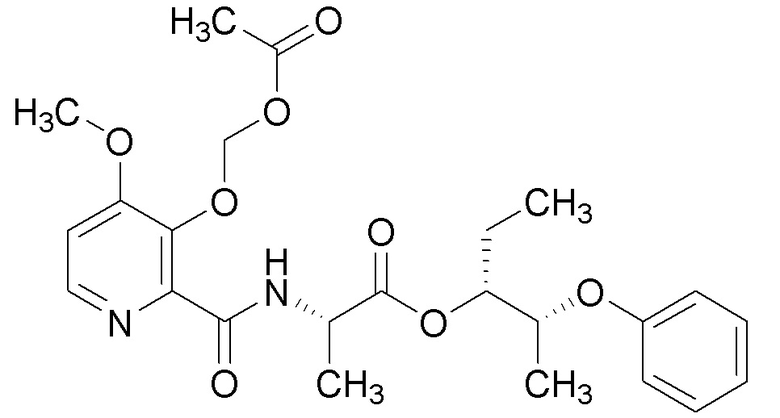
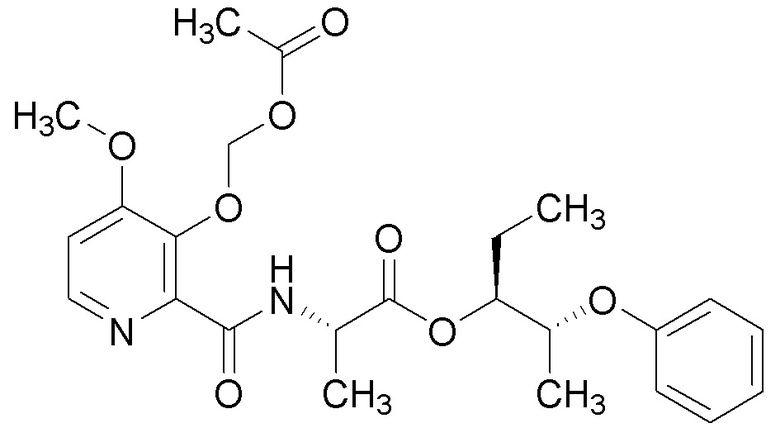
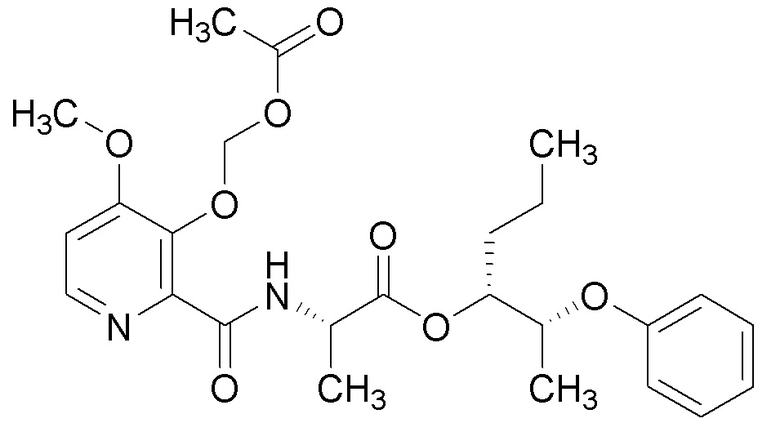
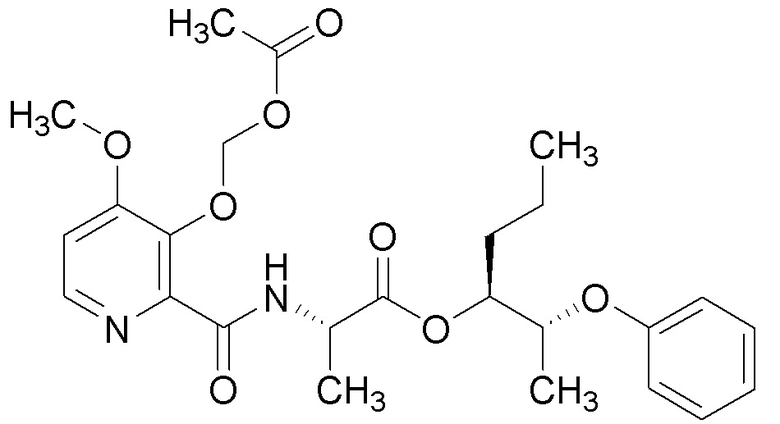
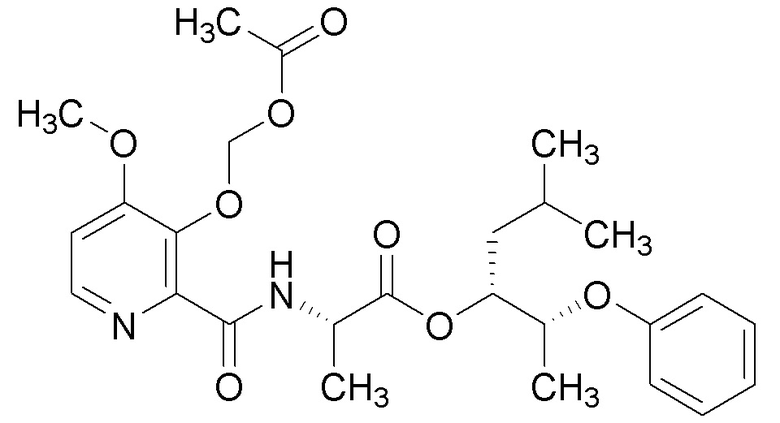
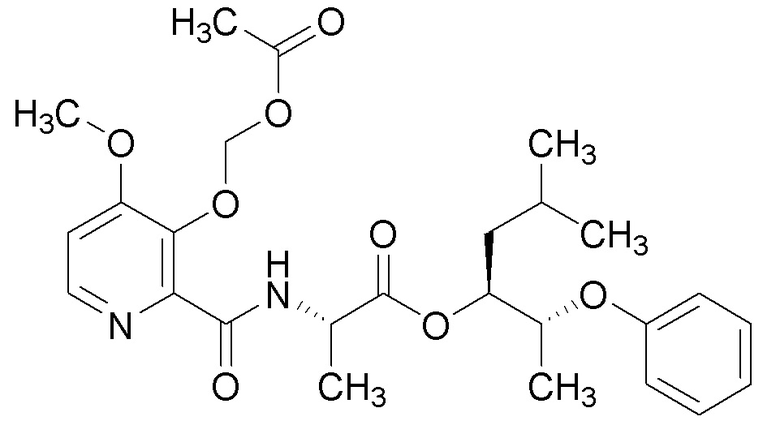
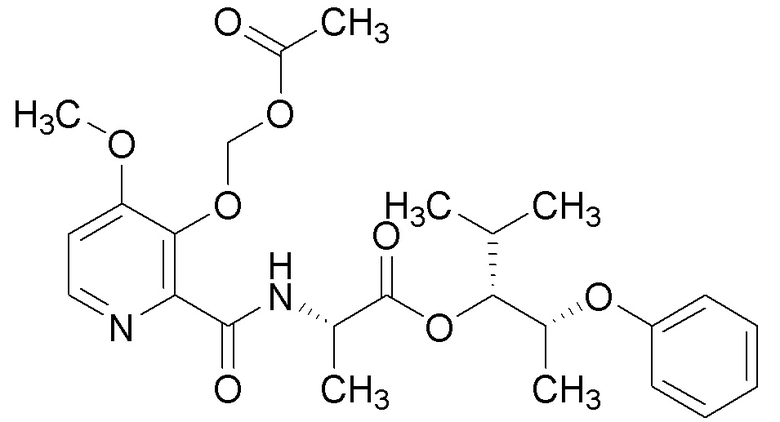
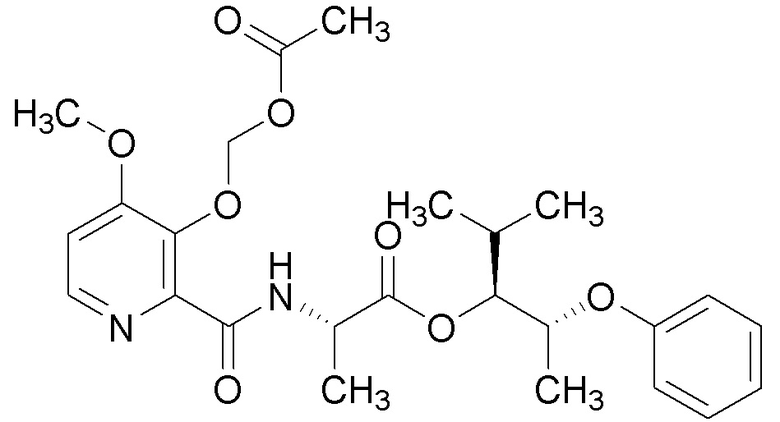
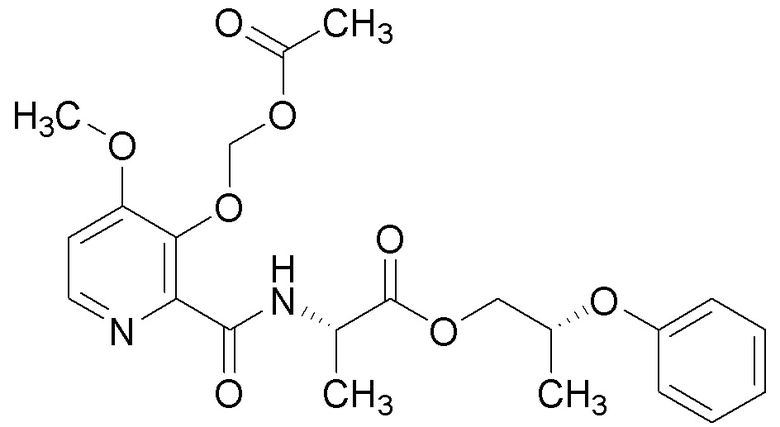
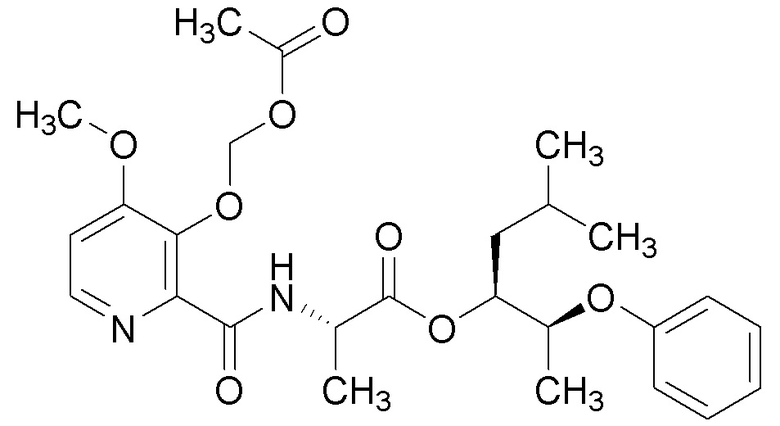
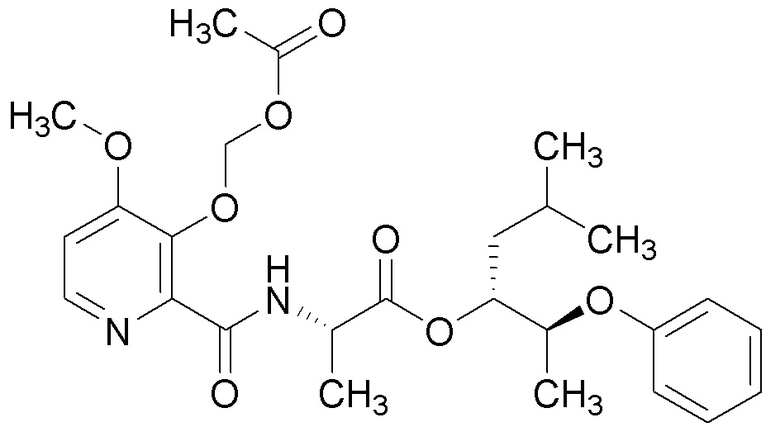
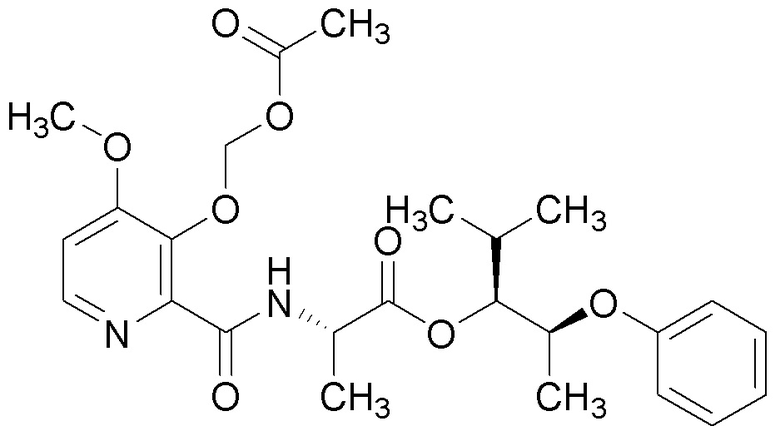
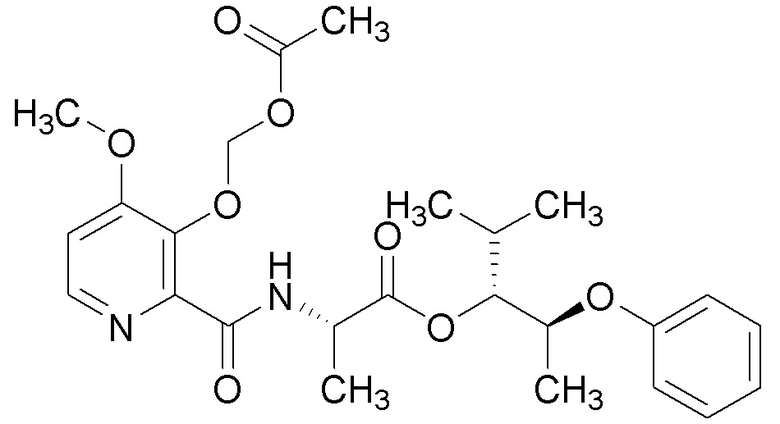
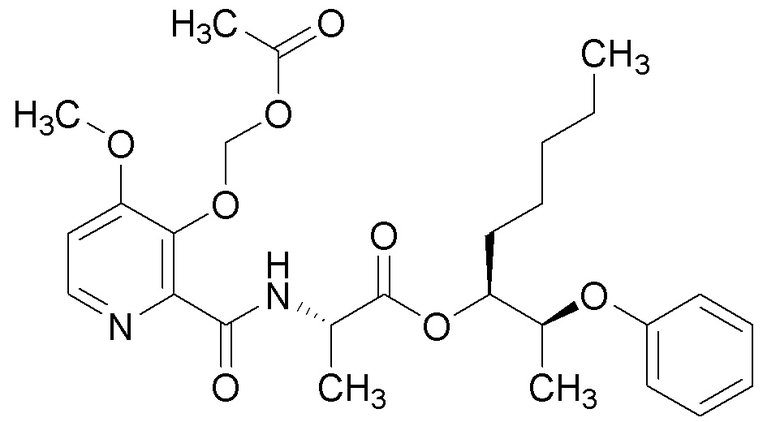
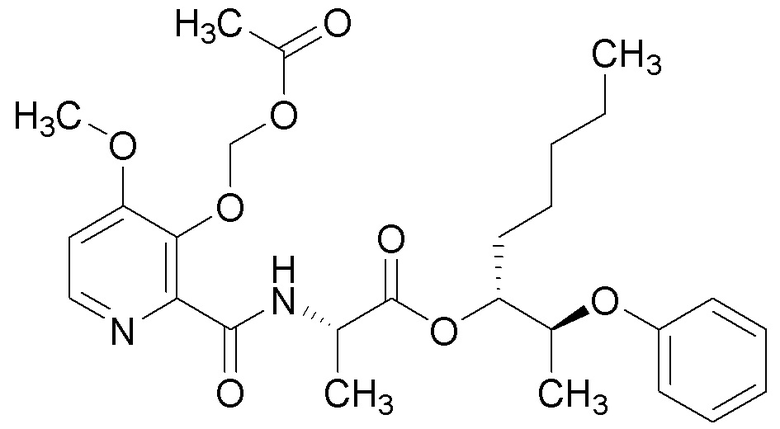
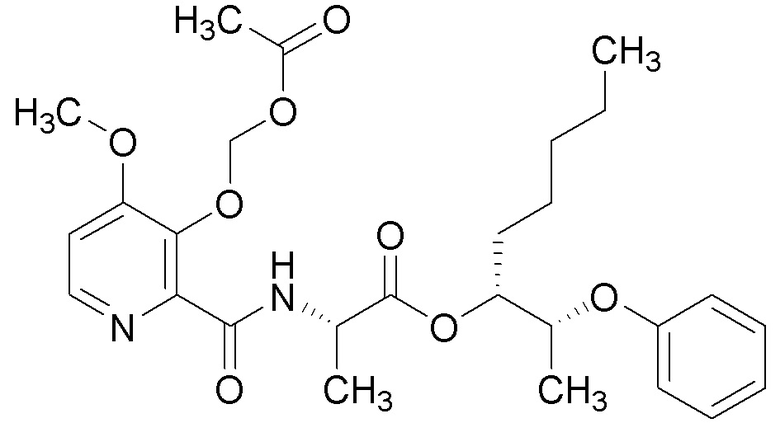
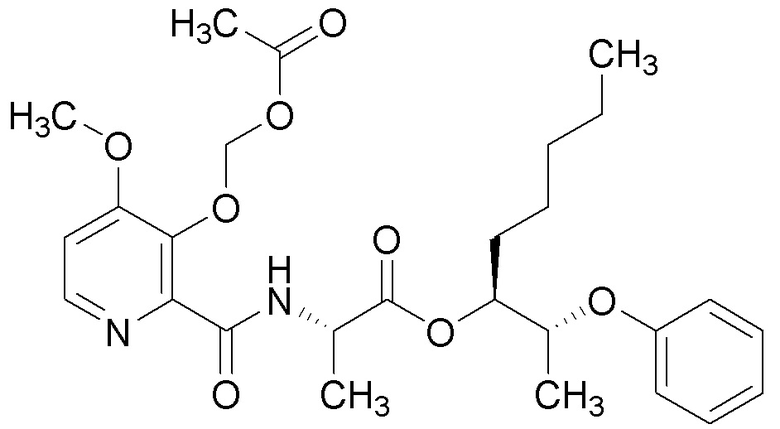
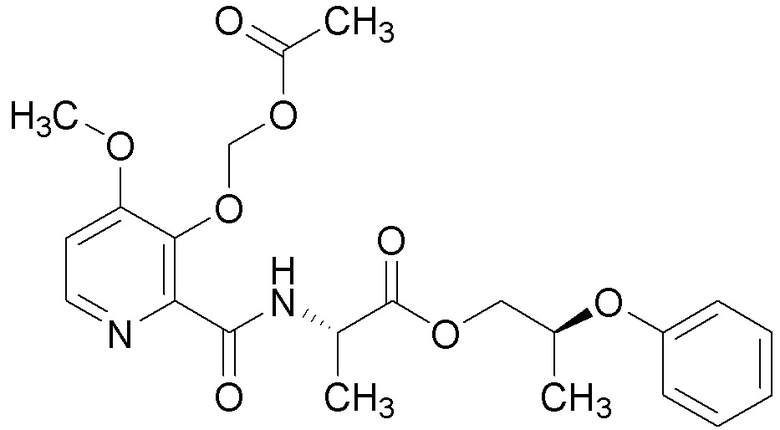
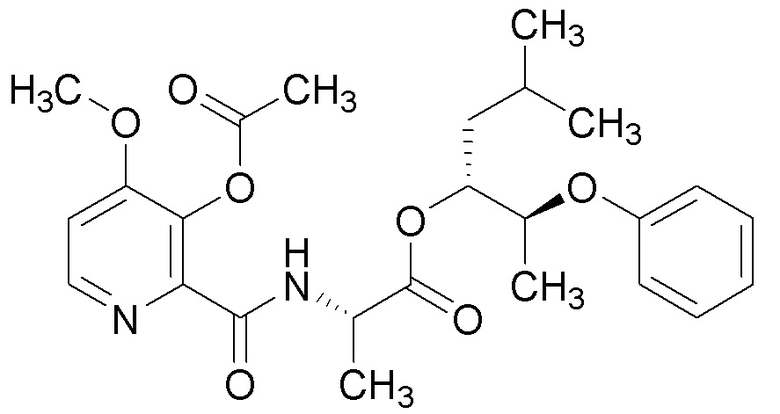
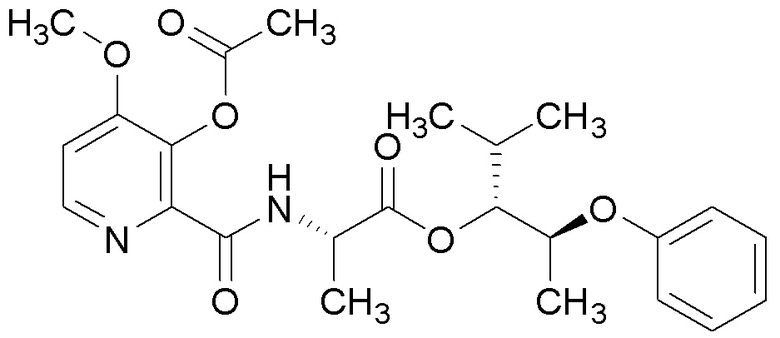
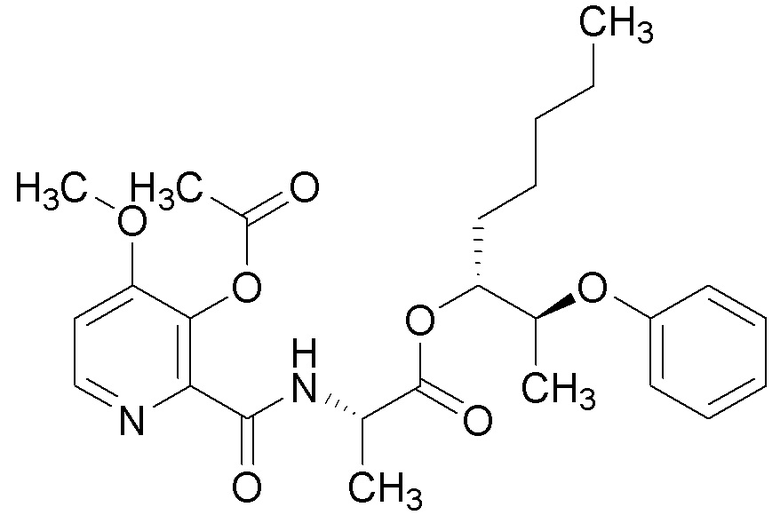
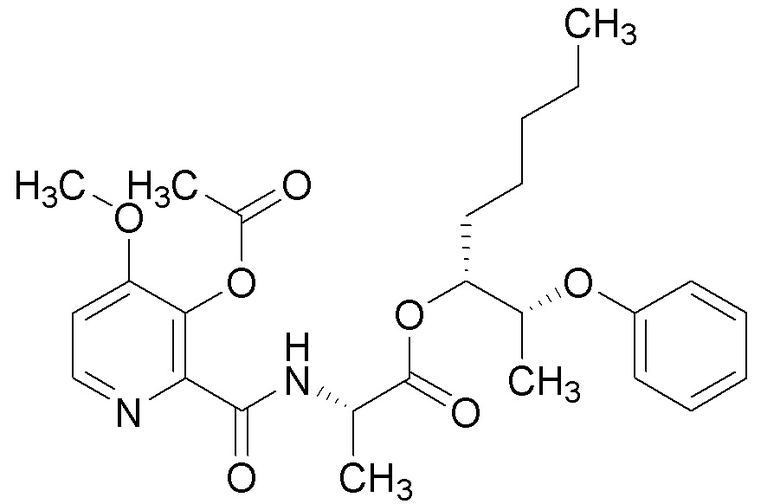
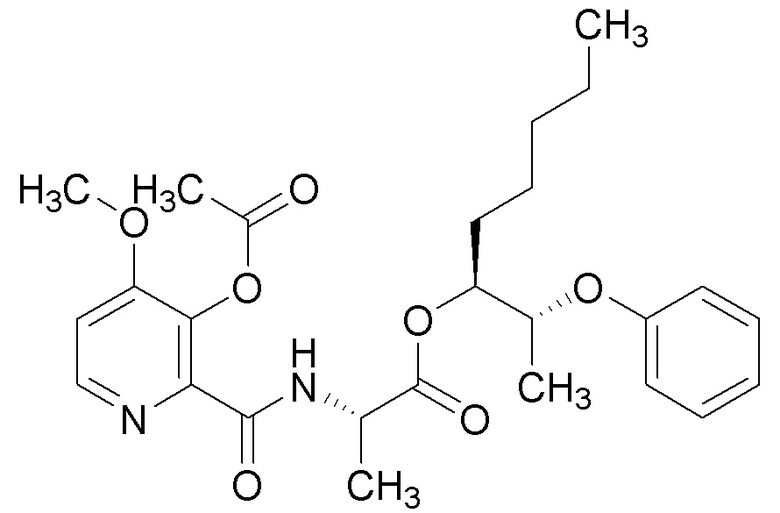
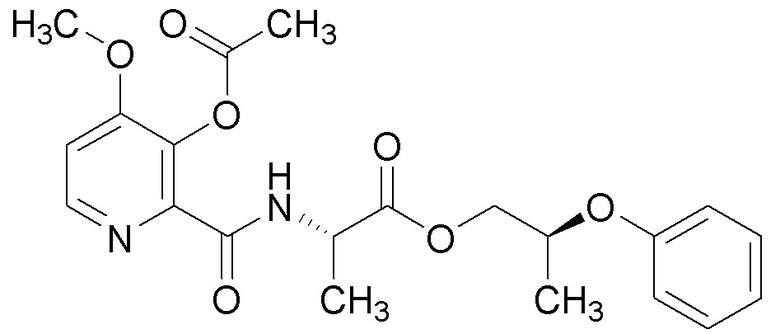
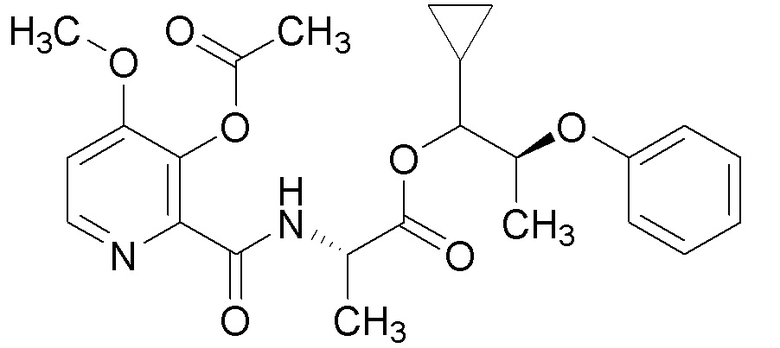
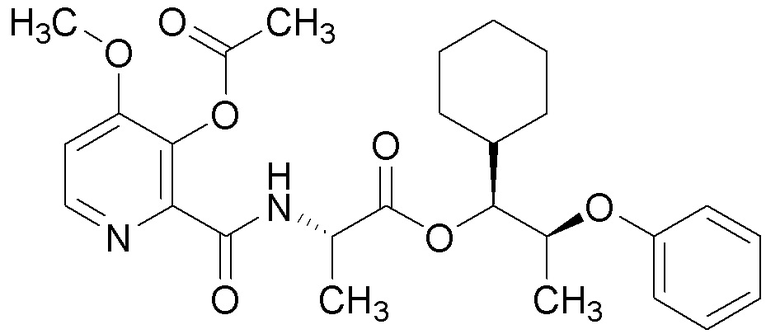
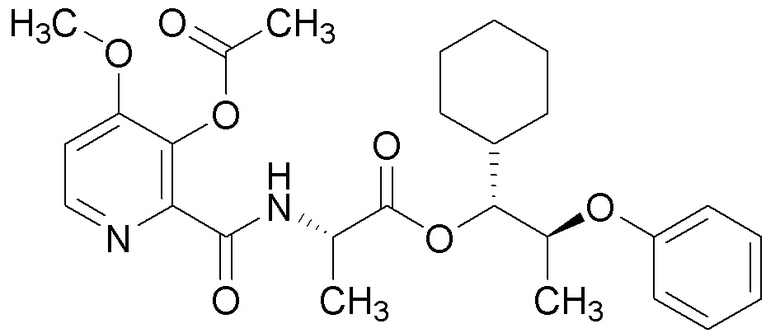
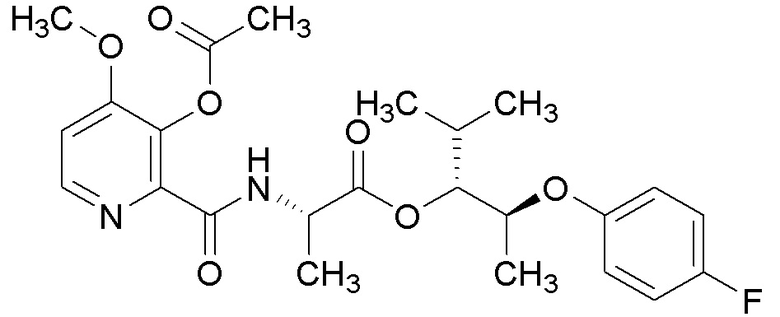
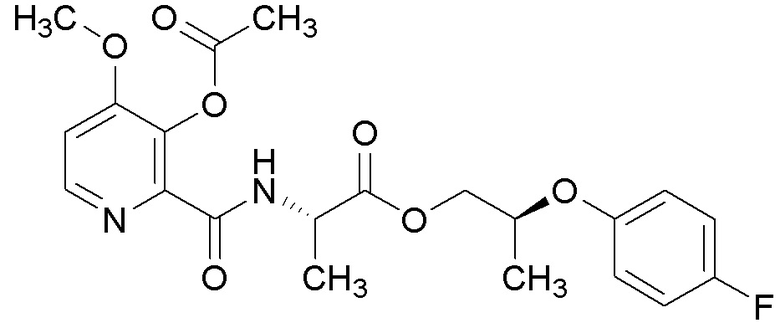
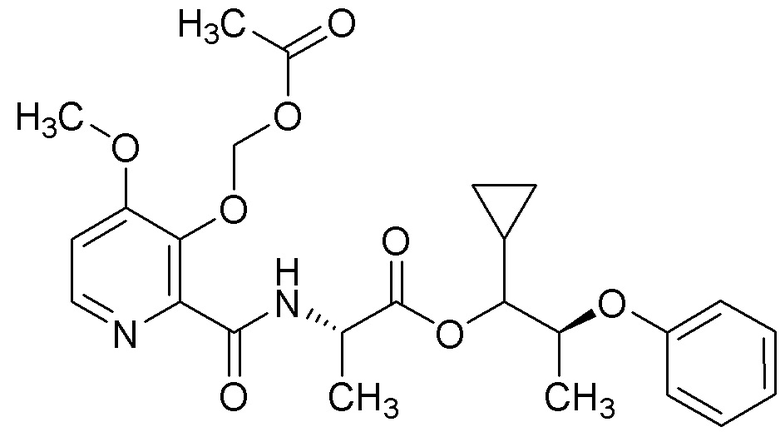
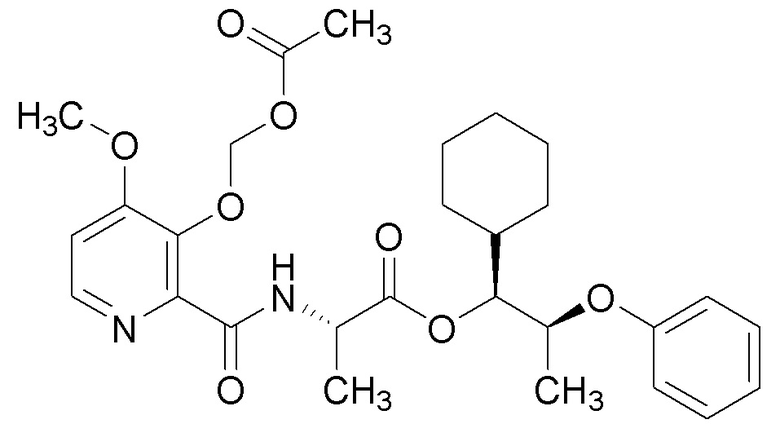
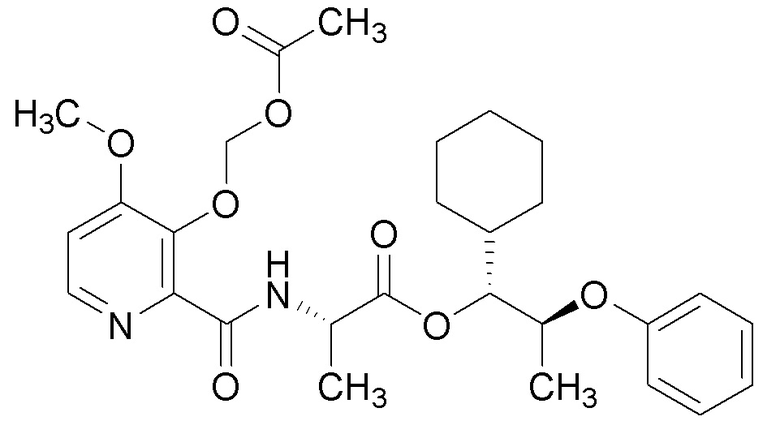
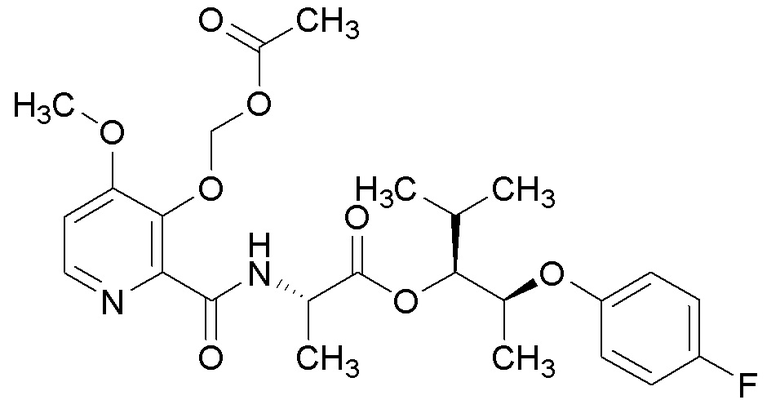
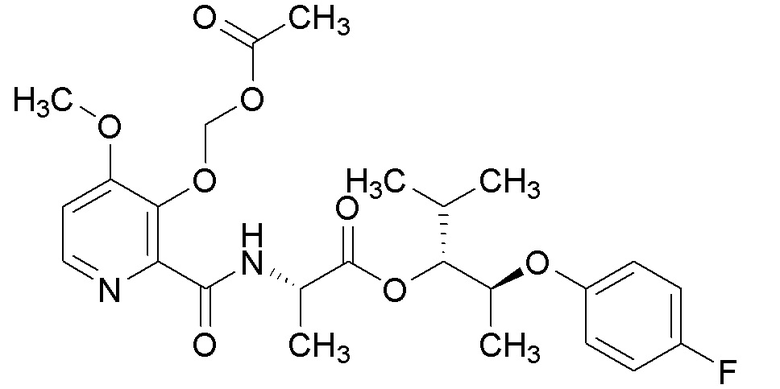
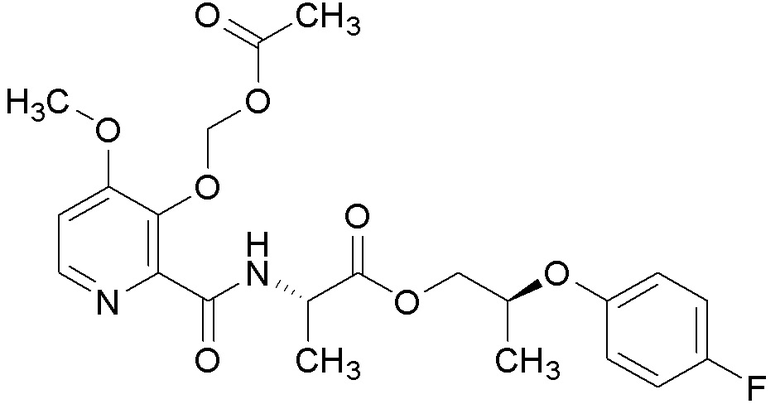
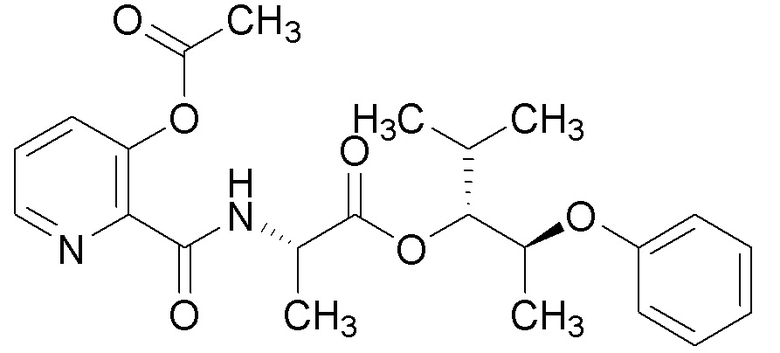
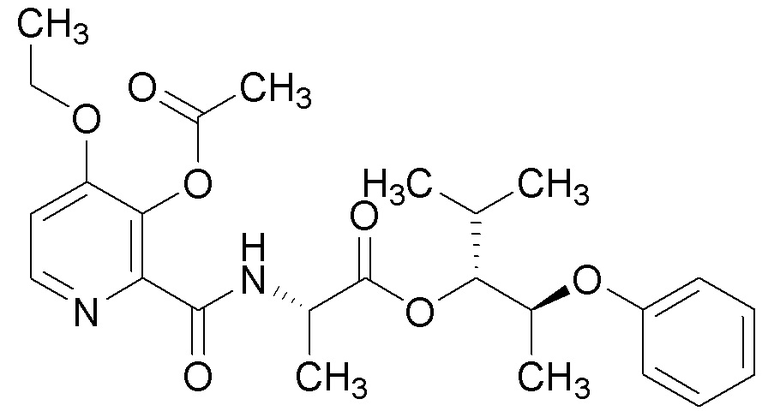
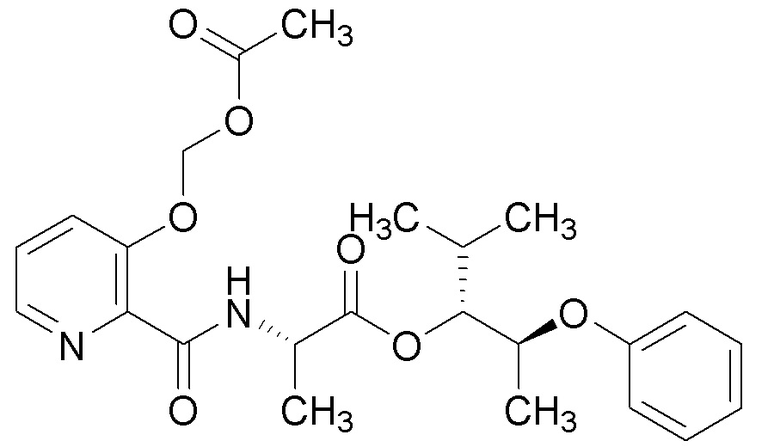
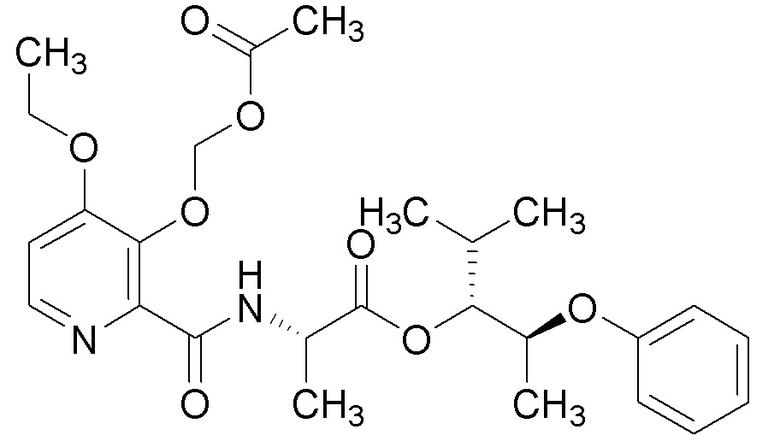
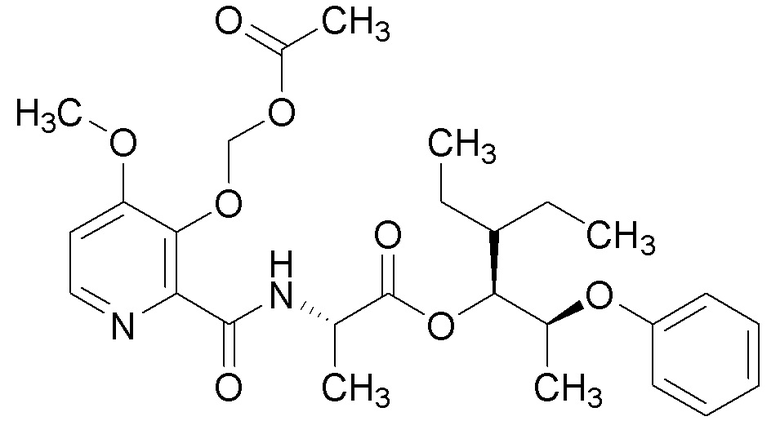
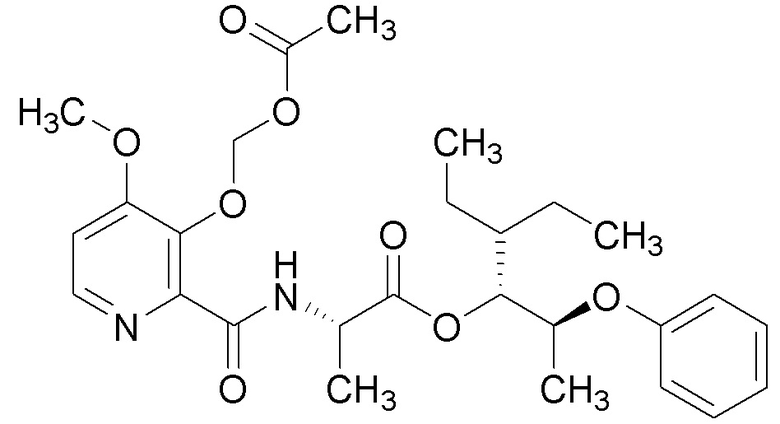
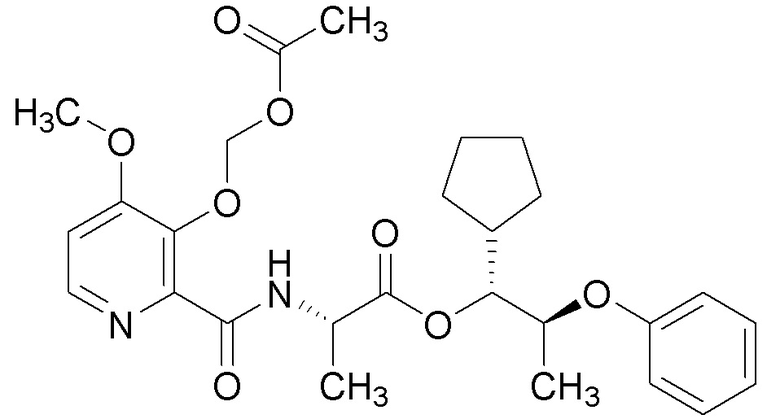
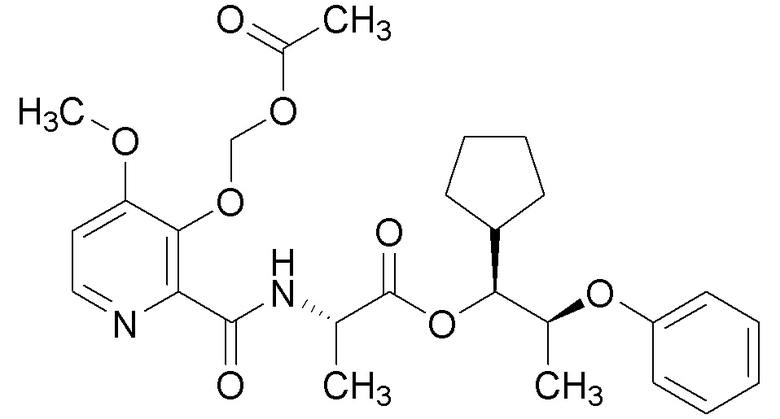
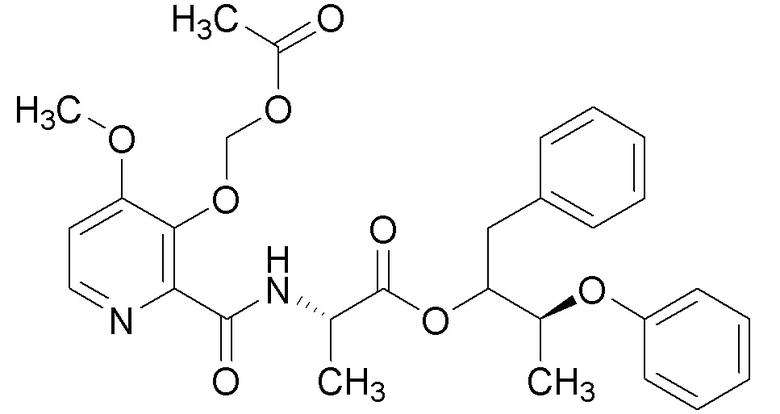
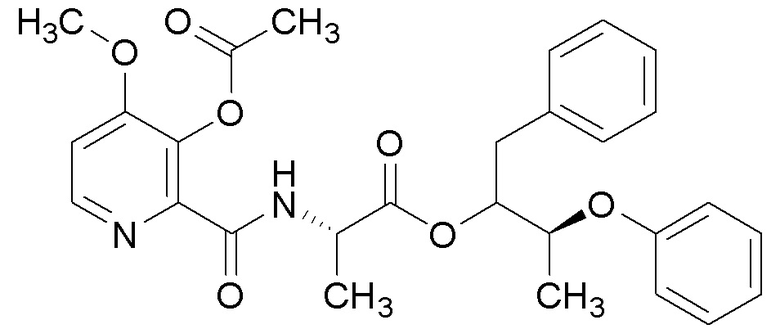
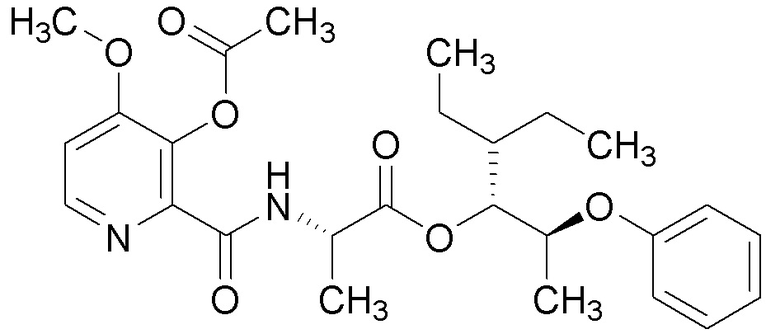
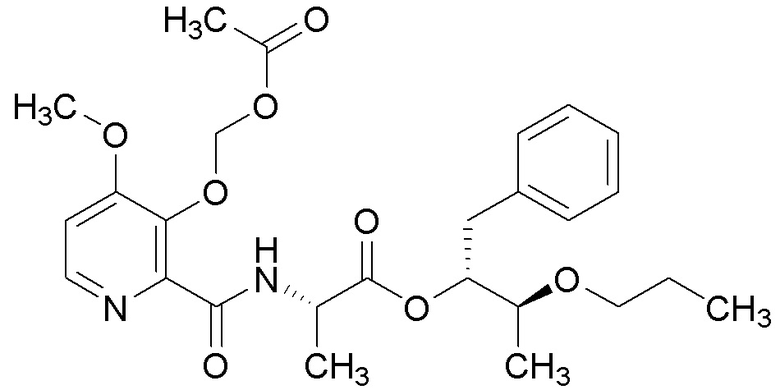
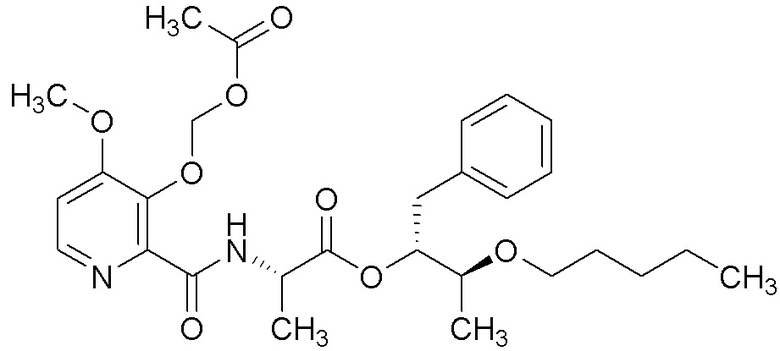
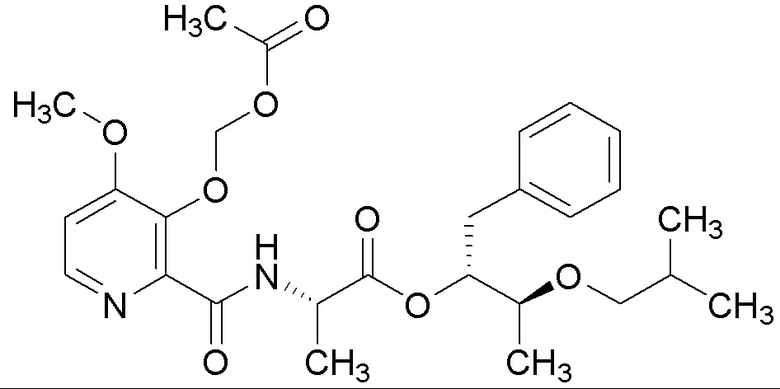
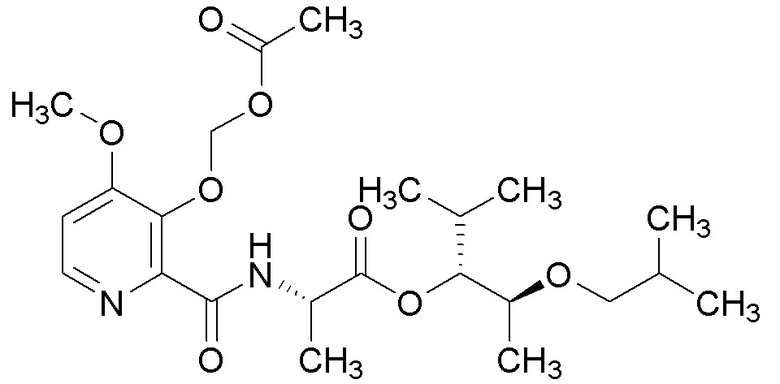
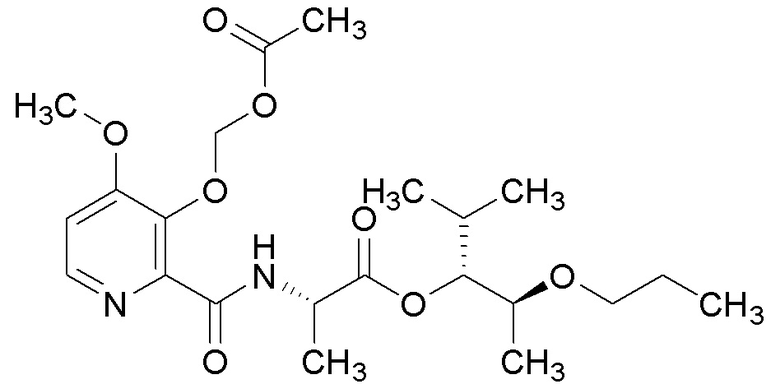
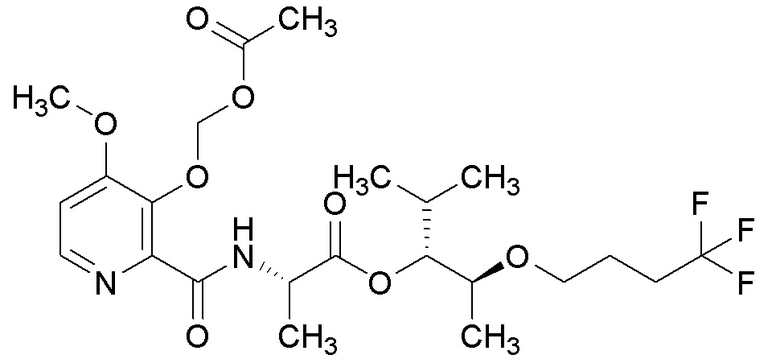
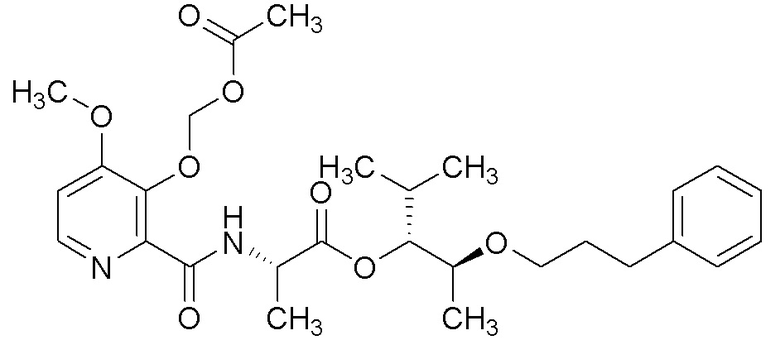
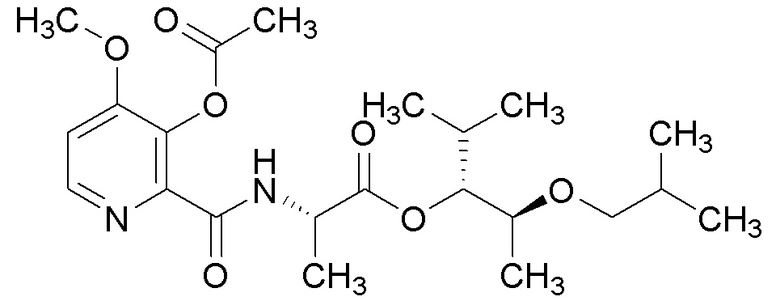
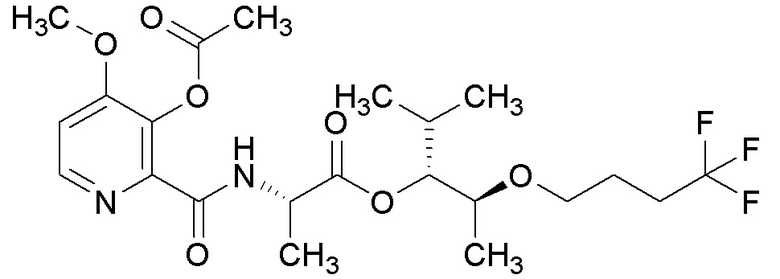
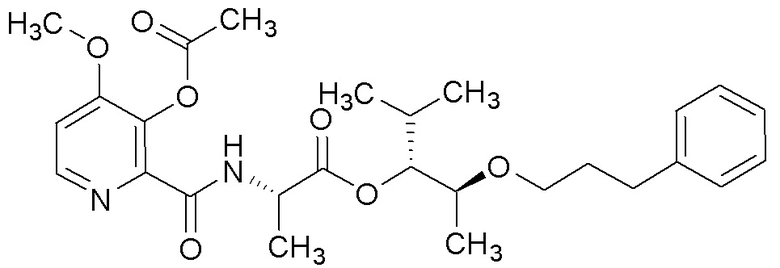
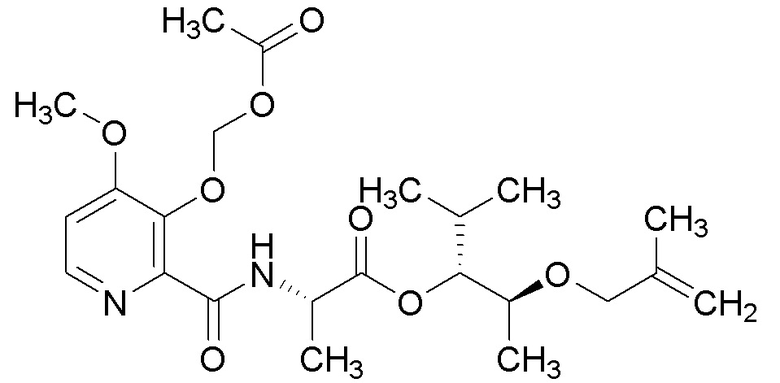
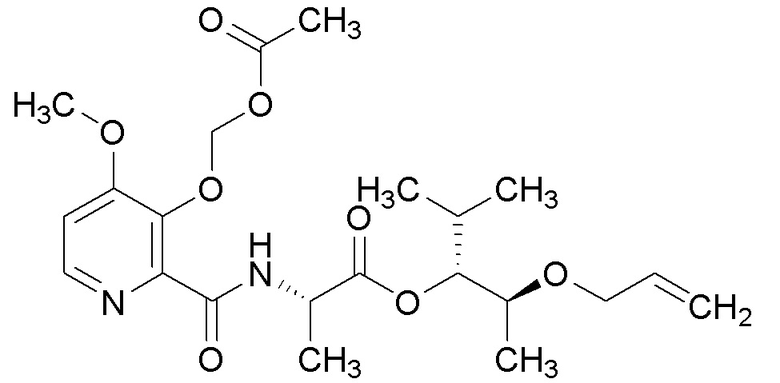
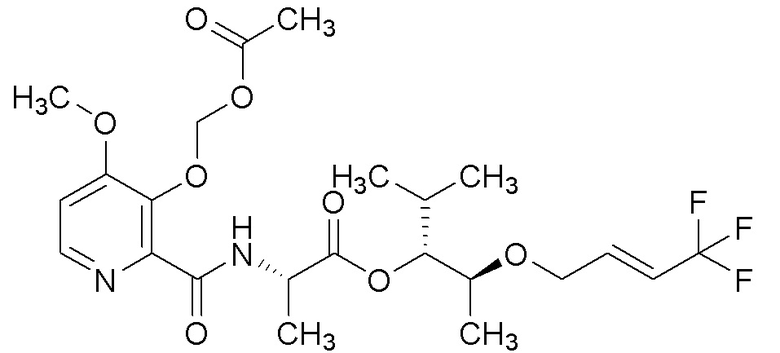
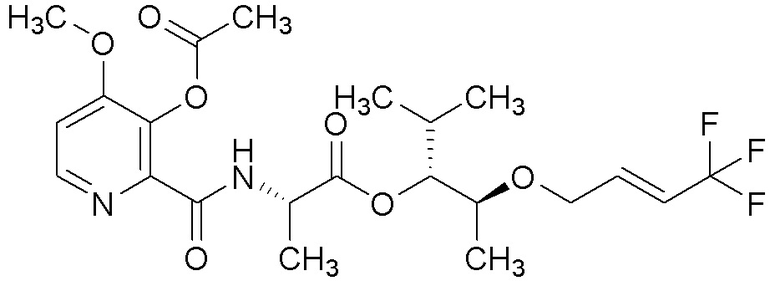
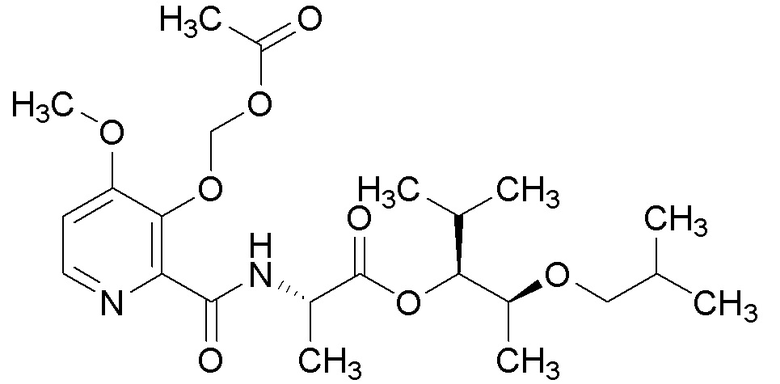
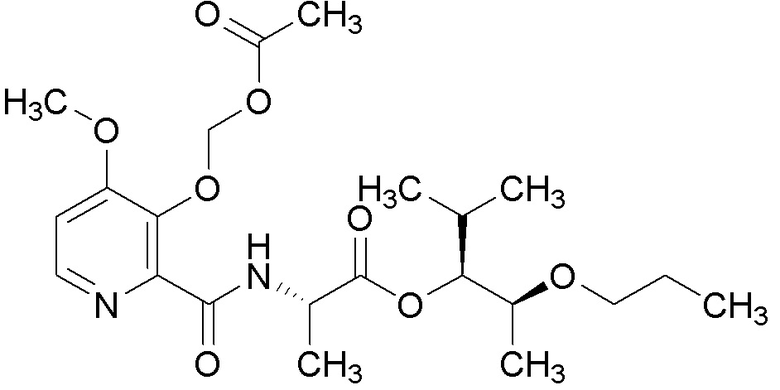
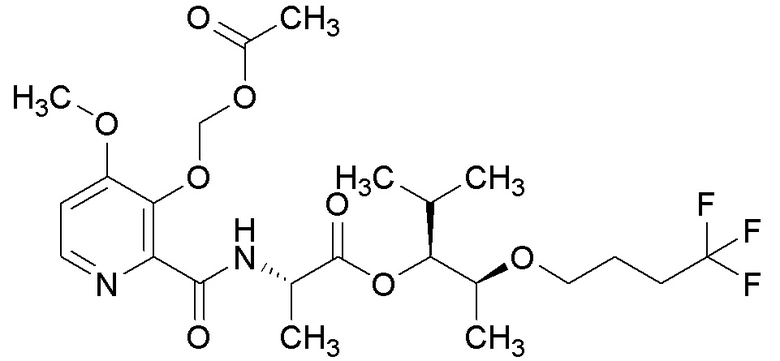
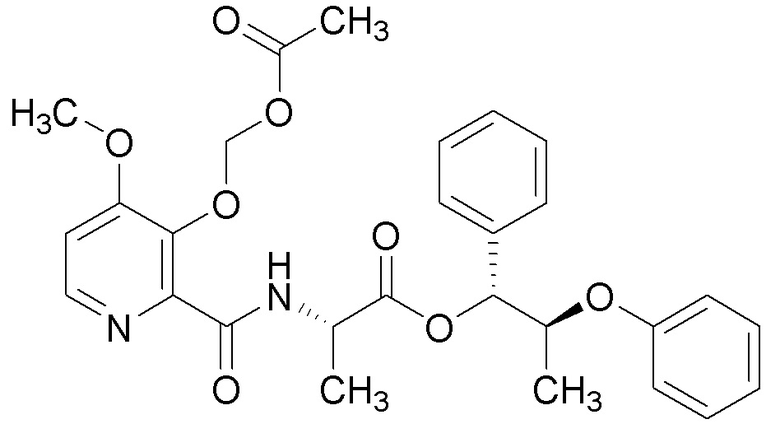
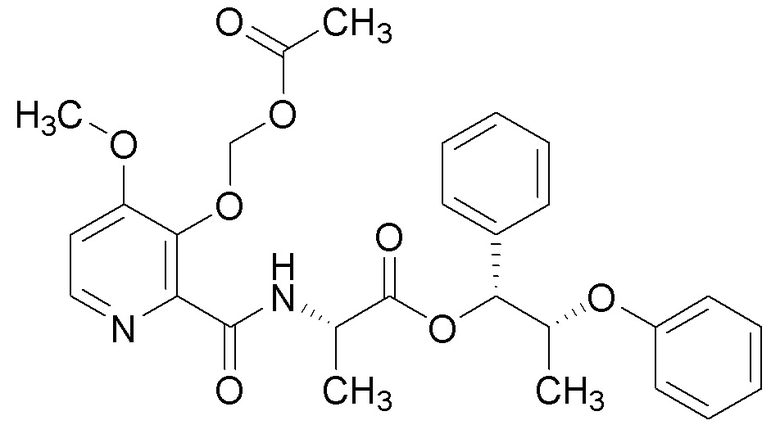
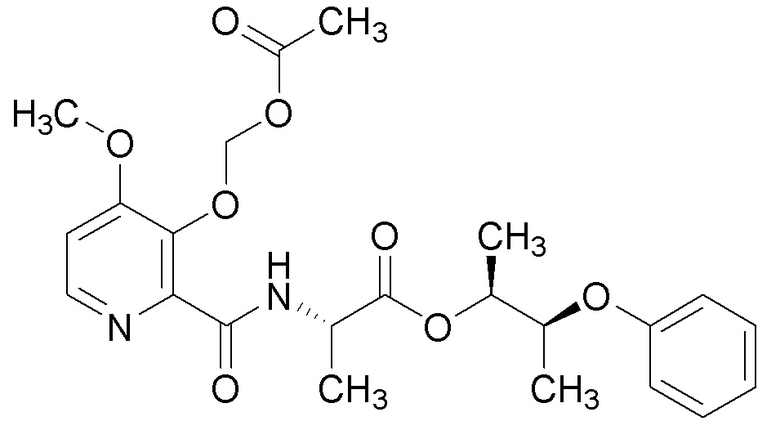
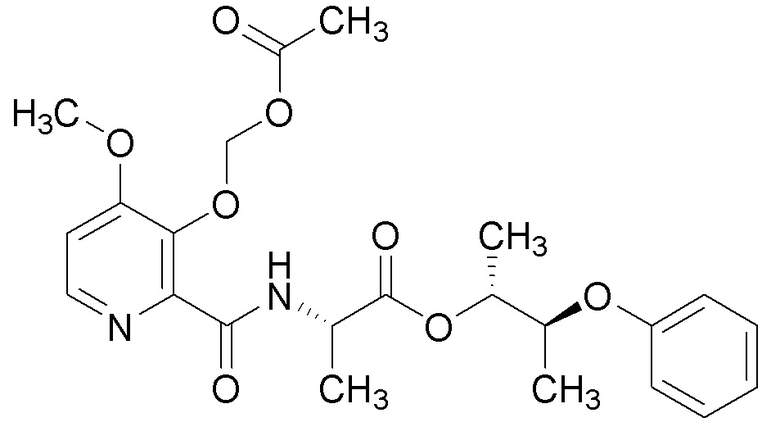
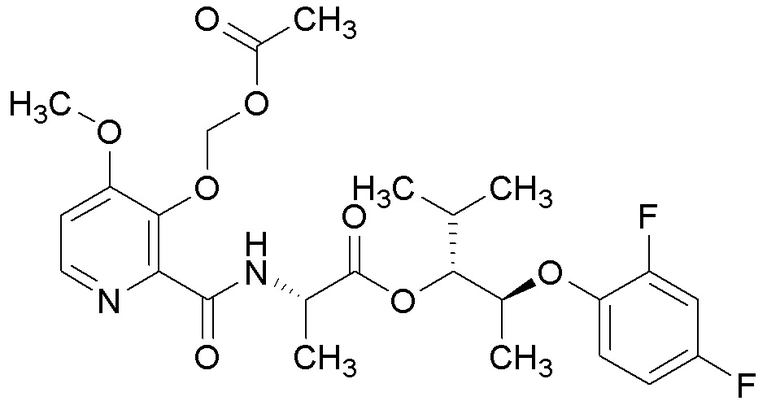
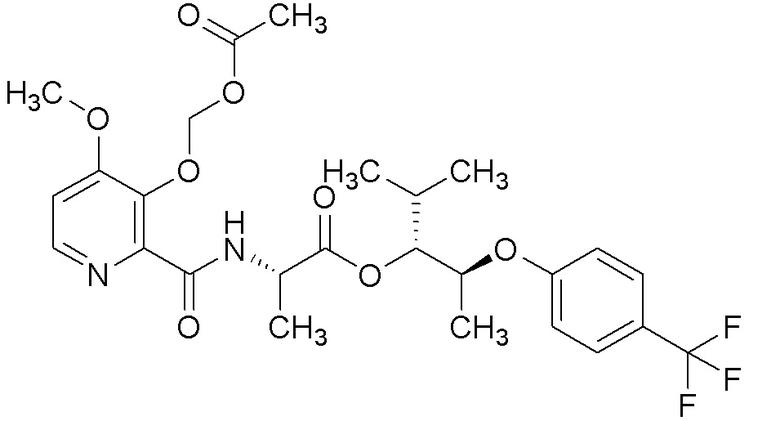
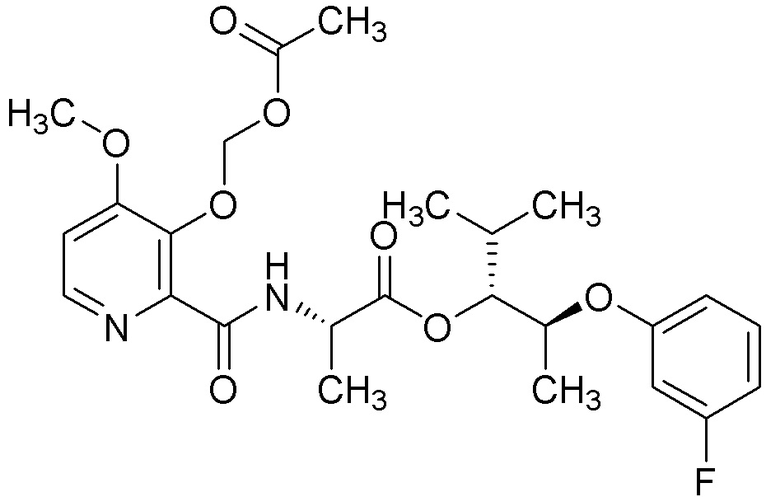
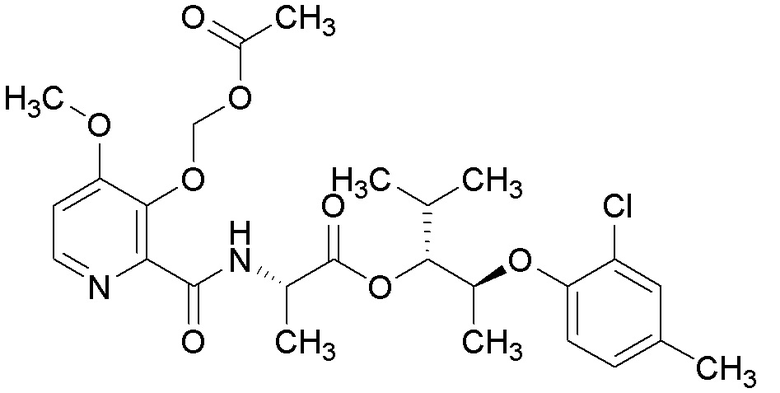
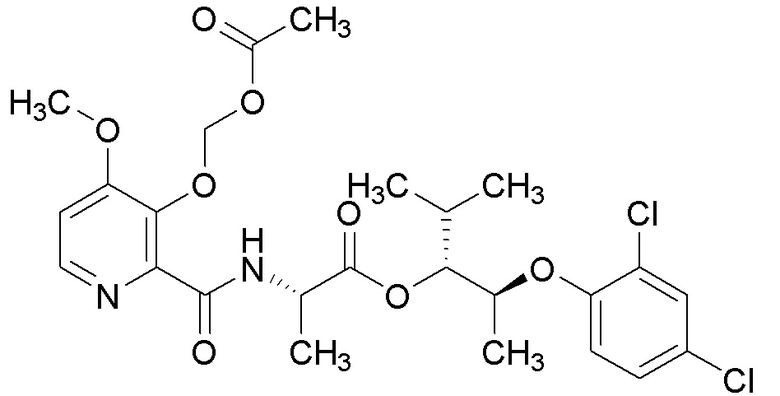
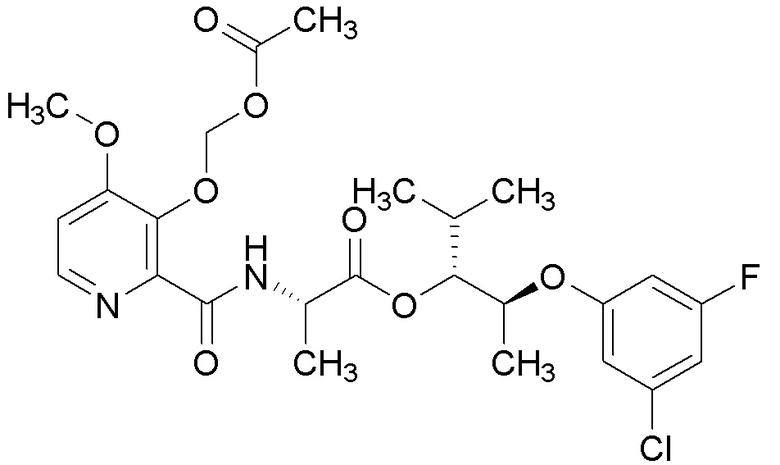
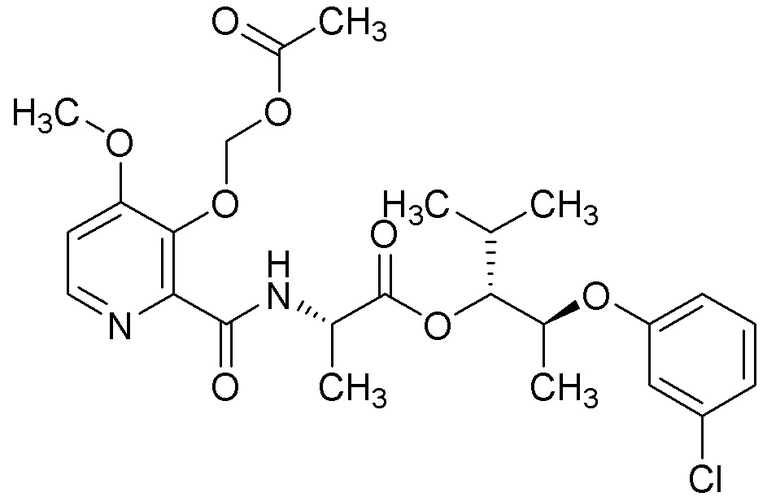
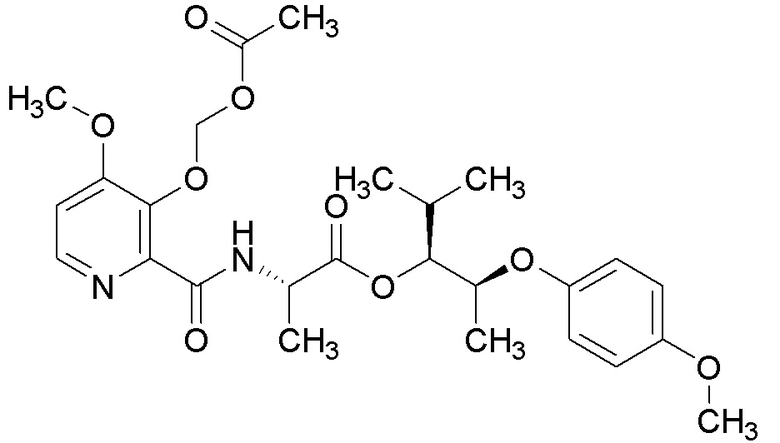
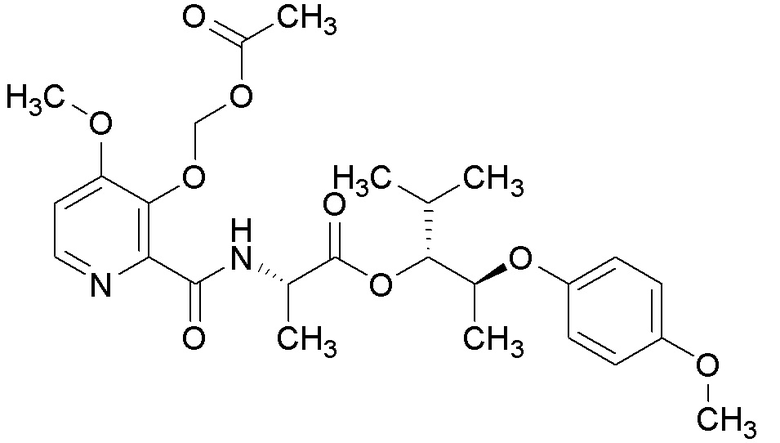
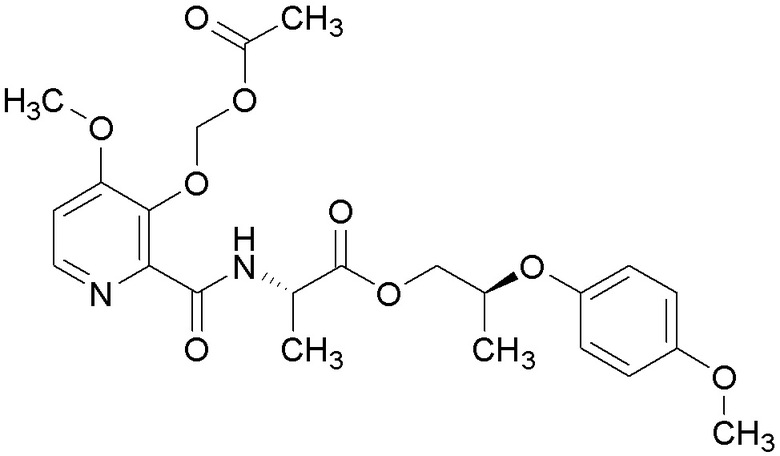
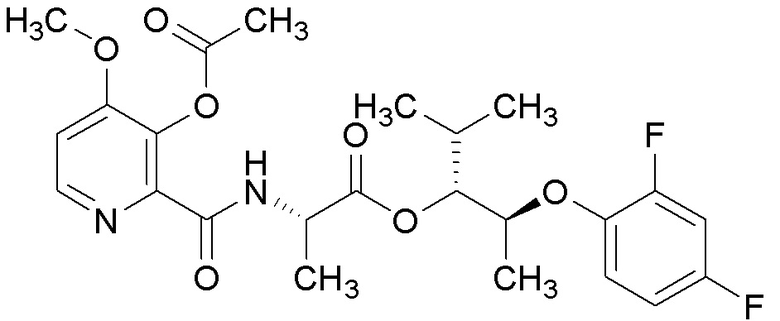
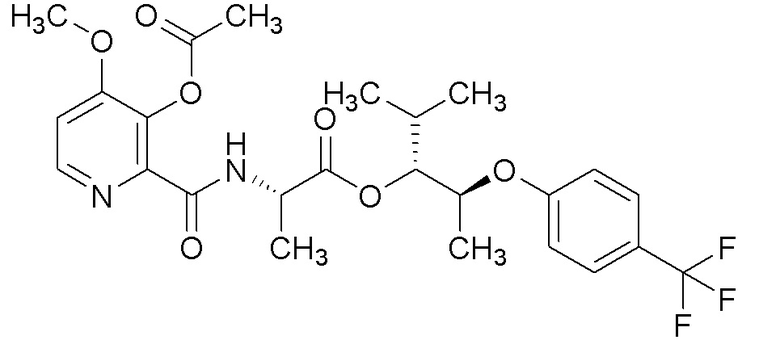
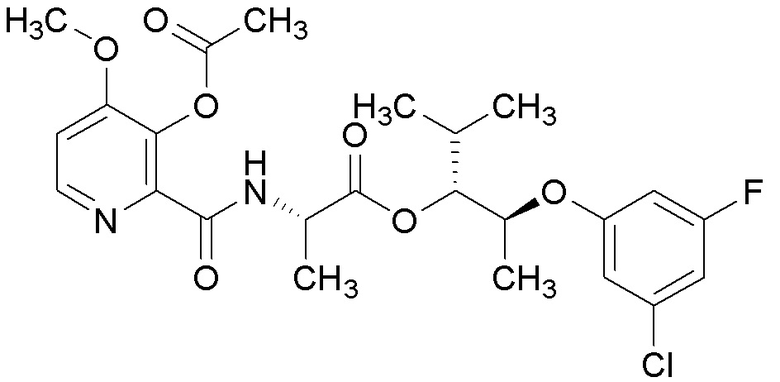
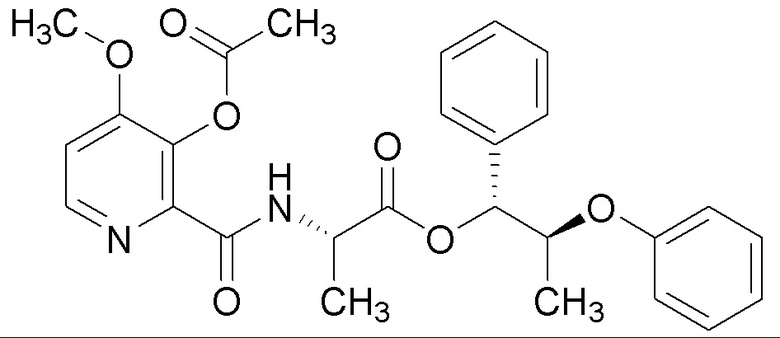
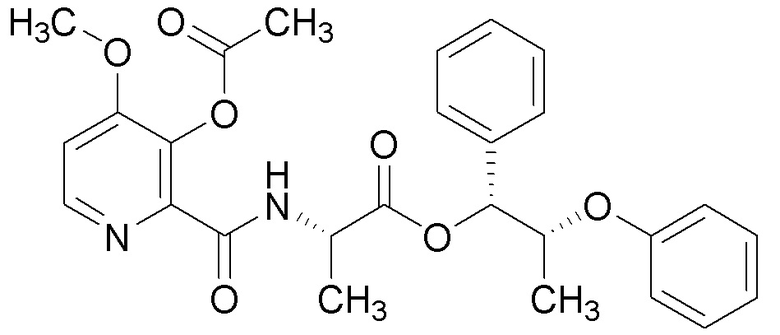
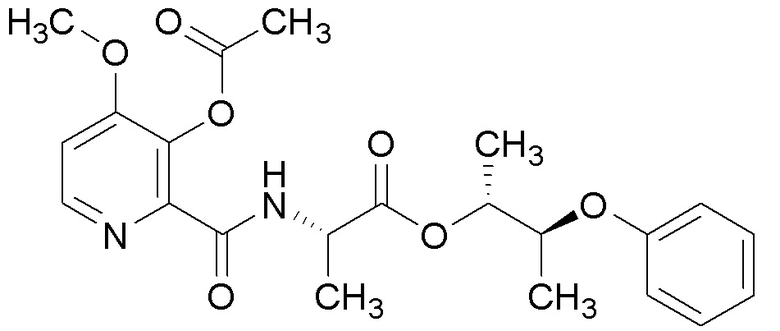
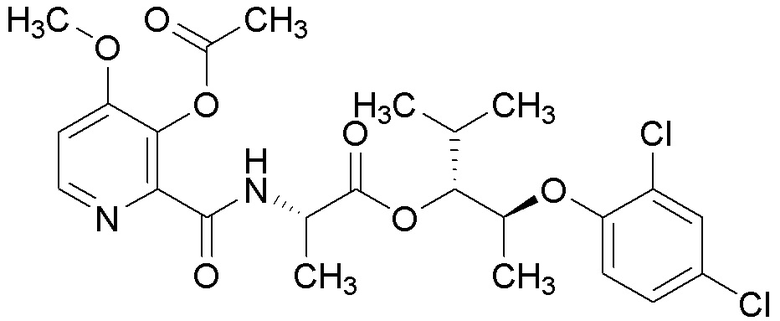
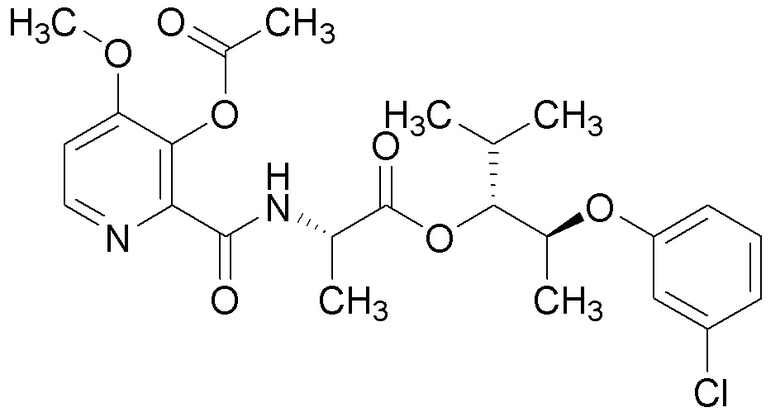
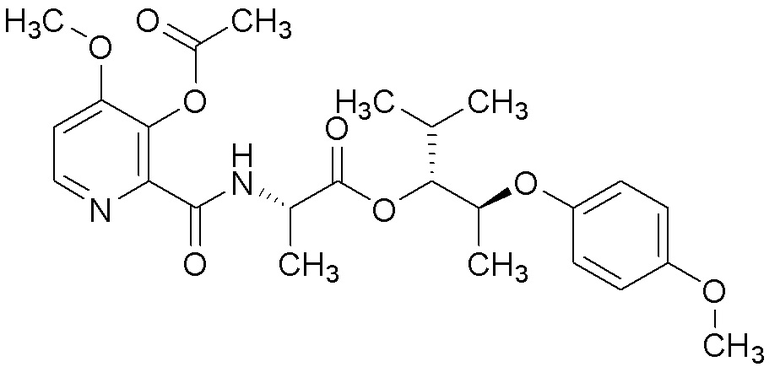
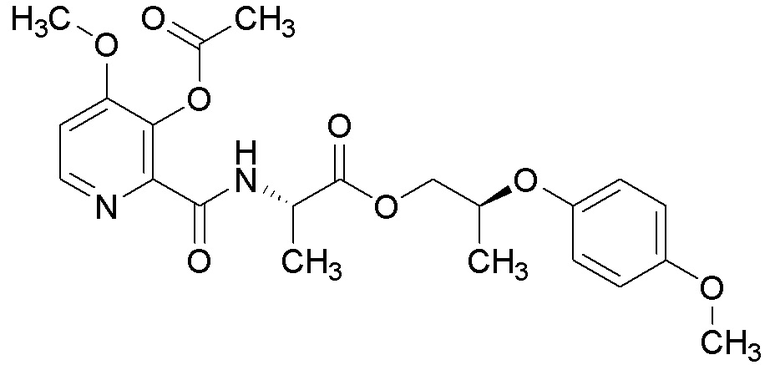
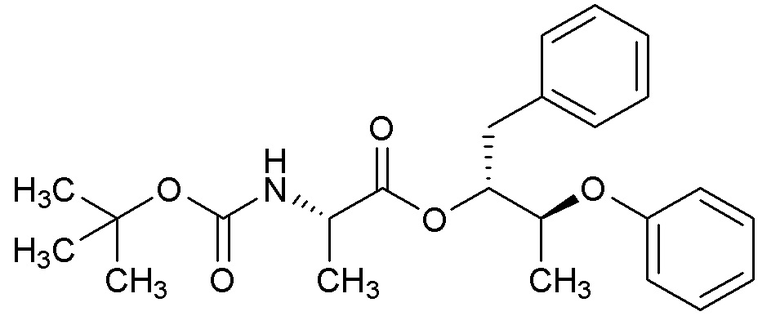
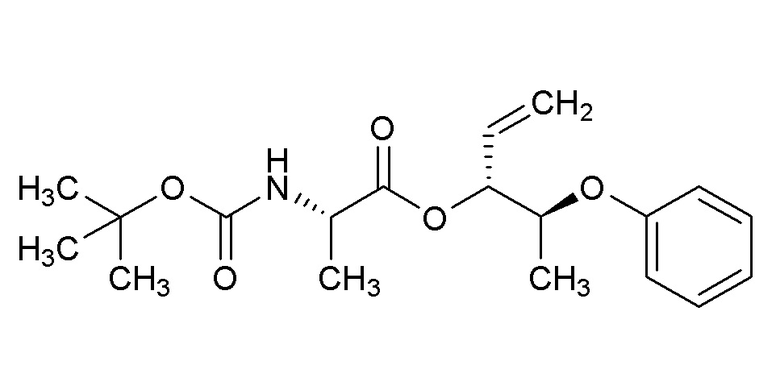
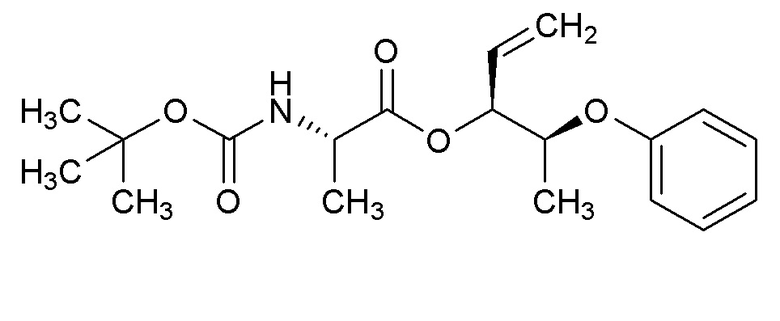
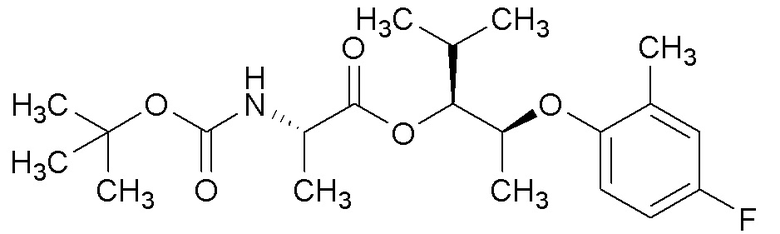
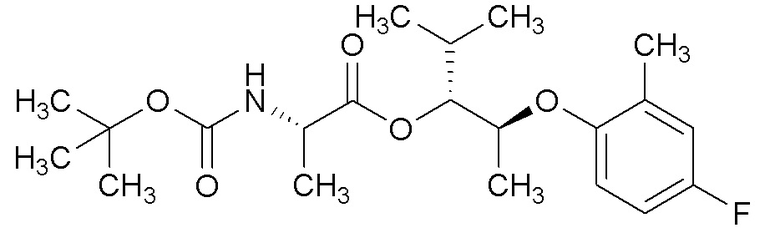
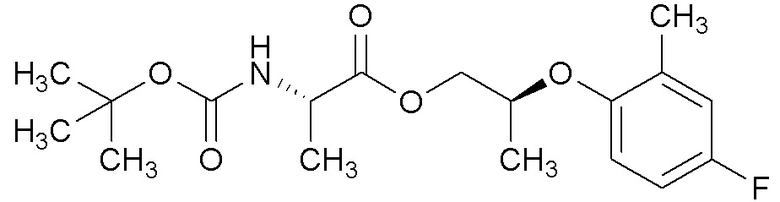
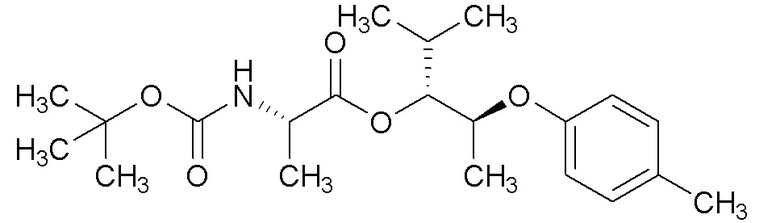
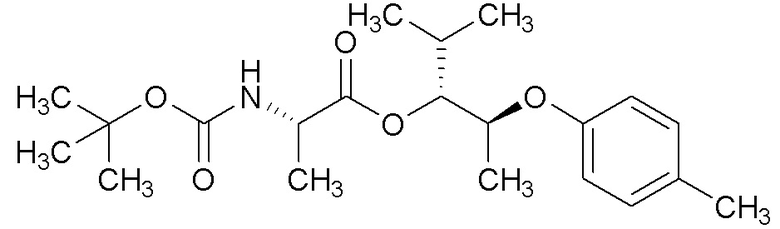
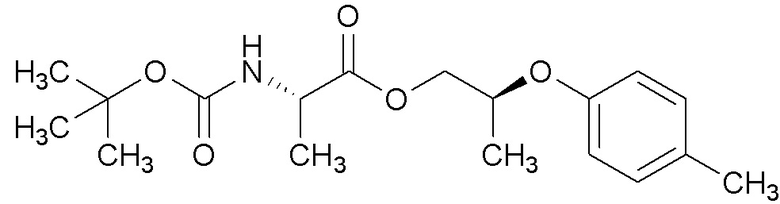
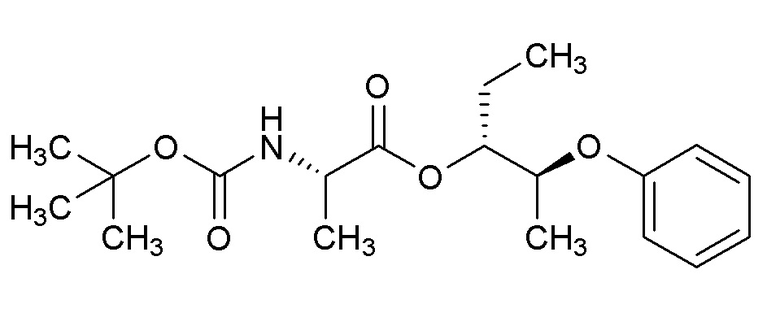
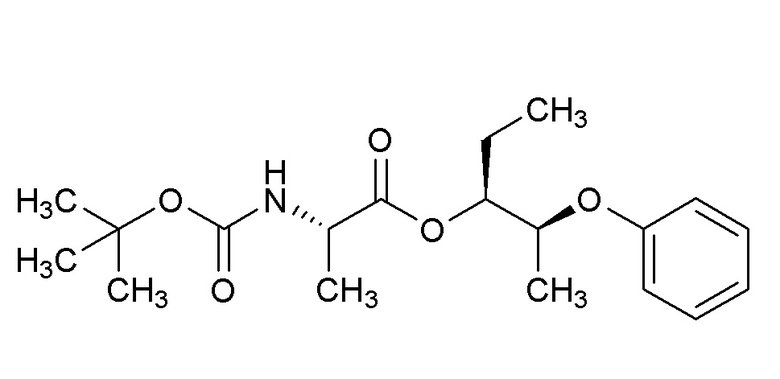
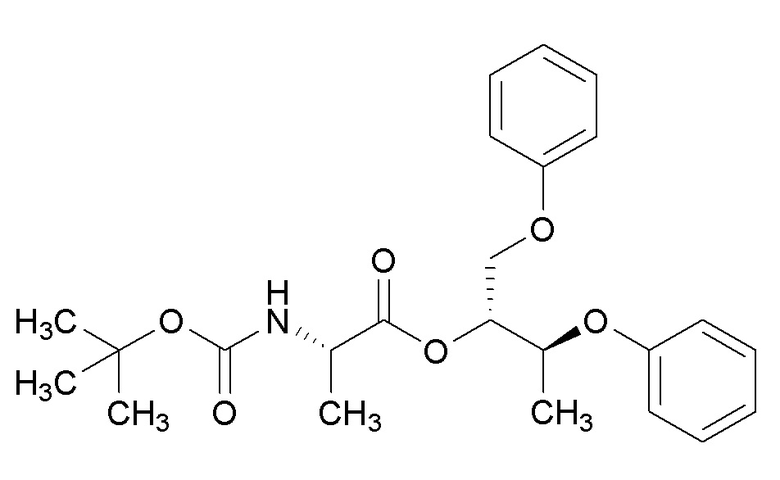
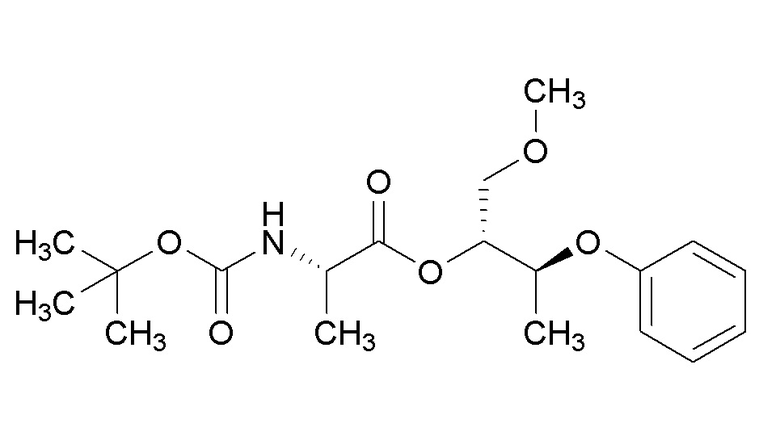
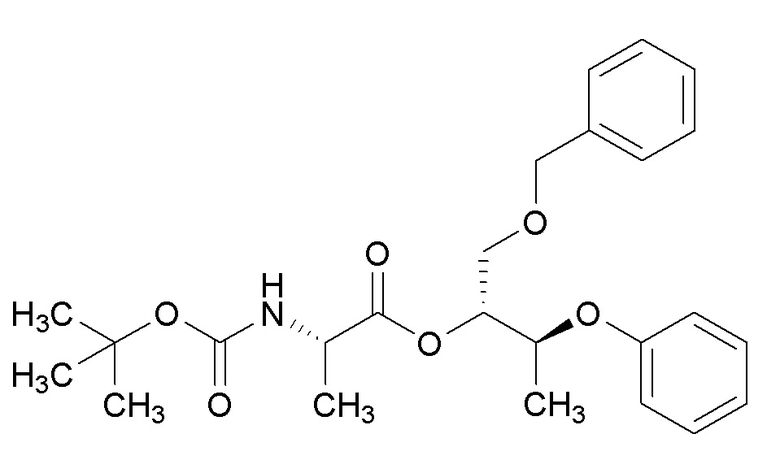
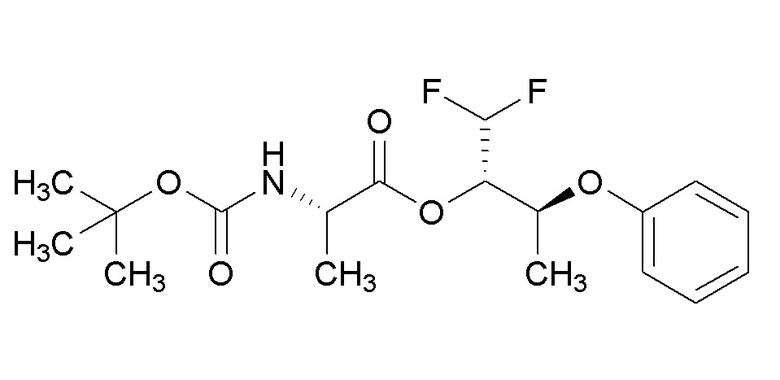
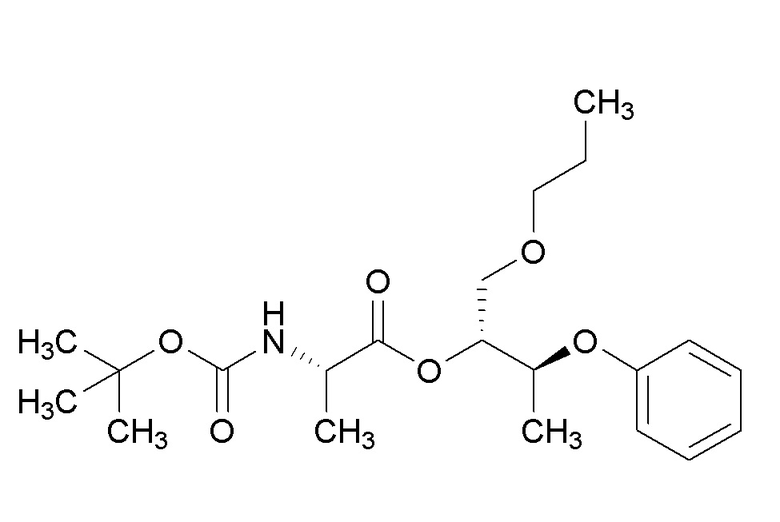
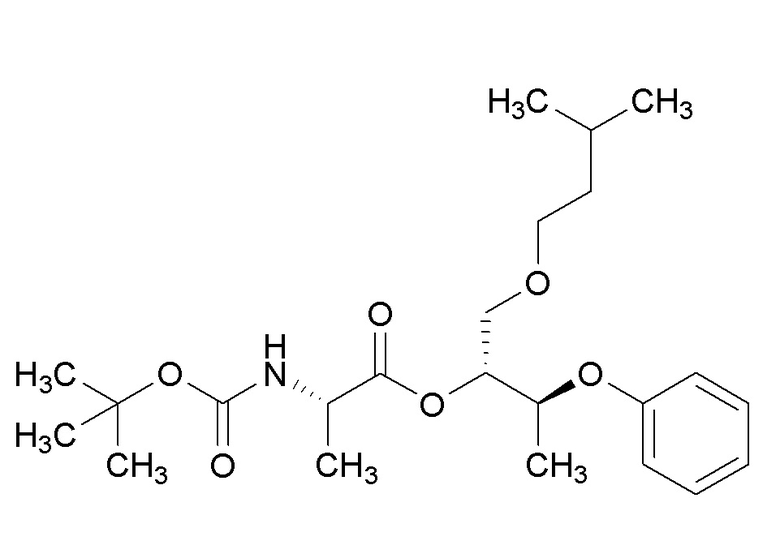
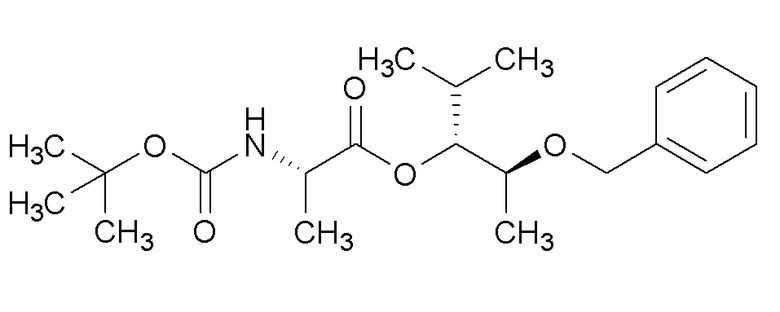
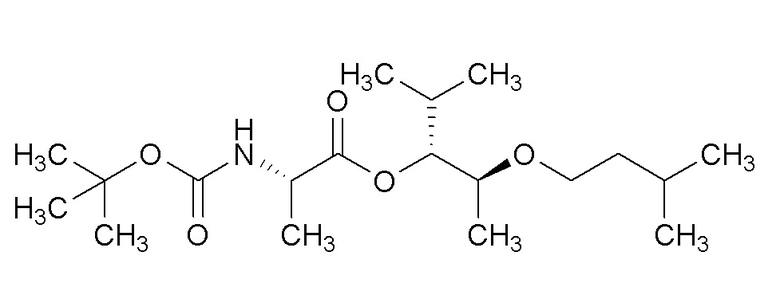
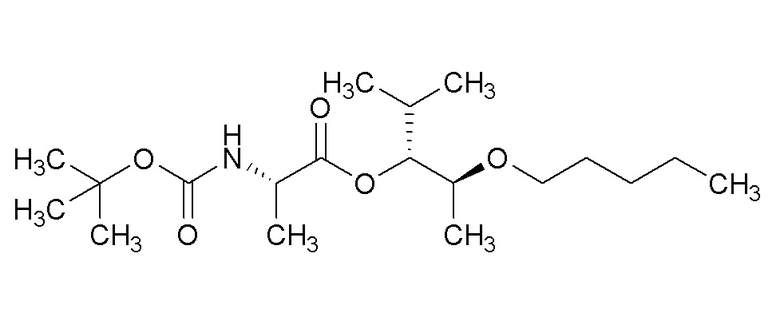
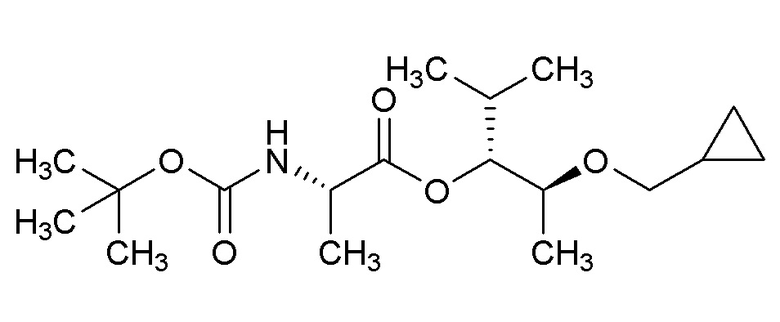
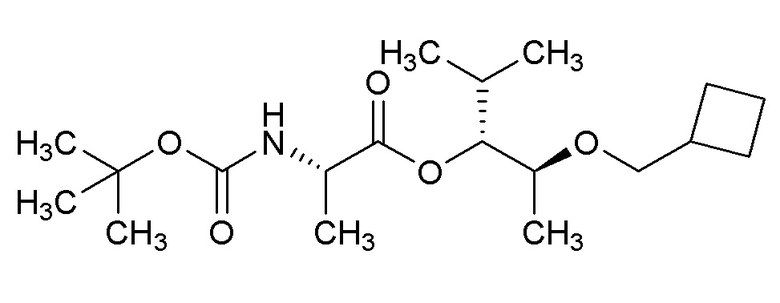
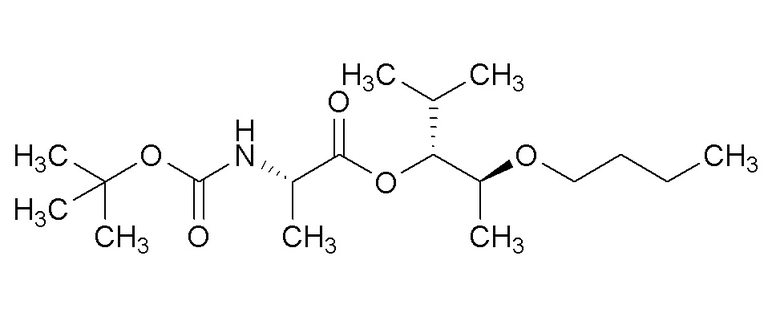
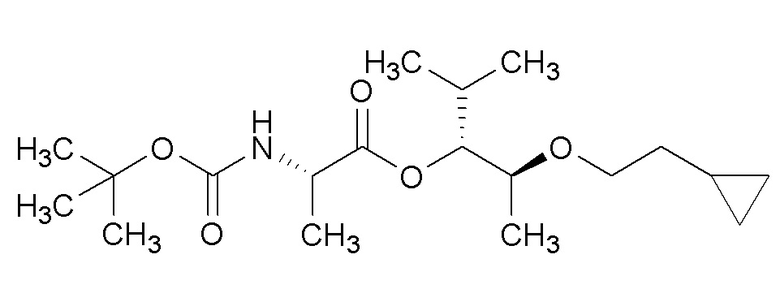
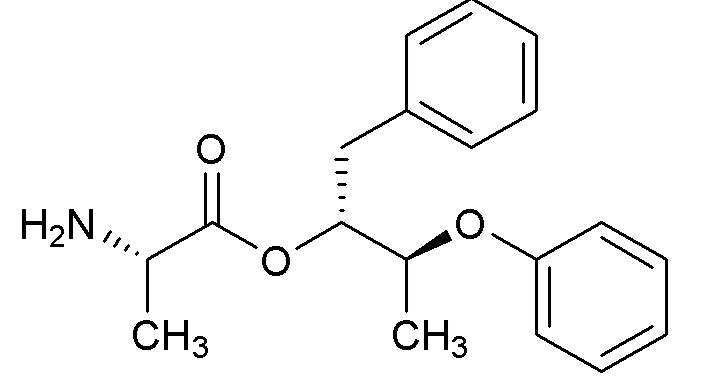
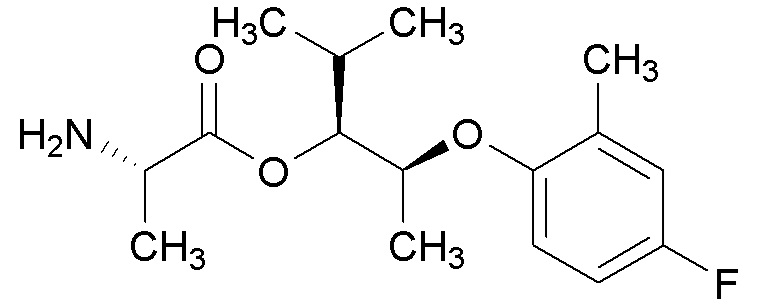
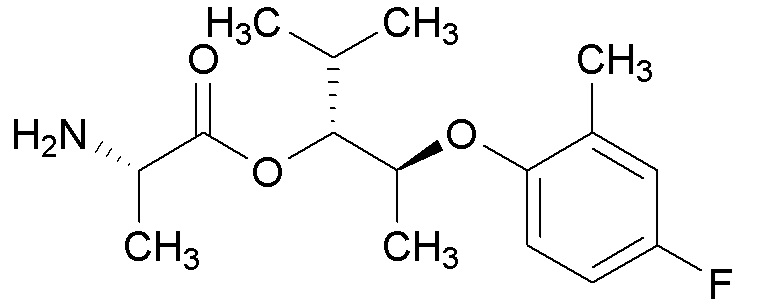
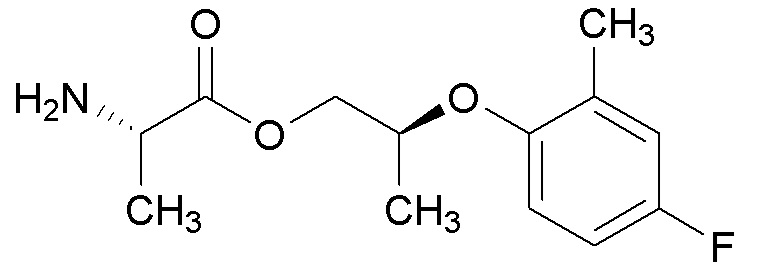
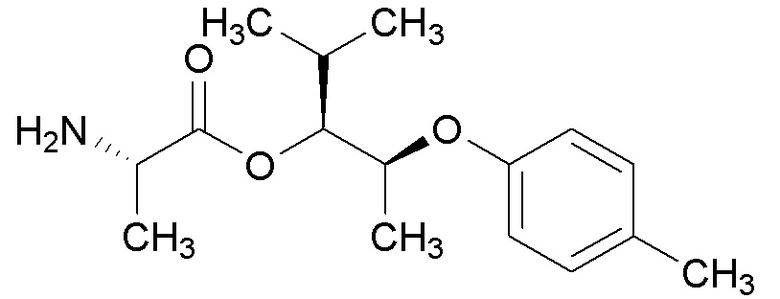
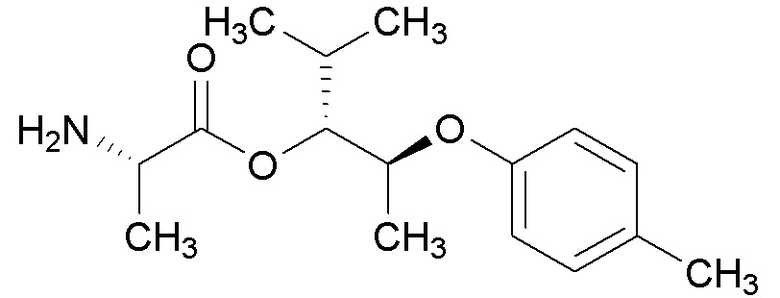
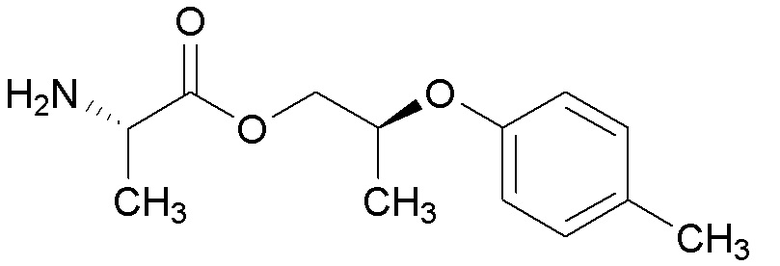
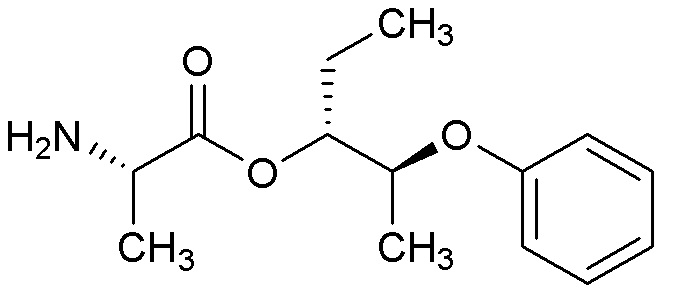
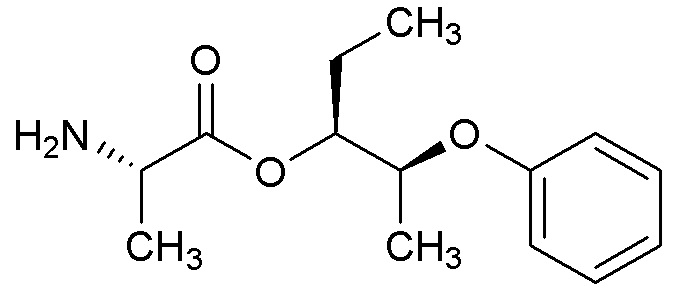
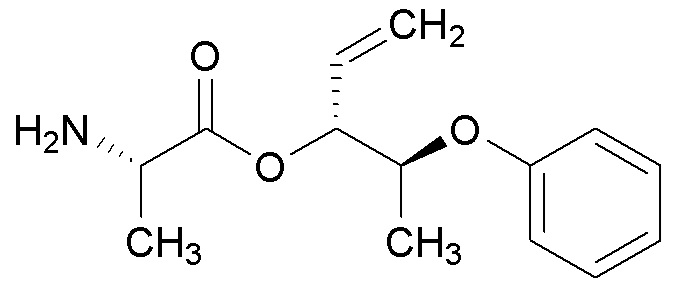
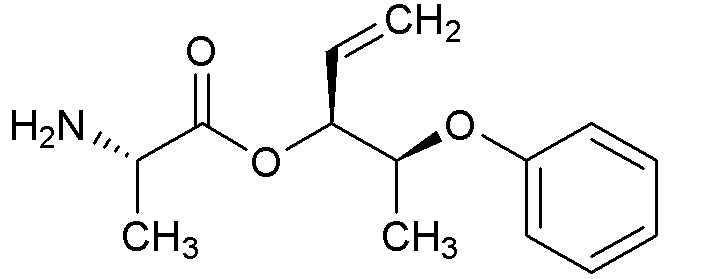
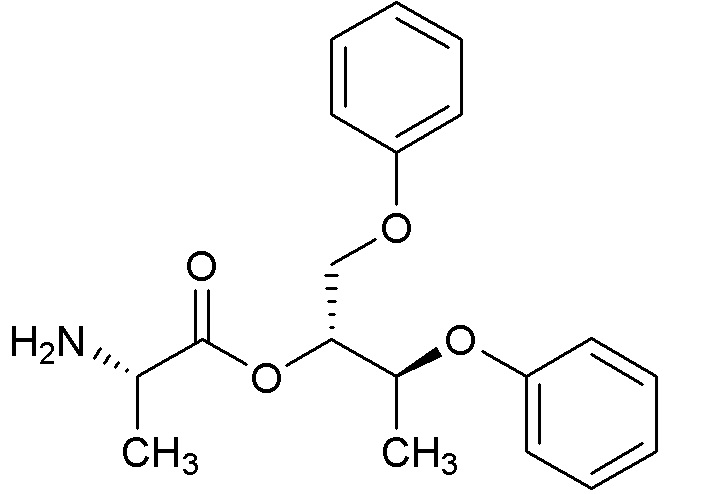
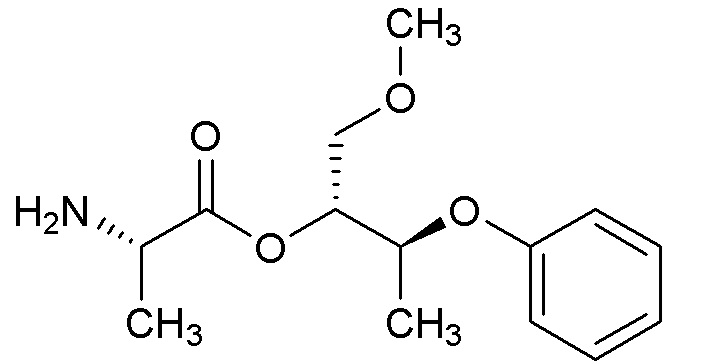
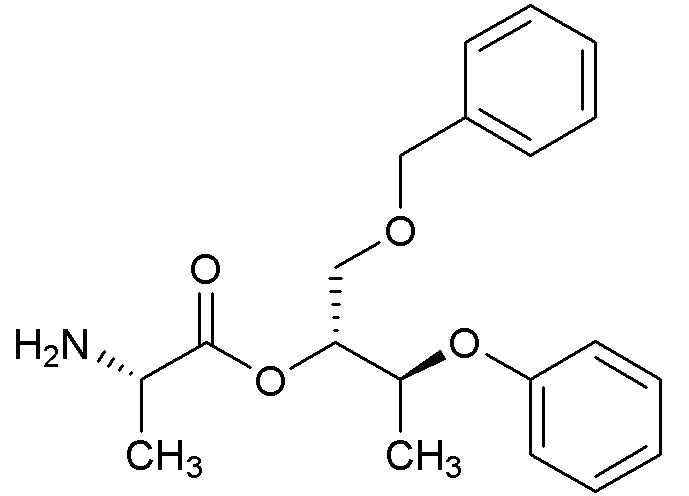
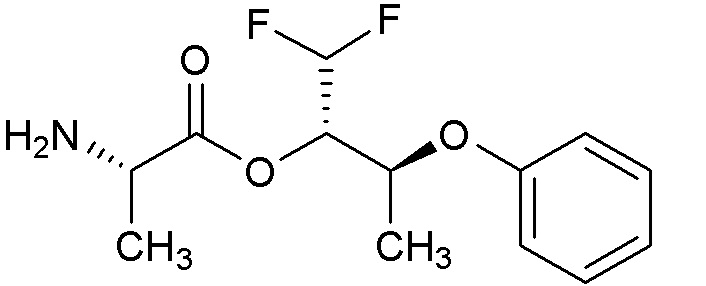
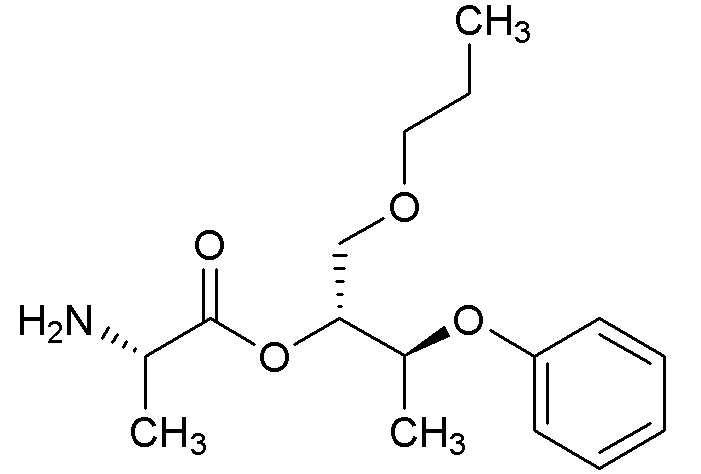
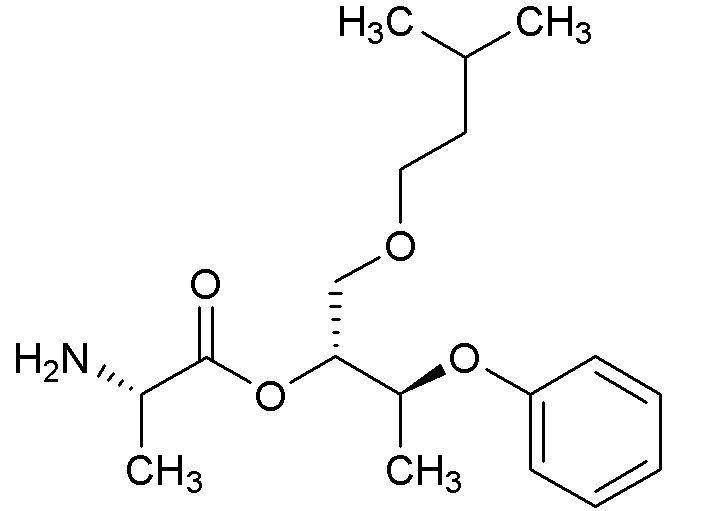
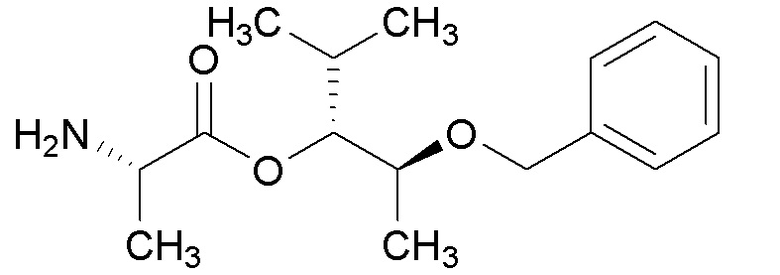
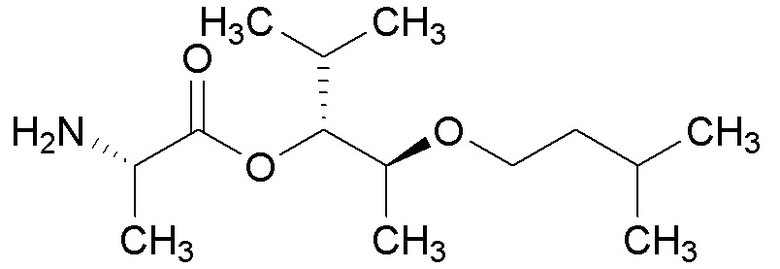
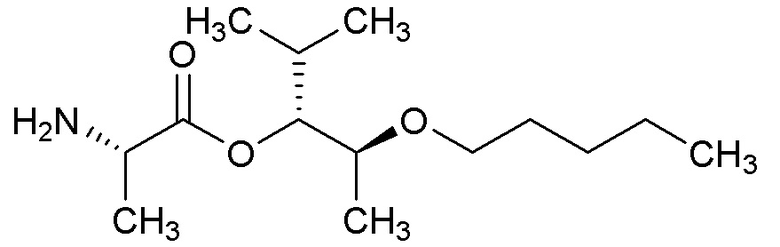
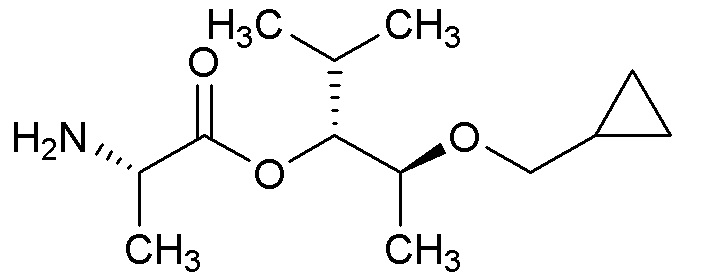
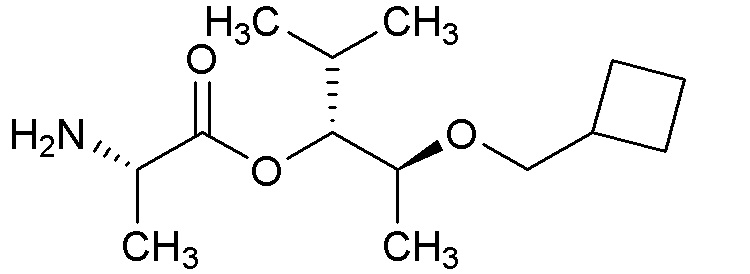
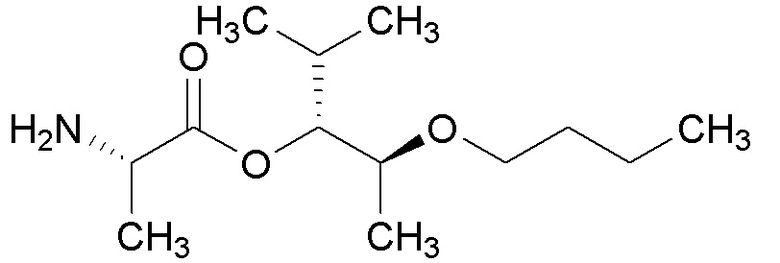
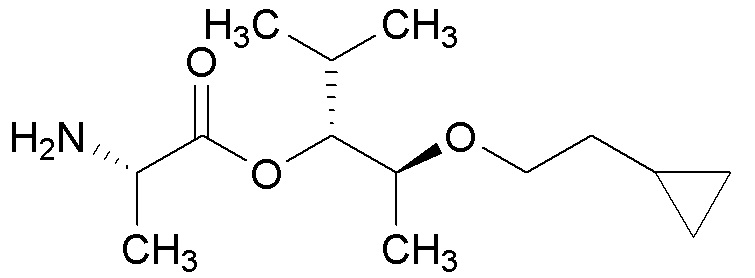
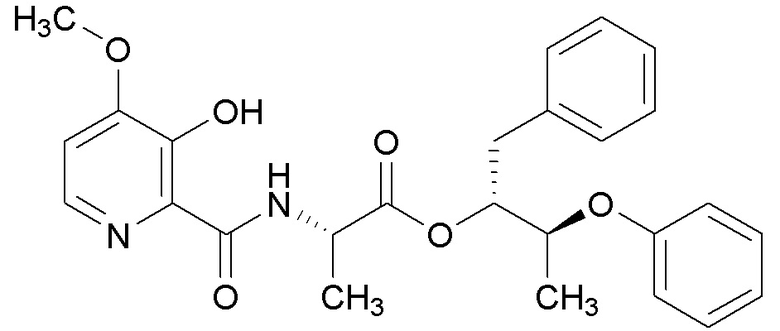
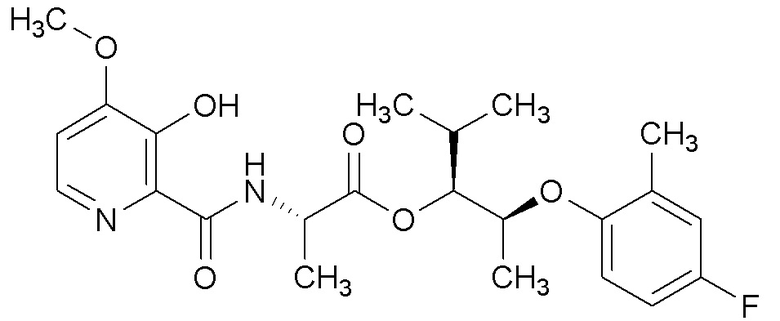
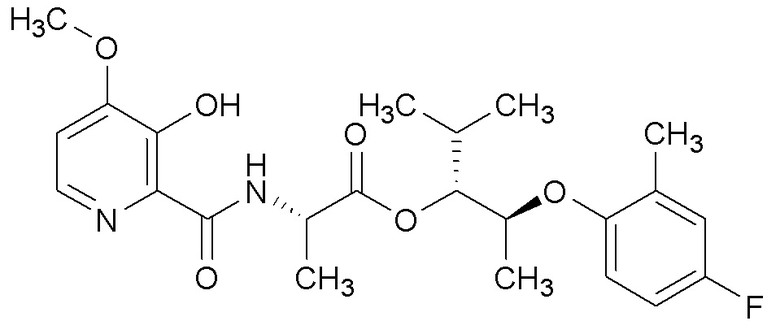
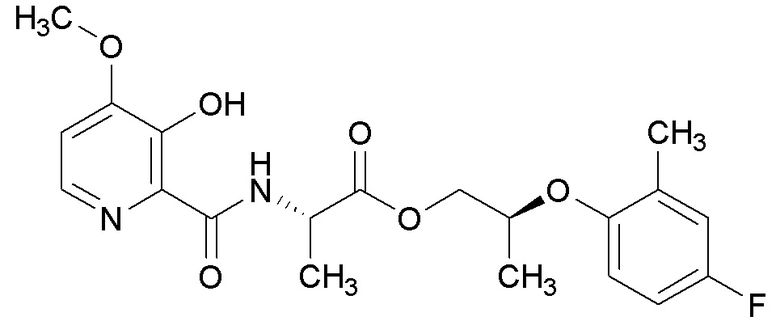
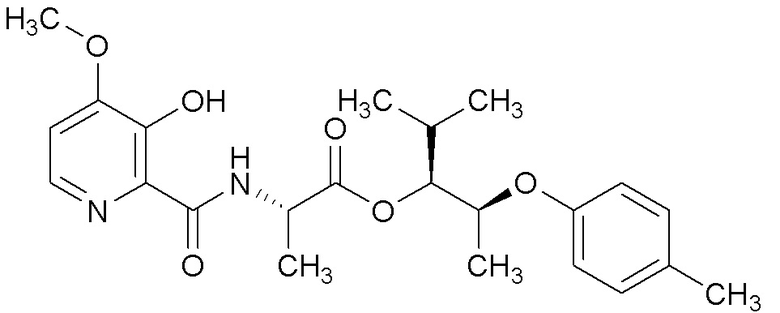
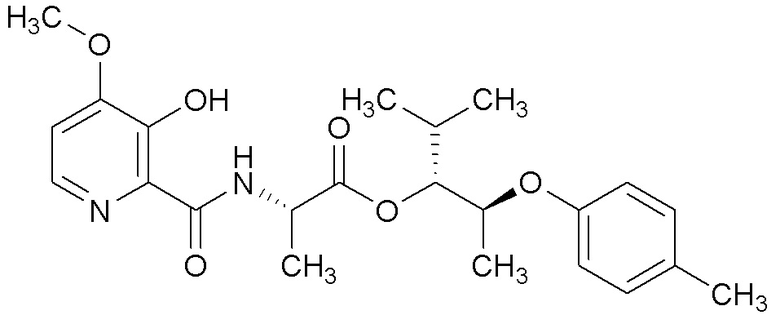
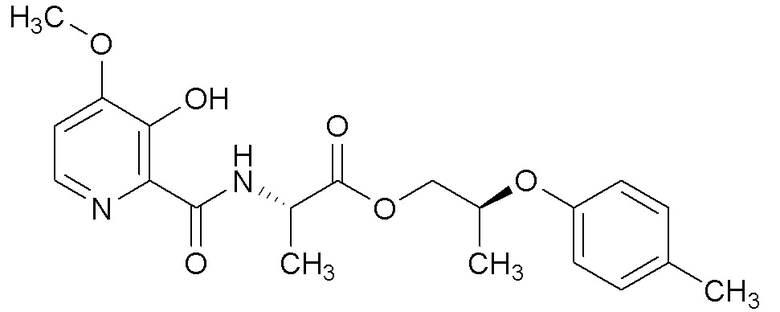
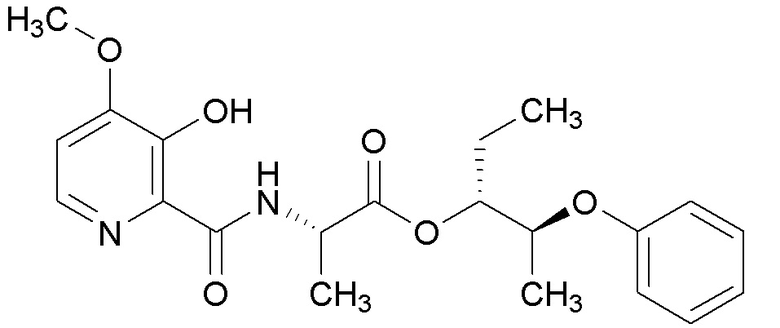
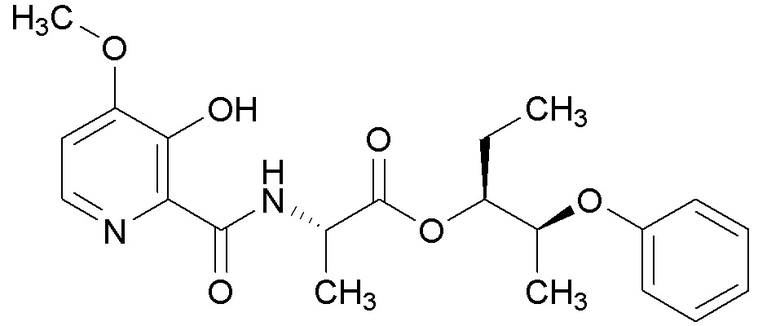
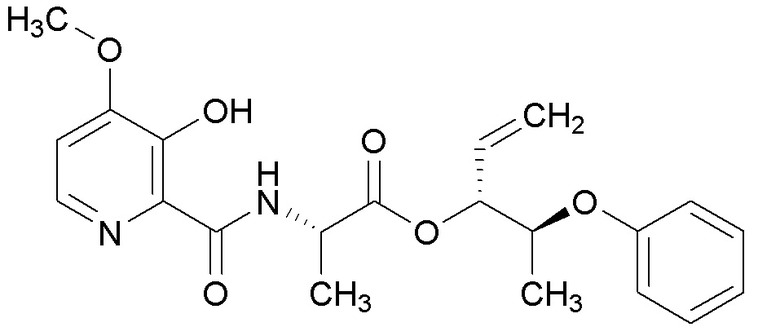
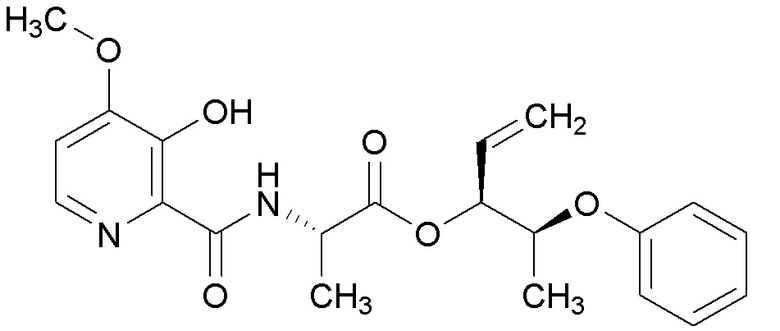
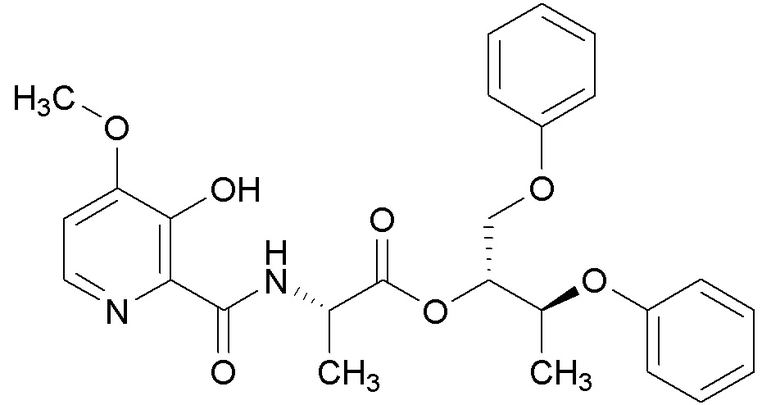
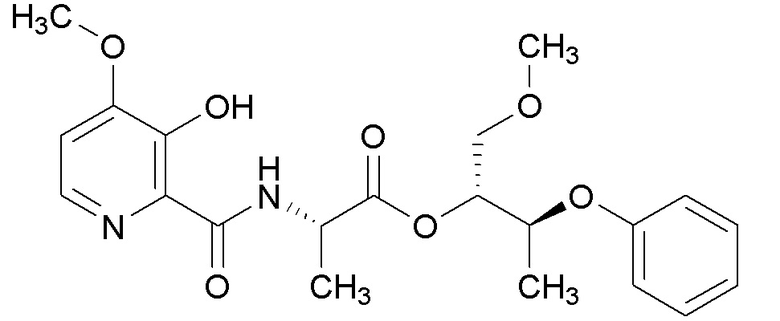
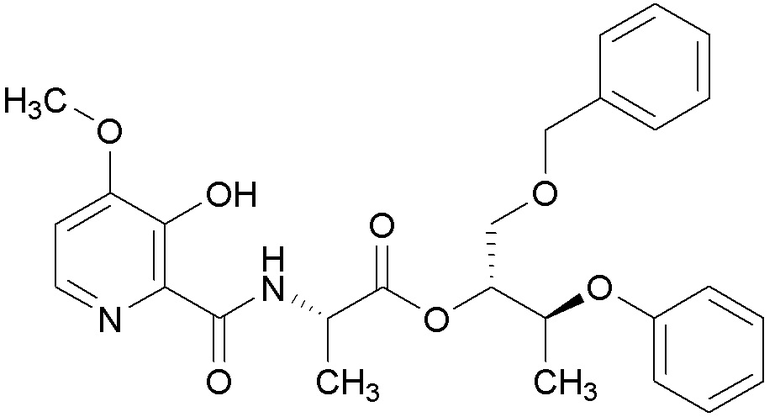
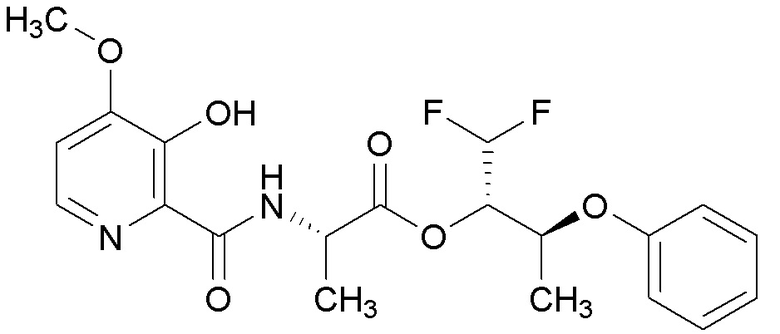
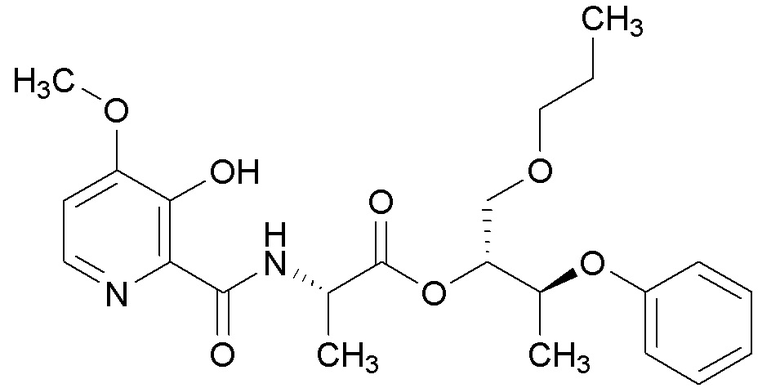
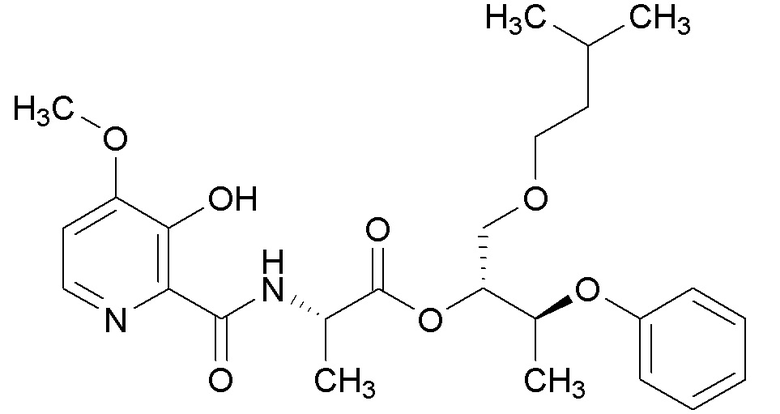
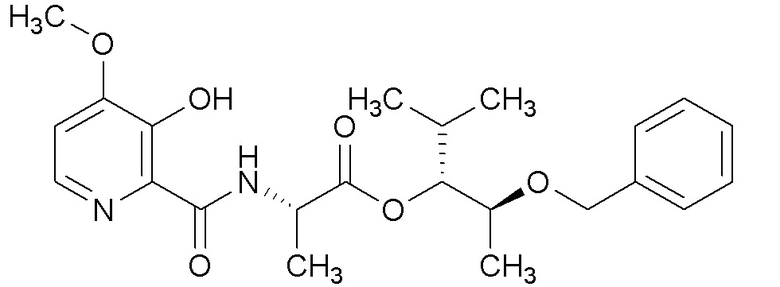
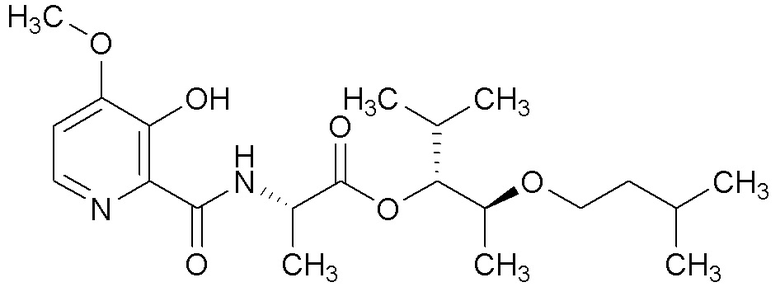
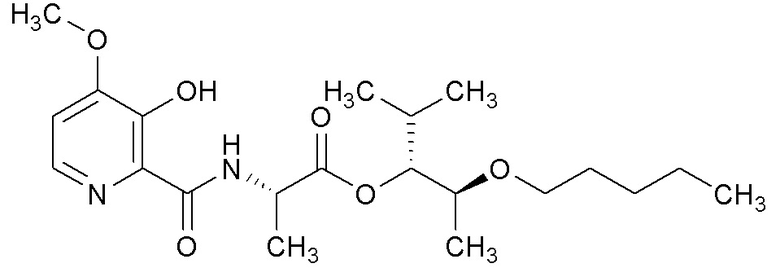
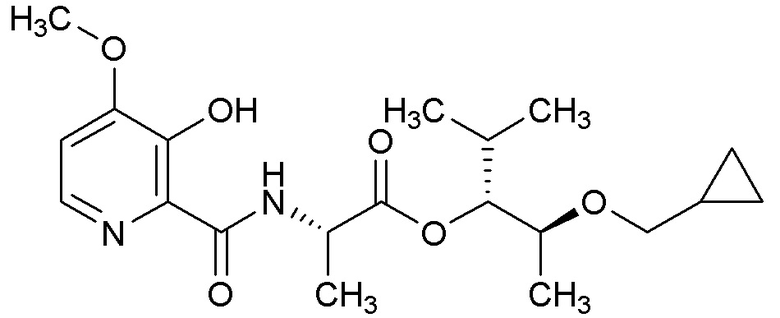
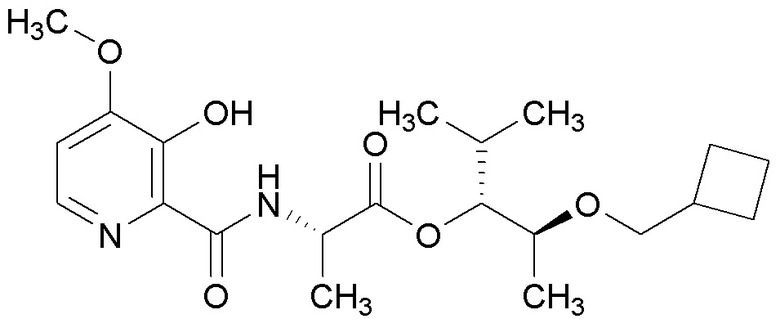
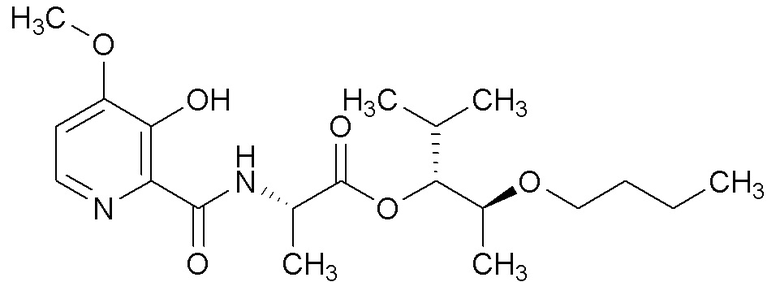
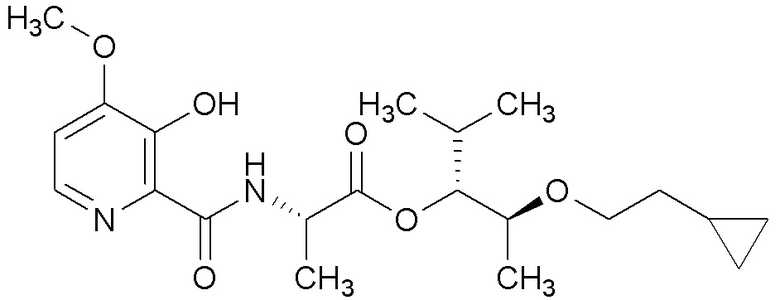
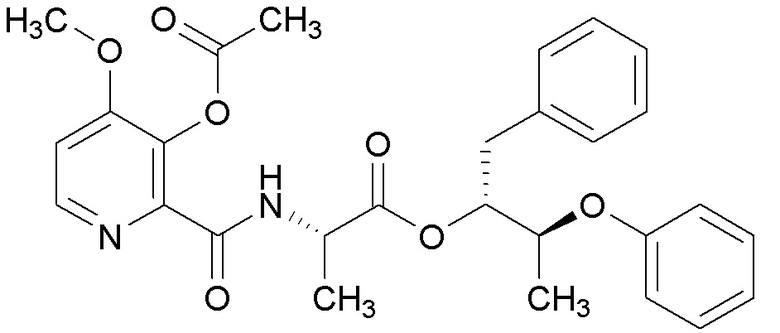
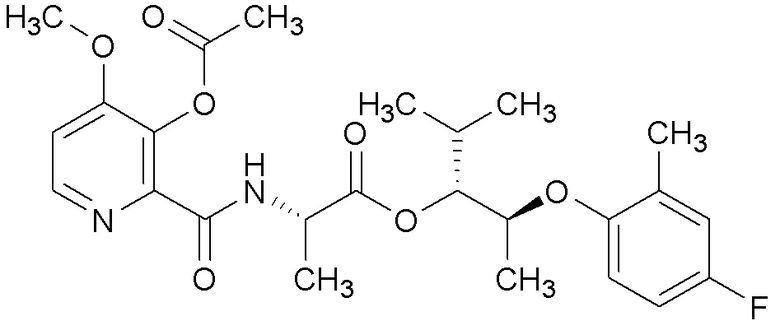
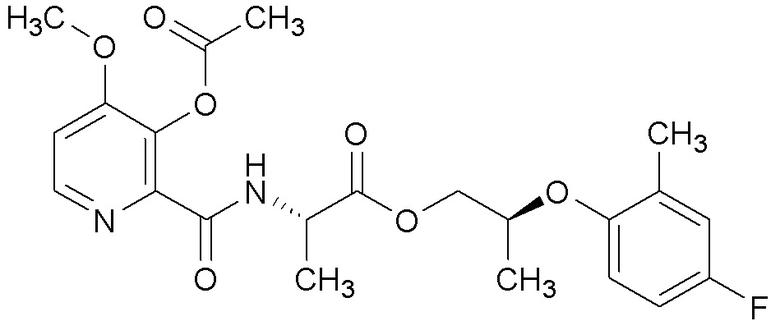
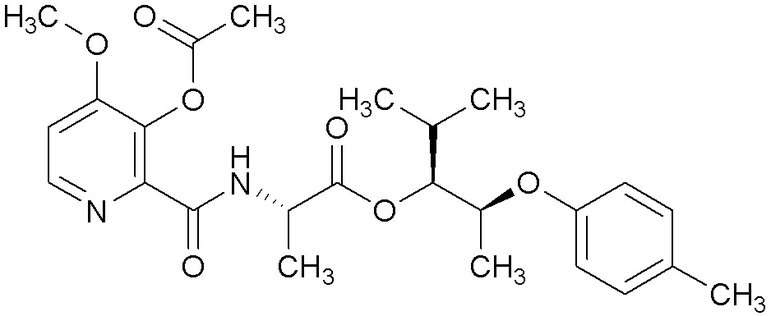
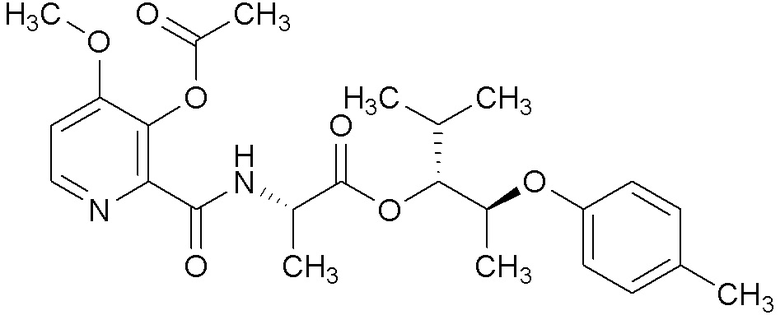
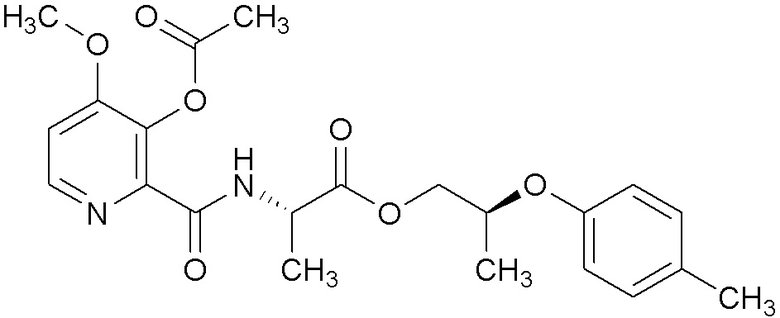
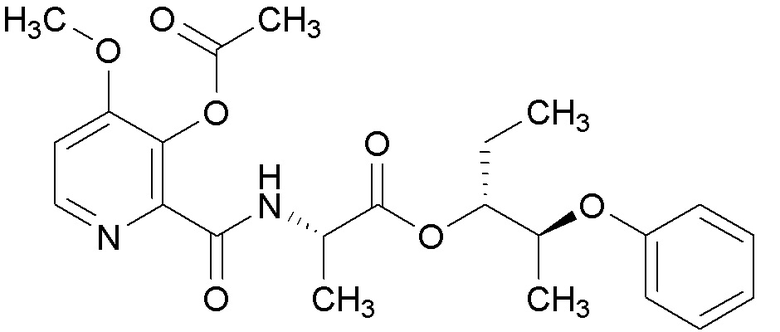
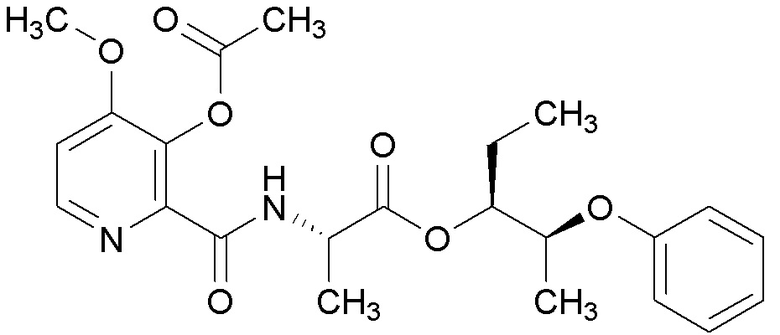
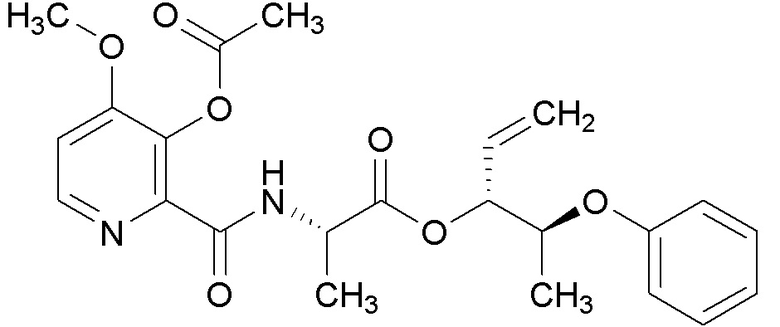
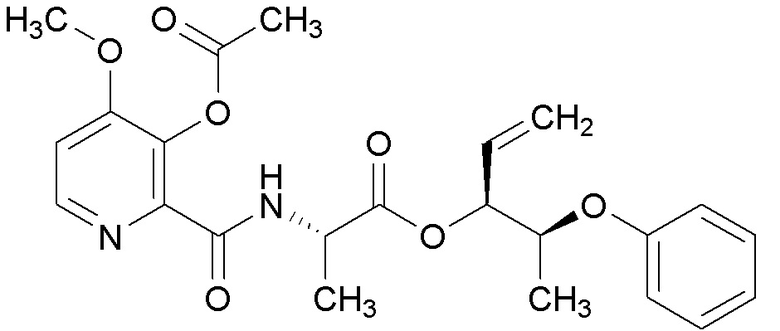
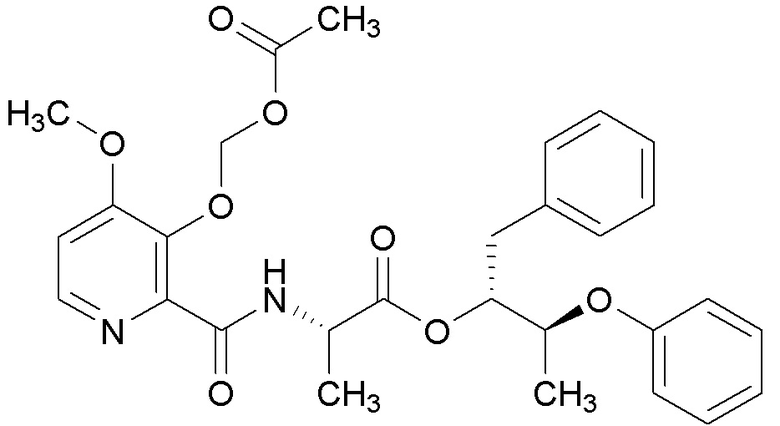
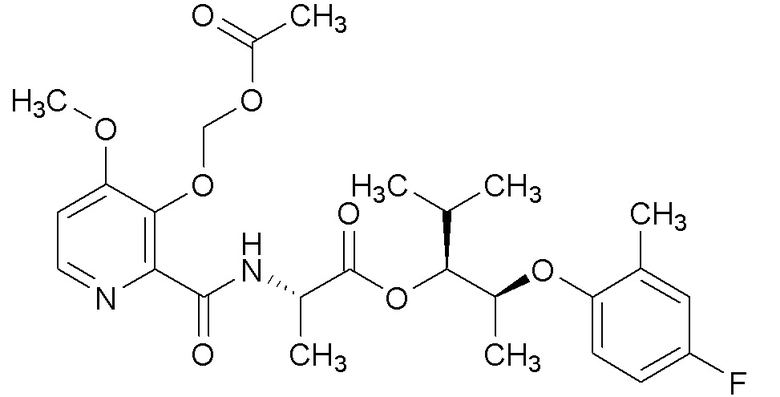
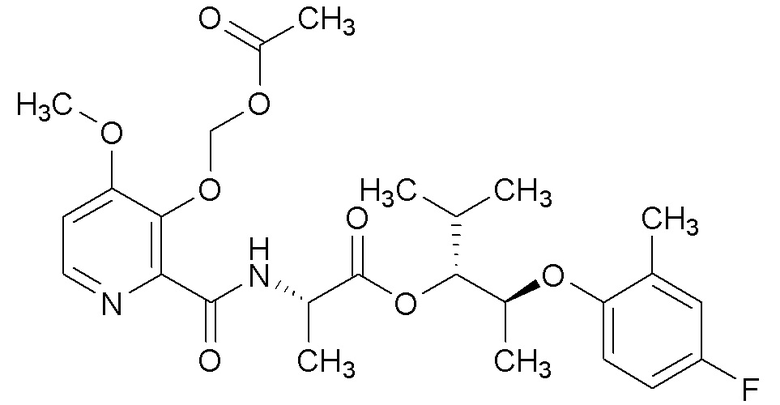
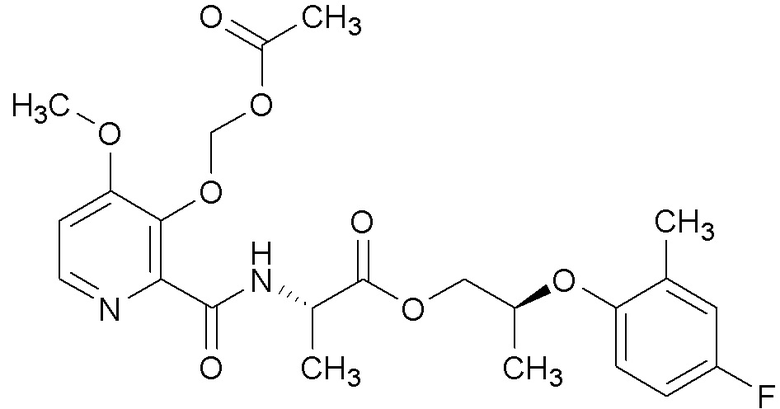
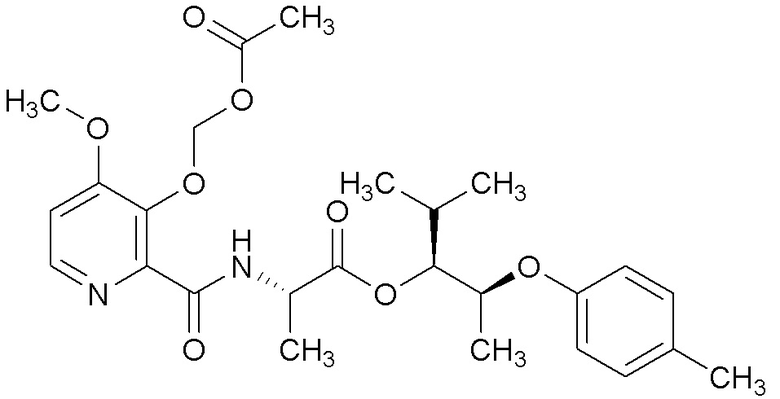
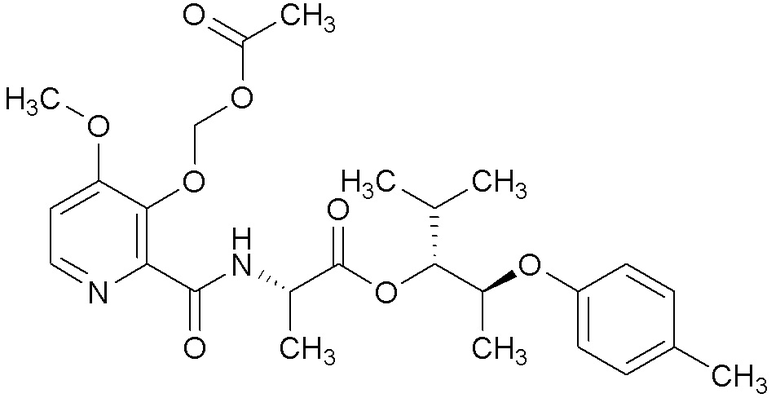
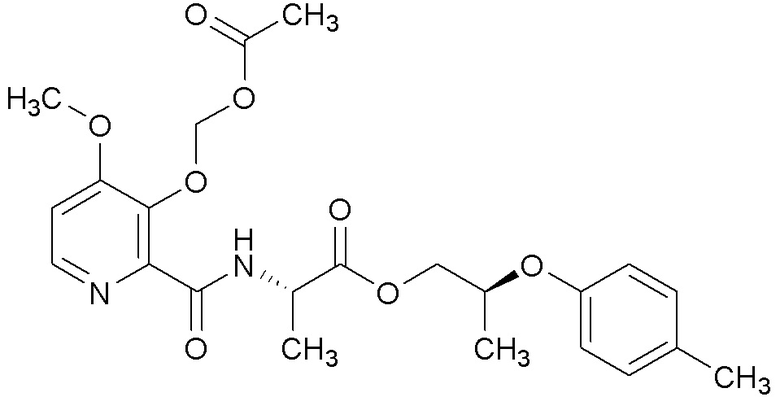
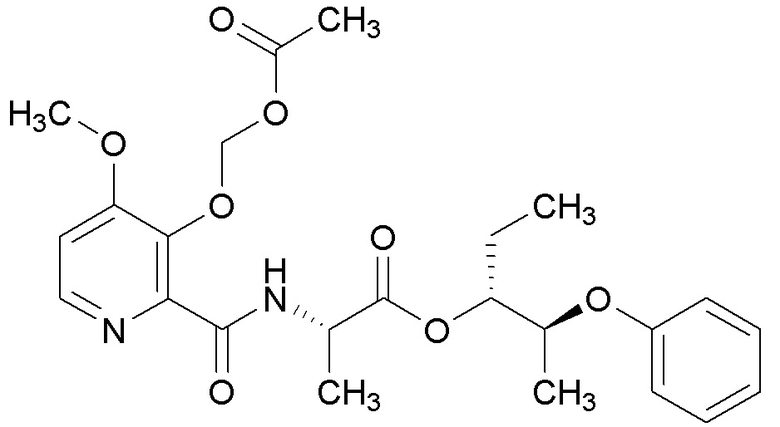
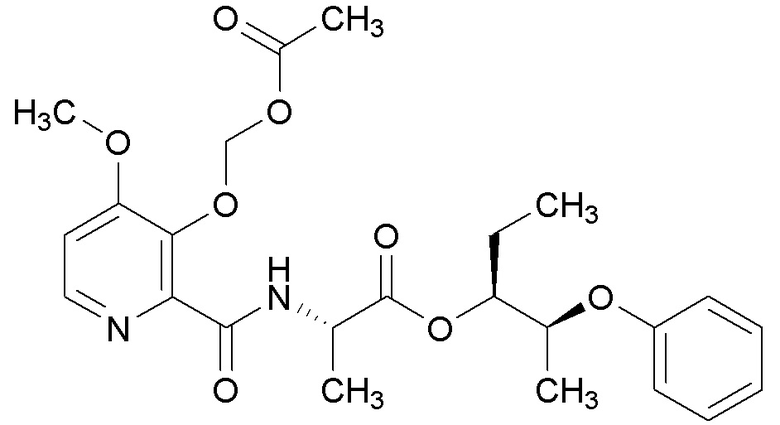
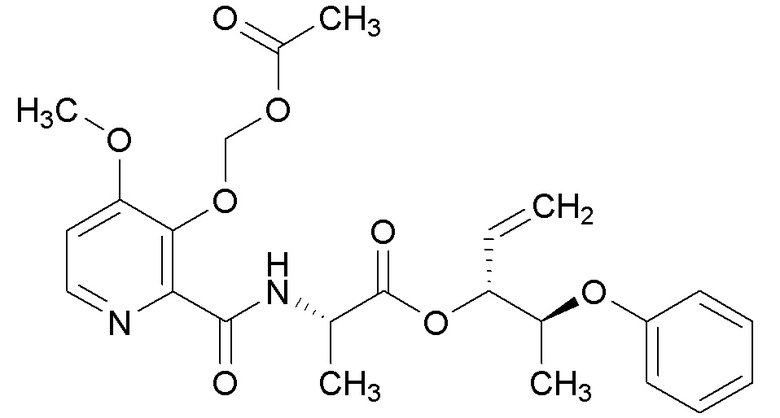
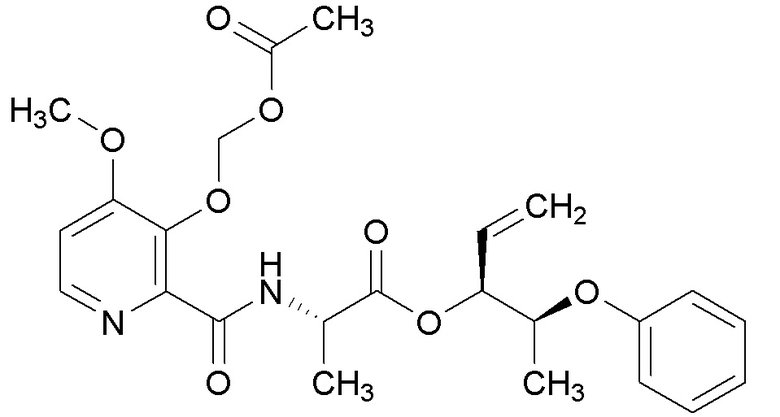
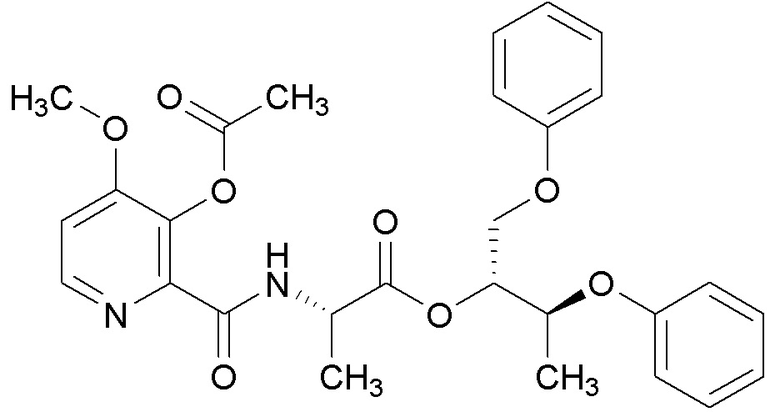
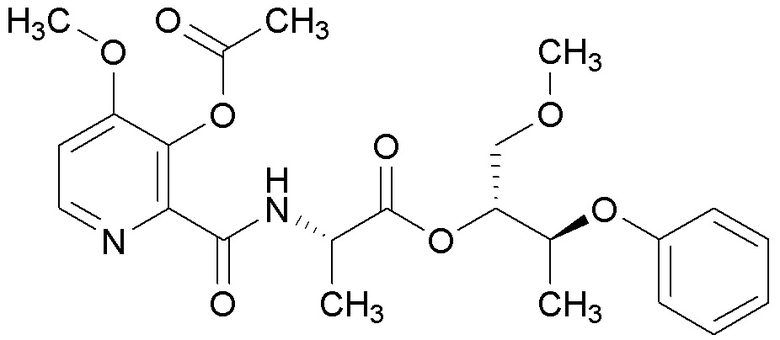
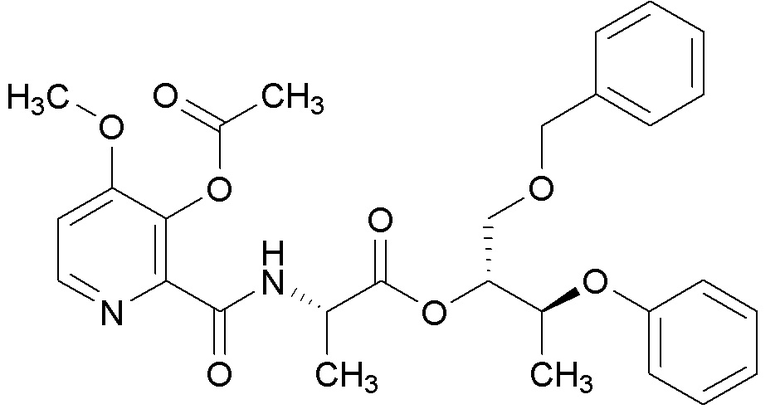
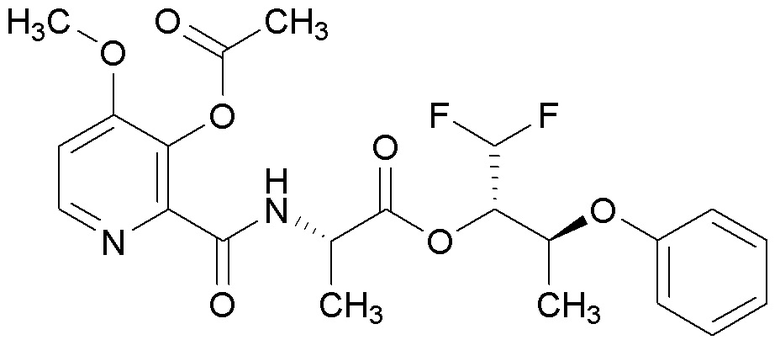
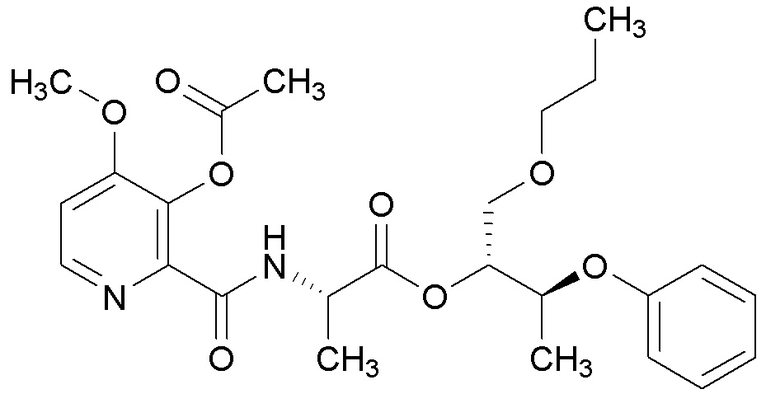
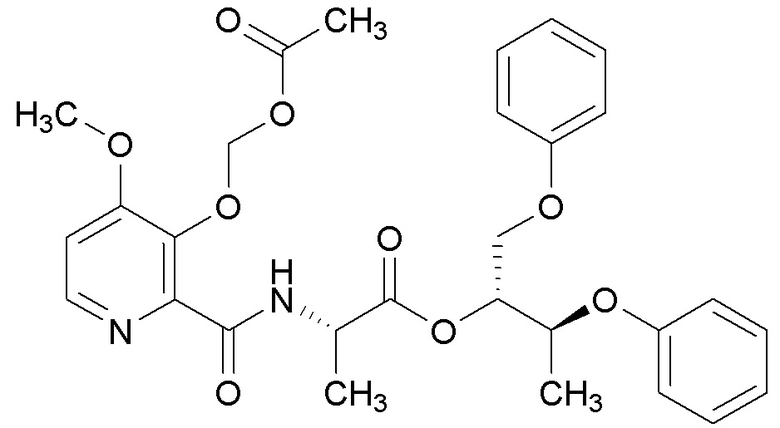
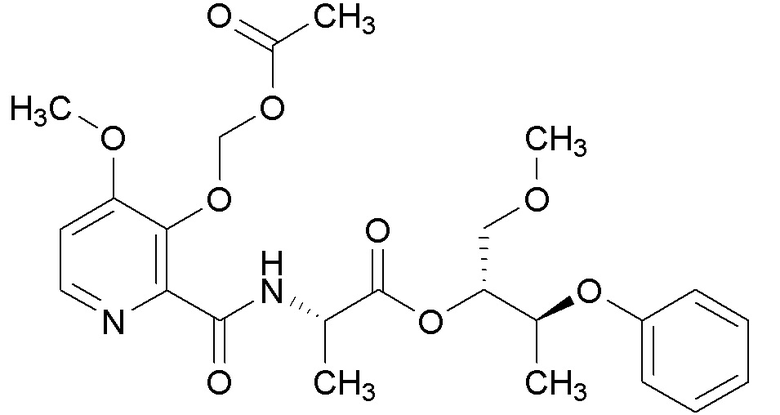
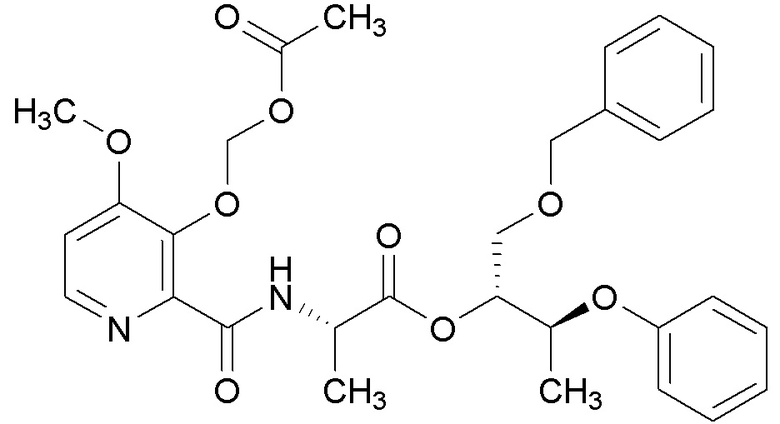
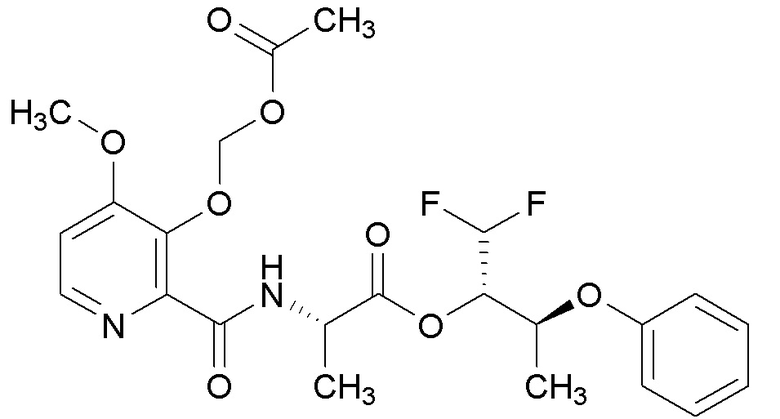
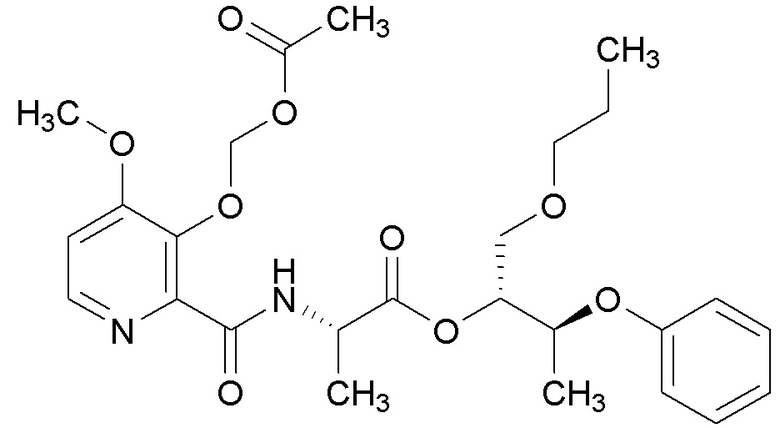
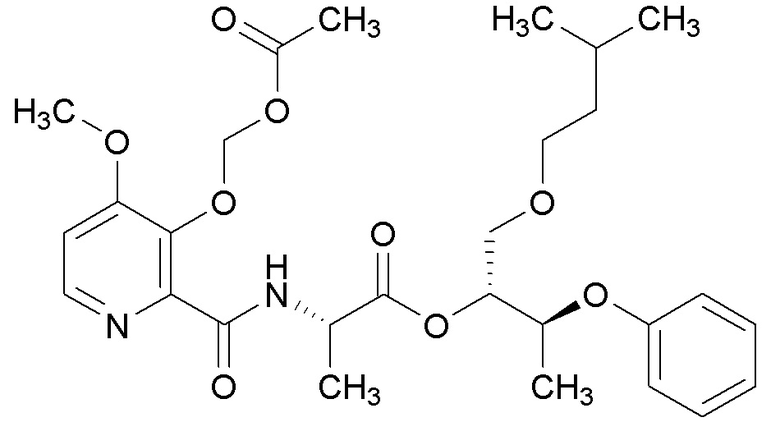
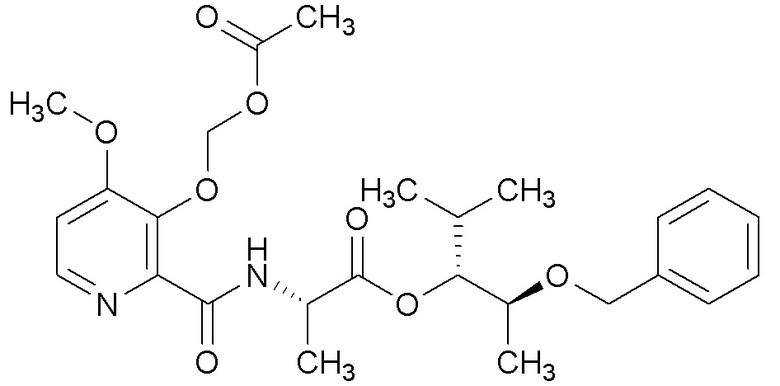
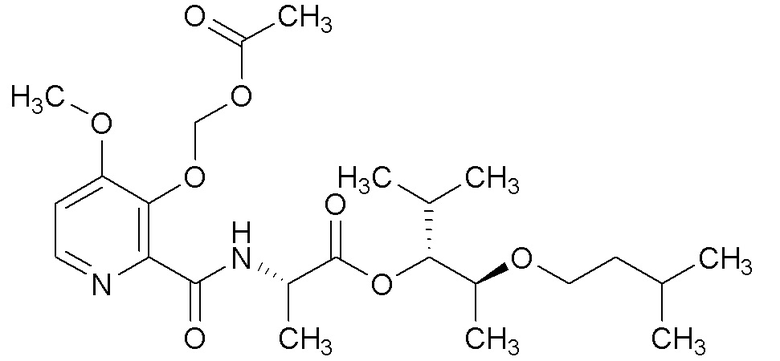
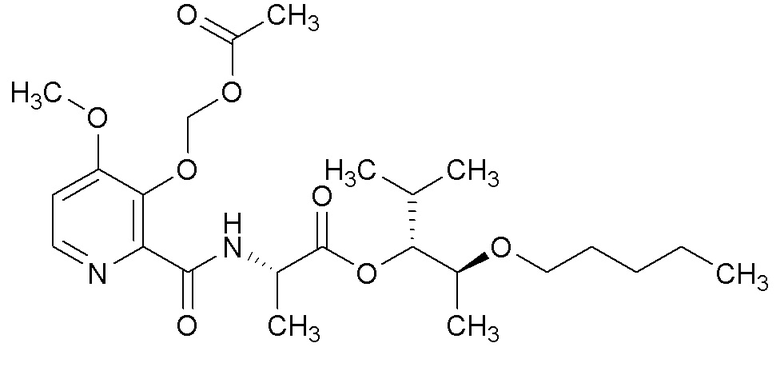
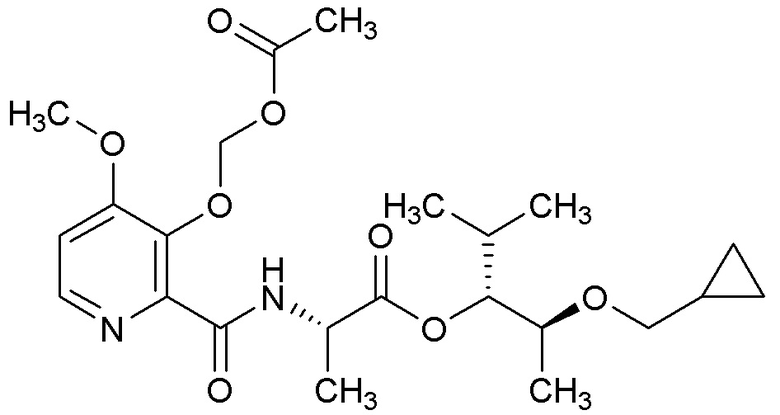
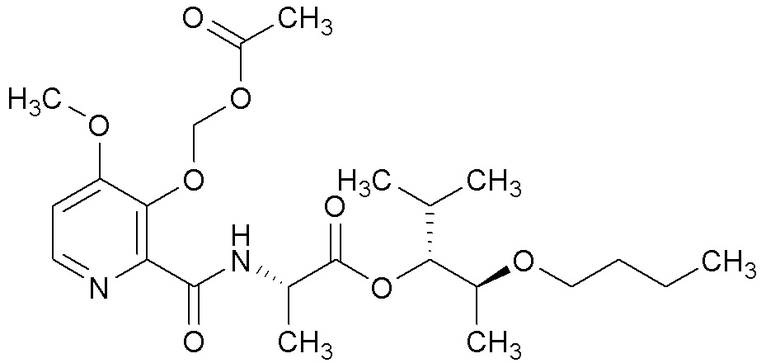
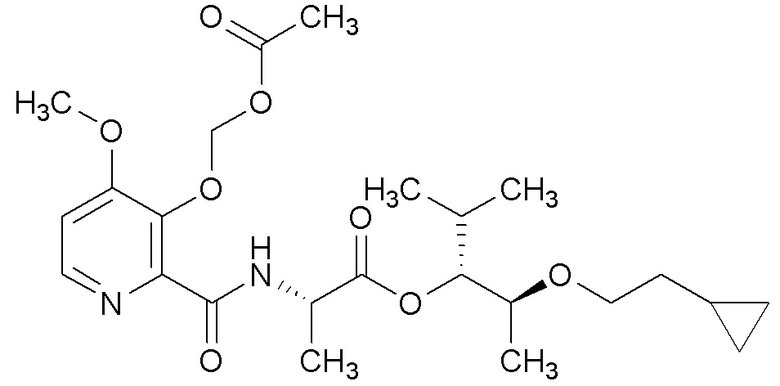
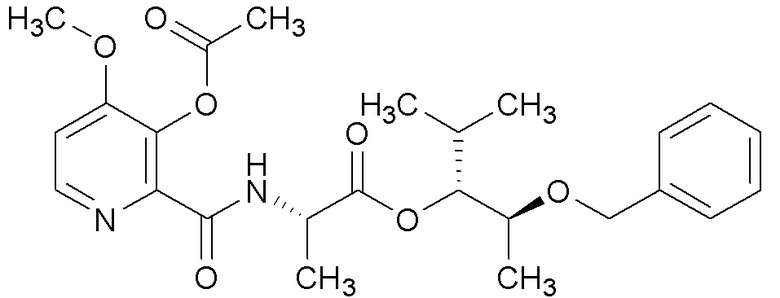
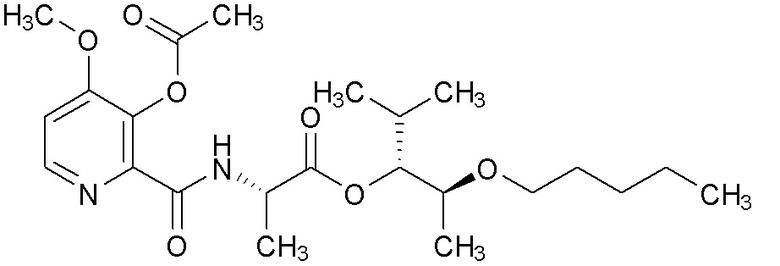
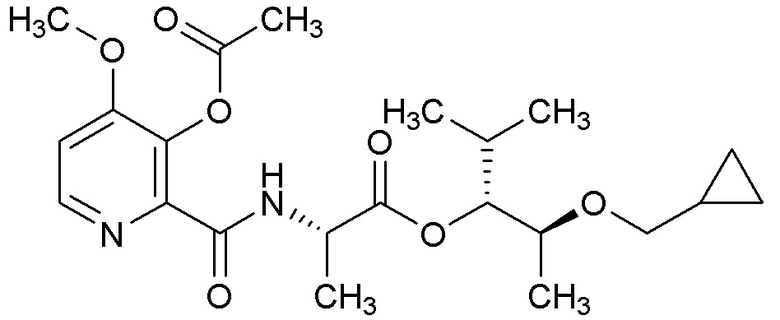
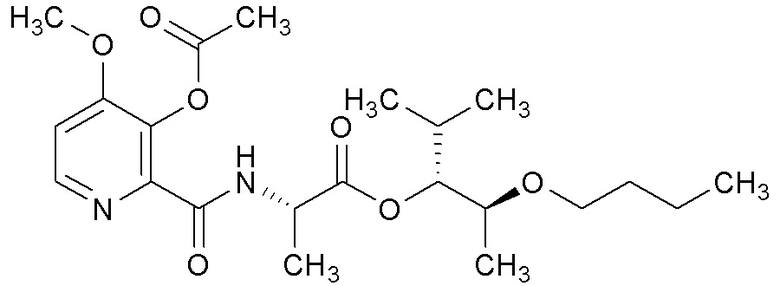
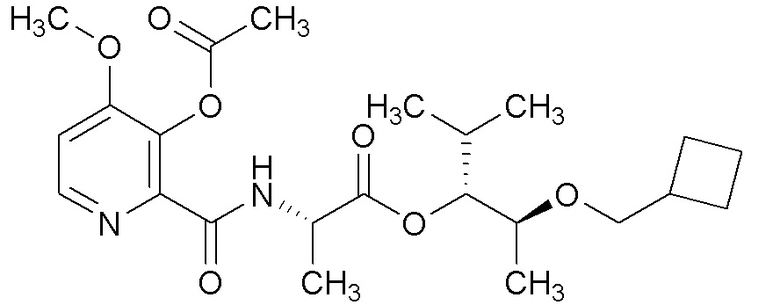
*Соед.№ - номер соединения
Аналитические данные

(1H, 13C или 19F)
13C ЯМР (101 МГц, CDCl3) δ 172,80, 155,06, 152,09, 133,00, 130,19, 127,60, 126,55, 125,29, 118,43, 116,99, 79,77, 76,39, 75,20, 49,38, 34,22, 28,32, 18,57, 15,60.
13C ЯМР (101 МГц, CDCl3) δ 172,96, 157,80, 155,05, 129,51, 121,19, 116,26, 115,59, 79,71, 76,45, 74,82, 49,49, 31,85, 28,32, 18,66, 15,64, 13,91.
13C ЯМР (101 МГц, CDCl3) δ 173,16, 157,94, 155,03, 129,54, 121,09, 115,83, 79,69, 77,54, 73,54, 49,47, 28,34, 22,45, 18,78, 15,47, 9,75.
13C ЯМР (101 МГц, CDCl3) δ 173,08, 157,66, 155,04, 129,53, 121,18, 116,07, 79,72, 77,59, 74,33, 49,40, 28,34, 23,21, 18,81, 15,21, 9,86.
13C ЯМР (101 МГц, CDCl3) δ 173,11, 157,91, 155,02, 129,54, 121,09, 115,83, 79,70, 75,94, 73,68, 49,46, 31,39, 28,34, 18,74, 18,62, 15,42, 13,90.
13C ЯМР (101 МГц, CDCl3) δ 173,05, 157,67, 155,02, 129,52, 121,18, 116,09, 79,71, 76,10, 74,70, 49,40, 32,16, 28,33, 18,84, 18,72, 15,15, 13,91.
13C ЯМР (101 МГц, CDCl3) δ 173,09, 157,84, 154,99, 129,54, 121,11, 115,85, 79,72, 74,32, 73,86, 49,45, 38,15, 28,34, 24,50, 23,50, 21,68, 18,72, 15,36.
13C ЯМР (101 МГц, CDCl3) δ 173,04, 157,70, 155,02, 129,52, 121,18, 116,10, 79,69, 75,12, 74,70, 49,39, 38,92, 28,33, 24,48, 23,47, 21,79, 18,87, 15,07.
13C ЯМР (101 МГц, CDCl3) δ 173,09, 158,01, 154,98, 129,53, 121,05, 115,79, 80,97, 79,63, 73,27, 49,50, 28,65, 28,36, 19,43, 18,80, 17,35, 16,15.
13C ЯМР (101 МГц, CDCl3) δ 173,03, 157,37, 155,08, 129,54, 121,11, 115,85, 79,75, 72,63, 49,42, 28,94, 28,34, 19,11, 18,89, 17,79, 14,86.
13C ЯМР (101 МГц, CDCl3) δ 173,16, 157,68, 155,04, 129,55, 121,33, 116,14, 79,81, 71,59, 67,48, 49,24, 28,32, 18,57, 16,84.
13C ЯМР (101 МГц, CDCl3) δ 173,17, 157,69, 129,54, 121,06, 115,73, 79,76, 74,44, 73,93, 49,42, 38,37, 28,34, 24,44, 23,49, 21,77, 18,82, 15,41.
13C ЯМР (101 МГц, CDCl3) δ 172,95, 157,88, 155,04, 129,51, 121,22, 116,34, 79,70, 75,29, 75,07, 49,50, 38,63, 28,33, 24,45, 23,55, 21,62, 18,59, 15,58.
13C ЯМР (101 МГц, CDCl3) δ 173,37, 157,76, 155,03, 129,53, 120,95, 115,61, 80,86, 73,02, 49,42, 28,60, 28,35, 19,44, 18,83, 17,22, 15,95.
13C ЯМР (101 МГц, CDCl3) δ 172,93, 157,44, 155,09, 129,54, 121,12, 115,92, 79,89, 79,77, 72,62, 49,55, 28,72, 28,35, 19,35, 18,86, 17,08, 15,50.
13C ЯМР (101 МГц, CDCl3) δ 173,23, 157,76, 155,03, 129,54, 121,03, 115,71, 79,74, 76,28, 73,71, 49,41, 31,61, 29,47, 28,34, 24,90, 22,44, 18,82, 15,47, 13,96.
13C ЯМР (101 МГц, CDCl3) δ 172,95, 157,83, 155,04, 129,52, 121,21, 116,30, 79,70, 76,71, 74,86, 49,50, 31,57, 29,75, 28,34, 25,02, 22,44, 18,71, 15,64, 13,95.
13C ЯМР (101 МГц, CDCl3) δ 173,12, 157,91, 154,99, 129,54, 121,10, 115,86, 79,71, 76,21, 73,70, 49,42, 31,56, 29,20, 28,35, 24,96, 22,43, 18,81, 15,43, 13,93.
13C ЯМР (101 МГц, CDCl3) δ 173,07, 157,68, 155,04, 129,52, 121,18, 116,10, 79,71, 76,33, 74,69, 49,42, 31,62, 30,05, 28,34, 25,08, 22,46, 18,84, 15,13, 13,97.
13C ЯМР (101 МГц, CDCl3) δ 173,20, 157,72, 155,08, 129,55, 121,31, 116,13, 79,80, 71,66, 67,57, 49,26, 28,32, 18,52, 16,75.
19F ЯМР (376 МГц, CDCl3) δ -123,45.
19F ЯМР (376 МГц, CDCl3) δ -123,19.
19F ЯМР (376 МГц, CDCl3) δ -122,87.
13C ЯМР (101 МГц, CDCl3) δ 172,13, 157,73, 155,06, 136,69, 129,51, 128,31, 128,23, 127,14, 121,40, 116,45, 79,81, 77,96, 76,09, 49,31, 28,34, 18,47, 15,34.
13C ЯМР (101 МГц, CDCl3) δ 172,19, 158,12, 154,98, 136,55, 129,57, 128,54, 128,48, 127,39, 121,30, 116,14, 79,69, 78,86, 75,51, 49,25, 28,33, 18,50, 16,25.
13C ЯМР (101 МГц, CDCl3) δ 172,92, 157,80, 155,07, 129,55, 121,09, 115,78, 79,77, 74,55, 72,87, 49,39, 28,35, 18,74, 15,35, 15,26.
13C ЯМР (101 МГц, CDCl3) δ 172,64, 157,95, 155,06, 129,53, 121,27, 116,40, 79,76, 75,47, 73,66, 49,41, 28,34, 18,54, 15,81, 15,01.
19F ЯМР (376 МГц, CDCl3) δ -116,82 (д, J=15,2 Гц), -138,26 (д, J=15,1 Гц).
19F ЯМР (376 МГц, CDCl3) δ -61,58.
19F ЯМР (376 МГц, CDCl3) δ -111,58.
13C ЯМР (101 МГц, CDCl3) δ 172,92, 155,10, 151,85, 130,31, 127,54, 126,37, 125,23, 116,24, 79,78, 79,35, 74,75, 49,54, 28,76, 28,35, 19,26, 18,80, 17,49, 15,01.
13C ЯМР (101 МГц, CDCl3) δ 172,97, 163,41 (д, J=248,0 Гц), 159,01 (д, J=12,3 Гц), 155,12, 135,49 (д, J=13,4 Гц), 112,14 (д, J=3,2 Гц), 109,04 (д, J=25,3 Гц), 102,09 (д, J=24,8 Гц), 79,89, 79,28, 73,49, 49,56, 28,78, 28,35, 19,22, 18,65, 17,34, 15,01.
19F ЯМР (376 МГц, CDCl3) δ -110,00.
13C ЯМР (101 МГц, CDCl3) δ 173,37, 155,04, 154,13, 151,79, 117,12, 114,71, 80,97, 79,69, 74,19, 55,70, 49,43, 28,60, 28,35, 19,45, 18,91, 17,29, 15,99.
13C ЯМР (101 МГц, CDCl3) δ 172,93, 155,09, 154,28, 151,51, 117,53, 114,73, 79,91, 79,73, 73,98, 55,68, 49,58, 28,73, 28,35, 19,36, 18,85, 17,15, 15,54.
13C ЯМР (101 МГц, CDCl3) δ 173,23, 155,08, 154,47, 151,72, 117,85, 114,73, 79,84, 73,06, 67,62, 55,70, 49,29, 28,34, 18,61, 16,85.
13C ЯМР (101 МГц, CDCl3) δ 172,93, 157,46, 155,07, 129,59, 121,19, 116,01, 79,74, 72,63, 49,62, 41,50, 28,30, 22,29, 21,16, 18,63, 15,88, 11,43.
13C ЯМР (75 МГц, CDCl3) δ 210,88, 172,86, 157,48, 155,05, 129,50, 121,10, 116,08, 78,73, 74,19, 40,83, 29,05, 28,33, 25,46, 24,94, 18,89, 15,00.
13C ЯМР (75 МГц, CDCl3) δ 173,33, 157,73, 129,54, 120,93, 115,59, 100,47, 99,99, 79,74, 79,61, 73,63, 49,46, 40,21, 29,11, 28,34, 25,27, 25,03, 18,90, 15,97.
13C ЯМР (126 МГц, CDCl3) δ 173,27, 155,03, 142,29, 111,93, 81,59, 79,65, 74,11, 72,89, 49,39, 28,42, 28,34, 19,68, 19,38, 18,94, 17,53, 15,59.
13C ЯМР (126 МГц, CDCl3) δ 172,98, 155,05, 142,36, 112,07, 79,75, 79,66, 73,61, 72,64, 49,52, 28,64, 28,33, 19,60, 19,33, 18,98, 17,51, 15,09.
13C ЯМР (126 МГц, CDCl3) δ 172,98, 155,04, 134,92, 116,76, 79,68, 73,60, 69,62, 49,53, 28,62, 28,33, 19,31, 18,96, 17,52, 15,17.
13C ЯМР (126 МГц, CDCl3) δ 173,02, 155,05, 136,65 (кв., J=6,3 Гц), 126,63-119,78 (м), 118,38 (кв., J=34,7, 34,1 Гц), 79,77, 79,28, 74,98, 66,43, 49,51, 28,69, 28,30, 19,21, 18,84, 17,85, 14,82.
13C ЯМР (126 МГц, CDCl3) δ 173,01, 155,05, 136,72, 132,19, 128,52, 127,62, 126,48, 126,23, 79,67, 73,59, 69,29, 49,55, 28,65, 28,33, 19,33, 18,97, 17,55, 15,26.
13C ЯМР (126 МГц, CDCl3) δ 172,68, 154,96, 137,45, 129,33, 128,30, 126,45, 79,64, 76,34, 49,26, 36,17, 28,79, 28,31, 19,44, 19,39, 18,54, 15,88.
13C ЯМР (126 МГц, CDCl3) δ 172,96, 155,07, 79,99, 79,65, 75,89, 74,45, 49,52, 28,76, 28,53, 28,33, 19,43, 19,38, 18,98, 17,21, 15,27.
13C ЯМР (126 МГц, CDCl3) δ 172,97, 155,07, 79,86, 79,65, 74,27, 70,63, 49,53, 28,57, 28,33, 23,22, 19,34, 18,98, 17,32, 15,34, 10,66.
13C ЯМР (126 МГц, CDCl3) δ 173,02, 155,06, 130,91-123,48 (m), 79,73, 79,48, 74,68, 66,91, 49,49, 30,75 (кв., J=28,7 Гц), 28,65, 28,30, 22,73 (кв., J=3,0 Гц), 19,25, 18,88, 17,67, 14,96.
13C ЯМР (126 МГц, CDCl3) δ 172,98, 155,05, 142,04, 128,45, 128,29, 125,72, 79,88, 79,67, 74,41, 68,02, 49,54, 32,37, 31,61, 28,60, 28,32, 19,35, 18,98, 17,42, 15,27.
13C ЯМР (126 МГц, CDCl3) δ 173,31, 155,04, 134,94, 116,73, 81,47, 79,65, 73,98, 69,87, 49,37, 28,40, 28,34, 19,41, 19,00, 17,33, 15,63.
13C ЯМР (126 МГц, CDCl3) δ 173,20, 155,02, 81,72, 79,63, 75,95, 74,53, 49,40, 28,79, 28,34, 19,50, 19,45, 19,36, 19,03, 17,57, 15,52.
13C ЯМР (126 МГц, CDCl3) δ 172,09, 168,71, 157,83, 155,36, 148,76, 140,48, 130,49, 129,54, 121,09, 115,78, 109,44, 77,96, 73,49, 56,08, 48,04, 22,46, 18,36, 15,52, 9,74.
13C ЯМР (126 МГц, CDCl3) δ 171,99, 168,74, 157,58, 155,35, 148,74, 140,47, 130,47, 129,53, 121,19, 116,01, 109,43, 77,98, 74,28, 56,07, 48,03, 23,13, 18,41, 15,13, 9,92.
13C ЯМР (126 МГц, CDCl3) δ 172,06, 168,71, 157,80, 155,36, 148,76, 140,48, 130,49, 129,54, 121,10, 115,79, 109,43, 76,38, 73,63, 56,08, 48,02, 31,37, 18,62, 18,34, 15,48, 13,90.
13C ЯМР (126 МГц, CDCl3) δ 171,96, 168,73, 157,60, 155,35, 148,74, 140,47, 130,48, 129,53, 121,18, 116,03, 109,42, 76,48, 74,63, 56,07, 48,02, 32,06, 18,77, 18,42, 15,07, 13,92.
13C ЯМР (126 МГц, CDCl3) δ 172,04, 168,71, 157,74, 155,37, 148,76, 140,48, 130,48, 129,54, 121,12, 115,81, 109,44, 74,81, 73,82, 56,08, 48,02, 38,16, 24,56, 23,49, 21,67, 18,29, 15,43.
13C ЯМР (126 МГц, CDCl3) δ 171,94, 168,71, 157,63, 155,34, 148,74, 140,46, 130,49, 129,52, 121,18, 116,03, 109,41, 75,07, 75,04, 56,07, 48,02, 38,80, 24,51, 23,45, 21,82, 18,42, 15,00.
13C ЯМР (126 МГц, CDCl3) δ 172,00, 168,68, 157,94, 155,35, 148,74, 140,44, 130,53, 129,52, 121,05, 115,73, 109,40, 81,36, 73,22, 56,07, 48,07, 28,62, 19,48, 18,36, 17,08, 16,20.
13C ЯМР (126 МГц, CDCl3) δ 171,89, 168,75, 157,31, 155,36, 148,75, 140,49, 130,50, 129,56, 121,14, 115,82, 109,44, 80,16, 72,58, 56,07, 48,00, 28,95, 19,10, 18,57, 17,93, 14,72.
13C ЯМР (126 МГц, CDCl3) δ 172,02, 168,75, 157,59, 155,37, 148,75, 140,48, 130,39, 129,55, 121,33, 116,08, 109,46, 71,54, 67,74, 56,08, 47,85, 18,18, 16,78.
13C ЯМР (101 МГц, CDCl3) δ 172,01, 168,76, 157,65, 155,40, 148,81, 140,48, 130,54, 129,54, 121,10, 115,75, 109,47, 74,92, 73,95, 56,07, 48,05, 38,39, 24,50, 23,47, 21,81, 18,38, 15,45.
13C ЯМР (101 МГц, CDCl3) δ 171,87, 168,80, 157,80, 155,37, 148,78, 140,47, 130,48, 129,51, 121,26, 116,32, 109,49, 75,56, 75,21, 56,06, 48,15, 38,52, 24,56, 23,50, 21,66, 18,15, 15,51.
13C ЯМР (101 МГц, CDCl3) δ 172,18, 168,74, 157,72, 155,37, 148,78, 140,45, 130,57, 129,52, 120,99, 115,64, 109,45, 81,23, 73,09, 56,06, 48,02, 28,61, 19,51, 18,41, 17,07, 15,99.
13C ЯМР (101 МГц, CDCl3) δ 171,72, 168,83, 157,40, 155,38, 148,79, 140,50, 130,49, 129,55, 121,16, 115,92, 109,51, 80,35, 72,63, 56,06, 48,17, 28,71, 19,36, 18,43, 17,11, 15,47.
13C ЯМР (101 МГц, CDCl3) δ 172,07, 168,77, 157,73, 155,39, 148,81, 140,47, 130,53, 129,54, 121,06, 115,73, 109,46, 76,75, 73,77, 56,07, 48,07, 31,60, 29,51, 24,90, 22,44, 18,33, 15,53, 13,94.
13C ЯМР (101 МГц, CDCl3) δ 171,85, 168,80, 157,78, 155,39, 148,81, 140,47, 130,51, 129,52, 121,26, 116,29, 109,49, 77,17, 74,78, 56,06, 48,15, 31,54, 29,61, 25,04, 22,44, 18,23, 15,59, 13,92.
13C ЯМР (101 МГц, CDCl3) δ 172,01, 168,74, 157,86, 155,40, 148,81, 140,47, 130,53, 129,54, 121,12, 115,85, 109,47, 76,66, 73,71, 56,08, 48,07, 31,53, 29,24, 24,94, 22,42, 18,31, 15,51, 13,91.
13C ЯМР (101 МГц, CDCl3) δ 171,94, 168,79, 157,65, 155,37, 148,78, 140,47, 130,50, 129,52, 121,20, 116,09, 109,48, 76,74, 74,69, 56,05, 48,09, 31,60, 29,96, 25,11, 22,44, 18,33, 15,08, 13,95.
13C ЯМР (101 МГц, CDCl3) δ 172,02, 168,81, 157,69, 155,38, 148,77, 140,49, 130,40, 129,54, 121,34, 116,14, 109,52, 71,68, 67,86, 56,06, 47,88, 18,12, 16,71.
19F ЯМР (376 МГц, CDCl3) δ -123,38.
19F ЯМР (376 МГц, CDCl3) δ -123,09.
13C ЯМР (101 МГц, CDCl3) δ 172,00, 168,83, 157,59 (д, J=239,3 Гц), 155,41, 153,78 (д, J=2,3 Гц), 148,79, 140,49, 130,37, 117,57 (д, J=8,0 Гц), 115,90 (д, J=23,1 Гц), 109,52, 72,87, 67,82, 56,08, 47,89, 18,09, 16,66.
19F ЯМР (376 МГц, CDCl3) δ -122,83.
13C ЯМР (101 МГц, CDCl3) δ 171,76, 168,49, 157,85, 157,41, 139,72, 131,21, 129,56, 128,78, 126,04, 121,18, 115,93, 80,39, 72,64, 48,15, 28,71, 19,37, 18,48, 17,11, 15,48.
13C ЯМР (101 МГц, CDCl3) δ 171,75, 168,88, 157,41, 154,74, 148,89, 140,43, 130,58, 129,56, 121,16, 115,92, 110,18, 80,35, 72,63, 64,67, 48,16, 28,71, 19,37, 18,46, 17,10, 15,48, 14,39.
13C ЯМР (126 МГц, CDCl3) δ 171,57, 168,59, 155,34, 148,73, 140,43, 137,33, 130,48, 129,31, 128,33, 126,51, 109,40, 77,83, 75,86, 71,26, 56,07, 47,92, 35,94, 23,24, 18,05, 16,02, 10,66.
13C ЯМР (126 МГц, CDCl3) δ 171,57, 168,59, 155,34, 148,73, 140,42, 137,34, 130,48, 129,31, 128,33, 126,51, 109,40, 77,82, 75,87, 69,66, 56,07, 47,91, 35,95, 29,73, 28,36, 22,52, 18,06, 16,02, 14,05.
13C ЯМР (126 МГц, CDCl3) δ 171,55, 168,59, 155,34, 148,73, 140,43, 137,37, 130,48, 129,32, 128,32, 126,50, 109,40, 77,90, 76,44, 76,07, 56,07, 47,92, 35,96, 28,79, 19,42, 19,37, 18,05, 15,93.
13C ЯМР (126 МГц, CDCl3) δ 171,79, 168,69, 155,34, 148,73, 140,46, 130,54, 109,40, 80,47, 75,94, 74,42, 56,07, 48,14, 28,76, 28,51, 19,42, 19,39, 19,36, 18,53, 17,23, 15,28.
13C ЯМР (126 МГц, CDCl3) δ 171,82, 168,70, 155,34, 148,73, 140,46, 130,54, 109,40, 80,34, 74,24, 70,69, 56,07, 48,14, 28,55, 23,21, 19,36, 18,53, 17,35, 15,34, 10,66.
13C ЯМР (126 МГц, CDCl3) δ 171,85, 168,74, 155,36, 148,75, 140,48, 130,48, 127,29 (кв., J=276,0 Гц), 109,43, 79,96, 74,67, 66,96, 56,07, 48,07, 30,71 (кв., J=28,9 Гц), 28,62, 22,72 (кв., J=3,1 Гц), 19,25, 18,43, 17,69, 14,96.
13C ЯМР (126 МГц, CDCl3) δ 171,86, 168,70, 155,33, 148,73, 142,02, 140,46, 130,52, 128,43, 128,26, 125,68, 109,40, 80,35, 74,38, 68,05, 56,06, 48,13, 32,36, 31,60, 28,58, 19,35, 18,55, 17,49, 15,23.
13C ЯМР (126 МГц, CDCl3) δ 171,83, 168,69, 155,34, 148,73, 142,32, 140,46, 130,54, 112,11, 109,40, 80,21, 73,54, 72,68, 56,07, 48,13, 28,62, 19,59, 19,34, 18,53, 17,56, 15,09.
13C ЯМР (126 МГц, CDCl3) δ 171,84, 168,70, 155,34, 148,74, 140,47, 134,87, 130,53, 116,83, 109,41, 80,16, 73,54, 69,66, 56,07, 48,14, 28,61, 19,31, 18,51, 17,56, 15,16.
13C ЯМР (126 МГц, CDCl3) δ 171,85, 168,75, 155,37, 148,75, 140,49, 139,14, 136,59 (кв., J=6,4 Гц), 130,45, 123,09 (кв., J=269,1 Гц), 118,41 (кв., J=33,9 Гц), 109,44, 108,37, 79,77, 74,96, 66,47, 56,07, 48,08, 28,66, 19,22, 18,39, 17,85, 14,84.
13C ЯМР (126 МГц, CDCl3) δ 172,05, 168,66, 155,33, 148,73, 140,44, 130,56, 109,38, 82,13, 75,92, 74,47, 56,06, 48,03, 28,80, 28,46, 19,45, 18,60, 17,56, 15,55.
13C ЯМР (126 МГц, CDCl3) δ 172,12, 168,67, 155,34, 148,73, 140,45, 130,57, 109,38, 82,03, 74,47, 70,76, 56,06, 48,00, 28,44, 23,26, 19,46, 18,60, 17,39, 15,66.
13C ЯМР (126 МГц, CDCl3) δ 172,04, 168,74, 155,36, 148,75, 140,49, 139,14, 130,49, 127,26 (кв., J=276,0 Гц), 109,44, 81,79, 74,64, 66,88, 56,07, 48,02, 30,73 (кв., J=28,6 Гц), 28,50, 22,81 (д, J=3,0 Гц), 19,38, 18,50, 17,47, 15,50.
13C ЯМР (101 МГц, CDCl3) δ 171,02, 168,84, 157,67, 155,39, 148,79, 140,49, 136,50, 130,47, 129,51, 128,36, 128,34, 127,17, 121,43, 116,42, 109,51, 78,38, 76,00, 56,07, 47,92, 18,05, 15,31.
13C ЯМР (101 МГц, CDCl3) δ 171,14, 168,71, 158,07, 155,38, 148,78, 140,44, 136,44, 130,52, 129,55, 128,68, 128,56, 127,42, 121,31, 116,13, 109,47, 79,40, 75,55, 56,07, 47,87, 18,01, 16,29.
13C ЯМР (101 МГц, CDCl3) δ 171,57, 168,79, 157,86, 155,39, 148,79, 140,48, 130,50, 129,52, 121,31, 116,38, 109,50, 75,42, 74,06, 56,07, 48,02, 18,12, 15,71, 15,00.
19F ЯМР (376 МГц, CDCl3) δ -116,78 (д, J=15,2 Гц), -138,19 (д, J=14,7 Гц).
19F ЯМР (376 МГц, CDCl3) δ -61,57.
19F ЯМР (376 МГц, CDCl3) δ -111,51.
13C ЯМР (101 МГц, CDCl3) δ 171,73, 168,79, 155,39, 150,74, 148,80, 140,48, 131,94, 131,01, 130,57, 128,03, 124,15, 115,98, 109,47, 80,19, 74,52, 56,07, 48,16, 28,74, 20,31, 19,33, 18,44, 17,46, 15,16.
13C ЯМР (101 МГц, CDCl3) δ 171,72, 168,81, 155,40, 151,81, 148,80, 140,51, 130,49, 130,31, 127,53, 126,42, 125,25, 116,28, 109,51, 79,83, 74,77, 56,08, 48,11, 28,75, 19,28, 18,37, 17,56, 14,96.
13C ЯМР (101 МГц, CDCl3) δ 171,71, 168,87, 163,40 (д, J=248,1 Гц), 158,95 (д, J=12,2 Гц), 155,44, 148,84, 140,54, 135,51 (д, J=13,5 Гц), 130,46, 112,15 (д, J=3,2 Гц), 109,55, 109,10 (д, J=25,2 Гц), 102,06 (д, J=24,7 Гц), 79,77, 73,50, 56,09, 48,11, 28,76, 19,26, 18,31, 17,30, 15,05.
19F ЯМР (376 МГц, CDCl3) δ -109,89.
13C ЯМР (101 МГц, CDCl3) δ 171,72, 168,84, 158,15, 155,42, 148,82, 140,52, 134,95, 130,49, 130,34, 121,35, 116,26, 114,16, 109,52, 80,08, 73,08, 56,08, 48,14, 28,74, 19,31, 18,37, 17,22, 15,25.
13C ЯМР (101 МГц, CDCl3) δ 172,15, 168,73, 155,38, 154,14, 151,75, 148,79, 140,43, 130,58, 117,15, 114,68, 109,44, 81,34, 74,28, 56,06, 55,68, 48,05, 28,60, 19,53, 18,50, 17,11, 16,03.
13C ЯМР (101 МГц, CDCl3) δ 171,73, 168,81, 154,30, 151,47, 148,81, 140,49, 139,13, 130,52, 117,53, 114,73, 109,50, 80,40, 73,99, 56,07, 55,68, 48,17, 28,73, 19,38, 18,46, 17,19, 15,52.
13C ЯМР (101 МГц, CDCl3) δ 172,04, 168,81, 155,41, 154,47, 151,69, 148,80, 140,48, 130,44, 117,86, 114,71, 109,51, 73,08, 67,94, 56,07, 55,68, 47,90, 18,19, 16,81.
13C ЯМР (101 МГц, CDCl3) δ 172,61, 168,89, 162,41, 159,49, 157,88, 146,66, 141,63, 137,55, 129,53, 121,05, 115,87, 109,75, 77,57, 73,42, 56,28, 48,13, 22,27, 20,74, 18,63, 15,35, 9,79.
13C ЯМР (101 МГц, CDCl3) δ 172,49, 168,89, 162,45, 159,48, 157,68, 146,66, 141,62, 137,54, 129,52, 121,15, 116,10, 109,74, 77,79, 74,36, 56,28, 48,11, 23,23, 20,75, 18,71, 15,25, 9,85.
13C ЯМР (101 МГц, CDCl3) δ 172,57, 168,88, 162,40, 159,49, 157,85, 146,66, 141,61, 137,55, 129,54, 121,06, 115,87, 109,75, 75,96, 73,54, 56,29, 48,11, 31,18, 20,74, 18,67, 18,61, 15,30, 13,91.
13C ЯМР (101 МГц, CDCl3) δ 172,46, 168,89, 162,42, 159,47, 157,69, 146,65, 141,61, 137,53, 129,51, 121,15, 116,12, 109,73, 76,30, 74,73, 56,28, 48,10, 32,21, 20,74, 18,72, 18,72, 15,19, 13,93.
13C ЯМР (101 МГц, CDCl3) δ 172,45, 168,89, 162,40, 159,47, 157,72, 146,66, 141,61, 137,53, 129,51, 121,15, 116,13, 109,73, 75,17, 74,90, 56,28, 48,09, 38,98, 24,48, 23,48, 21,86, 20,74, 18,73, 15,09.
13C ЯМР (101 МГц, CDCl3) δ 172,37, 168,90, 162,47, 159,48, 157,40, 146,67, 141,61, 137,54, 129,54, 121,08, 115,87, 109,75, 79,96, 72,63, 56,28, 48,14, 28,92, 20,75, 19,16, 18,82, 17,69, 14,94.
13C ЯМР (101 МГц, CDCl3) δ 172,53, 168,88, 162,49, 159,49, 157,68, 146,63, 141,52, 137,56, 129,53, 121,30, 116,19, 109,78, 71,62, 67,56, 56,29, 47,90, 20,75, 18,44, 16,88.
13C ЯМР (101 МГц, CDCl3) δ 172,72, 170,25, 163,00, 160,30, 157,89, 145,72, 144,02, 142,62, 129,53, 121,07, 115,88, 109,57, 89,59, 77,56, 73,46, 56,19, 48,30, 22,29, 20,86, 18,55, 15,36, 9,81.
13C ЯМР (101 МГц, CDCl3) δ 172,60, 170,25, 163,03, 160,28, 157,67, 145,71, 144,00, 142,60, 129,52, 121,16, 116,10, 109,57, 89,59, 77,75, 74,38, 56,18, 48,28, 23,22, 20,86, 18,59, 15,21, 9,89.
13C ЯМР (101 МГц, CDCl3) δ 172,68, 170,25, 163,00, 160,30, 157,86, 145,71, 144,04, 142,60, 129,53, 121,07, 115,89, 109,57, 89,60, 75,95, 73,58, 56,19, 48,28, 31,21, 20,86, 18,69, 18,53, 15,31, 13,91.
13C ЯМР (101 МГц, CDCl3) δ 172,57, 170,25, 163,02, 160,29, 157,69, 145,71, 144,01, 142,60, 129,52, 121,16, 116,12, 109,56, 89,60, 76,26, 74,74, 56,18, 48,26, 32,19, 20,86, 18,75, 18,60, 15,15, 13,93.
13C ЯМР (101 МГц, CDCl3) δ 172,66, 170,25, 162,99, 160,31, 157,79, 145,71, 144,05, 142,58, 129,53, 121,09, 115,91, 109,57, 89,61, 74,34, 73,71, 56,19, 48,27, 37,95, 24,58, 23,49, 21,72, 20,86, 18,48, 15,24.
13C ЯМР (101 МГц, CDCl3) δ 172,56, 170,24, 162,99, 160,29, 157,72, 145,70, 144,01, 142,61, 129,51, 121,16, 116,13, 109,55, 89,60, 75,18, 74,87, 56,18, 48,26, 38,95, 24,50, 23,47, 21,87, 20,86, 18,62, 15,07.
13C ЯМР (101 МГц, CDCl3) δ 172,64, 170,25, 162,95, 160,29, 157,99, 145,69, 144,03, 142,68, 129,52, 121,04, 115,86, 109,53, 89,63, 81,04, 73,32, 56,18, 48,37, 28,66, 20,86, 19,47, 18,59, 17,36, 16,14.
13C ЯМР (101 МГц, CDCl3) δ 172,50, 170,25, 163,05, 160,28, 157,40, 145,72, 143,99, 142,63, 129,55, 121,10, 115,88, 109,57, 89,58, 79,93, 72,69, 56,18, 48,27, 28,97, 20,86, 19,15, 18,72, 17,83, 14,87.
13C ЯМР (101 МГц, CDCl3) δ 172,64, 170,26, 163,06, 160,31, 157,68, 145,69, 144,07, 142,45, 129,53, 121,30, 116,17, 109,61, 89,58, 71,63, 67,54, 56,19, 48,12, 20,86, 18,32, 16,87.
13C ЯМР (101 МГц, CDCl3) δ 172,65, 170,26, 163,00, 160,31, 157,69, 145,71, 144,05, 142,59, 129,54, 121,05, 115,77, 109,56, 89,62, 74,51, 73,87, 56,19, 48,25, 38,26, 24,46, 23,49, 21,83, 20,86, 18,58, 15,36.
13C ЯМР (101 МГц, CDCl3) δ 172,49, 170,25, 163,02, 160,31, 157,80, 145,69, 144,05, 142,56, 129,51, 121,20, 116,32, 109,57, 89,63, 75,29, 56,18, 48,37, 38,75, 24,54, 23,54, 21,68, 20,86, 18,42, 15,60.
13C ЯМР (101 МГц, CDCl3) δ 172,83, 170,25, 162,99, 160,27, 157,77, 145,71, 143,98, 142,66, 129,51, 120,94, 115,66, 109,53, 89,59, 80,93, 73,13, 56,18, 48,26, 28,61, 20,87, 19,51, 18,62, 17,17, 15,97.
13C ЯМР (101 МГц, CDCl3) δ 172,39, 170,27, 163,07, 160,32, 157,45, 145,73, 144,05, 142,58, 129,56, 121,11, 115,93, 109,61, 89,62, 80,12, 72,63, 56,20, 48,43, 28,72, 20,88, 19,42, 18,69, 16,98, 15,63.
13C ЯМР (101 МГц, CDCl3) δ 172,70, 170,24, 162,99, 160,32, 157,76, 145,71, 144,06, 142,59, 129,53, 121,01, 115,75, 109,56, 89,63, 76,38, 73,68, 56,18, 48,26, 31,63, 29,36, 24,93, 22,43, 20,86, 18,59, 15,43, 13,97.
13C ЯМР (101 МГц, CDCl3) δ 172,49, 170,25, 163,02, 160,31, 157,77, 145,70, 144,05, 142,58, 129,51, 121,19, 116,27, 109,57, 89,62, 76,91, 74,82, 56,19, 48,35, 31,57, 29,81, 25,03, 22,45, 20,86, 18,51, 15,67, 13,94.
13C ЯМР (101 МГц, CDCl3) δ 172,68, 170,25, 162,99, 160,30, 157,86, 145,71, 144,03, 142,59, 129,53, 121,07, 115,89, 109,57, 89,59, 76,19, 73,58, 56,19, 48,28, 31,55, 29,02, 25,03, 22,43, 20,86, 18,55, 15,32, 13,92.
13C ЯМР (101 МГц, CDCl3) δ 172,56, 170,24, 163,00, 160,30, 157,68, 145,70, 144,02, 142,59, 129,52, 121,15, 116,12, 109,56, 89,62, 76,53, 74,70, 56,18, 48,27, 31,64, 30,04, 25,11, 22,44, 20,86, 18,63, 15,13, 13,98.
13C ЯМР (101 МГц, CDCl3) δ 172,67, 170,26, 163,07, 160,32, 157,72, 145,70, 144,07, 142,43, 129,54, 121,30, 116,17, 109,62, 89,58, 71,71, 67,67, 56,19, 48,13, 20,86, 18,30, 16,79.
13C ЯМР (101 МГц, CDCl3) δ 172,37, 168,90, 162,44, 159,50, 157,80, 149,25, 146,65, 141,59, 137,55, 129,51, 121,19, 116,32, 109,77, 75,27, 56,29, 48,21, 38,77, 24,53, 23,54, 21,69, 20,74, 18,50, 15,53.
13C ЯМР (101 МГц, CDCl3) δ 172,24, 168,88, 162,49, 159,50, 157,43, 146,68, 141,58, 137,55, 129,53, 121,09, 115,92, 109,79, 80,11, 72,60, 56,29, 48,28, 28,71, 20,73, 19,37, 18,72, 17,01, 15,52.
13C ЯМР (101 МГц, CDCl3) δ 172,36, 168,90, 162,44, 159,49, 157,76, 146,66, 141,60, 137,54, 129,51, 121,18, 116,27, 109,76, 76,89, 74,80, 56,28, 48,19, 31,57, 29,82, 25,01, 22,44, 20,74, 18,58, 15,60, 13,94.
13C ЯМР (101 МГц, CDCl3) δ 172,57, 168,89, 162,41, 159,50, 157,85, 146,66, 141,61, 137,55, 129,54, 121,06, 115,89, 109,76, 76,21, 73,55, 56,29, 48,11, 31,55, 28,99, 25,01, 22,43, 20,74, 18,61, 15,30, 13,93.
13C ЯМР (101 МГц, CDCl3) δ 172,44, 168,89, 162,45, 159,48, 157,68, 146,67, 141,59, 137,53, 129,51, 121,15, 116,12, 109,76, 76,56, 74,69, 56,28, 48,11, 31,64, 30,05, 25,08, 22,43, 20,73, 18,70, 15,16, 13,98.
13C ЯМР (101 МГц, CDCl3) δ 172,55, 168,86, 162,50, 159,49, 157,72, 146,65, 141,51, 137,55, 129,54, 121,30, 116,17, 109,80, 71,68, 67,66, 56,29, 47,91, 20,74, 18,42, 16,81.
13C ЯМР (126 МГц, CDCl3) δ 172,71, 168,93, 162,36, 159,43, 157,71, 146,67, 141,56, 137,48, 129,50, 120,91, 115,68, 109,71, 80,41, 72,45, 56,27, 48,05, 38,09, 29,53, 27,54, 26,13, 26,01, 25,87, 20,75, 18,80, 15,90.
13C ЯМР (126 МГц, CDCl3) δ 172,15, 168,93, 162,42, 159,46, 157,40, 146,66, 141,52, 137,51, 129,51, 121,05, 115,98, 109,76, 79,46, 72,14, 56,28, 48,23, 38,40, 29,69, 27,43, 26,22, 26,09, 25,85, 20,76, 18,77, 15,23.
13C ЯМР (126 МГц, CDCl3) δ 172,26, 168,92, 162,47, 159,48, 157,45 (д, J=238,9 Гц), 153,47 (д, J=2,2 Гц), 146,68, 141,48, 137,52, 117,31 (д, J=7,9 Гц), 115,90 (д, J=23,1 Гц), 109,79, 79,85, 73,74, 56,29, 48,21, 28,71, 20,75, 19,32, 18,71, 17,20, 15,29.
19F ЯМР (471 МГц, CDCl3) δ -123,25 (тт, J=8,4, 4,3 Гц).
13C ЯМР (126 МГц, CDCl3) δ 172,53, 168,91, 162,49, 159,47, 157,56 (д, J=239,0 Гц), 153,79 (д, J=2,2 Гц), 146,65, 141,38, 137,53, 117,57 (д, J=8,1 Гц), 115,90 (д, J=23,0 Гц), 109,82, 72,84, 67,58, 56,30, 47,86, 20,75, 18,40, 16,74.
19F ЯМР (471 МГц, CDCl3) δ -122,95 (тт, J=8,5, 4,4 Гц).
13C ЯМР (126 МГц, CDCl3) δ 172,82, 170,29, 162,95, 160,25, 157,71, 145,73, 143,97, 142,57, 129,50, 120,92, 115,67, 109,53, 89,58, 80,43, 72,44, 56,18, 48,20, 38,10, 29,53, 29,27, 27,57, 26,13, 26,01, 25,87, 18,70, 15,92.
13C ЯМР (126 МГц, CDCl3) δ 172,29, 170,30, 163,01, 160,29, 157,41, 145,70, 144,05, 142,48, 129,51, 121,07, 115,97, 109,56, 89,62, 79,48, 72,15, 56,18, 48,38, 38,41, 29,73, 27,39, 26,24, 26,10, 25,86, 20,88, 18,70, 15,33.
13C ЯМР (126 МГц, CDCl3) δ 172,76, 170,29, 162,97, 160,26, 157,33 (д, J=238,8 Гц), 153,79 (д, J=2,2 Гц), 145,71, 143,99, 142,51, 116,91 (д, J=7,8 Гц), 115,88 (д, J=22,9 Гц), 109,54, 89,56, 80,78, 74,21, 56,18, 48,23, 28,56, 20,88, 19,49, 18,62, 17,10, 15,86.
19F ЯМР (471 МГц, CDCl3) δ -123,48 (тт, J=8,2, 4,4 Гц).
13C ЯМР (126 МГц, CDCl3) δ 172,39, 170,30, 163,05, 160,29, 157,45 (д, J=238,9 Гц), 153,48 (д, J=2,3 Гц), 145,72, 144,04, 142,45, 117,29 (д, J=8,1 Гц), 115,91 (д, J=23,0 Гц), 109,59, 89,59, 79,86, 73,75, 56,19, 48,37, 28,70, 20,88, 19,36, 18,64, 17,12, 15,40.
19F ЯМР (471 МГц, CDCl3) δ -123,24 (тт, J=8,6, 4,4 Гц).
13C ЯМР (126 МГц, CDCl3) δ 172,65, 170,30, 163,07, 160,31, 157,56 (д, J=239,1 Гц), 153,78 (д, J=2,3 Гц), 145,70, 144,08, 142,28, 117,57 (д, J=7,9 Гц), 115,89 (д, J=23,0 Гц), 109,62, 89,55, 72,87, 67,59, 56,20, 48,10, 20,87, 18,26, 16,72.
19F ЯМР (471 МГц, CDCl3) δ -122,94 (тт, J=8,5, 4,4 Гц).
13C ЯМР (101 МГц, CDCl3) δ 172,22, 169,48, 162,43, 157,44, 147,46, 145,49, 141,20, 132,96, 129,54, 127,42, 121,11, 115,94, 80,18, 72,64, 48,29, 28,73, 21,04, 19,39, 18,74, 17,04, 15,53.
13C ЯМР (101 МГц, CDCl3) δ 172,26, 168,85, 162,55, 158,84, 157,45, 146,57, 141,67, 137,66, 129,53, 121,08, 115,94, 110,42, 80,10, 72,63, 64,98, 48,27, 28,72, 20,68, 19,38, 18,76, 17,01, 15,55, 14,28.
13C ЯМР (101 МГц, CDCl3) δ 172,45, 169,67, 163,05, 157,44, 153,38, 143,31, 140,47, 129,55, 127,77, 127,09, 121,11, 115,92, 87,50, 80,17, 72,63, 48,43, 28,72, 20,86, 19,42, 18,73, 16,97, 15,65.
13C ЯМР (101 МГц, CDCl3) δ 172,41, 170,18, 163,12, 159,55, 157,45, 145,61, 143,95, 142,71, 129,54, 121,09, 115,92, 110,27, 89,48, 80,10, 72,64, 64,86, 48,43, 28,71, 20,96, 19,41, 18,69, 16,96, 15,65, 14,37.
13C ЯМР (101 МГц, CDCl3) δ 172,68, 170,24, 162,95, 160,28, 157,79, 145,71, 143,97, 142,70, 129,51, 120,91, 115,66, 109,52, 89,61, 78,07, 73,44, 56,18, 48,24, 41,46, 22,07, 21,20, 20,86, 18,62, 16,23, 11,52, 11,32.
13C ЯМР (101 МГц, CDCl3) δ 172,36, 170,24, 163,05, 160,31, 157,48, 145,69, 144,05, 142,54, 129,54, 121,10, 115,98, 109,60, 89,60, 77,45, 72,67, 56,19, 48,42, 41,64, 22,48, 21,29, 20,86, 18,56, 16,00, 11,60, 11,48.
13C ЯМР (101 МГц, CDCl3) δ 172,33, 170,26, 163,02, 160,32, 157,56, 145,70, 144,04, 142,65, 129,50, 121,10, 116,13, 109,57, 89,64, 78,97, 74,33, 56,19, 48,43, 40,83, 29,14, 28,44, 25,51, 25,01, 20,86, 18,67, 15,18.
13C ЯМР (101 МГц, CDCl3) δ 172,78, 170,25, 163,01, 160,29, 157,80, 145,72, 144,01, 142,65, 129,53, 120,95, 115,70, 109,56, 89,61, 79,62, 73,79, 56,19, 48,36, 40,20, 29,20, 28,30, 25,32, 25,09, 20,86, 18,64, 16,02.
13C ЯМР (101 МГц, CDCl3) δ 172,21, 168,85, 162,44, 159,49, 157,46, 146,63, 141,57, 137,55, 129,52, 121,07, 115,97, 109,75, 72,65, 56,27, 48,25, 41,60, 22,43, 21,24, 20,72, 18,64, 15,91, 11,54, 11,44.
13C ЯМР (126 МГц, CDCl3) δ 172,21, 170,29, 162,88, 160,24, 145,69, 143,96, 142,52, 137,46, 129,36, 128,30, 126,45, 109,51, 89,57, 77,71, 75,94, 71,27, 56,17, 48,16, 35,96, 23,27, 20,88, 18,26, 16,13, 10,69.
13C ЯМР (126 МГц, CDCl3) δ 172,21, 170,29, 162,87, 160,25, 145,68, 143,97, 142,51, 137,46, 129,37, 128,30, 126,45, 109,51, 89,58, 77,70, 75,97, 69,67, 56,17, 48,17, 36,00, 29,76, 28,38, 22,52, 20,88, 18,27, 16,14, 14,06.
13C ЯМР (126 МГц, CDCl3) δ 172,18, 170,29, 162,86, 160,25, 145,68, 143,96, 142,52, 137,49, 129,37, 128,29, 126,44, 109,50, 89,58, 77,75, 76,43, 76,14, 56,17, 48,16, 36,02, 28,81, 20,88, 19,45, 19,39, 18,27, 16,03.
13C ЯМР (126 МГц, CDCl3) δ 172,43, 170,31, 162,95, 160,27, 145,70, 144,00, 142,55, 109,51, 89,62, 80,29, 75,92, 74,44, 56,17, 48,39, 28,76, 28,47, 20,89, 19,47, 19,44, 19,38, 18,77, 17,02, 15,46.
13C ЯМР (126 МГц, CDCl3) δ 172,45, 170,31, 162,96, 160,27, 145,70, 144,00, 142,56, 109,51, 89,62, 80,18, 74,27, 70,67, 56,17, 48,39, 28,51, 23,23, 20,89, 19,45, 18,77, 17,13, 15,52, 10,67.
13C ЯМР (126 МГц, CDCl3) δ 172,49, 170,30, 162,98, 160,29, 145,70, 144,03, 142,47, 131,30-123,76 (м), 109,54, 89,62, 79,79, 74,72, 66,96, 56,18, 48,34, 30,73 (кв., J=28,9 Гц), 28,58, 22,73 (кв., J=2,7 Гц), 20,88, 19,34, 18,69, 17,48, 15,15.
13C ЯМР (126 МГц, CDCl3) δ 172,48, 170,30, 162,95, 160,27, 145,69, 144,01, 142,52, 142,06, 128,45, 128,26, 125,68, 109,51, 89,62, 80,16, 74,41, 68,05, 56,17, 48,39, 32,39, 31,64, 28,54, 20,89, 19,45, 18,78, 17,27, 15,42.
13C ЯМР (126 МГц, CDCl3) δ 172,29, 168,93, 162,36, 159,43, 146,65, 141,58, 137,46, 109,70, 80,27, 75,91, 74,44, 56,27, 48,24, 28,75, 28,47, 20,75, 19,43, 18,84, 17,07, 15,38.
13C ЯМР (126 МГц, CDCl3) δ 172,37, 168,95, 162,40, 159,46, 146,66, 141,52, 137,51, 127,32 (кв., J=276,1 Гц), 109,75, 79,77, 74,72, 66,95, 56,29, 48,19, 30,73 (кв., J=28,9 Гц), 28,59, 22,73 (кв., J=3,1 Гц), 20,74, 19,31, 18,77, 17,57, 15,07.
13C ЯМР (126 МГц, CDCl3) δ 172,36, 168,96, 162,40, 159,44, 146,67, 142,07, 141,56, 137,48, 128,46, 128,26, 125,67, 109,72, 80,15, 74,42, 68,05, 56,28, 48,25, 32,37, 31,62, 28,56, 20,75, 19,40, 18,83, 17,35, 15,32.
13C ЯМР (126 МГц, CDCl3) δ 172,46, 170,31, 162,95, 160,27, 145,70, 144,00, 142,55, 142,37, 112,08, 109,52, 89,62, 80,04, 73,63, 72,69, 56,17, 48,39, 28,58, 20,89, 19,60, 19,43, 18,76, 17,34, 15,26.
13C ЯМР (126 МГц, CDCl3) δ 172,47, 170,31, 162,96, 160,27, 145,70, 144,00, 142,56, 134,94, 116,77, 109,52, 89,62, 80,00, 73,60, 69,66, 56,18, 48,39, 28,56, 20,89, 19,41, 18,75, 17,36, 15,33.
13C ЯМР (126 МГц, CDCl3) δ 172,49, 170,30, 163,00, 160,29, 145,71, 144,03, 142,45, 136,71 (д, J=6,5 Гц), 127,29-119,33 (m), 118,35 (кв., J=34,0 Гц), 109,56, 89,60, 79,61, 75,05, 66,51, 56,18, 48,35, 28,62, 20,88, 19,32, 18,64, 17,66, 15,05.
13C ЯМР (126 МГц, CDCl3) δ 172,36, 168,94, 162,42, 159,46, 146,67, 141,49, 137,51, 136,70 (кв., J=6,2 Гц), 126,66-119,76 (m), 118,36 (кв., J=33,9 Гц), 109,76, 79,58, 75,04, 66,49, 56,29, 48,19, 28,63, 20,74, 19,29, 18,72, 17,72, 14,98.
13C ЯМР (126 МГц, CDCl3) δ 172,70, 170,30, 162,93, 160,25, 145,72, 143,96, 142,66, 109,49, 89,60, 81,82, 75,93, 74,56, 56,17, 48,27, 28,81, 28,46, 20,89, 19,48, 19,45, 18,78, 17,61, 15,56.
13C ЯМР (101 МГц, CDCl3) δ 171,64, 170,25, 163,07, 160,31, 157,70, 145,68, 144,06, 142,50, 136,76, 129,49, 128,32, 128,25, 127,19, 121,37, 116,45, 109,60, 89,61, 78,19, 76,10, 56,19, 48,15, 20,85, 18,29, 15,40.
13C ЯМР (101 МГц, CDCl3) δ 171,77, 170,25, 162,97, 160,29, 158,06, 145,67, 144,03, 142,59, 136,54, 129,54, 128,53, 128,47, 127,43, 121,27, 116,18, 109,56, 89,61, 78,88, 75,46, 56,18, 48,11, 20,85, 18,25, 16,18.
13C ЯМР (101 МГц, CDCl3) δ 172,41, 170,25, 163,03, 160,31, 157,82, 145,71, 144,03, 142,59, 129,54, 121,07, 115,82, 109,57, 89,60, 74,55, 72,97, 56,18, 48,28, 20,86, 18,47, 15,28, 15,23.
19F ЯМР (376 МГц, CDCl3) δ -116,83 (д, J=15,1 Гц), -138,23 (дд, J=15,0, 1,3 Гц).
19F ЯМР (376 МГц, CDCl3) δ -61,56.
13C ЯМР (101 МГц, CDCl3) δ 172,37, 167,57 (д, J=538,8 Гц), 163,08, 162,46, 160,33, 158,80 (д, J=11,0 Гц), 145,72, 144,07, 142,56, 130,30 (д, J=10,1 Гц), 111,40 (д, J=2,9 Гц), 109,61, 107,90 (д, J=21,3 Гц), 103,52 (д, J=24,5 Гц), 89,62, 79,80, 73,07, 56,19, 48,40, 28,75, 20,86, 19,35, 18,61, 17,09, 15,39.
19F ЯМР (376 МГц, CDCl3) δ -111,60.
13C ЯМР (101 МГц, CDCl3) δ 172,38, 170,25, 163,04, 160,31, 150,80, 145,70, 144,04, 142,60, 131,84, 130,98, 128,04, 124,11, 115,94, 109,57, 89,63, 79,96, 74,53, 56,18, 48,42, 28,71, 20,87, 20,30, 19,39, 18,64, 17,25, 15,40.
13C ЯМР (101 МГц, CDCl3) δ 172,37, 170,24, 163,06, 160,31, 151,86, 145,70, 144,05, 142,50, 130,28, 127,54, 126,33, 125,22, 116,27, 109,61, 89,60, 79,61, 74,80, 56,19, 48,37, 28,72, 20,87, 19,34, 18,56, 17,37, 15,19.
13C ЯМР (101 МГц, CDCl3) δ 172,35, 170,25, 163,40 (д, J=248,0 Гц), 163,11, 160,34, 159,01 (д, J=12,4 Гц), 145,73, 144,09, 142,49, 135,47 (д, J=13,5 Гц), 112,13 (д, J=3,2 Гц), 109,64, 109,02 (д, J=25,3 Гц), 102,08 (д, J=24,8 Гц), 89,61, 79,49, 73,51, 56,20, 48,37, 28,77, 20,86, 19,29, 18,52, 17,21, 15,15.
19F ЯМР (376 МГц, CDCl3) δ -109,98.
13C ЯМР (101 МГц, CDCl3) δ 172,37, 170,25, 163,08, 160,32, 158,19, 145,72, 144,06, 134,93, 130,33, 129,54, 121,28, 116,27, 114,12, 109,61, 89,61, 79,81, 73,07, 56,19, 48,40, 28,74, 20,86, 19,35, 18,60, 17,10, 15,37.
13C ЯМР (101 МГц, CDCl3) δ 172,81, 170,23, 162,99, 160,27, 154,11, 151,81, 145,71, 143,97, 142,67, 117,18, 114,69, 109,55, 89,58, 81,03, 74,32, 56,18, 55,69, 48,29, 28,60, 20,86, 19,52, 18,68, 17,21, 16,01.
13C ЯМР (101 МГц, CDCl3) δ 172,39, 170,24, 163,06, 160,31, 154,25, 151,50, 145,72, 144,03, 142,59, 117,51, 114,72, 109,60, 89,60, 80,15, 73,97, 56,19, 55,69, 48,43, 28,72, 20,86, 19,42, 18,68, 17,06, 15,66.
13C ЯМР (101 МГц, CDCl3) δ 172,67, 170,26, 163,07, 160,31, 154,43, 151,72, 145,70, 144,06, 142,43, 117,87, 114,70, 109,62, 89,57, 73,11, 67,71, 56,19, 55,69, 48,14, 20,85, 18,34, 16,86.
19F ЯМР (376 МГц, CDCl3) δ -116,83 (д, J=15,1 Гц), -138,18 (дд, J=15,0, 1,3 Гц).
19F ЯМР (376 МГц, CDCl3) δ -61,54.
19F ЯМР (376 МГц, CDCl3) δ -109,97.
13C ЯМР (101 МГц, CDCl3) δ 171,52, 168,88, 162,49, 159,49, 157,68, 146,64, 141,52, 137,57, 136,75, 129,49, 128,33, 128,23, 127,14, 121,37, 116,45, 109,80, 78,16, 76,12, 56,28, 47,96, 20,75, 18,39, 15,31.
13C ЯМР (101 МГц, CDCl3) δ 171,66, 168,88, 162,39, 159,47, 158,04, 146,62, 136,50, 129,54, 128,52, 128,46, 128,10, 127,42, 127,39, 121,26, 116,18, 109,75, 78,93, 75,43, 56,28, 47,90, 20,74, 18,32, 16,16.
13C ЯМР (101 МГц, CDCl3) δ 172,07, 168,88, 162,47, 159,48, 157,88, 146,66, 141,59, 137,53, 129,51, 121,24, 116,38, 109,78, 75,51, 73,82, 56,28, 48,07, 20,74, 18,42, 15,75, 15,14.
13C ЯМР (101 МГц, CDCl3) δ 172,23, 168,85, 162,49, 159,50, 151,86, 146,67, 141,55, 137,55, 130,28, 127,53, 126,32, 125,24, 116,30, 109,81, 79,60, 74,79, 56,29, 48,22, 28,73, 20,73, 19,30, 18,60, 17,43, 15,08.
13C ЯМР (101 МГц, CDCl3) δ 172,21, 168,86, 162,48, 159,50, 158,17, 146,66, 137,56, 134,90, 130,31, 129,52, 121,26, 116,21, 114,16, 109,79, 79,80, 73,04, 56,28, 48,23, 28,73, 20,72, 19,30, 18,64, 17,11, 15,27.
13C ЯМР (101 МГц, CDCl3) δ 172,25, 168,86, 162,48, 159,50, 154,24, 151,49, 146,68, 141,59, 137,54, 117,52, 114,71, 109,80, 80,13, 73,95, 56,28, 55,68, 48,28, 28,72, 20,73, 19,38, 18,73, 17,10, 15,56.
13C ЯМР (101 МГц, CDCl3) δ 172,55, 168,87, 162,49, 159,49, 154,43, 151,73, 146,65, 141,51, 137,55, 117,88, 114,71, 109,81, 73,09, 67,71, 56,29, 55,70, 47,92, 20,74, 18,47, 16,89.
13C ЯМР (101 МГц, CDCl3) δ 172,66, 157,53, 154,96, 136,84, 129,54, 129,43, 128,39, 126,65, 121,28, 116,20, 79,70, 76,94, 74,12, 49,30, 36,29, 28,32, 18,40, 15,72.
13C ЯМР (101 МГц, CDCl3) δ 172,27, 157,82, 155,07, 132,06, 129,52, 121,41, 119,41, 116,52, 79,75, 77,31, 75,06, 49,39, 28,34, 18,51, 15,56.
13C ЯМР (101 МГц, CDCl3) δ 172,52, 157,70, 155,01, 131,81, 129,56, 121,21, 119,51, 115,85, 79,77, 76,85, 74,01, 49,38, 28,33, 18,70, 15,67.
13C ЯМР (101 МГц, CDCl3) δ 173,21, 156,78 (д, J=238,1 Гц), 155,02, 151,54 (д, J=2,2 Гц), 129,59 (д, J=7,6 Гц), 117,53 (д, J=22,7 Гц), 112,71 (д, J=8,4 Гц), 112,36 (д, J=22,7 Гц), 80,85, 79,72, 73,52, 49,41, 28,66, 28,31, 19,40, 18,71, 17,26, 16,42 (д, J=1,2 Гц), 15,84.
19F ЯМР (376 МГц, CDCl3) δ -124,33.
13C ЯМР (101 МГц, CDCl3) δ 172,98, 156,94 (д, J=238,5 Гц), 155,06, 151,40 (д, J=2,2 Гц), 129,85 (д, J=7,7 Гц), 117,60 (д, J=22,7 Гц), 113,27 (д, J=8,5 Гц), 112,39 (д, J=22,7 Гц), 80,02, 79,79, 73,29, 49,52, 28,87, 28,35, 19,33, 18,93, 17,45, 16,55, 15,06.
19F ЯМР (376 МГц, CDCl3) δ -124,10.
13C ЯМР (101 МГц, CDCl3) δ 173,21, 157,24 (д, J=239,0 Гц), 155,06, 151,87 (д, J=2,3 Гц), 130,10 (д, J=7,6 Гц), 117,48 (д, J=22,6 Гц), 114,96 (д, J=8,6 Гц), 112,59 (д, J=22,8 Гц), 79,90, 73,04, 67,63, 49,26, 28,33, 18,55, 16,88, 16,41.
19F ЯМР (376 МГц, CDCl3) δ -123,30.
13C ЯМР (101 МГц, CDCl3) δ 173,37, 155,61, 130,25, 129,97, 115,95, 115,64, 80,93, 79,68, 73,25, 49,43, 28,60, 28,35, 20,45, 19,44, 18,89, 17,27, 15,95.
13C ЯМР (101 МГц, CDCl3) δ 172,91, 155,32, 155,08, 130,42, 129,99, 115,95, 79,92, 79,73, 72,91, 49,59, 28,72, 28,35, 20,48, 19,35, 18,85, 17,08, 15,55.
13C ЯМР (101 МГц, CDCl3) δ 173,21, 155,57, 155,07, 130,70, 130,00, 116,23, 79,84, 72,03, 67,62, 49,28, 28,34, 20,48, 18,62, 16,79.
13C ЯМР (101 МГц, CDCl3) δ 172,98, 157,82, 155,06, 129,52, 121,21, 116,26, 79,73, 77,98, 74,52, 49,53, 28,34, 22,93, 18,71, 15,71, 9,79.
13C ЯМР (101 МГц, CDCl3) δ 173,29, 157,79, 155,07, 129,55, 121,03, 115,70, 79,75, 77,56, 73,54, 49,42, 28,35, 22,70, 18,79, 15,50, 9,70.
13C ЯМР (101 МГц, CDCl3) δ 172,87, 158,44, 157,43, 155,03, 129,59, 129,49, 121,54, 121,23, 116,32, 114,66, 79,85, 74,93, 72,68, 65,99, 49,43, 28,32, 18,58, 16,16.
13C ЯМР (101 МГц, CDCl3) δ 172,82, 157,56, 155,05, 129,55, 121,38, 116,27, 79,79, 75,12, 72,53, 70,67, 59,12, 49,44, 28,34, 18,67, 15,97.
13C ЯМР (101 МГц, CDCl3) δ 172,78, 157,55, 155,01, 137,82, 129,54, 128,36, 127,68, 127,60, 121,34, 116,22, 79,79, 75,22, 73,26, 72,44, 68,16, 49,40, 28,34, 18,70, 15,97.
19F ЯМР (376 МГц, CDCl3) δ -129,76 (д, J=292,4 Гц), -132,83 (д, J=292,5 Гц).
13C ЯМР (101 МГц, CDCl3) δ 172,78, 157,63, 155,03, 129,52, 121,31, 116,26, 79,76, 75,25, 73,09, 72,60, 68,64, 49,41, 28,35, 22,83, 18,74, 15,93, 10,50.
13C ЯМР (101 МГц, CDCl3) δ 172,78, 157,62, 155,03, 129,51, 121,30, 116,23, 79,78, 75,27, 72,55, 69,91, 68,70, 49,40, 38,43, 28,35, 25,00, 22,60, 22,56, 18,74, 15,92.
13C ЯМР (101 МГц, CDCl3) δ 172,92, 155,02, 79,92, 77,20, 74,33, 73,43, 49,55, 35,28, 28,56, 28,32, 24,99, 24,89, 19,34, 18,98, 18,54, 17,25, 15,37.
13C ЯМР (101 МГц, CDCl3) δ 171,54, 168,68, 157,56, 155,38, 148,79, 140,43, 136,76, 130,47, 129,56, 129,40, 128,41, 126,70, 121,35, 116,24, 109,48, 77,45, 74,16, 56,07, 47,95, 36,05, 17,94, 15,78.
13C ЯМР (101 МГц, CDCl3) δ 172,00, 168,73, 156,80 (д, J=238,3 Гц), 155,40, 151,52 (д, J=2,2 Гц), 148,80, 140,43, 130,49, 129,69 (д, J=7,5 Гц), 117,52 (д, J=22,6 Гц), 112,78 (д, J=8,4 Гц), 112,34 (д, J=22,8 Гц), 109,45, 81,24, 73,60, 56,07, 48,07, 28,71, 19,50, 18,33, 17,22, 16,39, 15,88.
19F ЯМР (376 МГц, CDCl3) δ -124,25.
13C ЯМР (101 МГц, CDCl3) δ 171,78, 168,80, 156,96 (д, J=238,4 Гц), 155,42, 151,37 (д, J=2,1 Гц), 148,82, 140,50, 130,50, 129,88 (д, J=7,6 Гц), 117,61 (д, J=22,7 Гц), 113,33 (д, J=8,6 Гц), 112,39 (д, J=22,8 Гц), 109,51, 80,48, 73,34, 56,08, 48,11, 28,87, 19,35, 18,46, 17,49, 16,52, 15,04.
19F ЯМР (376 МГц, CDCl3) δ -123,99.
19F ЯМР (376 МГц, CDCl3) δ -123,30.
13C ЯМР (101 МГц, CDCl3) δ 172,18, 168,72, 155,57, 155,37, 148,79, 140,43, 130,60, 130,29, 129,95, 115,67, 109,43, 81,31, 73,34, 56,06, 48,04, 28,60, 20,45, 19,52, 18,49, 17,11, 15,99.
13C ЯМР (101 МГц, CDCl3) δ 171,72, 168,82, 155,39, 155,27, 148,80, 140,49, 130,53, 130,48, 130,00, 115,95, 109,50, 80,41, 72,91, 56,07, 48,17, 28,71, 20,47, 19,37, 18,45, 17,11, 15,53.
13C ЯМР (101 МГц, CDCl3) δ 172,04, 168,80, 155,55, 155,40, 148,80, 140,48, 130,73, 130,45, 129,99, 116,25, 109,50, 72,05, 67,91, 56,07, 47,89, 20,48, 18,18, 16,75.
13C ЯМР (101 МГц, CDCl3) δ 171,90, 168,80, 157,75, 155,40, 148,81, 140,48, 130,52, 129,53, 121,26, 116,24, 109,50, 78,44, 74,46, 56,07, 48,14, 22,86, 18,29, 15,65, 9,81.
13C ЯМР (101 МГц, CDCl3) δ 172,12, 168,77, 157,75, 155,40, 148,80, 140,47, 130,54, 129,54, 121,06, 115,72, 109,47, 78,03, 73,61, 56,07, 48,05, 22,74, 18,37, 15,55, 9,69.
13C ЯМР (101 МГц, CDCl3) δ 171,21, 168,81, 157,75, 155,39, 148,80, 140,48, 131,89, 130,49, 129,53, 121,45, 119,72, 116,49, 109,50, 77,75, 75,01, 56,07, 47,99, 18,13, 15,50.
13C ЯМР (101 МГц, CDCl3) δ 171,38, 168,75, 157,69, 155,38, 148,78, 140,47, 131,70, 130,47, 129,54, 121,23, 119,91, 115,87, 109,49, 77,43, 74,08, 56,07, 48,02, 18,26, 15,74.
13C ЯМР (101 МГц, CDCl3) δ 171,76, 168,87, 158,42, 157,40, 155,38, 148,80, 140,48, 130,42, 129,60, 129,49, 121,58, 121,26, 116,31, 114,66, 109,51, 75,36, 72,71, 65,94, 56,05, 48,06, 18,11, 16,18.
13C ЯМР (101 МГц, CDCl3) δ 171,72, 168,83, 157,52, 155,40, 148,80, 140,49, 130,50, 129,55, 121,42, 116,26, 109,51, 75,53, 72,58, 70,61, 59,14, 56,07, 48,06, 18,19, 15,97.
13C ЯМР (101 МГц, CDCl3) δ 171,68, 168,82, 157,52, 155,39, 148,80, 140,48, 137,80, 130,48, 129,54, 128,36, 127,67, 127,56, 121,38, 116,23, 109,50, 75,68, 73,28, 72,47, 68,11, 56,06, 48,05, 18,20, 16,00.
13C ЯМР (101 МГц, CDCl3) δ 171,29, 168,98, 156,67, 155,45, 148,86, 140,57, 130,34, 129,72, 122,08, 116,38, 112,82 (дд, J=245,6, 243,0 Гц), 109,61, 73,45 (дд, J=22,7, 20,6 Гц), 71,70-71,53 (m), 56,10, 47,90, 17,96, 16,06 (д, J=2,1 Гц).
19F ЯМР (376 МГц, CDCl3) δ -129,59 (дд, J=292,9, 2,5 Гц), -132,79 (дд, J=293,3, 4,2 Гц).
13C ЯМР (101 МГц, CDCl3) δ 171,69, 168,81, 157,60, 155,40, 148,81, 140,48, 130,52, 129,53, 121,36, 116,26, 109,50, 75,72, 73,13, 72,64, 68,58, 56,07, 48,06, 22,83, 18,24, 15,95, 10,48.
13C ЯМР (101 МГц, CDCl3) δ 171,70, 168,80, 157,59, 155,41, 148,82, 140,47, 130,53, 129,53, 121,35, 116,23, 109,49, 75,74, 72,59, 69,95, 68,63, 56,08, 48,05, 38,43, 25,01, 22,60, 22,56, 18,24, 15,95.
13C ЯМР (126 МГц, CDCl3) δ 171,89, 168,70, 155,34, 148,74, 140,46, 138,30, 130,54, 128,34, 127,72, 127,57, 109,41, 80,13, 73,63, 70,65, 56,07, 48,13, 28,57, 19,35, 18,52, 17,48, 15,17.
13C ЯМР (126 МГц, CDCl3) δ 171,82, 168,69, 155,34, 148,73, 140,46, 130,55, 109,40, 80,40, 74,24, 67,28, 56,07, 48,14, 38,86, 28,54, 24,93, 22,69, 22,49, 19,39, 18,55, 17,31, 15,34.
13C ЯМР (126 МГц, CDCl3) δ 171,82, 168,69, 155,34, 148,73, 140,46, 130,55, 109,40, 80,33, 74,23, 69,05, 56,07, 48,14, 29,71, 28,55, 28,34, 22,50, 19,37, 18,56, 17,34, 15,36, 14,01.
13C ЯМР (126 МГц, CDCl3) δ 171,84, 168,70, 155,34, 148,73, 140,46, 130,55, 109,40, 80,08, 73,84, 73,57, 56,07, 48,14, 28,57, 19,35, 18,55, 17,40, 15,45, 10,81, 2,96, 2,94.
13C ЯМР (126 МГц, CDCl3) δ 171,82, 168,70, 155,34, 148,73, 140,46, 130,55, 109,40, 80,35, 74,23, 68,74, 56,07, 48,14, 32,12, 28,54, 19,36, 18,55, 17,33, 15,36, 13,89.
13C ЯМР (126 МГц, CDCl3) δ 171,82, 168,69, 155,34, 148,73, 140,46, 130,54, 109,40, 80,36, 74,35, 69,07, 56,07, 48,14, 35,13, 28,57, 19,36, 18,55, 17,38, 15,35, 7,93, 4,23, 4,11.
13C ЯМР (75 МГц, CDCl3) δ 172,07, 168,94, 162,36, 159,45, 157,46, 146,66, 141,47, 137,49, 136,80, 129,56, 129,48, 128,40, 126,67, 121,24, 116,15, 109,77, 77,11, 73,99, 56,31, 48,00, 36,25, 20,77, 18,30, 15,71.
19F ЯМР (376 МГц, CDCl3) δ -124,13.
13C ЯМР (75 МГц, CDCl3) δ 172,53, 168,93, 162,47, 159,46, 157,15 (д, J=238,8 Гц), 151,83 (д, J=2,2 Гц), 146,65, 141,34, 137,52, 130,08 (д, J=7,5 Гц), 117,42 (д, J=22,5 Гц), 114,85 (д, J=8,5 Гц), 112,55 (д, J=22,6 Гц), 109,82, 73,00, 67,70, 56,45-56,15 (m), 47,86, 20,76, 18,41, 16,86, 16,42.
19F ЯМР (376 МГц, CDCl3) δ -123,40.
13C ЯМР (75 МГц, CDCl3) δ 172,73, 168,95, 162,38, 159,42, 155,55, 146,69, 141,58, 137,46, 130,20, 129,95, 115,63, 109,71, 80,97, 73,31, 56,26, 48,08, 28,55, 20,77, 20,49, 19,50, 18,81, 17,13, 15,92.
13C ЯМР (75 МГц, CDCl3) δ 172,25, 168,95, 162,46, 159,46, 155,23, 146,70, 141,51, 137,50, 130,38, 129,99, 115,87, 109,78, 80,10, 72,74, 56,31, 48,26, 28,67, 20,77, 20,49, 19,37, 18,77, 16,98, 15,56.
13C ЯМР (75 МГц, CDCl3) δ 172,58, 168,94, 162,47, 159,45, 155,52, 146,68, 141,43, 137,51, 130,66, 129,99, 116,20, 109,79, 71,97, 67,68, 56,28, 47,89, 20,77, 20,50, 18,47, 16,81.
13C ЯМР (75 МГц, CDCl3) δ 172,41, 168,96, 162,45, 159,46, 157,69, 146,69, 141,50, 137,49, 129,52, 121,16, 116,17, 109,78, 78,10, 74,38, 56,28, 48,18, 23,00, 20,77, 18,61, 15,65, 9,80.
13C ЯМР (75 МГц, CDCl3) δ 172,67, 168,95, 162,43, 159,44, 157,72, 146,70, 141,51, 137,49, 129,54, 120,99, 115,67, 109,77, 77,60, 73,43, 56,31, 48,07, 22,52, 20,76, 18,66, 15,42, 9,72.
13C ЯМР (75 МГц, CDCl3) δ 171,72, 168,96, 162,46, 159,45, 157,71, 146,68, 141,45, 137,50, 132,04, 129,53, 121,38, 119,54, 116,46, 109,79, 99,99, 75,01, 56,28, 48,01, 20,77, 18,48, 15,51.
13C ЯМР (75 МГц, CDCl3) δ 171,92, 168,94, 162,43, 159,44, 157,66, 146,69, 141,44, 137,49, 131,65, 129,55, 121,17, 119,69, 115,82, 109,79, 76,91, 73,89, 56,28, 48,02, 20,76, 18,59, 15,62.
13C ЯМР (75 МГц, CDCl3) δ 172,20, 170,31, 162,94, 160,26, 157,47, 145,71, 144,00, 142,42, 136,84, 129,56, 129,47, 128,40, 126,66, 121,26, 116,15, 109,57, 89,56, 77,12, 74,05, 56,21, 48,17, 36,24, 20,87, 18,17, 15,79.
13C ЯМР (75 МГц, CDCl3) δ 172,68, 170,30, 162,95, 160,26, 156,72 (д, J=237,8 Гц), 151,53 (д, J=2,2 Гц), 145,71, 143,99, 142,44, 129,64 (д, J=7,5 Гц), 117,49 (д, J=22,9 Гц), 112,69 (д, J=8,5 Гц), 112,33 (д, J=22,9 Гц), 109,55, 89,55, 80,93, 73,56, 56,17, 48,25, 28,66, 20,87, 19,47, 18,53, 17,25, 16,44, 15,84.
19F ЯМР (376 МГц, CDCl3) δ -124,35.
13C ЯМР (75 МГц, CDCl3) δ 172,43, 170,32, 163,01, 160,29, 156,87 (д, J=238,2 Гц), 151,34 (д, J=2,1 Гц), 145,73, 144,05, 142,39, 129,83 (д, J=7,6 Гц), 117,57 (д, J=22,6 Гц), 113,23 (д, J=8,6 Гц), 112,37 (д, J=22,7 Гц), 109,59, 89,60, 80,14, 73,20, 56,22, 48,34, 28,80, 20,87, 19,37, 18,70, 17,32, 16,58, 15,15.
19F ЯМР (376 МГц, CDCl3) δ -124,10.
13C ЯМР (75 МГц, CDCl3) δ 172,65, 170,32, 163,05, 160,30, 157,14 (д, J=238,7 Гц), 151,83 (д, J=2,3 Гц), 145,70, 144,07, 142,23, 130,07 (д, J=7,8 Гц), 117,41 (д, J=22,7 Гц), 114,87 (д, J=8,4 Гц), 112,55 (д, J=22,8 Гц), 109,63, 89,55, 73,04, 67,70, 56,18, 48,09, 20,87 (д, J=1,9 Гц), 18,25, 16,85, 16,42.
19F ЯМР (376 МГц, CDCl3) δ -123,39.
13C ЯМР (75 МГц, CDCl3) δ 172,86, 170,31, 162,97, 160,24, 155,55, 145,74, 143,94, 142,56, 130,20, 129,95, 115,62, 109,53, 89,56, 80,98, 73,31, 56,17, 48,24, 28,56, 20,90, 20,46, 19,50, 18,68, 17,16, 15,93.
13C ЯМР (75 МГц, CDCl3) δ 172,38, 170,32, 163,03, 160,28, 155,24, 145,74, 144,01, 142,47, 130,39, 129,99, 115,86, 109,58, 89,58, 80,10, 72,75, 56,18, 48,40, 28,66, 20,88, 20,49, 19,40, 18,70, 16,93, 15,64.
13C ЯМР (75 МГц, CDCl3) δ 172,70, 170,32, 163,05, 160,29, 155,52, 145,72, 144,05, 142,34, 130,65, 129,99, 116,19, 109,60, 89,57, 72,00, 67,68, 56,18, 48,11, 20,87, 20,49, 18,34, 16,78.
13C ЯМР (75 МГц, CDCl3) δ 172,54, 170,32, 163,03, 160,27, 157,69, 145,75, 144,00, 142,47, 129,52, 121,16, 116,16, 109,58, 89,58, 78,11, 74,39, 56,22, 48,35, 22,99, 20,88, 18,54, 15,71, 9,81.
13C ЯМР (75 МГц, CDCl3) δ 172,79, 170,31, 163,01, 160,26, 157,73, 145,75, 143,99, 142,48, 129,54, 120,98, 115,66, 109,57, 89,56, 77,63, 73,49, 56,18, 48,24, 22,61, 20,90, 18,55, 15,47, 9,73.
13C ЯМР (75 МГц, CDCl3) δ 171,83, 170,32, 163,04, 160,27, 157,71, 145,73, 144,02, 142,40, 132,05, 129,52, 121,37, 119,55, 116,44, 109,59, 89,58, 76,63, 74,99, 56,18, 48,20, 20,88, 18,35, 15,55.
13C ЯМР (75 МГц, CDCl3) δ 172,06, 170,32, 162,99, 160,26, 157,67, 145,72, 144,02, 142,39, 131,69, 129,55, 121,17, 119,71, 115,81, 109,58, 89,55, 76,97, 73,96, 56,21, 48,20, 20,89, 18,45, 15,66.
13C ЯМР (126 МГц, CDCl3) δ 172,26, 168,93, 162,50, 159,45, 158,42, 157,36, 146,66, 141,43, 137,52, 129,58, 129,47, 121,48, 121,18, 116,26, 114,64, 109,78, 74,99, 72,58, 65,92, 56,29, 48,07, 20,76, 18,47, 16,12.
13C ЯМР (126 МГц, CDCl3) δ 172,23, 168,93, 162,45, 159,45, 157,49, 146,67, 141,49, 137,51, 129,53, 121,31, 116,21, 109,76, 75,22, 72,43, 70,65, 59,16, 56,29, 48,07, 20,76, 18,53, 15,93.
13C ЯМР (126 МГц, CDCl3) δ 172,20, 168,93, 162,45, 159,45, 157,50, 146,67, 141,48, 137,84, 137,51, 129,53, 128,35, 127,64, 127,57, 121,28, 116,18, 109,76, 75,37, 73,24, 72,33, 68,14, 56,28, 48,06, 20,76, 18,55, 15,96.
19F ЯМР (471 МГц, CDCl3) δ -129,77 (ддд, J=292,4, 54,1, 6,2 Гц), -132,75 (дд, J=293,4, 54,6 Гц).
13C ЯМР (126 МГц, CDCl3) δ 172,21, 168,93, 162,43, 159,45, 157,56, 146,67, 141,52, 137,51, 129,51, 121,25, 116,20, 109,75, 75,37, 73,09, 72,51, 68,60, 56,28, 48,05, 22,82, 20,76, 18,58, 15,89, 10,50.
13C ЯМР (126 МГц, CDCl3) δ 172,39, 170,30, 163,08, 160,26, 158,43, 157,36, 145,72, 144,04, 142,37, 129,59, 129,48, 121,49, 121,18, 116,26, 114,63, 109,58, 89,55, 75,04, 72,60, 65,97, 56,19, 48,27, 20,88, 18,34, 16,21.
13C ЯМР (126 МГц, CDCl3) δ 172,36, 170,31, 163,04, 160,27, 157,49, 145,72, 144,04, 142,45, 129,54, 121,32, 116,21, 109,57, 89,59, 75,25, 72,44, 70,67, 59,16, 56,19, 48,26, 20,88, 18,41, 16,01.
13C ЯМР (126 МГц, CDCl3) δ 172,33, 170,30, 163,03, 160,27, 157,50, 145,72, 144,03, 142,44, 137,83, 129,53, 128,35, 127,64, 127,58, 121,29, 116,17, 109,56, 89,57, 75,39, 73,24, 72,35, 68,16, 56,18, 48,25, 20,88, 18,42, 16,03.
19F ЯМР (471 МГц, CDCl3) δ -129,80 (ддд, J=292,2, 53,9, 6,1 Гц), -132,93 (ддд, J=292,3, 54,9, 17,7 Гц).
13C ЯМР (126 МГц, CDCl3) δ 172,34, 170,30, 163,02, 160,26, 157,56, 145,72, 144,02, 142,48, 129,51, 121,26, 116,20, 109,55, 89,58, 75,41, 73,09, 72,52, 68,63, 56,18, 48,24, 22,81, 20,88, 18,46, 15,97, 10,50.
13C ЯМР (126 МГц, CDCl3) δ 172,34, 170,30, 163,02, 160,27, 157,56, 145,72, 144,02, 142,49, 129,51, 121,25, 116,17, 109,55, 89,58, 75,42, 72,47, 69,89, 68,68, 56,18, 48,23, 38,40, 24,96, 22,60, 22,56, 20,88, 18,44, 15,96.
13C ЯМР (126 МГц, CDCl3) δ 172,52, 170,30, 162,95, 160,28, 145,69, 144,03, 142,53, 138,38, 128,33, 127,72, 127,54, 109,52, 89,63, 79,98, 73,67, 70,64, 56,18, 48,40, 28,53, 20,89, 19,44, 18,76, 17,24, 15,35.
13C ЯМР (126 МГц, CDCl3) δ 172,45, 170,30, 162,94, 160,28, 145,69, 144,02, 142,55, 109,51, 89,63, 80,23, 74,27, 67,27, 56,17, 48,40, 38,88, 28,49, 24,93, 22,70, 22,49, 20,90, 19,48, 18,79, 17,07, 15,53.
13C ЯМР (126 МГц, CDCl3) δ 172,45, 170,30, 162,94, 160,28, 145,69, 144,02, 142,55, 109,51, 89,64, 80,18, 74,26, 69,04, 56,17, 48,40, 29,72, 28,50, 28,34, 22,50, 20,90, 19,47, 18,79, 17,10, 15,56, 14,03.
13C ЯМР (126 МГц, CDCl3) δ 172,47, 170,30, 162,95, 160,28, 145,69, 144,02, 142,55, 109,51, 89,64, 79,97, 73,86, 73,55, 56,18, 48,40, 28,51, 20,90, 19,45, 18,78, 17,15, 15,64, 10,83, 2,98, 2,95.
13C ЯМР (126 МГц, CDCl3) δ 172,45, 170,30, 162,94, 160,28, 145,69, 144,02, 142,56, 109,51, 89,63, 80,20, 74,26, 68,72, 56,17, 48,40, 32,14, 28,50, 20,90, 19,47, 19,36, 18,79, 17,09, 15,55, 13,90.
13C ЯМР (126 МГц, CDCl3) δ 172,46, 170,30, 162,94, 160,28, 145,69, 144,02, 142,55, 109,51, 89,63, 80,19, 74,39, 69,05, 56,18, 48,39, 35,15, 28,53, 20,90, 19,44, 18,79, 17,16, 15,53, 7,95, 4,24, 4,10.
13C ЯМР (126 МГц, CDCl3) δ 172,38, 168,93, 162,38, 159,45, 146,66, 141,59, 138,39, 137,49, 128,33, 127,53, 109,71, 79,97, 73,66, 70,62, 56,28, 48,25, 28,53, 20,76, 19,42, 18,83, 17,30, 15,29.
13C ЯМР (126 МГц, CDCl3) δ 172,31, 168,93, 162,37, 159,44, 146,66, 141,61, 137,48, 109,70, 80,16, 74,26, 69,02, 56,27, 48,26, 29,72, 28,51, 28,34, 22,50, 20,76, 19,43, 18,87, 17,16, 15,48, 14,03.
13C ЯМР (126 МГц, CDCl3) δ 172,33, 168,93, 162,37, 159,44, 146,66, 141,61, 137,48, 109,71, 79,94, 73,86, 73,54, 56,28, 48,25, 28,52, 20,76, 19,41, 18,86, 17,21, 15,57, 10,83, 2,97, 2,95.
13C ЯМР (126 МГц, CDCl3) δ 172,32, 168,93, 162,37, 159,44, 146,66, 141,60, 137,48, 109,70, 80,18, 74,26, 68,71, 56,27, 48,25, 32,14, 28,51, 20,76, 19,43, 19,36, 18,87, 17,16, 15,47, 13,90.
*Соед.№ - Номер соединения.
Биологическое испытание, шкала оценки
Биологическая активность - Контроль PUCCRT и SEPTTR заболевания при нанесениях в большом объеме (100 ч/млн.)*
*Соед.№ - Номер соединения
*PUCCRT - Бурая ржавчина пшеницы (Puccinia triticina)
*SEPTTR - Пятнистость листьев пшеницы (Zymoseptoria tritici)
*1DP - защита 1 день
*3DC - лечение 3 дня
*ppm - частей на миллион.
Биологическая активность - Контроль PUCCRT и SEPTTR заболевания при нанесениях в малом объеме (121,5 г/Га)*
*Соед.№ - Номер соединения
*PUCCRT - Бурая ржавчина пшеницы (Puccinia triticina)
*SEPTTR - Пятнистость листьев пшеницы (Zymoseptoria tritici)
*1DP - защита 1 день
*3DC - лечение 3 дня
*г/Га - грамм на гектар
*ppm - частей на миллион.
Биологическая активность - Контроль PHAKP заболевания при нанесениях в большом объеме (25 ч/млн)*
*Соед.№ - Номер соединения
*PHAKPA - Азиатская ржавчина сои (Phakopsora pachyrhizi)
*1DP - защита 1 день
*3DC - лечение 3 дня
*ppm - частей на миллион.
Биологическая активность - 1DP*
Контроль заболевания при 100 ч/млн
Соед.№ - Номер соединения.
*1DP - защита 1 день
*ALTESO - Альтернариоз томатов (Alternaria solani)
*CERCBE - Пятнистость листьев сахарной свеклы (Cercospora beticola)
*COLLLA - Антракноз огуречных растений (Colletotricum lagenarium)
*LEPTNO - Септориоз колоса пшеницы (Leptosphaeria nodorum)
*PYRIOR - Пирикуляриоз риса (Pyricularia oryzae)
*RHYNSE - Ринхоспориоз ячменя (Rhyncosporium secalis)
*VENTIN - Парша яблок (Venturia inaequalis)
*ppm - частей на миллион.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ СОЕДИНЕНИЙ ПИКОЛИНАМИДА В КАЧЕСТВЕ ФУНГИЦИДОВ | 2015 |
|
RU2702088C2 |
| СОЕДИНЕНИЯ ПИКОЛИНАМИДА С ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2708392C2 |
| СОЕДИНЕНИЯ ПИКОЛИНАМИДА С ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2797810C2 |
| ПИКОЛИНАМИДЫ С ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2703402C2 |
| ПИКОЛИНАМИДЫ В КАЧЕСТВЕ ФУНГИЦИДОВ | 2015 |
|
RU2686987C2 |
| ПИКОЛИНАМИДНЫЕ СОЕДИНЕНИЯ С ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2687160C2 |
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ И ОТНОСЯЩИЕСЯ К НИМ СПОСОБЫ | 2013 |
|
RU2651369C1 |
| ПРИМЕНЕНИЕ СОЕДИНЕНИЙ ПИКОЛИНАМИДА С ФУНГИЦИДНЫМ ДЕЙСТВИЕМ | 2015 |
|
RU2704867C2 |
| ЛЕЧЕНИЕ ИНФЕКЦИЙ H. PYLORI С ПРИМЕНЕНИЕМ ИНГИБИТОРОВ MTAN | 2015 |
|
RU2663803C2 |
| ОБЩИЙ СИНТЕЗ МИРИАПОРОНОВ | 2003 |
|
RU2328492C2 |
Изобретение относится к сельскому хозяйству. Композиция для борьбы с грибковым патогеном содержит эффективное количество по меньшей мере одного соединения формулы 1
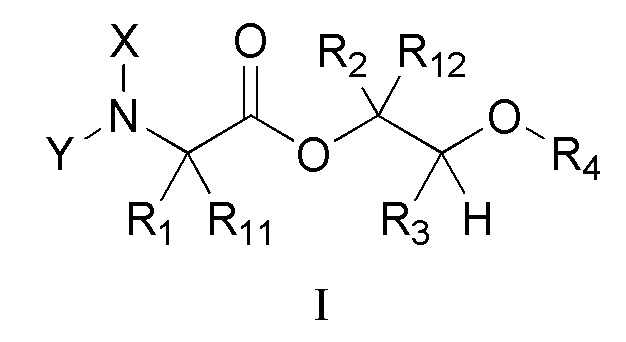
где
X представляет собой водород;
Y представляет собой водород, C(О)R5 или Q;
Q представляет собой
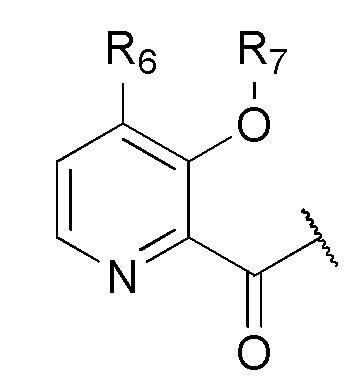 ;
;
R1 и R11 независимо выбраны из водорода или алкила;
R2 и R12 независимо выбраны из водорода, алкила, арила или алкенила, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R8;
R3 представляет собой метил;
R4 выбран из алкила, арила, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R8;
R5 выбран из алкокси, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R8;
R6 выбран из водорода, алкокси, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R8;
R7 выбран из водорода, -C(О)R9 или -CH2OC(О)R9;
R8 выбран из водорода, алкила, арила, галогена, алкенила, алкокси, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R10;
R9 представляет собой алкил;
R10 выбран из водорода, алкила, арила, галогена, алкенила, алкокси, и
фитологически приемлемый материал-носитель,
причем грибковый патоген представляет собой Бурую ржавчину пшеницы (Puccinia triticina), Пятнистость листьев пшеницы (Zymoseptoria tritici), Азиатскую ржавчину сои (Phakopsora pachyrhizi), Альтернариоз томатов (Alternaria solani), Пятнистость листьев сахарной свеклы (Cercospora beticola), Антракноз огуречных растений (Colletotricum lagenarium), Септориоз колоса пшеницы (Leptosphaeria nodorum), Пирикуляриоз риса (Pyricularia oryzae), Ринхоспориоз ячменя (Rhyncosporium secalis), Паршу яблок (Venturia inaequalis). 4 н. и 12 з.п. ф-лы. 7 табл.
1. Композиция для борьбы с грибковым патогеном, содержащая эффективное количество по меньшей мере одного соединения формулы 1
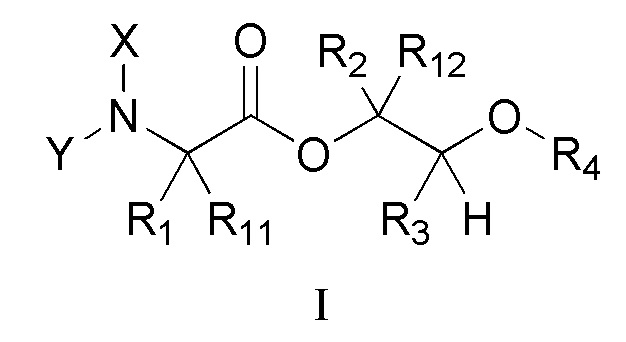
где
X представляет собой водород;
Y представляет собой водород, C(О)R5 или Q;
Q представляет собой
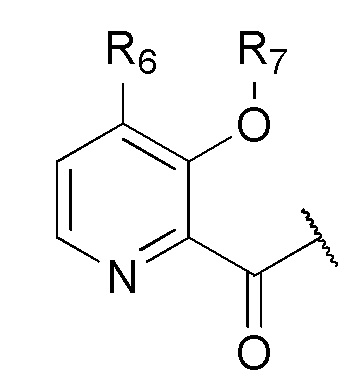 ;
;
R1 и R11 независимо выбраны из водорода или алкила;
R2 и R12 независимо выбраны из водорода, алкила, арила или алкенила, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R8;
R3 представляет собой метил;
R4 выбран из алкила, арила, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R8;
R5 выбран из алкокси, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R8;
R6 выбран из водорода, алкокси, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R8;
R7 выбран из водорода, -C(О)R9 или -CH2OC(О)R9;
R8 выбран из водорода, алкила, арила, галогена, алкенила, алкокси, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R10;
R9 представляет собой алкил;
R10 выбран из водорода, алкила, арила, галогена, алкенила, алкокси, и
фитологически приемлемый материал-носитель,
причем грибковый патоген представляет собой Бурую ржавчину пшеницы (Puccinia triticina), Пятнистость листьев пшеницы (Zymoseptoria tritici), Азиатскую ржавчину сои (Phakopsora pachyrhizi), Альтернариоз томатов (Alternaria solani), Пятнистость листьев сахарной свеклы (Cercospora beticola), Антракноз огуречных растений (Colletotricum lagenarium), Септориоз колоса пшеницы (Leptosphaeria nodorum), Пирикуляриоз риса (Pyricularia oryzae), Ринхоспориоз ячменя (Rhyncosporium secalis), Паршу яблок (Venturia inaequalis).
2. Композиция по п. 1, где X представляет собой водород, и Y представляет собой Q.
3. Композиция по п. 2, где R6 представляет собой алкокси.
4. Композиция по п. 3, где R7 представляет собой водород.
5. Композиция по п. 4, где R2 и R12 независимо выбраны из водорода или алкила, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R8.
6. Композиция по п. 4, где R4 представляет собой арил, необязательно замещенный 0, 1 или несколькими заместителями R8.
7. Композиция по п. 4, где R2 и R12 независимо выбраны из водорода или алкила, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R8, и R4 представляет собой арил, необязательно замещенный 0, 1 или несколькими заместителями R8.
8. Композиция по п. 3, где R7 выбран из -C(О)R9 или -CH2OC(О)R9.
9. Композиция по п. 8, где R2 и R12 независимо выбраны из водорода или алкила, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R8.
10. Композиция по п. 8, где R4 представляет собой арил, необязательно замещенный 0, 1 или несколькими заместителями R8.
11. Композиция по п. 8, где R2 и R12 независимо выбраны из водорода или алкила, каждый из которых необязательно замещен 0, 1 или несколькими заместителями R8, и R4 представляет собой арил, необязательно замещенный 0, 1 или несколькими заместителями R8.
12. Композиция по п. 11, где R9 выбран из -CH3, -CH2OCH2CH3, -CH2CH2OCH3, -CH(CH3)2, -CH2CH2CH2CH3, -циклопропила.
13. Композиция по пп. 1, 7, 11 или 12, причем грибковый патоген представляет собой один из Пятнистости листьев пшеницы (Zymoseptoria tritici), Бурой ржавчины пшеницы (Puccinia triticina), Парши яблок (Venturia inaequalis), Ринхоспориоза ячменя (Rhynchosporium secalis), пирикуляриоза риса (Pyricularia oryzae), Ржавчины сои (Phakopsora pachyrhizi), Пятнистости листьев свеклы (Cercospora beticola), Альтернариоза томатов (Alternaria solani).
14. Композиция для борьбы с грибковым патогеном, содержащая композицию по пп. 7, 11 или 12 и фитологически приемлемый материал-носитель.
15. Композиция для борьбы с грибковым патогеном, содержащая композицию по пп. 7, 11 или 12 и другой пестицид, включая фунгициды, инсектициды, нематоциды, майтициды, артроподициды, бактерициды и их комбинации.
16. Способ борьбы и предотвращения поражения грибами растения, включающий стадию: нанесения фунгицидно эффективного количества по меньшей мере одной из композиций по пп. 7, 11, 12, 13-15 по меньшей мере на одно из растений, область, прилегающую к растению, почву, адаптированную для поддержки роста растения, корень растения и листву растения.
| US 20060040995 A1, 23.02.2006 | |||
| US 20080070985 A1, 20.03.2008 | |||
| СПОСОБ КОНТРОЛЯ QoI РЕЗИСТЕНТНЫХ ПАТОГЕННЫХ ГРИБОВ | 2009 |
|
RU2527029C2 |
Авторы
Даты
2019-10-09—Публикация
2015-12-21—Подача