Изобретение относится к неорганической химии, а более конкретно, к протонопроводящему композитному материалу и способу его получения. Протонопроводящие материалы в виде мембран используются в топливных элементах на основе водорода. К свойствам таких мембран предъявляются следующие требования: высокая ионная проводимость при температуре эксплуатации, низкая газопроницаемость, низкий коэффициент диэлектрических потерь. При этом проводимость является ключевым параметром для материала мембраны, поскольку непосредственно влияет на энергоэффективность топливного элемента.
Перспективными материалами для изготовления мембран являются соединения семейства с общей формулой MmHn(XO4)(m+n)/2⋅yH2O (М=K, Rb, Cs, NH4, XO4=SO4, SeO4, HPO4). Одно из уникальных свойств соединений этого семейства, названных суперпротониками, - аномально высокая протонная проводимость при относительно невысокой температуре. Суперпротонная проводимость связана со структурными особенностями данных соединений и не завит от влажности, реальной структуры (дефектов) или влияния легирующих добавок.
Известен ряд материалов, обладающих суперпротонной проводимостью, например, гидросульфат цезия CsHSO4 [Nardy Т., Friesel М., Melander В.Е. Proton and deuteron conductivity in CsHSO4 and CsDSO4 by in situ isotopic exchange. Solid State Ionics 77 (1995) 105-110].
Однако, как показано в работе [В.А. Коморников и др. «Получение сложных гидросульфатфосфатов рубидия и цезия». Кристаллография, 2016, том 61, №4, с. 645-651] соединение Cs3(HSO4)2(H2PO4) кристаллизуется в ограниченном температурном интервале (до 40°С) в растворе, содержащем избыток дигидросульфата цезия.
В настоящее время в топливных элементах наиболее широко применяются электролитные мембраны на основе перфторсульфоновой кислоты, которые известны как Nafion [Leonard W. Niedrach, Schenectady, N.Y., патент США US 3,134,697]. Однако, мембраны Nafion обладают рядом существенных недостатков, ограничивающих их применение. К таким недостаткам можно отнести сложность получения и сильную зависимость величины протонной проводимости от влажности, что, в свою очередь, ограничивает температурный интервал работы мембран Nafion до 80°С.
Известна композитная протонпроводящая мембрана, содержащая микропористую кремниевую структуру, поры которой заполнены протонпроводящим полимерным материалом на основе Nafion (Заявка. US 20040197613 «Microfuel cells for use particularly in portable electronic devices and telecommunications devices» A1, H01M 8/04, опубл. 07.10.2004). Диаметр каналов пор составляет от 1 до 10 нм. Недостатком предлагаемого технического решения является то, что оптимальным режимом работы мембран является режим, требующий как увлажнения до 80%, так и нагрева до 80°С.
Известно соединение Cs6(H2SO4)3(H2PO4)4, проявляющее суперпротонные свойства и обратимый воспроизводимый суперпротонный фазовый переход при температуре ~115°С. Значение проводимости при температуре 125°С достигает 1 Ом-1 см-1. (Патент РФ №2636713, МПК: С30В 29/14; С30В 28/02; C01D 17/00; B22F 9/04, опубл. 27.11.2017 г.)
Наиболее близким техническим решением к предлагаемому изобретению являются композитные материалы состава Cs3(H2PO4)(HSO4)2/SiO2. (Ponomareva, V.G.; Shutova, Е.S. «Composite electrolytes Cs3(H2PO4)(HSO4)2/SiO2 with high proton conductivity». Solid State Ionics 2005, 176, 2905-2908) Эти материалы на основе Cs3(H2PO4)(HSO4)2 и диоксида кремния проявляют высокие значения проводимости (~10-2 Ом-1 см-1) в широком температурном диапазоне (от 50 до 200°С).
Недостатком композитного материала состава Cs3(H2PO4)(HSO4)2/SiO2, как и любого композитного материала с применением высокодисперсных оксидных фаз, является высокая газопроницаемость при его применении в качестве прессованной мембраны топливного элемента.
Технической задачей изобретения является создание композитного материала, обладающего более высоким значением протонной проводимости и более низким (по сравнению с прототипом) значением газопроницаемости, а также разработка способа его получения. Материал такого состава может быть использован в качестве протонообменной мембраны во многих областях техники (топливные элементы и ячейки, протонные насосы, газоанализаторы, конденсаторы и т.д.).
Техническим результатом изобретения является получение композитного материала xCs4(HSO4)3(H2PO4)-(1-х)AlPO4 для изготовления эффективных мембран для топливных элементов.
Достижение поставленной технической задачи и технического результата достигается тем, что для получения композитного материала по формуле xCs4(HSO4)3(H2PO4-(1-х)AlPO4 вначале получают гидроксид алюминия в процессе щелочного гидролиза раствора алюминий-аммониевых квасцов в избытке водного раствора аммиака по реакции:
NH4Al(SO4)2⋅12H2O+3NH3⋅H2O→Al(ОН)3↓+12H2O+2(NH4)2SO4,
затем отделяют осадок Al(ОН)3⋅nH2O, в котором значение коэффициента n устанавливают путем определения количество воды, теряемой в результате образования метагидроксида AlO(ОН), производят нейтрализацию Al(ОН)3⋅nH2O фосфорной кислотой по реакции:
Al(ОН)3⋅nH2O+Н3РО4→AlPO4+3H2O+nH2O,
упаривают раствор AlPO4+3H2O+nH2O до раствора, имеющего консистенцию густого сиропа. После выполнения перечисленных операций в названном сиропе растворяют размолотый монокристалл Cs4(HSO4)3(H2PO4) при соотношении Cs4(HSO4)3(H2PO4):AlPO4 от 9:1 до 1:1; после чего полученную смесь отливают в формы с последующей сушкой при температуре 60°С в течение 12 часов.
Существо изобретения поясняется схемами и фотографиями приведенными на фигурах.
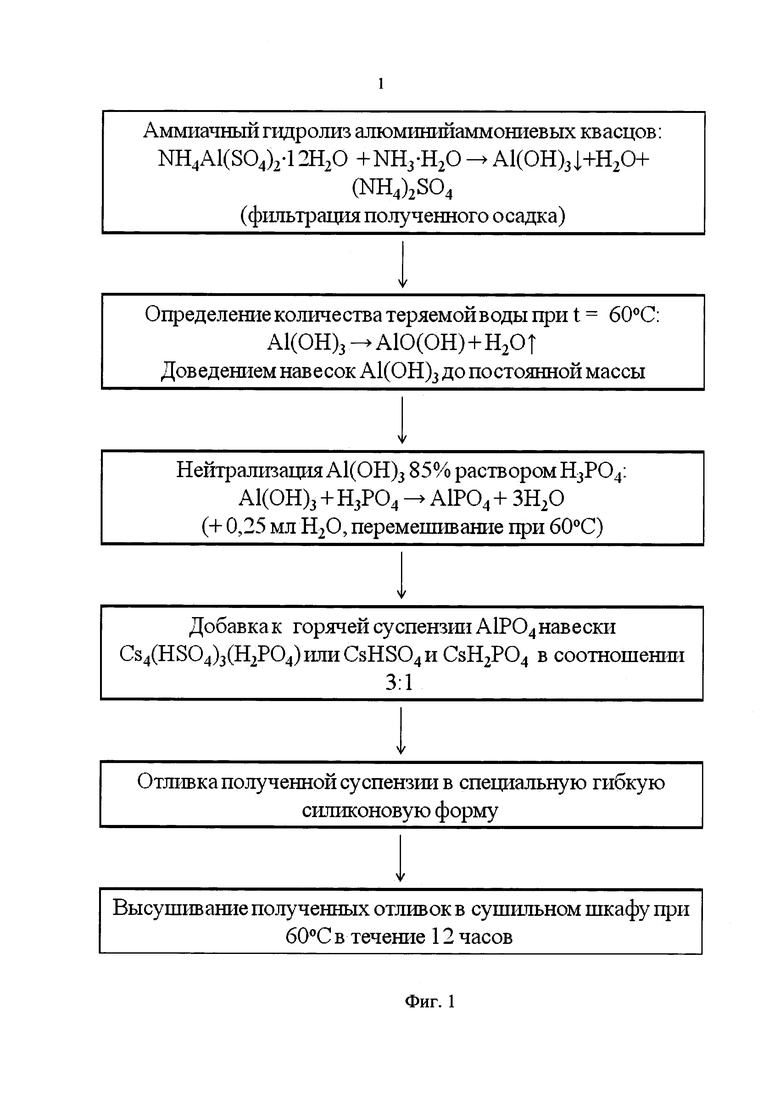
Фиг. 1 Схема технологических операций получения протонпроводящего композитного материала Xs4(Hso4)3(H2po4)-(1-X)Alpo4,
Фиг. 2 - фото образца композитного материала xCs4(HSO4)3(H2PO4)-(1-х)AlPO4 после высушивания в форме.
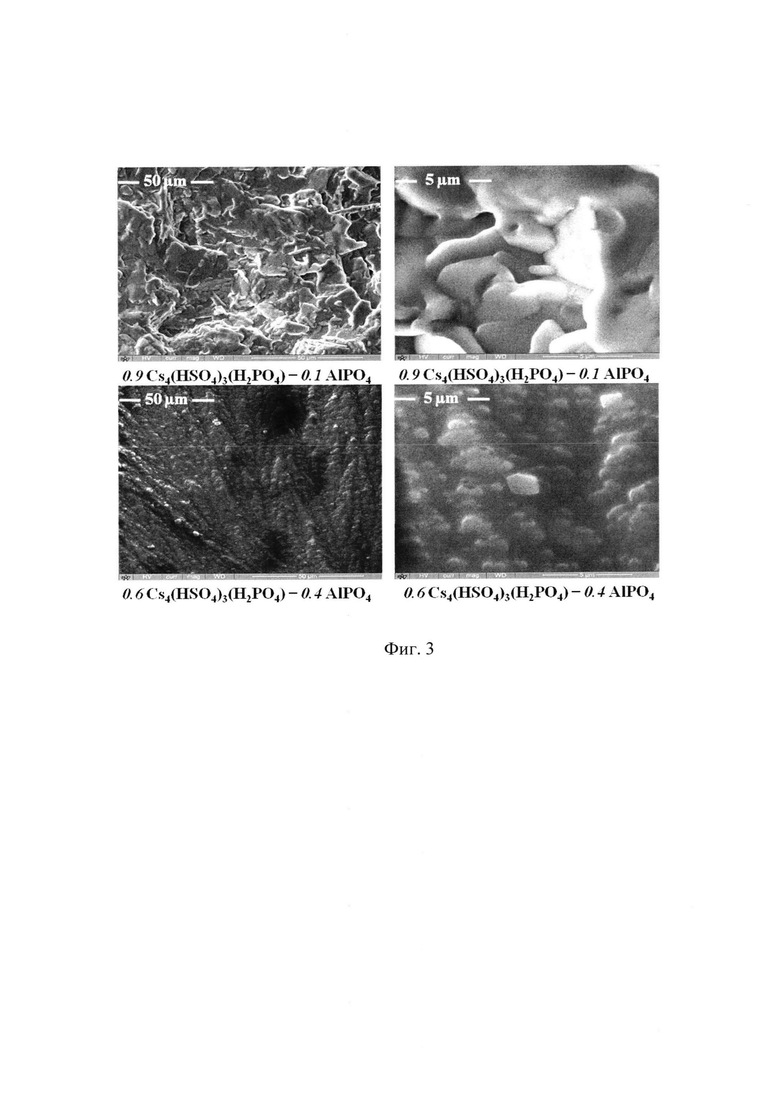
Фиг. 3 - Электронная микроскопия образцов композитного материала 0.9Cs4(HSO4)3(H2PO4)-0.1AlPO4 - верхний ряд; 0.6Cs4(HSO4)3(H2PO4)-0.4AlPO4 - нижний ряд.
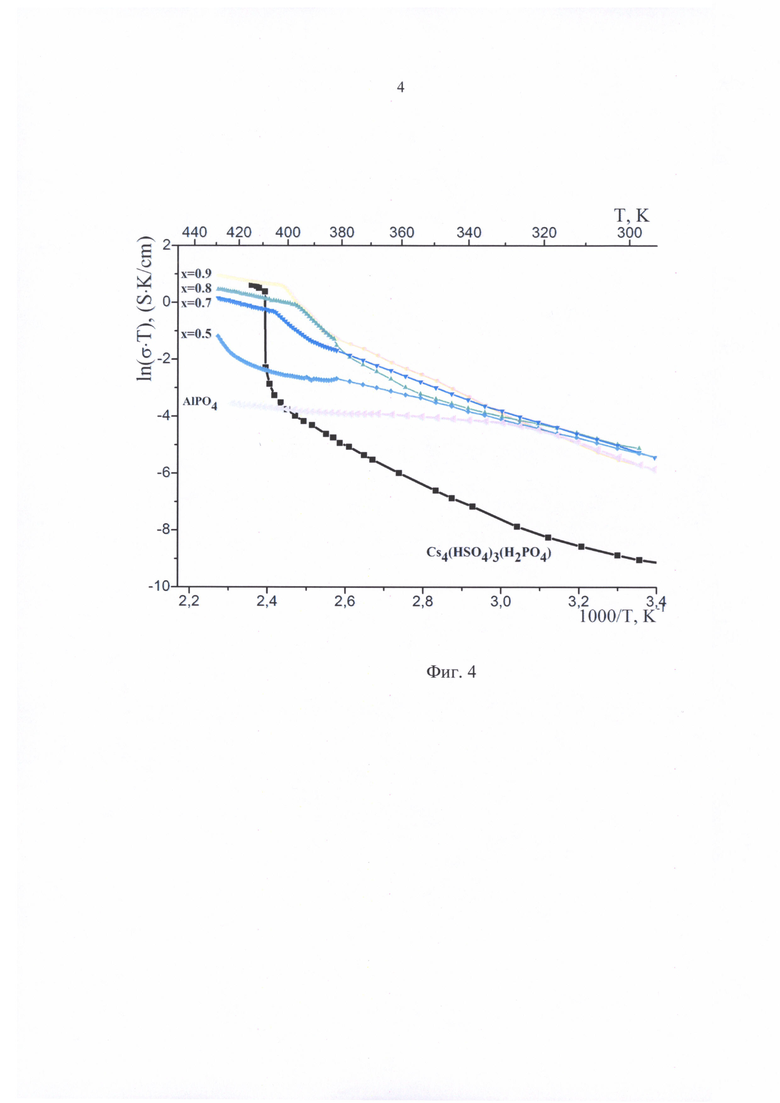
Фиг. 4 Температурная зависимость проводимости исследованных материалов.
Получение заявленного композитного материала осуществляют, начиная с синтеза алюмофосфатного компонента (AlPO4), и проводят в три этапа (Фиг 1). На первом этапе, получают гидроксид алюминия щелочным гидролизом раствора аммонийалюминиевых квасцов NH4Al(SO4)2⋅12H2O с избытком водного раствора аммиака по реакции:
NH4Al(SO4)2⋅12H2O+NH3⋅H2O→Al(ОН)3↓+H2O+(NH4)2SO4
Сразу же после коагуляции, осадок Al(ОН)3⋅nH2O отделяют фильтрованием при помощи колбы Бунзена и воронки Бюхнера на фильтровальной бумаге с использованием компрессора либо водоструйного насоса.
Свежеосажденный Al(ОН)3⋅nH2O от синтеза к синтезу получается всегда с разным содержанием воды в составе (т.е. не являлся весовой формой реактива). Учитывая это необходимо каждый раз устанавливать количество воды, теряемой при образовании оксида, либо метагидроксида алюминия в результате естественного высыхания или нагревания (т.е. значение коэффициента «n»). Для определения количества воды в составе Al(ОН)3⋅nH2O необходимо использовать предварительно доведенные до постоянного веса тигли.
Процедура доведения тиглей до постоянного веса является стандартной аналитической процедурой и осуществляется в несколько последовательных итераций нагревания-взвешивания. Отобранные тигли взвешиваются и помещаются в лабораторную трубчатую печь при температуре сушки/синтеза (в данном случае - 60°С) на 4 часа. Затем тигли вынимаются из печи и сразу помещаются в эксикатор для охлаждения до комнатной температуры (эксикатор необходим для того, чтобы нейтрализовать влияние атмосферной влажности) в течение получаса. После охлаждения тиглей в эксикаторе производится взвешивание тиглей, после чего тигли повторно помещают трубчатую печь на 2 часа. По прошествии 2 часов тигли вновь охлаждают в эксикаторе, взвешивают и возвращают в печь. Тигли считаются доведенными до постоянного веса в том случае, если в трех последовательных итерациях нагревания-взвешивания показания весов совпадают.
Определение количества воды в составе Al(ОН)3⋅nH2O делают следующим образом: в предварительно доведенные до постоянного веса тигли отбирают навески свежеосажденного гидроксида алюминия, затем тигли с навесками (после предварительного взвешивания) доводят также до постоянного веса при температуре синтеза 60°С. После чего проводят контроль фазового состава осушенных навесок методом рентгенофазового анализа. Установлено, что в применяемых условиях (температура синтеза 60°С) полученный гидроксид осушался до метагидроксида алюминия AlO(ОН).
Хороший технический результат достигается в тех случаях, когда свежеосажденный гидроксид алюминия содержит себе не менее 50 масс % воды.
Определив количество воды, теряемой свежеосажденным гидроксидом алюминия, рассчитывают количество фосфорной кислоты, которое необходимо для нейтрализация навески Al(ОН)3⋅nH2O по реакции:
Al(ОН)3⋅nH2O+H3PO4→AlPO4+3H2O+nH2O
После нейтрализации прозрачные растворы фосфата алюминия упаривают до густой сиропообразной консистенции. Далее к полученным вязким растворам добавляют навески размолотого монокристалла Cs4(HSO4)3(H2PO4), ранее осажденного из водного раствора. Полученные смеси отливают в специальные гибкие силиконовые формы, После застывания и высушивания отливки в виде тонких (0,5÷4,5 мм) пластин извлекались из форм для проведения дальнейших исследований (Фиг. 2).
Повышенная проводимость xCs4(HSO4)3(H2PO4)-(1-x)AlPO4 в сравнении с монокристаллом Cs4(HSO4)3(H2PO4) указывает на дополнительный вклад в проводимость алюмофосфатной добавки наряду с проводимостью по межфазной границе. Это позволяет предполагать способность алюмофосфатной добавки участвовать в процессе протонного транспорта наряду с протонпроводящей фазой Cs4(HSO4)3(H2PO4).
Осуществление процесса получения композиционного материала xCs4(HSO4)3(H2PO4)-(1-х)AlPO4 иллюстрируется нижеприводимыми примерами.
Пример 1. Для получения пластин материала xCs4(HSO4)3(H2PO4)-(1-х)AlPO4 размерами 1.5×20×15 мм был использованы Al(ОН)3⋅nH2O, 85% раствор Н3РО4 и Cs4(HSO4)3(H2PO4) в разных массовых соотношениях, в зависимости от необходимого значения параметрах (таблица 1).

Указанные компоненты смешивали в две стадии. Навеску Al(ОН)3⋅nH2O в лабораторном стакане заливали необходимым количеством 85% раствора H3PO4 с добавлением 0,25 мл дистиллированной воды, а затем подогревали и перемешивали. После получения прозрачного густого раствора производили добавку навески Cs4(HSO4)3(H2PO4) и перемешивали до полного растворения. Полученный горячий раствор помещали в гибкую силиконовую форму и переносили в сушильный шкаф на 12 часов при 60°С.
Пример 2. Для получения пластин материала xCs4(HSO4)3(H2PO4)-(1-x)AlPO4 размерами 1.5×20×15 мм были использованы Al(ОН)3⋅nH2O, 85% раствор H3PO4, CsHSO4 и Cs4H2PO4 в разных массовых соотношениях, в зависимости от необходимого значения параметра х (таблица 2).
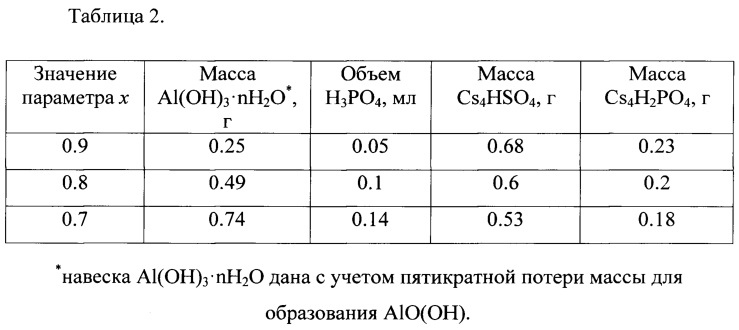
Указанные компоненты смешивали в две стадии. Навеску Al(ОН)3⋅nH2O в лабораторном стакане заливали необходимым количеством 85% раствора H3PO4 с добавлением 0.25 мл дистиллированной воды, подогревали и перемешивали. После получения прозрачного густого раствора производили добавку навесок компонентов CsHSO4 и CsH2PO4, и перемешивали до полного растворения. Полученный горячий раствор помещали в гибкую силиконовую форму и переносили в сушильный шкаф на 12 часов.
Фотографии, представленные на фиг. 2 иллюстрируют образец полученного предлагаемым способом высушенного композитного материала xCs4(HSO4)3(H2PO4)-(1-х)AlPO4, причем 2а- извлечение образца из формы. 2б- размеры образца после извлечения из формы.
Проведенная электронная микроскопия материала 0.9Cs4(HSO4)3(H2PO4)-0.1AlPO4 показала, что состояние материла, обусловлено способом получения и характеризуется высокой степенью дисперсности компонентов материала, высокой однородностью пространственного распределения фаз в материале и низкой пористостью (Фиг. 3). На этой фигуре 0.9Cs4(HSO4)3(H2PO4)-0.1AlPO4 - верхний ряд; 0.6Cs4(HSO4)3(H2PO4)-0.4AlPO4 - нижний ряд.
Высокая протонная проводимость обусловлена свойствами компонентов материала, а именно, собственной объемной протонной проводимостью фосфата алюминия, вклада проводимости по межфазным границам в суммарную протонную проводимость материала и высокой протонной проводимостью компонента Cs4(HSO4)3(H2PO4). Материал xCs4(HSO4)3(H2PO4)-(1-х)AlPO4 проявляет суперпротонные свойства и обратимый суперпротонный фазовый переход при температуре ~135°С. Значение проводимости при температуре 145°С достигает 1 Ом-1см-1 (Фиг 4). Диапазон значений параметра х включает значения 1>х≥0.7; в случае х=1 материал теряет, свои пластичные свойства и низкую газопроницаемость, а в случае х<0.7 протонпроводящие свойства материала значительно снижаются.
Проведенные эксперименты показали промышленную применимость композитного материала xCs4(HSO4)3(H2PO4)-(1-x)AlPO4. полученного предлагаемым способом.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения сложного гидросульфатфосфата цезия состава Cs(HSO)(HPO) | 2016 |
|
RU2636713C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КАТАЛИТИЧЕСКОГО ЭЛЕКТРОДА НА ОСНОВЕ ГЕТЕРОПОЛИСОЕДИНЕНИЙ ДЛЯ ВОДОРОДНЫХ И МЕТАНОЛЬНЫХ ТОПЛИВНЫХ ЭЛЕМЕНТОВ | 2012 |
|
RU2561711C2 |
| ВЫСОКОТЕМПЕРАТУРНАЯ ПРОТОНООБМЕННАЯ МЕМБРАНА, ИСПОЛЬЗУЮЩАЯ ПРОТОННЫЙ ПРОВОДНИК ИОНОМЕР/ТВЕРДОЕ ВЕЩЕСТВО, СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ И СОДЕРЖАЩИЙ ЕЕ ТОПЛИВНЫЙ ЭЛЕМЕНТ | 2003 |
|
RU2313859C2 |
| ПРОТОНПРОВОДЯЩИЕ КОМПОЗИЦИОННЫЕ ПОЛИМЕРНЫЕ МЕМБРАНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2005 |
|
RU2284214C1 |
| ПОЛИМЕРНЫЕ МЕМБРАНЫ ДЛЯ ТОПЛИВНЫХ ЭЛЕМЕНТОВ, ОСНОВАННЫЕ НА СМЕСЯХ АЗОТСОДЕРЖАЩИХ ПОЛИМЕРОВ И НАФИОНА ИЛИ ЕГО АНАЛОГОВ | 2013 |
|
RU2573523C2 |
| КОМПОЗИЦИОННЫЙ МАТЕРИАЛ ДЛЯ НИЗКОТЕМПЕРАТУРНЫХ ТОПЛИВНЫХ ЭЛЕМЕНТОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2016 |
|
RU2612688C1 |
| КОМПОЗИЦИОННЫЙ МАТЕРИАЛ ДЛЯ НИЗКОТЕМПЕРАТУРНЫХ ТОПЛИВНЫХ ЭЛЕМЕНТОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2016 |
|
RU2698475C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ МЕМБРАН-ЭЛЕКТРОДНЫХ БЛОКОВ | 2013 |
|
RU2563029C2 |
| СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННЫХ ПЕРФТОРИРОВАННЫХ СУЛЬФОКАТИОНИТНЫХ МЕМБРАН | 2012 |
|
RU2522566C2 |
| КОМПОЗИТНАЯ ПРОТОНПРОВОДЯЩАЯ МЕМБРАНА И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2007 |
|
RU2373990C2 |

Изобретение может быть использовано при создании протонообменных мембран, применяемых в топливных элементах на основе водорода. Композитный протонопроводящий материал имеет состав xCs4(HSO4)3(H2PO4)-(1-х)AlPO4, где х=0,5-0,9. Способ получения композитного материала включает получение гидроксида алюминия в процессе щелочного гидролиза раствора алюминий-аммониевых квасцов в избытке водного раствора аммиака. Отделяют осадок Al(ОН)3⋅nH2O, в котором значение коэффициента n устанавливают путем определения количества воды, теряемой в результате образования метагидроксида АlO(ОН) при осушении навесок свежеосажденного гидроксида алюминия. Проводят нейтрализацию Аl(ОН)3⋅nН2O фосфорной кислотой. Упаривают полученный раствор до консистенции густого сиропа и растворяют в нем размолотый кристалл Cs4(HSO4)3(H2PO4) при соотношении Cs4(HSO4)3(H2PO4):AlPO4 в интервале от 9:1 до 1:1. Полученную смесь отливают в формы с последующей сушкой при температуре 60°С в течение 12 ч. Изобретение позволяет получить материал, обладающий высокой протонной проводимостью и низкой газопроницаемостью. 2 н.п. ф-лы, 4 ил., 2 табл., 2 пр.
1. Композитный протонопроводящий материал состава xCs4(HSO4)3(H2PO4)-(1-х)AlPO4,
где х=0,5-0,9.
2. Способ получения композитного материала по п. 1, включающий получение гидроксида алюминия в процессе щелочного гидролиза раствора алюминий-аммониевых квасцов в избытке водного раствора аммиака по реакции:
NH4Al(SO4)2⋅12H2O+3NH3⋅H2O→Al(ОН)3↓+12H2O+2(NH4)2SO4,
отделение осадка Al(ОН)3⋅nH2O, в котором значение коэффициента n устанавливают путем определения количества воды, теряемой в результате образования метагидроксида Al(ОН), нейтрализацию Al(ОН)3⋅nH2O фосфорной кислотой по реакции:
Al(ОН)3⋅nH2O+H3PO4→AlPO4+3H2O+nH2O,
упаривание раствора AlPO4+3H2O+nH2O до раствора, имеющего консистенцию густого сиропа, растворение в названном растворе размолотого монокристалла Cs4(HSO4)3(H2PO4) при соотношении Cs4(HSO4)3(H2PO4):AlPO4, лежащем в интервале от 9:1 до 1:1; отливку полученной смеси в формы с последующей сушкой при температуре 60°С в течение 12 часов.
| PONOMAREVA V.G., SHUTOVA Е.S | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Приспособление для удаления таянием снега с железнодорожных путей | 1920 |
|
SU176A1 |
| Станок для откачивания воздуха и иных газов из электрических ламп накаливания | 1923 |
|
SU2905A1 |
| Способ получения сложного гидросульфатфосфата цезия состава Cs(HSO)(HPO) | 2016 |
|
RU2636713C1 |
| RU 2481427 C1, 10.05.2013 | |||
| KR 20080012791 A, 12.02.2008. | |||
Авторы
Даты
2019-10-15—Публикация
2018-10-16—Подача