Настоящее изобретение относится к области биомедицины, в частности молекулярной и клинической онкологии и молекулярной биологии, и касается системы маркеров для диагностики рака яичников путем оценки статуса метилирования генов микроРНК (miR-124a-3, miR-129-2, miR-193a и miR-107, система №1), а также системы маркеров для прогнозирования метастазирования (miR-137, miR-193a, miR-1258, miR-203 и miR-127, система №2).
Выявление метилирования, по крайней мере, одного гена из заявленной системы маркеров №1 в предположительно пораженной раком ткани человека, по сравнению со здоровой тканью яичников служит диагностическим признаком рака яичников. Для прогноза метастазирования требуется выявление метилирования, по крайней мере, 3-х генов из заявленной системы маркеров №2 в пораженной раком ткани человека. Заявленная система маркеров на основе генов микроРНК, система №1, позволяет с высокой чувствительность и специфичностью диагностировать рак яичников. Заявленная система маркеров №2 позволяет с высокой чувствительность и специфичностью прогнозировать наличие метастазов в лимфатических узлах и/или других тканях пациентки.
Рак яичников - наиболее летальный среди онкогинекологических злокачественных опухолей женщин [1, 2]. Более 70% случаев рака яичников выявляют на поздних стадиях, и уровень 5-летней выживаемости в среднем составляет 30%. При выявлении опухолей яичников на I-II клинических стадиях уровень 5-летней выживаемости достигает 70-90% [1, 2]. Однако на ранних стадиях этот вид рака выявляются только в 20% случаев. Главная причина этих проблем - отсутствие методов ранней диагностики. Кроме того, рак яичников отличает высокий метастатический и инвазивный потенциал, причем, метастазирование повышает множественную лекарственную устойчивость и резко снижает выживаемость пациенток. Эпигенетические маркеры, включая метилирование онко-супрессорных генов и профили экспрессии и метилирования микроРНК перспективны в диагностике и прогнозе течения рака, в частности рака яичников [3, 4]. Изменение уровня экспрессии некоторых генов, кодирующих белки или микроРНК, и метилирование CpG-островков промоторной области таких генов могут служить признаком наличия злокачественной опухоли или предсказания о возникновении рака, а также о возможном метастазировании, которое резко усугубляет заболевание.
Отбор генов микроРНК, связанных с развитием опухолей и ассоциированных с CpG-островками, проводили с привлечением алгоритмов, содержащихся в базе данных miR Walk 2.0 (http://zmf.umm.uni-heidelberg.de/apps/zmf/mirwalk2/index.html), и CpGcluster (http://bioinfo2.ugr.es/CpGcluster/).
Оценка статуса метилирования генов: miR-124a-3, miR-129-2, miR-193a и miR-107 в 54 образцах рака яичников и в 18 образцах яичников от пост-мортальных женщин без онкопатологии в анамнезе позволила на их основе составить систему маркеров (система №1) для диагностики этого заболевания. Оценка статуса метилирования генов: miR-137, miR-193a, miR-1258, miR-203 и miR-127, в группе из 17 образцов метастазирующего и 37 образцов неметастазирующего рака яичников позволила составить систему маркеров (система №2) для прогнозирования метастазирования. Сведений о выявлении метилирования 7 генов, вошедших в системы №1 и №2, а именно, miR-124a-3, miR-193a, miR-107, miR-137, miR-1258, miR-203 и miR-127, - при раке яичников в источниках информации не обнаружено. Гиперметилирование miR-129-2 при раке молочной железы и яичников изучено ранее на меньшей выборке образцов и приведено в нашей статье [5].
Ранее в патенте США (U.S. Pat. No. 7,507,536 (2009)) был предложен набор генов (TM4SF11, TNFRSF10B, RUNX3, ACTN1, FANCG) для диагностики и прогноза рака яичников [6]. Выявление метилирования хотя бы в одном маркере этой группы генов рассматривается как идентификация раковой клетки или выявление предрасположенности к возникновению рака яичников. Значения клинической чувствительности и специфичности для данной системы не приведены.
В качестве ближайшего аналога рассмотрим патент США (U.S. Pat. No. 9,410,956 (2016)) [7]. В этом патенте описаны маркеры для идентификации рака яичников и предсказания клинической картины заболевания, основанные на анализе изменений экспрессии группы генов микроРНК. Аберрантная экспрессия 4 микроРНК (miR-214, -199а*, -200а и -100) была детектирована прибл. в половине или более случаев рака яичников, преимущественно на поздних стадиях и при высокой степени анаплазии. Значения клинической чувствительности и специфичности для данной системы не приведены.
Задача заявляемой группы изобретений - расширить арсенал маркеров на основе генов микроРНК для диагностики рака яичников и предсказания наличия метастазирования.
Задача решена путем:
- разработки системы маркеров №1 на основе группы 4 генов микроРНК: miR-124-3, miR-129-2, miR-193a и miR-107 - для диагностики рака яичников, путем выявления метилирования, по крайней мере, у одного гена из этой группы.
- разработки системы маркеров №2 на основе группы из 5 генов микроРНК: miR-137, miR-193а, miR-1258, miR-203 и miR-127 - для прогнозирования метастазирования рака яичников, путем выявления метилирования у каких-либо трех генов из этой группы.
Диагностику рака яичников и прогноз метастазирования осуществляют по методу:
Берут образцы ткани яичников у лиц, обследуемых для выявления онкологического заболевания или с установленным диагнозом. Выделение и очистку ДНК из образцов ткани яичников проводят методом фенол-хлороформенной экстракции. Качество и точную концентрацию ДНК определяют спектрофотометрически по соотношению оптической плотности при длинах волн 260 и 280 нм. Далее проводят бисульфитную конверсию ДНК с последующей метилспецифичной ПЦР (МС-ПЦР) [5]. Для анализа метилирования каждой микроРНК методом МС-ПЦР используют две пары праймеров, специфичных как к метилированному, так и к неметилированному аллелю (Таблица 1). Продукты МС-ПЦР, представляющие собой фрагменты ДНК, разделяют электрофорезом в 2% агарозном геле, либо в 10% полиакриламидном геле (при длине продукта ПЦР менее 160 н.п.). Далее анализируют на наличие или отсутствие продуктов МС-ПЦР для праймеров, специфичных к метилированному и неметилированному аллелю. В качестве контролей для неметилированных аллелей используют коммерческий препарат ДНК #G1471 (Promega, США). В качестве позитивного контроля 100%-ого метилирования используют коммерческий препарат ДНК #SD1131 (Thermo Scientific, США) Соответствие фрагментов МС-ПЦР исследуемым генам проверяют прямым секвенированием обеих цепей продуктов МС-ПЦР. Диагностику рака яичников осуществляют по наличию метилирования, по крайней мере, у одного маркера системы №1. Прогноз метастазирования рака яичников осуществляют по наличию метилирования, по крайней мере, у трех маркеров системы №2.
Пример 1. Анализ метилирования генов микроРНК, используемых в заявляемой системе №1 для диагностики рака яичников и в заявляемой системе №2 для прогноза рака яичников, в образцах опухолей и онкологически здоровых тканях яичников.
Для диагностики отобраны 4 гена (система №1), для прогноза метастазирования - 5 генов (система №2), в сумме отобраны 8 маркеров. Для 8 исследуемых генов микроРНК метил-специфичную ПЦР (МС-ПЦР) проводили в 20 мкл реакционной смеси, содержащей 67 мМ Трис-HCl, рН 8.8, 16,7 мМ (NH4)2SO4, 0.01% Tween-20; 1,5 мМ MgCl2, 0.25 мМ каждого dNTP; 10-20 нг ДНК; 25 пмолей каждого праймера; 0,5 ед. Hot Start Taq ДНК полимеразы («СибЭнзим», Новосибирск). Амплификацию проводили по программе: 95°С, 5 мин; 35 циклов {95°С, 10 с; Тотж (см. Табл. 1), 20 с; 72°С, 30 с}; 72°С, 3 мин. ПЦР проводили на амплификаторе DNA Engine Dyad Cycler фирмы Bio-Rad (США). Праймеры, температура отжига и размер продуктов МС-ПЦР приведены в Таблице 1.
Для 54 пациентов с морфологически установленным диагнозом - эпителиальные опухоли яичников и 18 доноров, онкологически здоровых в анамнезе, проведен анализ метилирования заявляемой системы маркеров №1. Данные по клинико-гистологической характеристики образцов рака яичников и по метилированию маркеров: miR-124a-3, miR-129-2, miR-193a и miR-107 (система №1) и miR-137, miR-193a, miR-1258, miR-203 и miR-127 (система №2) приведены в качестве примера для 14 образцов опухолей (Таблица 2). Данные по метилированию 4 маркеров заявляемой системы 1 для диагностики рака яичников приведены для 18 доноров в Таблице 3. Сопоставление данных по метилированию маркеров системы №1 в образцах опухолей и доноров позволило показать применимость этой системы для диагностики рака яичников с высокой чувствительностью и специфичностью (см. пример 2).
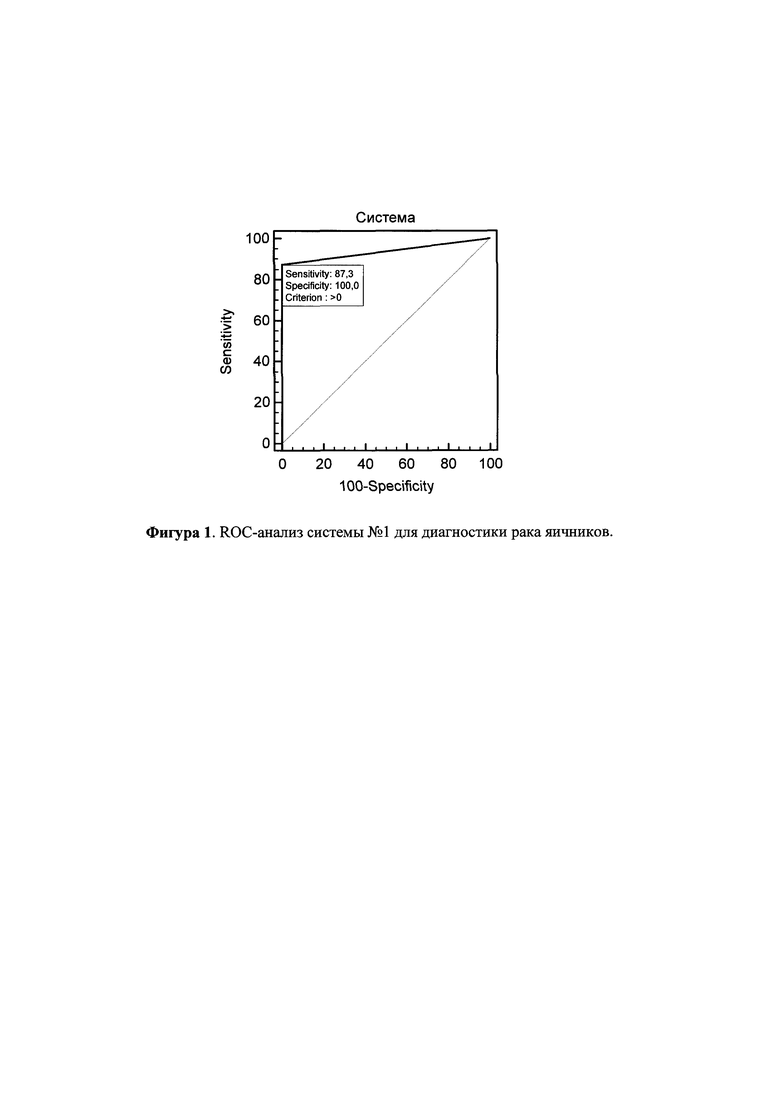
Пример 2. Оценка чувствительности и специфичности заявляемой системы маркеров №1 (miR-124a-3, miR-129-2, miR-193a и miR-107) для диагностики рака яичников.
Важным свойством заявляемой системы маркеров №1 является высокая клиническая чувствительность и специфичность при диагностике рака яичников. Так как метилирование 4 маркеров системы №1 не выявлено ни в одном из 18 исследованных образцов доноров (таблица 3), можно утверждать о возможности использовать заявляемую систему маркеров №1 для диагностики рака яичников со 100%-специфичностью. Наличие метилирования, по крайней мере, у одного маркера системы №1 выявлено у 47 из 54 пациенток с раком яичников (87% случаев). В соответствии с этими данными, клиническая чувствительность и специфичность заявляемой системы маркеров №1 (для диагностики рака яичников), рассчитанная методом ROC-анализа, составляют 87% и 100%, соответственно, AUC - 0,936. Таким образом, заявляемая система маркеров позволяет диагностировать рак яичников у пациенток истинно больных данным онкологическим заболеванием с высокой (в 87% случаев) клинической чувствительностью и строго специфично. Анализ системы №1 (для диагностики рака яичников) методом ROC-анализа показан на Фигуре 1. Согласно параметрам, оценивающим систему, достаточно выявления метилирования хотя бы одного из 4 маркеров данной системы для диагностирования злокачественных опухолей яичников у пациентки.
Пример 3. Оценка чувствительности и специфичности заявляемой системы маркеров №2 (miR-137, miR-193a, miR-1258, miR-203 и miR-127) для предсказания метастазирования рака яичников.
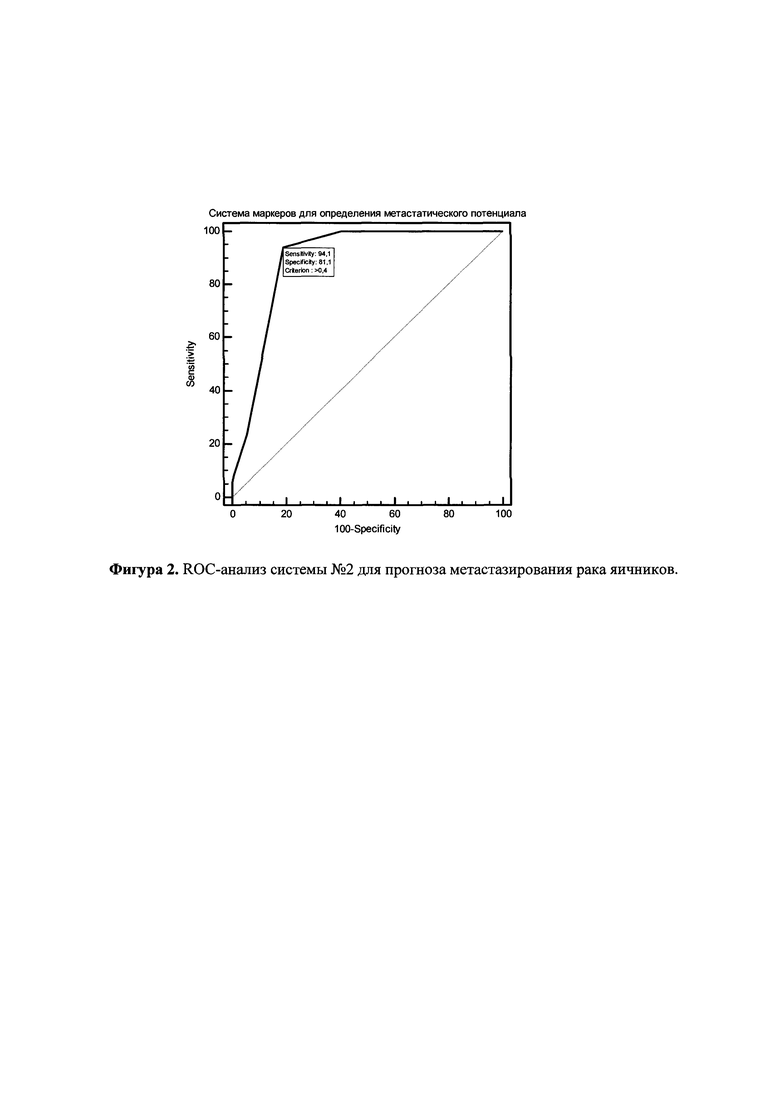
В соответствии с данными по клинико-гистологической характеристике 54 образца рака яичников разбили на две группы: без метастазирования - 37 образцов, с выявленным метастазированием в региональных лимфатических узлах или удаленных органах - 17 образцов. В табл. 2 в качестве примеров приведены данные по метилированию для 7 образцов без метастазирования и 7 образцов с метастазированием. Система маркеров №2 (miR-137, miR-193a, miR-1258, miR-203 и miR-127) позволяет различить уровень метилирования в этих двух группах и прогнозировать метастазирование у пациентки с высокой клинической чувствительностью 94% и специфичностью 81%, AUC - 0,892. Надежность системы определена методом ROC-анализа (Фигура 2). Согласно характеристикам данной системы, для предсказания метастазирования необходимо установление метилирования 3 из 5 маркеров (miR-137, miR-193a, miR-1258, miR-203 и miR-127) данной системы.
Заявляемые системы маркеров для диагностики рака яичников (система №1) и для прогноза метастазирования рака яичников (система №2) характеризуются тем, что
1. Система №1 позволяет диагностировать рак яичников с высокой клинической чувствительностью 87% и 100%-специфичностью; в источниках информации не обнаружено аналогичных систем с охарактеризованной чувствительностью и специфичностью.
2. Система №2 позволяет прогнозировать наличие или развитие метастазов у пациентов с раком яичников с высокой клинической чувствительностью 94% и специфичностью 81%; в источниках информации не обнаружено аналогичных систем с охарактеризованной чувствительностью и специфичностью.
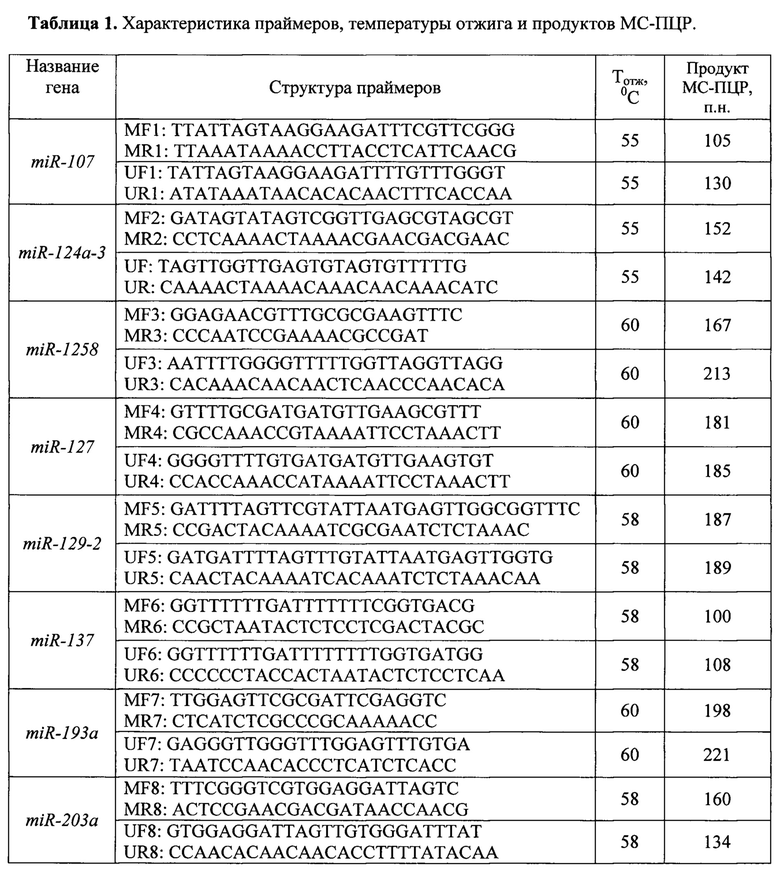
Примечания:
Праймеры подобраны авторами с использованием известных программ (Methyl Primer Express v. 1.0, Vector NTI v. 10.0 и т.п.).
Условия МС-ПЦР (Тотж) подобраны экспериментально.
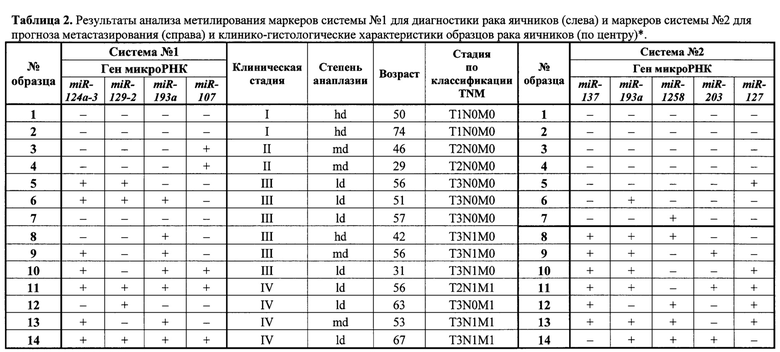
* Примечание. Исследованы 54 образца от 54 женщин больных раком яичников; в табл. 2 в качестве примера приведены данные для 14 образцов (группа без метастазов - 7 образцов, группа с метастазами - 7 образцов).
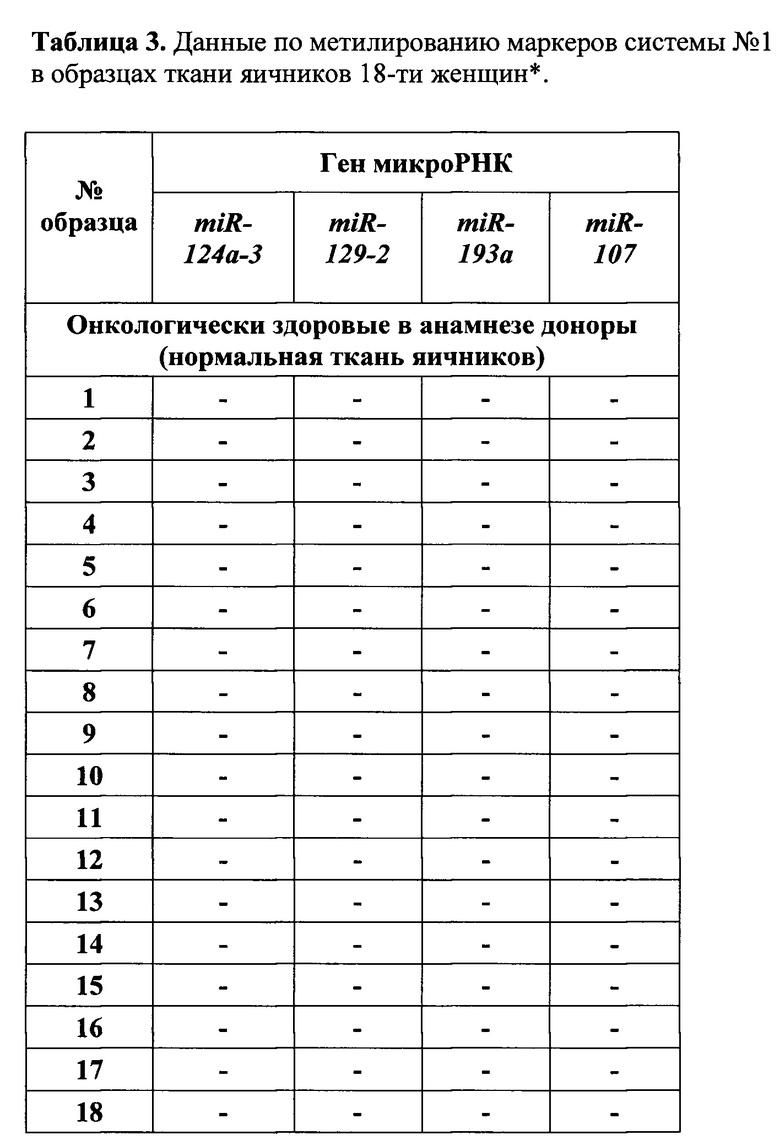
* Пост-мортальные лица, онкологически здоровые по данным анамнеза.
Цитированные источники научно-технической информации:
1. Engelberth, S.A., Hempel, N., and Bergkvist, M. (2014) Development of nanoscale approaches for ovarian cancer therapeutics and diagnostics, Crit. Rev. Oncog., 19, 281-315.
2. Coward, J.I., Middleton, K. and Murphy, F. (2015) New perspectives on targeted therapy in ovarian cancer, Int. J. Womens Health, 7, 189-203.
3. Kinose, Y., Sawada, K., Nakamura, K., and Kimura, T. (2014) The role of microRNAs in ovarian cancer, Biomed. Res. Int., 2014: 249393.
4. Dong, A., Lu, Y., Lu, B. (2016) Genomic/Epigenomic Alterations in ovarian carcinoma: translational insight into clinical practice, J Cancer. 7, 1441-1451.
5. Pronina I.V., Loginov V.I., Burdennyy A.M., Fridman M.V., Kazubskaya T.P., Dmitriev A.A., Braga E.A. (2016) Expression and DNA methylation alterations of seven cancer-associated 3p genes and their predicted regulator miRNAs (miR-129-2, miR-9-1) in breast and ovarian cancers. Gene. 576 (1 Pt 3): 483-491.
6. U.S. Pat. No. 7,507,536 (2009) Van Criekinge et al. Methylation markers for diagnosis and treatment of ovarian cancer.
7. U.S. Pat. No. 9,410,956 (2016) Cheng; Jin Q. Micro-RNA profiling in ovarian cancer.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ для прогнозирования метастазирования рака яичников на основе группы генов микроРНК | 2016 |
|
RU2666911C2 |
| Способ диагностики светлоклеточного почечно-клеточного рака и способ прогнозирования метастазирования на основе группы генов микроРНК | 2017 |
|
RU2683251C1 |
| Способ прогноза метастазирования рака яичников на основе набора генов длинных некодирующих РНК | 2023 |
|
RU2825782C1 |
| Способ для диагностирования рака яичников на основе набора генов длинных некодирующих РНК | 2021 |
|
RU2779550C1 |
| СИСТЕМА МАРКЕРОВ НА ОСНОВЕ ГРУППЫ ГЕНОВ МИКРОРНК ДЛЯ ДИАГНОСТИКИ НЕМЕЛКОКЛЕТОЧНОГО РАКА ЛЕГКОГО, ВКЛЮЧАЯ ПЛОСКОКЛЕТОЧНЫЙ РАК И АДЕНОКАРЦИНОМУ | 2012 |
|
RU2507268C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РЕЦИДИВИРОВАНИЯ СЕРОЗНОЙ КАРЦИНОМЫ ЯИЧНИКОВ | 2020 |
|
RU2749361C1 |
| Способ дифференциальной диагностики рака яичников, кистозных образований яичника и рака тела матки | 2024 |
|
RU2836527C1 |
| Способ для прогноза метастазирования рака молочной железы на основе набора генов длинных некодирующих РНК | 2022 |
|
RU2807480C1 |
| СПОСОБ ПРОГНОЗА МЕТАСТАЗИРОВАНИЯ ОПУХОЛЕЙ РАКА ЖЕЛУДКА | 2021 |
|
RU2806432C2 |
| Способ для диагностирования рака молочной железы на основе набора генов длинных некодирующих РНК | 2022 |
|
RU2795976C1 |
Изобретение относится к биотехнологии, в частности молекулярной биологии и онкологии. Описан способ для диагностики рака яичников на основе группы генов микроРНК путем выявления метилирования по крайней мере одного маркера из четырех, отличающийся тем, что маркерами системы являются гены: miR-124a-3, miR-129-2, miR-193a и miR-107. Заявляемый способ позволяет выявить рак яичников с высокой клинической чувствительностью и специфичностью. 2 ил., 3 табл., 1 пр.
Способ для диагностики рака яичников на основе группы генов микроРНК путем выявления метилирования по крайней мере одного маркера из четырех, отличающийся тем, что маркерами системы являются гены: miR-124a-3, miR-129-2, miR-193a и miR-107.
| WO 2011095623 A2, 11.08.2011 | |||
| WO 2011127219 A1, 13.10.2011 | |||
| Иващенко А.Т., Берилло О.А., Участие микро-РНК в онкогенезе, Вестник казахского национального медицинского университета, 2010 г., с | |||
| ПАРОПЕРЕГРЕВАТЕЛЬ ДЛЯ ЛОКОМОБИЛЬНЫХ КОТЛОВ | 1912 |
|
SU277A1 |
| WO 2011027019 A3, 28.04.2011. | |||
Авторы
Даты
2019-10-16—Публикация
2018-11-02—Подача