Изобретение относится к медицине, а именно фармакологии, урологии и может быть использовано для фармакологической коррекции оксалатного нефролитиаза.
По современным данным, эпидемиология МКБ сопоставима с таковой для сахарного диабета - каждый 11-ый житель развитых стран страдает нефролитиазом, а затраты на комплекс лечебных, профилактических и реабилитационных мероприятий только в США ежегодно превышает 10 млрд. долларов. При этом, несмотря на достижения современной урологии, основным методом литолиза почечных камней остается литотрипсия в различных ее вариантах, которая является весьма травматичным методом и сопровождается рядом серьезных побочных эффектов. На этом фоне фармакологическое сопровождение терапии МКБ в основном носит вспомогательный характер. Средств, обладающих специфической активностью при нефролитиазе, практически не существует.
Одним из наиболее современных подходов к разработке новых эффективных антилитогенных средств является так называемый протеомный подход, согласно которому мишенью для фармакологического литолиза уролита или профилактики его формирования является органическая матрица почечных камней. Учитывая белковую природу основных структурных и функциональных элементов матрицы, считается, что внешним лигандом, обладающим аффинитетом к данному типу «субстрата» (или процессам, определяющим его формирование), могут являться особые протеиновые и аминокислотные молекулы. На поиске таких молекул основана разработка новых антилитогенных средств.
Наиболее близким по достигаемому результату прототипом является пептидное средство, обладающее антилитогенным действием, получаемое путем уксуснокислой экстракции из свиных почек (патент РФ 2652339). Его вводят внутрь в дозе 15 мг. Способ обеспечивает антилитогенный эффект, выражающийся в 100%-ном разрушении крупных и средних камней в почках на фоне оксалатного нефролитиаза.
Недостатками названного средства являются невозможность точно установить биологически активные вещества, входящих в его состав и определяющих его лечебный эффект при мочекаменной болезни, а также наличие в составе средства значительного количества сопутствующих веществ.
Авторы предлагают новый способ протеомной коррекции оксалатного нефролитиаза, отличающийся высокой лечебной эффективностью.
Техническим результатом заявляемого изобретения является расширение ассортимента способов фармакологической коррекции окслатного нефролитиаза.
Технический результат достигается тем, что для протеомной коррекции окслатного нефролитиаза используется тетрапептид Leu-Ile-Lys-His (лейцин - изолейцин - лизин - гистидин).
Эффективность способа протеомной коррекции оксалатного нефролитиаза найдена экспериментальным путем.
Эксперименты по изучению эффективности способа протеомной коррекции оксалатного нефролитиаза были проведены на 20 самцах крыс Wistar средней массой 150 г), разделенных поровну на 2 группы: контрольная (моделирование оксалатного нефролитиаза) и подопытная (моделирование оксалатного нефролитиаза + введение тетрапептида Leu-Ile-Lys-His (лейцин - изолейцин - лизин - гистидин).
На протяжении эксперимента животные находились в индивидуальных клетках, приспособленных для сбора мочи, в условиях стандартного лабораторного рациона. По условиям эксперимента крысы были разбиты на 2 группы по 15 животных в каждой. В первой (контрольная группа) с целью моделирования оксалатного нефролитаза на протяжении 6 недель крысам предоставлялся в качестве питья в свободном доступе 1%-ный раствор этиленгликоля. Во второй (подопытная группа) крысы также 6 недель получали в свободном доступе 1%-ный раствор этиленгликоля, но при этом, начиная с 4-й недели, вплоть до конца эксперимента им ежедневно вводилось внутрь тетрапептид Leu-Ile-Lys-His в дозе 2,8 мг.
Еженедельно в течение эксперимента в каждой группе крыс производился сбор суточного объема мочи, в которой для оценки степени повреждения почечных тканей при моделировании оксалатного нефролитиаза на автоматическом биохимическом анализаторе DIRUI CS-T240 определялись концентрация белка, креатинина и активность маркерных ферментов повреждения нефротелия - лактатдегидрогеназы (ЛДГ) и γ-глютамилтрансферазы (ГГТ). С учетом суточного объема диуреза рассчитывалась экскреция белка и креатинина.
Для определения концентрации белка использовали биуретовый метод, который основан на образовании комплекса сине-фиолетового цвета с ионами меди, оптическая плотность которого прямо пропорциональна концентрации белка. Концентрация креатинина определялась кинетическим методом без депротеинизации, основанным на реакции Яффе образования красно-оранжевого окрашенного комплекса. Принцип метода определения активности ЛДГ основан на реакции восстановления пирувата до молочной кислоты, скорость реакции пропорциональна активности ЛДГ в пробе. В основе определения активности ГГТ лежит реакция переноса L-γ-глутамил-3-карбокси-п-нитроанилида на глицилглицин, которая катализируется данным ферментом с образованием окрашенного 5-амино-2-нитробензоат.
По истечении 6 недель эксперимента крыс подвергали эвтаназии под эфирным наркозом и извлекали обе почки, одна из которых использовалась для определения активности в почечной ткани процесса свободнорадикального окисления, а другая - для проведения морфологических исследований.
Активность процесса свободнорадикального окисления в почечной ткани оценивали по совокупности прооксидантных и антиоксидантных показателей. К первым были отнесены содержание тиобарбитуратреактивных продуктов (ТБРП) и общая прооксидантная активность (ОПА), а ко вторым - общая антиоксидантная активность (ОАА) и активность антиоксидантных ферментов: глутатионпероксидазы (ГПО), супероксиддисмутазы (СОД) и каталазы (КАТ).
Тиобарбитуратреактивные продукты (ТБРП) определяли колориметрическим методом, измеряя интенсивность окраски раствора в ходе химической реакции ТБРП с тиобарбитуровой кислотой. Общую прооксидантную активность (ОПА) оценивали по накоплению продуктов перекисного окисления ТВИН-80, реагирующих с тиобарбитуровой кислотой.
Общая антиоксидантная активность (ОАА) оценивалась как интегративный показатель активности всех ферментных и неферментных факторов нейтрализации свободных радикалов по степени угнетения Fe2+/аскорбатзависимого окисления ТВИН-80 гомогенетом ткани. Для определения активности глутатионпероксидазы (ГПО) измеряли концентрацию восстановленного глутатиона в цветной реакции с реактивом Эллмана. Активность супероксиддисмутазы (СОД) определялась по подавлению образования нитроформазана - окрашенного продукта окисления нитротетразолия супероксидными радикалами, образующимися при взаимодействии феназинметасульфата и никотинамдидинуклеотида (НАДН). Активность каталазы (КАТ) оценивали по подавлению ферментом окисления молибдата натрия пероксидом водорода.
Для проведения морфологических исследований почки фиксировались в 10%-ном растворе формалина, обрабатывались по стандартной методике, и изготавливался поперечный срез толщиной 6 мкм через почечный сосочек. Полученные срезы окрашивались гематоксилином и эозином, метенамин-серебром. Кальциевые депозиты идентифицировались гистохимическим методом Косса и при помощи компьютерной программы на снимках подсчитывалось количество кальциевых депозитов в поле зрения и определялся их размер. Морфометрические исследования проводили с использованием программных пакетов ImageJ 1.43 и AxioVision 3.1.
Статистическая обработка результатов проводилась с использованием компьютерной программы Statistica 12.0. Результаты биохимических исследований представлены медианой (М) и интерквартильным размахом (25%, 75%). Результаты морфометрических исследований представлены средним (М) и стандартной ошибкой среднего (m). Статистические сравнения между группами проводились с использованием непараметрических критериев Краскела-Уолесса и U-критерия Манна-Уитни, сравнения внутри группы относительно исходного уровня проводились с использованием непараметрического критерия Вилкоксона. Результаты признавались достоверными при значении показателя достоверности р<0,05.
Способ продемонстрирован фигурами:
Фигура 1 - по горизонтальной оси - название показателя и единицы измерения. По вертикальной оси - значение показателя. Значения представлены в виде медианы и минимума-максимума без учета выбросов (non-outlier range);
Фигура 2 - по горизонтальной оси - название показателя и единицы измерения. По вертикальной оси - значение показателя. Значения представлены в виде медианы и минимума-максимума без учета выбросов (non-outlier range);
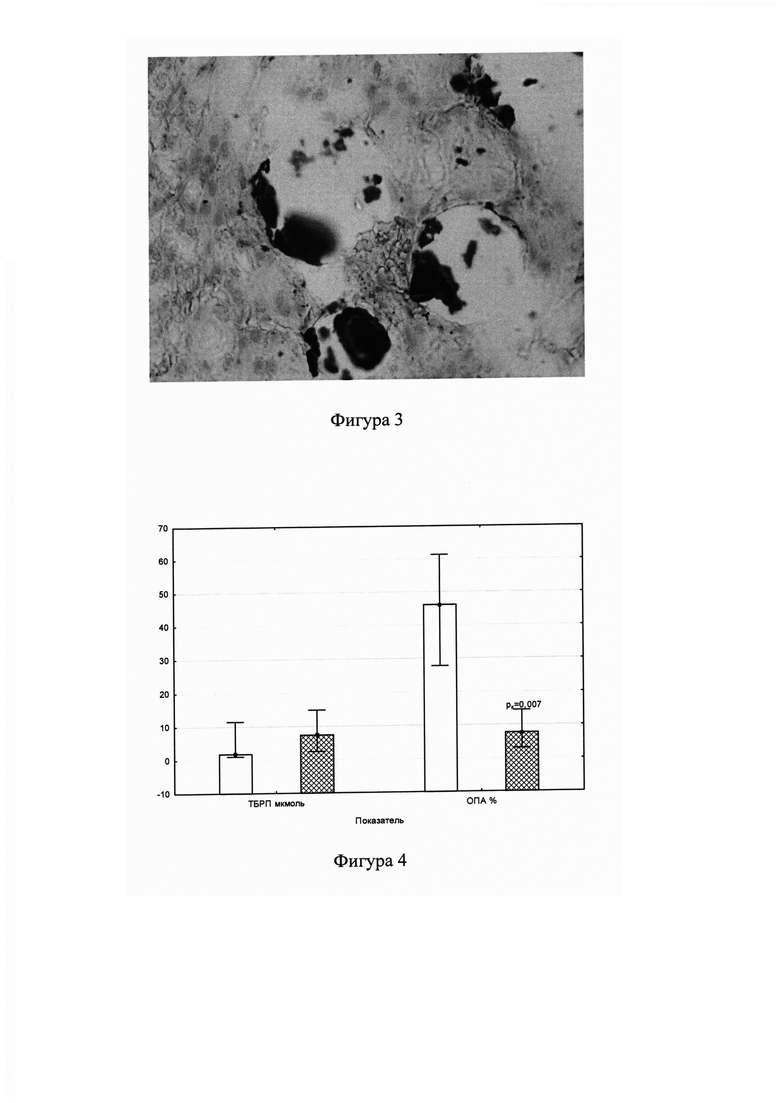
Фигура 3 - окраска по Косса. Увеличение ×400;
Фигура 4 - по горизонтальной оси - название показателя и единицы измерения. По вертикальной оси - значение показателя.  - контрольная группа,
- контрольная группа,  подопытная группа. Значения представлены в виде медианы и минимума-максимума без учета выбросов (non-outlier range). рк - уровень статистической значимости изменений значения соответствующего показателя относительно контрольной группы;
подопытная группа. Значения представлены в виде медианы и минимума-максимума без учета выбросов (non-outlier range). рк - уровень статистической значимости изменений значения соответствующего показателя относительно контрольной группы;
Фигура 5 - по горизонтальной оси - название показателя и единицы измерения. По вертикальной оси - значение показателя. -  контрольная группа, -
контрольная группа, -  подопытная группа. Значения представлены в виде медианы и минимума-максимума без учета выбросов (non-outlier range), рк - уровень статистической значимости изменений значения соответствующего показателя относительно контрольной группы.
подопытная группа. Значения представлены в виде медианы и минимума-максимума без учета выбросов (non-outlier range), рк - уровень статистической значимости изменений значения соответствующего показателя относительно контрольной группы.
Результаты исследований представлены в примерах.
Пример 1.
Результаты проведенных экспериментов показали, что у крыс контрольной группы наблюдались характерные биохимические признаки развития оксалатного нефролитиаза (Таблица 1).


Так, в течение эксперимента происходило снижение величины диуреза, экскреции креатинина и белка. Уровень мочеотделения на 4-ю и 5-ю недели уступал исходным значениям в 1,6 раза и в 2,1 раза соответственно (р=0,047 и р=0,025). При этом экскреция креатинина также достигла минимума на 5-ю неделю, когда она была меньше чем на исходном уровне в 2,7 раза (р=0,022). Экскреция белка достоверно снижалась уже со 2-й недели, достигая минимума на 42-й день периода наблюдений, кода она уступала исходным значениям в 13,5 раза (р=0,017).
Кроме того, возрастала активность маркерных ферментов повреждения почечного эпителия (Таблица 2).
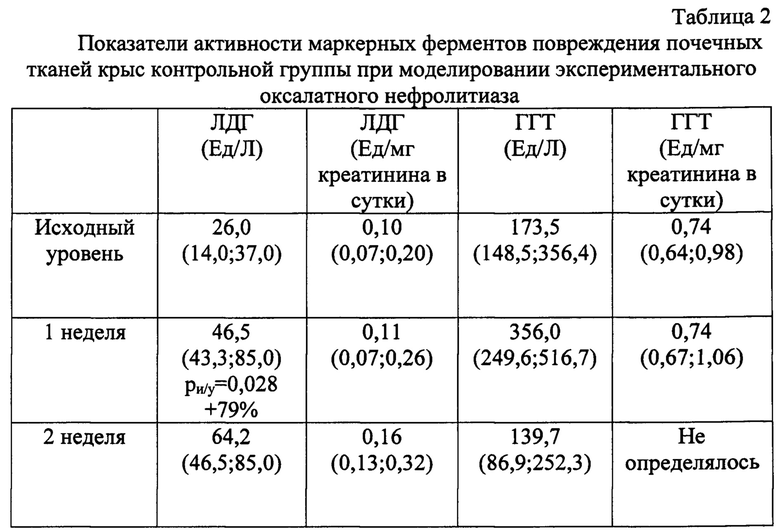

Активность ЛДГ, выраженная в Ед/Л, последовательно возрастала на протяжении всего периода наблюдений. Как следствие, к концу 6-й недели она в 3,3 раза превышала исходный уровень (р=0,022). Кроме того, активность ЛДГ, выраженная в Ед/мг креатинина в сутки, также возрастала, начиная с 5-й недели эксперимента.
В результате на 42-й день она превышала исходный уровень в 4,9 раза (р=0,017). Параллельно фиксировалась тенденция к росту активности ГГТ, выраженной в Ед/Л. За 6 недель периода наблюдений величина данного показателя возросла в 1,7 раза относительно исходного уровня.
Изучение активности процесса свободнорадикального окисления в почках крыс контрольной группы позволило определить следующие параметры оксидативного повреждения почек при моделировании нефролитиаза.
Показатели прооксидантного статуса - концентрация ТБРП и ОПА - имели значения 1,9 (1,3; 10,9) мкмоль и 46,0 (38,6; 54,0) % соответственно (Фиг. 1).
Показатели антиоксидантного статуса - ОАА, активность ГПО, активность КАТ и активность СОД - имели значения 58,1 (52,5; 63,5) %, 49,7 (37,4; 53,9) %, 48,2 (43,7; 50,9) % и 13,2 (11,7; 20,0) % соответственно (Фиг. 2).
Морфологическое исследование почек крыс контрольной группы показало, что при окраске гематоксилином и эозином на участках нефролитиаза эпителий канальцев находился в состоянии гиалиново-капельной дистрофии. Апикальный край клеток местами был разрушен, щеточная кайма местами не видна. Канальцы при этом выглядели кистозно-растянутыми. Клетки нефротелия выстилающего канальцы были разрушены, либо уплощены или атрофичны. Вокруг канальцев определялась слабо или умеренно выраженная воспалительная лимфо-плазмацитарная инфильтрация. Отмечались явления нефросклероза. Сосуды находились в состоянии выраженного полнокровия.
При гистохимическом окрашивании на кальций по методу Косса в канальцах почек крыс контрольной группы отмечали распложенные по одиночке или группами кристаллы депозитов камней коричневато-черного цвета различной формы и размера. Число депозитов в просветах канальцев варьировало от 6 до 19 и в среднем составляло 7,9±1,6 в поле зрения при увеличении ×400, при модальном значении 6 (Фиг. 3).
При проведении компьютерной морфометрии площадь депозитов камней составила от 48,8 мкм2 до 789,9 мкм2, в среднем - 298,8±34,2 мкм2. При более детальном анализе распределения камней в зависимости от их площади выявлено, что число депозитов камней площадью от 20 мкм2 до 100 мкм2 составило 16,7%, количество депозитов площадью от 100 мкм2 до 300 мкм2 составило 47,2% и содержание депозитов площадью более 300 мкм2 и более составило 36,1%. Гистограмма распределения депозитов камней имела сдвиг вправо и пик распределения находился в области площади камней от 100 мкм2 до 300 мкм2.
Пример 2.
Проведенные эксперименты показали, что при длительном применении пептида Leu-Ile-Lys-His для коррекции смоделированного нефролитиаза наблюдались существенные отличия в картине протекания патологии по сравнению с контрольной группой.
Изучение параметров экскреторной функции почек крыс подопытной группы показало, что динамика экскреции креатинина характеризовалась существенным ростом величины данного показателя в 5-ю и 6-ю недели периода наблюдений (Таблица 3).
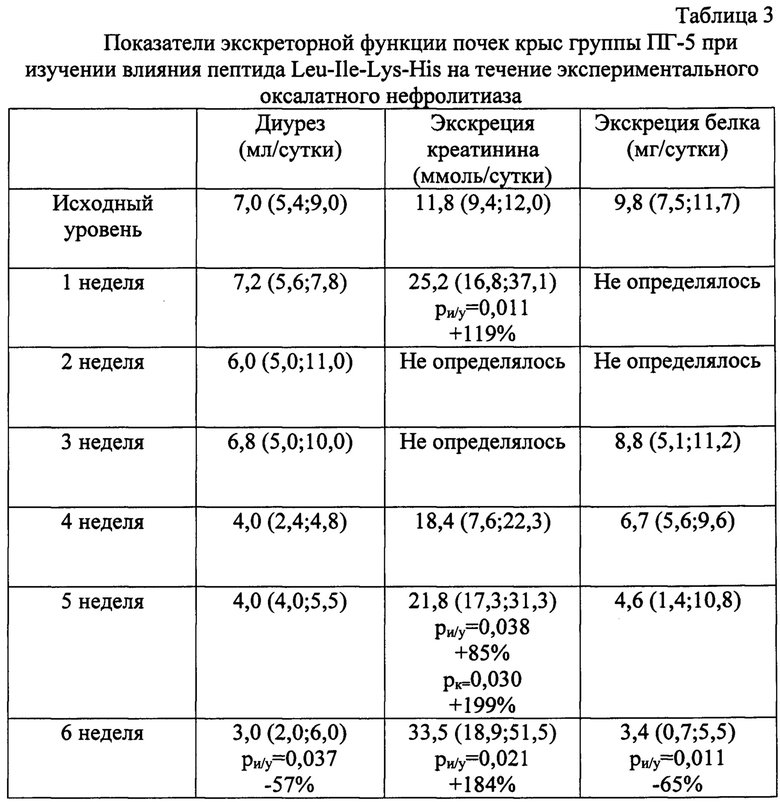

В результате она превышала исходный уровень на 85% и 184% соответственно (р=0,038 и р=0,021). Напомним, что в контрольной группе экскреция креатинина, напротив, снижалась во второй половине эксперимента. Как следствие, показатель экскреции креатинина на 5-й неделе статистически значимо превышал таковой в контрольной группе на 199% (р=0,030). Кроме того, менее выраженно, чем в контроле, ослаблялась экскреция белка. Поэтому достоверное отличие по сравнению с исходным уровнем было зафиксировано лишь к концу 6-й недели. Динамика диуреза также характеризовалась незначительной тенденцией к снижению.
Весьма существенные изменения происходили и в динамике активности маркерных ферментов повреждения почечного эпителия у крыс подопытной группы (Таблица 4).

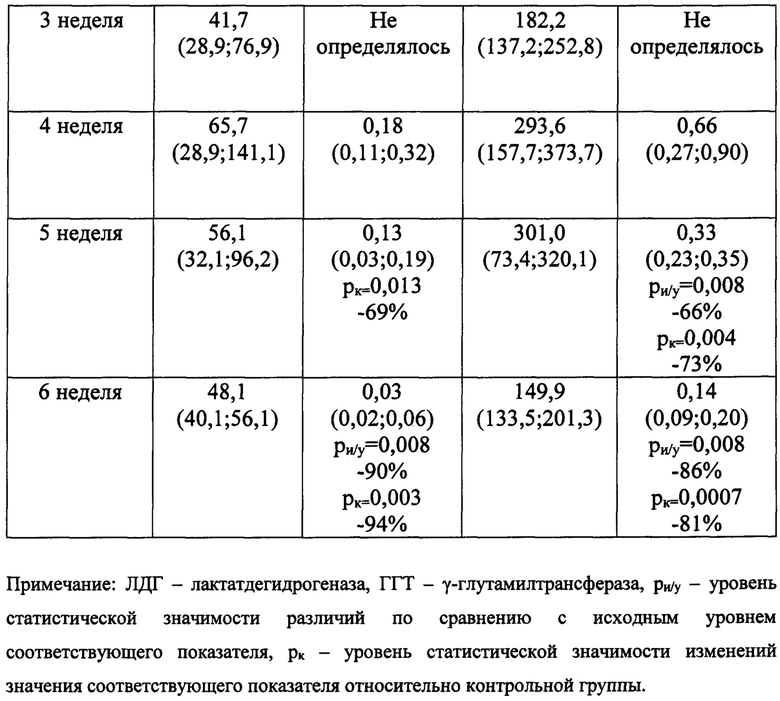
Оказалось, что активность ЛДГ, выраженная в Ед/Л, на протяжении всего эксперимента в целом оставалась стабильной без тенденции к росту, тогда как в контроле заболевания она статистически значимо возрастала в 5-ю и 6-ю недели.
Кроме того, активность ЛДГ, выраженная в Ед/мг креатинина в сутки, у крыс подопытной группы, начиная с 5-й недели эксперимента, снижалась и статистически значимо различалась с аналогичным показателем контрольной группы: в 5-ю неделю - на 69% (р=0,013), а в 6-ю неделю - на 94% (р=0,003).
Снижение описываемого показателю относительно исходного уровня в подопытной группе к концу эксперимента составило 90% (р=0,008). Аналогичная в целом динамика характеризовала изменения активности ГГТ в подопытной группе. Активность данного фермента, выраженная в Ед/Л, сохранялась стабильной весь период наблюдений без тенденции к росту. Активность ГГТ, выраженная в Ед/мг креатинина в сутки, в 5-ю и 6-ю недели существенно снижалась относительно исходного уровня: на 66% и 86% соответственно (р=0,008 и р=0,008). При этом она была статистически значимо меньше, чем в контрольной группе в аналогичный период времени: в 5-ю неделю - на 73% (р=0,004), а в 6-ю неделю - на 81% (р=0,0007).
Изучение активности процесса свободнорадикального окисления в почках крыс подопытной группы позволило установить, что после длительного применения пептида Leu-Ile-Lys-His в 6,0 раз относительно контрольной группы снизилась ОПА (Фиг. 4), составив при этом 7,7 (5,0; 13,0) (р=0,007). Концентрация ТБРП равнялась 7,5 (6,6; 10,7) мкмоль, что было больше, чем в контрольной группе, однако это различие не являлось статистически значимым.
На этом фоне активность антиоксидантного фермента КАТ после проведенного лечения ослабилась в 3,5 раза относительно контроля заболевания и равнялась 13,8 (10,5; 24,7) % (Фиг. 5, р=0,002). Общая антиоксидантная активность, активность ГПО и СОД составили 56,1 (53,9; 58,9) %, 59,8 (58,3; 66,4) % и 6,5 (3,5; 10,7) % соответственно и статистически не отличались от показателей контрольной группы.
Морфологическое исследование почек крыс подопытной группы показало, что в данной группе явлений нефролитиаза выявлено не было. Ткани почки находились в состоянии нормы, ни инкрустации канальцев солями кальция, ни формирования крупных конкрементов не наблюдалось.
| название | год | авторы | номер документа |
|---|---|---|---|
| Фармакологическое средство для лечения мочекаменной болезни | 2018 |
|
RU2679120C1 |
| ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ УРАТНОЙ НЕФРОПАТИИ | 2021 |
|
RU2760949C1 |
| Средство для лечения уратного нефролитиаза | 2021 |
|
RU2762139C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ УРАТНОГО НЕФРОЛИТИАЗА | 2021 |
|
RU2759237C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИЛИТОГЕННЫМ ДЕЙСТВИЕМ, АНТИЛИТАЛ | 2012 |
|
RU2484834C1 |
| Способ получения пептидного средства, обладающего антилитогенным действием | 2017 |
|
RU2652339C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ МОЧЕКАМЕННОЙ БОЛЕЗНИ | 2010 |
|
RU2451935C1 |
| СРЕДСТВО ДЛЯ СТИМУЛЯЦИИ ФИЛЬТРАЦИОННОЙ И ВЫДЕЛИТЕЛЬНОЙ ФУНКЦИИ ПОЧЕК ПРИ ТОКСИЧЕСКОЙ НЕФРОПАТОЛОГИИ | 1992 |
|
RU2008912C1 |
| СПОСОБ РЕАБИЛИТАЦИИ БОЛЬНЫХ С ЗАБОЛЕВАНИЕМ ПОЧЕК | 1999 |
|
RU2177324C2 |
| Способ терапии и профилактики прогрессирования хронической почечной недостаточности | 2021 |
|
RU2763661C2 |


Изобретение относится к медицине и касается применения тетрапептида Leu-Ile-Lys-His, лейцин - изолейцин - лизин - гистидин, в качестве средства для протеомной коррекции оксалатного нефролитиаза. Изобретение обеспечивает расширение ассортимента способов фармакологической коррекции оксалатного нефролитиаза и высокую антилитогенную активность. 5 ил., 4 табл., 2 пр.
Применение тетрапептида Leu-Ile-Lys-His, лейцин - изолейцин - лизин - гистидин, в качестве средства для протеомной коррекции оксалатного нефролитиаза.
| WO 2015002604 A1, 08.01.2015 | |||
| СПОСОБ ХРОНОТЕРАПИИ БОЛЬНЫХ ОКСАЛАТНОЙ НЕФРОПАТИЕЙ | 2004 |
|
RU2274457C1 |
| СПОСОБ ЛЕЧЕНИЯ НЕФРОЛИТИАЗА | 2001 |
|
RU2225175C2 |
| АЛАЕВ Д.С | |||
| и др | |||
| Нефролитиаз при первичном гиперпаратиреозе | |||
| Хирургия экстренная и плановая - инновации и опыт | |||
| Видоизменение прибора с двумя приемами для рассматривания проекционные увеличенных и удаленных от зрителя стереограмм | 1919 |
|
SU28A1 |
Авторы
Даты
2019-10-23—Публикация
2019-01-09—Подача