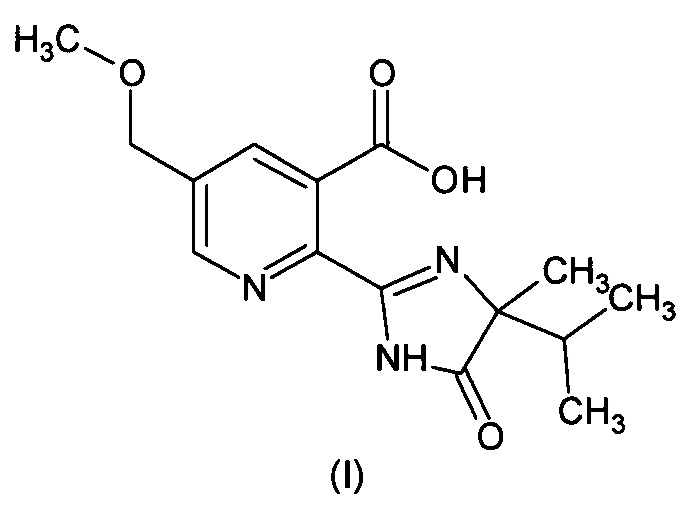
Изобретение относится к области получения пестицидов. Более конкретно, изобретение относится к технологии производства послевсходового гербицида имазамокса, имеющего химическую структуру (±)-2-[4,5-дигидро-4-метил-4-(1-метилэтил)-5-оксо-1H-имидазол-2-ил]-5-(метоксиметил)-3-пиридинкарбоновой кислоты (I). Его регистрационный номер в Реестре химической реферативной службы Американского химического общества CAS [114311-32-9]. Далее по тексту именуется «имазамокс».
В результате патентного поиска были отобраны следующие патенты.
В международных заявках WO №2010055042 и WO №2010066669 раскрыт способ получения (±)-2-[4,5-дигидро-4-метил-4-(1-метилэтил)-5-оксо-1H-имидазол-2-ил]-5-(метоксиметил)-3-пиридинкарбоновой кислоты из 5-метоксиметил-2,3-пиридиндикарбоновой кислоты. Способ многостадийный, включает получение ангидрида 5-метоксиметил-2,3-пиридиндикарбоновой кислоты из 5-метоксиметил-2,3-пиридиндикарбоновой кислоты ее взаимодействием с уксусным ангидридом, ацилирование полученным ангидридом 5-метоксиметил-2,3-пиридиндикарбоновой кислоты 2-амино-2,3-диметилбутиронитрила, гидролиз полученной 2-[[(1-циано-1,2-диметилпропил)амино]карбонил]-5-(метоксиметил)-пиридин-3-карбоновой кислоты в кислых условиях, внутримолекулярную циклизацию полученной 2-[[[1-(аминокарбонил)-1,2-диметилпропил]амино]карбонил]-5-(метоксиметил)-пиридин-3-карбоновой кислоты в щелочных условиях и выделение имазамокса из полученной соли в кислых условиях. Недостатком описанного способа является высокая стадийность, большое число технологических операций, необходимость применения контролируемого уксусного ангидрида (Постановление Правительства РФ от 30 июня 1998 г. №681 «Об утверждении перечня наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю в Российской Федерации») и сложность технологической реализации.
Известен способ получения оптически активной формы имазамокса. В патенте США №5973154 приведен пример получения 2-[(4R)-4,5-дигидро-4-метил-4-(1-метилэтил)-5-оксо-1H-имидазол-2-ил]-5-(метоксиметил)-3-пиридинкарбоновой кислоты CAS [221298-64-2]. Он заключается во взаимодействии диметилового эфира 5-метоксиметил-2,3-пиридиндикарбоновой кислоты с (R)-2-амино-2,3-диметилбутирамидом в безводном толуоле в присутствии трет-бутилата калия и последующем разложении полученной калиевой соли (R)-имазамокса концентрированной соляной кислотой. Выделение целевого продукта осуществляют путем экстракции массы после подкисления хлористым метиленом, осушки экстракта над сульфатом магния, очистки экстракта с использованием диоксида кремния, фильтрования и удаления растворителя при пониженном давлении. Основными недостатками описанного способа являются использование безводных растворителей при синтезе соли имазамокса и технологическая сложность выделения целевого продукта с большим количеством технологических операций. Осажденный после подкисления продукт экстрагируют исключительно хлористым метиленом. Использование этого легкокипящего (Ткип = 40°С) легковоспламеняющегося (Твсп = -14°С) органического растворителя приводит к большим потерям при его отгонке и регенерации. Также известно, что этот растворитель высококоррозионный, что налагает повышенные требования к материалам аппаратуры. Выход имазамокса составляет 73,5%, что близко к умеренному.
Задачей предлагаемого технического решения является улучшение технико-экономических показателей и упрощение технологического процесса получения имазамокса (I).
Техническим результатом является упрощение технологического процесса производства имазамокса, которое выражается в том, что исключено использование безводных растворителей, исключены стадии экстракции хлористым метиленом, осушки и очистки органического экстракта, упаривания хлористого метилена. В результате выход целевого продукта повышен до 83,6%.
Технический результат достигается путем использования способа получения (±)-2-[4,5-дигидро-4-метил-4-(1-метилэтил)-5-оксо-1H-имидазол-2-ил]-5-(метоксиметил)-3-пиридинкарбоновой кислоты (имазамокса) (I), включающего синтез соли имазамокса (IV) из диметилового эфира 5-метоксиметил-2,3-пиридиндикарбоновой кислоты (II) и (±)-2-амино-2,3-диметилбутирамида (III) в присутствии трет-бутилата натрия или калия в толуоле или ксилоле при нагревании, растворение полученной соли в воде и отделение толуола или ксилола, последующий перевод полученной соли имазамокса в целевой продукт под действием соляной или серной кислоты и выделение целевого продукта. Предварительно удаляют влагу из раствора диметилового эфира 5-метоксиметил-2,3-пиридиндикарбоновой кислоты и (±)-2-амино-2,3-диметилбутирамида в толуоле или ксилоле азеотропной отгонкой, процесс получения соли имазамокса ведут в атмосфере инертного газа, полученный раствор соли имазамокса очищают при перемешивании с 6-12 масс. % активированного угля (в расчете на исходный диметиловый эфир 5-метоксиметил-2,3-пиридиндикарбоновой кислоты) в течение 1-2 часов, отработанный активированный уголь отфильтровывают, полученный раствор соли имазамокса подкисляют до кислых значений рН, выделяют выпавший осадок целевого продукта фильтрованием, промывкой водой и высушиванием.
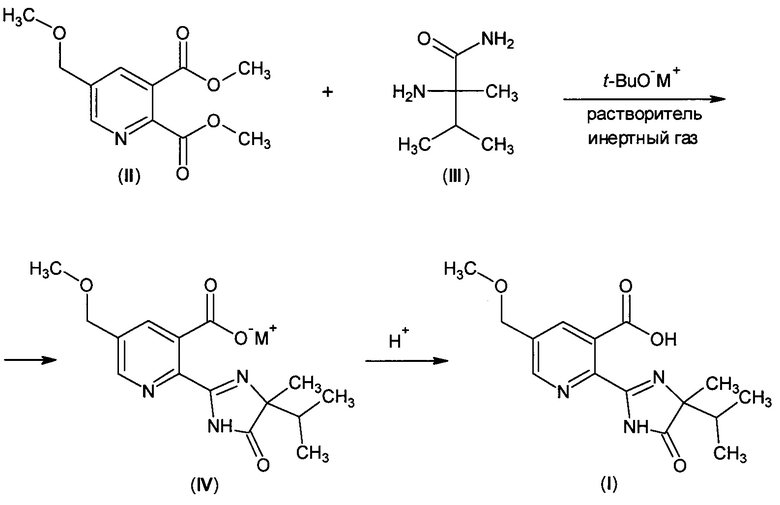
М=Na, K; растворитель = толуол, ксилол; Н+=HCl, H2SO4.
Изобретение иллюстрируется следующими примерами.
Пример 1 (сравнительный по прототипу).
Смесь 21,54 г (0,09 моль) диметилового эфира 5-метоксиметил-2,3-пиридиндикарбоновой кислоты II и 12,09 г (0,093 моль) (±)-2-амино-2,3-диметилбутирамида III в безводном толуоле перемешивают при комнатной температуре на протяжении 15 минут, прибавляют 9,12 г (0,095 моль) трет-бутилата натрия, выдерживают при перемешивании 5 минут и прибавляют еще 9,12 г (0,095 моль) трет-бутилата натрия. Реакционную массу нагревают при перемешивании до полного срабатывания соединения II (контроль ТСХ). По окончании реакции реакционную массу охлаждают до комнатной температуры и при перемешивании прибавляют воду для растворения натриевой соли имазамокса. Перемешивают до полного растворения твердой фазы в воде, перемешивание останавливают и полученной двухфазной системе дают разделиться. Представляющую собой раствор натриевой соли имазамокса водную фазу отделяют, при перемешивании прибавляют к ней концентрированную серную кислоту до значения рН ~ 3 и дважды экстрагируют хлористым метиленом. Экстракты объединяют, объединенный экстракт высушивают над сульфатом магния, прибавляют к нему диоксид кремния, перемешивают и отфильтровывают. Фильтрат упаривают при пониженном давлении досуха. Получают 19,8 г порошка имазамокса. Выход 72,1%.
Пример 2 (заявляемый способ).
В реактор синтеза соли имазамокса загружают 450 г (1,88 моль) диметилового эфира 5-метоксиметил-2,3-пиридиндикарбоновой кислоты II, толуол, и при перемешивании прибавляют 252,3 г (1,94 моль) 2-амино-2,3-диметилбутирамида III. Для удаления из полученного раствора влаги, привнесенной с сырьем и растворителем, реактор вакуумируют, нагревают и отгоняют влагу в азеотропной смеси с растворителем. После этого вакуумирование прекращают и в реактор подают азот. К раствору комнатной температуры при перемешивании прибавляют 191,4 г (1,99 моль) трет-бутилата натрия, выдерживают при перемешивании 5 минут и прибавляют еще 191,4 г (1,99 моль) трет-бутилата натрия. Реакционную массу нагревают при перемешивании с непрерывной подачей азота до полного срабатывания соединения II (контроль ТСХ). По окончании реакции содержимое реактора синтеза перекачивают в реактор выделения, охлаждают до комнатной температуры и при перемешивании прибавляют воду для растворения натриевой соли имазамокса. Перемешивают до полного растворения твердой фазы в воде, перемешивание останавливают и полученной двухфазной системе дают разделиться. Представляющую собой раствор натриевой соли имазамокса водную фазу отделяют в реактор очистки. К щелочной водной фазе в реакторе очистки прибавляют 6-12 масс. % активированного угля (в расчете на соединение II), перемешивают 1-2 часа и отфильтровывают от отработанного угля в реактор подкисления. К очищенному раствору натриевой соли имазамокса в реакторе подкисления при перемешивании прибавляют концентрированную серную кислоту до значения рН ~ 3. Полученную суспензию фильтруют, осадок на фильтре трижды промывают водой и высушивают на воздухе. Получают 480,2 г порошка имазамокса. Выход 83,6%.
Пример 3.
Способ получения имазамокса осуществлялся аналогично примеру 2. Отличие состояло в использовании трет-бутилата калия в качестве основания и ксилола в качестве растворителя. Получают 460,1 г порошка имазамокса с выходом 80,1%.
В результате использования предложенного способа значительно упрощается технологический процесс в целом. Сокращается число технологических операций, исключается сложно реализуемая стадия отгонки растворителя до сухого остатка. Исключается использование безводного растворителя для синтеза соли имазамокса, исключается использование легкокипящего легковоспламеняющегося органического растворителя (хлористого метилена). Улучшаются показатели процесса. Выход целевого продукта имазамокса повышается на 11,5% и составляет 83,6%. Растворитель может быть регенерирован с возвращением обратно в процесс до 85% от использованного количества.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения имазапира | 2022 |
|
RU2785158C1 |
| ГЕРБИЦИДНЫЕ КОМПОЗИЦИИ | 2007 |
|
RU2472343C9 |
| ДИГИДРОПИРИДИНОВЫЕ ПРОИЗВОДНЫЕ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1992 |
|
RU2086548C1 |
| НИТРАТНЫЕ СОЛИ ГИПОТЕНЗИВНЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 1999 |
|
RU2235097C2 |
| СОЕДИНЕНИЯ ОКСАЗОЛИДИНДИГАЛОАЦЕТАМИДА И СПОСОБ УМЕНЬШЕНИЯ ФИТОТОКСИЧЕСКОГО ДЕЙСТВИЯ ГЕРБИЦИДОВ | 1988 |
|
RU2093029C1 |
| Способ получения производных N-фенил-N-(4-пиперидинил)амида или их солей | 1978 |
|
SU867304A3 |
| 5,6-ДИЗАМЕЩЕННЫЕ 3-ПИРИДИЛМЕТИЛАММОНИЙ ГАЛОГЕНИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СПОСОБЫ ПОЛУЧЕНИЯ 5-(ЗАМЕЩЕННЫЙ МЕТИЛ)-2,3-ПИРИДИНДИКАРБОНОВЫХ КИСЛОТ | 1993 |
|
RU2090558C1 |
| НОВЫЙ МОНОГИДРАТ ПРОИЗВОДНОГО НАФТИРИДИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2008 |
|
RU2485127C2 |
| СИНЕРГИЧЕСКАЯ ГЕРБИЦИДНАЯ СМЕСЬ, СОДЕРЖАЩАЯ ПЕНОКСУЛАМ, ТРИКЛОПИР И ИМАЗЕТАПИР ИЛИ ИМАЗАМОКС, КОМПОЗИЦИЯ НА ОСНОВЕ СМЕСИ И СПОСОБ БОРЬБЫ С НЕЖЕЛАТЕЛЬНОЙ РАСТИТЕЛЬНОСТЬЮ | 2012 |
|
RU2601057C2 |
| АНЕЛЛИРОВАННЫЕ β--КАРБОЛИНЫ | 1996 |
|
RU2169148C2 |
Изобретение относится к области получения пестицидов, в частности к технологии производства послевсходового гербицида имазамокса, имеющего химическую структуру (±)-2-[4,5-дигидро-4-метил-4-(1-метилэтил)-5-оксо-1H-имидазол-2-ил]-5-(метоксиметил)-3-пиридинкарбоновой кислоты. Способ получения (±)-2-[4,5-дигидро-4-метил-4-(1-метилэтил)-5-оксо-1H-имидазол-2-ил]-5-(метоксиметил)-3-пиридинкарбоновой кислоты (имазамокса) включает синтез соли имазамокса из диметилового эфира 5-метоксиметил-2,3-пиридиндикарбоновой кислоты и (±)-2-амино-2,3-диметилбутирамида в присутствии трет-бутилата натрия или калия в толуоле или ксилоле при нагревании, растворение полученной соли в воде и отделение толуола или ксилола, последующий перевод полученной соли имазамокса в целевой продукт под действием соляной или серной кислоты и выделение целевого продукта. При этом предварительно удаляют влагу из раствора диметилового эфира 5-метоксиметил-2,3-пиридиндикарбоновой кислоты и (±)-2-амино-2,3-диметилбутирамида в толуоле или ксилоле азеотропной отгонкой, а процесс получения соли имазамокса ведут в атмосфере инертного газа. Полученный раствор соли имазамокса очищают при перемешивании с 6-12 мас.% активированного угля в расчете на исходный диметиловый эфир 5-метоксиметил-2,3-пиридиндикарбоновой кислоты в течение 1-2 ч и отработанный активированный уголь отфильтровывают. Полученный раствор соли имазамокса подкисляют до кислых значений рН, выделяют выпавший осадок целевого продукта фильтрованием, промывкой водой и высушиванием. Предлагаемый способ получения (±)-2-[4,5-дигидро-4-метил-4-(1-метилэтил)-5-оксо-1H-имидазол-2-ил]-5-(метоксиметил)-3-пиридинкарбоновой кислоты (имазамокс) обеспечивает упрощение технологического процесса производства имазамокса, которое выражается в том, что исключено использование безводного растворителя, исключены стадии экстракции высококоррозионными растворителями, осушки и очистки органического экстракта, упаривание хлорорганических соединений, а также обеспечивает выход целевого продукта до 83,6%.
Способ получения (±)-2-[4,5-дигидро-4-метил-4-(1-метилэтил)-5-оксо-1Н-имидазол-2-ил]-5-(метоксиметил)-3-пиридинкарбоновой кислоты (имазамокса), включающий синтез соли имазамокса из диметилового эфира 5-метоксиметил-2,3-пиридиндикарбоновой кислоты и (±)-2-амино-2,3-диметилбутирамида в присутствии трет-бутилата натрия или калия в толуоле или ксилоле при нагревании, растворение полученной соли в воде и отделение толуола или ксилола, последующий перевод полученной соли имазамокса в целевой продукт под действием соляной или серной кислоты и выделение целевого продукта, отличающийся тем, что предварительно удаляют влагу из раствора диметилового эфира 5-метоксиметил-2,3-пиридиндикарбоновой кислоты и (±)-2-амино-2,3-диметилбутирамида в толуоле или ксилоле азеотропной отгонкой, процесс получения соли имазамокса ведут в атмосфере инертного газа, полученный раствор соли имазамокса очищают при перемешивании с 6-12 мас.% активированного угля в расчете на исходный диметиловый эфир 5-метоксиметил-2,3-пиридиндикарбоновой кислоты в течение 1-2 ч, отработанный активированный уголь отфильтровывают, полученный раствор соли имазамокса подкисляют до кислых значений рН, выделяют выпавший осадок целевого продукта фильтрованием, промывкой водой и высушиванием.
| US 5973154 A1, 26.10.1999 | |||
| WO 2010066669 A1, 17.06.2010 | |||
| WO 2010055042 A1, 20.05.2010. |
Авторы
Даты
2019-11-21—Публикация
2019-03-25—Подача