Предлагаемое изобретение относится к биотехнологии, генной инженерии, медицинской микробиологии и может быть использовано для получения препаратов шаперона (Hfq) Vibrio cholerae в целях создания специфических сорбентов для связывания малых РНК, а также для изучения свойств, биохимической и биологической активности шаперона (Hfq) Vibrio cholerae.
Растворимый шаперон (Hfq) является регуляторным белком связывающий малые РНК холерных вибрионов (1, 2, 3). Выделение и очистка с последующим фракционированием малых РНК у холерного вибриона сопряжены с различными трудностями как-то отделение их от сопутствующей хромосомной и плазмидной ДНК, транспортной и матричной РНК (4). На практике эти задачи решаются применением многоступенчатых сложных этапов очистки включающих разделение молекул на хроматографических колонках и в полиакриамидных гелях с использованием специфических гидролитических ферментативных комлексов для ДНК, транспортной и матричной РНК(5).
В настоящее время существует проблема в разработке нового подхода в основе которого лежит прямое связывание малых РНК афинным белком шапероном Hfq V.cholerae иммобилизованным на латексных микрочастицах и прямое извлечение их смеси биомолекул. В свою очередь, для создания таких микрочастиц требуются препаративные количества искомого белка Hfq. Наиболее эффективным способом получения белка остается использование лабораторных штаммов Е.coli, содержащих и экспрессирующих клонированный ген hfq Vibrio cholera 01.
Известна рекомбинантная плазмида рЕТ28 [VcHfq], экспрессирующая клонированный в составе векторной плазмиды pET28b (Novagen) ген hfq Vibrio cholerae 017 в штамме E.coli BL21 (DE3) (6), однако продуктивность этого штамма как продуцента авторами не описана.
Однако о продуцирующей способности плазмиды рЕТ28 [VcHfq] данные отсутствуют, а недоступность для исследования в России не позволяет провести их.
Технической задачей предполагаемого изобретения является
- клонирование гена hfq в составе плазмидного вектора pQE30, обеспечивающего экспрессию чужеродных генов под контролем мощного Т5-промотора, и создание штамма E.coli - суперпродуцента рекомбинантного белка 6his-Hfq V.cholerae 01.
Задача решается путем создания:
- новой рекомбинантной плазмиды pHFQ2.21, экспрессирующей клонированный ген hfq холерного вибриона в штаммах кишечной палочки.
- штамма Escherichia coli Jm109 pHFQ2.21 - суперпродуцента Hfq холерных вибрионов посредством трансформации штамма Е. coli Jm109 рекомбинантной плазмидой pHfq.
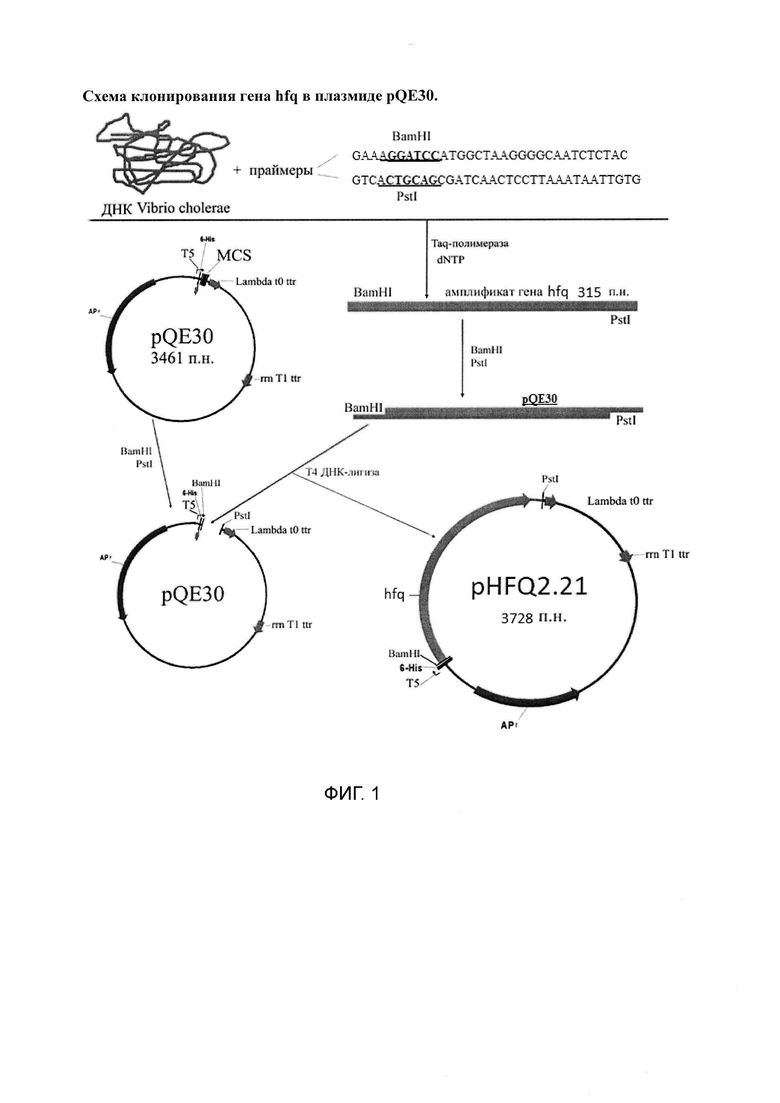
На фиг. 1 представлена схема конструирования рекомбинантной плазмиды pHFQ2.21.
Векторная плазмида pQE30 несет ген устойчивости к ампициллину (bla) и содержит промоторно-операторную область, включающую Т5-промотор и два расположенных тандемом lac-оператора, обеспечивающих максимальную репрессию синтеза Hfq в присутствии глюкозы, а также синтетический сайт связывания рибосомальной РНК, старт-кодон последовательность триплетов, кодирующих синтез гексагистидина (6-His), полилинкер (MCS) и два терминатора транскрипции (t0 фага лямбда и Т1 из rrnB-оперона Е. coli). Экспрессия клонированных генов происходит при индукции изопропил-β-D-тиогалактозидом (ИПТГ) и начинается с плазмидного старт-кодона, при этом образуется гибридный белок, перед первой аминокислотой которого располагается гексагистидиновый блок.
Плазмида pHFQ2.21 представляет собой генно-инженерный вариант, полученный путем встраивания в вектор pQE30 гена hfq V.cholerae O1 биовара El Tor (см. фиг. 1).
Будучи трансформирована в штамм кишечной палочки Jm103 либо Jm109, рекомбинантная плазмида экспрессирует клонированный ген под контролем Т5-промотора. Экспрессия гена подавляется в присутствии глюкозы и индуцируется ИПТГ.
Штамм E.coli Jm109pHFQ2.21 представляет собой генно-инженерный вариант, полученный путем трансформации рекомбинантной плазмиды pHFQ2.21 в штамм E.coli Jm109, и является продуцентом шаперона Hfq V.cholerae. Первичный продукт трансляции не подвергается протеолитическому процессингу и остается в виде про-шаперона (6his-Hfq) с молекулярной массой субъединицы около 11,2 кДа, который, тем не менее, обладает способностью к агрегации в гексамер и связывать малые РНК. Штамм депонирован в Государственной коллекции патогенных бактерий «Микроб» под номером КМ 2030.
Полученный штамм-продуцент характеризуется следующими признаками:
Культуралыю-морфологические свойства
В жидких питательных средах (бульоне Хоттингера, мясо-пептонном бульоне) образует равномерную муть, на плотных - круглые, выпуклые, гладкие, белые полупрозрачные колонии с ровным краем, тестообразной консистенции.
Физиолого-биохимические свойства
Штамм разлагает с образованием кислоты и газа глюкозу, арабинозу и ман-нит, не разлагает сахарозу, на среде Эндо образует лактозонегативные колонии. Ауксотроф.
Устойчивость к антибиотикам
Штамм устойчив к 50-100 мкг/мл ампициллина за счет экспрессии гена bla, находящегося в составе векторной плазмиды pQE30.
Способ получения и использования рекомбинантной плазмиды и штамма-продуцента иллюстрируется следующими примерами.
Пример 1. Клонирование гена hfq и получение рекомбинантной плазмиды
Для ПЦР-синтеза гена hfq используют праймеры, сконструированные заявителями на основе анализа нуклеотидной последовательности гена hfq в хромосоме (NC_002505.1):
прямой - 5'- GAAAGGATCCATGGCTAAGGGGCAATCTCTAC -3' и
обратный - 5'- GTCACTGCAGCGATCAACTCCTTAAATAATTGTGCT -3'.
Поскольку амплификаты необходимо встроить в плазмидный вектор pQE30 в ориентации, обеспечивающей направление транскрипции под контролем Т5-промотора, на 5'-конце каждого праймера внесен сайт рестрикции для эндонук-леазы, образующей липкие концы: BamHI для прямого праймера и PstI - для обратного (в приведенных последовательностях выделены жирным шрифтом и подчеркнуты) в соответствии с порядком расположения сайтов рестрикции в полилинкере векторной плазмиды.
Из токсигенного штамма V.cholerae Эль Тор 5879 (Музей живых культур Ростовского-на-Дону противочумного института) фенольным методом выделяют хромосомную ДНК, которая служит матрицей для синтеза искомого гена.
300 мкл реакционной смеси для полимеразной цепной реакции содержат 0,5 нг ДНК-матрицы и следующие компоненты в указанных концентрациях: по 2,5 мкл каждого праймера, по 2,5 мМ всех четырех дезоксинуклеотидтрифосфатов, 3 ед. Taq-полимеразы и 0,1 объема прилагаемого к ней 10-кратного буфера. Смесь разливают по 30 мкл в 0,5-мл пластиковые пробирки и осуществляют реакцию по следующей схеме: 94°С - денатурация (20 сек), 58°С - отжиг (10 сек), 72°С - синтез (10 сек). Всего проводят 30 циклов амплификации, в последнем цикле время синтеза увеличивают до 3 минут. По окончании реакции содержимое пробирок объединяют, очищают смесью фенол: хлороформ : изоамиловый спирт в соотношении 25:24:1 и осаждают этиловым спиртом.
Полученный таким образом ПЦР-амплификат длиной 315 п. н. и ДНК векторной плазмиды pQE30 гидролизуют эндонуклеазами рестрикции BamHI и PstI согласно рекомендациям фирмы - изготовителя ферментов, очищают смесью фенол : хлороформ : изоамиловый спирт (25:24:1) и осаждают этиловым спиртом. Осадок растворяют в минимальном объеме деионизованной воды и лигируют с использованием ДНК-лигазы фага Т4 и прилагаемого к ней буфера согласно рекомендациям изготовителя.
Лигазными смесями трансформируют электорокомпетентные клетки E.coli Jm109, приготовленные накануне. После процедуры электропорации (2,6 кВольт, +4°С, 25 мкФ, 200 Ом, кювета 2 мм) клетки разводят в 5 раз средой SOC с 0,5% глюкозы, подращивают в течение 1 ч и высевают на агар LB, содержащий 50 мкг/мл ампициллина и 0,5% глюкозы. Посевы инкубируют при 37°С. На следующие сутки выросшие ампициллинрезистентые колонии тестируют с помощью вышеприведенных праймеров и отбирают позитивные клоны, из которых выделяют плазмидную ДНК и подтверждают наличие вставок длиной -315 п. н. гидролизом этих плазмид эндонуклеазами рестрикции BamHI и PstI с последующим электрофорезом в 1% агарозном геле.
Пример 2. Изучение экспрессии клонированного гена Hfq в E.coli
В клетках E.coli, в отличие от V.cholerae, шаперон не подвергается протеолитическому процессингу и синтезируется в виде 6his-шаперона (6his-Hfq). Для выявления способности рекомбинантов к синтезу proHfq рекомбинантный штамм E.coli Jm109pHFQ2.21 (KM 2030), а также контрольный штамм, содержащий векторную плазмиду pQE30 без вставки, выращивают в жидкой среде LB, содержащей 50 мкг/мл ампициллина, в течение 3-4 ч при 37°С с шуттелированием при 120 об/мин и затем индуцируют 1 мМ ИПТГ в течение 1-2 ч, клетки осаждают центрифугированием, лизируют в буфере, содержащем 65 мМ трис-HCl рН 6.8, 1% SDS и 10 мМ 2-меркаптоэтанола, при температуре 99°С в течение 10 мин. Лизат подвергают электрофорезу в 8-20% градиентном полиакриламидном геле (ПААГ) с 0,1% SDS и окрашивают гель Coomassi Blue R250. В клеточном лизате выявляется мажорная белковая полоса в области ~12 кДа, что соответствует молекулярной массе искомого рекомбинантного белка, содержащего на N-конце гексагистидиновый блок. Процентное содержание бШэ-белка определяют с помощью программы Quantity One, оно составляет -10% суммарных клеточных белков штамма E.coli Jm109pHFQ2.21. В лизатах штамма E.coli Jm109 pHFQ2.21, выращенного без индукции ИПТГ, и контрольного штамма E.coli Jm109 pQE30 независимо от индукции данная мажорная полоса отсутствует.
Для определения локализации рекомбинантного proHfq клетки продуцента, выращенного с индукцией, разрушают ультразвуком на дезинтергаторе QSonica Q700 в течение 10 мин (40 импульсов по 5 сек, 357 Дж с перерывами в 10 сек; амплитуда 50) и подвергают электрофорезу растворимую фракцию клеток. Искомый белок выявляется в растворимой фракции штамма E.coli Jm109pHFQ2.21, где его содержание составляет ~10% суммарных клеточных белков.
Преимуществами полученного продуцента по сравнению с холерными вибрионами является высокий выход искомого белка, возможность культивирования без соблюдения режима работы с возбудителями особо опасных инфекций, отсутствие способности к синтезу каких-либо дополнительных биологически активных субстанций, которые могли бы затруднить его выделение и очистку, а по сравнению с известными рекомбинантными штаммами-продуцентами - непродолжительный период наращивания биомассы (4-6 часов включая индукцию), беспечивая возможность ускоренного получения препарата.
Источники информации
1. Aiba Н. Mechanism of RNA silencing by Hfq-binding small RNAs //Current opinion in microbiology. - 2007. - T. 10. - №. 2. - C. 134-139.
2. Sun X., Zhulin I., Wartell R.M. Predicted structure and phyletic distribution of the RNA-binding protein Hfq //Nucleic acids research. - 2002. - T. 30. - №. 17. - C. 3662-3671.
3. Васильева Ю.M., Гарбер M.Б. Регуляторная роль белка Hfq в жизнедеятельности бактериальных клеток (Обзор) (2002). Молекулярная биология (Москва), т. 36, 970-977.
4. Bohn С, Rigoulay С, Bouloc P. No detectable effect of RNA-binding protein Hfq absence in Staphylococcus aureus //BMC microbiology. - 2007. - T. 7. - №. 1. - C. 10.
5. Мурина B.H., Никулин А.Д. РНК-связывающие Sm-подобные белки бактерий и архей: сходство и различие структур и функций (Обзор) (2011). Успехи биологической химии, т. 51, 3-164.
6. Vincent Н. A. et al. Characterization of Vibrio cholerae Hfq provides novel insights into the role of the Hfq C-terminal region //Journal of molecular biology. - 2012. - T. 420. - №. 1-2. - C. 56-69.
Изобретение относится к биотехнологии, генной инженерии, медицинской микробиологии. Предложена рекомбинантная плазмида pHFQ2.21, экспрессирующая клонированный ген hfq (шаперона) Vibrio cholerae 01 биовара El Tor, встроенный по сайтам Bam HI-PstI в полилинкер векторной плазмиды pQE30, под контролем Т5-промотора. Указанной плазмидой трансформируют штамм Е. coli Jm109 с получением штамма Escherichia coli KM 2030, являющегося суперпродуцентом шаперона (Hfq) Vibrio cholerae 01 El Tor. Предложенный штамм депонирован в Государственной коллекции патогенных бактерий «Микроб». Содержание шаперона (Hfq) Vibrio cholerae 01 El Tor, находящегося внутри клеток в растворимой форме, составляет до 10% суммарных клеточных белков. Изобретение может быть использовано для получения препаратов шаперона (Hfq) Vibrio cholerae в целях создания специфических сорбентов для связывания малых РНК, а также для изучения свойств, биохимической и биологической активности шаперона (Hfq) Vibrio cholerae. 2 н.п. ф-лы, 1 ил., 2 пр.
1. Рекомбинантная плазмида pHFQ2.21, экспрессирующая клонированный ген hfq (шаперона) Vibrio cholerae 01 биовара El Tor, встроенный по сайтам Bam HI-PstI в полилинкер векторной плазмиды pQE30, под контролем Т5-промотора.
2. Штамм Escherichia coli KM 2030 Государственной коллекции патогенных бактерий «Микроб» представляет собой продукт, полученный путем трансформации рекомбинантной плазмиды pHFQ2.21 по п. 1 в штамм Е. coli Jm109, и является суперпродуцентом шаперона (Hfq) Vibrio cholerae 01 El Tor.
| VINCENT H.A | |||
| ET AL | |||
| Characterization of Vibrio cholerae Hfq Provides Novel Insights into the Role of the Hfq C-Terminal Region | |||
| J.Mol.Biol., 2012 Jun 29; 420(1-2):56-69 | |||
| ПИСАНОВ Р.В | |||
| и др | |||
| Роль малых РНК в контроле экспрессии генов, вовлеченных в реализацию патогенности Vibrio cholerae | |||
| Пробл | |||
| особо опасных инф., 2017; 2:36-39 | |||
| KAWAMOTO H | |||
| ET AL |
Авторы
Даты
2019-11-27—Публикация
2018-11-14—Подача