ОБЛАСТЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к использованию молекулярных маркеров в качестве средства обнаружения развития случаев респираторных инфекций. В частности, в процессе дифференциальной диагностики респираторных инфекций, вызванных респираторно-синцитиальным вирусом (SRV) и метапневмовирусом человека (MPV).
В частности, настоящее изобретение описывает использование маркеров IL-3, IL-12p40 и IL-33 для прогнозирования возникновения случаев рецидивирующих респираторных инфекций после бронхиолита, вызванных SRV.
ПРЕДЫДУЩИЙ УРОВЕНЬ ТЕХНИКИ
Респираторно-синцитиальный вирус (SRV) является наиболее широко распространенной причиной инфекции дыхательных путей и первопричиной госпитализации вследствие острой инфекции нижних дыхательных путей у грудных детей. Бронхиолит, вызванный SRV, связан с астмой и рецидивирующей бронхиальной обструкцией, тем не менее, объяснение механизмов, которые связаны с этим, не выявлено.
SRV представляет собой оболочечный вирус, который относится к семейству Paramyxoviridae и является одним из наиболее широко распространенных этиологических факторов острых инфекций дыхательных путей, вызывающих сверх нагрузку на системы общественного здравоохранения.
SRV приводит к заболеванию нижних дыхательных путей у пациентов любого возраста, с большей степенью тяжести инфекции у грудных детей младше 6 месяцев, в частности, у пациентов с хроническими или основными заболеваниями. У большинства грудных детей с бронхиолитом, вызванным SRV, в течение первых месяцев жизни развивается рецидивирующая бронхиальная обструкция и астма, но четкое определение конкретных механизмов, задействованных в иммунопатогенезе бронхиолита SRV, до сих пор отсутствует. Более того, текущие клинические параметры не позволяют прогнозировать возможность возникновения некоторых из этих хронических заболеваний позже у грудных детей, после того, как они переболели бронхиолитом, вызванным SRV.
Воспаление, вызванное этим вирусом, характеризуется наличием масштабной инфильтрации клеток в нижних дыхательных путях, преимущественно нейтрофилов. Такие изменения в легких были описаны как возникновение инфекции, вызванной SRV в эпителиальных клетках дыхательных путей, альвеолярных макрофагов и периферийных кровяных нейтрофилов, которая вызывает выделение определенных цитокинов и хемокинов. Эти молекулы характеризуются хемотактическими свойствами в отношении воспалительных клеток и других типов клеток. Дисбаланс цитокинов типа Th1/Th2 также был рассмотрен как ключевое событие при воспалении с миграцией клеток в результате инфекции, вызванной SRV, что может быть опосредовано эозинофилами и другими клетками, которые относятся к аллергической индукции, например, базофилы и мастоциты, которые могут способствовать развитию астмы. Более того, известно, что некоторые цитокины, образованные эпителиальными клетками дыхательных путей, непосредственно задействованы в аллергической индукции и астме, включая IL-25, IL-33 и тимусный стромальный лимфопоэтин (TSL).
Некоторые документы в отношении предыдущего уровня техники предусмотрены по использованию маркеров в качестве средства дифференциальной диагностики респираторных заболеваний, среди них: заявка на патент WO 2012169887 A2 относится к способу прогнозирования степени тяжести SRV, тем не менее, данный документ позволяет работать с маркерами OLFM4, CD177, ММР8, ММР9, РТХ3, IL-8, RANTES и CD4, а также их комбинациями, без указания использования маркеров IL-3, IL-12p40 и IL-33. В настоящем документе не подразумевается, что цитокины IL-33, IL12p40 или IL-3 имеют отношение к пациентам, у которых была обнаружена рецидивирующая бронхиальная обструкция или возможность развития астмы в будущем после заражения инфекцией, вызванной SRV.
В документе ЕР 1867734 А1 представлено описание использования молекулярных маркеров для диагностики и прогнозирования заболеваний. Тем не менее, заболевания, в отношении которых он предусмотрен, относятся к цереброваскулярному типу, он не относится к маркерам для диагностики респираторных заболеваний.
Верхние и нижние части дыхательных путей были проанализированы в ходе нескольких исследований при бронхиолите SRV у грудных детей. Цель настоящего изобретения состоит в раскрытии вариантов использования цитокинов IL-3, IL-12р40 и IL-33, молекулярных маркеров для прогнозирования возникновения рецидивирующей бронхиальной обструкции в будущем (IL-3 и IL12p40) или вероятного развития астмы (IL-33) на более поздних этапах жизни этих грудных детей из-за бронхиолита, вызванного заражением SRV.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
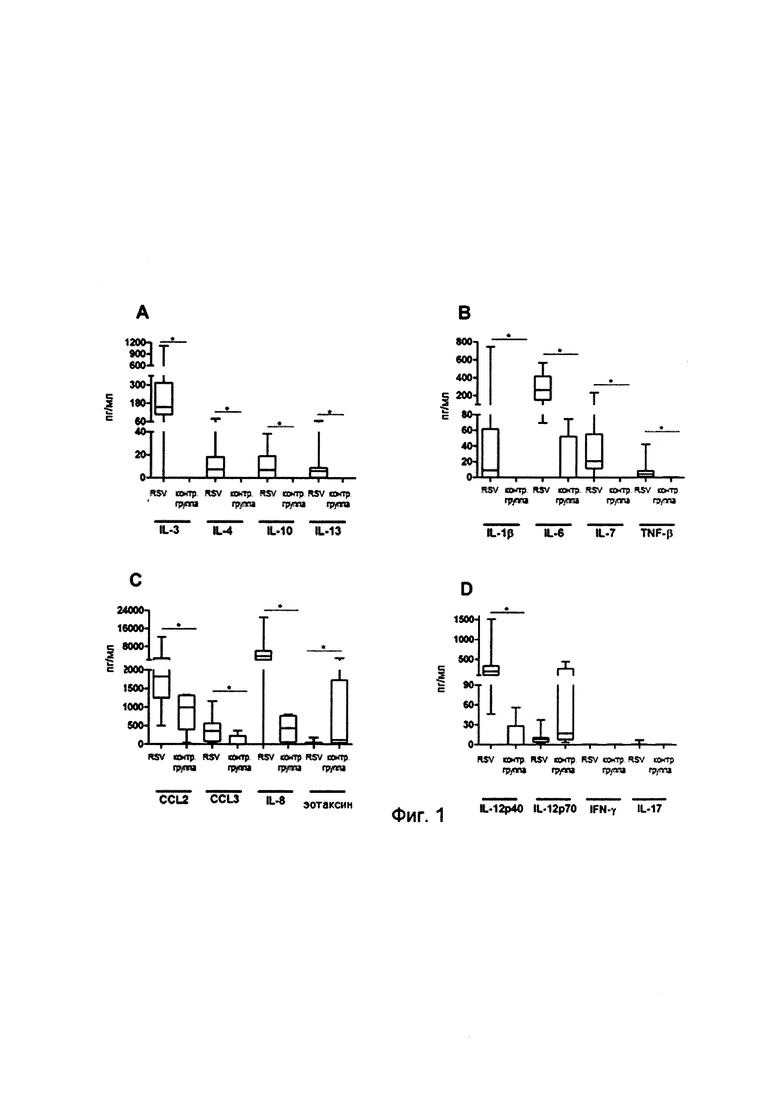
Фиг. 1. На фиг. 1 показан профиль получения цитокинов и хемокинов в жидкостях бронхоальвеолярных выделений (BALF) пациентов, зараженных SRV, по сравнению с контрольными группами. Определялась концентрация цитокинов и хемокинов в BALF грудных детей с бронхиолитом SRV и здоровых грудных детей в качестве контрольной группы, подверженных люминесцентному анализу. Концентрация цитокинов и хемокинов выражается в пг/мл и разделяются по группам согласно их вероятного среднего значения и диапазона их сравнения. Значимость бронхиолита посредством сравнения SRV (N=14) с грудными детьми в контрольной группе (N=5) определена с помощью непараметрического U-критерия Манна-Уитни (*значение Р<0,05 рассматривалось как статистически значимое). Получение IL-3, IL-4, IL-10 и IL-13 (a), IL-1β, IL-6, IL-7 и TNF-β (b), хемокинов CCL2/MCP-1, CCL3/MIP 1α, эотаксина и IL-8 (с), а также IL-12p40, IL-12р70, IFN-γ и EL-17 (d) анализировалось в образцах BALF.
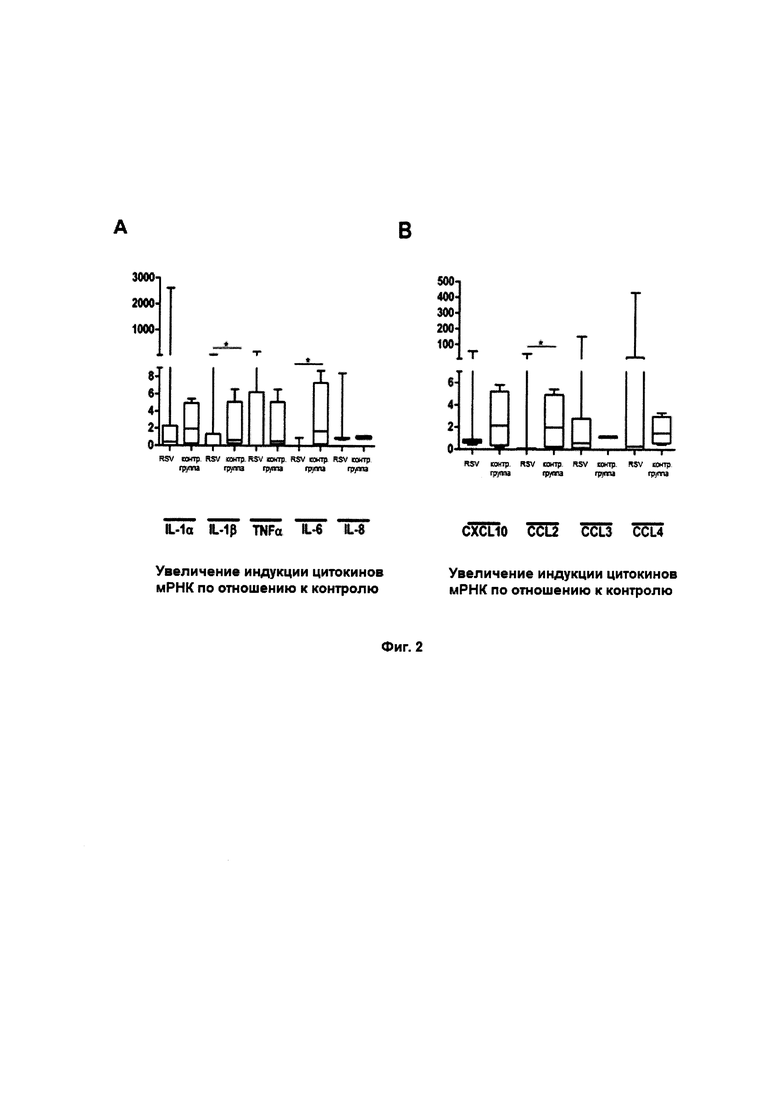
Фиг. 2. На фиг. 2 показаны профили получения цитокинов и хемокинов в образцах носоглоточных аспиратов (NPA) пациентов, зараженных SRV, по сравнению с лицами в контрольной группе. Экспрессия переносчика в NPA грудных детей с бронхиолитом SRV (N=14) сравнивалась с грудными детьми в контрольной группе (N=5) посредством относительного количественного определения (RQ) с помощью линейных разрушаемых зондов в количественной RT-PCR. Использовались специальные линейные разрушаемые зонды для амплификации цитокинов IL-1α, IL-1β, TNFα, IL-6 и IL-8 (а); хемокинов CXCL10, CCL2/MCP-1, CCL3/MIP-1α и CCL4/MIP-1β (b). Относительные концентрации переносчиков были выражены в виде увеличения частоты по отношению к относительной индукции в контрольных группах. Средние и вероятные значения показаны в виде горизонтальной полосы и прямоугольников соответственно (значение Р<0,05 рассматривалось как статистически значимое).
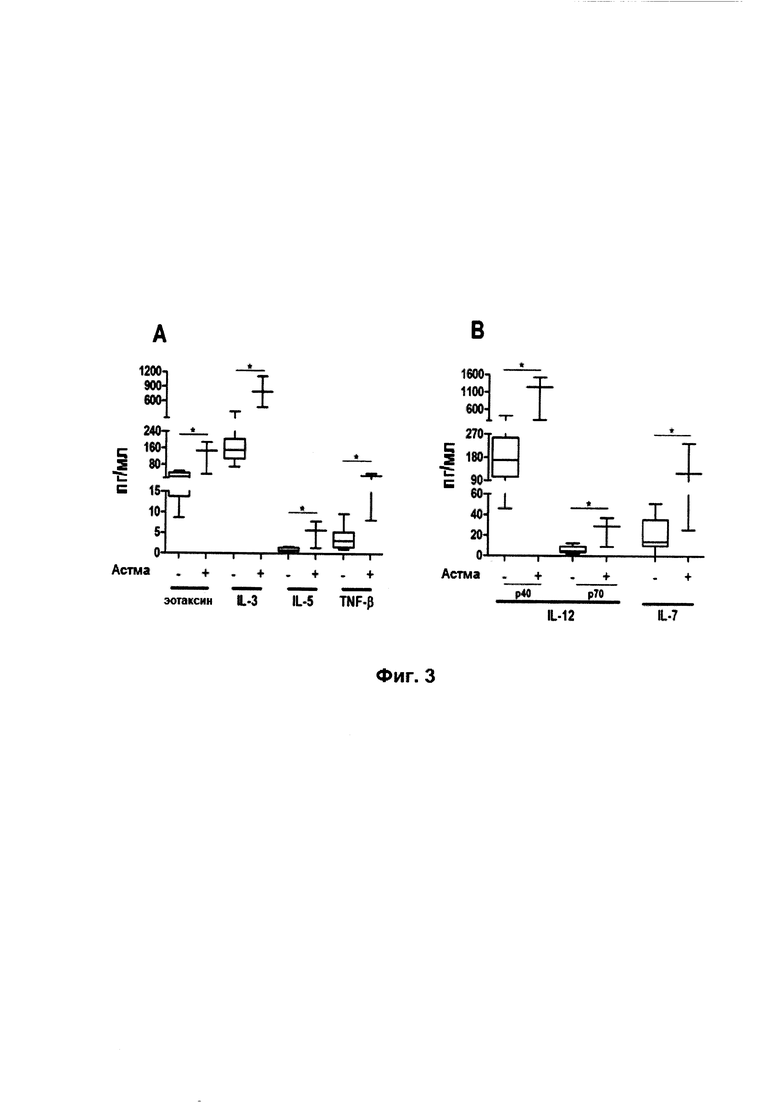
Фиг. 3. На фиг. 3 показано получение цитокинов и хемокинов в образцах BALF грудных детей с бронхиолитом SRV по развитию астмы за период последующего наблюдения. Концентрации цитокинов и хемокинов: Эотаксин, IL-3, IL-5, TNF-β (а) и IL-12p40, IL-12p70 и IL-7 (b), обнаруженные посредством люминесцентного анализа в образцах BALF грудных детей с бронхиолитом, вызванного SRV (N=14), анализировались по развитию астмы за период последующего наблюдения. Концентрации переносчиков выражаются в пг/мл и их средние и вероятные значения показаны в виде горизонтальных полос и прямоугольников соответственно (значение Р<0,05 рассматривалось как статистически значимое).
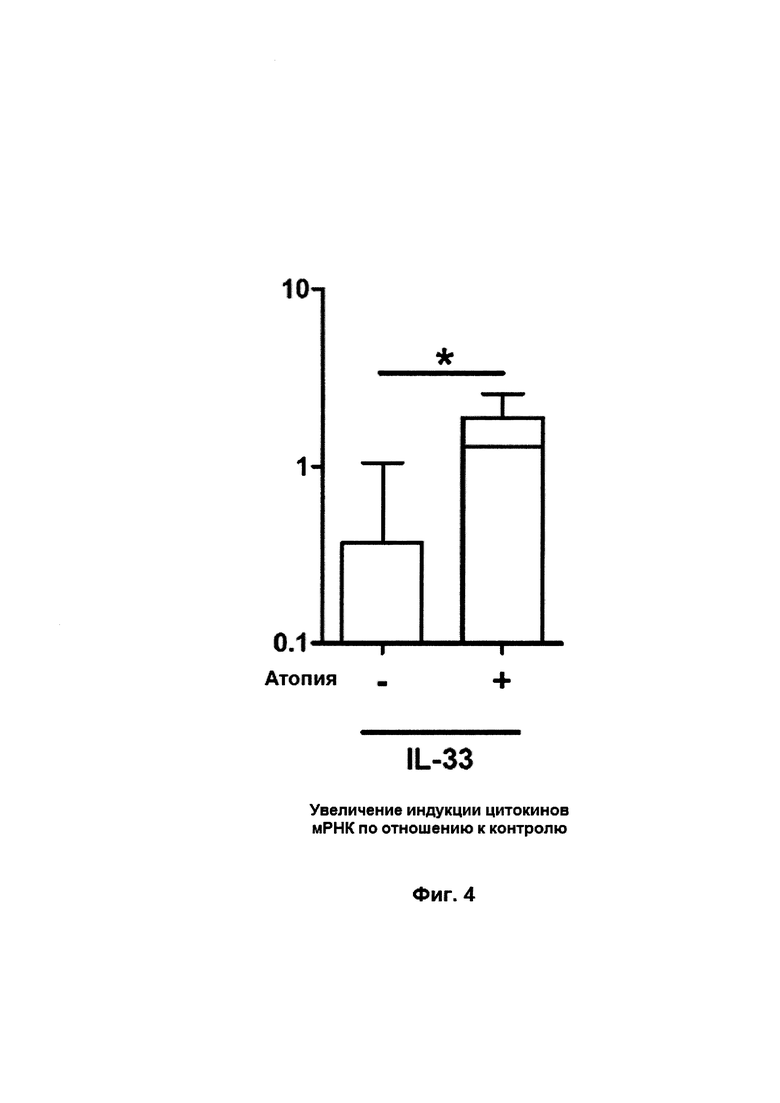
Фиг. 4. На фиг. 4 показано относительное количественное определение мессенджеров ARN IL-33 в носоглоточном аспирате грудных детей с бронхиолитом SRV, проанализированное с учетом случаев атопии в семье. Генная экспрессия IL-33 определялась в носоглоточном аспирате грудных детей с бронхиолитом SRV (N=14) с учетом или без учета случаев атопии в семье. Результаты показаны в виде увеличения частоты посредством относительной индукции контрольных групп. Средние и вероятные значения каждой группы показаны в виде горизонтальных полос и прямоугольников соответственно (значение *Р<0,05 рассматривалось как статистически значимое).
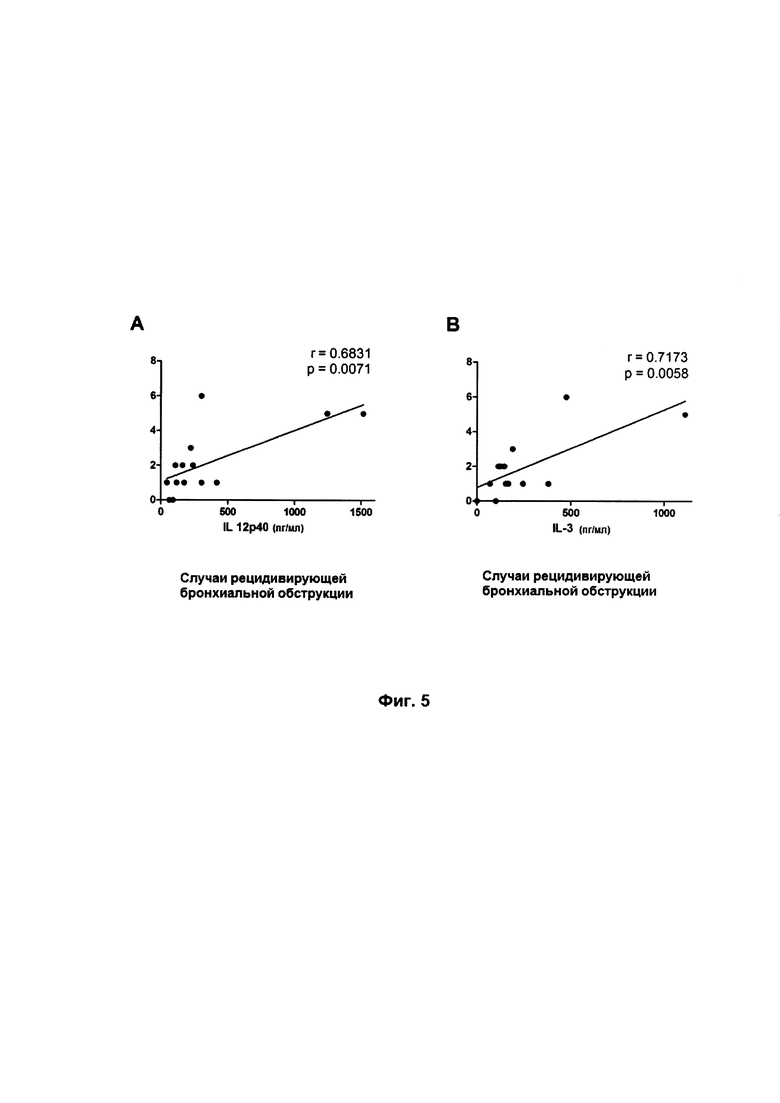
Фиг. 5. На фиг. 5 показана корреляция между IL-12p40 и IL-3 в образцах BALF пациентов, зараженных SRV, с количеством случаев рецидивирующей бронхиальной обструкции. Было установлено, что соответствие корреляция Пирсона между IL-12p40 (а) или IL-3 (b) и случаями рецидивирующей бронхиальной обструкции в образцах BALF грудных детей с SRV (14). Результаты выражаются в пг/мл для цитокинов и количестве случаев за период последующего наблюдения (значение *Р<0,05 рассматривалось как статистически значимое).
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящем изобретении описывается использование молекулярных маркеров IL-3, IL-12p40 и IL-33 в качестве маркеров для прогнозирования рецидивирующей бронхиальной обструкции (IL-3, IL-12p40) и вероятного развития астмы (IL-33) на более поздних этапах жизни этих грудных детей после бронхиолита, вызванного SRV, особенно у пациентов младше 12 месяцев.
Способ прогнозирования тяжести заболевания, вызванного заражением SRV и MPV, включает следующее:
- Амплификацию образцов респираторных секреций с помощью молекулярно-биологической процедуры, например, PCR, используя маркеры IL-3, IL-12p40 и IL-33;
- подсчет посредством способа молекулярного количественного определения, такого как ELISA, сверхэкспрессии последовательности-мишени в дополнение к маркерам IL-3, IL-33 или IL-12p40;
- соотношение на основании количественного определения полученной сверхэкспрессии и развития болезни, вызванной SRV: высокая вероятность развития бронхиальной обструкции, если концентрация в бронхоальвеолярных выделениях превышает 500 пг/мл IL-12p40 или IL-3; высокая вероятность развитие астмы, если концентрация в бронхоальвеолярных выделениях превышает 500 пг/мл IL-33.
ПРИМЕР
Ранее здоровые грудные дети младше 12 месяцев, госпитализированные из-за вирусного бронхиолита, были зарегистрированы в исследовании. Регистрируемые пациенты должны быть положительными по иммунофлуоресценции для SRV и должны быть младше 12 месяцев, при условии отсутствия факторов риска тяжелых заболеваний и с уровнем развития во время первой недели от заболевания легкой степени до средней степени, определенного по клиническим показателям. Грудные дети с хроническими заболеваниями, или получавшие кортикостероиды на момент регистрации, были исключены из исследования. В течение того же периода времени регистрировались здоровые грудные дети, которые подвергались инвазивной процедуре в результате неинфекционного заболевания (паховая грыжа=4; киста щитовидно-язычного протока=1). Образцы таких пациентов использовались в качестве контрольной группы.
Профили цитокина и хемокина оценивались в верхних и нижних дыхательных путях у грудных детей, страдающих от бронхиолита, вызванного заражением SRV. Также учитывались клинические результаты за период последующих трех лет. Носоглоточный аспират и BALF госпитализированных грудных детей в результате бронхиолита SRV и здоровых представителей контрольной группы объединялись и анализировались для обнаружения цитокинов и хемокинов посредством люминесцентного анализа и количественного определения RT-PCR в реальном времени. Вследствие этого оцениваемые уровни цитокинов типа Th2 (IL-3, IL-4, IL-10 и IL-13), провоспалительных цитокинов и хемокинов (IL-1β, IL-6, TNF-β, MCP-1/CCL2, MIP-1α/CCL3 и IL-8) наблюдались в BALF грудных детей с бронхтолитом SRV по сравнению с контрольными группами. Было установлено, что у пациентов, имеющих случаи атопии в семье, вырабатывались уровни IL-33 выше, чем у пациентов, не имеющих таких случаев (фиг. 4). Помимо этого была обнаружена прямая связь уровней IL-3 и IL-12p40 у грудных детей, зараженных SRV, с развитием рецидивирующей бронхиальной обструкции в дальнейшем. Фактически была обнаружена прямая связь между уровнями IL-12p40 и IL-3 в образцах BALF от пациентов, зараженных SRV, с рядом случаев заболевания рецидивирующей бронхиальной обструкцией в период наблюдений (корреляция Пирсона: r=0,68; р=0,0071; r=0,71; р=0,0058 соответственно) (фиг. 5).
В данных результатах подразумевается, что IL-3 и IL-12p40 - молекулярные прогностические параметры в отношении рецидивирующей бронхиальной обструкции, вызываемой SRV у грудных детей с бронхиолитом.
Были привлечены четырнадцать пациентов с бронхиолитом SRV и пять пациентов из контрольной группы. Грудные дети с бронхиолитом SRV были госпитализированы в среднем на период 4,5 дня (диапазон: 1-9 дней) со средним показателем тяжести, равным 4. Перед проведением процедуры всем пациентам была предоставлена возможность пройти кислородную терапию в первые два дня. У них не были обнаружены осложнения из-за процедуры, и они были выписаны в здоровом состоянии. За всеми пациентами осуществлялся контроль в течение трех лет без фактов госпитализации по другим причинам. Ведение контроля за одним пациентом в контрольной группе оказалось невозможным спустя 24 месяца. Оценочные клинические переменные были представлены: рецидивирующей бронхиальной обструкцией по врачебным данным, диагностикой астмы по врачебным данным и длительным применением терапии с кортикостероидами -признаками, между которыми не наблюдалось существенных различий в обеих группах в течение последующих клинических наблюдений. Критические признаки подытожены в таблице 1.
Выделение цитокинов и хемокинов в образцах BALF грудных детей с бронхиолитом SRV.
Уровни концентрации белков цитокинов и хемокинов в образцах BALF грудных младенцев с бронхиолитом SRV в сопоставлении с грудными детьми из контрольной группы измерялись путем люминесцентного анализа. В сравнении с контрольной группой повышенная концентрация наблюдалась в случаях IL-3, IL-4, IL-10, IL-13 (цитокины, относящиеся к Th2); IL-1β, IL-6, TNF-β (противовоспалительные цитокины); MCP-1/CCL2, MIP-1α/CCL3, IL-8 (хемокины); IL-12p40 (цитокины, относящиеся к Th1); и IL-7 (факторы возрастания) в образцах BALF грудных детей с бронхиолитом SRV. Также по сравнению с контрольной группой значительно пониженные показатели концентрации были обнаружены в отношении эотаксина (хемокин) и IL-12p70 в образцах BALF грудных детей с бронхиолитом SRV. Выработка IFN-γ (цитокин, относящийся к Th1) и IL-17 (цитокин, относящийся к Th17), в образцах BALF обнаружена не была ни у зараженных пациентов, ни у здоровых пациентов из контрольной группы (фиг. 1).
В образцах BALF пациентов, зараженных SRV, у которых развилась астма в период наблюдения, были обнаружены высокие показатели концентрации IL-12р40, IL-12p70 (цитокины, относящиеся к Th1), IL-3, IL-5 (цитокины, относящиеся к Th2), TNF-β (противовоспалительный цитокин), эотаксина (хемокин) и IL-7 (фактор возрастания) по сравнению с пациентами из контрольной группы, у которых она не развилась (фиг. 3). Кроме того, в носоглоточном аспирате пациентов с семейной историей атопии, зараженных SRV, наблюдалось существенное увеличение концентрации мессенджера ARN IL-33, приведенной к ГАФДГ, по сравнению с пациентами, у которых она не наблюдалась (фиг. 4).
Изобретение относится к биотехнологии и определению респираторных заболеваний с помощью молекулярных маркеров в качестве средства прогнозирования развития случаев респираторных инфекций. Профиль экспрессии гена молекулярных маркеров может определяться в биологических образцах посредством анализа ELISA, проточной цитометрии или PCR в реальном времени. На основании подтверждения этиологического фактора инфекции вместе с определением профиля молекулярных маркеров IL-3, IL-33 и IL12p40 будет прогнозироваться тяжесть заболевания. 2 н. и 1 з.п. ф-лы, 5 ил., 1 табл., 1 пр.
1. Применение молекулярных маркеров IL-3, IL-12p40 и IL-33, отличающееся тем, что они служат для прогнозирования рецидивирующей бронхиальной обструкции и астмы после бронхиолита, вызванных респираторно-синцитиальным вирусом человека (SRV).
2. Применение по п. 1, отличающееся тем, что одна из респираторных инфекций представлена бронхиолитом.
3. Способ прогнозирования рецидивирующей бронхиальной обструкции и астмы после бронхиолита, вызванных респираторно-синцитиальным вирусом человека (SRV), отличающийся тем, что он включает:
амплификацию и обнаружение маркеров IL-3, IL-12p40 и IL-33 с помощью молекулярно-биологической процедуры, например, PCR и ELISA;
подсчет сверхэкспрессии последовательности-мишени в дополнение к маркерам IL-3, IL-33 или IL-12p40;
соотношение на основании количественного определения полученной сверхэкспрессии и развития болезни, вызванной SRV:
высокая вероятность развития бронхиальной обструкции, если концентрация в бронхоальвеолярных выделениях превышает 500 пг/мл IL-12p40 или IL-3;
высокая вероятность развития астмы, если концентрация в бронхоальвеолярных выделениях превышает 500 пг/мл IL-33.
| Ronan Le Goffic et | |||
| al | |||
| Способ сопряжения брусьев в срубах | 1921 |
|
SU33A1 |
| КОЛЕСНЫЙ ТРАКТОР | 1923 |
|
SU1125A1 |
| Asuncion Mejias et | |||
| al | |||
| Motavizumab, A Neutralizing Anti-Respiratory Syncytial Virus (Rsv) Monoclonal Antibody Significantly Modifies The Local And Systemic Cytokine | |||
Авторы
Даты
2019-11-27—Публикация
2016-07-25—Подача