[0001] Настоящее изобретение относится к способу получения L-метионина ферментативной реакцией между предшественником L-метионина, диметилдисульфидом (DMDS) и органическим соединением-восстановителем. Изобретение относится также к двухстадийному способу получения L-метионина ферментативной реакцией между предшественником L-метионина и метилмеркаптаном, причем метилмеркаптан получают ферментативным гидрогенолизом DMDS.
[0002] Метионин представляет собой одну из незаменимых аминокислот в организме человека и широко применяется в качестве добавки для питания животных. Его применяют также в качестве исходного вещества для фармацевтических препаратов. Метионин выступает в качестве предшественника таких соединений, как холин (лецитин) и креатин. Он является также исходным веществом для синтеза цистеина и таурина.
[0003] S-аденозил-L-метионин (SAM) представляет собой производное соединение L-метионина и вовлечен в синтез различных нейротрансмиттеров в головном мозге. L-метионин и/или SAM ингибирует накопление липидов в организме и улучшает кровообращение в головном мозге, в сердце и в почках. L-метионин может быть использован также для облегчения расщепления, детоксикации и экскреции токсичных веществ или тяжелых металлов, таких как свинец. Он обладает противовоспалительным действием в отношении костей и болезней суставов и также представляет собой существенное питательное вещество для волос, противодействующее их преждевременному и нежелательному выпадению.
[0004] Метионин известен давно и его получают в промышленном масштабе химическими способами исходя из сырья, поступающего от нефтехимических предприятий, соответственно, например, описанию FR 2903690, WO 2008006977, US 2009318715, US 5990349, JP 19660043158 и WO 9408957. Без учета того факта, что эти способы получения не вписываются в процесс экологически перспективного развития, эти химические способы обладают недостатком, состоящим в получении смеси двух энантиомеров L и D в равных частях.
[0005] В литературных источниках были предложены полностью биологические синтезы бактериальной ферментацией с указанием преимущества, состоящего в отсутствии продуцирования L-энантиомера метионина, соответственно, например, описанию WO 07077041, WO 09043372, WO 10020290 и WO 10020681. Тем не менее, отсутствие до настоящего времени промышленной реализации в крупном масштабе позволяет предполагать, что эксплуатационные характеристики и/или себестоимость этих способов остаются неудовлетворительными.
[0006] Компанией "CJ Cheil-Jedang" и заявителем совместно были успешно реализованы в промышленном масштабе смешанные химико-биологические способы, в которых предшественник L-метионина получали бактериальной ферментацией и затем приводили в ферментативное взаимодействие с метилмеркаптаном для получения исключительно L-метионина (см. WO 2008013432 и/или WO 2013029690). В этих, хотя и очень высокопроизводительных, способах требуется осуществлять синтез in situ метилмеркаптана, в котором требуется осуществлять синтез водорода конверсией метана с водяным паром, синтез сероводорода гидрированием серы и синтез метилмеркаптана исходя из метанола и сероводорода, то есть требуется очень значительный парк оборудования, мало сопоставимый при реализации в промышленном масштабе с достаточно небольшим повышением годового производства по сравнению с уже существующим.
[0007] Таким образом, существует потребность в получении L-метионина смешанным способом, в котором парк оборудования, требуемый для синтеза метилмеркаптана, будет меньше, чем в случае синтеза исходя из водорода, сероводорода и метанола. В настоящем изобретении описывается именно этот аспект.
[0008] В настоящем изобретении предлагается на практике заменить метилмеркаптан в технологическом процессе, описанном далее (WO 2008013432 и/или WO 2013029690), диметилдисульфидом (DMDS):

[0009] В данном случае метилмеркаптан (MeSH) используют непосредственно на второй стадии. В настоящем изобретении предлагается заменить метилмеркаптан продуктом ферментативного гидрогенолиза диметилдисульфида на предварительной стадии или комбинировать совокупность реагентов в реакции по "однореакторной технологии", в случае которой из глюкозы и DMDS продуцируется L-метионин.
[0010] Касательно синтеза метилмеркаптана исходя из диметилдисульфида представленные далее элементы можно найти на предшествующем уровне техники.
[0011] В EP 0649837 предложен способ синтеза метилмеркаптана каталитическим гидрогенолизом с сульфидами переходных металлов исходя из диметилдисульфида с водородом. В этом способе, хотя и являющимся эффективным, требуются относительно высокие температуры около 200°C для достижения производительности, представляющей интерес в промышленном масштабе.
[0012] Специалистам в данной области техники известно также, что метилмеркаптан можно получать подкислением водного раствора метилмеркаптида натрия (CH3SNa). У этого способа имеется большой недостаток, состоящий в образовании большого количества солей, таких как хлорид натрия или сульфат натрия, в зависимости от того, применяют ли соляную или серную кислоту. Образующиеся водные солевые растворы часто очень трудно поддаются переработке, а остаточные количества веществ со зловонным запахом делают этот способ трудно реализуемым в промышленном масштабе.
[0013] К настоящему времени было найдено, что метилмеркаптан можно получать ферментативным восстановлением диметилдисульфида (DMDS) на предварительной стадии синтеза L-метионина, и неожиданным образом было найдено также, что это ферментативное восстановление DMDS можно осуществлять в ходе синтеза L-метионина.
[0014] Таким образом, целью настоящего изобретения является способ получения L-метионина, аналогичный способу, предложенному в международных заявках WO 2008013432 и/или WO 2013029690, и позволяющий отказаться от манипуляций с метилмеркаптаном или по меньшей мере уменьшить их объем, генерируя метилмеркаптан по реакции ферментативного катализа DMDS непосредственно перед использованием этого метилмеркаптана в синтезе метионина или генерируя метилмеркаптан по реакции ферментативного катализа DMDS in situ в реакторе синтеза L-метионина.
[0015] В частности, первой целью настоящего изобретения является способ получения L-метионина, который включает по меньшей мере стадии:
a) получения смеси, содержащей:
1) диметилдисульфид (DMDS);
2) каталитическое количество аминокислоты, содержащей тиольную группу, или пептида с тиольной группой;
3) каталитическое количество фермента, катализирующего реакцию восстановления дисульфидного мостика аминокислоты, содержащей тиольную группу, или пептида с тиольной группой;
4) органическое соединение-восстановитель в стехиометрическом количестве по отношению к дисульфиду, в частности DMDS;
5) каталитическое количество фермента, катализирующего реакцию дегидрирования указанного органического соединения-восстановителя;
6) каталитическое количество кофактора, являющегося общим для обоих ферментов каталитической системы (дегидрогеназы и редуктазы);
b) осуществления ферментативной реакции для получения метилмеркаптана (CH3SH);
c) введения предшественника L-метионина и взаимодействия этого предшественника с метилмеркаптаном, образовавшимся на стадии b), и
d) выделения и в случае необходимости очистки образовавшегося L-метионина.
[0016] Компоненты, указанные на стадии a), могут быть введены в любом порядке (порядок введения на стадии a) не является строгим). В варианте осуществления настоящего изобретения аминокислота, содержащая тиольную группу, и/или пептид, содержащий тиольную группу, может находиться в форме дисульфида этой аминокислоты и/или этого пептида соответственно, например глутатион может находиться в форме дисульфида глутатиона.
[0017] В общем случае, фермент, катализирующий восстановление дисульфидного мостика, образованного между двумя остатками аминокислоты, содержащей тиольную группу, или пептида с тиольной группой, представляет собой редуктазу. Термин "редуктаза" в дальнейшем описании употребляют для пояснения настоящего изобретения. Аналогичным образом, фермент, катализирующий дегидрирование органического соединения-восстановителя, используемого на стадии b), в общем случае называют дегидрогеназой, причем в дальнейшем описании для пояснения настоящего изобретения употребляют термин "дегидрогеназа".
[0018] Среди кофакторов, являющихся общими для обоих ферментов, катализирующих восстановление и дегидрирование, (редуктазы и дегидрогеназы) в качестве неограничительных примеров можно назвать флавиновые кофакторы и никотиновые кофакторы. Предпочтительно применяют никотиновые кофакторы и более предпочтительно никотинамидадениндинуклеотид (NAD) или еще более предпочтительно никотинамидадениндинуклеотидфосфат (NADPH). Перечисленные кофакторы преимущественно применяют в их восстановленных формах (например, NADPH, H+) и/или окисленных формах (например, NADP+), то есть они могут быть прибавлены к реакционной смеси в этих восстановленных и/или окисленных формах.
[0019] Организация и порядок введения компонентов с 1) по 6) на стадии a) могут быть реализованы различным образом. Ферментативную реакцию на стадии b) инициируют прибавлением одного из компонентов каталитической системы к смеси на стадии a): фермента или одного из соединений, вводимых в стехиометрическом количестве (дисульфида или органического соединения-восстановителя), или одного из соединений, вводимых в каталитическом количестве (аминокислоты, содержащей тиольную группу, или пептида с тиольной группой, или дисульфида, соответствующего указанному тиолу или пептиду, или также кофактора).
[0020] Таким образом, согласно одному из вариантов осуществления настоящего изобретения, способ получения L-метионина включает по меньшей мере стадии:
a') получения смеси, содержащей:
- диметилдисульфид (DMDS);
- каталитическое количество аминокислоты, содержащей тиольную группу, или пептида с тиольной группой;
- каталитическое количество редуктазы, соответствующей аминокислоте, содержащей тиольную группу, или пептиду с тиольной группой;
- каталитическое количество NADPH;
b') введения органического соединения-восстановителя в стехиометрическом количестве по отношению к диметилдисульфиду с каталитическим количеством соответствующей дегидрогеназы;,
c') осуществления ферментативной реакции для получения метилмеркаптана (CH3SH);
d') взаимодействия предшественника L-метионина с метилмеркаптаном, образовавшимся на стадии c'), и
e') выделения и в случае необходимости очистки образовавшегося L-метионина.
[0021] Согласно способу по настоящему изобретению метилмеркаптан, в общем случае образующийся в газообразном состоянии, непосредственно приводят в контакт с предшественником метионина соответственно дальнейшему описанию.
[0022] Способ синтеза L-метионина по настоящему изобретению прежде всего основан на ферментативном восстановлении диметилдисульфида органическим соединением-восстановителем, представляющим собой донор атомов водорода, а также, как будет определено далее, на представленной далее реакции с применением глюкозы в качестве органического соединения-восстановителя (донора атомов водорода):
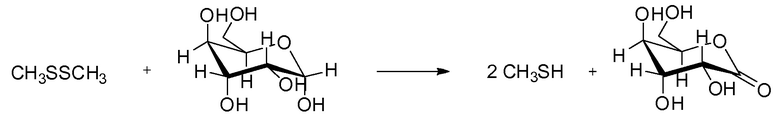
DMDS Глюкоза MeSH Глюконолактон
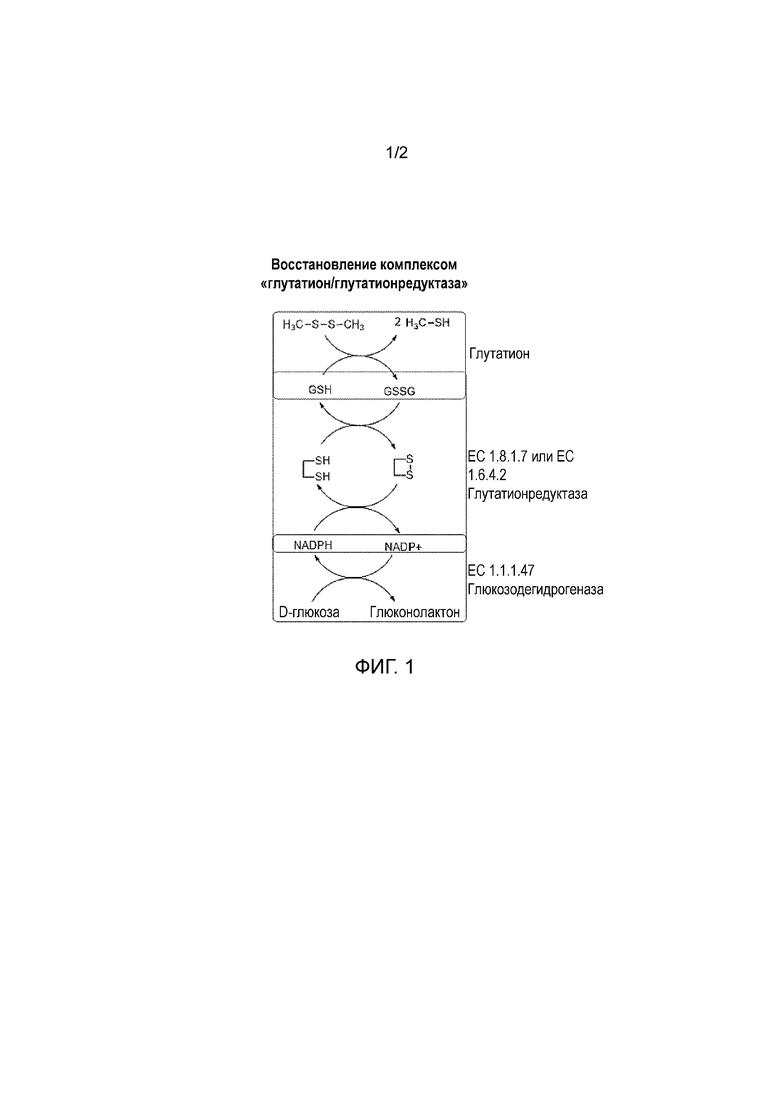
[0023] К настоящему времени было найдено, что эта реакция легко катализируется ферментативной системой, в которую входит аминокислота с тиольной группой или пептид с тиольной группой, например глутатион, в форме комплекса "(аминокислота или пептид)/соответствующая редуктаза", регенерируемого органическим соединением, являющимся донором атомов водорода, соответственно приведенному далее описанию фиг. 1.
[0024] Таким образом, согласно пояснению фиг. 1 пептид (показан глутатион) восстанавливает дисульфид (показан DMDS) до меркаптана (показан метилмеркаптан), превращаясь в пептид с дисульфидным мостиком (показан дисульфид глутатиона). Редуктаза как фермент (показана глутатионредуктаза, EC 1.8.1.7 или EC 1.6.4.2) регенерирует пептид (глутатион), окисляя при этом кофактор (показан "NADPH, H+"). При этом окисленная форма (показана "NADP+") восстанавливается посредством окислительно-восстановительного ферментативного комплекса, называемого комплексом "рециклинга", хорошо известного специалистам в данной области техники и содержащего соответствующую дегидрогеназу (показана глюкозодегидрогеназа с примером номера по классификации ферментов EC 1.1.1.47), и органического соединения-восстановителя (показана глюкоза). При этом получают окисленную форму органического соединения-восстановителя (показан глюконолактон).
[0025] В частности, пептид (в примере показан глутатион) восстанавливает диметилдисульфид до метилмеркаптана, превращаясь в пептид с дисульфидным мостиком (показан дисульфид глутатиона). Редуктаза как фермент (показана глутатионредуктаза, EC 1.8.1.7 или EC 1.6.4.2) восстанавливает пептид (глутатион), и этот же фермент регенерируется окислительно-восстановительным ферментативным комплексом, хорошо известным специалистам в данной области техники, например комплексом "NADPH/NADP+" (никотинадениндинуклеотидфосфатом (в восстановленной и окисленной форме)). В свою очередь NADP+ восстанавливается до NADPH посредством дегидрогеназы, соответствующей используемому органическому соединению-восстановителю (в данном случае посредством глюкозодегидрогеназы, EC 1.1.1.47), благодаря указанному органическому соединению-восстановителю (показана глюкоза), которое поставляет водород (является донором атомов водорода), превращаясь в свою окисленную форму (в данном случае в глюконолактон).
[0026] Согласно более предпочтительному варианту осуществления система "глутатион/дисульфид глутатиона", ассоциированная с глутатионредуктазой, позволяет согласно настоящему изобретению восстанавливать DMDS до метилмеркаптана.
[0027] Глутатион представляет собой трипептид, широко применяемый в биологии. Это соединение в восстановленной (глутатион) или окисленной (дисульфид глутатиона) форме образует окислительно-восстановительную пару, имеющую важное значение в клетках. В частности, глутатион является жизненно важным для обезвреживания тяжелых металлов в организме. Так, например, в WO 05107723 описана композиция, в которой глутатион применяют для получения хелатирующего препарата, в US 4657856 указано, что глутатион позволяет также разрушать пероксиды за счет глутатионпероксидазы, например превращать H2O2 в H2O. Наконец, глутатион позволяет также разрушать дисульфидные мостики, содержащиеся в белках (Rona Chandrawati, "Triggered Cargo Release by Encapsulated Enzymatic Catalysis in Capsosomes", Nano Lett, (2011), vol. 11, 4958-4963).
[0028] Согласно способу по настоящему изобретению каталитическое количество аминокислоты, содержащей тиольную группу, или пептида с тиольной группой, применяют для получения метилмеркаптана исходя из диметилдисульфида.
[0029] Среди аминокислот, содержащих тиольную группу и приемлемых для применения в способе по настоящему изобретению, в качестве неограничительных примеров можно назвать цистеин и гомоцистеин. Используемые ферментативные окислительно-восстановительные системы, которые могут регенерировать каталитический цикл таким образом, в этом случае представляют собой системы "цистеин/цистеинредуктаза" (EC 1.8.1.6) и "гомоцистеин/гомоцистеинредуктаза".
[0030] Предпочтительным может быть вариант использования гомоцистеина, поскольку эта аминокислота может быть получена исходя из OAHS (предшественника L-метионина), сероводорода (H2S) и метионинового фермента, то есть фермента, катализирующего реакцию, ведущую к образованию метионина. Таким образом, очень малое количество H2S в реакционной смеси создает in situ цикл, эквивалентный циклу с глутатионом.
[0031] Среди пептидов, содержащих тиольную группу и приемлемых для применения в способе по настоящему изобретению, в качестве неограничительных примеров можно назвать глутатион и тиоредоксин. Таким образом, система "глутатион/глутатионредуктаза", описанная ранее, может быть заменена системой "тиоредоксин (CAS № 52500-60-4)/тиоредоксинредуктаза (EC 1.8.1.9 или EC 1.6.4.5)".
[0032] Глутатион и система "глутатион/глутатионредуктаза" являются наиболее предпочтительными по настоящему изобретению по причине легкости обеспечения этими соединениями и их стоимости.
[0033] Среди органических соединений-восстановителей, которые могут быть использованы в рамках настоящего изобретения, наиболее предпочтительны соединения, являющиеся донорами атомов водорода, в числе которых наиболее приемлемые соединения представляют собой органические соединения-восстановители, являющиеся донорами атомов водорода и содержащие гидроксигруппы, такие как спирты, полиолы, сахара и другие соединения.
[0034] Применяемый фермент представляет собой фермент, способный дегидрировать соединение-донор атомов водорода, например алкогольдегидрогеназу. Глюкоза представляет собой сахар, особенно приемлемый для применения в способе по настоящему изобретению с глюкозодегидрогеназой для получения глюконолактона.
[0035] Согласно способу по настоящему изобретению в случае, когда ферментативное восстановление DMDS осуществляют в реакторе, отделенном от синтеза L-метионина, в стехиометрическом количестве используют только глюкозу, а все другие компоненты (глутатион, кофактор (например, NADPH) и оба фермента) используют в каталитическом количестве. В случае, когда реакцию ферментативного восстановления DMDS осуществляют совместно с синтезом L-метионина в одном реакторе, называемом реактором "однореакторной технологии", предшественник L-метионина также вводят в стехиометрическом количестве, в то время как дополнительные реагенты этого синтеза, такие как пиридоксальфосфат (PLP) и специфический для этой реакции фермент, вводят в каталитических количествах.
[0036] Значения концентраций пиридоксальфосфата и фермента, являющегося специфическим для предпочтительных предшественников, можно найти в международных заявках WO 2008013432 и/или WO 2013029690.
[0037] Преимущества, обеспечиваемые синтезом с ферментативным катализом метилмеркаптана исходя из диметилдисульфида, превосходят преимущества, обеспечиваемые способом с двумя последовательными стадиями или способом по "однореакторной технологии". Среди этих преимуществ можно назвать возможность работать с водным или водно-органическим раствором в очень мягких условиях по температуре и давлению и при значении pH, близком к нейтральному. Все эти условия типичны для способа, называемого "зеленым" или "экологически перспективным", и полностью совместимы с получением L-метионина соответственно описанию международных заявок WO 2008013432 и/или WO 2013029690.
[0038] Другое преимущество в случае, когда в способе используют диметилдисульфид, состоит в том, что образующийся метилмеркаптан, который в условиях реакции находится в газообразном состоянии, выходит из реакционной смеси по мере своего образования. Следовательно, метилмеркаптан может быть непосредственно использован после выхода из реактора в синтезе L-метионина соответственно, например, описанию WO 2008013432 и/или WO 2013029690, то есть исходя, например, из O-ацетилгомосерина или O-сукцинилгомосерина и ферментов, таких как O-ацетилгомосеринсульфгидрилаза или O-сукцинилгомосеринсульфгидрилаза соответственно.
[0039] Метилмеркаптан также может быть легко сжижен способами техники низких температур, например, при необходимости выделить его. В случае необходимости можно ускорять его выход из реакционной смеси, вводя барботированием с небольшим расходом инертный газ, преимущественно азот.
[0040] Уходящие газы, содержащие азот и метилмеркаптан, в случае потребности и в случае необходимости могут быть возвращены в первый реактор (ферментативное восстановление DMDS) после прохождения через второй реактор (синтез L-метионина), если метилмеркаптан не полностью превратился в L-метионин. Следовательно, способ по настоящему изобретению представляет собой способ синтеза L-метионина на двух последовательных ферментативных стадиях исходя из предшественника L-метионина и DMDS.
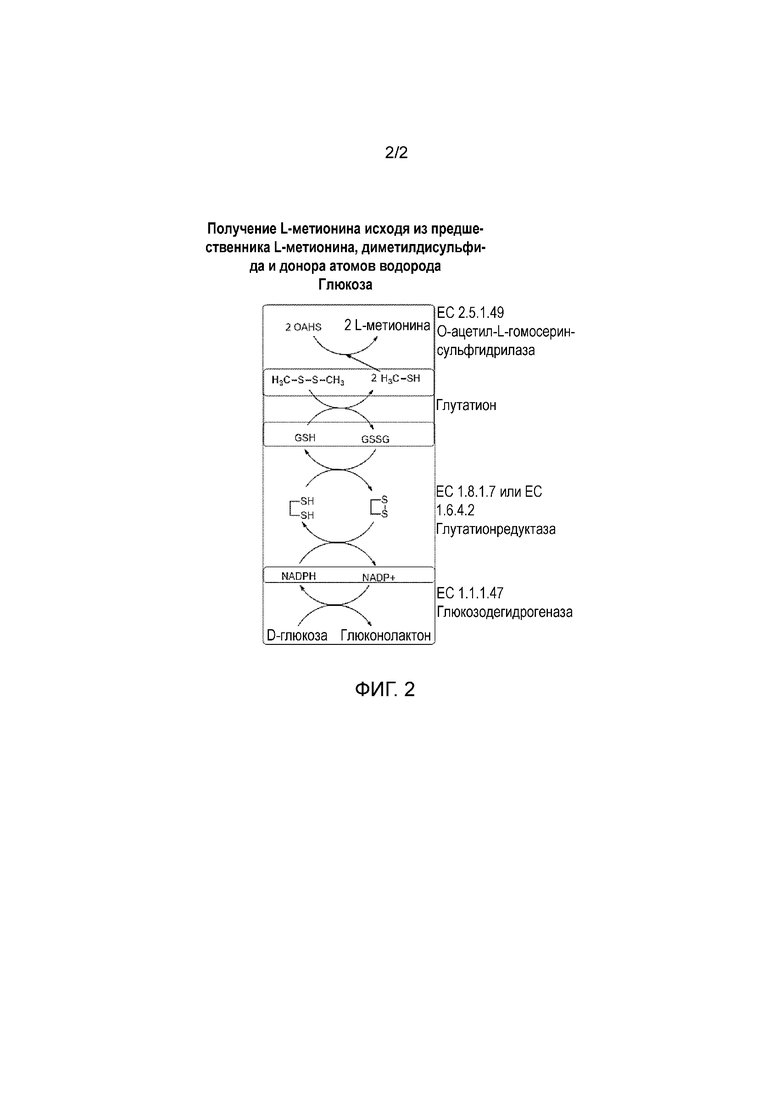
[0041] Также можно осуществлять синтез L-метионина в одном и том же реакторе. В этом случае к системе ферментативного восстановления DMDS (см. указанную ранее стадию a)) прибавляют все реагенты, необходимые для синтеза L-метионина, и закрывают реактор для избежания выброса метилмеркаптана, образующегося при ферментативном восстановлении DMDS in situ. При этом метилмеркаптан взаимодействует с предшественником L-метионина с образованием L-метионина. Таким образом, способ по настоящему изобретению представляет собой способ прямого синтеза L-метионина исходя из предшественника L-метионина и DMDS соответственно показанному на приведенной далее фиг. 2, на которой показан синтез исходя из OAHS, DMDS и глюкозы.
[0042] Диметилдисульфид (DMDS) может быть получен в другом месте исходя из метилмеркаптана и окислителя, такого как, например, кислород, сера или пероксид водорода, или также исходя из диметилсульфата и дисульфида натрия. DMDS может поступать также из смеси под названием "DiSulfide Oils" (DSO, дисульфидные масла), очищенной, например, перегонкой с реагентной обработкой соответственно описанию заявки WO 2014033399.
[0043] Восстановление ферментативным катализом DMDS может рассматриваться как способ, позволяющий избегать транспортировки метилмеркаптана от места его получения по существующим промышленным коммуникациям к месту его использования, если места являются разными. На практике, метилмеркаптан при комнатной температуре представляет собой токсичный газ с сильным зловонным запахом, что чрезвычайно усложняет его транспортировку, в настоящее время очень строго регламентированную в отличие от DMDS. Таким образом, DMDS может быть использован для получения метилмеркаптана непосредственно по месту его применения в синтезе L-метионина с уменьшением таким образом недостатков, связанных с токсичностью и запахом этого соединения, а также промышленных рисков, связанных с этим.
[0044] В случае способа синтеза, осуществляемого на двух последовательных стадиях, причем DMDS потребляется в реакции, а метилмеркаптан выходит из реакционной смеси по мере своего образования, при условии подачи в непрерывном режиме глюкозы и DMDS в реакционной смеси накапливается только продукт дегидрирования органического соединения-восстановителя, например глюконолактон. Когда концентрация глюконолактона превышает значение насыщения в условиях реакции, он осаждается и затем может быть выделен из реакционной смеси любым средством, известным специалистам в данной области техники.
[0045] Глюконолактон может быть использован во множестве вариантов применения. Его, например, используют в качестве пищевой добавки, известной под идентификатором E575. Глюконолактон гидролизуется в кислой водной среде с образованием глюконовой кислоты, также используемой в качестве пищевой добавки (E574). Глюконолактон используют также для производства тофу (см. CN 103053703) для пищевой промышленности.
[0046] Глюконолактон предпочтительно и преимущественно тогда, когда он представляет собой "отход" способа по настоящему изобретению, может заменять глюкозу в возможной реакции ферментации для получения как биоэтанола, так и любого другого соединения, получаемого ферментацией сахара или крахмала.
[0047] Действительно, некоторые бактерии при ферментации могут использовать глюконолактон в качестве источника углерода, что описано в публикации J.P. van Dijken "Novel pathway for alcoholic fermentation of gluconolactone in the yeast Saccharomyces bulderi, J. Bacteriol., (2002), Vol. 184(3), 672-678".
[0048] Очевидное преимущество глюконолактона в способе по настоящему изобретению состоит в возврате его в синтез предшественника L-метионина. Действительно, поскольку рассматриваемый синтез представляет собой бактериальную ферментацию с использованием глюкозы, то глюконолактон может легко заменить часть глюкозы. Этот возврат в этих условиях может давать весьма значительное экономическое преимущество.
[0049] Даже в случае, когда реакцию осуществляют в условиях "однореакторной технологии", указанных ранее, и при этом глюконолактон является значительно более растворимым, чем L-метионин, разделение реакционной смеси легко осуществить традиционными способами, хорошо известными специалистам в данной области техники.
[0050] В способе по настоящему изобретению могут быть использованы также другие сахара, например, можно заменить систему "глюкоза/глюконолактон/глюкозодегидрогеназа" системой "глюкозо-6-фосфат/6-фосфоглюконо-5-лактон/глюкозо-6-фосфатдегидрогеназа" (EC 1.1.1.49).
[0051] В способе по настоящему изобретению также можно использовать спирт вместо сахара и, таким образом, вместо системы "глюкоза/глюконолактон/глюкозодегидрогеназа" можно использовать общую систему "спирт/кетон или альдегид/алкогольдегидрогеназа" (EC 1.1.1) и более предпочтительно систему "изопропанол/ацетон/изопропанолдегидрогеназа" (EC 1.1.1.80).
[0052] Действительно, эта система позволяет получать исходя из DMDS и изопропанола смесь, образованную метилмеркаптаном (MeSH) и ацетоном и выходящую из реакционной смеси (в которой, следовательно, не происходит накопление ни одного соединения). MeSH и ацетон в случае необходимости могут быть легко разделены простой перегонкой.
[0053] Согласно одному из вариантов осуществления в способ по настоящему изобретению входит получение метилмеркаптана ферментативным восстановлением DMDS и затем осуществление реакции образовавшегося метилмеркаптана с предшественником L-метионина для получения L-метионина. В этом случае способ по настоящему изобретению включает по меньшей мере следующие стадии:
стадия 1: получение предшественника L-метионина, например, бактериальной ферментацией глюкозы (см. WO 2008013432 и/или WO 2013029690);
стадия 2: ферментативное восстановление DMDS в реакторе R1 с образованием метилмеркаптана, выходящего из реактора R1 (что соответствует указанным ранее стадиям с a') по c'));
стадия 3: ферментативный синтез L-метионина в реакторе R2 исходя из предшественника со стадии 1 и метилмеркаптана со стадии 2 (что соответствует указанной ранее стадии d'));
стадия 4 (в случае необходимости): возврат глюконолактона, образовавшегося на стадии 3, на стадию 1;
стадия 5: выделение и в случае необходимости очистка образовавшегося L-метионина (что соответствует указанной ранее стадию e')).
[0054] Описание условий, приемлемых для стадии 1, можно найти в международных заявках WO 2008013432 и/или WO 2013029690.
[0055] Температура осуществления реакции на стадии 2 находится в интервале от 10 до 50°C, предпочтительно от 15 до 45°C и более предпочтительно от 20 до 40°C.
[0056] Значение pH реакционной смеси может находиться в интервале от 6 до 8 и предпочтительно от 6,5 до 7,5. Значение pH реакционной смеси может быть установлено посредством буферного раствора. Наиболее предпочтительно следует выбирать, например, значение pH фосфатного буферного раствора с концентрацией 0,1 моль·л-1, равное 7,3.
[0057] Давление, устанавливаемое при осуществлении реакции, может находиться в интервале от давления ниже атмосферного до давления в несколько бар (в несколько сотен кПа) в зависимости от используемых реагентов и материалов. Пониженное давление на практике может обеспечивать более быстрое выделение в газообразном виде образующегося метилмеркаптана, но обладает недостатком, состоящим в увеличении давления насыщенных паров воды и DMDS, загрязняющих образующийся метилмеркаптан в несколько большем количестве. Предпочтительно может быть установлено давление в интервале от атмосферного до давления 20 бар (2 МПа) и наиболее предпочтительно следует работать при давлении в интервале от атмосферного до давления 3 бар (300 кПа).
[0058] Касательно идеальных условий на стадии 3 можно сослаться на международную заявку WO 2013029690 с возможной разницей, состоящей в подаче азота в реактор R1 с последующим направлением в реактор R2 и возврате газов из реактора R2 в реактор R1 при требуемом давлении, если метилмеркаптан не полностью прореагировал в реакторе R2.
[0059] Согласно другой модели (другому варианту) реализации способ по настоящему изобретению осуществляют в одном и том же реакторе (по "однореакторной технологии") и в этом случае он включает по меньшей мере следующие стадии:
стадия 1': получение предшественника L-метионина бактериальной ферментацией, например, глюкозы (аналогично указанной ранее стадии 1);
стадия 2': ферментативное восстановление DMDS в реакторе R1 с образованием in situ метилмеркаптана и совместный ферментативный синтез L-метионина в том же самом реакторе исходя из предшественника, полученного на стадии 1';
стадия 3' (в случае необходимости): возврат глюконолактона, образовавшегося на стадии 2, на стадию 1, и
стадия 4': выделение и в случае необходимости очистка образовавшегося L-метионина.
[0060] Описание условий, приемлемых для стадии 1', можно найти в международных заявках WO 2008013432 и/или WO 2013029690.
[0061] Для стадии 2' рабочие условия приведены далее.
[0062] Температура осуществления реакции находится в интервале от 10 до 50°C, предпочтительно от 15 до 45°C и более предпочтительно от 20 до 40°C.
[0063] Значение pH реакционной смеси преимущественно находится в интервале от 6 до 8 и предпочтительно от 6,2 до 7,5. Наиболее предпочтительно реакцию осуществляют при значении pH фосфатного буферного раствора с концентрацией 0,2 моль·л-1, равном 7,0.
[0064] Способ предпочтительно осуществляют при давлении в интервале от атмосферного до давления 20 бар (2 МПа) и наиболее предпочтительно при давлении в интервале от атмосферного до давления 3 бар (300 кПа).
[0065] Молярное соотношение "DMDS/предшественник L-метионина" находится в интервале от 0,1 до 10 и в общем случае от 0,5 до 5, при этом молярное соотношение предпочтительно соответствует стехиометрическому соотношению (молярное соотношение=0,5), но может иметь большее значение, если это оказывает положительное влияние на кинетику реакции.
[0066] Согласно тому или иному варианту по настоящему изобретению способ может быть осуществлен в периодическом или непрерывном режиме в стеклянном или металлическом реакторе при заданных рабочих условиях и применяемых реагентах.
[0067] Согласно тому или иному варианту способа по настоящему изобретению идеальное молярное соотношение "органическое соединение-восстановитель/DMDS" соответствует стехиометрическому соотношению (молярное соотношение=1), но может изменяться от 0,01 до 100, если специалистами в данной области техники будет замечена какая-либо необходимость, например, в том, чтобы DMDS вводить в непрерывном режиме, а органическое соединение-восстановитель вводить в реактор при пуске. Это молярное соотношение предпочтительно выбирают в интервале от 0,5 до 5 относительно совокупности реакционной смеси в целом.
[0068] Компоненты, содержащиеся в каталитическом количестве в смеси, полученной на указанной ранее стадии a), (аминокислота, содержащая тиольную группу, или пептид с тиольной группой, или также дисульфид, соответствующий указанной аминокислоте, или дисульфид, соответствующий указанному пептиду, редуктаза, дегидрогеназа, кофактор (например, NADPH)) могут быть без затруднений приобретены в коммерческой сети или получены способами, хорошо известными специалистам в данной области техники. Эти компоненты могут находиться в твердом или жидком виде и в порядке особого преимущества могут быть растворены в воде для использования в способе по настоящему изобретению. Применяемые ферменты также могут быть привиты к подложке (в случае ферментов, нанесенных на подложку).
[0069] Водный раствор ферментативного комплекса, содержащего аминокислоту или пептид, также может быть реализован способами, известными специалистам в данной области техники, например, пропиткой клеток, которые могут содержать эти компоненты. Этот водный раствор, состав которого представлен в приведенном далее примере 1, может быть использован с содержанием по массе в интервале от 0,01 до 20% по отношению к общей массе реакционной смеси. Предпочтительно может быть принято содержание в интервале от 0,5 до 10%.
[0070] Настоящее изобретение можно лучше понять при чтении приведенных далее примеров, которые не ограничивают объем патентной охраны настоящего изобретения.
ПРИМЕР 1. Способ с 2 последовательными стадиями
[0071] В реакторе R1, содержавший 150 мл фосфатного буферного раствора с концентрацией 0,1 моль/л и pH=7,30, вносили 10 мл ферментативного комплекса с глутатионом (Aldrich) и 19,2 г (0,1 моль) глюкозы. Раствор ферментативного комплекса содержал 185 мг (0,6 ммоль) глутатиона, 200 ед. глутатионредуктазы, 50 мг (0,06 ммоль) NADPH и 200 ед. глюкозодегидрогеназы. Реакционную смесь доводили до 25°C при механическом перемешивании. Первый отбор проб осуществляли в момент времени t=0. Далее диметилдисульфид (9,4 г, 0,1 моль) вносили в бюретку и вводили по каплям в реактор, при этом реакция начиналась сразу. В реактор подавали поток азота.
[0072] Анализ способом газовой хроматографии выходящих из реактора газов показал по существу только присутствие азота и метилмеркаптана (и следовое количество воды). Эти уходящие газы направляли в реактор R2. DMDS вводили в реактор R1 в течение 6 часов. Конечный анализ способом газовой хроматографии реакционной смеси из реактора R1 подтвердил отсутствие DMDS, а анализ способом СВЭЖХ/МС показал наличие следового количества глюкозы и присутствие почти исключительно глюконолактона (и следового количества глюконовой кислоты).
[0073] Параллельно во второй реактор R2, содержавший 75 мл фосфатного буферного раствора с концентрацией 0,1 моль·л-1 и pH=6,60, вводили 5 г O-ацетил-L-гомосерина (OAHS) (O-ацетилгомосерин был синтезирован исходя из L-гомосерина и уксусного ангидрида согласно публикации Sadamu Nagai "Synthesis of O-acetyl-L-homoserine, Academie Press, (1971), vol. 17, p. 423-424"). Раствор доводили до 35°C при механическом перемешивании.
[0074] Перед началом реакции осуществляли отбор (t=0) 1 мл реакционной смеси. Раствор пиридоксальфосфата (1,6 ммоль, 0,4 г) и O-ацетил-L-гомосеринсульфгидрилазы (0,6 г) растворяли в 10 мл воды и затем вносили в реактор.
[0075] Метилмеркаптан вводили в реактор R1 по ходу реакции, подавая с потоком азота. Реакция начиналась сразу. Образование L-метионина и исчезновение OAHS контролировали способом ВЭЖХ. Газы, уходящие из реактора R2, улавливали 20%-м водным раствором едкого натра (гидроксида натрия). Анализы показали, что 52% OAHS было превращено в L-метионин, а избыток DMDS был превращен в метилмеркаптан, обнаруженный в ловушке с гидроксидом натрия.
ПРИМЕР 2. Способ по "однореакторной технологии"
[0076] В реактор, содержавший 150 мл фосфатного буферного раствора с концентрацией 0,2 моль·л-1 и pH=7, вносили 10 мл ферментативного комплекса, 6 г (33 ммоль) O-ацетил-L-гомосерина (OAHS, O-ацетил-L-гомосерин был синтезирован исходя из L-гомосерина и уксусного ангидрида согласно публикации Sadamu Nagai "Synthesis of O-acetyl-L-homoserine, Academie Press, (1971), vol. 17, p. 423-424"). Раствор ферментативного комплекса содержал 185 мг (0,6 ммоль) глутатиона, 200 ед. глутатионредуктазы, 50 мг (0,06 ммоль) NADPH, 200 ед. глюкозодегидрогеназы, 0,4 г (1,6 ммоль) пиридоксальфосфата и 0,6 г O-ацетил-L-гомосеринсульфгидрилазы.
[0077] Реакционную смесь доводили до 27°C при механическом перемешивании. Первый отбор проб осуществляли в момент времени t=0. Далее диметилдисульфид (3 г, 32 ммоль) вносили в бюретку и вводили по каплям в реактор, который был закрыт для избежания какого-либо выделения метилмеркаптана, при этом реакция начиналась сразу. Ход реакции контролировали способом ВЭЖХ для отслеживаниия исчезновения OAHS и образования L-метионина. Через 6 часов 21% OAHS был превращен в L-метионин, что демонстрирует возможность получения L-метионина способом по "однореакторной технологии" исходя из предшественника L-метионина, DMDS и органического соединения-восстановителя.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ L-МЕТИОНИНА | 2016 |
|
RU2709715C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕРКАПТАНОВ ПУТЕМ ФЕРМЕНТАТИВНОГО ГИДРОГЕНОЛИЗА ДИСУЛЬФИДОВ | 2016 |
|
RU2709486C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕРКАПТАНОВ ПУТЕМ ФЕРМЕНТАТИВНОГО ГИДРОГЕНОЛИЗА ДИСУЛЬФИДОВ С ПОМОЩЬЮ ВОДОРОДА | 2016 |
|
RU2720091C1 |
| СПОСОБ ПОЛУЧЕНИЯ L-МЕТИОНИНА И РОДСТВЕННЫХ ПРОДУКТОВ | 2011 |
|
RU2598276C2 |
| Способ получения L-метионина и органической кислоты | 2011 |
|
RU2673190C1 |
| НОВАЯ О-АЦЕТИЛГОМОСЕРИН-СУЛЬФГИДРИЛАЗА ИЛИ ЕЕ МУТАНТНЫЙ БЕЛОК И СПОСОБ ПРЕОБРАЗОВАНИЯ В МЕТИОНИН С ИСПОЛЬЗОВАНИЕМ ТАКОВОЙ | 2011 |
|
RU2573928C2 |
| СПОСОБ ПОЛУЧЕНИЯ L-МЕТИОНИНА | 2016 |
|
RU2729012C2 |
| КОМПОЗИЦИЯ КОРМОВОЙ ДОБАВКИ И СОДЕРЖАЩАЯ ЕЕ КОМПОЗИЦИЯ КОРМА ДЛЯ ЖИВОТНЫХ | 2016 |
|
RU2692656C2 |
| ВАРИАНТ O-АЦЕТИЛГОМОСЕРИН-СУЛЬФГИДРИЛАЗЫ И СПОСОБ ПОЛУЧЕНИЯ L-МЕТИОНИНА С ИСПОЛЬЗОВАНИЕМ ЭТОГО ВАРИАНТА | 2016 |
|
RU2694041C1 |
| МИКРООРГАНИЗМЫ ДЛЯ ПРОИЗВОДСТВА МЕТИОНИНА С УЛУЧШЕННЫМ ВЫХОДОМ МЕТИОНИНА | 2014 |
|
RU2678757C2 |
Изобретение относится к биотехнологии, в частности к способу получения L-метионина ферментативной реакцией между предшественником L-метионина, диметилдисульфидом (DMDS) и органическим соединением-восстановителем. Получают смесь, содержащую 1) DMDS, 2) каталитическое количество аминокислоты, содержащей тиольную группу, или пептида с тиольной группой, 3) каталитическое количество редуктазы, катализирующей восстановление дисульфидного мостика аминокислоты, содержащей тиольную группу, или пептида с тиольной группой, 4) органическое соединение-восстановитель в стехиометрическом количестве по отношению к DMDS, 5) каталитическое количество дегидрогеназы, катализирующей реакцию дегидрирования указанного органического соединения-восстановителя, 6) каталитическое количество кофактора, являющегося общим для дегидрогеназы и редуктазы. Проводят ферментацию для получения метилмеркаптана (CH3SH). Вводят предшественник L-метионина. Осуществляют взаимодействие этого предшественника с CH3SH. Выделяют образовавшийся L-метионин. Изобретение позволяет отказаться от манипуляций с метилмеркаптаном или по меньшей мере уменьшить их объем, генерируя метилмеркаптан по реакции ферментативного катализа DMDS непосредственно перед синтезом L-метионина или in situ в реакторе синтеза L-метионина. 15 з.п. ф-лы, 2 ил., 2 пр.
1. Способ получения L-метионина, включающий по меньшей мере стадии:
a) получения смеси, содержащей:
1) диметилдисульфид;
2) каталитическое количество аминокислоты, содержащей тиольную группу, или пептида с тиольной группой;
3) каталитическое количество фермента, катализирующего реакцию восстановления дисульфидного мостика аминокислоты, содержащей тиольную группу, или пептида с тиольной группой, где указанным ферментом является редуктаза;
4) органическое соединение-восстановитель в стехиометрическом количестве по отношению к диметилдисульфиду;
5) каталитическое количество фермента, катализирующего реакцию дегидрирования указанного органического соединения-восстановителя, где указанным ферментом является дегидрогеназа;
6) каталитическое количество кофактора, являющегося общим для обоих ферментов каталитической системы, которыми являются дегидрогеназа и редуктаза;
b) осуществления ферментативной реакции для получения метилмеркаптана (CH3SH), используя смесь, полученную на стадии a);
c) введения предшественника L-метионина и взаимодействия этого предшественника с метилмеркаптаном, образовавшимся на стадии b), и
d) выделения образовавшегося L-метионина.
2. Способ по п. 1, включающий по меньшей мере стадии:
a') получения смеси, содержащей:
- диметилдисульфид (DMDS);
- каталитическое количество аминокислоты, содержащей тиольную группу, или пептида с тиольной группой;
- каталитическое количество редуктазы, соответствующей аминокислоте, содержащей тиольную группу, или пептиду с тиольной группой;
- каталитическое количество NADPH;
b') введения органического соединения-восстановителя в стехиометрическом количестве по отношению к диметилдисульфиду с каталитическим количеством фермента дегидрогеназы, соответствующего используемому органическому соединению-восстановителю;
c') осуществления ферментативной реакции для получения метилмеркаптана (CH3SH);
d') добавления предшественника L-метионина и взаимодействия предшественника L-метионина с метилмеркаптаном, образовавшимся на стадии c'), и
e') выделения образовавшегося L-метионина.
3. Способ по п. 1 или 2, в котором метилмеркаптан приводят непосредственно в контакт с предшественником метионина.
4. Способ по любому из пп. 1-3, в котором органическое соединение-восстановитель представляет собой органическое соединение-восстановитель, которое является донором атомов водорода, содержит гидроксигруппу и выбрано из спиртов, полиолов и сахаров.
5. Способ по любому из пп. 1-4, в котором органическое соединение-восстановитель выбирают из глюкозы, глюкозо-6-фосфата и изопропанола.
6. Способ по любому из пп. 1-5, в котором аминокислоту, содержащую тиольную группу, или пептид, содержащий тиольную группу, выбирают из цистеина, гомоцистеина, глутатиона и тиоредоксина.
7. Способ по любому из пп. 1-6, в котором предшественник L-метионина выбирают из O-ацетил-L-гомосерина и O-сукцинил-L-гомосерина.
8. Способ по любому из пп. 1-7, в котором метилмеркаптан применяет в синтезе L-метионина непосредственно после выхода из реактора.
9. Способ по п. 8, включающий по меньшей мере следующие стадии:
стадия 1: получение предшественника L-метионина;
стадия 2: ферментативное восстановление DMDS в реакторе R1 с образованием метилмеркаптана, выходящего из реактора R1;
стадия 3: ферментативный синтез L-метионина в реакторе R2 исходя из предшественника со стадии 1 и метилмеркаптана со стадии 2;
стадия 4: выделение образовавшегося L-метионина.
10. Способ по любому из пп. 1-7, в котором синтез метилмеркаптана исходя из DMDS и синтез L-метионина исходя из этого метилмеркаптана осуществляют в одном и том же реакторе.
11. Способ по п. 10, включающий по меньшей мере следующие стадии:
стадия 1': получение предшественника L-метионина бактериальной ферментацией глюкозы;
стадия 2': ферментативное восстановление DMDS в реакторе R1 с образованием in situ метилмеркаптана и совместный ферментативный синтез L-метионина в том же самом реакторе исходя из предшественника, полученного на стадии 1'; и
стадия 3': выделение образовавшегося L-метионина.
12. Способ по п. 11, дополнительно включающий стадию 2" между стадиями 2' и 3': возврат глюконолактона, образовавшегося на стадии 2', на стадию 1'.
13. Способ по любому из пп. 1-12, осуществляемый в периодическом или непрерывном режиме.
14. Способ по любому из пп. 1-13, в котором идеальное молярное соотношение "органическое соединение-восстановитель/DMDS" находится в интервале от 0,01 до 100, причем указанное молярное соотношение предпочтительно выбирают в интервале от 0,5 до 5 и наиболее предпочтительно молярное соотношение равно 1.
15. Способ по любому из пп. 1-14, в котором молярное соотношение "DMDS/предшественник L-метионина" находится в интервале от 0,1 до 10 и в общем случае от 0,5 до 5, при этом, предпочтительно, молярное соотношение является стехиометрическим.
16. Способ по любому из пп. 1-15, в котором температура осуществления ферментативной реакции находится в интервале от 10 до 50°C, предпочтительно от 15 до 45°C и более предпочтительно от 20 до 40°C.
| WO 2013029690 A1, 07.03.2013 | |||
| WO 2008013432 A1, 31.01.2008 | |||
| ПРИМЕНЕНИЕ ДИМЕТИЛДИСУЛЬФИДА ДЛЯ ПРОДУКЦИИ МЕТИОНИНА МИКРООРГАНИЗМАМИ | 2006 |
|
RU2413001C2 |
| РАСШИРИТЕЛЬНОЕ СОЕДИНЕНИЕ ЧАСТЕЙ СУДОВОЙ НАДСТРОЙКИ | 2009 |
|
RU2402453C1 |
| US 4059636 A, 22.11.1977 | |||
| US 2005260250 A1, 24.11.2005 | |||
| SZAJEWSKI R | |||
| P., WHITESIDES G | |||
| M | |||
| "Rate Constants and Equilibrium Constants for Thiol-Disulfide Interchange Reactions Involving Oxidized Glutathione" | |||
| J | |||
| Am | |||
| Chem | |||
| Soc., 1980, | |||
Авторы
Даты
2020-01-16—Публикация
2016-09-29—Подача