Способ моделирования дисфункции эндотелия и патологии внутренних органов в эксперименте
Изобретение относится к медико-биологической, патофизиологической науке и касается моделирования дисфункции эндотелия и патологии внутренних органов при экспериментальном интоксикационном синдроме в сочетании с L-NAME.
Известен способ моделирования дисфункции эндотелия in vitro, включающий одновременную инкубацию культуры эндотелиальных клеток, (см. патент RU №2490632, МПК2006.01 G01N 33/48, опубл. 20.08.2013 г.)
Недостатком аналога является то, что результаты исследований, проведенные in vitro, не согласовываются с данными, полученными in vivo, а также результаты исследований не внедрены в клинику.
Наиболее близким к заявленному техническому решению является способ моделирования дисфункции эндотелия и патологии внутренних органов в эксперименте, включающий воспроизведение метаболических нарушений посредством парентеральной экспозиции экспериментальным животным хлорида никеля в дозе 0,5 мг/кг от веса животного один раз в сутки в течение 30 дней, (см. статью Дзугкоева С.Г., Можаева И.В., Маргиева О.И. и др. "Влияние L-аргинина и его комбинации с L-карнитином на метаболические показатели дисфункции эндотелия в условиях интоксикации никеля хлоридом". Астраханский медицинский журнал, т. 12, №1, 2017 г., с. 44-49).
Недостатками прототипа является низкая точность и адекватность исследования патогенетических механизмов формирования дисфункции эндотелия и характера изменений метаболических показателей в крови и внутренних органах - почках, печени, миокарде и отсутствие исследования уровня экспрессии эндотелиальной NO-синтазы (NOS-3). Все исследования были проведены в сочетании с L-карнитином и L-аргинином как способ, направленный на достижение коррекции дисфункции эндотелия, а не на его моделирование.
Техническим результатом предлагаемого технического решения является повышение точности и адекватности исследования патогенетических механизмов формирования дисфункции эндотелия и характера изменений метаболических показателей в крови и внутренних органах - почках, печени, миокарде, уровня экспрессии эндотелиальной NO-синтазы (NOS-3), а также повышение эффективности, воспроизводимости, удобства, доступности, безопасности и снижение стоимости экспериментов.
Решение технического результата заключается в том, что в способе моделирования дисфункции эндотелия и патологии внутренних органов в эксперименте, включающим воспроизведение метаболических нарушений посредством введения экспериментальным животным парентеральной экспозиции хлорида никеля в дозе 0,5 мг/кг от веса животного один раз в сутки в течение 30 дней, согласно изобретению, в комбинации с хлоридом никеля дополнительно вводят экспериментальным животным парентерально ингибитор фермента - эндотелиальной NO-синтазы, продуцирующий оксид азота - L-NAME, в дозе 25 мг/кг от веса животного один раз в сутки в течение 30 дней.
Данный способ позволит повысить точность и адекватность исследования патогенетических механизмов формирования дисфункции эндотелия и характера изменений метаболических показателей в крови и внутренних органах - почках, печени, миокарде, уровень экспрессии эндотелиальной NO-синтазы (NOS-3), а также повысить эффективность, воспроизводимость, удобство, доступность, безопасность и снизить стоимость экспериментов.
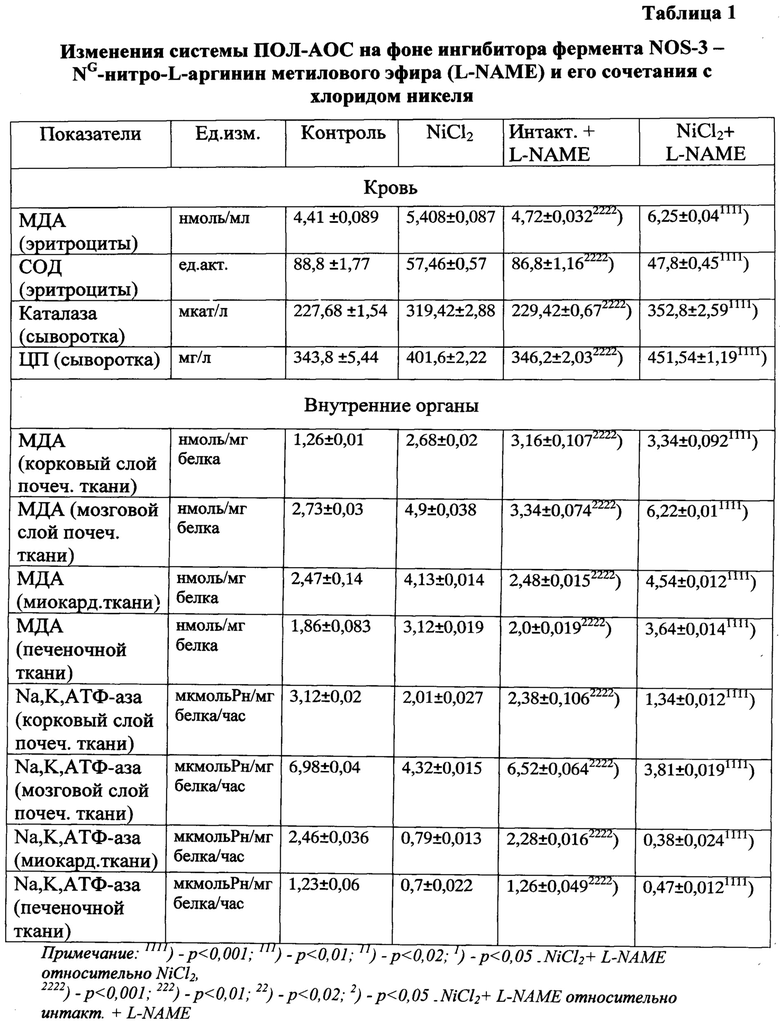
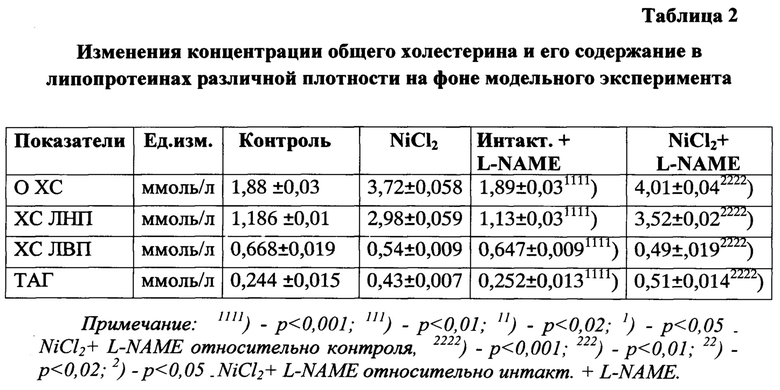
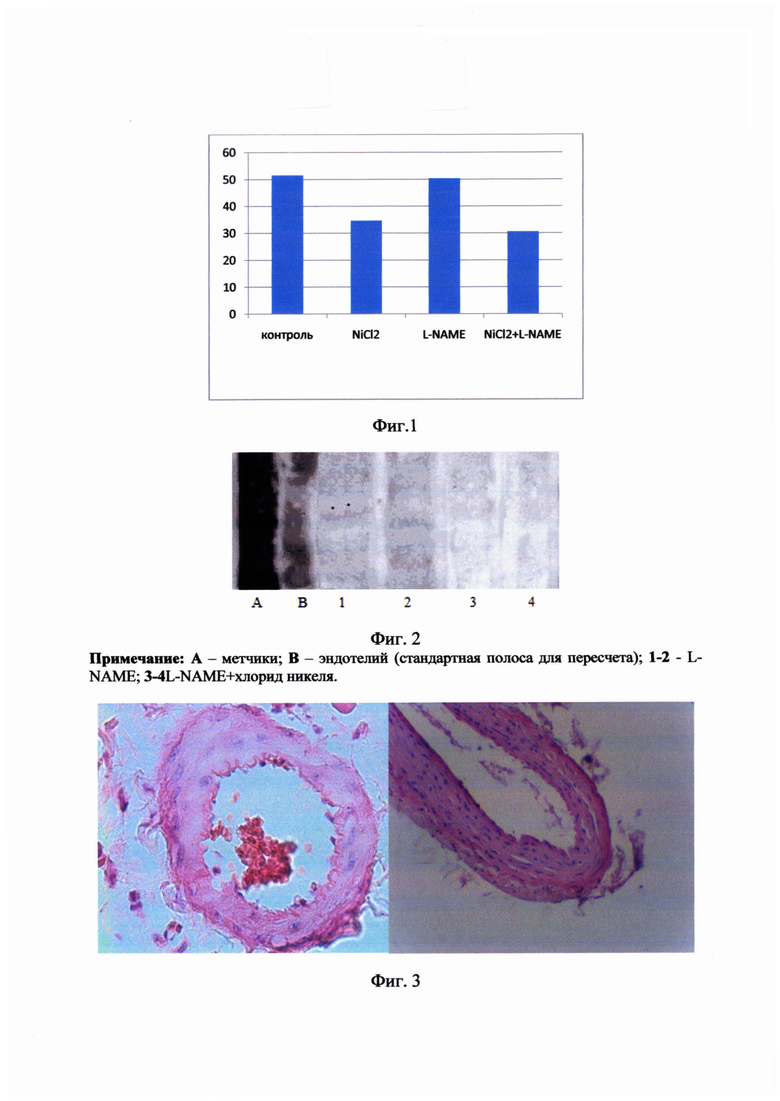
Сущность способа поясняется таблицами, где в таблице 1-представлено изменение системы ПОЛ-АОС на фоне комбинации ингибитора фермента эндотелиальной NO-синтазы - NG-нитроаргинин метилового эфира (L-NAME) с хлоридом никеля, а также в группах сравнения, в таблице 2 - изменение концентрации общего холестерина и его содержание в липопротеинах различной плотности на фоне модельного эксперимента, а также чертежами, где на фиг. 1 - изображено изменение содержания оксида азота под влиянием L-NAME + хлорид никеля, на фиг. 2 - изображена экспрессия эндотелиальной NO-синтазы в эндотелии аорты на фоне модельного эксперимента у крыс, на фиг. 3 - динамика изменения гистологических показателей в модельном эксперименте на фоне ингибитора фермента эндотелиальной NO-синтазы - NG-нитроаргинин метилового эфира (L-NAME) и его сочетания с хлоридом никеля.
Моделирование эндотелиальной дисфункции в эксперименте путем внутримышечного введения хлорида никеля в комбинации с ингибитором L-NAME, который вводят внутрибрюшинно в течение 30 дней вызывает нарушение окислительно-восстановительного потенциала организма, индуцирующее процессы ПОЛ в эритроцитах и происходит повышение концентрации МДА в гемолизате эритроцитов, в почечной, печеночной и миокардиальной тканях. Анализ активности ферментов антиокислительной системы (АОС) показал статистически достоверное снижение функциональной способности СОД в эритроцитах, повышение каталазы и концентрации ЦП в сыворотке крови. Разнонаправленный характер изменений адаптивных ферментов, скорее всего, объясняется их различной молекулярной структурой. Таким образом, никелевая интоксикация с ингибитором экспрессии эндотелиальной NO-синтазы (NOS-3 - фермент, продуцирующий оксид азота) в условиях нарушения окислительно-восстановительного потенциала сопровождалась снижением концентрации NOx - основного биохимического маркера дисфункции эндотелия. Данная модель характеризовалась нарушением обмена холестерина, гиперхолестеринемией и гипер-β-липопротеинемией, что способствовало повреждению эндотелия. Полученные результаты были подтверждены гистологическими данными аорты, почечной, печеночной и миокардиальной тканей. На срезах тканей внутренних органов интоксифицированных крыс в сочетании с L-NAME отмечались умеренная гиалиново - капельная дистрофия канальцев и расширение мочевых пространств; умеренная паренхиматозно-белковая дистрофия и частичное исчезновение гликогена в гепатоцитах; частичная фрагментация кардиомиоцитов; отмечалась плазматическая пропитка и умеренное утолщение сосудов микроциркуляторного русла. Нарушение метаболических процессов характеризовались снижением активности Na, K-АТФ-азы и повышением в крови специфических для органов ферментов - трансаминаз, ГГТП, щелочной фосфатазы.
Способ осуществляли следующим образом.
Моделировали дисфункцию эндотелия на линейных («Wistar») крысах, контрольных и интоксифицированных с L-NAME, который вводили внутрибрюшинно в дозе 25 мг/кг, а хлорид никеля, в дозе 0,5 мг/кг веса крысы вводили внутримышечно 30 дней. Проведение экспериментов соответствовали международным принципам гуманного отношения к животным («Правила проведения работ с использованием экспериментальных животных», Хельсинкская декларация). Эксперимент по выявлению метаболических нарушений, характеризующие дисфункцию эндотелия длился 30 дней. По окончании эксперимента забирали кровь из сердца, в отмытых эритроцитах определяли содержание МДА, СОД, а в сыворотке крови - активность каталазы и концентрацию ЦП и суммарных метаболитов NOx. В отдельном эксперименте определяли экспрессию эндотелиальной NO-синтазы в эндотелии аорты. Для выяснения причин нарушенной биодоступности NO определяли метаболизм холестерина. Проводили гистологические исследования. По окончанию эксперимента исследовалась интенсивность перекисного окисления липидов в гемолизате эритроцитов, почечной, печеночной и миокардиальной тканях по вторичному продукту - альдегиду малоновой кислоты (МДА). Об активности антиокислительной защиты клеток (АОЗ) в крови судили по активности каталазы, концентрации церулоплазмина (ЦП), а супероксиддисмутазы (СОД) в эритроцитах. Обмен ХС оценивали по концентрации общего ХС, его содержанию в липопротеинах низкой (ЛПНП) и высокой плотности (ЛПВП) и ТАГ. Определяли концентрацию суммарных метаболитов оксида азота (NOx) в реакции деазотирования, согласно модифицированному экспресс-методу Метельской В.А. О мембранных механизмах повреждения клеток органов судили по активности в клетках почечной, печеночной тканей и миокарде, АТФ-азы, активируемой Na и К, а также по активности в сыворотке крови - специфичных для органов энзимов: АлАТ, AcAT, ГГТП и щелочной фосфатазы.
В отдельном варианте исследовали уровень экспрессии eNOS в эндотелии аорты. Уровень экспрессии eNOS в эндотелии аорты определяли методом Метельской В.А., Тумановой Н.Г., Литинской О.А. (Оксид азота: роль в регуляции биологических функций, методы определения в крови человека // Лабораторная медицина. - 2005. - №7. - С. 19-24). Аорты извлекали, промывали физиологическим раствором и помещали в пластиковые пробирки, которые хранили в жидком азоте, после чего аорты обрабатывали соответственно методике. Полосу, соответствующую эндотелиальной NO-синтазе, детектировали в соответствии с ее молекулярной массой, устанавливаемой по сравнению с белками-метчиками. Пленку высушивали на воздухе, полосы сканировали и рассчитывали площадь под кривой с использованием программы Total Lab. Результаты представляли в условных единицах как отношение интенсивности полосы X к интенсивности полосы, принятой за контроль на каждой пленке. Аорта экспериментальных крыс подвергалась гистологическому исследованию микроскопически. Количественную оценку гистологических изменений структуры проводили по методу Автандилова с помощью цифрового фотоаппарата "Nikon", совмещенного с микроскопом. Исследование проводили в 4-х группах крыс-самцов линии Вистар:
- Контролем служили:
интактные крысы в количестве 20 голов (1 группа);
- Опытная группа:
Крысы с хлоридом никеля + L-NAME в дозе 25 мг/кг в течение 30 дней в количестве 20 голов (2 группа);
- Группы сравнения:
Интактные крысы + L-NAME в дозе 25 мг/кг в течение 30 дней в количестве 15 голов (3группа);
Крысы с хлоридом никеля в количестве 30 голов (4 группа).
Модель дисфункции эндотелия вызывали введением 0,5 мг/кг веса животного хлорида никеля в комбинации с L-NAME в дозе 25 мг/кг.
Сущность заявляемого способа подтверждена графически и таблицами: При статистической обработке данных рассчитывали среднее значение, величину стандартного отклонения. Различия считали достоверными при р<0,05.
Пример конкретного выполнения способа.
Результаты показали существенное повышение концентрации МДА в крови под влиянием хлорида никеля и L-NAME (с 4,41±0,08 нмоль/мл до 6,25±0,044 нмоль/мл (р<0,001). Данные анализа активности АОС выявили достоверное снижение активности СОД в эритроцитах (с 88,8±1,77 ед.акт. до 47,8±2,23 ед.акт. (р<0,001) и повышение данных каталазы и церулоплазмина. Несоответствие данных каталазы и ЦП является следствием повышенного образования Н2О2 и вследствие этого активации защитных механизмов (см. табл. 1).
Причиной сниженного образования NO явилось его взаимодействие с O2- и образования сильного окислителя пероксинитрита, а также снижение уровня экспрессии эндотелиальной NO-синтазы модифицированным L-аргинином - L-NAME. Ингибируется поток электронов между редуктазным и оксидазным доменами фермента. Такая молекулярная перестройка энзима оптимальна для продукции АФК, что и усугубляет выраженность окислительного стресса. Эти изменения способствовали снижению концентрации суммарных метаболитов NOx и корреляционный анализ показал наличие отрицательной связи с МДА (r=-0,74). (см. фиг. 1)
С другой стороны снижается доступность индуктора фермента L-аргинина, вследствие изменений в эндотелии сосудов. Анализ данных показал повышение концентрации общего холестерина (ОХС), ХС ЛПНП, снижение ХС ЛПВП и одновременное повышение ТАГ (см. табл. 2).
Для подтверждения участия эндотелиальной NO-синтазы исследовали уровень экспрессии NO продуцирующего фермента в экстрактах эндотелия аорты у экспериментальных крыс. Что касается самого NO-продуцирующего фермента, данные показали снижение уровня экспрессия эндотелиальной NO-синтазы на фоне L-NAME (см. фиг. 2).
Захват холестерина моноцитами приводит к его накоплению, образованию пенистых клеток с липидным содержимым, липидных пятен и полос, т.е. предатерогенным изменениям, что подтверждается гистологически (см. фиг. 3).
Развившаяся дисфункция эндотелия вызвала повреждение внутренних органов, в них интенсифицировался процесс ПОЛ и содержание конечных продуктов ПОЛ увеличилось в корковом и мозговом веществе соответственно на 153,8% и 91,2%, в печеночной и сердечной тканях на 79% и 70,8%. (см. табл. 1).
Преобладание окислительных процессов привело к нарушению гидрофобности цитоплазматических мембран, снижению активности Na, K-АТФ-азы в клетках внутренних органов и повышению активности в сыворотке крови АлАТ и АсАТ, ГГТП и экскреторного-щелочной фосфатазы.
Использование предлагаемого способа по сравнению с прототипом позволит повысить точность и адекватность исследования патогенетических механизмов формирования дисфункции эндотелия и характера изменений метаболических показателей в крови и внутренних органах - почках, печени, миокарде, уровень экспрессии эндотелиальной NO-синтазы (NOS-3), а также повысить эффективность, воспроизводимость, удобство, доступность, безопасность и снизить стоимость экспериментов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения эффективности лечения эндотелиальной дисфункции при метаболических и функциональных нарушениях у крыс в эксперименте | 2023 |
|
RU2808420C1 |
| Способ диагностики эндотелиальной дисфункции при метаболических и функциональных нарушениях | 2022 |
|
RU2790368C1 |
| СПОСОБ КОРРЕКЦИИ ОКИСЛИТЕЛЬНОГО СТРЕССА И НАРУШЕНИЯ NO ПРОДУЦИРУЮЩЕЙ ФУНКЦИИ ЭНДОТЕЛИЯ ПРИ СОСУДИСТЫХ ОСЛОЖНЕНИЯХ САХАРНОГО ДИАБЕТА В ЭКСПЕРИМЕНТЕ | 2013 |
|
RU2521279C1 |
| ПРИМЕНЕНИЕ ПРОИЗВОДНЫХ ОКСАТРИАЗОЛИЙ-5-ОЛАТА ДЛЯ ЛЕЧЕНИЯ СЕКСУАЛЬНЫХ РАССТРОЙСТВ | 2014 |
|
RU2600845C2 |
| Способ диагностики и лечения эндотелиальной дисфункции при метаболических нарушениях у больных с ишемической болезнью сердца второго функционального класса | 2020 |
|
RU2737416C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ЭНДОТЕЛИАЛЬНОЙ ДИСФУНКЦИИ, АССОЦИИРОВАННОЙ С СИСТЕМНЫМ ВОСПАЛЕНИЕМ НИЗКОЙ ГРАДАЦИИ И ОКИСЛИТЕЛЬНЫМ СТРЕССОМ | 2016 |
|
RU2618657C1 |
| СПОСОБ КОРРЕКЦИИ ЭНДОТЕЛИАЛЬНОЙ ДИСФУНКЦИИ НА МОДЕЛИ L-NAME-ИНДУЦИРОВАННОГО ДЕФИЦИТА ОКСИДА АЗОТА | 2023 |
|
RU2810415C1 |
| КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ЭНДОТЕЛИОПРОТЕКТОРНЫМ, ВАЗОДИЛАТИРУЮЩИМ И АНГИОПРОТЕКТОРНЫМ ЭФФЕКТОМ | 2011 |
|
RU2464019C1 |
| СПОСОБ ДИАГНОСТИКИ И КОРРЕКЦИИ ЭНДОТЕЛИАЛЬНОЙ ДИСФУНКЦИИ ПРИ СОСУДИСТЫХ ОСЛОЖНЕНИЯХ АЛЛОКСАНОВОГО ДИАБЕТА В ЭКСПЕРИМЕНТЕ | 2010 |
|
RU2455702C1 |
| Способ оценки эффективности эндотелиотропной терапии после реконструктивных операций на артериях | 2015 |
|
RU2611386C2 |
Изобретение относится к медико-биологической, патофизиологической науке и касается моделирования дисфункции эндотелия и патологии внутренних органов при экспериментальном интоксикационном синдроме в сочетании с L-NAME. Для этого воспроизводят метаболические нарушения посредством введения экспериментальным животным парентеральной экспозиции хлорида никеля в дозе 0,5 мг/кг от веса животного один раз в сутки в течение 30 дней, а также в комбинации с хлоридом никеля дополнительно вводят парентерально ингибитор фермента - эндотелиальной NO-синтазы, продуцирующий оксид азота, - L-NAME в дозе 25 мг/кг от веса животного один раз в сутки в течение 30 дней. Изобретение обеспечивает повышение точности и адекватности исследования патогенетических механизмов формирования дисфункции эндотелия и характера изменений метаболических показателей в крови и внутренних органах, а также повышение эффективности, воспроизводимости, удобства, доступности, безопасности и невысокую стоимость экспериментов. 3 ил., 2 табл., 1 пр.
Способ моделирования дисфункции эндотелия и патологии внутренних органов в эксперименте, включающий воспроизведение метаболических нарушений посредством введения экспериментальным животным парентеральной экспозиции хлорида никеля в дозе 0,5 мг/кг от веса животного один раз в сутки в течение 30 дней, отличающийся тем, что в комбинации с хлоридом никеля дополнительно вводят парентерально ингибитор фермента - эндотелиальной NO-синтазы, продуцирующий оксид азота, - L-NAME в дозе 25 мг/кг от веса животного один раз в сутки в течение 30 дней.
| ДЗУГКОЕВ С.А., МОЖАЕВА И.В., МАРГИЕВА О.И | |||
| и др | |||
| Влияние L-аргинина и его комбинации с L-карнитином на метаболические и функциональные показатели дисфункции эндотелия в условиях интоксикации никеля хлоридом | |||
| Астраханский медицинский журнал, т.12, N1, 2017, с.44-49 | |||
| ШИЛОВ А.В., МНИХОВИЧ М.В | |||
| и др | |||
| Морфологическая оценка эффективности |
Авторы
Даты
2020-01-24—Публикация
2019-08-07—Подача