Изобретение относится к медицине, а точнее к онкологии, и может быть использовано для определения эффективности таргетной терапии цетуксимабом у больных плоскоклеточным раком языка и слизистой дна полости рта.
Рак представляет собой сложное гетерогенное заболевание, которое регулируется на нескольких уровнях, с высокими показателями заболеваемости и смертности. Плоскоклеточный рак головы и шеи является седьмым, наиболее часто встречаемым раком, с заболеваемостью более полумиллиона ежегодных случаев (см. Rothenberg S. М, Ellisen L.W. The molecular pathogenesis of head and neck squamous cell carcinoma // J Clin Invest. 2012; 122(6):1951-1957; Esteller M. Epigenetics in cancer. N. // Engl. J. Med. 2008; 13:1148-1159). Развитие плоскоклеточных карцином головы и шеи (HNSCC) обусловлено генетическими нарушениями, вызываемыми факторами экологического риска, а также чрезмерным употреблением алкоголя и табака (см. Sharma S., Kelly Т.K., Jones P.A. Epigenetics in cancer // Carcinogenesis. 2010; 31:27-36). Плоскоклеточные карциномы полости рта (ПКПР) являются преобладающими формами HNSCC и составляют приблизительно 90% всех опухолей головы и шеи. Высокая смертность, связанная с ПКПР, обусловлена в основном локорегиональным развитием болезни (см. Foy J.P., Saintigny P., Goudot P., Schouman Т., Bertolus C. The promising impact of molecular profiling on treatment strategies in oral cancers. // J. Stomatol. Oral Maxillofac. Surg. 2017; 118: 242-247.; Irimie A.I., Ciocan C., Gulei D. et al. Current Insights into oral cancer epigenetics // Int. J. Mol. Sci. 2018; 19:670).
Несмотря на значительные улучшения в достижении локального контроля над заболеванием после хирургического вмешательства и увеличением выживаемости пациентов с первичными злокачественными опухолями полости рта, врачи сталкиваются с такой проблемой как сохранение функций ротовой полости - артикуляции, жевания и визуальной эстетики. Эффективное лечение прогрессирующих HNSCC (Т3 и Т4) предполагает использование мультидисциплинарных подходов с проведением многокурсовой химиотерапии и лучевой терапии (см. 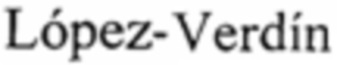 S., Lavalle-Carrasco J.,
S., Lavalle-Carrasco J., 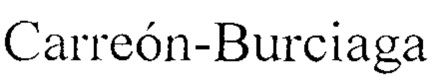 R. G. et al. Molecular Markers of Anticancer Drug Resistance in Head and Neck Squamous Cell Carcinoma: A Literature Review. // Cancers, 2018, 10(10), 376.). Схемы химиотерапии для опухолей головы и шеи включают в себя использование комбинаций таких химиотерапевтических агентов как цисплатин и доцетаксел, а также цисплатин и 5-фторурацил (см. Katori Н., Tsukuda М., Mochimatu I. et al. I trial of concurrent chemoradiotherapy with docetaxel, cisplatin and 5-fluorouracil (TPF) in patients with locally advanced squamous cell carcinoma of the head and neck (SCCHN) // Br. J. Cancer. 2004; 90:348-352; см. Umeda M., Komatsubara H., Ojima Y. et al. Lack of survival advantage in patients with advanced, resectable squamous cell carcinoma of the oral cavity receiving induction chemotherapy with cisplatin (CDDP), docetaxel (TXT) and 5-fluorouracil (5FU) // Kobe J. Med. Sci. 2004; 50:189-196). Наиболее используемой стратегией лечения для запущенных стадий HNSCC является применение цисплатина в дозе 100 мг/м2 на фоне радиотерапии. Однако эффективность лечения на основе цисплатина может быть ограничена, поскольку пациенты приобретают лекарственную устойчивость (см. Higuchi Е., Oridate N., Furuta Y. et al. Differentially expressed genes associated with ClS-diamminedichloroplatinum (II) resistance in head and neck cancer using differential display and cDNA microarray // Head Neck. 2003; 25:187-193).
R. G. et al. Molecular Markers of Anticancer Drug Resistance in Head and Neck Squamous Cell Carcinoma: A Literature Review. // Cancers, 2018, 10(10), 376.). Схемы химиотерапии для опухолей головы и шеи включают в себя использование комбинаций таких химиотерапевтических агентов как цисплатин и доцетаксел, а также цисплатин и 5-фторурацил (см. Katori Н., Tsukuda М., Mochimatu I. et al. I trial of concurrent chemoradiotherapy with docetaxel, cisplatin and 5-fluorouracil (TPF) in patients with locally advanced squamous cell carcinoma of the head and neck (SCCHN) // Br. J. Cancer. 2004; 90:348-352; см. Umeda M., Komatsubara H., Ojima Y. et al. Lack of survival advantage in patients with advanced, resectable squamous cell carcinoma of the oral cavity receiving induction chemotherapy with cisplatin (CDDP), docetaxel (TXT) and 5-fluorouracil (5FU) // Kobe J. Med. Sci. 2004; 50:189-196). Наиболее используемой стратегией лечения для запущенных стадий HNSCC является применение цисплатина в дозе 100 мг/м2 на фоне радиотерапии. Однако эффективность лечения на основе цисплатина может быть ограничена, поскольку пациенты приобретают лекарственную устойчивость (см. Higuchi Е., Oridate N., Furuta Y. et al. Differentially expressed genes associated with ClS-diamminedichloroplatinum (II) resistance in head and neck cancer using differential display and cDNA microarray // Head Neck. 2003; 25:187-193).
HNSCC характеризуются повышенной экспрессией эпидермального фактора роста (EGF). В связи с этим таргетный препарат цетуксимаб (Erbitux, Merck KGaA, Дармштадт, Германия) - химерное антитело, блокирующее моноклональный эпидермальный рецептор фактора роста (EGFR) был одобрен для лечения локального и распространенного плоскоклеточного рака головы и шеи в сочетании с радиотерапией, а также для рецидивирующих/метастатических опухолей вместе с другими химиотерапевтическими средствами. Этот препарат блокирует активацию рецептора, предотвращая опосредованное тирозинкиназой фосфорилирование белка, что приводит к антителозависимой клеточной цитотоксичности. Основными эффектами цетуксимаба являются активация апоптоза, ингибирование прогрессирования клеточного цикла, инвазии опухолевых клеток и ангиогенеза (см. Ansell A., Jedlinski A., Johansson А.С., Roberg K. Epidermal growth factor is a potential biomarker for poor cetuximab response in tongue cancer cells // J. Oral Pathol. Med. 2016; 45:9-16.).
При использовании цетуксимаба в сочетании с лучевой терапией и химиотерапией у пациентов с HNSCC выявлено увеличение выживаемости (см. Bonner J.A., Harari P.M., Giralt J. et al. Radiotherapy plus cetuximab for squamous-cell carcinoma of the head and neck // N. Engl. J. Med. 2006; 354:567-57; см. Merlano M., Occelli M. Review of cetuximab in the treatment of squamous cell carcinoma of the head and neck // Ther. Clin. Risk. Manag. 2007; 3:871-876). Однако, после того как было установлено, что лечение связано с лекарственной устойчивостью, опосредованной EGFR, было отмечено значительное повышение частоты рецидивов (см. Ohnishi Y., Minamino Y., Kakudo K., Nozaki M. Resistance of oral squamous cell carcinoma cells to cetuximab is associated with EGFR insensitivity and enhanced stem cell-like potency // Oncol. Rep.2014; 32:780-786).
Чувствительность лечения к противоопухолевым препаратам коррелирует с индивидуальными характеристиками пациентов и опухолевой гетерогенностью (см. Suzuki М., Ishikawa Н, Tanaka A., Mataga I. Heterogeneity of anticancer drug sensitivity in squamous cell carcinoma of the tongue // Hum. Cell. 2011; 24:21-29). Внутриопухолевая гетерогенность является одной из важнейших причин, ограничивающих эффективность таргетной терапии, и предполагает наличие клеток с уникальными геномами и разными свойствами, обеспечивающими различные потенции к прогрессированию и резистентности к терапии, в пределах одной опухоли, а также предполагает отличия между клепками первичных и вторичных опухолей и обеспечивает их разную чувствительность к терапии (см. Гервас П.А., Литвяков Н.В., Попова Н.О. и соавт. Проблемы и перспективы совершенствования молекулярно-генетической диагностики для назначения таргетных препаратов в онкологии // Сибирский онкологический журнал. - 2014. - №2 (62). - С. 46-55). Опухоли головы и шеи, проявляющие терапевтическую резистентность, могут происходить из опухолевых клеток с фенотипом эпителиально-мезенхимального перехода (ЭМП) (см. La Fleur L., Johansson А.С., Roberg K. A. CD44high/EGFRlow subpopulation within head and neck cancer cell lines shows an epithelial-mesenchymal transition phenotype and resistance to treatment // PLoS ONE. 2012; 7:e44071; см. Masui Т., Ota I., Yook J.I et al. Snail-induced epithelial-mesenchymal transition promotes cancer stem cell-like phenotype in head and neck cancer cells // Int. J. Oncol. 2014; 44:693-699). Эпителиально-мезенхимальный переход представляет собой обратимый клеточный процесс, который индуцируется главным образом паракринным механизмом малых молекул, связанных с фибробластами, ассоциированных с опухолью, где фактор роста опухоли β1 (TGF-β1) является одним из наиболее важных медиаторов (см. Fullar A., Kovalszky I., Bitsche М. et al. Tumor cell and carcinoma-associated fibroblast interaction regulates matrix metalloproteinases and their inhibitors in oral squamous cell carcinoma // Exp. Cell Res. 2012; 318:1517-1527; см. Xu L.N., Xu B.N., Cai J. et al. Tumor-associated fibroblast-conditioned medium promotes tumor cell proliferation and angiogenesis // Genet Mol. Res. 2013; 12: 5863-5871). TGF-β1 взаимодействует с аналогичными рецепторами TGF-β1 типа I и II, тирозин-киназы, которые активируют сигнальные пути Smad 2 и 3, образуя комплексы с Smad 4, которые действуют как факторы транскрипции, связанные с активацией ЕМТ (см. Katsuno Y., Lamouille S., Derynck R. TGF-β signaling and epithelial-mesenchymal transition in cancer progression // Curr. Opin. Oncol. 2013; 25:76-84). В исследовании на линиях клеток плоскоклеточного рака головы и шеи было показано, что снижение SMAD4 путей регуляции играет важную роль в индукции ЭМП и резистентности к цетуксимабу (см. Cheng Н, Fertig EJ, Ozawa Н, Hatakeyama Н, Howard JD et al. Decreased SMAD4 expression is associated with induction of epithelial-to-mesenchymal transition and cetuximab resistance in head and neck squamous cell carcinoma // Cancer Biol. Ther. - January 1, 2015; 16 (8); 1252-8).
Каскад реакций, вызываемый воздействием цетуксимаба на EGFR, близко связан с фактором роста эндотелия VEGF и ангиогенезом через фосфатидилинозитол-3-киназу, протеин-серин/треонин-киназу и mTOR. Соответственно, одним из важнейших противоопухолевых эффектов цетуксимаба является блокирование повышенной продукции VEGF и последующего неоангиогенеза в опухоли (см. Воронцова К.А., Черноглазова Е.В., Вышинская Г.В. таргетные препараты во второй линии противоопухолевой терапии диссеминированного колоректального рака // медицинский совет. - 2015. - №8. - С. 91-96). В ряде исследований было показано, что повышенная экспрессия VEGF связана с неблагоприятным прогнозом при ПКПР (см. Игнатова А.В., Мудунов A.M., Нариманов М.Н. Прогностическое значение биомаркеров при плоскоклеточном раке полости рта. Обзор литературы // Опухоли головы и шеи. - 2014. - №4. - С. 28-33).
Учитывая высокую стоимость таргетной терапии, поиск биомаркеров, позволяющих оценить эффективность терапии цетуксимабом у больных ПКПР, является достаточно актуальным.
Из патентных источников известно изобретение «Способы предсказания ответа трижды негативного рака молочной железы на терапию» (Патент на изобретение RU 2558931 С2, опубл. 10.08.2015, Бюл. №5).Способ включает: лизирование опухолевых клеток, взятых от трижды негативной опухоли молочной железы, для получения клеточного экстракта; определение уровня экспрессии VEGFR2 в клеточном экстракте; и сравнение полученного уровня экспрессии с эталонным уровнем экспрессии VEGFR2. Наличие низкого уровня экспрессии VEGFR2 предсказывает ответ на терапию противоопухолевым средством, где противоопухолевое средство представляет собой комбинацию бевацизумаба (Авастин), карбоплатина и паклитакселя. Однако данный способ прогнозирует ответ опухоли молочной железы, а не опухолей языка и слизистой дна полости рта и касается таргетного препарата бевацизумаб.
Также известен «Способ прогнозирования эффективности терапии эверолимусом у Больных метастатическим раком почки» (патент на изобретение RU 2616533 С1, опубл. 17.04.2017, Бюл. №11).Для этого в ткани опухоли на дооперативном этапе лечения авторы предлагают определять phospho-m-TOR и дополнительно определять содержание фактора, индуцированного гипоксией HIF-1α, сосудистого эндотелиального фактора роста VEGF и его рецептора VEGFR2. При значениях HIF-1α, VEGF, VEGFR2 в лунке более 16,2 УЕ/ мг белка в лунке; 100,5 и 82,2 пг/мг белка соответственно а также уровне phospho-m-TOR менее 5,5 пг/мг белка прогнозируют высокую эффективность терапии эверолимусом. При значениях HIF-1α, VEGF, VEGFR2 менее 16,2 УЕ/ мг белка в лунке, 100,5 и 82,2 пг/мг белка соответственно и уровне phospho-m-TOR более 5,5 пг/мг белка прогнозируют низкую эффективность терапии эверолимусом. Однако данный способ является дорогостоящим, поскольку проводят определение четырех показателей и не может быть применим для прогнозирования эффективности терапии цетуксимабом у больных плоскоклеточным раком языка и слизистой дна полости рта.
Наиболее близким к предлагаемому, является «Способ прогнозирования резистентности опухоли к таргетной терапии цетуксимабом у больных плоскоклеточным раком языка и слизистой дна полости рта» (Патент на изобретение RU 2626682 С1, опубл. 31.01.2017, Бюл. №12), включающий исследование крови, отличающийся тем, что за два дня до начала полихимиотерапевтического лечения с включением таргетной терапии цетуксимабом, у больного плоскоклеточным раком языка и слизистой дна определяют EGF, sEGFR, затем рассчитывают соотношение EGF/sEGFR и при значении этого соотношения в пределах 55,3-66,9 прогнозируют отсутствие резистентности опухоли к терапии цетуксимабом, а при значении этого показателя в пределах 92,6-117,8 прогнозируют наличие резистентности опухоли к терапии цетуксимабом. Однако в данном способе исследуют содержание других ростовых факторов, исследование проводят в крови, а не в опухолевой ткани, кроме того способ осуществляют до начала полихимиотерапевтического лечения, а не на его этапе - после второго курса полихимиотерапии с включением цетуксимаба.
Техническим результатом предлагаемого изобретения является определение эффективности таргетной терапии цетуксимабом у больных плоскоклеточным раком языка и слизистой дна полости рта.
Технический результат достигается тем, что после второго курса полихимиотерапевтического лечения с включением таргетной терапии цетуксимабом у больного плоскоклеточным раком языка и слизистой дна полости рта проводят трепанбиопсию опухоли, в полученном опухолевом образце определяют уровень факторов роста VEGF-A и TGF-β, рассчитывают соотношение VEGF-A/TGF-β и при величине этого соотношения ≥0,850 прогнозируют высокую эффективность терапии цетуксимабом, а при значении его ≤0,384 прогнозируют низкую эффективность терапии цетуксимабом; при значениях между указанными интервалами считают результат не определенным.
Способ осуществляют следующим образом.
Больным с гистологически верифицированным плоскоклеточным раком языка и слизистой дна полости рта T3-4N0-1M0 проводят полихимиотерапевтическое лечение с включением таргетной терапии цетуксимабом. Цетуксимаб вводят в дозировке 400 мг/м2 в 1 день и 250 мг/м2 еженедельно в сочетании с химиотерапией: цисплатин 100 мг/м2 в/в капельно в 1 день, 5-фторурацил 1000 мг/м2 в/в 96-часовая непрерывная инфузия 21-дневного цикла. После второго курса полихимиотерапии с включением цетуксимаба больному проводят трепанбиопсию опухоли. Образцы опухоли замораживают для дальнейшего хранения при температуре -70°C с последующим биохимическим исследованием. Перед исследованием образцы тканей гомогенизируют. Затем в 10% цитозольных фракциях, приготовленных на калий-фосфатном буфере рН 7.4, содержащим 0,1% Твин-20, методом ИФА с использованием стандартных тест-систем определяют уровень ростового фактора VEGF-A (BenderMedSystem, Австрия) и уровень ростового фактора TGF-β (BenderMedSystem, Австрия), рассчитывают соотношение VEGF-A/TGF-β и при величине этого соотношения ≥0,850 прогнозируют высокую эффективность терапии цетуксимабом, а при значении его ≤0,384 прогнозируют низкую эффективность терапии цетуксимабом. При значениях между указанными интервалами считают результат не определенным.
Изобретение «Способ прогнозирования эффективности таргетной терапии цетуксимабом у больных плоскоклеточным раком языка и слизистой дна полости рта» является промышленно применимым и может быть многократно воспроизведено в здравоохранении в лечебных учреждениях специализированного профиля при лечении онкологических больных данной локализацией злокачественного процесса.
Приводим примеры клинического применения способа.
Клинический пример №1.
Больной Р., 60 лет, поступил в отделение противоопухолевой лекарственной терапии №1 РНИОИ 05.09.2017 с диагнозом: рак языка T3N1M0, с метастазами в лимфоузлы шеи слева, кл.гр.2. Жалобы при поступлении на незаживающую язву в правой половине языка, боли в ротовой полости. На догоспитальном этапе выполнена биопсия опухоли, получено гистологическое заключение - G2 плоскоклеточный рак.
Status localis: на боковой поверхности языка справа опухолевый инфильтрат размерами до 3,5 см в диаметре, с нечеткими краями. Лимфоузлы шеи слева до 1 см.
Больному начата полихимиотерапия на фоне введения таргетной терапии. Цетуксимаб вводили в дозировке 400 мг/м2 в 1 день и 250 мг/м2 еженедельно в сочетании с химиотерапией: цисплатин 100 мг/м2 в/в капельно в 1 день, 5-фторурацил 1000 мг/м2 в/в 96-часовая непрерывная инфузия 21-дневного цикла.
После двух курсов полихимиотеравтического лечения по вышеописанной схеме была выполнена повторная трепанбиопсия опухоли с целью определения показателей VEGF-A и TGF-β. Соотношение VEGF-A/TGF-β у данного пациента составило 0,870, что прогнозирует высокую эффективность терапии цетуксимабом.
Пациенту было продолжено проведение полихимиотерапии с еженедельным введением цетуксимаба до 6 курсов.
После 6 курсов полихимиотерапевтического лечения с таргетной терапией цетуксимабом объективно отмечена положительная динамика: уменьшение опухоли на языке более чем в 2 раза - размер опухоли до 1,5 см (степень RECIST 55%), купирование болевого синдрома. Лимфоузлы шеи четко не пальпируются. Выполнено УЗИ шейно-надключичных, подчелюстных лимфоузлов: данных за поражение не выявлено.
В настоящее время больной наблюдается без признаков прогрессирования заболевания.
Клинический пример №2.
Больной К., 62 лет, поступил в отделение противоопухолевой лекарственной терапии №1 РНИОИ 10.09.2017 с диагнозом: рак слизистой дна полости рта T3N1M0, с метастазами в лимфоузлы шеи справа, кл.гр.2. Жалобы при поступлении на дискомфорт и боли во время приема пищи, язву в ротовой полости. Выполнена биопсия опухоли, получено гистологическое заключение - G2 плоскоклеточный рак.
Status localis: на слизистой дна полости рта слева в передних отделах опухолевый инфильтрат с изъязвлением 3,5×1,5 см. Лимфоузлы справа до 1,5 см в диаметре.
Больному начата полихимиотерапия на фоне введения таргетной терапии. Цетуксимаб вводили в дозировке 400 мг/м2 в 1 день и 250 мг/м2 еженедельно в сочетании с химиотерапией: цисплатин 100 мг/м2 в/в капельно в 1 день, 5-фторурацил 1000 мг/м2 в/в 96-часовая непрерывная инфузия 21-дневного цикла.
После двух курсов полихимиотеравтического лечения по вышеописанной схеме выполнена повторная трепанбиопсия опухоли с целью определения содержания VEGF-A и TGF-β. Соотношение VEGF-A/TGF-β у данного пациента составило 0,310, что прогнозирует низкую эффективность терапии цетуксимабом.
Пациенту было продолжено лечение по вышеописанной схеме, однако после 6 курсов полихимиотерапии отмечена отрицательная динамика. Объективно: в ротовой полости сохраняется инфильтрат прежних размеров, пальпируются увеличенные шейные лимфоузлы справа. На УЗИ лимфоузлы шеи справа до 2,5 см (увеличение размера лимфоузла на 45%). Учитывая прогрессирование заболевания, больному проведено хирургическое лечение в объеме: резекция дна полости рта, шейная лимфаденэктомия, трахеостомия. Гистологическое заключение: G2 плоскоклеточный рак с ороговением, в трех из девяти исследованных лимфатических узлов обширные метастазы плоскоклеточного рака. Далее пациент получал лучевую терапию по месту жительства.
Указанным способом было обследовано 30 больных плоскоклеточным раком языка и слизистой дна полости рта, медиана возраста составляла 57,2 года. Критерии включения в исследование предусматривали наличие у пациента плоскоклеточного рака языка и слизистой полости рта (T3-4N0-1М0), наличие рецидива заболевания или регионарного метастазирования, отсутствие отдаленных метастазов, ECOG≤l, нормальную функцию печени, почек и костного мозга. Оценивалось время до прогрессирования, степень дифференцировки опухоли, стадия заболевания.
Из 30 обследованных пациентов у 20 имела место высокая эффективность терапии цетуксимабом - у данной группы больных было отмечено развитие регрессии различной степени выраженности, а у 10 больных имела место низкая эффективность таргетной терапии - у этой группы больных были отмечены стабилизация или прогрессирование заболевания.
Технико-экономическая эффективность предложенного способа заключается в возможности индивидуализировать лечение больных плоскоклеточным раком языка и слизистой дна полости рта, своевременно проводить изменения схем лечебных мероприятий, что позволит достичь максимального клинического и экономического эффекта, учитывая высокую стоимость таргетных препаратов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования резистентности опухоли к таргетной терапии цетуксимабом у больных плоскоклеточным раком языка и слизистой дна полости рта | 2016 |
|
RU2626682C1 |
| СПОСОБ ЛЕЧЕНИЯ ПЛОСКОКЛЕТОЧНОГО Р-16 ПОЗИТИВНОГО РАКА РОТОГЛОТКИ | 2020 |
|
RU2751818C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАДИОЧУВСТВИТЕЛЬНОСТИ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ ВЕРХНИХ ДЫХАТЕЛЬНЫХ ПУТЕЙ | 2020 |
|
RU2735982C2 |
| Способ прогнозирования эффективности консервативного лечения плоскоклеточного рака ротоглотки | 2023 |
|
RU2817324C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ПРОГРЕССИИ В ОТДАЛЕННОМ ПЕРИОДЕ У БОЛЬНЫХ ПЛОСКОКЛЕТОЧНЫМ РАКОМ ГОЛОВЫ И ШЕИ | 2021 |
|
RU2765013C1 |
| СПОСОБ ЛЕЧЕНИЯ ПЛОСКОКЛЕТОЧНОГО РАКА ОРОФАРИНГЕАЛЬНОЙ ОБЛАСТИ | 2010 |
|
RU2429032C1 |
| Способ лечения местно-распространенного рака ротоглотки | 2020 |
|
RU2739294C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ МЕСТНО-РАСПРОСТРАНЕННЫМ РАКОМ ГЛОТКИ | 2005 |
|
RU2289364C1 |
| СПОСОБ ЛЕЧЕНИЯ ПЛОСКОКЛЕТОЧНОГО РАКА РОТОГЛОТКИ | 2018 |
|
RU2689875C2 |
| Способ дифференциальной диагностики рецидивных плоскоклеточных опухолей полости рта с фиброзом и гиперкератозом | 2018 |
|
RU2702974C1 |
Изобретение относится к медицине, а именно к онкологии, и может быть использовано для прогнозирования эффективности таргетной терапии цетуксимабом у больных плоскоклеточным раком языка и слизистой дна полости рта. Проводят исследование опухолевой ткани. После второго курса полихимиотерапевтического лечения с включением таргетной терапии цетуксимабом у больного плоскоклеточным раком языка и слизистой дна полости рта проводят трепанбиопсию опухоли. В полученном опухолевом образце определяют уровень факторов роста VEGF-A и TGF-β, рассчитывают соотношение VEGF-A/TGF-β. При величине этого соотношения ≥0,850 прогнозируют высокую эффективность терапии цетуксимабом. При значении его ≤0,384 прогнозируют низкую эффективность терапии цетуксимабом. При значениях между указанными интервалами считают результат не определенным. Способ обеспечивает определение эффективности таргетной терапии цетуксимабом у больных плоскоклеточным раком языка и слизистой дна полости рта за счет исследования содержания ростовых факторов VEGF-A и TGF-β в опухолевой ткани на этапе полихимиотерапевтического лечения – после второго курса полихимиотерапии с включением цетуксимаба. 2 пр.
Способ прогнозирования эффективности таргетной терапии цетуксимабом у больных плоскоклеточным раком языка и слизистой дна полости рта, включающий исследование опухолевой ткани, отличающийся тем, что после второго курса полихимиотерапевтического лечения с включением таргетной терапии цетуксимабом у больного плоскоклеточным раком языка и слизистой дна полости рта проводят трепанбиопсию опухоли, в полученном опухолевом образце определяют уровень факторов роста VEGF-A и TGF-β, рассчитывают соотношение VEGF-A/TGF-β и при величине этого соотношения ≥0,850 прогнозируют высокую эффективность терапии цетуксимабом, а при значении его ≤0,384 прогнозируют низкую эффективность терапии цетуксимабом; при значениях между указанными интервалами считают результат не определенным.
| Способ прогнозирования резистентности опухоли к таргетной терапии цетуксимабом у больных плоскоклеточным раком языка и слизистой дна полости рта | 2016 |
|
RU2626682C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИСХОДОВ ХИМИОЛУЧЕВОЙ ТЕРАПИИ ПЛОСКОКЛЕТОЧНЫХ КАРЦИНОМ ГОЛОВЫ И ШЕИ | 2012 |
|
RU2505818C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ РЕЦИДИВОВ У БОЛЬНЫХ РАКОМ СЛИЗИСТОЙ ОБОЛОЧКИ РТА | 2016 |
|
RU2635535C1 |
| БОЛОТИНА Л.В | |||
| и др | |||
| Практические рекомендации по лечению злокачественных опухолей головы и шеи | |||
| Злокачественные опухоли | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| ANSELL A | |||
| et al | |||
| Epidermal growth factor is a potential biomarker for poor cetuximab response in tongue cancer cells | |||
| J | |||
Авторы
Даты
2020-02-05—Публикация
2019-03-25—Подача