Настоящее изобретение относится к медицине и биологии, а более конкретно к цитологии, и может быть использовано для диагностики мутагенного (цитогенетического) и цитотоксического действия различных экзогенных и эндогенных факторов на организм человека и животных, а также для углубленного цитологического анализа.
Печень является основным органом метаболизма различных экзогенных и эндогенных химических соединений, при этом основные функционально активные клетки печени (гепатоциты) одними из первых подвергаются воздействию этих факторов. Их поражение неблагоприятно сказывается на состоянии других органов и всего организма в целом. Известно, что после рождения организма одноядерные диплоидные гепатоциты в течение короткого времени становятся полиплоидными, т.е. у них в 2, 4 или более раз увеличивается количество геномных наборов в клетке, поэтому нормальная популяция гепатоцитов в зрелом организме, в основном, содержит одноядерные или двуядерные полиплоидные клетки. У половозрелых мышей и крыс доля полиплоидных гепатоцитов составляет приблизительно 90%, а одноядерных диплоидных - только 10%, у человека соответственно - около 60% и 40%.
В настоящее время установлено, что плоидность гепатоцитов повышается при старении организма, после частичной гепатоэктомии, при воздействии оксидативного стресса, ряда токсикантов, метаболической перегрузке. В то же время отмечено снижение плоидности гепатоцитов в процессе образования гепатоклеточных карцином (Wang M-J. et al. 2017).
Широко обсуждается роль полиплоидных гепатоцитов в развитии патологии: жировой дистрофии, канцерогенеза. Выдвигаются новые идеи о положительной роли анеуплоидных клеток, образующихся в результате стресса. Так, Duncan A.W. с соавторами (2012) показали, что полиплоидные гепатоциты могут обеспечивать адаптацию печени при повреждении вследствие повышения доли клеток с количественно отличающимся геномом («повышения генетического разнообразия»). Важной, все более распространенной в мире патологией, вызывающей общественное беспокойство, в настоящее время является неалкогольная жировая болезнь печени (стеатоз печени). В последнее время особое значение придают изучению профиля полиплоидизации гепатоцитов при этом заболевании. Следовательно, определение индексов плоидности и ядерности может иметь прогностическое значение в отношении онкопатологии или других патологических состояний организма, что имеет большое значение для клиницистов.
Таким образом, новые подходы к изучению разных патологических состояний печени связаны с оценкой состояния гепатоцитов на клеточном уровне, их плоидности, определении доли генетически поврежденных клеток. Морфологические исследования печени, в основном, проводят на гистологических препаратах или биопсийных мазках. Однако это не позволяет оценивать каждую клетку индивидуально и проводить количественную оценку с определением доли генетически поврежденных клеток или клеток определенного класса ядерности/плоидности.
Для анализа цитогенетического действия различных факторов на клетки в настоящее время широко используют микроядериый тест - учитывают количество клеток с экстрануклеарными телами (микроядрами). Этот тест проводят как стандартный на полихроматофильных эритроцитах костного мозга мышей. Клетки других органов для этой цели используют редко, несмотря на то, что они могут быть более информативны. Основная причина - необходимость «разделить орган» на отдельные клетки (провести диссоциацию), сделать мазки, подобрать окраску для ядра и цитоплазмы, чтобы под микроскопом можно было анализировать отдельно лежащие клетки, хорошо окрашенные с четко определяемым ядром и, если есть, с экстрануклеарными структурами (микроядрами и протрузиями). Таких хорошо окрашенных отдельно лежащих клеток на препарате от каждого животного должно быть достаточное количество (не менее 1000). Эти критерии относятся, в том числе, к гепатоцитам.
Наиболее близким к заявленному является способ подготовки и цитомный анализ гепатоцитов лабораторных животных и человека для оценки цитогенетического и цитотоксического действия факторов разной природы, включающий получение отдельно лежащих гепатоцитов путем выделения печени у животных после эвтаназии или биопсии у человека, фиксации органа в 10% формалине, щелочной диссоциации клеток в течение 16 часов при 20°С, нанесения суспензии клеток методом мазка на сухое предметное стекло, окрашивание ацетоорсеином с докраской цитоплазмы светлым зеленым, анализа с помощью светового микроскопа 1000 гепатоцитов, описанный в методических рекомендациях «Оценка мутагенной активности факторов окружающей среды в клетках разных органов млекопитающих микроядерным методом» (Методические рекомендации. М., Межведомственный научный совет по экологии человека и гигиене окружающей среды, 2001. 22 с.), которые содержат раздел: «Микроядерный тест на гепатоцитах мышей и крыс». В них описана методика приготовления, диссоциации и окраски препаратов гепатоцитов.
Недостатками известного способа являются:
- длительность процедуры подготовки препаратов к исследованию;
- оценка цитогенетического эффекта исследуемых факторов только по одному показателю - учету клеток с микроядрами;
- оценка с помощью подготовленных препаратов только цитогенетического эффекта без учета цитотоксического действия.
Достигаемым при использовании предлагаемого изобретения техническим результатом является упрощение и удешевление способа получения клеток, повышение достоверности, информативности и эффективности оценки действия различных факторов на гепатоциты экспериментальных животных и человека путем одновременного анализа цитогенетического и цитотоксического действия.
Указанный технический результат достигается тем, что способ подготовки гепатоцитов лабораторных животных и человека, включает получение отдельно лежащих гепатоцитов путем выделения печени у животных после эвтаназии или биопсии у человека, фиксации органа в 10% формалине, щелочной диссоциации клеток, нанесения суспензии клеток методом мазка на сухое предметное стекло, окрашивание ацетоорсеином с докраской цитоплазмы светлым зеленым, анализа с помощью светового микроскопа 1000 гепатоцитов, при этом щелочную диссоциацию проводят при температуре 25-37°С в течение трех часов.
Цитомный анализ гепатоцитов лабораторных животных и человека, включающий определение показателей цитогенетического действия, таких как клетки с микроядрами, дополнительно предполагает учет клеток с ядерными протрузиями, клеток с межъядерными мостами, сумму клеток с этими показателями, шесть цитологических показателей, количественные изменения которых указывают на цитотоксическое действие исследуемых факторов, такие как одноядерные диплоидные (2n) гепатоциты, тетраплоидные (4n) гепатоциты, полиплоидные (≥8n) гепатоциты, двуядерные диплоидные (2n+2n) гепатоциты, тетраплоидные (4n+4n) гепатоциты и полиплоидные (≥8n+8n) гепатоциты, при этом определяют индекс плоидности как отношение суммы полиплоидных гепатоцитов к сумме диплоидных гепатоцитов и индекс ядерности как отношение суммы двуядерных гепатоцитов к сумме одноядерных гепатоцитов.
Проведение щелочной диссоциации при температуре 25-37°С в течение трех часов, позволяет значительно сократить время подготовки препаратов гепатоцитов к исследованию, при этом можно приготовить препараты в течение одного рабочего дня; не требуется суточный контроль процедуры.
Учет трех дополнительных цитогенетических показателей, шести цитологических показателей и двух индексов, таких как индекс плоидности и индекс ядерности гепатоцитов, позволяет значительно повысить информативность исследования, совместить оценку цитогенетического и цито токсического действия и определять ассоциации исследованных показателей, провести интегральную оценку влияния исследуемых факторов на печень, что очень важно для фундаментальной биологии и медицины.
Препараты отдельно лежащих гепатоцитов получают путем выделения печени у животных после эвтаназии или биопсии у человека, фиксации органа в 10% формалине, щелочной диссоциации клеток при температуре 25-37°С в течение трех часов, с помощью 50% КОН, нанесения суспензии клеток методом мазка на сухое предметное стекло, окрашивание ацетоорсеином с докраской цитоплазмы светлым зеленым, анализируют с помощью светового микроскопа 1000 гепатоцитов, определяют четыре показателя цитогенетического действия, такие как клетки с микроядрами, клетки с ядерными протрузиями, клетки с межъядерными мостами, сумму клеток с этими показателями, шесть цитологических показателей, количественные изменения которых указывают на цитотоксическое действие исследуемых факторов, такие как одноядерные диплоидные (2n) гепатоциты, тетраплоидные (4n) гепатоциты, полиплоидные (≥8n) гепатоциты, двуядерные диплоидные (2n+2n) гепатоциты, тетраплоидные (4n+4n) гепатоциты и полиплоидные (≥8n+8n) гепатоциты, индекс плоидности и индекс ядерности.
Предлагаемый способ подготовки материала к микроскопическому исследованию удобен, прост в исполнении, экономичен, не требует специального оборудования.
Микроядра отражают наличие хромосомных и геномных мутаций. Появление микроядер может быть связано либо с повреждением ДНК (микроядро образовано фрагментом хромосомы), либо с повреждением веретена деления (микроядро образовано одной или несколькими отставшими хромосомами, не вошедшими в основное ядро).
Протрузии - это ДНК-содержащие образования, прочно связанные с ядром, имеющие различную форму. По разным предположениям образуются в результате нарушения образования аберрантных хромосом и разрыва в процессе митоза хроматидных или хромосомных мостов. Также могут быть результатом выброса из ядра амплифицированной ДНК или комплексов репарации ДНК. В целом отражают цитогенетическое действие факторов.
Межъядерные мосты появляются в результате нерасхождения хромосом в процессе митоза. Микроядра, протрузии и мосты являются маркерами мутагенного эффекта.
Для оценки цитогенетического действия при исследовании интерфазных гепатоцитов мы предлагаем оценивать интегральный показатель - сумму клеток с цитогенетическими нарушениями в промилле.
Наличие цитогенетического действия исследуемого фактора диагностируют, если он вызывает статистически значимое повышение частоты гепатоцитов с микроядрами, протрузиями, межъядерными мостами и/или суммарно всех трех показателей (суммы клеток с цитогенетическими нарушениями в промилле) в группе воздействия по сравнению с контролем.
Одноядерные и двуядерные диплоидные, тетраплоидные и полиплоидные клетки определяют морфологически, учитывая количество ядер в клетке (одно или два) и размер ядер. Соответственно размер тетраплоидных ядер в два раза больше, чем двуядерных, а октоплоидных в два раза больше, чем тетраплоидных.
Образование двуядерных клеток связано с нарушением цитокинеза (формирования клеточной перегородки) после деления ядра надвое в процессе митоза. При образовании полиплоидных ядер происходит нарушение функции веретена деления (хромосомы не расходятся к полюсам и вместо двух дочерних ядер формируется одно полиплоидное). Процесс образования двуядерных и/или полиплоидных клеток рассматривается как показатель окончательной дифференцировки гепатоцитов и старения.
Мы предлагаем оценивать два интегральных показателя: индекс плоидности и индекс ядерности.
Индекс плоидности - отношение суммы полиплоидных гепатоцитов к сумме диплоидных гепатоцитов.
Индекс ядерности - отношение суммы двуядерных гепатоцитов к сумме одноядерных гепатоцитов.
Повышенный по отношению к контролю индекс плоидности указывает на повышение доли полиплоидных клеток у отдельного организма или в целом в опытной группе. Повышенный индекс ядерности, соответственно, указывает на повышение доли двуядерных клеток.
Эффективность предлагаемого цитомного анализа гепатоцитов апробирована при исследовании цитогенетического и цитотоксического действия факторов физической и химической природы: рентгеновского излучения (R-излучения) и сочетанного действия R-излучения и противолучевого препарата беталейкина.
Материал для исследования получен и проанализирован указанным выше способом. Исследованные показатели подтверждены примерами 1-2, результаты которых представлены в таблицах 1, 2 и на чертеже.
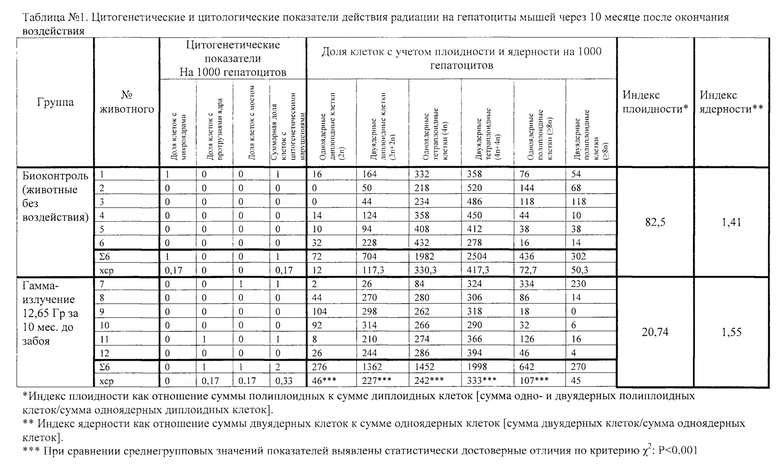
Пример 1. Хронический эксперимент проведен на самцах мышей F1(CBAxC57BL/6) 2 мес. возраста массой 18-13 г в начале эксперимента. Сравнивали две группы животных, каждая из которых состояла из 6 мышей: контрольную (мыши без воздействия) и опытную, животных которой облучали в начале исследования в дозе 12,65 Гр при мощности дозы 10 микрорентген в час. Эвтаназию животных, выделение печени для исследования и приготовление препаратов по указанной выше методике проводили через 10 месяцев после воздействия.
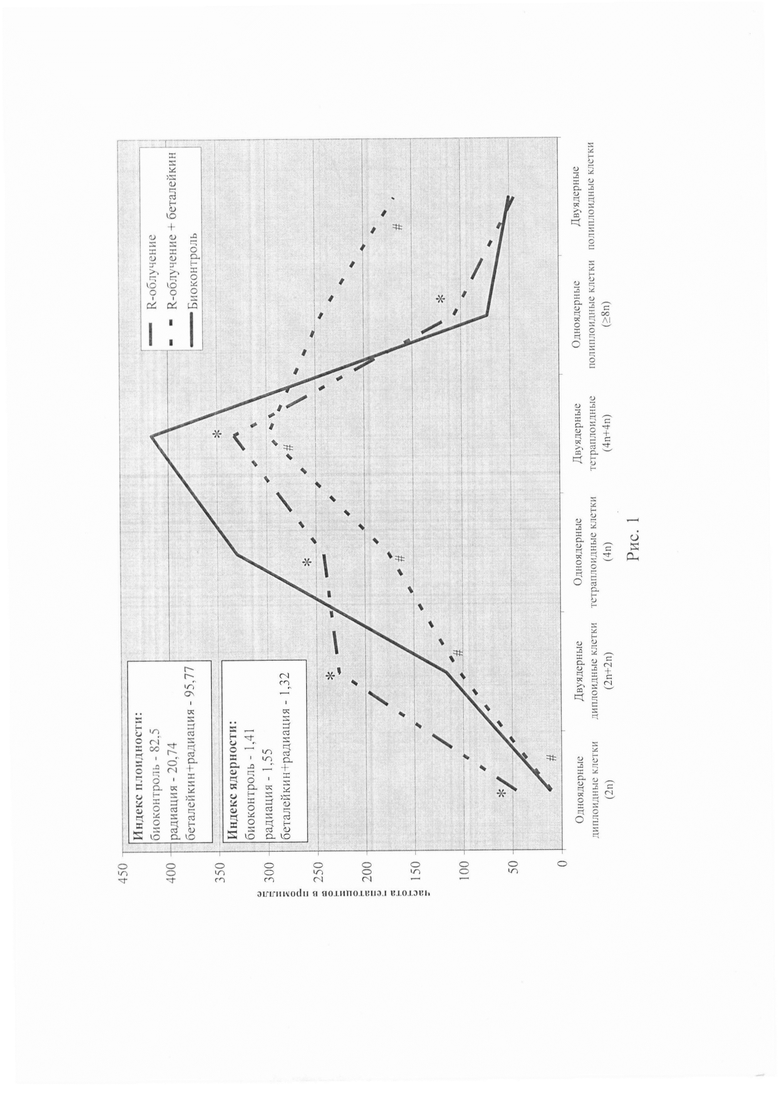
Результаты исследования представлены в таблице 1. Цитогенетическое действие R-излучения не выявлено при сравнении с контролем по показателям: частота клеток с микроядрами, протрузиями, межъядерными мостами, суммой клеток с цитогенетическими нарушениями. Цитотоксичсское действие R-излучения выявлено по сравнению с контролем при анализе цитологических показателей, характеризующих ядерность и плоидность. Отличия по всем показателям, кроме частоты двуядерных полиплоидных клеток оказались высоко значимы (Р<0,001). Индекс плоидности в контрольной группе составил 82,5, в опытной группе он был в 4 раза ниже и составил 20,74. Индекс ядерности, напротив, был немного выше, чем в контрольной группе (1,55 - в опыте, 1,41 - в контроле,). Эти данные представляют большой интерес, поскольку указывают на снижение полиплоидизации гепатоцитов через 10 месяцев после воздействия рентгеновского излучения.
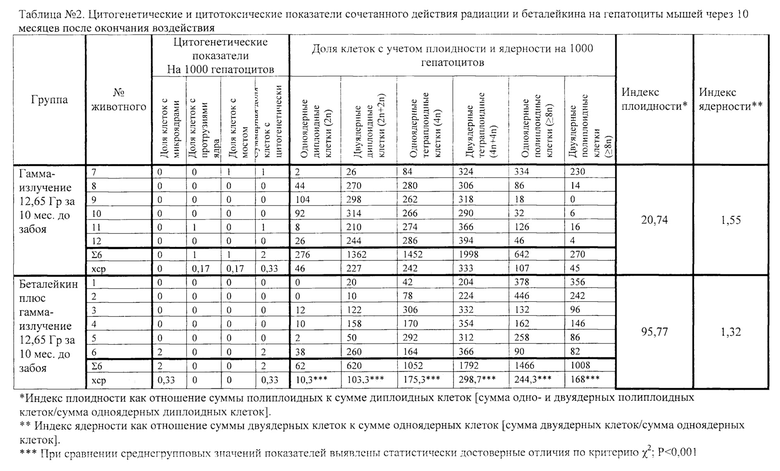
Пример 2. Хронический эксперимент проведен на самцах мышей F1(CBAxC57BL/6) 2 мес. возраста массой 18-23 г в начале эксперимента. Сравнивали две группы животных, каждая из которых состояла из 6 мышей, которых одновременно в начале исследования подвергали рентгеновскому облучению в дозе 12,65 Гр при мощности дозы 10 микрорентген в час. При этом во второй группе мышам внутрибрюшинно вводили беталейкин в дозе 3 мкг/кг за 2 часа до облучения. Эвтаназию животных, выделение печени и приготовление препаратов по указанной выше методике проводили через 10 месяцев после воздействия.
Результаты исследования представлены в таблице 2. Цитогенетическое действие R-излучения не выявлено при сравнении двух обследованных групп животных по показателям: частота клеток с микроядрами, протрузиями, межъядерными мостами, суммой клеток с цитогенетическими нарушениями. Сравнение цитотоксического действия R-излучения при изолированном воздействии и в сочетании с беталейкином выявило статистически достоверные отличия по всем цитологическим показателям, характеризующим ядерность и плоидность (Р<0,001). Индекс плоидности при изолированном действии R-излучения составил 20,74, а на фоне предварительного введения беталейкина он был почти в пять раз выше (95,77). Индекс ядерности, напротив, немного снижался с 1,55 до 1,32. Эти данные указывают на нормализацию плоидности и ядерности гепатоцитов, приближающейся к контрольному уровню (таблица 1) у животных, которым предварительно вводили противолучевой препарат беталейкин.
На рисунке 1, иллюстрирующем оба примера, приведена частота гепатоцитов разной плоидности/ядерности у животных трех групп: контрольной (сплошная линия); для группы животных через 10 месяцев после воздействия R-облучения (линия с чередованием коротких и длинных штрихов) и для группы рентгеновского облучения на фоне противолучевого средства беталейкина (линия с короткими штрихами). Статистически значимые отличия между показателями для первого примера отмечены звездочками; для второго - решетками. Из рисунка видно, что данные при сравнении каждого класса гепатоцитов кроме двуядерных полиплоидных клеток отличаются статистически достоверно.
В то же время способ, изложенный в прототипе, направленный на учет только клеток с микроядрами, не позволил бы в этих экспериментах выявить цитотоксическое действие радиации и эффективность противолучевого препарата беталейкина по показателям плоидности и ядерности, а также потребовал бы использование более сложных и длительных приемов подготовки препаратов гепатоцитов к исследованию.
Таким образом, предлагаемый способ цитомного анализа препаратов гепатоцитов для оценки цитогенетического и цитотоксического действия факторов разной природы является более информативным, простым в исполнении и экономически выгодным.
Примеры реализации предлагаемого технического решения.
Пример 1. Подготовка гепатоцитов к исследованию при температуре 25°С.
При подготовке гепатоцитов, выделенных у животных после эвтаназии зафиксированных в 10% формалине, проведении щелочной диссоциации клеток 50% КОН при 25°С в течение трех часов, нанесения суспензии клеток методом мазка на сухое предметное стекло, окрашивания ацетоорсеином с докраской цитоплазмы светлым зеленым получены следующие результаты: клетки лежат в «комках», конгломератах, отдельно лежащие клетки отсутствуют, что не позволяет увидеть ядро в каждой клетке, определить его плоидность, т.е. провести анализ и количественно учитывать показатели цитогенетического и цитотоксического действия невозможно.
Пример 2. Подготовка гепатоцитов к исследованию при температуре 37°С.
При подготовке гепатоцитов, выделенных у животных после эвтаназии, зафиксированных в 10% формалине, проведении щелочной диссоциации клеток 50% КОН при 37°С в течение трех часов, нанесения суспензии клеток методом мазка на сухое предметное стекло, окрашивания ацетоорсеином с докраской цитоплазмы светлым зеленым получены следующие результаты: клетки лежат отдельно, в каждой клетке четко определяется ядро, можно определить экстрануклеарные структуры (микроядра, протрузии, межъядерные мосты), определить количество ядер, их размер и, соответственно, плоидность, т.е. провести указанный цитомный анализ.
Пример 3. Цитомный анализ гепатоцитов для оценки цитогенетического и цитотоксического действия четыреххлористого углерода
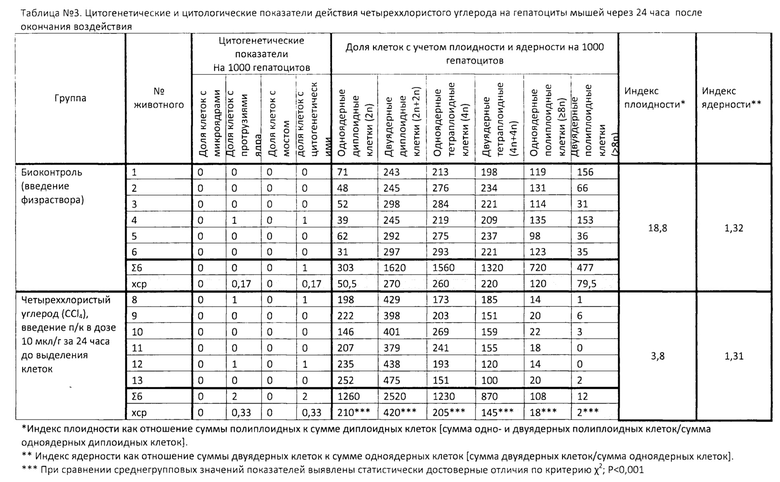
В таблице 3 представлены результаты исследования цитогенетического и цитотоксического действия четыреххлористого углерода. Эксперимент проведен на самцах мышей F1(CBAxC57BL/6) 2 мес. возраста массой 18-20 г, которым подкожно вводили токсикант в концентрации 10 мкг/г массы мыши. Мышам контрольной группы вводили по той же схеме физиологический раствор. Эвтаназию животных, выделение печени и приготовление препаратов по указанной выше методике проводили через 24 часа после воздействия.
Цитогенетическое действие четыреххлористого углерода не выявлено при сравнении двух обследованных групп животных по показателям: частота клеток с микроядрами, протрузиями, межъядерными мостами, суммой клеток с цитогенетическими нарушениями. Цитотоксическое действие четыреххлористого углерода выявлено при сравнении всех цитологических показателей, характеризующих ядерность и плоидность (Р<0,001). Индекс плоидности у животных контрольной группы составил 18,8, а у мышей, которым вводили четыреххлористый углерод, он снизился до 3,8. Индекс ядерности в краткосрочном эксперименте не изменился и составил 1,32 и 1,31 в контрольной и опытной группах. Полученные данные указывают на быстрое снижение частоты полиплоидных клеток печени в ответ на действие токсиканта. Механизмы и значимость таких изменений в настоящее время обсуждается в научной литературе.
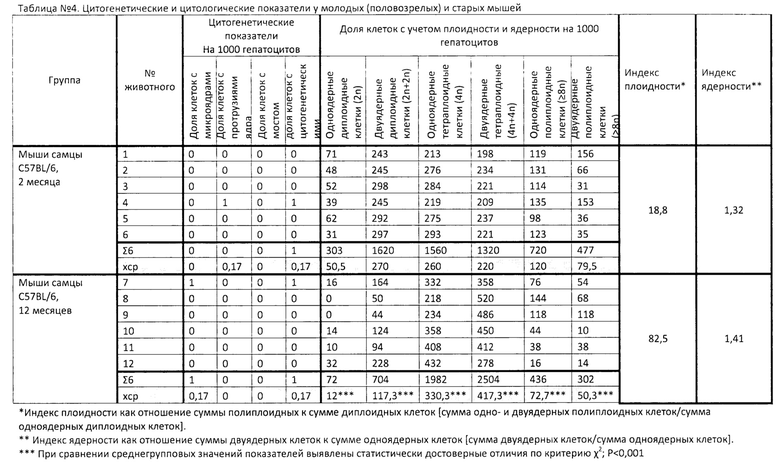
Пример 4. Цитомный анализ гепатоцитов для оценки цитогенетических и цитотоксических показателей у мышей при старении.
В таблице 4 представлены данные по исследуемым показателям у контрольных мышей F1(CBAxC57BL/6) двух возрастных групп: половозрелых двухмесячных мышей и стареющих мышей в возрасте 12 месяцев. Известно, что количество полиплоидных ядер в печени животных и человека с возрастом увеличивается. В таблице 4 представлены результаты по каждому животному двух возрастных групп, а также индексы ядерности и плоидности гепатоцитов. Установлен низкий (0,17%) не отличающийся в двух группах уровень цитогенетических нарушений. Однако выявлены статистически достоверные отличия по всем показателям плоидности и ядерности у молодых и старых животных. Индекс плоидности у старых животных увеличился в 4,5 раза с 18,8 до 82,5. Индекс ядерности у мышей двух возрастных отличался незначительно и составил 1,32 и 1,41 у молодых и старых животных соответственно. Таким образом, у старых животных основная масса гепатоцитов представлена одно- и двуядерными полиплоидными клетками.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ НЕИНВАЗИВНОЙ ДИАГНОСТИКИ ЦИТОГЕНЕТИЧЕСКОГО И ЦИТОТОКСИЧЕСКОГО ДЕЙСТВИЯ ФАКТОРОВ ОКРУЖАЮЩЕЙ СРЕДЫ НА ОРГАНИЗМ ЧЕЛОВЕКА | 2005 |
|
RU2292027C2 |
| СПОСОБ ВОССТАНОВЛЕНИЯ ПАРЕНХИМЫ ПОВРЕЖДЕННОЙ ПЕЧЕНИ КРЫС | 2009 |
|
RU2398290C1 |
| СПОСОБ СОЗДАНИЯ ИСХОДНОГО МАТЕРИАЛА ДЛЯ СЕЛЕКЦИИ РАСТЕНИЙ | 2002 |
|
RU2215407C2 |
| СПОСОБ ЭКСПРЕСС-ОЦЕНКИ СТЕПЕНИ ПОТЕНЦИАЛЬНОЙ ГЕНОТОКСИЧЕСКОЙ АКТИВНОСТИ ВЕЩЕСТВ И ФАКТОРОВ СРЕДЫ ПО НАЛИЧИЮ АНЕУПЛОИДИИ В ЛИМФОЦИТАХ ПЕРИФЕРИЧЕСКОЙ КРОВИ ЧЕЛОВЕКА, ОБРАЗОВАВШИХСЯ В РЕЗУЛЬТАТЕ КУЛЬТИВИРОВАНИЯ В УСЛОВИЯХ ЦИТОКИНЕТИЧЕСКОГО БЛОКА | 2011 |
|
RU2467329C1 |
| СПОСОБ СТИМУЛИРОВАНИЯ АПОПТОЗА | 2006 |
|
RU2340349C2 |
| СПОСОБ КОНТРОЛЯ ЗА ЛЕЧЕНИЕМ ОПУХОЛЕЙ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 1996 |
|
RU2079132C1 |
| СПОСОБ ЛАЗЕРНОГО СЛИЯНИЯ БЛАСТОМЕРОВ ВНУТРИ РАННИХ ДОИМПЛАНТАЦИОННЫХ ЭМБРИОНОВ МЛЕКОПИТАЮЩИХ БЕЗ НАРУШЕНИЯ ИХ ЦЕЛОСТНОСТИ | 2012 |
|
RU2495932C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ КЛЕТОК ПОЧКИ ЭМБРИОНА ОВЦЫ ДЛЯ РАЗМНОЖЕНИЯ ВИРУСОВ | 1987 |
|
SU1559700A1 |
| Способ прогнозирования риска развития заболеваний, являющихся причинами медицинских противопоказаний к работе с вредными факторами металлургического производства | 2020 |
|
RU2754802C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ КРАСНОГО ПЛОСКОГО ЛИШАЯ СЛИЗИСТОЙ ОБОЛОЧКИ РТА | 2022 |
|
RU2789238C1 |
Группа изобретений относится к медицине, а именно цитологии, и может быть использовано для оценки цитогенетического и цитотоксического действия различных факторов на гепатоциты экспериментальных животных и человека. Для этого получают препараты гепатоцитов из печени после эвтаназии животных или биопсии у человека. Затем препарат фиксируют в 10% формалине и проводят щелочную диссоциацию 50% КОН при температуре 25-37°С в течение трех часов. После этого наносят суспензию клеток методом мазка на сухое предметное стекло, окрашивание ацетоорсеином с докраской цитоплазмы светлым зеленым и анализируют с помощью светового микроскопа 1000 гепатоцитов. Цитомный анализ гепатоцитов включает определение следующих цитологических показателей: определение клеток с микроядрами, клеток с ядерными протрузиями, клеток с межъядерными мостами и сумму клеток с этими показателями. Дополнительно учитывают количественное изменение одноядерных диплоидных (2n), тетраплоидных (4n), полиплоидных (≥8n), двуядерных диплоидных (2n+2n), тетраплоидных (4n+4n) и полиплоидных (≥8n+8n) гепатоцитов. Затем рассчитывают индекс плоидности как отношение суммы полиплоидных гепатоцитов к сумме диплоидных гепатоцитов и индекс ядерности как отношение суммы двуядерных гепатоцитов к сумме одноядерных гепатоцитов. Группа изобретений обеспечивает упрощение способа подготовки гепатоцитов для анализа, а также повышение информативности оценки цитогенетического и цитотоксического действия различных факторов на организм. 2 н.п. ф-лы, 1 ил., 4 табл., 6 пр.
1. Способ подготовки препаратов гепатоцитов лабораторных животных и человека, включающий получение отдельно лежащих гепатоцитов путем выделения печени у животных после эвтаназии или биопсии у человека, фиксации органа в 10% формалине, щелочной диссоциации клеток, нанесения суспензии клеток методом мазка на сухое предметное стекло, окрашивание ацетоорсеином с докраской цитоплазмы светлым зеленым, анализа с помощью светового микроскопа 1000 гепатоцитов, отличающийся тем, что щелочную диссоциацию проводят при температуре 25-37°С в течение трех часов.
2. Цитомный анализ гепатоцитов лабораторных животных и человека, подготовленных согласно п. 1, включающий определение показателей цитогенетического действия, таких как клетки с микроядрами, отличающийся тем, что в нем дополнительно учитывают клетки с ядерными протрузиями, клетки с межъядерными мостами, сумму клеток с этими показателями, шесть цитологических показателей, количественные изменения которых указывают на цитотоксическое действие исследуемых факторов, такие как одноядерные диплоидные (2n) гепатоциты, тетраплоидные (4n) гепатоциты, полиплоидные (≥8n) гепатоциты, двуядерные диплоидные (2n+2n) гепатоциты, тетраплоидные (4n+4n) гепатоциты и полиплоидные (≥8n+8n) гепатоциты, при этом определяют индекс плоидности как отношение суммы полиплоидных гепатоцитов к сумме диплоидных гепатоцитов и индекс ядерности как отношение суммы двуядерных гепатоцитов к сумме одноядерных гепатоцитов.
| WO2014061244 A1, 24.04.2014 | |||
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТОВ ИЗОЛИРОВАННЫХ КЛЕТОК | 1994 |
|
RU2104524C1 |
| МОЛОДЫХ О.П., Морфологическое исследование печени мышевидных грызунов из районов антропогенных воздействий, авт | |||
| дисс | |||
| кбн., Новосибирск, 1996, стр | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2020-02-27—Публикация
2018-09-17—Подача