Ссылка на родственные заявки
Согласно настоящей заявке испрашивается приоритет в соответствии с заявкой на выдачу патента Китая №201510125962.4, поданной в Государственное ведомство по интеллектуальной собственности Китая 20 марта 2015 г., полное содержание которой включено в настоящий документ посредством ссылки.
Область техники, к которой относится настоящее изобретение
Настоящая заявка относится к области фармацевтической химии и более конкретно к соли производного хиназолина, способу ее получения и ее медицинскому применению.
Предшествующий уровень техники настоящего изобретения
Рецептор эпидермального фактора роста (EGFR) представляет собой тирозинкиназный рецептор, широко распространенный на поверхностях эпителиальных клеток, фибробластов, глиальных клеток, кератиноцитов млекопитающих и т.д. Сигнальный путь EGFR играет важную роль в таких физиологических процессах клеток, как рост, пролиферация, дифференцировка и подобное. Функциональная недостаточность таких протеин-тирозинкиназ, как EGFR и т.д., или нарушение в активности или клеточной локализации ключевых факторов в связанном с ними сигнальном пути могут вызывать появление опухолей, сахарного диабета, иммунных дефицитов и сердечно-сосудистых заболеваний.
N6-(1-акрилоилазациклогексан-4-ил)-N4-(3-хлор-4-фторфенил)-7-метокси-хиназолин-4,6-диамин характеризуется структурой, представленной формулой I
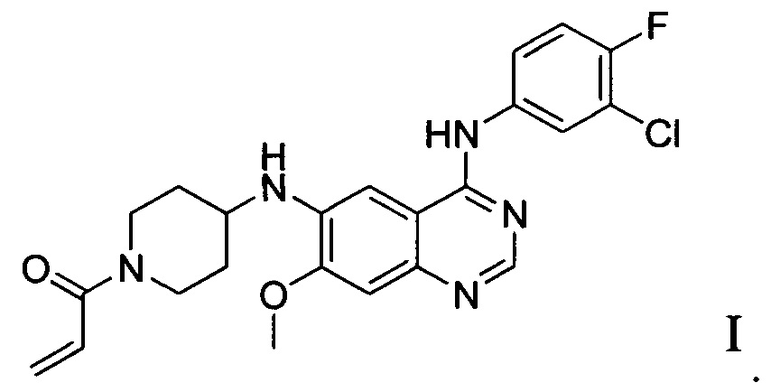
Соединение формулы I представляет собой селективный ингибитор рецептора эпидермального фактора роста. Он может конкурентно связываться с сайтом фосфорилирования тирозинкиназы на внутриклеточном домене, чтобы блокировать взаимодействие между сайтом фосфорилирования и АТР и тем самым ингибировать фосфорилирование тирозина и серии передачи нисходящих сигналов, а затем ингибировать рост опухолевых клеток. Следовательно, соединение формулы I можно использовать для лечения различных злокачественных опухолей, таких как немелкоклеточный рак легкого, злокачественная опухоль молочной железы и подобное. См. заявку на выдачу патента Китая №201310452885.4, которая полностью включена в настоящий документ посредством ссылки.
Краткое раскрытие настоящего изобретения
Согласно одному аспекту настоящая заявка относится к малеату соединения формулы I,
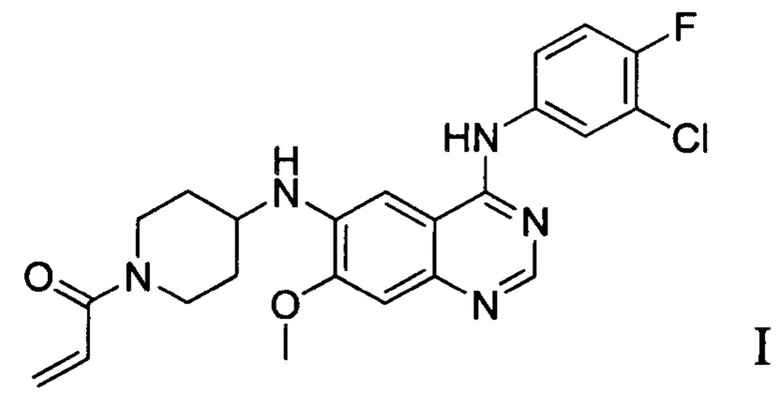
где молярное отношение малеиновой кислоты к соединению формулы I зависит от количества малеиновой кислоты, используемого в получении указанной соли. Например, молярное отношение соединения формулы I к малеиновой кислоте в малеате может находиться в диапазоне, составляющем 1:0,5-4.
Согласно другому аспекту настоящая заявка относится к способу получения малеата соединения формулы I, предусматривающему следующее: (1) получение раствора соединения формулы I; (2) приведение в контакт раствора соединения формулы I, полученного из стадии (1), с малеиновой кислотой; и (3) высушивание распылением реакционной смеси, полученной из стадии (2), с получением малеата соединения формулы I.
Согласно другому аспекту настоящая заявка относится к фармацевтической композиции, содержащей малеат соединения формулы I и фармацевтически приемлемый носитель, вспомогательное вещество, разбавитель и/или основу.
Согласно другому аспекту настоящая заявка относится к применению малеата соединения формулы I или его фармацевтической композиции в получении лекарственного средства для лечения опухоли.
Согласно другому аспекту настоящая заявка относится к способу лечения опухоли, предусматривающему введение малеата соединения формулы I или его фармацевтической композиции нуждающемуся в этом субъекту.
Согласно другому аспекту настоящая заявка относится к малеату соединения формулы I или его фармацевтической композиции для применения в лечении опухоли.
Подробное раскрытие настоящего изобретения
В последующем описании определенные конкретные детали предусмотрены для обеспечения полного понимания различных раскрытых вариантов осуществления. Тем не менее, специалистам в настоящей области техники будет понятно, что варианты осуществления можно реализовать на практике с помощью других способов, компонентов, материалов и подобного, вместо одного или нескольких из указанных конкретных деталей.
Если контекст не требует иного, во всем описании изобретения и следующей за ним формуле изобретения термин "содержать" и такие его вариации, как "содержит" и "содержащий", следует рассматривать в открытом и включающем смысле, т.е. "включая в себя без ограничения".
Ссылка во всем настоящем описании изобретения на "один вариант осуществления", или "вариант осуществления", или "другой вариант осуществления", или "некоторые варианты осуществления" означает, что конкретный обозначаемый элемент, структура или характеристики, описанные в связи с вариантом осуществления, включены по меньшей мере в один вариант осуществления. Соответственно, не обязательно все появления фраз "согласно одному варианту осуществления", или "согласно варианту осуществления", или "согласно другому варианту осуществления", или "согласно некоторым вариантам осуществления" в различных местах по всему настоящему описанию изобретения относятся к одному и тому же варианту осуществления. Кроме того, конкретные элементы, структуры или характеристики можно комбинировать любым подходящим образом в одном или нескольких вариантах осуществления.
Следует отметить, что используемые в настоящем описании изобретения и прилагаемой формуле изобретения формы единственного числа включают в себя ссылки на форму множественного числа, если контекст ясно не диктует иное. Таким образом, например, ссылка на реакцию, в которую вовлечен "катализатор", включает в себя единственный катализатор или два или больше катализаторов. Если иное прямо не указано в настоящем документе, также следует отметить, что термин "или", как правило, используют в его смысле, включающем в себя "и/или".
Согласно одному аспекту настоящая заявка относится к малеату соединения формулы I,
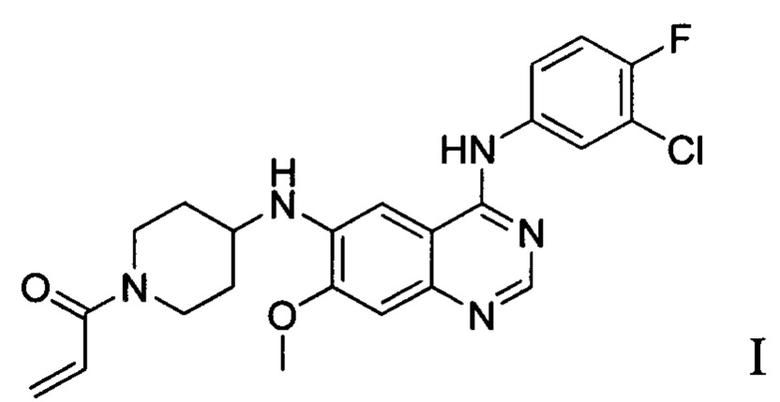
где молярное отношение малеиновой кислоты к соединению формулы I зависит от количества малеиновой кислоты, используемого в получении указанной соли. Например, молярное отношение соединения формулы I к малеиновой кислоте в малеате может находиться в диапазоне, составляющем 1:0,5-4.
Согласно некоторым вариантам осуществления настоящей заявки молярное отношение соединения формулы I к малеиновой кислоте в малеате составляет 1:1. Согласно другим вариантам осуществления настоящей заявки молярное отношение соединения формулы I к малеиновой кислоте в малеате составляет 1:2.
Согласно другому аспекту настоящая заявка относится к способу получения малеата соединения формулы I, предусматривающему следующее: (1) получение раствора соединения формулы I; (2) смешивание раствора соединения формулы I, полученного из стадии (1), с малеиновой кислотой; и (3) высушивание распылением реакционной смеси, полученной из стадии (2), для получения малеата соединения формулы I.
Согласно некоторым вариантам осуществления молярное отношение количества соединения формулы I к количеству малеиновой кислоты, используемому в способе получения, находится в диапазоне, составляющем 1:1-20, предпочтительно 1:1-15 и наиболее предпочтительно 1:1-10.
На стадии (1) способа получения соединение формулы I можно растворить в органическом растворителе для получения раствора соединения формулы I. Органический растворитель включает в себя все органические растворители, способные растворять соединение формулы I, такие как DMF.
На стадии (2) способа получения раствор соединения формулы I, полученный из стадии (1), можно смешивать с малеиновой кислотой или раствором малеиновой кислоты и при необходимости полученную реакционную смесь можно нагреть до подходящей температуры, например, 60°С-100°С, предпочтительно 80°С. Согласно некоторым вариантам осуществления раствор малеиновой кислоты представляет собой органический раствор малеиновой кислоты, полученный путем смешивания малеиновой кислоты с органическим растворителем. Согласно некоторым вариантам осуществления настоящей заявки органический растворитель представляет собой, например, DMF.
Согласно некоторым вариантам осуществления растворитель, смешивающийся с органическими растворителями, используемыми на стадии (1) и/или стадии (2), такой как вода, можно добавлять перед высушиванием распылением.
Согласно другому аспекту настоящая заявка относится к фармацевтической композиции, содержащей малеат соединения формулы I и фармацевтически приемлемый носитель, вспомогательное вещество, разбавитель и/или основу.
Используемый в настоящем документе термин "фармацевтическая композиция" относится к составу, полученному с помощью соединения согласно настоящей заявке и носителя, вспомогательного вещества, разбавителя и/или несущей среды, которые, как правило, являются общепринятыми в медицинской области техники для доставки биоактивного соединения в организм (например, организм человека). Цель фармацевтической композиции состоит в облегчении введения соединения согласно настоящей заявке в организм.
Используемый в настоящем документе термин "фармацевтически приемлемый носитель" относится к тем носителям и разбавителям, которые не вызывают существенную стимуляцию организма и не будут ухудшать биоактивность и свойства активного соединения. "Фармацевтически приемлемое вспомогательное вещество и/или несущая среда" относится к инертному веществу, которое вводят вместе с активным ингредиентом и которое является благоприятным для доставки активного ингредиента в организм. "Фармацевтически приемлемый носитель, вспомогательное вещество, разбавитель и/или основа" включают в себя без ограничения любые носители, вспомогательные вещества, основы, способствующие скольжению средства, подсластители, разбавители, консерванты, красители/красящие вещества, ароматизаторы, поверхностно-активные вещества, смачивающие средства, диспергирующие средства, разрыхлители, суспендирующие средства, стабилизаторы, изотонические средства, растворители или эмульгаторы и подобное, которые можно использовать для введения человеку или сельскохозяйственным животным. Неограничивающие примеры вспомогательного вещества включают в себя карбонат кальция, фосфат кальция, различные сахара и крахмалы, производные целлюлозы, желатины, растительные масла, полиэтиленгликоли и подобное.
Малеат соединения формулы I согласно настоящей заявке можно вводить в его чистой форме или в форме соответствующей фармацевтической композиции. Фармацевтическую композицию согласно настоящей заявке можно получить, комбинируя малеат соединения формулы I согласно настоящей заявке с соответствующим фармацевтически приемлемым носителем, разбавителем или вспомогательным веществом, и можно составить в твердые, полутвердые, жидкие или газообразные составы, такие как таблетки, пилюли, капсулы, порошки, гранулы, мази, эмульсии, суспензии, растворы, суппозитории, инъекции, средства для ингаляции, гели, микросферы, аэрозоли и подобное.
Типичные пути введения малеата соединения формулы I согласно настоящей заявке или его фармацевтической композиции включают в себя без ограничения пероральное, ректальное, трансмукозальное, энтеральное введение или локальное, трансдермальное, ингаляционное, парентеральное, сублингвальное, интравагинальное, интраназальное, внутриглазное, интраперитонеальное, внутримышечное, подкожное и внутривенное введение. Предпочтительный путь введения представляет собой пероральное введение.
Фармацевтическую композицию согласно настоящей заявке можно получить с использованием способа, известного специалисту в настоящей области техники, такого как общепринятый способ смешивания, способ растворения, способ гранулирования, способ производства драже, способ помола, способ эмульгирования, способ высушивания распылением и подобное.
Согласно предпочтительному варианту осуществления фармацевтическая композиция согласно настоящей заявке находится в пероральной форме. Для перорального введения фармацевтическую композицию можно составить путем смешивания активного соединения с фармацевтически приемлемым носителем, вспомогательным веществом, разбавителем и/или несущей средой, хорошо известными в настоящей области техники. Указанные носители, вспомогательные вещества, разбавители и/или несущие среды обеспечивают возможность составления фармацевтической композиции согласно настоящей заявке в виде таблеток, пилюль, леденцов, драже, капсул, жидкостей, гелей, сиропов, суспензий и подобного для перорального введения пациенту. Твердую пероральную композицию можно получить с помощью общепринятого способа смешивания, наполнения или изготовления таблеток.
При указанном введении дозировка малеата соединения формулы I составляет предпочтительно 0,01-200 мг/кг массы тела в день.
Согласно другому аспекту настоящая заявка относится к применению малеата соединения формулы I или его фармацевтической композиции в получении лекарственного средства для лечения опухоли.
Согласно другому аспекту настоящая заявка относится к способу лечения опухоли, предусматривающему введение малеата соединения формулы I или его фармацевтической композиции нуждающемуся в этом субъекту.
Согласно другому аспекту настоящая заявка относится к малеату соединения формулы I или его фармацевтической композиции для применения в лечении опухоли.
Согласно некоторым вариантам осуществления опухоль включает в себя без ограничения немелкоклеточный рак легкого и злокачественную опухоль молочной железы.
ПРИМЕРЫ
Пример 1 Получение соединения формулы I
Стадия 1: 4-хлор-7-фтор-6-нитрохиназолин
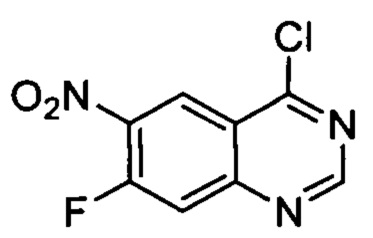
7-фтор-6-нитрохиназолин-4(3H)-он (2,0 г, 9,6 ммоль) и одну каплю N,N-диметилформамида нагревали с обратным холодильником в течение ночи в тионилхлориде (6 мл) и затем реакционную смесь концентрировали в вакууме. К остатку добавляли толуол и затем снова концентрировали в вакууме для удаления оставшегося тионилхлорида. Получали указанное в заголовке соединение (2 г, 92%).
Спектр ЯМР 1Н (CDCl3): δ 9,18 (1H, с), 9,05 (1Н, д, J=7,6 Гц), 7,95 (1Н, д, J=10,4).
Стадия 2: 3-хлор-N-(3,4-диметоксибензил)-4-фторанилин
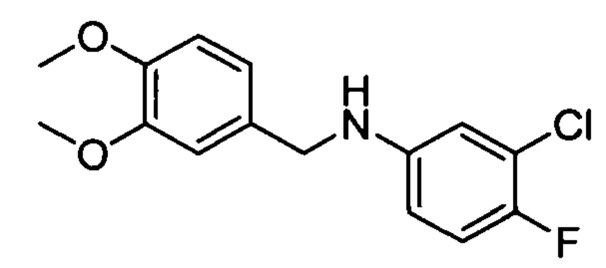
К 1,2-дихлорэтану (30 мл) добавляли 3-хлор-4-фторанилин (2,9 г, 20 ммоль) и 3,4-диметоксибензальдегид (3,3 г, 20 ммоль) и перемешивали при комнатной температуре в течение 1 ч. Затем добавляли натрийтриацетоксиборогидрид (10 г, 50 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь выливали в 100 мл воды и экстрагировали с дихлорметаном. Органическую фазу отделяли, отмывали насыщенным солевым раствором, высушивали на безводном сульфате натрия и концентрировали в вакууме с получением указанного в заголовке соединения (5,5 г, 93%).
Спектр ЯМР 1Н (CDCl3): δ 6,94-6,82 (4Н, м), 6,63-6,61 (1H, м), 6,45-6,41 (1Н, м), 4,18 (2Н, с), 3,98 (1Н, ушир.), 3,87 (3Н, с), 3,86 (3Н, с).
Стадия 3: N-(3-хлор-4-фторфенил)-N-(3,4-диметоксибензил)-7-фтор-6-нитрохиназолин-4-амин
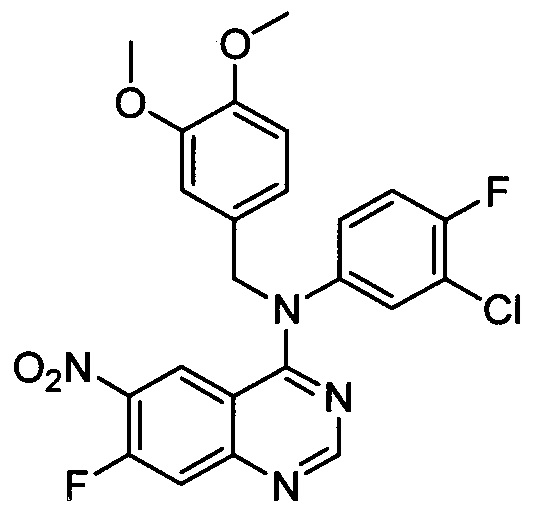
К ацетонитрилу (20 мл) добавляли 4-хлор-7-фтор-6-нитрохиназолин (2,1 г, 9,2 ммоль) и 3-хлор-N-(3,4-диметоксибензил)-4-фторанилин (2,7 г, 9,2 ммоль) и нагревали с обратным холодильником в течение 3 ч. После охлаждения реакционную смесь нейтрализовали с помощью раствора карбоната натрия и экстрагировали с этилацетатом. Органическую фазу отделяли, отмывали насыщенным солевым раствором, высушивали на безводном сульфате натрия и концентрировали в вакууме с получением указанного в заголовке соединения (3,6 г, 80%).
Стадия 4: N-(3-хлор-4-фторфенил)-N-(3,4-диметоксибензил)-7-метокси-6-нитрохиназолин-4-амин
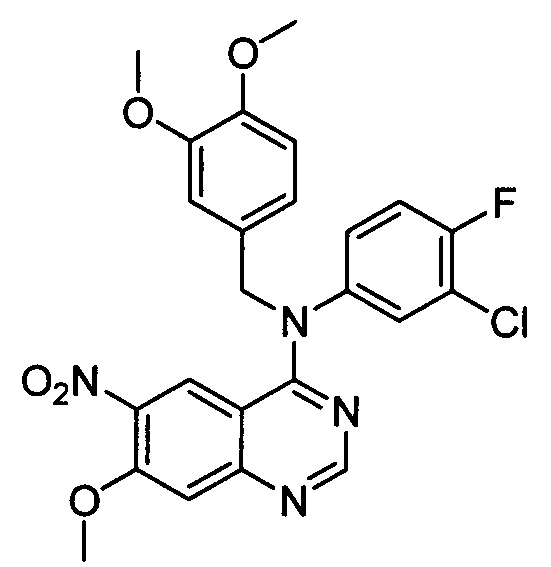
Металлический натрий (113 мг, 5,0 ммоль) добавляли к безводному метанолу (20 мл) и перемешивали при комнатной температуре в течение 10 минут. Затем добавляли N-(3-хлор-4-фторфенил)-N-(3,4-диметоксибензил)-7-фтор-6-нитрохиназолин-4-амин (2,4 г, 5,0 ммоль) и полученную реакционную смесь перемешивали при 40°С в течение 6 ч. После охлаждения смесь выливали в 100 мл воды и экстрагировали с этилацетатом. Органическую фазу отмывали насыщенным солевым раствором, высушивали на безводном сульфате натрия и концентрировали в вакууме с получением указанного в заголовке соединения (2,35 г, 94%).
Спектр ЯМР 1Н (CDCl3): δ 8,85 (1H, с), 7,57 (1Н, с), 7,35 (1Н, с), 7,23-7,19 (2Н, м), 7,00-6,96 (1Н, м), 6,84-6,78 (2Н, м), 5,35 (2Н, с), 4,05 (3Н, с), 3,88 (3Н, с), 3,83 (3Н, с).
Стадия 5: N4-(3-хлор-4-фторфенил)-N4-(3,4-диметоксибензил)-7-метоксихиназолин-4,6-диамин
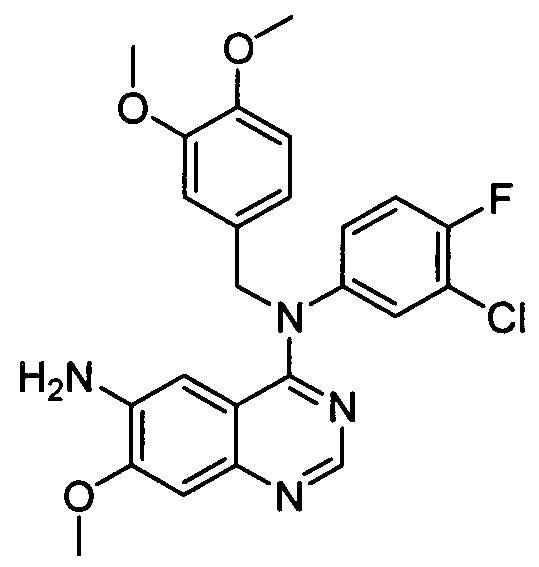
N-(3-хлор-4-фторфенил)-N-(3,4-диметоксибензил)-7-метокси-6-нитрохиназолин-4-амин (2,35 г, 4,7 ммоль) и никель Ренея (приблизительно 0,5 г) добавляли к тетрагидрофурану (100 мл). Атмосферу заменяли на газ водород и реакционную смесь перемешивали в течение ночи при комнатной температуре в атмосфере водорода (1 атм.). Смесь фильтровали и фильтрат концентрировали в вакууме с получением указанного в заголовке соединения (2 г, 90%).
Стадия 6: трет-бутил-4-{{4-[(3-хлор-4-фторфенил)(3,4-диметоксибензил)амино]-7-метоксихиназолин-6-ил}амино}пиперидин-1-карбоксилат
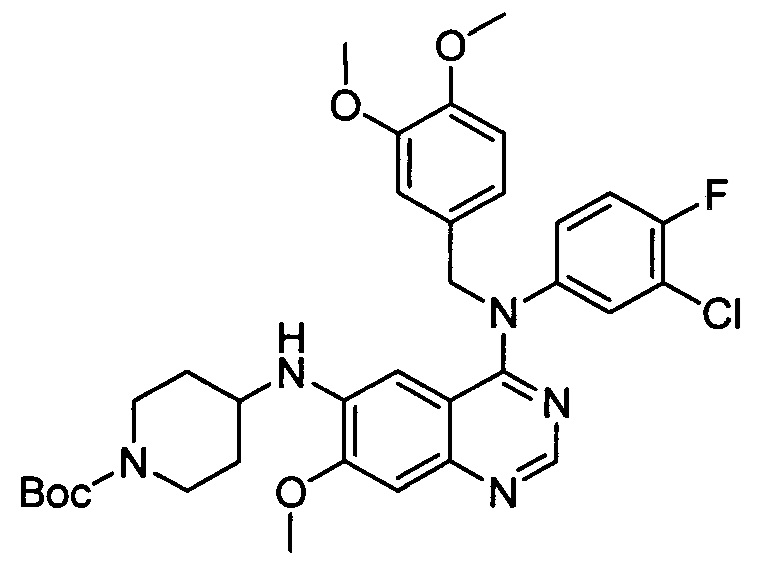
Раствор N4-(3-хлор-4-фторфенил)-N4-(3,4-диметокси-бензил)-7-метоксихиназолин-4,6-диамина (469 мг, 1,0 ммоль) и трет-бутил-4-оксопиперидин-1-карбоксилата (239 мг, 1,2 ммоль) в уксусной кислоте (10 мл) перемешивали при комнатной температуре в течение 2 ч и затем натрийтриацетоксиборогидрид (254 мг, 1,2 ммоль) добавляли к нему в одной части. После проведения реакции в течение 30 минут реакцию гасили путем медленного добавления воды и экстрагировали с этилацетатом. Полученную органическую фазу отмывали последовательно с помощью воды, 5% водного раствора NaHCO3 и насыщенного солевого раствора, высушивали на безводном сульфате натрия и концентрировали в вакууме. Остаток разделяли посредством колоночной хроматографии на силикагеле с получением указанного в заголовке соединения (404 мг, 62%).
Стадия 7: N6-(пиперидин-4-ил)-N4-(3-хлор-4-фторфенил)-7-метоксихиназолин-4,6-диамин
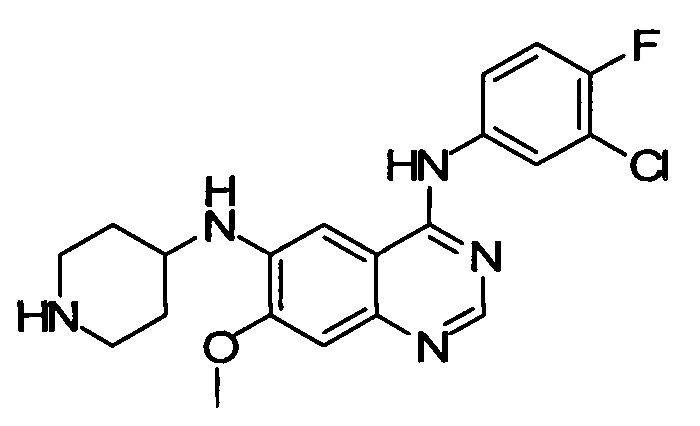
Раствор трет-бутил-4-{{4-[(3-хлор-4-фторфенил)(3,4-диметокси-бензил)амино]-7-метоксихиназолин-6-ил}амино}пиперидин-1-карбоксилата (0,4 г, 0,61 ммоль) в трифторуксусной кислоте (8 мл) перемешивали при 70°С в течение 6 ч. Как только реакция завершалась, реакционную смесь охлаждали и концентрировали в вакууме. Остаток суспендировали с этилацетатом и фильтровали с получением трифторацетата указанного в заголовке соединения (0,26 г, 83%).
Стадия 8: N6-(1-акрилоилпиперидин-4-ил)-N4-(3-хлор-4-фторфенил)-7-метоксихиназолин-4,6-диамин
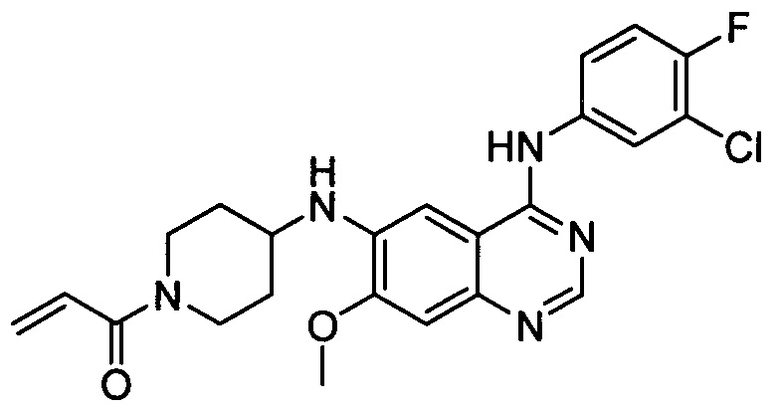
Раствор моно-трифторацетата N6-(пиперидин-4-ил)-N4-(3-хлор-4-фторфенил)-7-метокси-хиназолин-4,6-диамина (258 мг, 0,5 ммоль) и триэтиламина (202 мг, 2,0 ммоль) в тетрагидрофуране (10 мл) перемешивали при комнатной температуре в течение 30 минут. После охлаждения до 0°С добавляли по каплям раствор акрилоилхлорида (54 мг, 0,6 ммоль) в тетрагидрофуране (2 мл) и затем реакцию продолжали в течение следующих 30 минут. Реакцию завершали, гасили путем медленного добавления 5% раствора NaHCO3 и экстрагировали с этилацетатом. Полученную органическую фазу отмывали насыщенным солевым раствором, высушивали на безводном сульфате натрия и концентрировали в вакууме. Остаток разделяли посредством колоночной хроматографии на силикагеле с получением целевого продукта (150 мг, 66%).
Спектр ЯМР 1Н (DMSO-d6): δ 9,24 (1Н, с), 8,33 (1H, с), 8,09-8,08 (1H, м), 7,77-7,74 (1Н, м), 7,42-7,40 (1H, м), 7,23 (1Н, с), 7,06 (1Н, с), 6,85-6,81 (1Н, м), 6,10-6,06 (1Н, м), 5,66-5,64 (1H, м), 5,32-5,29 (1Н, м), 4,41-4,38 (1Н, м), 4,09-4,06 (1Н, м), 3,93 (3Н, с), 3,79-3,78 (1Н, м), 3,35-3,34 (1Н, м), 2,87-2,84 (1H, м), 2,03-2,01 (2Н, м), 1,44-1,41 (2Н, м).
Пример 2 Получение малеата соединения формулы I
5 г соединения формулы I растворяли в 100 мл DMF при комнатной температуре и непрерывно перемешивали до получения гомогенного раствора. К нему добавляли 6,3 г малеиновой кислоты и затем нагревали до 80°С и проводили реакцию в течение 2 ч. Затем 100 мл воды добавляли при указанной температуре и смесь напрямую высушивали распылением с получением 4,0 г желтого твердого порошка. Спектр XRD (рентгенодифракционный анализ) показал, что порошок представлял собой аморфный малеат соединения формулы I (1:1).
Пример 3 Получение цитрата, оксалата и ацетата соединения формулы I
Цитрат, оксалат и ацетат соединения формулы I соответственно получали таким же способом, как представлено в примере 2.
Пример 4 Исследование биодоступности
Процедура исследования: 15 собак породы бигль (с массой тела 7,4~9,4 кг) произвольным образом делили на 5 групп и вводили перорально суспензии соединения формулы I, его малеата, цитрата, оксалата и ацетата (которые рассчитывали в соответствии с количеством соединения формулы I) в CMC-Na (карбоксиметилцеллюлоза натрия) в дозировке, составляющей 5 мг/кг массы тела, соответственно. Образцы крови брали до и после введения (временные точки - 0,25, 0,5, 1, 2, 4, 6, 8, 12, 24 и 48 ч) и концентрацию соединения формулы I для каждого образца плазмы определяли с помощью ЖХ-МС (жидкостная хроматография с масс-спектрометрией) и затем рассчитывали биодоступность.
Процедура обнаружения:
Условия проведения хроматографии: метанол в качестве подвижной фазы А и 0,1% (объем/объем) водный раствор муравьиной кислоты в качестве подвижной фазы В, изократическое элюирование А:В=52:48; объемная скорость потока - 0,2 мл/мин; температура колонки - 35°С; и хроматографическая колонка - SHIMADZU Shim-pack VP-ODS С18 (5,0 мкм, 150 мм × 2,0 мм I.D., Shimadzu Corporation).
Условия масс-спектрометрии: источник ионов: источник ионизации ESI (ионизация электрораспылением), сканирование в режиме SIM (регистрация выбранных ионов), температура изогнутой установки для удаления растворителя (CDL) - 250°С, температура термостата - 200°С; напряжение CDL - 25 В; напряжение обнаружения +1,60 кВ; объемная скорость потока атомизированного газа - 1,5 л/мин; объемная скорость потока сухого газа - 2,0 л/мин.
Результаты исследования


Пример 5 In vitro исследование активности
1. Способ in vitro энзимологического исследования
Киназу EGFR, EGFR (Т790М, L858R) и HER2 экспрессировали и очищали посредством экспрессионной системы клеток насекомого или приобретали из коммерчески доступных продуктов.
Платформу для исследования киназной активности EGFR, EGFR (Т790М, L858R) и HER2 устанавливали на основании способа гомогенной флуоресценцией с временным разрешением (HTRF), предоставленного Cisbio Bioassays, и активность соединения определяли с помощью платформы. Соединение разводили при 3-кратном градиенте с помощью 100% DMSO, начиная с 100 нМ (EGFR и HER2) и 1 мкМ (EGFR-T790M/L858R), соответственно. Для каждой концентрации брали 4 мкл раствора и добавляли к 96 мкл реакционного буфера (50 мМ 4-гидроксиэтилпиперазинэтансульфоновая кислота (HEPES) (рН 7,0), 0,02% NaN3, 0,01% бычий сывороточный альбумин (BSA), 0,1 мМ ортованадат натрия, 5 мМ MgCl2, 50 нМ SEB (Cisbio, № по кат.: 61 SEBALB), 1 мМ DTT). Брали 2,5 мкл смеси и добавляли к 384-луночному планшету (OptiPlate-384, PerkinElmer) и затем добавляли 2,5 мкл киназы и однородно перемешивали с помощью центрифуги. Затем к этому добавляли 5 мкл АТР и субстрата тирозинкиназы (ТК) - биотина для инициации реакции. После того, как 384-луночный планшет инкубировали в инкубаторе при 23°С в течение определенного периода времени, реакцию останавливали путем добавления 5 мкл меченного Eu3+-криптатом антитела к ТК и 5 мкл стрептавидина-XL665. Значения флуоресценции считывали на Envision (PerkinElmer) после инкубации в течение 1 ч в инкубаторе. Значения IC50 соединения рассчитывали с использованием программного обеспечения GraphPad Prism 5.0.
2. Анализ безъякорной пролиферации клеток
NCI-H1975, клеточную линию немелкоклеточного рака легкого человека, и ВТ474, клеточную линию злокачественной опухоли молочной железы человека, культивировали в среде культивирования RPIM-1640 или DMEM, дополненной 10% фетальной бычьей сывороткой (FBS) в инкубаторе для клеток (37°С, 5% СО2). В исследовании соединения планшеты для культивирования предварительно покрывали 0,6% средой и клетки ресуспендировали с 0,3% агарозой с низкой температурой плавления и затем высевали в 96-луночный планшет с плотностью, составляющей 10000 клеток на лунку (100 мкл). Соединение разводили при 3-кратном градиенте, начиная с 10 мМ. Для каждой концентрации брали 2 мкл раствора и добавляли к 98 мкл среды культивирования и затем 5,3 мкл смеси добавляли к среде культивирования клеток (0,1% конечной концентрации DMSO, объем/объем). После обработки в течение одной недели (7 дней) добавляли 20 мкл реагента CellTiter-Blue® (Promega) и инкубировали при 37°С в течение 4 ч. Сигналы флуоресценции считывали на Envison (Perkin Elmer) и значения IC50 соединения для ингибирования клеточной пролиферации рассчитывали с использованием программного обеспечения GraphPad Prism 5.0.
Биологическая активность

Изобретение относится к новому малеату соединения формулы I, в котором молярное отношение соединения формулы I к малеиновой кислоте составляет 1:1. Соединение обладает свойствами ингибитора опухоли, опосредованной EGFR киназами, HER2 киназами или мутантными формами EGFR киназ L858R/T790M, и может быть использовано при лечении опухоли, опосредованной активностью указанных киназ, например, в случае, когда опухоль представляет собой немелкоклеточный рак легкого или злокачественную опухоль молочной железы. Формула I представляет собой соединение

4 н. и 2 з.п. ф-лы, 5 пр., 2 табл.
1. Малеат соединения формулы I,
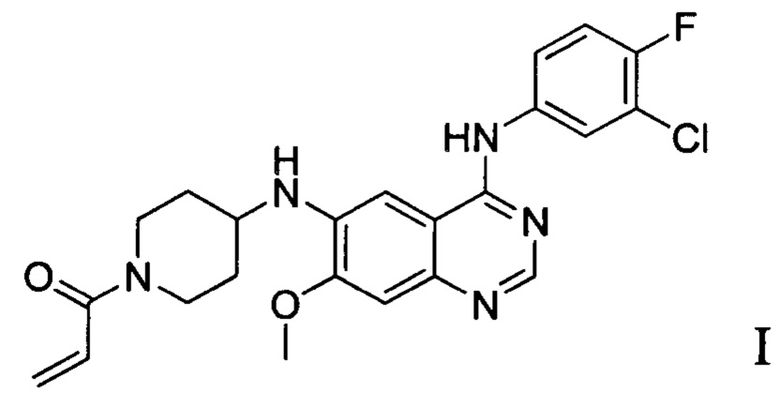 ,
,
в котором молярное отношение соединения формулы I к малеиновой кислоте составляет 1:1.
2. Фармацевтическая композиция, обладающая свойствами ингибировать опухоль, опосредованную EGFR киназами, HER2 киназами или мутантными формами EGFR киназ L858R/T790M, содержащая эффективное количество малеата соединения формулы I по п. 1 и фармацевтически приемлемый носитель, вспомогательное вещество и/или разбавитель.
3. Фармацевтическая композиция по п. 2, где опухоль представляет собой немелкоклеточный рак легкого или злокачественную опухоль молочной железы.
4. Применение малеата соединения формулы I по п. 1 в получении лекарственного средства для лечения опухоли, опосредованной EGFR киназами, HER2 киназами или мутантными формами EGFR киназ L858R/T790M.
5. Применение по п. 4, где опухоль представляет собой немелкоклеточный рак легкого или злокачественную опухоль молочной железы.
6. Способ лечения опухоли, опосредованной EGFR киназами, HER2 киназами или мутантными формами EGFR киназ L858R/T790M, включающий введение эффективного количества малеата соединения формулы I по п. 1 нуждающемуся в этом субъекту.
| Устройство для резки гардин | 1930 |
|
SU18716A1 |
| ПРОИЗВОДНЫЕ ХИНАЗОЛИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ДОСТИЖЕНИЯ АНТИПРОЛИФЕРАТИВНОГО ЭФФЕКТА | 1996 |
|
RU2153495C2 |
| CN 103948689 A, 30.07.2014 | |||
| CN 104513229 A, 15.04.2015 & EA 201600204 A1, опубл | |||
| Способ очистки нефти и нефтяных продуктов и уничтожения их флюоресценции | 1921 |
|
SU31A1 |
| Способ ударного бурения с одновременной обсадкой трубами | 1986 |
|
SU1481370A1 |
Авторы
Даты
2020-05-13—Публикация
2016-03-18—Подача