Область техники, к которой относится изобретение
Изобретение относится к области медицины, в частности к травматологии и ортопедии, и может быть использовано при хирургическом лечении больных со сложными переломами проксимального отдела плечевой кости, сопровождающимися дефицитом костной ткани.
Уровень техники
Наиболее тяжелые, многооскольчатые переломы проксимального отдела плечевой кости обычно развиваются у пожилых людей с плохим качеством кости. Осуществить репозицию и удержать отломки традиционными металлическими фиксаторами при таких переломах крайне трудно. Закономерными осложнениями становятся несращение перелома или неправильное сращение перелома в результате неудачной репозиции, или вторичного смещения [Jung S.W. et al. Factors that influence reduction loss in proximal humerus fracture surgery // Journal of orthopaedic trauma. - 2015. - T. 29. - №. 6. - C. 276-282.]. Возможным вариантом лечения является анатомическое эндопротезирование плечевого сустава. Функциональные исходы таких операций редко бывают удовлетворительными, т.к. для восстановления функции руки необходима фиксация большого и малого бугорков, а они при плохом качестве кости обычно разрушены и фиксировать их не удается. Возможно эндопротезирование плечевого сустава реверсивной конструкцией, но в публикациях отмечается большое количество осложнений при такой артропластике в остром периоде травмы. [Zumstein М.A. et al. Problems, complications, reoperations, and revisions in reverse total shoulder arthroplasty: a systematic review // Journal of shoulder and elbow surgery. - 2011. - T. 20. - №. 1. - P. 146-157.]. [Anakwenze O.A. et al. Reverse shoulder arthroplasty for acute proximal humerus fractures: a systematic review // Journal of shoulder and elbow surgery. - 2014. - T. 23. - №. 4. - P. 73-80]. Для фиксации многооскольчатых переломов проксимального отдела плечевой кости принято применять специализированные металлические пластины с блокирующимися в них винтами. Однако при плохом качестве кости развиваются такие осложнения как: прорезывание винтов, неправильное сращение с варусной деформацией, миграция винтов с вывинчиванием их из пластины [Launonen А.P. et al. Treatment of proximal humerus fractures in the elderly: a systematic review of 409 patients // Acta orthopaedica. - 2015. - Т. 86. - №. 3. - P. 280-285.] [Haasters F. et al. Complications of locked plating for proximal humeral fractures - are we getting any better? // Journal of shoulder and elbow surgery. - 2016. - T. 25. - №. 10. - P.. 295-303.; Biermann N. et al. Augmentation of plate osteosynthesis for proximal humeral fractures: a systematic review of current biomechanical and clinical studies // Archives of orthopaedic and trauma surgery. - 2019. - P. 1-25.]. Для предотвращения этих осложнений требуется укрепить зону разрушения кости. С этой целью аугментируют головку плечевой кости метилметакрилатным цементом. Недостатком такого решения является нагревание цемента в период полимеризации до значительных температур. Кроме того цемент токсичен, что может приводить к развитию синдрома имплантации костного цемента, и не деградирует в организме [Schliemann В. et al. Screw augmentation reduces motion at the bone-implant interface: a biomechanical study of locking plate fixation of proximal humeral fractures // Journal of shoulder and elbow surgery. - 2015. - T. 24. - №. 12. - P. 1968-1973; Hines С.B. Understanding Bone Cement Implantation Syndrome // AANA Journal. - 2018. - T. 86. - №. 6.].
Из уровня техники известны костные трансплантаты, используемые для укрепления области перелома. Они не токсичны и со временем деградируют. [Cha Н. et al. Treatment of comminuted proximal humeral fractures using locking plate with strut allograft // Journal of shoulder and elbow surgery. - 2017. - T. 26. - №. 5. - С 781-785. http://dx.doi.org/10.1016/j.jse.2016.09.055]. Известно использование крио консервированного аллогенного трансплантата из трубчатой части малоберцовой, локтевой или лучевой кости, которым укрепляют зону разрушения при сложных переломах проксимального отдела плечевой кости. [Hinds R.М. et al. Geriatric proximal humeral fracture patients show similar clinical outcomes to non-geriatric patients after osteosynthesis with endosteal fibular strut allograft augmentation // Journal of shoulder and elbow surgery. - 2015. - T. 24. - №. 6. - C. 889-896.]. К недостаткам таких трансплантатов можно отнести цилиндрическую форму, не обеспечивающую стабильность его положения в зоне перелома - трансплантат может проваливаться в костно-мозговой канал плечевой кости, для чего необходимы дополнительные приемы и средства его удержания до фиксации перелома. Такие трансплантаты почти не обладают остеокондуктивным эффектом, так как состоят из трубчатой части кости. Трансплантат также невозможно использовать в качестве носителя биологически активных веществ. Кроме того трансплантаты хранятся в замороженном состоянии в специальном оборудовании, перед проведением операции трансплантат размораживают, и в случае отсутствия потребности в использовании трансплантата, повторная заморозка с целью его применения уже исключена.
Наиболее близким к заявляемому решению является комбинированный костный аллотрансплантат и способ его получения (RU 2524618), который может быть использован при лечении больных с травматическими дефектами кости, с несросшимися переломами, ложными суставами, переломами с замедленной консолидацией. Комбинированный костный аллогенный трансплантат представляет собой не деминерализованный костный блок, полученный из губчатой кости донора, и содержащий по всему объему костного блока коллаген 1 типа человека в виде губки с мелкоячеистой структурой, полученной при лиофильной сушке костного блока, пропитанного раствором коллагена. Способ получения трансплантата включает изготовление не деминерализованного костного блока из губчатой кости донора, пропитку костного блока раствором коллагена 1 типа человека с последующей лиофилизацией при условиях, обеспечивающих превращение раствора коллагена в губку с мелкоячеистой структурой по всему объему костного блока. Биосовместимый комбинированный костный трансплантат обладает механической прочностью, остеокондуктивным эффектом и стимулирует остеогенез. Лиофилизация представляет последовательное прохождение следующих этапов: замораживание образцов до температуры -40°С, создание вакуума, поддержание данной температуры в течение 1 часа, повышение температуры до +36°С и выдержка образцов в течение 2 часов при данной температуре. Пропитку костного блока раствором коллагена осуществляют путем высверливания сквозных отверстий диаметром 2 мм в различных направлениях костного блока с последующим погружением его в 10% раствор коллагена 1 типа человека и прокачиванием шприцем (без использования иглы) раствора коллагена сквозь указанные отверстия.
Однако данный трансплантат не удобен для укрепления области перелома при переломах проксимального отдела плечевой кости, т.к. в этой зоне губчатая кость переходит в трубчатую и для армирования этой области нужен материал достаточно прочный на излом и обладающий цилиндрической формой. Трансплантат удобен для заполнения дефектов губчатой кости и стимуляции остеогенеза при нарушении консолидации перелома, но не подходит для укрепления перелома в диафизарной и метафизарной областей кости. Кроме того, способ насыщения трансплантата раствором коллагена не обеспечивает его максимальную насыщенность коллагеном - заполнения естественных и сформированных полостей, а также равномерность распределения коллагена по объему трансплантата, что значительно улучшает условия для фиксации и последующей дифференцировки мезенхимальных клеток.
Таким образом, технической проблемой является получение такого материала (трансплантата), который бы обеспечивал укрепление костной ткани плечевой кости и надежную фиксацию области перелома, с одной стороны, обладал остеокондуктивным эффектом, с другой стороны, и не требовал специальных условий хранения и предварительной обработки перед использованием.
Раскрытие изобретения
Техническим результатом изобретения является создание костного аллогенного трансплантата, обеспечивающего укрепление проксимального отдела плечевой кости при хирургическом лечении сложных многооскольчатых переломов плеча, сопровождающимися дефицитом костной ткани и создание условий для облегчения репозиции отломков и сращения перелома. Заявляемый трансплантат обладает также остеокондуктивными свойствами, может служить носителем биологически активных веществ и не требует специальных условий для хранения.
Укрепление костной ткани плечевой кости и надежная фиксация области перелома реализуются за счет наличия головки, которая не позволяет проваливаться трансплантату в костно-мозговой канал плечевой кости, удерживая его до фиксации перелома, заполняет дефект губчатой кости головки плеча, за счет наличия шейки и верхней части диафиза малоберцовой кости, которые армируют область перелома. Остеокондуктивный эффект реализуется за счет уменьшения массы кортикальной и губчатой не деминерализованной кости путем высверливания отверстий диаметром 2 мм на расстоянии 3-4 мм друг от друга и за счет наличия в естественных и сформированных путем высверливания полостях губки из аллогенного коллагена 1 типа. Губка обладает гигроскопичностью, т.е. при насыщении губки биологически активными веществами трансплантат может приобретать остеоиндуктивные свойства.
Заявляемый технический результат обеспечивается комбинированным костным аллогенным трансплантатом для лечения сложных переломов проксимального отдела плечевой кости, содержащим не деминерализованный костный блок, полученный из кости донора, представляющий собой фрагмент малоберцовой кости длиной 6-8 см, включающий головку, шейку и часть диафиза, снабженный по всей поверхности сквозными каналами, выполненными диаметром не более 2 мм, расположенными на расстоянии 3-5 мм друг от друга, при этом естественные полости и сформированные отверстия костного блока заполнены коллагеном 1 типа человека в виде губки с мелкоячеистой структурой, которая может быть сформирована лиофилизацией костного блока, пропитанного раствором коллагена.
Заявляемый технический результат обеспечивается также способом получения комбинированного костного аллогенного трансплантата для лечения сложных переломов проксимального отдела плечевой кости, включающего формирование из замороженной при температуре -40°С малоберцовой кости донора, фрагмента, включающего головку с шейкой и частью диафиза общей длиной 6-8 см; при формировании фрагмента удаляют надкостницу, хрящ и остатки мягких тканей, после чего по всей поверхности фрагмента формируют сквозные отверстия диаметром не более 2 мм на расстоянии 3-5 мм друг от друга с последующим его обезвоживанием, обезжириванием и сушкой, после чего полученный перфорированный костный блок пропитывают раствором коллагена 1 (водный) типа человека с последующей лиофилизацией при условиях, обеспечивающих превращение раствора коллагена в губку с мелкоячеистой структурой по всему объему костного блока, после чего полученный трансплантат обезвоживают, обезжиривают и сушат.
Пропитку костного блока раствором коллагеном осуществляют посредством центрифугирования, при этом костный блок помещают в контейнер с жесткими стенками заливают 0,75-0,8% раствором коллагена 1 типа человека так, чтобы он полностью покрыл кость, контейнер закрывают крышкой и помещают ее в центрифугу, центрифугирование проводят с ускорением 100g в течение 30 мин, после чего сеанс центрифугирования повторяют с добавлением раствора коллагена в контейнер до исходного уровня, количество сеансов выполняют до полного насыщения костного блока коллагеном, при котором после сеанса центрифугирования объем коллагена не перестанет уменьшаться.
Перфорированный костный блок обезжиривают, для чего его заливают смесью 95% спирта и эфира в соотношении 1:1 на сутки, затем заливают чистым эфиром на сутки.
Сушку полученного трансплантата осуществляют в вытяжном шкафу в течение 24 часов при комнатной температуре (18-24°С).
Краткое описание чертежей
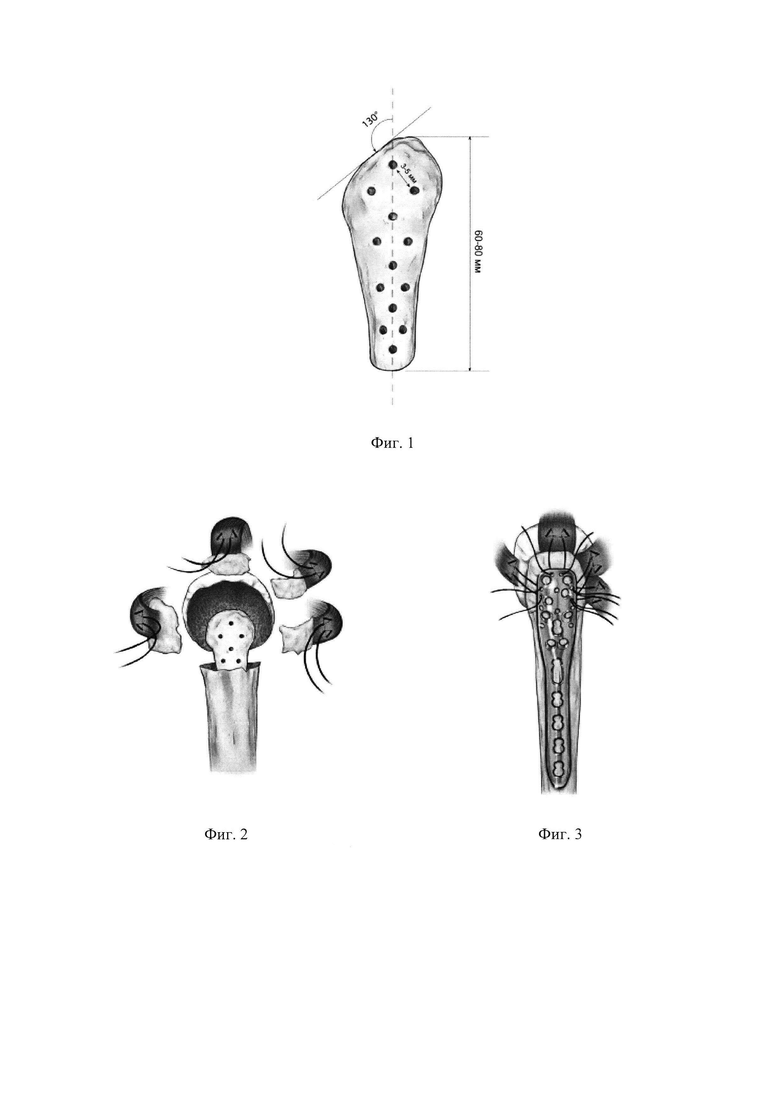
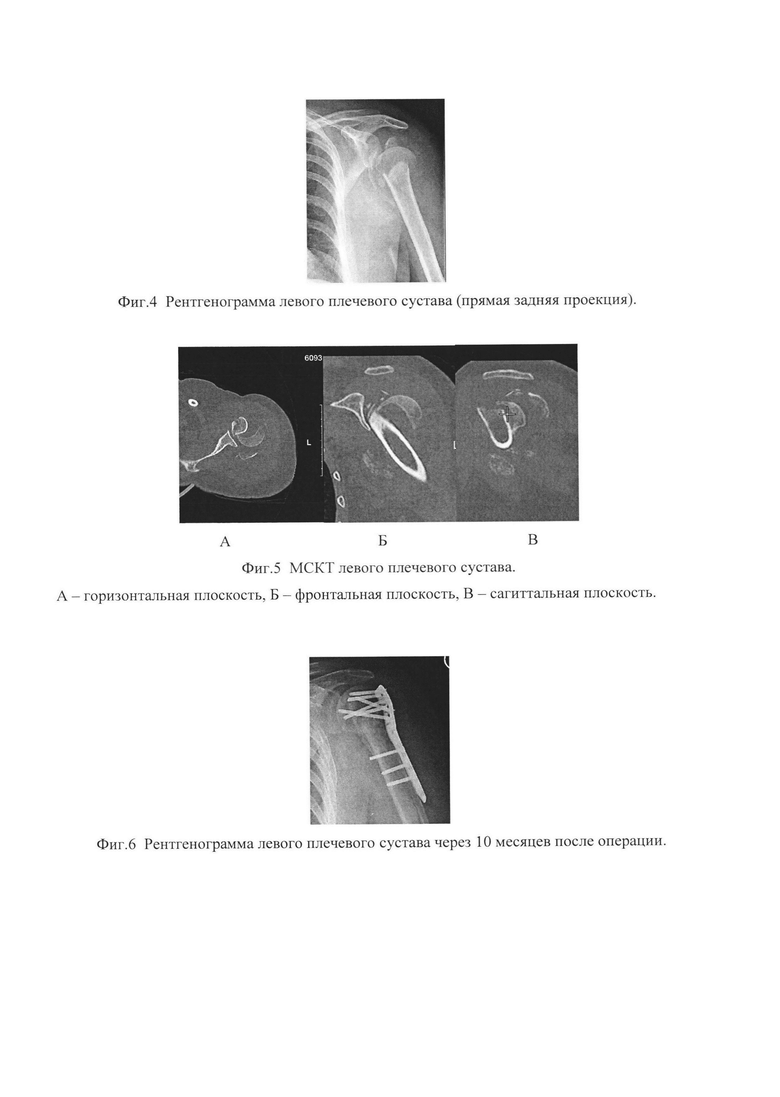
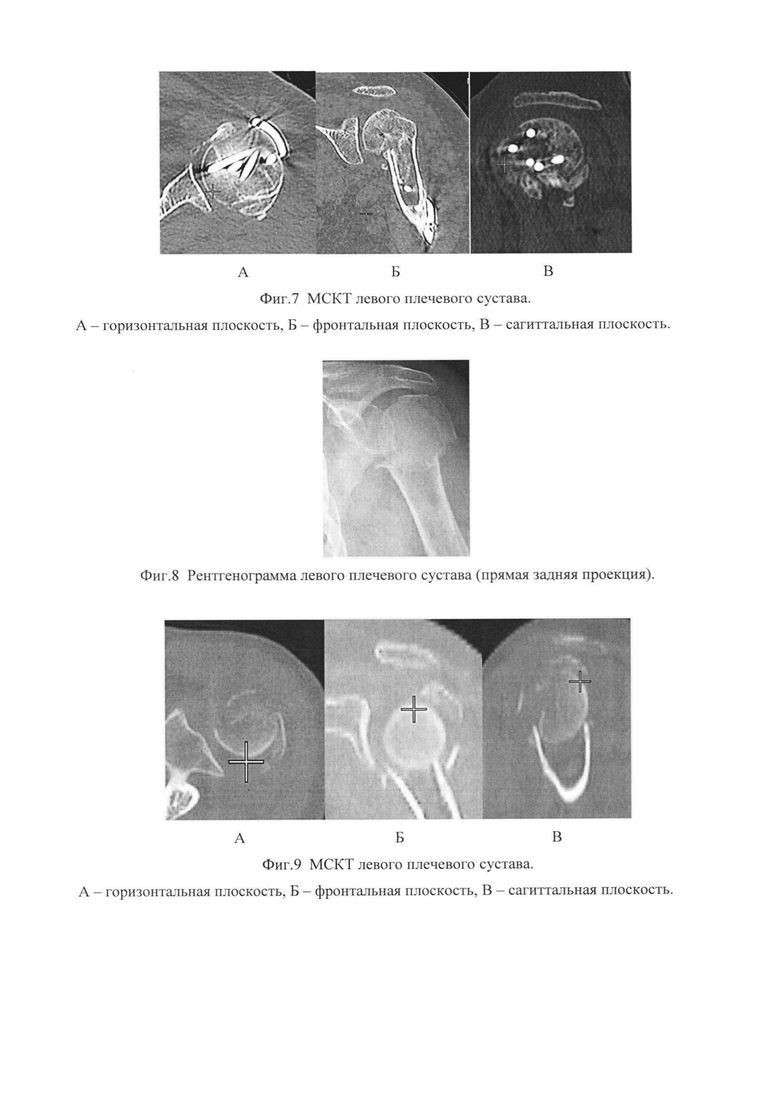
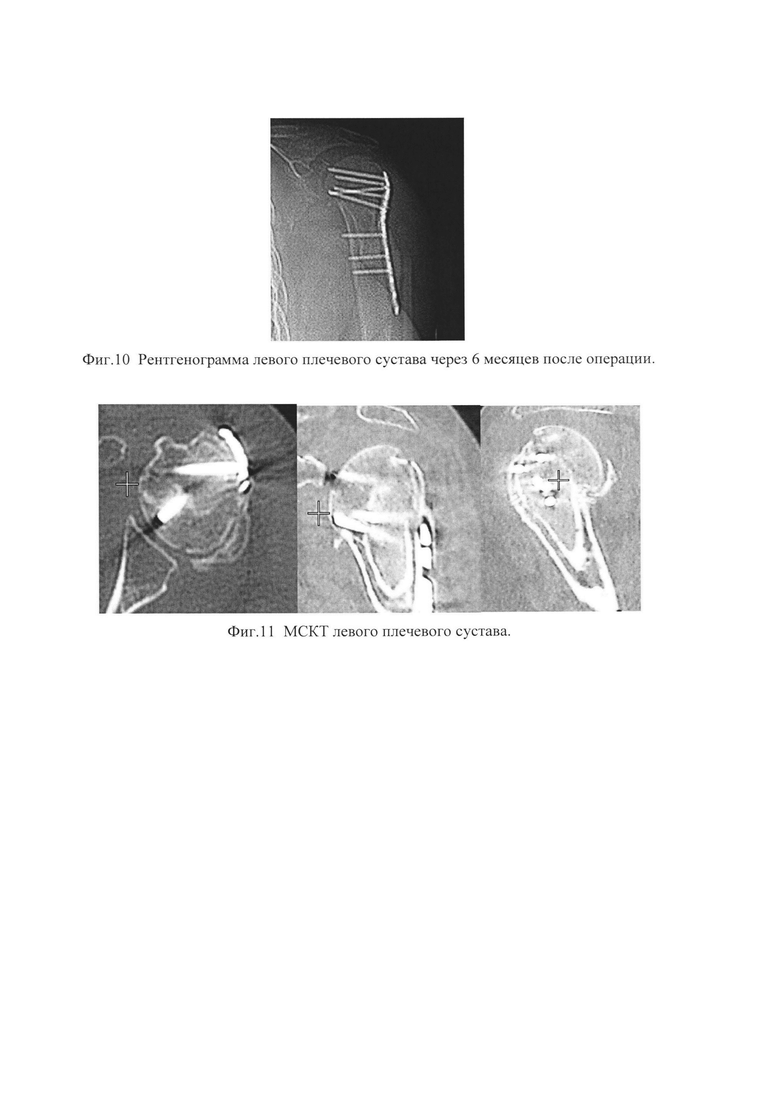
Изобретение поясняется чертежами, где на фиг. 1 представлен общий вид трансплантата, на фиг. 2 - показана схема установки трансплантата в костно-мозговой канал с прошиванием сухожилий вращающей манжеты плеча; на фиг. 3 представлен зафиксированный пластиной перелом проксимального отдела плечевой кости после репозиции отломков и прикрепленными к пластине сухожилиями. На фиг. 4-7 представлены результаты исследования конкретного пациента по примеру 1 с многооскольчатым переломом проксимального отдела плечевой кости с дефицитом костной ткани; в частности, на фиг. 4 представлена рентгенограмма левого плечевого сустава (прямая задняя проекция), на фиг. 5 - МСКТ левого плечевого сустава, А - горизонтальная плоскость, Б - фронтальная плоскость, В - сагиттальная плоскость; на фиг. 6 - рентгенограмма левого плечевого сустава через 8 месяцев после операции. Перелом срастается. Признаков коллапса головки плечевой кости нет. Еще прослеживается диафизарная перфорированная часть трансплантата; на фиг. 7 - МСКТ левого плечевого сустава. Трансплантат перестраивается - нет границы между собственной губчатой костью и губчатой костью трансплантата, что говорит о выраженном остеокондуктивном эффекте трансплантата, А - горизонтальная плоскость, Б - фронтальная плоскость, В - сагиттальная плоскость; на фиг. 8-11 представлены результаты исследования конкретного пациента по примеру 2 с многооскольчатым перелом проксимального отдела плечевой кости с дефицитом костной ткани, в частности, на фиг. 8 представлена рентгенограмма левого плечевого сустава (прямая задняя проекция); на фиг. 9 - МСКТ левого плечевого сустава, А - горизонтальная плоскость, Б - фронтальная плоскость, В - сагиттальная плоскость; на фиг. 10 - рентгенограмма левого плечевого сустава через 6 месяцев после операции. Перелом срастается. Небольшой коллапс головки плечевой кости. Еще прослеживается диафизарная перфорированная часть трансплантата, на фиг. 11 - МСКТ левого плечевого сустава. Трансплантат перестраивается - граница между собственной губчатой костью и губчатой костью трансплантата исчезает, что говорит о выраженном остеокондуктивном эффекте трансплантата.
Осуществление изобретения
Ниже представлено более детальное описание заявляемого решения.
Для изготовления трансплантата используют головку, шейку и часть диафиза малоберцовой кости, полученные в ходе посмертного донорства в соответствии с законом РФ от 22.12.1992 №4180-1 «О трансплантации органов и (или) тканей человека». Малоберцовую кость получают из голени кадавера не позднее 24 часов после смерти. Продольным наружным разрезом вдоль голени обнажают целиком малоберцовую кость, извлекают ее. Извлеченный материал замораживают при температуре -40°С и помещают в карантин до получения анализов на трансмиссивные инфекции.
После подтверждения отсутствия инфекций от замороженной малоберцовой кости отпиливают фрагмент, включающий головку малоберцовой кости с шейкой и частью диафиза таким образом, чтобы общая длина составила 6-8 см. Надкостницу, хрящ и остатки мягких тканей удаляют электрической ленточной пилой. Затем сверлом диаметром 2 мм формируют сквозные отверстия по всей поверхности кости на расстоянии 3-5 мм друг от друга, таким образом уменьшая массу кости и создавая ниши для заполнения раствором коллагена 1 типа. Полученный костный блок погружают в 3% раствор перекиси водорода и под вакуумный отсос минус 2 атмосферы для удаления жира и остатков костного мозга. Раствор перекиси водорода меняют каждые 20 минут, пока раствор не станет светлым. Следующим этапом, кость 3-4 раза промывают в физиологическом растворе и вновь погружают в 3% раствор перекиси водорода и оставляют в холодильной камере при температуре +4°С на медицинском шейкере. Через 12-20 часов костные фрагменты погружают для обезвоживания в 95% спирт и оставляют на сутки при температуре +4° на медицинском шейкере. После извлечения из спирта, для обезжиривания кость заливают смесью 95% спирта и эфира в соотношении 1:1 на сутки. Затем заливают чистым эфиром на сутки. Последним этапом пассивно сушат изделие в вытяжном шкафу в течение 24 часов. Костный блок готов для насыщения раствором коллагена 1 типа.
Для увеличения остеокондуктивного потенциала и увеличения гигроскопичности трансплантата кость насыщают водным раствором коллагена (например, с концентрацией 0,75-0,8% по объему) в специальной центрифуге. Трансплантат помещают в стерильный одноразовый контейнер с жесткими стенками и крышкой (например, пластиковую пробирку с винтовой крышкой). Контейнер заливают раствором коллагена 1 типа человека так, чтобы он полностью покрыл кость, контейнер закрывают крышкой и помещают ее в центрифугу. Центрифугирование проводят с ускорением 100g в течение 30 мин. Количество коллагена, находящегося в пробирке, в процессе центрифугирования уменьшается (уходит в кость), поэтому коллаген периодически добавляют так, чтоб он вновь покрывал трансплантат, и повторяют сеанс центрифугирования до тех пор, пока объем коллагена не перестанет уменьшаться. Это расценивают как полное насыщение кости коллагеном.
После насыщения изделия коллагеном его замораживают при температуре -80°, помещают в лиофильную камеру и лиофилизируют в течение 2,5-4 часов до полного высыхания коллагена. После лиофилизации раствор коллагена, который находится в костном трансплантате в сформированных каналах, трансформируется в гигроскопичную губку, обладающую выраженным остеокондуктивным эффектом и за счет своей гигроскопичности может быть носителем биологически активных веществ.
Данный трансплантат был использован при хирургическом лечении сложных многооскольчатых переломов проксимального отдела плечевой кости, сопровождающихся дефицитом костной ткани.
При наличии у больного трех-четырехфрагментного перелома проксимального отдела плечевой кости на фоне остеопороза, сопровождающегося дефицитом костной ткани, что диагностируется при компьютерной томографии плечевого сустава, стандартным дельто-пектоальным доступом обнажают проксимальный отдел плечевой кости. После идентификации поврежденных структур - головки плеча, большого и малого бугорков, последовательно прошивают сухожилия подлопаточной, надостной, подостной и малой круглой мышц нерассасывающимися нитями (например, Терилен 5, FiberWire 2). Пользуясь нитями как вожжами, разводят сухожилия и прикрепленные к ним остатки бугорков в стороны. Для обзора открываются костно-мозговой канал плечевой кости и субхондральная кость головки плечевой кости. Костно-хрящевая часть головки в такой ситуации напоминает яичную скорлупу. Полученный заранее в костном банке трансплантат для регидратации на 15 минут замачивают в физиологическом растворе или пропитывают биологически активными веществами, например, лизатом аутологичных тромбоцитов, богатой тромбоцитами плазмой, костным морфогенетическим белком. После этого трансплантат диафизарной частью вводят в костно-мозговой канал, куда он проваливается до головки. Одна из поверхностей головки малоберцовой кости является скошенной. Эту поверхность ориентируют на суставную впадину лопатки, т.к. угол между диафизом плечевой кости и головкой плечевой кости после репозиции должен составлять примерно 130°. Тягой за нити остатки бугорков и головки плеча натягивают на головку малоберцовой кости «как капюшон на голову». Скошенная поверхность головки малоберцовой кости позволяет ориентировать головку плечевой кости под углом примерно 130° без усилий. С помощью нитей сопоставляют большой и малый бугорки. Флюороскопом контролируют положение отломков. При удовлетворительном положении отломков проводят нити через специальные отверстия пластины с угловой стабильностью для проксимального отдела плеча (DC или PHILOS). Затягивают нити, тем самым правильно позиционируя пластину - на 5-10 мм дистальнее верхушки большого бугорка и кзади от гребня большого бугорка. Временно фиксируют пластину к головке центральной спицей. Наличие трансплантата позволяет это сделать, т.к. головка трансплантата, состоящая из губчатой кости замещает дефект костной ткани головки плечевой кости. Далее через пластину в головку вводят 2-3 проксимальных блокирующихся в пластине винта, которые благодаря трансплантату, прочно фиксируются в губчатой кости трансплантата и остатках субхондральной кости головки плечевой кости. Следующим этапом пластину крепят к диафизу плечевой кости кортикальным винтом в овальное отверстие. Пластина на диафизе должна располагаться кзади и параллельно по отношению к гребню большого бугорка. После этого фиксируют бугорки, затягивая и завязывая нити на пластине.
Клинический пример 1. Больная М. 56 лет, обратилась в НИИ СП после падения на улице. При поступлении диагностирован закрытый многооскольчатый перелом проксимального метаэпифиза левой плечевой кости со смещением (см. фиг. 4). На 7 сутки произведен остеосинтез проксимального метаэпифиза левой плечевой кости пластиной с угловой стабильностью с костной пластикой заявляемым комбинированным аллогенным трансплантатом из головки малоберцовой кости. В послеоперационном периоде проводилась попеременная иммобилизация руки косыночной повязкой в течение 6 недель, больная занималась лечебной гимнастикой. При контрольных рентгенографии и МСКТ через 8 месяцев после операции выявлено, что вторичного смещения отломков нет, перелом срастается, трансплантат перестраивается (см. фиг. 6, 7).
Клинический пример 2. Больная М. 76 лет, обратилась в НИИ СП после падения на улице. При поступлении диагностирован закрытый многооскольчатый перелом проксимального метаэпифиза левой плечевой кости со смещением (см. фиг. 8). На 4 сутки произведен остеосинтез проксимального метаэпифиза левой плечевой кости пластиной с угловой стабильностью с костной пластикой заявляемым комбинированным аллогенным трансплантатом из головки малоберцовой кости. В послеоперационном периоде проводилась попеременная иммобилизация руки косыночной повязкой в течение 6 недель, больная занималась лечебной гимнастикой. При контрольной рентгенографии и МСКТ через 6 месяцев после операции выявлено, что вторичного смещения отломков нет, перелом срастается, трансплантат перестраивается.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ СЛОЖНЫХ ПЕРЕЛОМОВ ПРОКСИМАЛЬНОГО ОТДЕЛА ПЛЕЧЕВОЙ КОСТИ | 2019 |
|
RU2721936C1 |
| Способ пластики костных дефектов головки плечевой кости при задних блокированных вывихах плечевой кости | 2024 |
|
RU2831905C1 |
| КОМБИНИРОВАННЫЙ КОСТНЫЙ АЛЛОТРАНСПЛАНТАТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2524618C1 |
| Способ реверсивного эндопротезирования плечевого сустава у больных с посттравматическим дефицитом костной ткани проксимального отдела плечевой кости с использованием персонифицированного 3D аугмента проксимального отдела плечевой кости | 2023 |
|
RU2810943C1 |
| СПОСОБ ОСТЕОСИНТЕЗА ПРИ ПЕРЕЛОМАХ ПРОКСИМАЛЬНОГО ОТДЕЛА ПЛЕЧЕВОЙ КОСТИ | 2019 |
|
RU2712298C1 |
| СПОСОБ ОСТЕОСИНТЕЗА ПРОКСИМАЛЬНОГО ОТДЕЛА ПЛЕЧЕВОЙ КОСТИ ПУТЕМ ПЕРИИМПЛАНТНОЙ ДИСТРАКЦИИ И ФИКСАЦИИ | 2023 |
|
RU2816627C1 |
| СПОСОБ НАСЫЩЕНИЯ КОЛЛАГЕНОМ ТРАНСПЛАНТАТА КОСТНОЙ ТКАНИ | 2020 |
|
RU2748991C1 |
| Способ хирургического лечения перелома проксимального отдела плечевой кости | 2016 |
|
RU2652573C1 |
| Способ пластики посттравматических околосуставных дефектов длинных трубчатых костей (варианты) | 2022 |
|
RU2798904C1 |
| СПОСОБ ЛЕЧЕНИЯ ПЕРЕЛОМОВ ПРОКСИМАЛЬНОГО КОНЦА ПЛЕЧЕВОЙ КОСТИ | 2003 |
|
RU2242187C2 |
Группа изобретений относится к медицине. Комбинированный костный аллогенный трансплантат для лечения сложных переломов проксимального отдела плечевой кости содержит не деминерализованный костный блок, полученный из кости донора, представляющий собой фрагмент малоберцовой кости длиной 6-8 см, включающий головку, шейку и часть диафиза, снабженный по всей поверхности сквозными каналами, выполненными диаметром не более 2 мм, расположенными на расстоянии 3-5 мм друг от друга, при этом отверстия костного блока заполнены коллагеном 1 типа человека в виде губки с мелкоячеистой структурой. Способ получения комбинированного костного аллогенного трансплантата включает формирование из замороженной при температуре -40°С малоберцовой кости донора, фрагмента, включающего головку с шейкой и частью диафиза общей длиной 6-8 см, при формировании фрагмента удаляют надкостницу, хрящ и остатки мягких тканей, после чего по всей поверхности фрагмента формируют сквозные отверстия диаметром не более 2 мм на расстоянии 3-5 мм друг от друга с последующим его обезвоживанием, обезжириванием и сушкой, после чего полученный перфорированный костный блок пропитывают раствором коллагена 1 типа человека с последующей лиофилизацией при условиях, обеспечивающих превращение раствора коллагена в губку с мелкоячеистой структурой по всему объему костного блока. Изобретения обеспечивают укрепление проксимального отдела плечевой кости при хирургическом лечении сложных многооскольчатых переломов плеча, сопровождающихся дефицитом костной ткани, и создание условий для облегчения репозиции отломков и сращения перелома. 2 н. и 4 з.п. ф-лы, 2 пр., 11 ил.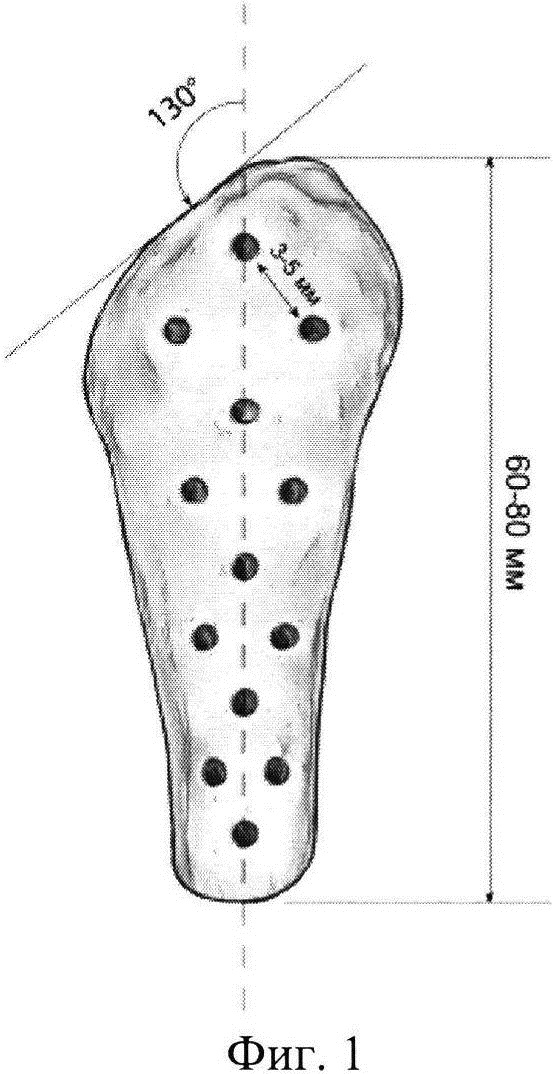
1. Комбинированный костный аллогенный трансплантат для лечения сложных переломов проксимального отдела плечевой кости, содержащий не деминерализованный костный блок, полученный из кости донора, представляющий собой фрагмент малоберцовой кости длиной 6-8 см, включающий головку, шейку и часть диафиза, снабженный по всей поверхности сквозными каналами, выполненными диаметром не более 2 мм, расположенными на расстоянии 3-5 мм друг от друга, при этом отверстия костного блока заполнены коллагеном 1 типа человека в виде губки с мелкоячеистой структурой.
2. Трансплантат по п. 1, характеризующийся тем, что коллаген 1 типа человека в виде губки с мелкоячеистой структурой в естественных полостях и отверстиях костного блока сформирован лиофильной сушкой костного блока, пропитанного раствором коллагена.
3. Способ получения комбинированного костного аллогенного трансплантата по п. 1 для лечения сложных переломов проксимального отдела плечевой кости, включающий формирование из замороженной при температуре -40°С малоберцовой кости донора, фрагмента, включающего головку с шейкой и частью диафиза общей длиной 6-8 см, при формировании фрагмента удаляют надкостницу, хрящ и остатки мягких тканей, после чего по всей поверхности фрагмента формируют сквозные отверстия диаметром не более 2 мм на расстоянии 3-5 мм друг от друга с последующим его обезвоживанием, обезжириванием и сушкой, после чего полученный перфорированный костный блок пропитывают раствором коллагена 1 типа человека с последующей лиофилизацией при условиях, обеспечивающих превращение раствора коллагена в губку с мелкоячеистой структурой по всему объему костного блока.
4. Способ по п. 3, характеризующийся тем, что пропитку костного блока раствором коллагеном осуществляют посредством центрифугирования, при этом костный блок помещают в контейнер с жесткими стенками, заливают 0,75-0,8 об.% раствором коллагена 1 типа человека так, чтобы он полностью покрыл кость, контейнер закрывают крышкой и помещают ее в центрифугу, центрифугирование проводят с ускорением 100g в течение 30 мин, после чего сеанс центрифугирования повторяют с добавлением раствора коллагена в контейнер до исходного уровня, количество сеансов выполняют до полного насыщения костного блока коллагеном, характеризующегося сохранением объема коллагена в контейнере после очередного центрифугирования.
5. Способ по п. 3, характеризующийся тем, что для обезжиривания перфорированный костный фрагмент заливают смесью 95% спирта и эфира в соотношении 1:1 на сутки, затем заливают чистым эфиром на сутки.
6. Способ по п. 3, характеризующийся тем, что сушку перфорированного костного фрагмента проводят в вытяжном шкафу в течение 24 часов.
| КОМБИНИРОВАННЫЙ КОСТНЫЙ АЛЛОТРАНСПЛАНТАТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2524618C1 |
| Стекатель для виноматериалов | 1955 |
|
SU105584A1 |
| БИОТРАНСПЛАНТАТ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ ДЕГЕНЕРАТИВНЫХ И ТРАВМАТИЧЕСКИХ ЗАБОЛЕВАНИЙ КОСТНОЙ ТКАНИ ЧЕЛЮСТНО-ЛИЦЕВОЙ ОБЛАСТИ | 2008 |
|
RU2380105C1 |
| Устройство для формирования в газовой среде многослойного облагороженного ковра из лигноцеллюлозных и подобных частиц | 1975 |
|
SU547369A2 |
| Фильтр для очистки жидкостей | 1990 |
|
SU1725963A1 |
| US 5977432 A1, 02.11.1999 | |||
| US 20180064548 A1, 08.03.2018. | |||
Авторы
Даты
2020-05-25—Публикация
2019-07-31—Подача