ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Данная заявка притязает на приоритет по предварительной заявке США № 62/091319, поданной 12 декабря 2014, и предварительной заявке США № 62/095673, поданной 22 декабря 2014, которые включены в нее путем ссылки во всей своей полноте во всех отношениях.
УРОВЕНЬ ТЕХНИКИ
[0002] Гидроксиметилфурфурол (ГМФ) и дизамещенные фурановые производные представляют собой ключевые промежуточные химикаты в производственной цепи, основанной на возобновляемых источниках углерода, например, лигноцеллюлозной биомассы. Желательными являются эффективные, масштабируемые процессы и способы, которые используют лигноцеллюлозную биомассу для получения с высокими выходами гидроксиметилфурфурола и дизамещенных фурановых производных.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0003] Настоящее изобретение предоставляет процессы, способы, системы и композиции для эффективного использования биомассы для производства гидроксиметилфурфурола, дизамещенных фурановых производных и сахаридов.
[0004] Здесь предоставлены способы конверсии целлюлозной пульпы в гидроксиметилфурфурол. Способы могут включать в себя: разделение потока обедненного лигнином гидролизата, содержащего ионы натрия в количестве не более 5%, чтобы тем самым получить первый поток, содержащий воду и гидроксиметилфурфурол; второй поток, содержащий воду и глюкозу; и третий поток, содержащий воду и целлобиозу; изомеризацию глюкозы во втором потоке, чтобы тем самым получить фруктозу; и дегидратацию фруктозы, чтобы тем самым получить продукт реакции, содержащий гидроксиметилфурфурол.
[0005] В раскрытых здесь способах способы могут дополнительно включать в себя: кондиционирование целлюлозной пульпы в растворителе, чтобы тем самым сформировать кондиционированную пульпу; гидролиз кондиционированной пульпы в водном растворе, содержащем кислый катализатор, чтобы тем самым получить поток гидролизата; и удаление по меньшей мере некоторого лигнина из потока гидролизата, чтобы тем самым получить поток обедненного лигнином гидролизата и обогащенную лигнином композицию, причем удаление включает в себя контроль pH водного раствора и разбавление водного раствора водой; где кондиционирование, гидролиз и удаление происходят перед разделением, изомеризацией и дегидратацией.
[0006] В раскрытых здесь способах растворитель может содержать ионную жидкость. В раскрытых здесь способах второй поток содержит ионную жидкость и третий поток содержит ионную жидкость. В раскрытых здесь способах способ может дополнительно включать в себя перенаправление потока обедненного лигнином гидролизата из первого сосуда во второй сосуд перед разделением, изомеризацией и дегидратацией. В раскрытых здесь способах способы могут дополнительно включать в себя рециркуляцию продукта реакции, причем рециркуляция включает в себя введение продукта реакции из дегидратации на разделение. В раскрытых здесь способах способы могут дополнительно включать в себя улавливание гидроксиметилфурфурола из продукта реакции, причем улавливание включает в себя адсорбцию на нефункциональном полимере гидроксиметилфурфурола из продукта реакции; и извлечение гидроксиметилфурфурола, причем извлечение включает в себя десорбцию растворителем. В раскрытых здесь способах продукт реакции может содержать органическую кислоту.
[0007] В раскрытых здесь способах улавливание может дополнительно включать в себя контроль pH продукта реакции выше pKa органической кислоты, так чтобы вода и органические анионы не адсорбировались на нефункциональном полимере. В раскрытых здесь способах pH продукта реакции можно контролировать так, что значение составляло более 5,8. В раскрытых здесь способах ионная жидкость может быть выбрана из хлорида 1-этил-3-метилимидазолия или хлорида 1-бутил-3-метилимидазолия. В раскрытых здесь способах способы могут дополнительно включать в себя осуществление конверсии ионной жидкости в ионную жидкость в гидроксидной форме, причем осуществление конверсии включает в себя приведение в контакт водного раствора ионной жидкости, содержащего ионную жидкость, с сильноосновной анионообменной смолой в гидроксидной форме. В раскрытых здесь способах изомеризация может включать в себя контроль pH, причем контроль включает в себя использование ионной жидкости в гидроксидной форме в качестве основания. В раскрытых здесь способах изомеризация может быть катализирована ионной жидкостью в гидроксидной форме. В раскрытых здесь способах ионная жидкость в гидроксидной форме может образовывать ионную жидкость в хлоридной форме, которую используют для дегидратации.
[0008] Здесь предоставлены способы рециркуляции ионной жидкости в замкнутом технологическом контуре. Способы могут включать в себя: приведение в контакт разбавленного водного потока, содержащего катион имидазолия, со смолой, причем приведение в контакт включает в себя адсорбцию катиона имидазолия на смоле, где смола представляет собой слабокислую катионообменную смолу в депротонированной форме; десорбцию катиона имидазолия, причем десорбция включает в себя приведение в контакт смолы с раствором, содержащим хлористоводородную кислоту; и повторное введение раствора и катиона имидазолия в замкнутый технологический контур для дальнейшего использования.
[0009] В раскрытых здесь способах замкнутый технологический контур может быть использован для спаривания реакции изомеризации с реакцией дегидратации. В раскрытых здесь способах реакция изомеризации может включать в себя изомеризацию глюкозы с образованием фруктозы, и где реакция дегидратации включает в себя дегидратацию фруктозы с образованием гидроксиметилфурфурола.
[0010] Здесь предоставлены системы для конверсии глюкозы в гидроксиметилфурфурол. Системы могут включать в себя: установку хроматографического разделения, выполненную с возможностью разделения потока, содержащего ионы натрия в количестве не более 5%, на первый поток, второй поток и третий поток; причем первый поток содержит воду и гидроксиметилфурфурол; второй поток содержит воду и глюкозу; и третий поток содержит воду и целлобиозу; установку изомеризации, выполненную с возможностью осуществления изомеризации глюкозы во фруктозу, причем изомеризация включает в себя обработку второго потока основанием, чтобы тем самым получить обработанный основанием второй поток; и установку дегидратации, выполненную с возможностью дегидратации фруктозы в гидроксиметилфурфурол.
[0011] В раскрытых здесь системах второй поток может включать в себя ионную жидкость и третий поток включает в себя ионную жидкость. В раскрытых здесь системах системы могут дополнительно включать в себя вторую установку хроматографического разделения, выполненную с возможностью разделения второго потока, чтобы тем самым получить поток продукта, содержащий глюкозу. В раскрытых здесь системах системы могут дополнительно включать в себя установку очистки глюкозы, выполненную с возможностью очистки потока продукта, содержащего глюкозу, в продукт глюкозы, причем установка очистки глюкозы включает в себя по меньшей мере одну установку, выбранную из сильнокислой катионной смолы, анионообменника, смолы с активированным углем или испарительной установки. В раскрытых здесь системах поток продукта может содержать глюкозу с содержанием глюкозы по меньшей мере 60% (масса/масса).
[0012] Здесь раскрыты способы конверсии целлюлозы в гидроксиметилфурфурол. Способы могут включать в себя получение по меньшей мере 60 г гидроксиметилфурфурола в качестве продукта на каждые 100 г целлюлозы, предусматриваемой в качестве исходного материала.
[0013] В раскрытых здесь способах по меньшей мере 63 г гидроксиметилфурфурола можно получить в качестве продукта на каждые 100 г целлюлозы, предусматриваемой в качестве исходного материала. В раскрытых здесь способах по меньшей мере 65 г гидроксиметилфурфурола можно получить в качестве продукта на каждые 100 г целлюлозы, предусматриваемой в качестве исходного материала. В раскрытых здесь способах по меньшей мере 67 г гидроксиметилфурфурола можно получить в качестве продукта на каждые 100 г целлюлозы, предусматриваемой в качестве исходного материала. В раскрытых здесь способах способы могут включать в себя гидролиз целлюлозы в первый поток сахара, содержащий по меньшей мере 80% глюкозы (масса/сухое вещество). В раскрытых здесь способах гидролиз может происходить в ионной жидкости. В раскрытых здесь способах ионная жидкость может быть выбрана из хлорида 1-бутил-3-метилимидазолия или хлорида 1-этил-3-метилимидазолия. В раскрытых здесь способах первый поток сахара может содержать целлобиозу, гидроксиметилфурфурол и органические кислоты.
[0014] В раскрытых здесь способах способы могут дополнительно включать в себя хроматографическое разделение второго потока сахара, содержащего гидроксиметилфурфурол, целлобиозу, ионную жидкость, глюкозу и фруктозу; причем хроматографическое разделение включает в себя применение последовательной хроматографии с симулированным движением стационарной фазы. В раскрытых здесь способах хроматографическое разделение может давать первый выходящий поток, второй выходящий поток и третий выходящий поток; причем первый выходящий поток содержит гидроксиметилфурфурол; второй выходящий поток содержит ионную жидкость и глюкозу; и третий выходящий поток содержит ионную жидкость и целлобиозу. В раскрытых здесь способах в последовательной хроматографии с симулированным движением стационарной фазы можно использовать смолу промышленной категории, включающую размеры бусин по меньшей мере 300 микрон. В раскрытых здесь способах способы могут включать в себя обработку второго выходящего потока основанием, причем обработка включает в себя изомеризацию по меньшей мере части глюкозы во фруктозу, чтобы тем самым получить обработанный основанием второй поток. В раскрытых здесь способах основание может содержать ионную жидкость, где ионная жидкость находится в гидроксидной форме.
[0015] В раскрытых здесь способах способы могут дополнительно включать в себя обработку обработанного основанием второго потока, причем обработка включает в себя дегидратацию фруктозы в гидроксиметилфурфурол, чтобы тем самым получить дегидратированный второй поток, причем дегидратация включает в себя применение дегидратирующего агента. В раскрытых здесь способах не более 10% глюкозы, присутствующей в обработанном основании втором потоке, может подвергаться реакции с дегидратирующим агентом.
[0016] В раскрытых здесь способах способы могут дополнительно включать в себя выделение гидроксиметилфурфурола, причем выделение включает в себя по меньшей мере одно из: обработку дегидратированного второго потока, причем обработка включает в себя использование гидрофобной смолы, чтобы тем самым уловить гидроксиметилфурфурол; десорбцию уловленного гидроксиметилфурфурола с гидрофобной смолы, причем десорбция включает в себя приведение нагруженной смолы в контакт с растворителем S2; прибавление органического растворителя; и дистилляцию растворителя S2, используя азеотропную дистилляцию. В раскрытых здесь способах растворитель S2 может представлять собой этилацетат.
[0017] В раскрытых здесь способах способы могут дополнительно включать в себя рециркуляцию ионной жидкости, причем рециркуляция включает в себя: обработку первой части потока ионной жидкости слабокислой катионообменной смолой, чтобы тем самым сформировать поток, обработанный слабокислой катионообменной смолой; прибавление растворителя к потоку, обработанному слабокислой катионообменной смолой; дистилляцию растворителя и воды, чтобы тем самым сформировать поток дегидратированной ионной жидкости; и введение в процесс ионной жидкости из потока дегидратированной ионной жидкости. В раскрытых здесь способах ионная жидкость из потока дегидратированной ионной жидкости может быть введена в реактор, содержащий целлюлозу, и где в реакторе целлюлоза подвергается гидролизу в глюкозу. В раскрытых здесь способах способы могут дополнительно включать в себя рециркуляцию ионной жидкости, причем рециркуляция включает в себя обработку потока, содержащего ионную жидкость, слабокислой катионообменной смолой, чтобы тем самым получить обработанный смолой поток, содержащий ионную жидкость; и повторное введение в процесс ионной жидкости из обработанного смолой потока. В раскрытых здесь способах ионная жидкость из обработанного смолой потока может быть повторно введена в композицию, содержащую по меньшей мере 70% глюкана (масса/сухое вещество). В раскрытых здесь способах по меньшей мере 99% ионной жидкости может быть рециркулировано, чтобы тем самым получить рециркулированную ионную жидкость. В раскрытых здесь способах рециркулированная ионная жидкость может содержать глюкозу или целлобиозу.
[0018] Здесь предоставлены композиции фурфуроловых продуктов. Композиции фурфуроловых продуктов могут содержать по меньшей мере 5% гидроксиметилфурфурола (масса/масса) и не более 95% растворителя (масса/масса), где растворитель выбран из 2-бутанола, 2-пропанола, тетралина или воды, или их сочетания. В раскрытых здесь композициях фурфуроловых продуктов композиции фурфуроловых продуктов могут дополнительно содержать по меньшей мере 50 ч.н.млрд. (части на миллиард) маркерной молекулы, где маркерная молекула выбрана из этилацетата, катиона ионной жидкости, фурфурола, аниона левулината, аниона формиата, левулиновой кислоты, муравьиной кислоты, глюкозы, фруктозы или маннозы.
[0019] Здесь предоставлены композиции потока ионной жидкости. Композиции потока ионной жидкости могут содержать: i) по меньшей мере 95% ионной жидкости (масса/масса); ii) от 0,1 до 2% целлобиозы (масса/масса); iii) не более 0,1% (масса/масса) фруктозы; iv) не более 0,1% (масса/масса) гидроксиметилфурфурола; v) не более 4% (масса/масса) воды; и vi) не более 2% (масса/масса) растворителя S3.
[0020] В раскрытых здесь композициях потока ионной жидкости композиции потока ионной жидкости могут дополнительно содержать по меньшей мере одну из следующих характеристик: i) от 0,1 до 3% глюкозы (масса/масса); ii) не более 0,1% (масса/масса) маннозы; iii) не более 0,1% (масса/масса) левулиновой кислоты; и iv) не более 0,1% (масса/масса) муравьиной кислоты. В раскрытых здесь композициях потока ионной жидкости композиции потока ионной жидкости могут дополнительно содержать по меньшей мере две из следующих характеристик: i) от 0,1 до 3% глюкозы (масса/масса); ii) не более 0,1% (масса/масса) маннозы; iii) не более 0,1% (масса/масса) левулиновой кислоты; и iv) не более 0,1% (масса/масса) муравьиной кислоты. В раскрытых здесь композициях потока ионной жидкости композиции потока ионной жидкости могут дополнительно содержать по меньшей мере три из следующих характеристик: i) от 0,1 до 3% глюкозы (масса/масса); ii) не более 0,1% (масса/масса) маннозы; iii) не более 0,1% (масса/масса) левулиновой кислоты; и iv) не более 0,1% (масса/масса) муравьиной кислоты. В раскрытых здесь композициях потока ионной жидкости растворитель S3 может представлять собой циклогексанол.
[0021] Здесь предоставлены композиции потока продукта глюкозы. Причем композиции потока продукта глюкозы содержат по меньшей мере 90% моносахаридов (масса/сухое вещество); и по меньшей мере 100 ч.н.млрд. маркерной молекулы, где маркерная молекула выбрана из катиона ионной жидкости, имидазола, производного имидазола, адъюванта имидазола-сахара, гидроксиметилфурфурола или растворителя S3. В композициях потока продукта глюкозы композиции потока продукта глюкозы могут дополнительно содержать по меньшей мере 95% C6-углевододов (масса/сухое вещество). В раскрытых здесь композициях потока продукта глюкозы композиции потока продукта глюкозы могут дополнительно содержать по меньшей мере 90% глюкозы (масса/сухой вес); и по меньшей мере один не являющийся глюкозой C6-углевод, где не являющийся глюкозой углевод представляет собой по меньшей мере на 90% маннозу (масса/масса).
[0022] Здесь предоставлены композиции целлюлозной остаточной пульпы. Композиции целлюлозной остаточной пульпы могут иметь: (i) долю C6-сахаров в твердом веществе по меньшей мере 77%; (ii) долю лигнина не более 15%; (iii) зольность не более 6%; и (iv) содержание C5-сахаров не более 2%. В раскрытых здесь композициях целлюлозной остаточной пульпы (i) доля C6-сахаров в твердом веществе может составлять по меньшей мере 90%; (ii) содержание лигнина может составлять не более 6%; и (iii) зольность может составлять не более 3%. В раскрытых здесь композициях целлюлозной остаточной пульпы (i) доля C6-сахаров в твердом веществе может составлять по меньшей мере 93%; (ii) содержание лигнина может составлять не более 5%; (iii) зольность может составлять не более 1%; и (iv) содержание C5-сахаров может составлять не более 1%. В раскрытых здесь композициях целлюлозной остаточной пульпы (i) доля C6-сахаров в твердом веществе может составлять по меньшей мере 96%; (ii) содержание лигнина может составлять не более 3%; (iii) зольность может составлять не более 0,1%; и (iv) содержание C5-сахаров может составлять не более 0,1%.
ВКЛЮЧЕНИЕ ПУТЕМ ССЫЛКИ
[0023] Все публикации, патенты и патентные заявки, упомянутые в данном описании включены в него путем ссылки в той же степени, как если бы каждая отдельная(ый) публикация, патент или патентная заявка был(а) бы конкретно и отдельно упомянут(а) как включенная(ый) путем ссылки.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0024] На Фиг. 1 проиллюстрирована схематичная диаграмма иллюстративных способов конверсии для конверсии биомассы в гидроксиметилфурфурол с необязательным сопутствующим производством очищенной глюкозы.
[0025] На Фиг. 2 проиллюстрирована схематичная диаграмма иллюстративных последующих способов конверсии для конверсии гидроксиметилфурфурол в различные продукты конверсии.
[0026] На Фиг. 3 проиллюстрирована схематичная диаграмма иллюстративного способа конверсии целлюлозной пульпы в гидроксиметилфурфурол с извлечением ионной жидкости и с необязательным сопутствующим производством очищенной глюкозы. Способ дополнительно подробно пояснен на Фиг. 4, Фиг. 5, Фиг. 6, Фиг. 7 и Фиг. 8.
[0027] На Фиг. 4 проиллюстрирована схематичная диаграмма иллюстративного способа гидролиза целлюлозной пульпы до моносахаридов в среде ионной жидкости и удаления и извлечения остаточного лигнина.
[0028] На Фиг. 5 проиллюстрирована схематичная диаграмма иллюстративного способа конверсии посредством стадий хроматографического разделения, изомеризации и дегидратации.
[0029] На Фиг. 6 проиллюстрирована схематичная диаграмма иллюстративного способа конверсии посредством стадий хроматографического разделения, изомеризации и дегидратации с необязательным отделением глюкозы в дополнение к отделению гидроксиметилфурфурола.
[0030] На Фиг. 7 проиллюстрирована схематичная диаграмма иллюстративного способа извлечения гидроксиметилфурфурола в виде раствора в растворителе, например, 2-бутаноле, из водного раствора; органические кислоты, присутствующие в водной фазе, остаются в водной фазе.
[0031] На Фиг. 8 проиллюстрирована схематичная диаграмма иллюстративного способа сушки ионной жидкости и ее рециркуляции для дальнейшего использования.
[0032] На Фиг. 9 проиллюстрированы результаты импульсного испытания, показывающие разделение хроматографией хлорида 1-этил-3-метилимидазолия, сахаридов и гидроксиметилфурфурола.
[0033] На Фиг. 10 проиллюстрированы результаты импульсного испытания, показывающие элюирование хлорида 1-бутил-3-метилимидазолия, сахаридов, гидроксиметилфурфурола и органических кислот.
[0034] На Фиг. 11 проиллюстрированы результаты импульсного испытания, показывающие разделение хроматографией глюкозы и хлорида 1-этил-3-метилимидазолия.
[0035] На Фиг. 12 проиллюстрирован временной профиль реакции изомеризации глюкозы во фруктозу в растворе, содержащем хлорид 1-бутил-3-метилимидазолия и гидроксид 1-бутил-3-метилимидазолия.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0036] Настоящее изобретение предоставляет процессы, способы, системы и композиции для эффективного использования биомассы для производства гидроксиметилфурфурола, дизамещенных фурановых производных и сахаридов. Гидроксиметилфурфурол и дизамещенные фурановые производные представляют собой промежуточные химикаты в производственной цепи, которая основана на биомассе. Биомасса может включать в себя лигноцеллюлозную биомассу, и конкретно целлюлозную остаточную пульпу. Биомасса, использованная в раскрытых здесь процессах и способах, не ограничена целлюлозной остаточной пульпой. Альтернативы целлюлозной остаточной пульпы включают в себя картон, картонные отходы, пульпу бумажного производства, растворимую пульпу, хлопковые волокна или линтер, или вторичную бумагу. Гидроксиметилфурфурол может быть извлечен в растворителе, который подходит для реакций конверсии гидроксиметилфурфурола в продукты конверсии. Гидроксиметилфурфурол может быть получен из сахаров целлюлозы, например, согласно процессам и способам конверсии (превращениям), которые раскрыты здесь. Гидроксиметилфурфурол, полученный согласно данному изобретению, может быть превращен во многие другие химические продукты. Раскрытые превращения облегчают получение ценных химикатов из биомассы.
[0037] Получение сахаров и продуктов конверсии сахаров из биомассы может включать в себя применение ионных жидкостей (ИЖ), как раскрыто здесь. Ионные жидкости и растворители с глубокой эвтектикой (РГЭ) могут растворять целлюлозу, включая кристаллическую целлюлозу. Данные высокозаряженные жидкости могут открывать кристаллическую структуру кристаллической целлюлозы, обнажая сахаридный полимер и могут содействовать его осахариванию или путем ацидолиза с помощью низкоконцентрированной минеральной кислоты (например, соляной кислоты), или путем ферментативного катализа. Описание ионных жидкостей можно также найти в патенте США 8790542; патенте США 9157130; заявке PCT/US2013/039194; патенте США 6177575 и заявке США 2010/0196967.
[0038] Целлюлозная остаточная пульпа может быть получена способами биологической переработки, такими как таковые, известные в данной области и примеры которые приведены в заявках PCT/US2013/039585 и PCT/US2013/068824. Желательно, чтобы исходный материал биомассы, например целлюлозная остаточная пульпа, содержал главным образом целлюлозу и остаточный уровень других компонентов биомассы, как описано здесь. Лигнин, зольность, гемицеллюлоза и экстрагируемые вещества, которые могут получаться в ходе переработки биомассы в целлюлозную пульпу, могут затруднять превращения и могут быть эффективно удалены для предотвращения их накопления, которое может происходить из-за рециркуляции растворителей, которые используются в процессе. В PCT/US2013/039585 и PCT/US2013/068824 раскрыты процессы и способы извлечения гемицеллюлозы, зольности и экстрагируемых веществ из биомассы в первом процессе извлечения. Остаточный лигноцеллюлозный материал может быть извлечен во втором процессе извлечения, чтобы удалить лигнин, что дает остаточную целлюлозную пульпу, по существу не содержащую лигнина, гемицеллюлоз, зольности и экстрагируемых веществ, давая в результате целлюлозную остаточную пульпу. Целлюлозная остаточная пульпа может быть получена описанными здесь процессами и способами из мягкой древесины, твердой древесины, багассы, листьев и стеблей сахарного тростника, однолетних культур, или другого сырья в виде биомассы, включая лесосечные отходы, щепа и мелкую стружку, и сельскохозяйственные или промышленные отходы.
[0039] Целлюлозную остаточную пульпу можно характеризовать известными методами характеризации. Например, целлюлозная остаточная пульпа может быть охарактеризована согласно Лабораторной аналитической методике, предусматриваемой Национальной лабораторией по изучению возобновляемой энергии в Техническом отчете NREL/TP-510-42618. Если вкратце, то лабораторная аналитической методика из NREL/TP-510-42618 включает в себя гидролиз целлюлозных и гемицеллюлозных полимеров в серной кислоте и определение растворенных сахаров, из чего можно рассчитать количество углеводов в биомассе, где лигнин определяют как оставшиеся твердое вещество. Примеры данных, полученных для целлюлозной остаточной пульпы, раскрыты здесь. Например, в примере 1, примере 2 и примере 3 описана целлюлозная остаточная пульпа из эвкалипта и сосны, а в примере 4 описана целлюлозная остаточная пульпа из багассы.
[0040] Предоставленная здесь целлюлозная остаточная пульпа может характеризоваться одним или более физическими свойствами.
[0041] В некоторых примерах целлюлозная остаточная пульпа может характеризоваться: (i) долей C6-сахаров в твердом веществе по меньшей мере 77% (масса/масса); (ii) долей лигнина не более 15% (масса/масса); (iii) зольностью не более 6% (масса/масса); и (iv) долей C5-сахаров в твердом веществе не более 2% (масса/масса). В некоторых примерах целлюлозная остаточная пульпа может характеризоваться: (i) долей C6-сахаров в твердом веществе по меньшей мере 90% (масса/масса); (ii) содержанием лигнина не более 6% (масса/масса); и (iii) зольностью не более 3% (масса/масса). В некоторых примерах целлюлозная остаточная пульпа может характеризоваться: (i) долей C6-сахаров в твердом веществе по меньшей мере 93% (масса/масса); (ii) долей лигнина не более 5% (масса/масса); (iii) зольностью не более 1% (масса/масса); и (iv) долей C5-сахаров в твердом веществе не более 1% (масса/масса). В некоторых примерах целлюлозная остаточная пульпа может характеризоваться: (i) долей C6-сахаров в твердом веществе по меньшей мере 96% (масса/масса); (ii) долей лигнина не более 3% (масса/масса); (iii) зольностью не более 0,1% (масса/масса); и (iv) долей C5-сахаров в твердом веществе не более 0,1% (масса/масса).
[0042] В некоторых примерах целлюлозная остаточная пульпа может характеризоваться: (i) долей C6-сахаров в твердом веществе по меньшей мере 70% масса/масса; (ii) долей глюкозы в твердом веществе по меньшей мере 70% масса/масса; (iii) долей C5-сахаров в твердом веществе не более 5% масса/масса; и (iv) суммарной долей сахаров в твердом веществе по меньшей мере 75% масса/масса. В некоторых примерах целлюлозная остаточная пульпа может характеризоваться: (i) долей альфа-целлюлозы не более 80, 70, 60, 50 или 40% масса/масса; (ii) долей бета-целлюлозы по меньшей мере 30, 40, 50 или 60% масса/масса; (iii) долей гамма-целлюлозы по меньшей мере 0,2, 0,5, 1 или 1,5% масса/масса; и (iv) долей экстрагируемых дихлорметаном не более 0,1% масса/масса. В некоторых примерах целлюлозная остаточная пульпа может характеризоваться: (i) средней длиной волокна не более 3, 2, 1 или 0,5 мм, (ii) средней шириной волокна примерно 20 микрометров; и (iii) содержанием мелкой фракции по меньшей мере 10, 20, 30, 40 или 50% масса/масса.
[0043] В некоторых примерах целлюлозная остаточная пульпа может характеризоваться одной или более, двумя или более, тремя или более, или четырьмя или более из следующих характеристик: (i) долей целлюлозы в твердом веществе по меньшей мере 80% (масса/масса); (ii) долей кристаллической целлюлозы в твердом веществе по меньшей мере 50% (масса/масса); (iii) долей лигнина в твердом веществе не более 15% (масса/масса); и (iv) долей гемицеллюлозного углевода в твердом веществе не более 6% (масса/масса). В некоторых примерах целлюлозная остаточная пульпа может характеризоваться долей целлюлозы в твердом веществе по меньшей мере 85% (масса/масса). В некоторых примерах целлюлозная остаточная пульпа может характеризоваться одной или более, двумя или более, тремя или более, или четырьмя или более из следующих характеристик: (i) долей целлюлозы в твердом веществе по меньшей мере 85% (масса/масса); (ii) долей кристаллической целлюлозы в твердом веществе по меньшей мере 50% (масса/масса); (iii) долей лигнина в твердом веществе не более 10% (масса/масса); и (iv) долей гемицеллюлозного углевода в твердом веществе не более 4% (масса/масса). В некоторых примерах целлюлозная остаточная пульпа может характеризоваться долей целлюлозы по меньшей мере 90% (масса/масса).
[0044] В некоторых примерах целлюлозная остаточная пульпа может характеризоваться одной или более, двумя или более, тремя или более, четырьмя или более, пятью или более, или шестью или более из следующих характеристик: (i) долей C6-сахаров в твердом веществе по меньшей мере 70% (масса/масса); (ii) долей глюкозы в твердом веществе по меньшей мере 70% (масса/масса); (iii) долей C5-сахаров в твердом веществе не более 5% (масса/масса); (iv) суммарной долей сахаров в твердом веществе по меньшей мере 75% (масса/масса); (v) следами Mg, Mn, Na, Zn не более 10 ч.н.м. (части на миллион); и (vi) следами Cu, Fe, K, Al, Cr не более 200 ч.н.м. В некоторых примерах целлюлозная остаточная пульпа может характеризоваться одной или более, двумя или более, тремя или более, четырьмя или более, пятью или более, шестью или более, семью или более, восьмью или более, девятью или более, десятью или более, одиннадцатью или более, или двенадцатью или более из следующих характеристик: (i) потерей массы при сушке от 2,0 до 5,0% или 1,5, 2,0, 2,5, 3,0, 3,5, 4,0, 4,5 или 5,0%; (ii) насыпной плотностью от 0,29 до 0,36 г/куб. см или 0,2, 0,25, 0,29, 0,3, 0,35, 0,36 или 0,4 г/куб. см; (iii) прохождением идентификационных испытаний A и B, описанных в Кодексе пищевых химикатов (FCC) (издание 5, 2004), где в испытании A получают белую непрозрачную, не содержащую пузырьков дисперсию, которая не образует надосадочную жидкость на поверхности, после того, как 100 мл дисперсии из 45 г целлюлозы в 255 мл воды смешивают в течение 5 минут в высокоскоростном порошковом смесителе (18000 об/мин), которую оставляют стоять в градуированном цилиндре на 100 мл в течение 3 часов, и где в испытании B 20 мл дисперсии смешивают с несколькими каплями содержащего йод раствора для испытаний и не образуется окрашивание от фиолетового до синего или не синее окрашивание; (iv) степенью полимеризации не более 350 единиц; (v) pH от 5,5 до 7,0 или 5,0, 5,5, 6,0, 6,5, 7,0 или 7,5; (vi) проводимостью не более 75 мкСм/см; (vii) остатком при сжигании не более 0,05% (масса/масса); (viii) содержанием водорастворимых веществ не более 12,5 мг/5 г; (viii) содержанием растворимых в эфире веществ не более 5,0 мг/10 г; (ix) содержанием тяжелых металлов не более 0,001% (масса/масса); (x) растворимостью в гидроксиде тетрааммиаката меди; (xi) размером частиц менее 250 микрон для по меньшей мере 10% (масса/масса); и (xii) размером частиц менее 150 микрон для по меньшей мере 50% (масса/масса).
[0045] В некоторых примерах целлюлозная остаточная пульпа может характеризоваться одной или более, двумя или более, тремя или более, четырьмя или более из следующих характеристик: (i) долей целлюлозы в твердом веществе по меньшей мере 90% (масса/масса); (ii) долей кристаллической целлюлозы в твердом веществе по меньшей мере 50% (масса/масса); (iii) долей лигнина в твердом веществе не более 10% (масса/масса); и (iv) долей гемицеллюлозного углевода не более 4% (масса/масса).
[0046] В некоторых примерах доля C6-сахаров в твердом веществе составляет не более 100% (масса/масса). В некоторых примерах доля C6-сахаров в твердом веществе составляет от 77 до 100% (масса/масса). В некоторых примерах доля C6-сахаров в твердом веществе составляет по меньшей мере 45, 50, 55, 60, 65, 70, 75, 80, 83, 85, 90, 95, 99 или 100% (масса/масса). В некоторых примерах содержание лигнина составляет по меньшей мере 0,001% (масса/масса). В некоторых примерах содержание лигнина составляет от 0,001 до 15% (масса/масса). В некоторых примерах содержание лигнина не превышает 15, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3, 2, 1, 0,5 или 0,05% (масса/масса). В некоторых примерах зольность составляет по меньшей мере 0,001% (масса/масса). В некоторых примерах зольность составляет от 0,001% до 6% (масса/масса). В некоторых примерах зольность не превышает 5, 4, 3, 2, 1, 0,5 или 0,05% (масса/масса). В некоторых примерах доля C5-сахаров в твердом веществе составляет по меньшей мере 0,001% (масса/масса). В некоторых примерах доля C5-сахаров в твердом веществе составляет от 0,001 до 2% (масса/масса). В некоторых примерах целлюлозная остаточная пульпа может характеризоваться долей C5-сахаров в твердом веществе не более 10, 5, 4, 3, 2, 1, 0,5 или 0,05% (масса/масса).
[0047] В некоторых примерах доля глюкозы в твердом веществе составляет по меньшей мере 45, 50, 55, 60, 65, 70, 75, 80, 83, 85, 90, 95 или 99% (масса/масса). В некоторых примерах суммарная доля сахаров в твердом веществе составляет по меньшей мере 45, 50, 55, 60, 65, 70, 75, 80, 83, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98 или 99% (масса/масса). В некоторых примерах остаточный лигнин может характеризоваться по меньшей мере 85, 90 или 95% нерастворимого в кислоте лигнина (масса нерастворимого лигнина/масса всего лигнина).
[0048] Количество неорганических примесей в образце целлюлозной остаточной пульпы может быть измерено атомно-эмиссионной спектрометрией с индуктивно связанной плазмой (ICP-AES). В некоторых примерах целлюлозная остаточная пульпа может характеризоваться количеством следовой серы не более 1000, 900, 800, 700, 600, 500, 400, 300, 200 или 100 ч.н.м. В некоторых примерах целлюлозная остаточная пульпа может характеризоваться количеством следового кальция не более 1000, 900, 800, 700, 600, 500, 400, 300, 200 или 100 ч.н.м. В некоторых примерах целлюлозная остаточная пульпа может характеризоваться количеством следового железа не более 1000, 900, 800, 700, 600, 500, 400, 300, 200 или 100 ч.н.м. В некоторых примерах целлюлозная остаточная пульпа может характеризоваться количеством следового калия не более 1000, 900, 800, 700, 600, 500, 400, 300, 200, 100 или 50 ч.н.м. В некоторых примерах целлюлозная остаточная пульпа может характеризоваться количеством следового магния не более 500, 400, 300, 200, 100, 90, 80, 70, 60, 50, 40, 30, 20 или 10 ч.н.м. В некоторых примерах целлюлозная остаточная пульпа может характеризоваться количеством следового натрия не более 500, 400, 300, 200, 100, 90, 80, 70, 60, 50, 40, 30, 20 или 10 ч.н.м. В некоторых примерах целлюлозная остаточная пульпа может характеризоваться количеством следового не более 500, 400, 300, 200, 100, 90, 80, 70, 60, 50, 40, 30, 20 или 10 ч.н.м. В некоторых примерах целлюлозная остаточная пульпа может характеризоваться не более 10 ч.н.м. Mg, Mn, Na и Zn и количеством следовых Cu, Fe, K, Al и Cr не более 200 ч.н.м.
[0049] В некоторых примерах целлюлозная остаточная пульпа может характеризоваться количеством целлюлозы по меньшей мере 80, 85, 90, 92, 94, 96, 98 или 99%. Потеря массы при сушке может представлять собой процент материала, выраженный как масса/масса, теряемый, когда целлюлозную остаточную пульпу сушат, переводя из твердого вещества в сухое твердое вещество. Для сушки целлюлозную остаточную пульпу можно нагревать в течение некоторого периода времени. Для сушки целлюлозную остаточную пульпу можно нагревать до температуры не более 200, 190, 180, 170, 160, 150, 140, 130, 120, 110, 100, 90, 80, 70, 60, 50, 40 или 30°C в течение некоторого периода времени. Период времени, в течение которого целлюлозную остаточную пульпу нагревают для сушки, может составлять не более 100, 90, 80, 70, 60, 50, 48, 40, 30, 24, 20, 16, 12, 10, 9, 8, 7, 6, 5, 4, 3, 2, 1 или 0,5 часов.
[0050] В некоторых примерах целлюлозная остаточная пульпа может характеризоваться высокой долей целлюлозы в твердом веществе, низкой долей лигнина в твердом веществе и низкой долей гемицеллюлозного углевода в твердом веществе. В некоторых аспектах целлюлозные композиции характеризуются высокой долей кристаллической целлюлозы в твердом веществе. В некоторых аспектах целлюлозные композиции характеризуются высокой долей целлюлозы в твердом веществе, низкой долей лигнина в твердом веществе, высокой долей кристаллической целлюлозы в твердом веществе и низкой долей гемицеллюлозного углевода в твердом веществе. В некоторых примерах целлюлозная остаточная пульпа может характеризоваться долей целлюлозы в твердом веществе по меньшей мере 90, 92, 94, 96, 98 или 99% (масса/масса). В некоторых примерах целлюлозная остаточная пульпа может характеризоваться долей кристаллической целлюлозы в твердом веществе по меньшей мере 50, 60, 70, 80, 90% (масса/масса). В некоторых примерах целлюлозная остаточная пульпа может характеризоваться долей лигнина в твердом веществе не более 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1% (масса/масса). В некоторых примерах целлюлозная остаточная пульпа может характеризоваться долей гемицеллюлозного углевода в твердом веществе не более 4, 3, 2 или 1% (масса/масса).
[0051] Обзор иллюстративных последовательных гидролиза, изомеризации и дегидратации целлюлозной пульпы в гидроксиметилфурфурол согласно раскрытым здесь вариантам осуществления представлен на Фиг. 1, Фиг. 2 и Фиг. 3. Как показано на Фиг. 1, (1) целлюлозную пульпу 1000 извлекают из биомассы и очищают на стадии биопереработки; (2) целлюлозную пульпу 1000 растворяют в ионной жидкости и осахаривают ацидолизом 1050; (3) полученный раствор в ионной жидкости, содержащий моносахариды, олигосахариды и полимерные сахариды, подвергают конверсии 1100, тем самым получая гидроксиметилфурфурол 1100-P1 и, необязательно, глюкозу 1100-P2. Как показано на Фиг. 2, (4) гидроксиметилфурфурол дополнительно превращают а продукты конверсии, что включает: (4)(i) окисление 1300 гидроксиметилфурфурола в 2,5-фурандикарбоновую кислоту (ФДКК) 1300-P1; (4)(ii) гидрирование 1600 гидроксиметилфурфурола с использованием 2-бутанола в качестве донора водорода с образованием 2,5-диметилфурана (ДМФ) 1600-P1 и метилэтилкетона (МЭК) 1600-P2; (5) циклоприсоединение 1700 2,5-диметилфурана к этилену с образованием п-ксилола 1700-P1; или (4)(iii) конверсию 2,5-диметилфурана реакцией 1500 раскрытия кольца в 1,6-гександиол 1500-P1. Стадии (1), (2), (3) и (4)(i) могут быть осуществлены последовательно без выделения промежуточных продуктов. Стадии (1), (2), (3) и (4)(ii) могут быть осуществлены последовательно без выделения промежуточных продуктов. Стадии (1), (2), (3), (4)(ii) и (5) могут быть осуществлены последовательно без выделения промежуточных продуктов. Стадии (1), (2), (3) и (4)(iii) могут быть осуществлены последовательно без выделения промежуточных продуктов.
[0052] На Фиг. 3 представлено схематичное описание ступенчатых способов получения гидроксиметилфурфурола из целлюлозной пульпы. Целлюлозная пульпа 1000 может быть сначала подвергнута кондиционированию в установке 100 кондиционирования в ионной жидкости, чтобы предоставить растворенную целлюлозу. Хлористоводородная кислота и вода могут быть добавлены для содействия гидролизу с тем, чтобы предоставить раствор моносахаридов, дисахаридов и гидроксиметилфурфурола в ионной жидкости. Основание и вода могут быть добавлены для нейтрализации раствора 251, и гумины и остаточный лигнин могут быть отделены. Основание может представлять собой гидроксидную форму ионной жидкости 252. Гидроксидная форма ионной жидкости 252 может быть получена в анионообменнике 250 ионной жидкости, что, таким образом, уменьшает количество соли, образующейся в способе. Например, ионы натрия могут присутствовать в количестве не более 0,5, 1, 1,5, 2, 2,5, 3, 3,5, 4, 4,5, 5 или 5,5%. Поток 101 раствора с уменьшенной кислотностью, содержащего сахариды, гидроксиметилфурфурол, органические кислоты, воду и ионную жидкость, может быть подан в процесс 300 конверсии. Поток 101 может быть разделен хроматографией, давая: (i) водный поток 301, содержащий гидроксиметилфурфурол и органические кислоты; (ii) поток 302 ионной жидкости/воды, содержащий моносахариды; и (iii) поток 303 ионной жидкости/воды, содержащий дисахариды. Как дополнительно подробно описано ниже и показано на Фиг. 5 и Фиг. 6, поток 302, содержащий моносахариды, может быть рециркулирован через ступени изомеризации 330 и дегидратации 350.
[0053] Поток 301 может быть передан в процесс 400 извлечения гидроксиметилфурфурола, где вода может быть удалена, а гидроксиметилфурфурол может быть отделен от органических кислот и воды и выделен в виде раствора в растворителе, подходящем для дальнейших, расположенных ниже по технологической схеме превращений. Поток 303 может быть передан на извлечение 500 ионной жидкости, где вода может быть удалена испарением, азеотропным испарением или адсорбцией, альтернативно или в сочетании. Целлобиоза может быть фракционирована с ионной жидкостью и может быть возвращена для дальнейшего гидролиза и последующей конверсии. Как дополнительно подробно описано ниже и показано на Фиг. 6, поток 302, содержащий моносахариды, может быть разделен на стадии второго хроматографического разделения 315, давая: (i) водный поток 316, содержащий глюкозу, и (ii) поток 317 ионной жидкости/воды, содержащий глюкозу. Поток 317 может быть рециркулирован через ступени изомеризации 330 и дегидратации 350. Поток 316 может быть передан для извлечения и очистки глюкозы, где глюкоза может быть извлечена и очищена по меньшей мере одним из способов, включая испарение, контакт с сильнокислой катионной (СКК) смолой, анионообменником, смолой со смешанными слоями (СС) или активированным углем (АУ). Каждый из них описан здесь подробнее.
[0054] Когда здесь упоминается диапазон числовых значений, то, если не указано иное, подразумевается, что диапазон включает в себя свои конечные точки и все целые числа и дробные части в данном диапазоне. Не подразумевается, что объем изобретения ограничен конкретными значениями, приведенными при задании диапазона. Все значения, указанные здесь, могут представлять собой ʺпримерноʺ указанное значение, или точно указанное значение, где термин ʺпримерноʺ относится к отклонению в приведенном числовом значении, которое может иметь место. Термин ʺпримерноʺ означает в пределах 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1% приведенного числового значения.
[0055] Использованные здесь термины ʺсахараʺ и ʺсахаридыʺ использованы взаимозаменяемо.
[0056] Подразумевается, что использованные здесь термины ʺсодержитʺ, ʺсодержащийʺ, ʺвключает в себяʺ, ʺвключающий в себяʺ, ʺимеетʺ, ʺимеющийʺ, ʺсодержит в себеʺ или ʺсодержащий в себеʺ, или любой их вариант охватывают неисключительное включение. Подразумевается, что использованный здесь термин ʺсостоящий изʺ охватывает исключительное включение. Подразумевается, что использованный здесь термин ʺсостоящий по существу изʺ охватывает исключение, ограниченное материалами, стадиями или компонентами, которые не оказывают существенного влияния на базовые новые характеристики заявленного предмета изобретения. Использованный здесь термин ʺсодержащийʺ охватывает термины ʺсодержащийʺ, ʺсостоящий по существу изʺ и ʺсостоящий изʺ. Например, композиция, смесь, процесс, способ, изделие или аппарат, который(ая) содержит перечень элементов, не обязательно ограничен(а) лишь данными элементами, но может включать в себя другие элементы, не перечисленные явным образом, или присущие такой(ому) композиции, смеси, процессу, способу, изделию или аппарату. Далее, если явно не указано на иное, ʺилиʺ относится к включающему или, а не к исключающему или.
I. Растворение и гидролиз целлюлозной пульпы
a) Растворение целлюлозной пульпы
[0057] Схематичная иллюстрация иллюстративных способов растворения целлюлозной пульпы и ее гидролиза до глюкозы представлена на Фиг. 4. Целлюлозная пульпа 1000 может быть кондиционирована 110 в подходящей жидкости для ее растворения и открытия кристаллической структуры целлюлозы, обеспечивая ее доступность для гидролиза. Кондиционирование может быть проведено путем перемешивания пульпы и жидкости в течение контролируемого времени и при контролируемой температуре. Подходящая жидкость может быть выбрана из ионных жидкостей или растворителей с глубокой эвтектикой. Подходящая жидкость может содержать рециркулированную ионную жидкость, содержащую целлобиозу. Поток рециркулированной ионной жидкости может быть обработан для удаления избыточной воды и примесей, как здесь описано более подробно. Такая рециркуляция может обеспечивать дальнейший гидролиз непрореагировавшей целлобиозы из предшествующих реакционных циклов, приводя, таким образом, к максимизации общего выхода гидроксиметилфурфурола из целлюлозы. Необязательно, поток 111 может быть перенесен в другой реакционный сосуд для проведения гидролиза 120. Альтернативно или в сочетании гидролиз 120 может быть проведен в том же сосуде, что и стадия 100 гидролиза (смотри Фиг. 3). Гидролиз 120 может быть инициирован прибавлением кислоты и воды к потоку 111. По завершении гидролиза pH можно повысить, например, за счет ионной жидкости в гидроксидной форме, и вода может быть прибавлена к потоку 121, чтобы вызвать осаждение сорастворенных остатков лигнина, в то время как целлюлоза может оставаться растворенной, лигнин может быть отфильтрован на стадии 130, а поток 131 после фильтрации лигнина может быть извлечен и очищен на стадии 140, чтобы отделить лигнин 1200 высокой чистоты. Повышение pH может быть реализовано прибавлением основной формы ионной жидкости, использованной в качестве растворителя. Дополнительное фильтрование для удаления гуминов может быть проведено перед изменением pH.
[0058] Целлюлозная пульпа может быть растворена в ионной жидкости или в растворителе с глубокой эвтектикой путем смешения пульпы в растворе расплавленной соли при температуре выше точки плавления ионной жидкости или растворителя с глубокой эвтектикой. По меньшей мере 5, 10, 15, 20 или 25 масса/масса целлюлозной пульпы может быть добавлено к расплавленной ионной жидкости или растворителю с глубокой эвтектикой, и смешение проводят при температуре от 100 до 150°C в течение по меньшей мере 30, 45, 60, 90, 120 180, 240, 300 или 360 минут.
[0059] Целлюлозная пульпа может быть предварительно обработана перед растворением в ионной жидкости для удаления остаточных количеств лигнина или золы. Остаточный лигнин может содержать по меньшей мере 85, 90, 95 или 99% нерастворимого в кислоте лигнина, масса/суммарная масса лигнина. Можно использовать любой процесс, подходящий для дополнительного удаления таких примесей, включая, но не ограничиваясь, промывку водой или основным раствором или кислым раствором, отбеливание окислителем или промывку раствором, содержащим растворитель.
[0060] Ионные жидкости представляют собой соли, которые при комнатных температурах являются жидкостями, а не кристаллическими веществами. Многочисленные ионные жидкости могут быть использованы в способах предварительной обработки настоящего изобретения. Ионная жидкость может подходить для предварительной обработки биомассы и для гидролиза целлюлозы термостабильной целлюлазой. Неограничивающие примеры подходящих ионных жидкостей приведены в ChemFiles (2006) 6(9) (Они коммерчески доступны от Sigma-Aldrich; Милуоки, Висконсин). Подходящие ионные жидкости включают в себя следующие, но не ограничены ими: алканат 1-алкил-3-алкилимидазолия, алкилсульфат 1-алкил-3-алкилимидазолия, метилсульфонат 1-алкил-3-алкилимидазолия, гидросульфат 1-алкил-3-алкилимидазолия, тиоцианат 1-алкил-3-алкилимидазолия и галогенид 1-алкил-3-алкилимидазолия, где ʺалкилʺ представляет собой алкильную группу, содержащую 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 атомов углерода, а ʺалканатʺ представляет собой алканат, содержащий 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 атомов углерода. ʺАлкилʺ может представлять собой алкильную группу, содержащую 1, 2, 3 или 4 атома углерода. ʺАлкилʺ может представлять собой метильную группу, этильную группу или бутильную группу. ʺАлканатʺ может представлять собой алканат, содержащий 1, 2, 3 или 4 атома углерода. ʺАлканатʺ может представлять собой ацетат. Галогенид может представлять собой хлорид.
[0061] Ионная жидкость может содержать ацетат 1-этил-3-метилимидазолия (ацетат EMIM), хлорид 1-этил-3-метилимидазолия (EMIM Cl), гидросульфат 1-этил-3-метилимидазолия (EMIM HOSO3), метилсульфат 1-этил-3-метилимидазолия (EMIM MeOSO3), этилсульфат 1-этил-3-метилимидазолия (EMIM EtOSO3), метансульфонат 1-этил-3-метилимидазолия (EMIM MeSO3), тетрахлоралюминат 1-этил-3-метилимидазолия (EMIM AlCl4), тиоцианат 1-этил-3-метилимидазолия (EMIM SCN), хлорид 1-бутил-3-метилимидазолия (BMIM Cl), гидросульфат 1-бутил-3-метилимидазолия (BMIM HOSO3), ацетат 1-бутил-3-метилимидазолия (BMIM MeSO3), метилсульфат 1-бутил-3-метилимидазолия (BMIM MeOSO3), тетрахлоралюминат 1-бутил-3-метилимидазолия (BMIM AlCl4), тиоцианат 1-бутил-3-метилимидазолия (BMIM SCN), этилсульфат 1-этил-2,3-диметилимидазолия (EDIM EtOSO3), метилсульфат трис(2-гидроксиэтил)метиламмония (MTEOA MeOSO3), хлорид 1-метилимидазолия (MIM Cl), гидросульфат 1-метилимидазолия (MIM HOSO3), метилсульфат 1,2,4-триметилпиразолия, метилсульфат трибутилметиламмония, ацетат холина, салицилат холина и тому подобное.
[0062] Ионная жидкость может содержать хлоридную ионную жидкость. Ионная жидкость может представлять собой соль имидазолия. Ионная жидкость может представлять собой хлорид 1-алкил-3-имидазолия, такой как хлорид 1-этил-3-метилимидазолия или хлорид 1-бутил-3-метилимидазолия.
[0063] Ионная жидкость может содержать соли пиридиния, соли пиридазиния, соли пиримидиния, соли пиразиния, соли имидазолия, соли пиразолия, соли оксазолия, соли 1,2,3-триазолия, соли 1,2,4-триазолия, соли тиазолия, соли изохинолия, соли хинолиния, соли изохинолиния, соли пиперидиния и соли пирролидиния. Иллюстративные анионы ионной жидкости включают в себя следующие, но без ограничения ими: галогены (например, хлорид, фторид, бромид и иодид), псевдогалогены (например, азид и изоцианат), алкилкарбоксилат, сульфонат, ацетат и алкилфосфат.
[0064] Ионная жидкость может быть выбрана так, что она представляет собой слабую кислоту Льюиса, когда находится в хлоридной форме, и слабое основание Льюиса в своей гидроксидной форме.
[0065] Ионная жидкость может содержать одно соединение или смесь соединений.
[0066] Приведение в контакт материала целлюлозной пульпы с ионной жидкостью может быть осуществлено при температуре от 100 до 160°C. Например, при температуре 100, 110, 120, 130, 140, 150 или 160°C. Стадию приведения в контакт с ионной жидкостью можно осуществлять в течение периода времени от 0,5 часа до 16 часов или в течение периода от 1 часа до 12 часов или в течение периода от 1 часа до 6 часов.
[0067] Целлюлозную пульпу можно растворять в растворителе с глубокой эвтектикой, содержащем систему хлорида холина-лимонной кислоты-моногидрата лимонной кислоты. Система хлорида холина-лимонной кислоты-моногидрата лимонной кислоты, которая может быть использована для растворения, может быть получена смешением хлорида холина, лимонной кислоты и моногидрата лимонной кислоты в соотношении 4:1:1 (по массе) при от 85 до 95°C.
b) Кислый гидролиз
[0068] Гидролиз может быть проведен путем прибавления кислоты в качестве катализатора гидролиза растворенной целлюлозы. Температура раствора ионной жидкости, содержащего растворенную целлюлозу, может быть отрегулирована перед прибавлением кислого катализатора. Данная регулировка может включать в себя охлаждение раствора до 100, 105, 110 или 115°C.
[0069] Кислый катализатор может содержать водный кислый раствор. Водные кислые растворы включают в себя следующие, но не ограничены ими: растворы хлористоводородной кислоты, растворы серной кислоты и их смеси. Водный кислый раствор может представлять собой раствор хлористоводородной кислоты. Водный кислый раствор может иметь концентрацию от 2,0 M до 12 M. Водный кислый раствор может иметь концентрацию кислоты не более 12, 11, 10, 9, 8, 7, 6, 5, 4, 3 или 2 M. Водный кислый раствор может иметь концентрацию кислоты не более 2 M. Водный кислый раствор, имеющий концентрацию от 2,0 M до 12 M, можно прибавлять к раствору материала целлюлозной пульпы в ионной жидкости. Водный кислый раствор, имеющий концентрацию от 2,0 M до 12 M, можно формировать прибавлением независимо водного кислого раствора, имеющего концентрацию по меньшей мере от 2,0 M до 12 M, и воды к раствору материала целлюлозной пульпы в ионной жидкости для получения водного раствора, имеющего концентрацию от 2,0 M до 12 M. Водный кислый раствор, имеющий концентрацию по меньшей мере от 2,0 M до 12 M, и воду можно прибавлять аликвотой к раствору материала целлюлозной пульпы в ионной жидкости. Водный кислый раствор, имеющий концентрацию по меньшей мере от 2,0 M до 12 M, и воду можно непрерывно прибавлять к раствору целлюлозной пульпы в ионной жидкости посредством насоса или другого средства непрерывного прибавления.
[0070] Прибавление водного кислого раствора к раствору, содержащему материал целлюлозной пульпы в ионной жидкости, может быть осуществлено при температуре от 60 до 110°C. Стадию прибавления можно осуществлять в течение периода времени от 0,5 до 6 часов.
[0071] Концентрацию кислоты в растворе ионной жидкости можно поддерживать постепенным прибавлением подходящих количеств кислоты и воды в ходе реакции. Водный кислый раствор, имеющий концентрацию от 2,0 M до 12 M, можно прибавлять к раствору материала целлюлозной пульпы в ионной жидкости. Водный кислый раствор можно прибавлять одной порцией или ступенчато. Водный кислый раствор можно непрерывно добавлять к раствору целлюлозной пульпы в ионной жидкости посредством насоса или другого средства непрерывного прибавления.
[0072] Прибавление водного кислого раствора к раствору материала целлюлозной пульпы в ионной жидкости можно осуществлять при температуре от 80 до 140°C.
[0073] Раствор ионной жидкости по окончании гидролиза может содержать глюкозу с выходом по массе по меньшей мере 50% от исходной целлюлозы, целлобиозу с выходом по массе по меньшей мере 5% от исходной целлюлозы и гидроксиметилфурфурол с выходом по массе по меньшей мере 1% от исходной целлюлозы. Такие растворы описаны в патенте США 8722878 или WO 2013/166237. Следует отметить, что 100% молярный выход гидролиза целлюлозы до глюкозы эквивалентен 110% выходу по массе. Раствор ионной жидкости может содержать с выходом по массе по меньшей мере 50, 60, 70, 80, 90 или 95% от исходной целлюлозы. По завершению реакции гидролиза растворенные твердые вещества в фазе ионной жидкости могут содержать по меньшей мере 94% глюкозы, по меньшей мере от 5 до 10% целлобиозы, по меньшей мере от 7 до 12% гидроксиметилфурфурола, не более 1,5% левулиновой кислоты и не более 1,5% муравьиной кислоты (все % приведены на сухие вещества для соотношения масса/масса). Массовый баланс продуктов целлюлозы, целлобиозы, гидроксиметилфурфурола, левулиновой кислоты и муравьиной кислоты количественно определяют путем отбора образцов реакционной смеси, разбавлением водой в десять раз, фильтрованием и впрыскиванием в колонку ВЭЖХ Aminex HPX-87H. Когда теоретический выход по массе составляет 110%, измеренный выход по массе может составлять по меньшей мере 105, 107, 109 или 110% выхода по массе. Высокий массовый баланс учитываемых определяемых веществ может указывать на то, что отсутствуют значительные потери целлюлозы в результате превращения в побочные продукты, отличные от количеств, обнаруженных для левулиновой и муравьиной кислоты. Раствор может содержать малое количество гуминов. Раствор может быть профильтрован через фильтр любого подходящего типа для улавливания и удаления гуминов, которые присутствуют в виде твердых частиц.
[0074] Целлюлозная пульпа может содержать остаток лигнина, таким образом, данный лигнин может присутствовать в растворе ионной жидкости либо растворенным, либо полурастворенным. Может быть желательно удалять такой лигнин из раствора. Раствор ионной жидкости может быть разбавлен водой в соотношении от 1:1 до 4:1, и pH можно регулировать от 3,3 до 4 или до 3,5 прибавлением гидроксидной формы ионной жидкости. Например, если использованная в качестве растворителя ионная жидкость представляет собой хлорид 1-этил-3-метилимидазолия, тогда прибавляют гидроксид 1-этил-3-метилимидазолия; если использованная в качестве растворителя ионная жидкость представляет собой хлорид 1-бутил-3-метилимидазолия, тогда прибавляют гидроксид 1-бутил-3-метилимидазолия и так далее. После регулировки pH и разбавления водой лигнин может быть осажден и может быть отфильтрован посредством любой подходящей фильтрационной установки. Фильтрат может быть промыт раствором 80:20 метилэтилкетона и воды, что вызывает растворение осадка в фазе метилэтилкетона. Раствор может быть приведен в контакт с сильнокислым катионообменником для улавливания всего остаточного катиона ионной жидкости на смоле. Затем растворенный лигнин может быть извлечен как раскрыто в PCT/US2013/039585 и PCT/US2013/068824.
[0075] Ионная жидкость может быть превращена в свою основную форму путем приведения в контакт водного раствора ионной жидкости с сильноосновной смолой в гидроксидной форме. Подходящие коммерческие сильноосновные анионные (SBA) смолы могут быть приобретены у Finex (AS 510 GC тип I, сильноосновный анионит, гелевая форма). Похожие сорта могут быть приобретены у других производителей, включая Lanxess AG, Purolite, Dow Chemicals Ltd. (или Rohm&Haas, компания Dow Chemicals). Альтернативно или в сочетании можно использовать макропористые смолы SBA. Смола может быть регенерирована в гидроксидную форму посредством периодического приведения в контакт с раствором гидроксида натрия. Данное превращение ионной жидкости в ее основную форму может обеспечивать все необходимое основание для контроля pH на разных стадиях процесса, ограничивая, таким образом, необходимость во введении гидроксида натрия или других оснований, которые образовывали бы соль в цикле ионной жидкости. Это может обеспечивать преимущество, поскольку соль, сформированная в цикле ионной жидкости, будет накапливаться, и ее удаление из цикла могло бы представлять собой весьма сложную задачу.
II. Конверсия гидролизата в гидроксиметилфурфурол
[0076] Способы превращения гидролизата целлюлозы в гидроксиметилфурфурол, описанные здесь, могут давать гидроксиметилфурфурол с высоким выходом. Гидролизат может содержать ионную жидкость в хлоридной форме, ионную жидкость в гидроксидной форме, глюкозу, целлобиозу, гидроксиметилфурфурол, органические кислоты и воду. Способы конверсии могут включать в себя по меньшей мере три технологические стадии, проводимые согласованно для достижения целевых высоких выходов гидроксиметилфурфурола. Теоретически максимальный выход по массе гидроксиметилфурфурола составляет 77,7% масса/масса целлюлозы, что эквивалентно 100% молярному выходу (выходу по углероду). Раскрытые здесь способы конверсии могут обеспечивать общий выход гидроксиметилфурфурола из целлюлозы, который составляет по меньшей мере 55, 60, 62, 64, 66 или 68% масса/масса. Пример способов конверсии в целом схематично проиллюстрирован на Фиг. 5. Способы конверсии гидролизата в гидроксиметилфурфурол могут включать в себя по меньшей мере следующие стадии: (1) хроматографическое разделение 310; (2) изомеризацию 330; и (3) дегидратацию 350. Способы конверсии могут включать в себя дополнительные стадии, включая следующие, но без ограничения ими: фильтрование, регулировку pH, контроль температуры, нагрев или охлаждение, испарение или разбавление.
a) Хроматографическое разделение
[0077] Как показано на Фиг. 6, поток 251 с уменьшенной кислотностью (смотри Фиг. 3), содержащий целлобиозу, глюкозу, гидроксиметилфурфурол и органические кислоты, а также воду и ионную жидкость, может быть подан на хроматографическое разделение 310. Концентрация глюкозы может составлять по меньшей мере 6, 7, 8, 9 или 10%, концентрация целлобиозы может составлять не более 1%, концентрация гидроксиметилфурфурола может составлять не более 3%, концентрация левулиновой кислоты и муравьиной кислоты, каждой, может составлять не более 1,5, 1, 0,1, 0,05% и концентрация воды может составлять от 20 до 30% (все выражены как масса/масса). Концентрация глюкозы может составлять от 2 до 5%, концентрация целлобиозы может составлять не более 1%, концентрация гидроксиметилфурфурола может составлять не более 2%, концентрация левулиновой кислоты может составлять не более 0,1%, концентрация муравьиной кислоты может составлять не более 0,1%, концентрация воды может составлять не более 70% (все выражены как масса/масса).
[0078] На хроматографической стадии подаваемая смесь, поток 251, может быть разделена на три потока: поток 301, содержащий гидроксиметилфурфурол, органические кислоты и воду; поток 302, содержащий глюкозу, другие сахариды и ионную жидкость; и поток 303, содержащий целлобиозу и ионную жидкость. Данное разделение может быть достигнуто выбором подходящей смолы, имеющей различное сродство к разным соединениям в подаваемой смеси, и применением подходящей последовательности стадий в аппарате с симулированным движением стационарной фазы. Описание хроматографии с симулированным движением стационарной фазы (SMB), включающей в себя использование хлорида 1-этил-3-метилимидазолия, хлорида 1-бутил-3-метилимидазолия и ацетата 1-этил-3-метилимидазолия, приведено в работе Caes (Глава 6 в работе Catalytic Systems for Carbohydrate Conversion, B.R. Caes, руководитель диссертации R.T. Raines, диссертация доктора философии, Университет Висконсин-Мэдисон) и в статье N.L. Mai et. al., Journal of Chromatography A, 1227 (2012) 67-72). Неограничивающие примеры отделения гидроксиметилфурфурола от ионной жидкости посредством симулированного движения стационарной фазы описаны здесь.
[0079] Двумя способами крупномасштабных хроматографических разделений являются последовательная хроматография с симулированным движением стационарной фазы (SSMB) и хроматография с симулированным движением стационарной фазы. В обоих способах можно использовать ряд колонок, наполненных подходящим сорбентом и соединенных последовательно. Могут иметься впускные отверстия для подаваемого материала и растворителя (который может включать в себя рециркулированный растворитель), и выпускные отверстия для двух или более продуктов (или других отделенных фракций). Введение раствора смеси, подлежащего разделению, можно периодически переключать между колонками по направлению движения потока жидкости, тем самым симулируя непрерывное движение сорбента относительно отверстий и жидкости. Симулированное движение стационарной фазы может проводиться в режиме непрерывного противопотока. Последовательную хроматографию с симулированным движением стационарной фазы можно рассматривать как усовершенствованный способ, который относится к типу последовательного режима. Его преимущества относительно хроматографии с симулированным движением стационарной фазы и относительно других, прежних способов, могут включать в себя меньшее число колонок, необходимых в последовательном способе с симулированным движением стационарной фазы, по сравнению со способом с симулированным движением стационарной фазы. Это может требовать меньше смолы, что может уменьшать связанную с этим стоимость установки крупной системы. Кроме того, профиль давления последовательной хроматографии с симулированным движением стационарной фазы можно лучше контролировать, чем профиль давления в других технологиях разделения, что может содействовать использованию более чувствительных смол. Кроме того, достигаемые выходы извлечения и/или чистота могут быть выше при использовании последовательной системы с симулированным движением стационарной фазы, чем получаемые в системах симулированным движением стационарной фазы.
[0080] Фракционирование гидроксиметилфурфурола и сахаров из смеси может быть достигнуто, используя сильнокислый катионообменник. Подходящие коммерческие сильнокислые катионные смолы могут быть приобретены у Purolite (Purolite PCR 642 H, Purolite PCR 450 Na, Purolite SSTPCR 541 Ca, Purolite PCR 145 Na) или у Dow Chemicals Ltd. (Dowex® 50WX4, протонная форма, или Dowex 99Ca/320, Ca2+-форма), похожие сорта могут быть приобретены у других производителей, включая Lanxess AG, или Finex. Гранулы сильнокислой смолы могут иметь размер 300±75 микрон. Сильнокислая катионная смола может представлять собой сортовую смолу для хроматографии. Форма смолы может быть изменена так, чтобы она содержала катион ионной жидкости, например, катион 1-этил-3-метилимидазолия или катион 1-бутил-3-метилимидазолия, сначала путем кондиционирования смолы по меньшей мере 6, 7, 8, 9 или 10 объемами соответствующей ионной жидкости в воде относительно объема неподвижного слоя. Значение pH подаваемого потока 251 может быть отрегулировано для получения pH от 3 до 6 прибавлением ионной жидкости в гидроксидной форме.
b) Изомеризация
[0081] Фруктоза может быть превращена в гидроксиметилфурфурол с более высокой селективностью и конверсией при данной температуре, чем глюкоза. Следовательно, для достижения высокого общего выхода гидроксиметилфурфурола из целлобиозы предпочтительным может быть ускорение изомеризации глюкозы во фруктозу. Изомеризация глюкозы во фруктозу может катализироваться растворенными или гомогенными основаниями (что касается реакции изомеризации, смотри публикации, включенные сюда путем ссылки: A.J. Seusabaugh Jr., P.L. Carey, CIM., 1967, 24; патент США 3684574). Неожиданно было обнаружено, что изомеризация глюкозы во фруктозу может катализироваться путем увеличения pH раствора воды/ионной жидкости прибавлением контролируемых количеств ионной жидкости в гидроксидной форме. Как показано на Фиг. 5, поток 302, выходящий из хроматографического разделения 310 и содержащий глюкозу, воду и ионную жидкость и имеющий pH не более 7, может быть смешан в смесителе 320 с потоком, содержащим ионную жидкость в гидроксидной форме и водой, чтобы повысить pH раствора до по меньшей мере 8, 9, 10, 11, 12 или 13. Перед регулировкой pH поток 302 может быть сконцентрирован испарением воды до заданной концентрации. Получаемый в результате поток 321 может быть перенесен в реактор 330 изомеризации, где его можно перемешивать в течение от 0,5 до 10 часов или от 5 до 7 часов или в течение 0,5, 1,0, 1,5, 2,0, 2,5, 3,0, 3,5, 4,0, 4,5, 5,0, 5,5, 6,0, 6,5, 7,0, 7,5, 8,0, 8,5, 9,0, 9,5 или 10,0 часов при температуре от 45 до 80°C или от 50 до 60°C или 40, 45, 50, 55, 60, 65, 70, 75, 80°C. Поток 321 может содержать от 1 до 10% или 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10% (масса/масса) глюкозы; от 17 до 25% или 17, 18, 19, 20, 21, 22, 23, 24 или 25% (масса/масса) ионной жидкости в хлоридной форме; и от 0,1 до 15% или 0,1, 0,5, 1, 3, 5, 7, 10 или 15% (масса/масса) ионной жидкости в гидроксидной форме. Конверсия глюкозы во фруктозу в таких условиях может составлять более 20 до 30% или 20, 25, 27, 29 или 30% (масса/масса) при селективности более 70 до 85% или 70, 75, 80 или 85%. Главным побочным продуктом изомеризации является манноза, образующаяся с селективностью от 8 до 13% или 8, 9, 10, 11, 12 или 13% относительно глюкозы.
[0082] Любой источник глюкозы может быть использован в качестве альтернативного источника для изомеризации в тех же условиях. Источник глюкозы может представлять собой коммерческий декстрозный сироп, получающийся из биомассы, такой как кукуруза, маис, картофель, пшеница, ячмень, рис и маниок, а также альтернативных лигноцеллюлозных источников. Альтернативные лигноцеллюлозные источники могут быть гидролизованы другими способами гидролиза и очищены до похожего уровня чистоты, что и поток глюкозы, который получается в результате осуществления раскрытого здесь способа гидролиза, то до достижения достаточного удаления гемицеллюлозных сахаридов, лигнина, зольности, органических кислот, экстрагируемых и других соединений в биомассе, отличных от глюкозы.
c) Дегидратация
[0083] Дегидратация фруктозы в гидроксиметилфурфурол может быть проведена в растворе воды/ионной жидкости в присутствии сильнокислой катионной смолы. Смесь, содержащая как фруктозу, так и глюкозу, может быть подвергнута химической реакции, в которой по меньшей мере часть фруктозы превращается в гидроксиметилфурфурол, а по меньшей мере часть глюкозы - не превращается. По меньшей мере от 50 до 99% или 50, 55, 60, 65, 70, 75, 80, 85, 89, 90, 95, 97 или 99% фруктозы может быть превращено в гидроксиметилфурфурол и по меньшей мере от 60 до 99% или 60, 65, 70, 75, 80, 85, 90, 95, 97 или 99% глюкозы - не превращено. Можно использовать макропористую сильнокислую катионную смолу.
[0084] Макропористые сильнокислые катионные смолы коммерчески доступны от нескольких поставщиков, например, макропористая смола Purolite PCR145K SAC (сильнокислый катионит)- тип C145, специальный сорт, Purolite NRW1600, Amberlite 200, Amberlite 252 и Amberlite FPC23 от Rohm and Haas, а также от других поставщиков. По меньшей мере некоторая часть сильнокислой катионной смолы может находиться в форме, имеющей катион ионной жидкости. Смолу можно периодически регенерировать до получения по меньшей мере части смолы в форме, имеющей катион ионной жидкости, что обеспечивает непрерывную работу. Фруктоза может быть дегидратирована в гидроксиметилфурфурол, тогда как глюкоза не реагирует с образованием нежелательных побочных продуктов.
[0085] Перед дегидратацией pH раствора можно отрегулировать посредством pH-регулировки 340 до кислого значения путем приведения раствора в контакт со слабокислой катионной (WAC) смолой в протонной форме. Данное приведение в контакт может также приводить по меньшей мере к частичному превращению смолы в форму, имеющую катион ионной жидкости, поскольку катион ионной жидкости обменивается с протонами, высвобожденными смолой. Значение pH потока 341 может быть дополнительно понижено прямым прибавлением кислоты. Кислота может быть выбрана так, чтобы соответствовать анионной части ионной жидкости, например, когда использованной ионной жидкостью является хлорид 1-этил-3-метилимидазолия или хлорид 1-бутил-3-метилимидазолия, кислота может представлять собой хлористоводородную кислоту. Регулировка pH путем pH-регулировки 340 обеспечивает возможность рециркуляции ионной жидкости и уменьшения по меньшей мере на 30 вплоть до 60, или на 30, 40, 50 или 60% суммарного потребления кислоты в способе, поскольку смола, использованная при pH-регулировке 340, может быть обратно переведена в протонную форму в последующем технологическом потоке, что дополнительно описано ниже.
[0086] Количество воды в потоке 341 можно контролировать испарением воды или прибавлением воды. Отрегулированный поток 341 может быть перенесен на дегидратацию 350 для осуществления дегидратации. Поток 341 может содержать от 4 до 10% глюкозы, от 1 до 4% фруктозы, от 15 до 45% воды (все в выражении масса/масса). На стадии дегидратации 350 в начале реакции дегидратации может содержаться от 5 до 15% (масса/масса) макропористой сильнокислой катионной смолы. Раствор можно перемешивать при температуре от 50 до 100°C, от 70 до 90°C, от 75 до 85°C или 50, 55, 60, 65, 70, 75, 80, 85, 90, 95 или 100°C в течение от 30 до 180, от 70 до 120 или от 80 до 100 минут для достижения конверсии фруктозы по меньшей мере от 85 до 98% или 85, 90, 95, 96, 97 или 98%, селективности по гидроксиметилфурфуролу по меньшей мере от 75 до 99% или 75, 80, 85, 90, 95, 96, 97, 98 или 99%. Дополнительные количества кислоты могут быть прибавлены в реактор дегидратации. Конверсия глюкозы в тех же условиях может составлять не более 5, 4, 3, 2 или 1%, и на совокупный сахар, составляющий массовый баланс, может приходиться по меньшей мере 90, 92, 94, 96, 98 или 99%. Микропористая сильнокислая катионная смола может быть отделена от раствора в конце реакции. Сильнокислая катионная смола может постепенно обменивать по меньшей мере некоторые из протонов на катион ионной жидкости. Обмененная сильнокислая катионная смола может быть регенерирована путем приведения ее в контакт с раствором хлористоводородной кислоты, что, таким образом, приводит к высвобождению катионов ионной жидкости в раствор. Данный отработанной кислый раствор, содержащий высвобожденные катионы ионной жидкости, может быть рециркулирован обратно на стадию кондиционирования и гидролиза 100. Данная рециркуляция может предотвращать потерю ионной жидкости и уменьшать подвод кислоты в совокупный процесс.
[0087] Получаемый в результате поток 351 может содержать от 3 до 10% глюкозы, не более 0,2% фруктозы, от 15 до 45% воды и от 1 до 3% гидроксиметилфурфурола, и может характеризоваться как кислый, имея pH не более 1. Значение pH потока 351 может быть отрегулировано до 2-3 pH-регулировкой 340 с помощью слабокислой катионной смолы, предварительно нагруженной по меньшей мере частично катионами ионной жидкости, что, таким образом, приводит к регенерации слабокислой катионной смолы в ее протонную форму. Данное колебательное использование слабокислой катионной смолы для снижения pH раствора перед дегидратацией и увеличения pH раствора после дегидратации может обеспечивать возможность сокращения общего подвода кислоты в процессе по меньшей мере на 30, 40, 50 или 60%. Слабоосновную катионную смолу можно периодически регенерировать с помощью кислоты, что обеспечивает возможность непрерывной работы. Регенерирующий раствор, содержащий кислоту и катионы ионной жидкости, может быть рециркулирован на стадию кондиционирования и гидролиза 100.
III. Отделение и очистка глюкозы
[0088] Может быть желательно отбирать некоторое количество гидролизованной целлюлозной пульпы в качестве очищенного продукта глюкозы для использования в целях, отличных от превращения в гидроксиметилфурфурол. Глюкоза имеет многочисленные применения в процессах в качестве сырья для ферментации и для процессов химического превращения, а также качестве пищевого и кормового продукта.
[0089] Способ, который производит глюкозу в качестве потока продукта, дополнительного к общей конверсии целлюлозной пульпы в гидроксиметилфурфурол, представлен на Фиг. 6, который представляет собой способ, альтернативный таковому, который представлен на Фиг. 5. Оба способа можно осуществлять параллельно, перенаправляя часть потока 302 в поток 311. Поток 311 может содержать от 1 до 8% глюкозы, и от 15 до 40% ионной жидкости может быть подано на второе хроматографическое разделение, так что получают поток 316 и поток 317. Поток 316 может представлять собой главным образом глюкозу в воде, имея концентрацию ионной жидкости не более 5, 4, 3, 2, 1 или 0,5%. Поток 317 может быть направлен обратно в процесс 300 конверсии. Каждое хроматографическое разделение может быть оптимизировано для суммарной концентрации подаваемого материала и конкретной концентрации подлежащих разделению соединений. Смола, использованная для второго хроматографического разделения, может быть той же самой, что использованная в первом хроматографическом разделении. Альтернативно можно использовать другую смолу. Кроме того, параметры потока могут быть изменены или оптимизированы для каждого хроматографического разделения, чтобы увеличить общий выход или чистоту продукта глюкозы, как известно в данной области.
[0090] Поток 316 может быть перенесен на стадию очистки глюкозы. Очистка может быть достигнута приведением данного потока в контакт по меньшей мере один раз с сильнокислой катионной смолой, смолой WBA, смолой со смешанными слоями или активированным углеродом или испарением. Поток может быть сначала приведен в контакт с сильнокислой катионной смолой, чтобы уловить остаточные катионы ионной жидкости, данные остаточные количества могут быть рециркулированы в процесс; поток 316 может быть приведен в контакт с анионообменником, чтобы нейтрализовать кислотность и удалить остаточные органические кислоты. Анионообменник может быть выбран из смолы WBA или жидкого анионообменника, например, аминной экстракционной органической фазы. Выбор ионообменника может основываться на эффективности и экономичности данной технологической стадии, например, если количество органической кислоты в растворе составляет более 0,1% по массе к массе сахара, предпочтительным может являться жидкий анионообменник. Активированный углерод можно использовать для удаления органических примесей. Сильнокислый катионообменник можно использовать для удаления остаточных катионов. Второй WBA можно использовать для нейтрализации. Испарение можно использовать для получения концентрации растворенного твердого вещества 30-50%. Смола со смешанными слоями может быть использована для окончательной очистки. Окончательное испарение может быть использовано для получения водного раствора с концентрацией глюкозы 70%.
[0091] Здесь предоставлены композиции, включая следующие, но без ограничения ими: композиция продукта глюкозы, предоставленная, например, как показано на Фиг. 5 и Фиг. 6.
[0092] Предоставленные здесь композиции могут содержать: i) по меньшей мере 95% C6-углеводов (масса/сухое вещество); ii) по меньшей мере 90% моносахаридов (масса/сухое вещество); iii) по меньшей мере 90% глюкозы (масса/сухое вещество); iv) по меньшей мере один не являющийся глюкозой C6-углевод, где по меньшей мере 90% не являющегося глюкозой C6-углевода приходится на маннозу (масса/масса); и v) по меньшей мере 100 ч.н.млрд. маркерной молекулы, где маркерная молекула выбрана из катиона ионной жидкости, имидазола, производного имидазола, адъюванта имидазола-сахара, гидроксиметилфурфурола или растворителя S3.
[0093] В некоторых примерах композиции могут содержать не более 99% C6-углеводов (масса/сухое вещество). В некоторых примерах композиции могут содержать от 95 до 99% или 90, 91, 92, 93, 94, 95, 96, 97, 98 или 99% C6-углеводов (масса/сухое вещество). В некоторых примерах композиции могут содержать не более 99% моносахаридов (масса/сухое вещество). В некоторых примерах композиции могут содержать от 90 до 99% или 90, 91, 92, 93, 94, 95, 96, 97, 98 или 99% моносахаридов (масса/сухое вещество). В некоторых примерах композиции могут содержать не более 99% глюкозы (масса/сухое вещество). В некоторых примерах композиции могут содержать от 90 до 99% или 90, 91, 92, 93, 94, 95, 96, 97, 98 или 99% глюкозы (масса/сухое вещество). В некоторых примерах композиции могут содержать не более 99% маннозы в качестве не являющегося глюкозой C6-углевода (масса/масса). В некоторых примерах композиции могут содержать от 90 до 99% или 90, 91, 92, 93, 94, 95, 96, 97, 98 или 99% маннозы в качестве не являющегося глюкозой C6-углевода (масса/масса). В некоторых примерах композиции могут содержать 5000 ч.н.м. (5000000 ч.н.млрд.) маркерной молекулы, где маркерная молекула выбрана из катиона ионной жидкости, имидазола, производного имидазола, адъюванта имидазола-сахара, гидроксиметилфурфурола или растворителя S3. В некоторых примерах композиции могут содержать от 100 ч.н.млрд. до 5000 ч.н.м. (5000000 ч.н.млрд.) маркерной молекулы, где маркерная молекула выбрана из катиона ионной жидкости, имидазола, производного имидазола, адъюванта имидазола-сахара, гидроксиметилфурфурола или растворителя S3.
[0094] В некоторых примерах композиции могут содержать 70% раствор глюкозы в воде. В некоторых примерах композиции могут содержать по меньшей мере 90, 91, 92, 93, 94, 95, 96 или 97% C6-сахаров. На глюкозу может приходиться по меньшей мере 60, 70, 80 или 90% сахаров в выражении на массу/суммарную массу сахаров, а на маннозу может приходиться по меньшей мере 90, 95 или 98% остаточного сахара. По меньшей мере 90, 91, 92, 93, 94, 95, 96, 97 или 98% сахара может находиться в мономерной форме. В некоторых примерах композиции могут содержать по меньшей мере 100 ч.н.млрд. до 5000 ч.н.м. маркерной молекулы, где маркерная молекула выбрана из катиона ионной жидкости, имидазола, производного имидазола, адъюванта имидазола-сахара, гидроксиметилфурфурола или растворителя S3.
IV. Извлечение гидроксиметилфурфурола
[0095] Поток 301 на Фиг. 3, Фиг. 5 и Фиг. 6 может представлять собой поток продукта, где поток продукта может содержать гидроксиметилфурфурол. Концентрация гидроксиметилфурфурола в потоке продукта может быть низкой, типично не более 5, 4, 3, 2 или 1% (масса/масса). Поток 301 может содержать остаточные количества органических кислот, образовавшихся в результате разложения гидроксиметилфурфурола или фурфурола, например, муравьиной кислоты и левулиновой кислоты. Желательным может быть осуществление рентабельного способа извлечения гидроксиметилфурфурола и его очистки от данного сильно разбавленного раствора. На Фиг. 7 представлены система и способ эффективного и энергосберегающего извлечения гидроксиметилфурфурола из разбавленного потока. Нефункциональная полимерная (NF) смола, которая обладает высоким сродством к гидроксиметилфурфуролу, может быть использована в адсорбционном концентрировании 410 для адсорбции продукта гидроксиметилфурфурола из разбавленного водного раствора, действуя, таким образом, в качестве ловушки. Подходящая нефункциональная полимерная смола может представлять собой Purolite Hypersol-Macronet® MN200 или любую другую подобную нефункциональную полимерную смолу, используемую в данной области техники. Данная нефункциональная полимерная смола не улавливает органические кислоты, когда они депротонированы, и таким образом, гидроксиметилфурфурол улавливается, в то время как органическая кислота элюируется промывкой путем контроля pH выше значения pH депротонирования данных кислот. Значение pH раствора можно отрегулировать в диапазоне от 6,5 до 7,5 путем примешивания ионной жидкости в гидроксидной форме перед приведением в контакт с нефункциональной полимерной смолой. После того как достигается почти полная или полная емкость смолы уловленный гидроксиметилфурфурол может быть десорбирован из смолы с помощью значительно уменьшенного объема раствора, состоящего из растворителя S2:вода в соотношении от 80:20 до 99:1.
[0096] Растворитель S2 может характеризоваться способностью растворять гидроксиметилфурфурол. Растворитель S2 может характеризоваться образованием гетерогенного азеотропа с водой, где точка кипения азеотропа составляет вплоть до 90°C и меньше, чем точка кипения растворителя S2. Предпочтительно, растворимость воды в растворителе низка и растворимость растворителя в водной фазе низка. Растворитель S2 может быть выбран из этилацетата, метанола, этанола, изопропанола, 1-бутанола, 2-бутанола или их сочетания. Растворитель S2 может представлять собой этилацетат.
[0097] Нефункциональная полимерная смола может быть использована для извлечения гидроксиметилфурфурола и удаления органических кислот, где этилацетат может действовать в качестве регенерационной среды. Адсорбционно-десорбционное действие стадии 410 может снижать энергозатраты на извлечение гидроксиметилфурфурола по меньшей мере в 5, 7, 10, 15 или 20 раз, поскольку масса растворителя в потоке 411 может быть уменьшена в 2, 4, 6, 8, 10, 20, 50 или 100 раз по сравнению с потоком 301, а также поскольку относительная доля воды к этилацетату может быть уменьшена со 100% масса/масса до 3-4% масса/масса. Поток 411 может быть перенесен на дистилляцию 420, где этилацетат может быть выпарен при 70,4°C или 70°C, 70,4°C, 70,5°C или 71°C. Поток пара 421 может быть перенесен на декантацию 430 для отделения воды от растворителя. Получаемый в результате поток 432 может содержать смесь этилацетата:воды в соотношении 97:3 и затем может быть рециркулирован для дальнейшего использования. Водная фаза 431 может быть перенесена в отпариватель 415 для удаления испарением остаточных количеств растворителя по потоку 417. Поток 416 может быть приведен в контакт со слабокислой катионной смолой в протонной форме для улавливания остаточных катионов ионной жидкости катионообменником 440, который может быть регенерирован путем приведения в контакт слабокислой катионной смолы с кислотой и рециркуляцией катионов ионной жидкости на стадию гидролиза. Водный поток, который отпарен от катионов ионной жидкости, может быть перенесен в установку обработки сточных вод, где органические кислоты могут быть ферментированы с получением метана. Растворитель с более высокой точкой кипения может быть прибавлен до, в ходе или после дистилляции в качестве подходящего сорастворителя для гидроксиметилфурфурола в случае необходимости для последующей стадии использования гидроксиметилфурфурола. Растворитель с более высокой точкой кипения может быть выбран из 2-бутанола, 2-пропанола, тетралина или воды или их сочетания. Растворитель с более высокой точкой кипения может представлять собой 2-бутанол. Продукт 1100 может содержать по меньшей мере 5, 10, 15, 20, 25 или 30% гидроксиметилфурфурола. Продукт 1100 может содержать по меньшей мере 50 ч.н.млрд. маркерной молекулы, где маркерная молекула выбрана из этилацетата, воды, катиона ионной жидкости, фурфурола, аниона левулината, аниона формиата, глюкозы, фруктозы, маннозы или аддуктов сахара и катиона ионной жидкости. Продукт 1100 может также содержать по меньшей мере 50 ч.н.млрд. маркерной молекулы, где маркерная молекула выбрана из этилацетата, катиона ионной жидкости, фурфурола, аниона левулината, аниона формиата, глюкозы, фруктозы или маннозы.
[0098] Здесь предоставлены композиции, включая следующие, но без ограничения ими: продукт 1100, предоставляемый как показано, например, на Фиг. 7.
[0099] Предоставленные здесь композиции могут содержать по меньшей мере 5% гидроксиметилфурфурола (масса/масса) и не более 95% растворителя (масса/масса), где растворитель выбран из 2-бутанола, 2-пропанола, тетралина или воды или их сочетания. В некоторых примерах композиции могут содержать по меньшей мере 50 ч.н.млрд. маркерной молекулы, где маркерная молекула выбрана из этилацетата, катиона ионной жидкости, фурфурола, аниона левулината, аниона формиата, левулиновой кислоты, муравьиной кислоты, глюкозы, фруктозы или маннозы. В некоторых примерах композиции могут содержать не более 50% гидроксиметилфурфурола (масса/масса). В некоторых примерах композиции могут содержать от 5 до 50% или 5, 10, 15, 20, 25, 30, 35, 40, 45 или 50% гидроксиметилфурфурола (масса/масса). В некоторых примерах композиции могут содержать не более 10% гидроксиметилфурфурола (масса/масса). В некоторых примерах композиции могут содержать от 5 до 10% гидроксиметилфурфурола (масса/масса). В некоторых примерах композиции могут содержать 5000 ч.н.м. (5000000 ч.н.млрд.) маркерной молекулы, где маркерная молекула выбрана из этилацетата, катиона ионной жидкости, фурфурола, аниона левулината, аниона формиата, левулиновой кислоты, муравьиной кислоты, глюкозы, фруктозы или маннозы. В некоторых примерах композиции могут содержать от 50 ч.н.млрд. до 5000 ч.н.м. (5000000 ч.н.млрд.) маркерной молекулы, где маркерная молекула выбрана из этилацетата, катиона ионной жидкости, фурфурола, аниона левулината, аниона формиата, левулиновой кислоты, муравьиной кислоты, глюкозы, фруктозы или маннозы.
V. Рециркуляция ионной жидкости
[0100] Ионные жидкости обладают преимуществами в качестве реакционных сред перед традиционными растворителями, поскольку они обычно являются нелетучими или невоспламеняемыми и поскольку некоторые ионные жидкости экологически безопасны благодаря своей низкой экотоксичности. Некоторые ионные жидкости могут быть высокоэффективными в растворении кристаллической целлюлозы. Потенциальным недостатком ионной жидкости может являться высокая стоимость. Полезной может быть разработка весьма эффективной рециркуляции ионной жидкости в раскрытых здесь способах во избежание непроизводительных потерь ионной жидкости и связанным с этим увеличенных затрат. Здесь предоставлены способы и процессы улавливания и/или рециркуляции ионной жидкости.
a) Улавливание катионов ионной жидкости в разбавленных водных потоках
[0101] Улавливание и/или рециркуляция ионной жидкости может включать в себя обработку каждого разбавленного водного потока (например, разбавленных водных потоков, направленных на обработку отходов) слабокислой катионной смолой, чтобы вызвать адсорбцию катиона ионной жидкости, например, катионной формы 1-этил-3-метилимидазолия или 1-бутил-3-метилимидазолия. Катион ионной жидкости может быть регенерирован путем приведения смолы в контакт с кислым потоком или такой поток может представлять собой выходящий поток сильнокислой катионной смолы, имеющий избыток протонов, с целью уменьшения совокупного использования воды и кислоты в способе.
b) Рециркуляция ионной жидкости для растворения целлюлозы
[0102] Раскрытые здесь способы могут включать в себя использование воды, и желательным может быть удаление воды из ионной жидкости в ходе рециркуляции для растворения целлюлозы, поскольку вода вызывает осаждение целлюлозы до того, как целлюлоза гидролизуется. Удаления воды можно добиться прибавлением растворителя S3, который смешивается с ионной жидкостью и водой и образует гетерогенный азеотроп с водой, где точка кипения азеотропа может составлять не более 100°C при 100 мм Hg и где смешиваемость растворителя с водой может составлять не более 1%. Растворитель S3 может представлять собой линейный или разветвленный C8-, C9-, C10-, C11- или C12-алкил, замещенный по меньшей мере одним заместителем, выбранным из гидрокси, оксо, нитрила или галогенида. Растворитель S3 может представлять собой линейный или разветвленный C5-, C6- или C7-арил, замещенный по меньшей мере одним заместителем, выбранным из гидрокси, оксо, нитрила или галогенида. Растворитель S3 может быть выбран из циклогексанола, 2-этил-1-гексанола, гексилхлорида, бутиронитрила, циклогексанона, циклопентанона, диизобутилкетона, дипропилкетона, мезитилоксида, метиламилкетона, 2,4-пентандиона, 2,3-дихлорпропанола, дихлопентадиена, этилбензола, стирола или ксилола. Азеотропная дистилляция может быть проведена при пониженном давлении при не более чем 100, 80 или 60°C. Энергические потребность для испарения 1 кг воды может быть уменьшена до не более чем 80, 70, 60, 50 или 40% энергии, требуемой для прямого испарения воды из фазы ионной жидкости.
[0103] Здесь предоставлены композиции, включая следующие, но без ограничения ими: поток 501, предоставляемый как показано, например, на Фиг. 8.
[0104] Предоставленные здесь композиции могут содержать: i) по меньшей мере 95% ионной жидкости (масса/масса); ii) от 0,1 до 2% целлобиозы (масса/масса); iii) не более 0,1% (масса/масса) фруктозы; iv) не более 0,1% (масса/масса) гидроксиметилфурфурола; v) не более 4% (масса/масса) воды; и vi) не более 2% (масса/масса) растворителя S3. В некоторых примерах композиции могут содержать: i) по меньшей мере 95% ионной жидкости (масса/масса); ii) от 0,1 до 2% целлобиозы (масса/масса); iii) не более 0,1% (масса/масса) фруктозы; iv) не более 0,1% (масса/масса) гидроксиметилфурфурола; v) не более 4% (масса/масса) воды; vi) не более 2% (масса/масса) растворителя S3; и иметь по меньшей мере одну из следующих характеристик: i) содержать от 0,1 до 3% глюкозы (масса/масса); ii) не более 0,1% маннозы (масса/масса); iv) не более 0,1% левулиновой кислоты (масса/масса); и v) не более 0,1% муравьиной кислоты (масса/масса).
[0105] В некоторых примерах композиции могут содержать: i) по меньшей мере 95% ионной жидкости (масса/масса); ii) от 0,1 до 2% целлобиозы (масса/масса); iii) не более 0,1% (масса/масса) фруктозы; iv) не более 0,1% (масса/масса) гидроксиметилфурфурола; v) не более 4% (масса/масса) воды; vi) не более 2% (масса/масса) растворителя S3; и иметь по меньшей мере две из следующих характеристик: i) содержать от 0,1 до 3% глюкозы (масса/масса); ii) не более 0,1% маннозы (масса/масса); iv) не более 0,1% левулиновой кислоты (масса/масса); и v) не более 0,1% муравьиной кислоты (масса/масса).
[0106] В некоторых примерах композиции могут содержать: i) по меньшей мере 95% ионной жидкости (масса/масса); ii) от 0,1 до 2% целлобиозы (масса/масса); iii) не более 0,1% (масса/масса) фруктозы; iv) не более 0,1% (масса/масса) гидроксиметилфурфурола; v) не более 4% (масса/масса) воды; vi) не более 2% (масса/масса) растворителя S3; и иметь по меньшей мере три из следующих характеристик: i) содержать от 0,1 до 3% глюкозы (масса/масса); ii) не более 0,1% маннозы (масса/масса); iv) не более 0,1% левулиновой кислоты (масса/масса); и v) не более 0,1% муравьиной кислоты (масса/масса).
[0107] В некоторых примерах предоставленные здесь композиции могут содержать по меньшей мере 94, 95, 96, 97, 98 или 99% ионной жидкости (масса/масса). В некоторых примерах предоставленные здесь композиции могут содержать не более 99,7% ионной жидкости (масса/масса). В некоторых примерах предоставленные здесь композиции могут содержать от 95 до 99,7% ионной жидкости (масса/масса). В некоторых примерах предоставленные здесь композиции могут содержать по меньшей мере 0,001% фруктозы (масса/масса). В некоторых примерах предоставленные здесь композиции могут содержать от 0,001 до 0,1% или 0,001, 0,005, 0,01, 0,05 или 0,1% фруктозы (масса/масса). В некоторых примерах предоставленные здесь композиции могут содержать по меньшей мере 0,001% гидроксиметилфурфурола (масса/масса). В некоторых примерах предоставленные здесь композиции могут содержать от 0,001 до 0,1% или 0,001, 0,005, 0,01, 0,05 или 0,1% гидроксиметилфурфурола (масса/масса). В некоторых примерах предоставленные здесь композиции могут содержать по меньшей мере 0,4% воды (масса/масса). В некоторых примерах предоставленные здесь композиции могут содержать от 0,4 до 4% или 0,4, 0,5, 1, 1,5, 2, 2,5, 3, 3,5 или 4% воды (масса/масса). В некоторых примерах предоставленные здесь композиции могут содержать по меньшей мере 0,2% растворителя S3 (масса/масса). В некоторых примерах предоставленные здесь композиции могут содержать от 0,2 до 2% или 0,2, 0,5, 1, 1,5 или 2% растворителя S3 (масса/масса). В некоторых примерах предоставленные здесь композиции могут содержать по меньшей мере 0,001% маннозы (масса/масса). В некоторых примерах предоставленные здесь композиции могут содержать от 0,001 до 0,1% или 0,001, 0,005, 0,01, 0,05 или 0,1% маннозы (масса/масса). В некоторых примерах предоставленные здесь композиции могут содержать по меньшей мере 0,001% левулиновой кислоты (масса/масса). В некоторых примерах предоставленные здесь композиции могут содержать от 0,001 до 0,1% или 0,001, 0,005, 0,01, 0,05 или 0,1% левулиновой кислоты (масса/масса). В некоторых примерах предоставленные здесь композиции могут содержать 0,001% муравьиной кислоты (масса/масса). В некоторых примерах предоставленные здесь композиции могут содержать от 0,001 до 0,1% или 0,001, 0,005, 0,01, 0,05 или 0,1% муравьиной кислоты (масса/масса).
[0108] В некоторых примерах предоставленные здесь композиции могут содержать по меньшей мере одно соединение, выбранное из целлобиозы, глюкозы, фруктозы, маннозы, гидроксиметилфурфурола, левулиновой кислоты, муравьиной кислоты, воды или растворителя S3. В некоторых примерах предоставленные здесь композиции могут содержать от 0,1 до 2% целлобиозы (масса/масса); от 0,1 до 3% глюкозы (масса/масса); не более 0,1, 0,05 или 0,01% фруктозы (масса/масса); не более 0,1, 0,05 или 0,01% маннозы (масса/масса); не более 0,1, 0,05 или 0,01% гидроксиметилфурфурола (масса/масса); не более 0,1, 0,05, 0,01, 0,005 или 0,001% левулиновой кислоты (масса/масса); не более 0,1, 0,05, 0,01, 0,005 или 0,001% муравьиной кислоты (масса/масса); 0,1, 0,5, 1, 1,5, 2, 2,5, 3, 3,5 или 4% воды (масса/масса); и не более 2, 1, 0,5, 0,1 или 0,05% растворителя S3 (масса/масса).
[0109] В некоторых примерах растворитель S3 представляет собой циклогексанол.
ПРИМЕРЫ
[0110] Хотя здесь продемонстрированы и описаны предпочтительные варианты осуществления настоящего изобретения, специалистам в данной области будет понятно, что такие варианты осуществления приведены лишь в качестве примера. Теперь специалистам в данной области могут прийти на ум многочисленные варианты, изменения и замены в пределах изобретения. Следует понимать, что различные альтернативы описанным здесь вариантам осуществления изобретения можно применять при реализации изобретения на практике. Предполагается, что нижеследующая формула изобретения определяет объем изобретения и что способы и структуры в пределах объема данной формулы изобретения и их эквиваленты охватываются формулой изобретения.
Пример 1 - Композиция целлюлозной остаточной пульпы, полученной из сосны и эвкалипта
[0111] Свежие древесные щепы подавали в реактор высокого давления и нагревали от 135°C до 145°C в течение от 1 до 3 часов в растворе, содержащем от 0,3 до 0,5% H2SO4 и 0,2% SO2. Оставшееся твердое вещество отделяли от жидкости, содержащей гемицеллюлозные сахара, зольность, органические кислоты, растворимый в кислоте лигнин и экстрагируемые. Твердое вещество промывали свежим кислым раствором и сушили.
[0112] Затем оставшееся лигноцеллюлозное вещество нагревали до 160-210°C в течение 1-3 часов а растворе, содержащем метилэтилкетон:воду в соотношении 1:1 и от 0,5 до 1,5% (масса/масса) уксусной кислоты. Оставшуюся пульпу отделяли, промывали насыщенным водой метилэтилкетоном и сушили. Композицию полученной в результате целлюлозной пульпы характеризовали согласно способу TP-510-42618, предложенному Национальной лабораторией по изучению возобновляемой энергии (NREL). Зольность определяли согласно способу NREL TP-510-42622.
Таблица 1A: Композиция целлюлозной остаточной пульпы
(номер)
(глюкоза)
%масс./масс.
(%масс./масс.)
%масс./масс.
%масс./масс.
%масс./масс.
%масс./масс.
(18789)
(53,2)
(18790)
(66,8)
(18791)
(47,3)
(18790)
(60,5)
Таблица 1B: Остаточные целлюлозные пульпы, полученные данным способом, анализировали с помощью индуктивно-связанной плазмы (ICP)
Пример 2 - Композиция целлюлозной остаточной пульпы, полученной из эвкалипта
[0113] Эвкалиптовое сырье обрабатывали для извлечения гемицеллюлозных сахаров, зольности и растворимого в кислоте лигнина, как описано в примере 1. Лигноцеллюлозный остаток измельчали для получения порошка с размером частиц примерно 1400 микрон. Измельченный порошок, массой приблизительно 20 г и влажностью 5%, загружали в реактор для работы под давлением. В реактор прибавляли 100 г воды и 80 г метилэтилкетона и уксусную кислоту в количестве от 0,5% до 2,5% масс./масс. относительно суммарного количества жидкостей. Реактор нагревали до 160-190°C в течение 1-3 часов. Реактор охлаждали и разделяли твердое вещество и жидкость. Твердое вещество промывали дополнительным количеством раствора насыщенного водой МЭК и сушили под вакуумом.
[0114] Количество целлюлозы и лигнина в оставшемся твердом веществе измеряли согласно NREL/TP-510-42618. Результаты указывают на высокую эффективность условий реакций по извлечению лигнина, после чего остается менее 5% твердого лигнина (масса/масса) в оптимальных условиях, причем достижим является значение 2%.
Таблица 2: Композиции целлюлозной остаточной пульпы
Пример 3 - Композиция целлюлозной остаточной пульпы, полученной из эвкалипта
[0115] Процедуру примера 2 масштабировали в пятнадцать раз, используя реактор для работы под давлением объемом семь литров. Полуистощенный эвкалиптовый материал измельчали, тестировали различные условия реакции и характеризовали композицию полученной в результате пульпы. Результаты сведены в Таблице 3.
Таблица 3: Композиция целлюлозной остаточной пульпы
Пример - Композиция целлюлозной остаточной пульпы, полученной из багассы
[0116] Багассу освобождали от зольности, используя несколько циклов режущей обработки и промывая при высоком давлении, чтобы привести к удалению камней, песка и зольности. Полученную в результате освобожденную от зольности биомассу обрабатывали путем нагрева с 0,5% H2SO4 (16:1 масса/масса) при 135-145°C в течение 0,5-3 часов, чтобы экстрагировать гемицеллюлозу, растворимый в кислоте лигнин (ASL), органическую кислоту и остаточную зольность. Затем остаточный лигноцеллюлозный материал нагревали до 160-210°C в течение от 1 до 3 часов в растворе, содержащем метилэтилкетон:воду в соотношении 1:1 и от 0,5 до 1,5% (масса/масса) уксусной кислоты. Остаточную пульпу отделяли, промывали насыщенным водой метилэтилкетоном и сушили. Композицию полученной в результате целлюлозной пульпы характеризовали согласно способу NREL TP-510-42618. Зольность определяли согласно способу NREL TP-510-42622.
Таблица 4: Композиция целлюлозной остаточной пульпы
Пример 5- Свойства растворимости целлюлозной остаточной пульпы
[0117] Пульпы характеризовали по их растворимости в воде и эфире в сравнении с Avicel PH-200. Результаты сведены в Таблице 5.
Таблица 5: Свойства растворимости различных целлюлозных пульп
мкСм/см
*Опубликовано в Интернете:
http://www.signetchem.com/downloads/datasheets/Fmc-biopolymer/Avicel-Ph-200-Specifications.pdf
Пример 6 - Композиция целлюлозной остаточной пульпы, полученной из багассы и эвкалипта
[0118] Багассовое и эвкалиптовое сырье обрабатывали как в примере 1, чтобы сначала извлечь гемицеллюлозу, а затем извлечь лигнин. Характеризовали целлюлозную остаточную пульпу. Результаты сведены в Таблице 6.
Таблица 6: Характеристики багассовой и эвкалиптовой целлюлозных пульп
Пример 7: Хроматографическое разделение гидроксиметилфурфурола/глюкозы/целлобиозы/ионной жидкости
[0119] Смесь глюкозы, гидроксиметилфурфурола, целлобиозы и хлорида 1-этил-3-метилимидазолия пропускали через смолу PCR-642 в форме 1-этил-3-метилимидазолия. Использовали колонку объемом 240 мл с диаметром 2,5 см и проводили эксперимент при 60°C. Колонку элюировали деионизированной водой со скоростью 8 мл/мин. Собирали фракции объемом 10 мл с суммарным объемом 600 мл и анализировали ВЭЖХ на колонке Aminex HPX-87H. Полученные в результате профили показаны на Фиг. 9.
Пример 8: Изомеризация глюкозы во фруктозу
[0120] Раствор 22% хлорида 1-бутил-3-метилимидазолия и 3% глюкозы в воде титровали до желаемого значения pH, используя 10% стоковый раствор гидроксида 1-бутил-3-метилимидазолия. Отвешивали 3,0 г стокового раствора в пять стеклянных сосудов, оборудованных мешальником и воздухонепроницаемой крышкой. Реакционные смеси нагревали, причем один сосуд извлекали и охлаждали каждый раз. Каждый образец разбавляли в десять раз 0,1 M раствором хлористоводородной кислоты (в воде) для нейтрализации основания и фильтровали образцы для впрыскивания на колонку Aminex HPX-87H и/или колонку Dionex CarboPac SA-10 HPAE с детектированием посредством импульсного амперометрического детектора (PAD). Результаты сведены в Таблице 6. Колонка HPX-87H не разделяет фруктозу, маннозу и ксилозу (C5-примесь в сахаре). Образцы с высокой селективностью к не являющемуся глюкозой сахару анализировали на колонке Dionex для распознавания фруктозы, маннозы и ксилозы.
Таблица 8: Изомеризация глюкозы во фруктозу
10%
Пример 9: Дегидратация фруктозы в гидроксиметилфурфурол
[0121] Реакцию дегидратации раствора, содержащего фруктозу, глюкозу, хлорид 1-бутил-3-метилимидазолия и воду, проводили используя сильнокислую катионную смолу в качестве катализатора. Условия реакции и продукты сведены в Таблице 9, причем данные указывают на высокоспецифичную конверсию фруктозы в гидроксиметилфурфурол и на то, что глюкоза главным образом не подвергается изменению. Протестированные сильнокислые катионные смолы представляли собой смолу Purolite CT275DR SAC Resin или Rohm & Haas Amberlyst-15.
Таблица 9: Дегидратация фруктозы в гидроксиметилфурфурол
Пример 10: Извлечение и очистка гидроксиметилфурфурола
[0122] Приблизительно 30 мл нефункциональной смолы Purolite Hypersol-Macronet® MN200, 535±85 мкм, промывали деионизированной водой в стакане в течение 30 минут. Промытой смолой в объеме 15 мл набивали колонку 25 мл. Смолу промывали водой в объеме, равном 2 объемам слоя (BV), со скоростью 0,8 мл/мин. Подаваемый раствор имел состав в соответствии с Таблицей 10, и pH подаваемого раствора регулировали до значения 7. Подаваемый материал загружали на колонку со скоростью 0,8 мл/мин. Всего через колонку пропускали 20 BV и фракционировали на образцы объемом 1 BV. Образцы фильтровали и анализировали посредством хроматографа ВЭЖХ, оборудованного колонкой Aminex HPX-87H. Органические кислоты проходили через колонку, не адсорбируясь смолой. Концентрация органических кислот после BV 3 согласовывалась с концентрацией в подаваемом материале. Концентрации органических кислот в первых двух объемах, равных объему слоя, были ниже таковой в подаваемом материале, поскольку он разбавлялся за счет промывки, оставшейся на колонке. Гидроксиметилфурфурол не обнаруживался в выходящем потоке вплоть до BV 17 и далее до более высокого BV, что указывало на то, что емкость смолы была полностью нагружена.
Таблица 10: Композиция подаваемого материала
Пример 11: Хроматографическое разделение гидроксиметилфурфурола/глюкозы/целлобиозы/ионной жидкости/органических кислот
[0123] Смесь глюкозы, гидроксиметилфурфурола, целлобиозы и хлорида 1-этил-3-метилимидазолия объемом 8 мл, имеющую композицию, представленную в Таблице 11, пропускали через смолу PUROLITE PCR 642 H в 1-этил-3-метилимидазолиевой форме. Использовали колонку объемом 250 мл с диаметром 2,5 см, эксперимент проводили при 60°C. Элюирование с колонки осуществляли деионизированной водой со скоростью 8 мл/мин. Собирали фракции объемом 10 мл при суммарном объеме 600 мл и анализировали посредством ВЭЖХ на колонке Aminex HPX-87H. Полученные в результате профили показаны на Фиг. 10.
Таблица 11: Композиция подаваемого материала
Пример 12: Хроматографическое разделение глюкозы и хлорида 1-этил-3-метилимидазолия
[0124] Смесь глюкозы и хлорида 1-этил-3-метилимидазолия пропускали через смолу PCR-642H в 1-этил-3-метилимидазолиевой форме. Использовали колонку объемом 240 мл с диаметром 2,5 см, эксперимент проводили при 60°C. Элюирование с колонки осуществляли деионизированной водой со скоростью 8 мл/мин. Собирали фракции объемом 10 мл при суммарном объеме 600 мл и анализировали посредством ВЭЖХ на колонке Aminex HPX-87H. Полученные в результате профили показаны на Фиг. 11.
Пример 13: Извлечение и очистка глюкозы
[0125] Смесь из 1-8% глюкозы, 15-40% 1-этил-3-метилимидазолия, примерно 1% левулиновой кислота и примерно 1% муравьиной кислоты подают в хроматографическую установку с сильнокислой катионной смолой. Получают раствор с пониженной концентрацией 1-этил-3-метилимидазолия от 0,5 до 5% и впоследствии приводят его в контакт со второй хроматографической установкой с сильнокислой катионной смолой для улавливания остаточных катионов 1-этил-3-метилимидазолия. Полученную в результате смесь нейтрализуют до pH 6-7 и остаточные левулиновую и муравьиные кислоты удаляют, используя аминную экстракционную органическую фазу. Активированный углерод используют для удаления остаточных органических примесей. Смесь испаряют в испарительной установке для получения содержания растворенного твердого вещества 40% и раствора 90% глюкозы в воде.
Пример 14: Рециркуляция ионной жидкости для растворения целлюлозы
[0126] 2-Этил-1-гексанол прибавляют к потоку 1-бутил-3-метилимидазолия, воды и сахаров. Поток подают в дистилляционную установку, где проводят азеотропную дистилляцию для удаления 1-бутил-3-метилимидазолия, используя вакуумный насос для регулировки давления до 125 торр. Точка кипения 2-этил-1-гексанола составляет 185°C, а азеотропная точка кипения воды и 2-этил-1-гексанола составляет 99,1°C. Содержание 2-этил-1-гексанола в азеотропе составляет 20% (масса/масса), где на воду приходится остаток 80%. 1-Бутил-3-метилимидазолий рециркулируют на предварительную обработку целлюлозной остаточной пульпы. Композиция рециркулированного 1-бутил-3-метилимидазолия представлена в Таблице 14.
Таблица 14: Композиция рециркулированного 1-бутил-3-метилимидазолия
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ОБРАБОТКИ ЛИГНОЦЕЛЛЮЛОЗНЫХ МАТЕРИАЛОВ | 2013 |
|
RU2634700C2 |
| СПОСОБ ДЕГИДРАТАЦИИ УГЛЕВОДСОДЕРЖАЩИХ КОМПОЗИЦИЙ | 2012 |
|
RU2608609C2 |
| СПОСОБ ПРЕВРАЩЕНИЯ ПОЛИСАХАРИДОВ В РАСПЛАВЕ ГИДРАТА МИНЕРАЛЬНОЙ СОЛИ | 2009 |
|
RU2503722C2 |
| ФРАКЦИОНИРОВАНИЕ ПОТОКА ЖИДКИХ ОТХОДОВ ОТ ПРОИЗВОДСТВА НАНОКРИСТАЛЛИЧЕСКОЙ ЦЕЛЛЮЛОЗЫ | 2010 |
|
RU2541037C2 |
| Способ получения 5-гидроксиметилфурфурола и этанола из целлюлозы | 2016 |
|
RU2636004C1 |
| СПОСОБ ПЕРЕРАБОТКИ ЛИГНОЦЕЛЛЮЛОЗНОГО СЫРЬЯ | 2012 |
|
RU2532107C2 |
| Штамм дрожжей Kluyveromyces marxianus ВКПМ Y-4290, применяемый для получения этанола на каталитических гидролизатах целлюлозы | 2016 |
|
RU2626544C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФУРАНОВЫХ СОЕДИНЕНИЙ ИЗ УГЛЕВОДОВ, ЦЕЛЛЮЛОЗЫ ИЛИ ЛИГНОЦЕЛЛЮЛОЗНОГО СЫРЬЯ | 2016 |
|
RU2628802C1 |
| ЗАМКНУТЫЙ СПОСОБ ПОЛУЧЕНИЯ ФУРФУРОЛА ИЗ БИОМАСС | 2015 |
|
RU2713659C2 |
| РАСТВОРИТЕЛИ НА ОСНОВЕ ЛИГНИНА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2017 |
|
RU2740758C2 |

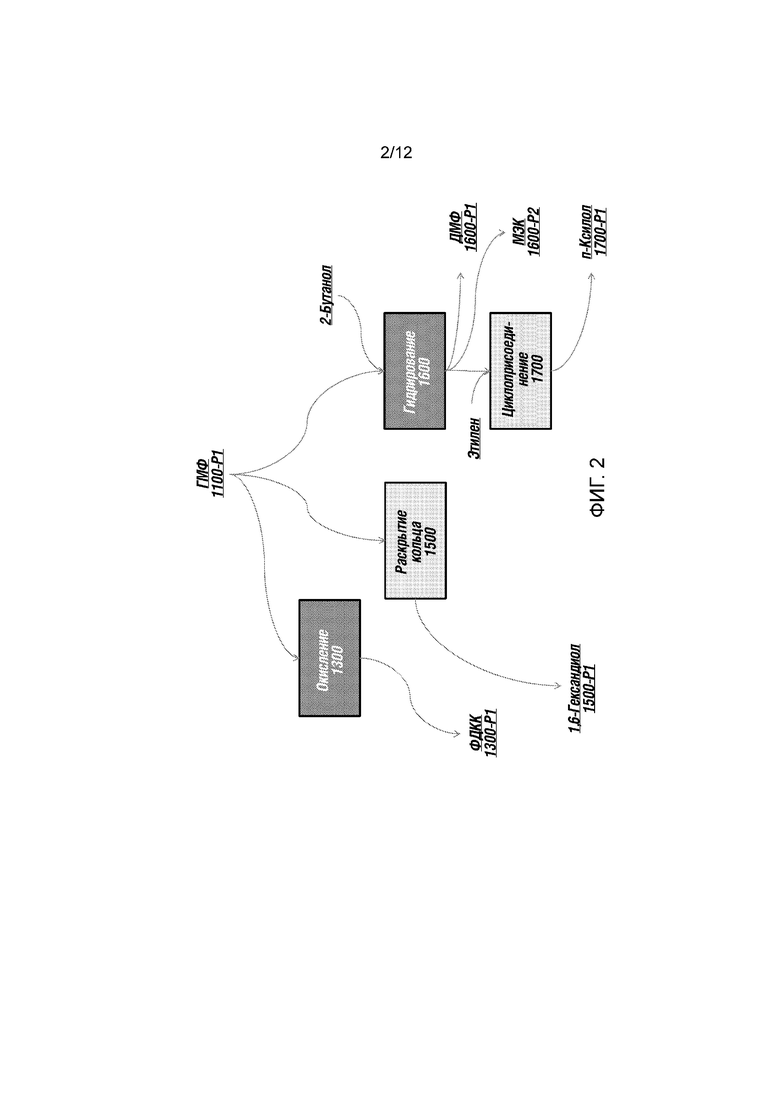
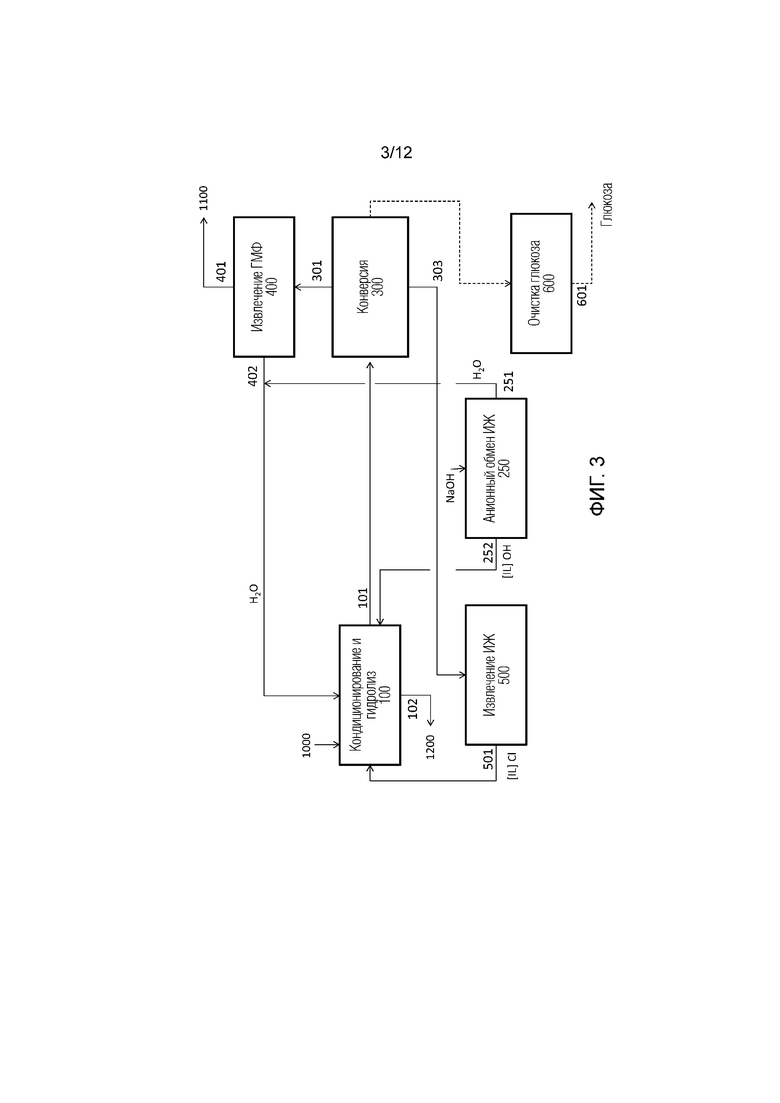
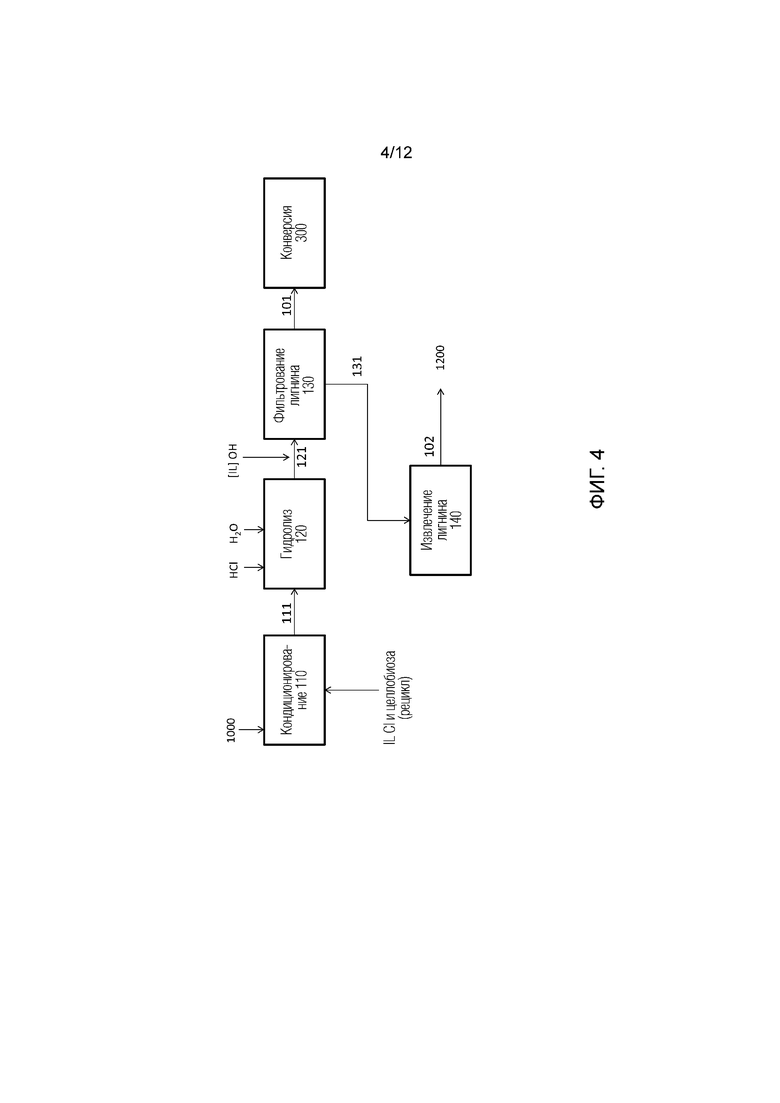
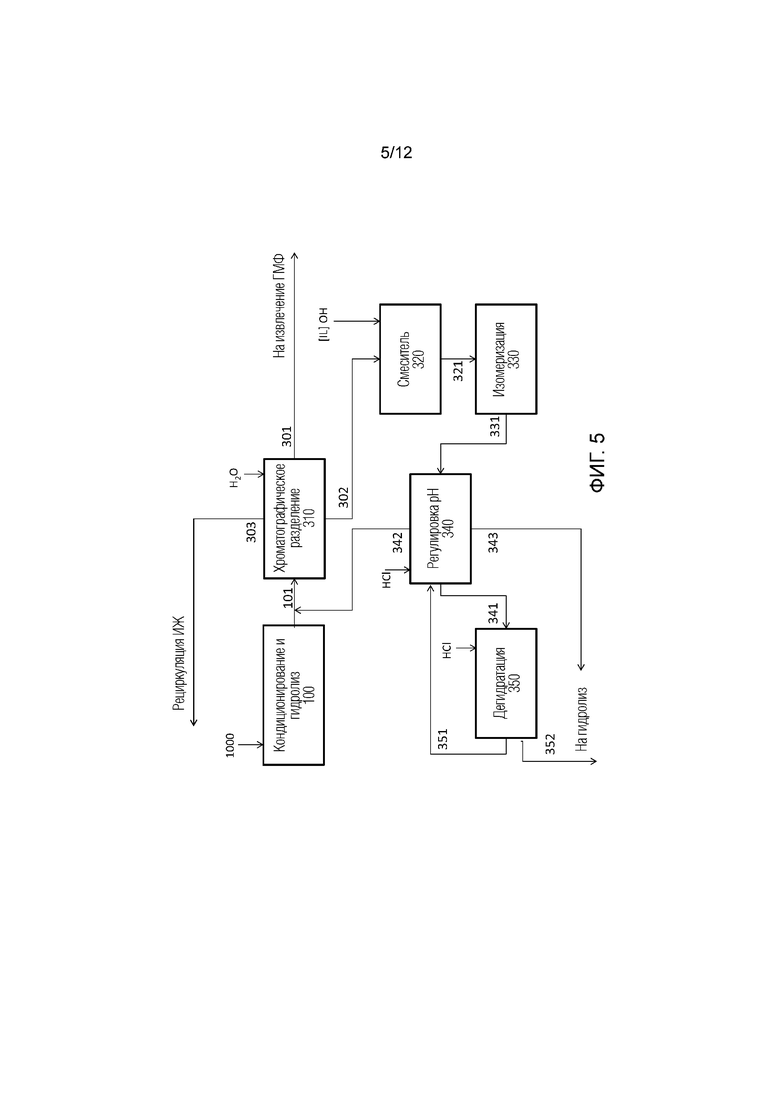
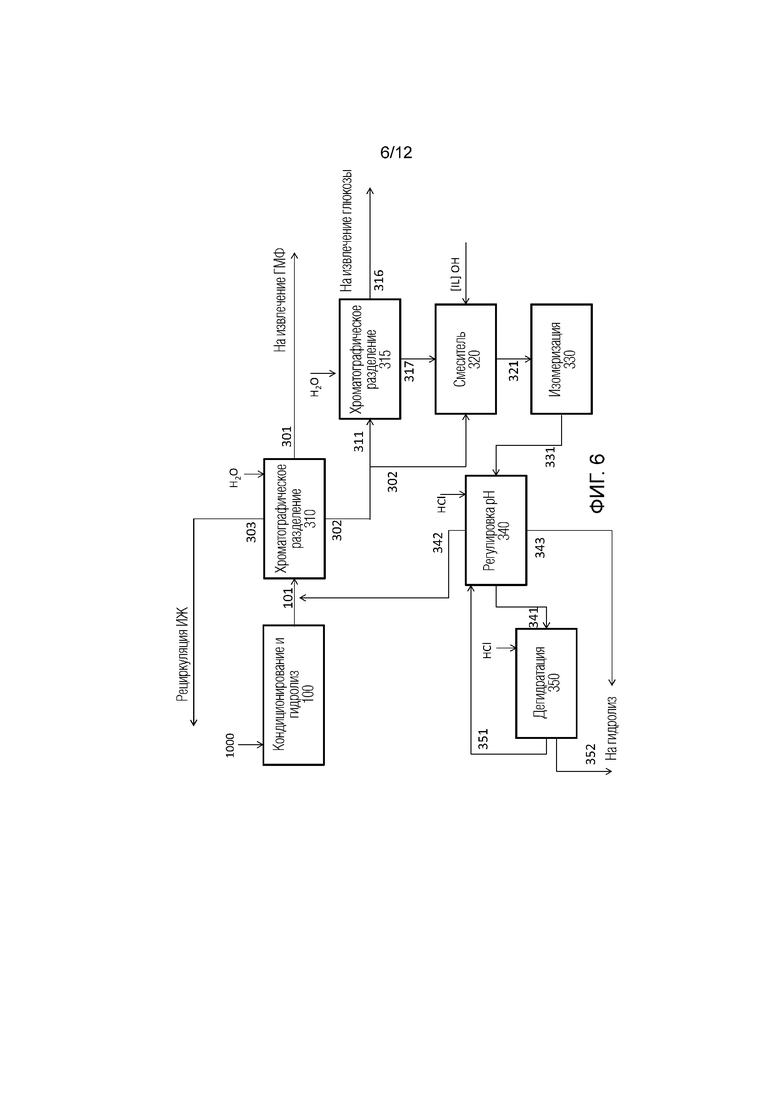
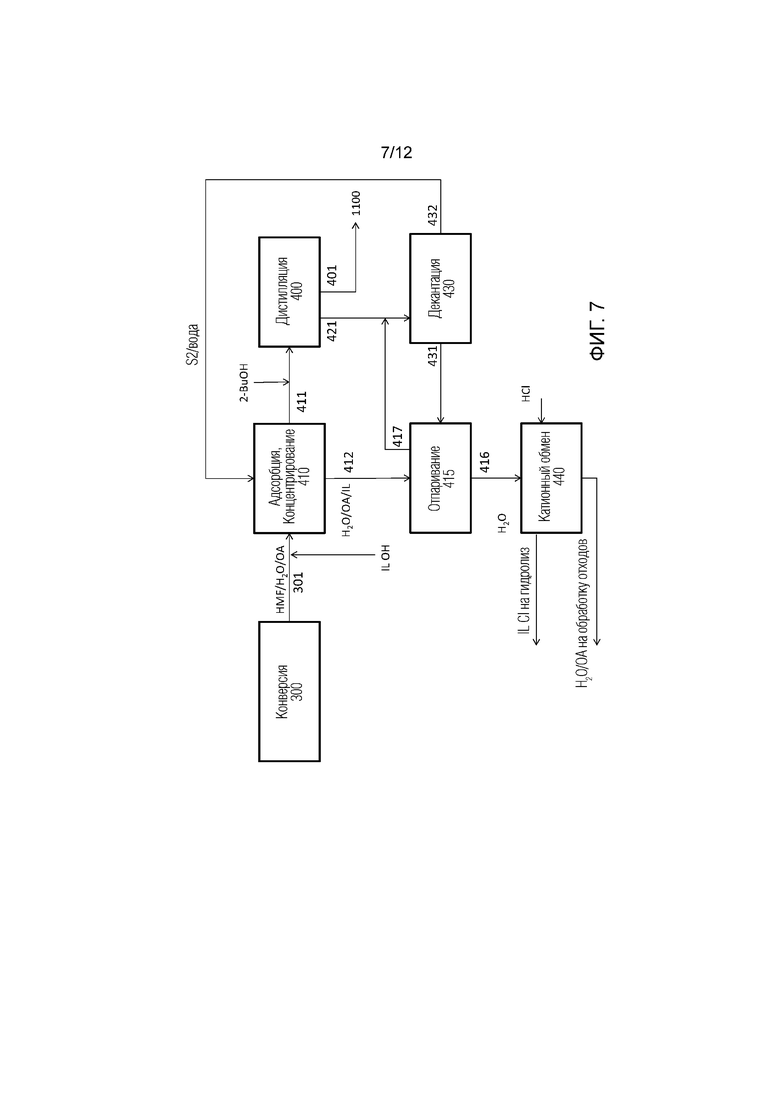
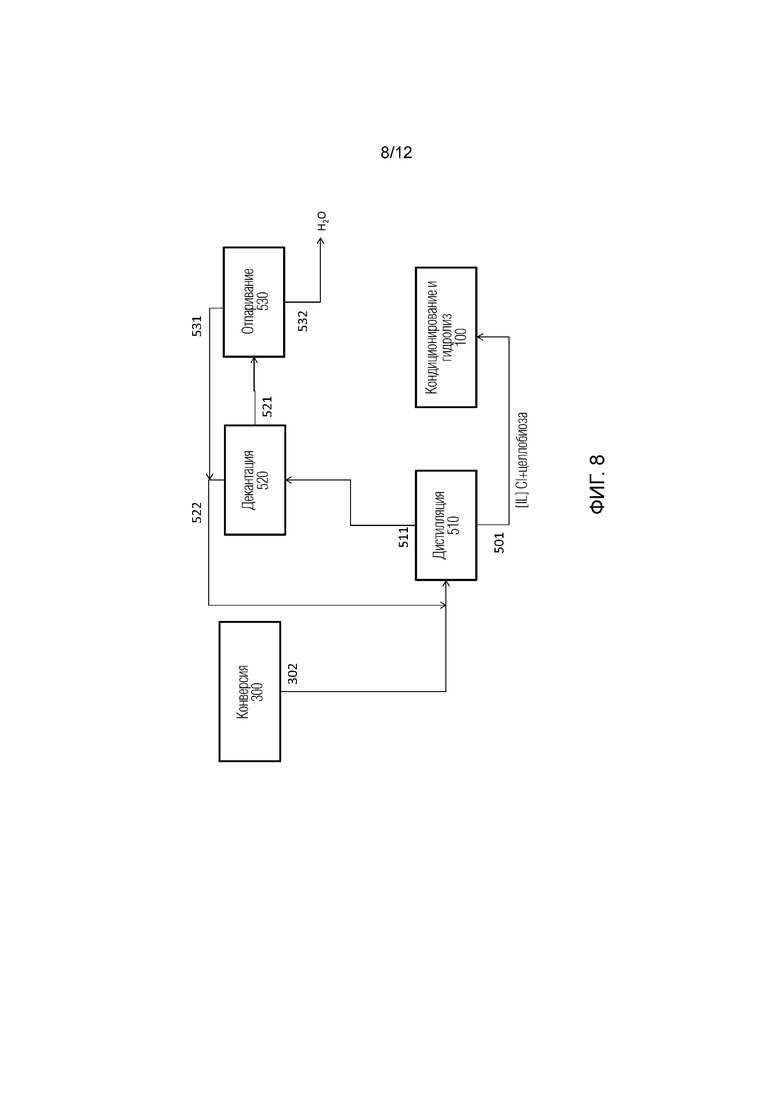

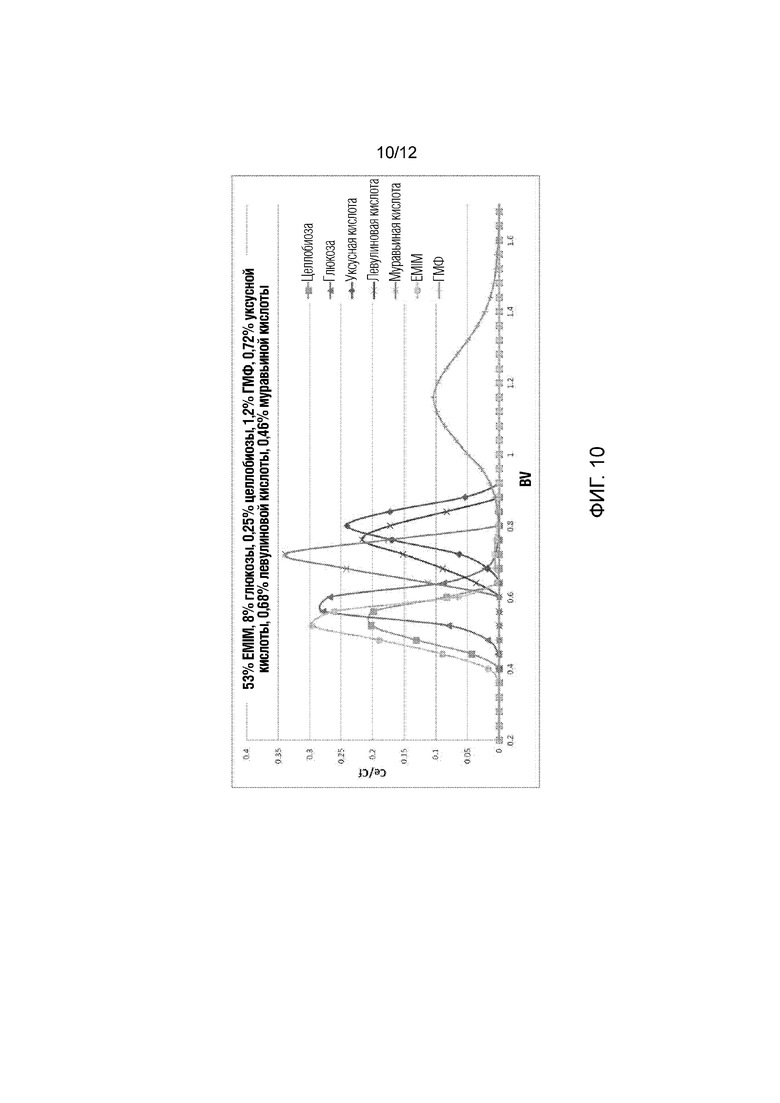


Настоящее изобретение может быть использовано в химической промышленности и относится к способам и системе получения гидроксиметилфурфурола из целлюлозы. Предложенный способ включает в себя: разделение потока гидролизата целлюлозной пульпы, содержащей 80% (масса/сухое вещество) целлюлозы, с зольностью менее 6%, с использованием установки хроматографического разделения, чтобы тем самым получить первый поток, содержащий воду и гидроксиметилфурфурол; второй поток, содержащий воду и глюкозу; и третий поток, содержащий воду и целлобиозу; изомеризацию глюкозы во втором потоке с получением фруктозы; дегидратацию фруктозы с получением продукта, содержащего гидроксиметилфурфурол; и рециркуляцию продукта реакции, причем рециркуляция включает в себя введение продукта реакции из дегидратации на разделение; или способ включает в себя: гидролиз целлюлозы с получением первого потока сахара, содержащего по меньшей мере 80% глюкозы (масса/сухое вещество) и воду; изомеризацию глюкозы в первом потоке сахара с получением фруктозы; дегидратацию фруктозы с получением продукта реакции, содержащего гидроксиметилфурфурол, и рециркуляцию части продукта реакции со стадии дегидратации на стадию разделения, получая тем самым по меньшей мере 60 г гидроксиметилфурфурола в качестве продукта на каждые 100 г целлюлозы, предусматриваемой в качестве исходного материала. Предложена система для конверсии глюкозы в гидроксиметилфурфурол, причем система включает в себя: установку хроматографического разделения, выполненную с возможностью разделения потока гидролизата целлюлозной пульпы, содержащей 80% (масса/сухое вещество) целлюлозы, с зольностью менее 6%, содержащего ионы натрия в количестве не более 5%, на первый поток, второй поток и третий поток; причем первый поток содержит воду и гидроксиметилфурфурол; второй поток содержит воду и глюкозу; и третий поток содержит воду и целлобиозу; установку изомеризации, выполненную с возможностью осуществления изомеризации глюкозы во фруктозу, причем изомеризация включает в себя обработку второго потока основанием, чтобы тем самым получить обработанный основанием второй поток; установку дегидратации, выполненную с возможностью дегидратации фруктозы в гидроксиметилфурфурол, и средство для рециркуляции потока, выполненное с возможностью доставки части продукта, содержащего гидроксиметилфурфурол, в установку хроматографического разделения. Предложены новые способы и система, эффективные для получения гидроксиметилфурфурола из целлюлозы. 3 н. и 40 з.п. ф-лы, 12 ил., 12 табл., 14 пр.
1. Способ получения гидроксиметилфурфурола, где способ включает:
разделение потока гидролизата целлюлозной пульпы, содержащей 80% (масса/сухое вещество) целлюлозы, с зольностью менее 6%, с использованием установки хроматографического разделения, чтобы тем самым получить первый поток, содержащий воду и гидроксиметилфурфурол; второй поток, содержащий воду и глюкозу; и третий поток, содержащий воду и целлобиозу;
изомеризацию глюкозы во втором потоке, чтобы тем самым получить фруктозу; и
дегидратацию фруктозы, чтобы тем самым получить продукт реакции, содержащий гидроксиметилфурфурол; и
рециркуляцию продукта реакции, причем рециркуляция включает в себя введение продукта реакции из дегидратации на разделение.
2. Способ по п. 1, дополнительно включающий в себя:
кондиционирование целлюлозной пульпы, содержащей целлюлозу и лигнин, в растворителе, чтобы тем самым сформировать кондиционированную пульпу;
гидролиз кондиционированной пульпы в водном растворе, содержащем кислый катализатор, чтобы тем самым получить поток гидролизата; и
удаление по меньшей мере некоторого лигнина из потока гидролизата, чтобы тем самым получить подаваемый поток и обогащенную лигнином композицию, причем удаление включает в себя контроль pH водного раствора и разбавление водного раствора водой;
где кондиционирование, гидролиз и удаление происходят перед разделением, изомеризацией и дегидратацией.
3. Способ по п. 2, где растворитель содержит ионную жидкость.
4. Способ по пп. 1, 2 или 3, где второй поток содержит ионную жидкость и третий поток содержит ионную жидкость.
5. Способ по пп. 1, 2, 3 или 4, дополнительно включающий в себя перенаправление подаваемого потока из первого сосуда во второй сосуд перед разделением, изомеризацией и дегидратацией.
6. Способ по пп. 1, 2, 3, 4 или 5, дополнительно включающий в себя:
улавливание гидроксиметилфурфурола из продукта реакции, причем улавливание включает в себя адсорбцию на нефункциональном полимере гидроксиметилфурфурола из продукта реакции; и
извлечение гидроксиметилфурфурола, причем извлечение включает в себя десорбцию растворителем.
7. Способ по п. 6, где продукт реакции содержит органическую кислоту.
8. Способ по п. 7, где улавливание дополнительно включает в себя контроль pH продукта реакции выше pKa органической кислоты, так чтобы вода и органические анионы не адсорбировались на нефункциональном полимере.
9. Способ по п. 8, где pH продукта реакции контролируют так, что его значение составляло более 5,8.
10. Способ по п. 3 или 4, где ионная жидкость выбрана из хлорида 1-этил-3-метилимидазолия или хлорида 1-бутил-3-метилимидазолия.
11. Способ по п. 10, дополнительно включающий в себя осуществление конверсии ионной жидкости в ионную жидкость в гидроксидной форме, причем осуществление конверсии включает в себя приведение в контакт водного раствора ионной жидкости, содержащего ионную жидкость, с сильноосновной анионообменной смолой в гидроксидной форме.
12. Способ по п. 11, где изомеризация включает в себя контроль pH, причем контроль включает в себя использование ионной жидкости в гидроксидной форме в качестве основания.
13. Способ по пп. 3, 4 или 12, где изомеризацию катализируют ионной жидкостью в гидроксидной форме.
14. Способ по п. 13, где ионная жидкость в гидроксидной форме образует ионную жидкость в хлоридной форме, которую используют для дегидратации.
15. Способ по п. 13, где замкнутый технологический контур используют для спаривания реакции изомеризации с реакцией дегидратации.
16. Способ по п. 14, где реакция изомеризации включает в себя изомеризацию глюкозы с образованием фруктозы, и где реакция дегидратации включает в себя дегидратацию фруктозы с образованием гидроксиметилфурфурола.
17. Система для конверсии глюкозы в гидроксиметилфурфурол, причем система включает в себя:
установку хроматографического разделения, выполненную с возможностью разделения потока гидролизата целлюлозной пульпы, содержащей 80% (масса/сухое вещество) целлюлозы, с зольностью менее 6%, содержащего ионы натрия в количестве не более 5%, на первый поток, второй поток и третий поток; причем первый поток содержит воду и гидроксиметилфурфурол; второй поток содержит воду и глюкозу; и третий поток содержит воду и целлобиозу;
установку изомеризации, выполненную с возможностью осуществления изомеризации глюкозы во фруктозу, причем изомеризация включает в себя обработку второго потока основанием, чтобы тем самым получить обработанный основанием второй поток;
установку дегидратации, выполненную с возможностью дегидратации фруктозы в гидроксиметилфурфурол; и
средство для рециркуляции потока, выполненное с возможностью доставки части продукта, содержащего гидроксиметилфурфурол, в установку хроматографического разделения.
18. Система по п. 17, где второй поток включает в себя ионную жидкость и третий поток включает в себя ионную жидкость.
19. Система по п. 17 или 18, дополнительно включающая в себя вторую установку хроматографического разделения, выполненную с возможностью разделения второго потока, чтобы тем самым получить поток продукта, содержащий глюкозу.
20. Система по п. 19, дополнительно включающая в себя установку очистки глюкозы, выполненную с возможностью очистки потока продукта, содержащего глюкозу, в продукт глюкозы, причем установка очистки глюкозы включает в себя по меньшей мере одну установку, выбранную из сильнокислой катионной смолы, анионообменника, смолы с активированным углем или испарительной установки.
21. Система по п. 20, где поток продукта, содержащий глюкозу, содержит по меньшей мере 60% глюкозы (масса/масса).
22. Способ конверсии целлюлозы в гидроксиметилфурфурол, причем способ включает в себя:
гидролиз целлюлозы с получением первого потока сахара, содержащего по меньшей мере 80% глюкозы (масса/сухое вещество) и воду;
изомеризацию глюкозы в первом потоке сахара с получением фруктозы;
дегидратацию фруктозы с получением продукта реакции, содержащего гидроксиметилфурфурол; и
рециркуляцию части продукта реакции со стадии дегидратации на стадию разделения, получая тем самым по меньшей мере 60 г гидроксиметилфурфурола в качестве продукта на каждые 100 г целлюлозы, предусматриваемой в качестве исходного материала.
23. Способ по п. 22, где по меньшей мере 63 г гидроксиметилфурфурола получают в качестве продукта на каждые 100 г целлюлозы, предусматриваемой в качестве исходного материала.
24. Способ по п. 23, где по меньшей мере 65 г гидроксиметилфурфурола получают в качестве продукта на каждые 100 г целлюлозы, предусматриваемой в качестве исходного материала.
25. Способ по п. 24, где по меньшей мере 67 г гидроксиметилфурфурола получают в качестве продукта на каждые 100 г целлюлозы, предусматриваемой в качестве исходного материала.
26. Способ по п. 22, где гидролиз происходит в ионной жидкости.
27. Способ по п. 26, где ионная жидкость выбрана из хлорида 1-бутил-3-метилимидазолия или хлорида 1-этил-3-метилимидазолия.
28. Способ по п. 26, где первый поток сахара содержит целлобиозу, гидроксиметилфурфурол и органические кислоты.
29. Способ по п. 26, дополнительно включающий в себя хроматографическое разделение второго потока сахара, содержащего гидроксиметилфурфурол, целлобиозу, ионную жидкость, глюкозу и фруктозу; причем хроматографическое разделение включает в себя применение последовательной хроматографии с симулированным движением стационарной фазы.
30. Способ по п. 29, где хроматографическое разделение дает первый выходящий поток, второй выходящий поток и третий выходящий поток; причем первый выходящий поток содержит гидроксиметилфурфурол; второй выходящий поток содержит ионную жидкость и глюкозу; и третий выходящий поток содержит ионную жидкость и целлобиозу.
31. Способ по п. 30, где в последовательной хроматографии с симулированным движением стационарной фазы используют смолу промышленной категории, включающую размеры бусин по меньшей мере 300 микрон.
32. Способ по п. 30, дополнительно включающий в себя обработку второго выходящего потока основанием, причем обработка включает в себя изомеризацию по меньшей мере части глюкозы во фруктозу, чтобы тем самым получить обработанный основанием второй поток.
33. Способ по п. 32, где основание содержит ионную жидкость, где ионная жидкость находится в гидроксидной форме.
34. Способ по п. 32, дополнительно включающий в себя обработку обработанного основанием второго потока, причем обработка включает в себя дегидратацию фруктозы в гидроксиметилфурфурол, чтобы тем самым получить дегидратированный второй поток, причем дегидратация включает в себя применение дегидратирующего агента.
35. Способ по п. 34, где не более 10% глюкозы, присутствующей в обработанном основании втором потоке, подвергается реакции с дегидратирующим агентом.
36. Способ по п. 35, дополнительно включающий в себя выделение гидроксиметилфурфурола, причем выделение включает в себя по меньшей мере одно из:
обработку дегидратированного второго потока, причем обработка включает в себя использование гидрофобной смолы, чтобы тем самым уловить гидроксиметилфурфурол;
десорбцию уловленного гидроксиметилфурфурола с гидрофобной смолы, причем десорбция включает в себя приведение нагруженной смолы в контакт с растворителем S2;
прибавление органического растворителя; и
дистилляцию растворителя S2, используя азеотропную дистилляцию.
37. Способ по п. 36, где растворитель S2 представляет собой этилацетат.
38. Способ по п. 26, дополнительно включающий в себя рециркуляцию ионной жидкости, причем рециркуляция включает в себя:
обработку первой части потока ионной жидкости слабокислой катионообменной смолой, чтобы тем самым сформировать поток, обработанный слабокислой катионообменной смолой;
прибавление растворителя к потоку, обработанному слабокислой катионообменной смолой;
дистилляцию растворителя и воды, чтобы тем самым сформировать поток дегидратированной ионной жидкости; и
введение в процесс ионной жидкости из потока дегидратированной ионной жидкости.
39. Способ по п. 38, где ионную жидкость из потока дегидратированной ионной жидкости вводят в реактор, содержащий целлюлозу, и где в реакторе целлюлоза подвергается гидролизу в глюкозу.
40. Способ по п. 26, дополнительно включающий в себя рециркуляцию ионной жидкости, причем рециркуляция включает в себя обработку потока, содержащего ионную жидкость, слабокислой катионообменной смолой, чтобы тем самым получить обработанный смолой поток, содержащий ионную жидкость; и повторное введение в процесс ионной жидкости из обработанного смолой потока.
41. Способ по п. 40, где ионную жидкость из обработанного смолой потока повторно вводят в композицию, содержащую по меньшей мере 70% глюкана (масса/сухое вещество).
42. Способ по п. 41, где по меньшей мере 99% ионной жидкости рециркулируют, чтобы тем самым получить рециркулированную ионную жидкость.
43. Способ по п. 42, где рециркулированная ионная жидкость содержит глюкозу или целлобиозу.
| Xinhua Qi et al., Cellulose, 2011, vol.18, 1327-1333 | |||
| Xinhua Qi et al., Cellulose, 2011, vol.18, 1327-1333 | |||
| Pan Wang et al., Bioresource Technology, 2011, 102, 4179-4183 | |||
| Yu Su et al., Applied Catalysis A: General, 2009, 361, 117-122 | |||
| WO 2008157617 A1, 24.12.2008 | |||
| Atsushi Takagaki et al., Chemical communicatios, 2009, N41, 2009, 6276-6278 |
Авторы
Даты
2020-06-01—Публикация
2015-12-11—Подача