Изобретение относится к медицине.
Известны средства, которые применяют в лечении хронического атрофического гастрита (ХАГ), а именно:
1. Плантаглюцид - препарат растительного происхождения, полученный из подорожника большого. Обладает противовоспалительным (Hussan F, Mansor AS, Hassan SN, Tengku Nor Effendy Kamaruddin TN, Budin SB, Othman F. Anti-Inflammatory Property of Plantago major Leaf Extract Reduces the Inflammatory Reaction in Experimental Acetaminophen-Induced Liver Injury // Evid Based Complement Alternat Med. 2015; 2015:347861. doi: 10.1155/2015/347861;  , Erten R.,
, Erten R.,  , Cengiz N., Yilmaz O. Hepatoprotective and anti-inflammatory activities of Plantago major L. Indian Journal of Pharmacology. 2009; 41(3): 120-124. doi: 10.4103/0253-7613.55211), спазмолитическим, обволакивающим действием, способствует регенерации тканей и активирует желудочную секрецию (Samuelsen А.В. The traditional uses, chemical constituents and biological activities of Plantago major. Journal of Ethnopharmacology. 2000;71(1-2):1-21. doi: 10.1016/s0378-8741(00)00212-9; Zubair M., Nybom H., Lindholm C, Rumpunen K. Major polyphenols in aerial organs of greater plantain (Plantago major L.), and effects of drying temperature on polyphenol contents in the leaves. Scientia Horticulturae. 2011; 128(4):523-529. doi:10.1016/ j. scienta. 2011.03.00).
, Cengiz N., Yilmaz O. Hepatoprotective and anti-inflammatory activities of Plantago major L. Indian Journal of Pharmacology. 2009; 41(3): 120-124. doi: 10.4103/0253-7613.55211), спазмолитическим, обволакивающим действием, способствует регенерации тканей и активирует желудочную секрецию (Samuelsen А.В. The traditional uses, chemical constituents and biological activities of Plantago major. Journal of Ethnopharmacology. 2000;71(1-2):1-21. doi: 10.1016/s0378-8741(00)00212-9; Zubair M., Nybom H., Lindholm C, Rumpunen K. Major polyphenols in aerial organs of greater plantain (Plantago major L.), and effects of drying temperature on polyphenol contents in the leaves. Scientia Horticulturae. 2011; 128(4):523-529. doi:10.1016/ j. scienta. 2011.03.00).
Однако, имеются сведения о его недостаточном противовоспалительном эффекте, и, кроме того, несмотря на улучшение клинической симптоматики болезни, гистологически, наоборот, отмечается усиление воспалительного процесса (Khalifeh MS, Hananeh W, Al-Rukibat R, Okour О, Boumezrag A. Clinical and histopathological evaluation of MDP/collagen induced arthritis rat model (MCIA) after treatment with Urtica dioica, plantago major and Hypericum perforatum L herbal mixture // Exp Anim. 2008 Apr; 57(2):101-10).
2. Солкосерил - репарант животного происхождения. Он улучшает транспорт кислорода и глюкозы к клеткам, находящимся в условиях гипоксии, повышает синтез внутриклеточного АТФ и способствует увеличению дозы аэробного гликолиза и окислительного фосфорилирования, активизирует репаративные и регенеративные процессы в тканях, стимулирует пролиферацию фибробластов и синтез коллагена стенки сосудов (https://health.mail.ru/drug/solcoseryl_1/).
Однако противовоспалительное действие солкосерила незначительно (Lalabonova Н, Daskalov Н. Clinical assessment of the therapeutic effect of low-level laser therapy on chronic recurrent aphthous stomatitis // Biotechnol Biotechnol Equip. 2014 Sep 3; 28(5):929-933). Это приводит к отсутствию стойкого лечебного эффекта.
3. Рибоксин (инозин) - относится к группе лекарственных средств, регулирующих метаболические процессы (https://health.mail.ru/drug/riboxin/). Препарат является предшественником для синтеза пуриновых нуклеотидов: аденозинтрифосфата и гуанозинтрифосфата, которые обеспечивают антигипоксический и цитопротекторный эффект (Gallo  ,
,  Suarez AJ,
Suarez AJ,  Fernandez FP. Ultrastructural study of the kidney subjected to warm ischemia and perfused with inosine // Arch Esp Urol. 2013 Dec; 66(10):945-55; Szabo G, Stumpf N, Radovits T, Sonnenberg K, Gero D, Hagl S, Szabo C, Bahrle S. Effects of inosine on reperfusion injury after heart transplantation. Eur J Cardiothorac Surg. 2006; 30:96-102; Veres G, Radovits T, Seres L, Horkay F, Karck M, Szabo G. Effects of inosine on reperfusion injury after cardiopulmonary bypass. J Cardiothorac Surg. 2010; 5:106), что способствует восстановлению слизистой оболочки желудка (Korepanov AM, Nazarov AM, Nikitin EN, Bazhenov EL Riboxine effectiveness in combined treatment of chronic atrophic gastritis // Klin Med (Mosk). 1999; 77(9):28-30).
Fernandez FP. Ultrastructural study of the kidney subjected to warm ischemia and perfused with inosine // Arch Esp Urol. 2013 Dec; 66(10):945-55; Szabo G, Stumpf N, Radovits T, Sonnenberg K, Gero D, Hagl S, Szabo C, Bahrle S. Effects of inosine on reperfusion injury after heart transplantation. Eur J Cardiothorac Surg. 2006; 30:96-102; Veres G, Radovits T, Seres L, Horkay F, Karck M, Szabo G. Effects of inosine on reperfusion injury after cardiopulmonary bypass. J Cardiothorac Surg. 2010; 5:106), что способствует восстановлению слизистой оболочки желудка (Korepanov AM, Nazarov AM, Nikitin EN, Bazhenov EL Riboxine effectiveness in combined treatment of chronic atrophic gastritis // Klin Med (Mosk). 1999; 77(9):28-30).
Однако, несмотря на то, что рибоксин ослабляет выработку медиаторов воспаления ( , Kuhel DG, Nemeth ZH, Mabley JG, Stachlewitz RF,
, Kuhel DG, Nemeth ZH, Mabley JG, Stachlewitz RF,  , Lohinai Z, Southan GJ, Salzman AL,
, Lohinai Z, Southan GJ, Salzman AL,  . Inosine inhibits inflammatory cytokine production by a posttranscriptional mechanism and protects against endotoxin-induced shock // J Immunol. 2000 Jan 15; 164(2):1013-9;
. Inosine inhibits inflammatory cytokine production by a posttranscriptional mechanism and protects against endotoxin-induced shock // J Immunol. 2000 Jan 15; 164(2):1013-9;  , Sitkovsky MV,
, Sitkovsky MV,  Trends Pharmacol Sci. Immunomodulatory and neuroprotective effects of inosine // 2004 Mar; 25(3):152-157), этот препарат не обеспечивает достаточный противовоспалительный эффект (патент РФ №2662077 «Средство для лечения хронического атрофического гастрита»).
Trends Pharmacol Sci. Immunomodulatory and neuroprotective effects of inosine // 2004 Mar; 25(3):152-157), этот препарат не обеспечивает достаточный противовоспалительный эффект (патент РФ №2662077 «Средство для лечения хронического атрофического гастрита»).
4. А-фетопротеин (α-фетопротеин, АФП) предложен для ликвидации признаков ХАГ (патент РФ №2662077 «Средство для лечения хронического атрофического гастрита»), а именно: значительного уменьшения дилятации венозных сосудов, нормализации состояния сосудов микроциркуляторного русла, ликвидации явлений агрегации эритроцитов в сосудах, устранения отека и инфильтрации клеточными элементами собственной пластинки слизистой желудка (преимущественно за счет уменьшения количества нейтрофилов и лимфоцитов); восстановления слизистой оболочки желудка (наблюдается увеличение размеров желез и уменьшение расстояния между ними, снижение выраженности признаков склеротических изменений, приобретение эпителием желез более высокоспециализированного строения, обусловленного восстановлением пула клеток, вырабатывающих желудочный сок и соляную кислоту в фундальном отделе, и ликвидацией очагов кишечной метаплазии в пилорическом отделе) (прототип).
Несмотря на выраженный терапевтический эффект от применения АФП, использованная форма лекарственного средства (водно-масляная эмульсия) не позволила в полной мере восстановить слизистую оболочку желудка в наиболее подверженном патологическим изменениям пилорическом отделе даже после применения препарата в течение 4 недель.
В этой связи поиск наиболее оптимальной формы лекарственного средства, позволяющей достичь новых результатов лечения хронического атрофического гастрита, представляет несомненную актуальность.
Известна липосома, содержащая рекомбинантный человеческий АФП, которая может содержать также рекомбинантный человеческий гранулоцитарный колониестимулирующий фактор (патент РФ №2642957).
Данная липосома предназначена для лечения местных радиационных поражений кожи. Содержащее ее лекарственное средство может применяться подкожно или трансдермально.
Раскрытие изобретения
Для лечения хронического атрофического гастрита (ХАГ) предлагается липосомальная (липосомная) форма α-фетопротеина (АФП), предназначенная для энтерального применения (введения).
Липосомальная форма АФП представляет собой водную суспензию липосом или лиофилизат.
Лиофилизат содержит АФП, липоид С-100, холестерин, лактозу, реополиглюкин, альфа-токоферол (витамин Е), натрия хлорид, натрий фосфорнокислый двузамещенный 12-водный, натрий фосфорнокислый однозамещенный 2-водный в следующем весовом соотношении компонентов:
АФП 0,040-0,160;
липоид С-100 - 41,6-43,8;
холестерин - 4,0-5,3;
альфа-токоферол (витамин Е) - 0,48-0,8;
лактоза - 70-120;
реополиглюкин - 4,0-6,0;
натрия хлорид - 7,0-9,0;
натрий фосфорнокислый двузамещенный 12-водный - 4,3-4,9;
натрий фосфорнокислый однозамещенный 2-водный - 0,5-0,7.
Водная суспензия липосом содержит АФП, липоид С-100, холестерин, лактозу, реополиглюкин, альфа-токоферол (витамин Е), натрия хлорид, натрий фосфорнокислый двузамещенный 12-водный, натрий фосфорнокислый однозамещенный 2-водный и воду в следующем весовом соотношении компонентов:
АФП 0,040-0,160;
липоид С-100 - 41,6 - 43,8;
холестерин - 4,0-5,3;
альфа-токоферол (витамин Е) - 0,48-0,8;
лактоза - 70-120;
реополиглюкин - 4,0-6,0;
натрия хлорид - 7,0-9,0;
натрий фосфорнокислый двузамещенный 12-водный - 4,3-4,9;
натрий фосфорнокислый однозамещенный 2-водный - 0,5-0,7.
вода - 800-1300.
Средний диаметр липосом составляет 0,18 мкм.
АФП выделен из пуповинной крови человека.
Техническими результатами предлагаемого изобретения являются следующие:
1) предлагаемое средство более полно восстанавливает слизистую оболочку фундального отдела желудка за 2 недели лечения, чем прототип (водно-масляная эмульсия АФП по патенту РФ №2662077) за 4 недели лечения;
2) через 2 недели лечения предлагаемым средством ликвидируются проявления хронического воспалительного процесса в фундальном отделе желудка, через 4 недели лечения - в нем полностью отсутствует воспалительная инфильтрация;
3) при лечении предлагаемым средством в пилорическом отделе желудка за 2 недели лечения достигается та же стадия ХАГ, которая при лечении прототипом достигается за 4 недели;
4) предлагаемое средство обеспечивает в пилорическом отделе за 2 недели лечения достижение той же степени ХАГ, которая при лечении прототипом достигается за 4 недели лечения: воспалительный процесс через 2 недели лечения предлагаемым средством в пилорическом отделе менее выражен, чем при лечении по прототипу в течение 4 недель;
5) лечение предлагаемым средством в течение 4-х недель позволяет восстановить слизистую оболочку в наиболее подверженном патологическим изменениям пилорическом отделе, что не достигается в тот же срок с помощью прототипа;
6) по сравнению с аналогами заявляемое средство обладает выраженным противовоспалительным эффектом;
7) указанные выше свойства предлагаемого средства сокращать срок лечения позволяют избежать или уменьшить вероятность возникновения побочных эффектов лечения, могущих возникнуть в связи с тем, что при длительном применении АФП повышается функциональная (пролиферативная и цитотоксическая) активность мононуклеарных лейкоцитов, что может проявиться в обострении имеющихся в организме хронических инфекционно-воспалительных заболеваний.
Наличие в липосомальной мембране холестерина и витамина Е в заявленных соотношениях обеспечивают относительную стабильность липосом в желудочно-кишечном тракте (до момента всасывания липидов в тонком кишечнике), и, соответственно, сохранение биологической активности АФП, заключенного в них.
Витамин Е в заявленном соотношении обеспечивает достаточное антиокислительное и стабилизирующее действие для сохранения биологической активности АФП в процессе получения липосом.
Лактоза и реополиглюкин в заявленном соотношении обеспечивают стабильность липосом в процессе лиофилизации.
Буферно-солевая основа в заявленном соотношении обеспечивает стабильность раствора АФП в процессе приготовления липосомального препарата.
Перечень фигур иллюстративного материала
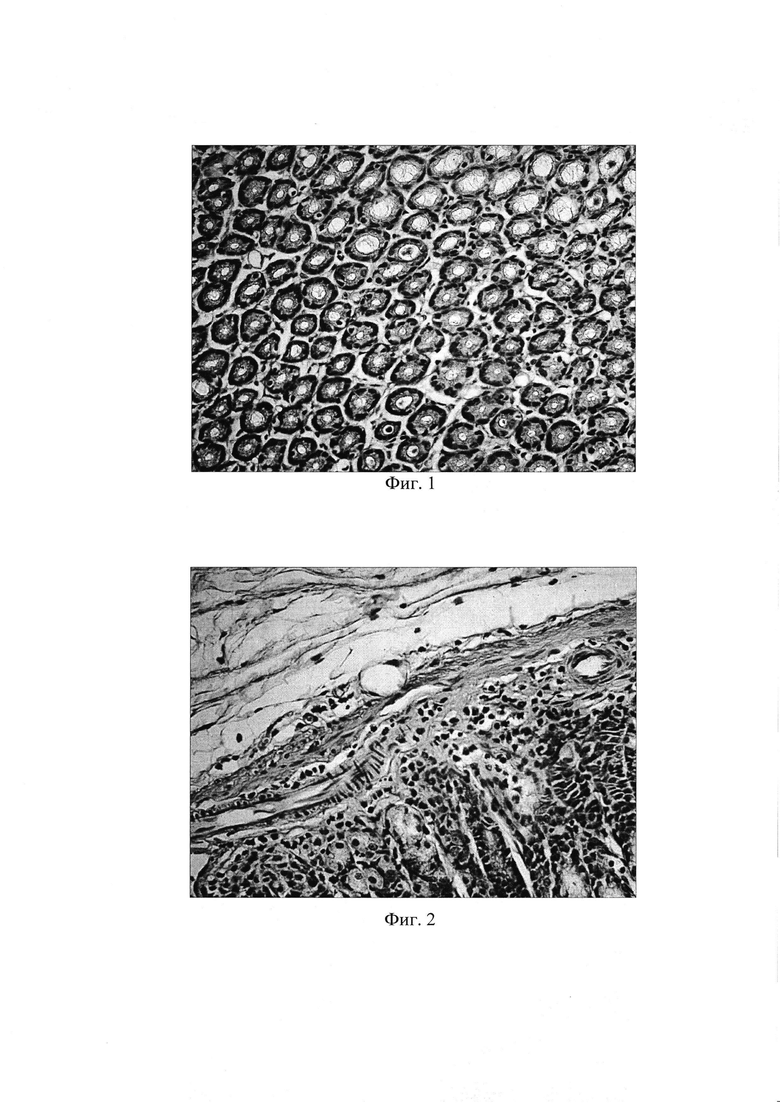
Фиг. 1. Слизистая фундального отдела желудка через 8 недель после начала введения салицилата натрия на фоне содержания животных на альтернативном посту: развитие склеротических изменений. Окр. гематоксилином и эозином, ув. 400.
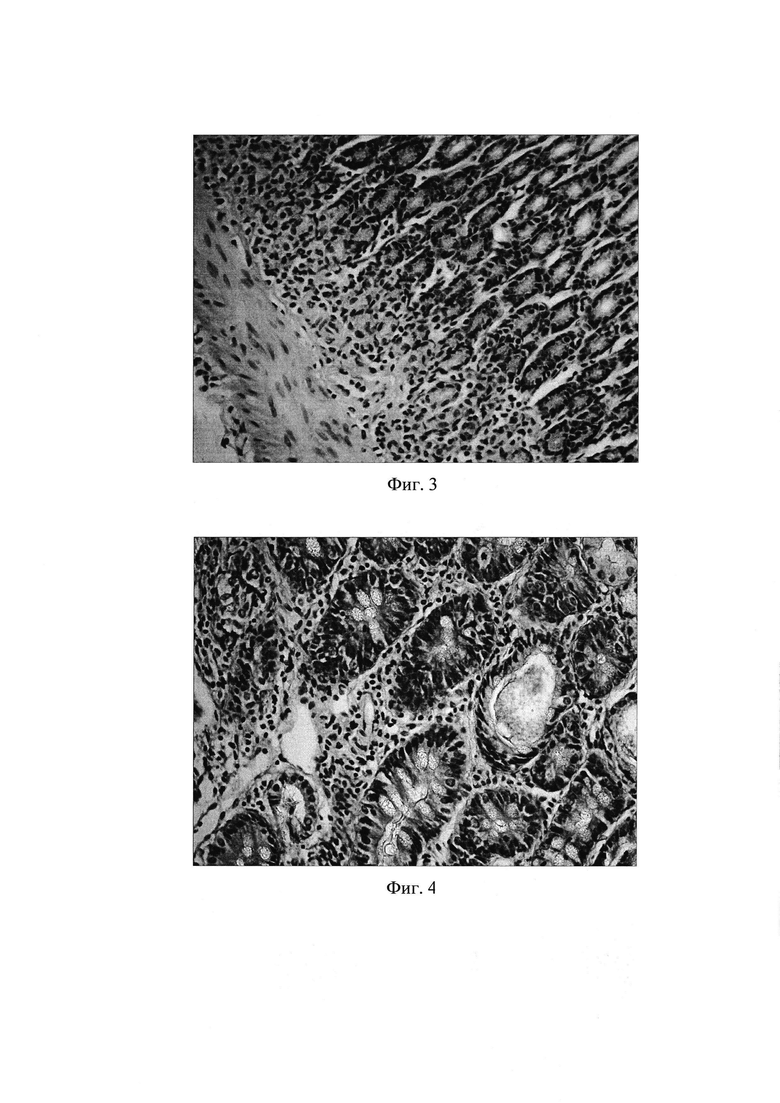
Фиг. 2. Слизистая фундального отдела желудка через 8 недель после начала введения салицилата натрия на фоне содержания животных на альтернативном посту: инфильтрация слизистой желудка как нейтрофильно-лейкоцитарными, так и макрофагальными элементами. Окр. гематоксилином и эозином, ув. 400.
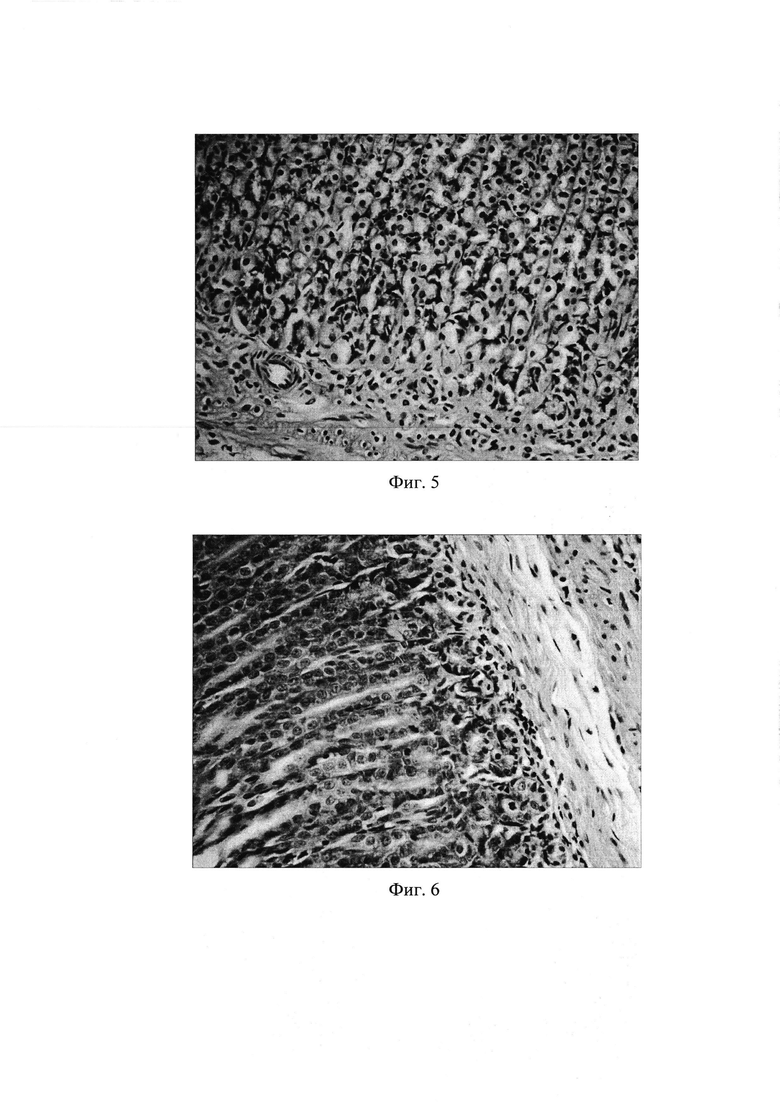
Фиг. 3. Слизистая пилорического отдела желудка через 8 недель после начала введения салицилата натрия на фоне содержания животных на альтернативном посту: инфильтрация слизистой желудка как нейтрофильно-лейкоцитарными, так и макрофагальными элементами. Окр. гематоксилином и эозином, ув. 400.
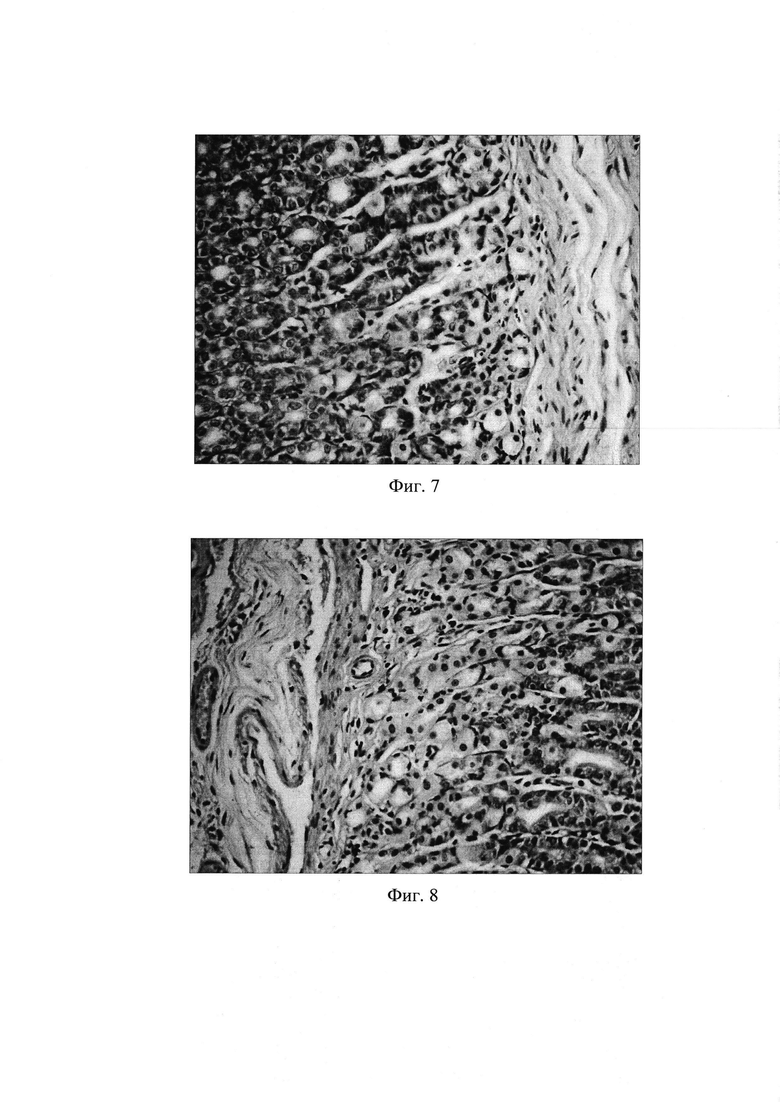
Фиг. 4. Слизистая пилорического отдела желудка через 8 недель после начала введения салицилата натрия на фоне содержания животных на альтернативном посту: наличие очагов кишечной метаплазии с бокаловидными клетками. Окр. гематоксилином и эозином, ув. 400.
Фиг. 5. Слизистая фундального отдела желудка через 2 недели введения водно-масляной эмульсии α-фетопротеина у животных с воспроизведенным ХАГ: снижение инфильтрации собственной пластинки нейтрофильно-лейкоцитарными и макрофагальными элементами. Окр. гематоксилином и эозином, ув. 400.
Фиг. 6. Слизистая пилорического отдела желудка через 2 недели введения водно-масляной эмульсии α-фетопротеина у животных с воспроизведенным ХАГ: снижение инфильтрации собственной пластинки нейтрофильно-лейкоцитарными и макрофагальными элементами, отсутствие признаков кишечной метаплазии, увеличение размеров желез, уменьшение расстояния между ними, приобретение эпителием желез более высокоспециализированного строения. Окр. гематоксилином и эозином, ув. 400.
Фиг. 7. Слизистая фундального отдела желудка через 4 недели введения водно-масляной эмульсии α-фетопротеина у животных с воспроизведенным ХАГ: отсутствие инфильтрации собственной пластинки нейтрофильно-лейкоцитарными и макрофагальными элементами, восстановление эпителием желез своего высокоспециализированного строения. Окр. гематоксилином и эозином, ув. 400.
Фиг. 8. Слизистая пилорического отдела желудка через 4 недели введения водно-масляной эмульсии α-фетопротеина у животных с воспроизведенным ХАГ: отсутствие инфильтрации собственной пластинки нейтрофильно-лейкоцитарными и макрофагальными элементами, ликвидация признаков атрофии слизистой. Окр. гематоксилином и эозином, ув. 400.
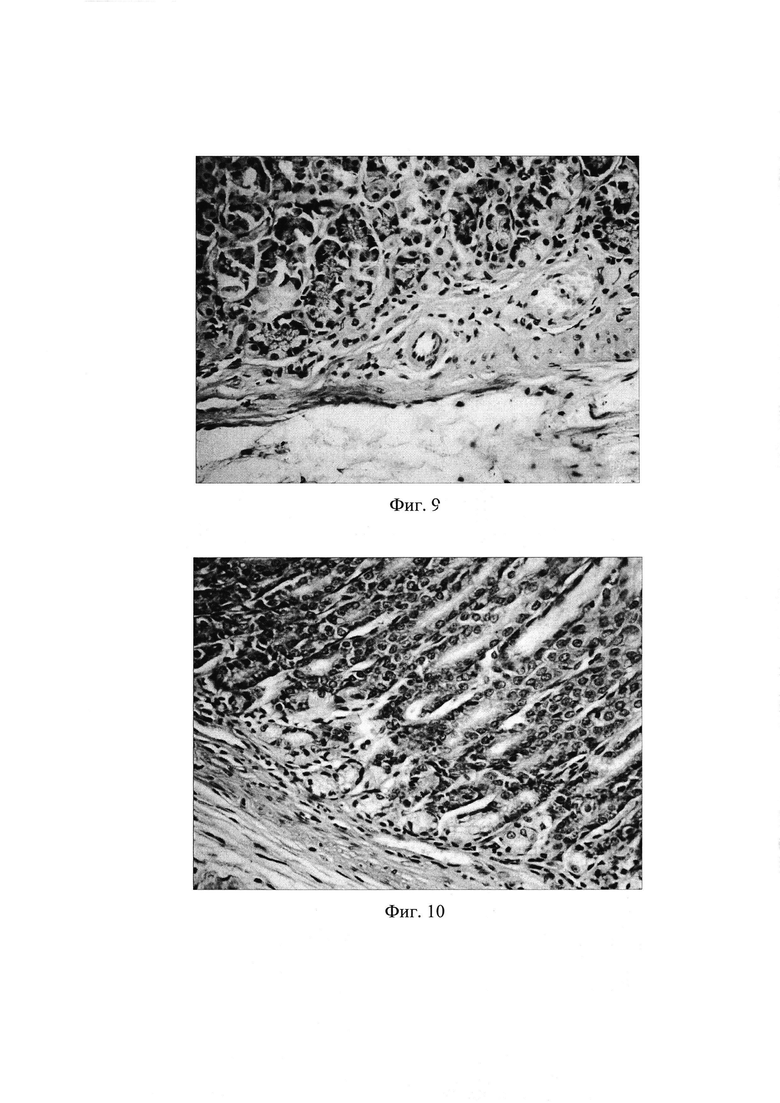
Фиг. 9. Слизистая фундального отдела желудка через 2 недели введения липосомальной формы α-фетопротеина у животных с воспроизведенным ХАГ: отсутствие инфильтрации собственной пластинки нейтрофильно-лейкоцитарными и макрофагальными элементами, полное восстановление эпителием желез своего высокоспециализированного строения. Окр. гематоксилином и эозином, ув. 400.
Фиг. 10. Слизистая пилорического отдела желудка через 2 недели введения липосомальной формы α-фетопротеина у животных с воспроизведенным ХАГ: отсутствие инфильтрации собственной пластинки нейтрофильно-лейкоцитарными и макрофагальными элементами, значительное восстановление эпителием желез своего высокоспециализированного строения. Окр. гематоксилином и эозином, ув. 400.
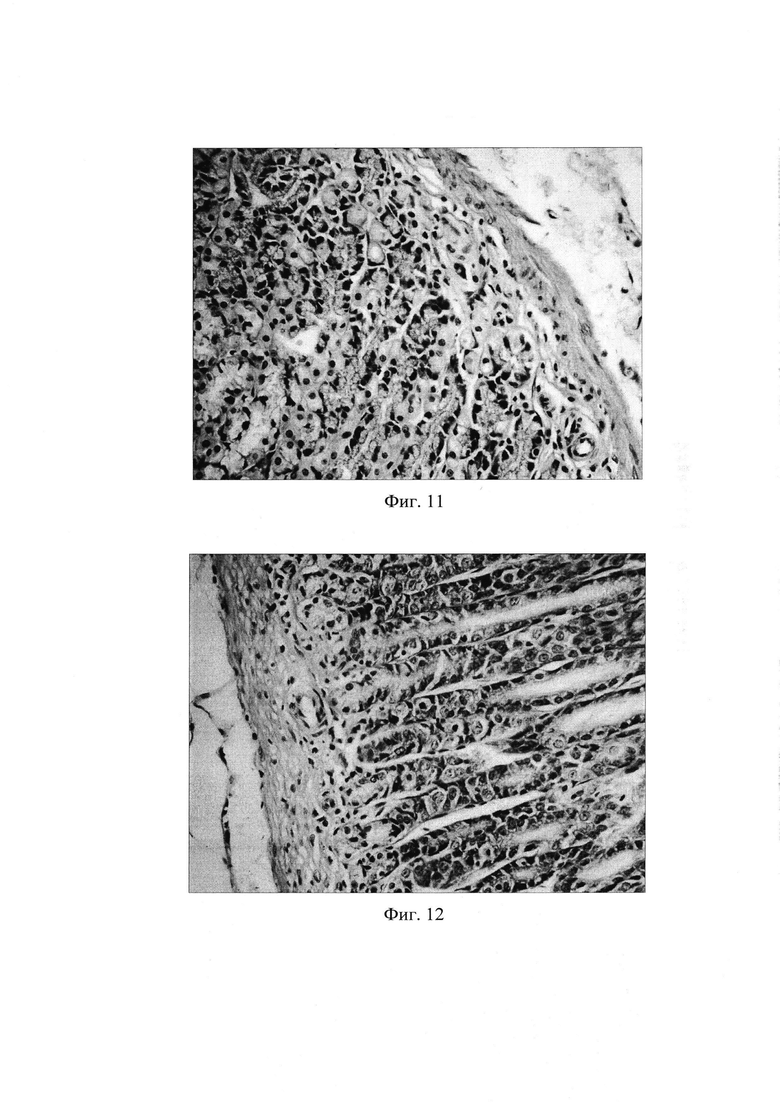
Фиг. 11. Слизистая фундального отдела желудка через 4 недели введения липосомальной формы α-фетопротеина у животных с воспроизведенным ХАГ: отсутствие инфильтрации собственной пластинки нейтрофильно-лейкоцитарными и макрофагальными элементами, полное восстановление эпителием желез своего высокоспециализированного строения. Окр. гематоксилином и эозином, ув. 400.
Фиг. 12. Слизистая пилорического отдела желудка через 4 недели введения липосомальной формы α-фетопротеина у животных с воспроизведенным ХАГ: отсутствие инфильтрации собственной пластинки нейтрофильно-лейкоцитарными и макрофагальными элементами, полное восстановление эпителием желез своего высокоспециализированного строения. Окр. гематоксилином и эозином, ув. 400.
Липосомы заявленного состава получают модифицированным методом экструзии мультиламеллярных везикул через поликарбонатные мембраны с размером пор 0,1 и 0, 2 мкм.
Краткая схема:
Получение липидной пленки (липоид, холестерин, витамин Е), эмульгирование в буферном растворе, экструзия с использованием фильтров с порами 0,2-0,1 микрона, формирование липосомально-белкового комплекса, лиофилизация во флаконах из объема 1 мл.
Пример получения заявленного липосомального средства
В круглодонную колбу (V=10 л), содержащую 200 мл этанола, вносят 8,48 г липоида С 100, растворяют при перемешивании, добавляют 0,94 г холестерина, растворенного в 20 мл смеси хлороформа с этанолом в объемном соотношении 1:2, перемешивают, добавляют 0,12 г альфа-токоферола и выпаривают под вакуумом до получения сухой липидной пленки на стенках колбы. После выпаривания продувают липидную пленку инертным газом для предотвращения окисления липидов. Добавляют в колбу раствор субстанции, содержащий 16 мг АФП человека, и содержащий кроме нее следующие компоненты:
Содержимое колбы перемешивают до полной гидратации липидной пленки в течение 30 мин при комнатной температуре. Полученную липосомальную суспензию подвергают под давлением инертного газа (аргон) формирующей и стерилизующей фильтрации через поликарбонатные мембранные фильтры (фирмы "Nuclepore") - вначале через фильтр с диаметром пор 0,2 мкм, затем - с диаметром пор 0,1 мкм. В асептических условиях разливают по 1 мл суспензии во флаконы, замораживают при -40°С и проводят лиофильную сушку препарата до достижения остаточной влажности (7±1) мас. %. Сразу после сушки флаконы с препаратом герметично укупоривают в атмосфере инертного газа в асептических условиях.
Для восстановления к лиофильно высушенному препарату добавляют 1,0 мл воды, флакон встряхивают до получения однородной водной суспензии.
Средний диаметр липосом, полученных методом экструзии мультиламеллярных везикул через поликарбонатные мембранные фильтры и имеющих заявляемый состав, составляет 0,18 мкм.
Описание и происхождение ингредиентов препарата
Биологически активная субстанция - АФП человека из пуповинной крови, электрофоретическая чистота не менее 92%, получен по методу, включающему иммуноаффинное фракционирование и гель-хроматографию (патент РФ №2123009, ФСП 42-0244098601).
Содержание белка в препарате: 80 мкг/мл, в том числе в составе липидно-белкового комплекса - не менее 70%.
Липоид С 100 (Lipoid С100) - фирма Lipoid GmbH (Германия, РУ №15370/01).
Холестерин - фирма MP Biochemicals, кат. №0210138280.
Витамин Е (альфа-токоферол) - фирма MP Biochemicals, кат. №0210056280.
Лактоза (Лактоза Фарма 200/15) - фирма ALPAVIT (Германия).
Реополиглюкин - Россия, peг. №: ЛСР-005290/10.
Натрия хлорид - Россия, «хч».
Натрий фосфорнокислый двузамещенный 12-водный - Россия, «хч».
Натрий фосфорнокислый однозамещенный 2-водный - Россия, «хч».
Обоснование изобретения
Было проведено сравнительное исследование терапевтического эффекта при ХАГ водно-масляной эмульсии (прототип) и липосомальной формы АФП, выделенного из пуповинной крови.
Материал и методы исследования
Эксперимент проведен на 36 половозрелых крысах-самцах Wistar с исходной массой тела 180-220 г. Для получения модели ХАГ 30-ти экспериментальным животным ежедневно один раз в день в течение 8 недель внутрижелудочно вводили 0,2 мл 2%-го раствора салицилата натрия в 30% растворе спирта, кроме того крысы содержались на альтернативном посту (2 дня - кормление, 1 сутки - отсутствие кормления) со свободным доступом к воде (далее - животные с воспроизведенным ХАГ) (Shao ХН, Yang YP, Dai J, Wu JF, Bo AH. Effects of He-Ne laser irradiation on chronic atrophic gastritis in rats World J Gastroenterol. 2005 Jul 7; 11(25):3958-61).
36 животных были поделены на 6 групп по 6 животных в каждой группе.
Группа 1 - интактные животные («Инт»).
Группа 2 («ХАГ 8», где цифра «8» обозначает 8 недель внутрижелудочного введения 0,2 мл 2%-го раствора салицилата натрия в 30% растворе спирта и содержания на альтернативном посту (2 дня - кормление, 1 сутки - отсутствие кормления) со свободным доступом к воде - животные с воспроизведенным ХАГ.
Группа 3 («ХАГ 8 + вмАФП 2», где «вмАФП 2» означает 2 недели введения водно-масляной эмульсии АФП) - животные с воспроизведенным ХАГ, которым в течение последующих двух недель ежедневно вводили энтерально водно-масляную эмульсию α-фетопротеина с содержанием АФП в дозе 15 мкг/кг. Животные выводились из эксперимента через 10 недель от его начала.
Группа 4 («ХАГ 8 + вмАФП 4», где «вмАФП 4» означает 4 недели введения водно-масляной эмульсии АФП) - животные с воспроизведенным ХАГ, которым в течение последующих четырех недель ежедневно вводили энтерально водно-масляную эмульсию α-фетопротеина с содержанием АФП в дозе 15 мкг/кг. Животные выводились из эксперимента через 12 недель от его начала.
Группа 5 («ХАГ 8 + лАФП 2», где «лАФП 2» означает 2 недели введения липосомальной формы АФП) - животные с воспроизведенным ХАГ, которым в течение последующих двух недель ежедневно вводили энтерально водную суспензию лиофилизата липосомальной формы а-фетопротеина с содержанием АФП в дозе 15 мкг/кг. Животные выводились из эксперимента через 10 недель от его начала.
Группа 6 («ХАГ 8 + лАФП 4», где «лАФП 4» означает 4 недели введения липосомальной формы АФП) - животные с воспроизведенным ХАГ, которым в течение последующих четырех недель ежедневно вводили энтерально водную суспензию лиофилизата липосомальной формы α-фетопротеина с содержанием АФП в дозе 15 мкг/кг. Животные выводились из эксперимента через 12 недель от его начала.
Липосомальное средство может быть введено энтерально не только в форме водной суспензии, но и в виде лиофилизата.
Желудок животных фиксировали в 12% формалине. Из залитых в парафин объектов делали серийные срезы толщиной 7 мкм. Морфология слизистой желудка оценивалась при обзорной микроскопии после окраски срезов гематоксилином Эрлиха и эозином. Муцин выявляли муцикармином с последующей докраской ядер гематоксилином Эрлиха. Кислые муцины выявляли альциановым синим при рН 1,0 с последующей докраской ядер кармалюмом Майера.
Оценивались основные признаки ХАГ, предложенные Сиднейской системой классификации хронического гастрита (Genta RM, Dixon MF. The Sydney system revised. Am J Gastroenterol 1995; 90:1039-41; Филипенко П.С, Великородный Г.Г. Морфологическая классификация хронического гастрита (Адаптированный вариант) // Успехи современного естествознания. - 2009. - №7. - С. 107-109), а именно: выраженность атрофии желудочных желез, которая определяет стадию хронического гастрита; лимфоплазмоцитарная и нейтрофильная инфильтрация, которые определяют степень хронического гастрита; а также признаки, не входящие в вышеуказанную классификацию, но отмечающиеся при ХАГ: содержание муцина и кислых муцинов (Mandal РK, Chakrabarti S, Ray A, Chattopadhyay В, Das S Mucin histochemistry of stomach in metaplasia and adenocarcinoma: An observation Indian J Med Paediatr Oncol. 2013 Oct; 34(4):229-33. doi: 10.4103/0971-5851.125232).
Определение относительной площади, занимаемой железами желудка, а также клеточными элементами инфильтратов, проводилось с помощью морфометрического комплекса на базе микроскопа Micros МС 300А, цифровой камеры СХ 13с («Ваumer Electric GmbH», Германия) и программного обеспечения ImageJ 1.42g (Национальный институт здоровья, США). Для каждой группы оценивалось по 48 изображений.
Статистическую обработку результатов исследования проводили с использованием программного пакета для статистической обработки SPSS v 17.0 for Windows. Для сравнения независимых групп использовали критерий Крускала-Уоллиса с последующим межгрупповым сравнением с помощью критерия Манна-Уитни. Различия между значениями сравниваемых параметров расценивали как статистически значимые при р<0,05. Полученные в ходе исследования данные представлены как медиана (Me) и интерквартильный размах (Q1; Q3).
Результаты исследования
Модель ХАГ (группа «ХАГ 8»)
При морфологическом исследовании срезов фундального и пилорического отделов желудка через 8 недель от начала введения салицилата натрия на фоне содержания животных на альтернативном посту (группа «ХАГ 8») был отмечен ряд признаков, характерных для ХАГ.
Фундальный отдел желудка
Наблюдалось:
1) истончение слизистой оболочки желудка, обусловленное атрофией желез с увеличением расстояния между ними, что подтверждалось достоверным уменьшением относительной площади желез и развитием склеротических изменений (фиг. 1);
2) значительное уменьшение количества главных, обкладочных и эндокринных клеток при увеличении количества мукоцитов, секретирующих слизь, при этом значительно возросла выработка кислых муцинов (сиаломуцина и сульфомуцина);
3) выраженная дилятация вен и микроциркуляторных сосудов с агрегацией эритроцитов в них, отмечались явления отека;
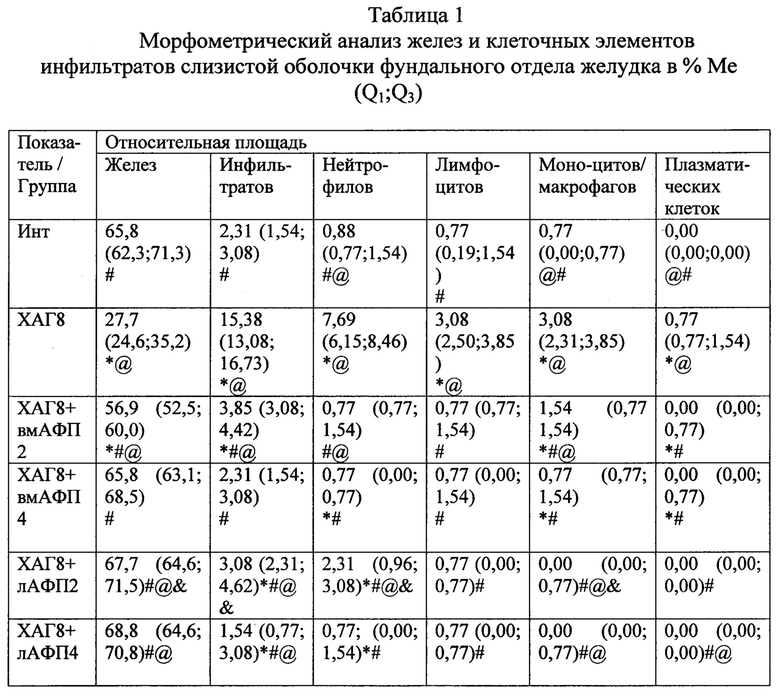
4) выраженная инфильтрация слизистой желудка как нейтрофильно-лейкоцитарными, так и макрофагальными элементами (фиг. 2), при этом выраженность вышеуказанной инфильтрации достоверно возросла по сравнению с интактными животными в 6,7 раза (таблица 1), соотношение клеточных элементов (нейтрофилы, лимфоциты, моноциты/макрофаги, плазматические клетки), образующих инфильтраты, составило 2,5:1:1:0.
Пилорический отдел желудка
В пилорическом отделе желудка было отмечено:
1) истончение слизистой оболочки желудка, обусловленное атрофией желез с увеличением расстояния между ними, что подтверждалось достоверным уменьшением относительной площади желез и развитием склеротических изменений;
2) значительное уменьшение количества эндокринных и обкладочных клеток при выраженном увеличении количества мукоцитов, секретирующих в основном кислые муцины (сиаломуцин и сульфомуцин);
3) выраженная дилятация вен и микроциркуляторных сосудов с агрегацией эритроцитов в них, отмечались явления отека;
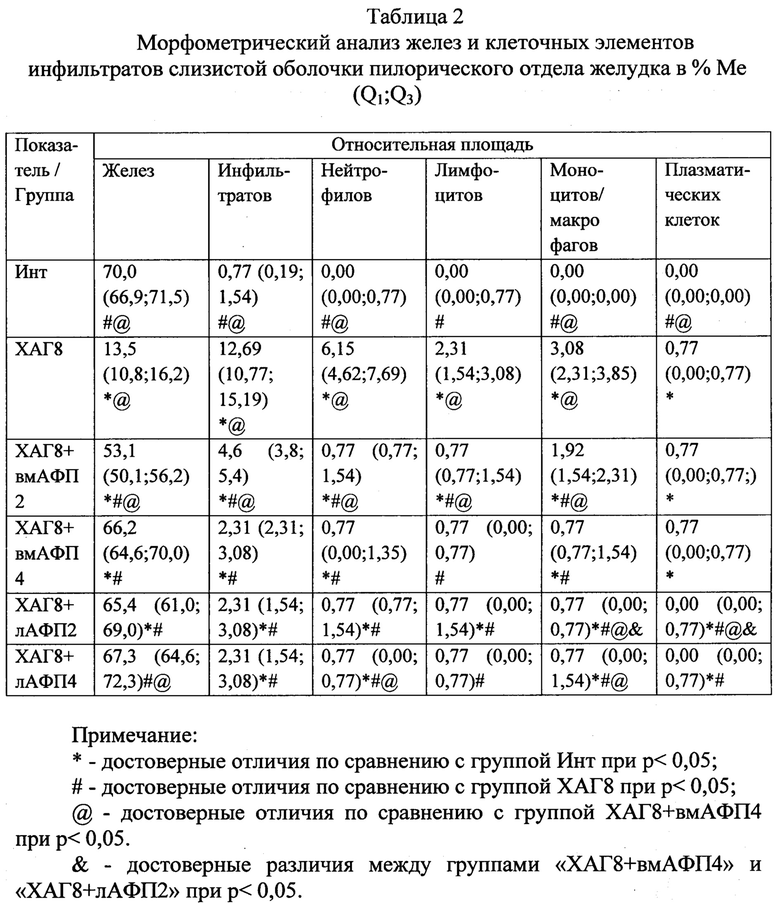
4) выраженная инфильтрация слизистой желудка как нейтрофильно-лейкоцитарными, так и макрофагальными элементами (фиг. 3), при этом выраженность вышеуказанной инфильтрации достоверно возросла по сравнению с интактными животными в 16,5 раз (таблица 2), соотношение клеточных элементов (нейтрофилы, лимфоциты, моноциты/макрофаги, плазматические клетки), образующих инфильтраты, составило 2,7:1:1,3:0,3;
5) наличие очагов кишечной метаплазии с бокаловидными клетками (фиг. 4).
Лечение ХАГ с помощью водно-масляной эмульсии АФП в течение 2-х недель (группа «ХАГ 8 + вмАФП 2»)
Фундалъный отдел
В фундальном отделе желудка отмечались:
1) признаки восстановления слизистой оболочки желудка, что характеризовалось увеличением относительной площади желез по сравнению с группой «ХАГ 8» в 2 раза и уменьшением расстояния между ними, а также некоторым снижением склеротических изменений;
2) эпителий желез приобрел более высокоспециализированное строение, что было обусловлено некоторым восстановлением пула клеток, вырабатывающих желудочный сок и соляную кислоту, и уменьшением количества клеток, секретирующих кислые муцины;
3) уменьшение дилятации вен и микроциркуляторных сосудов, отсутствовала агрегация эритроцитов в них, значительно уменьшились явления отека;
4) выраженность инфильтрации по сравнению с группой «ХАГ 8» снизилась в 4 раза (таблица 1, фиг. 5), преимущественно за счет уменьшения количества нейтрофилов и лимфоцитов. Соотношение клеточных элементов (нейтрофилы, лимфоциты, моноциты/макрофаги, плазматические клетки), образующих инфильтраты, составило 1:1:2:0, при этом относительная площадь нейтрофилов и лимфоцитов не отличалась от соответствующих показателей у интактных животных (группа «Инт»).
Пилорический отдел
В пилорическом отделе желудка отмечались:
1) признаки восстановления слизистой оболочки желудка, что характеризовалось увеличением относительной площади желез почти в 4 раза по сравнению с группой «ХАГ 8» и уменьшением расстояния между ними, а также некоторым снижением склеротических изменений;
2) эпителий желез приобрел более высокоспециализированное строение, что было обусловлено некоторым восстановлением пула обкладочных и эндокринных клеток и уменьшением количества клеток, секретирующих кислые муцины;
3) уменьшение дилятации вен и микроциркуляторных сосудов, отсутствовала агрегация эритроцитов в них, значительно уменьшились явления отека;
4) выраженность инфильтрации по сравнению с группой «ХАГ 8» снизилась в 2,8 раза (таблица 2, фиг. 6), преимущественно за счет уменьшения количества нейтрофилов и лимфоцитов, соотношение клеточных элементов (нейтрофилы, лимфоциты, моноциты/макрофаги, плазматические клетки), образующих инфильтраты, составило 1:1: 2,5:1;
5) отсутствовали очаги кишечной метаплазии.
Таким образом, применение водно-масляной эмульсии АФП в течение 2-х недель привело к уменьшению признаков ХАГ как в фундальном, так и в пилорическом отделах, а также к исчезновению кишечной метаплазии в пилорическом отделе желудка. Однако полностью ни восстановление слизистой оболочки, ни ликвидация признаков воспалительного компонента ХАГ не произошли.
Лечение ХАГ с помощью водно-масляной эмульсии АФП в течение 4-х недель (группа «ХАГ 8 + вмАФП 4»)
При морфологическом исследовани и препаратов желудка через 4 недели после начала применения водно-масляной эмульсии АФП (группа «ХАГ 8 + вмАФП 4») отмечалось дальнейшее уменьшение признаков ХАГ.
Фундальный отдел:
1) полностью восстановилась слизистая оболочка, о чем свидетельствовало отсутствие достоверных различий относительной площади желез от аналогичного показателя у интактных животных;
2) эпителий желез восстановил свое высокоспециализированное строение, что подтверждалось значительным восстановлением пула клеток, вырабатывающих желудочный сок и соляную кислоту, и снижением количества клеток, секретирующих кислые муцины;
3) отсутствовала дилатация вен и микроциркуляторных сосудов, отсутствовали явления отека;
4) относительная площадь иммунокомпетентных клеток (площадь инфильтратов) соответствует таковой в группе «Инт». При этом относительная площадь, занимаемая нейтрофилами, была статистически значимо ниже, чем в контрольной группе, а относительная площадь моноцитов/макрофагов - достоверно выше, при этом соотношение клеточных элементов (нейтрофилы, лимфоциты, моноциты/макрофаги, плазматические клетки) в фундальном отделе составило 1,1:1:1:0 (фиг. 7; таблица 1).
Пилорический отдел
Было отмечено:
1) дальнейшее восстановление слизистой оболочки, о чем свидетельствовало увеличение относительной площади желез, уменьшение расстояния между ними, а также снижение склеротических изменений. Однако полного восстановления до уровня интактных животных не произошло;
2) эпителий желез приобрел более высокоспециализированное строение, что было обусловлено умеренным восстановлением пула обкладочных и эндокринных клеток и уменьшением количества клеток, секретирующих кислые муцины;
3) уменьшение дилятации вен и микроциркуляторных сосудов, отсутствовала агрегация эритроцитов в них, отсутствовали явления отека;
4) выраженность инфильтрации уменьшилась в 2 раза по сравнению с группой «ХАГ 8 + вмАФП 2» (таблица 1), соотношение клеточных элементов (нейтрофилы, лимфоциты, моноциты/макрофаги, плазматические клетки), образующих инфильтраты, составило 1:1:1:1 (таблица 2, фиг. 8), при этом относительная площадь нейтрофилов, моноцитов/макрофагов и плазматических клеток была достоверно выше, чем у интактных животных;
5) отсутствовали очаги кишечной метаплазии.
Таким образом, применение водно-масляной эмульсии АФП в течение 4 недель привело в фундальном отделе желудка к полному восстановлению как относительной площади желез, так и их клеточного состава.
В пилорическом отделе отсутствовала кишечная метаплазия, но полного восстановления слизистой не произошло.
Пришли к норме показатели, отражающие содержание нейтрофилов и лимфоцитов в слизистой оболочке фундального отдела и лимфоцитов в пилорическом отделе, что свидетельствовало об уменьшении воспалительного компонента ХАГ.
Лечение ХАГ с помощью липосомальной формы АФП в течение 2-х недель (группа «ХАГ 8 + лАФП 2»)
При применении липосомальной формы АФП в течение 2 недель (группа «ХАГ 8 + лАФП 2») так же, как и в группе «ХАГ 8 + вмАФП 2», отмечалось выраженное уменьшение признаков ХАГ.
Фундалъный отдел Было отмечено:
1) полное восстановление слизистой оболочки желудка, о чем свидетельствовало отсутствие достоверных различий в относительной площади желез по сравнению с интактными животными (группа «инт»);
2) эпителий желез приобрел высокоспециализированное строение, что было обусловлено большим количеством главных, обкладочных и эндокринных клеток в данной группе по сравнению с группой «ХАГ8 + вмАФП4», что сочеталось со снижением до нормы количества клеток, секретирующих кислые муцины (сиаломуцин и сульфомуцина), наблюдавшихся при ХАГ;
3) отсутствие дилатации вен и микроциркуляторных сосудов, отсутствовали явления отека;
4) значительно снизилась по отношению к группе ХАГ8 инфильтрация клеточными элементами собственной пластинки слизистой желудка (фиг.9), которая, в отличие от группы «ХАГ8 + вмАФП 2», произошла за счет уменьшения количества лимфоцитов, макрофагов/моноцитов и плазматических клеток, что позволяет говорить о прекращении хронического воспалительного процесса. При этом относительная площадь лимфоцитов, макрофагов/моноцитов и плазматических клеток не отличалась от соответствующих показателей у интактных животных (группа «Инт»). Соотношение клеточных элементов (нейтрофилы, лимфоциты, моноциты/макрофаги, плазматические клетки) в фундальном отделе составляло 3:1:0:0.
Известно, что лимфоциты, макрофаги и нейтрофилы секретируют цитокины и ростовые факторы, регулирующие воспалительный процесс (Роль цитокинов в патогенезе злокачественных новообразований / Соснина А.В., Великая Н.В., Аутеншлюс А.И. - Новосибирск: Вектор-Бест, 2013. - 80 с.). Также известно, что для поддержания воспаления необходимо не столько количество иммунокомпетентных клеток, сколько их функциональная активность, выражающаяся в секреции про- и противовоспалительных цитокинов. Тот факт, что слизистая оболочка полностью восстановилась (относительная площадь желез и их клеточный состав соответствуют их уровню у интактных животных), несмотря на имеющее место достоверное повышение количества нейтрофилов при нормальном количестве лимфоцитов, плазматических клеток и макрофагов/моноцитов в собственной пластинке слизистой оболочки, свидетельствует о том, что данные иммунокомпетентные клетки уже утратили свой провоспалительный потенциал, и их присутствие не отражается отрицательно на состоянии слизистой оболочки.
Пилорический отдел
Были выявлены:
1) признаки восстановления слизистой оболочки желудка, что характеризовалось достоверным увеличением относительной площади желез в 4,9 раза по сравнению с группой «ХАГ8», а также выраженным снижением склеротических изменений;
2) эпителий желез приобрел более высокоспециализированное строение, что было обусловлено восстановлением пула обкладочных и эндокринных клеток и снижением до нормы количества клеток, секретирующих кислые муцины;
3) нормализация вен и микроциркуляторных сосудов, отсутствовала агрегация эритроцитов в них, отсутствовали явления отека;
4) выраженность инфильтрации по сравнению с группой «ХАГ 8» снизилась в пилорическом отделе в 5,5 раз (таблица 2, фиг. 10), преимущественно за счет уменьшения количества нейтрофилов и лимфоцитов. Соотношение клеточных элементов (нейтрофилы, лимфоциты, моноциты/макрофаги, плазматические клетки), образующих инфильтраты, составило 1:1:1:0.
Примечательным является тот факт, что относительная площадь макрофагов/моноцитов и плазматических клеток была достоверно ниже, чем в группе «ХАГ8 + вмАФП4», при достоверно одинаковой относительной площади нейтрофилов и лимфоцитов, что свидетельствует о том, что воспалительный процесс в пилорическом отделе стал менее выраженным, чем в группе с применением водно-масляной эмульсии в течение 4-х недель. Это подтверждается также тем, что относительная площадь желез в группах «ХАГ8 + вмАФП4» и «ХАГ8 + лАФП2» достоверно не отличалась, а клеточный состав в группе «ХАГ8 + лАФП2» восстановился более полно;
5) отсутствовали очаги кишечной метаплазии.
Таким образом, применение липосомальной формы АФП в течение 2-х недель привело к полному восстановлению как относительной площади желез фундального отдела желудка, так и их клеточного состава. В пилорическом отделе отсутствовала кишечная метаплазия, но полного восстановления слизистой не произошло.
Значительно уменьшились признаки воспалительного компонента ХАГ в фундальном отделе.
Лечение ХАГ с помощью липосомальной формы АФП в течение 4-х недель (группа «ХАГ 8 + лАФП 4»)
При морфологическом исследовании препаратов фундального отдела желудка через 4 недели после начала применения липосомальной формы АФП (группа «ХАГ 8 + лАФП 4») отмечалось дальнейшее уменьшение признаков ХАГ.
Фундальный отдел
Было отмечено:
1) сохранение состояния полного восстановления слизистой оболочки желудка, о чем свидетельствовало отсутствие достоверных различий в относительной площади желез по сравнению с интактными животными (группа «инт»);
2) эпителий желез имел высокоспециализированное строение, что было обусловлено высоким количеством главных, обкладочных и эндокринных клеток по сравнению с мукоцитами, особенно секретирующими кислые муцины (сиаломуцин и сульфомуцин);
3) сохранялось отсутствие дилатации вен и микроциркуляторных сосудов, отсутствовали явления отека;
4) полностью отсутствовала воспалительная инфильтрация (хотя этот показатель достоверно отличается от группы интактных животных, но он меньше) и в отличие от группы «ХАГ 8 + вмАФП 4» не только количество лимфоцитов, но и количество моноцитов/макрофагов и плазмоцитов в слизистой желудка соответствовало данному показателю у интактной группы животных (таблица 2, фиг. 11). Соотношение клеточных элементов (нейтрофилы, лимфоциты, моноциты/макрофаги, плазматические клетки) в фундальном отделе желудка составило 1:1:0:0.
Пжорический отдел
Было выявлено следующее:
1) полностью отсутствовали признаки атрофии слизистой, о чем свидетельствовал тот факт, что относительная площадь желез достоверно не отличалась от аналогичного показателя у интактных животных, склеротические изменения отсутствовали;
2) снижение секреции сиаломуцина и сульфомуцина при нормализации количества мукоцитов, секретирующих нейтральные муцины, а также восстановление пула обкладочных и эндокринных клеток, что характеризовало восстановление слизистой оболочки желудка и прежде всего функциональную активность желез его пилорического отдела;
3) нормализация диаметров вен и микроциркуляторных сосудов, отсутствовала агрегация эритроцитов в них, отсутствовали явления отека;
4) выраженность инфильтрации в пилорическом отделе уменьшилась в 5,5 раз по сравнению с группой «ХАГ8» и сохранялась на том же уровне что и в группе «ХАГ 8 + вмАФП 4» (таблица 2, фиг. 12), однако количество плазматических клеток было достоверно меньше. Соотношение клеточных элементов (нейтрофилы, лимфоциты, моноциты/макрофаги, плазматические клетки) в пилорическом отделе составило 1:1:1:0;
5) отсутствовали очаги кишечной метаплазии.
Таким образом, применение липосомальной формы АФП в течение 4 недель привело к полному восстановлению как относительной площади желез, так и их клеточного состава как в фундальном, так и в пилорическом отделе желудка. В фундальном отделе полностью ликвидировались признаки воспалительного компонента ХАГ. В наиболее измененном при ХАГ пилорическом отделе желудка в этом отношении сохранялись статистически значимые различия с интактными животными, однако их выраженность не отличалась от аналогичных показателей в группе «ХАГ8 + вмАФП4».
Сравнение результатов лечения ХАГ с помощью водно-масляной и липосомальной форм АФП показывает, как видно из вышеизложенного и из таблиц, что липосомальная форма оказывает более выраженное лечебное воздействие.
Следует отдельно рассмотреть и сравнить результаты лечения ХАГ с помощью водно-масляной формы АФП в течение 4-х недель и с помощью липосомальной формы в течение 2-х недель.
Сравнение результатов лечения ХАГ с помощью водно-масляной эмульсии АФП в течение 4-х недель и с помощью липосомальной формы АФП в течение 2-х недель показывает достижение в этих группах одинаковых или близких результатов в следующем.
Восстановление слизистой оболочки желудка
При сравнительном морфометрическом анализе фундального отдела желудка в группах «ХАГ8 + вмАФП4» и «ХАГ8 + лАФП2» было выявлено, что при применении липосомальной формы АФП состояние и строение желез восстановилось более полно за 2 недели, чем при использовании водно-масляной эмульсии АФП в течение 4-х недель (относительная площадь желез в сравниваемых группах «ХАГ8 + вмАФП4» и «ХАГ8 + лАФП2» статистически достоверно не отличалось от аналогичного показателя у интактных животных, но площадь желез в группе «ХАГ8 + лАФП2» была достоверно выше, чем в группе «ХАГ8 + вмАФП4»).
Полное восстановление слизистой оболочки желудка в фундальном отделе (относительная площадь желез и их клеточный состав соответствует их уровню у интактных животных) в группе «ХАГ8 + лАФП2», нормализация количества лимфоцитов, плазматических клеток и макрофагов/моноцитов в собственной пластинке слизистой оболочки в этой группе, несмотря на статистически значимое различие по количеству нейтрофилов между данной и интактной группой, свидетельствует о том, что вышеуказанные иммунокомпетентные клетки уже утратили свой провоспалительный потенциал, и их присутствие не отражается отрицательно на состоянии слизистой оболочки фундального отдела.
Таким образом, в фундальном отделе в группе «ХАГ8 + лАФП2» наблюдалось более полное восстановление слизистой оболочки желудка, достигнутое за 2 недели, чем в группе «ХАГ8 + вмАФП4», достигнутое за 4 недели.
В пилорическом отделе относительная площадь желез в группах «ХАГ8 + вмАФП4» и «ХАГ8 + лАФП2» была достоверно ниже, чем у животных в интактной группе, но между собой эти группы по указанному показателю статистически значимо не отличалось (таблица 1 и 2), что можно расценивать как одинаковую стадию ХАГ (Филипенко П.С, Великородный Г.Г. Морфологическая классификация хронического гастрита (Адаптированный вариант) // Успехи современного естествознания.- 2009. - №7. - С. 107-109).
Степень выраженности ХАГ в пилорическом отделе в группе «ХАГ8 + лАФП2» не отличается от таковой в группе «ХАГ8 + вмАФП4»
Сравнительный морфометрический анализ относительной площади клеточных элементов инфильтратов слизистой оболочки желудка в группах «ХАГ8 + вмАФП4» и «ХАГ8 + лАФП2» показал, что в наиболее измененном при ХАГ пилорическом отделе желудка достоверных различий относительной площади нейтрофилов и лимфоцитов, определяющих степень хронического гастрита (Филипенко П.С, Великородный Г. Г. Морфологическая классификация хронического гастрита (Адаптированный вариант) // Успехи современного естествознания.- 2009. - №7. - С. 107-109), не определялось (по отношению к интактной группе оба эти показателя были достоверно выше).
Известно, что альфа-фетопротеин повышает функциональную (пролиферативную и цитотоксическую) активность мононуклеарных лейкоцитов человека (Получение активированных лимфоцитов из мононуклеарных лейкоцитов периферической крови человека при воздействии альфа-фетопротеина/ Черешнев В.А., Лебединская О.В., Ахматова Н.К., Родионов С.Ю., Лебединская Е.А., Гаврилова Т.Е., Карамзин A.M., Киселевский М.В. // Сибирский онкологический журнал.- 2005. - №1. - с. 40-46; Влияние препарата «Профеталь» на функциональную активность мононуклеарных лейкоцитов и дендридных клеток человека/ Черешнев B.А., Лебединская О.В., Родионов С.Ю., Ахматова Н.К., Шубина И.Ж., Лебединская Е.А., Гаврилова Т.Е., Киселевский М.В. Медицинская иммунология. - 2005. - №5-6. - с. 525-534; Влияние препарата «Профеталь» на дифференцировку и функциональную активность мононуклеарных лейкоцитов человека/ Лебединская О.В., Велижева Н.П., Доненко Ф.В., Черешнев В.А., Родионов С.Ю., Ахматова Н.К., Шубина И.Ж., Лебединская Е.А., Киселевсеий М.В. Клеточные технологии в биологии и медицине. - 2006. - №2. - с. 108-116), что приводит к активизации воспалительного процесса.
Поскольку при применении АФП отмечается возможность не только усиления пролиферативной активности мононуклеарных лейкоцитов, но и возрастание цитотоксической способности лимфоцитов, NK- и NKT-клеток, которые являются потенциальными продуцентами провоспалительных цитокинов, длительное применение АФП может способствовать обострению имеющихся в организме хронических инфекционно-воспалительных заболеваний (Роль цитокинов в патогенезе злокачественных новообразований / Соснина А.В., Великая Н.В., Аутеншлюс А.И. Новосибирск: Вектор-Бест, 2013. - 80 с.).
Сокращение длительности лечения ХАГ позволяет избежать вышеуказанных осложнений.

| название | год | авторы | номер документа |
|---|---|---|---|
| Средство для лечения хронического атрофического гастрита | 2017 |
|
RU2662077C1 |
| Средство для лечения хронического атрофического гастрита | 2016 |
|
RU2623866C1 |
| ЛИПОСОМАЛЬНОЕ ПРОТИВОВИРУСНОЕ СРЕДСТВО НА ОСНОВЕ ИНТЕРФЕРОНА АЛЬФА-2b ЧЕЛОВЕКА В КАПСУЛИРОВАННОЙ ФОРМЕ ДЛЯ ВАГИНАЛЬНОГО ПРИМЕНЕНИЯ | 2014 |
|
RU2552851C1 |
| СПОСОБ АНТИХЕЛИКОБАКТЕРНОЙ ТЕРАПИИ | 2005 |
|
RU2277931C1 |
| СПОСОБ ОЦЕНКИ СОСТОЯНИЯ СЛИЗИСТОЙ ОБОЛОЧКИ ЖЕЛУДКА У ДЕТЕЙ | 2011 |
|
RU2469324C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА АЛЬФА-ФЕТОПРОТЕИНА | 1998 |
|
RU2123009C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ХИМИЧЕСКОГО ГАСТРИТА | 2010 |
|
RU2442227C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ ГАСТРОПАТИИ | 2009 |
|
RU2424578C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ХИМИЧЕСКОГО ГАСТРИТА В ЭКСПЕРИМЕНТЕ | 2009 |
|
RU2395125C1 |
| СПОСОБ ЛЕЧЕНИЯ ЯЗВЕННОЙ БОЛЕЗНИ ЖЕЛУДКА И ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ | 2007 |
|
RU2357741C1 |
Изобретение относится к области медицины и раскрывает применение средства, представляющего собой липосомальную форму α-фетопротеина (АФП). Липосомальная форма АФП может представлять собой водную суспензию липосом или лиофилизат. Водная суспензия липосом содержит АФП, липоид С-100, холестерин, лактозу, реополиглюкин, альфа-токоферол (витамин Е), натрия хлорид, натрий фосфорнокислый двузамещенный 12-водный, натрий фосфорнокислый однозамещенный 2-водный и воду в следующем весовом соотношении компонентов: АФП - 0,040-0,160; липоид С-100 - 41,6-43,8; холестерин - 4,0-5,3; альфа-токоферол (витамин Е) - 0,48-0,8; лактоза - 70-120; реополиглюкин - 4,0-6,0; натрия хлорид - 7,0-9,0; натрий фосфорнокислый двузамещенный 12-водный - 4,3-4,9; натрий фосфорнокислый однозамещенный 2-водный - 0,5-0,7; вода - 800-1300. Лиофилизат содержит вышеуказанные компоненты, кроме воды, в том же весовом соотношении. Средний диаметр липосом составляет 0,18 мкм. АФП выделен из пуповинной крови человека Изобретение позволяет за 2 недели лечения достигать тех же результатов в восстановлении слизистой оболочки желудка, что достигается прототипом (водно-масляной формой АФП) за 4 недели. 8 з.п. ф-лы, 12 ил., 2 табл., 1 пр.
1. Применение средства, представляющего собой липосомальную форму α-фетопротеина (АФП), для лечения хронического атрофического гастрита (ХАГ) путем энтерального введения указанного средства.
2. Средство по п. 1, отличающееся тем, что оно представляет собой водную суспензию липосом.
3. Средство по п. 1, отличающееся тем, что оно представляет собой лиофилизат.
4. Средство по п. 3, отличающееся тем, что оно содержит АФП, липоид С-100, холестерин, лактозу, реополиглюкин, альфа-токоферол (витамин Е), натрия хлорид, натрий фосфорнокислый двузамещенный 12-водный, натрий фосфорнокислый однозамещенный 2-водный.
5. Средство по п. 4, отличающееся тем, что его компоненты находятся в следующем весовом соотношении:
АФП - 0,040-0,160;
липоид С-100 - 41,6-43,8;
холестерин - 4,0-5,3;
альфа-токоферол (витамин Е) - 0,48-0,8;
лактоза - 70-120;
реополиглюкин - 4,0-6,0;
натрия хлорид - 7,0-9,0;
натрий фосфорнокислый двузамещенный 12-водный - 4,3-4,9;
натрий фосфорнокислый однозамещенный 2-водный - 0,5-0,7.
6. Средство по п. 2, отличающееся тем, что оно содержит АФП, липоид С-100, холестерин, лактозу, реополиглюкин, альфа-токоферол (витамин Е), натрия хлорид, натрий фосфорнокислый двузамещенный 12-водный, натрий фосфорнокислый однозамещенный 2-водный и воду.
7. Средство по п. 6, отличающееся тем, что его компоненты находятся в следующем весовом соотношении:
АФП - 0,040-0,160;
липоид С-100 - 41,6-43,8;
холестерин - 4,0-5,3;
альфа-токоферол (витамин Е) - 0,48-0,8;
лактоза - 70-120;
реополиглюкин - 4,0-6,0;
натрия хлорид - 7,0-9,0;
натрий фосфорнокислый двузамещенный 12-водный - 4,3-4,9;
натрий фосфорнокислый однозамещенный 2-водный - 0,5-0,7;
вода - 800-1300.
8. Средство по п. 1, отличающееся тем, что средний диаметр липосом составляет 0,18 мкм.
9. Средство по п. 1, отличающееся тем, что АФП выделен из пуповинной крови человека.
| ЛИПОСОМА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ МЕСТНЫХ РАДИАЦИОННЫХ ПОРАЖЕНИЙ КОЖИ, ПРИМЕНЕНИЕ ЛИПОСОМ И СПОСОБ ДЛЯ ЛЕЧЕНИЯ МЕСТНЫХ РАДИАЦИОННЫХ ПОРАЖЕНИЙ КОЖИ | 2016 |
|
RU2642957C2 |
| Средство для лечения хронического атрофического гастрита | 2017 |
|
RU2662077C1 |
| WO 2007126546 A1, 08.11.2007 | |||
| ЧЕРЕШНЕВ В.А | |||
| и др | |||
| Альфа-фетопротеин | |||
| Екатеринбург: УрО РАН, 2004 | |||
| Газогенератор для дров, торфа и кизяка | 1921 |
|
SU376A1 |
Авторы
Даты
2020-06-18—Публикация
2019-05-31—Подача